Спонтанный пневмоторакс
Спонтанный пневмоторакс – это проникновение воздуха в плевральную полость из окружающей среды вследствие нарушения целостности поверхности легкого. Принято различать первичный и вторичный (т.е. связанный с каким либо заболеванием легких) пневмоторакс.
Спонтанный пневмоторакс развивается, как правило, у мужчин молодого возраста, у женщин он встречается в 5 раз реже. Первый момент от развития пневмоторакса пациенты чаще жалуются на боль в грудной клетке на стороне пневмоторакса колющего или ноющего характера, ощущение затрудненного дыхания, кашель, как правило, сухой, снижение переносимости физической нагрузки. Через несколько дней часто появляется повышение температуры тела. Диагноз чаще не вызывает затруднений у опытного специалиста. При обзорной рентгенографии грудной клетки в двух проекциях в большинстве случаев удается установить диагноз.
Малый пневмоторакс не требует оперативного вмешательства, однако пациенты должны быть госпитализированы в стационар для наблюдения, обезболивания, проведения кислородотерапии.
Буллы могут встречаться и у здоровых людей и не обязательно приводят к развитию пневмоторакса. Причиной вторичного пневмоторакса является заболевание какое-либо легких, приводящее к разрушению легочной ткани. К таким заболеваниям относятся хроническая обструктивная болезнь легких, бронхиальная астма, лимфангиолейомиоматоз, диссеминированные процессы в легких, муковисцидоз и другие.
При расправлении легкого и прекращении поступления воздуха дренаж удаляют. При нерасправлении легкого или сохранении дефекта в легком необходимо оперативное вмешательство.
Риск рецидива первичного спонтанного пневмоторакса, как правило, составляет около 30% после первого эпизода. После второго около 60%, а после третьего около 80%. Поэтому в большинстве клиник рецидив пневмоторакса является показанием к оперативному вмешательству.
Оперативное вмешательство при спонтанном пневмотораксе выполняют под общей анестезией. Цель операции: герметизация дефекта в легком, краевая резекция легочной ткани, удаление плевры (оболочки, выстилающей внутреннюю поверхность грудной стенки) для создания сращений между легким и грудной стенкой с целью предотвращения повторных пневмотораксов. Оперативное вмешательство в 97-98% помогает предотвратить последующие рецидивы пневмоторакса.
Оперативное вмешательство выполняется при помощи эндоскопической техники из 3-4 маленьких разрезов размером 1-1,5см. Продолжительность операции 40-50 минут. Пациенты выписываются из стационара на 3-5 сутки после операции.
Продолжительность операции 40-50 минут. Пациенты выписываются из стационара на 3-5 сутки после операции.
Диагностическая и лечебная тактика при спонтанном пневмотораксе, использующаяся в нашем Центре, соответствует «Протоколам оказания лечебно-диагностической помощи при острых заболеваниях грудной полости (спонтанный пневмоторакс)» утвержденным Ассоциацией хирургов Санкт-Петербурга в 2007 году.
запись к врачу — ДокДок СПб
Пульмонологи Санкт-Петербурга — последние отзывы
Доктор внимательно провела осмотр, всё объяснила и помогла в решении вопроса. Я пойду к ней повторно!
На модерации, 24 апреля 2021
 На приеме она проанализировала мои снимки и дала дальнейшие рекомендации.
На приеме она проанализировала мои снимки и дала дальнейшие рекомендации.Людмила, 16 апреля 2021
Светлана, 19 апреля 2021
 Все было понятно и доступно.
Все было понятно и доступно.Любовь, 19 апреля 2021
Василий, 09 апреля 2021
 Она меня послушала, рассказала о заболевании и прописала методы лечения.
Она меня послушала, рассказала о заболевании и прописала методы лечения.Олег, 04 апреля 2021
Шахло, 02 апреля 2021
Приятный в общении и грамотный доктор. Она меня выслушала, все уточнила, назначила анализы и подсказала, в каком нужно двигаться направлении.
Она меня выслушала, все уточнила, назначила анализы и подсказала, в каком нужно двигаться направлении.
Владимир, 23 марта 2021
Хороший доктор. Она выслушала пациента и прописала лечение. Нам понравилось!
Артем, 22 марта 2021
Я рассказала доктору, что меня беспокоит. Она меня послушала, посмотрела мои документы и сделала все, что нужно. Приятный и красивый врач.
Она меня послушала, посмотрела мои документы и сделала все, что нужно. Приятный и красивый врач.
Ольга, 22 марта 2021
Показать 10 отзывов из 858Современные особенности видеоторакоскопического лечения спонтанного пневмоторакса как осложнения буллезной эмфиземы лёгкого: систематизированный обзор литературы | Токтохоев
1. Акопов А.Л., Агишев А.С. Видеоторакоскопическая костальная плеврэктомия при первичном и вторичном спонтанном пневмотораксе // Хирургия. — 2012. — № 11. — С. 15-18
2. Вачев А.Н., Адыширин-Заде Э.Э., Фролова Е.В. Оптимизация хирургической тактики при лечении больных со спонтанным пневмотораксом // Хирургия. — 2013. — № 6. — С. 26-28
— 2013. — № 6. — С. 26-28
3. Десятерик В.И., Ежеменский М.А., Михно С.П. Выбор метода плевродеза при лечении спонтанного пневмоторакса // Вестник неотложной и восстановительной медицины. — 2012. — Т. 13, № 2. — С. 260-262
4. Ежеменский М.А., Десятерик В.И., Михно С.П. Видеоторакоскопические вмешательства при лечении спонтанного пневмоторакса // Вестник неотложной и восстановительной медицины. — 2013. — Т. 14, № 3. — С. 336-338
5. Зайцев Д.А., Мовчан К.Н., Лишенко В.В. Возможности целенаправленного использования торакоскопии в улучшении результатов обследования и лечения пациентов со спонтанным пневмотораксом // Международный журнал прикладных и фундаментальных исследований. — 2015. — № 6-3. -С. 440-444
6. Клинические рекомендации по лечению спонтанного пневмоторакса: Утверждены на общем собрании Ассоциации торакальных хирургов России на IV Международном конгрессе «Актуальные направления современной кардиоторакальной хирургии» (28.06.2014 г.). — СПб., 2014. — С. 1-24
Клинические рекомендации по лечению спонтанного пневмоторакса: Утверждены на общем собрании Ассоциации торакальных хирургов России на IV Международном конгрессе «Актуальные направления современной кардиоторакальной хирургии» (28.06.2014 г.). — СПб., 2014. — С. 1-24
7. Корымасов Е.А., Бенян А.С., Пушкин С.Ю. Анализ ошибок и осложнений в лечении спонтанного пневмоторакса // Тольяттинский медицинский консилиум. — 2013. — № 3-4. — С. 44-51
8. Михеев А.В., Баскевич М.А. Аспекты хирургического лечения пациентов со спонтанным пневмотораксом // Наука молодых (Eruditio Juvenium). — 2013. -№ 4. — С. 44-51
9. Неретин А.В., Мотус И.Я. Совершенствование тактики лечения пациентов со спонтанным пневмотораксом // Уральский медицинский журнал. — 2013. -Т. 107, № 2. — С. 80-84
80-84
10. Олефиров А.С., Адыширин-Заде Э.Э., Андреев И.С. К вопросу о выборе тактики лечения больных с первым эпизодом первичного спонтанного пневмоторакса // Материалы XI съезда хирургов России. -Волгоград, 2012. — С. 254-255
11. Пахомов Г.Л., Хулайбергенов Ш.Н., Хаялиев Р.Я. К вопросу о тактике хирургического лечения неспецифического спонтанного пневмоторакса // Вестник экспериментальной и клинической хирургии. — 2010. — Т. 3, № 2. — С. 103-111
12. Пичуров А.А., Оржешковский О.В., Петрунькин А.М. Спонтанный пневмоторакс — анализ 1489 случаев // Вестник хирургии им. И.И. Грекова. — 2013. — Т. 172, № 5. — С. 82-88
13. Пландовский А.В. Выбор рациональной хирургической тактики у пациентов со спонтанным пневмотораксом // Военная медицина. — 2012. -№ 1 (22). — С. 90-94
— 2012. -№ 1 (22). — С. 90-94
14. Погодина А.Н., Воскресенский О.В., Николаева Е.Б., Бармина Т.Г., Паршин В.В. Современные подходы к лечению спонтанного пневмоторакса и спонтанной эмфиземы средостения // Атмосфера. Пульмонология аллергология. — 2011. — № 1. — С. 45-51
15. Савельев В.С., Константинова Г.Д. Нетуберкулезный спонтанный пневмоторакс. — М.: Медицина, 1969. — С. 136
16. Фунлоэр И.С., Жынжыров Б.К. Буллезная болезнь, осложнённая пневмотораксом, в условиях Кыргызстана // Вестник Кыргызско-Российского Славянского университета. — 2013. -Т. 13, № 4. -С. 180-184
17. Фунлоэр И.С., Жынжыров Б.К., Юсупов Т.К. Спонтанный пневмоторакс как следствие буллезной болезни // Вестник Кыргызско-Российского славянского университета. — 2011. — Т. 11, № 3. — С. 157-161
— 2011. — Т. 11, № 3. — С. 157-161
18. Чарышкин А.Л., Мелкий Д.А., Елущенко Л.В. Алгоритм лечения спонтанного пневмоторакса // Ульяновский медико-биологический журнал. — 2014. — № 3. — С. 15-18
19. Чикинев Ю.В., Пустоветова М.Е., Дробязгин Е.А. Результаты хирургического лечения рефрактерного спонтанного пневмоторакса // Медицина и образование в Сибири. — 2013. — № 6. — С. 67-73
20. Шевченко Ю.Л., Мальцев А.А. Тактика хирургического лечения и профилактики рецидива спонтанного пневмоторакса // Вестник национального медико-хирургического Центра им. Н.И. Пирогова. -2013. — Т. 8, № 1. — С. 116-119
21. Яблонский П.К., Атюков М.А., Пищик В.Е. Выбор лечебной тактики и возможности прогнозирования рецидивов у больных с первым эпизодом спонтанного пневмоторакса // Вестник СПбЕУ — 2010. — Сер. 11, Вып. 1. — С. 118-129
— Сер. 11, Вып. 1. — С. 118-129
22. Яблонский П.К., Петров А.С., Пищик В.Г., Атюков М.А., Оржешковский О.В. Спонтанный пневмоторакс: учебное пособие. — СПб.: СПб. гос. ун-т, 2013. — 42 с
23. Amin R, Noone G, Ratjen F (2013). Chemical pleurodesis versus surgical intervention for persistent and recurrent pneumothoraces in cystic fibrosis (Review). The Cochrane Library, Issue 1.
24. Billeter AT, Druen D, Franklin GA et al. (2013). Video-assisted thoracoscopy as an important tool for trauma surgeons: a systematic review. Langenbecks Arch. Surg., 398 (4), 515-523.
25. Chen JS, Hsu HH, Huang PM et al. (2012). Thora-coscopic pleurodesis for primary spontaneous pneumothorax with high recurrence risk: a prospective randomized trial. Ann. Surg., 255 (3), 440-445.
Ann. Surg., 255 (3), 440-445.
26. Forouls CN, Anastasiadis K, Charokopos N et al. (2012). A modified two-port thoracoscopic technique versus axillary minithoracotomy for the treatment or recurrent spontaneous pneumothorax: a prospective randomized study. Surg. Endosc., 12 (3), 607-614.
27. Ismail T, Anshar MF, How SH et al. (2010). Survey on the initial management of spontaneous pneumothorax. Med. J. Malaysia, 65 (3), 187-191.
28. Karangelis D, Nagarakis GI, Daskalopoulos M et al. (2010). Intrapleural instillation of autologous blood for persistent air leak in spontaneous pneumothorax is it as effective as it is safe. J. Cardiothorac. Surg., 17, 702-704.
29. Muramatsu T, Nishii T, Takeshita S et al. (2010). Preventing recurrence of spontaneous pneumothorax after thoracoscopic surgery: a review of recent results. Surg. Today., 40 (8), 696-699.
(2010). Preventing recurrence of spontaneous pneumothorax after thoracoscopic surgery: a review of recent results. Surg. Today., 40 (8), 696-699.
30. Nwaejike N, Aldam P, Pulmood T et al. (2012). A case of recurrent spontaneous pneumothorax during pregnancy treated with video assisted thoracoscopic surgery. BMJ Case Rep., 13, 610-612.
31. Vodicka J (2011). Are there any news in the management of spontaneous pneumothorax. Rozhl. Chir., 90 (11), 625-630.
32. Wakai A, Sullivan R, McCabe G (2013). Simple aspiration versus intercostals tube drainage for primary spontaneous pneumothorax in adults (Review). The Cochrane Library, 2, 1-19.
Спонтанный пневмоторакс — причины, симптомы, диагностика и лечение, прогноз
Спонтанный пневмоторакс – это патологическое состояние, характеризующееся внезапным нарушением целостности висцеральной плевры и поступлением воздуха из легочной ткани в плевральную полость. Развитие спонтанного пневмоторакса сопровождается остро возникающей болью в грудной клетке, одышкой, тахикардией, бледностью кожных покровов, акроцианозом, подкожной эмфиземой, стремлением пациента принять вынужденное положение. С целью первичной диагностики спонтанного пневмоторакса проводится рентгенография легких и диагностическая плевральная пункция; для установления причин заболевания требуется углубленное обследование (КТ, МРТ, торакоскопия). Лечение спонтанного пневмоторакса включает дренирование плевральной полости с активной или пассивной эвакуацией воздуха, видеоторакоскопические или открытые вмешательства (плевродез, удаление булл, резекцию легкого, пульмонэктомию и др.)
Развитие спонтанного пневмоторакса сопровождается остро возникающей болью в грудной клетке, одышкой, тахикардией, бледностью кожных покровов, акроцианозом, подкожной эмфиземой, стремлением пациента принять вынужденное положение. С целью первичной диагностики спонтанного пневмоторакса проводится рентгенография легких и диагностическая плевральная пункция; для установления причин заболевания требуется углубленное обследование (КТ, МРТ, торакоскопия). Лечение спонтанного пневмоторакса включает дренирование плевральной полости с активной или пассивной эвакуацией воздуха, видеоторакоскопические или открытые вмешательства (плевродез, удаление булл, резекцию легкого, пульмонэктомию и др.)
Общие сведения
Под спонтанным пневмотораксом в клинической пульмонологии понимают идиопатический, самопроизвольный пневмоторакс, не связанный с травмой или ятрогенными лечебно-диагностическими вмешательствами. Спонтанный пневмоторакс статистически чаще развивается у мужчин и преобладает среди лиц трудоспособного возраста (20-40 лет), что предопределяет не только медицинскую, но и социальную значимость проблемы.
Если при травматическом и ятрогенном пневмотораксе четко прослеживается причинно-следственная связь между заболеванием и внешним воздействием (травмой грудной клетки, пункцией плевральной полости, катетеризацией центральных вен, торакоцентезом, биопсией плевры, баротравмой и др.), то в случае спонтанного пневмоторакса такая обусловленность отсутствует. Поэтому выбор адекватной диагностической и лечебной тактики является предметом повышенного внимания пульмонологов, торакальных хирургов, фтизиатров.
Спонтанный пневмоторакс
Причины
Первичный спонтанный пневмоторакс развивается у лиц, не имеющих клинически диагностированной патологии легких. Однако при проведении диагностической видеоторакоскопии или торакотомии у данного контингента больных в 75-100% случаев выявляются субплеврально расположенные эмфизематозные буллы. Отмечена взаимосвязь между частотой спонтанного пневмоторакса и конституциональным типом пациентов: заболевание чаще возникает у худых высоких молодых людей. Курение увеличивает риски развития спонтанного пневмоторакса до 20 раз.
Курение увеличивает риски развития спонтанного пневмоторакса до 20 раз.
Вторичный спонтанный пневмоторакс может развиваться на фоне широкого круга патологий:
- заболеваний легких (ХОБЛ, муковисцидоза, бронхиальной астмы)
- инфекций дыхательных путей (пневмоцистной пневмонии, абсцедирующей пневмонии, туберкулеза). В случае прорыва в плевральную полость абсцесса легкого развивается пиопневмоторакс.
- интерстициальных болезней легких (саркоидоза Бека, пневмосклероза, лимфангиолейомиоматоза, гранулематоза Вегенера), системных болезней (ревматоидного артрита, склеродермии, синдрома Марфана, болезни Бехтерева, дерматомиозита и полимиозита)
- злокачественных новообразований (саркомы, рака легких).
К относительно редким формам спонтанного пневмоторакса относят менструальный и неонатальный пневмоторакс. Менструальный пневмоторакс этиологически связан с грудным эндометриозом и развивается у молодых женщин в первые двое суток от начала менструации. Вероятность рецидива менструального пневмоторакса, даже на фоне консервативной терапии эндометриоза, составляет около 50%, поэтому сразу после установления диагноза с целью предотвращения повторных эпизодов спонтанного пневмоторакса может выполняться плевродез.
Вероятность рецидива менструального пневмоторакса, даже на фоне консервативной терапии эндометриоза, составляет около 50%, поэтому сразу после установления диагноза с целью предотвращения повторных эпизодов спонтанного пневмоторакса может выполняться плевродез.
Неонатальный пневмоторакс – спонтанный пневмоторакс новорожденных встречается у 1-2% детей, в 2 раза чаще у мальчиков. Патология может быть связана с проблемами расправления легкого, респираторным дистресс-синдромом, разрывом ткани легкого при проведении ИВЛ, пороками развития легких (кистами, буллами).
Патогенез
Степень выраженности структурных изменений зависит от времени, прошедшего с момента возникновения спонтанного пневмоторакса, наличия исходных патологических нарушений в легком и висцеральной плевре, динамики воспалительного процесса в плевральной полости.
При спонтанном пневмотораксе имеет место патологическое легочно-плевральное сообщение, обусловливающее попадание и скопление воздуха в плевральной полости; частичный или полный коллапс легкого; смещение и флотация средостения.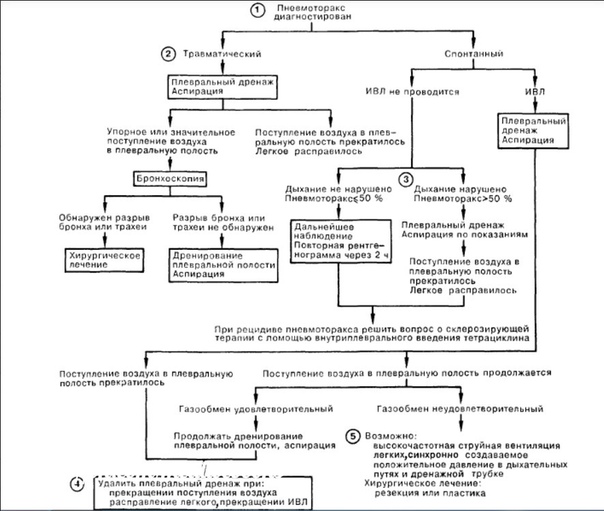
Воспалительная реакция развивается в полости плевры через 4-6 часов после эпизода спонтанного пневмоторакса. Она характеризуется гиперемией, инъекцией сосудов плевры, образованием незначительного количества серозного экссудата. В течение 2-5 суток нарастает отечность плевры, особенно на участках ее контакта с проникшим воздухом, увеличивается количество выпота, происходит выпадение фибрина на поверхность плевры.
Прогрессирование воспалительного процесса сопровождается разрастанием грануляций, фиброзной трансформацией выпавшего фибрина. Спавшееся легкое фиксируется в поджатом состоянии и становится неспособным к расправлению. В случае присоединения гемоторакса или инфекции со временем развивается эмпиема плевры; возможно образование бронхоплеврального свища, поддерживающего течение хронической эмпиемы плевры.
Классификация
По этиологическому принципу различают первичный и вторичный спонтанный пневмоторакс. О первичном спонтанном пневмотораксе говорят при отсутствии данных за клинически значимую легочную патологию. Возникновение вторичного спонтанного пневмоторакса происходит на фоне сопутствующих легочных заболеваний.
Возникновение вторичного спонтанного пневмоторакса происходит на фоне сопутствующих легочных заболеваний.
В зависимости от степени коллабирования легкого выделяют:
- частичный (малый, средний). При малом спонтанном пневмотораксе происходит спадение легкого на 1/3 от первоначального объема, при среднем – на 1/2.
- тотальный. При тотальном пневмотораксе легкое спадается более чем на половину.
По степени компенсации дыхательных и гемодинамических расстройств, сопровождающих спонтанный пневмоторакс, определены три фазы патологических изменений: фаза стойкой компенсации, фаза неустойчивой компенсации и фаза декомпенсации (недостаточной компенсации).
- Фаза стойкой компенсации наблюдается при спонтанном пневмотораксе малого и среднего объема; она характеризуется отсутствием признаков дыхательной и сердечно-сосудистой недостаточности, ЖЕЛ и МВЛ снижены до 75% от нормы.
- Фазе неустойчивой компенсации соответствует коллабирование легкого более чем на 1/2 объема, развитие тахикардии и одышки при физической нагрузке, значительное уменьшение показателей внешнего дыхания.

- Фаза декомпенсации проявляется одышкой в покое, выраженной тахикардией, микроциркуляторными нарушениями, гипоксемией, уменьшением значений ФВД на 2/3 и более от нормальных значений.
Симптомы спонтанного пневмоторакса
По характеру клинической симптоматики различают типичный вариант спонтанного пневмоторакса и латентный (стертый) вариант. Типичная клиника спонтанного пневмоторакса может сопровождаться умеренными или бурными проявлениями.
В большинстве случаев первичный спонтанный пневмоторакс развивается внезапно, среди полного здоровья. Уже в первые минуты заболевания отмечаются острые колющие или сжимающие боли в соответствующей половине груди, остро возникшая одышка. Выраженность боли варьирует от слабо интенсивной до очень сильной. Усиление болей происходит при попытке глубокого вдоха, кашле. Болевые ощущения распространяются на шею, плечо, руку, область живота или поясницы.
В течение 24 часов болевой синдром уменьшается или полностью исчезает, даже в том случае, если спонтанный пневмоторакс не разрешается. Ощущения дыхательного дискомфорта и нехватки воздуха возникают только при физической нагрузке.
Ощущения дыхательного дискомфорта и нехватки воздуха возникают только при физической нагрузке.
При бурных клинических проявлениях спонтанного пневмоторакса болевой приступ и одышка выражены крайне резко. Могут возникать кратковременные обморочные состояния, бледность кожи, акроцианоз, тахикардия, чувство страха и тревоги. Пациенты щадят себя: ограничивают движения, принимают положение полусидя или лежа на больном боку. Нередко развивается и прогрессирующе нарастает подкожная эмфизема, крепитация в области шеи, верхних конечностей, туловища. У пациентов с вторичным спонтанным пневмотораксом, виду ограниченности резервов сердечно-сосудистой системы, заболевание протекает тяжелее.
Осложнения
К осложненным вариантам течения спонтанного пневмоторакса относится развитие напряженного пневмоторакса, гемоторакса, реактивного плеврита, одномоментного двустороннего коллапса легких. Скопление и длительное нахождение инфицированной мокроты в коллабированном легком приводит к развитию вторичных бронхоэктазов, повторных эпизодов аспирационной пневмонии в здоровом легком, абсцессов. Осложнения спонтанного пневмоторакса развиваются в 4-5% случаев, однако они могут представлять угрозу для жизни пациентов.
Осложнения спонтанного пневмоторакса развиваются в 4-5% случаев, однако они могут представлять угрозу для жизни пациентов.
Диагностика
Осмотр грудной клетки выявляет сглаженность рельефа межреберий, ограничение дыхательной экскурсии на стороне спонтанного пневмоторакса, подкожную эмфизему, набухание и расширение вен шеи. На стороне коллабированного легкого отмечается ослабление голосового дрожания, тимпанит при перкуссии, при аускультации — отсутствие или резкое ослабление дыхательных шумов. Первостепенное значение в диагностике отводится:
- Лучевым методам. Рентгенография и рентгеноскопия грудной клетки позволяют оценить количество воздуха в плевральной полости и степень спадения легкого в зависимости от распространенности спонтанного пневмоторакса. Контрольные рентгеновские исследования проводятся после любых лечебных манипуляций (пункции или дренирования плевральной полости) и позволяют оценить их эффективность. В дальнейшем с помощью КТ высокого разрешения или МРТ легких устанавливается причина спонтанного пневмоторакса.

- Лечебно-диагностической торакоскопии. Высокоинформативным методом, используемым в диагностике спонтанного пневмоторакса, является торакоскопия. В процессе исследования удается выявить субплевральные буллы, опухолевые или туберкулезные изменения на плевре, осуществить биопсию материала для морфологического исследования.
Спонтанный пневмоторакс латентного или стертого течения необходимо дифференцировать от гигантской бронхолегочной кисты и диафрагмальной грыжи. В последнем случае дифдиагностике помогает рентгенография пищевода.
КТ ОГК. Спонтанный малый пневмоторакс вследствие разрыва буллы.
Лечение спонтанного пневмоторакса
Лечебные стандарты требуют как можно более ранней эвакуации скопившегося в полости плевры воздуха и достижения расправления легкого. Общепринятым стандартом является переход от диагностической тактики к лечебной. Таким образом, получение в процессе торакоцентеза воздуха является показанием к дренированию плевральной полости. Плевральный дренаж устанавливается во II межреберье по среднеключичной линии, после чего присоединяется к активной аспирации.
Плевральный дренаж устанавливается во II межреберье по среднеключичной линии, после чего присоединяется к активной аспирации.
Улучшение проходимости бронхов и эвакуация вязкой мокроты облегчают задачу расправления легкого. С этой целью проводятся лечебные бронхоскопии (бронхоальвеолярный лаваж, трахеальная аспирация), ингаляции с муколитиками и бронхолитиками, дыхательная гимнастика, оксигенотерапия.
Если в течение 4-5 суток не наступает расправления легкого, переходят к хирургической тактике. Она может заключаться в торакоскопической диатермокоагуляции булл и спаек, ликвидации бронхоплевральных свищей, осуществлении химического плевродеза. При рецидивирующем спонтанном пневмотораксе, в зависимости от его причин и также состояния легочной ткани, может быть показана атипичная краевая резекция легкого, лобэктомия или даже пневмонэктомия.
Прогноз
При первичном спонтанном пневмотораксе прогноз благоприятный. Обычно удается достичь расправления легкого минимально инвазивными способами. При вторичном спонтанном пневмотораксе рецидивы заболевания развиваются у 20-50% пациентов, что диктует необходимость устранения первопричины и избрания более активной лечебной тактики. Пациенты, перенесшие спонтанный пневмоторакс, должны находиться под наблюдением торакального хирурга или пульмонолога.
Пневмоторакс спонтанный › Болезни › ДокторПитер.ру
Пневмоторакс спонтанный — потеря отрицательного давления в плевральной полости, сопровождающаяся частичным или тотальным коллапсом легкого вследствие сообщения с внешней средой при целости грудной стенки. При задержке вновь поступающего воздуха в полости плевры возникает напряженный (вентильный) пневмоторакс, быстро ведущий к массивному коллапсу легкого и смещению органов средостения.
Признаки
Характерными симптомами являются внезапная интенсивная боль в грудной полости, возникающая нередко среди полного здоровья, нехватка воздуха, цианоз, тахикардия. Возможны снижение АД, отсутствие тактильно определяемого голосового дрожания, перкуторно — коробочный звук, дыхательные шумы снижены либо исчезают. Дыхательная недостаточность может пройти без разрешения пневмоторакса. Окончательный диагноз устанавливают при рентгенологическом исследовании. Спонтанный пневмоторакс может быть первичным и вторичным. Первичный возникает в результате прорыва субплевральных эмфизематозных булл, чаще в верхушках легких. Обычно это больные высокого роста с несоответственно меньшей массой тела. Пневмоторакс развивается в состоянии покоя, реже при нагрузке. Курящие более подвержены спонтанному пневмотораксу.
Вероятность рецидива без плевродеза составляет примерно 50 %. Вторичный спонтанный пневмоторакс чаще возникает на фоне хронических обструктивных заболеваний легких (туберкулез, силикотуберкулез, саркоидоз, бронхиальная астма, инфаркт легкого, ревматоидные заболевания, эхинококкоз). Клиника вторичного спонтанного пневмоторакса более тяжелая.
Описание
Менструальный пневмоторакс связан с менструальным циклом у женщин старше 25 лет. Возникает в первые 48 ч после начала менструации. Происхождение неизвестно. Для лечения используют препараты, подавляющие овуляцию. В противном случае — торакотомический плевродез.
Неонатальный пневмоторакс чаще наблюдается у новорожденных, примерно в 1-2 % (с клинической симптоматикой у 0,5 %), в 2 раза чаще у новорожденных мальчиков, обычно у доношенных и переношенных детей. Причина связана с механическими проблемами первого расправления легкого, а также респираторным дистресс-синдромом.
Диагностика
Диагностика рентгенологическая.
Лечение
Лечение спонтанного пневмоторакса преследует две цели: выведение воздуха из плевральной полости и снижение вероятности развития рецидива. Первая лечебная помощь — пункция плевральной полости и аспирация воздуха через прокол в третьем — четвертом межреберье по средне-ключичной линии и вслед за этим дренирование по Бюлау, особенно при напряженном пневмотораксе, применение обезболивающих средств. Для профилактики рецидива используют плевродез склерозирующими веществами, в частности тетрациклином внутриплеврально при расправленном легком.
Прогноз при первичном спонтанном пневмотораксе благоприятный, при вторичном — обусловлен течением основного заболевания.
© Большая медицинская энциклопедия
Другой спонтанный пневмоторакс — симптомы (признаки), лечение, лекарства
Раздел предназначен исключительно для медицинских и фармацевтических работников! Если Вы не являетесь медицинским и фармацевтическим работником — покиньте раздел! Условия использования- Номер класса:
- X
- Наименование класса:
- Болезни органов дыхания
- Номер блока:
- J90-J94
- Наименование блока:
- Другие болезни плевры
- Код заболевания:
- J93.1
Лечение спонтанного пневмоторакса преследует две цели: выведение воздуха из плевральной полости и снижение вероятности развития рецидива. Первая лечебная помощь — пункция плевральной полости и аспирация воздуха через прокол в третьем -четвертом межреберье по средне-ключичной линии и вслед за этим дренирование по Бюлау, особенно при напряженном пневмотораксе, применение обезболивающих средств. Для профилактики рецидива используют плевродез склерозирующими веществами, в частности тетрациклином в дозе 20 мг/кг внутриплеврально при расправленном легком.
Менструальный пневмоторакс связан с менструальным циклом у женщин старше 25 лет. Возникает в первые 48 ч после начала менструации. Происхождение неизвестно. Для лечения используют препараты, подавляющие овуляцию. В противном случае-торакотомический плевродез. Неонатальный пневмоторакс чаще наблюдается у новорожденных, примерно в 1-2% (с клинической симптоматикой у 0,5%), в 2 раза чаще у новорожденных мальчиков, обычно у доношенных и переношенных детей. Причина связана с механическими проблемами первого расправления легкого, а также респираторным дистресс-синдромом. Диагностика рентгенологическая. При клинической симптоматике — дренирование плевральной полости. Госпитализация в хирургический стационар.
Прогноз при первичном спонтанном пневмотораксе благоприятный, при вторичном -обусловлен течением основного заболевания.
Администрация сайта не осуществляет деятельность в сфере медицинских услуг. Консультации и рекомендации носят лишь информационный характер и не являются полноценной медицинской помощью. Любая медицинская помощь осуществляется только в специализированных медицинских учреждениях. При любых недомоганиях обратитесь к врачу.
КОММЕНТАРИИ
Уведомления
Написать сообщение
Буллезная эмфизема легких, осложненная спонтанным пневмотораксом Случай из практики
Буллезная эмфизема легких (БЭЛ) рассматривается как вариант эмфиземы легких и характеризуется деструкцией альвеолярных стенок с образованием полостей больше 1 см, которые и называются буллами. Болезнь представляется как БЭЛ. В то же время В.И. Стручков, В.А. Смоляр выделяют данную патологию как самостоятельную нозологическую форму и называют ее буллезной болезнью. Существует ряд теорий, объясняющих природу возникновения БЭЛ: генетическая, обструктивная, механическая, инфекционная, сосудистая и другие. Некоторые ученые рассматривают БЭЛ и спонтанный пневмоторакс (СП) у детей как проявление дисплазии соединительной ткани (ДСТ) и следствие дефицита магния. Дисплазия соединительной ткани — генетически детерминированное состояние, обусловленное нарушениями метаболизма соединительной ткани в эмбриональном и постнатальном периоде, особенно при дефиците микронутриентов, прежде всего магния. Синдром ДСТ характеризуется аномалиями структуры компонентов внеклеточного матрикса (волокон и основного вещества) с морфофункциональными изменениями различных органов и систем [1, 3, 11].
Признаками ДСТ бронхолегочной системы являются трахеобронхомаляция, трахеобронхомегалия, трахеобронхиальная дискинезия, бронхоэктазы, апикальные буллы и первичный спонтанный пневмоторакс; наблюдаются костносуставные изменения в виде деформации грудной клетки (воронкообразная, килевидная), позвоночника (сколиоз, гиперкифоз), конечностей (вальгусная, варусная), стопы (плоскостопия и др.), гипермобильность суставов. Наиболее часты у таких детей признаки ДСТ сердечнососудистой системы (пролапсы клапанов сердца), аневризмы сосудов (варикозное расширение вен и др.), а также вегетососудистая дистония. Отмечается значимое влияние микроэлементов (ионов магния) на процессы синтеза клетками соединительной ткани [5, 12].
Одной из частых причин буллезной эмфиземы легких является воспаление неспецифического характера, которое чаще локализуется в верхних отделах легких, особенно в области верхушек, где перфузия хуже, чем в других участках органа. Неспецифическое воспаление приводит к развитию ограниченной апикальной формы БЭЛ. Также важными причинами ее являются вирусные инфекции, что объясняется тропизмом слизистой оболочки бронхов и бронхиол к этим возбудителям и ведет к развитию обструктивного бронхиолита с растяжением участков легкого и образованием локальных буллезных изменений. Существует гипотеза об эластозависимом генезе БЭЛ, связанном с недостаточностью ингибитора эластазы — 1антитрипсина. Выдвинута концепция о генетической, семейной предрасположенности к развитию БЭЛ при нормальном содержании 1антитрипсина в сыворотке крови у пациентов [1, 5, 8]. Считается, что основным патомеханизмом возникновения БЭЛ является низкая ингибирующая активность ферментов в отношении нейтрофильной эластазы, что приводит к протеолитической деструкции респираторной ткани, в первую очередь эластических волокон. Важную роль в патогенезе БЭЛ играет нарушение бронхиальной проходимости и кровоснабжения легочной ткани. Патологоанатомическими причинами развития БЭЛ являются деструкция легочной паренхимы и обструкция дыхательных путей. Потеря легкими эластичности сопровождается необратимым затруднением вентиляции вследствие динамической компрессии воздухом проводящих путей при выдохе. Таким образом, БЭЛ является разновидностью эмфиземы, характеризуется наличием воздушных пузырей в их паренхиме и неоднородна по этиологии и патогенезу [2, 3, 9].
По распространенности различают локальную БЭЛ и генерализованную форму. По клиническому течению: без клинических проявлений и осложненную в виде пневмоторакса (рецидивного, перемежающегося, хронического). Частым осложнением БЭЛ является первичный спонтанный пневмоторакс. Так, по данным H. Westerlaen et al. (2006), M. Takahashi et al. (2008), 88–92 % случаев пневмоторакса приходятся на БЭЛ. СП развивается при обстоятельствах как способствующих повышению внутрилегочного давления (кашель, чихание, дефекация), так и без них — при ходьбе, в покое, во сне. Нередко при небольшой травме грудной клетки или при значительном физическом напряжении, во время занятий спортом, при поднятии грузов, полете на самолете и др.
Наиболее частыми симптомами у больных со спонтанным пневмотораксом как осложнением БЭЛ являются: внезапные и резкие боли в грудной клетке (справа или слева, либо реже — с обеих сторон), иногда иррадиирующие в область ключицы; одышка в покое и особенно одышка при физической нагрузке; затрудненное дыхание, особенно при вдохе; удушье, нехватка воздуха; изнуряющие приступы сухого кашля или кашля со слизистогнойной мокротой, которые сопровождаются общей слабостью, недомоганием, повышенной потливостью, головной болью, головокружением, учащенным сердцебиением. При объективном исследовании определяется тимпанит на стороне пневмоторакса, при аускультации — отсутствие дыхания на пораженной стороне, смещение сердца в здоровую сторону, тахикардия, увеличение печени. Рентгенологически в 99 % случаев установлено наличие воздуха в плевральной полости, но не всегда ясна причина, вызвавшая появление воздуха в плевральной полости.
Диагностическое значение в оценке причин пневмоторакса принадлежит торакоскопическому исследованию (50 % случаев). Этот метод результативнее, чем рентгенологический. Плевральная пункция является экстренной помощью независимо от причины, вызвавшей появление воздуха. При отсутствии положительного результата осуществляется дренирование плевральной полости. При показаниях проводится хирургическое лечение — пластика раневой поверхности легкого после резекции булл лоскутом париетальной плевры [4, 6, 7]. Правильно собранный анамнез отвечает на многие вопросы: с чего началось заболевание; с чем связано; какие инфекции перенес пациент; осложнения бронхопневмонией; отмечались ли приступы кашля, как часто пациент болел ОРВИ, отмечались ли приступы удушья; болел ли астмой или обструктивным бронхитом; не болел ли туберкулезом.
Приводим собственное наблюдение. Ребенок Н., 17 лет, находился в торакальном отделении областной клинической больницы г. Донецка в середине декабря 2012 г. по поводу локальной буллезной эмфиземы верхних долей легких, рецидивного (справа в 2010 г.), перемежающегося (слева в 2011 г.) пневмоторакса справа. Поступил в отделение с жалобами на боль в грудной клетке справа, одышку, затрудненное дыхание, чувство неполноты вдоха, кашель. До поступления за час отметил боль в грудной клетке среди полного здоровья. Обратился к хирургу, госпитализирован в ургентном порядке.
Из анамнеза жизни: ребенок от II беременности, протекавшей с угрозой прерывания в 5 недель, мать лежала на сохранении. Масса при рождении 3400 г, длина тела — 52 см, окружность головы — 35 см. Роды первые, срочные, осложненные преждевременным излиянием околоплодных вод и кефалогематомой. В 2 года перенес обструктивный бронхит. Ежегодно ОРВИ — до 3–4 раз в году, на диспансерном учете у аллерголога и лорврача по поводу респираторного аллергоза, аллергического ринита, хронического тонзиллита. В 7 лет — двусторонняя внебольничная верхнедолевая пневмония, в 11 и 12 лет — правосторонняя верхнедолевая и левосторонняя нижнедолевая пневмонии соответственно. В 9 лет — бронхиальная астма, выявлены бытовая и пыльцевая аллергия, поллиноз, диспластическая кардиопатия, килевидная деформация грудной клетки, кифосколиоз, пролапс митрального клапана (по данным ЭхоКГ).
Анамнез заболевания: ранее дважды находился на лечении в торакальном отделении. Первый раз госпитализирован в 14летнем возрасте по поводу правостороннего пневмоторакса, развившегося после физической нагрузки. Произведена операция: торакоцентез справа, торакоскопия, дренирование плевральной полости. В S1 выявлены мелкие буллы на фоне фиброза. Диагностирована локальная буллезная эмфизема верхней доли правого легкого, правосторонний пневмоторакс. Через год (в 15 лет) госпитализирован повторно по поводу перемежающегося пневмоторакса слева. На рентгенограмме органов грудной клетки слева в верхних отделах легочный рисунок не прослеживался, легкое поджато. Произведен торакоцентез, дренирование левой плевральной полости. На контрольной рентгенограмме: оба легких расправлены, жидкости и газа в плевральной полости не выявлено.
Последнее ухудшение наступило в декабре 2012 года, спустя 5 месяцев после предыдущего обострения повторилась внезапная острая боль в грудной клетке справа, появилась одышка. Госпитализирован повторно, произведена операция: видеоассистированная миниторакотомия справа, атипичная резекция верхней доли правого легкого с буллами, дренирование плевральной полости. На контрольной рентгенограмме: оба легких расправлены, жидкости, газов в плевральной полости нет. Справа апикально небольшие плевральные наслоения. В верхней доле правого легкого цепочки танталовых скрепок. В других отделах легких патологических теней нет. Сердце без изменений.
После выписки из хирургического отделения переведен в детское пульмонологическое отделение, где получал профилактическое лечение по поводу бронхиальной астмы, магне В6, диетотерапию. В настоящее время состояние пациента удовлетворительное, наблюдается хирургом и пульмонологом.
Таким образом, своевременная диагностика БЭЛ, адекватное хирургическое лечение развивающегося СП, плановое базисное и профилактическое лечение бронхиальной астмы у данного пациента позволили добиться стабильного улучшения состояния его здоровья, не допустить перехода БЭЛ из локальной в генерализованную форму и в итоге вернули пациента к полноценной жизни. Наряду с этим использование препаратов магния как средства патогенетического лечения синдрома дисплазии соединительной ткани может существенно улучшить качество жизни пациента во взрослом возрасте.
Bibliography1. Жындиров Б.К. Особенности клиники, диагностики и методов лечения буллезной болезни легких, осложненной спонтанным пневмотораксом: Автореф. дис… канд.мед.наук. — Бишкек, 2012. — 19 с.
2. Пахомов Г.Л., Исламбеков Э.С., Исмаилов Д.А. Тактика лечения неспецифического спонтанного пневмоторакса (методические рекомендации). — Ташкент, 2010. — 13 с.
3. Высоцкий А.Г. Буллезная эмфизема легких: этиология, патогенез, классификация // Новости медицины и фармации. Аллергология, пульмонология и иммунология. — 2008.
4. Гринцов Г.А. Роль одномоментных операций в лечении перемежающегося пневмоторакса // Вестник неотложной и восстановительной медицины. — 2008. — Т. 9, № 3. — С. 278280.
5. Курдюмова Н.В. Спонтанный пневмоторакс и дисплазия соединительной ткани. Фенотипические особенности пациентов // Вестник интенсивной терапии. — 2011. — № 3. — С. 5054.
6. Афендулов С.А. Хирургическая тактика при спонтанном пневмотораксе // Хирургия: Журнал им. Н.И. Пирогова. — 2010. — № 6. — С. 3135.
7. Крамаренко Ю.С. Видеоторакоскопия в лечении больных со спонтанным пневмотораксом // Укр. журнал малоінвазивної та ендоскопічної хірургії. — 2003. — Т. 7, № 4.
8. Бачерікова Ю.А. Мініінвазівні торакоскопічні методики при спонтанному пневмотораксі на тлі неспецифічних захворювань легень: Автореф. дис… канд.мед.наук. — Харків, 2009. — 19 с.
9. Аверкина Л.И. Особенности лечебной тактики при спонтанном пневмотораксе у больных с ХОЗЛ // Вестник хирургии им. И.И. Грекова. — 2010. — Т. 169, № 6. — С. 1721.
10. Лінчевський О.В. Діагностика та лікування спонтанного пневмотораксу: Автореф. дис… канд.мед.наук. — К., 2009. — 16 с.
11. Нестеренко З.В. Дисплазия соединительной ткани — медикосоциальный феномен ХХI века // Боль. Суставы. Позвоночник. — 2012. — № 1(05).
12. Нечаева Г.И., Викторова И.А., Громова О.А. и др. Дисплазии соединительной ткани у детей и подростков. Инновационные стационарсберегающие технологии диагностики и лечения в педиатрии. — М., 2010.
Лечение спонтанного пневмоторакса: Руководство Британского торакального общества по заболеваниям плевры, 2010 г.
Введение
Термин «пневмоторакс» был впервые введен Итардом, а затем Лаеннеком в 1803 и 1819 годах соответственно 1 и относится к воздуху в плевральной полости (т.е. между легким и грудной стенкой). В то время большинство случаев пневмоторакса было вторичным по отношению к туберкулезу, хотя некоторые из них были выявлены у здоровых пациентов («простой пневмоторакс»).Впоследствии эта классификация сохранилась, и первое современное описание пневмоторакса, встречающегося у здоровых людей (первичный спонтанный пневмоторакс, ПСП), было дано Кьоргаардом2 в 1932 году. Это серьезная глобальная проблема здравоохранения с зарегистрированной заболеваемостью 18–28 на 100 000 человек. случаев в год для мужчин и 1,2–6 / 100 000 для женщин3.
Вторичный пневмоторакс (SSP) связан с основным заболеванием легких, в отличие от PSP, хотя туберкулез больше не является наиболее распространенным основным заболеванием легких в развитом мире.Последствия пневмоторакса у пациентов с ранее существовавшим заболеванием легких значительно сильнее, и лечение потенциально более затруднено. Комбинированные показатели госпитализации для PSP и SSP в Великобритании составили 16,7 на 100 000 для мужчин и 5,8 на 100 000 для женщин, с соответствующими показателями смертности 1,26 на миллион и 0,62 на миллион в год в период с 1991 по 1995 год.4
С Что касается этиологии пневмоторакса, анатомические отклонения были продемонстрированы даже при отсутствии явного основного заболевания легких.Субплевральные пузыри и буллы обнаруживаются на верхушках легких при торакоскопии и компьютерной томографии почти в 90% случаев ПСП, 5 6 и, как полагают, играют определенную роль. Более поздние исследования аутофлуоресценции7 выявили пористость плевры в прилегающих областях, невидимую в белом свете. Малая обструкция дыхательных путей, опосредованная притоком воспалительных клеток, часто характеризует пневмоторакс и может проявляться в меньших дыхательных путях на более ранней стадии с «изменениями, подобными эмфиземе» (ELC) .8
Курение вовлечено в этот этиологический путь. пристрастие к курению связано с 12% риском развития пневмоторакса у здоровых курящих мужчин по сравнению с 0.1% среди некурящих.9 Пациенты с PSP, как правило, выше, чем пациенты из контрольной группы.10 11 Градиент отрицательного плеврального давления увеличивается от основания легкого к верхушке, так что альвеолы на верхушке легкого у высоких людей подвержены значительному более сильное растягивающее давление, чем у основания легкого, и эти векторы теоретически предрасполагают к развитию апикальных субплевральных пузырьков.12
Хотя это в некоторой степени противоречит здравому смыслу, нет никаких доказательств того, что существует связь между началом пневмоторакса и физическая активность, начало которой наиболее вероятно при малоподвижном образе жизни.13
Несмотря на очевидную взаимосвязь между курением и пневмотораксом, 80–86% молодых пациентов продолжают курить после первого эпизода PSP.14 Риск рецидива PSP достигает 54% в течение первых 4 лет, при наличии отдельных факторы риска, включая курение, рост и возраст> 60 лет.12 15 Факторы риска рецидива SSP включают возраст, легочный фиброз и эмфизему.15 16 Таким образом, следует направить усилия на прекращение курения после развития пневмоторакса.
Первые рекомендации Британского торакального общества (BTS) по лечению пневмоторакса были опубликованы в 1993 году.17 Более поздние исследования показали, что соблюдение этих рекомендаций улучшается, но остается неоптимальным только 20–40% среди не респираторного персонала и персонала отделения неотложной помощи. Было показано, что клинические руководства улучшают клиническую практику, 18 19 соблюдение связано со сложностью практических процедур20 и подкрепляется наличием доказательной базы.21 Вторая версия рекомендаций BTS была опубликована в 200322 г. и усилила тенденцию к более безопасным и безопасным процедурам. менее инвазивные стратегии ведения, а также подробные рекомендации по ряду связанных проблем и состояний.Он включал алгоритмы управления PSP и SSP, но исключал управление травмой. Это руководство направлено на консолидацию и обновление рекомендаций по пневмотораксу в свете последующих исследований и использования методологии SIGN. Это руководство не распространяется на травматический пневмоторакс.
SSP ассоциируется с более высокой заболеваемостью и смертностью, чем PSP. (D)
Особое внимание следует уделять отказу от курения, чтобы минимизировать риск рецидива.(D)
Пневмоторакс обычно не связан с физическими нагрузками. (D)
Клиническая оценка
Симптомы PSP могут быть минимальными или отсутствовать. Напротив, симптомы более выражены при SSP, даже если пневмоторакс относительно небольшой по размеру. (D)
Наличие одышки влияет на стратегию управления. (D)
Тяжелые симптомы и признаки респираторной недостаточности предполагают наличие напряженного пневмоторакса.(D)
Типичные симптомы боли в груди и одышки могут быть относительно незначительными или даже отсутствовать 23, поэтому требуется высокий индекс первоначального диагностического подозрения. Поэтому многие пациенты (особенно с ПСП) обращаются через несколько дней после появления симптомов.24 Чем дольше этот период времени, тем выше риск повторного расширения отека легких (RPO) .25 26 В целом, клинические симптомы связаны с симптомами. с SSP более серьезны, чем те, которые связаны с PSP, и у большинства пациентов с SSP возникает одышка, непропорциональная размеру пневмоторакса.27 28 Эти клинические проявления, таким образом, являются ненадежными индикаторами размера пневмоторакса.29 30 Когда тяжелые симптомы сопровождаются признаками кардиореспираторного дистресса, необходимо учитывать напряженный пневмоторакс.
Физические признаки пневмоторакса могут быть неуловимыми, но, как правило, включают уменьшение расширения легких, гиперрезонанс и снижение шума дыхания на стороне пневмоторакса. Дополнительные звуки, такие как «щелчки», иногда могут быть слышны в верхушке сердца.23 Наличие наблюдаемой одышки повлияло на последующее лечение в предыдущих руководствах.17 23 В сочетании с этими признаками цианоз, потоотделение, тяжелое тахипноэ, тахикардия и гипотония могут указывать на наличие напряженного пневмоторакса (см. Следующий раздел).
Измерения газов артериальной крови часто имеют отклонения от нормы у пациентов с пневмотораксом, при этом давление кислорода в артериальной крови (Pao 2 ) составляет <10,9 кПа у 75% пациентов, 31 но не требуются, если сатурация кислорода адекватна (> 92%). ) на воздухе помещения.Гипоксемия более выражена в случаях SSP31, Pao 2 составляет <7,5 кПа, вместе со степенью удержания углекислого газа в 16% случаев в большой серии.32 Тесты функции легких являются плохими предикторами наличия или размера. пневмотораксаx7 и, в любом случае, в этой ситуации лучше избегать тестов на форсирование выдоха.
Диагноз пневмоторакса обычно подтверждается методами визуализации (см. Ниже), которые также могут дать информацию о размере пневмоторакса, но клиническая оценка, вероятно, должна быть основным фактором, определяющим стратегию лечения, а также помогать в постановке первоначального диагноза.
Визуализация
Первичный диагноз
Для первичной диагностики пневмоторакса рекомендуются стандартные рентгеновские снимки грудной клетки в вертикальном положении на вдохе, а не снимки на выдохе. (A)
Широкое распространение цифровых изображений (PACS) требует осторожности при диагностике и дальнейших исследований, поскольку наличие небольшого пневмоторакса может быть не сразу очевидным. (D)
КТ сканирование рекомендуется для неопределенных или сложных случаев.(D)
Для диагностики и лечения пневмоторакса использовались следующие многочисленные методы визуализации:
Стандартный рентгеновский снимок грудной клетки в прямом положении.
Боковой рентген.
Экспираторные пленки.
Рентгеновские снимки в положении лежа на спине и в боковом положении в положении лежа.
Ультразвуковое сканирование.
Цифровая обработка изображений.
КТ сканирование.
Стандартный рентгеновский снимок грудной клетки в вертикальном положении
Это было основой клинического лечения первичного и вторичного пневмоторакса в течение многих лет, хотя, как известно, он имеет ограничения, такие как сложность точного количественного определения размера пневмоторакса.Основные технологические достижения последнего десятилетия привели к появлению цифровых изображений грудной клетки, так что обычные рентгеновские снимки грудной клетки больше не доступны в клинической практике в Великобритании или во многих других современных системах здравоохранения. Диагностический признак — смещение плевральной линии. Примерно в 50% случаев уровень воздух-жидкость виден в реберно-диафрагмальном углу, и иногда это единственная очевидная аномалия.33 Наличие буллезной болезни легких может привести к ошибочному диагнозу пневмоторакса с неблагоприятными последствиями для пациента. .Если существует неопределенность, крайне желательно КТ (см. Ниже).
Боковые рентгеновские снимки
Они могут предоставить дополнительную информацию, когда подозрение на пневмоторакс не подтверждается снимком грудной клетки 33, но, опять же, больше не используются в повседневной клинической практике.
Снимки выдоха
Считается, что они не дают дополнительных преимуществ при рутинной оценке пневмоторакса. 34–36
Рентгеновские снимки в положении лежа на спине и в боковом пролежне
Эти методы визуализации в основном используются для пациентов с травмами, которых нельзя безопасно перемещать .Они, как правило, менее чувствительны, чем рентгеновские лучи прямой передних конечностей для диагностики пневмоторакса37, 38 и были заменены ультразвуком или компьютерной томографией для пациентов, которые не могут принимать прямую позу.
Ультразвуковое сканирование
Специфические особенности ультразвукового сканирования — это диагностика пневмоторакса39, но на сегодняшний день основная ценность этого метода заключается в ведении пациентов с травмой в положении лежа на спине.40
Цифровая визуализация
Цифровая рентгенография (сообщение с архивами изображений) Systems, PACS) заменила обычную рентгенографию грудной клетки на пленке в большинстве больниц Великобритании за последние 5 лет, предоставив значительные преимущества, такие как увеличение, измерение и управление контрастом, простота передачи, хранения и воспроизведения.Относительно небольшое количество исследований касалось конкретного вопроса пневмоторакса и его диагностики, и они, как правило, были сосредоточены на экспертной диагностике (консультативными радиологами) и более разборчивых ведомственных (а не на базе палат) рабочих местах. Тем не менее, в ранних исследованиях были обнаружены некоторые трудности в диагностике пневмоторакса.41 42 С тех пор были технологические достижения, так что цифровые изображения теперь могут быть такими же надежными, как и более традиционные рентгеновские снимки грудной клетки в диагностике пневмоторакса, но были более недавних исследований, подтверждающих это, нет.Существуют различия между характеристиками (размер экрана, количество пикселей, контраст и люминесценция) и, следовательно, чувствительностью более дорогих ведомственных устройств и настольных и мобильных консолей, доступных в палате. В настоящее время рекомендуется, чтобы при принятии первичных диагностических решений на основе рентгеновского снимка грудной клетки была доступна диагностическая рабочая станция PACS для просмотра изображений.
Кроме того, цифровые изображения не поддаются измерению и расчетам размеров напрямую; требуется вспомогательная функция и использование курсора, но это почти наверняка более точно, чем использование линейки, и этому легко научиться.Клиницисты-неспециалисты и стажеры не всегда могут быть знакомы с этими функциями.
КТ-сканирование
Это можно считать «золотым стандартом» в обнаружении небольших пневмотораксов и оценке их размеров.43 Это также полезно при хирургической эмфиземе легких и буллезной болезни легких44 и для выявления неправильного размещения дренажа грудной клетки45 или дополнительная патология легких. Однако практические ограничения не позволяют использовать его в качестве исходного диагностического метода.
Размер пневмоторакса
При определении стратегии лечения размер пневмоторакса менее важен, чем степень клинического компромисса.(D)
Отличие «большого» от «малого» пневмоторакса по-прежнему заключается в наличии видимого края> 2 см между краем легкого и грудной стенкой (на уровне hilum) и легко измеряется с помощью системы PACS. (D)
Точные вычисления размера пневмоторакса лучше всего достигаются с помощью компьютерной томографии. (C)
Размер пневмоторакса плохо коррелирует с клиническими проявлениями.29 30 Клинические симптомы, связанные с вторичным пневмотораксом, в целом более серьезны, чем симптомы, связанные с первичным пневмотораксом, и могут казаться непропорциональными размеру пневмоторакса.27 28 Таким образом, клиническая оценка, вероятно, более важна, чем размер пневмоторакса. в определении стратегии управления.
Обычно для количественной оценки размера пневмоторакса использовали обычный рентген грудной клетки. Однако он имеет тенденцию занижать размер, потому что это двухмерное изображение, в то время как плевральная полость представляет собой трехмерную структуру.В рекомендациях BTS от 2003 года22 предлагалось использовать более точные методы расчета размеров, чем в их предшественнике в 1993 году, 15 с использованием функции куба двух простых измерений и того факта, что рентгенографический пневмоторакс 2 см приближается к 50% пневмотораксу по объему. Этот подход сопряжен с трудностями, в том числе с тем фактом, что некоторые пневмотораксы локализованы (а не однородны), поэтому коэффициенты измерения не могут быть применены. Нельзя предполагать, что форма легкого остается постоянной во время коллапса.46 Измерение отношения легкого к диаметру гемиторакса является точным и относительно простым с новыми системами PACS с помощью курсора, когда-то знакомого с дополнительными функциями PACS.
Выбор глубины 2 см — это компромисс между теоретическим риском травмы иглой при более мелком пневмотораксе и значительным объемом и продолжительностью времени до спонтанного разрешения большей глубины пневмоторакса.47 48 Предполагая симметричный рисунок легкого коллапс, тогда эта мера обычно проводится от грудной стенки до внешнего края легкого на уровне ворот (рис. 1).В рекомендациях США49 объем пневмоторакса оценивался путем измерения расстояния от верхушки легкого до купола, но этот метод имел тенденцию к завышению объема при локализованном верхушечном пневмотораксе. Бельгийские руководящие принципы использовали еще один метод для измерения размера пневмоторакса, и сравнения между различными методами показали плохое согласие50.
Рисунок 1Глубина пневмоторакса.
КТ-сканирование считается лучшим средством определения размера пневмоторакса51 и было откалибровано в эксперименте на модели легких.52
Варианты лечения пневмоторакса
Пациенты с ранее существовавшим заболеванием легких хуже переносят пневмоторакс, и во время постановки диагноза следует проводить различие между ПСП и ПСП для правильного ведения. (D)
Одышка указывает на необходимость активного вмешательства, а также поддерживающего лечения (включая кислород). (D)
Размер пневмоторакса определяет скорость разрешения и является относительным показателем для активного вмешательства.(D)
Первичный пневмоторакс возникает у пациентов без признаков другого основного заболевания легких. Хотя обычно присутствуют гистологические отклонения, связанные, в частности, с курением сигарет, они не проявляются симптомами или потерей функции. Напротив, вторичный пневмоторакс обычно возникает у пациентов с явным основным заболеванием легких, чаще всего с хронической обструктивной болезнью легких (ХОБЛ). Важно проводить это фундаментальное различие, поскольку пневмоторакс при ХОБЛ гораздо хуже переносится пациентом и имеет тенденцию менее благоприятно реагировать на вмешательства, а также потому, что основное заболевание легких требует дополнительно соответствующего лечения.Несколько серий показали снижение успешности аспирации у пациентов в возрасте> 50 лет, а также при хронических заболеваниях легких. Кажется вероятным, что у этих пожилых пациентов было нераспознанное основное заболевание легких. Этот возрастной критерий был включен в блок-схему для SSP в руководящих принципах 2003 г. и включен в новую блок-схему (рис. 2), что служит подсказкой для рассмотрения вероятности SSP. Другими критериями, важными в процессе принятия решения, являются наличие значительной одышки и размер пневмоторакса.Скорость разрешения / реабсорбции спонтанного пневмоторакса была оценена как от 1,25% до 2,2% от объема гемиторакса каждые 24 часа, 47 48 52 более высокая и более поздняя оценка52 была получена на основе компьютерной томографии. Таким образом, можно ожидать, что полный пневмоторакс спонтанно разрешится в течение 6 недель, а при наличии постоянной утечки воздуха, возможно, и дольше.
Рисунок 2Схема лечения спонтанного пневмоторакса.
Ведение PSP
Пациентам с PSP или SSP и значительной одышкой, связанной с пневмотораксом любого размера, необходимо проводить активное вмешательство.(A)
Грудные дренажи обычно требуются пациентам с напряженным или двусторонним пневмотораксом, которые должны быть госпитализированы. (D)
Наблюдение — это предпочтительный метод лечения маленьких PSP без значительной одышки. (B)
Отобранным бессимптомным пациентам с большим PSP можно вести только наблюдение. (A)
Пациентов с небольшим PSP без одышки следует рассматривать для выписки с ранним амбулаторным осмотром.Эти пациенты также должны получить четкую письменную рекомендацию вернуться в случае ухудшения одышки. (D)
И напряженный пневмоторакс, и двусторонний пневмоторакс являются потенциально опасными для жизни событиями, которые требуют введения дренажа грудной клетки. Поскольку такие пациенты обычно исключаются из исследований спонтанного пневмоторакса, нет никаких доказательств, на которых можно было бы основывать рекомендации, совет основывается на соображениях безопасности. Точно так же пациенты с сопутствующим большим плевральным выпотом (гидропневмоторакс) также были исключены из испытаний, но, вероятно, потребуют введения дренажа из грудной клетки и дальнейшего исследования (см. Отдельное руководство).Краткое изложение рекомендаций руководства показано на блок-схеме (рис. 2) с пояснительными деталями в тексте ниже.
Минимальные симптомы
Доказано, что консервативное лечение небольших пневмотораксов безопасно, 47 53 54 и пациентов, у которых нет одышки, можно лечить амбулаторно при условии, что они могут легко обратиться за медицинской помощью в случае ухудшения их симптомов. До 80% пневмотораксов, оцененных как менее 15%, не имеют постоянной утечки воздуха, а рецидивы у тех, кто лечится только под наблюдением, меньше, чем у тех, кто лечится дренированием грудной клетки.55 Рекомендуется раннее рассмотрение, чтобы гарантировать удовлетворительное решение и подкрепить рекомендации по образу жизни. Нет никаких доказательств того, что активное вмешательство уменьшает сопутствующую боль, что просто требует соответствующего обезболивания.
Симптоматический пневмоторакс
Само по себе наблюдение неприемлемо для пациентов с одышкой, которым требуется активное вмешательство (аспирация иглы или введение дренажа через грудную клетку). Выраженная одышка у пациента с небольшим PSP может предвещать напряженный пневмоторакс.55 Если пациент госпитализирован для наблюдения, там, где это возможно, следует дать дополнительный кислород с высокой скоростью потока.Помимо коррекции любой артериальной гипоксемии, 56 она приводит к четырехкратному увеличению скорости разрешения пневмоторакса57. При продолжающейся утечке воздуха механизмом может быть снижение парциального давления азота в плевральное пространство относительно кислорода, который легче всасывается. Кроме того, подобный эффект в плевральных капиллярах создает более благоприятный градиент резорбции.58
Аспирация иглой или дренаж грудной клетки?
Игла (14–16 G) аспирация (NA) так же эффективна, как и дренаж грудной клетки большого диаметра (> 20 F), и может быть связана с сокращением госпитализации и продолжительности пребывания в больнице.(A)
NA не следует повторять, если нет технических трудностей. (B)
После неудачного NA рекомендуется установка дренажа в грудную клетку малого диаметра (<14 F). (A)
Дренаж грудной клетки большого диаметра не требуется при пневмотораксе. (D)
Игольная аспирация (NA) была рекомендована в предыдущих руководящих принципах17 22 в качестве начального вмешательства для PSP на основе исследований59 60, показывающих эквивалентный успех введения дренажей грудной клетки большого диаметра, хотя это не было показано в другом исследовании.61 С тех пор дренирование грудной клетки по Сельдингеру (катетер поверх проволочного проводника) стало широко использоваться, и были опубликованы дальнейшие исследования. Рандомизированное контролируемое исследование в кувейтской популяции подтвердило эквивалентность между NA и дренированием грудной клетки (16 Fr), а также сокращение количества госпитализаций и продолжительности пребывания для NA.62 Меньшее исследование в Индии также подтвердило эквивалентность.63 Две недавние серии случаев сообщили об успешности НА 69% 64 и 50,5% 65. Несколько метаанализов66–68 были ограничены небольшим числом пациентов и исследований69–77, но подтверждают эквивалентность, при этом показатели успеха НА варьируются от 30% до 80% (см. доказательства таблица доступна на сайте BTS www.brit-thoracic.org.uk). В случае его проведения NA должна прекратиться после того, как будет всасано 2,5 л воздуха, дальнейшее повторное расширение маловероятно59 из-за вероятного наличия постоянной утечки воздуха.
Рекомендации, которые поощряют НА, не всегда соблюдаются78–82, и легкость введения дренажей с малым диаметром (<14 F) из грудной клетки Сельдингера может рассматриваться как более простой вариант лечения НА. Их успех был задокументирован в нескольких исследованиях 83–89, в которых использовались клапаны Геймлиха, облегчающие мобилизацию и амбулаторное лечение.Было показано, что дренаж грудной клетки малого диаметра имеет такой же процент успеха, как дренаж большого диаметра90, но при этом менее болезнен, 91 92 но не было рандомизированных контролируемых испытаний, сравнивающих их с NA. Более подробная информация об установке дренажа из грудной клетки и лечении, а также об осложнениях при установке дренажа из грудной клетки содержится в руководстве по плевральным процедурам. Катетерная аспирация была описана в последнем руководстве 22 с успехом до 59% и дальнейшим улучшением с добавлением клапанов Геймлиха и аспирации.93–95 Дренирование грудной клетки по Сельдингеру также позволило использовать «пошаговый» подход к ведению PSP, следуя заранее определенному пути, который завершается обращением к хирургическому специалисту при постоянной утечке воздуха.96
При выборе начального вмешательства для PSP следует принимать во внимание оператора. опыт и терпеливый выбор; NA менее болезненен, чем установка дренажа через грудную клетку60, но при неудаче примерно у одной трети пациентов потребуется вторая процедура. Другие национальные и согласованные рекомендации рекомендуют либо NA, либо установку дренажа грудной клетки малого диаметра, 97 или только установку дренажа грудной клетки.49 Мы считаем, что NA остается процедурой первого выбора в большинстве случаев. Повторная NA вряд ли будет успешной, если не возникнут технические трудности, такие как заблокированный или перекрученный катетер. Имеются некоторые ограниченные свидетельства того, что VATS является предпочтительной стратегией «спасения» после неудачного NA, 98 но это не обычная практика в настоящее время в Великобритании, где обычно используется установка дренажа грудной клетки малого диаметра. После успешного АН пациент может быть рассмотрен для выписки из больницы.
Всасывание
Всасывание не должно использоваться в повседневной жизни.(B)
Необходимо соблюдать осторожность из-за риска RPO. (B)
Рекомендуются системы всасывания большого объема с низким давлением. (C)
Постоянная утечка воздуха с неполным повторным расширением легкого или без него — обычная причина для рассмотрения возможности использования аспирации, хотя нет никаких доказательств того, что она используется в повседневной жизни. 99–101 Это произвольно. определяется как продолжающееся выделение пузырьков воздуха через дренаж грудной клетки через 48 часов на месте.Ретроспективный обзор 142 случаев пневмоторакса102 показал, что среднее время разрешения составляет 8 дней, что не связано с исходным размером пневмоторакса, но больше для SSP. Устойчивая утечка воздуха наблюдалась в 43 случаях, 30 из которых лечились отсасыванием. Теория, лежащая в основе роли всасывания, заключается в том, что воздух может удаляться из плевральной полости со скоростью, превышающей выход воздуха через разрыв во висцеральной плевре, и впоследствии способствовать заживлению путем наложения висцерального и париетального слоев плевры.Было высказано предположение, что оптимальное всасывание должно сопровождаться давлением от -10 до -20 см вод. Ст. 2 O (по сравнению с нормальным внутриплевральным давлением от -3,4 до -8 см вод. Ст. 2 O, в соответствии с дыхательным циклом), с возможность увеличения расхода воздуха до 15–20 л / мин.103 Другие формы всасывания не рекомендуются. Всасывание большого объема под высоким давлением может привести к похищению воздуха, гипоксемии или постоянным утечкам воздуха.104 Аналогичным образом следует избегать использования систем низкого объема с высоким давлением.105 Поэтому рекомендуются системы низкого давления большого объема, такие как насосы Вернона-Томпсона, или настенный отсос с адаптерами низкого давления.
Добавление отсасывания слишком рано после введения дренажа в грудную клетку может ускорить RPO, особенно в случае PSP, который мог присутствовать более нескольких дней, 106 и считается из-за дополнительного механического напряжения, приложенного к капиллярам. которые уже «протекают ».107 Клиническими проявлениями являются кашель, одышка и стеснение в груди после введения дренажа в грудную клетку.Заболеваемость может достигать 14% (выше у более молодых пациентов с большим PSP), хотя в большинстве случаев это не более чем радиологический феномен.106 Иногда отек легких проявляется в контралатеральном легком.108 Сообщалось о смертельных исходах. около 20% из 53 случаев в одной серии 108, поэтому следует проявлять осторожность в этой конкретной группе пациентов.
Направление к специалисту
Направление к терапевту необходимо в течение 24 часов после поступления.(C)
Комплексное управление дренажем лучше всего осуществлять в тех областях, где имеется опыт специалистов в области медицины и ухода за больными. (D)
Отсутствие повторного расширения пневмоторакса или постоянная утечка воздуха должны побуждать к раннему обращению к врачу-респиратору, предпочтительно в течение первых 24 часов. Таким пациентам может потребоваться длительный дренаж грудной клетки со сложным дренажом (отсасывание, изменение положения дренажа из грудной клетки) и взаимодействие с торакальными хирургами.Управление дренажем также лучше всего осуществляется медсестрами, обладающими специальными знаниями. Направление к хирургу обсуждается в следующем разделе.
Хирургическая эмфизема
Это хорошо известное осложнение дренажа грудной клетки.109 Как правило, оно имеет только косметическое значение, хотя и вызывает беспокойство у пациентов и их родственников и проходит самопроизвольно через несколько дней. Обычно это наблюдается в контексте неправильно расположенного, изогнутого, заблокированного или зажатого дренажа грудной клетки. Это также может произойти из-за дисбаланса между большой утечкой воздуха и дренажем из грудной клетки с относительно небольшим отверстием.Иногда острая обструкция дыхательных путей или компрессия грудной клетки могут приводить к респираторным нарушениям109, 110 и в этом случае использовались трахеостомия, декомпрессия кожного разреза и установка дренажей грудной клетки большого диаметра.109 В большинстве случаев лечение является консервативным.
Ведение SSP
Все пациенты с SSP должны быть госпитализированы как минимум на 24 часа и получать дополнительный кислород в соответствии с рекомендациями BTS по использованию кислорода. (D)
Большинству пациентов потребуется установка дренажа из грудной клетки малого диаметра.(B)
Всем пациентам потребуется раннее направление к терапевту. (D)
Людей с постоянной утечкой воздуха следует обсудить с торакальным хирургом через 48 часов. (B)
Как указывалось ранее, пациенты с меньшей вероятностью переносят SSP, чем PSP, из-за сопутствующего заболевания легких. Кроме того, менее вероятно, что утечка воздуха возникнет спонтанно, 111 112, так что большинству пациентов потребуется активное вмешательство.Показан кислород, 56 57 но осторожность требуется для пациентов с задержкой углекислого газа.113 Аспирация менее вероятна при SSP (см. Таблицу доказательств, доступную на веб-сайте BTS по адресу www.brit-thoracic.org.uk), но может быть рассматривается у симптомных пациентов с небольшим пневмотораксом, чтобы избежать введения дренажа грудной клетки. В противном случае рекомендуется установка дренажа из грудной клетки с малым отверстием; исследование, проведенное в программе самообучения 114, показало, что успехи аналогичны использованию дренажа большого диаметра. Всем пациентам с SSP рекомендуется раннее направление к терапевту как для лечения пневмоторакса, так и для лечения основного заболевания легких.Аналогичным образом, пациентов с постоянной утечкой воздуха следует обсудить с торакальным хирургом через 48 часов, 112 115, даже если многие из них вылезут спонтанно при консервативном лечении в течение 14 дней.111
Пациенты с SSP, но непригодные для операции
пациенты подвергаются повышенному риску постоянной утечки воздуха, но могут не подходить для хирургического вмешательства из-за тяжести основного заболевания легких или могут не желать продолжать лечение. Их оптимальное лечение является сложной задачей и требует тесного медицинского и хирургического взаимодействия.Медицинский плевродез является вариантом для таких пациентов, как и амбулаторное лечение с использованием клапана Геймлиха. 86
Выписка и последующее наблюдение
Пациентам следует рекомендовать вернуться в больницу, если развивается одышка. (D)
Все пациенты должны находиться под наблюдением респираторных врачей до полного разрешения. (D)
Следует избегать авиаперелетов до полного разрешения.(C)
Следует постоянно избегать дайвинга, за исключением случаев, когда пациенту была сделана двусторонняя хирургическая плеврэктомия и у него нормальная функция легких и послеоперационная компьютерная томография грудной клетки. (C)
Всем пациентам, выписанным после активного лечения или иным образом, следует дать устный и письменный совет немедленно вернуться в отделение неотложной помощи, если у них разовьется одышка. Рекомендуется, чтобы все пациенты находились под наблюдением терапевта-респираторного врача, чтобы гарантировать разрешение пневмоторакса, назначить оптимальную помощь при любом основном заболевании легких, объяснить риск рецидива и возможную последующую потребность в хирургическом вмешательстве, а также усилить рекомендации по образу жизни. по таким вопросам, как курение и авиаперелеты.Тем, у кого лечение ведется только под наблюдением или с помощью NA, следует рекомендовать вернуться на контрольный рентген грудной клетки через 2–4 недели для контроля разрешения. Пациентам с успешным повторным расширением легких до выписки из больницы также потребуется раннее обследование, поскольку рецидив может возникнуть относительно рано.
Поскольку нет никаких доказательств связи рецидива с физической нагрузкой, пациенту можно посоветовать вернуться к работе и возобновить нормальную физическую активность, как только исчезнут все симптомы, хотя разумно рекомендовать занятия спортом, предполагающим экстремальные нагрузки и физический контакт. следует отложить до полного разрешения.Пациенты должны быть осведомлены об опасности авиаперелетов при наличии в настоящее время закрытого пневмоторакса и им следует предостеречь от коммерческих полетов на большой высоте до тех пор, пока полное разрешение пневмоторакса не будет подтверждено рентгенологическим исследованием грудной клетки. Хотя нет никаких доказательств того, что авиаперелеты сами по себе вызывают рецидив пневмоторакса, последствия рецидива во время авиаперелета могут быть серьезными. Многие коммерческие авиалинии ранее произвольно рекомендовали 6-недельный интервал между событием пневмоторакса и авиаперелетом, но с тех пор это было изменено на период в 1 неделю после полного разрешения.В рекомендациях BTS по авиаперевозкам116 подчеркивается, что риск рецидива значительно снижается только через 1 год после первичного пневмоторакса, так что при отсутствии окончательной хирургической процедуры пациенты с SSP, в частности, могут решить минимизировать риск, отложив воздух. путешествовать соответственно. После пневмоторакса не следует постоянно заниматься дайвингом117, если только не была проведена очень надежная окончательная стратегия профилактики, такая как хирургическая плеврэктомия. В рекомендациях BTS по респираторным аспектам пригодности для дайвинга118 этот вопрос рассматривается более подробно.Курение влияет на риск рецидива, 12 15 поэтому рекомендуется прекратить курение. Беременность — это вопрос, который следует обсудить с более молодыми пациентками.
Медицинский химический плевродез
Химический плевродез может контролировать тяжелый или рецидивирующий пневмоторакс (A), но, поскольку хирургические варианты более эффективны, его следует использовать только в том случае, если пациент не желает или не может подвергнуться операции. (B)
Химический плевродез при пневмотораксе должен выполняться только специалистом по респираторным заболеваниям.(C)
Химический плевродез обычно рекомендуется врачами-респираторами, имеющими опыт торакоскопии. Закапывание веществ в плевральную полость должно приводить к асептическому воспалению с плотными спайками, ведущими в конечном итоге к плевральному симфизу. Наблюдается значительная частота рецидивов как первичного, так и вторичного пневмоторакса, 12 и усилия по уменьшению рецидивов путем введения различных склерозантов — через дренаж грудной клетки, торакоскопической хирургии с видеосвязью (VATS) или открытой хирургии — часто предпринимаются без четких руководящих принципов. направляют врачей в их использование.В подавляющем большинстве случаев профилактика рецидивирующего пневмоторакса должна проводиться хирургическим путем с использованием открытого доступа или подхода VATS, поскольку частота рецидивов после хирургического плевродеза с помощью торакотомии или VATS намного меньше, чем после простого медицинского плевродеза химическими препаратами, 32, 119, 120. 121, хотя прямые сравнительные исследования отсутствуют. Небольшое количество пациентов либо слишком слабы, либо не желают проходить какое-либо хирургическое лечение, и в этих ситуациях может потребоваться медицинский химический плевродез.
Многие склерозирующие агенты, подходящие для закапывания в плевральную полость, были изучены.32 119 122–125 Тетрациклин рекомендовался в качестве склерозирующей терапии первой линии как при первичном, так и при вторичном пневмотораксе, поскольку он оказался наиболее эффективным склерозирующим средством у животных. models.123 126 127 Однако в последнее время получить парентеральный тетрациклин для плевродеза стало труднее из-за проблем с производственным процессом. Миноциклин и доксициклин также оказались разумной альтернативой склерозирующим агентам на животных моделях.126 127
Частота рецидивов пневмоторакса является основным показателем успеха любых методов профилактики рецидивов. Хотя было показано, что тетрациклин снижает частоту ранних рецидивов, частота поздних рецидивов остается на уровне 10–20%, что является неприемлемо высоким по сравнению с хирургическими методами плевродеза.119 121 125 128 129 Тетрациклин может быть рекомендован для рецидивирующих первичных и вторичных пневмоторакс, когда хирургическое вмешательство невозможно, также можно использовать градуированный тальк на том основании, что он является наиболее эффективным средством при лечении злокачественного плеврального выпота, а также обычно используется для хирургического химического плевродеза.130–133 Существуют противоречивые данные о том, эффективен ли тетрациклин для лечения полностью развернутого пневмоторакса с постоянной утечкой воздуха.32 134 135 Крупнейшее из этих исследований, Veterans Administration Study, не поддерживало использование внутриплеврального тетрациклина для облегчить закрытие постоянной утечки воздуха.31 Macoviak и коллеги135 предполагают, что интраплевральный тетрациклин может облегчить закрытие постоянной утечки воздуха при условии, что легкое может быть расширено, так что может возникнуть симфиз.Точно так же существуют противоречивые данные о том, сокращает ли интраплевральный тетрациклин продолжительность пребывания в больнице с пневмотораксом.32 119 125
Дозировка интраплеврального тетрациклина требует уточнения. Almind119 обнаружил снижение частоты рецидивов в группе, получавшей тетрациклин в дозе 500 мг через дренаж грудной клетки, по сравнению с группой, получавшей только дренаж через зонд. Это снижение было незначительным. Исследование Veterans Administration Study [32], в котором использовался тетрациклин в дозе 1500 мг, показало значительное снижение частоты рецидивов пневмоторакса без значительных дополнительных осложнений.Таким образом, эта доза интраплеврального тетрациклина рекомендуется в качестве стандартной для медицинского плевродеза. В то время как боль чаще сообщалась в группе, получавшей тетрациклин в дозе 1500 мг, 32 других сообщили об отсутствии усиления боли при дозах 500 мг при условии адекватного обезболивания.119 Адекватное обезболивание может быть достигнуто с помощью внутриплеврального местного введения анестезия. Стандартные дозы (200 мг (20 мл) 1% лидокаина) значительно менее эффективны, чем большие дозы (250 мг (25 мл) 1% лидокаина), более высокие дозы, как было показано, увеличивают количество безболезненных эпизодов от От 10% до 70% без заметной токсичности.136
Химический плевродез с использованием градуированного талька — эффективная альтернатива тетрациклиновому плевродезу, но нет контролируемых испытаний, сравнивающих эти два метода лечения пневмоторакса. Проблема талькового плевродеза обсуждается в последующем разделе, посвященном хирургическому химическому плевродезу, поскольку большинство исследований с использованием талька связано с его использованием либо в торакоскопических, либо в открытых хирургических методах. Поскольку мы признаем, что химический плевродез уступает только хирургическому плевродезу, мы рекомендуем, чтобы химический плевродез проводился только терапевтами-респираторами или торакальными хирургами.
Направление к торакальным хирургам
Нет данных, на основании которых можно было бы определить идеальное время для торакального хирургического вмешательства в случае постоянной утечки воздуха. В прошлом широко пропагандировалась точка отсечения в 5 дней55, но она является произвольной. Chee et al. 111 показали, что 100% первичных пневмотораксов с постоянной утечкой воздуха в течение> 7 дней и лечением дренированием через трубку прошли через 14 дней. Кроме того, 79% пациентов с вторичным пневмотораксом и постоянной утечкой воздуха разрешились к 14 дням, без летального исхода ни в одной из групп.Однако хирургическое вмешательство имеет низкую заболеваемость128 129 137–140, а частота послеоперационных рецидивов низкая. 128 129 Хирургическое вмешательство уже через 3 дня имеет сторонников, 141 142, но нет доказательств того, что вмешательство до 5 дней необходимо для PSP. Каждый случай следует оценивать индивидуально с учетом его достоинств. Пациентов с пневмотораксом должен вести терапевт-респиратор, и заключение торакального хирурга часто составляет раннюю часть плана лечения.
Допустимые показания к хирургическому вмешательству должны быть следующими:
Второй ипсилатеральный пневмоторакс.
Первый контралатеральный пневмоторакс.
Синхронный двусторонний спонтанный пневмоторакс.
Устойчивая утечка воздуха (несмотря на 5–7 дней дренирования плевральной дренажной системы) или невозможность повторного расширения легких.
Спонтанный гемоторакс.143 144
Профессии в группе риска (например, пилоты, водолазы) .111 138 145–147
Беременность.
Все чаще выбор пациента будет играть роль в принятии решений, и даже те, у кого нет повышенного риска в случае пневмоторакса из-за своей профессии, могут выбрать хирургическое лечение после своего первого пневмоторакса, 148 149 взвешивая преимущества снижения риска рецидива по сравнению с хронической болью 150, парестезии151 или возможности увеличения затрат.152
Хирургические стратегии: открытая торакотомия или VATS?
Открытая торакотомия и плеврэктомия остаются процедурой с самой низкой частотой рецидивов (приблизительно 1%) при тяжелом или рецидивирующем пневмотораксе. (A)
Видеоассистированная торакоскопическая хирургия (VATS) с плеврэктомией и ссадинами плевры переносится лучше, но имеет более высокую частоту рецидивов примерно 5%. (A)
Хирургическое лечение стойкой утечки воздуха из пневмоторакса и предотвращение рецидивов преследуют две основные цели.Первой целью является резекция любых видимых пузырей или пузырьков на висцеральной плевре, а также стирание эмфиземоподобных изменений9 или плевральных пористостей под поверхностью висцеральной плевры.8 Вторая цель — создать симфиз между двумя противоположными поверхностями плевры, как дополнительное средство предотвращения рецидивов. В прошлом хирурги, как правило, отдавали предпочтение хирургическому плевродезу с ссадиной плевры, в то время как другие подчеркивали важность различных степеней плеврэктомии для предотвращения рецидивов.137 153 154 Хотя плеврэктомия может иметь небольшие преимущества перед ссадиной плевры, 137 часто используется комбинация этих двух методов.155–158 К сожалению, в этой области мало хороших сравнительных исследований методом случай-контроль.128 129 В последние годы, Менее инвазивные процедуры с использованием VATS стали более популярными с меньшей заболеваемостью, хотя и с несколько более высокой частотой рецидивов.
Открытая торакотомия с ссадиной плевры была оригинальным хирургическим методом лечения пневмоторакса, описанным Тайсоном и Крэндаллом в 1941 году.159 В 1956 году Gaensler представил париетальную плеврэктомию при рецидивирующем пневмотораксе, стимулируя плевральный симфиз за счет спаек между висцеральной плеврой и грудной стенкой.153 Считается также важным закрытие протекающей висцеральной плевры прямым прижиганием и лигированием или наложением швов связанных пузырьков147. Хотя открытая торакотомия имеет самую низкую частоту рецидивов пневмоторакса, существуют также меньшие хирургические процедуры с сопоставимой частотой рецидивов, но меньшей заболеваемостью.160 К ним относятся трансаксиллярная миниторакотомия с использованием разреза 5-6 см в подмышечной области с апикальной плеврэктомией и абразией плевры, применяемой при 1970-е годы.161 Открытая торакотомия обычно выполняется с ограниченным заднебоковым доступом и вентиляцией одного легкого. Это позволяет выполнить париетальную плеврэктомию с иссечением, сшиванием скобами или перевязкой видимых булл и ссадины плевры.162 Изолированная вентиляция легких во время открытой торакотомии упрощает визуализацию висцеральной плевры, чем во время процедуры VATS.163–165 Мета-анализ исследований, сравнивающих открытые с ограниченные процедуры или процедуры VATS128 129 показали более низкую частоту рецидивов (приблизительно 1%) при открытых процедурах, но большую кровопотерю, большую послеоперационную боль166 и более длительное пребывание в больнице.167 Некоторые нерандомизированные исследования не обнаружили существенных различий. 168. 169 Сложный метаанализ трех ретроспективных исследований и одного проспективного исследования, сравнивающего стоимость открытой торакотомии и VATS (не только для пневмоторакса), пришел к выводу, что общие экономические затраты на VATS были ниже 170, и его можно проводить без общей анестезии.149 В этой области необходимы проспективные рандомизированные исследования более высокого качества. Некоторые авторы предполагают, что VATS имеет значительное преимущество перед открытой торакотомией, включая более короткое послеоперационное пребывание в больнице, 145 162 167 171–173 уменьшение послеоперационной боли160 162 166 174 175 и улучшение газообмена в легких после операции, 176 хотя не все испытания подтвердили более короткое пребывание в больнице с НДС.169 177
Большая часть литературы содержит разнородные сравнения между PSP и SSP, но самый последний «клинический итог» 129 делает вывод, что плеврэктомия по VATS сравнима с открытой плеврэктомией, при этом несколько рандомизированных контролируемых исследований показали сокращение продолжительности пребывания в больнице, обезболивающее. Потребность и послеоперационная легочная дисфункция. Очевидно, это необходимо сопоставить с небольшим увеличением частоты рецидивов при использовании менее инвазивного доступа. 128
Хирургический химический плевродез
С появлением VATS для восстановления пневмоторакса и профилактики рецидивов использование хирургического химического плевродеза значительно сократилось.Предыдущие отчеты показали, что тальк может успешно обеспечить плевродез в 85–90% случаев, аналогично другим торакоскопическим методам лечения осложненного пневмоторакса.121 145 171 178 179 Мета-анализ успешности талькового плевродеза при лечении пневмоторакса показывает: общий показатель успешности составляет 91% .178 Тальк более высокого качества предпочтительнее тетрациклина, который в настоящее время менее доступен и связан с гораздо более высокой частотой рецидивов.120 Большая часть литературы, касающейся использования талька для достижения плевродеза, относится к его использованию в контроле. злокачественных плевральных выпотов, хотя тальк успешно применяется при вторичном пневмотораксе.180 На основе систематического обзора неконтролируемых исследований 5 г интраплеврального талька с помощью VATS обеспечивает эффективность 87% .178
После использования талька был описан респираторный дистресс-синдром у взрослых. Вероятно, это связано с размером частиц талька181 и маловероятно при использовании градуированного талька.182 183 Если тальк правильно стерилизован, частота возникновения эмпиемы очень низка.178 184 185 По-видимому, нет разницы между Плевродез талька и тальковой суспензии.Появление успешной и хорошо переносимой хирургии VATS приведет к сокращению использования хирургического химического плевродеза с тальком. Для тех пациентов, которые не хотят или слишком плохо себя чувствуют, чтобы проходить процедуру VATS, предпочтительным вариантом будет медицинский плевродез с тальком через дренаж грудной клетки.
Напряженный пневмоторакс
Напряженный пневмоторакс — это неотложная медицинская помощь, требующая повышенного внимания в определенных клинических ситуациях. (D)
Лечение кислородом и экстренной декомпрессией иглой.(D)
Стандартная канюля может быть недостаточно длинной при использовании во втором межреберье. (D)
Это неотложная медицинская помощь, которая может возникнуть в различных клинических ситуациях, поэтому для постановки правильного диагноза и эффективного лечения требуется высокий индекс подозрительности. Наиболее частые ситуации показаны в поле 1, хотя список не включает все возможные варианты. Он возникает в результате развития односторонней клапанной системы в месте разрыва плевральной мембраны, позволяющей воздуху попадать в плевральную полость во время вдоха, но предотвращающей выход воздуха во время выдоха с последующим повышением внутриплеврального давления. такое, что оно превышает атмосферное давление на протяжении большей части дыхательного цикла.В результате нарушение венозного возврата и снижение сердечного выброса приводят к типичным признакам гипоксемии и гемодинамическим нарушениям.186 187
Вставка 1 Типичные клинические ситуации, когда возникает напряженный пневмоторакс
Пациенты, находящиеся на ИВЛ в ОИТ.
Больные с травмами.
Пациенты реанимации (СЛР).
Заболевания легких, особенно острые проявления астмы и хронической обструктивной болезни легких.
Заблокированные, зажатые или смещенные дренажи грудной клетки.
Пациенты, получающие неинвазивную вентиляцию легких (НИВ).
Другая группа, например пациенты, проходящие курс лечения гипербарическим кислородом.
В недавнем обзоре188 были подчеркнуты важные различия между проявлениями у пациентов, находящихся на ИВЛ, и без ИВЛ, у которых это обычно наблюдается после травмы или реанимации. Первая группа связана с равномерно быстрым проявлением гипотонии, тахикардии, падением сатурации кислорода и сердечного выброса, повышенным инфляционным давлением и остановкой сердца.Это часто упускается из виду в отделении интенсивной терапии37, а также может произойти после назальной неинвазивной вентиляции (НИВ). Последняя группа бодрствующих пациентов демонстрирует большую вариабельность представлений, которые обычно прогрессируют с более медленной декомпенсацией. Тахипноэ, тахикардия и гипоксемия в конечном итоге приводят к остановке дыхания. Помимо этих общих физических признаков, наиболее частым латерализующим признаком, обнаруженным в обзоре 18 сообщений о клинических случаях188, было уменьшение поступления воздуха (50–75%), при этом признаки девиации трахеи, гиперэкспансии, гипомобильности и гиперрезонанса присутствовали только в меньшинстве.
Ни в одной из этих групп визуализация не особенно полезна; обычно недостаточно времени для получения рентгеновского снимка грудной клетки, и, даже если он доступен, размер пневмоторакса или наличие смещения средостения плохо коррелируют с наличием напряжения внутри пневмоторакса. Однако при наличии времени рентген грудной клетки может подтвердить наличие пневмоторакса (если нет уверенности) и правильной стороны.
Лечение заключается в использовании кислорода с высокой концентрацией и экстренной декомпрессии иглой, канюля обычно вводится во второе переднее межреберье по срединно-ключичной линии.Мгновенный выход воздуха в течение большей части дыхательного цикла является важным подтверждением диагноза и правильной латерализации. Стандартная канюля калибра 14 (4,5 см) может быть недостаточно длинной для проникновения через париетальную плевру, однако до одной трети пациентов имеют толщину стенки грудной клетки> 5 см во втором промежутке.189 Стенка грудной клетки может быть меньше глубоко в четвертом или пятом промежутке, и это может обеспечить альтернативное место для декомпрессии, или может потребоваться установка дренажа из грудной клетки, если первоначальная неудача лечения неэффективна.В любом случае грудной дренаж должен быть вставлен сразу после декомпрессии иглы, а канюля должна оставаться на месте до тех пор, пока в подводной системе уплотнения не будет подтверждено пузырение, чтобы подтвердить правильную функцию грудного дренажа.186
Пневмоторакс и беременность
Пневмоторакс рецидивы чаще встречаются во время беременности, представляют опасность для матери и плода и требуют тесного сотрудничества между врачами-терапевтами, акушерами и торакальными хирургами. (C)
Современные и менее инвазивные стратегии простого наблюдения и аспирации обычно эффективны во время беременности, с плановыми вспомогательными родами и регионарной анестезией в срок или в ближайшем будущем.(C)
Корректирующая хирургическая процедура (VATS) должна быть рассмотрена после родов. (D)
Хотя у женщин ПСП встречается реже, чем у мужчин, возникновение ПСП у женщин детородного возраста не является чем-то необычным. По-видимому, существует повышенный риск рецидива во время беременности и родов, 190 с потенциальным риском для матери и плода. Более ранняя литература в основном состоит из описаний клинических случаев и описаний различных и относительно инвазивных стратегий лечения, таких как длительный дренаж плевральной дренажной трубки во время родов, торакотомия во время родов, преждевременная индукция родов или кесарево сечение.В более поздних сериях случаев и обзоре литературы191 рекомендовано использование более современных консервативных методов ведения, для которых в настоящее время получены благоприятные результаты. Пневмоторакс, возникающий во время беременности, можно лечить простым наблюдением, если у матери нет одышки, нет дистресса плода и пневмоторакс небольшой (<2 см). В противном случае может быть выполнена аспирация, введение дренажа в грудную клетку зарезервировано для пациентов с постоянной утечкой воздуха.
Очень важно тесное сотрудничество между врачом-респиратором, акушером и торакальным хирургом.Чтобы избежать самопроизвольных родов или кесарева сечения, оба из которых были связаны с повышенным риском рецидива, наиболее безопасным подходом обычно будет выборное вспомогательное родоразрешение (щипцы или удаление вентуса) в ближайшем или ближайшем будущем с регионарной (эпидуральной) анестезией. При родоразрешении с помощью щипцов требуется меньше материнских усилий, что, следовательно, предпочтительнее. Если кесарево сечение неизбежно по акушерским соображениям, то спинальная анестезия предпочтительнее общей анестезии.
Из-за риска рецидива при последующих беременностях после выздоровления следует рассмотреть возможность минимально инвазивной хирургической процедуры VATS. Сообщалось об успешных беременностях и самопроизвольных родах без рецидива пневмоторакса после процедуры VATS.191
Катамениальный пневмоторакс
Менструальный пневмоторакс у женщин с пневмотораксом не диагностируется. (C)
Сочетание хирургического вмешательства и гормональных манипуляций требует сотрудничества с торакальными хирургами и гинекологами.(D)
Катамениал — это термин, происходящий от греческого значения «ежемесячно». Типичное сочетание боли в груди, одышки и кровохарканья, возникающее в течение 72 часов до или после менструации у молодых женщин, считается относительно редким. В медицинской литературе описано около 250 случаев, 192 но, вероятно, о большинстве случаев не сообщается. Большинство этих ссылок относятся к отдельным историям болезни или небольшим сериям. Сопутствующий пневмоторакс обычно правосторонний и имеет повышенную тенденцию к рецидивам, совпадающим с менструальным циклом.Во многих случаях имеются признаки тазового эндометриоза. Хотя этиология полностью не выяснена, осмотр поверхности плевральной диафрагмы при торакоскопии часто выявляет дефекты (называемые фенестрациями), а также небольшие отложения на эндометрии. Эти отложения также были замечены на висцеральной плевральной поверхности. Однако среди женщин, подвергающихся рутинному хирургическому лечению рецидивирующего пневмоторакса, менструальный пневмоторакс диагностируется у 25% .193 Таким образом, диагноз его может быть относительно заниженным.
Экстрагенитальный или «эктопический» эндометриоз — это редкое заболевание, которое может поражать практически любую систему органов и ткань в организме, причем грудная клетка является наиболее частым экстрагенитальным локализацией. Синдром торакального эндометриоза (TES) включает менструальный пневмоторакс, менструальный гемоторакс, менструальное кровохарканье и узелки в легких (пурпурного или коричневого цвета). Наиболее распространенной теорией, объясняющей феномен менструального пневмоторакса, является аспирация воздуха из брюшной полости и половых путей через диафрагмальные отверстия, но появление отложений эндометриоза на висцеральной плевральной поверхности повышает вероятность эрозии висцеральной плевры. альтернативный механизм.Считается, что кровохарканье возникает в результате внутрилегочных отложений эндометриоза, причем механизм, с помощью которого ткань эндометрия достигает легких, недостаточно изучен.
Стратегии лечения можно разделить на торакальные хирургические методы и гормональные манипуляции, хотя в прошлом применялись тотальная абдоминальная гистерэктомия и двусторонняя сальпиногистерэктомия. Техники торакальной хирургии были разнообразны и включают диафрагмальную резекцию или складки фенестрации, наблюдаемые при торакоскопии, наложение сетки или пластыря поверх этих фенестров, электрокоагуляцию эндометриозных отложений и плевродез.Эта вариабельность отражает общую неэффективность одного только хирургического вмешательства, частота рецидивов составляет до 30%. Документально подтверждена частота рецидивов. 194 При сочетании с аналогами гонадотропин-рилизинг-гормона наблюдается аменорея, но рецидивов удалось избежать с последующим периодом наблюдения до 4 лет. 195 Успешное ведение пациентов требует тесного сотрудничества между врачами-респираторами, торакальными хирургами и гинекологами.
Пневмоторакс и СПИД
В течение последних 20 лет наблюдалась сильная связь между ВИЧ-инфекцией и пневмотораксом.Исторически сложилось так, что до 5% больных СПИДом заболевали пневмотораксом196–198, и до 25% спонтанных пневмотораксов возникали у ВИЧ-инфицированных пациентов в больших городских условиях, где они были широко распространены27 28 199 Pneumocystis jiroveci (PJP) — ранее известно as Pneumocystis carinii (PCP) — инфекция считается основным этиологическим фактором этой ассоциации из-за тяжелой формы некротизирующего альвеолита, при которой субплевральная легочная паренхима замещается некротическими тонкостенными кистами и пневматоцеле.200 201 Введение распыленного пентамидина также было предложено в качестве возможного независимого фактора риска.196 Использование системных кортикостероидов также может способствовать заболеваемости у таких пациентов.202
Из-за гистопатологии, описанной выше, пневмоторакс, вызванный PJP, имеет склонность к более длительным утечкам воздуха, неудачам лечения, рецидивам и более высокой госпитальной летальности.203 У 40% этих пациентов может развиться двусторонний пневмоторакс. Было замечено, что неэффективность лечения коррелирует со степенью иммуносупрессии, что отражается в количестве CD4.203 Ввиду этих особенностей были разработаны стратегии ведения, которые включают раннее и агрессивное вмешательство, включая дренаж трубки, плевродез и хирургические методы, такие как плеврэктомия. 197, 199 .
За последние 5 лет, со времени выхода последних руководств по BTS, глобальный спектр ВИЧ-инфекции значительно изменился в результате более широкого использования как антиретровирусной терапии, так и профилактики PJP.В то время как бремя болезней остается очень высоким в слаборазвитых странах, прогноз для таких пациентов в западных обществах значительно улучшился, 206 где эта комбинация сейчас встречается гораздо реже. Поскольку в настоящее время ВИЧ становится все более хроническим заболеванием, связанным с высокой распространенностью курения и, следовательно, ХОБЛ, пневмотораксы могут стать более значительными, когда они возникают.
Однако смертность пациентов, которым требуется интенсивная терапия по поводу PJP при ВИЧ-инфекции, остается высокой, особенно когда пневмоторакс возникает во время вентиляции.Хотя антиретровирусная терапия, начатая до или во время госпитализации, может улучшить исход, 207 необходимо учитывать потенциальный риск «синдрома восстановления иммунитета».
Пневмоторакс и муковисцидоз
Развитие пневмоторакса у пациента с муковисцидозом требует раннего и агрессивного лечения с ранним обращением к хирургическому специалисту. (C)
Плевральные процедуры, включая плевродез, не оказывают значительного неблагоприятного воздействия на исход последующей трансплантации легких.(D)
Несмотря на то, что долгосрочная выживаемость значительно улучшилась, спонтанный пневмоторакс остается частым осложнением муковисцидоза, возникающим у 0,64% пациентов в год и у 3,4% пациентов в целом.208 Он чаще встречается у пожилых людей. Пациенты с более поздними стадиями заболевания легких и связаны с плохим прогнозом, средняя выживаемость составляет 30 месяцев.209 Контралатеральные пневмотораксы встречаются почти у 40% пациентов.209, 210 Также наблюдается повышенная заболеваемость с увеличением количества госпитализаций и измеримых показателей. снижение функции легких.208 В то время как небольшой пневмоторакс без симптомов может наблюдаться или аспирироваться, более крупные пневмотораксы требуют дренажа грудной клетки. Спавшееся легкое может быть жестким и ассоциироваться с задержкой мокроты, поэтому для повторного расширения требуется больше времени. В это время необходимы другие общие меры, такие как соответствующее лечение антибиотиками.
Одно только дренирование через грудную трубку имеет частоту рецидивов 50%, но такие вмешательства, как плеврэктомия, ссадина плевры и плевродез, имеют более низкую частоту. 211–213 Частичная плеврэктомия с вероятностью успеха 95% и незначительным снижением легочной функции является обычно считается методом выбора у пациентов с муковисцидозом и рецидивирующим пневмотораксом, которым можно провести хирургическое вмешательство.209 Для тех, кто не подходит для операции и у которых повторное расширение может занять несколько недель с дренажом и отсасыванием грудной клетки, плевродез предлагает альтернативную стратегию.209 Это считалось относительным противопоказанием для более поздней трансплантации из-за необходимости более длительная процедура трансплантации и чрезмерное кровотечение. 214 Более недавнее исследование 215 пришло к выводу, что предыдущие плевральные процедуры не должны рассматриваться как противопоказание для трансплантации, поскольку они не оказали значительного влияния на хирургический результат, хотя наблюдались более плотные плевральные спайки, чем в контрольной популяции.
Ятрогенный пневмоторакс
Было показано, что ятрогенный пневмоторакс встречается даже чаще, чем спонтанный пневмоторакс, в нескольких крупных обзорах, 216 217 наиболее частыми причинами являются трансторакальная пункционная аспирация (24%), пункция подключичного сосуда (22%), торакоцентез (22). %), биопсии плевры (8%) и ИВЛ (7%). 218 Это также осложнение трансбронхиальной биопсии. Во время трансторакальной пункционной пункции двумя основными факторами риска являются глубина поражения и наличие ХОБЛ.219 Крупное ретроспективное исследование в США показало, что частота 2,68% среди пациентов, перенесших торакоцентез 220, пока не найдена. Расположение пациента таким образом, чтобы процедура проводилась в зависимой зоне, не имело положительного эффекта.221 За исключением ятрогенного пенумоторакса, который возникает в отделениях интенсивной терапии, лечение кажется относительно простым с меньшей вероятностью рецидива (лежащие в основе факторы риска SP обычно не присутствует).Большинство разрешается спонтанно только наблюдением. Если требуется вмешательство, простая аспирация показала свою эффективность у 89% пациентов.94 В остальных случаях требуется дренаж грудной клетки, что более вероятно у пациентов с ХОБЛ.222
В отделении интенсивной терапии ятрогенный пневмоторакс — это заболевание. опасное для жизни осложнение, которое может наблюдаться у 3% пациентов.223 Тем, кто получает вентиляцию с положительным давлением, требуется установка дренажа грудной клетки, поскольку положительное давление поддерживает утечку воздуха.224
Заключительные замечания
Эти рекомендации по пневмотораксу отличаются от последних (2003 г.) рекомендаций BTS тем, что они были составлены в соответствии с методологией SIGN и, следовательно, потребовали тщательного анализа текущих основополагающих данных. К сожалению, существует относительно мало адекватных исследований, посвященных основным областям неопределенности, и мало дополнений к базе знаний за последние 7 лет. Тем не менее, некоторые тонкие изменения на практике произошли.Они включены вместе с освещением некоторых дополнительных актуальных тем, таких как менструальный пневмоторакс и проблема пневмоторакса во время беременности. Алгоритм лечения теперь проиллюстрирован на единой блок-схеме как для PSP, так и для SSP, и при этом немного меньше внимания уделяется размеру пневмоторакса и больше — клиническим особенностям. Тем не менее, тенденция к более консервативному лечению сохраняется, с наблюдением за многими пациентами с PSP, аспирацией для остальных и дренированием грудной клетки малого диаметра для устойчивых утечек воздуха.Визуализация пневмоторакса претерпела серьезные изменения в связи с появлением технологии PACS, и теперь описываются последствия этого. Хирургическая практика также получила развитие благодаря повсеместному внедрению менее инвазивных процедур (VATS), чем открытых торакотомий. Несмотря на то, что проблема лечения пневмоторакса у пациентов с муковисцидозом остается, после введения антиретровирусной терапии и профилактической терапии PJP, по крайней мере в странах с развитой системой здравоохранения, произошло значительное сокращение пневмоторакса у пациентов с ВИЧ.Есть надежда, что эти рекомендации основаны на своих предшественниках и приведут к улучшению ухода за пациентами с пневмотораксом, а также на то, что они информируют и поддерживают лечащих их врачей.
Лечение спонтанного пневмоторакса: современное состояние
Реферат
Спонтанный пневмоторакс остается серьезной проблемой для здоровья. Однако со временем произошли улучшения в патогенезе, диагностических процедурах и как медикаментозных, так и хирургических подходах к лечению.
Благодаря более совершенным методам визуализации теперь ясно, что в случае спонтанного пневмоторакса почти нет нормальной висцеральной плевры, и что пузырьки и пузыри не всегда являются причиной пневмоторакса. В первых эпизодах первичного спонтанного пневмоторакса наблюдение и простая аспирация являются признанными методами терапии первой линии, что доказано рандомизированными контролируемыми исследованиями. Аспирацию следует лучше продвигать в повседневной медицинской практике. В случае рецидивирующего или стойкого пневмоторакса простое нанесение талька при торакоскопии оказалось безопасным, рентабельным и не более болезненным, чем консервативное лечение с использованием дренажной трубки.Есть также новые экспериментальные данные, показывающие, что тальк, используемый в Европе, не вызывает серьезных побочных эффектов и в настоящее время является лучшим доступным средством для склерозирования плевры.
В качестве альтернативы, хирургические методы значительно улучшились и теперь стали менее инвазивными, особенно благодаря развитию торакоскопической хирургии с использованием видео. Исследования показывают, что торакоскопическая хирургия с помощью видео может быть более рентабельной, чем дренаж плевральной дренажной трубки при спонтанном пневмотораксе, требующей дренирования плевральной дренажной трубки, хотя она дороже простой торакоскопии и требует общей анестезии, интубации двухпросветной трубки и вентиляции.
Даны рекомендации по лечению пневмоторакса. При вторичном или осложненном первичном пневмотораксе, , т.е. , рецидивирующем или стойком пневмотораксе, следует предложить некоторое диффузное лечение висцеральной плевры либо с помощью талька при торакоскопии, либо с помощью торакоскопической хирургии с использованием видео. Более того, все эти новые методы должны быть лучше стандартизированы, чтобы можно было проводить сравнения в рандомизированных контролируемых исследованиях.
Спонтанный пневмоторакс (СП) определяется как наличие воздуха в плевральной полости.Он делится на первичный SP (PSP) и вторичный SP (SSP). SSP связан с основными заболеваниями легких, такими как муковисцидоз, хроническая обструктивная болезнь легких (ХОБЛ), СПИД, и т. Д. Таким образом, существуют две отдельные эпидемиологические формы SP, PSP, с пиком заболеваемости среди молодых людей, и SSP. , с пиком заболеваемости среди лиц старше 55 лет 1.
Травматический пневмоторакс (случайный или ятрогенный) 2, 3 здесь не обсуждается.
PSP остается серьезной проблемой для здоровья, с ежегодной заболеваемостью 18–28 на 100 000 населения среди мужчин и 1.2–6,0 на 100 000 населения у женщин 4. Годовая частота встречаемости SSP составляет 6,3 на 100 000 населения у мужчин и 2,0 на 100 000 населения у женщин 5, при этом заболеваемость изменяется во времени, 90 449 например, во время связанной со СПИДом Pneumocystis carinii пневмонии 1980-х и 1990-х годов 6, 7. Смертность SP может быть высокой, особенно у пожилых людей и пациентов с SSP 6. Течение SP остается непредсказуемым, с частотой рецидивов в диапазоне 25–54% 5, 8.
Столь высокая частота рецидивов стимулировала развитие множества различных терапевтических подходов (таблица 1⇓), включая медицинскую торакоскопию, простой и минимально инвазивный метод, а также торакотомию и торакоскопическую хирургию с видеосвязью (VATS), для которых требуется три или четыре операционных зала. точки входа и вспомогательная вентиляция с интубацией двухпросветной трубки.Однако для предотвращения рецидивов пневмоторакса все эти методы обычно сочетают в себе какой-либо плевродез, химический или механический, с абразией плевры или плеврэктомией 9, 10.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ И ПАТОФИЗИОЛОГИЯ
Первичный спонтанный пневмоторакс
Диагноз PSP обычно ставится с помощью рентгенографии грудной клетки в случае внезапной боли в груди и / или одышки. Вопреки распространенному мнению 4, физическая активность не играет роли в PSP.Рентгенография грудной клетки на выдохе не улучшает диагноз 11. В отличие от SSP, одышка является редкой жалобой, если нет полного или напряженного пневмоторакса. Курение — важный фактор риска развития ПСП. Пожизненный риск развития пневмоторакса у курящих мужчин составляет 12%, по сравнению с 0,1% у некурящих мужчин 12, 13. Недавно Группа по заболеваниям плевры Британского торакального общества (BTS) решительно подчеркнула взаимосвязь между рецидивом пневмоторакса и курением, чтобы поощрять бросить курить молодым пациентам 4.
Патофизиология пневмоторакса остается неизвестной. Общее предположение о том, что PSP является результатом разрыва пузырей, недавно обсуждалось 3. В 1937 году Sattler 14 идентифицировал пузыри на висцеральной плевре с помощью торакоскопии и пришел к выводу, что утечка воздуха, приводящая к пневмотораксу, была локализована в этих пузырях. С тех пор хирургическая буллэктомия считается необходимым лечением пневмоторакса, хотя гистопатологический анализ хирургически удаленных субплевральных пузырьков или булл не всегда выявлял дефекты, ответственные за просачивание воздуха в висцеральную плевру или удаленные буллы 15,16.Janssen et al. 17 сравнивали результаты видеоторакоскопии у пациентов с первым эпизодом и пациентов с рецидивирующим ПСП. Они больше не обнаружили пузырьков или пузырей у повторяющихся PSP, что позволяет предположить, что пузырьки и пузыри не являются основным фактором риска пневмоторакса. Что касается результатов только буллэктомии как лечения ПСП, три исследования, которые не были рандомизированы, предполагают, что буллэктомия без дополнительного плевродеза или плеврэктомии не предотвращает рецидив так же эффективно, как сочетание двух техник 18–20.Улучшение визуализации с помощью компьютерной томографии (КТ) показало диффузные и двусторонние пузыри у пациентов, излечившихся от одностороннего PSP 21, 22. Эти изменения обычно называют изменениями, подобными эмфиземе (ELC). ELC были обнаружены на КТ у 81% некурящих мужчин с дефицитом α 1 -антитрипсина с предыдущим PSP, и только у 20% контрольных субъектов того же возраста и курения без PSP 23. Эти связанные с курением изменения могут быть место разрушения легочной ткани, и способствуют возникновению SP.Однако нет никаких доказательств того, что ELC являются единственной причиной пневмоторакса. Курение провоцирует заболевание мелких дыхательных путей, т. Е. бронхиолитов, локализованных в мелких дыхательных путях. Это может привести к срабатыванию обратного клапана, при котором воздух будет задерживаться в небольших дыхательных путях из-за сужения воспаленных мелких дыхательных путей. В случае более высокого перепада давления, например при изменении атмосферного давления 24, в этих периферических дыхательных путях может произойти разрыв, приводящий к пневмотораксу. Совсем недавно Noppen et al. 25 описал случай рецидива PSP, при котором на висцеральной плевре не было обнаружено утечки воздуха или ELC.Автофлуоресцентная торакоскопия позволила визуализировать обширные участки легких с субплевральным накоплением флуоресцеина, что свидетельствует о наличии значительных участков паренхиматозных аномалий легких.
Таким образом, местоположение уникальных или диффузных участков утечки воздуха, ведущих к PSP, неизвестно. Воспаление дистальных отделов дыхательных путей из-за курения, по-видимому, играет ключевую роль. ELC диффузны, при PSP обнаруживаются двусторонние субплевральные изменения. Увеличена ли пористость висцеральной плевры у пациентов с PSP по сравнению с нормальными субъектами, как предполагают Охата и Сузуки 16? Таким образом, неудивительно, что лечение СП остается предметом непрекращающихся дискуссий.Тем не менее, кажется разумным предположить, что не доказано, что буллэктомия неразорвавшихся булл является необходимой для предотвращения рецидива, тогда как плевродез, который приводит к диффузному плевральному симфизу, может быть эффективным против любой из этих потенциальных причин пневмоторакса.
Вторичный спонтанный пневмоторакс
Спровоцировать ССП могут многие заболевания (таблица 2⇓). У пациентов с ХОБЛ заболеваемость соответствует заболеваемости ХОБЛ в общей популяции.SSP обычно возникает при одышке или дыхательной недостаточности и может быть опасным для жизни из-за плохого дыхательного резерва у этих пациентов 26, 27. Часто требует немедленного лечения. Он сопровождается ипсилатеральной болью в груди, гипоксемией или гипотонией, или даже гиперкапнией 28. Пневмоторакс всегда следует исключать в случае декомпенсированной ХОБЛ или муковисцидоза 29. Диагноз ставится на основании задне-передней рентгенографии грудной клетки. В случае сомнений диагноз всегда должен подтверждаться компьютерной томографией 30, поскольку отсрочка лечения SSP, по крайней мере, с помощью дренажной трубки, может быть вредной.
Как и в случае с PSP, патофизиология SSP является многофакторной и остается малоизученной. Как недавно указывалось, воздух попадает в плевральную полость через разорванные альвеолы в результате периферического некроза легких, как в случае пневмонии P. carinii 31. Однако не только пневмония P. carinii , но и туберкулез легких повышают риск пневмоторакса у человека. Больные СПИДом 32. Месячный пневмоторакс — это особый случай SSP, встречающийся у молодых женщин. Интересно, что проспективное исследование показало, что эндометриоз легко обнаруживается на диафрагме, но реже на висцеральной плевре 33.
При неполных знаниях о патофизиологии пневмоторакса существуют значительные разногласия относительно его наилучшего лечения. Однако все согласны с тем, что лечение пневмоторакса преследует две цели: 1) удалить воздух из плевральной полости, если это необходимо (PSP редко требует неотложной медицинской помощи), и 2) предотвратить рецидив пневмоторакса независимо от метода. Не каждого пациента с первым эпизодом пневмоторакса следует лечить удалением воздуха, если только нет большого пневмоторакса у пациента с симптомами.Если удаление воздуха оправдано, то три рандомизированных контролируемых испытания убедительно показали, что простая аспирация столь же эффективна, как и традиционный дренаж через дренаж через дренаж через дренажную дренажную трубку 34–36, с немедленным успехом ~ 80%. Поэтому его следует предлагать в качестве терапии первой линии при неосложненных первых эпизодах пневмоторакса (рис. 1⇓). Для простого наблюдения авторам не известно ни об одном крупном исследовании, в котором пытались бы измерить его успешность.
ЛЕЧЕНИЕ ПЛЕВРОДЕЗОМ С ИЛИ БЕЗ ТОРАКОСКОПИИ
Существуют широкие вариации ведения рецидивирующего СП, в зависимости от специальности ответственного врача и наличия терапевтических возможностей, включая VATS 37.Руководства по лечению SP, разработанные Британским торакальным обществом 4, 38 и Американским колледжем грудных врачей (ACCP) 39, плохо используются в клинической практике 40, 41.
Существует хороший консенсус и клинические доказательства того, что профилактика рецидивов PSP должна предлагаться после первого рецидива, особенно у пациентов с профессиональным риском 42. Таким образом, большинство врачей рекомендуют это после первого эпизода в случае SSP 4, 39. Однако, процедура оптимальной для предотвращения таких рецидивов остается спорной, главным образом, из-за отсутствие крупных рандомизированных проспективных контролируемых исследований, сравнивающих различные методы профилактики рецидивов, I.е. Буллэктомия по VATS плюс плевродез по сравнению с простой тальком при торакоскопии. Здесь обсуждается роль простой торакоскопии в лечении СП.
ПЕРВИЧНЫЙ СПОНТАННЫЙ ПНЕВМОТОРАКС
Терапевтическая задача при лечении ПСП заключается в предотвращении рецидивов, которые особенно часто возникают после второго эпизода 3, 5, 8. Рандомизированное исследование, сравнивающее рецидив пневмоторакса только после дренирования с рецидивом после дренажа плюс тетрациклин или тальк, выявило частоту рецидивов. 36, 13 и 8% соответственно 43.Совсем недавно в многоцентровом рандомизированном исследовании Европейское исследование медицинской видео-ассистированной торакоскопии сравнивало частоту рецидивов у пациентов с ПСП, получавших простой плевральный дренаж, и торакоскопических оболочек талька. Они обнаружили частоту рецидивов 34 и 5% соответственно после тщательного наблюдения в течение 5 лет в обеих группах 44. Более того, боль во время и через 1 месяц после госпитализации, а также нетрудоспособность не были выше при торакоскопическом приеме талька. группа (рис.2⇓). То же самое справедливо в отношении общих затрат на эту процедуру по сравнению с дренированием плевральной дренажной трубки, даже если авторы не приняли во внимание более высокую стоимость повторной госпитализации у тех пациентов, которые получали только консервативное лечение плевральной дренажной трубкой.
После первого рецидива вероятность последующих рецидивов постепенно увеличивается, до 62% для второго рецидива и 83% для третьего 45. Столь высокая частота рецидивов, особенно после второго эпизода, стимулировала поиск лучших методов, позволяющих достичь эффективный симфиз плевры, принимая во внимание тот факт, что КТ или торакоскопические доказательства булл во время оценки SP не позволяют прогнозировать рецидив и не обеспечивают основу для решений относительно хирургической резекции ELC 17, 29, 46.
Механизмы плевродеза
Плевродез для лечения СП предназначен для достижения симфиза между париетальной и висцеральной плеврой и предотвращения рецидива пневмоторакса. Механическая абразия плевры или плеврэктомия могут привести к повреждению мезотелиального слоя и достижению симфиза. Однако из более поздних исследований известно, что сам мезотелий может действовать как инициатор биологического каскада, ведущего к фибриногенезу 47. Клеточные и молекулярные механизмы, участвующие в плевродезе, включают: активацию каскада коагуляции плевры; отложение фибрина; рекрутирование, активация и пролиферация фибробластов; и отложение коллагена 48.Эти механизмы, приводящие к плевродезу, могут быть специфическими для используемого агента, но есть общий конечный путь в самих мезотелиальных клетках, активирующий каскад плевральной коагуляции, приводящий к фибриновым сетям и пролиферации фибробластов. Точный патогенетический механизм и факторы, влияющие на исход плевродеза, хорошо не известны. Однако очевидно, что склерозирующий агент должен достигать максимально возможной площади нормального мезотелия, чтобы получить лучший плевральный симфиз.Это также является причиной того, что для индукции плевродеза при пневмотораксе (при котором мезотелиальная поверхность почти полностью сохраняется) требуются гораздо более низкие дозы склерозирующего агента, чем при злокачественной мезотелиоме плевры 48.
Ссадина плевры
Есть несколько исследований, посвященных плевродезу, выполняемому только механической абразией марлей, без лечения ELC. В исследовании, проведенном на беспородных собаках, сравнивались различные методы плевродеза, e.грамм. тетрациклин, тальк, механическое истирание, неодим / иттрий-алюминиево-гранатовый лазер, фотокоагуляция и электрокоагуляция аргоновым лучом париетальной плевры. При оценке через 1 месяц механическая абразия была единственным методом плеврального симфиза, сравнимым с тальком 49. Анатомические и гистопатологические результаты четырех различных методов плевродеза (талька, талька, фокальной абразии марли с помощью ограниченной торакотомии и механической абразии с помощью торакоскопии с использованием имеющегося в продаже плеврального абразивного устройства) были измерены на модели на животных (собаки).Оценка плевродеза (по шкале от 0 до 4) составила 3,0 ± 0,7 для талька (p <0,05 по сравнению с тальком), 2,2 ± 1,7 для торакотомии и 1,6 ± 1,1 для суспензии талька. Спайки, образовавшиеся при трении марлевой салфеткой во время торакотомии, были в основном периоперационными, а абразивная обработка плевральным абразивом была неудовлетворительной 50.
Внутриплевральная инстилляция склерозирующих агентов
Идеальный склерозирующий агент плевры для лечения рецидивирующего ПСП должен быть эффективным, легко вводимым, безопасным, недорогим и широко доступным.Чаще всего используются антибиотики (тетрациклины), нитрат серебра (SN) и препараты талька. Однако экспериментальные исследования на животных показали, что тетрациклины менее эффективны, чем препараты талька при индукции плевродеза 49, и больше не доступны 51. Эритромицин может быть потенциальным кандидатом в качестве плеврального склерозанта, но это требует дальнейших клинических испытаний 52.
SN показал превосходство в качестве склерозирующего агента в экспериментальных исследованиях по сравнению с тетрациклином 53 и суспензией талька 54, 55.В клиническом исследовании, сравнивающем СН и тетрациклиновый плевродез, не было различий в частоте рецидивов, но в группе СН наблюдалась длительная госпитализация и большее количество побочных эффектов 56, вероятно, из-за системной воспалительной реакции, включающей повышение лактатдегидрогеназы, интерлейкина (ИЛ) -8 и производство фактора роста эндотелия сосудов 57. Недавно интраплевральная инъекция SN кроликам вызвала более интенсивную острую плевральную реакцию, чем внутриплевральная суспензия талька, с более высокими уровнями лейкоцитов и IL-8 в плевральной жидкости, в основном в течение первых 6 часов.Показатели макроскопического и микроскопического плевродеза были значительно выше у кроликов, получавших СН. Однако распределение толстых и тонких коллагеновых волокон не различается между двумя группами 57. Принимая во внимание тот факт, что у двух кроликов развился гемоторакс и у шести развился ателектаз, необходимы дальнейшие экспериментальные исследования, чтобы лучше определить правильную дозировку SN. Более того, необходимы экспериментальные и клинические исследования для сравнения внутриплевральной инъекции SN с объемом талька в симфизе, полученном макро и микроскопически, а также участвующих цитокинах и процессе фиброгенеза 58.
Pleurodesis
через через дренажную трубкуВведение склерозирующего агента через дренажную трубку является приемлемым подходом для профилактики пневмоторакса у пациентов, желающих избежать хирургического вмешательства, и для пациентов с повышенным хирургическим риском (, например, тяжелая сопутствующая патология или неконтролируемый кровоточащий диатез) 37, 39. Успех Показатели при использовании тетрациклина, миноциклина, доксициклина и суспензии талька занимают промежуточное положение между показателями, полученными только при дренировании плевральной дренажной трубки и торакоскопическом лечении 59, 60.
После разведения в изотоническом солевом растворе тальк можно вводить в плевральную полость через грудную трубку (суспензия талька) или с помощью талька с помощью торакоскопии . Хотя суспензия талька является широко используемой техникой, есть несколько недостатков, включая длительный дренаж плевры и неоднородность отложения талька в плевральном пространстве после закапывания суспензии талька 61, 62. Распределение суспензии талька может привести к локализации и неполному симфизу.Его главное преимущество — простота, так как его можно выполнять у постели больного. Однако при рассмотрении вопроса о применении тальковой суспензии следует обсудить другие практические вопросы. Стандартизация введения талька через дренажную трубку проблематична, поскольку врачи используют различные дозы талька и изотонических растворов, с зажимом дренажа или без него, а также плохо контролируют количество талька, оставшегося в плевральной дренажной трубке. При рассмотрении распределения талька используемые методы также весьма разнообразны.Некоторые врачи считают, что тальк автоматически равномерно распределяется в плевральном пространстве, в то время как другие предполагают, что пациенты должны быть повернуты, чтобы распределить тальк более равномерно 63. Все эти вопросы остаются спорными.
Плевродез тальком
через торакоскопиюТальк остается самым недорогим и эффективным средством для плевродеза 44, 49, 50, 61. За исключением США, стерильный тальк, не содержащий асбеста, широко используется для предотвращения рецидивов СП 44, 64–68.Как и в случае с другими агентами, наиболее частыми незначительными побочными эффектами являются боль в груди и жар. Среди острых побочных эффектов описаны респираторная недостаточность и смерть после обливания тальком или суспензии 69–72.
При всестороннем обзоре литературы, Sahn 73 обнаружил острую дыхательную недостаточность у 0,15% (одного из 659) пациентов, получавших тальк от пневмоторакса 74. Хотя существует несколько возможных причин, связанных или не связанных с частицами талька, При развитии такой дыхательной недостаточности после плевродеза постулируется, что внутриплевральный тальк перемещается в париетальные плевральные лимфатические узлы и транспортируется в лимфатические узлы средостения и грудной проток, где он попадает в системный кровоток, что приводит к системному воспалительному процессу, ведущему к острой респираторной болезни. дистресс-синдром 57.
В эксперименте на животных Werebe et al. 75 показали, что происходит системное всасывание талька. Однако элементарный состав и распределение частиц талька по размеру различаются от шахты к шахте, и это может привести к различиям в проницаемости плевры и системной дисперсии частиц после внутриплевральной инъекции 76. Совсем недавно было проведено еще одно экспериментальное исследование на животных с использованием калиброванного талька для плевродеза и плевродеза. повторение того же протокола не выявило системного распространения частиц талька (рис.3⇓) 75, 77.
Другим объяснением такой системной воспалительной реакции может быть трансплевральный перенос талька, вызывающий воспаление легких, как показано с суспензией талька на животных моделях 78. Однако, поскольку эти экспериментальные результаты были получены на мелких животных и могут быть связаны с различными вариациями в висцеральной плевры, было бы преждевременно экстраполировать их на человека. Более того, метод внутриплевральной инстилляции талька кажется сомнительным: суспензия талька — это слепой метод для плеврального симфиза, доставляющий склерозирующий агент под высоким давлением, который может повредить плевру и региональные органы (легкие, перикард, диафрагма, средостение, и т. Д.) .) и позволяет системное распространение талька.
Другим возможным механизмом может быть системная воспалительная реакция, вызванная внутриплевральной выработкой цитокинов, абсорбируемых системным кровообращением 57.
Однако недавнее исследование на людях сравнивало смешанный тальк (большинство частиц <15 мкм, что соответствует тальку, обычно используемому в США и Великобритании) сначала с тетрациклином, а затем с градуированным тальком (большинство частиц> 25 мкм, что соответствует европейскому стандарту). ) и ясно показали, что смешанный тальк вызывает более сильное системное воспаление, определяемое по гипоксемии, воспалению контралатерального легкого и С-реактивному белку, чем тетрациклин.При сравнении смешанного талька с градуированным тальком они обнаружили те же результаты, показывающие, что градуированный тальк вызывает значительно меньшие системные эффекты. Это убедительно свидетельствует о том, что применяемый в настоящее время в Европе градуированный тальк вызывает меньшую заболеваемость, и объясняет, почему побочные эффекты почти никогда не описывались европейскими врачами, которые применяли тальк с помощью торакоскопии более 70 лет 79.
Хотя тальк остается в плевральном пространстве в течение долгого времени после введения, по-видимому, существует относительно мало долгосрочных эффектов, в частности, нарушение функции легких 65, 80.
ВТОРИЧНЫЙ СПОНТАННЫЙ ПНЕВМОТОРАКС
Возникновение SSP у пациентов с основным заболеванием, таким как ХОБЛ, может быть опасным для жизни. Часто требуется госпитализация. Некоторое лечение, такое как установка дренажной трубки и плевродез, является обязательным, особенно после первого эпизода 39, 81. У 40–50% этих пациентов будет второй и опасный эпизод пневмоторакса, если плевродез не будет выполнен 46. A торакоскопический доступ (медицинский или хирургический) с плевродезом (ссадина плевры, частичная плеврэктомия или тальк) обычно предпочтительнее, чем инстилляция склерозирующего агента через дренажную трубку 82.Недавно Lee et al. 83 показали, что объем талька при торакоскопии безопасен даже для пациентов с запущенной ХОБЛ, подтверждая предыдущие исследования 84, 85.
Однако рандомизированных контролируемых исследований по ведению SSP не проводилось. Учитывая важность SP у пациентов с основными заболеваниями, в частности с ХОБЛ, необходимы многоцентровые исследования для проведения формального анализа решений и оценки ценности различных подходов к лечению 86.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ СПОНТАННОГО ПНЕВМОТОРАКСА
Хирургическое лечение путем торакотомии раньше было последним терапевтическим средством для лечения СП, которое нельзя было лечить с помощью меньших процедур, таких как наблюдение, ручная аспирация, дренирование или торакоскопия.Это было предпочтительное лечение рецидивирующего ипсилатерального или контралатерального пневмоторакса или пневмоторакса с постоянной утечкой воздуха, двустороннего синхронного пневмоторакса или пневмоторакса, возникающих у людей, чья профессия привела к изменению атмосферного давления, например, у пилотов и аквалангистов. Хирургический доступ осуществлялся либо через стандартную заднебоковую торакотомию, либо, что чаще, через меньшие разрезы. Терапевтическая процедура состояла из резекции поражений легких, пузырьков и пузырей и некоторого вида плевральной процедуры: частичной или полной плеврэктомии, ссадины плевры или химического плевродеза.Частота рецидивов при этих процедурах у больших групп пациентов после периода наблюдения ≤20 лет составляла 3–4% 87, 88.
В начале 1990-х адаптация большинства хирургических инструментов для эндоскопического использования, а также усовершенствование и миниатюризация видеокамер привели к радикальным изменениям в хирургической практике. Новый метод, названный VATS, сохранил весь диагностический и терапевтический потенциал традиционной торакоскопии, но позволил хирургу выполнять те же внутригрудные процедуры, которые выполнялись бы при торакотомии, что значительно расширило диапазон терапевтических показаний для эндоскопического доступа.Эндоскопические степлеры оказались очень полезными при лечении СП, так как резекция апикальных поражений могла быть легко выполнена (рис. 4⇓). Это привело к сдвигу в сторону режима НДС для ИП. От открытых процедур все чаще отказываются и прибегают к исключительным случаям. Это очевидно при поиске проиндексированных ссылок; большинство сообщений о хирургическом лечении СП с середины 1990-х годов касаются ВАТС. О торакотомии сообщают редко. Опрос членов ACCP показал, что во всех ситуациях, когда требовалось хирургическое лечение как PSP, так и SSP, практикующие американские пульмонологи и торакальные хирурги предпочитали видеоторакоскопический доступ 89.В 2001 году исследование Delphi среди членов ACCP снова показало предпочтение процедур VATS перед торакотомией с очень хорошим консенсусом 39. Однако в последних рекомендациях BTS торакотомия и плеврэктомия рассматриваются как процедуры выбора, поскольку они показывают наименьшую частоту рецидивов и считают процедуры VATS альтернативной стратегией из-за отсутствия крупных контролируемых клинических испытаний 4.
Хирургическое лечение торакотомией
Хотя стандартная заднебоковая торакотомия по-прежнему используется для лечения SP 90, недавние отчеты показывают, что предпочтение отдается меньшим разрезам: подмышечная торакотомия 91, 92, передняя торакотомия 93, боковая торакотомия с сохранением мышц 94 и различные виды задней, боковой и подмышечная мини-торакотомия 95.Мидстернотомия для одновременного лечения обоих легких выполняется в <1% случаев 95.
Операция проводится под общим наркозом. Внутригрудная процедура состоит из иссечения пузырьков и пузырей, обычно с помощью скоб, и лечения небольших буллезных поражений электрокоагуляцией или лазером. Лечение поражений легких почти всегда связано с некоторыми плевральными процедурами, которые считаются важными для предотвращения рецидивов в случае возникновения новых паренхиматозных поражений.Наиболее распространенной процедурой является механическая очистка париетальной плевры сухой марлей или электрохирургическим очистителем наконечников. Иногда также осторожно растирают висцеральную плевру 92, 94. Менее распространен химический плевродез с тетрациклином, который наносится на поверхность висцеральной плевры 94. В качестве альтернативы некоторые хирурги предпочитают париетальную плеврэктомию, обычно ограниченную верхней третью. или половина плевральной полости 90. Наконец, некоторые предпочитают избегать любого типа плевродеза или плеврэктомии и полагаются исключительно на лечение паренхиматозных поражений 93.
Частота осложнений колеблется от 0% в коротких сериях пациентов 91 до 16% в больших сериях 93. Общие осложнения включают постоянные утечки воздуха, обычно определяемые как утечки, продолжающиеся более 5 дней, и возникают у 5–7% пациентов 94, 95 , раневая инфекция (1,4–6,7%) 94, пневмония (2,4–8%) 93, 94, лихорадка (1,9–10%) 94, 95, повторная операция из-за кровотечения (1–2%) 90, 93 и плечо артрит (1,9%) 95. Другие осложнения, такие как остаточный пневмоторакс, инфекция мочевыводящих путей, острая задержка мочи, гематома или неврологический дефицит, встречаются редко 90.Смертность наступает примерно у 1% пациентов с хронической обструктивной болезнью легких и SSP и связана с медицинскими осложнениями или ухудшением основного заболевания легких 93.
Частота рецидивов может составлять от 0 до 91 или 1% 95 или возрастать до 5,3% 93. Некоторые авторы 94 различают ранние рецидивы (пневмоторакс, возникающий сразу после удаления дренажных трубок) и поздние рецидивы. Из 250 пациентов, получавших лигирование или ушивание булл и различные типы абразии и плеврэктомии 90, было три (1.2%) рецидивов, 2 (3,3%) из 60 пациентов, у которых была выполнена апикальная париетальная плеврэктомия через чрезаксиллярный доступ, и один (1%) из 93 пациентов, у которых была проведена механическая абразия. Не было рецидивов в группе из 74 пациентов, перенесших париетальную плеврэктомию от ворот до верхушки, или среди 23 пациентов, которым выполнялась апикальная плеврэктомия посредством заднебоковой или субмаммарной торакотомии. В серии из 120 пациентов, перенесших 132 процедуры торакотомии для клиновидной резекции паренхиматозных поражений без плевродеза или плеврэктомии, рецидив произошел у семи (5.3%) случаев 93, что невыгодно по сравнению с серией из 95 пациентов, леченных скобками резекции пузырьков и ссадины плевры, в которых рецидив произошел только у одного (1%) пациента 95, и с большей серией из 250 пациентов, у которых Некоторое лечение плевры было добавлено к удалению поражений легких, рецидив которых произошел у одного пациента 90.
Хирургическое управление по VATS
ВАТС обычно выполняется под общим наркозом и однодневной вентиляцией легких.Пациент находится в положении лежа на боку и подготовлен к стандартной заднебоковой торакотомии. Обычно необходимы три порта: один для торакоскопа и два для захватов легких и сшивающих устройств 96. Пациенты из группы высокого риска, обычно пожилые пациенты с тяжелым основным заболеванием легких, могут подвергаться VATS под местной и эпидуральной анестезией 97 или даже под местной анестезией и седация 98. Применение герметиков при утечках воздуха и резекция булл с помощью скоб и талька могут быть выполнены безопасно.
VATS позволяет выполнять те же внутригрудные процедуры, что и при торакотомии 99. Его преимущество состоит в том, что осмотр плевры и легких является более полным, чем при ограниченной торакотомии. Опрос торакальных хирургов из Клуба общей торакальной хирургии показал, что VATS является предпочтительным методом лечения рецидивирующего пневмоторакса 100.
Для лечения пузырьков и пузырей резекция скобками является наиболее распространенной процедурой 18, 19, 101–116.Другие процедуры включают отсечение булл на ножке 117, 118, перевязку или наложение петель на буллезные поражения 101, 103, 104, 118, а также электрокаутеризацию или лазерную абляцию пузырьков и мелких булл 104, 112, 118. Эти процедуры обычно связаны с паренхимой легких. с различными маневрами для создания плевродеза и предотвращения рецидивов. К ним относятся ссадина париетальной плевры сухой марлей или любым другим протирающим материалом (рис. 5⇓) 102–105, 107, 109–111, 113, 114, 116, апикальная плеврэктомия 67, 101–111, 113–116 и химическая, лазерный или электрокаутериальный плевродез 18, 19, 67, 104, 106, 114, 116.
Послеоперационные осложнения аналогичны таковым после торакотомии и встречаются у 1 106–27,4% 113 пациентов. Последний представляет собой тщательный сборник послеоперационных событий, некоторые из которых регрессировали спонтанно, например, плевральный выпот или паралич кожного нерва плеча, о которых другие группы могут не сообщать. В целом частота осложнений составляет <10% 18, 101, 102, 104, 105, 107, 108, 110, 115, а в некоторых сериях нет никаких осложнений 112, 114, 119.Большинство серий состоят из смеси пациентов с PSP и SSP. Те, кто сообщает об отдельной частоте осложнений для каждой группы пациентов, обнаружили более высокую частоту осложнений для пациентов с SSP, чем с PSP: 27,7 против 6,6% 106, 25 против 1,7% 107, 16 против 0% 108 и 33 против 12% 109 соответственно. Утечка воздуха — частое осложнение, особенно при SSP, которое может потребовать повторного вмешательства, либо торакотомии, либо второй процедуры VATS 102, 120.Как и при открытых процедурах, смертность редка и ограничивается пациентами с SSP. Хотя большинство из них можно экстубировать в конце операции, некоторым требуется искусственная вентиляция легких с возможной смертью из-за инфаркта миокарда, сердечной недостаточности или дыхательной недостаточности 108, 120.
Глобальная частота рецидивов колеблется от 0 103, 114 до 10% 112. Многие из этих рецидивов возникают из-за неудачного метода лечения. Клипирование, лигирование и наложение петель на пузырьки использовались в начале опыта различных групп и были связаны с частотой рецидивов до 11.5 101 и 22,2% 118. Эти методы не использовались в последней серии. Частота рецидивов также, по-видимому, обратно пропорциональна интенсивности лечения; чем больше процедур выполняется, особенно при сочетании процедур на легких и плевральной полости, тем меньше рецидивов. В неконтролируемой серии из 74 пациентов, леченных четырьмя различными методами, частота рецидивов для каждой процедуры составляла: лигирование утечки воздуха — 11,5%; клиновидная резекция пузырьков или пузырей — 7,1%; плеврэктомия — 6,35%; и плеврэктомия плюс лигирование утечек воздуха или клиновидная резекция очагов поражения, 5.6% 101. У 113 пациентов единственным независимым прогностическим фактором рецидива SP была неспособность идентифицировать и резектировать пузырек во время операции 104. В недавних сериях процедура выбора — резекция пузырей и пузырей скобами или клиновидная резекция пузырей. верхушка легкого при не выявленных очагах поражения и какой-то плевродез: механическая абразия, апикальная плеврэктомия или очаговая электрокоагуляция париетальной плевры. Эти процедуры приводят к частоте рецидивов 0–5% 18, 102, 105–108, 110, 113–115, 121.Только плевральные процедуры связаны с более высокой частотой рецидивов: 6,3% для апикальной плеврэктомии 101 и 9,9% для механического плевродеза 102. Полный плевродез предотвращает рецидивы лучше, чем частичный плевродез. У 339 пациентов с стадией III и IV по Вандершуерену PSP лечили с помощью лигирования или сшивания очагов поражения и субтотальной плеврэктомии или талька; у тех, кто лечился тальком, наблюдалась самая низкая частота рецидивов: 0 против 4,5% для сшивания скобами и пудража, а также лигирования и пудража при пневмотораксе III стадии; и 0.84% на сшивание скобами и пудраж при пневмотораксе IV стадии. Однако частота рецидивов на тех же стадиях пневмоторакса при выполнении субтотальной плеврэктомии вместо полового акта составила 4,70, 12,19 и 5,26% соответственно. То же самое наблюдалось у 93 пациентов с I и II стадией ПСП, получавших либо субтотальную плеврэктомию, либо только тальк, у которых частота рецидивов составила 6,45 и 4,8% соответственно 67.
Долгосрочные осложнения включают умеренную хроническую боль, обычно локализованную в области разрезов троакара, примерно у трети пациентов, особенно у тех, кто перенес плеврэктомию по сравнению с механическим плевродезом.Однако <4% требуют ежедневного приема лекарств 107. Кроме того, около 50% пациентов могут испытывать парестезию грудной стенки, отличную от боли в ране 122. Эти хронические осложнения, по-видимому, связаны с компрессией межреберных нервов во время операции. Некоторые авторы используют троакары только для торакоскопа, а другие инструменты вводят через межреберные разрезы в другие порты, чтобы минимизировать компрессию нерва. Было обнаружено, что использование игольчатых инструментов (диаметром 2 мм) снижает боль в послеоперационной ране 123 и остаточную невралгию 124.Наличие плотных плевральных спаек является показанием для перехода на стандартный VATS 125. Хотя опубликованный опыт скуден, игольная торакоскопия кажется столь же эффективной, как и обычная VATS, когда есть буллы <2 см и мало плевральных спаек.
Лечение рецидивов зависит от размера пневмоторакса и наличия утечек воздуха после введения дренажных трубок. При ограниченном пневмотораксе у стабильных пациентов рекомендуется покой и наблюдение. При необходимости повторной операции выполняются повторные ВАТС и торакотомия.Примерно в 50% случаев обнаруживаются остаточные пузыри или утечки воздуха; они обычно скрепляются скобами или лигируются, а также добавляется плевродез с помощью плеврэктомии, абразии или талька. При отсутствии поражений выполняется какой-то плевродез 102, 104, 105, 108–110, 126, 127.
Хирургические доступы к обоим легким
Одновременный двусторонний пневмоторакс и контралатеральный рецидив нередко являются показаниями к хирургическому лечению обеих сторон. Это было выполнено с использованием процедур двусторонней торакотомии или VATS и мидстернотомии.В недавнем отчете описывается двустороннее апикальное сшивание булл и апикальная плеврэктомия через подмышечную мини-торакотомию. После завершения ипсилатеральной стороны доступ к контралатеральной стороне достигается через средостение между телами первых грудных позвонков и пищеводом. Контралатеральную верхушку легкого захватывают и втягивают в открывшуюся плевральную полость, и апикальные поражения резектируют. Контралатеральная полость грудной клетки дренируется из открытой грудной клетки с помощью трубки, проходящей через отверстие средостения.У 13 пациентов не было осложнений. Эта процедура будет показана пациентам с поражениями, ограниченными верхушкой обоих легких, в качестве альтернативы лечению рецидивов после VATS, а также при известных поражениях контралатерального легкого, чтобы уменьшить дальнейшие рецидивы 128. Аналогичный подход был описан через VATS. В этом случае между грудиной и перикардом создается проход в контралатеральное плевральное пространство. Процедура была предпринята у шести пациентов и прошла успешно и без осложнений у четырех.У двух других был двусторонний ВАТС из-за спаек плевры 129. Однако исследование шести пациентов представляет собой слишком маленькую выборку, чтобы делать какие-либо выводы. Наиболее распространенной практикой является выполнение двух процедур VATS, либо в положении латерального пролежня, с изменением стороны после завершения одной стороны 130, либо в положении лежа на спине, изменяя места троакаров, два на передней подмышечной линии и один в области подмышечной впадины. среднеключичная линия через второе межреберье 96. Этот одновременный подход не связан с повышенной заболеваемостью или длительным пребыванием в больнице по сравнению с поэтапным двусторонним VATS 131.
Сравнение торакотомии и VATS
Было проведено два проспективных клинических испытания по сравнению торакотомии и VATS. В первом должным образом рандомизированном исследовании сравнивали VATS для PSP и SSP с ограниченной частичной боковой торакотомией с сохранением мышц 132. В группе VATS для PSP 72-часовое уменьшение объема форсированного выдоха за одну секунду и форсированной жизненной емкости легких были значительно ниже. У этой группы пациентов было более длительное время операции, потребовалось меньше анальгетиков в первые 12 часов после операции и было более короткое послеоперационное пребывание в больнице, но ни одно из этих различий не было значимым.В группе пациентов с SSP ни одно из различий не было значимым, за исключением времени операции, которое было больше для группы VATS. Авторы пришли к выводу, что VATS превосходит торакотомию при PSP, но сомневаются в его использовании при SSP. Второе испытание не было должным образом рандомизировано, поскольку пациенты выбирали процедуру после того, как врач объяснил их детали 133. Стоимость VATS была выше, чем стоимость трансаксиллярной мини-торакотомии, и лишь частично покрывалась медицинской страховкой; это могло внести предвзятость при выборе процедуры.В этом исследовании различия во времени операции, количестве анальгезии в первый послеоперационный день и продолжительности установки плевральной дренажной трубки не были значительными, хотя продолжительность операции и продолжительность плевральной дренажной трубки были короче в группе трансаксиллярной мини-торакотомии. Был сделан вывод, что ВАТС не показала преимущества перед мини-торакотомией.
В неконтролируемых исследованиях некоторые авторы сравнили свой первоначальный опыт лечения SP с помощью VATS с историческими сериями пациентов, перенесших торакотомию, подмышечную, ограниченную латеральную или заднебоковую.В этих сравнениях продолжительность дренажа была в целом меньше в группе VATS 107, 121, 134, 135 или той же 136; продолжительность госпитализации или послеоперационного пребывания также была короче 107, 121, 134, 135, 137, 138 или того же 136, 139; время операции было меньше для VATS 121, 135, одинаково для обеих процедур 136, 137 или больше для VATS, чем для торакотомии 138; пациенты, перенесшие VATS, нуждались в меньшем количестве наркотических анальгетиков, чем пациенты, перенесшие торакотомию 107, 134, 137; частота послеоперационных осложнений была ниже 134 или выше 137 в группе VATS или одинаковой в обеих группах 121; частота рецидивов была примерно такой же, но, похоже, было больше пациентов с рецидивами среди тех, кто прошел VATS 121, 134, 135, 138; объем оперативного кровотечения был меньше в группе ВАТС 121; пациенты группы ВАТС вернулись на работу ранее 107 137; и, наконец, VATS был дешевле, чем торакотомия 135.Сообщалось, что некоторые из этих преимуществ VATS, такие как более короткая продолжительность дренажа и госпитализации, а также более раннее возвращение к работе, действительны только для пациентов с PSP 107.
ЗАКЛЮЧЕНИЕ
Есть много вариантов в управлении ИП. Его патофизиология остается плохо изученной. Однако хорошо известно, что ПСП сильно влияет на курение у обоих полов. Ни один врач не должен упускать возможность пневмоторакса, особенно у молодых людей, побуждать к отказу от курения.Большинство молодых пациентов продолжают курить после первого эпизода ПСП, что свидетельствует о необходимости совершенствования клинических стратегий, чтобы лучше удовлетворять потребности данной возрастной группы 144.
При лечении пневмоторакса преследуются две цели: 1) удалить воздух и 2) предотвратить рецидив. В первых эпизодах ПСП нет сомнений в том, что наблюдение и простая аспирация являются общепринятыми методами лечения первой линии, что доказано рандомизированными контролируемыми исследованиями 34, 36. Однако, хотя аспирация рекомендована с середины 1980-х годов 145, 146, она остается плохо применяются и должны лучше продвигаться в повседневной медицинской практике.В случае неудачной аспирации следует ввести дренажную трубку и направить пациентов в специальные отделения легких с опытом работы в области медицины и медсестер, поскольку установка межреберной трубки может привести к серьезным осложнениям и даже смерти 147–150. Пациенты, которым требуется установка дренажной трубки, должны быть проинформированы о том, что простое введение талька при торакоскопии предотвращает рецидивы пневмоторакса без продления госпитализации или осложнений и является более экономичным, чем консервативное лечение с помощью межреберной трубки, как показано в рандомизированном контролируемом исследовании 44.
В клинических ситуациях, таких как SSP с потенциальной дыхательной недостаточностью, рецидивирующий PSP или стойкий пневмоторакс, лечение для предотвращения рецидива пневмоторакса является обязательным. Есть два основных варианта: медицинский плевродез с тальком с помощью простой торакоскопии или хирургический подход. Торакоскопическая очистка тальком — безопасная процедура даже в сложных программах SSP 83–85, и она была бы не более болезненной, чем дренирование грудной клетки, если бы торакоскописты улучшили свои навыки лечения боли 151.Недавно хирургическая бригада 64 опубликовала самое обширное на сегодняшний день исследование по лечению пневмоторакса, охватывающее более 1000 случаев, и показало, что торакоскопия под тальком была очень успешной с частотой рецидивов 5%.
С другой стороны, верно и то, что VATS оказался более рентабельным, чем дренаж плевральной дренажной трубки для аналогичных показаний 143, хотя это более дорогая процедура, чем торакоскопия, требующая общей анестезии, интубации двухпросветной трубки и вентиляции.Там нет никаких доказательств для рутинной резекции и волдырей пузырьков, что делает эту процедуру очень спорны для очень больших булл 3, за исключением или когда есть признаки утечки буллы, например, в упорном пневмотораксе. Хирургические методы значительно улучшились и теперь стали менее инвазивными. С начала 1990-х годов предпочтение отдается VATS перед торакотомией, хотя количество рецидивов после VATS обычно немного выше, чем после торакотомии. VATS позволяет выполнять широкий спектр процедур на паренхиме легких и плевральных поверхностях.Сочетание резекции пузырьков или пузырей скобами и некоторого рода плевродез, особенно абразии или плеврэктомии, по-видимому, дает наименьшую частоту рецидивов. VATS для SP не был адекватно сравнен с торакотомией в крупных рандомизированных клинических испытаниях ни по клинической эффективности, ни по стоимости. По прошествии многих лет, в течение которых оказалось технически возможным лечить СП с разумной заболеваемостью, пришло время стандартизировать используемую хирургическую технику и начать большие рандомизированные клинические испытания, чтобы ответить на три основных вопроса: 1) действительно ли VATS превосходит торакотомия; 2) насколько это рентабельно; и 3) правильное время для его начала.Есть также много других потенциальных областей дальнейших исследований в рандомизированных контролируемых испытаниях, таких как сравнение любой хирургической техники, такой как VATS, с торакоскопией с использованием простого талька, сравнение зажимных и не зажимающих стратегий после прекращения утечки воздуха, а также амбулаторное использование небольших катетеров, подключенных к клапанам Геймлиха. по сравнению с дренажом через межреберный дренаж грудной клетки после неудачной аспирации, и т. д.
Как показано в настоящей статье, торакальные хирурги и пульмонологи должны развивать больше синергизма и использовать рандомизированные контролируемые исследования, чтобы улучшить знания, накопленные обеими дисциплинами для лечения пневмоторакса, поскольку большинство исследований на сегодняшний день были нерандомизированными контролируемыми исследованиями.Это единственный способ ответить на довольно провокационный вопрос, который задают хирурги, о том, не является ли тенденция замены простой торакоскопии торакоскопической хирургией с помощью видеоизображения результатом славы более новых и дорогих методов 64. В 1997 году 152, редакционная статья приветствовала пятая годовщина видеоассистированной торакоскопической хирургии сообщила о более чем 500 публикациях по видеоассистированной торакоскопической хирургии и пришла к выводу, что большинство этих публикаций представляют очень мало тщательной научной оценки этой новой технологии.Пришло время более научно оценить старую технику, торакоскопию, открытую Якобеусом в 1910 году 10, а также торакоскопическую хирургию с помощью видео, которая была доступна с 1992 года. Это единственный способ уменьшить нынешнюю путаницу в отношении лучшего лечения. при пневмотораксе 153.
советов из других журналов — Американский семейный врач
Советы из других журналов
Am Fam Physician. 15 сентября 2000; 62 (6): 1398-1400.
Спонтанный пневмоторакс возникает у лиц, не страдающих клинически выраженным заболеванием легких. Два других типа пневмотораксов — травматические и ятрогенные. Вторичный пневмоторакс возникает как осложнение ранее существовавшего легочного заболевания (см. Сопроводительную таблицу). Сан и Хефнер недавно рассмотрели клиническое состояние спонтанного пневмоторакса.
Заболеваемость спонтанным пневмотораксом составляет от 7,4 до 18 случаев на 100 000 населения у мужчин в год. У женщин зарегистрированная заболеваемость составляет 1.От 2 до шести случаев на 100 000 населения в год. Типичный пациент — высокий худой мужчина от 10 до 30 лет. Риск пневмоторакса намного выше у курильщиков сигарет — до 20 раз выше, в зависимости от количества сигарет, выкуриваемых за день.
Просмотреть / распечатать таблицу
Классификация пневмоторакса по причине
Спонтанный | |
Первичный: клиническое заболевание легких отсутствует | |
Вторичное осложнение легкого клиническое очевидное осложнение | |
Травматическая | |
Проникающая травма грудной клетки | |
Тупая травма груди | |
Ятрогенная | Ятрогенная |
Торакоцентез и биопсия плевры | |
Баротравма |
Классификация пневмоторакса по причине 9
907 908Первичный: клиническое заболевание легких отсутствует
Вторичное: осложнение клинически очевидного заболевания легких
Травматическое
Проникающая травма груди
Ятрогенный
Трансторакальная игла Барботажная игла
Во время установки катетера в подключичную вену
8
Пациенты со спонтанным пневмотораксом не имеют клинически выраженных заболеваний легких.Однако исследования показали, что от 76 до 100 процентов имеют субплевральные буллы, диагностированные с помощью торакоскопической видео-хирургии. Исследования с использованием компьютерной томографии (КТ) показали, что почти у 90 процентов пациентов наблюдаются ипсилатеральные буллы. Точный механизм образования булл не установлен.
Большинство пациентов, перенесших спонтанный пневмоторакс, делают это в состоянии покоя. Обычно они испытывают ипсилатеральную боль в груди, которая сначала описывается как острая, а затем становится устойчивой.Распространенным симптомом часто бывает одышка. Даже при отсутствии лечения симптомы часто исчезают в течение 24 часов.
Медицинский осмотр может быть нормальным у пациентов с небольшим пневмотораксом (менее 15 процентов гемиторакса). Тахикардия — наиболее частая находка, и, в зависимости от объема пораженного легкого, другие физические признаки включают снижение подвижности грудной клетки, гиперрезонансную перкуссионную ноту, уменьшение фрески и уменьшение или уменьшение звуков дыхания.
Первоначальное лечение спонтанного пневмоторакса включает удаление воздуха из подплеврального пространства.При небольшом пневмотораксе дополнительный кислород быстро ускоряет реабсорбцию воздуха плеврой. Таким образом можно вести здоровых молодых пациентов, которые обычно выписывают из отделения неотложной помощи после шести часов наблюдения, если можно обеспечить тщательное наблюдение. Если пневмоторакс больше 15 процентов, аспирации воздуха пластиковым внутривенным катетером, катетером плевроцентеза нет. 7 к нет. 14 Можно сделать французский катетер малого диаметра или дренажную трубку. Эти методы обычно эффективны примерно у 70 процентов пациентов.Выписка уместна, если контрольная рентгенограмма грудной клетки после шести часов показывает разрешение пневмоторакса. В некоторых случаях плевральную трубку можно оставить на один или два дня и прикрепить к одностороннему клапану Геймлиха или к водонепроницаемому устройству, позволяющему передвигаться. Уровень успеха в этом сценарии обычно составляет 90 процентов, но снижается примерно до 50 процентов или меньше у пациентов, у которых есть рецидив.
Хирургическое вмешательство редко необходимо пациентам с первичным пневмотораксом и не рассматривается, если утечка воздуха не сохраняется в течение четырех-семи дней.Появление пузырей на компьютерной томографии не коррелировало с успехом спонтанного разрешения воздуха. Авторы этого обзора считают, что наличие или отсутствие пузырей не должно быть единственным критерием хирургического вмешательства.
Решение использовать склерозирующие агенты, такие как тальк, для предотвращения рецидива должно быть индивидуальным. Некоторые центры рекомендуют эту процедуру после первого эпизода. Авторы рекомендуют профилактические вмешательства после повторного ипсилатерального пневмоторакса. Было показано, что возраст является независимым фактором риска рецидива, при этом заболеваемость снижается у лиц старше 40 лет.Закапывание талька (обычно в дозе 2 г) может выполняться с помощью видеоторакоскопии или ограниченной торакотомии. Первая процедура менее инвазивна, но имеет несколько более высокую частоту неудач, которая может зависеть от учреждения.
Спонтанный пневмоторакс — торакальная группа
Определение пневмоторакса
Пневмоторакс — это ненормальное присутствие воздуха в пространстве между легкими и грудной полостью (известное как плевральная полость ), которое может привести к частичному или полному коллапсу соответствующего легкого.
Пневмоторакс можно классифицировать как:
- Травматический (в результате несчастного случая или другого лечения), или
- Спонтанное
Спонтанный пневмоторакс
Условия
Спонтанный пневмоторакс можно обозначить как:
- Первичный (PSP) при отсутствии какого-либо очевидного провоцирующего фактора, или
- Вторичный (SSP) , связанный с основными легочными заболеваниями или состояниями, такими как муковисцидоз, хроническая обструктивная болезнь легких (ХОБЛ), туберкулез, саркоидоз, злокачественные новообразования и т. Д.
Диагностика
Диагноз обычно ставится с помощью обычного рентгена грудной клетки. Тем не менее, для получения более подробной информации рекомендуется компьютерная томография.
Причины и симптомы
Большинство случаев первичного спонтанного пневмоторакса происходит из-за образования небольших воздушных мешочков ( пузырьков, ) в легких, которые разрываются, в результате чего воздух просачивается в плевральную полость. Это создает давление на легкое, что приводит к его коллапсу.
Сами по себе пузырьки не вызывают никаких симптомов и могут присутствовать долгое время, прежде чем они разорвутся (если они разорвутся). Обычно результатом разрыва является резкое начало боли в груди и затрудненное дыхание. Однако до 10 процентов пациентов могут протекать бессимптомно, в то время как другие имеют такие легкие симптомы, что они могут даже не обращаться за медицинской помощью.
Факторы риска
Хотя основная причина ПСП все еще плохо изучена, для первичного спонтанного пневмоторакса были установлены следующие корреляции и факторы риска:
- Курение
- Пол (мужчин 3.В 3 раза чаще, чем женщины, испытают это)
- Возраст (от 18 до 40 лет)
- Рост (высокий, худой)
- Семейный пневмоторакс
- Генетические нарушения
Чтобы уточнить, PSP сильно связана с курением у обоих полов; при этом риск увеличивается более чем в 20 раз у мужчин и почти в 10 раз у женщин по сравнению с рисками у некурящих. Курение вызывает воспаление мелких дыхательных путей, приводящее к повреждению тканей, которое называется эмфизематозоподобными изменениями (ELC) .
В целом ПСП чаще встречается у мужчин, чем у женщин. Ежегодная заболеваемость составляет от 7,4 до 18 на 100 000 мужчин и от 1,2 до 6 на 100 000 женщин. Первый пик заболеваемости у мужчин наступает в возрасте от 20 до 25 лет, а некоторые исследования показали, что первый пик заболеваемости у женщин задерживается в возрасте от 30 до 34 лет.
Обычно пациенты имеют высокий и худощавый габитус. Однако неясно, влияет ли высота на развитие субплевральных пузырьков или более отрицательное апикальное давление плевры вызывает разрыв уже существующих пузырьков.
Семейные кластеры этого состояния были зарегистрированы более чем у 10 процентов пациентов. Генетические нарушения, которые были связаны с PSP, включают синдром Марфана, гомоцистинурию и синдром Бирта-Хогга-Дуба (BHD).
Вопреки распространенному мнению, физическое усилие не было доказано как ускоряющий фактор; PSP обычно возникает в состоянии покоя. Другие описанные провоцирующие факторы (хотя и противоречивые) включают:
- Изменение атмосферного давления
- Громкая музыка
- Беременность (нераспознанный фактор риска)
Варианты лечения спонтанного пневмоторакса включают:
Выбор метода лечения зависит от многих факторов, в том числе от того, является ли пневмоторакс первым или рецидивирующим.При первом пневмотораксе обычно рекомендуется консервативное лечение.
Полное разрешение неосложненного пневмоторакса может занять до 10 дней. Частота рецидивов ПСП через пять лет колеблется от 28 до 32 процентов, большинство из них происходит в течение 1-2 лет после первого эпизода.
Некоторые пневмотораксы маленькие и ограничиваются верхушкой легкого; их часто можно наблюдать при тщательном наблюдении. У большинства этих пациентов проблема полностью решена, и примерно у 80 процентов больше не будет проблем с коллапсом легкого.
В случае более крупного пневмоторакса лечение обычно включает введение грудной трубки в легкое для повторного расширения и заживления. Это требует, чтобы трубка оставалась на месте в течение нескольких дней. Часто с этим можно справиться амбулаторно.
Операция показана в двух случаях:
- Если легкое остается нерасширенным после того, как плевральная дренажная трубка была на месте в течение достаточного периода времени, или
- При повторном пневмотораксе
В последнем случае значительно возрастает частота хронических и повторяющихся проблем; поэтому рекомендуется более радикальное хирургическое лечение.
Хирургическая процедура включает использование минимально инвазивной техники, при которой апикальные пузырьки удаляются вместе с частью слизистой оболочки грудной клетки ( плевры, ). Этот метод позволяет верхней части легкого прилегать к грудной стенке, предотвращая будущий коллапс. Для операции обычно требуется всего одна ночь в больнице и короткое выздоровление дома.
По нашему опыту, это лечение оказалось чрезвычайно эффективным, и у наших пациентов рецидивы после операции составляют менее одного процента.
Archivos de Bronconeumología
Archivos de Bronconeumologia — это научный журнал, который преимущественно публикует перспективные оригинальные исследовательские статьи, содержание которых основано на результатах, касающихся нескольких аспектов респираторных заболеваний, таких как эпидемиология, патофизиология, клиники, хирургия и фундаментальные исследования. Другие типы статей, такие как обзоры, редакционные статьи, несколько специальных статей, представляющих интерес для общества и редколлегии, научные письма, письма в редакцию и клинические изображения, также публикуются в журнале.Это ежемесячный журнал, который публикует в общей сложности 12 выпусков и несколько приложений, которые содержат статьи, относящиеся к разным разделам.
Все рукописи, поступившие в Журнал, оцениваются редакторами и отправляются на экспертную рецензию, в то время как их обрабатывает редактор и / или помощник редактора из группы. Журнал издается ежемесячно на испанском и английском языках. Таким образом, приветствуется подача рукописей, написанных на испанском или английском языках. Переводчики, работающие в журнале, берут на себя соответствующие переводы.
Рукописи будут представлены в электронном виде с использованием следующего веб-сайта: https://www.editorialmanager.com/ARBR/, ссылка на который также доступна через главную веб-страницу Archivos de Bronconeumologia.
Доступ к любой опубликованной статье на любом языке возможен через веб-страницу журнала, а также из PubMed, Science Direct и других международных баз данных. Кроме того, журнал также присутствует в Twitter и Facebook. Журнал выражает голос Испанского респираторного общества пульмонологии и торакальной хирургии (SEPAR), а также других научных обществ, таких как Латиноамериканское торакальное общество (ALAT) и Иберийско-американская ассоциация торакальной хирургии (AICT).
Авторы также могут присылать свои статьи под сопутствующим заголовком журнала в открытом доступе — Open Respiratory Archives .
Пневмоторакс самопроизвольный Артикул
[1]
Байг М.А., Маджид М.Б., Аттар Б.М., Хан З., Деметрия М., Ганди С.Р., Эффективность и безопасность постоянных плевральных катетеров при лечении гидроторакса печени: систематический обзор литературы. Cureus.6 августа 2018 г. [PubMed PMID: 30338185]
[3]
Hallifax RJ, Goldacre R, Landray MJ, Rahman NM, Goldacre MJ, Тенденции в частоте и рецидиве спонтанного пневмоторакса, принимаемого в стационаре, 1968-2016. ДЖАМА. 2018, 9 октября [PubMed PMID: 30304427]
[4]
Савицкий Е., О С.С., Ли Дж. М., Развитие эпидемиологии и лечение спонтанного пневмоторакса.ДЖАМА. 2018, 9 октября [PubMed PMID: 30304415]
[5]
Walker SP, Bibby AC, Halford P, Stadon L, White P, Maskell NA, Частота рецидивов первичного спонтанного пневмоторакса: систематический обзор и метаанализ. Европейский респираторный журнал. 2018 сен [PubMed PMID: 30002105]
[6]
Bertolaccini L, Congedo MT, Bertani A, Solli P, Nosotti M, Проект по оценке качества опубликованных руководств по лечению первичного спонтанного пневмоторакса от Итальянского общества торакальных хирургов.Европейский журнал кардио-торакальной хирургии: официальный журнал Европейской ассоциации кардио-торакальной хирургии. 1 ноября 2018 г. [PubMed PMID: 29788194]
[7]
Aguinagalde B, Aranda JL, Busca P, Martínez I, Royo I, Zabaleta J, SECT Руководство по клинической практике ведения пациентов со спонтанным пневмотораксом. Cirugia espanola. 2018 янв. [PubMed PMID: 29248330]
[8]
Schnell J, Beer M, Eggeling S, Gesierich W, Gottlieb J, Herth FJF, Hofmann HS, Jany B, Kreuter M, Ley-Zaporozhan J, Scheubel R, Walles T, Wiesemann S, Worth H, Stoelben E, Management of Спонтанный пневмоторакс и пост-интервенционный пневмоторакс: Немецкое руководство S3.Дыхание; международный обзор заболеваний грудной клетки. 24 июля 2018 г. [PubMed PMID: 30041191]
[9]
Wong A, Galiabovitch E, Bhagwat K, Управление первичным спонтанным пневмотораксом: обзор. Журнал хирургии ANZ. 5 июля 2018 г. [PubMed PMID: 29974615]
[10]
Харрис М., Рокер Дж., Паде К. Х., Пневмоторакс у педиатрических пациентов: стратегии управления для улучшения результатов для пациентов [дайджест].Практика детской неотложной медицинской помощи. 2017 г. 22 марта [PubMed PMID: 28745853]
[11]
Santos C, Gupta S, Baraket M, Collett PJ, Xuan W, Williamson JP, Результаты инициативы по повышению безопасности стационарного введения торакостомической трубки малого диаметра. Журнал внутренней медицины. 2018 сентября 19 [PubMed PMID: 30230151]
[12]
Сано А., Многопрофильный командный подход при осложненном пневмотораксе.Журнал грудных болезней. Июль 2018 г. [PubMed PMID: 30123534]
[13]
Li X, Su X, Chen B, Yao H, Yu Y, Ленг X, Lu Q, Wang C, Lei J, Ruetzler K, Fernando HC, Gilbert S, Ching Y, Filosso PL, Shen J, Zhu C, многопрофильный групповой подход в случае двустороннего натяжного пневмоторакса. Журнал грудных болезней. 2018 апр. [PubMed PMID: 29850161]
Спонтанный пневмоторакс | Американский колледж ветеринарных хирургов
Варианты лечения вашего питомца различаются в зависимости от тяжести клинических признаков .Первоначальная стабилизация имеет первостепенное значение, так как спонтанный пневмоторакс может быть опасным для жизни из-за сокращения соответствующей вентиляции. Ваш лечащий ветеринар сначала может порекомендовать торакоцентез . Это процедура, при которой в грудную полость вводится небольшая игла, чтобы удалить воздух вокруг легких, позволяя вашему питомцу дышать более комфортно. Это временное лечение не устраняет основную причину пневмоторакса, но позволяет легким более нормально расширяться, что может спасти жизнь вашего питомца.
Как правило, варианты долгосрочного лечения можно разделить на медикаментозное или хирургическое лечение. Основная причина спонтанного пневмоторакса диктует, какой вариант лечения будет наиболее подходящим. Ваш основной ветеринарный врач и ветеринарный врач, сертифицированный ACVS, будут работать с вами и вашим питомцем, чтобы принять наилучшее решение.
Лечение включает:
- Кислородная добавка
- Торакостомическая трубка (грудная трубка)
Кислородная терапия важна, потому что по мере коллапса легких, вторичного по отношению к потере отрицательного внутригрудного давления, способность доставлять кислород в организм также уменьшается.Предоставляя дополнительный кислород, это помогает организму доставлять достаточное количество кислорода к каждой системе органов. Торакостомические трубки — это полые трубки, вводимые через кожу в грудную полость (рис. 4). Это позволяет периодически или непрерывно удалять воздух из груди. Это помогает легким вашего питомца более нормально расширяться, посылая необходимый уровень кислорода остальным частям тела. Чаще всего спонтанный пневмоторакс не поддается лечению с медицинской точки зрения в течение длительного времени, и требуется хирургическое вмешательство для устранения основной причины утечки воздуха в грудную клетку.
Хирургическое лечение чаще всего включает удаление всей пораженной доли легкого путем проникновения в грудную клетку и выполнения лобэктомии легкого (рис. 5). Это может быть выполнено с использованием трех различных подходов к грудной полости: минимально инвазивной торакоскопии, средней стернотомии (через грудину) или боковой торакотомии (между ребрами). Каждый подход имеет свои преимущества в зависимости от основной причины заболевания, местоположения пораженной доли легкого и наличия оборудования.Ветеринарный врач, сертифицированный ACVS, рассмотрит конкретный случай вашего питомца, чтобы дать наилучшие рекомендации.
.

