Красная волчанка – лечение в клиниках МЕДСИ в Москве
Системная красная волчанка (СКВ) – хроническое аутоиммунное ревматическое заболевание. Диагноз СКВ может поставить только специалист, обладающий достаточным опытом. Трудности в диагностике заболевания связаны с разнообразной клинической картиной, когда на протяжении болезни появляются новые признаки заболевания, отражающие поражение различных органов и систем.
При постановке диагноза СКВ специалисты МЕДСИ основываются на совокупности клинических проявлений заболевания и данных лабораторной диагностики, кроме того, анализы крови, мочи, ультразвуковое, рентгенологическое исследования позволяют точно установить характер и степень повреждения внутренних органов, фазы активности заболевания.
В Клинике инновационной ревматологии Клинико-диагностического центра МЕДСИ на Белорусской проводится диагностика с помощью современных лабораторных и инструментальных методов исследования – определение аутоантител, комплемента, титра ревматоидного фактора, биохимический анализ крови, МРТ, МСКТ, УЗИ, рентгенография, выполняются функциональные тесты.
В Клинико-диагностическом центре на Белорусской ведет прием известный профессор-ревматолог Сергей Константинович Соловьев, доктор медицинских наук, заслуженный врач Российской Федерации. Сергей Константинович – создатель отечественной школы интенсивной терапии ревматических заболеваний, эксперт в области диагностики и лечения системной красной волчанки, тяжелых форм ревматоидного артрита, системных васкулитов и других заболеваний соединительных тканей.
Профессор Соловьев С.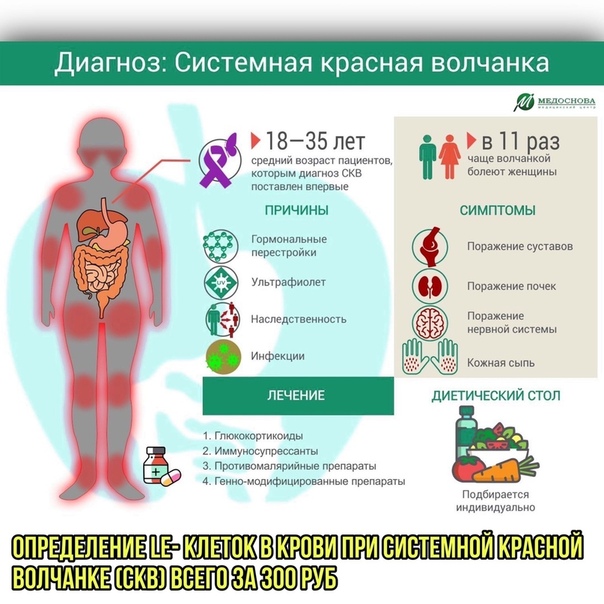 К. – автор Национальных клинических рекомендаций по диагностике и лечению СКВ, разработал уникальную методику лечения больных с системной красной волчанкой и тяжелыми формами ревматоидного артрита.
К. – автор Национальных клинических рекомендаций по диагностике и лечению СКВ, разработал уникальную методику лечения больных с системной красной волчанкой и тяжелыми формами ревматоидного артрита.
Разработанные Профессором методики терапии аутоиммунных ревматических заболеваний с использованием методов экстракорпоральной терапии и генно-инженерных биологических препаратов позволяют обеспечить не только максимальную выживаемость, но и высокий уровень качества жизни, возможность минимизировать прием гормональных препаратов или даже их полную отмену. Раннее распознавание болезни, своевременная и персонифицированная терапия, профессиональный мониторинг – основные принципы, которыми руководствуется Сергей Константинович в своей повседневной практике.
Алгоритм лечения системной красной волчанки современное состояние проблемы | Клюквина
 , испр. и доп. Под ред. акад. РАМН Е.Л. Насонова, М.: ГЭОТАР-Медиа, 2010: 429-481.
, испр. и доп. Под ред. акад. РАМН Е.Л. Насонова, М.: ГЭОТАР-Медиа, 2010: 429-481.2. Petri M. Epidemiology of systemic lupus erythematosus. Best Pract Res Clin Rheumatol., 2002, 16 (5): 847-858.
3. Клюквина Н.Г., Насонов Е.Л. Особенности клинических и лабораторных проявлений системной красной волчанки. Современная ревматология, 2012, 4: 40-48.
4. Насонов Е.Л., Александрова Е.Н., Новиков А.А. Аутоиммунные ревматические заболевания — проблемы иммунопатологии и персониицированной терапии. Вестник РАМН, 2015, 2: 169-182.
5. GillisJ, Yazdany J, Trupin I, Julian L. Et al. Medicaid and access to care among persons with systemic lupus erythematosus. Arthr. Rheum., 2007, 57: 601-607.
7. Haubitz M. Exploring new territory: the move towards individualized treatment. Lupus, 2007, 16: 227-231.
8. Mehmedbasic A. Algorithms in the diagnosis and treatment of systemic lupus erythemato-sus. Interna Med, 2010, 18(3): 157-161.
9. Chatham WW, Kimberly RP. Treatment of lupus with corticosteroids. Lupus, 2001, 10: 140-147.
10. Bertsias GK, loannidis JPA, Bombardieri S et al. EULAR recommendations for the management of Systemic Lupus Erythematosus. Report of a Task Force of the European Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Ann. Rheum. Dis., 2008, 67: 195-205.
Report of a Task Force of the European Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Ann. Rheum. Dis., 2008, 67: 195-205.
11. Соловьев С.К., Асеева Е.А. Системная красная волчанка. Современные критерии диагноза, мониторинг активности и рекомендации по терапии. Пособие для врачей. Под ред. Е.Л. Насонова. Киев: Морион, 2013. 47 с.
12. Parker BJ, Bruce IN. High dose methylpredniso-lone therapy for the treatment of severe systemic lupus erythematosus. Lupus, 2007, 16: 387-393.
13. Соловьев С.К., Асеева Е.А., Торгашина А.В. Интенсифицированная терапия аутоиммунных ревматических заболеваний. РМЖ, 2010, 11(375), 18: 748-751.
14. Лечение ревматических заболеваний ударными дозами метилпреднизолона.
15. Иванова М.М. Эволюция методов лечения системной красной волчанки. Избранные лекции по клинической ревматологии. Под ред. В.А. Насоновой, Н.В. Бунчука. М.: Медицина, 2001: 91-100.
16. Клюквина Н.Г., Насонов Е.Л. Фармакотерапия системной красной волчанки: современные рекомендации. РМЖ, 2010, 18(382): 1108-113.
17. Houssiau F. Thirty years of cyclophosphamide: assessing the evidence. Lupus, 2007, 16: 212-216.
18. Ginzler EM, Wofsy D, Isenberg D et al. Nonrenal disease activity following mycophenolate mofetil or intravenous cyclophosphamide as induction treatment for lupus nephritis. Arthr Rheum., 2010, 62(1): 211-221.
20. Appel GB, Contreras G, Dooley MA et al. Mycophenolate mofetil versus Cyclophosphamide for induction treatment of lupus nephritis. J. Am. Soc. Nephrol., 2009, 20: 1103-1112.
21. Rovin BH, Parikh SV, Hebert LA, Chan TM, Mok CC, Ginzler EM et al. Lupus nephritis: induction therapy in severe lupus nephritis — should MMF be considered the drug of choice? Clin J Am Soc Nephrol, 2013, 8: 147-53.
22. Nossent HC, Koldingsnes W. Long-term efficacy of azathioprine treatment for proliferative lupus nephritis. Rheumatology (Oxford), 2000, 39: 969.
Rheumatology (Oxford), 2000, 39: 969.
23. Насонов Е.Л. Метотрексат. Перспективы применения в ревматологии. М.: Филоматис, 2005: 154-179.
24. Sugiyama М, Ogasawara Н, Kaneko H et al. Effect of extremely low dose cyclosporine treatment on the thrombocytopenia in systemic lupus erythematosus. Lupus, 1999, 7(1): 53-56.
Инфекционные осложнения как предикторы неблагоприятного исхода у больной с системной красной волчанкой (клиническое наблюдение) | Никитина
1. Heinlen L.D., McClain M.T., Merrill J. et al. Clinical criteria for systemic lupus erythematosus precede diagnosis and associated autotoanibodies are present before clinical symptoms. Arthiritis Rheum. 2007; 56(7):2344-2351. doi: 10.1002/art.22665
doi: 10.1002/art.22665
2. Doria A., Iaccarino L., Ghirardello A. et al. Long-term prognosis and causes of death in systemic lupus erythematosus. Am. J. Med.2006; 119(8):700-706. doi: 10.1016/j.amjmed.2005.11.034
3. Белов Б.С., Соловьев С.К., Клюквина Н.Г. и др. Коморбидные инфекции у больных системной красной волчанкой: современное состояние проблемы. Научнопрактическая ревматология. 2016;54(4):469-477. doi: http://dx.doi.org/10.14412/1995-4484-2016-469-477.
4. Александрова О.Л., Бутенко И.А., Никитина Н.М., Нам И.Ф., Ребров А.П. Тяжелое течение системной красной волчанки — трудности и возможности терапии. Клиницист, 2013; 3-4: 62-66. doi: 10.17650/1818-8338-2013-3-4-62-66.
5. Цанян М.Э., Соловьев С.К., Торгашина А.В. и др. Эффективность терапии ритуксимабом у больных рефрактерной к стандартной терапии системной красной волчанкой при длительном динамическом наблюдении. Научнопрактическая ревматология. 2014;52(2):159-168. doi: http://dx.doi.org/10.14412/1995-4484-2014-159-168.
Цанян М.Э., Соловьев С.К., Торгашина А.В. и др. Эффективность терапии ритуксимабом у больных рефрактерной к стандартной терапии системной красной волчанкой при длительном динамическом наблюдении. Научнопрактическая ревматология. 2014;52(2):159-168. doi: http://dx.doi.org/10.14412/1995-4484-2014-159-168.
6. Doria A., Canova M., Tonon M. et al. Infections as triggers and complications of systemic lupus erythematosus. Autoimmun Rev. 2008; 8 (1): 24-28. doi: 10.1016/j.autrev.2008.07.019
7. Dubula T., Mody G.M. Spectrum of infections and outcome among hospitalized South Africans with systemic lupus erythematosus. Clin. Rheumatol. 2015;34(3):479-488. doi: 10.1007/s10067-014-2847-0.
8. Bosch X., Guilabert A., Pallares L. et al. Infections in systemic lupus erythematosus: a prospective and controlled study of 110 patients. Lupus. 2006; 15(9):584-589. doi: 10.1177/0961203306071919.
Lupus. 2006; 15(9):584-589. doi: 10.1177/0961203306071919.
9. Samotij D., Reich A. Biologics in the Treatment of Lupus Erythematosus: A Critical Literature Review. Biomed. Res. Int. 2019; 2019:8142368. doi: 10.1155/2019/8142368.
Системная красная волчанка
«Не тратьте силы, возьмите молоток побольше» Закон силы Энтони
Эритема на лице
ДИАГНОСТИКА
• Общий анализ крови.• Общий анализ мочи.
• LE-клетки.
• Антитела антинуклеарные, к двуспиральной ДНК.
• Антитела к кардиолипину.
• Липидограмма, гликемия, креатинин, рСКФ.
• Рентгенография грудной клетки.
• Биопсия почки.
• Шкала SLEDAI: 0 — ремиссия, ≤4 — низкая активность.
Дискоидная сыпь
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ (EULAR/ACR, 2019)
Антитела антинуклеарные ≥1:80 на HEp-2 клетках (или эквивалентный тест) +• Лихорадка >38°C: 2 балла.

• Лейкопения <4•109/л: 3 балла.
• Тромбоцитопения <100•1012/л: 4 балла.
• Аутоиммунный гемофтиз: 4 балла.
• Делирий: 2 балла.
• Психоз: 3 балла.
• Судроги: 5 баллов.
• Нерубцовая алопеция: 2 балла.
• Язвы в полости рта: 2 балла.
• Подострая кожная или дискоидная волчанка: 4 балла.
• Острая кожная волчанка: 6 баллов.
• Плевральный или перикардиальный выпот: 5 баллов.
• Острый перикардит: 6 баллов.
• Поражение суставов: 6 баллов.
• Протеинурия >0.5 г/сут: 8 балла.
• Волчаночный нефрит II или V класса по биопсии: 8 баллов.
• Волчаночный нефрит III или IV класса по биопсии: 10 баллов.
• Антифосфолипидные антитела (к кардиолипину, β2GP1, волчаночный антикоагулянт): 2 балла.
• Низкие С3 или С4 системы комплемента: 2 балла.
• Низкие С3 и С4 системы комплемента: 3 балла.
• Антитела к dsDNA или Smith: 6 баллов.
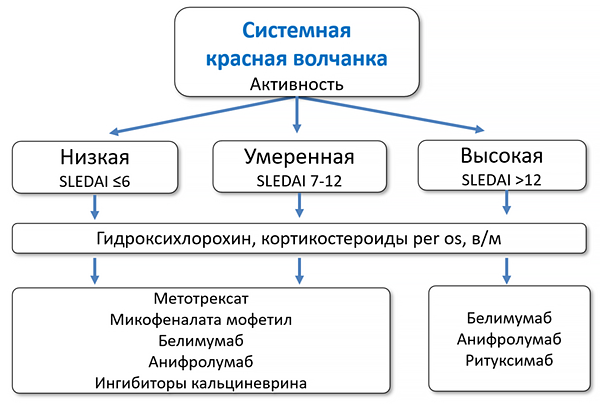
Ds системной красной волчанки: ≥10 баллов.
Распространенность системной красной волчанки и возраст
Rees F, et al. Ann Rheum Dis. 2016;75:136–41.
КЛАССИФИКАЦИЯ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКИ
• Течение: острое, подострое, хроническое.• Фаза: активная (I–III степени), ремиссия.
• Клинико-морфологическое поражение: cимптом «бабочки», капилляриты, кожная пурпура, дискоидная волчанка, полиартрит, плеврит, перикардит, миокардит, нефрит, менингоэнцефалит, полирадикулоневрит, полинейропатия.
Риск инфаркта миокарда при системной красной волчанке
Chou C, et al. Int J Cardiol. 2014;174:751–3.
ФОРМУЛИРОВКА ДИАГНОЗА
□ Системная красная волчанка, острая. [M32.1]□ Системная красная волчанка, хроническая, мембранозный гломерулонефрит, ХБП C2. [M32.1]
□ Системная красная волчанка, ремиссия.
 [M32.1]
[M32.1]Лечение системной красной волчанки без нефрита (EULAR, 2019)
ЛЕЧЕНИЕ
• Гидроксихлорохин.• Кортикостероиды: преднизолон, метилпренизолон.
• Цитостатики: азатиоприн, метотрексат, микофенолата мофетил, циклофосфамид.
• Ингибиторы кальциневрина: такролимус, циклоспорин.
• Биологические препараты: белимумаб, ритуксимаб.
Динамика смертности от системной красной волчанки
Yen E, et al. Ann Int Med. 2017;167:777–85.
ПОКАЗАНИЯ ДЛЯ НАЗНАЧЕНИЯ ИММУНОДЕПРЕССАНТОВ (Kelley’s Textbook of Rheumatology)
Общие• Поражение важных органов или выраженное поражение других органов, рефрактерное к лечению первой линии.
• Недостаточный ответ или невозможность лечения кортикостероидами в приемлемых дозах длительное время.
Локальные
• Пролиферативный или мембранозный нефрит (нефритический или нефротический синдром).
• Тяжелая тромбоцитопения <20•109/л.
• Тромботическая тромбоцитопеническая пурпура.
• Тяжелая гемолитическая или апластическая анемия, или иммунная нейтропения без эффекта кортикостероидов.
• Волчаночный пневмонит или альвеолярные геморрагии.
• Миокардит со сниженной функцией левого желудочка, перикардит с угрожающей тампонадой.
• Абдоминальный васкулит.
• Поперечный миелит, церебрит, психоз рефрактерные к котикостероидам, множественный мононеврит, тяжелая периферическая нейропатия.
Частота атеросклеротических бляшек при системной красной волчанке
Roman M, et al, 2003.
Лечение системной красной волчанки в Израиле
Врачи Топ Ихилов – это специалисты, обладающие богатейшим опытом в лечении различных заболеваний, даже сложных системных поражений, таких как красная волчанка. Ревматологи нашей клиники достигают поразительных успехов в борьбе с тяжелыми системными заболеваниями благодаря не только своим знаниям и навыкам, но и передовому оборудованию, а также применяемым прогрессивным методикам и постоянному внедрению новых, более эффективных. Как результат – устранение осложнений патологии на долгие годы и повышение качества жизни пациента.
Как результат – устранение осложнений патологии на долгие годы и повышение качества жизни пациента.
Методы лечения, или как наши врачи побеждают болезнь
Поскольку красная волчанка является системным заболеванием, поражающим многие органы и системы органов, то и лечение ее требует комплексного подхода.
- Медикаментозное лечение направлено как на купирование симптомов болезни, так и на коррекцию активности иммунной системы. Воспалительные процессы, болезненные ощущения, отечность устраняют с помощью глюкокортикостероидов – стероидных гормонов коры надпочечников. Их назначают в период обострения болезни: вначале – в ударных дозах, которые в дальнейшем постепенно снижают. Стероидные препараты в небольших поддерживающих дозах пациент может принимать в течение нескольких месяцев или даже лет. Для профилактики тромбозов и изъязвлений назначают антималярийные препараты, которые также устраняют кожные проявления болезни (сыпь), снимают болевые ощущения.
 Иммунодепрессанты применяют для регуляции работы иммунной системы. Моноклональные антитела, разработанные специально для лечения красной волчанки, являются инновационными и эффективными препаратами, поскольку их воздействие направлено на угнетение выработки антител, атакующих собственные клетки организма.
Иммунодепрессанты применяют для регуляции работы иммунной системы. Моноклональные антитела, разработанные специально для лечения красной волчанки, являются инновационными и эффективными препаратами, поскольку их воздействие направлено на угнетение выработки антител, атакующих собственные клетки организма. - Лечение системной красной волчанки в Израиле стволовыми клетками. Не созревшие клетки костного мозга пациента вводят в поврежденный участок. Благодаря их свойству перерождаться в любые клетки организма происходит стимуляция регенеративных процессов и восстановление тканей в очаге патологии.
- Экстракорпоральная детоксикация подразумевает очищение крови от токсических веществ. С этой целью применяют плазмаферез и гемосорбцию – оба метода осуществляются вне организма, с использованием специальных аппаратов. Отличие состоит в том, что при плазмаферезе из крови выделяют плазму, которая содержит токсины, и заменяют ее плазмозаменителями. А гемосорбция – это внепочечное очищение крови с помощью специальных сорбентов, удерживающих токсические вещества, без отделения от нее плазмы.

Диагностика системной красной волчанки в Израиле
День 1-й – диагностика в Топ Ихилов начинается с консультации врача
В день приезда пациент попадает на прием к ведущему ревматологу нашей клиники – без ожиданий в очередях и задержек. Врач собирает анамнез, изучает предоставленные пациентом результаты диагностических обследований, если он уже проходил диагностику, назначает дообследование для точной идентификации болезни.
День 2-й – инструментальная и лабораторная диагностика
Диагностика системной красной волчанки в Израиле проходит с применением ультрасовременной техники и передовых методик.
- Люмбальная пункция.
- Биопсия кожи.
- ПЭТ-КТ внутренних органов.
- Иммунологическое исследование крови на наличие антител.
- Анализы крови на выявление волчаночных LE-клеток.
- Исследование синовиальной жидкости.
- Рентгенографическое исследование суставов.
- Тесты «панель коллагенозов».
- Стресс-эхокардиография.

- Допплеровское исследование сосудов.
День 3-й – комиссия врачей принимает решение по программе терапии
Во избежание врачебной ошибки решение о заключительном диагнозе и программе терапии принимает консилиум врачей – ревматолог, нефролог, невролог, гематолог, офтальмолог, кардиолог. Изучив данные диагностических исследований, специалисты сообща составляют больному индивидуальный план лечения.
Лечение системной красной волчанки в Израиле: цены
Пациенты при выборе зарубежной клиники учитывают не только высокое качество предоставления медицинских услуг, но и их стоимость. И отдают предпочтение медицинским центрам с оптимальным и разумным соотношением цена – качество, а именно – израильским клиникам. Поскольку цены в Израиле и в частности в МЦ Топ Ихилов на 30-50% ниже, чем в медицинских учреждениях Западной Европы и США.
Узнать стоимость лечения системной красной волчанки в Израиле вы можете на нашем сайте или у наших консультантов, которые рассчитают вам стоимость вашей программы диагностики и терапии. Просто позвоните нам по телефону или заполните онлайн-заявку. Мы всегда на связи.
Просто позвоните нам по телефону или заполните онлайн-заявку. Мы всегда на связи.
Выбирайте Топ Ихилов – мы возвращаем здоровую жизнь
Лечение системной красной волчанки в Израиле: отзывы пациентов говорят без прикрас о наших преимуществах – о талантливых врачах, о суперсовременном, невиданном ими в отечественных клиниках оборудовании, о доступных ценах.
- Наши ревматологи – настоящие ассы в лечении системных заболеваний организма.
- Один из главных этапов терапии – 100% точная диагностика как залог грамотного побора терапевтической программы и успешного лечения.
- В нашей клинике применяются передовые, разрабатываются новые и внедряются революционные методики и технологии.
- Доступные цены без предоплаты и комиссий.
- 24-часовая забота сотрудников международного отдела. Мы решаем все ваши проблемы быстро и без дополнительных расходов с вашей стороны.
- 5
- 4
- 3
- 2
- 1
 8 из 5)
8 из 5)Кишечный микробиом и системная красная волчанка
Кишечный микробиом и системная красная волчанкаЗащитные эффекты потребления пробиотиков при сердечно-сосудистых заболеваниях при системной красной волчанке
Néstor de la Visitación, Iñaki Robles-Vera, Marta Toral, Juan Duarte.
Protective Effects of Probiotic Consumption in Cardiovascular Disease in Systemic Lupus Erythematosus.
Nutrients 2019, 11(11), 2676
Резюме: Распространенность почечных и сердечно-сосудистых заболеваний (ССЗ) у пациентов с системной красной волчанкой (СКВ) выше, чем в общей популяции. Недавно была описана причинная роль кишечной микробиоты в развитии иммунных реакций при СКВ. Потребление пробиотиков изменяет состав кишечной микробиоты, предотвращая прогрессирование СКВ. Целью данного обзора является изучение роли кишечной микробиоты в развитии почечных и сердечно-сосудистых заболеваний при СКВ и того, как пробиотики могут быть терапевтическим вариантом. Несмотря на убедительные данные о положительном влиянии пробиотиков при развитии аутоиммунитета и нефрита при СКВ, только в нескольких исследованиях описано защитное действие Lactobacillus на важные факторы риска сердечно-сосудистых заболеваний, такие как дисфункция эндотелия и гипертония у мышей. Профилактические эффекты пробиотиков при почечной и сердечно-сосудистых заболеваниях у людей еще не установлены.
Целью данного обзора является изучение роли кишечной микробиоты в развитии почечных и сердечно-сосудистых заболеваний при СКВ и того, как пробиотики могут быть терапевтическим вариантом. Несмотря на убедительные данные о положительном влиянии пробиотиков при развитии аутоиммунитета и нефрита при СКВ, только в нескольких исследованиях описано защитное действие Lactobacillus на важные факторы риска сердечно-сосудистых заболеваний, такие как дисфункция эндотелия и гипертония у мышей. Профилактические эффекты пробиотиков при почечной и сердечно-сосудистых заболеваниях у людей еще не установлены.
Системная красная волчанка (СКВ) — это хроническое аутоиммунное заболевание, характеризующееся аномально функционирующими В-лимфоцитами [1], которые способствуют усиленному производству аутоантител, которые вызывают образование и отложение иммунных комплексов, которые повреждают многие органы и ткани [2]. Хотя причины этого неизвестны, широко распространено мнение, что СКВ является следствием воздействия факторов окружающей среды на людей с генетической предрасположенностью, приводящих к нарушению самотолерантности и к активации / увеличению врожденных иммунных клеток и аутореактивных лимфоцитов [3].
СКВ ассоциируется с заболеваниями почек и сердечно-сосудистой системы (ССЗ) [4]. В частности, считается, что артериальная гипертензия является наибольшим фактором риска сердечных осложнений в популяциях волчанки [5]. Фактически, от 33% до 74% пациентов с СКВ, как было описано, имеют гипертонию [6]. Тем не менее, патофизиологические механизмы, способствующие развитию СКВ-гипертензии, изучены недостаточно [7]. Несколько исследований с использованием самок мышей NZB / WF1, спонтанной модели СКВ, которая имитирует болезнь человека и развивает гипертонию, продемонстрировали, что в патогенез гипертонии вносят вклад несколько факторов, включая воспалительные цитокины, фактор некроза опухоли TNF-α и окислительный стресс. Эти медиаторы, способствующие локальному воспалению и последующей почечной и сосудистой дисфункции [8, 9, 10], вероятно, являются следствием первичной дисрегуляции иммунной системы [11]. Артериальная гипертензия связана с инфильтрацией иммунных клеток в адвентицию и периадвентициальный жир, а также с активацией Т-клеток, которые выделяют провоспалительные цитокины, такие как интерлейкин IL-17a, интерферон IFN-γ и TNF-α [12, 13]. Однако Т, а не В-клетки играют ключевую роль в модуляции артериального давления в ответ на опосредованную ангиотензином II гипертонию [12]. Гипертония у самок мышей NZB / WF1 связана с низким содержанием ренина в плазме и не чувствительна к соли. В этой модели СКВ у мышей лечение анти-CD20 антителом, которое снижало процентное содержание В-клеток в селезенке и количество анти-двухцепочечных ДНК антител (анти-dsDNA) в плазме, предотвращало развитие артериальной гипертензии [14]. Это исследование подчеркивает важность B-клеток в прогрессировании СКВ-гипертензии. Однако точная роль гиперактивных Т-лимфоцитов и В-лимфоцитов, являющихся центральными для развития аутоиммунных нарушений, в патогенезе гипертонии остается неясной. Некоторые исследования показывают, что иммунные клетки, окислительный стресс и воспаление связаны в самосохраняющемся цикле, который значительно способствует повреждению почек и сосудистым заболеваниям, связанным с гипертонией при СКВ [8]. Активация Т-клеток происходит во вторичных лимфоидных органах и локально в органах-мишенях, особенно в почках и кровеносных сосудах.
Однако Т, а не В-клетки играют ключевую роль в модуляции артериального давления в ответ на опосредованную ангиотензином II гипертонию [12]. Гипертония у самок мышей NZB / WF1 связана с низким содержанием ренина в плазме и не чувствительна к соли. В этой модели СКВ у мышей лечение анти-CD20 антителом, которое снижало процентное содержание В-клеток в селезенке и количество анти-двухцепочечных ДНК антител (анти-dsDNA) в плазме, предотвращало развитие артериальной гипертензии [14]. Это исследование подчеркивает важность B-клеток в прогрессировании СКВ-гипертензии. Однако точная роль гиперактивных Т-лимфоцитов и В-лимфоцитов, являющихся центральными для развития аутоиммунных нарушений, в патогенезе гипертонии остается неясной. Некоторые исследования показывают, что иммунные клетки, окислительный стресс и воспаление связаны в самосохраняющемся цикле, который значительно способствует повреждению почек и сосудистым заболеваниям, связанным с гипертонией при СКВ [8]. Активация Т-клеток происходит во вторичных лимфоидных органах и локально в органах-мишенях, особенно в почках и кровеносных сосудах. Презентация неоантигена усиливается окислительным стрессом в антигенпрезентирующих клетках посредством продукции изокеталей (высокореактивных гамма-кетоальдегидов – ред.), которые усиливают воспалительные реакции. Эффекторные механизмы, вызываемые цитокинами, включают фиброз, вазоконстрикцию и дисбаланс Na+ / H+ (рис. 1).
Презентация неоантигена усиливается окислительным стрессом в антигенпрезентирующих клетках посредством продукции изокеталей (высокореактивных гамма-кетоальдегидов – ред.), которые усиливают воспалительные реакции. Эффекторные механизмы, вызываемые цитокинами, включают фиброз, вазоконстрикцию и дисбаланс Na+ / H+ (рис. 1).
Рисунок 1. Схема, представляющая аутоиммунные механизмы, участвующие в развитии почечных и сосудистых изменений. AngII, ангиотензин II; ET-1, эндотелин-1; IFN-γ, интерферон-γ; IL-17a, интерлейкин 17a; NF-kB, ядерный фактор-kB; ROS, активные формы кислорода; Treg, регуляторные T-клетки (модифицированный из [10]).
Однако, хотя традиционные факторы риска, связанные с атеросклерозом, включая гипертонию, присутствуют у больных волчанкой, они не полностью объясняют высокую частоту ишемических событий, о которых сообщалось до настоящего времени [15]. Это подразумевает, что другие факторы, присущие самой болезни, вносят вклад в сердечно-сосудистую нагрузку, наблюдаемую у этих пациентов, такую как клинические, генетические и иммунологические факторы. Длительность заболевания, хроническое повреждение органов и активность заболевания являются важными клиническими факторами развития ССЗ в условиях СКВ. Генетические данные об атеросклерозе, связанном с волчанкой, довольно скудны. Присутствие аллеля rs10181656 (G) сигнального преобразователя и активатора фактора транскрипции 4 (STAT-4) или преобладание минорного аллеля A и генотипа AA варианта rs12583006 B-клеточного активирующего фактора (BAFF) придавали повышенную восприимчивость к артериальным событиям и ишемическому цереброваскулярному заболеванию в контексте СКВ. Дисбаланс между повреждением эндотелия в результате нескольких инсультов (отложение окислительных липопротеинов низкой плотности oxLDL, аутоантител, интерферона типа I (IFNs), нейтрофильных внеклеточных ловушек NETs) и атеропротективными механизмами, по-видимому, является центральным событием для иммунологических факторов, способствующих атеросклерозу в условиях волчанки [16].
Длительность заболевания, хроническое повреждение органов и активность заболевания являются важными клиническими факторами развития ССЗ в условиях СКВ. Генетические данные об атеросклерозе, связанном с волчанкой, довольно скудны. Присутствие аллеля rs10181656 (G) сигнального преобразователя и активатора фактора транскрипции 4 (STAT-4) или преобладание минорного аллеля A и генотипа AA варианта rs12583006 B-клеточного активирующего фактора (BAFF) придавали повышенную восприимчивость к артериальным событиям и ишемическому цереброваскулярному заболеванию в контексте СКВ. Дисбаланс между повреждением эндотелия в результате нескольких инсультов (отложение окислительных липопротеинов низкой плотности oxLDL, аутоантител, интерферона типа I (IFNs), нейтрофильных внеклеточных ловушек NETs) и атеропротективными механизмами, по-видимому, является центральным событием для иммунологических факторов, способствующих атеросклерозу в условиях волчанки [16].
В настоящее время лечение и управление СКВ в основном базируется на нестероидных противовоспалительных препаратах, глюкокортикоидах, гидроксихлорохине и иммуносупрессивных агентах [17]. Прогресс в лечении СКВ привел к значительному улучшению прогноза. Тем не менее, лечение СКВ является сложной задачей из-за неблагоприятных последствий традиционной терапии и возникновения рефрактерных заболеваний. В действительности, кортикостероиды и терапии азатиоприна были связаны с повышенной частотой сердечно-сосудистых заболеваний у больных волчанкой. Поэтому существует настоятельная необходимость в новых стратегиях лечения, которые позволили бы нам лечить почечные и сердечно-сосудистые заболевания у пациентов с волчанкой без ущерба для состояния их здоровья.
Прогресс в лечении СКВ привел к значительному улучшению прогноза. Тем не менее, лечение СКВ является сложной задачей из-за неблагоприятных последствий традиционной терапии и возникновения рефрактерных заболеваний. В действительности, кортикостероиды и терапии азатиоприна были связаны с повышенной частотой сердечно-сосудистых заболеваний у больных волчанкой. Поэтому существует настоятельная необходимость в новых стратегиях лечения, которые позволили бы нам лечить почечные и сердечно-сосудистые заболевания у пациентов с волчанкой без ущерба для состояния их здоровья.
Таким образом, различные исследования показали, что дисбиоз кишечного микробиома был связан с аутоиммунными заболеваниями, такими как диабет 1 типа, воспалительное заболевание кишечника, ревматоидный артрит и рассеянный склероз. Однако мало известно о роли кишечной микробиоты при СКВ как у животных, так и у людей [18, 19, 20]. Таким образом, следует учитывать включение пробиотических добавок в управление риском сердечно-сосудистых заболеваний. Фактически, добавление в течение длительного периода времени мультивидовых пробиотических смесей оказывает благоприятное и дозозависимое влияние на функцию печени и липидный профиль в модели на крысах, а также может оказывать благоприятное влияние на сердечно-сосудистые нарушения [21].
Фактически, добавление в течение длительного периода времени мультивидовых пробиотических смесей оказывает благоприятное и дозозависимое влияние на функцию печени и липидный профиль в модели на крысах, а также может оказывать благоприятное влияние на сердечно-сосудистые нарушения [21].
Кроме того, манипулирование кишечной микробиотой может привести к разработке новых методов лечения у больных СКВ.
В частности, мы рассматриваем изменения в микробиоте, связанной с СКВ, и обсуждаем современные знания о влиянии пробиотиков с иммуномодулирующими свойствами на развитие почечной и сердечно-сосудистой патологии на животных моделях и на людских волчанках в качестве новых методов лечения.
2. Кишечная микробиота и системная красная волчанкаМикробиом млекопитающих состоит из уникального набора микроорганизмов (то есть бактерий, архей, грибов и вирусов), связанных с различными нишами в теле и на теле. В микробиоте кишечника преобладают Firmicutes и Bacteroidetes и, в меньшей степени, Actinobacteria, Proteobacteria, Synergistetes, Verrucomicrobia и Fusobacteria. Тем не менее, кишечная микробиота постоянно адаптируется к изменениям образа жизни, таким как диета, гормоны и физические упражнения [22]. В последние годы было выявлено несколько параметров здоровья и заболеваний, связанных с изменениями в микробиоме кишечника человека.
Тем не менее, кишечная микробиота постоянно адаптируется к изменениям образа жизни, таким как диета, гормоны и физические упражнения [22]. В последние годы было выявлено несколько параметров здоровья и заболеваний, связанных с изменениями в микробиоме кишечника человека.
2.1. Дисбиоз у больных системной красной волчанкой
Здоровую кишечную микробиоту человека трудно идентифицировать, принимая во внимание ее индивидуальную изменчивость и пластичность. Тем не менее, экологические параметры микробной стабильности, такие как богатство и разнообразие, часто используются в качестве показателей здоровья кишечника, поскольку они обратно связаны с хроническими заболеваниями [23]. Волчанка была связана с несколькими изменениями в микробиоте кишечника (таблица 1), которые могут быть связаны с проявлениями патологии. Тем не менее, эти изменения еще не до конца понятны, поскольку существуют различия между людьми из разных стран [24]. Были описаны противоречивые результаты, связывающие СКВ с изменениями экологических параметров, таких как богатство и разнообразие. На самом деле, He et al. [24] показали значительно более низкое альфа-разнообразие (филогенетическое разнообразие (PD) всего дерева и наблюдаемых видов) у пациентов с СКВ, без различий по Шеннону (Shannon) или Симпсону (Simpson). Согласно этому, Li et al. [25] описали снижение показателей разнообразия как Chao (видового богатства) и наблюдаемых видов у пациентов с СКВ. В отличие от Hevia et al. [18] не обнаружили существенных различий ни в каких показателях альфа-разнообразия (Chao, PD всего дерева, наблюдаемые виды, индексы Шеннона и Симпсона). Возможно, эти несоответствия могут быть объяснены влиянием пола, возраста, прогрессирования заболевания и генетического фона.
На самом деле, He et al. [24] показали значительно более низкое альфа-разнообразие (филогенетическое разнообразие (PD) всего дерева и наблюдаемых видов) у пациентов с СКВ, без различий по Шеннону (Shannon) или Симпсону (Simpson). Согласно этому, Li et al. [25] описали снижение показателей разнообразия как Chao (видового богатства) и наблюдаемых видов у пациентов с СКВ. В отличие от Hevia et al. [18] не обнаружили существенных различий ни в каких показателях альфа-разнообразия (Chao, PD всего дерева, наблюдаемые виды, индексы Шеннона и Симпсона). Возможно, эти несоответствия могут быть объяснены влиянием пола, возраста, прогрессирования заболевания и генетического фона.
Таблица 1. Изменения кишечной микробиоты у пациентов с системной красной волчанкой (СКВ).
Пациенты | Отно-шение F/B | Альфа-разнообра-зие | Тип | Семья | Род | Вид | |
Женщины C | ↓F/B | нет изменений | ↓Firmicutes | ↓Lachnospiraceae | 18 | ||
Женщины A | ↓F/B |
↓Наблюда-емые виды | ↓Firmicutes ↑Bacteroidetes ↑Actinobacteria ↑Proteobacteria | ↑Bacteroidaceae | ↓Pseudobutyvibrio | 24 | |
Women A | ↓F/B | ↓Видовое богатство (Chao) | ↓Tenericutes | ↑Streptococcaceae ↑Lactobacillaceae | ↓Mollicutes | ↑Streptococcus anginosus mucosae | 25 |
Женщины | нет изме-нений | ↑Proteobacteria | ↑Blautia | 26 | |||
Женщины | ↓ Видовое богатство (Chao) | ↓Ruminococcaceae | ↑Blautia | ↓Ruminococcus gnavus | 27 |
C, европеоид; AA, афроамериканец; A, азиат; WH, белый латиноамериканец; BH, Черный латиноамериканец; F/B, фирмикуты/бактероиды. ↓ Уменьшение, ↑ Увеличение
Когда микробиота была более глубоко проанализирована, авторы обнаружили определенные различия, которые могли бы объяснить ее роль в СКВ. На уровне типов, по-видимому, наблюдается явное увеличение Bacteroidetes, Actinobacteria и Proteobacteria и сокращение Firmicutes у пациентов с СКВ, при этом эти изменения стабильны между пациентами разных стран [24]. Недавно было описано снижение тенерикутов (Tenericutes) и повышение количества фузобактерий (Fusobacteria) при СКВ [25]. В целом, эти изменения характеризуются дисбактериозом кишечника, связанным с изменением соотношения Firmicutes / Bacteroidetes (F / B) (увеличение Bacteroidetes и уменьшение Firmicutes), хотя некоторые авторы не обнаружили существенных различий в этом параметре между СКВ и здоровыми пациентами [26]. На уровне семьи пациенты с СКВ из разных исследований представили разные результаты. He et al. [24] описали, как у пациентов с СКВ в Испании было выявлено истощение Lachnospiraceae и Ruminococcaceae и обогащение Bacteroidaceae и Prevotellaceae, но у больных СКВ из Китая только Prevotellaceae показали значительное увеличение [24]. Кроме того, рикенеллы (Rikenellaceae), стрептококки (Streptococcaceae), лактобациллы (Lactobacillaceae) и мегасферы (Megasphaera) могут усиливать СКВ.
На уровне типов, по-видимому, наблюдается явное увеличение Bacteroidetes, Actinobacteria и Proteobacteria и сокращение Firmicutes у пациентов с СКВ, при этом эти изменения стабильны между пациентами разных стран [24]. Недавно было описано снижение тенерикутов (Tenericutes) и повышение количества фузобактерий (Fusobacteria) при СКВ [25]. В целом, эти изменения характеризуются дисбактериозом кишечника, связанным с изменением соотношения Firmicutes / Bacteroidetes (F / B) (увеличение Bacteroidetes и уменьшение Firmicutes), хотя некоторые авторы не обнаружили существенных различий в этом параметре между СКВ и здоровыми пациентами [26]. На уровне семьи пациенты с СКВ из разных исследований представили разные результаты. He et al. [24] описали, как у пациентов с СКВ в Испании было выявлено истощение Lachnospiraceae и Ruminococcaceae и обогащение Bacteroidaceae и Prevotellaceae, но у больных СКВ из Китая только Prevotellaceae показали значительное увеличение [24]. Кроме того, рикенеллы (Rikenellaceae), стрептококки (Streptococcaceae), лактобациллы (Lactobacillaceae) и мегасферы (Megasphaera) могут усиливать СКВ. Эти изменения на уровне семьи и типа связаны с изменениями на уровне родов. На уровне родов мы можем выделить изменения в Pseudobutyvibrio, Dialister, Lactobacillus, Bifidobacterium, Mollicutes, RF39, Faecalobacterium, Cryptophyta и Roseburia, которые истощаются у пациентов с СКВ. С другой стороны, роды Rhodococcus, Eggerthella, Klebsiella, Prevotella, Eubacterium, Flavonifractor и Blautia обогащены при этой патологии [24, 25, 26]. Анализ микробиоты кишечника у пациентов с патологией в стадии ремиссии обнаружил увеличение в роде Bifidobacterium [25]. На видовом уровне некоторые виды были повышены в кишечной микробиоте СКВ [25], в частности, Streptococcus anginosus, Lactobacillus mucosae и Veinella dispar. Эти изменения сопровождались снижением Ruminococcus gnavus и Bacteroidesiformis [27].
Эти изменения на уровне семьи и типа связаны с изменениями на уровне родов. На уровне родов мы можем выделить изменения в Pseudobutyvibrio, Dialister, Lactobacillus, Bifidobacterium, Mollicutes, RF39, Faecalobacterium, Cryptophyta и Roseburia, которые истощаются у пациентов с СКВ. С другой стороны, роды Rhodococcus, Eggerthella, Klebsiella, Prevotella, Eubacterium, Flavonifractor и Blautia обогащены при этой патологии [24, 25, 26]. Анализ микробиоты кишечника у пациентов с патологией в стадии ремиссии обнаружил увеличение в роде Bifidobacterium [25]. На видовом уровне некоторые виды были повышены в кишечной микробиоте СКВ [25], в частности, Streptococcus anginosus, Lactobacillus mucosae и Veinella dispar. Эти изменения сопровождались снижением Ruminococcus gnavus и Bacteroidesiformis [27].
Это может быть важной вехой в этом вопросе, что Li et al. [25] обнаружили положительную корреляцию между индексом активности системной красной волчанки (SLEDAI) и количеством стрептококков (Streptococcus), Кампилобактерий (Campylobacter) и S.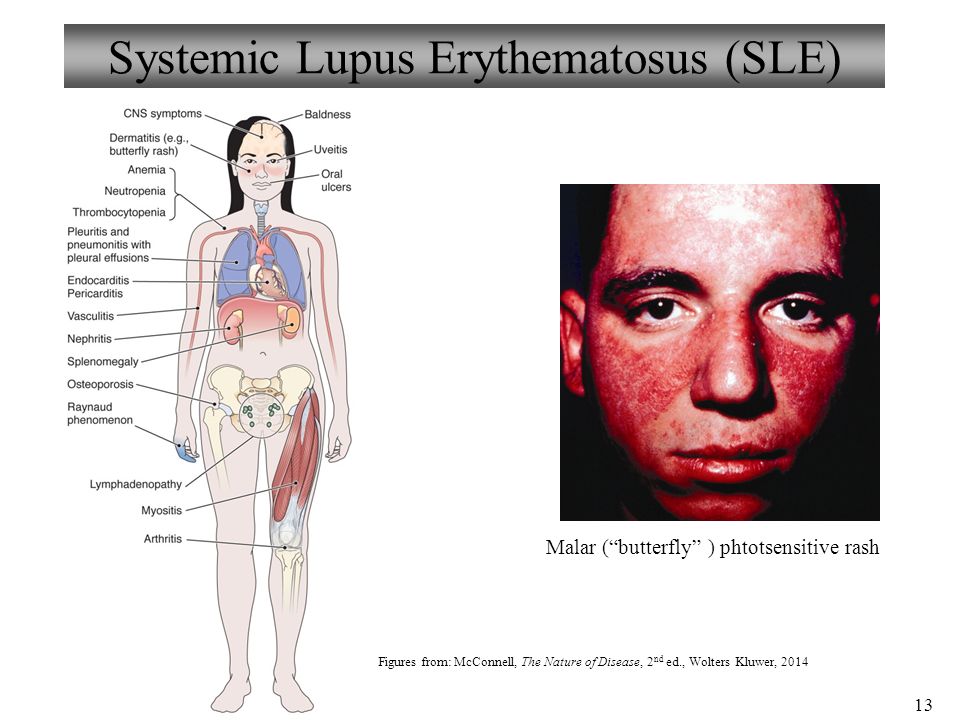 anginosus в фекальной пробе больных СКВ.
anginosus в фекальной пробе больных СКВ.
2.2. Дисбиоз у мышей с системной красной волчанкой
Изучая микробиоту на моделях животных, исследования выявили некоторые различия с людьми и даже между различными моделями животных (Таблица 2). Сосредоточив внимание на генетических моделях животных, были описаны изменения в составе микробиоты кишечника в ходе патологии; обнаружено более высокое разнообразие в NZB / WF1, MRL / Mp-Faslpr (lpr) и SNF1 и toll-подобном рецепторе TLR-7.1, когда СКВ уже установлена и даже на ранней стадии СКВ [26,28]. В последнее время не наблюдалось значительных изменений между самками мышей NZB / WF1 (33 недели) и контрольными мышами соответствующего возраста в отношении микробного богатства, разнообразия и равномерности [29]. Что касается соотношения фирмикутов к бактроидам (F/B), то консенсус не был достигнут, поскольку некоторые авторы обнаружили снижение этого параметра [20], но другие не обнаружили каких-либо изменений в мышах NZB/WF1 или lpr [26,29].
Таблица 2. Изменения кишечной микробиоты на разных моделях волчанки на животных.
Модели мышиной красной волчанки | Отно- шение F/B | Альфа- разно-образие | Тип | Семья | Род | Вид | |
NZB/WF1 | ↓F/B или отсутствие изменений | ↑α-разно-образие или отсутствие изменений | ↓Firmicutes ↑Bacteroidetes | Стадия, предшествующая SLE | 26 | ||
MRL/lpr | ↓F/B или отсутствие изменений | ↑α-разно-образие или отсутствие изменений | ↓Firmicutes ↑Bacteroidetes | ↓Lactobacillaceae | ↓Lactobacillus | 19 | |
SNF1 | ↓F/B или отсутствие изменений | ↑α-разно-образие | ↓Firmicutes ↑Bacteroidetes | ↑Rikenellaceae | Стадия, предшествующая SLE | 1 | |
TLR-7. | ↓F/B | ↑α-разно-образие | ↓Firmicutes ↑Bacteroidetes | ↓Clostridaceae | ↓Turicibacter | ↑Lactobacillus reuteri | 31 |
F/B, Firmicutes/Bacteroidetes; SLE, системная красная волчанка. ↓ Сокращение, ↑ Увеличение.
В целом, в моделях NZB/WF1, lpr и SNF1 и TLR-7.1 на уровне типа присутствуют изменения, которые аналогичны изменениям у пациентов-людей, а именно повышенным Bacteroidetes и уменьшенным Firmicutes. Тем не менее, основные изменения происходят в рамках таких подуровневых категорий, как семья и роды. На уровне семейства в модели мыши lpr было обнаружено снижение Lactobacillaceae и более высокое обилие Rikenellaceae, Desulfovibrionaceae, Ruminococcaceae, Lachnospiraceae или Streptococcaceae [19,28]. Эти изменения обычно связаны с изменениями в нескольких родах, таких как Tenericutes, Mollicutes, Butyrivibrio и Roseburia, которые были увеличены в этой модели. Напротив, другие роды были сокращены, такие как Lactobacillus или Bifidobacterium [28]. Кроме того, было обнаружено, что модулируется род Анаэростипес (Anaerostipes), который был отрицательно коррелирован с активностью волчанки [26]. Анаэростипес способен поддерживать состояние здоровья кишечника за счет способности производить бутират.
Эти изменения обычно связаны с изменениями в нескольких родах, таких как Tenericutes, Mollicutes, Butyrivibrio и Roseburia, которые были увеличены в этой модели. Напротив, другие роды были сокращены, такие как Lactobacillus или Bifidobacterium [28]. Кроме того, было обнаружено, что модулируется род Анаэростипес (Anaerostipes), который был отрицательно коррелирован с активностью волчанки [26]. Анаэростипес способен поддерживать состояние здоровья кишечника за счет способности производить бутират.
Кроме того, из этих изменений в модели SNF1, склонной к волчанке, авторы описали некоторые аналогичные изменения, описанные в других моделях на животных, такие как обилие Rikenellaceae или Lachnospiraceae [1]. Тем не менее, другие обнаружили различия в этой модели между стадиями, предшествующими заболеванию, и стадиями заболевания, демонстрируя повышенный уровень Lactobacillus, который обычно уменьшается на других моделях на животных и на людях. Другие роды, такие как Clostridium, Dehalobacterium, Oscillospira, Dorea и Bilophila, также могут быть повышены [26].
Другой основной животной моделью СКВ является NZB / WF1, в которой микробиота страдает изменениями, подобными lpr и людям, на уровнях типа, семейства и рода. У мышей NZB / WF1 в микробиоте кишечника обнаруживается более высокое содержание лактобацилл, что может быть связано с более тяжелыми клиническими признаками, особенно с нарушением системного аутоиммунитета и почечной функции [26]. У мышей с lpr некоторые бактерии из рода Anerostipes, такие как Akkermansia muciniphila, были значительно уменьшены от стадии, предшествующей заболеванию, до стадии заболевания, а также, по-видимому, уменьшены бактерии из рода Lactobacillus или Bifidobacterium [32]. Недавно у самок с гипертонической болезнью NZB / WF1 мы обнаружили, что кишечная микробиота этих мышей имела значительно более высокое содержание Pedobacter, Lactobacillus и Prevotella, чем контрольная группа соответствующего возраста, без изменений в других родах, таких как Bifidobacterium [29].
В последние годы была описана новая модель, модель TLR-7. 1, и микробиота была проанализирована Zegarra-Ruiz et al. [30]. Найденные изменения аналогичны найденным в других моделях животных. Микробиота характеризуется увеличением в семействах Coriobacteriaceae и Rikenallecea и уменьшением числа Clostridaceae. На уровне рода выделяются такие признаки у Prevotella и Desulfovibrio и уменьшается численность Turicibacter, Bifidobacterium, Coprobacillus и Anaerostipes. Наконец, они обнаружили увеличение вида Lactobacillus reuteri, который также был обнаружен в брыжеечных лимфатических узлах (MLNs), селезенке и печени, связывая его перемещение с развитием СКВ.
1, и микробиота была проанализирована Zegarra-Ruiz et al. [30]. Найденные изменения аналогичны найденным в других моделях животных. Микробиота характеризуется увеличением в семействах Coriobacteriaceae и Rikenallecea и уменьшением числа Clostridaceae. На уровне рода выделяются такие признаки у Prevotella и Desulfovibrio и уменьшается численность Turicibacter, Bifidobacterium, Coprobacillus и Anaerostipes. Наконец, они обнаружили увеличение вида Lactobacillus reuteri, который также был обнаружен в брыжеечных лимфатических узлах (MLNs), селезенке и печени, связывая его перемещение с развитием СКВ.
2.3. Дисбиоз кишечника при волчанке связан с синдромом «дырявой кишки», изменениями в популяциях иммунных клеток и сердечно-сосудистыми осложнениями
Помимо этих изменений, в микробиоте кишечника у пациентов и на животных моделях СКВ наблюдается изменение эпителия кишечного барьера, характеризующееся нарушением соединительных белков, таких как окклюдин, зонулин и клаудин, и увеличением проницаемости кишечника, измеряемой с помощью изотиоцианата флуоресцеина (FITC) [19]. Исследователи связывают эти изменения с течением СКВ, потому что некоторые бактерии и их структурные компоненты или продукты бактериального метаболизма могут проникать через кишечный эпителий и достигать крови и даже нескольких органов.
Исследователи связывают эти изменения с течением СКВ, потому что некоторые бактерии и их структурные компоненты или продукты бактериального метаболизма могут проникать через кишечный эпителий и достигать крови и даже нескольких органов.
Недавно Manfredo-Vieira et al. [31] показали, как Enterococcus gallinarum способен транслоцироваться из кишечника в печень и активировать продукцию анти-dsDNA антител через активацию TLR-7/8 у генетически предрасположенных хозяев ((NZW × BXSB) F1 мышей и пациентов с СКВ). Фактически, лечение антибиотиками предотвратило смертность в этой модели животных, подавило рост E. gallinarum в тканях и устранило патогенные аутоантитела и Т-клетки. Таким образом, Katz-Agranov et al. [32] обнаружили отрицательную корреляцию между уровнями Synergistetes в кишечнике и титрами антител к dsDNA в плазме крови и уровнем IL-6. IL-6 может способствовать как увеличению дифференцировки Т-хелпера Th27, так и продукции IL-17a, который является важным фактором аутоиммунитета при СКВ [33,34].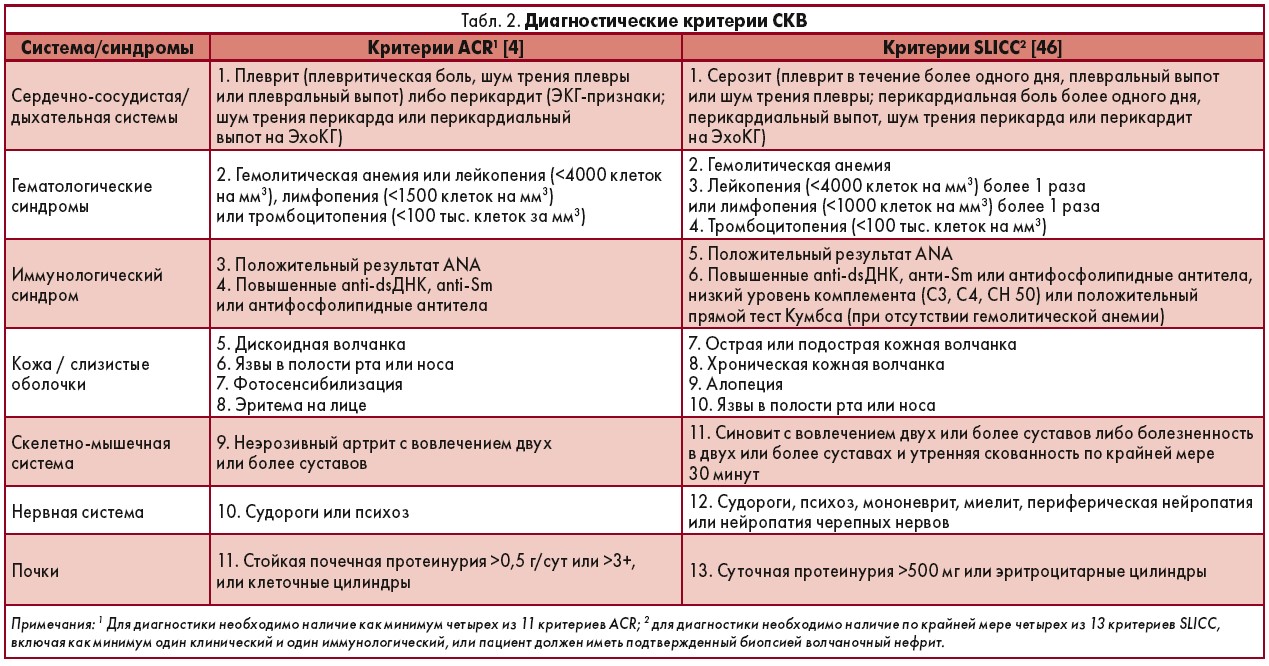 В связи с этим в исследованиях in vitro фекальная микробиота больных СКВ была более сильным индуктором Th27 [35].
В связи с этим в исследованиях in vitro фекальная микробиота больных СКВ была более сильным индуктором Th27 [35].
Помимо модуляции уровней антител к анти-dsDNA, бактерии могут модулировать иммунную систему другими способами, вызывая полезные или вредные эффекты в ходе СКВ. Другие возможные механизмы модуляции иммунной системы могут быть индуцированы компонентами бактерий, такими как липополисахарид (LPS), который происходит из стенки грамотрицательных бактерий, принадлежащих к Bacteroidetes (этот тип повышен в микробиоте кишечника мышей с СКВ), и, таким образом, через активацию TLR4, индуцируя продукцию провоспалительных цитокинов, таких как TNF-α, IL-6 и интерфероны типа I (IFN-α, IFN-γ), которые повышены у пациентов с СКВ, а также у животных модели СКВ [36].
IFN-α также может быть индуцирован через TLR-7, локус высокого риска для чрезмерной активации зондирования РНК, который чрезмерно экспрессируется при СКВ [31]. Этот высокий уровень IFN-α способен индуцировать эндотелиальную дисфункцию у больных СКВ [37]. Воспалительные цитокины взаимодействуют с важными регуляторными системами кровяного давления, такими как ренин–ангиотензиновая система и симпатическая нервная система [38]. Роль IL-6 конкретно не изучалась при СКВ-гипертензии. Показано также, что TNF-α повышен в сыворотке крови больных СКВ и может коррелировать с активностью заболевания [39]. Этанерцепт, клинически доступный рекомбинантный рецептор TNF-α, снижающий биологическую активность TNF-α, снижает среднее артериальное давление в модели СКВ у самок мышей, что позволяет предположить, что TNF-α механически способствует развитию гипертонии [40].
Воспалительные цитокины взаимодействуют с важными регуляторными системами кровяного давления, такими как ренин–ангиотензиновая система и симпатическая нервная система [38]. Роль IL-6 конкретно не изучалась при СКВ-гипертензии. Показано также, что TNF-α повышен в сыворотке крови больных СКВ и может коррелировать с активностью заболевания [39]. Этанерцепт, клинически доступный рекомбинантный рецептор TNF-α, снижающий биологическую активность TNF-α, снижает среднее артериальное давление в модели СКВ у самок мышей, что позволяет предположить, что TNF-α механически способствует развитию гипертонии [40].
Активация TLR4 также способствует повышению артериального давления и слабому сосудистому воспалению, которое проявляется у спонтанно гипертензивных крыс [41]. Фактически, TLR4 — / — мыши продемонстрировали полную защиту артериального давления от хронической эндотелиальной синтазы оксида азота (eNOS), вызванной блокадой гипертензии [42]. Бактериальный LPS стимулируют и усиливают экспрессию TLR4 в сосудистой системе, что приводит к увеличению продукции NADPH-оксидаз-зависимого супероксида, воспалению и эндотелиальной дисфункции [43,44]. Таким образом, повышенная активация TLR4 может быть связана с развитием и поддержанием артериальной гипертензии при СКВ. Фактически, повышенные уровни LPS в плазме крови ранее были описаны как у пациентов с СКВ [45,46,47], так и у мышей с гипертензивной СКВ [29].
Таким образом, повышенная активация TLR4 может быть связана с развитием и поддержанием артериальной гипертензии при СКВ. Фактически, повышенные уровни LPS в плазме крови ранее были описаны как у пациентов с СКВ [45,46,47], так и у мышей с гипертензивной СКВ [29].
Кроме того, некоторые бактерии продуцируют короткоцепочечные жирные кислоты (SCFAs), которые способны активировать рецепторы свободных жирных кислот с полезными [48] или вредными эффектами при патологии. Clostridium и Lachnospiraceae являются продуцентами бутирата, который посредством активации рецептора, связанного с G-белком GPR-109a, способствует дифференцировке регуляторных Т-клеток в толстой кишке, селезенке и лимфатических узлах, а также IL-18, следовательно, способен к подавлению воспаления [49]. С другой стороны, содержание ацетата и пропионата в образцах стула пациентов с СКВ, по-видимому, повышено, но Rodríguez-Carrio et al. [50] не обнаружили различий в уровнях бутирата. Эти изменения в продукции бактериальных побочных продуктов могут быть вызваны изменениями в некоторых метаболических путях. Пути деградации гликанов несколько завышены в микробиоте больных СКВ, вероятно, из-за более высокого обилия Bacteroidetes у этих пациентов [51]. Лечение ванкомицином показало снижение регуляции биосинтеза LPS [52].
Пути деградации гликанов несколько завышены в микробиоте больных СКВ, вероятно, из-за более высокого обилия Bacteroidetes у этих пациентов [51]. Лечение ванкомицином показало снижение регуляции биосинтеза LPS [52].
В настоящее время исследователи ищут способы модуляции микробиоты кишечника для улучшения прогноза этого заболевания. В соответствии с этим, некоторые бактерии могут коррелировать с этапами ремиссии в ходе патологии или даже с изменениями, проводимыми в некоторых методах лечения. Katz-Agranov et al. [32] доказали, что лечение ретинолом уменьшало Erysipelotrichaceae и увеличивало Lachnospiraceae и Rikenellaceae, восстанавливая некоторые изменения, наблюдаемые при волчанке. Лечение дексаметазоном или преднизоном [53] (глюкокортикоиды, широко применяемые у больных СКВ) позволило увеличить Альфа-разнообразие (индекс Шеннона), что может привести к более стабильному сообществу [26]. Лечение преднизоном позволило уменьшить количество типов Proteobacteria и Deferribacteres. Модуляция кишечной микробиоты индуцировала несколько изменений на уровне рода, которые характеризовались увеличением Prevotella и Anaerostipes и уменьшением Rikenella, Mucispirillum, Oscillospira и Bilophila [53].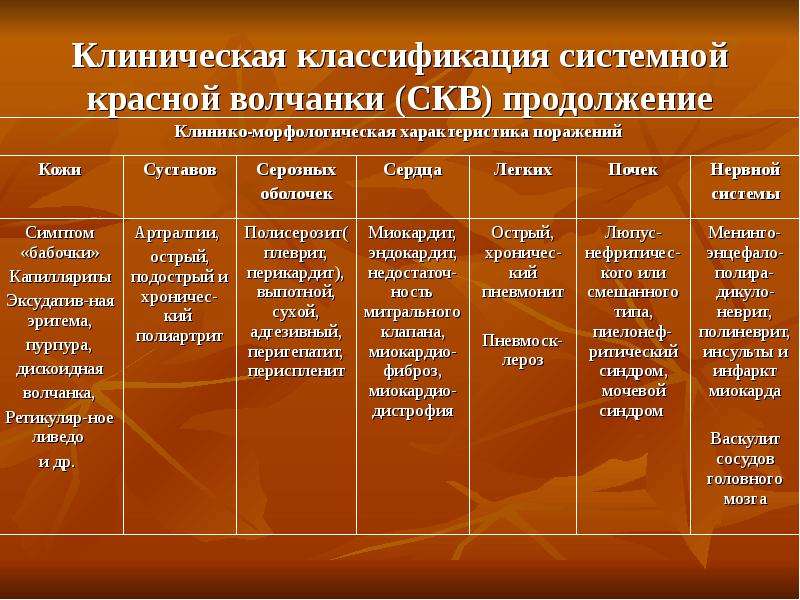 Антибактериальная терапия ванкомицином позволила удалить Clostridiales и Bacteroidales, одновременно увеличивая количество лактобацилл, таких как L. rhamnosus и L. reuteri [19].
Антибактериальная терапия ванкомицином позволила удалить Clostridiales и Bacteroidales, одновременно увеличивая количество лактобацилл, таких как L. rhamnosus и L. reuteri [19].
Таким образом, полученные данные свидетельствуют о том, что почечные и сердечно-сосудистые осложнения, связанные с СКВ, являются следствием иммунного ответа, усугубленного большим количеством антигенпрезентирующих бактерий, таких как Lachnospiraceae или Bacteroidetes, и снижением обилия Firmicutes в микробиоме кишечника, что приводит к снижению уровня бутирата, дисфункции Т-клеток и возникновению хронического воспаления и сердечно-сосудистого риска (Рис.2) [54]. Однако неясно, является ли дисбактериоз кишечника при СКВ причиной или следствием [35]. Современные данные свидетельствуют о том, что кишечные микробы могут быть вовлечены в инициацию и усиление аутоиммунных заболеваний, таких как СКВ. Несмотря на недавний прогресс в понимании того, как эти микробы влияют на патофизиологию волчанки, исследования все еще ограничены. Недавно была установлена связь между микробиотой кишечника, пулом свободных жирных кислот в сыворотке крови и биомаркерами активации эндотелия у больных волчанкой, что подчеркивает системный эффект кишечной микробиоты в этом состоянии [50]. Тем не менее, нет прямой связи между дисбиозом кишечника и эндотелиальной дисфункцией и гипертензией при СКВ. Возможно, что уменьшение поляризации Th27 за счет увеличения количества бактерий, продуцирующих бутират, или уменьшение эндотоксемии за счет улучшения целостности кишечника, или уменьшение продукции аутоантител как за счет уменьшения количества комменсальных бактерий, содержащих РНК-связывающий аутоантиген, структурные гомологи Ro60 [55], так и за счет предотвращения транслокации специфических бактерий, таких как Enterococcus gallinarum [31] или Lactobacillus reuteri [30] во вторичные лимфатические органы и печень, может предотвратить сердечно-сосудистые осложнения при СКВ.
Недавно была установлена связь между микробиотой кишечника, пулом свободных жирных кислот в сыворотке крови и биомаркерами активации эндотелия у больных волчанкой, что подчеркивает системный эффект кишечной микробиоты в этом состоянии [50]. Тем не менее, нет прямой связи между дисбиозом кишечника и эндотелиальной дисфункцией и гипертензией при СКВ. Возможно, что уменьшение поляризации Th27 за счет увеличения количества бактерий, продуцирующих бутират, или уменьшение эндотоксемии за счет улучшения целостности кишечника, или уменьшение продукции аутоантител как за счет уменьшения количества комменсальных бактерий, содержащих РНК-связывающий аутоантиген, структурные гомологи Ro60 [55], так и за счет предотвращения транслокации специфических бактерий, таких как Enterococcus gallinarum [31] или Lactobacillus reuteri [30] во вторичные лимфатические органы и печень, может предотвратить сердечно-сосудистые осложнения при СКВ.
Рисунок 2. Сдвиг микробиома в СКВ вызывает сердечно-сосудистый риск. У пациентов с СКВ было замечено, что уменьшение популяции Firmicutes, производящих бутират, приводит к снижению выработки бутирата. Это уменьшенное производство бутирата приводит к неспособности Т-клеток должным образом дифференцироваться у больных волчанкой, что приводит к индукции хронического воспалительного состояния, характерного для этого заболевания (модифицировано из [44]).
У пациентов с СКВ было замечено, что уменьшение популяции Firmicutes, производящих бутират, приводит к снижению выработки бутирата. Это уменьшенное производство бутирата приводит к неспособности Т-клеток должным образом дифференцироваться у больных волчанкой, что приводит к индукции хронического воспалительного состояния, характерного для этого заболевания (модифицировано из [44]).
Из-за вышеупомянутых открытий, и особенно из-за истощения Lactobacillus и Bifidobacterium в микробиоте кишечника, присутствующей в моделях СКВ lpr, исследователи считали, что лечение больных волчанкой с помощью бактериальных добавок (Таблица 3), таких как различные штаммы Lactobacillus, которые уже показали некоторые эффекты при других аутоиммунных заболеваниях [56,57], может помочь улучшить симптоматику заболевания. На самом деле Mu et al. [19] показали, что добавки с Lactobacillus spp. у мышей lpr проявляется поразительный эффект, смягчающий волчаночный нефрит и продлевающий выживаемость. Эти эффекты связаны со снижением уровней анти-dsDNA в плазме, вызванных потреблением пробиотиков.
Эти эффекты связаны со снижением уровней анти-dsDNA в плазме, вызванных потреблением пробиотиков.
Таблица 3. Пробиотические эффекты на разных моделях волчанки животных.
Пробиотик | Модель | Наблюдаемые эффекты | |
Lactobacillus delbrueckii subsp. lactis PTCC 1743 | ↓Th27 ↓IL-17a ↓Th2 ↓IFN-γ | ||
Lactobacillus rhamnosus ATCC 9595 | ↓RORγ ↓Th27 ↓Th2 ↓IFN-γ | ||
Ruminococcus obeum DSM25238 | In vitro | ↓Th27/Th2 соотношение | |
Blautia coccoides DSM935 | In vitro | ↓Th27/Th2 соотношение | |
Lactobacillus reuteri GMNL 263 | NZB/W F1 | ↑FoxP3 ↑Treg ↓TLR-4 ↓TLR-5 ↓TLR-7 ↓TLR-9 | |
↓IL-1β ↓TNF-α ↓IL-6 | |||
Bifidobacterium bifidum LMG13195 | In vitro | ↓ Активация Т-лимфоцитов | |
Lactobacillus fermentum CECT5716 | NZB/W F1 | ↓ В и Т лимфоциты ↓IL-17a ↓IFN-γ ↓TNF-α ↓IL-21 | |
Lactobacillus reuteri GMNL 89 | NZB/W F1 | ↓TLR-4 ↓TLR-5 ↓TLR-7 ↓TLR-9 | |
↓IL-1β ↓TNF-α ↓IL-6 | |||
Lactobacillus paracasei GMNL 32 | NZB/W F1 | ↓TLR-4 ↓TLR-5 ↓TLR-7 ↓TLR-9 | |
↓IL-1β ↓TNF-α ↓IL-6 | [63] |
FoxP3, белок, транскрипционный фактор развития регуляторных Т-клеток; IFN, интерферон; IL, интерлейкин; RORγ, RAR-related orphan receptor gamma; Th, T-хелпер; TLR, толл-подобный рецептор; TNF-α, фактор некроза опухоли альфа; Treg, регуляторная Т-клетка. ↓снижение, ↑увеличение.
↓снижение, ↑увеличение.
Эти микроорганизмы, которые в адекватных количествах могут принести пользу здоровью принимающего хозяина, получают название пробиотиков. Хотя некоторые ограничения должны применяться к этому термину согласно последней комиссии Международной научной ассоциации пробиотиков и пребиотиков (ISAPP), объединяющей только продукты, которые поставляют живые микроорганизмы с подходящим жизнеспособным количеством четко определенных штаммов с разумным ожиданием предоставления преимуществ для благополучия хозяина под этим названием [58]. Предыдущие данные показали, что пробиотические добавки могут быть эффективными в профилактике и лечении сердечно-сосудистых заболеваний у женщин в постменопаузе с ожирением. Фактически, добавление мультивидового пробиотика Ecologic® Barrier благоприятно модифицировало как функциональные, так и биохимические маркеры сосудистой дисфункции, снижало систолическое артериальное давление [59] и улучшало кардиометаболические параметры [60]. Эти защитные эффекты связаны с более низкими уровнями LPS в плазме, обнаруживаемыми у женщин с пробиотическими добавками. Однако до сих пор неизвестно, улучшает ли потребление пробиотиков эндотелиальную дисфункцию у больных СКВ.
Эти защитные эффекты связаны с более низкими уровнями LPS в плазме, обнаруживаемыми у женщин с пробиотическими добавками. Однако до сих пор неизвестно, улучшает ли потребление пробиотиков эндотелиальную дисфункцию у больных СКВ.
Физиологические реакции на различные пробиотики оказались последовательно разнообразными. Как правило, эти микроорганизмы вызывают иммунные сдвиги, которые эффективно уменьшают воспалительную реакцию, таким образом, улучшая симптоматику аутоиммунных заболеваний. Некоторые из наиболее часто наблюдаемых механизмов в лечении СКВ связаны с модуляцией Th27 и T регуляторных (Treg) популяций лимфоцитов [61]. Тем не менее, задействованы и другие, менее изученные механизмы.
Согласно Mardani et al. [61], введение пробиотика Lactobacillus delbrueckii subsp. Lactis PTCC 1743 на модели СКВ-мышей, индуцированных пристаном, смогло улучшить симптомы заболевания, уменьшая популяции Th27 и экспрессию одного из его основных цитокинов, IL-17a, хорошо известного как важнейшего элемента в развитии и поддержании воспаления. В дополнение к этому, другой пробиотический микроорганизм, Lactobacillus rhamnosus ATCC 9595, продемонстрировал способность модулировать гамма-рецептор, связанный с рецептором ретиноевой кислоты (RORγ), транскрипционный фактор, участвующий в созревании лимфоцитов Th27, что объясняет способность уменьшать эту лимфоцитарную популяцию. Оба пробиотика были также способны уменьшать популяции Th2 и его цитокин IFN-γ, который рассматривается как один из основных механизмов, участвующих в генерации воспалительного ответа.
С другой стороны, Lactobacillus reuteri GMNL 263 показал другой путь в генетической мышиной модели СКВ NZB/W F1 [62]. Этот микроорганизм может повышать экспрессию Treg-лимфоцитов и уровень транскрипционного фактора FoxP3. Эти клетки отвечают за регуляцию провоспалительных лимфоцитов, упомянутых выше, и имеют выраженный противовоспалительный характер. Помимо этого, уровни общих рецепторов патоген-ассоциированных молекулярных паттернов (PAMPs), таких как TLR-4, TLR-5, TLR-7 и TLR-9, которые опосредуют развитие воспаления, также снижались в печени при лечении пробиотиками, а также увеличивалась антиоксидантная активность. Вышеупомянутые изменения в TLRs и окислительном стрессе были также обнаружены в аналогичных экспериментах с пробиотиками Lactobacillus paracasei GMNL 32 (GMNL-32) и Lactobacillus reuteri GMNL 89, хотя эффекты Lactobacillus reuteri GMNL 263 на экспрессию Treg в этих случаях отсутствовали. Кроме того, в этих трех методах лечения, посредством подавления ядерного фактора kB (NF-kB) и митоген-активированных протеинкиназных сигнальных путей (сигнальных путей MAPK), наблюдалось снижение печеночных провоспалительных цитокинов IL-1β, TNF-α и IL-6 [63,64]. Интересно, что лечение GMNL-32 уменьшило гипертрофию левого желудочка в этой генетической модели волчанки.
Кроме того, дендритные клетки, подвергнутые воздействию микробиоты СКВ, обогащенной Bifidobacterium bifidum LMG13195, как правило, при совместном культивировании с наивными Т-клетками снижают активацию этих лимфоцитов по сравнению с нормальной микробиотой СКВ in vitro. В тех же условиях, но с использованием штамма Ruminococcus obeum DSM25238 и Blautia coccoides DSM935 вместо штамма Bifidobacterium, после восстановления Т-клеток, полученных в результате совместной инкубации, наблюдалось снижение соотношения Th27/Th2, что изменяло картину воспаления по сравнению с нормальной микробиотой СКВ. Однако при изучении уровней экспрессии IFN-γ и IL-17a достоверных различий не наблюдалось [35].
Самки мышей NZB/WF1 имеют ряд характеристик, согласующихся с СКВ человека, включая отложение иммунного комплекса в клубочке, аутоантитела к dsDNA, альбуминурию и, что важно, эндотелиальную дисфункцию и гипертензию [65]. Хроническое потребление Lactobacillus fermentum CECT5716 (LC40) у самок мышей NZB/WF1 позволило увеличить количество бифидобактерий в кишечнике. LC40 снижал активность волчанки и спленомегалию у мышей с СКВ. Он также улучшал целостность кишечного барьера, снижая уровень LPS в плазме, что, в свою очередь, снижало иммунную активацию, проявляющуюся снижением содержания T и B-клеток в брыжеечных лимфатических узлах (MLNs) и провоспалительных цитокинов, таких как IL-17a, IFN-γ, TNF-α и IL-21 в плазме крови. Поскольку пробиотик предотвращал развитие провоспалительного ответа, были предотвращены осложнения, связанные с СКВ, такие как сердечная и почечная гипертрофия. Кроме того, высокое кровяное давление и нарушение эндотелий-зависимой вазодилатации сосудов были предотвращены L. fermentum в результате снижения фосфорилирования эндотелиальной синтазы оксида азота eNOS на ингибирующем участке Thr495 и снижения активности NADPH-оксидазы, обычно рассматриваемой как основной источник активных форм кислорода в сосудистой системе, что улучшает биодоступность оксида азота [29] (Рис.3).
Рисунок 3. Предполагаемый механизм, с помощью которого введение Lactobacillus fermentum CECT5716 (LC40) может предотвратить активность системной красной волчанки, эндотелиальную дисфункцию и гипертонию в модели NZB / WF1 (на основе данных из публикации № [29]).
Таким образом, коррекция микробиома СКВ с помощью диетического вмешательства показала ослабление симптомов СКВ и, в одном случае, его сердечно-сосудистых осложнений, отмечая эту стратегию как возможный новый терапевтический подход к этому заболеванию.
Как видно из приведенных выше примеров, несмотря на наличие более четкой картины элементов, участвующих в эффекте пробиотиков при СКВ, особенно роли Treg и Th27 модуляции, необходимо лучшее понимание основных механизмов пробиотиков, что не только позволит лучше нацеливать и отбирать микроорганизмы, но также может пролить некоторый свет на развитие и причины СКВ и его почечных и сердечно-сосудистых осложнений.
4. ВыводыДанный обзор открывает новые возможности для профилактики СКВ и ее почечных и сердечно-сосудистых нарушений, а также модуляции микробиоты кишечника путем введения некоторых пробиотических штаммов. Однако следует проявлять осторожность при экстраполяции этих данных на человека из-за возможных различий в поведении микробиоты кишечника животного и человека. На самом деле, относительное обилие лактобацилл, по-видимому, является нормальным у больных СКВ в стадии ремиссии [18], что может изменить возможную применимость лечения лактобациллами в клинической практике у людей. Хотя это и не диета сама по себе, существует распространенное мнение, что ферментированные продукты, содержащие пробиотики, изменяют микробиоту кишечника и приносят пользу здоровью хозяина. Однако, ферментированные продукты редко содержат достаточное количество специфических пробиотических организмов. Кроме того, имеются ограниченные доказательства роли пробиотиков в качестве модуляторов микробиоты кишечника человека, и последние данные свидетельствуют о том, что даже дополнительные количества пробиотиков оказывают ограниченное воздействие на экологию кишечника человека [66]. С другой стороны, состав кишечной микробиоты у большой популяции больных гипертонической болезнью СКВ неизвестен.
Ответ на эти вопросы может прояснить не только механизмы, участвующие в защитном действии конкретных пробиотических бактерий, но также их потенциал в лечении СКВ у человека. Принимая во внимание, что патофизиологический механизм, участвующий в развитии расстройства у этих пациентов, может варьировать и что механизмы улучшения течения СКВ специфическими пробиотиками неизвестны, стоит исследовать, можем ли мы выбрать конкретный пробиотический штамм для получения преимуществ у конкретного пациента с СКВ. Вместе взятые, доклинические и клинические данные указывают на необходимость дальнейших исследований для оценки профиля безопасности, прежде чем любой из этих пробиотиков может быть продан для клинического лечения гипертонии, метаболических и сосудистых осложнений при СКВ. Однако мы предполагаем, что полезные бактерии, способные уменьшать дисбактериоз, улучшать барьерную функцию кишечника и уменьшать эндотоксемию, могут предотвращать сосудистые осложнения у больных СКВ. К сожалению, при консультации по данному обзору на сайте Clinicaltrials.gov еще не было включено ни одного исследования пациентов с СКВ с пробиотиками (ClinicalTrials.gov это база данных частных и финансируемых государством клинических исследований, проводимых по всему миру – ред.).
Источник: Néstor de la Visitación, Iñaki Robles-Vera, Marta Toral, Juan Duarte. Protective Effects of Probiotic Consumption in Cardiovascular Disease in Systemic Lupus Erythematosus. Nutrients 2019, 11(11), 2676
К разделу: Микрофлора и аутоиммунные заболевания
Литература
- Johnson, B.M.; Gaudreau, M.C.; Al-Gadban, M.M.; Gudi, R.; Vasu, C. Impact of dietary deviation on disease progression and gut microbiome composition in lupus-prone SNF1 mice. Clin. Exp. Immunol. 2015, 181, 323–337. [Google Scholar] [CrossRef] [PubMed]
- Sanz, I.; Lee, F.E. B cells as therapeutic targets in SLE. Nat. Rev. Rheumatol. 2010, 6, 326–337. [Google Scholar] [CrossRef] [PubMed]
- La Paglia, G.M.C.; Leone, M.C.; Lepri, G.; Vagelli, R.; Valentini, E.; Alunno, A.; Tani, C. One year in review 2017: Systemic lupus erythematosus. Clin. Exp. Rheumatol. 2017, 35, 551–561. [Google Scholar] [PubMed]
- Liu, Y.; Kaplan, M.J. Cardiovascular disease in systemic lupus erythematosus: An update. Curr. Opin. Rheumatol. 2018, 30, 441–448. [Google Scholar] [CrossRef]
- Bartels, C.M.; Buhr, K.A.; Goldberg, J.W.; Bell, C.L.; Visekruna, M.; Nekkanti, S.; Greenlee, R.T. Mortality and cardiovascular burden of systemic lupus erythematosus in a US population-based cohort. J. Rheumatol. 2014, 41, 680–687. [Google Scholar] [CrossRef]
- Frostegård, J. Systemic lupus erythematosus and cardiovascular disease. Lupus 2008, 17, 364–367. [Google Scholar] [CrossRef]
- Ryan, M.J. The pathophysiology of hypertension in systemic lupus erythematosus. Am. J. Physiol. Regul. Integr. Comp. Physiol. 2009, 296, R1258–R1267. [Google Scholar] [CrossRef]
- Wu, J.; Saleh, M.A.; Kirabo, A.; Itani, H.A.; Montaniel, K.R.; Xiao, L.; Chen, W.; Mernaugh, R.L.; Cai, H.; Bernstein, K.E.; et al. Immune activation caused by vascular oxidation promotes fibrosis and hypertension. J. Clin. Investig. 2016, 126, 50–67. [Google Scholar] [CrossRef]
- Guzik, T.J.; Korbut, R.; Adamek-Guzik, T. Nitric oxide and superoxide in inflammation and immune regulation. J. Physiol. Pharmacol. 2003, 54, 469–487. [Google Scholar]
- Small, H.Y.; Migliarino, S.; Czesnikiewicz-Guzik, M.; Guzik, T.J. Hypertension: Focus on autoimmunity and oxidative stress. Free Radic. Biol. Med. 2018, 125, 104–115. [Google Scholar] [CrossRef]
- Taylor, E.B.; Ryan, M.J. Understanding mechanisms of hypertension in systemic lupus erythematosus. Ther. Adv. Cardiovasc. Dis. 2017, 11, 20–32. [Google Scholar] [CrossRef] [PubMed]
- Guzik, T.J.; Hoch, N.E.; Brown, K.A.; McCann, L.A.; Rahman, A.; Dikalov, S.; Goronzy, J.; Weyand, C.; Harrison, D.G. Role of the T cell in the genesis of angiotensin II induced hypertension and vascular dysfunction. J. Exp. Med. 2007, 204, 2449–2460. [Google Scholar] [CrossRef] [PubMed]
- Madhur, M.S.; Lob, H.E.; McCann, L.A.; Iwakura, Y.; Blinder, Y.; Guzik, T.J.; Harrison, D.G. Interleukin 17 promotes angiotensin II-induced hypertension and vascular dysfunction. Hypertension 2010, 55, 500–507. [Google Scholar] [CrossRef] [PubMed]
- Mathis, K.W.; Wallace, K.; Flynn, E.R.; Maric-Bilkan, C.; LaMarca, B.; Ryan, M.J. Preventing autoimmunity protects against the development of hypertension and renal injury. Hypertension 2014, 64, 792–800. [Google Scholar] [CrossRef]
- Esdaile, J.M.; Abrahamowicz, M.; Grodzicky, T.; Li, Y.; Panaritis, C.; du Berger, R.; Côte, R.; Grover, S.A.; Fortin, P.R.; Clarke, A.E.; et al. Traditional Framingham risk factors fail to fully account for accelerated atherosclerosis in systemic lupus erythematosus. Arthritis Rheum. 2001, 44, 2331–2337. [Google Scholar] [CrossRef]
- Giannelou, M.; Mavragani, C.P. Cardiovascular disease in systemic lupus erythematosus: A comprehensive update. J. Autoimmun. 2017, 82, 1–12. [Google Scholar] [CrossRef]
- Chan, V.S.; Tsang, H.H.; Tam, R.C.; Lu, L.; Lau, C.S. B-cell-targeted therapies in systemic lupus erythematosus. Cell. Mol. Immunol. 2013, 10, 133–142. [Google Scholar] [CrossRef]
- Hevia, A.; Milani, C.; López, P.; Cuervo, A.; Arboleya, S.; Duranti, S.; Turroni, F.; González, S.; Suárez, A.; Gueimonde, M.; et al. Intestinal dysbiosis associated with systemic lupus erythematosus. MBio 2014, 5. [Google Scholar] [CrossRef]
- Mu, Q.; Zhang, H.; Liao, X.; Lin, K.; Liu, H.; Edwards, M.R.; Ahmed, S.A.; Yuan, R.; Li, L.; Cecere, T.E.; et al. Control of lupus nephritis by changes of gut microbiota. Microbiome2017, 5, 73. [Google Scholar] [CrossRef]
- Li, B.; Selmi, C.; Tang, R.; Gershwin, M.E.; Ma, X. The microbiome and autoimmunity: A paradigm from the gut-liver axis. Cell. Mol. Immunol. 2018, 15, 595–609. [Google Scholar] [CrossRef]
- Skrypnik, K.; Bogdański, P.; Łoniewski, I.; Reguła, J.; Suliburska, J. Effect of probiotic supplementation on liver function and lipid status in rats. Acta Sci. Pol. Technol. Aliment.2018, 17, 185–192. [Google Scholar] [CrossRef] [PubMed]
- Gentile, C.L.; Weir, T.L. The gut microbiota at the intersection of diet and human health. Science 2018, 362, 776–780. [Google Scholar] [CrossRef] [PubMed]
- Cotillard, A.; Kennedy, S.P.; Kong, L.C.; Prifti, E.; Pons, N.; Le Chatelier, E.; Almeida, M.; Quinquis, B.; Levenez, F.; Galleron, N.; et al. Dietary intervention impact on gut microbial gene richness. Nature 2013, 500, 585–588. [Google Scholar] [CrossRef] [PubMed]
- He, Z.; Shao, T.; Li, H.; Xie, Z.; Wen, C. Alterations of the gut microbiome in Chinese patients with systemic lupus erythematosus. Gut Pathog. 2016, 8, 64. [Google Scholar] [CrossRef] [PubMed]
- Li, Y.; Wang, H.; Li, X.; Li, H.; Zhang, Q.; Zhou, H.; He, Y.; Li, P.; Fu, C.; Zhang, X.; et al. Disordered intestinal microbes are associated with the activity of Systemic Lupus Erythematosus. Clin. Sci. 2019, 133, 821–838. [Google Scholar] [CrossRef] [PubMed]
- Luo, X.M.; Edwards, M.R.; Mu, Q.; Yu, Y.; Vieson, M.D.; Reilly, C.M.; Ahmed, S.A.; Bankole, A.A. Gut Microbiota in Human Systemic Lupus Erythematosus and a Mouse Model of Lupus. Appl. Environ. Microbiol. 2018, 84. [Google Scholar] [CrossRef]
- Azzouz, D.; Omarbekova, A.; Heguy, A.; Schwudke, D.; Gisch, N.; Rovin, B.H.; Caricchio, R.; Buyon, J.P.; Alekseyenko, A.V.; Silverman, G.J. Lupus nephritis is linked to disease-activity associated expansions and immunity to a gut commensal. Ann. Rheum. Dis.2019, 78, 947–956. [Google Scholar] [CrossRef]
- Zhang, H.; Liao, X.; Sparks, J.B.; Luo, X.M. Dynamics of gut microbiota in autoimmune lupus. Appl. Environ. Microbiol. 2014, 80, 7551–7560. [Google Scholar] [CrossRef]
- Toral, M.; Robles-Vera, I.; Romero, M.; de la Visitación, N.; Sánchez, M.; O’Valle, F.; Rodriguez-Nogales, A.; Gálvez, J.; Duarte, J.; Jiménez, R. Lactobacillus fermentum CECT5716: A novel alternative for the prevention of vascular disorders in a mouse model of systemic lupus erythematosus. FASEB J. 2019, 33, 10005–10018. [Google Scholar] [CrossRef]
- Zegarra-Ruiz, D.F.; El Beidaq, A.; Iñiguez, A.J.; Lubrano Di Ricco, M.; Manfredo Vieira, S.; Ruff, W.E.; Mubiru, D.; Fine, R.L.; Sterpka, J.; Greiling, T.M.; et al. A Diet-Sensitive Commensal Lactobacillus Strain Mediates TLR7-Dependent Systemic Autoimmunity. Cell Host Microbe 2019, 25, 113–127. [Google Scholar] [CrossRef]
- Manfredo Vieira, S.; Hiltensperger, M.; Kumar, V.; Zegarra-Ruiz, D.; Dehner, C.; Khan, N.; Costa, F.R.C.; Tiniakou, E.; Greiling, T.; Ruff, W.; et al. Translocation of a gut pathobiont drives autoimmunity in mice and humans. Science 2018, 359, 1156–1161. [Google Scholar] [CrossRef] [PubMed]
- Katz-Agranov, N.; Zandman-Goddard, G. The microbiome and systemic lupus erythematosus. Immunol. Res. 2017, 65, 432–437. [Google Scholar] [CrossRef] [PubMed]
- Chen, X.Q.; Yu, Y.C.; Deng, H.H.; Sun, J.Z.; Dai, Z.; Wu, Y.W.; Yang, M. Plasma IL-17A is increased in new-onset SLE patients and associated with disease activity. J. Clin. Immunol. 2010, 30, 221–225. [Google Scholar] [CrossRef] [PubMed]
- Kimura, A.; Kishimoto, T. IL-6: Regulator of Treg/Th27 balance. Eur. J. Immunol. 2010, 40, 1830–1835. [Google Scholar] [CrossRef] [PubMed]
- López, P.; de Paz, B.; Rodríguez-Carrio, J.; Hevia, A.; Sánchez, B.; Margolles, A.; Suárez, A. Th27 responses and natural IgM antibodies are related to gut microbiota composition in systemic lupus erythematosus patients. Sci. Rep. 2016, 6, 24072. [Google Scholar] [CrossRef] [PubMed]
- Yu, C.F.; Peng, W.M.; Schlee, M.; Barchet, W.; Eis-Hübinger, A.M.; Kolanus, W.; Geyer, M.; Schmitt, S.; Steinhagen, F.; Oldenburg, J.; et al. SOCS1 and SOCS3 Target IRF7 Degradation to Suppress TLR7-Mediated Type I IFN Production of Human Plasmacytoid Dendritic Cells. J. Immunol. 2018, 200, 4024–4035. [Google Scholar] [CrossRef]
- Buie, J.J.; Renaud, L.L.; Muise-Helmericks, R.; Oates, J.C. IFN-α Negatively Regulates the Expression of Endothelial Nitric Oxide Synthase and Nitric Oxide Production: Implications for Systemic Lupus Erythematosus. J. Immunol. 2017, 199, 1979–1988. [Google Scholar] [CrossRef]
- Harrison, D.G.; Guzik, T.J.; Lob, H.E.; Madhur, M.S.; Marvar, P.J.; Thabet, S.R.; Vinh, A.; Weyand, C.M. Inflammation, immunity, and hypertension. Hypertension 2011, 57, 132–140. [Google Scholar] [CrossRef]
- Weckerle, C.E.; Mangale, D.; Franek, B.S.; Kelly, J.A.; Kumabe, M.; James, J.A.; Moser, K.L.; Harley, J.B.; Niewold, T.B. Large-scale analysis of tumor necrosis factor α levels in systemic lupus erythematosus. Arthritis Rheum. 2012, 64, 2947–2952. [Google Scholar] [CrossRef]
- Venegas-Pont, M.; Manigrasso, M.B.; Grifoni, S.C.; LaMarca, B.B.; Maric, C.; Racusen, L.C.; Glover, P.H.; Jones, A.V.; Drummond, H.A.; Ryan, M.J. Tumor necrosis factor-alpha antagonist etanercept decreases blood pressure and protects the kidney in a mouse model of systemic lupus erythematosus. Hypertension 2010, 56, 643–649. [Google Scholar] [CrossRef]
- Bomfim, G.F.; Dos Santos, R.A.; Oliveira, M.A.; Giachini, F.R.; Akamine, E.H.; Tostes, R.C.; Fortes, Z.B.; Webb, R.C.; Carvalho, M.H. Toll-like receptor 4 contributes to blood pressure regulation and vascular contraction in spontaneously hypertensive rats. Clin. Sci. 2012, 122, 535–543. [Google Scholar] [CrossRef] [PubMed]
- Sollinger, D.; Eißler, R.; Lorenz, S.; Strand, S.; Chmielewski, S.; Aoqui, C.; Schmaderer, C.; Bluyssen, H.; Zicha, J.; Witzke, O.; et al. Damage-associated molecular pattern activated Toll-like receptor 4 signalling modulates blood pressure in L-NAME-induced hypertension. Cardiovasc. Res. 2014, 101, 464–472. [Google Scholar] [CrossRef] [PubMed]
- Liang, C.F.; Liu, J.T.; Wang, Y.; Xu, A.; Vanhoutte, P.M. Toll-like receptor 4 mutation protects obese mice against endothelial dysfunction by decreasing NADPH oxidase isoforms 1 and 4. Arterioscler. Thromb. Vasc. Biol. 2013, 33, 777–784. [Google Scholar] [CrossRef] [PubMed]
- Toral, M.; Gómez-Guzmán, M.; Jiménez, R.; Romero, M.; Sánchez, M.; Utrilla, M.P.; Garrido-Mesa, N.; Rodríguez-Cabezas, M.E.; Olivares, M.; Gálvez, J.; et al. The probiotic Lactobacillus coryniformis CECT5711 reduces the vascular pro-oxidant and pro-inflammatory status in obese mice. Clin. Sci. 2014, 127, 33–45. [Google Scholar] [CrossRef] [PubMed]
- Shi, L.; Zhang, Z.; Yu, A.M.; Wang, W.; Wei, Z.; Akhter, E.; Maurer, K.; Costa Reis, P.; Song, L.; Petri, M.; et al. The SLE transcriptome exhibits evidence of chronic endotoxin exposure and has widespread dysregulation of non-coding and coding RNAs. PLoS ONE2014, 9, e93846. [Google Scholar] [CrossRef] [PubMed]
- Issara-Amphorn, J.; Surawut, S.; Worasilchai, N.; Thim-Uam, A.; Finkelman, M.; Chindamporn, A.; Palaga, T.; Hirankarn, N.; Pisitkun, P.; Leelahavanichkul, A. The Synergy of Endotoxin and (1→3)-β-D-Glucan, from Gut Translocation, Worsens Sepsis Severity in a Lupus Model of Fc Gamma Receptor IIb-Deficient Mice. J. Innate Immun.2018, 10, 189–201. [Google Scholar] [CrossRef]
- Ogunrinde, E.; Zhou, Z.; Luo, Z.; Alekseyenko, A.; Li, Q.Z.; Macedo, D.; Kamen, D.L.; Oates, J.C.; Gilkeson, G.S.; Jiang, W. A Link Between Plasma Microbial Translocation, Microbiome, and Autoantibody Development in First-Degree Relatives of Systemic Lupus Erythematosus Patients. Arthritis Rheumatol. 2019. [Google Scholar] [CrossRef]
- Arpaia, N.; Campbell, C.; Fan, X.; Dikiy, S.; van der Veeken, J.; deRoos, P.; Liu, H.; Cross, J.R.; Pfeffer, K.; Coffer, P.J.; et al. Metabolites produced by commensal bacteria promote peripheral regulatory T-cell generation. Nature 2013, 504, 451–455. [Google Scholar] [CrossRef]
- Singh, N.; Gurav, A.; Sivaprakasam, S.; Brady, E.; Padia, R.; Shi, H.; Thangaraju, M.; Prasad, P.D.; Manicassamy, S.; Munn, D.H.; et al. Activation of Gpr109a, receptor for niacin and the commensal metabolite butyrate, suppresses colonic inflammation and carcinogenesis. Immunity 2014, 40, 128–139. [Google Scholar] [CrossRef]
- Rodríguez-Carrio, J.; López, P.; Sánchez, B.; González, S.; Gueimonde, M.; Margolles, A.; de Los Reyes-Gavilán, C.G.; Suárez, A. Intestinal Dysbiosis Is Associated with Altered Short-Chain Fatty Acids and Serum-Free Fatty Acids in Systemic Lupus Erythematosus. Front. Immunol. 2017, 8, 23. [Google Scholar] [CrossRef]
- Martens, E.C.; Lowe, E.C.; Chiang, H.; Pudlo, N.A.; Wu, M.; McNulty, N.P.; Abbott, D.W.; Henrissat, B.; Gilbert, H.J.; Bolam, D.N.; et al. Recognition and degradation of plant cell wall polysaccharides by two human gut symbionts. PLoS Biol. 2011, 9, e1001221. [Google Scholar] [CrossRef] [PubMed]
- Mu, Q.; Tavella, V.J.; Kirby, J.L.; Cecere, T.E.; Chung, M.; Lee, J.; Li, S.; Ahmed, S.A.; Eden, K.; Allen, I.C.; et al. Antibiotics ameliorate lupus-like symptoms in mice. Sci. Rep.2017, 7, 13675. [Google Scholar] [CrossRef] [PubMed]
- He, Z.; Kong, X.; Shao, T.; Zhang, Y.; Wen, C. Alterations of the Gut Microbiota Associated with Promoting Efficacy of Prednisone by Bromofuranone in MRL/lpr Mice. Front. Microbiol. 2019, 10, 978. [Google Scholar] [CrossRef]
- Kasselman, L.J.; Vernice, N.A.; DeLeon, J.; Reiss, A.B. The gut microbiome and elevated cardiovascular risk in obesity and autoimmunity. Atherosclerosis 2018, 271, 203–213. [Google Scholar] [CrossRef] [PubMed]
- Greiling, T.M.; Dehner, C.; Chen, X.; Hughes, K.; Iñiguez, A.J.; Boccitto, M.; Ruiz, D.Z.; Renfroe, S.C.; Vieira, S.M.; Ruff, W.E.; et al. Commensal orthologs of the human autoantigen Ro60 as triggers of autoimmunity in lupus. Sci. Transl. Med. 2018, 10. [Google Scholar] [CrossRef] [PubMed]
- Schiffer, C.; Lalanne, A.I.; Cassard, L.; Mancardi, D.A.; Malbec, O.; Bruhns, P.; Dif, F.; Daëron, M. A strain of Lactobacillus casei inhibits the effector phase of immune inflammation. J. Immunol. 2011, 187, 2646–2655. [Google Scholar] [CrossRef] [PubMed]
- Zamani, B.; Golkar, H.R.; Farshbaf, S.; Emadi-Baygi, M.; Tajabadi-Ebrahimi, M.; Jafari, P.; Akhavan, R.; Taghizadeh, M.; Memarzadeh, M.R.; Asemi, Z. Clinical and metabolic response to probiotic supplementation in patients with rheumatoid arthritis: A randomized, double-blind, placebo-controlled trial. Int. J. Rheum. Dis. 2016, 19, 869–879. [Google Scholar] [CrossRef] [PubMed]
- Hill, C.; Guarner, F.; Reid, G.; Gibson, G.R.; Merenstein, D.J.; Pot, B.; Morelli, L.; Canani, R.B.; Flint, H.J.; Salminen, S.; et al. Expert consensus document. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nat. Rev. Gastroenterol. Hepatol. 2014, 11, 506–514. [Google Scholar] [CrossRef]
- Szulińska, M.; Łoniewski, I.; Skrypnik, K.; Sobieska, M.; Korybalska, K.; Suliburska, J.; Bogdański, P. Multispecies Probiotic Supplementation Favorably Affects Vascular Function and Reduces Arterial Stiffness in Obese Postmenopausal Women-A 12-Week Placebo-Controlled and Randomized Clinical Study. Nutrients 2018, 10, 1672. [Google Scholar] [CrossRef]
- Szulińska, M.; Łoniewski, I.; van Hemert, S.; Sobieska, M.; Bogdański, P. Dose-Dependent Effects of Multispecies Probiotic Supplementation on the Lipopolysaccharide (LPS) Level and Cardiometabolic Profile in Obese Postmenopausal Women: A 12-Week Randomized Clinical Trial. Nutrients 2018, 10, 773. [Google Scholar] [CrossRef]
- Mardani, F.; Mahmoudi, M.; Esmaeili, S.A.; Khorasani, S.; Tabasi, N.; Rastin, M. In vivo study: Th2-Th27 reduction in pristane-induced systemic lupus erythematosus mice after treatment with tolerogenic Lactobacillus probiotics. J. Cell. Physiol. 2018, 234, 642–649. [Google Scholar] [CrossRef] [PubMed]
- Tzang, B.S.; Liu, C.H.; Hsu, K.C.; Chen, Y.H.; Huang, C.Y.; Hsu, T.C. Effects of oral Lactobacillus administration on antioxidant activities and CD4 + CD25 + forkhead box P3 (FoxP3) + T cells in NZB/W F1 mice. Br. J. Nutr. 2017, 118, 333–342. [Google Scholar] [CrossRef] [PubMed]
- Hsu, T.C.; Huang, C.Y.; Liu, C.H.; Hsu, K.C.; Chen, Y.H.; Tzang, B.S. Lactobacillus paracasei GMNL-32, Lactobacillus reuteri GMNL-89 and L. reuteri GMNL-263 ameliorate hepatic injuries in lupus-prone mice. Br. J. Nutr. 2017, 117, 1066–1074. [Google Scholar] [CrossRef] [PubMed]
- Hu, W.S.; Rajendran, P.; Tzang, B.S.; Yeh, Y.L.; Shen, C.Y.; Chen, R.J.; Ho, T.J.; Vijaya Padma, V.; Chen, Y.H.; Huang, C.Y. Lactobacillus paracasei GMNL-32 exerts a therapeutic effect on cardiac abnormalities in NZB/W F1 mice. PLoS ONE 2017, 12, e0185098. [Google Scholar] [CrossRef] [PubMed]
- Ryan, M.J.; McLemore, G.R., Jr. Hypertension and impaired vascular function in a female mouse model of systemic lupus erythematosus. Am. J. Physiol. Regul. Integr. Comp. Physiol. 2007, 292, R736–R742. [Google Scholar] [CrossRef]
- Zmora, N.; Zilberman-Schapira, G.; Suez, J.; Mor, U.; Dori-Bachash, M.; Bashiardes, S.; Kotler, E.; Zur, M.; Regev-Lehavi, D.; Brik, R.B.; et al. Personalized Gut Mucosal Colonization Resistance to Empiric Probiotics Is Associated with Unique Host and Microbiome Features. Cell 2018, 174, 1388–1405. [Google Scholar] [CrossRef]
Будьте здоровы!
ССЫЛКИ К РАЗДЕЛУ О ПРЕПАРАТАХ ПРОБИОТИКАХ
- ПРОБИОТИКИ
- ДОМАШНИЕ ЗАКВАСКИ
- БИФИКАРДИО
- КОНЦЕНТРАТ БИФИДОБАКТЕРИЙ ЖИДКИЙ
- ПРОПИОНИКС
- ЙОДПРОПИОНИКС
- СЕЛЕНПРОПИОНИКС
- МИКРОЭЛЕМЕНТНЫЙ СОСТАВ
- ПРОБИОТИКИ С ПНЖК
- БИФИДОБАКТЕРИИ
- ПРОПИОНОВОКИСЛЫЕ БАКТЕРИИ
- ПРОБИОТИКИ И ПРЕБИОТИКИ
- СИНБИОТИКИ
- РОЛЬ МИКРОБИОМА В ТЕРАПИИ РАКА
- АНТИОКСИДАНТНЫЕ СВОЙСТВА
- АНТИОКСИДАНТНЫЕ ФЕРМЕНТЫ
- АНТИМУТАГЕННАЯ АКТИВНОСТЬ
- МИКРОФЛОРА КИШЕЧНОГО ТРАКТА
- МИКРОБИОМ ЧЕЛОВЕКА
- МИКРОФЛОРА И ФУНКЦИИ МОЗГА
- ПРОБИОТИКИ И ХОЛЕСТЕРИН
- ПРОБИОТИКИ ПРОТИВ ОЖИРЕНИЯ
- МИКРОФЛОРА И САХАРНЫЙ ДИАБЕТ
- ПРОБИОТИКИ и ИММУНИТЕТ
- МИКРОБИОМ И АУТОИММУННЫЕ БОЛЕЗНИ
- ПРОБИОТИКИ и ГРУДНЫЕ ДЕТИ
- ПРОБИОТИКИ, БЕРЕМЕННОСТЬ, РОДЫ
- ДИСБАКТЕРИОЗ
- ВИТАМИННЫЙ СИНТЕЗ
- АМИНОКИСЛОТНЫЙ СИНТЕЗ
- АНТИМИКРОБНЫЕ СВОЙСТВА
- СИНТЕЗ ЛЕТУЧИХ ЖИРНЫХ КИСЛОТ
- СИНТЕЗ БАКТЕРИОЦИНОВ
- ФУНКЦИОНАЛЬНОЕ ПИТАНИЕ
- АЛИМЕНТАРНЫЕ ЗАБОЛЕВАНИЯ
- ПРОБИОТИКИ ДЛЯ СПОРТСМЕНОВ
- ПРОИЗВОДСТВО ПРОБИОТИКОВ
- ЗАКВАСКИ ДЛЯ ПИЩЕВОЙ ПРОМЫШЛЕННОСТИ
- НОВОСТИ
Современное течение и лечение системной красной волчанки (по материалам Хабаровского края)
1. Адамян Н.В.,Соловьев С.К., Гамбаров С.С. и др. Нарушение иммуногенеза у больных системной красной волчанкой.//Тер,ар\ив № 5,1989, с.43-45//.
2. Алекберова З.С., Ананьева Л.П., Саморядова О.П. и др. Особенности системной красной волчанки, развившейся в постклимактерическом периоде.//Тер.архив №12,1989, с. 95-98//.
3. Алекберова З.С., КотельниковаГ.П., Фоломеев М.Ю. Аортальные пороки при системной красной волчанке //Тер.архив № 5,1989, с. 35-37//.
4. Алекберова З.С., Насонова В.А., Решетняк Т.М., В.Г. Цитланадзе и др. Особенности системной красной волчанки у русских и грузин.//Науч.-практ.реьмат. № 2, 2001, с. 13-17//.
5. Алекберова З.С., Решетняк Т.М., Кошелева Н.М., Александрова Е.Н. и др. Антифосфолипидный синдром при системной красной вол чайке :оценка диагностических и классификационных критериев.// Клин.медицина № 6,1996, с. 39-41//.
6. Алекберова З.С., Решетняк Т.М., Родеиска-Лоповок С.Г., Александрова Е.Н.и др. Васкулопатия у больных системной красной волчанкой с антифосфолипидным синдромом. // Тер.архив № 5, 1995, с. 41-44//.
7. Алекберова Э.С., Насонов Е.Л., Прудникова Л.З. и др. Клиническое значение определения волчаночного антикоагулянта и антител к кардиолипину //Тер.архив № 7, 1988, с.84-87//.
8. Александрова Е.Н., Насонов Е.Л., Быховская С.Ю. Естественная цитотоксичность у больных системной красной волчанкой.//Тер.архив№ 5,1984, с.29-32.//.
9. Александрова Е.Н., Насонов Е.Л., Ковалев В.Ю. Количественный иммуноферментный метод определения антител к кардиолипину в сыворотке крови // Клин.ревмат.№ 4, 1995, с.35-39//.
10. Бажанов Н.Н., Меньшиков И В. Сложные нарушения сердечного ритма и проводимости у больных системной красной волчанкой //Кардиология № 12, 1989, с.108-110//
11. П. Бажанов Н.Н., Петухова Н.В. Некоторые вопросы диагностики и тактики ведения больных системной красной волчанки //Клин.мед. № 1,1990, с. 124-130//.
12. Баранов А.А. Клинико- иммунные аспекты патологии сосудов при системных васкулитах и некоторых ревматических заболеваниях: //Автореф.дис.Д-ра меднаук. Ярославль, 1998//.
13. Белокриницкий Д.В., Дудкина Л.И., Тарасова Л.П. Теофиллиновый тест в оценке состояния клеточного иммунитета у детей с различным течением системной красной волчанки.// Лаб.дело № 8,1989, с. 54-56.//.
14. Близнюк О.И., Иванова М.М. Хроническая усталость при системной красной волчанке: взаимосвязь с активностью болезни и депрессией // Клин.ревмат. № 5,1995, с. 17-19//.
15. Близнюк О.И., РаденскаС.Г., Соловьев С.К., Иванова М.М., Насонова В.А. Ретроспективный клинико-морфологический анализ поражений центральной нервной системы у больных системной красной волчанкой. // Клин.ревматология № 4,1995,с 22-25//.
16. Бобкова И.Н., Полянцева Л .Р., Тареева И.Е. и др. Клиническое значение определения фактора Виллебранда у больных волчаночным нефритом. //Тер.архив № 5,1995, с. 14-16//.
17. Буланова Т.Д., Ле Го А., Алекберова З.С. и др. Изучение циркулирующих иммунобластов в периферической крови больных системной красной волчанки и других ревматических заболеваний //Тер архив № 6, 1980. с 64 *7//
18. Бунятян К.А. Исследование особенностей регуляции иммунного ответа при системно., красной волчанке и системной склеродермии у детей.//Дис.канд.мед.наук. М. 1986,135с.//.
19. Веналис А.И., Матулис А.А., Мишкините Г.А. и др. Иммунологическая и биохимическая характеристика циркулирующих иммунных комплексов при ревматоидном артрите и системной красной волчанке .//Тер.архив № 7,1983, с.24-28//.
20. Войтенок Н.Н. Интерлейкин-2 //Тер.архив№ 5,1988, с. 42-46//.
21. Галактионов В.Г. Графические модели в иммунологии. М.»Медицина», 1986, 238с.
22. Гарумова Л.М. Клинико- иммунологическая характеристика васкулита при системной красной волчанке.//Автореф.дис. .канд.мед.наук,1989,26с.//.
23. Гарумова Л.М., Насонов Е.Л., Алекберова З.С. и др. Иммуноглобулины при системной красной волчанкеЖлин. мед. № 6,1989, с. 91-94//.
24. Гомова Т.Д. Варианты течения системной красной волчанки (по материалам Тульской областной больницы) /Яер.архив № 4,1994, с.54-57//.
25. Городецкий В.М., Рыжко В.В. Плазмаферез в терапии заболеваний, обусловленных иммунной патологией //Тер.архив № 6,1984, с. 19-25//.
26. Гринин В.М., Грачев Ю.В., Смирнов А.В. Особенности неврологического статуса больных с асептическим некрозом височно- челюстного сустава при системной красной волчанке, тезисы. //Науч.-практ.ревматология № 4, 2000, с.39//.
27. ГрининВ.М, ЛисицинаТ.А , Смирнов А.В. Поражение височно-нижнечелюстных суставов при системной красной волчанке //Клин.ревма тология, №2, 1995, с. 6-9//.
28. Грицман Н.Н. Поражение сердца при коллагеновых заболеваниях.М- Медицина ,1971,196с.
29. Грицман Н.Н., Ахназарова В.Д., Иванова М.М. и др. Морфологические и иммуногистохимические изменения в почках и коже при системной красной волчанке под влиянием лечения. //Ревматология № 3, 1983, с.41-45//.
30. Гуртовая Г.П., Седов К.Р Клиническая характеристика системной красной волчанки в условиях Восточной Сибири.//Тер.архив № 6,1982, с.60-63//.
31. Дворяковский И.В., Коберидзе J1.L1I. Клиническое значение допплерографии при гломерулонефрите у детей //Визуализация в клинике, выпуск 1, № I, август 1992, с. 23-26//.
32. Демин А.А., Сентякова М.М. Сравнительная оценка циклической полихимиотерапии и непрерывного лечения двумя иммунодепрессантами люпус-нефрита.//Тер.архив №1,1979, с.71-76//.
33. Демин А.А., СентяковаТ.Н., Сперанский А.И и др. Эволюция волчаночного нефрита: клинические и морфологические аспекты. // Клин.ревматология № 3, 1995, с. 14-17//.
34. Демин А.А., Сперанский А.И., Сентякова Т.Н. и др. Цикулирующие иммунные комплексы, иммуноглобулины, фагоцитирующая активность нейтрофилов в оценке активности и эффективности лечения системной красной волчанки .//Тер. архив №8,1985, с.52-57//.
35. Досин Ю.М. Комплексное клинико- иммунологическое исследование показателей иммунитета и системы фагоцитоза у больных ревматоидным артритом и системной красной волчанки.//Автореф.дис. .канд.мед.наук, М.,1982,20с,//.
36. Дядык А.И., Василенко И.В., Сиияченко О.В. и др. Патогенетическая терапия волчаночного гломерулонефрита.//Тер.архнв № 8, 1992, с. 119-123.//.
37. Дядык А.И., Василенко И.В., Синяченко О.В. и др. Эффективность глюкокортикоидной и цитостатической терапии волчаночного гломерулонефрита//Тер.архив №IO,1992,c.l) 1-114//.
38. Дядык А.И., Тарадин Г.Г., Багрий А.Э. Волчаночиый миокардит (обзор литературы) //Клин.ревматология № I. 1997, с.24-28//.
39. Дядык А.И., Тарадин Г.Г., Багрий А.Э. и др. Поражение клапанного аппарата сердца при системной красной волчанке.//Клин.ревматология №1,1996, с. 2-7//.
40. Елисеева Л.Н., Давыдова А.Ф., Сорокина Т.Н. и др. Сравнительная эффективность пульс-терапии стероидами и цитостатиками при люпус- нефрите, тезисы //Науч.-практ. ревматология №4, 2000, с.46//.
41. Елубаева В.И., Мач Э.С., Решетняк Т.М., Алекберова З.С. Церебральное кровообращение у больных системной красной волчанкой с антифосфолипидным синдромом.// Тер.архив № I, 1994, с.16-18//.
42. Ефуни С.С. Этиология и патогенез аутоиммунных заболеваний.//Тер.архив № 12, 1991, с.2832//.
43. Жданова Т.В. Иванова А.В., Лесняк О.М. и др. Влияние пульс- терапии циклофосфаном и метипредом на клинико- лабораторные признаки активности люпус- нефрита //материалы научно-практ.конф., тезисы, Москва , 1996,с.26-27//.
44. Журавлев Г.И. Клинико-иммунологическая характеристика системной красной волчанки. //Дис.докт.мед.наук. Л.,1972//
45. Иванова А.В., Насонов Е.Л., Соловьев С.К. и др. Циркулирующие иммунные комплексы (ПЭГ-тесты) при системной красной волчанке.//Тер. архив №6, 1982,с.63-68//.
46. Иванова М.М. Патогенетическая терапия, реабилитация и прогноз больных системной красной волчанки с преимущественным поражением почек.//Автореф.дис. .докт.мед.наук, М.,1984,48с.//.
47. Иванова М.М. Системная красная волчанка: клиника, диагностика и лечение // Клин.ревматология № I, 1995, с.2-19//.
48. Иванова М.М. ЦНС-люпус: проблемы, достижения (результаты Ю- летнего клинико-инструментального исследования) (лекция).//Тер.архив № 5, 2001, с. 25-29//.
49. Иванова М.М., Близнюк О.И. Лечение больных системной красной волчанкой с поражением центральной нервной системы //Вест.дермат. № 2, 1994, с.64-67//.
50. Иванова М.М., Близнюк О.И. Системная красная волчанка с поражением центральной нервной системы // Клин.медицина № 6, 1989, с. 15-20//.
51. Иванова М.М., Близнюк О.И., Тодуа Ф.И. и др. Поражение центральной нервной системы при системной красной волчанке.// Клин.медицина № 12,1989, с. 93-97//,
52. Иванова М.М., Близнюк О.И., Травкина Т.И. Длительное парентеральное применение циклофосфана больных системной красной волчанкой с поражением центральной нервной системы //Тер.архив № 5,1995, с.45-47//.
53. Иванова М.М., Каратеев Д.Е., Лучихина Е.Л. Основные методы и индивидуальные программы лечения больных системной красной волчанкой//Клин. мед.№ 5, 2000, с. 45-49//,
54. Иванова М.М., Насонова В.А., Соловьев С.К. и др Контролируемое испытание циклофосфамида, азатиоприна и хлорамбуцила при волчаночном нефрите (двойной слепой метод)//Вопросы ревм. № 2,1981, с. 16-18//.
55. Иванова М.М., Соловьев С.К., Сперанский А.И. и др. Внутривенное введение ударных доз метил преднизолона (пульс-терапия) при люпус-нефрите //Тер.архив № 7,1983, c.l 14-119//.
56. Иванова М.М., Спикулев Ю.К., Близнюк О.И. и др. Количественная характеристика циркулирующих иммунных комплексов у больных системной красной волчанки с поражением центральной нервной системы.//Клин.мед. №3,1991, с.58-60//.
57. Каландадзе Н.Г. Ранняя диагностика, особенности лечения и диспансеризации больных системной красной волчанкой. //Автореф.дисс.канд.мед.наук, М., 1988, 32с.//.
58. Карабаева А. С. Особенности системной красной волчанки с поздним началом (после 45 лет) //Автореф. дисс. канд.мед.наук, М., 2001, 27с.//.
59. Караулов А.В., Балашов К.Е. Клеточный иммунитет при аутоиммунных заболеваниях //Тер.архив № 4,1991, с,147-150//.
60. Кейтель В. Иммуносупрессивная терапия при ревматоидном артрите и коллагенозах //Иммуносупрессивная химиотерапия//Под ред. Д.Нелиусе, 1984, с.107-142//.
61. Кирпичникова Г.И., Неверов В.А., Ремезов А.П. Иммунитет, иммунодефициты, иммуноориентированная терапия (пособие для врачей) //С.-Петербург, 1997, 45с.//
62. Клиническая нефрология /Под ред.Тареева E.M.-M.I983.-T.2, с. 133-161/.
63. Клюквина Н.Г., Баранов А.А., Александрова Е.Н., Насонов Е.Л. С-реактивный белок при системной красной волчанке у мужчин: связь с тромботическими осложнениями. //Клин.мед.№8,1997, с. 24-27//.
64. Клюквина НГ , Котельникова Г П , Насонов Е.Л., Алекберова З.С. Кардиальная патология у мужчин, больных системной красной волчанкой и вторичным антифосфолипидным синдромом. //Клин.ревматология № 3,1996, с. 47-50//.
65. Козловская Н.Л., Кабаеикова Г.С. Варшавский В.А., Швецов М.Ю. Особенности поражения почек у больной системной красной волчанкой с антифосфолипидным синдром // Клин.мед. №3,1995, с. 93-96//.
66. Коненков В.И. Короткова И10., Прокофьев В.Ф. и др. Иммунологическая и иммуногенетическая разнородность системной и дискоидной красной волчанки //Тер.архив №5,1989. с 31-34//
67. Константинова Н.А., Ковальчук Л.В. Диагностическое и прогносшческое значение показателей гуморального и клеточного иммунитета у больных системной красной волчанки //Сов мед №5, 1983, с 30-34 //
68. Кочи М.Н. Клиническая патология беременности и новорожденного . пер с англ -М 1986-с -394-414
69. Краснова Т.Н., Швецов М.Ю., Иванова Л.В. и др Современные возможности лечения гломерулонефритов //Тер.архив №6. 2001, с. 76-78//.
70. Красовский И.И., Шкодин И.В., Владимиров Н.Н. О гематологических «масках» при системной красной волчанке .//Тер. архив №5, 1995,с. 58-61//.
71. Крифус О.И., Жансарина А.Х., Цой И.Г. Значение лабильности экспрессии Е-рецепторов лимфоцитов для информативности теофиллинового теста в норме и при вирусной гепатите В //Лабор.дело № 19, с.6! -64//.
72. Кутырина И.М., Тареева И.Е., Герасименко О.И. и др. Использование ингибиторов ангиотензинпревращающего фермента при хронических диффузных заболеваниях почек. //Тер.архив №5,1995, с. 20-23//.
73. Лебедев К.А., Понякина И.Д. //Иммунограмма в клинической практике. М.»Наука»,1990, 223с.//
74. Лесняк О.М. Изучение наследственности, антигенов гистосовместимости и некоторых имуннологических параметров в семьях больных системной красной волчанкой. //Автореф. канд. дисс., М. 1987, с. I -34//.
75. Лисица К.В., Анисимова Л.П., Смолянинова Н.Г. и др. Компьютерный анализ фазовой структуры спектра допплеровского сдвига частот при ультразвуковом исседовании почечных артерий.//Визуализация в клинике № 5, декабрь 1994, с. 1-4.//
76. Лисица К.В., Рогоза А.Н., Самко А.Н. и др. Метод оценки степени стенозирования почечных артерий.//Визуализация в клинике № 8, июнь 1996,с. 37-42//.
77. Лучихина Е.Л. Анализ структуры летальных исходов при системной красной волчанке.//Автореф.дис. .канд.мед.наук, М.,1998, 24с.//.
78. Мазур М.В, Мошняга М.Г., В.М.Жук и др. О распространенности системной красной волчанки в Молдове//Тер.архив № 11,1992, с .93-95//.
79. Малдыкова X. Субтипы волчанки- связь клинических и иммунологических признаков //Тер.архив №11,1992,с. 88-92//
80. Матвиенков Г.П., Досин Ю.М., Калия Е.С. и др. Исследование взаимосвязей показателей клеточного и гуморального иммунитета у больных системной красной волчанкой.//Тер.архив № 12, 1982, с. 44-48//.
81. Матулис А., Гуобис Г., Станкайтене Д.и др. Эффективность и показания к применению иммунорегулируюшей терапии системных ревтических заболеваний //Тер.архив №6,1986, с. 19-27//.
82. Михеев М.М. Актуальные вопросы неврологии и нейрохирургии,- M.I963.
83. Насонов Е.Л. Циркулирующие иммунные комплексы при заболеваниях внутренних органов.//Автореф.дис. .докт мед.наук .М., 1986,42с.//.
84. Насонов Е.Л. Иммунные комплексы при ревматических заболеваниях // Иммунология заболев соед.тк. М., 1984, с. 104-158//.
85. Насонов Е.Л., Александрова Л.З., Корнеева и др. Антитела, реагирующие с антигеном вируса иммунодефицита человека при системной красной волчанке: лож но-положительные результаты или признаки вирусной инфекции.//Вопросы вирусол.№ 4,1988-33, с.504-509//.
86. Насонов Е.Л., Баранов А.А., Шилкина Н.П., Алекберова З.С. Патология сосудов при антифосфолипидном синдроме: (Клиника, диагностика, лечение).-М.; Ярославль, 1995.
87. Насонов Е.Л., Бекетова Т.В., Баранов А.А., и др. Антинейтрофильные цитоплазматические антитела при системных васкулитах.//Клин.медицина№11-12,1992, с. 21-27//.
88. Насонов Е.Л., Карпов Ю.А., Алекберова З.С. и др. Антифосфолипидный синдром: кардиологические аспекты//Тер.архив № II, 1993,с. 80-85//.
89. Насонов Е.Л., Соловьев С.К., Иванова М.М. и др. Иммунологические эффекты пульс-терапии при системной красной волчанке //Тер.архив № 7,1986, с. 49-54//.
90. Насонов Е.Л., Соловьев С.К., Поверенный A.M., Иванова М.М., и др. Циркулирующие иммунные комплексы и клинико-иммунологические подтипы системной красной волчанки(сообщение 2). //Тер.архив №5, 1989, с.38-43//.
91. Насонов Е.Л., Сура D.B. Современные подходы к иммунологической диагностике аутоиммунных и иммунокомплексных болезней.//Тер.архив № 6, 1988, с. 144-150//.
92. Насонова В.А. Активная патогенетическая терапия системных ревматических заболеваний //Тер.архив № 8,1985, с.3-6//.
93. Насонова В.А. Системная красная волчанка.-М., Медицина, 1972.
94. Насонова В.А., Алекберова З.С., Калашникова Л.А., Решетняк Т.М. Поздняя диагностика системной красной волчанки с антифосфолипидным синдромом // Тер.архив № II, 1997, с. 50-54//.
95. Насонова В.А., Астапенко М.Т. Клинич.ревматология-М.Медицина, 1990, с. 143-175.
96. Насонова В.А., Кончакова М.И. Течение системной красной волчанки с неврологическими синдромами.//Клин.медицина № 6, 1996, с 46-49//.
97. Насонова В.А., Кончакова М.И. Точение системной красной волчанки с неврологическими синдромами //Вопр ревматологии № 3, 1965, с. 12-16//
98. Насонова В.А., Несговорова Л.И., Самойлова С.И. и др. Отдаленные результаты кортикостероидной терапии больных СКВ //Тер архив № 7,1979, с 70-77//
99. Насонова В А., Фоломеева ОМ Медико-социальное значение 13 класса болезней для населения России. //Науч.-практ.ревмат. № I, 2001, с. 7-15//.
100. Насонова В.А., Фоломеева О.М., Амирджанова В.Н. и др. Болезни костно- мышечной системы и соединительной ткани в России: динамика статистических показателей за 5 лет (1994-1998г г.).//Науч-практ ревмат. № 2, 2000, с 4-12//.
101. Неретин В.Я., Одинокова В.А., Кирьянов В.А. и др. Иммуносупрессивная терапия некоторых аутоиммунных заболеваний нервной системы //Сов.медицина № 12,1990, с.31-34//.
102. Нечипоренко Н.А., Балла А.А., Анащенко С.П. Ультразвуковой мониторинг больных опухолями почки, перенесших органосохраняющие операции.//Визуализация в клинике № 6, июнь, 1995, с.5-8.//
103. ПО. ПетровР.В. Иммунология.М.»Медицина», 1987,415с.
104. Петров Р.В., Лебедев К.А. и др.//Физиология человека, 1986,т.!2,№ 1, с.94-99//.
105. Пизова Н.В., Спирин Н.Н., Дряженкова И.В. и др. Особенности течения нарушений мозгового кровообращения при ревматических заболеваниях//2 Всерос.съезд ревм.Дула, 1997, с. 146//.
106. Поверенный A.M., Антитела к ДНК, их происхождение и значение в патогенезе аутоиммнных болезней. «Итоги науки и техники, 1986.-Иммунология, 17, с. 129-146//.
107. Полтырев А.С., Кауфман Е.В., Барашков И.Г. Прогноз и выживаемость больных системной красной волчанкой с синдромом Рейно. //Клин.ревматология №2, 1995, с. 39-40//.
108. Полянцева Л.Г., Бобкова И.Н., Тареева И.Е. и др. Активатор плазминогена тканевого типа у больных волчаночным нефритом // Тер.архив № 5,1995, с. 17-19//.
109. Потехина Р.Н., Шилкина Н.П., Полтырев А.С. Гематологический синдром в клинике системной красной волчанки //Тер архив№ 7,1979, с 64-67//
110. Преображенский Д.В. Клинико-иммунологические особенности системной красной волчанки у больных с гипокомплементемией и гипогаммаглобулинемией. Автореф. Дис. канд.мед. наук. М. 1982.
111. Преображенский Д.В., Астахова Т. А., Барботько М.Л. Клиническое значение сывороточных гаммаглобулинов при системной красной волчанке //Тер.архив № 6, 1980, с. 67-71//.
112. Преображенский Д.В, Буйлов С.П. Иммунокомплексные механизмы патогенеза системной красной волчанки //Клин.мед. № 9, 1986, с. 17-30//.
113. Прудникова Л.З., Алекберова З.С., Насонов Е.Л. и др. Тромбэмболические осложнения у больных системной красной волчанкой //Тер.архив № 7, 1989, с. 98-100//.
114. Раденска С.Г., Насонова В.А. Васкулиты и васкулопатии- общие признаки и характерные особенности (лекция) //Тер.архив №11, 1998, с.58-59//.
115. Расулов У.Р. Клинико-иммунологичнекая характеристика больных системной красной волчанкой, живущих в условиях жаркого климата.//Тер.архив № 5, 1989, с. 121-125//.
116. Расулов У.Р. Особенности клинического течения диффузных болезней соединительной ткани(системной красной волчанки и системной склеродермии) в условиях Таджикистана. //Автореф.дисс.док.мед.наук, 1990//.
117. Рязанцева Г.А., Шаханина К.Л., Ароян А.А. и др. Значение определения антител с нативной ДНК при системной красной волчанке и других ревматических заболеваний (сравнение изучения радиоизотопной и иммуноферментной техники).//Тер.архив № 8,1987,
118. Сажина Е.Г. Клинико- иммунологическая эффективность интенсивной терапии у больных системной красной волчанкой.//Дис.канд. мед. наук., М., 1990, 138с.//.
119. Саложин К.В., Насонов Е.Л., Беленков Ю.Н. Роль артериальной клетки в иммунопатологии//Тер.архив, 1992, №3, с. 150-157//.
120. Сатыбалдыев A.M., Сычев Г.Л., Иванова М.М и др. О значении криоглобулинемии в клинике ревматических болезней на примере жителей Москвы (оседлое население) и Тынды (пришлое население Сибири).//Тер.архив № 11,1998, с.60-64//.
121. Сентякова Т.Н. Системная красная волчанка в современной терапевтической клинике (анализ поражений внутренних органов и лечения в проспективном исследован и и).//Автореф.дис. докт. мед. наук, Новосибирск, 1997,45с.//
122. Сентякова Т.Н. Сравнительная оценка эффективности циклической полихимиотерапии и непрерывного лечения двумя им му но депрессантам и системной красной волчанки.//Автореф.дис.канд.мед.наук, М., 1981, 29с.//.
123. Сентякова Т.Н., Демин А.А., Чапаева А.В. и др. Эволюция системной красной волчанки, тезисы.//Науч -практ.ревматология № 4, 2000, с.91//.
124. Сентякова Т.Н., Чижов Н.Н., Демин А.А. и др. Роль вирусов гепатита В и С в полиморфизме клинических проявлений системной красной волчанки, тезисы. //Науч,-практ.ревматология № 4, 2000, с.91//.
125. Серов В.В., Зайратьянц О.В. Аугоиммунизация: новые факты, спорные вопросы и перспективы изучения.//Тер.архив № 6, 1991, с .4-11//.
126. Скрябина Э.Г., Чередеев А.Н., Петракова К.В. Возможности и ограничения теста чувствительности Е-розеткообразования к теофиллину для диагностики состояния T-системы человека.//Лаб.дело № ,1998,с.855-861//
127. Соколов Е.И. Клиническая иммунология, руководство для врачей. М.»Мед.’\ 1998, 270сс.86-91//.
128. Соловьев С.К. Влияние цитотоксических им му но депрессантов на клинико-иммунологические, морфологические и микроциркуляторные нарушения у больных волчаночным нефритом //Автореф.дис. .кандмед.наук.М.,1980, 29с.//.
129. Соловьев С.К. Коментарий к реферату статьи Связь риска смерти при системной красной волчанке с различными клиническими проявлениями болезни //Межд.жур.мед.практики № I, 1997, с. 44-45//.
130. Соловьев С.К., Иванова М.М. Экстравысокие (ударные) дозы метил преднизолона при волчаночном нефрите //Тер.архив № 4,1980, с. 121 -123//.
131. Соловьев С.К., Иванова М.М., Насонова Е.Л. и др. Комбинированное применение ударных доз 6-мети л преднизолона и циклофосфана у больных системной красной волчанкой //Тер.архив№ 8, 1985, с. 7-12//.
132. Соловьев С.К., Иванова М.М, Чикликчи А.С. Интенсивная терапия аутоиммунных заболеваний.//Клин.ревм. № 5, 1995, с.2-4//.
133. Соловьев С К., Насонова В.А. Синхронная интенсивная терапия у больных системной красной волчанкой с неблагоприятным прогнозом.//Вест.акад.мед.наук№12, 1998, с.32-35//.
134. Сперанский А.И., Ароян А А„ Иванова С.М. идр. Клинико- иммунологические аспекты антинуклеарных антител при системной красной волчанке. //Ревмат № 5, 1984, с. 28-34.//.
135. Стоянович Л., Савич М., Станкович Д. И др. Волчаночный цереброваскулит: парадоксы клиники и слабости диагностики. //2 Всерос.съезд ревм.,Тула, 1997, с. 175//.
136. Сыкулев Ю.К., Соловьев С.К., Сажина Е.Г. и др. Циркулирующие иммунные комплексы в сыворотке больных системной красной волчанки //Клин мед №7,1988,с 46-49//.
137. Тареев Е.М., Петровский Б.В.,Кузин М.И. Основы нефрологии. М.,»Медицина», 1972, т.1, с.379-380.
138. Тареева И.Е. Лечение волчаночного нефрита// Тер.архив № 3, 1980, с. 50-55//.
139. Тореева И.Е. Механизм прогнозирования гломерулонефрита//Тер архив № 6,1988, с.3-7//.
140. Тареева И.Е., Козловская Л.В., Кабаенкова Г.С. и др. Тромбоцитопения у больных волчаночным нефритом.//Тер.архив № 5, 1995, с. 9-13//.
141. Тареева И Е„ Козловская Л В., Романова М.Д. и др. Нарушение гемостаза при волчаночном нефрите.// Тер.архив №11,1992, с. 49-52//.
142. Тареева И.Е., Швецов М.Ю., Краснова Т.Н. и др. Артериальная гипертония при волчаночном нефрите. // Тер.архив № 6, 1997, с. 13-17//.
143. Тареева И.Е., Швецов М.Ю., Кутырина И.М. и др. Гемодинамические механизмы прогрессирования волчаночного нефрита .// Тер.архив № 6,1998, с. М -14//.
144. Тищенко В.А., Бекетова Т.В., Семенкова Е.С. и др. Антинейтрофильные цитоллазматические антитела при гранулематозе Вегенера: анализ с помощью иммуноферментного и иммунофлюоресцентного методов. //Тер.архив № 5,1994, с. 48-51//.
145. Травкина И.В. Клинико- иммунологическая и магнито-резонансно- томографическая характеристика поражений центральной нервной системы у больных системной красной волчанки.//Дис.докт.мед.наук, М.,1993//.
146. Травкина И.В., Иванова М.М., Насонов Е.Л, Антитела к фосфолипидам при системной красной волчанке. //Вест, дермат. № 11-12,1992, с.19-24//.
147. Травкина И.В., Иванова М.М., Насонов ЕЛ. и др. Клинико- иммунологическая характеристика поражения ЦНС при системной красной волчанке, связь с антителами к кардиолипину.//Тер.архив№ 5,1992, с. 10-13//.
148. Фоломеева О.М. Подгруппы больных системной красной волчанкой //Тер.архив №5, 1989, с. 26-3!//.
149. Фоломеева О.М., Амирджанова В.Н., Якушева Е.О. и др. Анализ структуры 13 класса болезней. //Росс.ревмат., №1, 1998, с.2-7//.
150. Фоломеева О.М., Буланова Т.Д., Березова Н.Ю. Лимфоцитотоксические и антимозговые антитела у больных системной красной волчанкой с поражением нервной системы.//Тер.архив № 7, 1983, с. 28-32.//
151. Харлап Г.В., Смолянинова Н.Г. Возможности дуплексного сканирования в оценке почечного кровотока у больных хроническими заболеваниями почек с артериальной гипертонией //Визуализация в клинике № 8, июнь,1996, с.32-36//.
152. Шехтман М.М. Экстрагенитальная патология и беременность. М.1987, с. 208-217.
153. Шилкина Н.П., ПолтыревА.С., Прибытков Ю.Н. Клинико-патогенетические аспекты синдрома Рейно при некоторых ревматичеких заболевайиях.//Кл.ревмат.№ 2, 1995,с.40-41//.
154. Шилкина Н.П., Романов Б.А., Полтырев А.С. и др. Функциональная активность полиморфно- ядерных лейкоцитов при системной краской волчанки и узелковом периартериите//Ревматология № 1,1991, с. 3-6//.
155. Шилов Е.М., КрасноваТ.Н., ИвановА.А., Тареева И.Е. Клиническое испытание нового метода лечения хронического нефрита сверхвысокими дозами циклофосфана. //Клин.медицина № 3, 1995, с. 86-90//.
156. Шишкин В.И., Белендер М.Э., Писарева Н.В. и др. Циркулирующие иммунные комплексы при гломерулонефрите и системной красной волчанки, клинико-иммунологические корреляции. //Тер.архив № 6,1981, с. 30-34//.
157. Appel GB Cohen DJ Pirani CL Meltzer J1 Estes D Long-term follow-up of patients with lupus nephritis. A study based on the classification of the World Health Organization.//Am J Med., 1987, Nov, 83(5):877-85//.
158. Appel GB, Valeri A. The course and treatment of lupus nephritis. //Annu. Rev. Med.,1994;45:525-537//.
159. Arima M, Takahara S, lhara H. et al: Predicability of renal allograft prognosis during rejection crisis by ultrasonic Doppler flow technique.// Urology, 19,389,1982//.
160. Asherson RA, Kahamshta MA, Gil A. et al. Cerebrovascular disease and antiphospholipid antibodies in systemic lupus erythematosus, lupus-like disease and primary antibodies syndrom.//Amer.J/Med/-1989.-vol.86.N-4.p.-39l-399//.
161. Asherson RA, Mercey D, Phillips G. et al. Recurrent stroke and multiinfarct dementia in systemic lupus erythematosus: association with antiphospholipid antibodies//Ann.rheum.Dis -1987.vol.-46,p.-605-6l MI.
162. Asherson RA, Piette JC The catastrophic antiphospholipid syndrome 1996. acute multi-organ failure associated with antiphospholipid antibodies: a review of 31 patients. Lupus 1996 Oct;5(5):4l4-417//.
163. Austin H.A., Klippel J.H., Ballow J.E. et al Therapy of lupus nephritis: controlled trial of prednisone and cytotoxic drugs //New Eng.J. Med., 1986, vol.3l4,p.6l4-619//.
164. Bacon P.A. Aetiopathegenesis of vasculitis //HellenJ.Rheumatol. l992,vol.4(suppl.6), p. 187194//.
165. Bakir AA, Levy PS, Dunea G The prognosis of lupus nephritis in African-Americans a retrospective analysis. //Am J Kidney Dis 1994 Aug;24(2): 159-171 //.
166. Ballow J.E., Austin H.A., Muenz L.R. et al. Effect of treatment on the evolution of renal abnormalitils in lupus nepphritis//New Engl.J. Med., 1984, vol. 311,8, p.491 495//.
167. Bhimma R, Coovadia HM, Adhikari M Improved outcome of systemic lupus erythematosus among children in Durban. //South Africa. Ann Trop Paediatr 1994; 14(2): 119-124//.
168. Bray V., West S. Kristo D. Simultaneous presentation of thrombotic thrombocytopenic purpura and systemic lupus erythematosus//Southern medical J,1994, 8, vol. 87, p.827-830//.
169. Brennan DC Yui MA Wuthrich RP Kelley VE Tumor necrosis factor and IL-l in New Zealand Black/White mice. Enhanced gene expression and acceleration of renal injury.// J Immunol (1989 Dec I) 143(11):3470-5//.
170. Bussel A, Bou lech far H, Nairn R Immunoglobulins or plasma exchange? Synchronization of plasma exchange and intravenous polyvalent immunoglobulins. A consecrtive study of 11 patients. Ann Med Interne (Paris) 1993; 144(8) :532-538//.
171. Clark W.F., Williams W., Cattran D.C. et al. A controlled trial of chronic plasma exchange therapy in SLE//Proc.Amer.Soc.Nephrol.,1983,p.86-90//.
172. Couillault G, Gouyon JB, Chalopin JM, Rifle G Value of plasma exchange in neurologic complications of acute disseminated lupus erythematosus children. //Arch Fr Pediatr 1985 Jan;42(l):4l-43//
173. Couriel D, Weinstein R Complications of therapeutic plasma exchange: a recent assessment. //J Clin Apheresis l994;9(l):l-5//.
174. Cruickshank B. The basic pattern of tissue damage and pathology of systemic lupus erythematosus//Dubois lupus erythematosus//Ed.by DJ.Wallace, E.L.Dubois.-Philadelphia,l987.p.53-71//.
175. Csipo I, Kavai M, Kiss E, Bedo Z, Csongor J, Szegedi G, Philbert F, Cohen JH Serum complement activation of SLE patients during plasmapheresis. //Autoimmunity I997;25(3):I39-146//.
176. Cui HL, Ma L, Zhu RQTherapeutic plasmapheresis in systemic lupus erythematosus). //Chung Hua Nei Ко Tsa Chih 1990 Jul;29(7):422-424//
177. Dafna D. Prognosis and Treatment of Systemic Lupus Erythematosus //Current Opinion in Rheumatology, 1996, 8; p. 430-437//.
178. Decker J.L. On survivorship in the nephritis of SLE.//Arth.Rhem., 1975,18.p.497-500//.
179. Decker J.L. The management of systemic lupus erythematosus //Arthr.&Rheum.,l982, vol.25, 7, p.891-894//.
180. Decker JL, Steinberg AD, Reinertsen JL et al Systemic lupus erythematosus: evolving concepts //Ann.intern.Med.-l979-vol.9l,p-587-604//.
181. Dielzel W , Gutter W , Meffert H et al polyclonal В cell activation in acute phase of systemic lupus erythematosus-aspects of pathogenic significance Hi invest, Dermatol,1982, 78, p 87-90///
182. Dimitrios T Boumpas, Howard A Austin et all, Systemic Lupus Erythmatosus Emerging Concepts//Annals of Internal Medicine, V 122-12, 1995, p-940-950,(part l),V 123-1, 1995, (part 2)p 42-53//
183. Dinkel E , Ertel M , Dittrich M et al Kidney size in childhood Sonographical growth charts for kidney length and volume //Pediatric Radiology, 15, 38, 1985//
184. Donadio JV, Holley KE, Ferguson RH, Gestrup DM Treatment of diffuse proliferative lupus nephritis with prednisone and combined prednison and cyc!ophosphamide//New Engl J Med ,1978, Vol 299, p 1151-1155//
185. Donadio JV Jr, Hart GM, Bergstralh EJ, Holley KE Prognostic determinants in lupus nephritis a long-term clmicopathologic study// Lupus 1995 Apr,4(2) 109-115//
186. Drenkard С Villa AR Garcia-Padilla С Perez-Vazquez ME Alarcon-Segovia D Remission of systematic lupus erythematosus// Medicine (Baltimore), 1996, Mar,75(2) 88-98//
187. Emlen W , Neibur J Kadera R Accelerated in vitro appoptosis of lymphocytes from patients with systemic lupus erythmatosus// J Immunol l994,voll52p 3685-3892//
188. Enckson R, Franklin W, Emlen W Treatment of hemorrhagic lupus pneumonitis with plasmoferesis//Seminars Arthr Rheum 1994 2 vol 24 p 114-123//
189. Esdaile JM Abrahamowicz M MacKenzie T Hayslett JP Kashgarian M The time-dependence of long-term prediction in lupus nephritis // Arthritis Rheum (1994 Mar) 37(3) 35°-68//
190. Esdaile JM, Abrahamowicz M MacKenzie T Hayslett JP, Kashgarian M The time-dependence of long-term prediction in lupus nephritis //Arthritis Rheum 1994 Mar 37(3) 359-368//
191. Esdaile JM Joseph L MacKenzie T, Kashgarian M, Hayslett JP The pathogenesis and prognosis of lupus nephritis information from repeat renal biopsy //Semm Arthritis Rheum 1993 Oct,23(2) 135-148//
192. Fessler BJ, Boumpas DT Severe major organ involvement in systemic lupus erythematosus Diagnosis and management //Rheum Dis Clin North Am 1995 Feb,21(1) 81-98//
193. Fukuda M, Kamiyama Y, Kawahara K, Kawamura K, Mori T, Honda M The favourable effect of cyclophosphamide pulse therapy in the treatment of massive pulmonary haemorrhage in systemic lupus erythematosus. //Eur J Pediatr 1994 Mar; 153(3): 167-170//.
194. Funauchi M, Ikoma S, Enomoto H, Ohno M, Kinoshita K, Horiuchi A, Kurata High-affinity anti-DNA antibody parallels clinical course of immunoadsorption therapy for systemic lupus erythematosus. Intern Med 1996 May;35(5):367-372//
195. Garin EH, Sleasman JW, Richard GA, Iravani AA, Fennell RS Pulsed methylprednisolone therapy compared to high dose prednisone in systemic lupus erythematosus nephritis. //Eur J Pediatr 1986 Oct;l45(5):380-383//
196. Geffner J.R., Trevani A.S., Schatner M. et al Activation of human neutrphils and monocytes induced by immune complexes prepared with cationized antibodies or antigens //Clin. Immunol.Immunopathol., 1993,vol.69, p.9-15//.
197. Ginzler E.M., Diamond H.S.,Weiner M.et al.A multicenter study of outcome in systemic lupus erythmatosus.l.Entry variables as predictor of prognosis //Arth.Rheum.,1982.,vol.25, 6, p.60l-6! ML
198. Ginzler EM., Blumental DR. Renal involvement in SLE: clinical and pathological spectrum //Rheumatology:The Kidney and Rheumatic Disease/Eds P.A.Bacon N.M.Hadler.London.-l982.-P.2-20//.
199. Gladman DD Indicators of disease activity, prognosis, and treatment of systemic lupus erythematosus. //Curr Opin Rheumatol 1994 Sep;6(5):487-492//.
200. Gladman DD Prognosis and treatment of systemic lupus erythematosus. //Curr Opin Rheumatol1995 Sep;7(5):402-408//.
201. Gladman DD Prognosis and treatment of systemic lupus erythematosus. //Curr Opin Rheumatol1996 Sep;8(5):430-437//.
202. Gladman DD Prognosis of systemic lupus erythematosus and factors that affect it. //Curr Opin Rheumatol 1992 Oct;4(5):68l-687//.
203. Gladman DD, Urowitz MB, Ong A, Gough J, MacKinnon A Lack of correlation among the 3 outcomes describing SLE: disease activity, damage and quality of life. Clin Exp Rheumatol 1996 May;14(3):305-308//.
204. Glassock R.J., Cohen A.H., Adler S.G., Ward H.J. Secondary glomerular diseases//The Kidney/Eds B.M.Brener, F.C. Recor, Philadelphia, 1986, vol.1, p. 1014-. 084//.
205. Hanly JG, Hong C, Zayed E, Jones JV, Jones E Immunomodulating effects of synchronised plasmapheresis and intravenous bolus cyclophosphamide in systemic lupus erythematosus. //Lupus 1995 Dec;4(6):457*463//.
206. Hara 1. Immunopathologica) stadies on lupus nephritis; detection of antibodies to nuclea ribonucleoprotein(RNP) and Sm in kidney eluates./ZOcavama l.Z.,1983,95,p.283-294//.
207. Harisdangkul V Nilganuwonge S Rockhold L Cause of death in systemic lupus erythematosus: a pattern based on age at onset.//South Med J (1987 Oct) 80(10): 1249-53//.
208. Hubbard HC, Portnoy В Systemic lupus erythematosus in pregnancy treated with plasmapheresis. //Br. J. Dermatol., 1979, Jul;l0l(l):87-89//.
209. Ito S, Watanabe T, Saeki T.et al Outcome of patients with chronic systemic lupus erythematosus. //Ryumachi 1995 Jun;35(3):505-5H//.
210. Jain R„ Chartash E., Susin M et al Systemic lupus erythematosus complicated by thrombotic microangiopathy //Seminars in Arth. Rheum.,vol.24, 3, p 173-182//.
211. Jarrousse B, Bianchi P, Lhote F, Gayraud M, Leon A, Ribard P. Kahn MF, Guillevin L Synchronization of plasma exchange and cyclophosphamide in severe systemic diseases. A consecutive study of 10 patients. //Presse Med., 1993, Feb 27;22(7):293-298//.
212. Jordan SC, Ho W, Ettenger R, Salusky IB, Fine RN Plasma exchange improves the glomerulonephritis of systemic lupus erythematosus in selected pediatric patients. //Pediatr Nephrol 1987 Jul;l(3):276-280//.
213. Kaine Jeffrey L., Leslie E.Kahl Which laboratory tests are useful in diagnosing SLE?//The Journal of Musculoskeletal Medicine,1992-1 l,p.-l5-27//.
214. Kallenberg C., Cohen G.M., Nervaert et all //Immunol.Today, 1991, V.12, p.6l//.
215. Kamuran Konca,Eren Erken. Do Antineutrophil Cytoplasmic Antibodies Correlate with Disease Activity in Systemic Lupus Erythmatosus?/J.of Rheumat., 1996-23:11, p.-2007//.
216. Karlson EW, Daltroy LH, Lew RA et al The relationship of socioeconomic status, race, and modifiable risk factors to outcomes in patients with systemic lupus erythematosus. //Arthritis Rheum 1997 Jan;40(l):47-56//.
217. Kaufman R.I., Herrmmann W.A., Meijer C.I.et al Circulating and tissue bound immune complexes in allergic vasculites: relationship between immunoglobulin class and clinical features.// Clin.Exp.lmmunol., 1980,41 ,p.459-470//.
218. Kennet J.M., Taylor & William H. Marks Use of Doppler imaging for evalution of dysfunctoin in renal allografts//American Journal of Roentgenology, 155, 536, 1990//.
219. Klippel JH. Is aggressive therapy effective in lupus? //Rheum Dis. Clin North. Am., 1993:19:249-61//.
220. Klippel JH Systemic lupus erythematosus: demographics, prognosis, and outcome. //J. Rheumatol. Suppl. 1997, May;48:67-71//.
221. Konca K., Erken Eren Do Antineutrophil Cytoplasmic Antibodies Correlate with Disease Activity in Systemic Lupus Erythmatosus?//J.of Rheumat., 1996,23:11, p.-2007//.
222. Laitman RS Glicklich D Sablay LB Grayzel Al Barland P Bank N Effect of long-term normalization of serum complement levels on the course of lupus nephritis see commentsJ//Am J Med (1989 Aug) 87(2): 132-8//.
223. Lamberts SW The glucocorticoid insensitivity syndrome. //Horm Res I996;45 Suppl 1:2-4//.
224. Lamberts SW, Huizenga AT, de Lange P.et al tClinical aspects of glucocorticoid sensitivity .//Steroids 1996 Apr;61 (4): 157-160//.
225. Leaker В., Failey K.F., Dowling J., Kincaid-Smith P. Lupus nephritis: clinical and pathological correlation //QuartJ.Med.-l987.-Vol.62,N23 P.-163-179//.
226. Liebling MR, McLaughlin K, Boonsue S.et al Monthly pulses of methyl prednisolone in SLE nephritis. //J. Rheumatol. 1982 JuI;9(4):543-548//.
227. Makino H, Haramoto T, Shikata К, Ogura T, Ota Z Minimal-change nephrotic syndrome associated with systemic lupus erythematosus //Am J Nephrol, 1995,15(5) 439-441//
228. Marshall S , Dressier R, D Agati Membranous Lupus Nephritis with Cytoplasmic Antibody-Associated Segmental Necrotizing and Crescentic Glomerulonephritis//American Journal of Kidney Diseases, V 29 1-1975, p 119-124//
229. McLaughlin J, Gladman DD, Urowitz MB Kidney biopsy in systemic lupus erythematosus II Sur/ival analyses according to biopsy results // Arthritis Rheum (1991 Oct) 34( 10) 1268-73//
230. Mills J A Systemic lupus erythematosus, review articles //Med progress,vol 330, 26 p 18711879//
231. Mitic 1, Fele D, Lenert P et al Methyl prednisolone pulse therapy in the early phases of lupus nephritis //Srp Arh Celok Lek 1996,124 Suppl I 67-69//
232. Mitsias P, Levme S Large cerebral vessel occlusive disease in systemic lupus erythematosus //Neurology, March, 1994, p 385-393//
233. Mokrzycki MH, Kaplan AA Therapeutic plasma exchange complications and management //Am J Kidney Dis 1994 Jun 23(6) 817-827//
234. Molina J Drencard С et a! Systemic lupus erythematosus in males A study of 107 Latin American patients//J of Rheum , 1995 vol 75, 3 p-124-130//
235. Moran Michael G Psychiatric Aspects of Rheumatology Hi of Rheumat V-19 1996-3 p 575586//
236. Morito С Sano H et al Corielation between clinical activity of systemic lupus erythematosus and the amounts of DNA in DNA/anti-DNA antibody immune complexes Hi Immunol 1982 129 p I960 1965//
237. Mosca M Pasquariello A Tavoni A Monconi L Moneta I Innocenti M Bencivelh W Bombardieri S Predictors of renal outcome in diffuse proliferative glomerulonephritis in systemic lupus erythematosus //Lupus 1997 6(4) 371-378//
238. Murali R, Jeyaseelan L Rajaratnam Set al Systemic lupus erythematosus in Indian patients prognosis, survival and life expectancy//Nath Med J India, 1997 Jul 10(4) 159-164//
239. Nesher G Hanna V E et al Ttrombotic microangiopathic hemolytic anemia in systemic lupus erythematosus//Seminars in Arth & Rheum ,vol 24,3(Dec ) I994,p 165-172//
240. Nesher G , Osborn Th Moore T Parvovirus infection mimicking systemic lupus erythematosus //Seninars in Arth Rheum , 1995 5, vol 24, p 297-303//
241. Neumann К, Wallace DJ, Azen C.et al Lupus in the 1980s: III. Influence of clinical variables, biopsy, and treatment on the outcome in 150 patients with lupus nephritis seen at a single center .//Semin Arthritis Rheum t995 Aug;25(l):47-55//.
242. Neuwelt CM, Lacks S, Kaye BR et al Role of intravenous cyclophosphamide in the treatment of severe neuropsychiatric systemic lupus erythematosus.//Am J Med 1995 Jan;98(l):32-4I//.
243. Nishija K., Chikazawa H., Nishimura S. Anti-Neutrophil Cytoplasmic Antibody in Patients with Systemic Lupus Erythematosus is Unrelated to Clinical Features //Clinical Rheumat., 1997, 16-1, p.70-75//.
244. Norris C.S., Pfeiffer J.S, Ritgers S.E. et al Nonivasive evalution of renal artery stenosis and renovascular resistence//Journal of Vascular Surgery, 1,192,1984//.
245. Nossent HC Henzen-Logmans SC Vroom TM Berden JH Swaak TJContribution of renal biopsy data in predicting outcome in lupus nephritis. Analysis of 116 patients.//Arthritis Rheum (1990 Jul) 33(7):970-7//.
246. Partridge AJ, Karlson EW, Daltroy LH et al Risk factors for early work disability in systemic lupus erythematosus: results from a multicenter study. //Arthritis Rheum 1997 Dec;40(l2):2l99-2206//.
247. Pauzner R„ Urowitz M., Dafna G. Antineutrophil Cytoplasmic Antibodies in Systemic Lupus Erythmatosus Hi. Rheumat, 1994,21:9,1670-1673//.
248. Piatt J.F. Doppler ultrasound of the kidney. //Serum Ultrasound C.T., MR. 18(1): 22-32, 1997, Feb.//
249. Piatt J.F., Rubin J.M, Ellis J.H. Lupus nephritis: predictive value of conventional and Doppler US and comparison with serologic and biopsy parameters.// Radiology, 203 (I)- 82-6, 1997, Apr.//
250. Quismorio F.P. Cardiac abnormalities in systemic lupus erythematosus//Ed. by D.J.Wallace, B.H.Hahn.-Lea&Febiger,Philadelphia//London,1993.-Chapt.-3 p.-332-342//.
251. Rachel Pauzner, Murray Urowitz, Dafna D, Gladman D. Antineutrophil Cytoplasmic Antibodies in Systemic Lupus Erythmatosus//J.Rheumat., 1994,2: 1670-3//.
252. Reneto A, Sinico C.P., Monica Waldendorf et al ANCA-Associated Vasculitides //Immumolojical and Clinical Aspects,N.York, 1993,p.385-387,381-384//.
253. Rheumatology//Klippel, John H Dieppe Paul A. Systemic Lupus Erythmatosus // p.6. 2.17.19//.
254. Rigsby C.M, Taylor K.J.M, Wiltin G. et all Renal allografts in acute rejection: evalution using duplex sonography //Radiology, 158,375, 1986//.
255. Robinson T Neuwelt CM Neuropsychiatry lupus and hormones //Ann Med Interne (Paris) 19% 147(4) 276 280//
256. Saito M Nakabayashi К Maemura С et al Morphologic transformation of renal lesions by steroid treatment and its therapeutic implication in a patient with lupus nephritis //Ryumachi 1990 Jun 30(3) 190 195//
257. Samtleben W Blumenstein M Habersetzer R et al Treatment of emergency situations in autoimmune diseases with plasma exchange //Acta Med Austriaca 1982 9(3) 93 97//
258. Schildermans F Dequeker J Van de Putte I Plasmapheresis combined with corticosteroids and cyclophosphamide in uncontrolled active systemic lupus erythematosus //J Rheumatol 1979 Nov 6(6) 687 690//
259. Schneider M Bernmg T Waldendorf M et al Immunoadsorbent plasma perfusion in patients with systemic lupus erythematosus Hi Rheumatol 1990 Jul 17(7) 900 907//
260. Schur P H Systemic lupus erythmatosus//Rheumatology and Immunology 2 Edition Ed by A S Cohen and J С Bennett Grune &Stratton Inc Orlando Toronto 1986 p 247 257//
261. Shayakul С Ong aj yooth L Chirawong Pet al Lupus nephritis in Thailand clinicopathologic findings and outcome in 569 patients // Am J Kidney Dis (1995 Aug) 26(2) 300 7//
262. Segovia Alarcon D Cabral A Antibodies in syc emic lupus erythematosus //Current op In Rheum V 8 1996 p 403 407//
263. Shnabel Armin Csemok Elena Isenberg David A Antmeutrophil Cytoplasmic Antibodies in Systemic Lupus Erythematosus//Aithr&Rheumat V 38 1995 5 p 633 637/
264. Sibbit W L Mathews P M Bankhurst A D The natural killer cell in SLE defects in effector lytic activity and response to interferon and interferon inducter//J Clin Invest 1983 71 p 1230 1239//
265. Sinico RA Pozzi С Radice A et al Clinical Significance of Antmeutrophil Cytoplasmic Antibodies with Specificity for Lactofernn in Renal Diseases //Amer J of Kidney Diseases V 22 2 1993 p 253 260//
266. Sinico С P Reneto A Monica CP et al ANCA Associated Vasculitides Immunolojical and Clinical Aspects //N York 1993 p 385 387 381 384//
267. Sloan RP Schwartz MM Korbet SM Borok RZ Long term outcome in systemic lupus erythematosus membranous glomerulonephritis Lupus Nephritis Collaborative Study Group /J Am Soc Nephrol 1996 Feb 7(2) 299 305//
268. Spronk P.E., Bootsma H., Horst G. et alt Antineutrophil Cytoplasmic Antibodies in Systemic Lupus Erythematosus //Brit J. of Rheumat., 1996, 35, p.625-630//.
269. Spronk P.E., terBorg E.J., Kallenberg C.G. Patients with systemic lupus erythematosus and Jaccoud’s arthropathy: a clinical subset with an increased С reactive protein response? //Ann.rheum.Dis., 1992-vol.51.-p.358-361//.
270. Steinberg A.D. The treatment of lupus nephritis pathological spectrum //Rhematology /Ed. P.A.Bacon, N.M.Hadler.-Kidney int.1986//.
271. Stoll T, Seifert B, Isenberg DA SLICC/ACR Damage Index is valid, and renal and pulmonary organ scores are predictors of severe outcome in patients with systemic lupus erythematosus. //Br J Rheumatol 1996 Mar;35(3):248-254//.
272. Takei S. Maeno N. Shigemori M. et al Clinical features of Japanese children and adolescents with systemic lupus erythematosus: results of 1980-1994 survey. //Acta Paediatr Jpn 1997 Apr;39(2):250-256//.
273. Tan E.M. Autoimmunity and appoptosis// J. Exp.Med., 1994, vol. 179, p. 1083-1086//.
274. Tan EM, Cohen AS, Fries JT et al The 1982 revised criteria for the classification of systemic lupus erythematosus./ Arthritis Rheum. 1982;25:1271 -1277//.
275. Tax E.J., Kramers C., Van Brugen M.C. et al Appoptosis, nucleosomes and nephritis in systemic lupus erythmatosus//Kidney int., 1995, vol 48, p.666-673
276. Valbonesi M, Florio G, Lercari G.et al Plasma exchange: the cost/benefit ratio and the critical revision of indications.//Int J Artif Organs 1993 Dec;l6 Suppl 5:173-176//.
277. Vlachoyiannopoulos PG, Karassa FB, Karakostas KX.et al Systemic lupus erythematosus in Greece. Clinical features, evolution and outcome: a descriptive analysis of 292 patients. //Lupus 1993 Oct;2(5):303-312//.
278. Von Feld J. M, Systemic lupus erythematosus//Postgrad. Medicine, 1995, vol.97, 4, p.79-94//.
279. Wakai S. The criteria for indication of plasma exchange on lupus nephritis.// Nippon Jinzo Gakkai Shi 1990 Jun;32(6}:703-713 //.
280. Walace D., Quismorio F. The elusive search for geographic clusters of systemic lupus erythematosus//Arth. Rheum.,1995, 11, vol 38, p.1564-1567//.
281. Ward M., Pyun E., Studenski S. Mortality risks associated with specific clinical manifestations of systemic lupus erythematosus. //Arch Intern Med 1996 Jun 24; 156( 12): 1337-1344//.
282. Wong S.N. Renal blood flow pattern by noninvasive doppler ultrasound in normal children and acute renal failure patients//.Radiology, vol.-1-P. 1014-1084//.
283. Wu MJ, Shu KH, Cheng CH, Lian JD Complications of membrane-filtration plasma exchange. //Chung Hua I Hsueh Tsa Chih (Taipei) 1997 Sep;60(3):l47-I54//.
284. You DL, Tzen KY, Kao PF.et al Quantitative cerebral perfusion SPECT in systemic lupus erythematosus with severe central nervous involvement-before and after methylprednisolone pulse therapy. Hi Neuroimaging 1998 Jan;8(l):55-57//.
285. Zielinski C, Muller C, Smolen J Use of plasmapheresis in therapy of systemic lupus erythematosus: a controlled study.// Acta Med Austriaca 1988; 15(5): 155-158//.
Лечение системной красной волчанки
Клинические критерии
Острая кожная — скуловая сыпь, буллезная волчанка, токсический эпидермальный некролиз, вариант волчанки, макулопапулезная сыпь, светочувствительная волчанка
Хроническая кожная сыпь — сыпь при дискоидной волчанке, гипертрофическая (бородавчатая) волчанка, панникулит волчанки, волчанка слизистой оболочки, красная волчанка, опухшая волчанка, обморожение, дискоидная волчанка
Язвы в полости рта или носа — на небе, щеках, языке или носу при отсутствии других причин
Алопеция без рубцов — при отсутствии других причин
Артрит — синовит с поражением 2 или более суставов, характеризующийся припухлостью, излиянием или болезненностью 2 или более суставов и утренней скованностью не менее 30 минут
Серозит — типичный плеврит продолжительностью более одного дня, плевральный выпот, шум трения плевры или типичная боль в перикарде более одного дня, выпот в перикард, шум трения перикарда или перикардит по ЭКГ
Поражение почек — соотношение белок мочи: креатинин или суточный белок мочи с содержанием белка> 500 мг / 24 часа или цилиндры красных кровяных телец
Неврологические симптомы — судороги, психоз, множественный мононеврит, миелит, периферическая или краниальная нейропатия, состояние острой спутанности сознания
Гемолитическая анемия — при отсутствии других причин
Лейкопения — при отсутствии других причин
Тромбоцитопения — при отсутствии других причин
Иммунологические критерии
Антинуклеарные антитела
Антитела против дцДНК — выше контрольного диапазона (или> 2 раза, если тестируется с помощью ELISA)
Антитела против Смита
Антифосфолипидные антитела — положительный волчаночный антикоагулянт, ложноположительный экспресс-тест на реагин плазмы, антитело к кардиолипину со средним или высоким титром, положительный анти-b2-гликопротеин
Низкое дополнение C3, C4, CH50
Положительный тест прямого Кумбса — при отсутствии гемолитической анемии
* Для постановки диагноза пациенты должны иметь 4 или более из перечисленных критериев, по крайней мере, 1 клинический и 1 лабораторный критерий
двухцепочечная ДНК дцДНК
Иммуноферментный анализ ELISA
Источник: ссылка 1
Системная красная волчанка.Лечение волчанки; информация
Системная красная волчанка (СКВ) — мультисистемное аутоиммунное заболевание, включающее сложные патогенетические механизмы, которые могут проявляться в любом возрасте. Чаще всего она проявляется у женщин репродуктивного возраста, хотя СКВ все чаще выявляется после 40 лет, особенно у европейцев [1] .
Заболевание склонно к рецидивам и ремиссиям, что приводит к значительной заболеваемости из-за вспышек активности болезни и накопленных повреждений, с повышенным риском преждевременной смерти, в основном из-за инфекции или сердечно-сосудистых заболеваний. [1] .
Красная волчанка описывает типичную сыпь при СКВ, а термин «системный» подчеркивает возможность поражения многих органов. Причина СКВ неизвестна.
Эпидемиология
[1]- Волчанка поразила почти 1 из 1000 населения Великобритании в 2012 году. Стандартизированная по возрасту заболеваемость в Великобритании составляет 8,3 на 100 000 в год для женщин и 1,4 на 100 000 в год для мужчин в Великобритании.
- Самый высокий уровень заболеваемости наблюдается у лиц афро-карибского происхождения, 31 год.4 / 100,000 / год по сравнению с 6,7 / 100,000 / год для белых европейцев происхождения
. Средний возраст постановки диагноза составляет 48,9 года, но он ниже у лиц африканского происхождения в Великобритании и Северной Америке.
Факторы риска
- Определенные типы лейкоцитарного антигена DRB1 человека чаще встречаются у пациентов с волчанкой — например, DR3 и DR2.
- Пациенты с дефектным геном комплемента C4 (нулевой аллель C4A) также заболевают волчанкой.
- К факторам окружающей среды относятся ультрафиолет, вирусы (например, вирус Эпштейна-Барра) и некоторые лекарства.К лекарственным средствам, которые вызывают лекарственную волчанку, относятся хлорпромазин, метилдопа, гидралазин, изониазид, d-пеницилламин и миноциклин.
Презентация
- СКВ — это ремиттирующее и рецидивирующее заболевание с множеством различных проявлений [2, 3] .
- Симптомы и признаки часто неспецифические — например, усталость (может быть тяжелой и изнуряющей), недомогание, лихорадка, спленомегалия, лимфаденопатия, потеря веса, артралгия и усталость, язвы в полости рта, светочувствительная кожная сыпь, плевритные боли в груди, головная боль, парестезии. сухость глаз (сухой кератоконъюнктивит) и сухость во рту, феномен Рейно, легкое выпадение волос и миалгия.
- Симптомы волчанки могут варьироваться от незначительных ноющих болей и сыпи до опасного для жизни заболевания.
- Поражение любого крупного органа имеет тенденцию развиваться в течение пяти лет после начала заболевания.
- Артралгия:
- Боли в суставах и мышцах являются обычным явлением, часто с утренней скованностью.
- Опухание суставов необычно, и артрит обычно не вызывает эрозии.
- У некоторых пациентов развивается деформация и подвывих суставов при поражении сухожилий и периартикулярных мягких тканей (артропатия Жакку).
- Периферический симметричный порхающий полиартрит является типичным.
- Часто встречается вторичная фибромиалгия.
- Феномен Рейно встречается примерно у одной пятой пациентов, но часто протекает в легкой форме.
- Слизисто-кожные:
- Фоточувствительная сыпь.
- Классический признак — скуловая сыпь («бабочка»), часто вызываемая солнечным светом. Он эритематозный, может усиливаться и вызывать зуд. Защищает носогубные складки:
- Дискоидная красная волчанка: может возникать при отсутствии каких-либо системных признаков.Обычно это происходит в местах, подверженных воздействию солнечных лучей. Это эритематозное, хорошо разграниченное и связанное с шелушением:
Дискоидная волчанка
- Другие проявления включают livedo reticularis, диффузную или пятнистую алопецию без рубцов и васкулитные высыпания. Язвы во рту могут быть большими, множественными и болезненными.
- Легочные: плеврит, фиброзирующий альвеолит, облитерирующий бронхиолит. Пациенты с вторичным антифосфолипидным синдромом (APLS) имеют повышенный риск тромбоэмболии легочной артерии.
- Сердечно-сосудистые: перикардит, гипертония, эндокардит Либмана-Сакса, повышенный риск ишемической болезни сердца.
- Почечный: нефрит часто протекает бессимптомно и обнаруживается по протеинурии, гематурии, гипертонии или повышению уровня мочевины или креатинина в сыворотке. Гломерулонефрит часто встречается у пациентов с волчанкой.
- Психоневрологические: тревога и депрессия — обычное явление. У пациентов также могут развиваться психозы, судороги, невропатия, менингит и органический мозговой синдром.
- Волчанка может быть связана практически с любым неврологическим проявлением.Инсульты могут быть вызваны васкулитом или тромбозом, связанным с APLS.
Диагноз
[4]Система классификации СКВ Американского колледжа ревматологии предполагает, что человек может быть классифицирован как страдающий волчанкой, если присутствуют четыре или более из следующих 11 критериев (которые не обязательно должны возникать в в одно и то же время, но может накапливаться за несколько лет):
- Малярная сыпь.
- Дискоидная волчанка.
- Светочувствительность.
- Язвы полости рта или носоглотки.
- Неэрозивный артрит с поражением двух или более периферических суставов.
- Плеврит или перикардит.
- Поражение почек со стойкой протеинурией или клеточными цилиндрами.
- Судороги или психоз.
- Гематологическое нарушение: гемолитическая анемия или лейкопения или лимфопения или тромбоцитопения.
- Иммунологическое заболевание: антитела против ДНК или антитела против Sm или антитела против фосфолипидов.
- Положительное антинуклеарное антитело.
Однако Международный индекс сотрудничающих клиник по системной волчанке 2012 (SLICC-12) более чувствителен и может позволить классифицировать пациентов как имеющих СКВ на более ранней стадии развития болезни.
Исследования
[1]СКВ — мультисистемное аутоиммунное заболевание. Диагноз требует сочетания клинических признаков и наличия хотя бы одного значимого иммунологического отклонения. Если есть клиническое подозрение на волчанку, следует проверить анализы крови, включая серологические маркеры.
- При подозрении на СКВ полезными скрининговыми исследованиями являются общий анализ мочи, общий анализ крови, СОЭ или вязкость плазмы и антинуклеарный фактор.
- Общий анализ мочи: в качестве начального теста на протеинурию / гематурию.
- Общий анализ крови и СОЭ:
- Легкая нормохромная нормоцитарная анемия является обычным явлением. Анемия у пациентов с волчанкой может быть вызвана лекарствами или хроническим заболеванием, но иногда она возникает из-за гемолитической анемии. В этом случае может потребоваться проверка антител Кумбса, количества ретикулоцитов и гаптоглобинов.
- Лейкопения и тромбоцитопения возникают часто, но также могут быть вызваны иммуносупрессивной терапией.
- СОЭ повышена, но уровень СРБ может быть нормальным, если нет интеркуррентной инфекции или серозита.
- Серология:
- Антинуклеарные антитела (АНА) присутствуют примерно у 95% пациентов с СКВ. Если тест отрицательный, клиническая вероятность наличия у пациента СКВ низкая. Положительный результат АНА встречается примерно у 5% взрослого населения и сам по себе имеет низкую диагностическую ценность при отсутствии клинических признаков аутоиммунного ревматического заболевания.
- Наличие антител против дцДНК, низкие уровни комплемента или антител против Смита (Sm) являются высокопрогнозирующими факторами диагноза СКВ у пациентов с соответствующими клиническими признаками. Антитела против Ro / La и против RNP являются менее специфическими маркерами СКВ, поскольку они обнаруживаются при других аутоиммунных ревматических заболеваниях, а также при СКВ.
- Антифосфолипидные антитела следует тестировать у всех пациентов с волчанкой на исходном уровне, особенно у тех, у кого в анамнезе есть неблагоприятная беременность или события артериального / венозного тромбоза.Подтверждающими тестами на антифосфолипидный синдром являются положительные результаты на антикоагулянт против волчанки, антитела против кардиолипина (IgG, IgM) и / или анти-бета-2 гликопротеин-1 (IgG, IgM) в двух случаях с интервалом не менее 12 недель.
- Другие исследования будут зависеть от вовлеченности системы — например, МРТ головного мозга, эхокардиограмма, биопсия почек.
- Женщины с СКВ имеют значительно повышенный риск преждевременного атеросклероза, и этот риск не зависит от установленных факторов риска сердечно-сосудистых заболеваний. Поэтому очень важен мониторинг всех факторов риска сердечно-сосудистых заболеваний.
Сопутствующие заболевания
- APLS.
- Синдромы перекрытия: некоторые пациенты с «волчанкой» не имеют чистой СКВ, как описано, но имеют общие черты с другими заболеваниями соединительной ткани, такими как склеродермия, полимиозит, ревматоидный артрит и синдром Шегрена.
- Они предрасположены к другим аутоиммунным заболеваниям, таким как тиреоидит. У них также выше частота лекарственной аллергии и повышенный риск заражения.
- Пациенты с СКВ также подвержены повышенному риску некоторых других сопутствующих заболеваний, включая атеросклероз, гипертензию, дислипидемию, диабет, остеопороз, аваскулярный некроз и злокачественные новообразования (особенно неходжкинскую лимфому) [6] .
Ведение
Пациентам часто требуется серьезная консультация по поводу их индивидуального прогноза и симптомов. По возможности избегайте пребывания на солнце и пользуйтесь солнцезащитными экранами. Выявить и лечить любую первопричину (например, анемию, депрессию) и поощрять регулярные аэробные упражнения.
- Боли в суставах и мышцах, головные боли и скелетно-мышечные боли в груди поддаются лечению простыми анальгетиками и нестероидными противовоспалительными препаратами (НПВП) — последние следует применять с осторожностью из-за рисков для желудочно-кишечного тракта, почек и сердечно-сосудистой системы.
- Когда простой анальгезии и НПВП недостаточно для контроля симптомов или заболевания, рассматривается дополнительное лечение, в зависимости от отдельных задействованных систем:
- Кортикостероиды.
- Гидроксихлорохин.
- Циклофосфамид предназначен для лечения опасных для жизни заболеваний, особенно волчаночного нефрита, васкулита и церебральных заболеваний.
- Микофенолят мофетил [7] :
- Микофенолят мофетил может привести к усилению полной ремиссии заболевания по сравнению с внутривенным циклофосфамидом с приемлемым профилем нежелательных явлений.
- Кальциневрин в сочетании с микофенолятмофетилом в более низких дозах может улучшить индукцию ремиссии заболевания по сравнению с внутривенным введением циклофосфамида.
- Азатиоприн может увеличить рецидив заболевания в качестве поддерживающей терапии по сравнению с мофетилом микофенолят.
- Азатиоприн используется в качестве стероидсберегающего средства. В качестве альтернативы циклофосфамиду азатиоприн намного безопаснее, но, вероятно, менее эффективен, особенно при активном нефрите. Азатиоприн действительно предрасполагает к инфекции, но в меньшей степени, чем терапия циклофосфамидом или кортикостероидами.
- Другие иммунодепрессанты, применяемые при тяжелой СКВ, включают метотрексат и циклоспорин.
- Внутривенное введение объединенных высоких доз гаммаглобулина и гранулоцитарно-колониестимулирующего фактора играет роль в аутоиммунной тромбоцитопении и нейтропении. Внутривенные иммуноглобулины все чаще используются для лечения резистентной волчанки, а также играют роль у пациентов с сопутствующей инфекцией и активной волчанкой, для которых иммуносупрессивное лечение часто не подходит.
- Белимумаб (модулятор цитокинов) подавляет активность стимулятора В-лимфоцитов.Белимумаб лицензирован в качестве дополнительной терапии у пациентов с активной, аутоантителопозитивной СКВ с высокой степенью активности заболевания, несмотря на стандартную терапию [8] .
- Другие «биологические препараты», которые использовались для лечения резистентной СКВ, включают антагонисты TNF, ритуксимаб, абатацепт, тоцилизумаб и экулизумаб [9] .
- Пациенты, которые серьезно болеют опасным для жизни заболеванием, могут пройти плазмаферез в качестве меры задержки, пока иммуносупрессивная терапия не вступит в силу.
- Пациентам с волчанкой следует предложить вакцинацию от гриппа; им не следует делать живые прививки.
Нейропсихиатрическая СКВ
[10]- Глюкокортикоиды и иммуносупрессивная терапия показаны, когда считается, что нейропсихиатрическая СКВ отражает воспалительный процесс (неврит зрительного нерва, поперечный миелит, периферическую невропатию, рефрактерные судороги и психоз) наличие генерализованной волчаночной активности.
- Имеются доказательства очень низкого качества, что циклофосфамид более эффективен в уменьшении симптомов нейропсихиатрического вовлечения при СКВ по сравнению с метилпреднизолоном [11] .
- Антитромбоцитарная / антикоагулянтная терапия показана, когда проявления связаны с антифосфолипидными антителами, особенно с тромботическими сердечно-сосудистыми заболеваниями.
Рекомендации Британского общества ревматологов
[1]Ведение легкой формы СКВ
- Лечение легкой неорганической болезни включает в себя модифицирующие болезнь препараты гидроксихлорохин и метотрексат, а также короткие курсы НПВП для контроля симптомов. Эти препараты позволяют избежать приема кортикостероидов или снизить их дозу.
- Преднизолон в низкой дозе до 7,5 мг / день или меньше может потребоваться для поддерживающей терапии. Препараты для местного применения могут использоваться при кожных проявлениях и внутрисуставных инъекциях при артрите.
- Солнцезащитные кремы с высоким фактором UVA и UVB важны для лечения и предотвращения поражений кожи, вызванных УФ-излучением. Пациентов также следует проинформировать о том, как избегать попадания солнечных лучей и использовать защитную одежду.
Ведение СКВ средней степени тяжести
- Ведение СКВ средней степени тяжести включает более высокие дозы преднизолона (до 0.5 мг / кг / сут), или применение метилпреднизолона в дозах внутримышечно или внутривенно.
- Иммунодепрессанты часто требуются для борьбы с активным заболеванием и являются стероидсберегающими агентами. Они также могут снизить риск долгосрочного повреждения.
- Метотрексат, азатиоприн, микофенолятмофетил, циклоспорин и другие ингибиторы кальциневрина следует рассматривать в случаях артрита, кожных заболеваний, серозита, васкулита или цитопении, если гидроксихлорохина недостаточно.
- В рефрактерных случаях можно рассмотреть возможность применения белимумаба или ритуксимаба.
Ведение тяжелой СКВ
- Пациентам с тяжелой СКВ, включая почечные и психоневрологические проявления, необходимо тщательное обследование, чтобы исключить другие этиологии, включая инфекцию.
- Лечение зависит от основной этиологии (воспалительной и / или тромботической), и пациентов следует лечить соответственно иммуносупрессией и / или антикоагулянтами.
- Иммуносупрессивные схемы лечения тяжелой активной СКВ включают в себя метилпреднизолон внутривенно или пероральный преднизолон в высоких дозах (до 1 мг / кг / день), чтобы вызвать ремиссию самостоятельно или чаще в рамках протокола лечения другим иммунодепрессивным препаратом.
- Микофенолятмофетил или циклофосфамид используются в большинстве случаев волчаночного нефрита и при рефрактерных тяжелых непочечных заболеваниях.
- Биологическая терапия белимумабом или ритуксимабом может быть рассмотрена в индивидуальном порядке, если пациенты не смогли применить другие иммунодепрессанты из-за неэффективности или непереносимости.
- Внутривенный иммуноглобулин и плазмаферез могут быть рассмотрены у пациентов с рефрактерной цитопенией, тромботической тромбоцитопенической пурпурой, быстро ухудшающимся острым состоянием спутанности сознания и катастрофическим вариантом антифосфолипидного синдрома.
Контрацепция, фертильность и беременность
- Гормоны эстрогена могут обострить волчанку, но оральные противозачаточные таблетки с минимальной дозой эстрогена можно назначать осторожно, при условии, что в анамнезе нет мигрени, гипертонии или тромбоза и если антикардиолипиновые антитела отрицательны. Однако существует повышенный риск тромбоза.
- Фертильность нормальная, и беременность безопасна при легкой или стабильной волчанке. При тяжелой волчанке беременность следует отложить до тех пор, пока болезнь не станет лучше контролироваться. [12] :
- Заболеваемость беременными — обычное явление, особенно если у женщины есть антифосфолипидные антитела.
- Осложнения включают повторяющуюся преждевременную потерю беременности, преэклампсию, ограничение внутриутробного развития и преждевременные роды. Женщины подвержены повышенному риску тромбоза, особенно в послеродовом периоде.
- Риск беременности значительно возрастает при наличии волчаночного нефрита, гипертонии и активного заболевания, особенно во время зачатия [13] .
- Существовавшее ранее заболевание почек может ухудшиться во время беременности, и гипертонию трудно контролировать.
- Низкомолекулярный гепарин и низкие дозы аспирина в настоящее время являются лечением выбора для женщин с APLS и выкидышем в анамнезе.
Прогноз
[1]Хотя выживаемость с СКВ улучшилась за последние 40 лет, люди с СКВ по-прежнему умирают на 25 лет моложе, чем в среднем в Великобритании.
- Смерть от активной волчанки в Великобритании встречается редко. Однако сообщалось о 10% смертности в течение 20 лет при среднем возрасте смерти 53,7 года.
- Около трети пациентов с СКВ в Великобритании заболевают волчаночным нефритом. Пациенты африканского происхождения, как правило, в молодом возрасте заболевают волчаночным нефритом в Великобритании, США и других странах и имеют значительный риск развития терминальной стадии почечной недостаточности (ТПН) и преждевременной смерти.
- В одной британской когорте ТПН встречалась у 20% пациентов с волчаночным нефритом в течение 10 лет после постановки диагноза, а средний возраст смерти у пациентов с волчаночным нефритом составлял 40,3 года со средним сроком 7,5 лет между развитием волчаночного нефрита и смертью.
Терапия системной красной волчанки (СКВ): старое и новое
Tsokos GC. Системная красная волчанка. N Engl J Med. 2011; 365: 2110–21.
Релле М., Фоер Б., Швартинг А. Эпигенетические аспекты системной красной волчанки. Rheumatol Ther. 2015; 2: 33–46.
PubMed PubMed Central Google Scholar
Бодис Г., Тот В., Швартинг А. Роль лейкоцитарных антигенов человека (HLA) в аутоиммунных заболеваниях.Rheumatol Ther. 2018; 5: 5–20.
PubMed PubMed Central Google Scholar
Аринджер М., Костенбадер К., Дайх Д. и др. Европейская лига против ревматизма / Американский колледж ревматологии 2019 критерии классификации системной красной волчанки. Ann Rheum Dis. 2019; 78: 1151–9.
PubMed Google Scholar
Borchers AT, Keen CL, Shoenfeld Y, Gershwin ME.Выживание бабочки и волка: тенденции смертности от системной красной волчанки. Autoimmun Rev.2004; 3: 423–53.
PubMed Google Scholar
Frodlund M, Reid S, Wetterö J, Dahlström Ö, Sjöwall C, Leonard D. Большинство шведских пациентов с системной красной волчанкой все еще страдают необратимым поражением органов: факторы, связанные с накоплением повреждений в двух региональных когортах. Волчанка. 2019; 28: 1261–72.
CAS PubMed PubMed Central Google Scholar
Вильгельм Т.Р., Магдер Л.С., Петри М. Ремиссия при системной красной волчанке: стойкая ремиссия встречается редко. Ann Rheum Dis. 2017; 76: 547–53.
PubMed Google Scholar
Тани С., Вагелли Р., Стагнаро С., Карли Л., Моска М. Ремиссия и низкая активность заболевания при системной красной волчанке: достижимая цель даже при меньшем количестве стероидов? Реальные данные моноцентрической когорты. Lupus Sci Med. 2018; 5: e000234.
PubMed PubMed Central Google Scholar
Франклин К., Лау С.С., Наварра С.В. и др. Определение и первоначальная проверка состояния низкой активности волчанки (LLDAS). Ann Rheum Dis. 2016; 75: 1615–21.
CAS PubMed Google Scholar
Голдер В., Кандане-Ратнаяке Р., Хой А.Ю. и др. Связь состояния низкой активности волчанки (LLDAS) с качеством жизни, связанным со здоровьем, в многонациональном проспективном исследовании. Arthritis Res Ther. 2017; 19:62.
PubMed PubMed Central Google Scholar
Morand EF, Mosca M. Лечение СКВ до достижения цели, ремиссии и низкой активности заболевания. Лучшая практика Res Clin Rheumatol. 2017; 31: 342–50.
PubMed Google Scholar
Ли SJ, Silverman E, Bargman JM. Роль противомалярийных средств в лечении СКВ и волчаночного нефрита. Нат Рев Нефрол. 2011; 7: 718–29.
CAS PubMed Google Scholar
Meinão IM, Sato EI, Andrade LE, Ferraz MB, Atra E.Контролируемое исследование хлорохиндифосфата при системной красной волчанке. Волчанка. 1996; 5: 237–41.
PubMed Google Scholar
Аларкон Г.С., МакГвин Дж., Бертоли А.М. и др. Влияние гидроксихлорохина на выживаемость пациентов с системной красной волчанкой: данные LUMINA, многоэтнической когорты США (LUMINA L). Ann Rheum Dis. 2007; 66: 1168–72.
PubMed PubMed Central Google Scholar
Ponticelli C, Moroni G. Гидроксихлорохин при системной красной волчанке (СКВ). Экспертное мнение Drug Saf. 2017; 16: 411–9.
CAS PubMed Google Scholar
Зонана-Накач А., Барр С.Г., Магдер Л.С., Петри М. Повреждение системной красной волчанки и его связь с кортикостероидами. Ревматоидный артрит. 2000; 43: 1801–8.
CAS PubMed Google Scholar
Гладман Д.Д., Уровиц М.Б., Рахман П., Ибаньес Д., Там Л.-С. Накопление повреждений органов с течением времени у пациентов с системной красной волчанкой. J Rheumatol. 2003; 30: 1955–9.
PubMed Google Scholar
Thamer M, Hernán MA, Zhang Y, Cotter D, Petri M. Преднизон, волчаночная активность и необратимое повреждение органов. J Rheumatol. 2009; 36: 560–4.
CAS PubMed PubMed Central Google Scholar
Апостолопулос Д., Моран EF. Это никуда не делось: проблема использования глюкокортикоидов при волчанке остается. Ревматология (Оксфорд). 2017; 56: i114 – i12222.
CAS Google Scholar
Gourley MF, Austin HA 3rd, Scott D, et al. Метилпреднизолон и циклофосфамид, по отдельности или в комбинации, у пациентов с волчаночным нефритом. Рандомизированное контролируемое исследование. Ann Intern Med. 1996. 125: 549–57.
CAS PubMed Google Scholar
Houssiau FA, Vasconcelos C, D’Cruz D, et al. Иммуносупрессивная терапия при волчаночном нефрите: исследование Euro-Lupus Nephritis, рандомизированное исследование низких и высоких доз внутривенного циклофосфамида. Ревматоидный артрит. 2002; 46: 2121–31.
CAS PubMed Google Scholar
Парих С.В., Алмаани С, Бродский С, Ровин Б.Х. Обновленная информация о волчаночном нефрите: Core Curriculum 2020. Am J Kidney Dis. 2020. https://doi.org/10.1053/j.ajkd.2019.10.017.
Лю З., Чжан Х., Лю З. и др. Мультитаргетная терапия для индукционного лечения волчаночного нефрита: рандомизированное исследование. Ann Intern Med. 2015; 162: 18–26.
PubMed Google Scholar
Rovin BH, Solomons N, Pendergraft WF 3rd, et al. Рандомизированное контролируемое двойное слепое исследование, сравнивающее эффективность и безопасность воклоспорина с различными дозами и плацебо в достижении ремиссии у пациентов с активным волчаночным нефритом.Kidney Int. 2019; 95: 219–31.
CAS PubMed Google Scholar
Угарте-Хил М.Ф., Аларкон GS. Системная красная волчанка: терапевтический вызов XXI века. Clin Rheumatol. 2014; 33: 441–50.
PubMed Google Scholar
Eriksson P, Wallin P, Sjöwall C. Клинический опыт сиролимуса в отношении эффективности и безопасности при системной красной волчанке.Front Pharmacol. 2019; 10: 82.
CAS PubMed PubMed Central Google Scholar
Лай З.В., Келли Р., Винанс Т. и др. Сиролимус у пациентов с клинически активной системной красной волчанкой, резистентной к обычным лекарствам или не переносящей их: открытое исследование фазы 1/2 в одной группе. Ланцет. 2018; 391: 1186–96.
CAS PubMed PubMed Central Google Scholar
Merrill JT, Neuwelt CM, Wallace DJ, et al. Эффективность и безопасность ритуксимаба при активной системной красной волчанке средней и тяжелой степени: рандомизированная двойная слепая оценка системной красной волчанки фазы II / III в исследовании ритуксимаба. Ревматоидный артрит. 2010; 62: 222–33.
CAS PubMed PubMed Central Google Scholar
Rovin BH, Furie R, Latinis K, et al. Эффективность и безопасность ритуксимаба у пациентов с активным пролиферативным волчаночным нефритом: оценка волчаночного нефрита с исследованием ритуксимаба.Ревматоидный артрит. 2012; 64: 1215–26.
CAS PubMed Google Scholar
Witt M, Grunke M, Proft F, et al. Клинические результаты и безопасность лечения ритуксимабом пациентов с системной красной волчанкой (СКВ) — результаты общенациональной когорты в Германии (GRAID). Волчанка. 2013; 22: 1142–9.
CAS PubMed Google Scholar
Маккарти Э.М., Саттон Э., Несбит С. и др.Краткосрочная эффективность и безопасность терапии ритуксимабом при рефрактерной системной красной волчанке: результаты Регистра биологических препаратов Британской группы по оценке волчанки. Ревматология (Оксфорд). 2018; 57: 470–9.
CAS Google Scholar
Fanouriakis A, Kostopoulou M, Alunno A, et al. Обновление рекомендаций EULAR по ведению системной красной волчанки в 2019 г. Ann Rheum Dis. 2019; 78: 736–45.
CAS PubMed Google Scholar
Маккей Ф., Вудкок С.А., Лоутон П. и др. У мышей, трансгенных по BAFF, наряду с аутоиммунными проявлениями развиваются лимфоцитарные нарушения. J Exp Med. 1999; 190: 1697–710.
CAS PubMed PubMed Central Google Scholar
Schneider P, MacKay F, Steiner V, et al. BAFF, новый лиганд из семейства факторов некроза опухоли, стимулирует рост В-клеток. J Exp Med. 1999; 189: 1747–56.
CAS PubMed PubMed Central Google Scholar
Винсент Ф. Б., Моран Э. Ф., Маккей Ф. BAFF и врожденный иммунитет: новые терапевтические мишени для системной красной волчанки. Immunol Cell Biol. 2012; 90: 293–303.
CAS PubMed Google Scholar
Strand V, Леви Р.А., Сервера Р. и др. Улучшение связанного со здоровьем качества жизни с помощью белимумаба, специфического ингибитора стимулятора В-лимфоцитов, у пациентов с аутоантител-положительной системной красной волчанкой из рандомизированных контролируемых исследований BLISS.Ann Rheum Dis. 2014; 73: 838–44.
CAS PubMed Google Scholar
Наварра С.В., Гусман Р.М., Галлахер А.Е. и др. Эффективность и безопасность белимумаба у пациентов с активной системной красной волчанкой: рандомизированное плацебо-контролируемое исследование фазы 3. Ланцет. 2011; 377: 721–31.
CAS PubMed Google Scholar
Фьюри Р., Петри М., Замани О. и др.Рандомизированное плацебо-контролируемое исследование фазы III белимумаба, моноклонального антитела, которое ингибирует стимулятор В-лимфоцитов, у пациентов с системной красной волчанкой. Ревматоидный артрит. 2011; 63: 3918–30.
CAS PubMed PubMed Central Google Scholar
Stohl W., Schwarting A, Okada M, et al. Эффективность и безопасность подкожного введения белимумаба при системной красной волчанке: 52-недельное рандомизированное двойное слепое плацебо-контролируемое исследование.Arthritis Rheumatol. 2017; 69: 1016–27.
CAS PubMed PubMed Central Google Scholar
Iaccarino L, Andreoli L, Bocci EB, et al. Клинические предикторы ответа и отмены белимумаба у пациентов с системной красной волчанкой в реальных условиях. Результаты большого многоцентрового общенационального исследования. J Autoimmun. 2018; 86: 1–8.
CAS PubMed Google Scholar
Schwarting A, Schroeder JO, Alexander T, et al. Первые практические сведения об использовании белимумаба и его результатах в повседневной клинической практике лечения системной красной волчанки в Германии: результаты исследования OBSErve, Германия. Rheumatol Ther. 2016; 3: 271–90.
PubMed PubMed Central Google Scholar
Дули М.А., Хоуссио Ф., Аранов С. и др. Влияние лечения белимумабом на почечные исходы: результаты 3 фазы клинических испытаний белимумаба у пациентов с СКВ.Волчанка. 2013; 22: 63–72.
CAS PubMed Google Scholar
Марджотта DPE, Баста Ф., Батани В., Афельтра А. Белимумаб и низкие дозы микофенолятмофетила в качестве индукционной терапии волчаночного нефрита IV класса: серии случаев и обзор литературы. BMC Nephrol. 2018; 19:54.
PubMed PubMed Central Google Scholar
Schwarting A, Relle M, Meineck M, et al.Экспрессия BAFF, происходящая из эпителиальных клеток почечных канальцев, опосредует повреждение почек и коррелирует с активностью пролиферативного волчаночного нефрита у мышей и мужчин. Волчанка. 2018; 27: 243–56.
CAS PubMed Google Scholar
Sjöwall C, Cöster L. Белимумаб не может предотвратить волчаночный нефрит у серологически активных пациентов с продолжающейся непочечной активностью. Scand J Rheumatol. 2014; 43: 428–30.
PubMed Google Scholar
Ставери С, Карокис Д, Лиосис SC. Новое начало волчаночного нефрита у двух пациентов с СКВ вскоре после начала лечения белимумабом. Semin Arthritis Rheum. 2017; 46: 788–90.
CAS PubMed Google Scholar
Parodis I, Vital EM, Jönsen A, et al. De novo lupus nephritis во время лечения белимумабом. Плакат представлен на 12-й Европейской встрече по волчанке. https://doi.org/10.1136/lupus-2020-eurolupus.181.
Teng YKO, Bruce IN, Diamond B, et al. Фаза III, многоцентровое, рандомизированное, двойное слепое, плацебо-контролируемое, 104-недельное исследование подкожного введения белимумаба в комбинации с ритуксимабом у взрослых с системной красной волчанкой (СКВ): протокол исследования BLISS-BELIEVE. BMJ Open. 2019; 9: e025687.
PubMed PubMed Central Google Scholar
Джонс А., Мюллер П., Дор С.Дж. и др. Белимумаб после терапии истощения В-клеток у пациентов с системной красной волчанкой (BEAT Lupus) Протокол: проспективное многоцентровое двойное слепое рандомизированное плацебо-контролируемое 52-недельное клиническое исследование фазы II.BMJ Open. 2019; 9: e032569.
PubMed PubMed Central Google Scholar
Бекар К.В., Оуэн Т., Данн Р. и др. Длительные эффекты краткосрочной терапии истощения анти-CD20 В-клеток при системной красной волчанке у мышей. Ревматоидный артрит. 2010; 62: 2443–577.
CAS PubMed PubMed Central Google Scholar
Гуальтиеротти Р., Борги МО, Героса М. и др.Успешная последовательная терапия ритуксимабом и белимумабом у пациентов с активной системной красной волчанкой: серия случаев. Clin Exp Rheumatol. 2018; 36: 643–7.
PubMed Google Scholar
Мартинес Т., Гарсия-Робледо Дж. Э., Плата I и др. Механизмы действия и исторические факты об использовании внутривенных иммуноглобулинов при системной красной волчанке. Autoimmun Rev.2019; 18: 279–86.
PubMed Google Scholar
Сактисвари Р., Д’Круз Д. Внутривенный иммуноглобулин в терапевтическом арсенале системной красной волчанки: систематический обзор и метаанализ. Медицина (Балтимор). 2014; 93 (16): e86.
CAS Google Scholar
Кронбихлер А., Брезина Б., Кинтана Л.Ф., Джейн ДР. Эффективность плазмафереза и иммуноадсорбции при системной красной волчанке и антифосфолипидном синдроме: систематический обзор. Аутоиммунный Rev.2016; 15: 38–49.
PubMed Google Scholar
Штуммволл Г.Х., Аринджер М., Смолен Дж.С. и др. Иммуноадсорбция IgG снижает активность системной красной волчанки и протеинурию: долгосрочное обсервационное исследование. Ann Rheum Dis. 2005; 64: 1015–21.
CAS PubMed PubMed Central Google Scholar
Stummvoll GH, Schmaldienst S, Smolen JS, Derfler K, Biesenbach P.Волчаночный нефрит: длительная иммуноадсорбция (IAS) снижает протеинурию и стабилизирует общую активность заболевания. Пересадка нефрола Dial. 2012; 27: 618–26.
CAS PubMed Google Scholar
Guan SY, Cai HY, Wang P, et al. Связь между циркулирующим 25-гидроксивитамином D и системной красной волчанкой: систематический обзор и метаанализ. Int J Rheum Dis. 2019; 22: 1803–13.
CAS PubMed Google Scholar
Parisis D, Bernier C, Chasset F, Arnaud L. Влияние табакокурения на риск заболевания, активность и терапевтический ответ при системной красной волчанке: систематический обзор и метаанализ. Autoimmun Rev.2019; 18: 102393.
PubMed Google Scholar
Margiotta DPE, Basta F, Dolcini G, et al. Физическая активность и малоподвижный образ жизни у больных системной красной волчанкой. PLoS ONE. 2018; 13: e0193728.
PubMed PubMed Central Google Scholar
Merrill JT, Shanahan WR, Scheinberg M, Kalunian KC, Wofsy D, Martin RS. Результаты фазы III исследования блисибимода, селективного ингибитора фактора активации В-клеток, у субъектов с системной красной волчанкой (СКВ): результаты рандомизированного двойного слепого плацебо-контролируемого исследования. Ann Rheum Dis. 2018; 77: 883–9.
CAS PubMed Google Scholar
Merrill JT, Wallace DJ, Wax S и др. Эффективность и безопасность атасцепта у пациентов с системной красной волчанкой: результаты 24-недельного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования фазы IIb в параллельных группах.Arthritis Rheumatol. 2018; 70: 266–76.
CAS PubMed PubMed Central Google Scholar
Merrill JT, van Vollenhoven RF, Buyon JP, et al. Эффективность и безопасность подкожного табалумаба, моноклонального антитела к фактору активации B-клеток, у пациентов с системной красной волчанкой: результаты 52-недельного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования ILLUMINATE-2. . Ann Rheum Dis. 2016; 75: 332–40.
CAS PubMed Google Scholar
Изенберг Д.А., Петри М., Калунян К. и др. Эффективность и безопасность подкожного введения табалумаба у пациентов с системной красной волчанкой: результаты 52-недельного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования ILLUMINATE-1 фазы III. Ann Rheum Dis. 2016; 75: 323–31.
CAS PubMed Google Scholar
Редди В., Кляйн С., Изенберг Д.А. и др. Обинутузумаб вызывает более высокую цитотоксичность В-клеток по сравнению с ритуксимабом в образцах пациентов с ревматоидным артритом и системной красной волчанкой. Ревматология (Оксфорд). 2017; 56: 1227–37.
CAS Google Scholar
Васкес А., Баэна А., Гонсалес Л.А. и др. Изменено рекрутирование Lyn, Syk и ZAP-70 в липидные рафты активированных В-клеток при системной красной волчанке. Сотовый сигнал. 2019; 58: 9–19.
PubMed Google Scholar
Клаус М.Э., Уоллес Д.Д., Фьюри Р.А. и др. Эффективность и безопасность эпратузумаба при средней и тяжелой активной системной красной волчанке: результаты двух рандомизированных двойных слепых плацебо-контролируемых исследований фазы III. Arthritis Rheumatol. 2017; 69: 362–75.
CAS PubMed PubMed Central Google Scholar
Merrill JT, Burgos-Vargas R, Westhovens R, et al.Эффективность и безопасность абатацепта у пациентов с неопасными для жизни проявлениями системной красной волчанки: результаты двенадцатимесячного многоцентрового исследовательского рандомизированного двойного слепого плацебо-контролируемого исследования фазы IIb. Ревматоидный артрит. 2010; 62: 3077–87.
CAS PubMed Google Scholar
Фьюри Р., Николлс К., Ченг Т-Т и др. Эффективность и безопасность абатацепта при волчаночном нефрите: двенадцатимесячное рандомизированное двойное слепое исследование.Arthritis Rheumatol. 2014; 66: 379–89.
CAS PubMed Google Scholar
Висванатан С., Данилюк С., Пташински Р. и др. Эффекты BI 655064, антагонистического антитела к CD40, на клинические и биомаркерные переменные у пациентов с активным ревматоидным артритом: рандомизированное двойное слепое плацебо-контролируемое исследование фазы IIa. Ann Rheum Dis. 2019; 78: 754–60.
CAS PubMed PubMed Central Google Scholar
Александр Т., Сарферт Р., Клотше Дж. И др. Бортезомиб, ингибирующий протеасомы, истощает плазматические клетки и облегчает клинические проявления рефрактерной системной красной волчанки. Ann Rheum Dis. 2015; 74: 1474–8.
CAS PubMed PubMed Central Google Scholar
Исии Т., Танака Ю., Каваками А. и др. Многоцентровое двойное слепое рандомизированное контролируемое исследование для оценки эффективности и безопасности бортезомиба в качестве средства лечения рефрактерной системной красной волчанки.Мод Ревматол. 2018; 28: 986–92.
CAS PubMed Google Scholar
Alunno A, Padjen I, Fanouriakis, Boumpas DT. Патогенетическая и терапевтическая значимость передачи сигналов JAK / STAT при системной красной волчанке: интеграция различных воспалительных путей и перспективы их ингибирования с помощью перорального средства. Ячейки. 2019; 8 (8): 898. https://doi.org/10.3390/cells8080898.
Wallace DJ, Furie RA, Tanaka Y, et al.Барицитиниб при системной красной волчанке: двойное слепое рандомизированное плацебо-контролируемое исследование фазы 2. Ланцет. 2018; 392: 222–31.
CAS PubMed Google Scholar
Weckerle CE, Franek BS, Kelly JA, et al. Сетевой анализ ассоциаций между активностью интерферона-α в сыворотке крови, аутоантителами и клиническими особенностями системной красной волчанки. Ревматоидный артрит. 2011; 63: 1044–53.
CAS PubMed PubMed Central Google Scholar
Kalunian KC, Merrill JT, Maciuca R, et al. Фаза II исследования эффективности и безопасности ритонализумаба (интерферон-α rhuMAb) у пациентов с системной красной волчанкой (ROSE). Ann Rheum Dis. 2016; 75: 196–202.
PubMed Google Scholar
Фьюри Р., Хамашта М., Меррилл Дж. Т. и др. Анифролумаб, моноклональное антитело против рецептора интерферона-α, при средней и тяжелой системной красной волчанке. Arthritis Rheumatol.2017; 69: 376–86.
CAS PubMed PubMed Central Google Scholar
Morand EF, Furie R, Tanaka Y, et al. Испытание анифролюмаба при активной системной красной волчанке. N Engl J Med. 2020; 382: 211–21.
CAS PubMed Google Scholar
Blanco LP, Pedersen HL, Wang X и др. Улучшение митохондриального метаболизма и уменьшение воспаления после ослабления мышиной волчанки с помощью аналога кофермента Q10 идебенона.Arthritis Rheumatol. 2020; 72: 454–64.
CAS PubMed Google Scholar
Перл А. Окислительный стресс в патологии и лечении системной красной волчанки. Nat Rev Rheumatol. 2013; 9: 674–86.
CAS PubMed PubMed Central Google Scholar
Lai ZW, Hanczko R, Bonilla E, et al. N -ацетилцистеин снижает активность заболевания, блокируя мишень рапамицина млекопитающих в Т-клетках пациентов с системной красной волчанкой: рандомизированное двойное слепое плацебо-контролируемое исследование.Ревматоидный артрит. 2012; 64: 2937–46.
CAS PubMed PubMed Central Google Scholar
Jury EC, Isenberg DA, Mauri C, Ehrenstein MR. Аторвастатин восстанавливает экспрессию Lck и передачу сигналов, связанных с липидным рафтом, в Т-клетках пациентов с системной красной волчанкой. J Immunol. 2006; 177: 7416–22.
CAS PubMed Google Scholar
Гарфолл А.Л., Маус М.В., Хван В.Т. и др.Химерные антигенные рецепторные Т-клетки против CD19 при множественной миеломе. N Engl J Med. 2015; 373: 1040–7.
CAS PubMed PubMed Central Google Scholar
Qin H, Dong Z, Wang X и др. CAR Т-клетки, нацеленные на BAFF-R, могут преодолеть потерю антигена CD19 при злокачественных опухолях В-клеток. Sci Transl Med. 2019; 11: eaaw9414. https://doi.org/10.1126/scitranslmed.aaw9414.
Miliotou AN, Papadopoulou LC. CAR Т-клеточная терапия: новая эра в иммунотерапии рака.Curr Pharm Biotechnol. 2018; 19: 5–18.
PubMed Google Scholar
Kansal R, Richardson N, Neeli I, et al. Устойчивое истощение В-клеток CAR-Т-клетками, нацеленными на CD19, является высокоэффективным лечением волчанки у мышей. Sci Transl Med. 2019; 1: eaav1648.
Клацманн Д., Аббас А.К. Перспективы терапии низкими дозами интерлейкина-2 при аутоиммунных и воспалительных заболеваниях. Nat Rev Immunol. 2015; 15: 283–94.
CAS PubMed Google Scholar
Хе Дж, Чжан Р., Шао М. и др. Эффективность и безопасность низких доз ИЛ-2 при лечении системной красной волчанки: рандомизированное двойное слепое плацебо-контролируемое исследование. Ann Rheum Dis. 2020; 79: 141–9.
PubMed Google Scholar
Grabar S, Groh M, Bahuaud M, et al. Пневмококковая вакцинация пациентов с системной красной волчанкой: многоцентровое плацебо-контролируемое рандомизированное двойное слепое исследование. Вакцина. 2017; 35: 4877–85.
PubMed Google Scholar
Элефанте Э, Тани С., Стагнаро С. и др. Влияние усталости на качество жизни, связанное со здоровьем, и восприятие болезни в моноцентрической когорте пациентов с системной красной волчанкой. RMD Open. 2020; 6 (1): e001133. https://doi.org/10.1136/rmdopen-2019-001133.
PubMed PubMed Central Google Scholar
Баста Ф., Марджотта ДПЭ, Вадакка М. и др.Является ли утомляемость причиной потери трудоспособности при системной красной волчанке? Результаты систематического обзора литературы. Eur Rev Med Pharmacol Sci. 2018; 22: 4589–97.
CAS PubMed Google Scholar
Schwarting A, Möckel T, Lütgendorf F, et al. Усталость при СКВ: диагностическое и патогенное влияние аутоантител против рецептора N -метил-D-аспартата (NMDAR). Ann Rheum Dis. 2019; 78: 1226–344.
CAS PubMed Google Scholar
Чжэн Р., Гонсалес А., Юэ Дж. И др. Эффективность и безопасность добавок витамина D у пациентов с системной красной волчанкой: метаанализ рандомизированных контролируемых исследований. Am J Med Sci. 2019; 358: 104–14.
PubMed Google Scholar
Системная красная волчанка — Консультант по терапии рака
I. Что нужно знать каждому врачу.
Системная красная волчанка (СКВ) — это аутоиммунное заболевание, которое может проявляться целым рядом симптомов, чаще всего включая артрит, сыпь, гематологическое заболевание, заболевание почек и воспаление серозных поверхностей сердца и легких.Однако СКВ может поражать практически любую ткань тела и имитировать ряд других заболеваний, что усложняет диагностику СКВ.
Существует 11 диагностических критериев, определенных Американским колледжем ревматологии. Традиционно, пациенту, который соответствует 4 из 11 критериев, ставится диагноз СКВ. Однако жалобами могут быть неспецифические конституциональные признаки, такие как усталость, жар и потеря веса. Считается, что основное заболевание опосредуется аутоантителами и иммунными комплексами, которые напрямую связываются с тканями.
II. Диагностическое подтверждение: Вы уверены, что у вашего пациента системная красная волчанка?
Пересмотренные критерии диагностики системной красной волчанки
Четыре из одиннадцати подтверждают наличие системной красной волчанки
Скуловая сыпь — это плоская или выпуклая эритематозная сыпь над скуловым возвышением. Он имеет тенденцию щадить носогубные складки.
Дискоидная сыпь — это выпуклая круглая эритематозная сыпь с прилипшим кератотическим шелушением и закупоркой фолликулов.
К гематологическим нарушениям, достаточным для соответствия диагностическим критериям СКВ, относятся следующие:
◦ Гемолитическая анемия
◦ Лейкопения (<4000 / мм3)
◦ Лимфопения (<1500 / мм3)
◦ Тромбоцитопения (<100 000 / мм3) при отсутствии нежелательных препаратов.
Заболевание почек включает стойкую протеинурию (> 500 мг в день) или клеточные цилиндры (эритроциты, гемоглобин, гранулярные, тубулярные или смешанные).
Аномальные титры АНА должны быть при отсутствии лекарств, о которых известно, что они связаны с лекарственной волчанкой.
К иммунологическим нарушениям, достаточным для соответствия диагностическим критериям СКВ, относятся следующие:
◦ Анти-двухцепочечные ДНК-антитела (Anti-DS ДНК)
◦ Анти-Смит-антитела (Anti-SM)
◦ Антифосфолипидные антитела
◦ Наличие волчаночного антикоагулянта
◦ Ложноположительный серологический тест на сифилис, положительный результат не менее 6 месяцев
Неврологические расстройства включают судороги в отсутствие нежелательных лекарств или известных метаболических нарушений (например,грамм. кетоацидоз, уремия, электролитные нарушения) или психоз в отсутствие нежелательных лекарств или известных метаболических нарушений (например, кетоацидоз, уремия, электролитные нарушения).
Серозит включает плеврит или перикардит.
Язвы в полости рта обычно безболезненны и могут поражать также носоглотку.
Артрит должен поражать два или более периферических сустава и включать болезненность, отек или излияние.
Светочувствительность — это кожная сыпь в результате более сильной, чем ожидалось, реакции на солнечный свет.
A. История, часть I: Распознавание образов:
СКВ — системное заболевание, которое проявляется различными способами. Не существует «типичного пациента» с СКВ, поскольку это заболевание сильно варьируется.
B. История, часть 2: Распространенность:
СКВ чаще всего поражает женщин репродуктивного возраста. Женщины преобладают 9: 1. Общая распространенность СКВ в США оценивается в 15–50 на 100 000 человек.Самый высокий уровень распространенности зарегистрирован в Бразилии. В Соединенных Штатах люди африканского, латиноамериканского или азиатского происхождения имеют повышенную распространенность СКВ и большее поражение жизненно важных органов.
C. История, часть 3: конкурирующие диагнозы, которые могут имитировать системную красную волчанку.
СКВ сложно диагностировать, потому что она может проявляться множеством способов практически в любом органе. К другим системным заболеваниям, которые могут проявляться аналогично СКВ, относятся следующие:
Лептоспироз
Болезнь Лайма
Гонорея распространенная
ВИЧ
Васкулит
Постстрепток
Сифилис
оккальный гломерулонефрит
Псориаз
Атопический дерматит
Вирусные синдромы
Смешанное заболевание соединительной ткани
Синдром Шегрена
Ревматоидный артрит
Системный склероз
Лимфома
Лейкемия
Криоглобулинемия
Тромботическая тромбоцитопеническая пурпура (ТТП)
Диссеминированная внутрисосудистая коагуляция (ДВС)
Идиопатическая тромбоцитопеническая пурпура (ИТП)
Аутоиммунная гемолитическая анемия (АИГА)
Микроангиопатическая гемолитическая анемия (MAHA)
Одной из ключевых отличительных черт СКВ является эпидемиология.Распространенность увеличивается у женщин детородного возраста. Положительные антиядерные антитела (ANA) И положительные анти-DS ДНК или анти-SM антитела являются отличительной особенностью СКВ. От восьмидесяти до девяноста процентов всех пациентов с СКВ имеют ту или иную форму кожно-слизистых симптомов. Также важно определить, принимает ли пациент какие-либо лекарства, которые могут вызвать лекарственную волчанку. Наиболее распространены прокаинамид, гидралазин и изониазид.
D. Результаты физикального осмотра.
Дерматологический
Дискоидные поражения представляют собой отдельные эритематозные бляшки, покрытые чешуей, которая распространяется на расширенные волосяные фолликулы.Они, как правило, находятся на лице, волосистой части головы, за ушами и на шее. Центральное атрофическое рубцевание может наблюдаться при запущенных поражениях.
Подострая кожная красная волчанка (СКВЛ) обычно поражает женщин европеоидной расы. Сыпь представляет собой эритематозную папулезную сыпь, которая может прогрессировать в папулосквамозное или псориазообразное поражение.
Самая распространенная сыпь — скуловая сыпь. Это эритематозная и отечная сыпь, покрывающая переносицу и скуловые возвышения.Он имеет тенденцию щадить носогубные складки. Это НЕ связано с папулами или пустулами.
Алопеция обычно связана с СКВ. Он может быть диффузным или пятнистым.
Язвы в полости рта, если они есть, обычно обнаруживаются на слизистой оболочке щек, языка и неба. Как правило, они безболезненны. Подобные язвы могут быть обнаружены в носу и аногенитальной области.
Пациенты с СКВ могут иметь крапивницу, пальпируемую пурпуру, язвы пальцев или кровоизлияния из осколков из-за васкулита, связанного с СКВ.
Опорно-двигательный аппарат
Полиартрит — частая находка. Чаще всего наблюдается припухлость и болезненность мягких тканей в руках, запястьях и коленях.
Миозит может возникнуть, но это необычно. У большинства пациентов есть миалгии и слабость без истинного миозита. Слабость часто затрагивает дельтовидные мышцы и четырехглавые мышцы.
Неврологический
СКВ может проявляться потерей памяти, спутанностью сознания или даже психозом.
Сосудистые
СКВ может проявляться признаками окклюзии сосудов или недостаточности, таких как инсульт, инфаркт миокарда, тромбоз глубоких вен и тромбоэмболия легочной артерии.
Из-за тромбоцитопении могут появиться легкие кровоподтеки или кровотечения.
Сердечный
Наиболее частым сердечным проявлением является перикардит. Может присутствовать трение.
Эндокардит Либманна-Сакса может привести к клапанной недостаточности.Могут присутствовать срыгивающие шумы.
Из-за легочной гипертензии при осмотре могут быть обнаружены повышенное вздутие яремных вен, отек нижних конечностей, громкий легочный компонент S2 и трикуспидальная регургитация.
Легочные
Плеврит — обычное явление, но трение плевры обычно не приветствуется.
Хрипы могут быть слышны у пациентов с волчаночной пневмонией.
Желудочно-кишечный тракт
Поражение желудочно-кишечного тракта сильно варьируется и варьируется от болезненности отскока до тошноты, рвоты и диареи в зависимости от вовлеченных структур.
Офтальмологический
Пятна ваты на сетчатке — наиболее частое поражение глаз при СКВ.
E. Какие диагностические тесты следует провести?
Антинуклеарные антитела (ANA)
Общий анализ крови
Общий анализ мочи
Если ANA положительный, то анти-DS ДНК или анти-SM антитело
Если есть поражение почек, следует заказать определение уровня C3 и точечного соотношения белок / креатинин
1.Какие лабораторные исследования (если таковые имеются) следует заказать для установления диагноза? Как следует интерпретировать результаты?
Низкие титры антинуклеарных антител могут случайно обнаруживаться у ряда пациентов. Как правило, титр больше 1:80 увеличивает вероятность СКВ и требует последующих анализов.
ДНК анти-DS и анти-SM специфичны для СКВ.
CBC является ключевым. Если у пациента анемия, можно назначить мазок крови, фракционированный билирубин, гаптоглобин и / или ЛДГ, чтобы определить, есть ли у пациента гемолитическая анемия.Многие пациенты страдают анемией хронического воспаления, но это не соответствует диагностическим критериям СКВ. Однако тромбоцитопения, лимфопения и лейкопения являются частью диагностических критериев.
Анализ мочи должен показать активный осадок во время обострения, включая цилиндры и протеинурию (> 2+ на индикаторной полоске). Хроническое заболевание может проявляться только протеинурией и минимальным количеством клеток или цилиндров.
Уровни комплемента могут быть нормальными, если у пациента нет острого обострения СКВ, несмотря на признаки предыдущего повреждения почек, например протеинурию или повышенный креатинин.Ожидается, что точечный уровень протеина / креатинина будет выше 0,5 при активном и нелеченом хроническом заболевании.
2. Какие визуализационные исследования (если таковые имеются) следует заказать, чтобы помочь установить диагноз? Как следует интерпретировать результаты?
Электрокардиография (ЭКГ) может помочь установить диагноз перикардита. Ожидаемыми результатами являются диффузная элевация ST и / или депрессия PR. Напряжение может быть низким в зависимости от количества жидкости в перикардиальном мешке.
III. Управление по умолчанию.
Ведение зависит от поражения органов и степени тяжести.
НПВП используются для лечения:
Легкий артрит
Миалгии
Серозит
Головные боли
Системные кортикостероиды, эквивалентная доза от 5 до 30 мг преднизона используется для лечения следующего:
Системные кортикостероиды, эквивалентная доза преднизона 1-2 мг / кг / день, используются для лечения следующих более серьезных проявлений:
Перикардит
Миокардит
Гломерулонефрит
Гемолитическая анемия
Альвеолярное кровоизлияние
Симптомы со стороны ЦНС
Системный васкулит
Пульс-метипреднизолон (1 г внутривенно) можно вводить на срок до трех дней при угрожающих жизни проявлениях СКВ.Циклофосфамид, микофенолятмофетил или азатиоприн можно использовать для пациентов, резистентных к кортикостероидам. Циклофосфамид или микофенолят мофетил используются при тяжелом волчаночном нефрите. Их должны назначать опытные врачи.
Противомалярийные средства, в частности гидроксихлорохин, являются препаратами первой линии для лечения СКВ легкой степени.
Гидроксихлорохин используется для следующих целей:
Гидроксихолорохиин обычно начинают с 200 мг / день и повышают до 200 мг два раза в день.
Кумадин, титрованный до МНО 2,0–3,0, используется для лечения синдрома антифосфолипидных антител. Низкомолекулярный гепарин плюс аспирин используется беременным женщинам с синдромом антифосфолипидных антител и рецидивирующей потерей плода.
Ритуксимаб, моноклональное антитело, которое нацелено на антиген клеточной поверхности, CD20, на В-клетки, оказывает благоприятное воздействие на пациентов с СКВ. Дальнейшие исследования в настоящее время продолжаются.
A. Немедленное управление.
Пульсовый метилпреднизолон (1 г внутривенно) следует назначать при любых опасных для жизни проявлениях СКВ.В противном случае см. Дополнительные сведения в разделе «Управление по умолчанию».
B. Советы медицинского осмотра для руководства.
Должно быть выполнено подробное обследование слизистых оболочек и кожи, включая ротоглотку, носоглотку и кожу. Язвы в полости рта, скуловая сыпь, дискоидная сыпь или признаки светочувствительности указывают на фармакологическую терапию. Характерная для васкулита сыпь без побледнения свидетельствует о применении системных кортикостероидов.
Необходимо провести подробное обследование опорно-двигательного аппарата с целью выявления артрита, суставных выпотов и болезненности суставов.Легкие симптомы можно лечить с помощью НПВП. Более серьезные симптомы требуют системных кортикостероидов.
Шум трения перикарда указывает на перикардит и необходимость в системных кортикостероидах.
C. Лабораторные тесты для отслеживания реакции и корректировок в управлении.
Креатинин следует тщательно контролировать у пациентов с гломерулонефритом. В начале лечения следует проверять креатинин каждый день.
Анти-DS ДНК-антитела коррелируют с активностью заболевания у некоторых пациентов с гломерулонефритом.Титр будет увеличиваться при обострении болезни и снижаться при ответе на терапию.
Скорость оседания эритроцитов и С-реактивный белок уменьшаются при соответствующем лечении обострения СКВ. Они могут оставаться повышенными у пациентов с устойчивостью к кортикостероидам. У пациентов, устойчивых к кортикостероидам, следует рассмотреть альтернативный препарат, такой как гидрохлорохин или азатиоприн, в зависимости от тяжести симптомов.
D. Долгосрочное управление.
Гидроксихлорохин используется для лечения легких конституциональных, кожных и скелетно-мышечных симптомов и может уменьшить количество обострений заболевания.Доза составляет 200 мг или 400 мг в день. Пациенты, получающие гидроксихлорохин, должны ежегодно контролировать изменения сетчатки.
Азатиоприн (2-2,5 мг / кг / день) используется в качестве кортикостероидного сберегающего средства для пациентов с легкой или умеренной активностью заболевания. Это альтернатива циклофосфамиду для пациентов, нуждающихся в поддерживающей терапии волчаночного нефрита.
Продолжительность приема циклофосфамида при волчаночном нефрите различна. Одна рекомендация — ежемесячные дозы (500 мг / м 2 ) циклофосфамида внутривенно в течение 6 месяцев, затем 2 квартальные дозы циклофосфамида, а затем ежедневный прием азатиоприна в течение 2 лет.
Кумадин, титрованный до МНО 2,0–3,0, используется для лечения синдрома антифосфолипидных антител.
Пациентам с СКВ требуется значительный объем знаний о своем заболевании, а также о том, как распознать признаки обострения и обратиться за медицинской помощью.
E. Распространенные ловушки и побочные эффекты управления
Кратковременное употребление кортикостероидов может привести к гипергликемии, эмоциональной уязвимости и даже психозу. Длительное употребление может привести к глаукоме, катаракте, остеопорозу, иммуносупрессии и синдрому Кушинга (центральное ожирение, абдоминальные стрии, гипертония, сахарный диабет и нарушение липидного обмена).
Противомалярийные средства, такие как гидроксихлорохин, могут вызывать побочные эффекты со стороны желудочно-кишечного тракта, такие как боль в животе, тошнота, рвота, диарея или вздутие живота. Они также могут вызывать ретинопатию и требуют ежегодного офтальмологического обследования. Эти лекарства могут вызвать гиперпигментацию ногтей, слизистых оболочек и кожи (особенно на участках, подверженных воздействию солнца). Гидроксихлорохин может вызывать гипогликемию и снижать потребность в инсулине у диабетиков с СКВ. Противомалярийные препараты могут вызывать гемолитическую анемию у пациентов с дефицитом глюкозо-6-фосфатдегидрогеназы (G6PD).
Азатиоприн может вызывать миелосупрессию. Его не следует применять пациентам, принимающим аллопуринол от подагры, поскольку это также приводит к миелосупрессии. Азатиоприн метаболизируется в печени и выводится почками. Он требует периодического контроля функции почек и печени, и может потребоваться соответствующая корректировка дозировки.
Циклофосфамид может вызывать угнетение костного мозга, наузу, рвоту, иммуносупрессию и карциному мочевого пузыря. Также существует связь с геморрагическим циститом и дисплазией шейки матки.
Микофенолятмофетил может вызывать побочные эффекты со стороны желудочно-кишечного тракта, такие как тошнота, диарея и вздутие живота. Он также вызывает подавление иммунитета и миелосупрессию.
IV. Лечение сопутствующих заболеваний
НЕТ
A. Почечная недостаточность.
Снижение дозы препарата азатиоприна. Избегание НПВП.
B. Печеночная недостаточность.
Тщательный мониторинг использования азатиоприна, циклофосфамида и гидроксихлорохина.
C. Систолическая и диастолическая сердечная недостаточность
Без регулировки.
D. Заболевание коронарной артерии или заболевание периферических сосудов
Избегайте длительного приема НПВП.
E. Диабет или другие эндокринные проблемы
Гидроксихлорохин обладает гипогликемическими свойствами и может вызывать гипогликемию или снижение потребности в инсулине у пациентов с диабетом.
Использование кортикостероидов приведет к гипергликемии и повышению потребности в инсулине.
J. Проблемы гематологии или коагуляции
Циклофосфамид, микофенолятмофетил и азатиоприн могут вызывать угнетение костного мозга.
V. Переход на лечение
НЕТ
B. Ожидаемая продолжительность пребывания.
Переменная в зависимости от поражения органов и степени тяжести.
C. Когда пациент готов к выписке.
Когда больше не требуется внутривенное введение лекарств и он может без проблем выполнять повседневную деятельность.
D. Организация последующего наблюдения в клинике
НЕТ
1. Когда и с кем следует организовать наблюдение в клинике.
Ревматология в течение 2-4 недель.
Нефрология для больных волчаночным нефритом. При поступлении по поводу волчаночного нефрита наблюдение в течение 2-4 недель.
2. Какие анализы следует провести перед выпиской, чтобы лучше всего получить возможность первого посещения клиники.
Не применимо.
3.Какие анализы следует заказать амбулаторно до или в день посещения клиники.
Если у пациента волчаночный нефрит, подходит основная метаболическая панель и фосфор.
Пациентам, принимающим азатиоприн, микофенолятмофетил или циклофосфамид, следует назначить полную метаболическую панель для отслеживания функции печени и почек.
СКВ вызывает ускоренный атеросклероз, и эти пациенты подвержены риску ишемической болезни сердца.Рассмотрите возможность проверки уровня липидов в сыворотке крови.
F. Прогноз и консультирование пациентов.
10-летняя выживаемость составляет примерно 85%. У большинства пациентов есть ремиттирующий и рецидивирующий курс. Однако у небольшого числа пациентов наблюдается серьезное поражение ключевых органов, что приводит к увеличению заболеваемости и смертности.
VI. Меры безопасности и качества пациентов
НЕТ
B. Соответствующая профилактика и другие меры по предотвращению реадмиссии.
Пациенты с СКВ должны пройти все прививки.Они должны получать пневмовакс и ежегодную вакцину против гриппа.
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
Системная красная волчанка | DermNet NZ
Автор: Hon A / Prof Amanda Oakley, дерматолог, Гамильтон, Новая Зеландия, февраль 2015 г.
Введение
Красная волчанка (LE) — это группа разнообразных стойких аутоиммунных воспалительных заболеваний.
Системная красная волчанка (СКВ) поражает несколько органов (например, кожу, суставы и почки), а анализы крови выявляют циркулирующие аутоантитела. Клинические признаки СКВ сильно различаются и могут совпадать с другими заболеваниями и состояниями. Поражение кожи или кожная волчанка (CLE) поражает 80% пациентов с SLE.
СКВ иногда называют острой красной волчанкой, а кожные особенности могут быть описаны как острая кожная волчанка.
Что вызывает системную красную волчанку?
Факторы, приводящие к СКВ, включают:
Проявления СКВ связаны с потерей регуляции иммунной системы пациента.
- Ядерные белки не обрабатываются должным образом.
- Ядерный мусор накапливается внутри клетки.
- Это приводит к выработке аутоантител против ядерных белков.
- Иммунные комплексы не удаляются.
- Система дополнения активирована.
- Воспаление приводит к повреждению клеток и тканей.
Кто заболевает системной красной волчанкой?
СКВ может поражать мужчин и женщин любого возраста. Ежегодно на 100 000 человек выявляется около 2–7 новых случаев. СКВ гораздо чаще встречается у женщин, чем у мужчин, и чаще всего возникает в возрасте от 15 до 45 лет.
СКВ более распространена и более серьезна у курильщиков. Курение также снижает эффективность противомалярийных препаратов и других методов лечения.
Аутоантитела могут присутствовать у людей, у которых нет проявлений болезни.
Каковы кожные особенности системной красной волчанки?
Около 80% пациентов с СКВ имеют поражение кожи (кожная ЛВ), и примерно у четверти из них это первый признак СКВ. Он может проявляться как специфичные для LE или неспецифические для LE проявления. LE-специфические поражения, как правило, индуцируются или усугубляются воздействием ультрафиолетового излучения и локализуются на участках, подверженных воздействию солнца, таких как лицо, шея, V шеи и верхняя часть спины.
Специфическая кожная СКВ
Кожная волчанка (СКВ) имеет специфические острые, подострые и хронические проявления.
- Обычно СКВ проявляется острой СКВ.
- Примерно у половины пациентов с подострой кожной LE развивается СКВ легкой степени
- Только 5% пациентов с хронической CLE имеют СКВ, так как CLE представляет собой кожную проблему без поражения других органов.
Острая CLE
- Фиолетовая эритема на центральной скуле лица или «бабочка» с резкой отсечкой по боковым краям, проходит без рубцевания (может привести к стойкой телеангиэктазии)
- Буллезная системная красная волчанка: пузырчатая сыпь, если она тяжелая, может напоминать токсический эпидермальный некролиз
- Макулопапулезная сыпь, напоминающая патологическую лекарственную сыпь
- Эрозии и язвы слизистой оболочки (губ, носа, рта, половых органов)
- Фоточувствительность: волчаночная сыпь в основном появляется на участках, подвергшихся воздействию солнца.Фоточувствительность может быть легкой или очень сильной, при этом сыпь появляется после минимального воздействия света.
- Диффузное облысение (безрубцовая алопеция) с ломкими стержнями волос
Подострый кожный LE
- Плоские чешуйчатые пятна, напоминающие псориаз, часто в виде сети
- Кольцевые (кольцевидные) полициклические (перекрывающиеся круговые) поражения
- Поражения рассасываются с минимальным рубцеванием
- Поражает туловище и руки
- Вспышки на солнце, обычно не затрагивают лицо и руки
Хроническая CLE
Острая кожная красная волчанка
См. Другие изображения острой СКВ.
Подострая кожная волчанка по SLE
Дополнительные изображения кожной красной волчанки.
Хроническая кожная волчанка
Неспецифическая кожная СКВ
Неспецифическая кожная СКВ относится к особенностям, связанным с основным заболеванием, а не с аутоиммунной атакой. Эти особенности могут возникать при других заболеваниях соединительной ткани и аутоиммунных заболеваниях.
- Капиллярная телеангиэктазия ногтевой складки
- Феномен Рейно (белые пальцы рук и ног от холода)
- Васкулопатия кончиков пальцев (закупорка мелких кровеносных сосудов тромбом)
- Диффузное истончение волос без ломкости
- Крапивница, которая может быть нейтрофильной при биопсии
- Кожный васкулит: пальпируемая пурпура или крапивница
- Livedo reticularis (сетка кровеносных сосудов) у 20–30% пациентов с СКВ
- Папулезный муциноз (отложения муцина на коже)
- Кожный кальциноз (отложения кальция в коже)
Неспецифическая кожная красная волчанка
Каковы системные признаки системной красной волчанки?
При СКВ могут возникать многочисленные системные особенности, которые могут привести к критическому заболеванию.
- Общие: усталость, недомогание, хроническая боль, лихорадка с обострениями
- Суставы: артрит или синовит, вызывающие отек, боль и утреннюю скованность
- Легкие: плеврит или плевральный выпот
- Сердце: перикардит или выпот в перикард
- Почки: белок, цилиндры с мочой, гломерулонефрит
- Мозг: судороги, психоз, спутанность сознания
- Нервная система: множественный мононеврит, миелит, периферическая невропатия
- Кровь: пониженное количество эритроцитов, лейкоцитов и тромбоцитов
Как диагностируется системная красная волчанка?
СКВ иногда бывает трудно диагностировать из-за большого разнообразия форм заболевания и наличия подобных симптомов у людей, не страдающих этим заболеванием.Было предпринято несколько попыток помочь клиницистам в постановке диагноза, включая критерии Американского колледжа ревматологов для классификации СКВ (пересмотренные в 1997 г.). В 2012 году критерии были пересмотрены Международной сотрудничающей клиникой по системной волчанке (SLICC) [1].
Используя критерии SLICC, СКВ диагностируется, если у пациента с течением времени наблюдается одно из следующих событий:
- Четыре критерия, включая ≥ одного клинического критерия и ≥ одного иммунологического критерия
- Подтвержденный биопсией волчаночный нефрит и антинуклеарные антитела или антитела против двухцепочечной ДНК
Эти критерии зависят от истории болезни, клинического обследования, исключения других причин симптомов и результатов исследований, включая анализы крови и биопсию пораженной ткани.Четыре из 17 критериев SLICC относятся к коже.
Клинические критерии
- Острая или подострая кожная волчанка
- Хроническая кожная волчанка
- Язвы во рту
- Безрубцовая алопеция
- Синовит с поражением 2 или более суставов
- Серозит, поражающий легкие или сердце
- Поражение почек
- Неврологическое поражение
- Гемолитическая анемия
- лейкопения или лимфопения
- Тромбоцитопения
Иммунологические критерии
- Повышенный уровень ANA
- Повышенный уровень антител против дцДНК
- Наличие анти-Sm
- Положительные антифосфолипидные антитела (волчаночный антикоагулянт, ложноположительный быстрый плазменный реагин, антикардиолипиновые антитела с высоким титром, положительный анти-2-гликопротеин I)
- Низкие уровни дополнения
- Положительный прямой тест Кумбса
* Международные сотрудничающие клиники системной волчанки SLICC; Антиядерное антитело ANA; Анти-дцДНК анти-двухцепочечная ДНК
Индекс площади и тяжести кожной красной волчанки (CLASI)
Индекс площади и тяжести кожной красной волчанки (CLASI) был разработан в попытке классифицировать степень тяжести CLE.[2] Оценка активности и повреждений, вызванных заболеванием, рассчитывается для каждого из 12 анатомических участков (подробности см. В оригинальной опубликованной статье).
Общая оценка активности складывается из:
- Степень покраснения (0–3) и шкала (0–2)
- Поражение слизистой оболочки (0–1)
- Недавнее выпадение волос (0–1), безрубцовая алопеция (0–3)
Общая оценка повреждений складывается из:
- Степень диспигментации (0–2) и рубцевания (0–2)
- Сохранение диспигментации более 12 месяцев увеличивает вдвое балл по шкале диспигментации
- Рубцы кожи головы (0,3,4,5,6)
Результаты биопсии
Пациентам с СКВ часто проводится биопсия кожи.
- Острый CLE: неспецифический дерматит.
- Подострый CLE: признаки волчанки, отмеченные в эпидермисе и поверхностной дерме
- Хроническая дискоидная CLE: типичные признаки волчанки с атрофией и рубцеванием
- Прямая иммунофлуоресценция положительна на защищенной от солнца здоровой коже в SLE
Анализы крови
Множественные аутоантитела обычно присутствуют при СКВ, часто в высоких титрах (см. Иммунологические критерии выше). Относительно кожных заболеваний при СКВ:
- Около 70% пациентов с подострой ХКВ имеют положительные экстрагируемые ядерные антитела анти-Ro (также называемые анти-SSA) и анти-La (также называемые анти-SSB).
- Anti Ro / La также связан с синдромом Шегрена и риском неонатальной красной волчанки.
- Низкий уровень комплемента в сыворотке при СКВ был связан с уртикарным васкулитом и заболеванием почек.
- Антифосфолипидные антитела связаны с сетчатым ливедо, тромбозом и осложнениями беременности (антифосфолипидный синдром).
- Антитела к аннексину 1 могут быть диагностическим маркером дискоидной CLE
Пациенты с СКВ также должны иметь функцию почек, печени и щитовидной железы и маркеры воспаления, такие как С-реактивный белок (СРБ), иммуноглобулины и ревматоидный фактор.
Фотопровокационные тесты
Фотопровокационные тесты иногда проводятся для подтверждения того, что кожная сыпь вызывается воздействием ультрафиолетового или видимого излучения определенных длин волн.
Другие тесты
Другие тесты зависят от пораженного органа. Они могут, например, включать:
- Анализы мочи на гиалиновые цилиндры, креатинин, белок и кровь
- Артериальное давление
- Рентген грудной клетки, УЗИ, КТ и МРТ
- Электрокардиограф (ЭКГ) и эхокардиография
- Тестирование нервов и мышц
- Осмотр офтальмологический
- Эндоскопия желудочно-кишечного тракта
- Биопсия почки.
Как лечить системную красную волчанку?
Профилактические меры
Следующие меры необходимы для снижения вероятности обострения и повреждения органов.
Местная терапия
Прерывистые курсы сильнодействующих местных кортикостероидов важны в лечении CLE. Их следует аккуратно наносить на кожные поражения.
Также можно использовать мазь с ингибиторами кальциневрина такролимус и крем пимекролимус.
Системная терапия
Лечение СКВ зависит от преобладающих органов, вовлеченных в заболевание. Обычно любой из следующих препаратов можно использовать отдельно или в комбинации.
CLE также иногда лечат с помощью:
Каковы перспективы системной красной волчанки?
СКВ приводит к хроническому заболеванию с обострениями и периодами ремиссии. У некоторых пациентов со временем исчезают все признаки активного заболевания.
Волчанка и лекарства — Better Health Channel
Волчанка (системная красная волчанка или СКВ) является хроническим заболеванием, которое возникает в результате неправильной работы иммунной системы.Иммунная система предназначена для выявления инородных тел (таких как бактерии и вирусы) и нападения на них, чтобы сохранить ваше здоровье. Однако в случае волчанки ваша иммунная система по ошибке атакует такие ткани, как кожа, суставы, почки, слизистая оболочка сердца и легких, вызывая продолжающееся воспаление и боль.
Большинство людей с волчанкой имеют легкую форму заболевания, но время от времени случаются обострения.
Приливы — это периоды, когда ваши симптомы (например, сыпь, боль и усталость) становятся более интенсивными.Они непредсказуемы и могут возникнуть из ниоткуда. Они часто возникают из-за стресса и воздействия ультрафиолетового (УФ) света.
Волчанка чаще всего возникает у женщин детородного возраста. Неизвестно, что вызывает волчанку, однако похоже, что ваши гены могут играть роль, а также триггеры, такие как болезнь, травма или период стресса.
Лекарства для лечения волчанки
Лекарства от волчанки не существует, однако существуют различные лекарства, которые могут помочь очень эффективно ее контролировать.Если ваше состояние контролируется на ранней стадии, вероятность последующих осложнений может быть снижена. Существует также множество стратегий, которые вы можете использовать для управления своим состоянием, включая физическую активность и изменение образа жизни.
Лекарства могут помочь справиться с симптомами и помочь контролировать вашу сверхактивную иммунную систему. Поскольку люди с волчанкой испытывают разные симптомы и в разной степени, не существует универсального лечения. Вам может потребоваться комбинация различных лекарств, в том числе:
- болеутоляющих (анальгетиков)
- нестероидных противовоспалительных препаратов (НПВП)
- кортикостероидов
- гидроксихлорохина (или противомалярийных)
- , модифицирующих болезнь противоревматические препараты (БПВП)
- иммунодепрессанты.
Нестероидные противовоспалительные препараты (НПВП)
НПВП используются для уменьшения воспаления, боли и лихорадки, связанных с волчанкой. Они включают лекарства, отпускаемые без рецепта, такие как ибупрофен (например, Нурофен®), или лекарства, отпускаемые по рецепту, такие как Вольтарен®, Целебрекс® и Орудис®.Основные побочные эффекты НПВП возникают в желудочно-кишечном тракте, особенно в желудке и пищеводе (пищевод), где они могут вызывать расстройство желудка, язвы и даже кровотечения (кровотечение внутри вашего тела).Иногда люди, принимающие НПВП, также принимают лекарства, защищающие желудок, чтобы защитить себя от этого.
Более новые НПВП, такие как Celebrex® или Arcoxia®, могут иметь меньший риск побочных эффектов со стороны желудочно-кишечного тракта. Чтобы свести к минимуму побочные эффекты, НПВП следует принимать только по назначению. Также известно, что НПВП
вызывают повышение артериального давления и задержку жидкости, а также могут нарушать функцию почек у людей с волчанкой. По этой причине их обычно избегают людям, у которых заболевание почек вызвано волчанкой (волчаночный нефрит).Существует некоторая дискуссия о безопасности НПВП для людей с риском сердечных заболеваний, поскольку в некоторых исследованиях сообщается о повышении риска сердечного приступа и инсульта. Люди с волчанкой подвержены более высокому риску сердечных заболеваний, поэтому важно обсудить с врачом риски и преимущества использования НПВП.
Гидроксихлорохин
Лекарства, такие как гидроксихлорохин (Плаквенил®), называются антималярийными, потому что они изначально использовались для лечения малярии.Теперь мы знаем, что они очень эффективны при контроле активности иммунной системы при хронических состояниях, таких как волчанка. Обычно принимаемый в виде одной или двух таблеток в день, гидроксихлорохин уменьшает проблемы с кожей и суставами, связанные с волчанкой. У людей, принимающих гидроксихлорохин, реже возникают обострения волчанки, поэтому большинство ревматологов рекомендуют принимать его всем людям с волчанкой в течение длительного времени.
Побочные эффекты противомалярийных препаратов возникают редко. Иногда они могут вызывать сыпь или расстройство желудка (включая диарею).Если доза слишком высока, они могут вызвать повреждение глаз, но это крайне редко при использовании правильной дозы. Однако рекомендуется ежегодная проверка зрения.
Кортикостероиды
Кортикостероиды, также известные как стероиды, кортизон, преднизон и преднизолон, представляют собой синтетические гормоны, имитирующие действие кортизона, естественного гормона, вырабатываемого надпочечниками. Эти лекарства обычно принимают в форме таблеток, но могут вводиться инъекции при особенно тяжелых обострениях волчанки.
Дозировка зависит от тяжести симптомов и общего состояния здоровья человека, включая возраст и вес. Основная функция стероидов — лечить воспаление. Они также помогают уменьшить боль и жар.
Стероиды также ослабляют активность иммунной системы, что помогает уменьшить тяжесть ваших симптомов. Очень важно не сокращать дозу, не посоветовавшись с врачом.
Основная проблема стероидов в том, что они имеют серьезные побочные эффекты.Все побочные эффекты связаны с принимаемой дозой, поэтому вы и ваш врач часто будете использовать другие стратегии, чтобы убедиться, что вы принимаете минимально возможную дозу.
Потенциальные побочные эффекты кортикостероидов включают:
- изменения настроения
- истончение кожи, приводящее к легким синякам
- увеличение веса из-за повышенного аппетита и снижения метаболизма
- остеопороз — обычно людям с низкой плотностью костей дают кальций и витамины Добавки D для противодействия этому
- риску диабета и высокого кровяного давления
- нежелательного роста волос
- повышенного риска инфекций из-за подавления вашей иммунной системы
- катаракты (только при длительном применении).
Хотя эти побочные эффекты звучат плохо, большинство людей, использующих стероиды для лечения волчанки, в конечном итоге используют очень низкие дозы с минимальными побочными эффектами, даже если их начальная доза высока. Разница между хорошо контролируемой волчанкой и волчанкой, влияющей на ваше здоровье, может заключаться в нескольких миллиграммах стероидов, поэтому избегать их любой ценой не рекомендуется.
Если вас действительно беспокоит прием кортикостероидов, открыто и честно поговорите с врачом о том, что вас беспокоит. Вместе вы сможете найти решение, которое поможет вам справиться с волчанкой и избавит вас от беспокойства.
Иммунодепрессанты
Симптомы волчанки вызваны аномальной активностью иммунной системы, специализированной группы клеток и химических веществ, которые борются с инфекцией. Иммунодепрессанты, такие как азатиоприн, циклофосфамид и метотрексат, уменьшают симптомы волчанки за счет снижения активности иммунной системы.
Азатиоприн используется для лечения волчанки, а также для лечения других иммунных заболеваний и трансплантации органов. Метотрексат — очень часто используемое лекарство при ревматоидном артрите и считается настолько безопасным, что теперь является стандартным лечением.Микофенолат все чаще используется, особенно для лечения волчанки почек.
Каждое из этих лекарств оказывает определенное действие на волчанку и определенные побочные эффекты, поэтому каждое из них следует применять под тщательным наблюдением специалиста.
Меры предосторожности при приеме лекарств от волчанки
Не меняйте дозы и не прекращайте прием каких-либо лекарств, не посоветовавшись предварительно с врачом.
Некоторые лекарства от волчанки могут опасно взаимодействовать с другими лекарствами. Никогда не принимайте лекарства от других заболеваний, если они не назначены тем же врачом, который лечит вашу волчанку.Сюда входят лекарства и добавки, отпускаемые без рецепта врача.
Другие лекарства и добавки могут влиять на лечение волчанки или вызывать побочные эффекты. В зависимости от лекарств, которые вы принимаете для лечения волчанки, вам может потребоваться пройти обычные анализы (например, глазные анализы или анализы крови), чтобы убедиться, что лекарства не вызывают каких-либо побочных эффектов.
Прием лекарств от волчанки
Важно, чтобы вы знали, что попадает в ваш организм, особенно когда речь идет о лекарствах.Исследования показывают, что хорошо осведомленные люди лучше справляются со своим состоянием. Информационные листы о лекарствах, используемых для лечения волчанки, можно получить в Австралийской ревматологической ассоциации, у вашего врача или фармацевта.
Постарайтесь принимать лекарства в соответствии с предписаниями, в правильных дозах и в рекомендованное время суток. Лучше не вносить изменения в лекарства, не посоветовавшись со своим лечащим врачом, включая врача и других специалистов, особенно если вы планируете прекратить или увеличить курс лечения.
Другое лечение волчанки
Помимо лекарств, другие методы лечения, которые могут помочь вам управлять волчанкой, включают:
- ограничение пребывания на солнце
- нанесение солнцезащитного лосьона
- регулярные физические упражнения
- ежегодные прививки от гриппа
- регулярные медицинские осмотры- ups
- здоровое и сбалансированное питание
- управление стрессом
- ограничение алкоголя.
Куда обратиться за помощью
Использование гидроксихлорохина (HCQ) и риски при лечении системной красной волчанки
Исследователи изучают представления пациентов с СКВ о рисках ретинопатии, вызванной HCQ, и призывают к повышению уровня информированности пациентов.Плюс: как HCQ попадает в пандемию COVID-19.
Гидроксихлорохин считается эффективным методом лечения системной красной волчанки (СКВ) для поддержания ремиссии заболевания и снижения риска необратимого повреждения почек. Несколько исследований показали, что гидроксихлорохин (HCQ) улучшает выживаемость, снижает частоту обострений, сводит к минимуму риски повреждения основных органов и оказывает защитное действие на здоровье сердечно-сосудистой системы при СКВ. 1–4
Также было продемонстрировано, чтоHCQ имеет более низкий риск лекарственной токсичности, чем другие модифицирующие болезнь противоревматические препараты (DMARD). 5 Лекарство обычно хорошо переносится, наиболее частыми побочными эффектами являются желудочно-кишечные расстройства, дерматологические изменения и головная боль. (См. Ниже примечание автора относительно использования HCQ во время пандемии COVID-19. )
Необратимая ретинопатия — один из наиболее опасных долгосрочных побочных эффектов HCQ. Риск оценивается ниже 2%, когда HCQ должным образом дозируется из расчета <5 мг / кг фактической массы тела при соответствующем офтальмологическом мониторинге. 6 Рекомендации Американской академии офтальмологии (AAO) по скринингу гидроксихлорохиновой и хлорохиновой ретинопатии выявили несколько факторов риска развития ретинопатии, вызванной HCQ: 7
- дозировка более 5 мг / кг / день фактической массы тела
- срок использования> 5 лет
- тамоксифен использовать
- почечная недостаточность
- ранее существовавшее заболевание сетчатки и желтого пятна.
В соответствии с рекомендациями AAO стандартным лечением пациентов из группы низкого риска является базовая офтальмологическая оценка с последующим ежегодным наблюдением через 5 лет непрерывного использования HCQ или хлорохина. 7 Ретинопатию обычно проверяют с помощью оптической когерентной томографии в спектральной области и автоматических тестов поля зрения. 7
Несмотря на положительные эффекты HCQ при СКВ, нередко встречаются пациенты с опасениями по поводу ретинопатии, вызванной HCQ; некоторые пациенты могут решить прекратить прием гидроксихлорохина из-за этих опасений. Однако отсутствуют данные о восприятии пациентами СКВ рисков и преимуществ лечения гидроксихлорохином. Пациенты, которые самостоятельно прекращают прием гидроксихлорохина без каких-либо признаков ретинопатии, могут быть без нужды лишены преимуществ препарата. 8 Цели этого исследования заключались в оценке восприятия пациентами СКВ рисков и преимуществ, связанных с использованием HCQ, и их осведомленности о факторах риска ретинопатии, вызванной HCQ.
Гидроксихлорохин считается эффективным вариантом лечения системной красной волчанки и в настоящее время также используется для лечения COVID-19. (Изображение: istock)
Методы
пациентов были набраны для участия через электронную рассылку базы данных Lupus Alliance of Upstate New York (LAUNY) с марта по апрель 2019 года.LAUNY — это некоммерческая организация, основанная в 1976 году, которая обслуживает 33 округа штата Нью-Йорк. В списке рассылки было около 3000 электронных писем, включая пациентов с СКВ и их родственников. Электронные письма были отправлены всем 3000 членам с просьбой добровольно принять участие в анонимном опросе, щелкнув ссылку в электронном письме. Это электронное приглашение было отправлено дважды с интервалом в две недели в феврале 2019 года.
Данные опроса были автоматически записаны с использованием платформы документов Google.Участвующим лицам не предоставлялось никакого финансового вознаграждения или подарков. Участие было добровольным, анонимным и ограничивалось взрослыми от 18 лет и старше. Исследование было одобрено Комитетом по обзору фармацевтического колледжа и медицинских наук Олбани.
Анкета
Собранные демографические переменные включали возраст, пол, вес, рост, самопровозглашенную расу и самый высокий уровень образования. Мы собрали данные об использовании участниками рецептурных препаратов, безрецептурных препаратов и лекарственных трав для лечения СКВ.Собранная информация, связанная с заболеванием, включала продолжительность СКВ, продолжительность и текущую дозу (если используется в настоящее время) HCQ, проводились ли исходные и последующие офтальмологические оценки (насколько им известно), а также история любых аномальных офтальмологических результатов.
Кроме того, восприятие участниками рисков и преимуществ лечения HCQ было запрошено с помощью электронного вопросника. Пациентов просили ответить на утверждения, используя следующие варианты: полностью согласен, согласен, не согласен, категорически не согласен, я не знаю, или , неприменимо e.Соответствующие описательные статистические методы использовались для описания демографических характеристик пациентов, их восприятия и осведомленности о рисках.
Результаты
Всего в опросе приняли участие 94 респондента. Демографические данные представлены в таблице I. Большинство респондентов составили женщины (98%). Среднее время с момента постановки диагноза СКВ респондентам составило 10 лет. Почти вся когорта (97%) были выпускниками средней школы, а 70% имели степень младшего специалиста или более высокую степень. Из 94 респондентов 18 (19%) сообщили, что проходили офтальмологический осмотр в прошлом.
Почти все респонденты (n = 89; 94%) были либо текущими, либо бывшими пользователями HCQ (см. Таблицу II). Эта группа была определена как «когорта анализа HCQ». Другие часто назначаемые препараты от СКВ, такие как белимумаб, микофенолятмофетил, азатиоприн, циклоспорин А, циклофосфамид, использовали от 4% до 24% респондентов. Ответив на открытый вопрос, респонденты сообщили, что они использовали следующие рецептурные, безрецептурные или растительные препараты, связанные с СКВ:
- метотрексат (n = 7)
- такролимус (n = 1)
- кортикостероид (пероральный или местный, n = 29)
- НПВП (n = 17)
- куркума (n = 6)
- рыбий жир (n = 5)
- DHEA (дегидроэпиандростерон) (n = 4)
- CBD (каннабидиол) (n = 3)
- медицинская марихуана (n = 2)
- глюкозамин / хондроитин (n = 2)
- налтрексон в низких дозах (n = 1)
- кофермент Q, (n = 1)
- травы (например, алоэ, расторопша).
Когорта HCQ была дополнительно проанализирована в отношении предполагаемого риска, пользы и осведомленности анкеты (см. Таблицу III). Восемьдесят шесть человек (97%) сообщили о прохождении регулярных офтальмологических осмотров. Исходное обследование глаз было зарегистрировано у 73 (82%). Девяносто два процента (n = 82) сообщили, что их ревматологи сообщили им о ретинопатии, связанной с HCQ, а 74% (n = 66) восприняли ретинопатию как серьезный побочный эффект. Напротив, только 43% (n = 38) пациентов HCQ сообщили, что фармацевты предоставляли им информацию о ретинопатии.Значительная часть (n = 59, 66%) респондентов была проинформирована о ретинопатии, вызванной HCQ, через Интернет. Большая часть когорты HCQ (n = 57, 64%) желала продолжать получать HCQ, и относительно небольшой процент (n = 14, 16%) желали обсудить прекращение HCQ из-за опасений по поводу ретинопатии. Одна треть когорты (n = 29, 33%) хотела обсудить общие побочные эффекты HCQ со своими медицинскими работниками.
Большая часть когорты HCQ относительно не знала о факторах риска токсичности HCQ для сетчатки.Почти 60% (n = 53) респондентов либо неверно знали о связи между функцией почек и токсичностью HCQ (n = 18), либо признали, что не знали об этой связи (n = 35). Только одна треть респондентов знала о дозировке HCQ в зависимости от веса, чтобы избежать токсичности для сетчатки (n = 29). Пятнадцать процентов (n = 13) респондентов были обеспокоены возможными лекарственными взаимодействиями HCQ.
Авторы оценили дозировку HCQ в зависимости от веса в анализируемой когорте. Из 94 респондентов 66 человек были текущими пользователями HCQ.Два человека предоставили неверные дозы HCQ, а три человека не указали свой вес, что позволило провести оценку у 61 респондента опроса на предмет пригодности дозирования HCQ на основе веса. Критерий превышения дозы HCQ был> 5 мг / кг / день. Двадцать человек из 61 (33%) были отнесены к категории лиц с передозировкой на основании их собственного веса и суточной дозы HCQ.
Обсуждение
В представленном обзоре 89 пациентов с СКВ, которые ранее или в настоящее время использовали HCQ, мы обнаружили, что примерно четверть не знали о ретинопатии, вызванной HCQ.Незнание индивидуальных факторов риска ретинопатии, вызванной HCQ, колебалось от 13% до 39%. Кроме того, несмотря на то, что 92% пациентов были проконсультированы относительно токсичности HCQ их ревматологами, а 97% проходили регулярные офтальмологические осмотры, тем не менее, каждый шестой был обеспокоен токсичностью глаз до такой степени, что рассматривал возможность прекращения приема препарата.
Большинство участников этого исследования сообщили об использовании гидроксихлорохина в настоящем или прошлом. Точно так же Уоллес и др. Сообщили об использовании HCQ у большинства испытуемых в их когорте. 9 В представленной когорте 80% пациентов сообщили о прохождении базового офтальмологического скринингового обследования до начала HCQ. Почти все участники (97%) регулярно наблюдались у офтальмолога. В предыдущих исследованиях сообщалось о различных данных о соблюдении врачами офтальмологических рекомендаций в отношении мониторинга токсичности HCQ в диапазоне от 50 до 85%. 10-12
Более 90% пациентов сообщили, что их ревматолог обсуждает ретинопатию как побочный эффект.Однако более 50% пациентов не помнят, чтобы их фармацевты обсуждали эту тему. Большинство пациентов признали ретинопатию серьезным побочным эффектом HCQ, и 16% субъектов выразили желание прекратить прием HCQ из-за опасений отравления сетчаткой. Как и в представленном исследовании, Кабрал сообщил, что 21% пациентов с СКВ были обеспокоены токсичностью HCQ. 13 Кабрал пришел к выводу, что страх был фактором, влияющим на приверженность, поэтому пациенты знали, что HCQ хорошо переносится и может улучшить приверженность.
Девятнадцать процентов респондентов представленных анкет сообщили, что в анамнезе были отклонения от нормы при офтальмологическом обследовании. Этот процент считается высоким, учитывая, что средняя продолжительность терапии нашей когорты составляла всего 5 лет, и большая часть токсичности HCQ для сетчатки возникает после более длительного приема препарата. Однако, поскольку авторы не смогли уловить специфическую природу глазных аномалий в когорте HCQ, неясно, представляли ли они ретинопатию, связанную с HCQ.
Интересно, что хотя большинство пациентов знали о риске ретинопатии, связанной с HCQ, только две трети признали, что продолжительность терапии и доза лекарства связаны с этим риском.Кроме того, почти половина когорты (46%) либо отрицали какие-либо знания, либо имели неверные знания относительно дозирования HCQ в зависимости от веса. Пациенты не могли оценить свой риск ретинопатии, связанной с HCQ, и это могло помешать им точно оценить вероятность развития этого осложнения.
Ограничения
Это исследование имеет ограничение в том, что в когорте анализа HCQ могла быть ошибка отбора, поскольку респонденты могли отличаться от тех, кто отказался от участия.Такое смещение может объяснить, почему респонденты были высокообразованными, а 85% имели хотя бы какое-то высшее образование. В-третьих, низкая частота ответов на анкету и географически ограниченная территория (на основе рассылки в Нью-Йорке) когорты, возможно, ухудшили результаты, поскольку они были распространены на всех пациентов с СКВ. Наконец, поскольку это исследование было самооценкой, авторы не могли проверить достоверность представленных медицинских оценок, таких как частота посещений офтальмолога или характер патологических обследований глаз.
Заключение
В целом, результаты показывают, что обучение пациентов относительно ретинопатии, вызванной HCQ, должно быть усилено. Поскольку во время визитов в офис время часто ограничено, следует рассмотреть новые образовательные подходы, включая использование онлайн-ресурсов, групп поддержки пациентов и подробные консультации фармацевтов и других смежных медицинских работников.
Информирование пациентов о факторах риска, связанных с более высокой вероятностью ретинопатии, важно для обеспечения надлежащего дозирования в зависимости от веса, функции почек, сопутствующего употребления наркотиков и соблюдения рекомендаций по офтальмологическому обследованию.Авторы предполагают, что такие подходы могут привести к лучшему пониманию пациентами ретинопатии, вызванной HCQ, лучшему соблюдению режима лечения и снижению частоты этого осложнения.
Обновление авторов: HCQ и COVID-19Этот проект был завершен в мае 2019 года, а рукопись была подготовлена позже, в 2019 году, когда пандемия COVID-19 была непредвиденной. На момент публикации этой статьи пандемия нового коронавируса распространялась по всему миру, и по совпадению гидроксихлорохин (HCQ) рассматривался как потенциально эффективное средство для улучшения исхода COVID-19.
Однако в июне 2020 года NEJM опубликовал данные рандомизированного контролируемого исследования, которые продемонстрировали, что «после воздействия COVID-19 с высоким или умеренным риском гидроксихлорохин , а не предотвращал болезнь, совместимую с COVID-19, или подтвержденную инфекцию при использовании. в качестве постконтактной профилактики в течение 4 дней после заражения ». Кроме того, РКИ показало больше побочных эффектов при использовании HCQ, чем при использовании плацебо (40,1% против 16,8%).
1 июля 2020 года FDA выпустило заявление, в котором предостерегает от использования гидроксихлорохина или хлорохина для лечения COVID-19 вне больниц или клинических испытаний из-за риска нарушений сердечного ритма.Дополнительные исследования, опубликованные летом 2020 года, в том числе статья JAMA , не обнаружили «клинической пользы от гидроксихлорохина» для людей, подвергшихся воздействию COVID-19. В NEJM Коэн поставил под сомнение продолжающееся использование HCQ в испытаниях, полученных на сегодняшний день.
Тем не менее, сообщалось о нехватке HCQ из-за институциональных и индивидуальных накоплений. Следовательно, пациенты, которые использовали HCQ для лечения своих ревматических состояний (например, СКВ, ревматоидный артрит, синдром Шегрена), могут подвергаться риску не получать лекарства, на которые они полагались в течение многих лет.
Наконец, в соответствии с фокусом этой статьи на SLE, пациенты и клиницисты должны знать, что HCQ не свободна от побочных эффектов и что следует обсуждать соотношение риска и пользы, чтобы принимать решения, ориентированные на пациента, в индивидуальных обстоятельствах и тяжести заболевания.
…
* Опубликовано в Интернете перед печатью в апреле 2020 г. Рецензировано Джеффри Фудином, PharmD, DAIPM, FCCP, FASHP
Раскрытие информации: Это исследование было частично поддержано Программой внутренних исследований Национального института артрита, скелетно-мышечных и кожных заболеваний Национальных институтов здравоохранения.На момент проведения этого исследования доктора. Квон и Банерджи были связаны с Центром ревматологии в Олбани, штат Нью-Йорк. Доктор Фаррелл получает часть своей постоянной зарплаты от компании Janssen.
Последнее обновление: 5 октября 2020 г.
Как врачи могут управлять ревматическими и иммунными заболеваниями во время COVID-19
.
 Иммунодепрессанты применяют для регуляции работы иммунной системы. Моноклональные антитела, разработанные специально для лечения красной волчанки, являются инновационными и эффективными препаратами, поскольку их воздействие направлено на угнетение выработки антител, атакующих собственные клетки организма.
Иммунодепрессанты применяют для регуляции работы иммунной системы. Моноклональные антитела, разработанные специально для лечения красной волчанки, являются инновационными и эффективными препаратами, поскольку их воздействие направлено на угнетение выработки антител, атакующих собственные клетки организма.
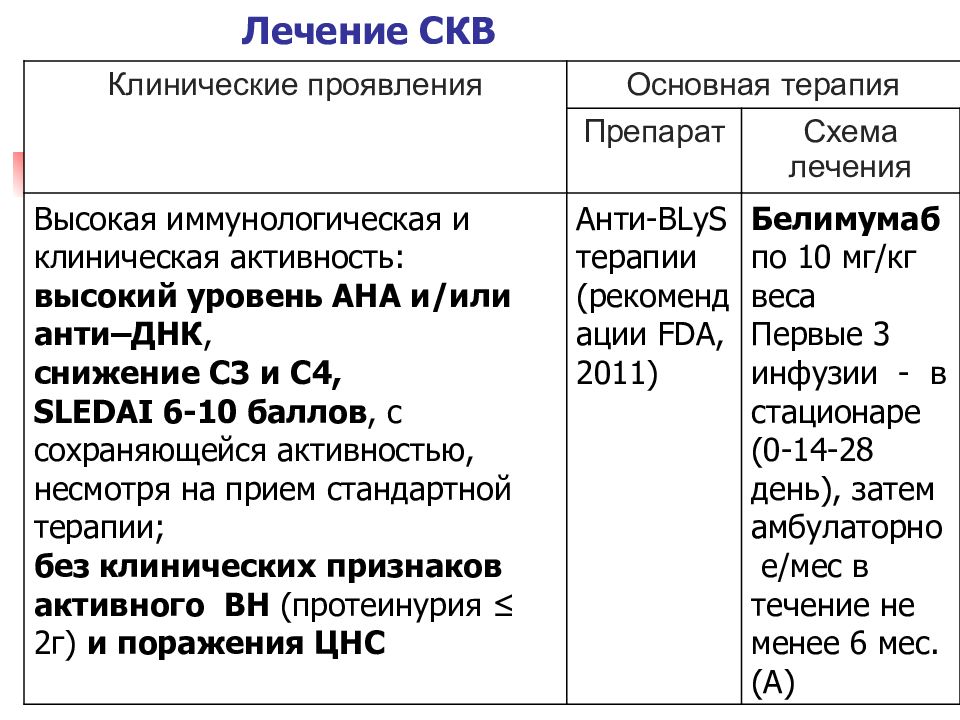
 2 ± 10.7 лет
2 ± 10.7 лет 33 ± 13.39 лет), 7 C (49.42 ± 8.51 лет)
33 ± 13.39 лет), 7 C (49.42 ± 8.51 лет)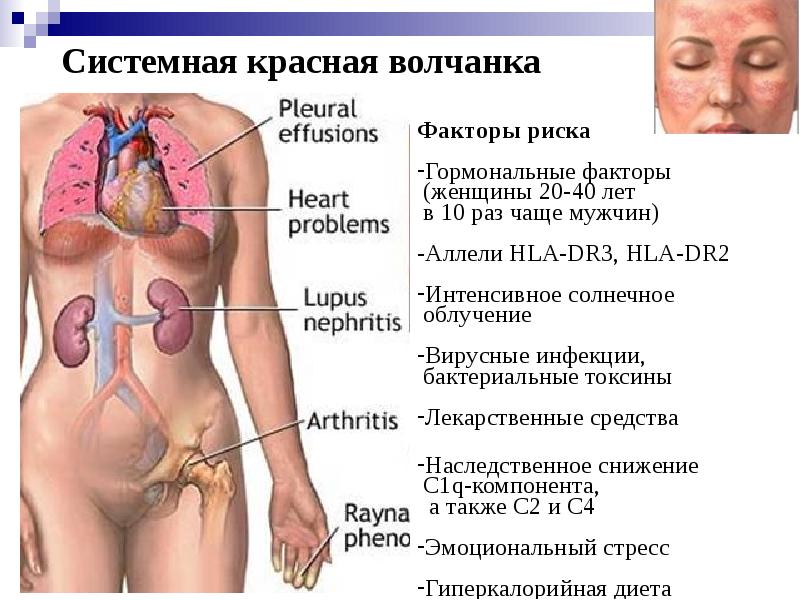 1
1