в чем опасность болезни Saratovnews.ru
Стригущий лишай у человека является распространенным дерматологическим заболеванием, которым можно заразиться от животных и заболевших людей. При подозрении на болезнь, пациент должен обратиться к врачу за назначением квалифицированного лечения.
ЧТО ПРЕДСТАВЛЯЕТ СОБОЙ СТРИГУЩИЙ ЛИШАЙ У ЧЕЛОВЕКА
Данная разновидность лишая – в числе наиболее распространенных патологий. В зоне риска – молодежь и дети. Но может быть диагностирован лишай у пациента другой возрастной категории.
Это грибковое заболевание. Источник – больное животное или человек. Благоприятными условиями для заражения являются следующие факторы:
- легкомысленное отношение к правилам личной гигиены;
- сниженный иммунитет;
- любые повреждения поверхности кожи.
ПУТИ ЗАРАЖЕНИЯ
Данная разновидность лишая – заразное заболевание, передающееся контактно-бытовым путем. В детской среде источником заражения часто становятся бездомные животные – щенки и котята, пораженные недугом. Достаточно просто погладить животное или поиграть с ним.
Условиями заражения от другого человека являются такие факторы:
- Использование общих предметов, например, расчесок.
- Непосредственный контакт с больным человеком.
Больше всего к грибкам, которые вызывают лишай, предрасположены маленькие дети. Это связано с тем, что с возрастом происходит формирование устойчивости кожи к патогенной микрофлоре.
Грибок, являющийся источником стригущего лишая, может сохраняться на различных поверхностях месяцами, представляя угрозу для окружающих.
СИМПТОМЫ: КАК РАСПОЗНАТЬ БОЛЕЗНЬ
После заражения болезни проходит инкубационный период, который может составлять от буквально нескольких дней до нескольких недель. На следующей стадии болезни начинают проявляться симптомы лишая, показанные на фото.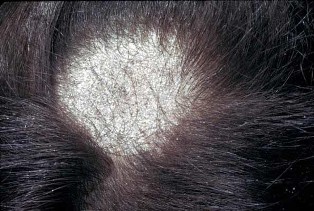
- поверхность кожи;
- ногти;
- волосистая часть головы.
В зависимости от зоны поражения отличаются симптомы болезни:
- Ногти. Появляются сероватые пятна на ногтевых пластинах, которые становятся со временем больше и приводят к повышенной ломкости. Больной ощущает жжение в пораженной области и испытывает зуд.
- Волосистая часть головы. В начале заболевания появляются очаги с выраженными краями под волосами, кожа на которых меняет цвет и шелушится. Волосы в этом месте меняют структуру, топорщатся, ломаются и выпадают.
- Открытая кожа. Проявляются красные пятна, образуются пузыри, которые лопаются, оставляя после себя корочки.
Как выглядят симптомы в зависимости от зоны поражения, можно увидеть на фото в сети.
При форме заболевания, которая сопровождается нагноениями, симптомы более яркие:
- увеличение лимфатических узлов;
- крупные бляшки, диаметром до 10 сантиметров, которые имеют неровную поверхность и бугристость;
- общее плохое самочувствие;
- высыпания по типу крапивницы;
- увеличение температуры тела;
- отечность пораженных зон;
- болезненность в пострадавших от болезни зонах;
- образование рубцов.
Развитие заболевания проходит стадии развития: от начальной до активной.
ДИАГНОСТИКА
Точно поставить диагноз «стригущий лишай» может только специалист, так как отдельные проявления часто сигнализируют о других заболеваниях. Для этого больной должен посетить дерматолога или врача-миколога, специализирующегося на грибковых поражениях организма.
Возбудителем лишая данного типа может быть один из видов грибка:
- трихофития;
- микроспория.

Отдельно следует упомянуть трихофитию инфильтративно-нагноительную, которой заболевший человек может заразиться только от животных. Такая разновидность стригущего лишая сопровождается сильным воспалением и развитием гнилостных процессов. Длиться такое заболевание может от 60 до 100 дней, оставляя после себя рубцы. На волосистой части головы в месте, где находится шрам, волосы уже не растут.
Стандартная диагностика включает:
- Врачебный осмотр.
- Соскоб.
- Анализ на выявление грибка с применением специального оборудования.
- Забор волос.
Из собранного материала в лабораторных условиях делают посев, чтобы получить информацию о микрофлоре. При этом становится известна также чувствительность грибка к лекарствам.
МЕТОДИКА ЛЕЧЕНИЯ
Этот вид лишая – излечимое заболевание. Чем раньше начнется лечение, тем быстрее будет достигнут результат. Обычно полный курс терапии составляет до двух месяцев. Он включает целый комплекс мер.
Среди назначенных врачом препаратов могут быть следующие:
- противогрибковые препараты для перорального приема;
- применение мазей;
- антибиотики;
- гормональные лекарства.
Комплекс мероприятий по лечению стригущего лишая должен подбираться врачом с учетом особенностей течения заболевания. При не доведении лечения до конца или игнорирования лечебных мероприятий болезнь может перейти в хроническую форму. Наиболее часто врачами диагностируются рецидивы трихофитии ногтевых пластин.
Лечение стригущего лишая может проводиться в стационаре или в домашних условиях.
МЕРЫ ПРОФИЛАКТИКИ
Так как в группе риска – дети, то необходимо обеспечивать регулярный медицинский осмотр. К мерам профилактики относятся также:
- соблюдение правил гигиены;
- своевременные прививки и периодические осмотры домашних животных;
- исключение контактов с больными животными и людьми.

При попадании здорового человека в коллектив, в котором есть инфицированные стригущим лишаем, профилактические меры должны подбираться дерматологом или врачом-микологом.
По завершению лечения пациент должен пройти повторный осмотр для подтверждения полного выздоровления. И в будущем придерживаться профилактических мер. При грамотном, своевременно начатом лечении заболевание в большинстве случаев проходит без последствий.
Материалы взяты с Plastichno.com
Микроспория у человека — фото, симптомы, лечение и препараты
Микроспория, называемая в народе стригущий лишай, является заразным заболеванием, передающимся от больных животных. Именно поэтому характерные пятна на коже чаще всего появляются у детей, любящих возиться с кошками и собаками (особенно бездомными).
Для предотвращения распространения патологических пятен у больного и заражения здоровых людей следует знать первые признаки, характерные начальной стадии микроспории и обязательные лечебные мероприятия.
Микроспория — что это такое?
Микроспория — это кожное заболевание из группы микозов, спровоцированное заражением грибком Микроспорум. Проявления (признаки) возникают как на гладкой, так и на волосистой части кожных покровов (смотрите фото).
Внедряясь в кожу, грибок образует колонии в волосяных луковицах кожи головы или пушковых волос, покрывающих почти все тело. Однако очаги микроспории, хотя и крайне редко, могут возникать и на участках, полностью лишенных волос, — ладонях, подошве, ногтях.
Микроспория высоко контагиозна (заразна), при этом источником заражения являются больные животные.
В природе микроспорией могут болеть собаки и кошки, кролики, крупные домашние животные (свиньи, козы, лошади, овцы), а также дикие звери (обезьяны, лисы, тигры, песцы). Заражение происходит не только при прямом контакте с заболевшим животным, но и при попадании на руки человека шерсти и чешуек с предметами ухода и кормом, через подстилку и другой инвентарь.
Заражение происходит не только при прямом контакте с заболевшим животным, но и при попадании на руки человека шерсти и чешуек с предметами ухода и кормом, через подстилку и другой инвентарь.
Причем у животных заболевание часто протекает скрыто: очаги поражения обнаруживаются только при просвечивании люминесцентной лампой (зеленое свечение). Лишь иногда на голове, лапах или хвосте можно заметить очаги с торчащими обломками волосков и чешуйками.
Не исключена передача грибка от больного человека к здоровому. Заразиться можно даже при контакте с необработанной одеждой человека, болевшего некоторое время назад. Грибок микроспории, благодаря шестислойной оболочке и ребрам в виде паутинки, довольно устойчив во внешней среде и сохраняет жизнеспособность до 3 месяцев вне организма человека или животного.
Микроспория у детей — особенности болезни
Распространенность микроспории кожи у детей объясняется следующими фактами:
- Особая «любовь» возиться с бездомными котятами и щенками.
- Несоблюдение строгих правил гигиены — немытые руки.
- Недостаточная иммунная защита, ослабление иммунитета частыми простудными заболеваниями.
- В кожном сале у взрослых имеются органические кислоты, негативно влияющие на размножение грибка. Кожный иммунитет у детей менее развит.
- Частое травмирование кожи (порезы, ссадины, расчесы и мелкие ранки), которые способствуют распространению заболевания при попадании грибка.
- Необъяснимый с медицинской точки зрения факт — рыжеволосые дети практически не болеют стригущим лишаем.
Признаки микроспории у человека, фото
микроспория гладкой кожи, фото
фото микроспории у человека
Инкубационный период при микроспории составляет 5-7 дней при заражении от животного и до 4-6 недель — при заражении от больного человека.
Внешние проявления микроспории зависят от локализации патологического очага.
Микроспория гладкой кожи
Изначально появляется красное пятно округлой формы, с четкими границами, несколько возвышающееся над кожей. Очень быстро по периферии формируется валик с мельчайшими пузырьками и корочками, а грибковое пятно разрастается до 3 см.
Очень быстро по периферии формируется валик с мельчайшими пузырьками и корочками, а грибковое пятно разрастается до 3 см.
Центральная часть патологического очага бледнеет и покрывается достаточно крупными отрубевидными чешуйками. Чаще всего обнаруживается 1 — 3 очага на лице, шее, верхних конечностях.
Зуд при микроспории присутствует, однако не столь интенсивный, как, например, при аллергических высыпаниях.
Микроспория волосистой части головы
Чаще всего возникает в области темени и висков, а также на макушке. Выглядит колония грибка так: центральное крупное пятно, достигающее 5 см, и более мелкие (до 1,5 см) отсевы по окружности. При росте центральное пятно может поглощать близлежащие мелкие очаги.
Микроспория на голове у человека в начальной стадии формирует очаговое шелушение. При более близком рассмотрении можно увидеть беловатую «манжету» вокруг волосков, растущих внутри пятна. Это указывает на размножение грибка в устье волос, которое уже спустя неделю приводит к их обламыванию.
Внешне это выглядит как подстриженное на уровне 4-6 см пятно. Обломанные, с сероватым налетом волоски являются пристанищем для грибковых спор. Измененное положение волосяных «пеньков» при поглаживании сохраняется, в отличие от здоровых волос.
Собственно кожа головы в очагах поражения несколько гиперемирована, отечна и покрыта мелкими чешуйками белого или сероватого цвета.
Нетипичные формы
- Микроспория ногтей — ближе к краю среза ногтя образуется тусклое пятно, в дальнейшем приобретающее белый окрас. Ногтевая пластина в очаге поражения становится мягкой и легко крошится.
- Нагноившаяся микроспория — следствие неправильного лечения. На фоне очага формируются багрово-синюшные узелки и гнойнички. Возможно повышение температуры и увеличение близрасположенных лимфоузлов.
- Отягощенная микроспория — протекает хронически на фоне серьезных внутренних заболеваний (туберкулез, артриты и т. д.). При этом на фоне очагового или диффузного шелушения формируются участки алопеции (проплешины), заметна общая разреженность волосяного покрова.
 Обломки волос достигают длины 10-15 мм и не имеют серых чехлов из спор грибка.
Обломки волос достигают длины 10-15 мм и не имеют серых чехлов из спор грибка. - Микроспория лобка — чревата заражением полового партнера. Разветвленная кровеносная система этой области приводит к быстрому разрастанию пятен на половые губы, внутреннюю часть бедер и нижнюю часть живота. Также достаточно быстро присоединяется бактериальная инфекция с формированием инфильтратов, покрытых гнойными корками.
Лечение микроспории у человека, препараты
фото препаратов
Чем раньше распознана микроспория и назначено полноценное ее лечение, тем быстрее наступит выздоровление. Основное направление в лечении микроспории у человека — уничтожение грибка. С учетом высокой устойчивости микроспорума местное противогрибковое лечение дополняется высокими дозами системных антимикотиков, особенно при массированном поражении гладкой кожи или длинных волос.
Лекарственные средства для местного лечения микроспории:
- Клотримазол — нетоксичная, но не отличающаяся высокой эффективностью мазь является препаратом выбора для лечения микроспории у детей до 3 лет и беременных.
- Изоконазол, Бифоназол — дают высокий процент аллергической реакции.
- Кетоконазол — высокоэффективен, но обладает высокой токсичностью.
- Тербинафин — лучший препарат при микроспории в отношении нетоксичности, эффективности и цены. Это самое недорогое и эффективное средство от стригущего лишая, более дорогой аналог — Ламизил.
- Мази, содержащие серу (серно-салициловая, серно-дегтярная, серная) и раствор йода — в лечении микроспории применяются в сочетании с противогрибковыми наружными средствами.
- Комбинированные средства (Тридерм, Микозолон, Травокорт), имеющие в составе кортикостероиды, — целесообразны только при осложненной нагноением микроспории. Следует помнить: гормональные мази при длительном применении провоцируют атрофию кожи.
В комплекс лечения микроспории волосистой части головы входит:
- Антимикотический антибиотик Гризеофульвин — препарат выбора, достаточно токсичен.
 Для детей до 3 лет выпускается в виде суспензии.
Для детей до 3 лет выпускается в виде суспензии. - Необходимы высокие дозы препарата — 22 мг/кг массы тела. Нельзя принимать вместе с пенициллинами (одновременный прием вызывает аллергическую реакцию).
- Гепатопротекторы (Карсил, Лив-52 и другие) — для снижения токсичности Гризеофульвина и защиты печени.
- Противоглистные препараты (Декарис) — дегельментизация необходима для повышения эффективности антимикотиков и уменьшения иммуноснижающего воздействия Гризеофульвина.
- Тербинафин в таблетках (Ламизил) — менее токсичная альтернатива Гризеофульвину, не уступающая ему по эффективности.
Обязательные мероприятия при выявлении микроспории у человека:
- Удаление поврежденных волосков (эпиляция, ежедневное бритье).
- Мытье головы дважды в неделю.
- Регулярная смена белья.
- Ограничение контакта с больным человеком. Изоляция ребенка из ДОУ, школы при лечении микроспории у детей.
- Осмотр контактировавших с больным человеком людей.
- Осмотр домашних животных ветеринаром.
- Дезинфекция предметов ухода (полотенца, расчески), одежды, детских игрушек с помощью дезсредств. Генеральная уборка.
Все лечение занимает 3-6 недель. Выздоровление констатируется при отрицательном анализе соскоба с места повреждения.
Не стоит надеяться на народные средства. Микроспория — грибковая болезнь, и лечить ее обязательно антимикотиками. Домашние методы (протирание уксусом и т. д.) нередко обладают прижигающим действием, а дополнительное раздражение может спровоцировать распространение инфекции. Не исключено получение ожогов.
Профилактика микроспории
Для исключения заболевания микроспорией необходимо соблюдать следующие правила:
Исключить контакт с бродячими животными.
Покупать домашних животных только после осмотра ветеринаром. Периодически проводить профилактические осмотры домашних питомцев.
Карантинные мероприятия при выявлении микроспории у ребенка: изоляция из детсада/школы, дезинфекционные мероприятия, наблюдение контактировавших с больным.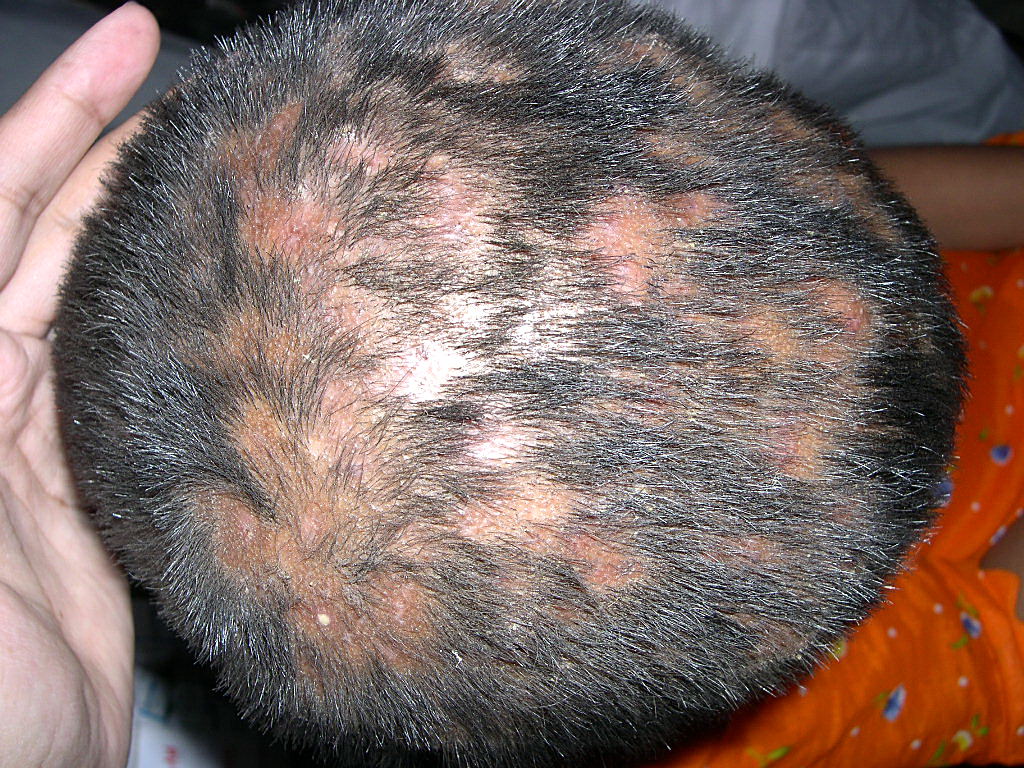
Микроспория — Ханты-Мансийский клинический кожно-венерологический диспансер
Микроспория – грибковое заболевание, при котором поражаются кожа и волосы, а в исключительно редких случаях и ногтевые пластинки. Название этого грибкового заболевания происходит от имени его возбудителя – гриба рода Микроспорум. Заболевание известно также как “стригущий лишай”, что обусловлено особенностями его проявления.
Попав на кожу, гриб внедряется в нее и начинает размножаться. При расположении вблизи волосяных луковиц споры гриба прорастают, приводя к поражению волоса. Довольно быстро распространяясь по поверхности волоса, гриб разрушает кутикулу, между чешуйками которой скапливаются споры. Таким образом, гриб окружает волос, формируя чехол, и плотно заполняет луковицу.
Микроспория является самой распространенной грибковой инфекцией, не считая грибка стоп. Заболевание встречается повсеместно. Микроспория обладает высокой заразностью, чаще страдают дети. Взрослые же болеют редко – преимущественно молодые женщины. Редкость заболевания микроспорией взрослых, особенно с поражением волосистой части головы, и обычно наступающее самостоятельное выздоровление при начале подросткового периода объясняется наличием в волосах взрослых людей органических кислот, замедляющих рост гриба.
Основной источник заболевания – кошки (обычно котята), реже собаки. Заражение микроспорией происходит при непосредственном контакте с больным животным или предметами, инфицированными шерстью или чешуйками. Попав в почву, гриб сохраняет жизнеспособность только в течение 1–3 месяцев. Таким образом, почва является лишь фактором передачи инфекции и не служит ее природным источником.
Симптомы микроспории
Проявления микроспории у животных характеризуются участками облысения на морде, наружных поверхностях ушных раковин, а также на передних, реже задних, лапах. Зачастую внешне здоровые кошки могут быть носителями гриба.
Сезонные колебания заболеваемости связаны с приплодами у кошек, а также более частым контактом детей с животными в летний период. Подъем заболеваемости микроспорией начинается в конце лета, пик приходится на октябрь–ноябрь, снижение до минимума наступает в марте–апреле.
Инкубационный период при зоонозной микроспории составляет 5–7 дней. Характер проявлений микроспории обусловлен расположением очагов поражения и глубиной проникновения возбудителя.
Выделяют микроспорию гладкой кожи и микроспорию волосистой части головы.
Микроспория гладкой кожи
В месте внедрения гриба появляется отечное, возвышающееся красное пятно с четкими границами. Постепенно пятно увеличивается в диаметре. По краю формируется непрерывный возвышающийся валик, представленный мелкими узелками, пузырьками и корочками. В центральной части пятна происходит разрешение воспаления, вследствие чего она приобретает бледно-розовую окраску, с отрубевидным шелушением на поверхности. Таким образом, очаг имеет вид кольца.
Количество очагов при микроспории гладкой кожи, как правило, невелико (1–3). Их диаметр колеблется от 0,5 до 3 см. Наиболее часто очаги располагаются на коже лица, шеи, предплечий и плеч. Субъективных ощущений нет или беспокоит умеренный зуд.
У новорожденных и детей раннего возраста, а также у молодых женщин нередко отмечаются выраженные воспалительные явления и минимальное шелушение.
У лиц, склонных к аллергическим реакциям (в частности, у больных атопическим дерматитом), грибок нередко маскируется проявлениями основного процесса и не всегда своевременно диагностируется. Применение же местных гормональных препаратов лишь усиливает распространение грибковой инфекции.
К редкой разновидности микроспории следует отнести поражение кожи ладоней, подошв и ногтевых пластинок. Для поражения ногтей характерно изолированное поражение ногтевой пластины, обычно ее внешнего края. Вначале формируется тусклое пятно, приобретающее со временем белую окраску.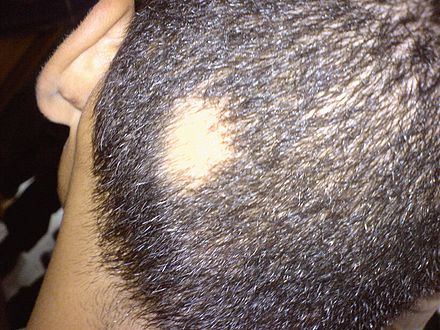 Ноготь в области побеления становится более мягким и хрупким, а впоследствии может разрушиться.
Ноготь в области побеления становится более мягким и хрупким, а впоследствии может разрушиться.
Микроспория волосистой части головы
Поражение волосистой части головы микроспорией встречается преимущественно у детей 5–12 лет. Принято считать, что редкость этой формы у взрослых объясняется наличием у них в волосах органических кислот, замедляющих рост гриба. Этот факт косвенно подтверждает самостоятельное выздоровление детей в период полового созревания, когда происходит изменение состава кожного сала. Интересно, что микроспория волосистой части головы практически не встречается у детей с рыжими волосами.
Очаги микроспории волосистой части головы располагаются главным образом на макушке, в теменной и височной областях. Обычно присутствуют 1–2 крупных очага величиной от 2 до 5 см, с округлыми или овальными очертаниями и четкими границами. По краю крупных очагов могут быть отсевы – мелкие очажки диаметром 0,5–1,5 см. В начале заболевания на месте заражения образуется участок шелушения. В первые дни гриб располагается только в устье волосяной луковицы. При ближайшем рассмотрении можно заметить беловатую кольцевидную чешуйку, окружающую волос наподобие манжетки. На 6–7-й день микроспория распространяется на сами волосы, которые становятся хрупкими, обламываются над уровнем окружающей кожи на 4–6 мм и выглядят как бы подстриженными (отсюда название “стригущий лишай”). Оставшиеся пеньки выглядят тусклыми, покрыты чехликом серовато-белого цвета, представляющим собой споры гриба. Если пеньки “погладить”, они отклоняются в одном направлении и в отличие от здоровых волос не восстанавливают свое первоначальное положение. Кожа в очаге поражения, как правило, слегка покрасневшая, отечна, поверхность ее покрыта серовато-белыми мелкими чешуйками.
Нагноительная форма
При нагноительной форме микроспории на фоне значительного воспаления, формируются мягкие узлы синюшно-красного цвета, поверхность которых покрыта гнойничками. При надавливании сквозь отверстия выделяется гной. Формированию нагноительной формы микроспории способствуют нерациональная (обычно местная) терапия, наличие серьезных сопутствующих заболеваний, позднее обращение к врачу.
Формированию нагноительной формы микроспории способствуют нерациональная (обычно местная) терапия, наличие серьезных сопутствующих заболеваний, позднее обращение к врачу.
Фото: микроспория гладкой кожи и волосистой части головы
Лечение микроспории гладкой кожи и микроспории волосистой части головы проводится только дерматологом в специализированном диспансере.
Профилактика
Профилактика микроспории заключается в своевременном выявлении, изоляции и лечении больных микроспорией. В детских учреждениях следует проводить периодические медицинские осмотры. Выявленного больного микроспорией ребенка необходимо изолировать от других детей и направить на лечение в специализированный стационар. Вещи, принадлежащие больному, подлежат дезинфекции.
Обязательно обследуются родственники и контактировавшие с больным лица. Особое внимание следует уделять домашним животным, поскольку именно они часто служат источником инфекции. Больные микроспорией животные либо уничтожаются, либо им проводится полноценное противогрибковое лечение.
Автор:
Копирование информации разрешено с указанием автора и источника
Микроспория собак
Микроспория (от греч. мikros – маленький и spora –семя, посев), микроспороз, стригущий лишай – заразная болезнь (микоз животных, вызываемая грибами рода Microsporum, характеризующаяся поражением кожи и ее производных. Болеет микроспорией и человек.
Этиология:
Основной возбудитель – М. сams (M.lanosum) – микроспорум. Поражающий кошек, собак , пушных зверей, кроликов, морских свинок, лошадей, овец, коз, свиней, оленей, обезьян, тигров. М. Gypseum (гипсовидный микроспорум) вызывает микроспорию у лошадей, собак, кошек, телят, морских свинок, крыс, мышей.
Источник возбудителя инфекции – больные животные, выделяющие его во внешнюю среду с пораженными волосами (шерстью) и чешуйками. Факторы передачи – предметы ухода, одежда, корма, подстилка, загрязненные шерстью больных животных. Основные носители микроспории – кошки, особенно бездомные.
Основные носители микроспории – кошки, особенно бездомные.
Локализация: кожа
Основные симптомы:
Микроспория животных протекает чаще всего в скрытой форме, выявляясь только при лиминесцентной диагностике. Под ультрафиолетовыми лучами пораженные микроспорией волосы дают изумрудно-зеленое свечение. В редких случаях визуально можно обнаружить на коже небольшие очаги с обломанными волосами и мелкими чешуйками. У собак и кошек очаги располагаются на голове, лапах и хвосте. Очаги округлой формы покрыты бело-сероватыми корками. Пораженные волоски легко выдергиваются.
Диагноз:
Устанавливают на основании эпизоотологических и клинических данных и результате люминесцентной диагностике микроспорических исследований. Микроспорию следует отличать от трихофитии, фавуса и чесотки.
Лечение:
Для лечения используют противогрибковые препараты.
Профилактика:
Вакцинация. Раннее выявление больных животных и их изоляция.
Микроспория человека:
Люди в основном заражаются от больных животных – кошек и собак. Болеют преимущественно дети. На коже появляются круглые или овальные красные пятна с ярким воспалительным ободком и шелушением в центральной части, на волосистой части головы – шелушащиеся участки округлых очертаний, на которых пораженные волосы коротко обламываются и приобретают беловато-серую окраску.
Современные особенности клиники и лечения МИКРОСПОРИИ | #04/01
Каковы источники и пути передачи микроспории?
Какова клиника типичной микроспории и ее атипичных форм?
Какова рациональная терапия микроспории?
Зооантропонозная микроспория — самое распространенное высококонтагиозное заболевание кожи и волос, общее для человека и животных. Для него характерно поражение жестких волос головы, верхней губы, подбородка, бровей, ресниц, лобка, половых губ, а также пушковых волос гладкой кожи.
Возбудителями микроспории являются зоофильные, антропофильные и геофильные грибы рода микроспорум. Из более чем 20 видов этого гриба наибольшее значение в патологии человека имеет зоофильный гриб — пушистый микроспорум. Это своеобразный гриб-космополит, практически единственный возбудитель микроспории в мире, за исключением стран Африки.
Микроспория преобладает в странах Европы, особенно в Средиземноморье, США и Южной Америке, Японии, Израиле, Кувейте, Катаре, Арабских Эмиратах [1, 3, 5, 7, 9].
Сегодня микроспория получила наибольшее распространение даже в регионах с традиционно высокой заболеваемостью трихофитией. Так, в Дагестане, Узбекистане, Таджикистане, Туркменистане, Башкортостане, Казахстане, Армении, где ранее наблюдались единичные случаи микроспории, сегодня она составляет до 83–99,7% всех грибковых заболеваний волос [3, 5].
В России заболеваемость микроспорией составляет около 71,6 на 100 тыс. населения. В Москве и Московской области на ее долю приходится 96,2% всех дермафитий с поражением волос [3].
Микроспорией в основном (до 65%) болеют дети, в том числе и новорожденные.
Основным источником заражения (80,5%) являются кошки, преимущественно бродячие. Особую опасность представляют кошки, живущие при лечебных учреждениях, поскольку они заражают отягощенных больных. Однако могут быть опасны и кошки, продаваемые на Птичьем рынке, вблизи Уголка Дурова, а также в зоомагазинах и специальных клубах, хотя они и снабжены специальными сертификатами, а некоторые из них даже вакцинированы. Мы были свидетелями того, как дорогостоящая, элитной породы кошечка, отличающаяся особенной красотой формы и окраса, стала источником заражения трех поколений в семье. Подаренная на день рождения внучке, она инфицировала ее дедушку и бабушку, саму виновницу торжества, а также ее родителей.
У большинства кошек, которые служат источником заражения, очаги микроспории определяются клинически в виде участков облысения на коже мордочки, вокруг рта и носа, на наружных поверхностях ушных раковин, передних и задних лапках, на хвосте. Кожа в очагах облысения представляется шелушащейся с наличием неравномерно обломанных волос, иногда наблюдается рост новых волос в центре таких очагов. Под лампой Вуда определяется характерное для микроспории зеленое свечение пораженных волос.
Кожа в очагах облысения представляется шелушащейся с наличием неравномерно обломанных волос, иногда наблюдается рост новых волос в центре таких очагов. Под лампой Вуда определяется характерное для микроспории зеленое свечение пораженных волос.
У другой группы кошек очаги могут быть не видны на глаз, но выявляются при люминесцентном обследовании. Наконец, примерно у 2–2,4% кошек очаги не видны на глаз, не выявляются под лампой Вуда, однако при посеве вычесанных у них волос можно получить культуру пушистого микроспорума.
Хотя одним из синонимов пушистого микроспорума является микроспорум канис (собачий), собаки в качестве источника заражения фигурируют лишь у 4% больных микроспорией.
К редким животным, которые болеют микроспорией и могут стать источником заражения людей, относят обезьян, тигров, львов, диких и домашних свиней (особенно поросят), лошадей, овец, серебристо-черных лисиц, кроликов, крыс, мышей, хомяков, морских свинок и других мелких грызунов, а также птиц — голубей, ворон, кур, на которых охотятся больные кошки. Животные инфицируются от самих кошек или от их шерсти, попавшей на растения, солому, зерно. Кроме того, пушистый микроспорум могут переносить на своих лапках домашние насекомые, в частности тараканы.
У 5,5% больных микроспорией источниками заражения становятся люди — родственники, друзья, соседи — при несоблюдении элементарных санитарно-гигиенических правил, а также сексуальные партнеры при локализации очагов микоза на наружных половых органах, лобке, животе, верней части бедер.
Бомжи и нищие, помимо педикулеза и чесотки, могут стать переносчиками и грибковых заболеваний.
Предметы обихода — коляска, оставляемая на ночь в подъезде и облюбованная кошками, игрушки, расчески, белье и т. д. становятся источником заражения у 2-2,5% больных микроспорией.
Рисунок 1. Микроспория гладкой кожи Микроспория гладкой кожи |
Заболеваемость микроспорией неодинакова в течение года и во многом зависит от появления у кошек, представляющих собой основной источник инфекции, котят, более подверженных инфицированию и заболеванию микроспорией. Хотя беременность у кошек продолжается семь недель и потомство появляется несколько раз в году, можно выделить два всплеска заболевания микроспорией у человека. Первый приходится на май-июнь и связан не только с рождением притягательных для детей котят, но и с большей свободой детей в летнее время, большим контактом их с животным миром при переезде в деревню, на дачу, в оздоровительные, спортивные и трудовые лагеря. Другой подъем заболеваемости наблюдается в сентябре — ноябре, когда дети возвращаются в город и тщательно осматриваются не только родителями, но и медработниками при поступлении их в школы, детские сады. При этом выявляются как свежие, так и стертые, прежде не распознанные формы микроспории [3].
| Рисунок 2. Диссеминированные очаги микроспории |
Инкубационный период при микроспории обычно составляет пять — семь дней. После него на гладкой коже, преимущественно на открытых участках лица, шеи, груди, верхних и нижних конечностей, появляются единичные (от одного до трех) округло-овальные эритематосквамозные пятна величиной 1–4 см в диаметре, четко очерченные периферическим валиком (рис. 1). Если же котенка греют под рубашкой, берут в постель, а первичные очаги микоза растирают при мытье мочалкой, возникают многоочаговые, диссеминированные варианты микроспории (рис. 2). Распространению и слиянию очагов микоза также способствует нерациональное лечение, в частности смазывание кортикостероидными кремами.
| Рисунок 3. Очаги микроспории с «пеньками» волос, окутанных чехликами |
Типичные очаги микроспории на голове располагаются обычно на макушке, в теменной и височных областях. Они выглядят как округло-овальные «плешинки» до 3–5 см в диаметре с четкими границами и «отсевами» вблизи них. Волосы в очагах тусклые, все обломаны на одном уровне, на высоте 4–6 мм, как бы подстрижены. Видимо, поэтому микроспорию в быту называют «стригущим лишаем». Поверхность очага микоза представляется шероховатой, шагреневой за счет выступающих «пеньков» волос, окутанных сероватыми или беловатыми чехликами (рис. 3). Под лампой Вуда пораженные волосы светятся ярким зеленым светом, напоминая только что скошенный луг.
Они выглядят как округло-овальные «плешинки» до 3–5 см в диаметре с четкими границами и «отсевами» вблизи них. Волосы в очагах тусклые, все обломаны на одном уровне, на высоте 4–6 мм, как бы подстрижены. Видимо, поэтому микроспорию в быту называют «стригущим лишаем». Поверхность очага микоза представляется шероховатой, шагреневой за счет выступающих «пеньков» волос, окутанных сероватыми или беловатыми чехликами (рис. 3). Под лампой Вуда пораженные волосы светятся ярким зеленым светом, напоминая только что скошенный луг.
Микроспория традиционно считается болезнью детского возраста. Однако в настоящее время этим микозом нередко болеют и взрослые. Сказываются, видимо, неблагоприятные социальные и экологические условия, рост нейроэндокринных заболеваний и иммунодефицитных состояний. Если в 1932 г. А. М. Ариевич наблюдал микроспорию у 6 взрослых на 6000 пациентов, то сейчас на долю взрослых приходится до 35% случаев заболевания. Женщины болеют в четыре раза чаще мужчин.
У детей микроспория, как правило, диагностируется своевременно, атипичные формы и ошибки в диагностике наблюдаются в 5% случаев, у взрослых этот показатель возрастает почти в четыре раза и составляет 19% случаев [3].
Из атипичных форм микроспории особого внимания заслуживают стертые, трихофитоидные разновидности. Они наблюдаются не так уж редко: у 8,5% больных, причем у взрослых в 2,5 раза чаще. Такая микроспория протекает незаметно, почти не беспокоит больных и не заставляет их сразу же обратиться к врачу. Ее нередко путают с себореидами, себорейным дерматитом, псориазом и другими заболеваниями, а неправильно подобранное лечение не приносит результатов. В связи с этим такие варианты микроспории приобретают хронический характер, становясь причиной дальнейшей дессиминации микоза у самого заболевшего и его распространения в окружающей среде. Зафиксирована продолжительность трихофитоидной микроспории от семи месяцев до двух лет.
Такие формы микроспории обычно характерны для отягощенных больных (туберкулез, болезнь Шегрена, пеллагроидный дерматит и др.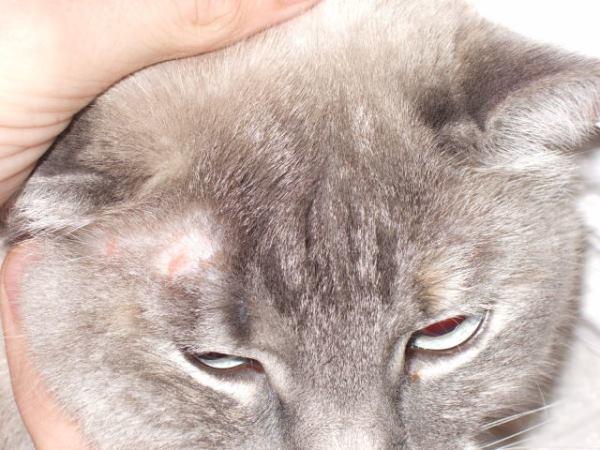 ). Клинически они проявляются диффузным или очаговым шелушением, разреженностью волос или формированием участков очаговой алопеции. Волосы в очагах тусклые, без чехликов, обломаны по-разному — на уровне кожи и на высоте 10–15 мм. Участки алопеции то очень мелкие, с булавочную головку, то гигантские, полициклических очертаний при слиянии.
). Клинически они проявляются диффузным или очаговым шелушением, разреженностью волос или формированием участков очаговой алопеции. Волосы в очагах тусклые, без чехликов, обломаны по-разному — на уровне кожи и на высоте 10–15 мм. Участки алопеции то очень мелкие, с булавочную головку, то гигантские, полициклических очертаний при слиянии.
На гладкой коже очаги микроспории представляются маловоспалительными, слегка шелушащимися или депигментированными округло-овальными пятнами. При их слиянии могут возникнуть полициклические очаги микоза, размытые, расплывчатые, без четких границ, слегка зудящие. У одной из наших больных, 69-летней любительницы кошек, трихофитоидная микроспория волосистой кожи головы не была диагностирована два года. В прошлом она перенесла туберкулезный лимфаденит и мезоденит, длительно (в течение 10 лет) принимала поддерживающие дозы преднизолона по поводу синдрома Шагрена. Микроспория проявлялась у нее шелушением волосистой кожи головы, выпадением волос, преимущественно в затылочной области, зудом. Все явления усиливались в теплое время года и стихали в холодное. Заболевание длительно и безуспешно лечили средствами, применяемыми при себорейном дерматите или псориазе. Диагностировать микроспорию помогло появление свежих типичных очагов микоза на коже лица и шеи. Кода больную побрили, то оказалось, что в патологический процесс вовлечена практически вся волосистая кожа головы. Со всех очагов микоза на голове, лице, шее, а также со сквамозно-кератотических высыпаний на коже ладоней была получена идентичная культура пушистого микроспорума.
Иногда необычный источник заражения также вводит врача в заблуждение, и микроспория может не диагностироваться даже у детей, что приводит к трихофитоидной форме. Так, восьмилетняя девочка заболела после недельного контакта с больным голубем, которого они с отцом отбили у кошки, видимо больной этим микозом. Выхаживая голубя, девочка брала его на руки, пеленала, кормила. На макушке у ребенка появилось четко очерченное пятно, покрытое серебристыми чешуйками. Волосы в очаге не были обломаны, субъективные ощущения отсутствовали.
Волосы в очаге не были обломаны, субъективные ощущения отсутствовали.
У девочки диагностировали псориаз, лечение проводили дипросаликом и дитрастиком. За это время кожный процесс распространился на всю волосистую кожу головы, осложнился фолликулитами и перифолликулитами. Изменения расценили как осложнение псориаза вторичной пиококковой флорой, и терапию дополнили антибиотиком — геоксизоном и фукарцином. Состояние ребенка все ухудшалось. Волосы выпадали в большом количестве, при их расчесывании девочка испытывала боль. С предположительным диагнозом «дискоидная красная волчанка» пациентка была направлена в ЦНИКВИ.
При детальном осмотре определилось диффузное шелушение всей кожи головы, разреженность волос, атрофические плешинки, которых было особенно много в теменно-затылочной области. Местами шелушение было незначительным, но хорошо определялись участки рубцовой атрофии различной величины и формы, без четких границ, почти без воспалительных явлений. Вблизи рубцово измененной кожи волосы легко выпадали, были тусклыми, истонченными, скрученными, неравномерно преломляли свет. Длина волос сохранялась или они обламывались то на уровне кожи, то на высоте 10–15 мм. Поскабливание кожи в очагах было болезненным. По снятии чешуйко-корочек кожа представлялась влажной и воспаленной. После бритья и мытья оказалось, что вся поверхность головы покрыта множественными очагами поражения (более 60), некоторые из них были величиной с чечевичное зерно, другие составляли 2-3 см в диаметре, были также гигантские площадки 8х12 см. Определялись увеличенные и болезненные заднешейные и околоушные лимфатические узлы. Микроскопически выявлены скопления мелких спор на поверхности пораженных волос. Под лампой Вуда определялось не совсем характерное серовато-беловатое свечение. Однако на питательной среде получена типичная культура пушистого микроспорума. Таким образом, поздняя диагностика и неадекватное лечение привели к тому, что очаг поверхностной микроспории, обычно проходящей без каких-либо последствий, осложнился диссеминацией грибкового процесса по всей волосистой коже головы, формированием участков рубцовой атрофии и очаговой алопеции, лимфаденитами.
Быть может, еще большего внимания и настороженности заслуживают глубокие — инфильтративно-нагноительные, керионподобные или гранулематозные варианты микроспории с ярко выраженной симптоматикой. Они регистрируются у 4,5–6,5% больных этим микозом. Для них характерны тяжелое течение, болезненность, подъемы температуры и другие симптомы интоксикации. Течение заболевания осложняется лимфаденитами и аллергическими высыпаниями, быстрым исходом в рубцовую атрофию и необратимую очаговую алопецию.
Как правило, глубокие формы микроспории возникают у ослабленных детей или взрослых, преимущественно у женщин с эндокринной или иммунной патологией (дисфункция половых и щитовидной желез, гипофизарный нанизм, лимфогранулематоз, болезни крови). Иногда поверхностные варианты микроспории трансформируются в инфильтративно-нагноительные под влиянием неадекватного лечения, а также повторяющихся травм, в том числе мочалкой во время мытья, походов в парные. Способствуют этому частые морские купания, а главное, постоянное пребывание во влажном, тесно прилегающем купальном костюме.
У взрослых очаги глубокой микроспории обычно выявляются на коже голеней или лобка и половых губ, у детей — на волосистой коже головы.
Керионподобные очаги микоза представляются крупными, сливными, занимающими обширные участки волосистой кожи головы либо всю область лобка и наружных половых губ. Это обычно конгломерат из слившихся и нагноившихся болезненных фолликулитов, перифолликулитов и абсцедирующих элементов. Из-за отека, инфильтрации и импетигинизации очаги микроспории возвышаются над уровнем кожи. Их поверхность покрыта грубыми гнойными корками со склеенными в них расшатанными и частично расплавленными волосами. По удалении корок и волос из зияющих отверстий волосяных фолликулов как мед из сот (керион-медовая сота) выделяется сливкообразный гной. Регионарные лимфоузлы увеличены и болезненны. Для таких больных характерны выраженные симптомы интоксикации, аллергические высыпания вплоть до узловатой эритемы голеней. Нередко подобные формы микроспории ошибочно принимаются за язвенно-вегетирующую пиодермию, инфильтративно-нагноительную трихофитию, псориаз, осложненный пиодермией.
Нередко подобные формы микроспории ошибочно принимаются за язвенно-вегетирующую пиодермию, инфильтративно-нагноительную трихофитию, псориаз, осложненный пиодермией.
У молодых девушек с гипертрихозом возможно возникновение глубокой микроспории голеней, обычно принимаемой за васкулит, гранулему Майокки, ретикулез. В этих случаях сравнительно мелкие (2-3 см в диаметре), глубокие, единичные, фолликулярно-узловатые очаги располагаются на голени в виде кольца.
Приводим достаточно характерную историю формирования инфильтративно-нагноительной микроспории у семилетнего мальчика. Все началось с появления обычного для этого микоза небольшого круглого очага облысения в левой теменной области. Волосы в нем были характерно обломаны. Однако родители связали появление данного очага не с контактом с котенком, а с падением с велосипеда, поверхностной ссадиной и ее загрязнением, тем более что оба события совпали по времени. Очаг рассматривался в связи с этим как пиодермический. Лечение кортикостероидными кремами и антибактериальными средствами спровоцировало распространение грибкового процесса на всю левую половину головы. Из-за отека, инфильтрации, нагноения, увеличения шейных и предушно-заушных лимфоузлов голова и лицо казались асимметричными. Поверхность кожи в очаге микоза была покрыта грубыми гнойными и гнойно-кровянистыми корками со склеенными в них и разреженными волосами. При малейшем движении головой и шеей ребенок испытывал сильную боль. Мальчик был вялым, апатичным, бледным, периодически наблюдались подъемы температуры. Наряду с вышеописанным атипичным очагом микоза на голове появились характерные мелкие очаги микоза в области левой брови, на лбу и виске. В них при люминесцентном обследовании выявлено типичное зеленое свечение. Диагноз подтвержден микроскопически и выделением из всех очагов микоза идентичной культуры пушистого микроспорума.
К атипичной по локализации и течению можно отнести инфильтративно-нагноительную микроспорию кожи лобка и половых губ. Такая форма микроспории нередко (по нашим данным, в двух из пяти случаев) приводит к инфицированию сексуальных партнеров. Ввиду атипичности локализации и течения такая форма микроспории не сразу диагностируется. Ошибочное и неадекватное лечение делает клинические проявления еще более нехарактерными.
Такая форма микроспории нередко (по нашим данным, в двух из пяти случаев) приводит к инфицированию сексуальных партнеров. Ввиду атипичности локализации и течения такая форма микроспории не сразу диагностируется. Ошибочное и неадекватное лечение делает клинические проявления еще более нехарактерными.
В настоящее время локализация очагов микроспории на коже лобка и половых губ увеличилась по сравнению с 1976 годом более чем в десять раз. Особенности анатомического строения данной области, изобилующей кровеносными сосудами и нервными окончаниями, способствует быстрому формированию глубоких инвазивных, чрезвычайно болезненных инфильтратов, появлению осложнений в виде лимфаденитов и аллергических высыпаний, возникновению симптомов интоксикации из-за всасывания лизированных тканей, бактерий, грибов и продуктов их жизнедеятельности.
Приводим более подробно истории болезней двух женщин, одна из которых инфицировала сексуального партнера, другая сама была инфицирована при сексуальном контакте.
| Рисунок 4. Инфильтративно-нагноительная микроспория у 18-летней больной. «Отсевы» на коже живота и бедер |
У 18-летней женщины микроспория не была диагностирована в течение четырех месяцев. Заразилась она от своего больного микроспорией племянника, использовав для мытья его мочалку. Поверхностный очаг микроспории на коже паховой складки разрешился после недельного смазывания 2%-ным раствором йода. Больная считала эпизод исчерпанным. Поэтому, когда спустя полтора месяца на коже лобка появились поверхностные шелушащиеся очаги, она никак не связала их с недолеченной микроспорией. Смазывания кортикостероидными кремами (подозрение на аллергические высыпания), частые морские купания (больная в это время находилась на море) и почти постоянное пребывание в тесно облегающем бикини привели к распространению патологического процесса как по поверхности, так и в глубину. Сформировались фолликулиты, перифолликулиты, абсцедирующие элементы, слившиеся в единый, возвышающийся над поверхностью кожи конгломерат. Появились «отсевы» на передней поверхности обоих бедер и коже нижней части живота (рис. 4). Поверхность очагов микоза покрылась грубыми гнойными и гнойно-кровянистыми корками. Увеличились и стали болезненными паховые лимфоузлы. На симметричных участках обеих голеней появились болезненные подкожные узлы. Заболевание было расценено как глубокая язвенно-вегетирующая пиодермия, осложненная узловатой эритемой голеней. Больную безуспешно лечили оксациллином, кефзолом, вибрамицином в комбинации с короткими курсами преднизолона. Болезненность, симптомы интоксикации только нарастали. Диагностировать микроспорию помогло появление типичного очага микоза на коже живота у сексуального партнера больной. После детального обследования женщины, как предполагаемого источника микроспории, была диагностирована ее инфильтративно-нагноительная форма. Клинический диагноз был подтвержден микроскопически, люминесцентно и культурально.
Сформировались фолликулиты, перифолликулиты, абсцедирующие элементы, слившиеся в единый, возвышающийся над поверхностью кожи конгломерат. Появились «отсевы» на передней поверхности обоих бедер и коже нижней части живота (рис. 4). Поверхность очагов микоза покрылась грубыми гнойными и гнойно-кровянистыми корками. Увеличились и стали болезненными паховые лимфоузлы. На симметричных участках обеих голеней появились болезненные подкожные узлы. Заболевание было расценено как глубокая язвенно-вегетирующая пиодермия, осложненная узловатой эритемой голеней. Больную безуспешно лечили оксациллином, кефзолом, вибрамицином в комбинации с короткими курсами преднизолона. Болезненность, симптомы интоксикации только нарастали. Диагностировать микроспорию помогло появление типичного очага микоза на коже живота у сексуального партнера больной. После детального обследования женщины, как предполагаемого источника микроспории, была диагностирована ее инфильтративно-нагноительная форма. Клинический диагноз был подтвержден микроскопически, люминесцентно и культурально.
Похожая история заболевания была у больной 25 лет, которая заразилась от больного микроспорией. Через неделю после сексуального контакта над лобком появилось яркое зудящее пятно, быстро покрывшееся чешуйко-корочками. Больная в это время лечилась от уреоплазмоза, и пятно было расценено как аллергическое. Под влиянием короткой терапии кремом тридерм пятно побледнело и стало практически незаметным. Через месяц после этого эпизода во время пребывания на море на коже лобка появились поверхностные шелушащиеся высыпания, слившиеся в обширный очаг фигурных очертаний. Решив, что это аллергические высыпания, больная использовала крем лоринден и 2%-ный салициловый спирт. Для удобства смазывания больная сбрила волосы на лобке. Это спровоцировало распространение процесса в глубину. Образовался чрезвычайно болезненный инфильтрат из глубоких фолликулярно-узловатых элементов. Диагностирована глубокая пиодермия. Применяли перорально цифран и вильпрофен, наружно фукарцин и линкомициновую пасту. Однако болезненность, инфильтрация и импетигинизация только нарастали. Для уточнения диагноза по прошествии двух месяцев от начала заболевания больная была направлена в ЦНИКВИ.
Однако болезненность, инфильтрация и импетигинизация только нарастали. Для уточнения диагноза по прошествии двух месяцев от начала заболевания больная была направлена в ЦНИКВИ.
| Рисунок 5. Обширный возвышающийся очаг инфильтративно-нагноительной микроспории у 25-летней больной. Увеличение паховых лимфоузлов |
На лобке, занимая всю его центральную часть, переходя на кожу наружных половых губ и скручиваясь жгутами в верхней и боковой частях, располагался обширный инфильтрат, возвышающийся на 1-2 см над уровнем кожи. Его контуры были подчеркнуты ярким периферическим валиком. Кожа над очагом микоза была синюшно-коричневого цвета, напряженная, растянутая, с бугристой поверхностью (рис. 5). Прикосновение к очагу оказалось необычайно болезненным. Волосы на лобке полностью сохраняли свою длину, привычный для микроспории чехлик не определялся. Центральная часть очага поражения практически была лишена волос. Оставшиеся волосы эпилировались с трудом, эпиляция сопровождалась выраженной болезненностью. Паховые лимфоузлы оказались увеличены и болезненны. На тыльной стороне обеих кистей имелись папуло-везикулезные микроспориды. При люминесцентном обследовании очага микоза на лобке и половых губах обнаруживалось характерное зеленое свечение. Микроскопически выявлялись мелкие споры, располагавшиеся на волосе и внутри него. На питательной среде получена типичная культура пушистого микроспорума.
Лечение больных микроспорией представляется важной, социально значимой проблемой.
От этого заболевания обычно страдают не только дети, но и их родители. Из-за высокой контагиозности микоза детям запрещается посещение детских садов и школ. Они пропускают школьные занятия, оказываются на долгое время оторванными от детского коллектива. Родители вынуждены прерывать работу, брать больничные листы по уходу. Таким образом, семье наносится ощутимый моральный и материальный ущерб.
Таким образом, семье наносится ощутимый моральный и материальный ущерб.
Скорейшее выздоровление больных микроспорией достигается при своевременном распознавании микоза и адекватном лечении. Оно включает сочетанное применение системных и наружных противогрибковых средств вкупе с патогенетическими препаратами. Последние повышают эффективность лечения и снижают частоту и выраженность побочных реакций и осложнений.
У больных микроспорией используют два системных антимикотика: антибиотик гризеофульвин и ламизил. Причем антимикотики применяют у больных микроспорией в высоких дозах. Дело в том, что возбудитель микоспории отличается самой высокой устойчивостью по сравнению с другими грибами-дерматофитами. Например, суточная доза гризеофульвина, равная у больных руброфитией 16 мг/кг, трихофитией — 18 мг/кг, при микоспории должна быть увеличена до 22 мг/кг. Высокая устойчивость спор пушистого микроспорума обусловлена наличием у них очень плотной шестислойной оболочки, усиленной продольными и циркулярными реберными выступами [11].
Гризеофульвин — хлорсодержащий антибиотик, продукт биосинтеза плесневых грибов рода пенициллиум. Поэтому при приеме гризеофульвина и одновременном лечении антибиотиками пенициллинового ряда очень часто возникают кожно-слизистые аллергические осложнения. Суточная доза гризеофульвина, которая подбирается из расчета 22 мг на килограмм веса, делится на три-четыре равные части и принимается с одной чайной ложкой растительного масла. Масло стимулирует эвакуацию желчи и способствует растворению гризеофульвина. Кроме того, благодаря наличию в нем витамина Е (a-токоферола) замедляется метаболизм гризеофульвина и увеличивается длительность действия препарата. Гризеофульвин лучше усваивается в кислой среде, поэтому целесообразно запивать его каким-нибудь кислым соком (брусничным, клюквенным, лимонным, яблочным и др.).
Для снижения гепатотоксичности гризеофульвина его рекомендуется принимать с гепатопротекторами — печеночными сборами, лив-52, карсилом, силибором и др.
Учитывая худшую всасываемость гризеофульвина при наличии гельминтов, до или во время гризеофульвинотерапии показана дегильминтация [8]. Для этого назначаются различные антигельминтные препараты, например декарис (левамизол), который освобождает от гельминтов и в то же время обладает иммуномодулирующими свойствами. Гризеофульвин несколько усиливает иммунодефицитные состояния, на фоне которых, как правило, возникает микроспория. Левамизол нивелирует иммуносупрессивное действие гризеофульвина. Во время гризеофульвинотерапии обычно обостряются очаги фокальной инфекции, которые становятся источниками суперинфицирования очагов микоза, поэтому показана их санация.
Курс непрерывного лечения гризеофульвином продолжается 1,5-2 месяца. Вначале его применяют ежедневно до того, как будут получены два отрицательных анализа на грибы с интервалом в семь дней; затем антибиотик применяют две недели через день и еще две недели два раза в неделю. По окончании терапии проводится контрольное клинико-лабораторное обследование, и в случае отрицательных результатов больной считается излеченным. Хотя гризеофульвин является достаточно щадящим препаратом, он все же обладает гепато-, нефро- и нейротоксичностью, фотосенсибилизирующими, эмбриотоксическими и коканцерогенными свойствами.
Гризеофульвин противопоказан при гепатитах, перенесенных не более года тому назад и проявляющихся субъективными ощущениями и/или повышенным уровнем билирубина и печеночных ферментов; язвенной болезни желудка и двенадцатиперстной кишки; заболеваниях почек; невритах, особенно зрительных и слуховых нервов; злокачественных и быстрорастущих доброкачественных опухолях; болезнях крови; фотодерматозах и близких к ним состояниях; нарушении мозгового кровообращения; маточных и других кровотечениях.
Следует учитывать, что адекватная доза гризеофульвина у больных микроспорией не должна превышать предельно допустимую — 1,0 г (8 таблеток). В противном случае проявляются токсико-аллергические свойства антибиотика.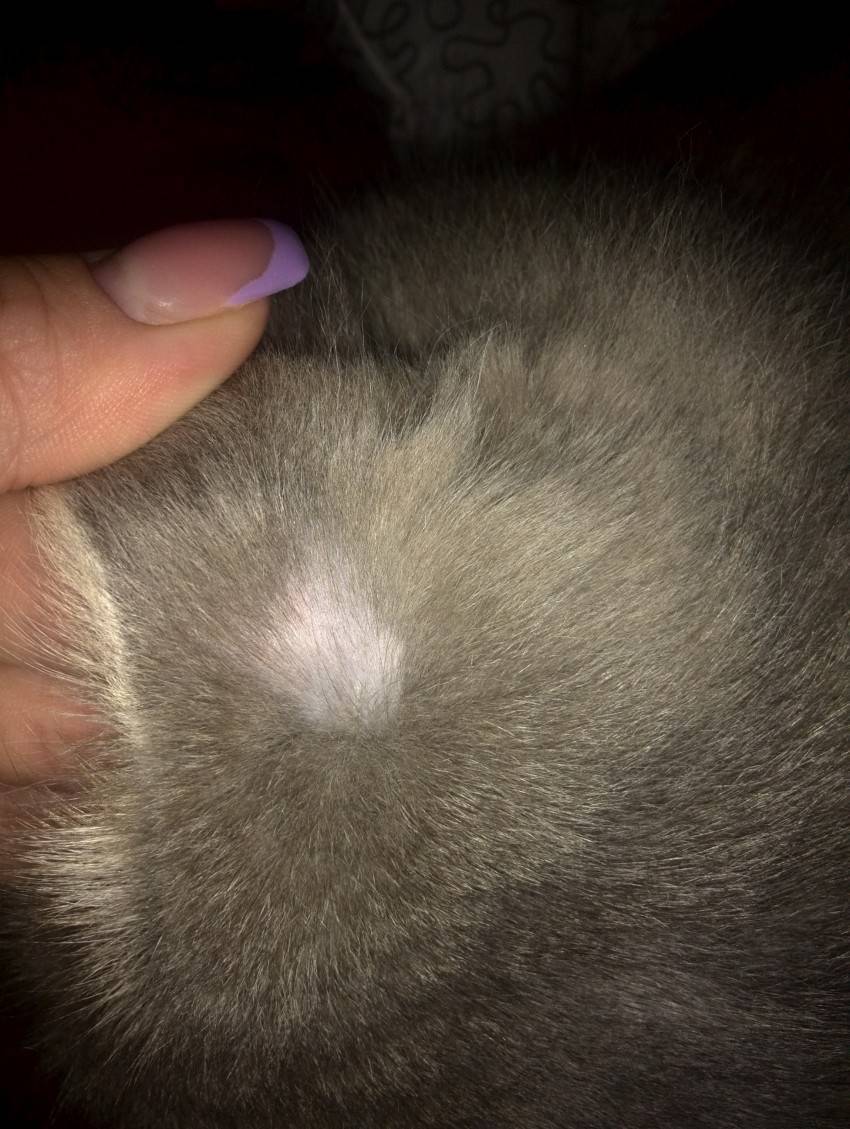 У взрослых и крупных детей с массой тела более 60 кг назначение адекватной дозы препарата практически не представляется возможным.
У взрослых и крупных детей с массой тела более 60 кг назначение адекватной дозы препарата практически не представляется возможным.
Достойной альтернативой гризеофульвину является тербинафин (торговое название ламизил) фирмы «Новартис».
Препарат обладает высокой активностью в отношении различных видов грибов. Особенно же он активен в отношении грибов-дерматофитов, возбудителей самых распространенных дерматофитий: руброфитии — у взрослых и микроспории — у детей.
Ламизил подавляет чрезвычайно чувствительную именно у грибов (в 10 тыс. раз чувствительнее, чем у человека) скваленовую эпоксидазу. В результате на самых ранних этапах (на уровне скваленового эпоксидазного цикла) блокируется формирование эргостерола — основного компонента цитоплазматических мембран грибковой клетки. Не получая этого строительного материала, грибковая клетка становится ущербной, не может расти и развиваться, а только выживает. Таким образом проявляется фунгистатическое действие ламизила. Однако преобладающим у этого антимикотика является фунгицидное действие. Оно напрямую зависит от накопления в клетке скваленов, исключенных из цикла дальнейших превращений в эргостерол. Эти активные высокомолекулярные углеводороды накапливаются в грибковой клетке. Причем объем скваленовых гранул постепенно увеличивается, т. к. они активно экстрагируют липиды из клеточных мембран. В конце концов клеточная мембрана с нарушенной структурой не выдерживает, разрывается, приводя к гибели клетки [6, 7].
Ламизил не требует каких-то определенных условий приема, быстро всасывается в желудочно-кишечном тракте. Его уровень в крови стабилен. Препарат практически не взаимодействует с различными медикаментозными средствами, а также ферментными системами, включая цитохром Р-450. Его действие избирательно и направлено в основном на грибковую клетку. В кожу и ее придатки ламизил поступает путем простой диффузии, а также экскреции сальными железами.
К особенностям распространения ламизила благодаря липофильности и связи с хиломикронами относится его лимфатический транспорт. По лимфатическим сосудам ламизил непосредственно достигает инфильтративно-нагноительных и абсцедирующих очагов микоза с лимфаденитами и лимфангитами. В связи с этим наблюдается наибольшая активность ламизила у больных тяжелыми осложненными инфильтративно-нагноительными формами дерматофитий с поражением волос. По данным М. Цой и М. Д. Алаевой (1996), при поверхностной трихофитии ламизил ускорял процесс выздоровления на 3,3 дня, при инфильтративной — на 6,3 дня, при нагноительной — на 8,2 дня по сравнению с терапией гризеофульвином [10].
По лимфатическим сосудам ламизил непосредственно достигает инфильтративно-нагноительных и абсцедирующих очагов микоза с лимфаденитами и лимфангитами. В связи с этим наблюдается наибольшая активность ламизила у больных тяжелыми осложненными инфильтративно-нагноительными формами дерматофитий с поражением волос. По данным М. Цой и М. Д. Алаевой (1996), при поверхностной трихофитии ламизил ускорял процесс выздоровления на 3,3 дня, при инфильтративной — на 6,3 дня, при нагноительной — на 8,2 дня по сравнению с терапией гризеофульвином [10].
Быстрое разрешение осложненных форм дерматофитий при терапии ламизилом связано, таким образом, с его высокой противогрибковой активностью, лимфатическим транспортом, выраженными антибактериальными свойствами, сравнимыми с действием гентамицина, а также противовоспалительным действием. Последнее обусловлено подавлением пероксидазной активности гидроксильных радикалов полиненасыщенных жирных кислот.
Выше мы уже отмечали высокую устойчивость пушистого микроспорума к антимикотикам. В связи с этим Н. С. Потекаев и соавт. (1997) наблюдали излечение больных микроспорией детей с поражением длинных и пушковых волос, которым назначался ламизил по 94 мг в сутки при массе тела до 20 кг и 186 мг в сутки при массе тела от 20 до 40 кг, что на 50% превышает дозу, предлагаемую в аннотации к препарату [4].
У взрослых, больных осложненными формами микроспории, мы с успехом проводили короткие, но насыщенные курсы терапии ламизилом. Препарат назначали в суточной дозе 7 мг/кг или по две таблетки (500 мг) в день. В ближайшие три-четыре недели мы наблюдали полное разрешение очагов микроспории у всех без исключения больных. Начинали отрастать здоровые волосы там, где не развилась рубцовая атрофия, попутно разрешались микроспориды, включая очаги узловатой эритемы голеней, становились безболезненными и уменьшались в размерах регионарные лимфоузлы. Ни в одном случае не отмечено каких-либо побочных явлений, а также отклонений в биохимическом статусе [6].
Хочется еще отметить лучшую переносимость ламизила по сравнению с его аналогом — экзифином фирмы «Д-р Редди’с». Одна из наших больных стала по собственной инициативе принимать вместо ламизила более дешевый экзифин. По прошествии четырех-пяти дней приема экзифина в суточной дозе 500 мг у нее на внутренней поверхности обеих предплечий появились зудящие папуло-везикулезные аллергиды. Они разрешились после использования адсорбентов и антигистаминных средств. После возобновления терапии ламизилом в суточной дозе 500 мг аллергиды не появились.
И еще один момент: в семье одной из наших больных все, кроме нее, переболели респираторными инфекциями. Мы связали ее устойчивость с повышением защитных сил организма в результате приема ламизила. Известно, что ламизил не действует отрицательно на метаболическую активность лейкоцитов, хемотаксис, фагоцитоз. Более того, под влиянием терапии ламизилом улучшаются показатели клеточно-опосредованного иммунитета, что связывают с высвобождением большого количества антигенного материала в результате гибели грибковых клеток [12].
Эффективность лечения больных микроспорией повышается при одновременном применении системных антимикотиков и наружных средств. Наряду с эпиляцией и еженедельным бритьем волос применяют 2%-ную настойку йода, которой смазывают очаги микоза по утрам. Вечерами в них втирают отечественные противогрибковые мази: серно-салициловую, серную, серно-дегтярную, бифосин. Такое йодно-мазевое лечение отличается высокой эффективностью при дешевизне и доступности.
При сравнительно спокойных очагах микроспории их целесообразно смазывать один раз в день 10%-ным салицилово-хинозоловым димексидом, который достаточно быстро приводит к разрешению очагов микоза на волосистой коже головы.
При инфильтративно-нагноительной микроспории для освобождения очагов микоза от корок и гноя применяют компрессные повязки с 10-20%-ными растворами ихтиола, 5%-ным раствором мумие в димексиде, 50%-ным раствором корня солодки, а также примочки с 0,5-1%-ными растворами хлоргиксидина биглюконата (гибитана) или ультразвуковые орошения 0,5%-ным раствором этого препарата с помощью аппарата «Росса» [2, 5].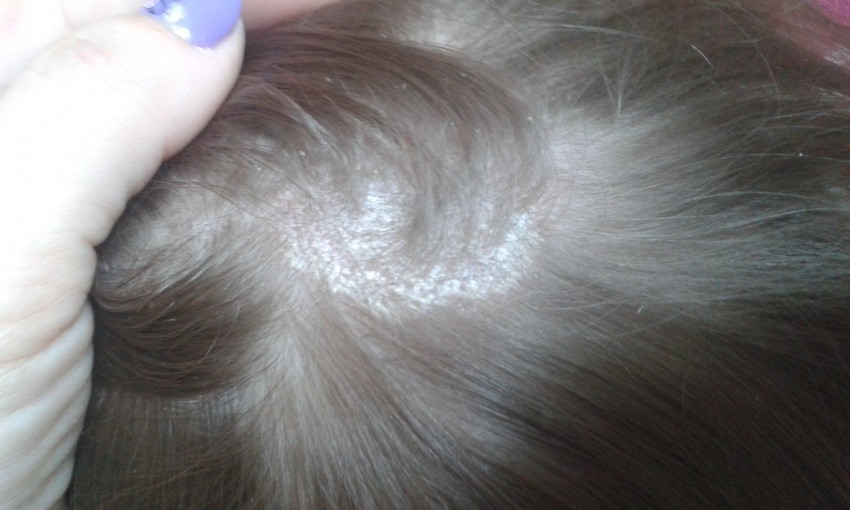
В качестве наружных антимикотиков можно воспользоваться эффективными зарубежными азольными и аллиламиновыми соединениями. Среди них мы отдаем предпочтение 1%-ному ламизиловому крему, 1%-ному крему микоспор и 1%-ному крему травоген. Указанные препараты, как правило, хорошо переносятся, т. к. обладают противовоспалительными свойствами. При островоспалительных явлениях не требуется их комбинация с кортикостероидными средствами. В то же время они обладают выраженной противогрибковой активностью, а ламизиловый крем — еще и антибактериальным действием, что важно для санации очагов микроспории, осложненных вторичной пиококковой флорой.
Включение наружных противогрибковых средств в комплекс лечебных мероприятий у больных микроспорией позволяет достичь быстрого выздоровления при наименьшей курсовой дозе дорогостоящих и небезразличных для организма системных антимикотиков.
Литература
1. Ахметова А. К. Клинико-иммунологическая характеристика микроспории и трихофитии: Автореф. дис… канд. мед. наук. Алматы, 1994. 25 с.
2. Бивалькевич В. Г., Леонов Д. А. // Тез. докл. научн-практ. конф. дерм-венерол. Урала, Сибири и Дальнего Востока. Екатеринбург, 1995. 16 с.
3. Мохамад Юсуф. Клинико-эпидемиологические особенности микроспории в современных условиях и разработка лечения новыми медикаментозными средствами: Автореф. дис. канд. мед. наук. М., 1996. 18 с.
4. Потекаев Н. С. Кудрина М. И., Потекаев Н. Н. // Вестн. дерматол., 1997, № 5. С. 69.
5. Рейимкулыев Б. Р. Эпидемиология зооантропонозных дерматофитий в Туркменистане. Влияние климато-географических особенностей и организация социальной медицинской помощи: Автореф. дис… докт. мед. наук. М., 1997. 25 с.
6. Рукавишникова В. М. Микозы стоп. М: МСД, 1999. 317 с.
7. Суворова К. Н. Куклин В. Т., Рукавишникова В. М. Детская дерматовенерология: Рук-во для врачей-курсантов последипломного образования. Казань, 1996. 441 с.
441 с.
8. Умаханов А. Х. Клиническое течение и эффективность специфической терапии дерматофитий волосистой кожи головы у детей с сопутствующими гельминтами: Автореф. дис… канд. мед. наук М., 1999. 27 с.
9. Фахретдинова Х. С. Клинико-эпидемиологические особенности современной микроскопии: Автореф. дис… докт. мед. наук М., 1999. 27 с.
10. Цой М. Р., Алаева М. Д. // Тез. докл. VII Росс. съезда дерматологов и венерологов. Казань, 1996. Ч. 2. С. 96.
11. Шадыев Х. К. Ультраструктура Microsporum canis и ее изменения под влиянием гризеофульвина: Автореф. дис… канд. мед. наук. М., 1976. 17 с.
12. Birnbaum J, Cooper K., Elewsky B. // 5 th Internet. Summit of cutan antifungal therapy. Singapore, 1998. № 33.
Микроспория у детей — как долго ее надо лечить и в чем заключается профилактика этого заболевания
Микроспория — заболевание, вызываемое микроскопическими грибками, которые размножаются в поверхностных слоях кожи. Болезни кожных покровов, вызванные патогенными грибами, называют “дерматомикозами”.По распространенности микроспория уступает только грибковым поражениям стоп, а у детей она занимает первое место среди всех микозов. В первую
очередь ею страдают дети дошкольного и младшего школьного возраста, взрослые практически не болеют, за исключением молодых женщин. Это связано с тем, что кожа взрослых выделяет ряд органических кислот, которые подавляют развитие патогенных грибков. По этой причине в период полового созревания часто происходит самоизлечение от микроспории.Основными клиническими проявлениями этого заболевания являются очаговые поражения кожи и волосистой части головы. Волосы обламываются на уровне 4—8 мм над кожей и выглядят сероватыми, как бы припудренными, на каждом волоске виден беловатый “чехол”. Место поражения на коже представляет собой красноватое пятно с неровными, но довольно четкими краями. Вокруг пораженного участка образуется возвышающийся валик из мелких узелков.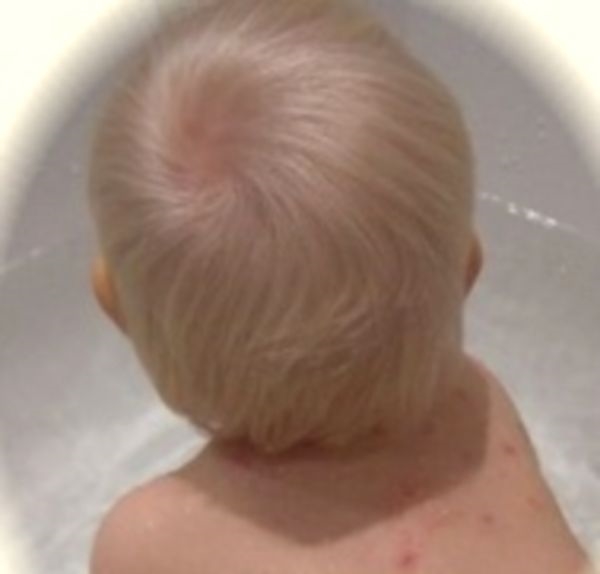 Пятно постепенно увеличивается в размерах и может принимать причудливые формы, к примеру, в виде кольца в кольце. Очагов поражения, как правило, не более трех-четырех, но могут быть и множественные, их размер обычно не превышает 3—4 см. Чаще сыпь локализуется на предплечьях, коже лица и шеи, иногда страдают другие участки тела.
Пятно постепенно увеличивается в размерах и может принимать причудливые формы, к примеру, в виде кольца в кольце. Очагов поражения, как правило, не более трех-четырех, но могут быть и множественные, их размер обычно не превышает 3—4 см. Чаще сыпь локализуется на предплечьях, коже лица и шеи, иногда страдают другие участки тела.
Диагностикой и лечением этой болезни занимаются дерматологи. Обычно постановка диагноза не вызывает затруднения, однако существуют и атипичные формы, отличающиеся от классической клинической картины. Особая сложность в поставке диагноза может быть у детей, страдающих аллергическими реакциями, в частности, атопическим дерматитом. В этом случае микроспория маскируется под проявлением основного процесса и не всегда своевременно диагностируется, а используемые для лечения дерматита
гормональные мази только способствуют распространению микоза. Для постановки точного диагноза необходимы микробиологические исследования (микроскопия и посев на специальные среды). Существует и экспресс-метод — использование лампы “черного света” (лампы Вуда). Это люминесцентная лампа, стекло которой практически не пропускает видимый спектр лучей, только ультрафиолет. Пораженные участки в ее лучах светятся ярко-зеленым светом. Подобные устройства применяются не только в дерматологии, но и в криминалистике — для выявления следов биологических жидкостей и проверки подлинности документов.При лечении микроспории используют наружные противогрибковые препараты, а при поражении волосистой части головы обязательно назначаются специальные антибиотики для приема внутрь в таблетках или суспензиях. После двухнедельного курса проводят повторное микробиологическое исследование, при отрицательном результате анализа лечение продолжают, однако врач меняет схему лечения этим же препаратом. Общий курс лечения составляет полтора-два месяца, прерывать его нельзя ни в коем случае. Каждые две недели требуется лабораторный контроль. В ходе лечения необходимо еженедельно сбривать волосы и регулярно мыть голову.
Поскольку основным источником этого заболевания являются молодые животные (котята, щенки), прежде всего бездомные, необходимо ограничить контакт детей с ними. Но и домашний питомец может заразиться микроспорией, если он находится на улице без присмотра. Представляет опасность и любой человек с этим заболеванием, поэтому обязательно обследуются все родственники и контактировавшие с больным люди. Основа профилактики — правила личной гигиены: нельзя пользоваться чужими расческами и головными уборами.
Юрий Кузьменков, врач РНПЦ “Кардиология”.
Сфера интересов доктора — терапия, кардиология, эндокринология.
Ждем ваших вопросов, друзья!
Заметили ошибку? Пожалуйста, выделите её и нажмите Ctrl+Enter
Микроспория или стригущий лишай у собак: фото, симптомы и лечение
Микроспория более известна как стригущий лишай – весьма распространенное дерматологическое заболевание. Также к этой группе относится трихофития и парша. Опасны эти болезни еще и потому, что передаются от животного к человеку. Заражение происходит спорами гриба, которые могут быть не только на шерсти больного животного, но и на подстилке, игрушках и даже почве. У микроспорий может образовываться огромное число спор, этим и объясняется высокая степень заразности болезни. Также грибки демонстрируют высокую устойчивость к температурам и дезинфекции, они не любят повышенную влажность и прямые солнечные лучи, в тени же сохраняют жизнеспособность в течение нескольких месяцев. Некоторые виды грибов могут выживать до 10 лет без носителя.
Чаще всего заболевают молодые и не привитые собаки. Как таковой сезонности у лишая нет, после попадания микроспор на кожу, они начинают усиленно размножаться, вызывая воспаление эпидермиса, разрушение структуры волос собаки.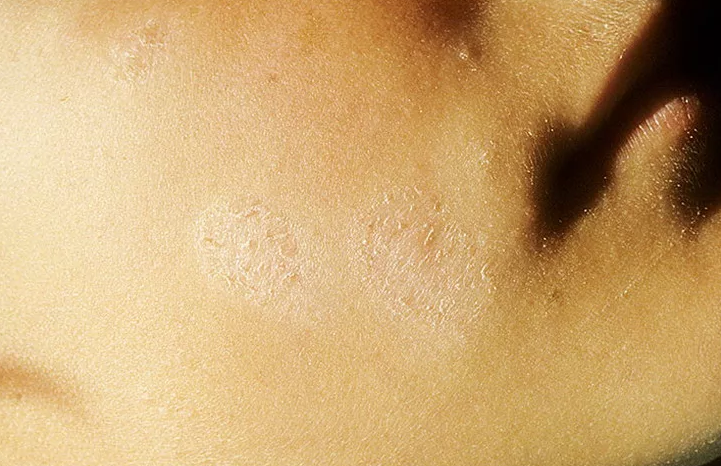 Если грибок проникнет глубже, он может вызвать абсцесс или дерматит, поэтому лечить микроспорию (стригущий лишай) нужно своевременно.
Если грибок проникнет глубже, он может вызвать абсцесс или дерматит, поэтому лечить микроспорию (стригущий лишай) нужно своевременно.
Формы и симптомы стригущего лишая или микроспории
- Поверхностная. Проявляется пятнами с хорошо очерченными границами, имеют овальную или круглую форму, окрашены в розовато-красный цвет. Очень быстро очаг инфекции распространяется по морде и туловищу собаки, на пятнах появляются беловатые чешуйки, волоски начинают выпадать;
- Глубокая. В фолликулах волос начинается гнойный воспалительный процесс, при надавливании может появляться гной. Зона вокруг пораженных волосков покрывается серо-белым налетом, плотными корочками;
- Скрытая. Воспалительный процесс присутствует, но характерных симптомов как таковых нет. Шерсть начинает выпадать, животное расчесывает кожу, могут появиться признаки аллергической реакции. Чаще всего эта форма встречается у взрослых собак;
- Атипичная (стертая). Проявляется в основном летом: характерные кругов нет, образования напоминают бородавки, потертости, припухлости или ссадины. Без лабораторных анализов определить, что это именно лишай невозможно.
Отметины локализуются на ушах, морде, лапах, потом переходят на другие части тела. Чтобы поставить диагноз, ветеринар проводит лабораторные исследования. Часто используется так называемая лампа Вуда: под люминесцентной лампой волоски светятся изумрудным цветом. Также берется соскоб чешуек или обломанные волоски с пораженного участка.
Лечение стригущего лишая (микроспории)
Лечение проводят в строгой последовательности: сначала кожу собак обрабатывают водой с мылом, потом смазывают салициловым спиртом или салициловой мазью. Внутрь собаке дают антибиотики, наиболее распространен гризеофульвин в дозировке на 1 кг веса 15-20 мг. Курс лечения рассчитан на 20 дней, потом через 10 дней его повторяют. Также используются различные мази на основе трихоцетина – их выписывает ветеринар с учетом индивидуальных особенностей собаки.
Поскольку микроспоры очень устойчивы, на пораженных местах может сохраняться инфекция, поэтому наблюдаться специалистом собака должна как минимум 1,5 месяца. Каждые 15 дней нужно проводить обследование люминесцентным методом. Обязательно обработайте помещение смесью из 1% гидроксида натрия и 2% формальдегида. Постирайте все подстилки, продезинфицируйте миски и игрушки питомца, соблюдайте правила гигиены.
Что касается профилактики, первое и самое важное – не допускайте контакта с зараженными животными. Также активно применяется моно- и поливалентная вакцинация: «Поливак», «Вакдерм», «Микканис», «Микродерм» и прочие препараты. При появлении других симптомов или ухудшении состояния собаки, свяжитесь с ветеринарным врачом!
Микроспоридиоз — Инфекционные болезни — Справочник Merck Professional Edition
Для пациентов со СПИДом: начало или оптимизация антиретровирусной терапии (АРТ)
При желудочно-кишечном, кожном, мышечном или диссеминированном микроспоридиозе — пероральный прием альбендазола или фумагиллина (при наличии), в зависимости от вида инфекции
Для лечения кератоконъюнктивита, пероральный альбендазол и фумагиллин для местного применения
Для пациентов со СПИДом важно начало или оптимизация АРТ.Продолжительность антимикробной терапии и результат зависят от уровня восстановления иммунитета при АРТ.
Антимикробное лечение микроспоридиоза зависит от вида заражающих микроспоридий, иммунного статуса человека-хозяина и задействованных органов. Данные о вариантах лечения ограничены. Рекомендуется консультация специалиста.
Альбендазол (400 мг перорально 2 раза в день для взрослых или 7,5 мг / кг 2 раза в день для детей в течение 2–4 недель) часто эффективен для контроля диареи у пациентов с кишечными инфекциями, вызванными E. кишечник и другие чувствительные микроспоридии. Инфекции у иммунокомпетентных пациентов могут исчезнуть спонтанно или через неделю лечения. Альбендазол имеет минимальную эффективность при лечении E. bieneusi . Альбендазол (400 мг 2 раза в день для взрослых или 7,5 мг / кг 2 раза в день для детей в течение 2–4 недель) также использовался для лечения кожного, мышечного или диссеминированного микроспоридиоза, вызванного бактериями E. виды микроспоридий.
кишечник и другие чувствительные микроспоридии. Инфекции у иммунокомпетентных пациентов могут исчезнуть спонтанно или через неделю лечения. Альбендазол имеет минимальную эффективность при лечении E. bieneusi . Альбендазол (400 мг 2 раза в день для взрослых или 7,5 мг / кг 2 раза в день для детей в течение 2–4 недель) также использовался для лечения кожного, мышечного или диссеминированного микроспоридиоза, вызванного бактериями E. виды микроспоридий.
Фумагиллин перорально по 20 мг 3 раза в день в течение 14 дней использовался для лечения кишечника E.bieneusi , но она имеет потенциально серьезные побочные эффекты, включая тяжелую обратимую тромбоцитопению у половины пациентов. Фумагиллин для перорального применения недоступен в США.
Глазной микроспоридиальный кератоконъюнктивит можно лечить с помощью альбендазола 400 мг перорально 2 раза в день и глазных капель фумагиллина. Местные фторхинолоны, а также местный вориконазол были эффективны у некоторых пациентов. Когда местная и системная терапия неэффективны, может быть полезна кератопластика.Результат обычно очень хороший у иммунокомпетентных пациентов; у пациентов со СПИДом это зависит от уровня восстановления иммунитета при АРТ.
микроспоридий — EyeWiki
Микроспоридии с вытянутой полярной нитью. [1]Микроспоридии — облигатные внутриклеточные спорообразующие паразитические грибы. Они способны заразить многие виды животных. У человека они могут инфицировать многие органы, в том числе глаз. Они широко распространены по всему миру и считаются новой причиной инфекционных заболеваний, особенно среди пациентов с ослабленным иммунитетом.
Организм
Микроспоридии — это тип микроорганизмов, состоящий примерно из 1200 видов, способных инфицировать множество различных животных, особенно рыб и насекомых. 15 видов были связаны с инфекциями у людей. К ним относятся Anncaliia (ранее Barachiola ), algerae, A. connori, A. vesicularum, Encephalitozoon cuniculi, E. hellem, E. кишечник, Enterocytozoon biuneusi, Mircosporidium ceylonensis, M. africanum, Nosema ocularum, Plendis., Trachipleistophora hominis, T anthropophthera, Vittaforma corneae и Tubulinosema acridophagus . E. cuniculi, E. Кишечник и E. bieneusi были обнаружены у некоторых домашних и диких животных, а E. hellem — у птиц. E. bieneusi и V. corneae виды были связаны с инфекцией человека.
Жизненный цикл микроспоридий [2]В последние десятилетия микроспоридии привлекли к себе большее внимание из-за их связи со стойкой диареей и системным заболеванием у пациентов со СПИДом. [3] Повышение осведомленности и развитие генетической технологии позволили лучше классифицировать и изучать несколько видов патогенных микроспоридий. [4]
Микроспоридии — облигатные внутриклеточные паразитические грибы, первоначально классифицируемые как простейшие. [5] В микроспоридиях отсутствуют типичные митохондрии, поэтому изначально считалось, что они разветвились до эндосимбиотического развития митохондрий на эволюционном дереве. Это ставится под сомнение, поскольку генетическое секвенирование выявило гены, кодирующие митохондриальные белки, и дальнейшую идентификацию того, что считается митохондриальными остатками в ультраструктуре клетки.Полное секвенирование генов микроспоридий Encephalitozoon cuniculi предоставило важные доказательства, подтверждающие гипотезу о том, что микроспоридии — это изысканно специализированные атипичные грибы, которые эволюционно утратили свои митохондрии, сохранив при этом полученные из митохондрий органеллы, называемые митосомами. [6] [7] [8] Экологически устойчивые споры — это инфекционная форма микроспоридий. Заражение клетки-хозяина достигается за счет использования специальной спиральной органеллы, уникальной для микроспоридий, называемой полярным канальцем.Эта структура может быть продемонстрирована при визуализации ультраструктуры спор. Изменения осмотического давления внутри споры заставляют полярную трубку или полярную нить разворачиваться и расширяться в направлении эукариотической клетки-хозяина с последующим переносом клеточного содержимого микроспоридий (спороплазмы). Попав в хозяина, паразитические микроспоридии размножаются внутриклеточно, заполняя цитоплазму. В конце концов, когда споры достигают зрелости, клетка-хозяин лизирует их и выпускает в окружающую среду. [4]
Клинические особенности
Впервые выявленная при ВИЧ-1-инфекции в условиях хронической диареи, микроспоридии с тех пор были обнаружены как вызывающие множество системных и глазных инфекций как у лиц с ослабленным иммунитетом, так и у иммунокомпетентных людей.
Первый хорошо задокументированный случай поражения глаз у людей произошел в 1973 году, когда Эштон и Вирашина описали 11-летнего мальчика со стромальным кератитом, вызванным микроспоридиями. [9] В целом, существует два довольно разных клинических проявления глазного микроспоридиоза.Стромальный кератит характерен для инфекции у здоровых людей, в то время как с ослабленным иммунитетом, особенно у пациентов со СПИДом, чаще развиваются кератоконъюнктивит и эпителиальная кератопатия. Однако клиническое проявление может быть различным и может включать переднюю или среднюю инфильтрацию, передний увеит или даже грубый некроз и перфорацию роговицы.
Острота зрения варьируется от 20/20 до 20/100, часто без потери остроты зрения после разрешения болезни. Симптомы обычно включают покраснение, ощущение инородного тела, снижение остроты зрения и светобоязнь.Атипичный точечный эпителиальный кератит, связанный с конъюнктивитом, также может возникать у здоровых людей с удовлетворительными результатами лечения. Одно исследование 4822 пациентов с микробным кератитом в Индии показало, что у 19 (0,4%) из них был подтвержден микроспоридиальный кератит. У всех этих пациентов были отмечены мультифокальные, конечно, точечные, приподнятые эпителиальные поражения. Во всех случаях также отмечался негнойный конъюнктивит от легкой до умеренной степени, часто с папиллярными и / или фолликулярными реакциями. [10] [11] Эпителиальные изменения могут перерасти в центральный нуммулярный или дискообразный кератит до разрешения. [12] Одно исследование также задокументировало диффузный эндотилиит с отеком роговицы и лимбитом как дополнительные клинические признаки инфекции, которая исчезла с помощью местного лечения стероидами. [12]
Передача нечеткая. Микроспоридии могут оставаться в латентном состоянии в организме хозяина, и реактивация может происходить во время иммунного нарушения. Передача может быть возможна от хозяев, не подозревающих, что они являются носителями микроспоридий. Сообщалось о случае передачи микроспоридиального кератоконъюнктивита через донорский трансплантат роговицы, что подтверждает эту возможность. [13] О микроспоридиозе все чаще сообщается у реципиентов солидных трансплантатов органов. Тем не менее, остается неясным, передается ли инфекция донорской тканью или приобретается хозяином в течение следующего периода подавления иммунитета. [14]
| Клинические проявления микроспоридий | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Источник: CDC DPDx Microsporidiosis
Изображение на просвечивающем электронном микроскопе паразитов Encephalitozoon Кишечник , содержащихся в паразитофорной вакуоли (ПВ). Вы можете увидеть как развивающиеся, формы E.interstinalis , так и зрелые споры (черные стрелки). Источник CDC Public Health Image Library (PHIL) [15]Просвечивающая электронная микроскопия
Золотым стандартом идентификации микроспоридий является просвечивающая электронная микроскопия (ПЭМ).ТЕА может также использоваться для идентификации видов конкретного организма. Однако TEM не является широко доступным и непрактичным для рутинной диагностики. Кроме того, это непомерно дорого и требует много времени. [16]
Образец глазных микроспоридий с окраской трихромом. [17]Микроскопия
Существует множество гистохимических методов диагностики с помощью исследования образцов жидкости (моча, кал, слизь и т. Д.) При диссеминированных инфекциях. Флуоресцентные отбеливатели, такие как Calcofluor white, можно использовать для воздействия на стенки хитиновых спор.Модифицированное (концентрированное) окрашивание трихромом также можно использовать отдельно или в сочетании с окрашиванием по Граму или окрашиванием серебром Вартина-Старри для идентификации организмов. [16] [12] Метод Chromotrope 2R — широко используемая техника окрашивания, при которой стенка спор окрашивается в ярко-красный цвет, часто с периферийной полосой, напоминающей пояс, который также окрашивает розово-красный цвет. Выполнение этого метода может занять около 90 минут, и была разработана «техника быстрого горячего хромотропа», позволяющая окрашивать менее чем за 10 минут с адекватным цветовым контрастом.Эти споры окрашены в темно-фиолетовый цвет, а также демонстрируют более темную центральную полосу. Споры микроспоридий, ассоциированные с инфекцией человека, имеют размер от 1 до 4 мкм в зависимости от вида. [16] Препарат КОН со соскобами роговицы также проводился для идентификации микроспоридий с 1% кислотостойким окрашиванием, используемым в качестве подтверждающего метода. [10] [11]
Иммунофлуоресцентный анализ (IFA)
IFA доступны для микроспоридий с использованием моноклональных и / или поликлональных антител. [16]
Молекулярные методы (ПЦР)
CDC предлагает молекулярную идентификацию Enterocytozoon bieneusi, Encephalitozoon Кишечник, Encephalitozoon hellem и Encephalitozoon cuniculi с использованием анализа видоспецифической полимеразной цепной реакции (ПЦР). Эти методы обычно используются в исследовательских лабораториях, но не в клинико-диагностических учреждениях. [4] Эти четыре вида микроспоридий теперь можно идентифицировать с помощью одного микрочипа с использованием клинических образцов. [18]
Инфекция среди людей происходит во всем мире с самой высокой распространенностью среди ВИЧ-инфицированных лиц с диареей и менее 100 CD4 + Т-клеток на мм крови. 3 крови. Большинство микроспоридиальных инфекций, связанных со СПИДом, связано с Enterocytozoon bieneusi, , что связано с хронической диареей и истощением. Менее 50 CD4 + Т-клеток на мм. 3 крови связано с инфекциями как E. bieneusi , так и E. кишечника . [19] [20] [21]
Источник инфекции остается неясным, но инфекционные генотипы человека были идентифицированы у домашних, сельскохозяйственных и диких животных, что позволяет сделать вывод о возможной зоонозной этиологии. [22] Остается сильная связь с воздействием почвы, ношением контактных линз и местным лечением стероидами при глазных инфекциях. [12]
Идентификация микроспоридий в водных источниках привела к их включению в Список кандидатов на загрязняющие вещества 2 Агентства по охране окружающей среды (EPA), [23] , а также классификации Национальных институтов здравоохранения (NIH) как Патогены биозащиты категории B. [24]
Описаны различные возможные методы лечения микроспоридиального кератита. У пациентов с ослабленным иммунитетом из-за ВИЧ восстановление их иммунного статуса с помощью антиретровирусных препаратов было связано с исчезновением клинических симптомов. [4] Было также зарегистрировано, что ингибиторы аспартил-протеазы ВИЧ напрямую ингибируют рост Encephalitozoon Кишечник в культуре ткани. [25] Альбендазол, который ингибирует сборку микротрубочек, также эффективен против нескольких микроспоридий, включая Encephalitozoon spp.при системном заболевании. [26] Системные противогрибковые препараты также использовались для лечения микроспоридных инфекций у больных СПИДом. [27]
Фумагиллин, антибиотик и антиангиогенный агент, полученный из Aspergillus fumigatus , оказался эффективным против Encephalitozoon sp. и Enterocytozoon bieneusi . Несмотря на токсичность при системном применении, местное применение хорошо переносится и эффективно лечит кератоконъюнктивит. [28]
Местные фторхинолоны (ципрофлоксацин 0,3%, моксифлоксацин 0,5%, гатифлоксацин 0,5%, левофлоксацин 0,5% и норфлоксацин 0,3%) в качестве монотерапии или в комбинации с местным фумагиллином и / или системным лечением альбендазолом изучались. микроспоридиального кератита. Разрешение произошло в 99% случаев при местной монотерапии фторхинолоном. [12]
Медицинское лечение может быть долгосрочным, и после прекращения лечения может возникнуть рецидив.В случае сильного истончения и некроза роговицы проникающая кератопластика может быть единственным надежным методом лечения. [29]
- ↑ https://www.cdc.gov/dpdx/microsporidiosis/index.html
- ↑ https://www.cdc.gov/dpdx/microsporidiosis/index.html
- ↑ Desportes I, Le Charpentier Y, Galian A, et al. Возникновение нового микроспоридиана: Enterocytozoon bieneusi n.g., n. sp., в энтероцитах больного СПИДом человека. J Protozool. 1985; 32: 250-254.[PubMed: 4009510]
- ↑ 4,0 4,1 4,2 4,3 Дидье, Элизабет С. и Луи М. Вайс. «Микроспоридиоз: текущее состояние». Current Opinion in Infectious Diseases, Vol. 19, нет. 5, 2006, стр. 485–492., DOI: 10.1097 / 01.qco.0000244055.46382.23.
- ↑ Vossbrinck, C. R., et al. «Последовательность рибосомной РНК предполагает, что микроспоридии являются чрезвычайно древними эукариотами». Природа, т. 326, нет. 6111, 1987, стр. 411–414., DOI: 10.1038 / 326411a0.
- ↑ Thomarat, Fabienne, et al.«Филогенетический анализ полной последовательности генома Encephalitozoon Cuniculi подтверждает грибковое происхождение микроспоридий и выявляет высокую частоту быстро развивающихся генов». Журнал молекулярной эволюции, т. 59, нет. 6, 2004, стр. 780–791., DOI: 10.1007 / s00239-004-2673-0.
- ↑ Катинка, Майкл Д. и др. «Последовательность генома и уплотнение генов паразита эукариот Encephalitozoon Cuniculi». Природа, т. 414, нет. 6862, 2001, стр. 450–453., DOI: 10.1038 / 35106579.
- ↑ Гилл, Эрин Э., и Наоми М. Фаст. «Оценка взаимосвязи микроспоридий и грибов: комбинированный филогенетический анализ восьми генов». Джин, т. 375, 2006, стр. 103–109., DOI: 10.1016 / j.gene.2006.02.023.
- ↑ Эштон Н., Вирашина П.А. 1973. Энцефалитозооноз (нозематоз) роговицы. Br J Ophthalmol 57: 669-674.
- ↑ 10,0 10,1 Joseph, Joveeta, et al. «Клинический и микробиологический профиль микроспоридиального кератоконъюнктивита в Южной Индии». Офтальмология, т.113, нет. 4, 2006 г., стр. 531–537., DOI: 10.1016 / j.ophtha.2005.10.062.
- ↑ 11,0 11,1 Sharma, S, et al. «Микроспоридии: новые глазные патогены». Индийский журнал медицинской микробиологии, вып. 23, нет. 2, 2005, с. 80., DOI: 10.4103 / 0255-0857.16045.
- ↑ 12,0 12,1 12,2 12,3 12,4 Ло, Раймонд С. и др. «Растущая распространенность микроспоридиального кератита в Сингапуре». Офтальмология, т. 116, нет.12, 2009, стр. 2348–2353., DOI: 10.1016 / j.ophtha.2009.05.004.
- ↑ Kakrania, R, et al. «Микроспоридический кератоконъюнктивит в трансплантате роговицы». Глаз, т. 20, нет. 11, 2005, стр. 1314–1315., DOI: 10.1038 / sj.eye.6702178.
- ↑ Шварц Б. С. и С. Д. Мохортер. «Паразитарные инфекции при трансплантации твердых органов». Американский журнал трансплантологии, т. 13, вып. s4, 2013, pp. 280–303., DOI: 10.1111 / ajt.12120.
- ↑ https://phil.cdc.gov/Details.aspx?pid=142
- ↑ 16.0 16,1 16,2 16,3 «DPDx — Лабораторная идентификация паразитов, вызывающих озабоченность в области общественного здравоохранения». Центры по контролю и профилактике заболеваний, Центры по контролю и профилактике заболеваний, 29 декабря 2017 г., www.cdc.gov/dpdx/microsporidiosis/index.html.
- ↑ https://www.cdc.gov/dpdx/microsporidiosis/index.html
- ↑ Wang, Z., et al. «Одновременное обнаружение четырех видов патогенных микроспоридий человека из клинических образцов с помощью олигонуклеотидного микрочипа.”Журнал клинической микробиологии, вып. 43, вып. 8, 2005, стр. 4121–4128., DOI: 10.1128 / jcm.43.8.4121-4128.2005.
- ↑ Морпет, Сьюзен К. и Натан М. Тильман. «Диарея у больных СПИДом». Современные варианты лечения в гастроэнтерологии, т. 9, вып. 1, 2006, стр. 23–37., DOI: 10.1007 / s11938-006-0021-8.
- ↑ Шварц, Дэвид А. и др. «Патологические особенности и демонстрация иммунофлуоресцентных антител при глазном микроспоридиозе (Encephalitozoon Hellem) у семи пациентов с синдромом приобретенного иммунодефицита».»Американский журнал офтальмологии, вып. 115, нет. 3, 1993, стр. 285–292., DOI: 10.1016 / s0002-9394 (14) 73577-9.
- ↑ Вебер Р. и Р. Т. Брайан. «Микроспоридиальные инфекции у иммунодефицитных и иммунокомпетентных пациентов». Клинические инфекционные болезни, т. 19, нет. 3, 1994, стр. 517–521., DOI: 10.1093 / Clinids / 19.3.517.
- ↑ Mathis, A., et al. «Зоонозный потенциал микроспоридий». Обзоры клинической микробиологии, т. 18, нет. 3, 2005, стр. 423–445., DOI: 10.1128 / cmr.18.3.423-445.2005 г.
- ↑ «Список кандидатов на загрязняющие вещества 2 — CCL 2». EPA, Агентство по охране окружающей среды, 29 сентября 2016 г., www.epa.gov/ccl/contaminant-candidate-list-2-ccl-2#microbial-list.
- ↑ «NIAID Emerging Infective Infectious Diseases / Pathogens». Национальный институт аллергии и инфекционных заболеваний, Министерство здравоохранения и социальных служб США, 23 мая 2018 г., www.niaid.nih.gov/research/emerging-infectious-diseases-pathogens.
- ↑ Menotti, J., et al. «Ингибирующая активность ингибиторов аспартил-протеазы вируса иммунодефицита человека против Encephalitozoon Intestinalis, оцениваемая с помощью количественного ПЦР-анализа на культуре клеток.”Противомикробные средства и химиотерапия, т. 49, нет. 6, 2005, стр. 2362–2366., DOI: 10.1128 / aac.49.6.2362-2366.2005.
- ↑ Tremoulet, Adriana H., et al. «Терапия альбендазолом от микроспоридиозной диареи у иммунокомпетентных детей Коста-Рики». Журнал детских инфекционных болезней, вып. 23, нет. 10, 2004, стр. 915–918., DOI: 10.1097 / 01.inf.0000141724.06556.f9.
- ↑ Йи, Ричард В. и др. «Разрешение микроспоридиальной эпителиальной кератопатии у пациента со СПИДом». Офтальмология, т.98, нет. 2, 1991, стр. 196–201., DOI: 10.1016 / s0161-6420 (91) 32331-5.
- ↑ Champion, L., et al. «Фумагиллин для лечения микроспоридиоза кишечника у реципиентов почечного трансплантата». Американский журнал трансплантологии, т. 10, вып. 8, 2010, стр. 1925–1930., DOI: 10.1111 / j.1600-6143.2010.03166.x.
- ↑ Вт EY. Акантамеба и другие паразитарные инфекции роговицы. В: Krachmer JH, Mannis MH, Holland EJ. Роговица. 3-е изд. Том 1. Филадельфия: Эльзевьер / Мосби; 2011.
Microsporidia — обзор | Темы ScienceDirect
11.2.5 Microsporidia
Микроспоридии исторически ассоциировались с простейшими, но в последнее десятилетие были реклассифицированы в королевстве грибов как тип микроспоридий (Keeling, 2009). Тем не менее, их биология и морфология уникальны и сильно отличаются от других грибов. Спора является инфекционным агентом, и инфекционный процесс чаще всего включает в себя проглатывание спор хозяином, быстрое прорастание спор в кишечнике хозяина с быстрым внедрением ядра и связанной цитоплазмы в эпителиальную клетку кишечника через тонкую полую полярную нить. вывернут из спор.Затем микроспоридиан развивается внутри клетки-хозяина. Вертикальная передача трансовариальным и трансовумным путями также распространена среди микроспоридий, как и промежуточные хозяева. Хозяева микроспоридий охватывают широкий диапазон, от протистов до теплокровных позвоночных, но в целом каждый вид в некоторой степени специфичен для хозяина. См. Solter et al. (2012b) для обзора биологии микроспоридий. Один вид, Paranosema (Nosema) locustae (Canning), был зарегистрирован как микробный пестицид и коммерциализирован в Соединенных Штатах для борьбы с кузнечиками (USEPA, 2000).В целом, однако, усилия по биоконтролю микроспоридий были больше сосредоточены на инокулятивных или аугментативных подходах, для которых требуется меньшее количество инфекционных спор, чем при обильном использовании.
Отличительной особенностью микроспоридий является их облигатное внутриклеточное развитие. Таким образом, эти организмы могут массово продуцироваться только in vivo, в их хозяевах (Henry, 1985) или в культуре клеток беспозвоночных (Visvervara et al., 1999). Например, P. locustae получают путем перорального заражения кузнечиков дозой, оптимальной для образования спор, позволяя патогенам размножаться в организме хозяина, фрагментируя трупы на мельнице и суспендируя мацерат в воде.После удаления частей насекомых фильтрацией полученную суспензию спор дополнительно очищают и включают в состав носителя из пшеничных отрубей (Генри, 1985). Споры P. locustae перед приготовлением можно хранить в охлажденной стерильной воде, лиофилизировать или сушить в вакууме. Зараженные трупы также можно сушить и хранить до дальнейшей обработки. Отсылаем читателя к Solter et al. (2012a) и Solter et al. (2012b) для получения дополнительной информации о методах массового производства микроспоридий.
(PDF) Терапевтические стратегии для инфекций микроспоридий человека
Didier, Maddry, Brindley, Stovall & Didier
12
Expert Rev. Anti Infect. Ther. 3 (3), (2005)
57 Rauz S, Tuft S, Dart JK, Bonshek R,
Luthert P, Curry A. Ультраструктурное исследование
двух случаев микроспоридиального кератита стромы
. J. Med. Microbiol.
53, 775–781 (2004).
58 Дэвис Р.М., шрифт RL, Кейслер М.С., Shadduck
JA.Микроспоридиоз роговицы. История болезни
, включая ультраструктурные наблюдения.
Офтальмология 97, 953–957 (1990).
59 Shadduck JA, Meccoli RA, Davis R, шрифт
RL. Выделение микроспоридиана от пациента
человека. J. Infect. Дис. 162, 773–776
(1990).
60 Silveira H, Консервирование ЕС. Vittaforma corneae
n. гребень. для микроспоридиума человека
Nosema corneum Shadduck, Meccoli, Davis
& Font, 1990, на основании его ультраструктуры в печени
экспериментально инфицированных бестимусных мышей
.J. Eukaryot. Microbiol. 42, 158–165
(1995).
61 Deplazes P, Mathis A, van Saanen M et al.
Двойная микроспоридиальная инфекция, вызванная
Vittaforma corneae и Encephalitozoon
hellem у пациента со СПИДом. Clin Infect
Dis. 27, 1521–1524 (1998).
62 Orenstein JM, Gaetz HP, Yachnis AT,
Frankel SS, Mertens RB, Didier ES.
Диссеминированный микроспоридиоз при СПИДе:
Спасены ли какие-либо органы? AIDS 11, 385–386
(1997).
63 Orenstein JM, Chiang J, Steinberg W,
Smith PD, Rotterdam H, Kotler DP.
Микроспоридиоз кишечника как причина
диареи при иммунодефиците человека
инфицированных вирусом пациента: сообщение о 20 случаях.
Hum. Патол. 21. С. 475–481 (1990).
64 Orenstein JM, Tenner M, Cali A, Kotler
DP. Микроспоридиан, ранее не описанный у людей
, инфицировал
энтероцитов и макрофагов, и
ассоциировался с диареей у пациента с синдромом приобретенного иммунодефицита
.
Hum. Патол. 23, 722–728 (1992).
65 Кали А., Такворян П. Развитие
морфология и жизненные циклы микроспоридий
. В: The Microsporidia and
Microsporidiosis. Wittner M, Weiss LM
(Eds), Американское общество микробиологии,
WA, USA, 85–128 (1999).
66 Гарсия LS. Лабораторная идентификация микроспоридий
. J. Clin. Microbiol. 40,
1892–1901 (2002).
67 Федорко Д.П., Хиджази Ю.М.Применение молекулярных методов
для диагностики микроспоридиальной инфекции
. Emerg. Заразить. Дис.
2, 183–191 (1996).
68 Франзен К., Мюллер А. Молекулярные методы
для обнаружения, видовой дифференциации и
филогенетический анализ микроспоридий.
Clin. Microbiol. Ред. 12, 243–285 (1999).
69 Weiss LM. Молекулярная филогения и
диагностических подходов к микроспоридиям.
Contrib.Microbiol. 6. С. 209–235 (2000).
70 Dowd SE, Gerba CP, Enriquez FJ, Pepper
IL. ПЦР-амплификация и виды
определение микроспоридий в
фиксированных формалином фекалиях после иммуномагнитного разделения
. Прил. Environ. Microbiol. 64,
333–336 (1998).
71 Орланди PA, Lampel KA. Безэкстракционный,
шаблонный препарат на основе фильтра для быстрого
и чувствительного ПЦР обнаружения патогенных паразитических простейших
.J. Clin. Microbiol. 38,
2271–2277 (2000).
72 Carnevale S, Velásquez JN, Labbé JH et al.
Диагностика Enterocytozoon bieneusi с помощью
ПЦР в образцах стула, элюированных с фильтра
бумажных дисков. Clin. Диаг. Лаборатория. Иммунол. 7,
504–506 (2000).
73 Сорель Н., Гийо Э., Телье М. и др.
Разработка иммуномагнитного метода
разделения — полимеразная цепная реакция
(IMS-PCR) Анализ, специфичный для
Enterocytozoon bieneusi в пробах воды.
J. Appl. Microbiol. 94, 273–279 (2003).
74 Subrungruang I, Mungthin M,
Chavalitshewinkoon-Petmitr P, Ransin R,
Naaglor T, Leelayoova S.Оценка
методов экстракции ДНК и ПЦР для
обнаружения энтероцитозоатов
0004 биопрепаратов энтероцитозоола0004 в образцах стула0005. J. Clin. Microbiol. 42,3490–3494 (2004).
75 Сингх М., Кейн Дж. Дж., Макинли Л. и др.
Обнаружение антител к Nosema cuniculi
(Protozoa: Microscoporidia) в сыворотке крови человека и
животных методом непрямой флуоресценции антител
.Юго-Восточная Азия J. Trop.
Мед. Общественное здравоохранение 13, 110–113 (1982).
76 Bergquist R, Morfeldt-Mansson L, Pehrson
PO, Petrini B, Wasserman J. Антитело
против Encephalitozoon cuniculi в Швеции
гомосексуальных мужчин. Сканд. J. Infect. Дис. 16,
389–391 (1984).
77 Hollister WS, Canning EU, Willcox A.
Доказательства широкого распространения
антител к Encephalitozoon cuniculi
(Microspora) у человека предоставлены ELISA
и другими серологическими тестами.Паразитология
102 (Pt 1), 33–43 (1991).
78 Van Gool T, Biderre C, Delbac F,
Wentink-Bonnema E, Peek R, Vivares CP.
Серодиагностические исследования у иммунокомпетентного человека
, инфицированного
Encephalitozoon cuniculi. J. Infect. Дис.
189, 2243–2249 (2004).
79 Кучерова-Посписилова З., Дитрих О. Серологическое наблюдение
нескольких групп по
пациентов с использованием антигенов Encephalitozoon
hellem и E.cuniculi к микроспоридиям
у больных. Folia Parasitol.
(Praha) 45, 108–112 (1998).
80 Кучерова-Посписилова З., Secor WE, Moura
H et al. Тест ELISA для обнаружения человеческих антител
в сыворотке, реактивных с
Encephalitozoon Кишечник. J. Eukaryot.
Microbiol. (Дополнение), 73–74 (2001).
81 дель Агила С., Руэда С., Де ла Камара С.,
Феной С. Серопревалентность
антител против энцефалитоза у испанских
иммунокомпетентных субъектов.J. Eukaryot.
Microbiol. (Дополнение), 75–78 (2001).
82 Карри А., Смит Х.В. Возникающие патогены:
isospora, cyclospora и microsporidia.
Parasitology 117 (Suppl.), 143–159 (1998).
83 Зейтц Х.М., Траммер Т. Оппортунистические
инфекции, вызываемые простейшими паразитами.
Tokai J. Exp. Clin. Med. 23, 249–257
(1998).
84 Shadduck JA, Pakes SP.
Энцефалитозооноз (нозематоз) и
токсоплазмоз.Являюсь. J. Pathol. 64, 657–671
(1971).
85 Lopez-Velez R, Turrientes MC, Garron C
et al. Микроспоридиоз у путешественников с диареей
из тропиков. J. Travel Med. 6,
223–237 (1999).
86 Müller A, Bialek R, Kamper A,
Fatkenheuer G, Salzberger B, Franzen C.
Обнаружение микроспоридий у путешественников с диареей
. J. Clin. Microbiol. 39, 1630–2632
(2001).
87 Valperga SM, de Jogna Prat SA, de Valperga
GJ et al.Споры микроспоридий в кале
образца малышей, с диареей или без
, из Тукумана, Аргентина. Ред.
Argent. Microbiol. 31, 157–164 (1999).
88 Chokephaibulkit K, Wanachiwanawin D,
Tosasuk K, Pavitpok J, Vanprapar N,
Chearskul S. Кишечные паразитарные инфекции
среди людей с иммунодефицитом
среди
инфицированных вирусом больных, инфицированных вирусом больных в БангкокеТаиланд.Юго-Восточная Азия J. Trop. Med.
Public Health 32, 770–775 (2001).
89 Mungthin M, Suwannasaeng R, Naaglor T,
Areekul W., Leelayoova S. Бессимптомный
кишечный микроспоридиоз у тайских сирот
и работников детских учреждений. Пер. R. Soc. Троп.
Мед. Hyg. 95, 304–306 (2001).
90 Tumwine JK, Kekitiinwa A, Nabukeera N,
Akiyoshi, DE, Buckholt MA, Tzipori S.
Enterocytozoon bieneusi среди детей
с диареей, посещающих больницу Мулаго в
Уганда.Являюсь. J. Trop. Med. Hyg. 67,
299–303 (2002).
91 Wanachiwanawin D, Chokephaibulkit K,
Lertlaituan P, Ongrotchanakun J, Chinabut
P, Thakerngpol K. Кишечный
микроспоридиоз у ВИЧ-инфицированных детей
с диареей. Юго-Восточная Азия J. Trop. Med.
Public Health 33, 241–245 (2002).
Microsporidium Артикул
Непрерывное образование
Microsporidia — необычайно большая группа уникальных эукариотических облигатных внутриклеточных паразитов, которых биологи изучают более 150 лет.Микроспоридии — хорошо адаптированные патогены и важные сельскохозяйственные паразиты, поражающие медоносных пчел, шелкопрядов и других насекомых. Организм также является паразитом для рыб, грызунов, кроликов, приматов и человека. Это мероприятие рассматривает с упором на его патофизиологию и презентацию, а также подчеркивает роль межпрофессиональной команды в его управлении.
Цели:
- Обобщите рекомендованное управление микроспоридии.
- Обрисуйте типичное представление пациента с микроспоридиями.
- Обзор патофизиологии микроспоридий.
- Объясните стратегии межпрофессиональной команды для улучшения координации помощи и коммуникации в отношении ведения пациентов с микроспоридиями.
Введение
Microsporidia — необычно большая группа уникальных эукариотических облигатных внутриклеточных паразитов, которых биологи изучают более 150 лет. Microsporidia — хорошо адаптированные патогены и важные сельскохозяйственные паразиты, поражающие медоносных пчел, шелкопрядов и других насекомых. Организм также является паразитом для рыб, грызунов, кроликов, приматов и человека. В этой статье представлен обзор Microsporidia с акцентом на последние биологические открытия.
Этиология
Биологи изучают Microsporidia более 150 лет. Микроспоридии включают 187 родов приблизительно с 1500 видами.Микроспоридии повсеместно распространены в окружающей среде; они эволюционировали уникальным и сложным образом, так что они не только выживают в окружающей среде, но также могут жить внутри других клеток. [1]
Классификация Microsporidia основана на микроскопической морфологии и ультраструктурных характеристиках спор. Диапазон хозяев во многих случаях несовместим с филогенетическими отношениями, которые в дальнейшем выявляются молекулярными методами посредством генетического секвенирования рРНК, которое в настоящее время используется в качестве основного способа определения таксономии.[2]
Эпидемиология
Микроспоридии у животных
Инфекция Microsporidia , также известная как микроспоридиоз, встречается во всем мире. Заражение происходит через широко известные в сельском хозяйстве патогены и приводит к потере ресурсов. К классическим видам относятся Nosema apis и Nosema ceranae , которые заражают медоносных пчел. Исследования показали, что уровень смертности пчел, инфицированных N.ceranae составляет почти 94%, и инфицированные популяции обычно умирают в течение 8 дней. Через три дня после заражения наблюдаемые зрелые споры внутри клеток-хозяев сигнализируют о завершении жизненного цикла паразита. Паразит поражает как верхушку складок, так и базальные клетки эпителия пчелы, и инфекция быстро распространяется между эпителиальными клетками [3].
Другими примерами заражения микроспоридиями являются виды Loma salmonae , поражающие лосося, и виды Thelohania , поражающие креветок.Заражение Loma salmonae может вызывать системные симптомы, включая значительные изменения в жабрах. Паразит также поражает сердце, селезенку, почки и псевдоветвь инфицированных морских или пресноводных рыб.
Микроспоридии у людей
В начале века у людей инфекция этим условно-патогенным микроорганизмом не была широко признана. В 1924 году исследователи впервые предположили, что Microsporidia, инфицировали людей, и до 1985 года было опубликовано лишь несколько отчетов о человеческом микроспоридиозе.После этого Microsporidia стали все более широко признаваться во всем мире как условно-патогенные инфекционные агенты, и в настоящее время Microsporidia признаны возникающими организмами во многих областях как развитых, так и развивающихся стран [4]. Microsporidia широко распространена во всем мире среди детей, путешественников, реципиентов органов, пожилых людей, пациентов со злокачественными заболеваниями и диабетом, а также пациентов с ВИЧ. [4] В развитых странах частота случаев микроспоридиоза у пациентов с ВИЧ постепенно снижается благодаря антиретровирусной терапии и улучшению гигиены.
Среди почти 1500 описанных видов только 17 являются патогенами для человека, и некоторые из них включают Enterocytozoon bieneusi , Encephalitozoon , Anncaliia , Enter africocytozoon , Tubulinosema sporidium и Trachipleistophora hominis . В большинстве случаев E. bieneusi и Encephalitozoon Кишечник были двумя видами, наиболее часто обнаруживаемыми у инфицированных людей.[5]
В развитых странах уровни распространенности инфекции Microsporidia у ВИЧ-серопозитивных людей с диареей колеблются от 2% до 78%, в зависимости от степени иммуносупрессии и лечения. У ВИЧ-серопозитивных людей без диареи частота инфицирования колеблется от 1,4% до 4,3% [6]. У лиц, не инфицированных ВИЧ, уровни распространенности серотипа колеблются от 1,3% до 22% среди доноров крови, беременных женщин, рабочих скотобойни и лиц с неизвестными причинами диареи (возможно, вызванной инфекцией Microsporidia ).[7]
Патофизиология
Клиническое проявление
Клинические проявления инфекции микроспоридий варьируются от бессимптомной инфекции до симптоматической инфекции, которая включает диарею, миозит, кератит и бронхит. Хотя энцефалит встречается редко, он также может возникать [8]. Среднее время инкубации болезни во время передачи через пищевые продукты составляет примерно 7 дней от даты появления симптомов до начала заболевания (от 3 до 15 дней).У ВИЧ-инфицированных пациентов инфекция микроспоридиями становится все более серьезной причиной заболеваемости и вызывает серьезные желудочно-кишечные (ЖКТ) и диссеминированные заболевания. В редких случаях E. bieneusi вызывает легочные инфекции или поражает желчные протоки, что приводит к холециститу и холангиту. [7] Сообщения об окулярных инфекциях микроспоридиями редки, но чаще встречаются у лиц с ослабленным иммунитетом, чем у иммунокомпетентных людей.
Остается неизвестным, какая часть титра спор необходима для инфицирования человека, но, по-видимому, он варьируется между разными подвидами.Споры, поражающие людей, обычно имеют размер от 1 до 4 микрометров, а у детей с бессимптомной картиной, по-видимому, 1,2 x 10 спор E . bieneusi на грамм фекалий. Принимая во внимание, что у ВИЧ-инфицированных пациентов концентрация спор E. bieneusi варьируется от 4,5 x 10 до 4,4 x 10 на миллилитр диарейных фекалий, всего 10 спор за 24 часа.
Факторы риска
Факторы риска, связанные с инфекцией микроспоридий, включают сексуальные контакты между мужчинами, внутривенное употребление наркотиков, воздействие болотной воды или зоны орошения сельскохозяйственных культур, воздействие воды с выделениями, использование бассейна и гидромассажных ванн или профессиональный контакт с водой.[7]
Передача
Передача микроспоридий происходит в основном через пищевые продукты (болезнь пищевого происхождения), включая рыбу и ракообразных (креветки, омары, моллюски и др.) В глобальной пищевой цепи. Передача также происходит через воду, включая орошение сельскохозяйственных культур, морскую воду, питьевую воду, грунтовые воды, сточные воды, фекалии в окружающей среде и ил. [9] Вертикальная передача от матери к потомству также наблюдалась у кроликов, овец и нечеловеческих приматов.Зоонозная передача через животных, выступающих в качестве резервуаров, также была отмечена в некоторых исследованиях. [10] [9] Передача фекально-оральным путем и аэрозолями может происходить редко, но и в случаях инфицирования людей [11].
История и физика
В 1838 году Глюдж описал самое раннее сообщение о существовании микроспоридий, когда паразит инфицировал рыбу. Позже она получила название Glugea anomala. В 1857 году профессор Карл Вильгельм фон Нагели распознал первую микроспоридию Nosema bombycis. [12] [1] N. bombycis инфицировал как Lepidoptera , так и Hymenoptera , вызывая болезнь пебрина / перца, названную профессором Жаном Луи Арманом де Quatrefages de Breau в Париже. Болезнь заразила яйца тутового шелкопряда, в результате чего личинки покрылись черноватыми пятнами. Болезнь, вызванная N. bombycis , была тяжелой и почти уничтожила европейскую шелковую промышленность во Франции, Италии и Германии. Нагели сначала рассмотрел этого паразита как дрожжеподобный организм и классифицировал его как Schizomycetes , консенсусную группу дрожжей и бактерий.
Дальнейшие исследования микроспоридий включали исследование Луи Пастера с его знаменательным исследованием N. bombycis . Он предложил меры по борьбе с пебриновой болезнью и ее профилактике, которые не только значительно спасли шелковую промышленность в Европе, но и стали основным источником влияния микробной теории болезни Пастера. Таксономическое определение микроспоридий было спорным в течение нескольких лет, и многие исследователи предположили, что это одноклеточные водоросли, споры дрожжей, организм, связанный с грибами, и даже как опухолевые клетки или деградированные эритроциты.[1] [12]
После серии исследований патогена тутового шелкопряда Бальбиани обнаружил, что этот организм не обладает некоторыми характеристиками Schizomycetes , но имеет общие черты с Sporozoa . Следовательно, в 1882 году Бальбиани впервые предложил отдельный таксон Microsporidia для N. bombycis , который в то время был единственным названным микроспоридиумом. В 1977 году Спраг обозначил тип Microspora , который был обновлен в 1992 году [13]. Позже, Microsporidia были сочтены примитивными простейшими , но молекулярный филогенетический анализ показал, что эти организмы не примитивны, а выродились.
В 2008 году считалось, что Microsporidia связаны с грибами как сестринская группа или базальная ветвь. [14] Биологи обратили свое внимание на Microsporidia шелкопряда и обнаружили, что похожие организмы во всем мире распространены среди различных видов животных, как правило, среди беспозвоночных и рыб, но также и среди людей.
Согласно последней классификации 2012 г., Microsporidia представляют собой одноклеточные эукариотические (протистовые) паразиты, принадлежащие к классу или супергруппе, включающим SAR.[2] Члены этой группы включают Stramenopila, Alveolata, Foraminifera, Cercozoa и Polycystinea. [2]
Морфология и жизненный цикл
Микроспоридии — это эукариотические облигатные внутриклеточные организмы, имеющие овальную форму под микроскопом и имеющие внутрицитоплазматическую мембранную систему ядерной оболочки и разделение хромосом на митотическом веретене. У микроспоридий нет пероксисом, но есть везикулярные тельца Гольджи и примитивная митохондриально-подобная органелла, отсутствующая в геноме, называемая митосомой.[15] Характеристики спор включают их различную форму и размер, и теперь эта характеристика используется для определения их таксонов. Споры преломлены и покрыты электронно-плотной белковой экзоспорой, электронно-просвечивающей эндоспорой и внутренней мембраной или плазмалеммой. [12]
Microsporidia производит экологически устойчивые споры из-за своей трубчатой формы, которая позволяет им выдавливать свою спиральную внутреннюю полярную трубку, тем самым инокулируя свое содержимое в ближайшего хозяина. [8] Благодаря своей электронной плотности, гликопротеиновой и хитиновой клеточной структуре, споры микроспоридий относительно нечувствительны к температуре, могут выжить при широкомасштабном засолении воды и химических веществах и сохраняться, несмотря на длительные периоды обезвоживания.
Жизненный цикл микроспоридии состоит из двух отдельных стадий: мерогония, или стадия пролиферации, и спорогония, или стадия инфицирования, или стадия созревания. Вкратце, жизненный цикл Microsporidia составляет:
- Споры попадают в хозяина при проглатывании или вдыхании. Происходит прорастание, приводящее к расширению полярной трубки и инъекции спороплазмы в цитоплазму клетки-хозяина через инъекционную трубку, известную как полярная трубка, уникальная специализированная инвазивная структура.Введенная спороплазма у некоторых видов также является частью гликокаликса. [15] Этот гликокаликс представляет собой структуру, которая проникает в клетки-хозяева и передает питание микроспоридиям.
- Спороплазма позже развивается в меронты, что является стадией пролиферации; здесь репликация происходит путем слияния с образованием многоядерных плазмодий. При этом клеточные мембраны меронта утолщаются и образуют споронты.
- Споронты делятся и развиваются в споробласт, который позже переходит в зрелую стадию спор без дополнительного размножения.Зрелая форма снабжена инъекционным аппаратом. Наличие инъекционного аппарата в споре является характеристикой, которая четко определяет микроспоридии как монофилетический таксон.
- Позже клетки-хозяева растягиваются зрелыми спорами, что приводит к разрыву и высвобождению спор во внешнюю среду или соседние клетки внутри тела. При однократном заражении Microsporidia может размножаться в многочисленные споры, создавая основу огромного репродуктивного потенциала, что приводит к их высокой патогенной способности.
Оценка
Microsporidia трудно обнаружить из-за их небольшого размера, медленно инфицирующих свойств, а иногда и бессимптомного инфицирования. Таким образом, во всем мире существует много неустановленных случаев диареи. Организм необходимо визуализировать с использованием специальных методов с привлечением специального лабораторного оборудования и обученного персонала для характеристики инфекции.
Обнаружение Microsporidia основано на исследовании кала под микроскопом.Однако новые методы окрашивания, включая окрашивание трихромом и флуоресцентное окрашивание с использованием оптических отбеливателей, могут оказаться полезными. Микроспоридии можно окрашивать окрашиванием по Граму, окрашиванием карбол-фуксином и окрашиванием серебром. [8]
Иммуноблоттинг, иммуноферментный анализ (ELISA) и иммунофлуоресцентный анализ (IFA) с использованием моноклональных и поликлональных антител также являются полезными серологическими анализами для характеристики микроспоридий. [8] Однако серологические тесты у людей с ВИЧ ненадежны из-за иммунодефицита.[6]
Молекулярная характеристика, включая полимеразную цепную реакцию (ПЦР) и нуклеотидное секвенирование, является многообещающим высокочувствительным анализом с чувствительностью более 90% для быстрой характеристики инфицированных человеком микроспоридий. Массив может одновременно обнаруживать все 4 вида Microsporidia с чувствительностью 10 спор на 100 микролитров образца фекалий. [8] В течение нескольких часов врач может интерпретировать результат путем выделения генетического / нуклеинового материала Microsporidia и ферментативного амплификации определенной последовательности в термоциклических условиях, а затем сравнить ее с контролем.Для определения генотипа микроспоридий у инфицированного хозяина последовательность рРНК является золотым стандартом для дальнейшей характеристики.
Анализы in vitro и in vivo также разработаны для размножения микроспоридий в исследовательских целях. Microsporidia обычно размножается в клетках или тканях насекомых или амплифицируется при инокуляции in vivo, например, рост N. bombycis в ткани яичников Bombyx mori и N . ceranae , привитые видам Apis или медоносной пчелой.[3] Исследования показывают, что Microsporidia из образцов, включая мочу, мокроту, бронхоальвеолярный лаваж, фекалии, двенадцатиперстную кишку, соскоб конъюнктивы, биопсию роговицы, спинномозговую жидкость, биопсию мышц и ткань мозга, могут расти в линиях клеток млекопитающих [16]. ] Такие паразиты, как Nosema algerae, , микроспоридийный паразит комаров, можно выращивать в лабораторных колониях и размножать в условиях in vitro в клеточной линии почек свиньи. In vitro культур рыб, Microsporidia были успешно продемонстрированы с использованием культур эпителиальных клеток Aedes albopictus при 28 ° C.Полезны анализы как in vivo, так и in vitro; однако эти методы требуют обученного персонала, соответствующих помещений и подходящего оборудования.
Лечение / менеджмент
Часто назначаемые препараты для лечения инфекции Microsporidia у животных и людей включают альбендазол и фумагиллин. В прошлом также испытывались органические соединения ртути, такие как Ноземак. Однако Ноземак был менее эффективен против паразитов и более токсичен для сельскохозяйственных пчел, чем фумагиллин.Фумагилин обладает амебицидными свойствами, и исследования in vivo показывают, что фумагиллин подавляет развитие Nosema apis у пчел. Альбендазол эффективен и действенен против видов Encephalitozoon , инфицирующих людей и животных, но имеет переменную эффективность против Enterocytozoon bieneusi. Альбендазол ингибирует полимеризацию тубулина, а также используется как глистогонное и противогрибковое средство. [7]
Дифференциальная диагностика
- Бактериальный гастроэнтерит
- Воспалительное заболевание кишечника
Улучшение результатов команды здравоохранения
Подобно другим патогенам и инфекционному контролю, Microsporidia следует лечить и предотвращать с помощью улучшенной гигиены.Улучшенное регулирование источников воды, а также мониторинг экскрементов в почве и воде важны для уменьшения передачи болезней, передающихся через воду. Решающее значение имеют строгое регулирование и процедура улучшения гигиены в производстве или производстве пищевой цепи, включая разведение, переработку, хранение и упаковку для контроля загрязнения пищевых продуктов и распространения патогенов.
(Щелкните изображение, чтобы увеличить)
Микроспоридум-легкий и ЭМ
Изображение предоставлено S Bhimji MD
Микроспоридиоз
Какие еще названия для этого состояния? (Также известен как / Синонимы)- Инфекция Microspora
- Инфекция Microsporan
- Инфекция Microsporidea
- Микроспоридиоз — это инфекция, вызванная группой внутриклеточных грибов, известных под общим названием микроспоридии.Передача инфекции человеку происходит через загрязненную воду
- Микроспоридии — очень большое семейство паразитических грибов, для которых характерно образование спор. Споры представляют собой одноклеточные размножающиеся формы грибов, которые обладают высокой устойчивостью к разрушению. В эту классификацию включено более 1200 видов.
- Известно, что 15 видов микроспоридий инфицировали людей. Известно, что каждый из этих видов инфицирует определенные типы тканей и, следовательно, проявляет широкий спектр видоспецифичных симптомов
- Однако, как сообщается, диарея и боль в животе являются общими для большинства инфекций.Поставщик медицинских услуг обычно диагностирует микроспоридиоз при исследовании образца стула.
- Меры лечения могут включать комбинацию антипаразитарных и противомикробных препаратов, чтобы помочь пострадавшему. После заражения людям часто требуется пожизненное лечение симптомов.
- Однако прогноз микроспоридиоза обычно благоприятный при адекватном лечении. Методы профилактики микроспоридиоза четко не указаны
- Люди всех возрастов, рас, этнических групп и полов подвержены заражению различными формами микроспоридиоза
- Сообщается о микроспоридиозе в той или иной форме, такой как желудочно-кишечный, глазной, респираторный и мочеполовой тракт Микроспоридиоз во всех регионах мира
Хотя микроспоридиоз может развиться у любого человека, риск заражения инфекцией наиболее высок у людей с ослабленным иммунитетом, что может происходить из-за таких состояний, как:
- ВИЧ-инфекция и СПИД
- Принятие лекарств для иммунитета подавление (например, во время трансплантации органов)
- Химиотерапия и / или лучевая терапия для лечения рака
Важно отметить, что наличие фактора риска не означает, что человек получит заболевание.Фактор риска увеличивает шансы получить заболевание по сравнению с человеком без факторов риска. Некоторые факторы риска важнее других.
Кроме того, отсутствие фактора риска не означает, что человек не заболеет этим заболеванием. Всегда важно обсудить влияние факторов риска с вашим лечащим врачом.
Каковы причины микроспоридиоза? (Этиология)Микроспоридиоз вызывается инфекцией и быстрым распространением споровой формы Microsporidia, грибкового паразита, в организме человека-хозяина.
- Микроспоридии распространяются в форме устойчивых спор (одноклеточный организм, способный выживать в течение продолжительных периодов времени в суровых условиях, прежде чем перейти к стадии размножения)
- Эти паразиты имеют характерные полярные канальцы (очень похожие на выдвижная рука), которую они могут выступать из себя и использовать для проникновения в клетки людей, которых они заразили. Грибы используют эту руку для распространения и размножения внутри клеток своего хозяина
- Известно, что эти грибы в первую очередь заражают насекомых, но контакт человека с загрязненной спорами водой может способствовать распространению микроспоридий среди людей-хозяев
- 15 видов Известно, что у микроспоридий есть человеческие хозяева.Заражение разных частей тела происходит в зависимости от конкретного вида. Из 15 6 наиболее распространенных видов заражают следующие области человеческого организма-хозяина:
- Anncaliia algerae — инфекция кожи или глубоких мышц
- Anncaliia connori — глазная (относящаяся к глазу) инфекция
- Encephalitozoon cuniculi — респираторные и мочеполовые инфекции
- Encephalitozoon heliem — респираторные и мочеполовые инфекции
- Encephalitozoon Кишечник — Инфекция желудочно-кишечного тракта или желудочно-кишечного тракта, которая может распространяться на глазные, мочеполовые и респираторные системы инфекция тракта
Из-за широкого спектра видов микроспоридий, которые потенциально могут вызывать микроспоридиоз, симптомы этой инфекции могут различаться по типу и степени тяжести среди пораженных людей.Диарея характерна для большинства типов инфекций.
Симптомы, характерные для 6 распространенных микроспоридиальных инфекций, включают:
- Anncaliia algerae
- Инфекция кожи
- Инфекция глаз, вызывающая кератоконъюнктивит (воспаление роговицы глаза), вызывающая ощущение инородного тела, боль в глазах, светочувствительность, покраснение, слезотечение или помутнение зрения
- Миозит (воспаление мышечной ткани от легкого до сильного)
- Anncaliia connori
- Сердечно-сосудистые инфекции могут вызывать сердечную недостаточность
- Инфекции почечной системы могут вызывать почечную недостаточность или другие нарушения мочевого баланса
- Инфекции эндокринной системы могут вызывать гормональный дисбаланс
- Распространенные или широко распространенные инфекции (включая кровоток) могут вызывать различные заболевания, связанные с кровью
- Encephalitozoon cuniculi
- Церебральные инфекции, вызывающие судороги ion
- Распространенные или широко распространенные инфекции (вовлекающие кровоток) могут вызывать различные заболевания, связанные с кровью
- Encephalitozoon hellem
- Инфекция глаз, носовых пазух и тканей носа может вызвать кератоконъюнктивит, который может вызвать инородный ощущения тела, боль в глазах, светочувствительность, покраснение, чрезмерное слезотечение или помутнение зрения
- Респираторные инфекции могут вызывать затруднение дыхания
- Распространенные или широко распространенные инфекции (включая кровоток) могут вызывать различные заболевания, связанные с кровью
- Encephalitozoonestiveis
- Инфекция эпителия кишечника может вызвать диарею, мальабсорбцию и истощение (включая потерю веса)
- Инфекция печени, которая может вызвать желтуху
- Инфекция почечной системы
- Инфекция толстой кишки , желчный пузырь
- Инфекция легких 900 03 Инфекция конъюнктивы (мембрана, покрывающая инфекции глаз / век) и носовых пазух, которая может вызвать кератоконъюнктивит, который приводит к ощущению инородного тела, боли в глазах, светочувствительности, покраснению, чрезмерному слезотечению или помутнению зрения Vittaforma corneae
- Инфекция глаза, приводящая к кератоконъюнктивиту, вызывающему ощущение инородного тела, боль в глазах, светочувствительность, покраснение, слезотечение или помутнение зрения
Диагноз микроспоридиоза ставится на основании следующих данных:
- Полный медицинский осмотр и оценка симптомов
- Оценка истории болезни
- Исследование фекалий инфицированного человека с помощью световой микроскопии.Обычно это делается с помощью химического окрашивания, которое позволяет дифференцировать ядерный и цитоплазматический материал
Хотя в большинстве случаев идентификации паразита может быть достаточно для лечебных целей, для определения конкретных видов микроспоридий, присутствующих у инфицированного человека, может потребоваться дополнительный анализ. . К ним могут относиться:
- Просвечивающая электронная микроскопия (ТЕМ): метод микроскопии с разрешением до 10 000 раз больше, чем у светового микроскопа.Характеристика конкретных видов микроспоридий в основном основана на количестве, расположении и расположении ветвей полярных канальцев. Однако ТЕА является дорогостоящим и трудоемким, поэтому часто не используется, если это не считается необходимым.
- Полимеразная цепная реакция (ПЦР), в которой видоспецифический образец ДНК амплифицируется для исследования, может использоваться для идентификации видов микроспоридий, которые участвует
- Иммунофлуоресценция, при которой используются флуоресцентные антитела для связывания белков, характерных для конкретных видов микроспоридиальных инфекций.
Многие клинические состояния могут иметь похожие признаки и симптомы.Ваш лечащий врач может провести дополнительный тест, чтобы исключить другие клинические состояния и поставить окончательный диагноз.
Каковы возможные осложнения микроспоридиоза?Возможные осложнения микроспоридиоза могут включать:
- Непоправимый ущерб, нанесенный инфицированным системам органов из-за задержки или отсутствия лечения
- Слепота
- Могут быть затронуты следующие органы:
Тяжелая органная недостаточность наряду с сопутствующие осложнения могут быть фатальными.
Как лечится микроспоридиоз?Лечение микроспоридиоза часто бывает сложным, и полное искоренение микроспоридий с помощью медикаментозного лечения достигается редко. Из-за широкого спектра инфекций и симптомов, связанных с микроспоридиозом, лекарства, отпускаемые по рецепту, обычно нацелены на определенные типы инфекции и сочетаются с лекарствами, используемыми для лечения симптомов микроспоридиоза.
Обычно используются следующие типы лекарств:
- Глистогонное средство для приема внутрь.Хотя глистогонные средства используются для уничтожения паразитических червей, они могут применяться при микроспоридиозе для облегчения таких симптомов, как стойкая диарея. Примеры глистогонных препаратов включают альбендазол
- Пероральный препарат фумагиллин, противомикробный препарат, может быть назначен при желудочно-кишечных симптомах
- При глазных симптомах глазные капли, содержащие альбендазол и / или фумагиллин бицилогексиламмоний, могут быть назначены для облегчения симптомов
- . капли неэффективны, для восстановления пораженной роговицы может потребоваться хирургическое вмешательство.
- Антиретровирусное лечение является основным лечением для людей с подавленным / ослабленным иммунитетом, инфицированных микроспоридиями.Это может помочь им восстановить свою иммунную систему и позволить им лучше бороться с инфекцией
- Некоторым больным с ослабленным иммунитетом может помочь терапия альбендазолом
Профилактика микроспоридиоза может быть возможна путем фильтрации всех форм воды, предназначенной для потребления (особенно в районах с низким уровнем регулирования источников питьевой воды), поскольку микроспоридии передаются через воду.
Каков прогноз микроспоридиоза? (Результаты / решения)Прогноз микроспоридиоза следующий:
- Лечение может быть успешным в снижении инфицирования микроспоридиозом, если его лечить на ранней стадии. Полное искоренение микроспоридий с помощью медикаментозного лечения бывает редко
- Микроспоридиоз часто требует длительного лечения, а рецидивирующие симптомы часто требуют повторного лечения
- Без лечения тяжелая инфекция может привести к отказу систем органов, что приведет к смерти от осложнения
- Агентство по охране окружающей среды США (EPA) официально включило микроспоридии в список кандидатов на загрязнение (CCL) EPA
- Споры микроспоридий имеют микроскопические размеры, имеют круглой аморфной формы и имеют характерный полярный каналец, выступающий из центрального тела.Полярный каналец типа микроспор уникален для паразитов микроспоридий. Никакие другие известные организмы не обладают этой функцией.
- Только недавно было обнаружено, что микроспоридиоз присутствует у иммунокомпетентных людей (людей с нормально функционирующей иммунной системой). Однако у здоровых людей эта инфекция все еще встречается крайне редко.
Легочная инфекция микроспоридиями после аллогенной трансплантации костного мозга
Микроспоридии являются облигатными эукариотическими внутриклеточными протозойными паразитами Phylum Microspora.Микроспоридиоз (заражение микроспоридиями) был продемонстрирован у большого числа видов позвоночных и беспозвоночных. У людей восемь из 150 родов вызывают заболевания (Brachiola, Enterocytozoon, Encephalitozoon, Nosema, Pleistophora, Septata, Trachipleistophora и Vittaforma.) 1000 видов в филуме. 3
Способ передачи микроспоридий неизвестен.Микроспоридии попадают в окружающую среду с калом, мочой и респираторными выделениями инфицированных животных. Неизвестно, передаются ли люди инфекции от человека к контакту с человеком, окружающей средой, другими млекопитающими или насекомыми. 3 Неясно, является ли инфекция у лиц с ослабленным иммунитетом вновь приобретенной инфекцией или реактивацией латентной инфекции, приобретенной до иммуносупрессии. 13 Следует отметить, что микроспоридиум вида Encephalitozoon cuniculli III обнаружен у собак, а у нашего пациента были собаки, а также кошки и крысы.
Микроспоридии могут вызывать широкий спектр заболеваний. 3 У большинства пациентов инфекция ограничена желудочно-кишечным трактом и желчевыводящими путями. У пациентов с ослабленным иммунитетом может развиться хроническая тяжелая некровятая немукоидная диарея с потерей веса и мальабсорбцией жира или гепатитом и перитонитом. Другие распространенные проявления микроспоридиальной инфекции включают кератоконъюнктивит, синусит, инфекцию мочевыводящих путей, миозит и инфекции нижних дыхательных путей. В редких случаях у пациентов могут развиться церебральные инфекции, уретрит, кожные инфекции, остеомиелит и абсцессы.Легочные инфекции были обнаружены в основном с микроспоридиями из рода Encephalitozoon. Большинство пациентов с инфекциями дыхательных путей также страдают системным или кишечным микроспоридиозом, но существуют отдельные случаи поражения легких. 3,14 К сожалению, данные о распространенности микроспоридиальной колонизации легких не известны.
Наш пациент и ранее описанный пациент с BMT отличаются от большинства пациентов с ВИЧ тем, что у обоих было первичное легочное заболевание. У пациентов с ВИЧ желудочно-кишечные заболевания являются наиболее частым проявлением, а изолированное заболевание легких встречается редко. 3,4 Поражение желудочно-кишечного тракта также было обнаружено после трансплантации солидных органов. И у нашего пациента, и у другого пациента с ТКМ были желудочно-кишечные симптомы с паралитической кишечной непроходимостью, но биопсия желудочно-кишечного тракта дала отрицательный результат на микроспоридии. Кроме того, у обоих пациентов с трансплантацией костного мозга было обнаружено несколько патогенов в легких. Неизвестно, какой организм вызвал большинство симптомов у каждого пациента; однако было отмечено гораздо большее количество микроспоридий по сравнению с другими патогенами.Возможно, что между организмами существовал синергетический или аддитивный эффект, или что один организм служил воротами входа для другого, вызывая повреждение паренхимы легких. Неизвестно, были ли у нашего пациента микроспоридии в других тканях за пределами пищевода, сигмовидной кишки и легких, поскольку вскрытие не проводилось.
Просвечивающая электронная микроскопия (ПЭМ) образцов тканей должна использоваться для подтверждения диагноза микроспоридиоза. 15 К сожалению, ПЭМ дорог, трудоемок и требует много времени.ПЭМ также менее чувствительна, чем световая микроскопия и цитология, при исследовании кала или мочи. Световая микроскопия образцов ткани, залитых пластиком, с использованием различных специальных красителей (толуидиновый синий, модифицированный трихром, коричневый по Бренну, Вартин-звездчатый) может дать довольно чувствительные и специфические результаты при использовании в комбинации. 15 Световая микроскопия и цитология кала, мочи, бронхоальвеолярного лаважа и спинномозговой жидкости достаточно надежны; однако это менее чувствительные и специфические диагностические инструменты.Самый простой метод, используемый для диагностики микроспоридиоза у пациентов с желудочно-кишечными заболеваниями, — это исследование образцов кала с помощью светового микроскопа, но для этого требуются несколько образцов и специальные методы, включая осаждение и концентрацию спор. 3 К сожалению, ни световая микроскопия, ни электронная микроскопия не помогают при видообразовании. Молекулярный анализ необходим для видообразования, но доступен только в исследовательских целях.
Следует отметить, что изначально предполагалось, что у нашего пациента токсоплазмоз.Токсоплазма и микроспоридии являются внутриклеточными организмами схожего размера и внешнего вида, но их можно различить с помощью иммуногистохимических и специальных красителей. В частности, микроспоридии хорошо окрашиваются модификацией Брауна – Бренна окраски по Граму, 15 , в то время как токсоплазмы — нет. Поскольку многие патологи могут не учитывать микроспоридии при дифференциальной диагностике легочных инфекций у пациентов с трансплантатом, было бы важно предложить специальное окрашивание на микроспоридии, если у реципиента трансплантата диагностирован токсоплазмоз при биопсии.
Результаты лечения микроспоридиоза антимикробными препаратами плохие. Было показано, что альбендазол полезен при лечении симптомов и лишь в редких случаях излечивает заболевание у пациентов с желудочно-кишечными инфекциями, вызванными Encephalitozoonestiveis . 16 Недавно в двойном слепом плацебо-контролируемом исследовании 10 сравнивали фумагиллин с контролем у 12 пациентов с ослабленным иммунитетом и кишечным микроспоридиозом с видами Enterocytozoon bieneusi и обнаружили заметное улучшение симптомов и устранение микроорганизмов при культивировании стула.



 Обломки волос достигают длины 10-15 мм и не имеют серых чехлов из спор грибка.
Обломки волос достигают длины 10-15 мм и не имеют серых чехлов из спор грибка. Для детей до 3 лет выпускается в виде суспензии.
Для детей до 3 лет выпускается в виде суспензии.