Анализы на вирус Эпштейн-Барр — цена в Санкт-Петербурге, сдать кровь на анализ в СЗЦДМ
Вирус Эпштейна-Барр (далее — ВЭБ), официально — Human gammaherpesvirus 4, — один из 8 известных науке типов герпесвирусов и, с высокой вероятностью, самый распространённый вирус человека.
Например, в США у более 90 % взрослых и 50 % детей есть признаки инфицирования ВЭБ. Американские врачи считают, что оставшиеся 10 % взрослых просто не обследованы. В России медики определяют уровень инфицированности взрослого населения 97 %.
Медики предполагают, что всё взрослое население земли заражено вирусом, потому что передаётся он чрезвычайно просто — со слюной (при поцелуе, пользовании общей посудой, чихании, когда вы делитесь пищей, которую уже откусили) и генитальным секретом, а сохраняется в организме до конца жизни. Выявлены случаи передачи вируса с кровью при её переливании и бытовом попадании «кровь в кровь».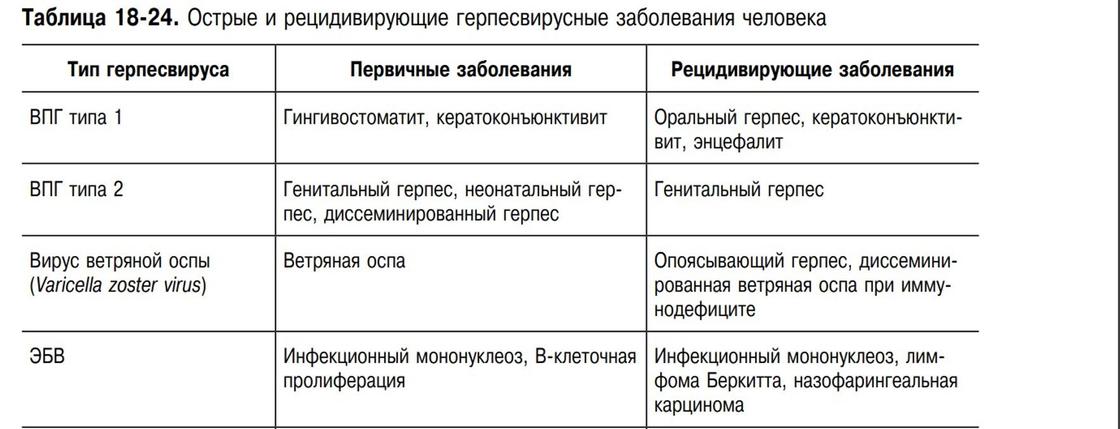
Особый случай — инфицирование при пересадке органов. В связи с распространением трансплантаций подобные инфекции встречаются всё чаще и вызывают нетипичные осложнения и заболевания после трансплантации.
У большинства людей ВЭБ «хранится» в клетках в латентной форме и активируется при благоприятных ему условиях — критическом снижении иммунитета, стрессе, другом заболевании и т. д. Но часто реактивация происходит без видимых причин — учёным только предстоит выявить её причины.
Опасность вируса в том, что в активной форме он становится причиной инфекционного мононуклеоза, связан с возникновением лимфомы Беркитта, гемофагоцитарного лимфогистиоцитоза, лимфомы Ходжкина, рака желудка, рака носоглотки, лимфомы центральной нервной системы, синдрома Алисы в стране чудес (нарушение восприятия), острой мозжечковой атаксии (нарушение походки, движений).
По данным, полученным врачами Cincinnati Children’s Hospital Medical Center — Медицинского центра Цинцинатти (США), ВЭБ может послужить причиной развития рассеянного склероза, целиакии, системной красной волчанки, диабета I типа, ювенильного идиопатического артрита, ревматоидного артрита. Даже хроническая усталость человека связана напрямую с ним.
Даже хроническая усталость человека связана напрямую с ним.
Перейти к анализам
У большинства людей заражение вирусом происходит бессимптомно или с незначительными проявлениями, которые быстро проходят. Организм вырабатывает к вирусу стойкий иммунитет, и человек живёт с «законсервированным» в клетке вирусом всю жизнь.
Но анализ на ВЭБ часто необходим, чтобы отличить одну инфекцию от другой и назначить эффективное лечение. Вирус «маскируется» под ОРВИ, гепатит, ангину с устойчиво высокой температурой (до 10 % всех случаев ангины), при которой увеличиваются лимфоузлы. В большинстве случаев ВЭБ вызывает инфекционный мононуклеоз. Особенно реактивна инфекция у подростков и в возрасте до 5 лет, причём у мальчиков она проходит в острой форме в 2 раза чаще, чем у девочек.
Симптомы заражения при постепенном развитии:
-
ухудшается самочувствие;
-
температура повышается до субфебрильных показателей — 37,1—38,0 °C;
-
появляются катаральные симптомы — отёчность носа и носоглотки, заложенность, слизистая носоглотки становится красной, нёбные миндалины тоже краснеют;
-
лимфатические узлы — подчелюстные, на затылке, шее) отёчные, на ранней стадии — неболезненные или со слабыми болезненными ощущениями.

Симптомы заражения при остром начале болезни:
-
резкое повышение температуры до 38—39 °C;
-
лихорадка с ознобом и повышенным потоотделением;
-
головная боль;
-
боль в скелетных мышцах;
-
боль в горле при сглатывании;
-
увеличение лимфоузлов.
У заражённых увеличиваются селезёнка, печень, появляется сыпь на 3—5 день. Иногда увеличенная селезёнка разрывается.
Однако единой, характерной симптоматики не существует — признаки заражения учёные объединили в «мононуклеозоподобный синдром». Потому при любых проявлениях необходимо сдать анализы на обнаружение вируса.
Направление на анализы даёт терапевт, инфекционист, врач общей практики, педиатр. Исследование проводится на различном биоматериале — сыворотке крови, мазках и соскобах слизистой ротоглотки, урогенитального тракта, слюне, цереброспинальной жидкости, лейкоцитах периферической крови.
Исследование проводится на различном биоматериале — сыворотке крови, мазках и соскобах слизистой ротоглотки, урогенитального тракта, слюне, цереброспинальной жидкости, лейкоцитах периферической крови.
Для выявления инфекции чаще прочего проводят серологические тесты. Однако часто требуется комплексное тестирование, потому что серологические тесты в случаях переливания крови, иммунодефицита и некоторых других противоречат друг другу. Точную клиническую картину в сложных случаях даёт ПЦР-диагностика на ДНК ВЭБ.
Вирус определяется только лабораторными способами, причём в большинстве случаев требуется несколько тестов, чтобы исключить прочие инфекционные заболевания.
Общий анализ крови на вирус Эпштейна-Барр
Общий анализ крови не позволяет установить точно ВЭБ. Определение лейкоцитоза, лимфоцитоза, атипичных мононуклеаров свидетельствует лишь о наличии инфекционного заболевания, но не даёт его идентифицировать.
Если общий анализ крови вызывает подозрения на ВЭБ, проводят дополнительные исследования.
Биохимический анализ
В биохимическом анализе при инфицировании ВЭБ наблюдают:
-
повышение АЛТ, или аланинаминотрансферазы, — фермента печени, почек, поджелудочной железы;
-
повышение АСТ, или аспартатаминотрансферазы, — фермент преимущественно клеток сердца и печени;
-
повышение ЩФ, или щелочной фосфатазы;
-
повышение билирубина — главного компонента желчи;
-
понижение нейтрофилов;
-
понижение тромбоцитов.

Изменение биохимических показателей печени характерны для 90 % инфицированных.
Гетерофильный тест
Гетерофильный тест, или реакция Пауля и Буннеля, основана на определении в сыворотке крови противобараньих агглютининов. Тест выявляет гетерофильные антитела, и при титре 1:224 ставится диагноз мононуклеоза.
Гетерофильный тест даёт положительный результат у 60 % инфицированных спустя 2 недели после обнаружения симптомов и у 90 % инфицированных спустя месяц после первых клинических проявлений. Потому точность его невелика, а на начальной стадии он не помогает определить ВЭБ, т. к. титр гетерофильных тел повышается и в ответе на другую вирусную инфекцию.
Чувствительность теста у детей составляет менее 70 %, а способность идентифицировать вирус — менее 20 %. С возрастом пациентов польза теста и его чувствительность/специфичность увеличиваются.
Серологические исследования
Жизнедеятельность ВЭБ в организме (завершённый и незавершённый литический (активный) цикл, латентная фаза) происходит на фоне выработки специфических антител к белкам вируса. Исследование антител позволяет определить и дифференцировать острую форму, перенесённую инфекцию и хроническую инфекцию вирусом.
Исследование антител позволяет определить и дифференцировать острую форму, перенесённую инфекцию и хроническую инфекцию вирусом.
На ранних стадиях (3—4 недели после заражения и до 3—4 месяцев после) определяются иммуноглобулины IgG к ранним антигенам EA — их считают маркерами острой стадии инфекции, хотя нередко они выявляются и при хроническом инфицировании.
Иммуноглобулины IgG к VCA — капсидному белку — определяются в момент проявления болезни и считаются маркерами острого стадии болезни. Они пропадают через несколько недель. Однако есть люди, у которых VCA-IgM не определяются, потому всегда необходимо комплексное тестирование.
Антиген EBNA IgG не определяется на начальной стадии заболевания, потому свидетельствует о перенесённой или хронической инфекции. Последняя отличается высоким титром антигена.
ПЦР диагностика
ПЦР-диагностика относится к высокочувствительным тестам при инфицировании ВЭБ. Для её проведения используют лейкоцитарную фракцию крови.
Для её проведения используют лейкоцитарную фракцию крови.
Если ДНК вируса выявляется в плазме крови, то ставится диагноз инфекции в активной форме. ДНК вируса выявляется даже в период латентной фазы у людей, признанных клинически здоровыми — 0,1–1 копий/106 клеток. Хроническая и острая стадия выявляются количественной ПЦР.
Если вирусная нагрузка высока, она может ассоциироваться с большим риском тяжёлых осложнений и требует антивирусной терапии. ДНК в ликворе говорит, что вирус активно размножается в нервной системе — эту ПЦР-диагностику ВЭБ проводят, когда выявляют этиологию поражения нервной системы.
ПЦР проводят при выявлении опухолей, тяжёлых осложнений. В этом случае ДНК вируса обнаруживают в лимфоузлах, слизистой кишечника, биоптатах печени. ПЦР необходимо и при заболеваниях, возникших после трансплантации органов.
Однако отрицательный результат ПЦР-диагностики не исключает репликации вируса в лимфоузлах, костном мозге, дерме, желудке и кишечнике. Потому ПЦР рекомендовано использовать всегда в сочетании с серологическими методами диагностики ВЭБ.
Потому ПЦР рекомендовано использовать всегда в сочетании с серологическими методами диагностики ВЭБ.
Не заразиться ВЭБ в современном мире почти невозможно. Для этого пришлось бы исключить всякие контакты с людьми, причём с рождения, никого не целовать, не вступать в сексуальные отношения.
Как ни парадоксально, но лучше, если заражение случится в детском возрасте, потому что дети легче переносят инфекцию (как, к примеру, и ветряную оспу, вызванную также герпесвирусом, только 3 типа), у них вырабатывается стойкий иммунитет.
Инфицирование в детстве характерно для стран с низким уровнем жизни, в подростковом и взрослом — с высоким уровнем жизни. Играет роль санитарная культура, общая культура людей. Но она же приводит и к более серьёзным последствиям инфекции, потому что иммунный ответ человека, живущего в благоприятных условиях, намного слабее.
Только иммунитет способен защитить нас от вируса Эпштейна-Барр. Попав в организм, он сохраняется в нас до конца жизни в латентной фазе. Снижение иммунитета, вызванное заболеваниями, образом жизни, ведёт к реактивации ВЭБ и непредсказуемым последствиям — учёным пока удалось только выявить ассоциированные с вирусом заболевания (о чём мы говорили вначале), но не установить закономерность их развития.
Попав в организм, он сохраняется в нас до конца жизни в латентной фазе. Снижение иммунитета, вызванное заболеваниями, образом жизни, ведёт к реактивации ВЭБ и непредсказуемым последствиям — учёным пока удалось только выявить ассоциированные с вирусом заболевания (о чём мы говорили вначале), но не установить закономерность их развития.
Инфекции против ВЭБ также не существует. Обезопасить себя можно хотя бы от повторного заражения, не целуясь, не пользуясь чужой посудой, едой, зубными щётками и другими личными вещами.
При появлении каких-либо симптомов заболевания следует обратиться к врачу или самостоятельно прийти в лабораторию, чтобы сдать анализы на выявление ВЭБ.
Если заражение обнаружено (острая фаза), то нужно отказаться от выхода на работу, посещения общественных мест, потому что вы становитесь распространителем инфекции, обеспечить себе покой, обильное питьё, хорошо питаться. При возникновении тяжёлых симптомов следует немедленно обратиться к врачу — будет назначено симптоматическое лечение, поддерживающая терапия.
В обычной жизни хорошей профилактикой станет укрепление иммунитета — спорт, здоровый образ жизни, отказ от ежедневного применения дезинфицирующих средств, например — спиртовых гелей, антибактериального мыла и подобных. Ваш иммунитет должен ежедневно испытывать напряжение, чтобы «оставаться в форме», а иммунный ответ был высоким.
В АО «СЗДЦМ» вы сможете пройти все тесты на определение ВЭБ по низкой цене. Так как диагностика в большинстве случаев требует комплексного тестирования, исследования в медицинских центрах и лабораторных терминалах АО «СЗДЦМ» не станет финансово обременительным для вас — стоимость услуги в наших медучреждениях доступна для всех категорий населения.
Наши врачи-специалисты назначат вам только необходимые анализы, которые позволят поставить точный диагноз. Первое исследование и общий анализ крови можно сделать и без назначения врача, но последующие (если будут подозрения) мы рекомендуем делать только по назначению, чтобы не проводить бесполезных в вашем случае тестов.
Сдать любые анализы на ВЭБ вы можете в наших медицинских центрах и лабораторных терминалах. Выбрать ближайшее к вам медучреждение можно по карте, таблице или выпадающему меню.
Рядом с названием медучреждения вы увидите точный адрес, часы работы, а по карте легко составить маршрут для посещения лаборатории на общественном транспорте или личном автомобиле.
Вирус Эпштейна-Барр: диагностика инфекционного мононуклеоза
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна-Барр относится к семейству герпесвирусов, подсемейство g-герпесвирусов — вирус герпеса человека IV типа. Вирусная частица состоит из нуклеоида, капсида и оболочки.
Вирусная частица состоит из нуклеоида, капсида и оболочки.
Нуклеоид содержит двухцепочечную ДНК, он окружен капсидом, состоящим из белковых субъединиц. Нуклеоид и капсид (нуклеокапсид) окружены липидсодержащей внешней оболочкой, образующейся из ядерной или наружной мембраны клетки-хозяина, в которую ещё до начала сборки вирусной частицы встраиваются некоторые вирусные белки.
При инфицировании вирус проникает в эпителий ротоглотки и слюнных желёз человека и вызывает активную инфекцию с лизисом клеток и высвобождением вирусных частиц, в результате чего вирус обнаруживается в слюне. Кроме того, он может проникать в В-лимфоциты и эпителий носоглотки и вызывать латентную инфекцию. Вирус Эпштейна-Барр можно обнаружить в оральных секретах здоровых, но латентно инфицированных людей. Вирус тропен к В-лимфоцитам, Т-лимфоциты он не поражает. Проникнув в лимфоциты, вирус Эпштейна-Барр может вызывать их трансформацию, в результате которой образуются способные к неограниченной пролиферации клоны атипичных лимфоцитов, содержащие кольцевую вирусную ДНК в виде плазмиды.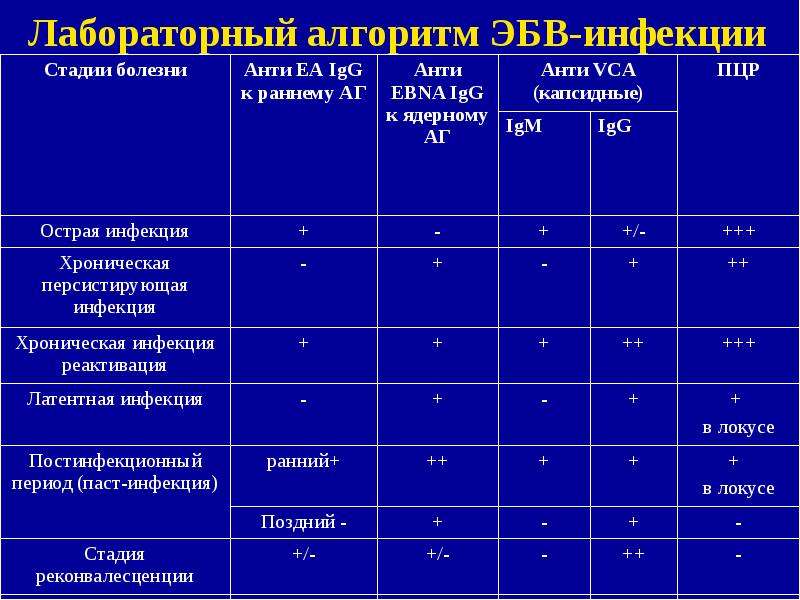 Рецептором вируса на эпителиальных клетках и В-лимфоцитах служит молекула CD21, которая служит также рецептором фрагмента комплемента C3d. Вирус запускает как гуморальный, так и клеточный ответ. Среди образующихся антител есть специфические к антигенам вируса и неспецифические, гетерофильные. Последние появляются в результате поликлональной активации В-лимфоцитов (это может быть причиной интерференции при проведении ряда серологических исследований у людей с активной инфекцией вирусом Эпштейна-Барр). Главную роль в элиминации данной инфекции играет клеточный иммунитет. При острой инфекции первичная репродукция вируса в В-лимфоцитах сменяется выраженной пролиферацией Т-лимфоцитов с соотношением CD4/CD8 меньше 1.
Рецептором вируса на эпителиальных клетках и В-лимфоцитах служит молекула CD21, которая служит также рецептором фрагмента комплемента C3d. Вирус запускает как гуморальный, так и клеточный ответ. Среди образующихся антител есть специфические к антигенам вируса и неспецифические, гетерофильные. Последние появляются в результате поликлональной активации В-лимфоцитов (это может быть причиной интерференции при проведении ряда серологических исследований у людей с активной инфекцией вирусом Эпштейна-Барр). Главную роль в элиминации данной инфекции играет клеточный иммунитет. При острой инфекции первичная репродукция вируса в В-лимфоцитах сменяется выраженной пролиферацией Т-лимфоцитов с соотношением CD4/CD8 меньше 1.
Острая инфекция вирусом Эпштейна-Барр известна под названиями инфекционный мононуклеоз, болезнь Филатова, моноцитарная ангина, идиопатическая железистая лихорадка, болезнь Афейффера, острый доброкачественный лимфобластоз.
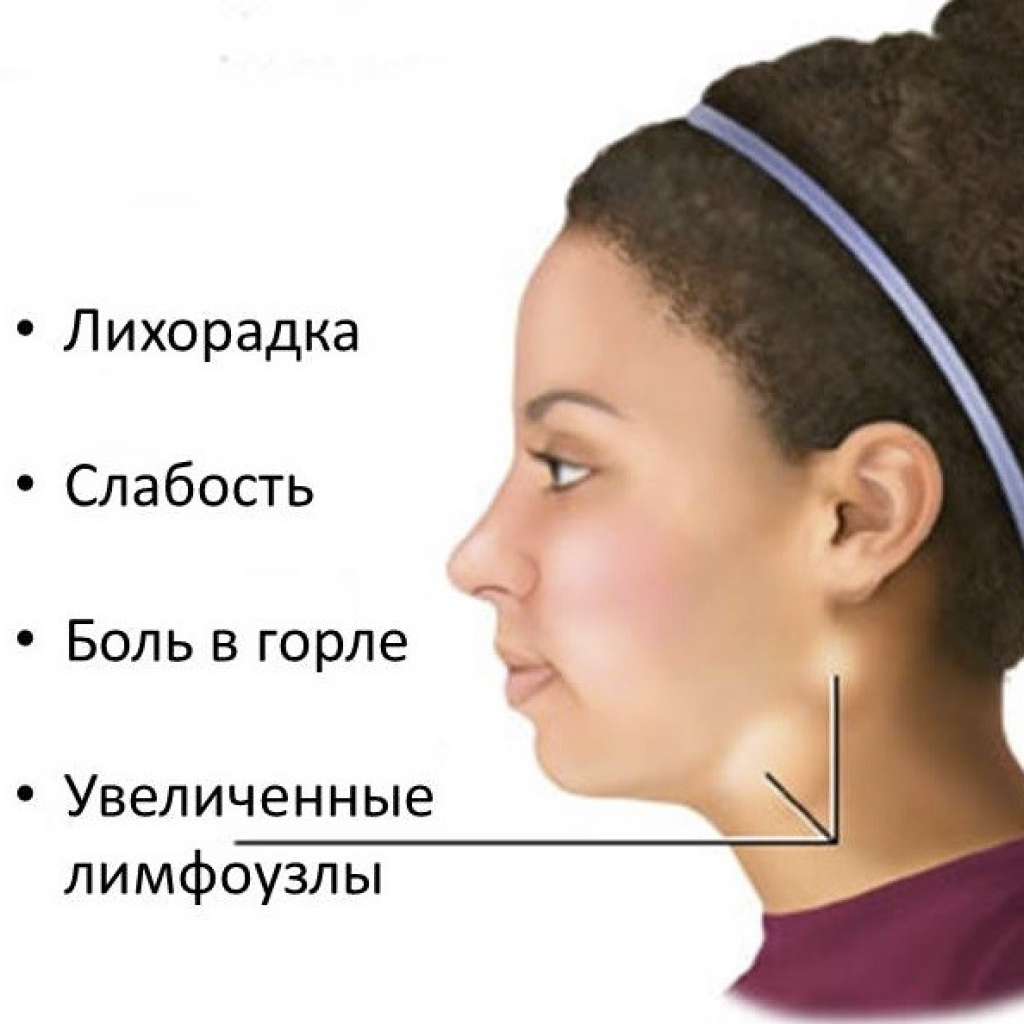
Вирус Эпштейна-Барр — главная причина мононуклеоподобного синдрома (хотя острая первичная инфекция, вызванная этим вирусом, и инфекционный мононуклеоз не являются синонимами). Для острой инфекции характерно повышение температуры, боли в горле и увеличение заднешейных лимфоузлов (реже – переднешейных и локтевых, встречается генерализованное увеличение лимфоузлов). В 50% случаев выявляется увеличение селезенки, в 10 — 30% случаев – увеличение печени. Другими проявлениями инфекции могут быть сыпь и периорбитальный отек. Изредка наблюдаются осложнения, в том числе, неврологические, изменения со стороны системы крови в виде гемолитической или апластической анемии, нейтропении, тромбоцитопении. После перенесённого заболевания иногда подолгу сохраняется фарингит, увеличение лимфоузлов, утомляемость и неспособность концентрации внимания.
Для острой инфекции характерно повышение температуры, боли в горле и увеличение заднешейных лимфоузлов (реже – переднешейных и локтевых, встречается генерализованное увеличение лимфоузлов). В 50% случаев выявляется увеличение селезенки, в 10 — 30% случаев – увеличение печени. Другими проявлениями инфекции могут быть сыпь и периорбитальный отек. Изредка наблюдаются осложнения, в том числе, неврологические, изменения со стороны системы крови в виде гемолитической или апластической анемии, нейтропении, тромбоцитопении. После перенесённого заболевания иногда подолгу сохраняется фарингит, увеличение лимфоузлов, утомляемость и неспособность концентрации внимания.
Заболевание малоконтагиозно. Инкубационный период (период активного размножения и распространения вируса по всей лимфоидной ткани) может длиться от 30 до 50 суток. Инфицирование данным вирусом в любом возрасте, а у детей особенно, в большинстве случаев может протекать бессимптомно или как респираторная инфекция. Доля серопозитивных лиц (имеющих специфические антитела к антигенам вируса) уже среди подростков в разных странах составляет от 50 до 90%, среди взрослых людей серологические признаки инфекции обнаруживаются почти в 100% случаев. Вирус выделяется со слюной, передается через поцелуи и другие контакты слизистой со слюной или загрязнёнными ею предметами. Трансплацентарная передача вируса происходит редко. Иммунитет при инфекционном мононуклеозе стойкий.
Доля серопозитивных лиц (имеющих специфические антитела к антигенам вируса) уже среди подростков в разных странах составляет от 50 до 90%, среди взрослых людей серологические признаки инфекции обнаруживаются почти в 100% случаев. Вирус выделяется со слюной, передается через поцелуи и другие контакты слизистой со слюной или загрязнёнными ею предметами. Трансплацентарная передача вируса происходит редко. Иммунитет при инфекционном мононуклеозе стойкий.
Хотя канцерогенность вируса окончательно не доказана, есть основания полагать, что он может играть роль в развитии ряда злокачественных новообразований – лимфомы Беркитта, рака носоглотки, лимфогранулематоза и ряда посттрансплантационных лимфопролиферативных синдромов. На фоне нарушения клеточного иммунитета (СПИД, иммуносупрессия при трансплантации и пр.) вирус Эпштейна — Барр может вызывать инфекционный мононуклеоз с летальным исходом или лимфопролиферативные синдромы с развитием В-клеточных лимфом.
Лабораторная диагностика инфекционного мононуклеоза
Диагностика инфекционного мононуклеоза основывается на клинической картине, характерных изменениях в клиническом анализе крови (в ИНВИТРО тесты №5 – клинический анализ крови, №119 – лейкоцитарная формула) и результатах серологических тестов (в ИНВИТРО — №186 – анти-VCA IgM, №187 – анти-EBNA IgG, №255 – анти-EA IgG). Ко второй неделе заболевания развивается относительный и абсолютный лимфоцитоз с присутствием 10 — 20% атипичных мононуклеаров. Гематологические изменения, напоминающие картину инфекционного мононуклеоза, могут наблюдаться и при цитомегаловирусной инфекции, токсоплазмозе, острых респираторных вирусных заболеваниях, ветряной оспе, кори, инфекционных гепатитах и других заболеваниях. Поэтому для постановки дифференциального диагноза целесообразно проведение серологических тестов. Антитела к антигенам вируса появляются достаточно быстро, и исследование в остром периоде заболевания даже однократное взятие сыворотки на разные виды антител может дать достаточно точное представление о наличии иммунитета или восприимчивости пациента к инфекции вирусом Эпштейна-Барр, текущей инфекции или реактивации.
Ко второй неделе заболевания развивается относительный и абсолютный лимфоцитоз с присутствием 10 — 20% атипичных мононуклеаров. Гематологические изменения, напоминающие картину инфекционного мононуклеоза, могут наблюдаться и при цитомегаловирусной инфекции, токсоплазмозе, острых респираторных вирусных заболеваниях, ветряной оспе, кори, инфекционных гепатитах и других заболеваниях. Поэтому для постановки дифференциального диагноза целесообразно проведение серологических тестов. Антитела к антигенам вируса появляются достаточно быстро, и исследование в остром периоде заболевания даже однократное взятие сыворотки на разные виды антител может дать достаточно точное представление о наличии иммунитета или восприимчивости пациента к инфекции вирусом Эпштейна-Барр, текущей инфекции или реактивации.
Дополнительным подтверждением течения острых стадий инфекции может служить выявление ДНК вируса Эпштейна — Барр в крови и/или слюне методом ПЦР (в ИНВИТРО тесты №351КР – определение вирусной ДНК в крови, №351ВПТ — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в выпоте, №351МОЧ — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в моче, №351НОС — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в соскобе эпителиальных клеток слизистой носа, №351РОТ — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в соскобе эпителиальных клеток ротоглотки, №351СВ — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в сыворотке крови, №351СЛН — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в слюне, №351СМЖ — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в спинномозговой жидкости, №351СП — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в секрете простаты, эякуляте, №351УРО — Вирус Эпштейна-Барр, определение ДНК (Epstein Barr virus, DNA) в соскобе эпителиальных клеток урогенитального тракта
). ПЦР-тестирование особенно полезно для выявления данной инфекции у новорождённых, когда серологические исследования мало информативны вследствие незрелости иммунной системы, а также в сложных и сомнительных случаях.
ПЦР-тестирование особенно полезно для выявления данной инфекции у новорождённых, когда серологические исследования мало информативны вследствие незрелости иммунной системы, а также в сложных и сомнительных случаях.
Серологические тесты.
При литическом жизненном цикле вируса сначала появляются каскадом различные регуляторные белки ранней фазы (ранние антигены, early antigens, EA), к которым относятся используемые в различных тест-системах ЕА-D (p54), EA-R (p85), EA p138. Позже образуются структурные белки вируса — вирусные капсидные антигены (virus capsid antigens, VCA), мембранные белки (membrane antigens, MA). При латентной инфекции образуются только некоторые белки, в число которых входит Эпштейна-Барр ядерный (нуклеарный) антиген (Epstein-Barr nuclear antigens, EBNA, NA). Специфическая серологическая диагностика инфекции основана на использовании комбинации тестов, выявляющих наличие IgG и IgM антител к различным белкам-антигенам вируса, что позволяет дифференцировать инфекцию и уточнить стадию патологического процесса. В серологической диагностике острого мононуклеоза используется также тест на гетерофильные антитела.
В серологической диагностике острого мононуклеоза используется также тест на гетерофильные антитела.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Современные подходы к диагностике и лечению инфекционного мононуклеоза Эпштейна
УДК 616.988.55-071-059
Е.Б. Наговицына
СОВРЕМЕННЫЕ ПОДХОДЫ К ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ИНФЕКЦИОННОГО МОНОНУКЛЕОЗА ЭПШТЕЙНА — БАРР-ВИРУСНОЙ
ЭТИОЛОГИИ
Хабаровский филиал ФГБУ «Дальневосточный научный центр физиологии и патологии дыхания»
Сибирского отделения РАМН — НИИ охраны материнства и детства, 680022, ул. Воронежская, 49, корп. 1, тел. 8-(4212)-98-05-91, e-mail: [email protected], г. Хабаровск
Воронежская, 49, корп. 1, тел. 8-(4212)-98-05-91, e-mail: [email protected], г. Хабаровск
Резюме
Повсеместное распространение инфекции, связанной с вирусом Эпштейна — Барр в мире, и разнообразие клинических проявлений ассоциированных с ней заболеваний требуют применения современных и адекватных методов лабораторной диагностики, позволяющих правильно оценить стадию вирусной инфекции. Не разработаны четкие стандарты лечения пациентов с инфекционным мононуклеозом из-за отсутствия средств этиотропной терапии и специфической профилактики.
В представленном обзоре суммированы современные взгляды о возможностях лабораторной диагностики и лечения Эпштейна — Барр-вирусной инфекции с использованием широкого спектра лекарственных и иммуннокор-ригирующих препаратов.
Ключевые слова: инфекционный мононуклеоз, вирус Эпштейна — Барр, диагностика, лечение.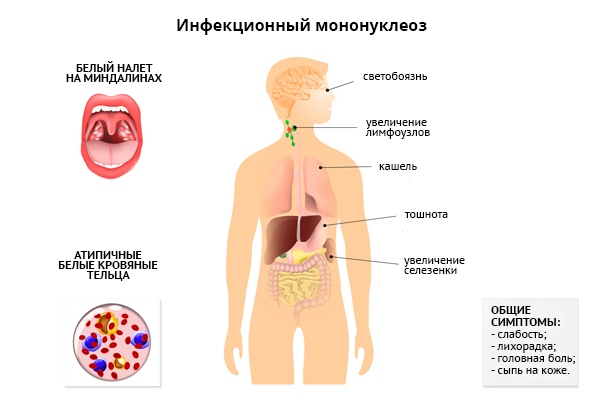
E.B. Nagovitsyna
MODERN APPROACHES TO DIAGNOSTICS AND TREATMENT OF EPSTEIN-BARR VIRUS INFECTIOUS
MONONUCLEOSIS
Khabarovsk Branch of the Far Eastern Research Center of Respiratory Physiology and Pathology — Research Institute of Mother
and Child Health Care, Khabarovsk
Summary
World spread infection caused by Epstein — Barr virus, and a variety of clinical manifestations associated with these diseases require the use of modern and appropriate methods of laboratory diagnostics, to assess the stage of a viral infection properly. Precise standards for the treatment of patients with infectious mononucleosis has not been worked out due to the lack of etiological therapy and specific prevention.
This review summarizes the current views on the possibilities of laboratory diagnostics and treatment of Epstein-Barr viral infection using a wide range of medicinal and immunocorrecting medications.
Key words: infectious mononucleosis, Epstein-Barr virus, diagnostics, treatment.
Проблема инфекционного мононуклеоза (ИМ) этиологически обусловленного вирусом Эпштейна — Барр (ВЭБ) в РФ остается весьма актуальной. Это связано не только с широкой циркуляцией возбудителя среди населения и тропностью его к иммунокомпентент-ным клеткам, но и с особенностями течения инфекции в разные возрастные периоды. В повседневной практике чаще приходится сталкиваются с клинически манифестными формами первичной Эпштейна -Барр-вирусной инфекции (ЭБВИ), которая протекает благоприятно и обычно заканчивается выздоровлением, но с пожизненной персистенцией вируса в организ-ме[1, 6, 8, 12, 16] Однако в 10-25 % случаев инфицирования острая инфекция может иметь неблагоприятные последствия с формированием хронических форм заболевания и развитием лимфопролиферативных и онкологических процессов [2, 6, 22, 23, 27].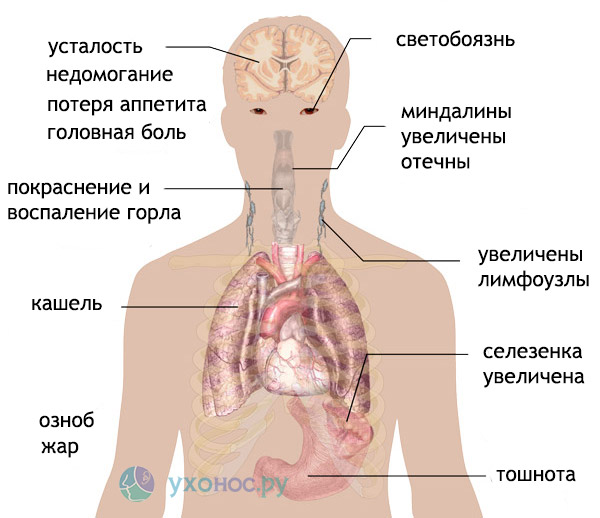 Отсутствие средств специфической профилактики и этиотропной терапии также не дает возможности прогнозировать исход инфекции.
Отсутствие средств специфической профилактики и этиотропной терапии также не дает возможности прогнозировать исход инфекции.
Современная диагностика ИМ должна быть комплексной и включать: общеклинические лабораторные исследования, определение серологических маркеров
ЭБВИ в сыворотке крови методом иммуноферментно-го анализа (ИФА), ПЦР — диагностику, иммуноблот [2, 6, 8, 11, 30].
В периферической крови у больных ИМ чаще наблюдается лейкоцитоз (до 20*109/л), абсолютное или относительное снижение нейтрофилов, абсолютный лимфоцитоз, единичные плазматические клетки. Наиболее значимым гематологическим маркером ИМ являются атипичные мононуклеары. Процент последних может варьировать и достигать 60-80 % в разгар заболевания с постепенным снижением по мере выздоровления. Более чем в 90 % случаев при ИМ изменены биохимические показатели функции печени. В сыворотке крови повышена активность трансаминаз (АСТ) и щелочной фосфатазы, а у 40 % больных увеличена концентрация билирубина.
В сыворотке крови повышена активность трансаминаз (АСТ) и щелочной фосфатазы, а у 40 % больных увеличена концентрация билирубина.
Однако все перечисленные изменения не являются строго специфичными для ВэБ-инфекции (их можно обнаружить и при других вирусных инфекциях) [12].
В последние годы в практической медицине широко используются специфические методы диагностики ЭБВИ, в том числе серологическое обследование методом ИФА. Основой целью серодиагностики ЭБВИ
является выявление стадии инфекционного процесса. В ответ внедрение вируса организм вырабатывает антитела различных классов, выявление которых позволяет не только диагностировать ЭБВИ, но и определять сроки инфицирования [2, 6, 10, 16, 19, 29, 32].
Дополнительным маркером, который позволяет разграничить первичную инфекцию от реинфицирова-ния или реактивации и установить примерные сроки перенесенной ЭБВИ, является индекс авидности (ИА). Авидность — величина, характеризующая прочность связи и сродство специфических антител и антигена. В ходе развития иммунного ответа после инфицирования антитела эволюционируют, постепенно увеличивается их соответствие антигенным структурам возбудителя, повышается эффективность их связывания, т. е. наблюдается рост авидности антител.
Авидность — величина, характеризующая прочность связи и сродство специфических антител и антигена. В ходе развития иммунного ответа после инфицирования антитела эволюционируют, постепенно увеличивается их соответствие антигенным структурам возбудителя, повышается эффективность их связывания, т. е. наблюдается рост авидности антител.
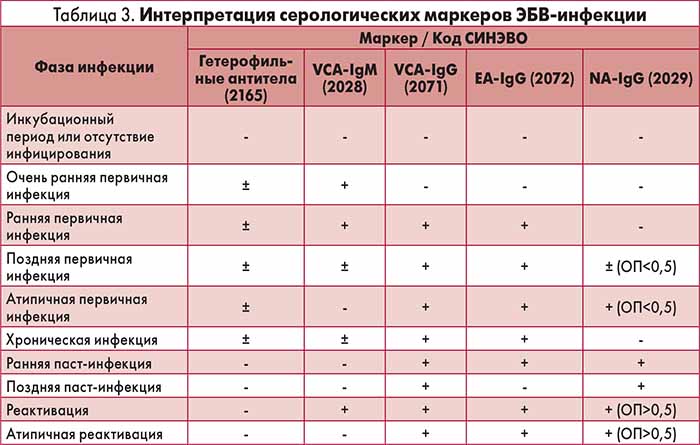
Основные серологические маркеры ЭБВИ и возможная интерпретация результатов серологического обследования представлены в таблицах 1 и 2 [11].
Таблица 1
Серодиагностика ВЭБ-инфекции
Антиген ВЭБ Класс обнаруживаемых АТ Выявляются
Viral capsid antigen -вирусныи капсид-ный антиген (VCA) анти-IgM VCA с момента появления клиники заболевания и следующие 4-6 недель
анти-IgG VCA обычно через 4-6 недель после ^М VCA, сохраняются пожизненно
Early antigen -ранний антиген ВЭБ (EA) анти-IgG EA с первой недели болезни до 3-6 месяцев
Нуклеиновые кислоты ВЭБ (EBNA) анти-IgG EBNA через 1-3 месяца от начала болезни, сохраняются пожизненно
Таблица 2
Интерпретация результатов обследования методом ИФА при ЭБВИ
Фазы инфекции VCA Индекс авидности EA IgG EBNA IgG
IgM IgG
Отсутствие инфекции (инкубационный период) — — н/о — —
Очень ранняя первичная инфекция + — н/о — —
Ранняя первичная инфекция + + <60 % + —
Поздняя первичная инфекция +/- + 60-70 % + +/-
Паст-инфекция — + >70 % — +
Реактивация +/- + >70 % + +
Поздняя паст-инфекция, иммуносупрессия — + >70 % — —
Параллельно с определением серологических маркеров у больных с подозрением на инфекционный мононуклеоз проводят выявление ДНК возбудителя методом ПЦР в крови или другом биологическом материале (слюна, мазки из ротоглотки биоптаты печени, лимфоузлов, слизистой кишечника и т./ebvhorizontal-5b0d188404d1cf00360140ca.jpg) д. Оценка результатов данного метода в клинической практике затруднена, так как высокая чувствительность ПЦР не дает возможности отличить здоровое носительство от инфекции с активной репликацией вируса. Поэтому ряд авторов указывают на необходимость использования количественного варианта ПЦР [11, 12, 25]. При этом считают, что определение в пробе 10-100 копий
д. Оценка результатов данного метода в клинической практике затруднена, так как высокая чувствительность ПЦР не дает возможности отличить здоровое носительство от инфекции с активной репликацией вируса. Поэтому ряд авторов указывают на необходимость использования количественного варианта ПЦР [11, 12, 25]. При этом считают, что определение в пробе 10-100 копий
ДНК ВЭБ (1 000 ГЭ/мл в 1 мл образца), характеризует здоровое носительство, а выявление 100 и более копий (10 000 ГЭ/мл в 1 мл образца) позволяет установить активную фазу ЭБВИ.
Метод ПЦР особенно эффективен для обнаружения ВЭБ у новорожденных, когда определение серологических маркеров малоинформативно вследствие не сформировавшейся иммунной системы, а также в сложных и сомнительных случаях диагностики ВЭБ инфекции у взрослых [3, 4].
Важную информацию о течении инфекции может дать использования иммуноблота — высокоспецифичного и высокочувствительного референс-метода, подтверждающего диагноз у пациентов с положительными или неопределенными результатами анализов, полученных, в т.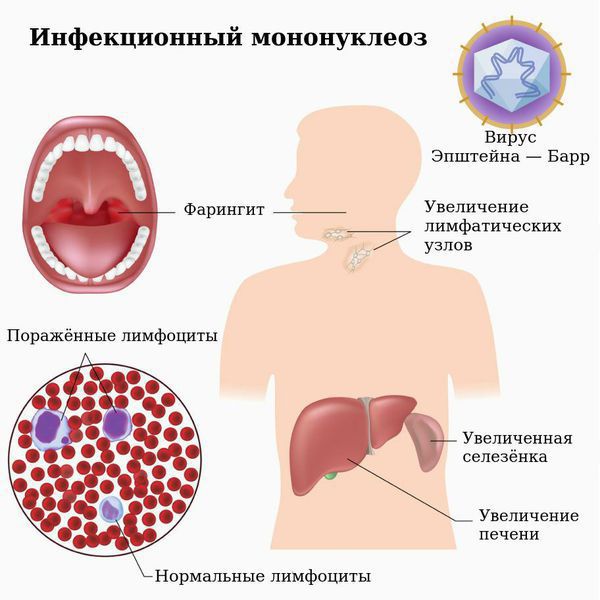 ч. при помощи ИФА. Метод основан на выявлении антител к отдельным белкам антигена возбудителя. Уникальность иммуноблота заключается в его высокой информативности и достоверности получаемых результатов [4, 10, 11].
ч. при помощи ИФА. Метод основан на выявлении антител к отдельным белкам антигена возбудителя. Уникальность иммуноблота заключается в его высокой информативности и достоверности получаемых результатов [4, 10, 11].
Основной целью терапии инфекционного монону-клеоза является не только купирование симптомов заболевания, но и перевод острой инфекции в латентную и, тем самым снижение риска развития хронической ЭБВИ и ассоциированных с ней лимфопролифератив-ных, онкологических и аутоимунных заболеваний
До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ВЭБ. Также как до сих пор нет четкой патогенетически обоснованной схемы лечения больных, а имеющиеся указания носят рекомендательный характер [2, 8, 18].
Лечение больных ИМ, как правило, проводится в амбулаторных условиях, изоляции пациентов не требуется. Показаниями к госпитализации являются: длительная лихорадка, выраженный синдром интоксикации, тяжелый тонзиллит и/или ангина, желтуха, анемия, обструкция дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, со стороны сердечно-сосудистой и дыхательной систем) [18].
Показаниями к госпитализации являются: длительная лихорадка, выраженный синдром интоксикации, тяжелый тонзиллит и/или ангина, желтуха, анемия, обструкция дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, со стороны сердечно-сосудистой и дыхательной систем) [18].
Базисная терапия инфекционного мононуклеоза включает охранительный режим, симптоматическую терапию: адекватную регидратацию (обильное питье), полоскание горла антисептиками, жаропонижающие по показаниям. Применение антибиотиков оправдано в случаях присоединения бактериальной инфекции, которая проявляется в выраженных воспалительных изменениях со стороны гемограммы и явлений ла-кунарной или некротической ангины. Препаратами выбора являются цефалоспорины 2-3-го поколения, современные макролиды, карбапенемы [22]. Противогрибковые препараты показаны при подозрении на грибковую этиологию тонзиллита. В случаях развития некротической ангины, когда возможно в поражении миндалин участвуют анаэробные бактерии, используют метронидазол [20].
Глюкокортикостероиды (преднизолон, дексамета-зон и др.) рекомендуются больным с тяжелым течением Эпштейна — Барр-инфекционного мононуклеоза, обструкцией дыхательных путей, неврологическими
и гематологическими осложнениями (тяжелая тром-боцитопения, гемолитическая анемия) [2, 16, 22, 28].
Течение и исход многих инфекционных заболеваний зависят от способности системы интерферона (ИФН) быстро реагировать на внедрение возбудителя. Синтез интерферонов является одной из ранних реакций врожденного иммунитета в ответ на попадание патогенов. В результате образуется эндогенный интерферон ИФН, который препятствует проникновению инфекционного агента внутрь клетки, запуская цито-токсический ответ и адаптивный иммунитет, обеспечивая эффективную защиту организма от вирусных и бактериальных инфекций.
В последние годы все чаще для лечения ЭБВИ стали применять рекомбинантные а-интерфероны (интрон, роферон, реоферон). У. Wu и соавт. [33] (1996) показали, что рекомбинантный а-интерферон укорачивает длительность эпизода инфекционного мононуклеоза у детей по сравнению с контрольной группой. Л.В. Крамарь и др. [7] (2012) рекомендуют интерферон а-2Ь (виферон, генферон-лайт, кипферон и др.) для лечения Эпштейна -Барр-вирусного инфекционного мононуклеоза. Препараты а-интерферонов тормозят репликацию вирусов за счет разрушения вирусной матричной РНК, модулируют иммунный ответ, стимулируют выработку цитокинов, повышают функциональную активность макрофагов и нейтрофилов. Входящие в их состав природные антитоксиданты (витамины А и С) стабилизируют клеточные мембраны. Данная группа препаратов особенно показаны детям первых 3 лет жизни и старшим подросткам, больных ИМ, так как именно в эти возрастные периоды заболевание протекает особенно тяжело.
У. Wu и соавт. [33] (1996) показали, что рекомбинантный а-интерферон укорачивает длительность эпизода инфекционного мононуклеоза у детей по сравнению с контрольной группой. Л.В. Крамарь и др. [7] (2012) рекомендуют интерферон а-2Ь (виферон, генферон-лайт, кипферон и др.) для лечения Эпштейна -Барр-вирусного инфекционного мононуклеоза. Препараты а-интерферонов тормозят репликацию вирусов за счет разрушения вирусной матричной РНК, модулируют иммунный ответ, стимулируют выработку цитокинов, повышают функциональную активность макрофагов и нейтрофилов. Входящие в их состав природные антитоксиданты (витамины А и С) стабилизируют клеточные мембраны. Данная группа препаратов особенно показаны детям первых 3 лет жизни и старшим подросткам, больных ИМ, так как именно в эти возрастные периоды заболевание протекает особенно тяжело.
Препараты, относящиеся к группе индукторов ИФН, обладают выраженными противовирусными и иммуномодулирующими свойствами, Отличающимися по своей химической природе они действуют на разные этапы репродукции вирусов и звенья врожденного и адаптивного иммунитета, что объясняет расширяющиеся масштабы их применения в терапии вирусных инфекций. Для лечения больных при быстро развивающихся вирусных инфекциях необходимо использовать индукторы, способные к быстрому синтезу раннего эндогенного ИФН [5, 9, 15].
Для лечения больных при быстро развивающихся вирусных инфекциях необходимо использовать индукторы, способные к быстрому синтезу раннего эндогенного ИФН [5, 9, 15].
К этой группе препаратов относится циклоферон, при применении которого уже через 2 часа увеличивается концентрация эндогенного ИФН в крови, а через 4-6 часов — в тканях легких. Циклоферон показан при средне-тяжелом и тяжелом течение ИМ внутрь или п/эн-терально. Лечебный эффект усиливается при сочетании
с обработкой слизистой оболочки нёбных миндалинах 5 % линиментом циклоферона.
В последние годы для лечения больных ИМ Эпштейна — Барр-вирусной этиологии применяют инозин пранобекс (гроприносин, изоприназин). Препарат обладает иммуномодулирующей активностью и неспецифическим противовирусным действием [13, 14, 16].
Ряд авторов в комплексной терапии ЭБВИ рекомендует внутривенное введение препаратов иммуноглобулинов (ИГ) класса G (привиджен, интратек, интрагло-бин, и др. ), содержащих не менее 95 % IgG [5, 14]. В отличие от а-ИФН препараты ИГ действуют преимущественно на внеклеточно расположенные частицы ВЭБ. Этиотропный эффект выражается в вируцидном и вирустатическом действии препарата и развитии антителозависимой комплемент-опосредованной ци-тотоксичности, особенно актуальной в профилактике виремии при персистирующей ЭБВИ. G. Ferrara и соавт. [21] (2012) рекомендуют использование препаратов иммуноглобулинов для внутривенного введения в комбинации с антимикробными химиопрепартами при тяжелых, трудно поддающихся лечению формах болезни.
), содержащих не менее 95 % IgG [5, 14]. В отличие от а-ИФН препараты ИГ действуют преимущественно на внеклеточно расположенные частицы ВЭБ. Этиотропный эффект выражается в вируцидном и вирустатическом действии препарата и развитии антителозависимой комплемент-опосредованной ци-тотоксичности, особенно актуальной в профилактике виремии при персистирующей ЭБВИ. G. Ferrara и соавт. [21] (2012) рекомендуют использование препаратов иммуноглобулинов для внутривенного введения в комбинации с антимикробными химиопрепартами при тяжелых, трудно поддающихся лечению формах болезни.
Наиболее дискуссионным остается вопрос назначения противовирусной терапии больным ИМ [18, 24, 26, 31, 34]. Среди препаратов, которые могут быть использованы в качестве этиотропных, рекомендуют входящие в группу ациклических нуклеозидных аналогов (АННА) — ацикловир, валацикловир (валтрекс) и т. д. Несомненно, что одной из причин перехода острой ЭБВИ в хроническую, является высокая вирусная нагрузка при острой инфекции. Уровень свободной ДНК вируса в крови прямо коррелирует с тяжестью заболевания. Уменьшение вирусной нагрузки в крови под действием ациклических нуклеозидов позволяет снизить эти риски. Однако следует помнить, что эффективное действие АНА возможно только в остром периоде заболевания или при реактивации инфекции, когда происходит активная репликации вирусных частиц. Именно в этих случаях происходит синтез вирусных ферментов, активирующих лекарственные, которые в свою очередь подавляют синтез вирусной ДНК. При латентном течении инфекции этого не происходит и применение указанных препаратов неэффективно [8, 18, 22].
Уровень свободной ДНК вируса в крови прямо коррелирует с тяжестью заболевания. Уменьшение вирусной нагрузки в крови под действием ациклических нуклеозидов позволяет снизить эти риски. Однако следует помнить, что эффективное действие АНА возможно только в остром периоде заболевания или при реактивации инфекции, когда происходит активная репликации вирусных частиц. Именно в этих случаях происходит синтез вирусных ферментов, активирующих лекарственные, которые в свою очередь подавляют синтез вирусной ДНК. При латентном течении инфекции этого не происходит и применение указанных препаратов неэффективно [8, 18, 22].
Таким образом, залогом успешного лечения Эп-штейна — Барр-вирусного инфекционного мононуклео-за должна быть комплексная терапия и индивидуальная тактика ведения конкретного больного, как на этапе амбулаторного, так и стационарного наблюдения.
Литература
1. Боковой А.Г. Герпесвирусные инфекции у детей -актуальная проблема современной клинической практики // Детские инфекции. — 2010. — Т. 9, № 2. — С. 3-7.
Боковой А.Г. Герпесвирусные инфекции у детей -актуальная проблема современной клинической практики // Детские инфекции. — 2010. — Т. 9, № 2. — С. 3-7.
2. Виговская О.В., Крамарев С.А., Дорошенко В.О., Шпак И.В. Инфекционный мононуклеоз Эпштейна -Барр-вирусной этиологии: вопросы этиологии, патоге-
неза, иммуногенеза, лечения // Лечащий врач. — 2012. -№ 4. — С. 29-34.
3. Долгих Т.И. Современная стратегия лабораторной диагностики герпесвирусных инфекций, ассоциированных с перинатальной патологией // Справочник заведующего КДЛ. — 2011. — № 4. — С. 21-32.
4. Долгих Т.И. Современная стратегия лабораторной диагностики герпесвирусных инфекций, ассоциированных с перинатальной патологией // Справочник заведующего КДЛ. — 2011. — № 5. — С. 24-34.
5. Ершов Ф.И. Антивирусные препараты: справочник. — 2-е изд. — М., 2006. — 311 с.
Ершов Ф.И. Антивирусные препараты: справочник. — 2-е изд. — М., 2006. — 311 с.
6. Каражас Н.В., Малышев Н.А., Рыбалкина Т.Н. и др. Современные аспекты герпесвирусной инфекции. Эпидемиология, клиника, диагностика, лечение и профилактика: методические рекомендации. — М.: Спецкнига. — 2012. — 128 с.
7. Крамарь Л.В., Карпухина О.А. Комплексная терапия Эпштейна — Барр-вирусной инфекции у детей // Архив внутренней медицины. — 2012. — № 1. — С. 25-28.
8. Краснов В.В. Инфекционный мононуклеоз. Клиника, диагностика, современные принципы лечения. -СПб.: Н. Новгород, 2003. — 75 с.
9. Коваленко А.Л., Шафранская Е.Г., Мухояро-ва Е.Н., Валеев В.В. Циклоферон. Лечение и профилактика гриппа и других ОРВИ: Сборник научных работ. — СПб.: Тактик-Студио, 2015. — 184 с.
10. Лабораторная диагностика инфекционных заболеваний: справочник под ред. В.И. Покровского, М.Г. Твороговой, Г.А. Шипулина. — М.: Бином. -2013. — 648 с.
Лабораторная диагностика инфекционных заболеваний: справочник под ред. В.И. Покровского, М.Г. Твороговой, Г.А. Шипулина. — М.: Бином. -2013. — 648 с.
11. Львов Н.Д., Дудукина Е.А. Ключевые вопросы диагностики Эпштейна — Барр-вирусной инфекции // Инфекционные болезни. — 2013. — № 3. — С. 24-32.
12. Малашенкова И.К., Дидковский Н.А., Сарсания Ж.Ш., Жарова М.А. и др. Клинические формы хронической Эпштейн — Барр-вирусной инфекции: вопросы диагностики и лечения // Лечащий врач. — 2003. -№ 9. — С. 8-10.
13. Савенкова М.С., Афанасьева А.А., Мина-сян В.С., Тюркина С.И. Лечение часто болеющих детей со смешанной инфекцией // Вопросы современной педиатрии. — 2011. — Т. 10. — № 4. — С. 83-88.
14. Савенкова М.С., Савенков М.П., Афанасьева А.А., Абрамова Н.А. Возможности противовирусной и иммуномодулирующей терапии в лечении гриппа, ОРВИ, герпес-вирусных инфекций. — М, 2015. — 20 с.
— М, 2015. — 20 с.
15. Сетдикова Н.Х., Латышева Т.В., Ильина Н.И. Иммуномодуляторы: перспективные направления исследования и практическое применение // Аллергология и иммунология. — 2012. — № 1. — С. 14-19.
16. Симоновьян Э.Н., Денисенко В.Б., Бовта-ло Б.Ф., Григорян А.В. Эпштейна-Барр вирусная инфекция у детей: современные подходы к диагностике и лечению // Лечащий врач. — 2007. — № 7. — С. 36-41.
17. Шестакова И.В., Ющук Н.Д. Эпштейна — Барр-вирусная инфекция у взрослых: вопросы патогенеза, клиники и диагностики // Лечащий врач. — 2010. -№ 10. — С. 40-44.
18. Шестакова И.В. Лечить или не лечить Эпштей-на — Барр-вирусную инфекцию: подробный обзор различных тактик // Инфекционные болезни. — 2013. -№ 3. — С. 12-24.
19. Ambinder R. F., Lin L. Mononucleosis in the laboratory // J. Infect. Dis. — 2005. — Vol. 192. — P. 1503-1504.
F., Lin L. Mononucleosis in the laboratory // J. Infect. Dis. — 2005. — Vol. 192. — P. 1503-1504.
20. Fota-Markowcka H., et al. Profile of microorganisms isolated in nasopharyngeal swabs from the patients with acute infectious mononucleosis // Wiad. Lek. -2002. — Vol. 55, № 34. — P. 150-157.
21. Ferrara G., Zumla A., Maeurer M. Intravenous immunoglobulin (IVIg) for refractory and difficult-to-treat infections // Am. J. Med. — 2012. — Vol. 125, № 10. -P. 1036.e1-1036.e8.
22. Gershburg E., Pagano J.S. Epstein Barr infections: prospects for treatment // J. Antimicrob. Chemother. 2005. — Vol. 56, № 2. — P. 277-281.
23. Li Z. Y., Lou J. G., Chen J. Analysis of primary symptoms and disease spectrum in Epstein — Barr-virus infected children // Zhonghua Er Ke Za Zhi. — 2004. -Vol. 42, № 1.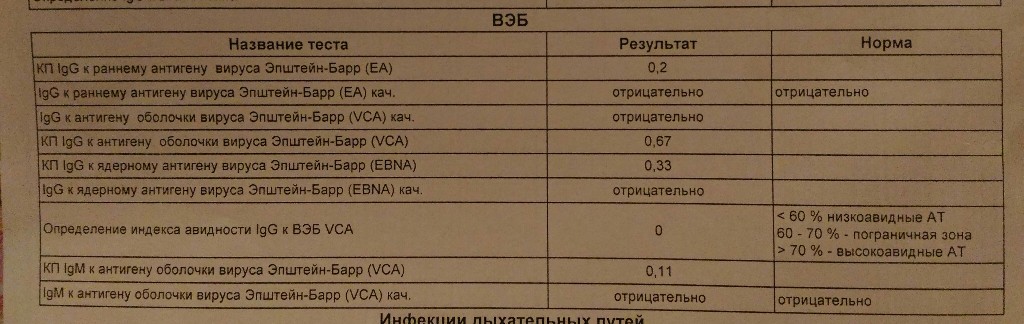 — P. 20-22.
— P. 20-22.
24. Mark H. Ebell Epstein — Barr-virus infectious mononucleosis // Fam.Physician. — 2004. — Vol. 70, № 7. -P. 1279-1287.
25. Maurmann S., Fricke L., Wagner H.-J., et al. Molecular Parameters for Precise Diagnosis of Asymptomatic Epstein — Barr-virus Reactivation in Healthy Carriers // J. Clin. Microbiol. — Dec. 2003. — P. 5419-5428.
26. Okano M., Gross G. Advanced therapeutic and prophylactic strategies for Epstein — Barr-virus infection in immunocompromised patients // Expert. Rev. Anti. Infect. Ther. — 2007. — Vol. 5, № 3. — P. 403-413.
27. Ralf D. Hess. Routine Epstein — Barr-virus Diagnostics from the Laboratory Perspective: Still Challenging after 35 Years // J. Clin. Microbiol. — Aug. 2004. -P. 3381-3387.
28. Roy M., Bailey B., Amre D.K., et al. Dexametha-sone for the treatment of sore throat in children with suspected infectious mononucleosis: a randomized, doubleblind, placebocontrolled, clinical trial // Arch. Pediatr. Adolesc. Med. 2004. — Vol. 158. — P. 250-254.
Roy M., Bailey B., Amre D.K., et al. Dexametha-sone for the treatment of sore throat in children with suspected infectious mononucleosis: a randomized, doubleblind, placebocontrolled, clinical trial // Arch. Pediatr. Adolesc. Med. 2004. — Vol. 158. — P. 250-254.
29. Schaade L., Kleines M., Heausler M. Application of virusspecific immunoglobulin M (IgM), IgG, and IgA antibody detection with a polyantigenic enzymelinked immunosorbent assay for diagnosis of EpsteinBarr virus infections in childhood // J. Clin. Microbiol. — 2001. -Vol. 39. — P. 39023905.
30. Schooley R.T. Epstein — Barr-virus (infectious mononucleosis). In: Mandell. Principles and Practice of Infectious Diseases. 5-th ed. — 2000. — P. 1599-1608.
31. Tynell E., Aurelius E., Bransdell A., et al. // Acyclovir and prednisolone treatment of acute infectious mononucleosis: a multicenter double-blind, placebo-controlled study // J. Infect.Dis. — 1996. — Vol. 174. -P. 324-331.
Infect.Dis. — 1996. — Vol. 174. -P. 324-331.
32. Walling D.M., Brown A.L., Etienne W., et al. Multiple EpsteinBarr virus infections in healthy individuals // J. Virol. — 2003. — Vol. 77. — P. 6546-6550.
33. Wu Y., Luo C., Lu Z., et al. Curative effect of interferonalpha in children with infectious // Hua Xi Yi Ke Da Xue Xue Bao. — 1996. — Vol. 27 (1). — P. 82-84.
34. Zacny VL., Gershburg E., Davis M.G., et al. Inhbition ofEpsteinBarr virus replication byabenzimidazole Lriboside: novel antiviral mechanism of 5,6dichloro2(iso propylamino)1betaLribofuranosyl 1Hbenzimidazole // J. Virol. — 1999. — Vol. 73. — P. 1122-1128.
Literatire
1. Bokovoy A. G. Herpes virus infection in children — a topical problem of modern clinical practice // Children’s infections. — 2010. — Vol. 9, № 2. — P. 3-7.
— 2010. — Vol. 9, № 2. — P. 3-7.
2. Vigovskya O.V., Kramarev S.A., Doroshenko VA., Shpak I.V Infectious mononucleosis of Epstein-Barr virus etiology: etiology, pathogenesis, immunogenesis, treatment // Attending physician. — 2012. — № 4. — P. 29-34.
3. Dolgikh T.I. Modern strategy for laboratory diagnosis of herpesvirus infections associated with perinatal pathology // Guide head CDL. — 2011, № 4. — P. 21-32.
4. Dolgikh T.I. Modern strategy for laboratory diagnosis of herpesvirus infections associated with perinatal pathology // Guide head CDL. — 2011, № 5. — P. 24-34.
5. Ershov F.I. Antiviral drugs. Reference. 2-nd edition. — M., 2006. — 311 p.
6. Karazhas N.I., Malyshev N.A., Rybalkina T.N., et al. Modern aspects of herpes infections. Epidemiology, clinic, diagnostics, treatment and prevention: guidelines. — M.: Spetskniga. — 2012. — 128 p.
Epidemiology, clinic, diagnostics, treatment and prevention: guidelines. — M.: Spetskniga. — 2012. — 128 p.
7. Kramar L.V., Karpukhina O.A. Combined therapy of Epstein — Barr-viral infection in children // Archives of internal medicine. — 2012. — № 1. — P. 25-28.
8. Krasnov V.V. Infectious mononucleosis. Clinical features, diagnostics, modern principles of treatment. -SPb.: N. Novgorod, 2003. — 75 p.
9. Kovalenko A.L., Shafranskaya E.G., Saharova E.N., Valeev V.V. Cicloferon. Treatment and prevention of influenza and other viral respiratory infections: Collection of scientific works. — SPb.: Tactics Studio, 2015. — 184 p.
10. Laboratory diagnosis of infectious diseases: Handbook ed. by V.I. Pokrovsky, M.G. Tvorogova, G.A. Shipu-lin. — M.: Binom. — 2013. — 648 p.
11. L’vov N.D. Dudukina E.A. Key issues in the diagnosis of Epstein — Barr virus infection // Infectious diseases. — 2013. — № 3. — P. 24-32.
L’vov N.D. Dudukina E.A. Key issues in the diagnosis of Epstein — Barr virus infection // Infectious diseases. — 2013. — № 3. — P. 24-32.
12. Malashenkova I.K., Didkovsky N.A., Sarsania J.S., Zharova M.A., et al. Clinical forms of chronic Epstein-Barr-virus infection: diagnosis and treatment // Treating physician. — 2003. — № 9. — P. 8-10.
13. Savenkova M.S., Afanas’eva A.A., Minasyan VS., Tyurkin S.I. Treatment of frequently ill children suffering from mixed infections // Current Pediatrics. — 2011. -Vol. 10, № 4. — C. 83-88.
14. Savenkova M.S., Savenkov M.P., Afanasiev A.A., Abramova N.A. Possible antiviral and immunomodulatory therapy in the treatment of influenza, SARS, herpes-viral infections. — M., 2015. — 20 p.
15. Setdikova N.X., Latysheva T.V., Il’ina N.A. Immunomodulators: promising research directions and practical application // Allergology and immunology. — 2012. -№ 1. — P. 14-19.
— 2012. -№ 1. — P. 14-19.
16. Simonovyan E.N., Denisenko VB., Butala B.F., Grigoryan A.V Epstein-Barr virus infection in children: current approaches to diagnosis and treatment // Treating physician. — 2007. — № 7. — P. 36-41.
17. Shestakova I.V, Yushchuk N.D. Epstein-Barr-vi-rus infection in adults: problems of pathogenesis, clinics and diagnostics // Attending physician. — 2010. — № 10. -P. 40-44.
18. Shestakova I.V. To treat or not to Treat Epstein-Barr virus infection: a detailed overview of the different tactics // Infectious diseases. — 2013. — № 3. — P. 12-24.
19. Ambinder R.F., Lin L. Mononucleosis in the laboratory // J. Infect. Dis. — 2005. — Vol. 192. — P. 1503-1504.
20. Fota-Markowcka H., et al. Profile of microorganisms isolated in nasopharyngeal swabs from the patients with acute infectious mononucleosis // Wiad. Lek. -2002. — Vol. 55, № 34. — P. 150-157.
Lek. -2002. — Vol. 55, № 34. — P. 150-157.
21. Ferrara G., Zumla A., Maeurer M. Intravenous immunoglobulin (IVIg) for refractory and difficult-to-treat infections // Am. J. Med. — 2012. — Vol. 125, № 10. -P. 1036.e1-1036.e8.
22. Gershburg E., Pagano J.S. Epstein Barr infections: prospects for treatment // J. Antimicrob. Chemother. 2005. — Vol. 56, № 2. — P. 277-281.
23. Li Z. Y., Lou J. G., Chen J. Analysis of primary symptoms and disease spectrum in Epstein-Barr virus infected children // Zhonghua Er Ke Za Zhi. — 2004. -Vol. 42, № 1. — P. 20-22.
24. Mark H. Ebell Epstein-Barr virus infectious mono-nucleosis // Fam.Physician. — 2004. — Vol. 70, № 7. -P. 1279-1287.
25. Maurmann S., Fricke L., Wagner H.-J., et al. Molecular Parameters for Precise Diagnosis of Asymptomatic Epstein-Barr Virus Reactivation in Healthy Carriers // J. Clin. Microbiol. — Dec. 2003. — P. 5419-5428.
Clin. Microbiol. — Dec. 2003. — P. 5419-5428.
26. Okano M., Gross G. Advanced therapeutic and prophylactic strategies for EpsteinBarr virus infection in immunocompromised patients // Expert. Rev. Anti. Infect. Ther. — 2007. — Vol. 5, № 3. — P. 403-413.
27. Ralf D. Hess. Routine Epstein — Barr-Virus Diagnostics from the Laboratory Perspective: Still Challenging after 35 Years // J. Clin. Microbiol. — Aug. 2004. -P. 3381-3387.
28. Roy M., Bailey B., Amre D.K., et al. Dexametha-sone for the treatment of sore throat in children with suspected infectious mononucleosis: a randomized, doubleblind, placebocontrolled, clinical trial // Arch. Pediatr. Adolesc. Med. 2004. — Vol. 158. — P. 250-254.
29. Schaade L., Kleines M., Heausler M. Application of virusspecific immunoglobulin M (IgM), IgG, and IgA antibody detection with a polyantigenic enzymelinked immunosorbent assay for diagnosis of EpsteinBarr virus infections in childhood // J. Clin. Microbiol. — 2001. -Vol. 39. — P. 39023905.
Clin. Microbiol. — 2001. -Vol. 39. — P. 39023905.
30. Schooley R. T. EpsteinBarr virus (infectious mono-nucleosis). In: Mandell. Principles and Practice of Infectious Diseases. 5-th ed. — 2000. — P. 1599-1608.
31. Tynell E., Aurelius E., Bransdell A., et al. // Acyclo-vir and prednisolone treatment of acute infectious mono-nucleosis: a multicenter double-blind, placebo-controlled study // J. Infect.Dis. — 1996. — Vol. 174. — P. 324-331.
32. Walling D.M., Brown A.L., Etienne W., et al. Multiple EpsteinBarr virus infections in healthy individuals // J. Virol. — 2003. — Vol. 77. — P. 6546-6550.
33. Wu Y., Luo C., Lu Z., et al. Curative effect of interferonalpha in children with infectious // Hua Xi Yi Ke Da Xue Xue Bao. — 1996. — Vol. 27 (1). — P. 82-84.
34. Zacny V.L., Gershburg E., Davis M.G., et al. propylamino)1betaLribofuranosyl lHbenzimidazole // J. Inhbition of EpsteinBarr virus replication byabenzimidazole Virol. — 1999. — Vol. 73. — P. 1122-1128. Lriboside: novel antiviral mechanism of 5,6dichloro2(iso
Zacny V.L., Gershburg E., Davis M.G., et al. propylamino)1betaLribofuranosyl lHbenzimidazole // J. Inhbition of EpsteinBarr virus replication byabenzimidazole Virol. — 1999. — Vol. 73. — P. 1122-1128. Lriboside: novel antiviral mechanism of 5,6dichloro2(iso
Координаты для связи с авторами: Наговицына Елена Борисовна — канд. мед. наук, старший научный сотрудник Хабаровского филиала ФГБУ «Дальневосточный научный центр физиологии и патологии дыхания» Сибирского отделения РАМН — НИИ охраны материнства и детства, тел. 8-(4212)-980-591, +7-914-771-67-48, e-mail: [email protected].
□□□
УДК 616.2-022.7-053.2:001.8 «2004/2015»(571.62)
О.В. Островская1, Г.Н. Холодок1, Н.В. Морозова2, Н.М. Ивахнишина1, Е.Б. Наговицына1, М.А. Власова1, Н.Г. Сидорчук1
ЧАСТОТА РЕСПИРАТОРНОГО МИКОПЛАЗМОЗА У ДЕТЕЙ ХАБАРОВСКОГО КРАЯ С 2004 ГОДА
1 Хабаровский филиал ФГБУ «Дальневосточный научный центр физиологии и патологии дыхания» Сибирского отделения РАМН — НИИ охраны материнства и детства, 680022, ул. Воронежская, 49, корп. 1, тел./факс 8-(4212)-35-63-35, 35-65-91, e-mail: [email protected]; Дальневосточный государственный медицинский университет, 680000, ул. Муравьева-Амурского, 35, тел. 8-(4212)-76-13-96, e-mail: [email protected], г. Хабаровск
Воронежская, 49, корп. 1, тел./факс 8-(4212)-35-63-35, 35-65-91, e-mail: [email protected]; Дальневосточный государственный медицинский университет, 680000, ул. Муравьева-Амурского, 35, тел. 8-(4212)-76-13-96, e-mail: [email protected], г. Хабаровск
Резюме
Проведено изучение частоты респираторного микоплазмоза у детей в Хабаровском крае. Описана вспышка респираторного микоплазмоза среди школьников в г. Хабаровске и п. Ванино в августе 2004 г. — феврале 2005 г. Особенностями вспышки было медленное развитие в течение 6 месяцев, наличие школьных и семейных очагов инфекции, высокая частота носительства и легких форм. В течение 2005-2015 гг. методом ПЦР обследован 3 941 ребенок в возрасте от 6 месяцев до 12 лет, госпитализированный по поводу внебольничной пневмонии в клинику Института охраны материнства и детства Частота выявления ДНК M.pneumoniae у детей с внебольничными пневмониями варьировала от 2,2 до 16,2 %, отмечено ежегодное повышение выявляемости микоплазм в сентябре-ноябре. Эпидемических вспышек не зарегистрировано.
Эпидемических вспышек не зарегистрировано.
Ключевые слова: дети, респираторный микоплазмоз, полимеразная цепная реакция.
O.V. Ostrovskaya1, G.N. Kholodok1, N.V. Morozova3, N.M. Ivakhnishina1, E.B. Nagovitsynai, M.A. Vlasova\ N.G. Sidorchuk1
RESPIRATORY MYCOPLASMOSIS MORBIDITY AND INCIDENCE RATE IN CHILDREN OF THE KHABAROVSK REGION SINCE 2004
Research Institute of Mother and Child Health Care;
2Far Eastern State Medical University, Khabarovsk
Summary
Respiratory mycoplasmosis incidence rate in the children of the Khabarovsk Region has been studied. An outbreak of respiratory mycoplasmosis in Khabarovsk and Vanino schoolchildren from August 2004 till February 2005 is reported. Specific features of the outbreak were found out to have a slow progression of the disease for six months, infection occurrence at schools and family settings, high rates of incidence and mild cases. Throughout 2005-2015, a PCR method was applied to examine 3,941 children aged 6 months to 12 years who were admitted to our hospital for community-acquired pneumonia. An average annual M. pneumoniae DNA detection index varied from 2,2 to 16,2 %; an annual increase in Mycoplasma detection was found out to take place in September-November. No epidemic outbreaks were reported.
Specific features of the outbreak were found out to have a slow progression of the disease for six months, infection occurrence at schools and family settings, high rates of incidence and mild cases. Throughout 2005-2015, a PCR method was applied to examine 3,941 children aged 6 months to 12 years who were admitted to our hospital for community-acquired pneumonia. An average annual M. pneumoniae DNA detection index varied from 2,2 to 16,2 %; an annual increase in Mycoplasma detection was found out to take place in September-November. No epidemic outbreaks were reported.
Key words: children, respiratory mycoplasmosis, polymerase chain reaction.
Проявления респираторного микоплазмоза разнообразны: здоровое носительство, самокупирующееся заболевание, протекающее по типу воспалительных инфекций дыхательных путей (ринит, фарингит, тра-
хеобронхит) со сравнительно легким, чаще субклиническим течением, и атипичная пневмония./153/153.jpg) Myco-plasma pneumoniae является основным возбудителем респираторного микоплазмоза. Наиболее часто это
Myco-plasma pneumoniae является основным возбудителем респираторного микоплазмоза. Наиболее часто это
Существуют ли инфекции, способные спровоцировать рак? Онкогенные инфекции
В настоящее время доказано, что от 15 до 20% новообразований человека имеют вирусное происхождение.
Вирусами называют мельчайшие организмы, большую часть из которых нереально разглядеть, даже используя обыкновенный микроскоп. Они состоят из небольшого количества ДНК и РНК генов, которые находятся в белковой капсуле. Эти вирусы проникают в живые клетки, где впоследствии начинают размножаться. Бывают также вирусы вызывающие рак, которые могут помещать свою ДНК в клетки, в скором времени спровоцировав появление онкологических заболеваний. Характерной чертой онкогенных вирусов является то, что они могут стимулировать клетки размножаться с необычно высокой скоростью, что может привести к повреждению генетического материала в этих клетках. Дополнительные факторы, такие как курение или воздействие определенных канцерогенов, могут вызывать окончательное превращение нормальных клеток в раковые. Эти воздействия (дополнительные факторы), наряду с индивидуальными генетическими особенностями каждого человека, могут объяснить, почему у некоторых людей с онкогенными инфекциями развивается рак, а у других нет.
Дополнительные факторы, такие как курение или воздействие определенных канцерогенов, могут вызывать окончательное превращение нормальных клеток в раковые. Эти воздействия (дополнительные факторы), наряду с индивидуальными генетическими особенностями каждого человека, могут объяснить, почему у некоторых людей с онкогенными инфекциями развивается рак, а у других нет.
К онковирусам относятся инфекции, которые провоцируют появление раковых заболеваний, а также вирусы, которые способствуют развитию воспалительных процессов, носящих хронический характер.
По заключению экспертов Международного Агентства по Изучению Рака (МАИР) прямым канцерогенным действием на человека обладают следующие вирусы:
- вирусы гепатита В и С, вызывающие рак печени;
- определенные типы папилломавирусов человека, являющиеся причинным агентом рака шейки матки, некоторых опухолей ано-генитальной области и других локализаций;
- вирус Эпштейна-Барр, принимающий участие в возникновении целого ряда злокачественных новообразований;
- герпесвирус человека 8-го типа, играющий важную роль в возникновении саркомы Капоши, первичной выпотной лимфомы, болезни Кастлемана и некоторых других патологических состояний;
- вирус Т-клеточного лейкоза человека, являющийся этиологическим агентом Т-клеточного лейкоза взрослых, перHIVной выпотной лимфомы (Primary Effusion Lymphoma, PEL), а также тропического спастического парапареза (TSP) и ряда других неонкологических заболеваний;
- вирус иммунодефицита человека (ВИЧ), не обладающий трансформирующими генами, но создающего необходимые условия (иммунодефицит) для возникновения рака.

Все они включены в санитарные правила и нуждаются в кратких комментариях.
Вирусы гепатита В и С (HBV, HCV)
В настоящее время существует глобальная эпидемия вируса гепатита В (HBV): на планете инфицировано этим вирусом более 350 млн. человек. Каждый год от инфекции HВV умирает 2 млн. человек, из них более 300 тыс. от рака печени. Вирусом гепатита С в мире инфицировано более 170 млн. человек, и их число ежегодно увеличивается на 3–4 млн. По данным экспертов, вирус гепатита С ежегодно становится причиной смерти 250–350 тыс. человек от цирроза, печеночной недостаточности и гепатоцеллюлярной карциномы. Из общего числа случаев рака печени (гепатокарцином) более половины связано с инфицированием HBV, четверть — с инфицированием HCV и 22% случаев — с другими причинами.
Инфицированность населения HBV колеблется от низкой, не превышающей 2% в США и странах Западной Европы, до высокой в странах Африки и Юго-Восточной Азии, приближающейся к 10%. Россия по уровню инфицированности населения HBV занимает промежуточное положение. В окружающих Россию странах (Средняя Азия, Закавказье, Молдавия) инфицированность населения по данным ВОЗ достигает 8%.
В окружающих Россию странах (Средняя Азия, Закавказье, Молдавия) инфицированность населения по данным ВОЗ достигает 8%.
Пути заражения вирусом гепатита В (HBV): перинатальный (от матери к плоду), парентеральный (главным образом с кровью или другими биологическим жидкостями больного человека, попадающими непосредственно в кровь инфицируемого, особенно при употреблении инъекционных наркотиков) и половым путем. Заразиться можно в местах, где собираются лица, употребляющие инъекционные наркотики, в салонах пирсинга и татуажа, парикмахерских (маникюр, педикюр — при совместном пользовании общими бритвами и маникюрными принадлежностями). Половой контакт с партнером носителем инфекции в 30% случаев заканчивается инфицированием партнера. Велика вероятность заразиться вирусом, если человек имеет много половых партнеров. У инфицированной HBV матери может родиться инфицированный ребенок. Заражение происходит при родах или нарушении целостности плаценты в ходе беременности. Вирус гепатита B обнаруживается в слюне, слезах, моче и кале инфицированных лиц. Риск заражения, хотя и незначительный, существует при попадании их на поврежденную кожу и слизистые оболочки другого человека. С пищей, при разговоре, т. е. контактно-бытовым путем гепатит В не передается.
Риск заражения, хотя и незначительный, существует при попадании их на поврежденную кожу и слизистые оболочки другого человека. С пищей, при разговоре, т. е. контактно-бытовым путем гепатит В не передается.
Пути заражения вируса гепатита С (HCV): в основном такие же как при HBV. Половой путь передачи гепатита С мало актуален (не более 3–5%), однако значение его возрастает при наличии большого количества партнеров, случайных связей. От инфицированной матери плоду вирус гепатита С передается редко, не более, чем в 5% случаев и только в процессе родов при прохождении родовых путей. Не отмечена передача вируса с молоком матери и контактно-бытовым путем.
Профилактика. Исходя из вирусной природы указанных заболеваний, вакцинация является наиболее эффективным способом предотвращения распространения инфекции, возникновения острого и хронического гепатита, а, следовательно, и рака печени. В 1980 г. приготовлена вакцина против вируса гепатита В. Согласно рекомендациям, принятым в 1999 г. в США и практикуемым в России, вакцина рекомендована для лиц от 0 до 19 лет. В настоящее время во многих странах мира, включая Россию, введена обязательная вакцинация против гепатита В (HBV) среди новорожденных, детей раннего возраста, подростков и лиц из групп риска. С целью профилактики распространения HBV и рака печени проводится тестирование всех беременных и доноров крови на поверхностный антиген вируса (HbsAg) и антитела к нему (HBs).
Согласно рекомендациям, принятым в 1999 г. в США и практикуемым в России, вакцина рекомендована для лиц от 0 до 19 лет. В настоящее время во многих странах мира, включая Россию, введена обязательная вакцинация против гепатита В (HBV) среди новорожденных, детей раннего возраста, подростков и лиц из групп риска. С целью профилактики распространения HBV и рака печени проводится тестирование всех беременных и доноров крови на поверхностный антиген вируса (HbsAg) и антитела к нему (HBs).
Вирусы папилломы человека (HPV)
Вирусы папилломы человека (HPV) принадлежат к группе Papillomavirus и являются вирусами, которые поражают клетки эпителия эктодермального происхождения (кожа, слизистые половых органов, ротовой полости).
В настоящее время известно более 100 типов HPV, которые могут вызывать бородавки на различных частях тела, но лишь немногие из них связывают с различными злокачественными новообразованиями. Некоторые штаммы вируса папилломы распространяются половым путем и вызывают остроконечные бородавки. Передаваемые половым путем вирусы папилломы связаны с развитием рака шейки матки, полового члена и анального прохода (последние встречаются не так часто). К группе высокого онкогенного риска относят наиболее распространенные в Европе и в России 16-й и 18-й типы вируса (HPV 16 и HPV 18), а также менее распространенные 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы, ответственные, соответственно, за возникновение 65–75% и 18–20% случаев рака шейки матки (РШМ). Раннее обнаружение и лечение может уменьшить риск рака шейки матки, поэтому врачи советуют женщинам с выявленными вирусами папиломы периодически проводить тест мазок Папаниколау. Вирус папилломы человека является довольно распространенными венерическим заболеваниям с несколькими миллионами новых случаев инфицирования, диагностируемых каждый год.
Передаваемые половым путем вирусы папилломы связаны с развитием рака шейки матки, полового члена и анального прохода (последние встречаются не так часто). К группе высокого онкогенного риска относят наиболее распространенные в Европе и в России 16-й и 18-й типы вируса (HPV 16 и HPV 18), а также менее распространенные 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы, ответственные, соответственно, за возникновение 65–75% и 18–20% случаев рака шейки матки (РШМ). Раннее обнаружение и лечение может уменьшить риск рака шейки матки, поэтому врачи советуют женщинам с выявленными вирусами папиломы периодически проводить тест мазок Папаниколау. Вирус папилломы человека является довольно распространенными венерическим заболеваниям с несколькими миллионами новых случаев инфицирования, диагностируемых каждый год.
Пути заражения. Передача инфекции осуществляется половым путем, возможны перинатальный (от матери к плоду) и оральный пути заражения. Большинство лиц обоего пола инфицируется вирусом в первые годы половой жизни. В последние 20–30 лет уровень инфицированности существенно возрос. У 90% женщин HPV инфекция протекает без явных клинических проявлений и вирус исчезает самостоятельно через год после инфицирования под влиянием иммунной системы организма. В трети случаев вирусную ДНК можно выявить более чем через год и в 10% — более чем через два года. Инфекция данным вирусом очень распространена среди здоровых женщин. К 50-летнему возрасту ею переболевает 8 женщин из 10.
В последние 20–30 лет уровень инфицированности существенно возрос. У 90% женщин HPV инфекция протекает без явных клинических проявлений и вирус исчезает самостоятельно через год после инфицирования под влиянием иммунной системы организма. В трети случаев вирусную ДНК можно выявить более чем через год и в 10% — более чем через два года. Инфекция данным вирусом очень распространена среди здоровых женщин. К 50-летнему возрасту ею переболевает 8 женщин из 10.
Факторами риска для развития рака шейки матки служат раннее начало половой жизни, частая смена партнеров, сопутствующие урогенитальные инфекции (например, хламидийная или герпетическая), снижение клеточного иммунитета, гормональные воздействия (аборт, беременность, прием гормональных контрацептивов и др.), курение, неправильное питание (дефицит фолиевой кислоты), а также индивидуальные генетические особенности.
Профилактика. После того, как была окончательно доказана роль вирусной инфекции в развитии РШМ, были разработаны несколько вариантов вакцин. В России зарегистрирована и активно используется вакцина «Гардасил».
В России зарегистрирована и активно используется вакцина «Гардасил».
Герпесвирус Эпштейна-Барр (EBV)
Вирус Эпштейн-Барра широко известен как вирус, который вызывает инфекционный мононуклеоз. Вирусом Эпштейн-Барра инфицировано практически всё население планеты. В развивающихся странах почти у каждого ребенка к пятилетнему возрасту выявляются антитела к этому вирусу. В развитых странах инфицированность несколько меньше: в США антитела выявляются у 50% выпускников средних школ, к сорока годам антитела к этому вирусу появляются у 90% населения. 15–25% взрослых являются выделителями вируса.
Данный вирус передается через контакт с жидкостью полости рта и носа инфицированного человека. Дети редко имеют выраженные симптомы вируса Эпштейн-Барра, но даже если они есть, симптомы, как правило, являются такими же, как при широко распространенных вирусных инфекциях. Вирус Эпштейн-Барра после заражения остается в организме, главным образом в лимфоцитах, всю остальную части жизни человека. Он находится в состоянии покоя в течение большей части времени, иногда проявляя себя, но не причиняя никакого реального вреда. При ослаблении организма и снижении защитных сил иммунной системы — вирус может активироваться и вызывать более агрессивные воздействия. Вирус Эпштейн-Барра ассоциируется, в первую очередь с развитием лимфобластомы, болезни Ходжкина, лимфомы носоглотки и лимфомы Беркитта, редкой формой рака, возникающего в лимфатических узлах. Кроме лимфобластомы, следует назвать такие вызываемые вирусом доброкачественные и злокачественные новообразования, как волосатоклеточная лейкоплакия полости рта, рак носоглотки и др., возникающие на фоне иммунодефицита организма различного происхождения.
Он находится в состоянии покоя в течение большей части времени, иногда проявляя себя, но не причиняя никакого реального вреда. При ослаблении организма и снижении защитных сил иммунной системы — вирус может активироваться и вызывать более агрессивные воздействия. Вирус Эпштейн-Барра ассоциируется, в первую очередь с развитием лимфобластомы, болезни Ходжкина, лимфомы носоглотки и лимфомы Беркитта, редкой формой рака, возникающего в лимфатических узлах. Кроме лимфобластомы, следует назвать такие вызываемые вирусом доброкачественные и злокачественные новообразования, как волосатоклеточная лейкоплакия полости рта, рак носоглотки и др., возникающие на фоне иммунодефицита организма различного происхождения.
Пути заражения. Основной путь передачи вируса — воздушно-капельный, но наиболее часто передача вируса происходит при непосредственных контактах слизистой рта (поцелуях). Заражение возможно и через содержащие вирус пищевые продукты, а также бытовым путём через руки и предметы обихода, при переливании крови и других парентеральных вмешательствах. Зафиксирован также половой путь передачи.
Зафиксирован также половой путь передачи.
Ко-факторы. Поскольку у большинства лиц, инфицированных EBV, какой-либо патологии не возникает, то для ее появления, включая злокачественные новообразования, очевидно, необходимо воздействие на организм дополнительных факторов. Среди известных следует назвать паразитарные инфекции типа малярии; массивную инфекцию EBV в. раннем детском возрасте; ослабление иммунной системы; хроническое недоедание, а также использование в пищу продуктов, обладающих коканцерогенным действием; влияние любых факторов, вызывающих хромосомные мутации. Таким образом, можно сделать вывод, что инфицирование EBV является важным, но недостаточным условием для возникновения ассоциированных с ним онкологических заболеваний, чтобы возникла опухоль, необходимо действие ряда дополнительных факторов.
Герпесвирус саркомы Капоши (KSHV/HHV-8)
Открытый в 1994 г. герпесвирус саркомы Капоши в семействе герпесвирусов обозначен под номером 8 (HHV-8).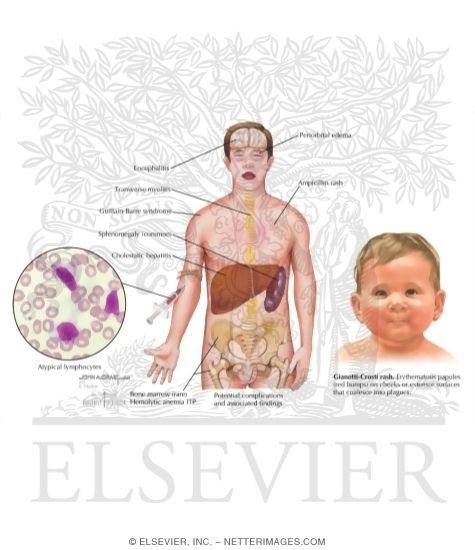 В настоящее время считается доказанной его этиологическая роль в возникновении довольно редко встречающихся заболеваний, а именно саркомы Капоши (СК), выпотной В-клеточной лимфомы полостей тела (PEL) и болезни Кастлемана.
В настоящее время считается доказанной его этиологическая роль в возникновении довольно редко встречающихся заболеваний, а именно саркомы Капоши (СК), выпотной В-клеточной лимфомы полостей тела (PEL) и болезни Кастлемана.
Распространенность HHV-8. Инфицированность населения HHV-8 в различных географических регионах существенно отличается и варьирует от долей процента в США и большинстве стран Западной Европы до 8–10% в странах Средиземноморья (Греция, Италия). Самый высокий процент серопозитивных лиц обнаружен в странах Восточной, Центральной и Западной Африки — странах, эндемичных для СК, где уровень инфицированности населения этим вирусом достигал 50–70%. В России уровень инфицированности HHV-8 среди доноров крови находится в пределах 4%.
Пути заражения. Основной путь передачи HHV-8 — половой, но также со слюной (при поцелуе), и с кровью (редко).
Профилактика. Учитывая половой путь передачи вируса основной профилактической мерой является практика безопасного секса, лечение хронического уропростатита у больных с выявленным HHV-8 в эякуляте и/или секрете предстательной железы, применение противовирусных препаратов в группах риска (больные, нуждающиеся в трансплантации органов и ВИЧ-инфицированные).
Профилактическая анти-вирусная (противоопухолевая) вакцина не создана, над ее изготовлением ведется работа.
Вирус Т-клеточного лейкоза человека (HTLV-1)
Вирус Т-клеточного лейкоза человека (HTLV-1) — это онкогенный ретровирус, являющийся этиологическим фактором Т-клеточного лейкоза/лимфомы взрослых, протекающей чрезвычайно агрессивно со средней продолжительностью жизни около 6 месяцев, и нейро-дегенеративного заболевания под названием HTLV-1-ассоциированная миелопатия или тропического спастического парапареза. В регионах с высокой инфицированностью данным вирусом диагностируются также ассоциированные с вирусом увеиты, артриты, базедова болезнь, инсулинзависимый диабет, синдром Цезаря и др.
Распространенность. Спорадические случаи HTLV-1 инфекции встречаются во многих странах мира, включая Россию. Эндемичными же для этой инфекции являются некоторые регионы Японии, Южной Америки, Африки и часть стран Карибского бассейна.
Пути заражения. Существуют 3 основных пути передачи инфекции от инфицированных лиц: а) с молоком матери; б) при половом контакте главным образом через сперму; и в) с переливаемой кровью при гемотрансфузиях.
Существуют 3 основных пути передачи инфекции от инфицированных лиц: а) с молоком матери; б) при половом контакте главным образом через сперму; и в) с переливаемой кровью при гемотрансфузиях.
Ко-факторы. У большинства лиц, инфицированных HTLV-1, какой-либо патологии не возникает. После заражения вирусом ATL регистрируют не более чем у 1–5% вирусоносителей даже в эндемических для этого заболевания регионах и после длительного латентного периода, длящегося порой десятилетиями. Факторами, способствующими развитию ATL, являются паразитарные инфекции типа эписторхоза, использование иммунодепрессантов любого происхождения, ВИЧ-инфекция и др.
Профилактика. Для профилактики инфекции рекомендованы: отмена кормления грудным молоком младенцев инфицированными матерями; предохраняемый секс и контроль на присутствие HTLV-1 донорской крови не только в регионах с высоким уровнем распространения HTLV-1 среди населения, но и в других, т. к. переливание инфицированной вирусом крови, может способствовать его распространению и появлению заболеваний, связанных с HTLV-1 там, где они сейчас отсутствуют.
Вирус иммунодефицита человека, HIV (ВИЧ)
Этот вирус был открыт в 1983 г. и его ассоциация с синдромом приобретенного иммунодефицита (СПИД) доказана в 1984 г. Как уже упоминалось ранее, ВИЧ не обладает трансформирующим геном (онкогеном). Инфицированные им клетки (главным образом СD4+ Т-клетки и макрофаги) не подвергаются усиленной пролиферации (делению), а разрушаются, вызывая у инфицированного лица нарастающую степень иммунодефицита, и создавая тем самым условия, необходимые для возникновения опухоли. Доказано, что у больных СПИД`ом примерно 50% новообразований ассоциировано с Эпштейн-Барр вирусом или герпес вирусом саркомы Капоши (HHV-8). Чаще всего у таких больных диагностируют саркому Капоши либо одну из разновидностей не-ходжкинских лимфом. Характеристика этих новообразований, механизмы канцерогенеза, а также методы профилактики и лечения даны в предыдущих разделах, их можно найти также в многочисленных отечественных и зарубежных публикациях.
Заключение
Несмотря на различную организацию онкогенных вирусов человека, неодинаковый спектр их клеток-мишеней, они обладают рядом общих биологических свойств, а именно:
- вирусы лишь инициируют патологический процесс, усиливая пролиферацию (разрастание ткани организма путём размножения клеток делением) и генетическую нестабильность инфицированных ими клеток;
- у инфицированных онкогенными вирусами лиц возникновение опухоли, как правило, событие нечастое: один случай новообразования возникает среди сотен, иногда тысяч инфицированных;
- продолжительность латентного периода от инфицирования до возникновения опухоли составляет иногда десятилетия;
- у большинства инфицированных лиц возникновение опухоли не является обязательным, но они могут составить группу риска, с более высокой возможностью ее возникновения;
- для злокачественной трансформации инфицированных клеток в организме человека необходимы дополнительные факторы и условия, приводящие к возникновению опухоли.
Профилактика активации вирусов и развития рака
- отказ от курения;
- коррекция питания и образа жизни;
- сокращение воздействия канцерогенных веществ;
- повышение защитной функции организма;
- определение и терапия заболеваний, находящихся в предраковой стадии;
- наблюдение групп высокого риска появления онкологий;
- диагностика рака на ранних стадиях.
Можно ли заразиться раком от больного человека, либо от носителя вируса?
То, что окружающие в безопасности рядом с онкобольными людьми, уже неоднократно доказано и подтверждено проведенными опытами. В 19 веке французским хирургом был выделен экстракт рака молочной железы. Затем он ввел его себе, и еще нескольким людям, участвовавшим в опыте добровольно, этот экстракт под кожу. В месте, куда была проведена инъекция, начались острые воспалительные процессы, которые прошли спустя несколько дней. Опыт в скором времени был проведен еще раз и результаты оказались те же.
Современные ученые также проводили исследования, которые подтвердили, что заразиться раком от другого человека невозможно. Медицинские работники провели анализ 350 тысяч процедур переливания крови, проводимые в течение 35 лет. У трех процентов доноров был обнаружен рак, однако ни один из людей, которым переливали кровь онкобольных, не был заражен.
Еще один важный вывод после проведенных медицинских исследований — генетика на появление раковых образований влияет гораздо больше, чем вирусы и другие факторы. Это значит, что попавший в организм онковирус имеет в развитии рака практически нулевую значимость, тогда как сбой в генетическом коде — ключевую.
Выводы
Вирусы, вызывающие рак — очень опасны для жизни и здоровья человека. Их профилактика и своевременная диагностика поможет максимально снизить риск появления серьезных последствий. При появлении каких-либо признаков вирусной инфекции необходимо срочно обратиться к компетентному специалисту и сдать анализы, которые помогут их выявить и вовремя принять необходимые меры.
Инфекционный мононуклеоз (мононуклеоз, EBV-мононуклеоз) — Медицинский округ Южного Невады
Что такое инфекционный мононуклеоз?
Инфекционный мононуклеоз — это вирусное заболевание, поражающее определенные клетки крови. Это вызвано вирусом Эпштейна-Барра (EBV), который является членом семейства вирусов герпеса. Большинство случаев возникают спорадически; вспышки редки.
Кто заболевает инфекционным мононуклеозом?
В то время как большинство людей когда-нибудь в жизни подвергаются воздействию вируса Эпштейна-Барра, у очень немногих развиваются симптомы инфекционного мононуклеоза.
- В слаборазвитых странах дети подвергаются воздействию в раннем детстве, и у них вряд ли разовьются заметные симптомы.
- В развитых странах, таких как Соединенные Штаты, возраст первого контакта может быть отложен до более старшего детства и молодого взрослого возраста, когда вероятность появления симптомов выше.
- По этой причине он чаще распознается у старшеклассников и студентов.
Как распространяется инфекционный мононуклеоз?
Вирус передается от человека к человеку через слюну (на руках, игрушках или при поцелуях). В редких случаях вирус передается при переливании крови.
Каковы симптомы инфекционного мононуклеоза?
Симптомы включают в себя
- Лихорадка
- Больное горло
- Опухшие гланды
- Чувство усталости
- Иногда поражаются печень и селезенка.
Продолжительность от одной до нескольких недель. Заболевание очень редко заканчивается летальным исходом. После заражения очень маленькие дети могут не иметь никаких симптомов.
Как скоро появляются симптомы?
Симптомы появляются через 4-6 недель после заражения.
Как долго человек может распространять инфекционный мононуклеоз?
Вирус выделяется из горла во время болезни и в течение одного года после заражения.
После первоначального заражения вирус имеет тенденцию к длительному бездействию, а затем может реактивироваться и снова выделяться из глотки.
Как лечить инфекционный мононуклеоз?
В подавляющем большинстве случаев не требуется никакого лечения, кроме отдыха. Людям с сильной болью в горле следует обратиться к врачу.
Может ли человек снова заболеть инфекционным мононуклеозом?
Люди, которые заболевают, редко заболевают снова.
Что может сделать человек, чтобы минимизировать распространение инфекционного мононуклеоза?
Избегайте действий, связанных с передачей жидкостей организма (обычно слюны) тем, кто в настоящее время или недавно был инфицирован этим заболеванием.
В настоящее время вакцины для предотвращения инфекционного мононуклеоза не существует.
Где я могу получить больше информации?
Обратитесь к врачу или в отдел эпидемиологии Южного Невады по телефону (702) 759-1300.
Вирус Эпштейна — Барр
(Epstein-Barr virus, Вирус Герпеса Человека 4 типа).
Краткое название: ВЭБ, ВГЧ-4, EBV, HHV-4.
Классификация: Семейство: Герпесвирусы, Подсемейство: y — герпесвирусы (гамма- герпесвирус).
В 1961 году английский хирург Денис Парсон Беркитт, работавший в Уганде, представил научный доклад, который свидетельствовал о том, что в некоторых странах Африки, где жарко и влажно, у детей с частотой 8 случаев на 100 000 населения встречается особое онкологическое заболевание, получившее впоследствии название «Лимфома Беркитта».
Выяснением причин, вызывающих это заболевание, занялись ученые М. А. Эпштейн, Ю. М. Барр и Ачонг (Epstein, Barr & Achong). В 1964 году ими в образцах опухоли, присланной доктором Беркиттом, при помощи электронного микроскопа был открыт ранее неизвестный герпес-вирус, получивший название «Вирус Эпштейн — Барр».
Этот вирус вызывает сразу несколько заболеваний: первое — инфекционный мононуклеоз или болезнь поцелуев. Передается через слюну, при рукопожатиях, через игрушки, при переливании крови, при оральном сексе и поцелуях. Инфицируются в основном дети и молодежь. До 50% деток в возрасте до 5 лет, живущие в развивающихся странах, носят в себе ВЭБ, который они получили от матерей. В развитых странах такой же процент инфицированных наблюдается среди 18 летних. В США 95% взрослых, которые достигли 35 летнего возраста, инфицированы вирусом Эпштейн- Барр.
Течение болезни: После инкубационного периода, длительность которого может достигать 1-2 месяца, вирус начинает активно размножаться на покровных клетках носа и глотки, а также в лимфатических узлах. Болезнь дебютирует с озноба и резкого подъема температуры до 38-40 градусов С, симптомов ОРЗ, ангины, фарингита и лихорадки. Больные жалуются на головную боль, потливость, боли при глотании.
Размножившись, вирус попадает в кровь, которая разносит его по всем органам человеческого тела. Вирусные частицы находят в слюнных железах, шейке матки, лимфоузлах, печени и селезенке. Вирус выделяется в окружающую среду со слизью из шейки матки и слюной больного человека. Если ощупать пациента, то в разных частях тела будут обнаруживаться увеличенные, безболезненные лимфатические узелки.
Характерным для мононуклеоза явл. увеличение узлов на затылке, под подбородком и в углах нижней челюсти.
У 50% больных может увеличиться селезенка, печень. У людей с ослабленным иммунитетом (иммунодефицит, СПИД) поражается сердце и нервная система. В тяжелых случаях возможно возникновение желтухи и даже разрыв селезенки. О разрыве селезенке могут свидетельствовать внезапно возникшие резкие боли в животе слева, в области желудка. При этом развивается кровотечение, которое может вызывать, головокружение, сердцебиение и затруднение дыхания. Если пациент с разрывом селезенки в течении 20-60 минут не будет доставлен в хирургическое отделение, то он неминуемо погибнет.
Апофеозом жизни вируса в организме человека является «победа» над белыми кровяными тельцами, выражающаяся в резком уменьшение их количества, и свойств. Изменяется, так называемая, формула крови.
Заболевание проходит самостоятельно в течение нескольких недель или 1-2х месяцев.
Диагностика: Как правило, диагноз можно поставить при остром течении по 3 основным симптомам: лихорадка, фарингит и увеличение лимфоузлов. Важна лабораторная реакция на наличие антител, позволяющая определить стадию заболевания.
Первая помощь: при повышении температуры и болях дать больному теплое питье и парацетамол. Обратиться к инфекционисту или терапевту.
Лечение: Специфических противовирусных препаратов и вакцин на сегодняшний день не изобретено. Рекомендован постельный режим, обильное питье. При болях в горле — полоскание соленой водой или содой. В случает лихорадки и повышения температуры пациенту дают парацетамол или ибупрофен или тайленол. Аспирин настоятельно не рекомендуется из-за риска развития синдрома Рейе. В течении 1 месяца после выздоровления следует избегать занятий спортом и воздержаться от посещения физкультуры в школе.
Антибиотики не могут помочь при инфекционном мононуклеозе, так как инфекция имеет вирусную природу. Они назначаются врачом лишь при гнойных осложнениях. При поражении внутренних органов применяются кортикостероиды.
Не выявлено связи между инфекционным мононуклеозом и лимфопролиферативными заболеваниями.
Второе заболевание, вызываемое вирусом Эпштейн — Барр — Лимфома Беркитта.
Встречается только в Африке (Нигерия, Гвинея Бисау, Уганда). Болеют, как правило, дети от 4 до 8 лет. Опухоль, вызванная вирусом Эпштейн — Барр, поражает яичники и верхнюю или нижнюю челюсть, лимфатические узлы, надпочечники и почки. Вирус находят в лимфобластах и лимфатических узлах. Известно, что ВЭБ провоцирует назофарингиальную карциному и является одной из причин лимфогранулематоза.
Лечение: При лимфоме Беркитта по назначению онколога применяется препарат «Неосар» (циклофосфамид, цитоксан) в виде раствора для инъекций и таблеток.
В настоящее время разрабатывается вакцина, защищающая здорового человека от инфицирования вирусом Эпштейн — Барр.
Вирус Эпштейна-Барр (ВЭБ) — ОВУМ – медицинская лаборатория в Кемерοво
Описание
Описание анализа
Вирус Эпштейна-Барр (ВЭБ) – это ДНК-содержащий вирус, является вирусом герпеса человека 4-го типа, относится к подсемейству гамма-герпесвирусов. ВЭБ имеет глобальное распространение и обнаруживается у населения всего земного шара.
Заразиться можно от больного человека и от здорового носителя вируса. ВЭБ передается от человека к человеку воздушно-капельным путем (при чихании, кашле, через слюну, при поцелуях), контактно-бытовым путем (через предметы), при половых контактах, при беременности вирус может проходить через плаценту и инфицировать плод, вирус может передаваться при переливании крови.
ВЭБ поражает эпителиальные клетки слизистых оболочек (дыхательных путей, пищеварительной системы, половых органов), а также клетки иммунной системы, в том числе В-лимфоциты, в которых происходит размножение вируса.
Чаще всего вирусом заражаются в детстве. У детей инфекция в основном протекает бессимптомно или в стертой форме (в виде респираторной инфекции). У взрослых людей в 90% случаев инфекция также протекает без признаков заболевания.
Инфицирование ВЭБ может проявляться в виде инфекционного мононуклеоза: повышается температура тела, возникает боль в горле, увеличиваются лимфатические узлы, печень и селезенка. При проведении клинического анализа крови выявляется увеличение лимфоцитов, могут быть обнаружены атипичные мононуклеары.
После первичного инфицирования вирус Эпштейна—Барр остается в организме пожизненно, персистируя в В-лимфоцитах и отдельных клетках эпителия. В определенных условиях, при снижении иммунитета, гормональных перестройках, после перенесенных заболеваний, вирус может активироваться.
При хроническом течении инфекции может развиться синдром хронической усталости.
ВЭБ может принимать участие в развитии некоторых опухолей: лимфомы Беркетта, карциномы носоглотки, болезни Ходжкина, саркомы Капоши. Заболевания, вызванные вирусом Эпштейн-Барр, встречаются редко. Чаще они развиваются у лиц с генетической предрасположенностью или выраженным иммунодефицитным состоянием.
Что показывает ПЦР анализ на вирус Эпштейна-Барр?
ПЦР анализ является прямым методом диагностики, т.е. обнаруживает непосредственно возбудителя инфекции в исследуемом материале.
Исследование проводится методом ПЦР в режиме реального времени. ПЦР тест определяет участки ДНК ВЭБ в биологическом материале (в крови, ликворе, соскобах, моче, и др.) и показывает его количество — вирусную нагрузку.
Определение количества вируса позволяет оценивать динамику лечения.
Кому показано обследование на вирус Эпштейна-Барр методом ПЦР?
- Людям с проявлениями инфекционного мононуклеоза.
- Людям с подозрением на инфекцию, вызванную ВЭБ.
Результата анализа
Полученный результат исследования обязательно должен интерпретировать лечащий врач с учетом всех данных о состоянии здоровья пациента и комплекса проведенных лабораторных анализов.
Правила подготовки
Мононуклеоз | Детский медицинский кабинет
Инфекция, вызванная вирусом Эпштейна-Барра (ВЭБ), широко известная как мононуклеоз или «мононуклеоз», может возникнуть в любом возрасте, но чаще всего встречается в подростковом и раннем взрослом возрасте. Как правило, чем моложе человек, когда он становится моно, тем лучше — дети меньше болеют им и выздоравливают быстрее, чем подростки, а подросткам, в свою очередь, легче, чем взрослым!
Mono работает в три этапа. Во-первых, продромальный период длится 1-2 недели с небольшими симптомами или вообще без них.Во-вторых, острая фаза продолжительностью от 2 до 6 недель, во время которой человек может сильно заболеть лихорадкой, опухшими железами, сильной болью в горле и истощением. И в-третьих, фаза выздоровления, продолжающаяся от 2 до 6 месяцев, в течение которой острые симптомы исчезли, но пациент страдает пониженной физической и умственной энергией, выносливостью и легкой утомляемостью. Во время острой фазы и фазы выздоровления люди подвергаются повышенному риску разрыва селезенки в случае тупой травмы живота. Во время любой из этих фаз не существует никакого лечения, кроме поддерживающей терапии (жидкости, обезболивание, контроль температуры).
В большинстве случаев к моменту постановки диагноза ВЭБ острая фаза наступает через неделю или больше. На этом этапе полезны следующие меры:
- Примите ацетаминофен (Тайленол) или ибупрофен (Адвил или Мотрин), чтобы снизить температуру и уменьшить боль от боли в горле.
- Полоскать горло четыре раза в день теплой водой, смешанной с чайной ложкой антацида или соли.
- Если глотать больно, попробуйте есть более мягкую пищу. Особенно хороши молочные коктейли и холодные напитки.Избегайте апельсинового или грейпфрутового сока.
- Принимайте поливитамины каждый день.
- Не делитесь напитками или столовым серебром с другими.
- Пейте много жидкости, не менее 8 стаканов в день.
- Отдыхайте, когда чувствуете усталость. Вам не нужно оставаться в постели, если вы чувствуете себя достаточно хорошо, чтобы встать.
ВЭБ заразен, но только при тесном контакте, например, поцелуях, совместном использовании посуды или продолжительном домашнем контакте. Обычно это НЕ передается через случайные социальные контакты, которые могут произойти в классе.ВЭБ является членом семейства вирусов герпеса и, как и другие вирусы герпеса после первичной инфекции, живет в организме пациента (внутри подмножества белых кровяных телец) всю оставшуюся жизнь. В этом латентном состоянии он безвреден, но периодически проходит фазы репликации, во время которых индивидуум-хозяин выделяет вирус и заразен для ВЭБ, несмотря на отсутствие симптомов на всю оставшуюся жизнь. Таким образом, вопрос о том, чтобы быть «более не заразным», не имеет большого значения и не имеет отношения к тому, когда человеку следует вернуться в школу.
Обычно мы рекомендуем, чтобы дети или подростки с ВЭБ возвращались в школу на этапе выздоровления, в основном, как только они «почувствуют себя готовыми»; но с некоторыми модификациями, чтобы компенсировать их пониженную выносливость. Самым важным из них является запрет на занятия всеми контактными видами спорта (футбол, борьба, хоккей и т. Д.) В течение 6 недель с момента начала заболевания (острая фаза) из-за риска разрыва селезенки. Отказ от тренажерного зала и других физических нагрузок в течение первых 4-6 недель после возвращения в школу также может быть разумным только из-за недостатка энергии.В тяжелых случаях следует также рассмотреть возможность уменьшения объема домашних заданий и / или укороченного учебного дня на некоторое время после возвращения. Дети, находящиеся на этапе выздоровления в монотерапии, должны иметь возможность пойти в кабинет медсестры, чтобы отдохнуть или вздремнуть, если они почувствуют в этом потребность и в течение учебного дня.
Железистая лихорадка — Болезни и состояния
Большинство людей с железистой лихорадкой выздоравливают через две-три недели и больше не испытывают никаких проблем.
Однако в некоторых случаях могут развиться осложнения.Некоторые из основных осложнений, связанных с этим заболеванием, описаны ниже.
Длительная усталость
Более 1 из каждых 10 человек с железистой лихорадкой будут испытывать длительную усталость, которая длится в течение шести или более месяцев после первоначального заражения. Неизвестно, почему у некоторых людей утомляемость длится дольше.
Некоторые эксперты считают, что это может быть форма синдрома хронической усталости (СХУ). Это плохо изученное состояние, которое вызывает стойкую усталость и ряд других симптомов, таких как головные боли и боли в суставах.
Постепенный план упражнений для восстановления сил и энергии может помочь предотвратить и уменьшить длительную усталость.
Уменьшение клеток крови
В некоторых случаях железистая лихорадка может привести к уменьшению количества клеток крови. Может снизить уровень:
- эритроцитов (анемия) — из-за них вы чувствуете усталость и одышку
- лейкоцитов (нейтропения) — это может сделать вас более склонным к развитию вторичной инфекции
- тромбоцитов — это может вызвать у вас синяки и кровотечение
В большинстве случаев уменьшение количества клеток крови невелико и вызывает лишь легкие симптомы.Эти проблемы должны исчезнуть сами по себе в течение нескольких недель или месяцев.
Разрыв селезенки
Около половины людей, у которых развивается железистая лихорадка, имеют опухшую селезенку. Это не представляет никаких непосредственных проблем со здоровьем, но есть небольшой риск разрыва (разрыва).
Главный признак разрыва селезенки — резкая боль в левой части живота (живота).
Обратитесь в местное отделение неотложной помощи (A&E) или наберите 999, чтобы вызвать скорую помощь, если у вас железистая лихорадка и у вас развиваются сильные боли в животе.
Риск разрыва селезенки невелик и встречается всего в 1 из каждых 500–1000 случаев железистой лихорадки, но это может быть опасно для жизни, поскольку может вызвать сильное внутреннее кровотечение.
В некоторых случаях может потребоваться экстренная операция для удаления увеличенной или разорванной селезенки (спленэктомия).
Разрыв селезенки обычно возникает в результате повреждения, вызванного интенсивными физическими нагрузками, например, контактными видами спорта.
Поэтому очень важно избегать этих действий в течение как минимум месяца после появления симптомов железистой лихорадки.
Будьте особенно осторожны в течение второй и третьей недели болезни, так как именно в это время селезенка наиболее уязвима.
Осложнения неврологического характера
Менее чем в 1 из 100 случаев вирус Эпштейна-Барра (EBV) может поражать нервную систему и вызывать ряд неврологических осложнений, в том числе:
- Синдром Гийена-Барре — воспаление нервов, вызывающее такие симптомы, как онемение, слабость и временный паралич
- Паралич Белла — мышцы на одной стороне лица временно ослабляются или парализованы
- вирусный менингит — инфекция защитных оболочек, окружающих головной и спинной мозг; вирусный менингит, хотя и неприятен, гораздо менее опасен, чем бактериальный менингит, который опасен для жизни
- энцефалит — инфекция головного мозга ,00
Эти осложнения часто требуют специального лечения, но более четырех из каждых пяти человек с ними полностью выздоравливают.
Вторичная инфекция
В небольшом количестве случаев первоначальная инфекция ослабляет вашу иммунную систему и позволяет бактериям заражать части тела. Это называется вторичной бактериальной инфекцией.
Возможные вторичные инфекции, которые могут развиться во время железистой лихорадки, включают серьезные состояния, такие как пневмония (инфекция легких) и перикардит (инфекция мешка, окружающего сердце).
Вторичные инфекции обычно возникают у людей с очень слабой иммунной системой, например у людей с ВИЧ или СПИДом, или у тех, кто проходит химиотерапию.
Если у вас ослабленная иммунная система и у вас развивается железистая лихорадка, в качестве меры предосторожности вас могут направить в больницу для лечения у специалиста. Это позволит тщательно следить за вашим здоровьем и лечить любые вторичные инфекции.
Тест на вирус Эпштейна-Барра: процедура, результаты и интерпретация
Вирус Эпштейна-Барра — это вирус семейства герпесов. Врач может проверить наличие этого вируса с помощью простого анализа крови, называемого тестом на вирус Эпштейна-Барра.
Вирус Эпштейна-Барра очень распространен, и большинство людей в какой-то момент своей жизни поражается им.
Вирус Эпштейна-Барра очень заразен, и люди заражаются им через контакт со слюной или другими биологическими жидкостями. Когда человек заразился вирусом один раз, он остается в организме в спящем состоянии и может реактивироваться в любой момент.
У детей вирус часто не вызывает никаких симптомов. Однако у подростков и взрослых он может вызывать моно- или мононуклеоз, а также может быть связан с другими заболеваниями, включая некоторые виды рака.
Симптомы заражения вирусом Эпштейна-Барра аналогичны симптомам некоторых других болезней. Из-за этого сходства врачи могут порекомендовать тест на вирус Эпштейна-Барра или тест на ВЭБ, чтобы определить, есть ли у человека текущая или перенесенная вирусная инфекция Эпштейна-Барра.
Симптомы заражения вирусом Эпштейна-Барра включают:
В некоторых случаях печень или селезенка человека также могут опухать и увеличиваться в размерах.
Поделиться на PinterestТест на вирус Эпштейна-Барра используется для определения наличия определенных антител.Когда человек заражен вирусом Эпштейна-Барра, его иммунная система выделяет белки, известные как антитела, для борьбы с вирусом. Тест на вирус Эпштейна-Барра проверяет их кровь на антитела к вирусу Эпштейна-Барра с помощью простого анализа крови.
Присутствие этих антител подтвердит, что кто-то болел вирусом Эпштейна-Барра в прошлом или в настоящее время имеет активную инфекцию.
Медицинский техник выполняет тест на антитела к вирусу Эпштейна-Барра так же, как и любой другой простой анализ крови.Никакой подготовки не требуется.
Техник будет использовать следующие шаги:
- проверить руку на наличие подходящей вены, из которой можно взять кровь
- очистить область антисептиком
- обернуть эластичную ленту вокруг плеча, в результате чего вена набухнет. кровь
- используйте небольшую иглу для взятия образца крови
- удалите иглу и наложите марлю на место инъекции, чтобы предотвратить кровотечение
Кровь будет отправлена в лабораторию для проверки наличия вируса Эпштейна-Барра антитела.
Врач может порекомендовать человеку пройти тест на вирус Эпштейна-Барра, если у него проявляются симптомы инфекции или мононуклеоза, особенно если его тест на мононуклеоз уже дал отрицательный результат.
Симптомы могут включать:
- опухшие железы
- ригидность шеи
- боль в горле
- усталость
- лихорадка
- головная боль
- увеличение селезенки
Врач с большей вероятностью назначит этот тест, если человек находится в в подростковом возрасте или в возрасте до 20 лет.
Результаты теста на вирус Эпштейна-Барра могут быть либо «нормальными», либо «ненормальными».
Если результаты возвращаются как «нормальные», это означает, что лаборатория не обнаружила ни одного вируса Эпштейна-Барра. вирусные антитела в крови. В этом случае маловероятно, что у человека есть вирус Эпштейна-Барра или мононуклеоз.
Когда тест проводится слишком рано после заражения, в крови может быть недостаточно антител для получения положительного результата. Поэтому, если у человека симптомы не исчезнут и врач не может найти другую причину, может потребоваться повторный тест через 2 недели.
Если результаты теста нормальные, человек все еще может заразиться вирусом Эпштейна-Барра в какой-то момент в будущем.
Если результаты теста на вирус Эпштейна-Барра «ненормальные», это означает, что лаборатория обнаружила одно из трех или комбинацию антител Эпштейна-Барра. Эти антитела дают врачам информацию о том, когда произошел вирус:
- Если антитело, называемое VCA IgG, присутствует, значит, вирус Эпштейна-Барра возник когда-то недавно или в прошлом.
- Если антитело VCA IgM присутствует без ядерного антигена Эпштейна-Барра (EBNA), вирус, вероятно, активен в настоящее время или возник совсем недавно.
- Если присутствует антитело к EBNA, это означает, что вирус заразился, по крайней мере, 6-8 неделями ранее, но, возможно, дольше, поскольку этому антителу требуется некоторое время для развития после заражения и оно остается в организме на всю жизнь.
Не существует лекарств от вируса Эпштейна-Барра или мононуклеоза. Однако врач может порекомендовать следующее, чтобы облегчить симптомы:
- Больше отдыхайте.
- Избегайте физических нагрузок до исчезновения симптомов.
- Пейте много жидкости, чтобы избежать обезвоживания.
- Снимите боль в горле с помощью парацетамола или ибупрофена.
- Полощите горло соленой водой несколько раз в день.
Люди с активным случаем мононуклеоза могут быстрее почувствовать себя лучше, если они уменьшат свою активность до тех пор, пока болезнь не исчезнет. Если делать слишком много и слишком рано, это может привести к рецидиву или более длительному восстановлению.
Поднятие тяжестей или физические нагрузки могут увеличить риск разрыва селезенки — редкого, но опасного для жизни осложнения мононуклеоза.
Вирус Эпштейна-Барра поражает людей по-разному. Некоторые люди, особенно дети, могут не знать, что у них есть вирус, в то время как у других симптомы могут проявляться в течение недель или месяцев.
Обычно симптомы исчезают в результате активной инфекции Эпштейна-Барра или мононуклеоза через 1-2 месяца. После выздоровления вирус остается в организме бездействующим, и тест на антитела к вирусу Эпштейна-Барра по-прежнему работает. Вирус может реактивироваться в любой момент, но обычно не вызывает симптомов.
Хотя большинство людей с вирусом Эпштейна-Барра выздоравливают, может существовать связь между вирусом Эпштейна-Барра и хроническими заболеваниями и раками, включая лимфому Беркитта и лимфому Ходжкина.
В редких случаях вирус Эпштейна-Барра может оставаться активным и вызывать длительные симптомы.
Детские новообразования, ассоциированные с вирусом Эпштейна-Барра | Архив детских инфекционных болезней
3.1. Принципы
Вирус Эпштейна-Барра (EBV) был выделен из клеток лимфомы Беркитта почти 50 лет назад (1964 г.) (1).Это двухцепочечный ДНК-вирус из семейства Herpesviridae с доказанной связью с раком. Этот вирус имеет определенный тропизм к В-клеткам, но может инфицировать Т-клетки, естественные клетки-киллеры и эпителиальные клетки. Более 90% населения мира являются носителями вируса (2). Этот вирус может вызывать скрытую пожизненную инфекцию (3), а возраст первичной инфекции варьируется в разных обществах в зависимости от социально-экономических факторов. Данные показывают, что плохой социально-экономический фон связан с более высоким уровнем антител в более молодом возрасте, что объясняется более высокой вероятностью заражения этим заболеванием в более раннем возрасте (4).Первичная болезнь ВЭБ протекает бессимптомно в детстве, но синдром инфекционного мононуклеоза (ИМ) может возникать как самоизлечивающееся заболевание у подростков с лихорадкой, недомоганием, спленомегалией, фарингитом и атипичным лимфоцитозом (5). Во время фазы IM может произойти реактивация лимфоида, которая саморазрешается за счет реакции Т-клеток против пролиферации инфицированных В-клеток. Распространение компонентов вириона, включая вирусную ДНК и белки, может происходить в литической фазе, но латентная фаза сопровождается экспрессией шести ядерных антигенов (EBNA 1, 2, 3A, 3B, 3C и LP), двух некодирующих малых РНК (EBER 1 и 2) и три латентных мембранных белка (LMP1, 2A и 2B) (6).За репликацией вируса Эпштейна-Барра в литической фазе следует латентная (антиген-отрицательная) фаза, сопровождающаяся инфицированием В-клеток памяти (7). Обнаружено, что вирус Эпштейна-Барра обладает мощным трансформирующим агентом роста В-клеток, с помощью которого он может способствовать лимфомагенезу через онкогенные механизмы (8). Эта онкогенная способность связана с латентным периодом и механизмами экспрессии генов вируса. Есть три типа задержки. В каждый латентный период экспрессируются разные антигены. В латентный период 1 экспрессируются EBER и EBNA1.При задержке 2 экспрессируются LMP1 и 2, а при задержке 3 — EBER, все шесть EBNA и два LMP. Некоторые типы опухолей, положительных по ВЭБ, имеют специфические экспрессии генов, которые могут не точно соответствовать этим трем латентным категориям. Вирус Эпштейна-Барра может быть ответственным за многие В-клеточные лимфопролиферативные расстройства, такие как лимфома Ходжкина (классический тип), LPD, связанные с вирусом иммунодефицита, посттрансплантационные и связанные с иммунодефицитом LPD, а также лимфома Беркитта. Кроме того, этот вирус может быть связан с группой Т-клеточных лимфом периферического происхождения, такой как носовые естественные киллеры / экстранодальные Т-клеточные лимфомы, ангиоиммунобластные Т-клеточные лимфомы, аденокарцинома желудка и опухоли гладких мышц.Вирус Эпштейна-Барра связан со многими карциномами. Обнаружение EBNA1 в опухолевой ткани — интересный критерий для рассмотрения EBV как ответственного вируса (9).
3.2. Лимфоидные злокачественные новообразования, связанные с вирусом Эпштейна-Барра
Многие лимфоидные злокачественные новообразования вызваны скрытой инфекцией ВЭБ. На вирус Эпштейна-Барра приходится 20% случаев лимфомы Беркитта (ЛБ) у иммунокомпетентных людей в развивающихся странах. Приблизительно все случаи BL африканского типа, 50% случаев лимфомы Ходжкина, а также некоторые типы крупноклеточной В-клеточной лимфомы (диффузного типа) и Т-клеточной лимфомы вызваны ВЭБ.Лимфопролиферативные расстройства, связанные с ВЭБ, можно разделить на две группы; первая группа происходит от В-клеток, а вторая связана с Т-клетками или естественными киллерами (Т / НК). LPD, ассоциированные с вирусом Эпштейна-Барра, имеют четыре подтипа, включая классическую лимфому Ходжкина, лимфому Беркитта, лимфопролиферативные расстройства, вторичные после трансплантации, и LPD, связанные с ВИЧ. LPD, сопровождающиеся ВИЧ, можно разделить на четыре группы: первичная лимфома ЦНС, диффузная В-клеточная лимфома (иммунобластная), вирус герпеса человека 8 (HHV 8) и плазмобластная лимфома.Лимфопролиферативные нарушения NK и T-клеток, связанные с EBV, делятся на три категории: периферическая (неуточненная) T-клеточная лимфома, T-клеточная лимфома (ангиоиммунобластный тип) и носовая T / NK-клеточная лимфома (экстранодальный тип) (10).
3.3. Лимфома Ходжкина, ассоциированная с вирусом Эпштейна-Барра,
Лимфома Ходжкина в детском возрасте составляет примерно 10% всех диагностированных случаев лимфомы Ходжкина. Более того, 30-50% случаев лимфомы Ходжкина связаны с EBV (EBV-положительной лимфомой Ходжкина).Этот тип лимфомы Ходжкина чаще встречается как подтип со смешанной клеточностью и часто встречается у детей и пожилых людей (> 45 лет) (11).
3.4. Гистопатология лимфомы Ходжкина
При лимфоме Ходжкина обнаруживаются два патологических образования: преобладающие узловые лимфоциты (NLPHL) и классическая лимфома Ходжкина (CHL). Узловатые лимфоциты с преобладанием лимфоцитов, составляющие 5% случаев лимфомы Ходжкина, могут иметь генотип зародышевого центра и, как правило, не являются EBV-положительными. Классическая лимфома Ходжкина имеет генотип пост-зародышевого центра и делится на четыре подтипа: смешанная клеточность (MCHL), узловой склероз (NSHL), истощение лимфоцитов (LDHL) и обогащение лимфоцитами (LRHL).Наиболее распространенными подтипами последовательно являются NSHL и MCHL. И ЛПНП, и ЛРЛП составляют менее 5% всех случаев ХЛ. В большинстве случаев смешанной клеточности и подтипов с истощением лимфоцитов EBV может быть обнаружен почти в 40% клеток Ходжкина Рида-Штернберга (HRS) классической лимфомы Ходжкина (11). Детская лимфома Ходжкина обычно более распространена по мужскому полу и в 30-35% случаев относится к подтипам смешанной клеточности. Вирус Эпштейна-Барра был обнаружен в 15-20% случаев NSHL и никогда не был обнаружен в LRHL; эти два подтипа имеют лучший прогноз.Следовательно, при классическом типе лимфомы Ходжкина ВЭБ-инфекция имеет тесную связь с прогнозом. В HL ДНК EBV-ДНК в крови бесклеточная. Таким образом, внеклеточная ДНК EBV может показывать опухолевую нагрузку и воспаление или разрушение клеток иммунитета. В результате внеклеточная ДНК может быть биомаркером для прогноза или оценки тяжести заболевания (12).
3,5. Лимфома Ходжкина с положительной реакцией на вирус Эпштейна-Барра у пациентов с иммунодефицитом
Заболеваемость ХЛС у ВИЧ-инфицированных в 10 раз выше, чем среди населения в целом, и большинство этих случаев относятся к подтипам ВЭБ-положительной реакции (8).Хотя ретровирусная терапия в сочетании с химиотерапией часто может привести к полной ремиссии, частота оппортунистических инфекций у этих пациентов увеличивается (13).
3,6. Влияние ВЭБ на прогноз лимфомы Ходжкина
Результаты исследований влияния ВЭБ на прогноз лимфомы Ходжкина противоречивы. В исследовании взрослого населения Швеции пациенты с EBV-положительной лимфомой Ходжкина имели больше симптомов и имели более низкую выживаемость, чем пациенты с EBV-отрицательной лимфомой Ходжкина (14).Хотя EBV-положительная лимфома Ходжкина у молодых людей связана с улучшением выживаемости без болезней, это состояние не влияет на общую выживаемость (15). Эти конфликты могут быть связаны с возрастом участников этих исследований. В исследовании Chabay et al. в Южной Америке EBV играл роль в патогенезе подтипа смешанной клеточности, но в их педиатрических исследованиях статус EBV не влиял на прогноз лимфомы Ходжкина (16).
Протокол лечения идентичен как для EBV-положительных, так и для EBV-отрицательных случаев лимфомы Ходжкина и в большинстве случаев приводит к длительной ремиссии, но у пациентов с рецидивирующей EBV-положительной лимфомой Ходжкина прогноз неблагоприятный (17).
3,7. Лимфома Беркитта
Лимфома Беркитта (BL) чаще встречается у мужчин, чем у женщин, и чаще всего диагностируется у детей. Лимфома Беркитта — это агрессивная злокачественная опухоль B-клеточного происхождения, которую можно разделить на три формы с различным географическим распределением, включая спорадический BL, эндемический BL и ВИЧ-ассоциированный BL. Отличительной чертой всех опухолей BL является транслокация между одним из локусов легкой или тяжелой цепи иммуноглобулинов (Ig) и геном MYC. Спорадический БЛ редко ассоциируется с ВЭБ.Эндемический БЛ более чем в 95% всех случаев связан с ВЭБ и более распространен в гиперэндемичных по малярии районах, таких как Африка и другие части мира (18). Лимфома Беркитта имеет один из самых высоких показателей пролиферации клеток среди различных новообразований (время удвоения опухоли составляет от 24 до 48 часов) (19). Спорадическая BL часто поражает брюшную полость, но проявления эндемической BL обычно возникают в челюстях и почках, хотя их можно увидеть в брюшной полости, яичниках, лицевых костях и других экстранодальных участках (18).Более того, у носителей ВИЧ заболеваемость БЛ в 10–100 раз выше, чем у нормальной популяции (20). Основным гистопатологическим признаком этого новообразования является масса мелких нерасщепленных злокачественных В-клеток, которые сливаются с неопухолевыми макрофагами, которые могут создавать небо со звездным видом (18).
Антиген Ki67 положительный почти в 100% клеток. Другой характеристикой BL является перестройка гена иммуноглобулина. Кроме того, транскрипты EBV-кодируемых малых РНК (EBER) -позитивных клеток обнаруживаются методом гибридизации in-situ в случаях, связанных с EBV.Лечение БЛ сопряжено с риском синдрома лизиса опухоли из-за большого времени удвоения опухолевых клеток. Однако использование уратоксидазы (расбуриказы) может уменьшить эти осложнения. Спорадический исход БЛ, особенно в странах с высоким уровнем доходов, намного лучше, чем у других типов БЛ (21). Сегодня методы визуализации играют роль в прогностической и терапевтической оценке лимфомы Беркитта, а ПЭТ-КТ может продемонстрировать гиперметаболическую активность в анатомических местах опухоли (22).
3.8. Диффузная В-крупноклеточная лимфома
Этот тип лимфомы редко проявляется у детей младше 4 лет, и его частота может увеличиваться с детства до второго десятилетия жизни (23).Диффузная крупноклеточная B-клеточная лимфома является вариантом неходжкинских лимфом высокой степени злокачественности и имеет два подтипа: активированная B-клеточная (ABC) диффузная крупноклеточная B-лимфома (DLBCL) и DLBCL, подобная B-клеточному центру зародыша. Примерно 10% случаев DLBCL являются EBV-положительными. EBV-положительные случаи DLBCL имеют более высокий уровень экстранодального поражения, более резистентное заболевание и более агрессивное клиническое течение (8). В DLBCL опухолевые клетки часто экспрессируют маркеры пан-В-клеток (CD 20, CD 79-a), и большинство этих клеток являются CD30-положительными, но не имеют экспрессии CD15 (9).Этот тип неходжкинской лимфомы часто может поражать экстранодальные участки, включая кожу, миндалины, желудок и легкие. Неблагоприятные прогностические факторы включают высокий международный прогностический индекс, фенотип активированных В-клеток и пожилой возраст (24). Относительно редкая подгруппа EBV-положительных DLBCL проявляется при наличии хронического воспаления. Этот тип злокачественных новообразований встречается в полостях тела, особенно при лимфоме, связанной с пиотораксом (PAL). Хронический плеврит или хронический пиоторакс в анамнезе связан с PAL (25).Другие EBV-положительные DLBCL, связанные с хроническим воспалением, встречаются у пациентов с металлическими имплантатами костей и суставов, хроническими язвами ног и хроническим остеомиелитом (26). Другая подгруппа DLBCL встречается у ВИЧ-инфицированных пациентов. Недавние исследования показали, что в целом от 30% до 35% этих опухолей являются EBV-положительными (8)
3.9. Посттрансплантационное лимфопролиферативное заболевание
Реципиенты моложе 18 лет при трансплантации органов имеют в два-четыре раза более высокий риск развития посттрансплантационного лимфопролиферативного расстройства (ЛТПН), чем взрослые пациенты после трансплантации (27).Среди реципиентов солидных органов риск ВЭБ-положительного В-лимфопролиферативного расстройства (B-LPD) увеличивается из-за длительной иммуносупрессии. В первый год после трансплантации LPD имеет острое течение, и пациенты могут иметь повышенный риск посттрансплантационной лимфомы, особенно DLBCL, в течение жизни, который пропорционален степени подавления иммунитета (28). Большинство посттрансплантационных лимфом являются агрессивными и ВЭБ-положительными.
Заболеваемость PTLD колеблется от 0.От 5% до 30% и сильно варьируется в зависимости от пересаженного органа, статуса ВЭБ у донора и реципиента трансплантата, а также режима приема лекарств для подавления иммунитета. Эти расстройства часто представляют собой В-клеточные новообразования. Кроме того, сопутствующая цитомегаловирусная инфекция, получение обедненного Т-лимфоцитами костного мозга и интенсивность иммуносупрессии играют решающую роль в патогенезе PTLD. Это заболевание обычно возникает при комбинированной трансплантации печени и почек с последующей последовательной трансплантацией сердца, легких и почек.Посттрансплантационные лимфопролиферативные расстройства, которые проявляются у реципиентов трансплантата костного мозга, обычно имеют донорское происхождение, но при трансплантации твердых органов они обычно возникают у реципиентов. Вирусная нагрузка выше при использовании цельной крови по сравнению с сывороткой при оценке ПЦР, хотя биопсия должна быть сделана для подтверждения присутствия вируса (29). Главный компонент лечения PTLD — снижение иммуносупрессии. Другие методы лечения включают противовирусные препараты, интерфероны, моноклональные антитела, клеточную терапию и химиотерапию (30).Вирус Эпштейна-Барра приблизительно на 100% связан с PTLD, ассоциированным с лимфомой Ходжкина. ВЭБ-отрицательные PTLD составляют примерно 20% всех случаев и часто возникают на поздней стадии (31).
3.10. Опухоль гладкой мышцы
Гладкомышечная опухоль (SMT) — это необычная опухоль, которая может возникать у людей с иммунодефицитом. Это может также произойти у пациентов с инфекцией вируса иммунодефицита человека и в условиях после трансплантации; он также может быть врожденным. Он встречается у 60% пациентов после трансплантации и является второй по распространенности опухолью у пациентов со СПИДом.Связь между EBV-инфекцией и иммунодефицитом была впервые описана в 1970 году, а ее четкая связь была подтверждена в 1995 году (32). Кроме того, SMT может возникать при состояниях первичного иммунодефицита, таких как мутация ATM, ADA, IL2RG, ZAP70, CARMIL2 и дефицит GATA2. Пациенты с EBV-положительной SMT должны быть обследованы на иммунодефицит. Патогенез этой опухоли недостаточно изучен (33).
Известно, что гибридизация EBV-РНК in-situ может отличить EBV-ассоциированный SMT от лейомиом глубоких мягких тканей.Эта идентификация важна для правильного распознавания этой категории SMT, поскольку они могут демонстрировать непредсказуемое поведение (34).
При инфекциях человека обнаруживаются два разных типа ВЭБ. Тип 2 отвечает за трансформацию у пациентов с ослабленным иммунитетом (35). Обычно паттерн латентного типа 3 выражен, и клетки положительны по EBNA 2, 3 и LMP1 (36). Серологический анализ вируса Эпштейна-Барра у большинства этих пациентов положительный, но он не имеет прямого отношения к бремени болезни или рецидива (37).Более того, EBV передается на слизистую оболочку через слюну через рецепторы CD21 на В-клетках. Следовательно, клетки SMT могут экспрессировать CD21 на своей поверхности (38), за исключением клеток посттрансплантационного подтипа (PT-SMT). В некоторых опухолях EBV-SMT происходит сверхэкспрессия myc, что приводит к клеточной гиперплазии (39). Пролиферации SMT-клеток способствует активация пути mTOR и запускается LMP2, мембранным белком латентного периода EBV (40). Мультифокальные клоны SMT-анализа показывают, что внедрение EBV и их возникновение у отдельного пациента вызвано скорее независимыми первичными поражениями, чем метастазами (41).
Клиническими признаками посттрансплантационной SMT (PT-SMT), врожденного иммунодефицита SMT (CI-SMT) и HIV-SMT являются боль и дисфункция органа в зависимости от локализации и размера опухоли. Их размеры могут быть от 5 до 21 см в диаметре. Этот тип опухоли имеет тенденцию возникать либо в одном месте, либо в нескольких местах (42). При ВИЧ-SMT наиболее часто регистрируемые случаи встречаются в ЦНС, желудочно-кишечном тракте, коже, гортани, глотке, печени и надпочечниках (43), но в случаях PT-SMT наиболее частым участком поражения является печень, хотя легкие, гортань. могут быть поражены глотка, кишечник, селезенка, почки, мозг и, в редких случаях, надпочечники и радужная оболочка (44).Наиболее вероятный дифференциальный диагноз этой опухоли — неходжкинская лимфома на фоне иммунодефицита, такого как PTLD (45).
3.11. Рак носоглотки
Связь между карциномой носоглотки (NPC) и EBV была установлена ранее в 1973 году. Всемирная организация здравоохранения (ВОЗ) классифицировала карциному носоглотки на два основных гистологических типа: ороговевающая плоскоклеточная карцинома (тип I) и некератинизирующаяся плоскоклеточная карцинома. карцинома (типы II и III), по внешнему виду опухолевых клеток под световым микроскопом.Некератинизирующий тип далее подразделяется на дифференцированную некератинизирующую карциному (тип II) и недифференцированную карциному (тип III), которые преимущественно являются EBV-положительными (46). Подобные признаки описаны в тимусе, миндалинах, желудке, легких и коже, названных недифференцированной карциномой носоглоточного типа или лимфоэпителиомоподобной карциномой, которая может быть EBV-положительной в желудке (47). Ни одна опухоль человека не ассоциируется с EBV как неороговевающая карцинома носоглотки.Хотя EBV может сохраняться как латентная инфекция в B-клетках памяти, присутствие этого вируса в ткани носоглотки как латентного вируса не постулируется; таким образом, литическая экспрессия играет важную роль в его онкогенезе. Вирус Эпштейна-Барра не обнаруживается в нормальных эпителиальных клетках, даже в тканях, прилегающих к EBV-положительным NPC (48). Более того, постулируется, что карциномы in situ являются вероятными предшественниками повреждений NPC. Кроме того, LMP1 (латентный мембранный белок EBV) экспрессируется во всех первичных тканях NPC.Этот белок индуцирует специфический эффект на злокачественные фенотипы, включая клеточный цикл (Cyclin D1, Op18, EGFR, p53, STAT3), перепрограммирование метаболизма (гексокиназа 2), ангиогенез (фактор роста эндотелия сосудов), эпителиально-мезенхимальную передачу (EMT), метастазирование. и инвазия (хемокиновый рецептор 4 с мотивом CXC) и апоптоз (49). Другими скрытыми генами являются EBNA1, EBNA2, LMP2, BART2 и miR-BART (50). Метилировано более 60% генов-супрессоров опухолей. Это гиперметилирование может происходить за счет активации ДНК-метилтрансферазы1 в клетках и митохондриях под действием LMP1.Этот эпигенетический механизм играет важную роль на ранней стадии NPC (51). Литическая фаза EBV-инфекции, в отличие от латентной фазы в других опухолях, отвечает за свойство онкогенеза. У пациентов с NPC экспрессируются высокие уровни белков литической фазы BALF1 / BCRF1 / BHRF1, а вирусная нагрузка ДНК и антитела к вирусному капсиду (VCA) увеличиваются (52). Рак носоглотки располагается в боковой или задней стенке носоглотки вокруг ямки Розенмюллера. Этот рак может протекать бессимптомно с некоторыми первичными симптомами в течение длительного времени, что затрудняет его раннюю диагностику.Он имеет тенденцию распространяться в окологлоточное пространство. Метастазы в лимфатические узлы возникают в 70–90% случаев и в 50% случаев односторонние (53). Возрастной диапазон составляет от 10 до 59 лет, и в детстве это не распространено. Наиболее характерными симптомами являются безболезненное образование шеи у 60%, заложенность носа у 50%, головная боль у 54%, потеря слуха у 32%, носовое кровотечение у 10%, тризм у 4%, потеря зрения и диплопия / косоглазие у 2%. (54).
3.12. Синдром гемофагоцитарного лимфогистиоцитоза
Это клинико-патологический синдром с нарушением регуляции иммунной системы и гиперцитокинемией, клинически характеризующийся спленомегалией, лихорадкой, цитопенией, гепатомегалией, коагулопатией и нарушениями центральной нервной системы, которые могут сопровождаться умеренным плеоцитозом и гиперпротеинемией спинномозговой жидкости.В 2004 году Общество гистиоцитов представило пять диагностических критериев HLH, включая (1) лихорадку, (2) цитопении, поражающие по крайней мере две из трех ветвей периферической крови, (3) спленомегалию, (4) гемофагоцитоз в костном мозге, селезенке, или лимфатические узлы, и (5) гипертриглицеридемия и / или гипофибриногенемия. Более того, были описаны три дополнительных критерия, включая (6) гиперферритинемию, (7) низкую или отсутствующую активность NK-клеток и (8) высокие уровни растворимого рецептора интерлейкина 2. Для выполнения условия должны присутствовать пять из восьми критериев, но пациенты с молекулярным диагнозом, совместимым с HLH, не обязательно должны соответствовать диагностическим критериям (55).Без лечения смерть может наступить из-за полиорганной недостаточности (56). Вирус Эпштейна-Барра по неизвестным причинам тесно связан с HLH в Азии (57). Первичный HLH может возникать у пациентов с генетическими причинами HLH или положительным семейным анамнезом (58). Дифференцировать первичную EBV-инфекцию и HLH очень сложно (59). Подтверждающим диагностическим тестом для идентификации EBV-HLH является определение геномной ДНК EBV в сыворотке, лимфатическом узле и костном мозге с помощью ПЦР и гибридизации in situ (60).
Мазки костного мозга на EBV-HLH показывают фагоцитоз гематологических элементов, таких как эритроциты и тромбоциты, а положительное окрашивание костного мозга на EBV-кодируемую РНК (EBER) выявляет лимфоциты, широко инфицированные EBV (61).
3,13. Лечение EBV-ассоциированных новообразований
Новообразования, ассоциированные с вирусом Эпштейна-Барра, часто плохо поддаются интенсивным протоколам химиотерапии; следовательно, при этих злокачественных новообразованиях необходимо использовать режимы, направленные на вирусные мишени (62).Эти методы лечения включают подходы иммунотерапии, интерфероны и нацеленные на небольшие молекулы аспекты биологии вируса (63).
3,14. Противовирусные препараты
Многие противовирусные препараты обладают некоторой анти-EBV активностью. Ганцикловир и ацикловир не являются препаратами выбора при лимфоидных заболеваниях, связанных с ВЭБ. Эти два препарата обладают активностью против литического ВЭБ. В литической форме EBV ацикловир и ганцикловир превращаются геном вирусной тимидинкиназы в свои активные и токсичные формы.Включение этих токсичных метаболитов в ДНК приводит к преждевременному апоптозу. Одним из способов решения этой проблемы является совместное введение этих противовирусных агентов с 5-азацитидином в качестве деметилирующего соединения, которое индуцирует ген литического цикла (64). Feng et al. показали, что у мышей с тяжелым комбинированным иммунодефицитом (SCID) добавление доксорубицина или гемцитабина к ганцикловиру оказывало более ингибирующее действие на лимфопролиферативное заболевание, вызванное EBV, чем одна химиотерапия (65).
Фоскарнет — еще один противовирусный препарат, механизм действия которого не зависит от присутствия вирусной тимидинкиназы и нацелен на вирусную ДНК-полимеразу. Oertel и Riess показали полную ремиссию с фоскарнетом у пациентов с лимфопролиферативными заболеваниями, связанными с ВЭБ (66). Цидофовир является мощным ингибитором репликации EBV in vitro, и его действие направлено против ДНК-полимеразы EBV.
Ксенотрансплантаты носоглотки в значительной степени подвержены противоопухолевому воздействию этого препарата (67).Совместное введение цидофовира и ритуксимаба (моноклональное антитело к CD20) может привести к полной ремиссии при посттрансплантационных лимфопролиферативных нарушениях, экспрессирующих CD20 (68). Зидовудин — антиретровирусное средство для лечения ВИЧ. Введение зидовудина с интерфероном могло вызвать апоптоз in vitro в EBV-положительных лимфомных клетках пациента со СПИДом (69). Другой фармакологический агент — гидроксимочевина, влияющая на уничтожение внехромосомных элементов ДНК. Механизм действия этого препарата заключается в устранении EBV-эписом в EBV-положительных клеточных линиях лимфомы Беркитта (63).
3,15. Иммунотерапия
Одним из методов иммунотерапии при лечении EBV-положительной неходжкинской лимфомы является адоптивный перенос EBV-специфических цитотоксических Т-лимфоцитов (CTL) (69). CTL могут быть введены непосредственно от донора пациенту или могут быть введены после размножения in vitro для восстановления компетентности иммунной системы. Генерация ВЭБ-специфичных CTL от серопозитивных здоровых доноров может занять от 8 до 12 недель. Этот метод может устранить лимфопролиферативные нарушения после трансплантации аллогенных гемопоэтических стволовых клеток.У пациентов с ВЭБ-положительными лимфопролиферативными заболеваниями, которые являются реципиентами трансплантации солидных органов, Т-клетки от донора не приносят особой пользы, поскольку опухоль всегда возникает в В-клетках реципиента (70). Для новообразований, не связанных с ВЭБ, опыт использования ЦТЛ, специфичных для ВЭБ, ограничен (30). Лукас и др. продемонстрировали роль аллогенных EBV-специфических CTL в лечении рецидивирующей, резистентной EBV-положительной болезни Ходжкина (71). Наиболее важные осложнения адоптивной иммунной терапии включают резистентность опухоли и болезнь «трансплантат против хозяина» (GVHD).Этиологически резистентность опухоли, вероятно, связана с мутациями эпитопа EBV, которые распознаются CTL или другими способами, такими как продукция цитокинов, включая интерлейкин 10 (IL-10) (72). В настоящее время ведутся исследования по производству вакцин против ВЭБ, направленных на защиту от первоначальной инфекции или повышение иммунитета при опухолях, связанных с инфекцией ВЭБ. Необходимо разработать клинические испытания, чтобы определить, может ли вакцина против ВЭБ снизить частоту посттрансплантационных лимфопролиферативных расстройств (73).
3.16. Моноклональные антитела
Доступность ритуксимаба открывает возможности для лечения В-клеточного ДПД, ассоциированного с EBV. Частота ответа на ритуксимаб колеблется от 70% до 100% (63). Кроме того, при посттрансплантационной лимфоме IL-6 действует как фактор роста; таким образом, пробуются моноклональные антитела против ИЛ-6 (72). У пациентов с лимфомами высокого риска или клинически агрессивными лимфомами необходима дополнительная терапия. Было показано, что сочетание ритуксимаба и химиотерапии, состоящей из циклофосфамида, доксорубицина, винкристина и преднизолона (CHOP), увеличивает выживаемость (74).
| Определение (MEDLINEPLUS) | Инфекционный мононуклеоз, или «мононуклеоз», — это инфекция, обычно вызываемая вирусом Эпштейна-Барра. Вирус распространяется через слюну, поэтому его иногда называют «болезнью поцелуев». Моно чаще всего встречается у подростков и молодых людей.Однако получить его можно в любом возрасте. Симптомы моно включают
Иногда может наблюдаться опухоль селезенки. Серьезные проблемы случаются редко. Анализ крови может показать, есть ли у вас моно. Большинство людей поправляются через две-четыре недели.Однако через несколько месяцев вы можете чувствовать усталость. Лечение направлено на облегчение симптомов и включает лекарства от боли и лихорадки, полоскания теплой соленой водой, а также достаточный отдых и жидкости. |
| Определение (MSHCZE) | Infekční onemocnění způsobené herpetickým virem EBV, méně často CMV.Postihuje především mladší jedince a přenáší se přímým kontaktem (вирус, который вылечит до слина и может быть нарушен — «nemoc z líbání»). Inkubační doba je průměrně okolo 2 týdnů, ale i kratší či delší. Нейч. se projevuje horečkou, zduřením mízních uzlin, angínou, někdy bývají lehce postižena i játra, vzácněji další orgány. Proliferace B lymfocyt vede k infiltraci lymfatických orgánů (спленомегалия, лимфаденопатия). (Cit. Velký lékařský slovník online, 2013 http://lekarske.slovniky.cz/) |
| Определение (MSH) | Распространенная острая инфекция, обычно вызываемая вирусом Эпштейна-Барра (HERPESVIRUS 4, HUMAN).Наблюдается увеличение количества мононуклеарных лейкоцитов и других атипичных лимфоцитов, генерализованная лимфаденопатия, спленомегалия и иногда гепатомегалия с гепатитом. |
| Определение (CSP) | острое заболевание, характеризующееся лихорадкой и увеличением лимфатических узлов и аномальным увеличением мононуклеарных лейкоцитов или моноцитов в кровотоке; не очень заразен; некоторые считают, что это может передаваться при поцелуях. |
| Концепции | Заболевание или синдром ( T047 ) |
| МСХ | D007244 |
| ICD9 | 075 |
| ICD10 | B27 , B27.0, В27.9 |
| SnomedCT | 186667007, 26851006, 154359004, 186670006, 187460007, 314131007, 271558008, 186668002 |
| Английский | Железистая лихорадка, мононуклеоз, инфекционный, мононуклеоз, лихорадка, железистый, ИНФЕКЦИОННЫЙ мононуклеоз, инфекционный мононуклеоз, неуточненный, инфекционный мононуклеоз, неуточненный, [X] инфекционный мононуклеоз, неуточненный, [X] инфекционный мононуклеоз, инфекционный мононуклеоз, мононуклеоз, инфекционный мононуклеоз, инфекционный мононуклеоз, мононуклеоз, инфекционный мононуклеоз , инфекционный мононуклеоз (диагноз), инфекционный мононуклеоз, инфекционный мононуклеоз, инфекционный мононуклеоз, моноцитарная стенокардия, инфекционный мононуклеоз [заболевание / обнаружение], железистая лихорадка, болезнь Пфайффера, гамма-герпесвирусный мононуклеоз (диагностика, мононуклеоз), мононуклеоз вируса Кисси (диагностика), ), Инфекционный мононуклеоз (и болезнь Пфайффера) (расстройство), болезнь Пфайффера (расстройство), [X] инфекционный мононуклеоз, неуточненный (расстройство), мононуклеоз, болезнь Пфайффера, железистая лихорадка, инфекционный мононуклеоз, гаммагерпесвирусный мононуклеоз лихорадка, ИМ — Инфекционный мононуклеоз, Инфекционный мононуклеоз, ИМ — Инфекционный мононуклеоз, гамма-герпесвирусный мононуклеоз (нарушение), инфекционный мононуклеоз (нарушение), Эпштейна-Барра; инфекционный мононуклеоз, болезнь Филатова; поцелуи, гамма-герпесвирус; инфекционный мононуклеоз, болезнь поцелуев, поцелуи; болезнь, моноцитарная; ангина, мононуклеоз, инфекционный; Эпштейн-Барр, мононуклеоз, инфекционный; гаммагерпесвирусный, мононуклеоз, инфекционный, ангина; моноцитарный, Инфекционный мононуклеоз (заболевание) [Неясно] |
| Голландский | инфекционный мононуклеоз, инфекционный мононуклеоз, клиркоортс, Эпштейна-Барра; инфекционный мононуклеоз, стенокардия; monocytotica, болезнь; поцелуи, гамма-герпесвирус; инфекционный мононуклеоз, поцелуи; болезнь, моноцитоз; стенокардия, инфекционный мононуклеоз; Эпштейн-Барр, инфекционный мононуклеоз; гамма-герпесвирус, мононуклеоз дверной гамма-герпесвирус, инфекционный мононуклеоз, niet gespecificeerd, инфекционная мононуклеоза, инфекционный мононуклеоз, Pfeiffer-klierkoorts, Ziekte van Pfeiffer |
| Французский | Fièvre glandulaire, Mononucléose Infectieuse, Maladie du baiser, MNI (MonoNucléose Infectieuse), |
| немецкий | Druesenfieber, Инфекционный мононуклеоз, Инфекционный мононуклеоз, nicht naeher bezeichnet, Инфекционный мононуклеоз, Мононуклеозный герпес, Гамма-герпесвирен, инфекционный мононуклеоз, Мононуклеоз, инфекционный мононуклеоз, Dr. |
| Испанский | Fiebre glandular, enfermedad de Pfeiffer, enfermedad de Pfeiffer (trastorno), [X] mononucleosis influencciosa, no especificada, [X] mononucleosis infcciosa, no especificada (trastorno), мононуклеоз гаммагерпесвирус, инфекционный моноционуклеоз, инфекционный моноциотический ангионуклеоз ), инфекционный мононуклеоз (трасторно), инфекционный мононуклеоз, мононуклеоз вируса герпеса дель группы гамма (трасторно), мононуклеоз вируса герпеса группы гамма, вирус мононуклеоза порового герпеса группы гамма, мононуклеоз инфекционного вируса гриппа, Grupo grupo, мононуклеоз7 |
| Шведский | Körtelfeber |
| Японский | セ ン ネ ツ, デ ン セ ン セ イ ク シ ョ ウ, 感染 性 単 細胞 症, パ イ フ ェ ル 病, 伝 染 性 単 核 球 症, 伝 染 単, 伝 染 性 単 球 増 加 症, 感染 性 単 核 症, 感染 性 単 球 増 加, 感染 性 単 球 増 加 症, 流行 性腺, 腺 熱 |
| Чешский | инфекционный мононуклеоз, Инфекционный мононуклеоз, Пфайфферова немоц, моноцитарная стенокардия, žlázová horečka |
| финский | Mononukleoosi |
| Русский | АНГИНА МОНОЦИТАРНАЯ, ЖЕЛЕЗИСТАЯ ЛИХОРАДКА, БОЛЕЗНЬ ФИЛАТОВА, БОЛЕЗНЬ ПФАЙФФЕРА, МОНОНУКЛЕОЗ ИНФЕКЦИОННЫЙ, АНГИНА МОНОЦИТАРНАЯ, БОЛЕЗНЬ ПФЕЙФУРАКА, МОНОЦИТАРНАЯ, БОЛЕЗНЬ ПФЕЙФУРАКА, ФИЛЕЗНОВАЯ ПЕРЕДАВАЮЩАЯСЯ 90, ФИЛЕЗНЬ ПФЕЙФУРАКА, БОЛЕЗНЬ ПФЕЙФУРА, БОЛЕЗНЬЮ ПФАЙФЕРА, ФИЛЕЗНОВАЯ ИНФОРМАЦИЯ. |
| корейский | 감마 헤르페스 바이러스 성 단핵구증, 상세 불명 의 감염성 단핵구증, 감염성 단핵구증 |
| Итальянский | Febbre ghiandolare, Febbre ghiandolare di Pfeiffer, Mononucleosi infettiva |
| Хорватский | ИНФЕКЦИОЗНА МОНОНУКЛЕОЗА |
| Польский | Mononukleoza zakaźna |
| Венгерский | инфекционный мононуклеоз, мононуклеоз, фертезо, мононуклеоз, фертезо, Pfeifer-féle mirigyláz |
| Норвежский | Mononukleose, Kyssesyke, Kjertelfeber |
| Португальский | Мононуклеозная инфекция, Febre Glandular, Мононуклеозная инфекция |
Вирус Эпштейна-Барра во время беременности | Американская ассоциация беременности
Вирус Эпштейна-Барра (EBV) или вирус герпеса человека 4 является частью семейства вирусов герпеса человека и является наиболее распространенным вирусом человека.У большинства людей будут доказательства (антитела к ВЭБ в крови) предшествующей инфекции ВЭБ к 35 годам. После заражения ВЭБ вы носите вирус на всю оставшуюся жизнь, хотя обычно в спящем состоянии. После первоначального заражения ВЭБ вирус может перейти в спящий режим и оставаться латентным в течение многих лет, пока что-то не вызовет его повторное появление. Иногда это приводит к появлению моно во время беременности.
Могут ли дети заразиться ВЭБ?
У здоровых младенцев и взрослых часто нет явной инфекции с момента первого введения EBV.Подростки и молодые люди, а также пациенты с ослабленной иммунной системой (люди со СПИДом и другими иммунными заболеваниями) могут видеть более серьезные симптомы и у них может развиться инфекционный мононуклеоз («мононуклеоз»).
Хотя EBV — не единственный вирус, который может вызывать инфекционный мононуклеоз, это наиболее частая причина. У подростков и молодых людей каждая четвертая инфекция EBV приводит к инфекции мононуклеоза.
EBV также может вызывать множество других заболеваний и состояний, включая, помимо прочего:
- Вирусный менингит
- Энцефалит
- Поперечный миелит
- Неврит зрительного нерва
- Паралич лицевых мышц или одной стороны тела
- Острая мозжечковая атаксия
- Синдром Гийена-Барре
- Панкреатит
- Миокардит
- Пневмония
- Болезнь легких
- Лимфоцитоз
- Ослабленная иммунная система
Чтобы узнать больше об этих других возможных заболеваниях, посетите веб-сайт CDC здесь.Если вас беспокоят какие-либо симптомы, немедленно позвоните своему врачу.
Как распространяется?
Вирус распространяется в основном через слюну, но может распространяться через все жидкости организма. «Мононуклеоз», или инфекционный мононуклеоз, — это распространенная инфекция, которая может возникнуть в результате ВЭБ, и среди подростков ее часто называют «болезнью поцелуев» из-за того, что она легко передается через слюну.
Каковы симптомы ВЭБ-инфекции?
Симптомы EBV-инфекции могут включать:
- Лихорадка
- Боль в горле
- Истощение
- Сыпь на коже
- Увеличение лимфатических узлов шеи
- Увеличение печени и селезенки
Эти симптомы должны длиться столько же, сколько и любое другое распространенное заболевание, обычно не дольше 1-2 недель.Иногда усталость может длиться дольше.
Помните, что многие дети и здоровые взрослые не испытывают никаких симптомов, или симптомы могут показаться обычным детским заболеванием или простудой. Наиболее подвержены этим симптомам люди с ослабленной или плохо функционирующей иммунной системой (люди с ВИЧ / СПИДом, некоторые беременные женщины, подростки и, возможно, даже в большей степени люди с подростковой беременностью).
Каковы симптомы инфекционного мононуклеоза?
Симптомы инфекционного мононуклеоза сходны с симптомами ВЭБ, но более серьезны.Они могут включать:
- Лихорадка
- Крайнее истощение
- Боль в горле
- Кожная сыпь
- Головные боли
- Боли в теле
- Увеличение лимфатических узлов шеи и подмышек
- Опухание печени и / или селезенки
Вы можете избавиться от этих симптомов через 1-2 недели, но иногда может потребоваться больше времени, чтобы вернуться к нормальному уровню энергии (от нескольких недель до 6 месяцев). Если ваши симптомы сохраняются через шесть или более месяцев после постановки диагноза, вам может быть поставлен диагноз — редкая хроническая активная инфекция ВЭБ.Вам следует обратиться к врачу, если ваши симптомы не исчезнут через две недели, особенно через шесть месяцев.
Имейте в виду, что, хотя ВЭБ является наиболее частой причиной инфекционного мононуклеоза, это не единственная возможная причина. Другие причинные факторы включают цитомегаловирус (ЦМВ), токсоплазмоз, гепатит A / B / C, ВИЧ, краснуху (корь) или аденовирус.
Как диагностируется ВЭБ?
Поскольку симптомы ВЭБ аналогичны симптомам многих других легких заболеваний, лучший способ определить инфекцию ВЭБ — это анализ крови на антитела, специфичные к ВЭБ.Если эти антитела присутствуют, это указывает на присутствие EBV.
У меня инфекционный мононуклеоз; как я узнаю, что это от ВЭБ?
Инфекционный мононуклеоз обычно диагностируется только на основании симптомов; однако иногда необходимо определить причину. В этом случае тестирование со следующими результатами может указывать на инфекцию ВЭБ:
- Аномальные лейкоциты
- Количество лейкоцитов выше нормы
- Меньше нейтрофилов
- Меньше тромбоцитов
- Белки / ферменты, указывающие на атипичную функцию печени
Как лечить ВЭБ-инфекцию?
Поскольку это вирус, вариантов лечения, кроме уменьшения симптомов, не так много.Болеутоляющие и жаропонижающие средства, такие как ибупрофен или ацетаминофен, могут уменьшить любые боли в теле и снизить температуру. Отдых и надлежащая гидратация (вода, напитки с электролитами) — полезные методы борьбы с симптомами.
Беременным женщинам можно принимать ацетаминофен для снижения температуры и лечения болей в теле — избегайте ибупрофена.
Если я заболею инфекционным мононуклеозом от ВЭБ, есть ли другое лечение?
Ответ зависит от тяжести вашего заболевания. Ваш врач должен будет наблюдать за инфекционным мононуклеозом и принимать указанные выше меры для уменьшения симптомов, а также длительный период отдыха.Если инфекция отрицательно влияет на ваши органы (в частности, на селезенку и / или печень), ваш врач может принять меры для их лечения. Поскольку инфекционный мононуклеоз может вызвать увеличение селезенки, не занимайтесь контактными видами спорта, чтобы избежать разрыва селезенки.
Как я могу избежать заражения или передачи ВЭБ и / или инфекционного мононуклеоза?
Поскольку вирус может передаваться через слюну и другие жидкости организма, избегайте поцелуев и совместного использования напитков, еды, зубных щеток; также избегайте анального, вагинального или орального полового акта с кем-то, кто, как вы знаете, болен ВЭБ, или если у вас ВЭБ.
ВЭБ и инфекционный мононуклеоз во время беременности
Будет ли лечение одинаковым, если я беременна и болею ВЭБ или инфекционным мононуклеозом?
Обычно да, лечение будет таким же. Вместо ибупрофена следует использовать ацетаминофен, чтобы уменьшить лихорадку и головные боли / боли в теле. Отдых и гидратация имеют решающее значение, особенно во время беременности, поскольку развитие плода зависит от наличия гидратированной и хорошо отдохнувшей матери.
Наибольшую озабоченность вызывает (1) сведение к минимуму инфекций или повреждений органов и (2) обеспечение того, чтобы температура матери не поднималась слишком высоко и не оставалась высокой слишком долго.Это связано с тем, что развивающийся ребенок более чувствителен к температуре, чем тело матери. Высокая температура может вызвать выкидыш (первая половина беременности), врожденные дефекты (первый триместр) и / или преждевременные роды (если лихорадка связана с инфекцией органа).
Могут ли дети получить моно?
Исследования, проводившиеся с 1980-х годов, дали разные ответы на этот вопрос. Некоторые исследования показывают, что нет корреляции между реактивацией ВЭБ во время беременности и врожденной инвалидностью или ранними родами / низкой массой тела при рождении.Совсем недавно одно исследование продемонстрировало связь между значительной реактивацией ВЭБ и ранними родами и низкой массой тела при рождении. Другой обнаружил связь между депрессивными симптомами у матери примерно на 32 неделе и поздней активацией ВЭБ перед родами.
Необходимы дополнительные исследования активации ВЭБ и ее влияния на беременность и плод. Почти все исследования согласны с тем, что реактивация ВЭБ не связана со смертью плода. Если исключить из уравнения высокую температуру, возможно, что активация ВЭБ или инфицирование во время беременности могут быть связаны с ранними родами и низкой массой тела при рождении.
Передается ли вирус моему ребенку?
В некоторых исследованиях сообщалось об инфицировании ВЭБ новорожденного, рожденного от матери с ВЭБ, хотя процент был небольшим. Нет четких указаний на то, передается ли вирус внутриутробно или во время родов. Поговорите со своим врачом о любых вмешательствах, которые, по его мнению, необходимы для предотвращения передачи.
Хорошая новость заключается в том, что даже если ВЭБ передается от вас вашему ребенку, ВЭБ в младенчестве и детстве обычно протекает бессимптомно, и лишь у немногих детей наблюдаются эпизоды инфекции.Кроме того, у большинства людей ВЭБ будет к 35 годам, поэтому велика вероятность, что ваш ребенок когда-нибудь заразится ВЭБ.
Безопасно ли кормить моего ребенка грудью, если у меня ВЭБ, а у него нет?
Данные показывают, что ВЭБ может присутствовать в грудном молоке, но пока нет исследований, которые определяли бы, приводит ли это к передаче младенцу.
Лучше всего поговорить с врачом о своем статусе ВЭБ и о том, как он влияет на вашу беременность и ребенка после родов.
Хотите узнать больше?
Составлено с использованием информации из следующих источников:
1. CDC: О ВЭБ: https://www.cdc.gov/epstein-barr/about-ebv.html
2. CDC: О мононуклеозах: https://www.cdc.gov/epstein-barr/about-mono.html
3. CDC: для поставщиков медицинских услуг: https://www.cdc.gov/epstein-barr/hcp.html
4. Клиника Мэйо: мононуклеоз и Эпштейн-Барр: Какая связь?
https://www.mayoclinic.org/diseases-conditions/mononucleosis/expert-answers/mononucleosis/faq-20058444
5.Клиника Мэйо: мононуклеоз: диагностика и лечение.
https://www.mayoclinic.org/diseases-conditions/mononucleosis/diagnosis-treatment/treatment/txc-20165946
6. Клиника Мэйо: мононуклеоз: может ли он рецидивировать?
https://www.mayoclinic.org/diseases-conditions/mononucleosis/expert-answers/mononucleosis/faq-20058564
7. Персистирующая инфекция вируса Эпштейна-Барра и беременность. J Infect Dis. Июнь 1983 г.
https://www.ncbi.nlm.nih.gov/pubmed/6304207
8.Инфекция вируса Эпштейна-Барра во время беременности — проспективное контролируемое исследование. Reprod Toxicol. 25 августа 2008 г. 10.1016 / j.reprotox.2008.04.004
https://www.ncbi.nlm.nih.gov/pubmed/18534816?
9. Инфекционный мононуклеоз во время беременности: отчет о трех женщинах и их младенцах, изученных проспективно. Pediatr Infect Dis. Июль 1984 г.
https://www.ncbi.nlm.nih.gov/pubmed/6473132
10. Инфекции вируса Эпштейна-Барра во время беременности: проспективное исследование. J Pediatr.Март 1984 г.
https://www.ncbi.nlm.nih.gov/pubmed/6323662
11. Инфекция вируса Эпштейна-Барра во время беременности и риск неблагоприятного исхода беременности. BJOG. 22 сентября 2005 г. doi: 10.1111 / j.1471-0528.2005.00764.x
https://onlinelibrary.wiley.com/doi/10.1111/j.1471-0528.2005.00764.x/full
12. Депрессивные симптомы матери, связанные с реактивацией вируса Эпштейна-Барра на поздних сроках беременности. Научные отчеты. 31 октября 2013 г. doi: 10.1038 / srep03096
https: // www.nature.com/articles/srep03096
13. Рекомендации по грудному вскармливанию при материнских инфекциях. J. Pediatr. (Рио Дж.), Ноябрь 2004 г. https://dx.doi.org/10.1590/S0021-75572004000700010
https://www.scielo.br/scielo.php?pid=s0021-75572004000700010&script=sci_arttext&tlng=en
14. Изучение передачи вируса Эпштейна-Барра от матери ребенку с помощью вложенных ПЦР. J Virol. Октябрь 1996 г.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1/
15.Инфекция вируса Эпштейна-Барра (EBV) в младенчестве. J Clin Virol. Апрель 2001.
https://www.ncbi.nlm.nih.gov/pubmed/11255098
16. Livestrong: Влияние высокой температуры на беременность.
https://www.livestrong.com/article/243511-effects-of-high-temperature-on-pregnancy/
Mono: симптомы, диагностика и варианты лечения
Инфекционный мононуклеоз, в просторечии называемый «мононуклеозом», представляет собой доброкачественную инфекцию, характеризующуюся лихорадкой, увеличением лимфатических узлов и утомляемостью, которая может продолжаться в течение недель или месяцев.Моно также называют железистой лихорадкой и, в просторечии, «болезнью поцелуев».
Причины
По данным Центров по контролю и профилактике заболеваний (CDC), наиболее частой причиной моно является вирус Эпштейна-Барра (EBV), который встречается во всем мире и поражает большую часть населения какой-то момент в их жизни. По данным Американской академии семейных врачей, моно чаще всего встречается у людей в возрасте от 15 до 35 лет. По данным CDC, около 25 процентов подростков и молодых людей, инфицированных EBV, разовьются инфекционным мононуклеозом.
Инфекционный мононуклеоз также может быть вызван другими вирусами, по словам доктора Сола Р. Хаймса, доцента клинической педиатрии детской больницы Стоуни-Брук. «Это клиническое заболевание на самом деле может быть вызвано несколькими вирусами — вирусом Эпштейна-Барра, цитомегаловирусом (ЦМВ) — а также некоторыми, которые мы еще не можем диагностировать», — сказал он. «Часто мы говорим, что у кого-то есть« моноподобное заболевание », когда мы не можем найти причину, но клиническая картина соответствует моно. Независимо от причины, у всех этих пациентов наблюдается аналогичное медленное, но в конечном итоге улучшение возвращается к норме.«
Моно известен как« болезнь поцелуев », потому что, по данным Национального института здоровья (NIH), он в основном передается через слюну. Он также может передаваться через общую посуду и капли аэрозоля при кашле и чихании». Обмен ими телесный. жидкости, в том числе слюна, во время поцелуев — распространенный способ передачи ВЭБ-инфекции в развитых регионах мира, особенно среди подростков », — сказал доктор Амар Сафдар, доцент медицины Медицинского центра Лангоне при Нью-Йоркском университете, сказал Live Science.
«Хорошая новость заключается в том, что моно не так заразно, как простуда», — сказал Live Science доктор Сэмпсон Дэвис, врач из Медицинского центра Сент-Майклс в Ньюарке, Нью-Джерси.
Симптомы
Согласно данным CDC, тремя классическими симптомами инфекционного мононуклеоза являются лихорадка, боль в горле и увеличение лимфатических узлов. Хотя он может в дальнейшем перерасти в опухоль селезенки, гепатит, желтуху и, в редких случаях, воспаление сердца (миокардит), инфекционный мононуклеоз почти никогда не заканчивается смертельным исходом.«Симптомы более выражены у подростков и подростков. Взрослые часто обладают иммунитетом к вирусу, и поэтому симптомы не такие агрессивные», — сказал Дэвис.
Утомляемость — частая жалоба среди пациентов с мононуклеозом. Британское исследование 2006 года изучило медицинские записи 1438 пациентов и показало, что у них в четыре раза больше шансов почувствовать усталость после инфекционного мононуклеоза, и это чувство обычно длится около восьми недель для большинства пациентов.
Диагностика и тесты
Согласно NIH, история болезни пациента, в дополнение к подсчету лейкоцитов или тестов на антитела, должна подтверждать диагноз.Может быть проведен экспресс-тест на фарингит, поскольку стрептококковая инфекция иногда сопровождает боль в горле при инфекционном мононуклеозе.
Хотя врачи могут попытаться ощупать признаки увеличенной селезенки во время медицинских осмотров, эта практика дает точность только от 27 до 58 процентов при обнаружении действительно увеличенной селезенки, согласно статье 2004 года в журнале American Family Physician. Следовательно, невозможность почувствовать увеличенную селезенку не должна использоваться для исключения вероятности инфекционного мононуклеоза.
Осложнения
Хотя спонтанный разрыв селезенки является редким осложнением и, по оценкам, встречается в 0,1–0,5% случаев мононуклеоза, согласно статье 2007 года в журнале Pediatrics, он все еще вызывает серьезную озабоченность. Согласно статье 2008 года, написанной для Американского медицинского общества спортивной медицины, селезенка уязвима к разрывам в течение первых трех-четырех недель появления симптомов, независимо от размера селезенки. Поэтому спортсмены должны возобновить только легкую, бесконтактную деятельность после трех недель появления симптомов и отложить занятия контактными видами спорта на срок до семи недель или более, в зависимости от вида спорта.Согласно статье, занятия, связанные с нагрузкой на брюшной пресс, такие как гребля или тяжелая атлетика, заслуживают особого внимания.
Лечение
В настоящее время не существует одобренных правительством противовирусных препаратов для лечения острой ВЭБ-инфекции. «От моно нет лекарства. Это вирусная инфекция», — сказал Дэвис. «Вирус в конечном итоге уходит, но это может занять несколько недель. Mono вызывается вирусом, и поэтому антибиотики бесполезны».
Большинство методов лечения инфекционного мононуклеоза направлено на уменьшение симптомов.Кортикостероиды могут быть полезны при лечении таких осложнений, как сильный отек горла и миндалин. По данным клиники Мэйо, антибиотики могут быть использованы, если у пациента также есть ангина, хотя ампициллин или амоксициллин могут вызвать сыпь.
Дэвис сказал Live Science, что поддерживающая терапия — лучший способ лечения моно. Он дал следующие советы:
- Больше отдыхайте. Сон помогает организму бороться с инфекцией.
- На какое-то время воздержитесь от занятий спортом и физических упражнений, а также других физических нагрузок.Это помогает защитить селезенку. Удар или падение могут привести к разрыву селезенки, что может быть опасно для жизни.
- Предотвратите обезвоживание, выпив много жидкости. Обезвоживание может ухудшить ваше самочувствие.
- Полоскание с соленой водой и леденцы от боли в горле.
- Принимайте ацетаминофен (Тайленол) или ибупрофен (Адвил, Мотрин) от болей, болей и лихорадки. Не принимайте аспирин.
Пациенты с синдромом поствирусной хронической усталости с высоким уровнем антител, особенно против EBV-ассоциированного ядерного антигена, такого как вирусный капсидный антиген EBV (VCA), и других антигенов, таких как ранний антиген EBV, показали пользу от длительной терапии пероральными противовирусными препаратами. такие агенты, как валганцикловир, согласно исследованию, проведенному Медицинским центром Стэнфордского университета.«К этим типам лечения следует подходить с осторожностью, поскольку потенциальная токсичность лекарств и неопределенная польза делают эту рекомендацию далекой от того, чтобы стать стандартом лечения», — сказал Сафдар.
У пациентов с тяжелой иммуносупрессией реактивация ВЭБ и дисфункция органов, включая вирусные заболевания, поражающие головной мозг, печень, сердце и легкие, и в редких случаях почки; системные противовирусные препараты, такие как ганцикловир и цидофовир, были использованы с неоднозначными результатами. Подобная терапия также использовалась для пациентов с подавлением функции костного мозга, связанным с ВЭБ; — снова с противоречивыми результатами, — пояснил Сафдар.
Восстановление
«Люди считают, что хроническая моноинфекция, которая может вызывать проблемы в течение многих лет, — обычное дело. На самом деле это не так, — сказал Хаймс. ВЭБ — вирусное заболевание в той же семье, что и герпес и ветряная оспа (ветряная оспа). Хаймс объяснил, что, как и другие члены семейства вирусов герпеса, вирус может оставаться в вашем теле. Однако вирус находится в спящем состоянии и очень редко повторно активируется, обычно во время стресса. «Хроническая активная инфекция Эпштейна-Барра — это то, что мы на самом деле видим только у людей с иммунными проблемами — пациентов с трансплантатами, пациентов с ВИЧ или людей, рожденных без какой-либо части их иммунной системы или иммунной функции», — сказал Хаймс.Лабораторное тестирование может выявить хроническое присутствие вируса и исключить его, поэтому его легко диагностировать.



