причины, симптомы и лечение в статье уролога Закуцкий А. Н.
Дата публикации 11 октября 2018Обновлено 22 сентября 2020
Определение болезни. Причины заболевания
Острый пиелонефрит — это воспалительное заболевание почек бактериальной причины с преимущественным поражением лоханки, чашечек и межуточной ткани паренхимы почек. В Международной классификации болезней отказались от термина «острый пиелонефрит», заменив его на «острый интерстициальный нефрит».[3]
Пиелонефрит следует отличать от гломерулонефрита. Обе формы нефрита характеризуются воспалением паренхимы почек, но при пиелонефрите поражается межуточная ткань, а при гломерулонефрите — клубочки почек. Поэтому пиелонефрит называют «интерстициальным нефритом», от слова «интерстиций» — межуточная ткань, а гломерулонефрит можно назвать «клубочковым нефритом», от слова «гломерула» — почечный клубочек.[2]
Причина пиелонефрита — бактериальная инфекция. Среди возбудителей заболевания лидирует кишечная палочка (Escherichia coli). Реже встречаются другие микробы, такие как протей, энтерококк, синегнойная палочка и стафилококк.[4]
Особую опасность представляют БЛРС+ бактериями. Аббревиатура «БЛРС» расшифровывается как «бета-лактамазы расширенного спектра действия». БЛРС — это группа бактериальных ферментов, которые позволяют бактериям игнорировать антибиотики. Благодаря БЛРС бактерии расщепляют и нейтрализуют несколько групп антибактериальных препаратов, включая пенициллины и цефалоспорины. Продуцировать подобные ферменты могут далеко не все микробы, довольно часто эта способность наблюдалась у кишечной палочки и клебсиеллы пневмонии. Современные микробиологические лаборатории всегда отмечают подобные микробы либо русской аббревиатурой БЛРС+, либо английским аналогом ESBL+. Согласно европейским данным, БЛРС, продуцируемые кишечной палочкой, встречаются в 10% случаев, а клебсиелла пневмонии продуцирует БЛРС в 20% случаев. Таким образом, проблема БЛРС+ бактерий имеет важное клиническое значение.[8]
Таким образом, проблема БЛРС+ бактерий имеет важное клиническое значение.[8]
Острый пиелонефрит может возникнуть в любом возрасте и у любого пола. Чаще всего заболевание возникает у женщин активного репродуктивного возраста, что объясняется особенностями строения женской мочеполовой системы. Однако нередко пиелонефрит выявляют у детей и половозрелых мужчин, поэтому возраст и пол заболевавшего не могут быть использованы в качестве дифференциального признака данного заболевания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы острого пиелонефрита
Для острого пиелонефрита типично сочетание высокой температуры с болями в области воспалённой почки. Если почка располагается на своём месте, то боль беспокоит в проекции рёберно-позвоночного угла. При опущении почки боль возникает по фланкам живота. Пиелонефрит может затрагивать как одну почку, так и обе почки, соответственно боль может беспокоить как с одной стороны, так и с обеих сторон одновременно.
Выраженность боли может быть различной — от умеренной до интенсивной. Как правило, боль носит постоянный характер и не зависит от положения тела или движений. Иными словами, невозможно найти такое положение в кровати, когда боль будет беспокоить меньше или пройдет совсем. Также верно и то, что движения туловищем в виде сгибания, разгибания или поворотов не приводят к обострению болей.
В отдельных случаях боль носит приступообразный характер. Это характерно для пиелонефритов, которые возникают на фоне закупорки мочевых путей камнем. Если при классической почечной колике боль между приступами отступает совсем, то при сопутствующем пиелонефрите болевой синдром сохраняется и между приступами.
Общая симптоматика при пиелонефрите характеризуется повышение температуры. Как правило, температура достигает 38-40 градусов. Повышение температуры сопровождается ознобом. Также характерно максимальное повышение температуры в вечернее время с резким падением температуры в утренние часы. Кроме повышения температуры могут быть и другие проявления общего отравления организма в виде слабости, вялости, усталости и отсутствия аппетита.
Кроме повышения температуры могут быть и другие проявления общего отравления организма в виде слабости, вялости, усталости и отсутствия аппетита.
Развитие острого пиелонефрита может сопровождаться изменения со стороны мочеиспускания, хотя это не является обязательным условием. Можно отметить появление мути в моче и неприятного запаха. Кроме того, воспалённая моча потенциально способна спровоцировать учащённое мочеиспускание. В целом мочевые симптомы выходят на первый план только в том случае, если острый пиелонефрит осложняет уже имеющееся воспаление мочевого пузыря.[1][4]
Патогенез острого пиелонефрита
Бактерия попадает в почку либо с кровью, либо с мочой. Кровяной занос бактериальной инфекции получил название «гематогенного» пути передачи. Иногда врачи говорят о нисходящем пути развития острого пиелонефрита. Например, тот же нелеченный бронхит может осложниться развитием пиелонефрита за счёт обильного поступления бактерий в кровь. Нужно понимать, что почки фильтруют кровь со всего организма, поэтому пиелонефрит может осложнить любой несвоевременно пролеченный гнойник, даже расположенный в ногах или руках.
Альтернативой кровяному пути попаданию бактерий является мочевой путь распространения микробов. В научной литературе такой путь передачи возбудителя именуется «уриногенным», от слова «урина» — моча. Раньше такой путь заражения называли «восходящим», так как инфекция фактически «карабкается» вверх из мочевого пузыря. Вот почему очень важно своевременно пролечивать воспаление мочевого пузыря в виде цистита, не дожидаясь распространения бактерий вверх в почку.
Уриногенный путь передачи особенно характерен для детей из-за широкого распространения пузырно-мочеточникового рефлюкса. Так называют заброс мочи из мочевого пузыря обратно в почку. Несмотря на широкое распространение рефлюкса именно в детском возрасте, многие взрослые страдают аналогичным заболеванием. Особенно часто рефлюкс, то есть обратный заброс мочи, наблюдается при переполнении мочевого пузыря. Поэтому очень важно своевременно опорожнять мочевой пузырь.[8]
Особенно часто рефлюкс, то есть обратный заброс мочи, наблюдается при переполнении мочевого пузыря. Поэтому очень важно своевременно опорожнять мочевой пузырь.[8]
Классификация и стадии развития острого пиелонефрита
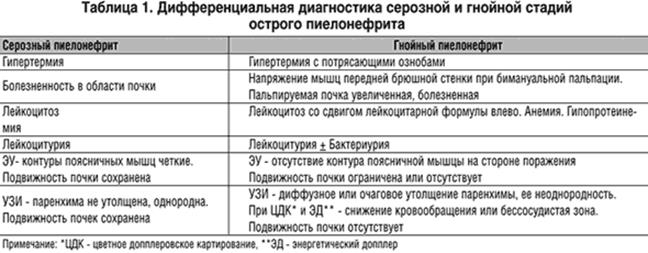
Традиционно острый пиелонефрит подразделяют на серозный и гнойный, хотя гнойный пиелонефрит является скорее осложнением острого пиелонефрита.
Существует несколько форм гнойного пиелонефрита:
- апостематозный пиелонефрит;
- абсцесс почки;
- карбункул почки;
- некротический папиллит;
- эмфизематозный пиелонефрит.
Если гнойников много, и они небольшие по размеру, то говорят об апостематозном пиелонефрите. В том случае, если гнойник большой и одиночный, то мы имеем дело с абсцессом почки.
Почечный абсцесс нужно дифференцировать с карбункулом почки. Карбункул — это часть почечной паренхимы, погибшая вследствие закупорки крупного почечного сосуда микробным эмболом. Рано или поздно погибшие от эмболии ткани подвергаются гнойному расплавлению, что приводит к абсцедированию карбункула.
Особой формой острого пиелонефрита является некротический папиллит — это грозное и смертельно опасное заболевание. К счастью, эта болезнь встречается настолько редко, что даже опытные урологи со стажем работы в несколько десятков лет могут вспомнить лишь несколько случаев данной формы острого пиелонефрита. При некротической папиллите происходит некроз, то есть омертвление и гибель почечного сосочка. Это сопровождается почечной недостаточностью и появлением крови в моче. Причина некротического папиллита сходна с причиной карбункула: закупорка почечного сосуда микробным эмболом. Только при папиллите страдает сосуд, питающий почечный сосочек.[4]
Также пиелонефрит можно подразделить на первичную и вторичную форму. Первичный острый пиелонефрит развивается в интактной почке, то есть без аномалий развития, камней и значимых нарушений оттока мочи. Вторичный острый пиелонефрит возникает на фоне заболеваний, которые нарушают пассаж мочи. Между вторичной формой острого пиелонефрита и первичным обострением хронического пиелонефрита очень тонкая грань, поэтому в МКБ-10 введён код № 12 «Тубулоинтерстициальный нефрит, не уточнённый как острый или хронический».[3]
Вторичный острый пиелонефрит возникает на фоне заболеваний, которые нарушают пассаж мочи. Между вторичной формой острого пиелонефрита и первичным обострением хронического пиелонефрита очень тонкая грань, поэтому в МКБ-10 введён код № 12 «Тубулоинтерстициальный нефрит, не уточнённый как острый или хронический».[3]
Осложнения острого пиелонефрита
Местные осложнения острого пиелонефрита включают апостематоз, абсцесс почки, эмфизематозный пиелонефрит, а также тромбоз почечных сосудов либо в виде карбункула почки, либо в виде некротизирующего папиллита.[10]
Эмфизематозный пиелонефрит является исключительно редким заболеванием и отличается от прочих гнойных осложнений пиелонефрита появлением пузырьков газа. Воздушные скопления могут быть в почечной паренхиме, полостной системе почек или даже в паранефральной клетчатке. К счастью, эмфизематозный пиелонефрит встречаются существенно реже других гнойных осложнений почки.[7]
Среди системных осложнений нужно отметить острую почечную недостаточность и синдром системной воспалительной реакции (сепсис). Именно поэтому часть пациентов нуждается в госпитализации в урологические стационары. В условиях стационара проводится регулярный контроль анализов и УЗИ для своевременного выявления осложнений острого пиелонефрита.[4]
Некоторые осложнения пиелонефрита в большей степени ассоциированы с хронической формой этого заболевания, но так как острый пиелонефрит может перейти в хронический, то нельзя не упомянуть о таком важном осложнении как мочекаменная болезнь. В некоторых ситуациях воспаление почечной паренхимы вызывают уреаза-продуцирующие микробы. Уреаза — это фермент, который позволяет бактериям расщеплять мочевину из мочи. После срабатывания фермента мочевина расщепляется до углекислоты и аммиака. Именно эти два компонента запускают сложный биохимический каскад, который приводит к образованию инфекционных камней: струвита и гидроксиапатита. К счастью, самый частый возбудитель пиелонефрита — кишечная палочка — не умеет производить уреазу, этой способностью обладают другие более редкие возбудители пиелонефрита — протей, клебсиелла и синегнойная палочка.
Важным осложнением острого пиелонефрита является хроническая форма этого заболевания. Именно поэтому очень важно диспансерное наблюдение после удачного излечения острого пиелонефрита. Словосочетание «диспансерное наблюдение» немного пугает своей бюрократической составляющей, но по сути это означает необходимость контролировать анализы мочи в течение минимум трёх месяцев после перенесённого острого пиелонефрита.
Диагностика острого пиелонефрита
Минимальный объём обследований:
- общий анализ мочи;
- посев мочи на флору с определением чувствительности к антибиотикам;
- клинический анализ крови;
- анализ крови на креатинин;
- УЗИ почек и мочевого пузыря.
Общий анализ мочи
Типичным для пиелонефрита является повышение уровня лейкоцитов и обнаружение бактерий. Могут быть и другие неспецифичные для данного заболевания изменения, включая повышенный уровень белка или положительный тест на нитриты. Обнаружение большого количества эритроцитов требует проведения дифференциальной диагностики с мочекаменной болезнью и гломерулонефритом.
Посев мочи на флору и чувствительность к антибиотикам
Этот анализ имеет смысл сдавать до назначения антибиотиков. Посев мочи позволяет выявить возбудитель пиелонефрита и определить наиболее эффективные антибактериальные препараты.
Клинический анализ крови
Неспецифическим признаком пиелонефрита является повышенный уровень лейкоцитов со сдвигом лейкоцитарной формулы влево. Как правило, больной с острым пиелонефритом повторяет клинический анализ крови два или три раза во время лечения. Данный анализ позволяет оценить эффективность антибактериальной терапии и своевременно сигнализировать о развитии гнойных осложнений в воспаленной почке.
Анализ крови на креатинин
Этот анализ является обязательным для всех пациентов с пиелонефритом прежде всего потому, что в ряде случаев острый пиелонефрит может осложниться развитием острой почечной недостаточности. Кроме того, анализ крови на креатинин необходим для решения вопроса о рентгенологическом исследовании почек с применением контраста.
Кроме того, анализ крови на креатинин необходим для решения вопроса о рентгенологическом исследовании почек с применением контраста.
УЗИ почек и мочевого пузыря
Ультразвуковое исследование позволяет исключить обструктивный пиелонефрит, связанный с нарушением оттока мочи из почки. Кроме того, УЗИ почек необходимо для своевременного выявления апостематоза, абсцесса и карбункула в паренхиме почки. Все вышеперечисленные термины используются для описания осложнений острого пиелонефрита.
Важнейшим преимуществом ультразвукового исследования является возможность повторения этого исследования в динамике без нанесения какого-либо вреда или даже дискомфорта организму. Важно помнить, что нормальные результаты УЗИ не исключают наличие острого пиелонефрита.
Рентгеновское обследование почек: внутривенная урография или компьютерная томография почек с внутривенным контрастированием.
Рентгеновское обследование почек является самым точным и достоверным методом диагностики. Традиционный рентген в виде внутривенной урографии подразумевает обязательное внутривенное введение йодсодержащего контраста. Это не всегда возможно из-за сопутствующих причин: аллергия на йод, приём гормонов щитовидной железы и повышенный уровень креатинина в крови. По сути, в настоящее время внутривенная урография необходима только для установления степени нефроптоза при опущении почек.
Значительно более широко применяется КТ почек (компьютерная томография). КТ относится к рентгеновским методам исследования, однако его информативность значительно выше, чем у обычного рентгена. Вопрос о введении йодсодержащего внутривенного контраста решается лечащим урологом индивидуально с каждым пациентом.[2][4]
Лечение острого пиелонефрита
Стационарное лечение обычно требуется для беременных, детей, пожилых людей, пациентов с ослабленным иммунитетом, плохо контролируемым диабетом, после трансплантации почек и, конечно же, всех людей с обструкцией мочевых путей. Также желательно госпитализировать людей с острым пиелонефритом единственной существующей или единственно функционирующей почки. Здоровые, молодые, небеременные женщины, которые болеют неосложнённым пиелонефритом, могут лечиться амбулаторно.
Также желательно госпитализировать людей с острым пиелонефритом единственной существующей или единственно функционирующей почки. Здоровые, молодые, небеременные женщины, которые болеют неосложнённым пиелонефритом, могут лечиться амбулаторно.
Обычно острый пиелонефрит требует исключительно медикаментозного лечения. Показания к хирургическому лечению возникают крайне редко.
Основу лечения острого пиелонефрита составляют антибиотики и нестероидные противовоспалительные средства. НПВС уменьшают болевой синдром, ослабляют симптомы интоксикации и помогают справиться с высокой температурой. Антибактериальная терапия острого пиелонефрита требует отдельного разбора.
Первоначальный выбор антибиотика при остром пиелонефрите является эмпирическим. Через 4-7 дней антибактериальная терапия может быть скорректирована по результатам посева мочи. Эмпирический выбор антибиотика остаётся на усмотрение лечащего врача.
В национальных рекомендациях в качестве средства выбора при остром пиелонефрите указаны фторхинолоны второго и третьего поколения.[4] Тоже самое сказано и в рекомендациях Европейской ассоциации урологов. Между тем, ещё в 2016 году FDA (Управление по контролю качества пищевых продуктов и лекарственных препаратов) рекомендовала отказаться от использования данных антибиотиков из-за большого количества осложнений в отношении связок, суставов и периферических нервов.[6] Поэтому в качестве первой линии терапии рекомендуют использовать цефалоспорины третьего поколения.
Наиболее широко используемым цефалоспорином третьего поколения является цефтриаксон. Активно практикуется ступенчатая терапия с плавным переходом от внутривенно вводимого антибиотика к его пероральному аналогу. С внутривенного цефтриаксона можно перейти на пероральный цефиксим, который также относится к цефалоспоринам третьего поколения. Цефиксим больше известен под своими торговыми названиями: «Супракс», «Супракс солютаб» и «Панцеф».
Часто можно встретить комбинацию из двух антибиотиков для лечения острого пиелонефрита. Как правило, комбинируют цефалоспорины с фторхинолонами или аминогликозидами. Аминогликозиды в виде амикацина обладают явным нефротоксическим действием, поэтому их использование для эмпирической терапии оправдано только в тяжёлых случаях. В целом выбор антибиотика — на усмотрение лечащего врача.[9]
Как правило, комбинируют цефалоспорины с фторхинолонами или аминогликозидами. Аминогликозиды в виде амикацина обладают явным нефротоксическим действием, поэтому их использование для эмпирической терапии оправдано только в тяжёлых случаях. В целом выбор антибиотика — на усмотрение лечащего врача.[9]
Показания к оперативному лечению возникают при гнойной форме воспаления и остром вторичном пиелонефрите. При вторичном пиелонефрите главная цель хирургического вмешательства состоит в дренировании мочи. Это можно сделать как путём установки почечного стента, так и благодаря чрезкожной пункционной нефростомии.
Гнойная форма острого пиелонефрита требует ревизии и декапсуляции почки, вскрытия гнойных очагов или даже нефрэктомии при гнойном разрушении большей части почки.[4]
Прогноз. Профилактика
Прогноз при пиелонефрите благоприятный. Большинство острых пиелонефритов успешно лечатся амбулаторно, и лишь небольшая доля случаев требует госпитализации. Тем не менее сохраняется определённый процент летальный исходов. Причиной неблагоприятного течения заболевания являются возраст старше 65 лет, присоединение острой почечной недостаточности, несвоевременно выявленные гнойные осложнения, требующие хирургического вмешательства, и тяжёлые сопутствующие заболевания наподобие декомпенсированного сахарного диабета.[5]
Составление плана индивидуальной профилактики начинается с изучения истории конкретного заболевания. В частности, необходимо ответить на вопрос, каким образом бактерии попали в почку: с кровью или с мочой? При гематогенном пути заражения необходимо санировать имеющиеся в организме очаги хронической инфекции, исключить переохлаждение и проводить профилактику сезонных простудных заболеваний. При уриногенном пути заражения необходимо заняться профилактикой воспалительных заболеваний мочевого пузыря.
В случае вторичной формы острого пиелонефрита целесообразно восстановить нормальный отток мочи из поражённой почки.
Вне зависимости от пути попадания микробов в почку всем пациентам рекомендуется потреблять достаточное количество жидкости и разнообразные урологические сборы растительного происхождения.[4]
Лечение пиелонефрита в домашних условиях — аппараты ОРИОН.
Укажите Ваше основное заболевание
Заболевания суставов:
артрозы, гонартроз, коксартроз, деформирующий остеоартроз, артриты, ревматоидный артрит, плечелопаточный периартрит, бурсит, тендовагинит, эпикондилит (локоть теннисиста), подагра, пяточная шпора
Заболевания позвоночника:
остеохондроз, протрузии, грыжи межпозвонковых дисков, шейно-плечевой радикулит, плексит, грудной радикулит, пояснично-крестцовый радикулит, ишиас
Сердечно-сосудистые заболевания:
гипертоническая болезнь, аритмия, кардиалгия, стенокардия, кардиомиопатия, ишемическая болезнь сердца (ИБС), сердечная недостаточность, последствия инфаркта
Заболевания нервной системы:
невриты, неврозы, невралгии, болевые синдромы, ишиалгии, мигрени, головные боли, в том числе метеозависимые, сосудисто-мозговая недостаточность, последствия инсульта, опоясывающий лишай, герпес и постгерпетические боли, ВСД
Заболевания вен и артерий:
варикозное расширение вен, тромбофлебит, трофические язвы, атеросклероз, облитерирующий эндартериит, диабетическая ангиопатия ног
Травмы и посттравматические осложнения:
вывихи, растяжения, разрывы связок, переломы, трещины костей, ушибы, гематомы, глубокие раны, укусы животных, абсцесс, панариций, фурункулез, флегмона, пролежни, ожоги, обморожения, послеоперационные осложнения
Лор-заболевания:
риниты, гайморит, синусит, отиты, ангина, тонзиллит, фарингит, ринофарингит, ларингиты, ларинготрахеиты, осиплость, охриплость, потеря голоса
Бронхо-легочные заболевания:
ОРВИ, грипп, бронхиты, трахеобронхиты, катар верхних дыхательных путей, пневмония, бронхиальная астма
Урологические заболевания:
простатит, доброкачественная гиперплазия простаты (ДГПЖ, аденома простаты), недержание мочи, энурез, цистит, уретрит, баланит, баланопостит, генитальный герпес, мочекаменные диатезы, пиелонефрит
Сексуальные расстройства:
эректильная дисфункция, преждевременная эякуляция, задержка эякуляции, ретардированная эякуляция, торможение оргазма
Заболевание почек пиелонефрит — лечение, симптомы и причины.

Пиелонефрит – одно из самых распространенных заболеваний почек у женщин или мужчин. Да и, скорее всего одно из самых известных. Острый пиелонефрит — это острый инфекционный процесс, поражающий почечную паренхиму и полостную систему, его еще называют инфекцией верхних мочевыводящих путей. Различные бактерии попадают в организм по мочевыводящим путям. Бактерии из мочевого пузыря чрез мочеточник проникают в почечную лоханку, паренхиму. Разберем основные признаки, симптомы и причины пиелонефрита.
Почему возникает острый пиелонефрит?
Хоть пиелонефрит является инфекционным заболеванием, его специфического возбудителя нет. Причиной могут стать микробы, которые постоянно обитают в организме, так же попадают из внешней среды. Если судить по анализам мочи, то в ней наиболее часто обнаруживаются кишечная и паракишечная палочки, бактерии группы протея, стафилококк, энтерококк, синегнойную палочку. Доказана также этиологическая роль микоплазм, вирусов и грибов. Для возникновения пиелонефрита недостаточно лишь проникновения микроорганизмов в почку. Для этого необходимы предрасполагающие факторы.
Кто рискует заболеть пиелонефритом?
Им можно заболеть в любом возрасте. Чаще болеют дети до семи лет, женщины 18-30 лет. У последних это связано с началом половой жизни, с беременностью и родами (у 5% беременных наблюдается пиелонефрит). Рискуют так же заболеть пиелонефритом пожилые мужчины, у которых имеется аденома предстательной железы, уретритом или простатитом. У детей пиелонефрит занимает второе-третье место по частоте заболевания. И еще предрасполагающим фактором является мочекаменная болезнь, сахарный диабет, туберкулез. Не стоит так же исключать из причин пониженный иммунитет. Среди взрослого населения пиелонефрит встречается у 100 человек на 100000 населения, у детей у 480–560.
Признаки острого пиелонефрита.
Общая слабость, боль в боку, которая может отдавать в пах, боль в пояснице, температура. Это основные симптомы заболевания. И обычно заболевание пиелонефритом сопровождается частыми позывами на мочеиспускание. Этот симптом бывает почти у половины всех заболевших. Если говорить более подробно – температура повышается, чуть ли не до 40 градусов, — это состояние схоже с тем, когда болеешь гриппом. Боль в пояснице, как правило, с одной стороны. У каждого они различны, но если их охарактеризовать, то можно назвать тупыми болями (не резкими). Если наблюдаются такие симптомы, то лучше сразу вызвать врача на дом. Острый пиелонефрит нужно срочно лечить, поскольку если запустить заболевание оно может перейти в хроническую форму. Так же может осложняться паранефритом, некрозом почечных сосочков.
Это основные симптомы заболевания. И обычно заболевание пиелонефритом сопровождается частыми позывами на мочеиспускание. Этот симптом бывает почти у половины всех заболевших. Если говорить более подробно – температура повышается, чуть ли не до 40 градусов, — это состояние схоже с тем, когда болеешь гриппом. Боль в пояснице, как правило, с одной стороны. У каждого они различны, но если их охарактеризовать, то можно назвать тупыми болями (не резкими). Если наблюдаются такие симптомы, то лучше сразу вызвать врача на дом. Острый пиелонефрит нужно срочно лечить, поскольку если запустить заболевание оно может перейти в хроническую форму. Так же может осложняться паранефритом, некрозом почечных сосочков.
Диагностика.
Правильная диагностика – пожалуй, самое важное с чего стоит начинать борьбу с пиелонефритом. Не торопитесь делать скоропалительные выводы, если где-то прочитали про симптомы пиелонефрита, сравнили их со своими и решили, что у вас именно пиелонефрит. Даже специалист, только выслушав ваши жалобы, не скажет на сто процентов, что это пиелонефрит. Его симптомы схожи со многими заболеваниями, связанных с воспалением мочевыводящих путей. Для диагностики делаются специальные анализы крови, мочи, УЗИ почек, анализы на инфекции и нередко требуется компьютерная томография.
Лечение.
Лечение пиелонефрита долгий и трудоемкий процесс. Если не соблюдать все рекомендации врача болезнь может перейти в хроническую форму и единственным методом лечения может остаться только хирургический. Желательно острый пиелонефрит лечить в стацион6аре под наблюдением специалистов. Больным назначают антибиотики (после проведенных проб на чувствительность микрофлоры пациента) в сочетании с сульфаниламидами и специальную диету. Больному рекомендуют выпивать в день не менее 2-2,5 литров жидкости. Когда температура спадает, назначаются тепловые процедуры (согревающие компрессы).
Если в течение первой недели лечения (3-5 дней) улучшения состояния не происходит, потребуются новые обследования, чтобы исключить сопутствующие заболевания. Если же все пойдет успешно, то интенсивное лечение острого пиелонефрита продлиться до 6 недель. Ну а окончательное излечение уже зависит полностью от самого пациента. Начинается самый сложный процесс – не запустить болезнь снова.
Если же все пойдет успешно, то интенсивное лечение острого пиелонефрита продлиться до 6 недель. Ну а окончательное излечение уже зависит полностью от самого пациента. Начинается самый сложный процесс – не запустить болезнь снова.
Профилактика.
Профилактику пиелонефрита здоровые люди могут искать в причинах и предрасполагающих факторах. А для тех, кто перенес острый пиелонефрит, — главное соблюдать все рекомендации врача. Пожалуй, самое сложное из них соблюдать определенную диету, — никаких соленостей, копченостей, шоколада, алкогольных напитков. Больше овощей, фруктов, натуральных соков, минеральной воды. Хотя если вдуматься,- ничего сложного в этом нет, если есть желание оберегать свое здоровье всеми способами.
Лечение хронического пиелонефрита | mgzt.ru
Этиология болезни, наблюдения, рекомендации
Как известно, хронический пиелонефрит – неспецифический инфекционно-воспалительный процесс в канальцевой системе почки, преимущественно бактериальной этиологии, характеризующейся поражением почечной лоханки (пиелит), чашечек и паренхимы почки (в основном её межуточной ткани).
Неосложнённые инфекции мочевыводящих путей относятся к числу наиболее распространённых бактериальных независимо от возраста пациентов, особенно у женщин. Они также являются одной из частых причин госпитализации среди пожилых людей и наиболее распространённым показателем для выписки рецептов на антибиотики в первичном звене здравоохранения многих стран.
Согласно имеющейся статистике, хронический пиелонефрит среди всех заболеваний мочеполовых органов с воспалительной неспеци фической природой диагностируется в 60-65% случаев. Причём 20-30% их являются следствием острого пиелонефрита.
Кратко остановимся на этиологии болезни. По данным Bertoni et al. (2017) при пиелонефритах в 70% случаев выделяется кишечная палочка, в 17% – сапрофитирующий стафилококк, в 7% – протей, в 4% – клебсиелла и в 0,7% – энтерококк и псевдомонас аэругиноза.
Могут быть и микробные ассоциации, однако следует помнить, что, несмотря на многообразие возбудителей, клинические эксперименты доказали роль моноинфекции в возникновении воспаления лоханок. Если результаты бактериального посева выявляют несколько микроорганизмов, можно предположить загрязнение посуды для сбора мочи. Как уже говорилось, наиболее частой причиной хронического пиелонефрита является уропатогенная кишечная палочка (E.coli).
Лечение хронического пиелонефрита – весьма сложная задача. Само собой разумеется, что если это инфекционное заболевание, то в первую очередь при нём показаны антибиотики. В рекомендуемые для лечения хронических пиелонефритов входят почти все группы имеющихся в наше время антибиотиков: полусинтетические пенициллины, цефалоспорины, налидиксовая кислота, аминогликозиды, фторхинолоны, оксихинолины, нитрофураны и некоторые химиопрепараты – сульфаниламиды.
Все эти препараты можно применять как в стационарных, так и в амбулаторных условиях. Hensey et al. (2017) провели анализ амбулаторного и стационарного лечения с парентеральным введением антибиотиков. Авторы нашли, что существенной разницы при этом не было. Амбулаторное лечение при этом было значительно дешевле.
Все показанные антибиотики применяются нами в стационаре per os в средних дозах коротким курсом 7 дней или длительным – 14. Если состояние больного тяжёлое, то ему назначаем комбинации антибактериальных средств или вводим внутривенно в больших дозах. Представляют интерес данные Dawson-Hahn et al. (2017). Они произвели метаанализ систематических обзоров и выявили, что применение антибиотиков коротким курсом (7 дней) является столь же эффективным, как и более длительные курсы (14 дней) при большинстве микробов, встречающихся в лечебной практике при хронических пиелонефритах. То же явление подтвердили van Nieuwkoop et al. (2017). Они провели рандомизированное, двойное слепое, плацебоконтролируемое исследование эффективности такого лечения у мужчин и женщин.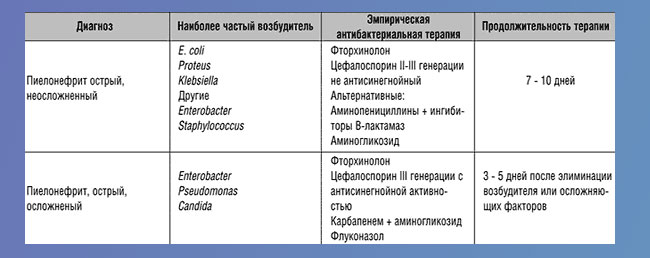
Авторы не выявили доказательной разницы между леченными 7 и 14 дней при анализе. Клиническое излечение наступило у 90% пациентов-мужчин, получавших 7-дневный курс, и у 95%, тех, кто получал 14-дневное лечение.
У женщин клиническое улучшение имело место в 94 и 93% у тех, кто лечился в течение 7 и 14 дней соответственно. Бактериологический анализ был примерно в таких же показателях. Долгосрочные наблюдения подтвердили эти выводы.
Имеются также сторонники длительных курсов антибиотикотерапии, например в течение 8 недель. Конкретную продолжительность терапии можно определить и по санации мочи от микробной флоры.
Мы предпочитаем проводить больным с хроническим, особенно часто рецидивирующим, пиелонефритом один короткий или пролонгированный курс в стационаре, а затем рекомендовать дома примерно следующее 3-месячное профилактическое лечение в домашних условиях:
Первый цикл (в первый месяц за проведением курса в стационаре):
1. Моксифлоксацин (авелокс) внутрь по 0,4 по 1 таблетке на ночь 7 дней.
2. На 3-й и 6-й дни — фуросемид по 80 мг внутрь 1 раз в день.
3. Аскорбиновая кислота внутрь по 1 г на полстакана воды после еды 2 раза в сутки также 7 дней.
4. Одновременно обильное питьё — мочегонный чай, настой толокнянки или отвар кукурузных рылец.
Второй цикл (второй месяц после лечения в стационаре):
Аугментин 500/125 или 875/125 по 1 таблетке 3 раза в день внутрь до еды — 7 дней, остальное — всё как при первом цикле
Анализы мочи 2 раза в неделю, 2 недели — общие, по Нечипорен-ко и тест на бактерии. Если моча полностью очистилась, на этом лечение можно пока прекратить. Если же количество лейкоцитов или число бактерий выше нормы -провести третий цикл.
Третий цикл (третий месяц после основного лечения):
Фуразолидон или фурагин 0,05 по 2 таблетки или фурамаг 0,05 по 2 капсулы внутрь 3 раза в день после еды 7 дней. Остальное — всё как при первом цикле.
После 3 циклов примерно 1 раз в 15 дней производить анализ мочи. Если при 3-кратной проверке в ней лейкоцитов будет не более 5-6 в поле зрения, далее лечение не проводить. Если будет больше, провести ещё 3 цикла с приёмом ко-тримоксазола (бисептол) по 1 таблетке 480 мг, затем бактрим форте 960 мг 4 раза в день 5 дней, затем ципрофлоксацина (ципролет) по 500 мг по 1 таблетке 2 раза в день или амикацина по 0,5-1 г внутримышечно 2 раза в день 10 дней.
Если при 3-кратной проверке в ней лейкоцитов будет не более 5-6 в поле зрения, далее лечение не проводить. Если будет больше, провести ещё 3 цикла с приёмом ко-тримоксазола (бисептол) по 1 таблетке 480 мг, затем бактрим форте 960 мг 4 раза в день 5 дней, затем ципрофлоксацина (ципролет) по 500 мг по 1 таблетке 2 раза в день или амикацина по 0,5-1 г внутримышечно 2 раза в день 10 дней.
Выше говорилось, что при хронических пиелонефритах рекомендуются различные группы антибиотиков. Kranz et al. (2017) в случаях неосложнённого пиелонефрита лёгкой и умеренной форм в качестве пероральных антибиотиков рекомендуют использовать цефподоксим, цефтибутен, ципрофлокса-цин или левофлоксацин. V.E.Tverdot et al. (2012) провели сравнительное исследование влияния фторхино-лонов и р-лактамов на клинические и биохимические проявления хронического пиелонефрита. Результаты исследования показали, что применение фторхинолонов и |3-лактамов в лечении больных хронических пиелонефритов на почве нефролитиаза приводит к значительному облегчению клинических симптомов заболевания, а также к восстановлению структурно-функционального состояния мембран сегментоядерных лейкоцитов. Наиболее отчётливый и ранний клинико-лабораторный эффект был получен на фоне применения фторхинолонов.
Нельзя не упомянуть и о ксантогранулематозном хроническом пиелонефрите. Название связано с тем, что при этом заболевании вокруг чашечек почек и абсцессов в почечной паренхиме отмечают скопление ксантомных, или «пенистых» клеток, нагруженных липидами. По Li, Parwani (2011), Chandanwale (2013), Auregan et al. (2015) и др., — это редкое хронинических пиелонефритов на почве нефролитиаза приводит к значительному облегчению клинических
симптомов заболевания, а также к восстановлению структурно-функционального состояния мембран сегментоядерных лейкоцитов. Наиболее отчётливый и ранний клинико-лабораторный эффект был получен на фоне применения фторхинолонов.
Мы до сих пор не упоминали один из лучших препаратов лечения инфекций мочевых путей — фосфомицина трометамол. В то же время он один из лучших уроантибиотиков с чрезвычайно малой резистентностью к нему. В отечественной литературе есть мнение, что его следует применять лишь при инфекции нижних моче-выводящих путей — циститах, но не пиелонефритах. В зарубежной печати имеются другие мнения.
В то же время он один из лучших уроантибиотиков с чрезвычайно малой резистентностью к нему. В отечественной литературе есть мнение, что его следует применять лишь при инфекции нижних моче-выводящих путей — циститах, но не пиелонефритах. В зарубежной печати имеются другие мнения.
Так, Perrault et al. (2017) в случаях, когда сложно определить, где локализуется инфекция (а это не такая уж редкая ситуация) рекомендуют применять фосфомицин. Они, кстати, провели анализ стоимость — эффективность (очень важный момент для российского скудного бюджета на здравоохранение). Сравнивалась стоимость -эффективность фосфомицина и сульфонамидов, фторхинолонов и нитрофуранов. Было доказательно установлено, что включение фосфомицина в лечение существенно не увеличивало стоимость лечения инфекций мочевых путей.
Авторы делают вывод, что фосфомицин — безопасное и эффективное средство для лечения инфекций мочевых путей с неясной локализацией и возбудителем. К нему пока мало устойчивых бактерий, принимается он внутрь (есть и парентеральные формы) в виде гранул, разведённых в воде, как правило, однократно в дозе 2 г. В том числе и по этой причине стоимость его применения не выше стоимости лечения другими препаратами.
К сожалению, лечение инфекций нижних и верхних мочевыводящих путей создают проблемы в клинической практике в связи с их высокой распространённостью и рецидивированием, а также бы-стропрогрессирующим повышением устойчивости уропатогенных бактерий к антибиотикам. К примеру, в работе Bertoni et al. (2017) было показано, что в Испании выявляется следующая устойчивость бактерий к антибиотикам, при лечении инфекций мочевыводящих путей: ампициллин + сульбактам 37%, цефалексин 28%, триме-топрим/сульфаметоксазол 22%, нитрофурантоин 12%, гентамицин 7% и ципрофлоксацин 5%.
В связи с этим в настоящее время весь мир бьёт тревогу по поводу быстрого нарастания устойчивости бактерий к антибиотикам. К сожалению, в последние годы новые антибиотики не создаются — слишком дорого и желающих вкладывать деньги в лекарства, эффективность которых писана, как говорится, вилами по воде, нет.
Одним из выходов из создающегося положения являются поиски методов восстановления чувствительности микробов к антибиотикам. Sims et al. (2017) провели проспективное, рандомизированное двойное слепое исследование по определению способности р-лактамазного ингибитора релебактама и циластатина (антибиотик из группы карбапенемов) восстанавливать активность имипенема в отношении имипенем нечувствительных микроорганизмов. Они лечили группы больных с инфекциями мочевыводящих путей комбинациями имипенем/цила-статин + релебактам в дозе 250 и 125 мг и имипенем/циластатин без релебактама.
В целом авторы нашли, что такие комбинации становятся высокодейственными в отношении не чувствительных к имипинему бактерий.
Ряд учёных предлагают антибактериальную терапию дополнять физио- или бальнеотерапевтичес-кими процедурами, что значительно улучшает степень оздоровления организма. E.N.Slobodian et al. (2017) рекомендуют лечение хронического пиелонефрита минеральной грязью. Авторы считают, что при этой болезни, как правило, возникает тубулоинтерстици-альный фиброз, а грязелечение приводит к дефиброзирующему эффекту, изменяет структуру и функции внеклеточного матрикса. Системный ответ на грязевую терапию проявляется в виде изменений в метаболизме межклеточного матрикса и коллагена соединительной ткани, которые обычно и стимулируют фиброгенез и развитие тубулоинтерстициальных расстройств.
G.M.Nurtdinova, L.P.Chrnyshova, E.S.Galimova (2011) рекомендуют к традиционной терапии хронического пиелонефрита добавлять магнито- и лазеротерапию. Проведя проспективное наблюдение 70 пациентов с хроническим пиелонефритом, 30 из которых в дополнение к традиционной терапии получали магнито-лазе-ротерапию, авторы нашли, что такое комбинированное лечение ведёт к значительному снижению продолжительности основных клинических проявлений заболевания, нормализации иммунной системы и выработке цитокинов. I.P.Kudriashova, T.P.Ospel’nikova, F.I.Ershov (2011) выявили, что у всех больных хроническими пиелонефритами снижена способность лейкоцитов синтезировать интерфероны в крови, особенно интерферон гамма. В связи с этим они провели лечение таких больных с добавлением к традиционной терапии циклоферона по стандартной схеме. Установлено, что такая терапия значительно стимулировала продукцию интерферона альфа и гамма по сравнению с группой, получающей только стандартную терапию. Ретроспективное обследование 5 пациентов показало, что и через год эта способность лейкоцитов продуцировать интерфероны сохранилась.
В связи с этим они провели лечение таких больных с добавлением к традиционной терапии циклоферона по стандартной схеме. Установлено, что такая терапия значительно стимулировала продукцию интерферона альфа и гамма по сравнению с группой, получающей только стандартную терапию. Ретроспективное обследование 5 пациентов показало, что и через год эта способность лейкоцитов продуцировать интерфероны сохранилась.
I.V.Gordiushina et al. (2011) нашли, что добавление антиоксидантного препарата цитофлавин к традиционной терапии больных хроническим пиелонефритом снижает интенсивность процессов перекис-ного окисления и сохраняет анти-оксидантный статус. Такое действие нормализует соотношение фосфолипидных фракций плазмы крови и мембран клеток, что улучшает защитный статус организма. С этой же целью E.V.Ivanishkina (2010) предлагает включать микроволновую резонансную терапию в комплексное лечение больных хроническим пиелонефритом.
Нельзя не упомянуть и о ксантогранулематозном хроническом пиелонефрите. Название связано с тем, что при этом заболевании вокруг чашечек почек и абсцессов в почечной паренхиме отмечают скопление ксантомных, или «пенистых» клеток, нагруженных липидами. По Li, Parwani (2011), Chandanwale (2013), Aur gan et al. (2015) и др., – это редкое хроническое заболевание, имеющее под собой деструктивный гранулематозный процесс почечной паренхимы в связи с длительной обструкцией мочевыводящих путей и инфекции. Чаще встречается у женщин. Типичный пациент с ксантогранулематозным пиелонефритом – женщина средних лет с длительно текущей рецидивирующей инфекцией мочевых путей и камнями в почках. Тем не менее возраст больных имеет широкий диапазон – от новорождённых до пожилых людей.
Наиболее распространёнными симптомами являются боли в боку или брюшной полости, симптомы поражения нижних мочевыводящих путей, лихорадка, пальпирование почки, выраженная гематурия и потеря веса. Частые лабораторные показатели – лейкоцитоз и анемия. При посеве чаще всего выявляют Escherichia сoli и Proteus mirabilis. Компьютерная томография является наиболее оптимальным методом выявления этого пиелонефрита. Биоптаты выявляют гранулема-тозный воспалительный инфильтрат, состоящий из нейтрофилов, лимфоцитов, плазматических клеток, ксантоматозных гистиоцитов и мультинуклеарных гигантских клеток.
Компьютерная томография является наиболее оптимальным методом выявления этого пиелонефрита. Биоптаты выявляют гранулема-тозный воспалительный инфильтрат, состоящий из нейтрофилов, лимфоцитов, плазматических клеток, ксантоматозных гистиоцитов и мультинуклеарных гигантских клеток.
Процесс может быть локальным или генерализованным, даже с переходом воспалительных инфильтратов в забрюшинное пространство и соседние структуры – мышцы, селезёнку, толстую кишку, крупные сосуды.
Лечение – как консервативное (антибиотики), так и хирургическое – в зависимости от состояния пациента. Представляет интерес, что заболевание часто выявляется у тихоокеанских маорийцев. Наиболее частой причиной у них являются коралловидные конкременты (51,4%), ведущие к обструкции, что и приводит у 22,9% из них к ксан-тогранулематозному хроническому пиелонефриту. Хирургическое лечение весьма травматично, но остаётся единственным методом, хотя при этом до- и послеоперационное лечение антибиотиками играет важную роль.
Несколько слов об эмфизематозном пиелонефрите. В зарубежной литературе есть целый ряд статей, посвящённых данной форме болезни (Саади et al., 2017 и др.). Эмфизематозный пиелонефрит – некротизирующая инфекция почечной паренхимы и околопочечной клетчатки, заболевание, характеризующееся наличием воздуха в пределах паренхимы мочевыво-дящих путей и периренального пространства. Эмфизематозный пиелонефрит является редким осложнением трансплантации почек. Его тяжесть связана, в частности, с нарушением сопротивляемости организма иммуносупрессирован-ных пациентов.
Ибрагим ШАМОВ, профессор.
Пиелонефрит при беременности — цены на лечение, симптомы и диагностика заболевания в клинике «Мать и дитя» в Москве
Пиелонефрит — это инфекционно-воспалительное заболевание бактериальной природы, поражающее ткань и лоханку почки. В запущенной стадии может сопровождаться формированием гнойных очагов в почке (карбункулов, абсцессов) и развитием сепсиса.
Женщины молодого возраста страдают пиелонефритом в 4-5 раз чаще, чем мужчины, это связано с анатомическими особенностями строения мочеполовой системы.
Пиелонефрит у мужчин в подавляющем большинстве случаев связан с нарушением оттока мочи из почки, обусловленным мочекаменной болезнью, структурой мочеточника или различными аномалиями развития почек и мочевых путей.
Также прямыми или косвенными предрасполагающими факторами к развитию пиелонефрита являются: беременность, сахарный диабет, почечная недостаточность и рецидивирующие инфекции мочевых путей, семейный анамнез.
Для острого пиелонефрита характерны:
- высокая температура тела;
- боль в поясничной области;
- изменения в моче, характерные для воспалительного процесса.
Наибольшее значение в диагностике пиелонефрита имеют клинические (симптомы) и лабораторные методы исследования. Обязательными являются: проведение общего и бактериологического исследований мочи, общего и биохимического анализов крови.
Учитывая принципиальную разницу в лечебной тактике при неосложненном и осложненном остром пиелонефрите, для их дифференциальной диагностики методом выбора является ультразвуковое исследование (УЗИ) почек. Экспертное УЗИ позволяет выявлять основные осложняющие факторы пиелонефрита (нарушенный отток мочи, камни, абсцессы) у подавляющего большинства больных.
В случае необходимости более детального изучения состояния почек и мочевых путей выполняется мультиспиральная компьютерная томография с контрастированием — этот метод обладает максимальной информативностью и диагностической точностью.
Лечение при остром неосложненном пиелонефрите в большинстве случаев консервативное.
Для быстрого и комплексного обследования с целью установки диагноза, подбора лекарственной терапии, снижения риска хронизации процесса и снятия симптомов интоксикации мы рекомендуем госпитализацию, в стационаре в течение нескольких часов будет проведено обследование в необходимом объеме, и начата комплексная этиотропная терапия.
В случае, если по результатам обследования установлено, что причиной пиелонефрита является нарушение оттока мочи из почки (например, из-за камня), врачи-урологи ГК «Мать и дитя», владеющие самыми современными и щадящими методами устранения обструкции и эндоскопического удаления камня, выполнят его удаление, что минимизирует сроки лечения и существенно снизит риск рецидива заболевания.
Запишитесь на консультацию к врачу-урологу.
Симптоматика, диагностика и лечение острых воспалительных заболеваний почек у больных сахарным диабетом | Курбатов
Cахарный диабет (СД), являясь одним из наиболее распространенных заболеваний в мире, представляет собой острейшую медико-социальную проблему, приоритетную для систем здравоохранения всех стран [1]. Неоспоримый прогресс в лечении СД привел, с одной стороны, к увеличению продолжительности жизни этих больных, а с другой – к возрастанию частоты различных осложнений данного заболевания. Нарушение углеводного обмена оказывает негативное влияние практически на все органы и системы организма, в том числе на мочеполовую систему. Среди основных урологических осложнений при СД наиболее часто встречаются инфекции мочевых путей (ИМП) и тесно связанные с ними воспалительные заболевания почек.
Особенности развития и течения ИМП у больных СД
Одним из основных специфических процессов при СД является повышение концентрации глюкозы в моче на фоне гипергликемии. Глюкозурия является одним из наиболее важных факторов риска развития ИМП у пациентов с СД в результате подавления фагоцитоза и, возможно, клеточного иммунитета, а также способствуя адгезии бактерий, хотя в эксперименте очень высокая концентрация глюкозы в моче (свыше 55 ммоль/л) подавляет их рост. В конечном итоге, длительная выраженная глюкозурия является фактором риска повреждения серозно-мукоидного слоя уротелия с развитием ИМП. Патогенетическими факторами, обусловливающими развитие ИМП и воспалительных заболеваний почек при СД, являются также [2, 3]:
токсическое воздействие гипергликемии;
микро- и макроангиопатии, способствующие ишемии почек;
автономная нейропатия, приводящая к нейрогенной дисфункции мочевого пузыря и хронической задержке мочи;
недостаток гликогена, приводящий к ухудшению условий питания клубочково-канальцевого аппарата;
гипергликемия, снижающая фагоцитарную активность лейкоцитов и бактерицидность крови.

При СД1 развитию ИМП способствует длительное течение болезни, более раннее (в течение первых 4–5 лет) и стойкое развитие периферической и автономной нейропатии. [4].
Спектр патогенных микроорганизмов, вызывающих ИМП у больных СД, сходен с таковым у пациентов без СД [5]. Однако по данным других авторов, соотношение пациентов с СД к пациентам без СД по наличию бактериурии составляет 26,8/15,5, по поражению урологического тракта – 8,7/2,2 и выявлению – Escherichia Coli 8,9/3,4 [6]. Установлено, что СД увеличивает риск развития восходящего из нижних отделов мочевых путей острого пиелонефрита (ОП), возбудителем которого служат представители рода Enterobacteriaceae и Enterococcus faecalis. Часто у женщин, страдающих СД, в этой роли выступают также представители рода Klebsiella (25% у пациенток с СД по сравнению с 12% у пациенток без СД) [7].
К вирулентности бактериальной клетки и способности закрепиться на поверхности слизистой перед моментом ее внедрения имеет отношение ряд установленных факторов бактериального сцепления, т.н. фимбрии. Фимбрии 1 типа имеются практически у всех типов Escherichia Coli, которые обеспечивают связывание с рецепторами клеток слизистой влагалища, и в меньшей степени с рецепторами защитного мукополисахаридного слоя, выстилающего слизистую мочевых путей. Для бактерий с фимбриями 2-го типа (Р-фимбриями) более характерна склонность к сцеплению с гликолипидами субстанций различных групп крови, которые секретируются уротелием. Р-фимбрии, в отличие от фимбрий 1 типа, в большей степени имеют способность к сцеплению и поражению мочевых путей, вызывая ИМП и пиелонефрит. В исследованиях А. Хопельман, С. Гирлингс (2000), выявлено повышение адгезии кишечной палочки с фимбриями 1 типа к уроэпителию женщин с СД по сравнению со здоровыми людьми [8].
Важным фактором защиты макроорганизма от инфекции является уровень половых гормонов, в частности: эстрогенов и прогестерона – для женщин, и тестостерона для мужчин. Уротелий вырабатывает и выделяет на поверхность мукополисахаридную субстанцию, образующую адгезивный защитный слой. Образование этого мукополисахаридного слоя считается гормонально-зависимым процессом: эстрогены влияют на его синтез, прогестерон на его выделение эпителиальными клетками [9]. Подтверждается также и роль тестостерона в воздействии на рецепторы уротелия. Показано, что у пациентов с СД на фоне снижения уровней половых гормонов, повышен риск развития ИМП [10, 11, 12].
Уротелий вырабатывает и выделяет на поверхность мукополисахаридную субстанцию, образующую адгезивный защитный слой. Образование этого мукополисахаридного слоя считается гормонально-зависимым процессом: эстрогены влияют на его синтез, прогестерон на его выделение эпителиальными клетками [9]. Подтверждается также и роль тестостерона в воздействии на рецепторы уротелия. Показано, что у пациентов с СД на фоне снижения уровней половых гормонов, повышен риск развития ИМП [10, 11, 12].
Острые воспалительные заболевания почек у больных СД
К воспалительным заболеваниям почек относят острый пиелонефрит (ОП) и хронический пиелонефрит (ХП), который может быть как следствием ОП, так и самостоятельной формой заболевания. Для описания форм и стадийности процесса у больных с диагнозом пиелонефрита пользуются классификацией Н.А. Лопаткина (рис. 1), которая наиболее полно отражает различные формы воспалительного процесса в почке [13].
ОП определяется как инфекционно-воспалительное заболевание почечной паренхимы и чашечно-лоханочной системы с преимущественным поражением интерстициальной ткани. Длительная декомпенсация углеводного обмена является фактором риска развития и прогрессирования острого инфекционно-воспалительного процесса в почках, однако, сам пиелонефрит не является осложнением СД. ОП и его хронизация являются факторами, усугубляющими течение такого грозного специфического осложнения как диабетическая нефропатия.
Особое внимание клиницистов обращено на острые гнойно-деструктивные формы течения ОП, в связи с быстрым прогрессированием заболевания и реальной опасностью для жизни больных в случаях развития септических состояний. В случае обструкции мочевыводящих путей (камни почек и мочеточников, опухоль мочевого пузыря, аденома простаты и др.) алгоритмы диагностики и лечения ИМП кардинально меняются, поэтому эти случаи требуют отдельного рассмотрения.
ОП у пациентов с СД может быть как асимптоматическим (при ареактивности иммунной системы, или частичном иммунном дефиците), так и протекать манифестно [14]. Полагают, что снижение общей иммунной резистентности предрасполагает к персистенции возбудителей ИМП [15].
Полагают, что снижение общей иммунной резистентности предрасполагает к персистенции возбудителей ИМП [15].
При необструктивном ОП микроорганизмы достигают мочевых путей гематогенно или по лимфатическим путям [16]. Установлено, что больные СД особенно уязвимы для быстрого прогрессирования инфекции в почечной паренхиме и ее последующих осложнений. Комбинация СД и ОП ведет к возникновению порочного круга, когда активный воспалительный процесс в паренхиме почки отрицательно влияет на функцию клубочково-канальцевого аппарата, одновременно усугубляя инсулиновую недостаточность в связи с нарастанием ацидоза. В свою очередь, нарушение метаболизма и отчетливое снижение микроциркуляции ухудшают течение гнойной инфекции в почках, что получило название «синдрома взаимного отягощения» (рис. 2) [17].
Дополнительным фактором, усугубляющим развитие ОП, является эндотелиальная дисфункция, которая на фоне длительного воздействия гипергликемии приводит к нарушению ангиогенеза и гемостаза [18]. При этом происходит снижение синтеза NO и повышение концентрации эндотелина-1 в почечных сосудах, что в результате приводит к их спазму, агрегации тромбоцитов, адгезии моно- и тромбоцитов. Развившаяся дисфункция эндотелия усиливает патологическое воздействие инфекционного процесса на ткани почки. Осевшие в почечных клубочках микроорганизмы вызывают повреждение эндотелия с нарушением проницаемости, вплоть до полной его деструкции, и проникают в просвет канальцев, а затем выводятся с мочой. Именно поэтому значительная бактериурия в первые двое суток заболевания пиелонефритом может быть его единственным симптомом. В последующие дни вокруг бактериальных тромбов развивается воспалительный процесс с образованием лейкоцитарных инфильтратов в межуточной ткани.
Декомпенсированный СД часто сопровождается состоянием иммунодефицита, при котором инфекционные процессы протекают более агрессивно. Возможно, по этой причине развитие ОП является не столько результатом агрессии микроорганизмов, сколько результатом предрасполагающего к инфицированию состояния макроорганизма [19].
ОП часто протекает как тяжелое инфекционное заболевание, представляющее угрозу для жизни больного. Противоречивые данные об особенностях клиники, течения заболевания и недостаточная изученность механизмов развития ОП у больных с СД обусловливают трудности его диагностики, лечения и профилактики. На секционном материале ОП выявляется у 20% больных с СД, умерших от различных других причин, т.е. не имевших первичного диагноза ОП [20].
У пациентов с СД, как и в общей популяции, преобладает односторонний воспалительный процесс. Однако при выраженной декомпенсации СД повышается риск развития двустороннего пиелонефрита. Как правило, клинически болезнь начинается остро – с высокой температуры, лихорадки, дизурии, болей в поясничной области. В крови отмечается лейкоцитоз, увеличение СОЭ. У больных СД исследование мочи обнаруживает наличие бактерий и большое количество лейкоцитов, однако у данной категории больных может также выявляться и нормальный клеточный состав осадка мочи, отсутствие бактериурии.
В типичных случаях при СД поражаются верхние отделы мочевых путей, вплоть до развития диффузно-гнойной (апостематозный пиелонефрит) или гнойно-деструктивной формы заболевания (карбункул, абсцесс). Частота развития гнойных форм пропорциональна тяжести течения и степени нарушения углеводного обмена.
Не менее чем у трети больных ОП манифестирует в виде гнойного процесса: апостематозного пиелонефрита, карбункула или абсцесса. Известно, что в 34% случаев у больных без СД ОП переходит в гнойные формы [21]. При несвоевременной диагностике и запоздалой терапии заболевания у пациентов на фоне СД, острый серозный пиелонефрит переходит в гнойные формы у большинства больных [22]. В этих случаях заболевание сопровождается выраженной интоксикацией и при несвоевременном лечении может развиться септический шок, при котором смертность превышает 60% [23, 24, 25]. Необходимо помнить, что у больных ОП на фоне декомпенсации СД время перехода от серозной в гнойную форму укорачивается, при этом клиническая картина может не иметь выраженных проявлений. Однако прогрессирование заболевания можно предполагать по внезапному ухудшению показателей углеводного обмена. На нарастание тяжести процесса может указывать резкое ухудшение гликемии.
Однако прогрессирование заболевания можно предполагать по внезапному ухудшению показателей углеводного обмена. На нарастание тяжести процесса может указывать резкое ухудшение гликемии.
При СД мощный инфекционный процесс может стать предпосылкой для быстрого развития пиогенной инфекции. Пациенты с СД склонны к развитию редко диагностируемого интерстициального нефрита необычной формы – нефрита, вызываемого газообразующими микроорганизмами и сопровождающегося высоким уровнем смертности (эмфизематозный пиелонефрит). Гистологически он характеризуется острой пиогенной инфильтрацией с формированием микроабсцессов и высоким риском развития в дальнейшем острой почечной недостаточности (ОПН). Путь проникновения этих микроорганизмов может быть гематогенным. Даже в отсутствие препятствий оттоку мочи острая инфекция в паренхиме способна незаметно прогрессировать до развития внутрипочечного абсцесса, с распространением на околопочечную клетчатку. Следует особо отметить, что эмфизематозная инфекция урологического тракта встречаются почти всегда и только среди больных СД [13], и является жизнеугрожающим состоянием, смертность при этой форме достигает 90% [26].
Трудности в выявлении ОП при СД возникают в связи с отсутствием ярко выраженных локальных симптомов, и отчасти маскированием клинической картины ОП тяжелыми проявлениями диабета. Стертость болевого синдрома у больных с длительно декомпенсированным СД и лихорадкой неясного генеза, при отсутствии изменений в анализах мочи, является основанием для урологического обследования с целью исключения ОП [27]. У больных с СД наличие ОП может быть не установлено при нормальном клеточном составе мочи, отсутствии бактериурии, протеинурии. Подобная сложная ситуация может наблюдаться при апостематозном пиелонефрите, карбункуле и абсцессе без дренирования гнойного экссудата в чашечно-лоханочную систему. Поэтому, необходимо использовать все имеющиеся в наличии у врача лабораторные возможности и современные лучевые методы исследования (ЛМИ) для своевременной постановки диагноза.
Традиционно диагностика ОП базируется на учете результатов комплексного обследования, включающего данные анамнеза, клинической картины заболевания, лабораторных и лучевых методов исследования. Положение с диагностикой ОП значительно улучшилось с появлением новых высокотехнологичных диагностических средств, таких как ультразвуковое исследование (УЗИ) и мульти-спиральная компьютерная томография (МСКТ). Эти методы изменили представление о возможностях диагностики воспалительных заболеваний почек. Установлено, что ранней лучевой диагностике гнойных форм ОП при СД принадлежит основная роль в распознавании патологического процесса, а также в установлении стадии и формы заболевания, в динамическом наблюдении при консервативной терапии и мониторинге состояния органов (почек и окружающих тканей) [28].
Среди лучевых методов УЗИ на сегодняшний день является наиболее доступным, информативным и экономически оправданным методом диагностики ОП. К недостаткам ультрасонографии относится невозможность оценки выделительной функции почек [29]. УЗИ и допплерографическое исследование (ДГИ) более информативны по сравнению с экскреторной урографией (ЭУ) в оценке состояния почечной паренхимы. Эти методы позволяют оценивать глубину и степень деструкции, дифференцировать диффузное поражение от фокального, а также регистрировать распространение воспалительного процесса в ретроперитонеальную область [30, 31, 32]. ДГИ в диагностике ОП дает информацию о структурно-функциональном состоянии кровотока в почках и эласто-тонических свойствах сосудов [33]. Поскольку нарушения гемодинамики являются одним из ведущих звеньев патогенеза ОП, то получение сведений об изменении основных показателей этого процесса во многом позволяет определить тяжесть патологических изменений, от которых зависит время и вид лечебных мероприятий.
МСКТ обладает несомненными преимуществами перед другими методами визуализации в оценке глубины и распространенности воспалительного процесса в почке и в перинефральных тканях [34, 35]. МСКТ с контрастированием является современным объективным методом исследования и ранней диагностики ОП у больных с СД, способствующим четкой визуализации патологического процесса и дифференцированию различных форм ОП. МСКТ обладает более высокой контрастной чувствительностью, что дает возможность выявлять структурные изменения почечной паренхимы [36].
МСКТ с контрастированием является современным объективным методом исследования и ранней диагностики ОП у больных с СД, способствующим четкой визуализации патологического процесса и дифференцированию различных форм ОП. МСКТ обладает более высокой контрастной чувствительностью, что дает возможность выявлять структурные изменения почечной паренхимы [36].
В получении необходимой информации о характере патологического процесса ЛМИ дополняют друг друга. Это обстоятельство благоприятствует своевременному выбору лечебной тактики, уменьшению количества необратимых поражений почек у больных СД. Для профилактики развития данного состояния необходимо постоянно мониторировать течение инфекционного процесса. Так, в остром периоде выполнение УЗИ и ДГИ почек должно выполняться до двух раз в день.
Особенности лечения острых воспалительных заболеваний почек у больных сахарным диабетом
Назначение антибактериальной терапии при ОП следует обязательно проводить одновременно с коррекцией сахароснижающей терапии для снижения уровня гликемии максимально близко к предполагаемым индивидуальным целевым значениям. Пациентов с СД 2, находящихся в режиме диетотерапии или принимающих пероральные сахароснижающие препараты, следует немедленно перевести на инсулинотерапию с полной отменой таблетированных гипогликемизирующих препаратов и в дальнейшем, до разрешения ситуации, вести как хирургических больных.
Антибактериальная терапия ОП должна начинаться без промедления. Эмпирическая терапия подразумевает выбор антибиотиков, которые являются активными в отношении наиболее частых возбудителей этого вида инфекций. Согласно рекомендациям Европейской ассоциацией урологов (2008) по лечению инфекций мочевых путей, у пациентов с пиелонефритом в стадии гнойного воспаления рекомендуется терапия фторхинолонами, аминопенициллинами с ингибиторами β-лактамаз, цефалоспоринами II–III поколения и аминогликозидами. Однако известно, что применение аминогликозидов у пациентов с СД, в связи с их выраженной нефротоксичностью, возможно только в исключительных случаях и под тщательным контролем функции почек.
Особое место в лечении ОП занимают карбопенемы. По данным Европейской Ассоциации Урологов (2008) данная группа препаратов обладает сверхшироким спектром действия: активны в отношении большинства грамположительных, грамотрицательных и анаэробных микроорганизмов. Поэтому они являются препаратами второго ряда при лечении тяжелых форм воспалительных процессов мочевыводящих путей. По нашему мнению, при развитии ОП у больных с СД, в отдельных случаях, карбопенемы могут применяться и как препараты первого ряда.
Объем антибактериальной терапии подбирается с учетом формы воспалительного процесса и тяжести нарушения углеводного обмена. Функциональное состояние почек оценивается по уровню креатинина и мочевины крови, от которых зависят суточные дозы антибактериальных препаратов.
Согласно мнению отечественных и зарубежных специалистов, ОП следует рассматривать как острое хирургическое заболевание, при котором в большинстве случаев больные подлежат оперативному вмешательству на почке [5, 22, 33]. Ухудшение клинической картины заболевания, отсутствие положительной динамики в показателях гликемии, повышение количества лейкоцитов крови, нейтрофильный сдвиг влево в процессе проводимой интенсивной терапии свидетельствуют о неадекватности лечения и необходимости хирургического вмешательства. Считается приоритетным выполнение органосохраняющих операций с ликвидацией гнойно-деструктивных очагов. В то же время, многие авторы указывают на необходимость выполнения у больных с СД сразу органоуносящей операции при первичном гнойном пиелонефрите, мотивируя это меньшим риском развития септических осложнений и летального исхода. Так, по данным ряда авторов послеоперационная летальность при ОП у больных СД достигает 28,7% [13, 37].
При незначительной положительной динамике после 2–3 дней активного лечения, или в случаях развития рецидива в период 2-х недель после окончания терапии, показано повторное исследование мочи с определением чувствительности флоры к антибиотикам и дополнительным УЗИ почек. Если возбудитель мало- или не чувствителен к применяемому антибактериальному препарату, показано продолжение интенсивного курса терапии в течение 10–14 суток со сменой препаратов.
Если возбудитель мало- или не чувствителен к применяемому антибактериальному препарату, показано продолжение интенсивного курса терапии в течение 10–14 суток со сменой препаратов.
Если при повторном бактериальном исследовании мочи с определением чувствительности к антибиотикам установлено, что рецидив вызван тем же патогенным микроорганизмом, что и первичный эпизод инфекции, то для полного выздоровления обычно требуется 6-недельный курс терапии.
Особый интерес представляют сообщения о том, что даже в некоторых случаях гнойных форм ОП возможно успешное лечение консервативными методами, при условии своевременной диагностики и раннего начала терапии. Так, Coelho R.F. et al. (2007 г.) были проанализированы 65 случаев гнойного ОП. Изолированные абсцессы почек наблюдали у 24,6% пациентов; у остальных было сочетание абцессов почки и паранефрия. Предрасполагающим фактором развития гнойного пиелонефрита чаще всего был СД (28%). Многие больные были госпитализированы с уже запущенным гнойно-деструктивным процессом в почках, о чем свидетельствуют положительные результаты бактериального исследования крови у 40% больных, тем не менее 60% пациентов с сочетанными абсцессами были пролечены традиционными хирургическими методами, а 73% больных с изолированными почечными абсцессами были излечены консервативно. Был сделан важный вывод, что комбинированные абсцессы почки и паранефрия подлежат обязательному оперативному лечению, а мелкие отграниченные абсцессы почки могут быть разрешены одним консервативным лечением [38]. При наблюдении таких больных в отдаленном периоде, по результатам лучевых методов, не отмечали развития участков нефросклероза и необратимых рубцовых изменений в почках, что подтверждено также данными литературы [39, 40, 41].
Согласно нашему опыту, консервативная терапия больных с гнойными формами пиелонефрита на фоне СД, вполне возможна, при своевременной правильной диагностике, адекватной комбинированной терапии, с использованием мощных современных химиопрепаратов и обязательным ежечасным контролем уровня гликемии (on-line контроль при использовании СGMS). В этой ситуации имеется высокий шанс не только достижения стойкой положительной динамики, но и в возможности избежать хирургического вмешательства. Однако на фоне субкомпенсированного или декомпенсированного СД, а также уже имеющихся микро- и макрососудистых осложнений, период разрешения гнойных форм ОП может быть дольше, чем у пациентов без СД. В этом случае очень важна длительная антибиотикотерапия с комплексом мер по коррекции и стабилизации углеводного обмена и имеющихся осложнений СД.
В этой ситуации имеется высокий шанс не только достижения стойкой положительной динамики, но и в возможности избежать хирургического вмешательства. Однако на фоне субкомпенсированного или декомпенсированного СД, а также уже имеющихся микро- и макрососудистых осложнений, период разрешения гнойных форм ОП может быть дольше, чем у пациентов без СД. В этом случае очень важна длительная антибиотикотерапия с комплексом мер по коррекции и стабилизации углеводного обмена и имеющихся осложнений СД.
Основными возбудителями инфекции при пиелонефрите являются бактерии, однако определенная роль может принадлежать и грибкам. При развитии пиелонефрита на фоне СД имеется высокий риск развития кандидоза мочевой системы. Патогенные свойства Candida alb., обусловливающие поражение различных органов, включая мочевые пути, проявляются только при существенном ослаблении иммунологической защиты. В структуре возбудителей из грибковых разновидностей у больных, страдающих поражением мочевых путей, в 50% вызвано Candida alb. [42], и может достигать 32,5% из числа всех разновидностей возбудителей ОП [43].
Кандидозный пиелонефрит, как правило, развивается гематогенно на фоне системного кандидоза у больных, длительно получавших антибиотики или иммуносупрессивные препараты, а также при онкозаболеваниях или СД. Гораздо реже отмечается восходящий путь инфекции, к которому предрасполагают аномалии мочевых путей, длительная их катетеризация. Гематогенный кандидозный пиелонефрит отмечается с одинаковой частотой у мужчин и женщин, а восходящий грибковый пиелонефрит диагностируется преимущественно у женщин. Его развитию часто предшествует наличие кандидозного цистита, уретрита. Однако диагностические критерии этих состояний, в отличие от бактериальной ИМП, разработаны недостаточно. Считается, что обнаружение в 1 мл средней порции мочи 10–15 тыс. колоний Candida свидетельствует о грибковом поражении мочевыводящих путей.
При лечении кандидозной инфекции у больных СД необходимо учитывать следующие особенности [44]:
при осложнениях СД, нарушении обменных процессов, и наличии многочисленных сопутствующих заболеваний у большинства больных, особенно у лиц пожилого возраста, предпочтителен толерантный противогрибковый препарат, высокоэффективный и без токсических побочных действий, как например, флуконазол и др.
 ;
;при длительном хроническом течении заболевания и, как правило, вялотекущем процессе, требуется применять продолжительную схему лечения в адекватных разовых и курсовых дозах;
после проведения основного курса лечения больной должен оставаться на диспансерном учете, при этом не исключаются профилактические курсы лечения системными и местными антимикотиками.
Известно, что длительное течение ХП при СД приводит к нефросклерозу. Его развитие у пациентов, перенесших ОП, зависит от многих факторов: объема повреждения почки, длительности процесса, сопутствующей патологии. В исследованиях Европейской Ассоциации Урологов (2006) показано, что у 55% прежде здоровых пациентов, в дальнейшем перенесших ОП, выявляется повреждение паренхимы. При повторном обследовании через 3–6 месяцев эти повреждения сохранялись у 77% больных. В целом, исходом необструктивного ОП может стать формирование рубцов паренхимы (локального нефросклероза), визуализируемых современными методами диагностики. Тем не менее, эти рубцы не приводят к развитию хронической почечной недостаточности.
Таким образом, с целью профилактики инфекционно-воспалительных заболеваний почек, скрининг ИМП при СД должен проводиться ежегодно. Данные отечественных и зарубежных исследователей по распространенности, этиологии, патогенезу, лечению и клинической значимости ИМП, в том числе, течению пиелонефрита при СД, свидетельствуют о важности изучения данной проблемы. Особое внимание должно быть уделено исследованию механизмов развития инфекционно-воспалительных заболеваний мочеполовых органов и мочевыводящих путей у больных СД, с разработкой новых профилактических и лечебных алгоритмов, что, безусловно, позволит не только продлить жизнь пациенту с СД, но и значительно повысить ее качество.
1. Сунцов Ю.И., Дедов И. И., Шестакова М.В. Скрининг осложнений СД как метод оценки качества лечебной помощи больным. Москва. 2008.
И., Шестакова М.В. Скрининг осложнений СД как метод оценки качества лечебной помощи больным. Москва. 2008.
2. Levison M.E., Pitsakis P.G. Effect of insulin treatment on the susceptibility of the diabetic rat to Escherichia соli-induced pyelonephritis. J. Infect Dis 1984; 150:554-60.
3. Шамхалова М.Ш., Чугунова Л.А. Инфекции мочевых путей у больных сахарным диабетом: диагностика, профилактика, лечение. // Сахарный диабет. — 2001. — № 3 (12), с. 24-29.
4. Светлова Г.Н. Диабетическая периферическая сенсомоторная нейропатия у детей: роль клинико-метаболических и генетических факторов. Дис. канд. мед. наук. Москва. 2008.
5. Ludwig E. Urinary tract infections in diabetes mellitus // Orv Hetil. 2008 Mar 30;149(13):597-600.
6. Carton J.A., J.A. Maradona, F.J. Nuno, R. Fernandez-Alvarez, F. Perez- Gonzalez and V. Asensi. Diabetes mellitus and bacteraemia: a comparative study between diabetic and non-diabetic patients, Eur J Med 1 (1992), pp. 281-287.
7. Geerlings S.E., Stolk R.P., Camps M.J.L., Netten P.M., Hoekstra J.B.L., Bouter K.P., Bravenboer B., Collet T.J., Jansz A.R., Hoepelman I.M. Prevalence and risk factors for asymptomatic bacteriuria in women with diabetes mellitus. ICAAC 1999: abstr 607.
8. Хопельман А., Гирлингс С. Инфекции мочевыводящих путей при сахарном диабете// Клиническая микробная и антимикробная химиотерапия, 2000; № 2 — с. 40-45.
9. Лоран О.Б., Синякова Л.А., Косова И.В. Лечение и профикактика хронического рецидивирующего цистита у женщин. Consilium medicum, № 7, том 6, 2004.
Лоран О.Б., Синякова Л.А., Косова И.В. Лечение и профикактика хронического рецидивирующего цистита у женщин. Consilium medicum, № 7, том 6, 2004.
10. Pradidarcheep W. Lower urinary tract symptoms and its potential relation with late-onset hypogonadism. Aging Male. 2008 Jun;11 (2):51-5.
11. Hassan J.M., Pope JC., Revelo P., Adams MC., Brock J.W., Demarco R.T. The role of postoperative testosterone in repair of iatrogenic hypospadias in rabbits. J. Pediatr Urol. 2006 Aug;2 (4):329-32. Epub 2006 Apr. 27.
12. Salmi S., Santti R., Gustafsson JA., Ma..kela.. S. Co-localization of androgen receptor with estrogen receptor beta in the lower urinary tract of the male rat. J Urol. 2001 Aug;166 (2):674-7.
13. Лопаткин Н.А. Урология.// М.: Медицина. 1992.
14. Joshi N., G.M. Caputo, M.R. Weitekamp and A.W. Karchmer. Infections in patients with diabetes mellitus, N Engl J Med 341 (1999), p. 1906-1912.
15. Schranz D.B., Lenmark A. Immunology in diabetes: an update. Diabetes Metab. Rev. 1998; 14(1): 3-29.
16. Roberts J.A. Aetiology and pathophysiology of pyelonephritis // Am J Kidney Dis.- 1991.- Vol.17.- р.1-9.
17. Переверзев А.С. Особенности инфекций мочевых путей у пациентов с сахарным диабетом. Здоровье Украины. № 8, 2006.
18. Шестакова М.В., Северина А.С. Эндотелиальная дисфункция, система ангиогенеза и система гемостаза при сахарном диабете. Москва. 2005.
Шестакова М.В., Северина А.С. Эндотелиальная дисфункция, система ангиогенеза и система гемостаза при сахарном диабете. Москва. 2005.
19. Довлатян А.А., Касабов А.В. Острый пиелонефрит при сахарном диабете. Урология №6; 2003.
20. Мостофи Ф.И, Смит Д.Е. Почки. М.: Медицина. 1972.
21. Журавлев В.Н. Острый пиелонефрит. Материалы пленума правления Всероссийского общества урологов. Екатеринбург 15-18 октября 1996. Москва. 1996. С. 5-12.
22. Довлатян А.А. Лечение острого гнойного пиелонефрита у больных с сахарным диабетом. Тер. арх. 1993; 65 (6): 35-39.
23. Козлов В.А. Плазмоферез и плазмосорбция в лечении урологических больных.// Автореф. дисс. докт. мед. наук. М., 1989. С. 50.
24. Пытель Ю.А., Волкова В.С. Комплексная терапия с офлоксацином воспалительных урологических заболеваний. // Антибиотики и химиотерапия. — № 9, 1996.- C. 41.- C. 86-88.
25. Шулутко Б.И. Нефрология. Современное состояние проблемы. С-Петербург: Ренкор. 2002. С. 419.
26. Dutta P., Bhansali A, Singh SK, Gupta KL, Bhat MH, Masoodi SR, Kumar Y. Presentation and outcome of emphysematous renal tract disease in patients with diabetes mellitus. Urol Int 2007; 78(1): 13-22.
27. Hoepelman A. I., Meiland R, Geerlings SE. Pathogenesis and management of bacterial urinary tract infections in adult patients with diabetes mellitus. Int. J. Antimicrob Agents 2003; 22 (Suppl 2): 35-43.
Pathogenesis and management of bacterial urinary tract infections in adult patients with diabetes mellitus. Int. J. Antimicrob Agents 2003; 22 (Suppl 2): 35-43.
28. Курбатов Д.Г., Дубский С.А. Лучевые методы исследования в диагностике острого пиелонефрита. М.: Медпрактика — 2007.- 98 с.
29. Anne Paterson. Urinary tract infection: an update on imaging strategies.- Eur Radiol.- 2004.- Vol.14.- L.89-L.100.
30. Зубовский Г.А. Ультразвуковая диагностика и электропунктура М. 1992.- С. 133.
31. Хитрова А.Н., Митьков В.В. Ультразвуковое исследование почек. В кн.: Клиническое руководство по ультразвуковой диагностике // Ред. В.В.Митьков.- М.: 1996.- Т. 1.- С. 200-256.
32. Sakarya M.E., Arslan H., Erkoc R., et al. The role of power Doppler ultrasonography in the diagnosis of acute pyelonephritis // Br J Urol.-1998.- Vol.81.- № 3.- P. 360-363.
33. Игнашин Н.С., Сафаров Р.М., Ходырева Р.Л. и др. Диагностика острого пиелонефрита с применение лучевых методов// Здравоохранение Башкортостана. № 5.- 2001.- С. 97-101.
34. Goldman S.M., Fishman E.K. Upper urinary tract and MRI. // Semin Ultrasound CT MR.- 1991.-Vol.12.- P.335-360.
35. Kawashima A., LeRoy A.J. Radiologic evaluation of patients with renal infections// Infect Dis Clin North Am.- 2003.- Vol.17.- № 2.- P.433-456. Review.
36. Дубский С.А. Лучевые методы исследования в ранней диагностике острого пиелонефрита. Дисс. канд. мед. наук. Москва., 2005.
37. Астахов Ю.И. Плазмоферез в комплексном лечении пиелонефрита, осложненного уросепсисом гнойной интоксикации//Автореф. дисс. канд. мед. наук. Барнаул. 1993.- С.21.
38. Coelho RF et al. Renal and perinephric abscesses: analysis of 65 consecutive cases.World journal of surgery 2007 Feb; 31(2):431-6.
39. Hoddick W., Jeffrey R.B.- Goldberg H.l. et al. CT and sonography of severe renal and perirenal infections // Am. J. Roentg.-1983.- Vol. 140.- № 3.- р. 517-520.
40. Hoffman E.P., Mindelzun R.E., Anderson R.U. Computed tomography in acute pyelonephritis associated with diabetes.// Radiology.- 1980.- Vol. 135.- № 3.- р. 691-695.
41. Hricak H., Cruz C., Romanski R. et al. Renal parenchymal disease: sonographic histologic correlation // Radiology — 1982. — Vol. 144. — P. 141-146.
42. Willis A.M., et al. The influence of antifungal drugs on virulence properties of Candida alb. in patient with diabetes mellitus.// Oral Surg. Med. — 2001-№91(3).-p.317-321.
43. Бурова С.А. Проблемы грибковых заболеваний человека. // Российский журнал кожных и венерологических болезней № 1 — 1998; С. 39-41.
44. Penk A., Pittrow L. Therapeutic experience with fluconazole in the treatment of fungal infections in diabetic patients. // Mycoses. -1999-№ 42 Suppl.2-p.97-100.
Пиелонефрит
У здорового человека моча стерильна, но бактерии способны проникать в мочевые пути из близко расположенных органов (кишечника, половых органов) восходящим путем (через мочеиспускательный канал, мочевой пузырь и мочеточники), а также через лимфатическую и кровеносную систему, и размножаться в мочевой системе. Пиелонефрит также развивается в тех случаях, когда нарушается отток мочи из почки.Пиелонефритом может заболеть человек любого возраста, но чаще им болеют дети до 7 лет, женщины 18-30 лет, у которых появление пиелонефрита связано с началом половой жизни, беременностью или родами, и пожилые мужчины, страдающие аденомой простаты, простатитом или уретритом. Также одной из наиболее частых причин пиелонефрита является мочекаменная болезнь с частыми почечными коликами.
Вероятность развития пиелонефрита возрастает при снижении общего иммунитета организма, сахарном диабете, туберкулезе, гиповитаминозе и хронических воспалительных заболеваниях.
Пиелонефрит может быть острым и хроническим.
При остром пиелонефрите внезапно, резко повышается температура до 39-40оС, появляются слабость, озноб, головная боль, обильное потоотделение, возможны тошнота и рвота. Одновременно с температурой появляются боли в пояснице, как правило, с одной стороны. Боли носят тупой характер, но интенсивность их может быть различная.
Если заболевание развивается на фоне мочекаменной болезни, то атаке пиелонефрита обычно предшествует приступ почечной колики.
При отсутствии лечения заболевание либо переходит в хроническую форму, либо развиваются нагноительные процессы почки, которые проявляются ухудшением состояния человека и резкими скачками температуры (от 35-36оС утром до 40-41оС вечером).
Хронический пиелонефрит, как правило, является следствием недолеченного острого пиелонефрита, когда острое воспаление снято, но не удалось полностью уничтожить всех возбудителей в почке или восстановить нормальный отток мочи из почки.
Хронический пиелонефрит может постоянно беспокоить тупыми ноющими болями в пояснице, особенно в сырую холодную погоду. В некоторых случаях он приводит к стойкому повышению артериального давления. Кроме того, хронический пиелонефрит время от времени обостряется, и тогда у человека появляются все признаки острого процесса.
Диагноз
Проблема диагностики пиелонефрита заключается в том, что симптомы этого заболевания сходны с симптомами других заболеваний, связанных с воспалением мочевыводящих путей. Поэтому необходимо обращение к квалифицированному врачу-урологу.
Проводятся анализы крови, мочи, а также дополнительные исследования: УЗИ почек, рентгеновские исследования с использованием контрастных веществ. Чтобы определить вид инфекции необходимо сделать бактериологический посев пробы мочи и ПЦР-анализ на инфекции, а для исключения опухолевых процессов используют метод компьютерной томографии.
Лечение
Для лечения пиелонефрита применяют лекарственные методы, однако в тяжелых случаях, при запущенном заболевании дело может дойти и до хирургического лечения.
Профилактика
Профилактика пиелонефрита заключается, прежде всего, в том, чтобы вылечить заболевание, которое может привести к его развитию, как, например, мочекаменная болезнь и аденома простаты, а также любые заболевания, сопровождающиеся нарушением оттока мочи из почки.
Беременным женщинам необходимо не реже 1 раза в месяц проводить бактериологический анализ мочи.
Хронический пиелонефрит — заболевания мочеполовой системы
Общий анализ мочи и посев мочи
Хронический пиелонефрит подозревается у пациентов с рецидивирующими инфекциями мочевыводящих путей (ИМП) и острым пиелонефритом в анамнезе. Однако у большинства пациентов, за исключением детей с пузырно-мочеточниковым рефлюксом (ПМР), такого анамнеза нет. Иногда диагноз подозревают, потому что типичные результаты случайно отмечаются при визуализирующем исследовании.Симптомы, поскольку они нечеткие и неспецифические, могут не указывать на диагноз.
Общий анализ мочи, посев мочи и обычно визуализирующие исследования. Осадок в моче обычно скудный, но присутствуют почечные эпителиальные клетки, зернистые цилиндры и, иногда, цилиндры лейкоцитов (WBC). Протеинурия присутствует почти всегда и может находиться в нефротическом диапазоне, если ПМР вызывает обширное поражение почек. Когда поражены обе почки, дефекты концентрирующей способности и гиперхлоремический ацидоз могут появиться до того, как наступит значительная азотемия.Посев мочи может быть стерильным или положительным, обычно на грамотрицательные микроорганизмы.
Первоначальная визуализация обычно выполняется с помощью УЗИ, спиральной компьютерной томографии или внутривенной урографии (ВВУ). Отличительным признаком хронического пиелонефрита (обычно с рефлюксом или обструкцией) при визуализации обычно является большой, глубокий, сегментарный, грубый кортикальный рубец, обычно доходящий до одной или нескольких почечных чашечек. Верхний полюс — наиболее частое место. Почечная кора утрачивается, а паренхима почек истончается. Вовлеченная почечная ткань может локально гипертрофироваться с сегментарным увеличением.Может присутствовать расширение мочеточника, отражающее изменения, вызванные хроническим тяжелым рефлюксом. Подобные изменения могут возникнуть при туберкулезе мочевыводящих путей.
В XPN в посевах мочи почти всегда вырастают P. mirabilis или E. coli . КТ выполняется для обнаружения камней или других препятствий. Визуализация показывает бессосудистую массу с различной степенью распространения вокруг почки. Иногда для дифференциации рака (например, почечно-клеточного рака) может потребоваться биопсия или исследование ткани, удаленной во время нефрэктомии.
Левофлоксацин по сравнению с цефтриаксоном для лечения острого пиелонефрита у иранских взрослых
Название: Левофлоксацин в сравнении с цефтриаксоном для лечения острого пиелонефрита у взрослых иранцев
ОБЪЕМ: 20
Автор (ы): Шабнам Тегерани, Ферештех Эльяси и Сара Аболгасеми *
Место работы: Исследовательский центр инфекционных болезней и тропической медицины, Университет медицинских наук Шахида Бехешти, Тегеран, Исследовательский центр инфекционных болезней и тропической медицины, Университет медицинских наук Шахида Бехешти, Тегеран, Исследовательский центр инфекционных болезней и тропической медицины, Университет Шахида Бехешти наук, Тегеран
Ключевые слова: Острый пиелонефрит, инфекции мочевыводящих путей, левофлоксацин, цефтриаксон.
Резюме: Введение: Острый пиелонефрит — одна из самых распространенных бактериальных инфекций. Варианты начального лечения пиелонефрита включают цефалоспорин расширенного спектра действия или фторхинолон. В этом исследовании мы стремились сравнить клинические результаты пациентов, получавших цефтриаксон, с теми, кто получал левофлоксацин для лечения острого пиелонфрита.
Методы. В этом рандомизированном открытом исследовании госпитализированных взрослых с острым пиелонефритом лечили цефтриаксоном (1 г внутривенно каждые 12 часов) или левофлоксацином (750 мг внутривенно ежедневно) в течение как минимум 7 дней.Клинические и микробиологические характеристики сравнивались у пациентов, получавших цефтриаксон и левофлоксацин.
Результаты. Всего было рандомизировано 59 пациентов: 30 — в группу цефтриаксона и 29 — в группу левофлоксацина. Клинический ответ у 68,0% пациентов в группе цефтриаксона и 56,0% пациентов в группе левофлоксацина был излечен. Микробиологический ответ (уровень эрадикации патогенов) составил 68,7% в группе цефтриаксона и 21,4% в группе левофлоксацина.(Значение P = 0,00028) Escherichia coli была наиболее частым патогеном (n = 31), за ней следовали Klebsiella pneumoniae (n = 21). Высокие показатели устойчивости были обнаружены к котримоксазолу (55%), ципрофлоксацину (48%) и цефтриаксону (34,4%) изолированной кишечной палочки. Точно так же все изоляты K. pneumoniae были устойчивы к ципрофлоксацину.
Выводы. Наше исследование показывает, что цефтриаксон был более эффективным, чем левофлоксацин, в лечении острого пиелонфрита на основании микробиологического ответа, но не было статистически значимых различий между группами лечения в скорости клинического излечения.Устойчивость уропатогенов к наиболее часто используемым антибиотикам была относительно высокой. Выбор схемы лечения на основе результатов тестирования чувствительности и сокращение продолжительности терапии в настоящее время рекомендуются как наиболее важные подходы к снижению распространения устойчивости к антибиотикам во всем мире.
Пиелонефрит у мелких животных — Мочевыделительная система
Инфекция почек (пиелонефрит) обычно возникает из-за восходящих бактерий, хотя возможно гематогенное распространение.Организмы и предрасполагающие причины аналогичны бактериальному циститу. Ренолиты и уретеролиты, которые препятствуют нормальному оттоку мочи из почечной лоханки, могут способствовать этому. Животные, подверженные риску развития пиелонефрита, — это очень молодые, очень старые, с ослабленным иммунитетом или с недостаточной способностью концентрировать мочу. Во многих случаях основная причина не идентифицирована. Факторы вирулентности, связанные с конкретными бактериальными штаммами, играют роль в обеспечении колонизации уротелия, особенно при пиелонефрите, вызванном Escherichia coli .Тот факт, что пиелонефрит обычно восходящий и двусторонний, предполагает, что эти факторы вирулентности более важны, чем считалось ранее.
Животные с острым пиелонефритом могут проявлять боль в почках или в боку, лихорадку, недомогание, а иногда и рвоту, полиурию и полидипсию. Анализ мочи показывает протеинурию, пиурию, бактериурию и / или гематурию. В свежем осадке мочи могут присутствовать цилиндры лейкоцитов. Посев мочи обычно положительный; общий анализ крови может показать лейкоцитоз со сдвигом влево.Биохимический профиль может быть нормальным или показывать азотемию (преренальную или почечную) и / или гиперглобулинемию. У животного может быть почечная недостаточность. Хронический пиелонефрит распознать труднее, поскольку клинические признаки могут быть незаметными или отсутствовать. Часто наблюдаются полиурия и полидипсия. Во многих случаях болезнь остается нераспознанной до тех пор, пока не возникает почечная недостаточность. Хотя аномалии в анализе мочи присутствуют, они часто менее драматичны, чем при острой почечной инфекции. Единичный посев мочи может быть отрицательным, если количество бактерий низкое.Другие полезные диагностические тесты включают ультразвуковое исследование брюшной полости и внутривенную пиелографию. Оба исследования могут показать расширение одной или обеих почечных лоханок, вторичное по отношению к воспалению и частичной непроходимости. Асимметричный размер почек и архитектурные изменения с расширением лоханки почек с большой вероятностью указывают на хронический пиелонефрит. В некоторых случаях нефропиелоцентез под контролем УЗИ полезен для получения образца мочи из расширенной почечной лоханки для анализа и посева.
Пиелонефрит следует агрессивно лечить антибиотиками широкого спектра действия на основе посева мочи и анализа на чувствительность к противомикробным препаратам в течение 4–8 недель.Инфекция может реагировать на те же антибиотики, которые рекомендованы для лечения цистита, но показаны более частые приемы (например, амоксициллин трижды, а не два раза в день) и / или более высокие дозировки. Часто эффективны фторхинолон или комбинация фторхинолона с β-лактамным антибиотиком. Дозировки должны быть такими же, как и при других инфекциях мягких тканей. Животных с лихорадкой, анорексией, обезвоживанием или азотемией следует госпитализировать для внутривенного введения антибиотиков и инфузионной терапии. Инфузионная терапия может предотвратить прогрессирование острого пиелонефрита в острое азотемическое повреждение почек и улучшить перфузию почек и улучшить уремические признаки у животных, уже страдающих уремией.У животных с острым пиелонефритом может восстановиться нормальная функция почек в зависимости от степени повреждения, нанесенного до лечения. В случаях хронического пиелонефрита с сильно гидронефротической нефункциональной почкой после стабилизации состояния животного методом выбора может быть нефрэктомия. Это устранит источник инфекции и, возможно, спасет противоположную почку. Внутривенная пиелография и / или сцинтиграфия почек полезны для оценки относительной функции каждой почки. Если обе почки серьезно поражены, единственной альтернативой является лечение.Во многих случаях возможно восстановление хронической стабильной почечной недостаточности.
Посев мочи следует производить в течение первых 5–7 дней терапии для оценки эффективности антибиотиков. Анализ мочи и посев следует повторять через 3–7 дней после терапии, а затем ежемесячно в течение 3 месяцев подряд. Если все эти посевы отрицательны, интервал между посевами мочи может постепенно увеличиваться. Животные с пиелонефритом подвержены высокому риску сохранения или рецидива инфекции, а также вторичных инфекций на других участках (например, бактериального эндокардита и дискоспондилита).
% PDF-1.7 % 65 0 объект > эндобдж xref 65 92 0000000016 00000 н. 0000002973 00000 н. 0000003090 00000 н. 0000003651 00000 п. 0000003779 00000 п. 0000003805 00000 н. 0000004406 00000 н. 0000005116 00000 п. 0000005824 00000 н. 0000006449 00000 н. 0000006873 00000 н. 0000006984 00000 н. 0000007097 00000 п. 0000007747 00000 н. 0000008207 00000 н. 0000009417 00000 н. 0000009637 00000 н. 0000010574 00000 п. 0000010788 00000 п. 0000011417 00000 п. 0000011965 00000 п. 0000012424 00000 п. 0000012678 00000 п. 0000013624 00000 п. 0000014264 00000 п. 0000014741 00000 п. 0000015034 00000 п. 0000015624 00000 п. 0000016671 00000 п. 0000017527 00000 п. 0000017654 00000 п. 0000017925 00000 п. 0000018197 00000 п. 0000018794 00000 п. 0000019104 00000 п. 0000019130 00000 п. 0000019326 00000 п. 0000019688 00000 п. 0000020187 00000 п. 0000021091 00000 п. 0000021752 00000 п. 0000022104 00000 п. 0000022643 00000 п. 0000023278 00000 п. 0000024676 00000 п. 0000025632 00000 п. 0000029458 00000 п. 0000029528 00000 п. 0000029813 00000 п. 0000029983 00000 н. 0000033537 00000 п. 0000033794 00000 п. 0000058761 00000 п. 0000058850 00000 п. 0000066971 00000 п. 0000067041 00000 п. 0000075080 00000 п. 0000075341 00000 п. 0000079878 00000 п. 0000084388 00000 п. 0000084469 00000 п. 0000084498 00000 п. 0000084624 00000 п. 0000084721 00000 п. 0000084867 00000 п. 0000085121 00000 п. 0000087898 00000 п. 0000088322 00000 п. 0000088833 00000 п. 0000089134 00000 п. 0000092477 00000 п. 0000092960 00000 п. 0000093523 00000 п. 0000093630 00000 н. 0000094652 00000 п. 0000094965 00000 п. 0000095322 00000 п. 0000095431 00000 п. 0000096358 00000 п. 0000096670 00000 п. 0000097026 00000 п. 0000097190 00000 п. 0000099205 00000 н. 0000099587 00000 н. 0000100002 00000 н. 0000100175 00000 н. 0000102458 00000 н. 0000102852 00000 н. 0000103267 00000 н. 0000120543 00000 н. 0000123127 00000 н. 0000002136 00000 п. трейлер ] / Назад 457299 >> startxref 0 %% EOF 156 0 объект > поток hb«b`8 P Ȁ
Инфекция почек (пиелонефрит); Симптомы, лечение, профилактика
Обзор
Что такое инфекция почек (пиелонефрит)?
Инфекция мочевыводящих путей может поражать нижние пути, особенно мочевой пузырь (цистит), простату (простатит) или верхние отделы и почки (пиелонефрит).Обычно это бактериальная инфекция. Заболевание встречается примерно у трех-семи из каждых 10 000 человек в Соединенных Штатах. Возникновение у беременных составляет около 2 процентов. Это легко поддается лечению, если диагностировано на ранней стадии.
Бактерия кишечной палочки (кишечная палочка) вызывает около 90 процентов инфекций почек. Бактерии мигрируют из половых органов через уретру (трубку, по которой моча выводится из организма) в мочевой пузырь и вверх по трубкам (мочеточникам), соединяющим мочевой пузырь с почками.
Некоторые бактерии, например стафилококковые инфекции, могут попадать в почки с кровотоком.
Симптомы и причины
Каковы причины инфекций почек (пиелонефрита)?
Обычно бактерии выводятся с потоком мочи.Однако несколько проблем могут увеличить риск почечной инфекции. Эти проблемы могут включать:
- Структурные аномалии (стриктуры, стенты, камни, хирургическое вмешательство), блокирующие отток мочи.
- Увеличенная предстательная железа (доброкачественная гиперплазия предстательной железы), сдавливающая уретру.
- Обратный поток (рефлюкс) мочи из мочевого пузыря в почки.
- Если ваша иммунная система затронута (низкое количество лейкоцитов, прием некоторых лекарств, ВИЧ, рак, трансплантация органов).
- Беременность, во время которой увеличивающаяся матка может сдавливать мочеточники и уменьшать отток мочи, позволяя бактериям мигрировать в почки.
- Неконтролируемый сахарный диабет.
Каковы симптомы почечной инфекции?
Ряд симптомов могут указывать вашему врачу на то, что у вас может быть почечная инфекция. Чем серьезнее симптомы, тем больше вероятность заражения почки. Симптомы инфекции почек включают:
- Внезапное начало озноба
- Температура выше 100 градусов по Фаренгейту
- Боль в паху, пояснице или боку
- Тошнота
- Рвота
- Спазм мышц живота
Более общие симптомы инфекции верхних отделов почек включают:
- Покрасневшая или покрасневшая кожа
- Болезненное мочеиспускание
- Повышенное мочеиспускание
- Непродуктивные попытки помочиться, несмотря на чувство крайней необходимости
- Общие недомогания
- Мутная моча
- Моча ненормального цвета
- Кровь в моче
- Моча с неприятным запахом
Если у вас возникнут какие-либо из этих внезапных симптомов, обратитесь за медицинской помощью.
Диагностика и тесты
Как диагностируется инфекция почек (пиелонефрит)?
Два общих лабораторных теста выполняются для диагностики почечных инфекций (пиелонефрита). Образец мочи исследуют под микроскопом, чтобы определить, присутствуют ли белые и / или эритроциты.Мочу также отправляют в лабораторию, чтобы проверить, не растут ли бактерии в посеве мочи. Если человек очень болен, ему также могут быть отправлены посевы крови. Штамм культивируемых бактерий будет определять тип терапии, используемой в вашем лечении.
Пиелонефрит часто можно лечить без рентгеновских исследований, если только ваш врач не подозревает, что это может быть дополнительная проблема. КТ-сканирование дает изображения структур и органов, и это сканирование обычно выполняется без контраста (красителя). Иногда для оценки может быть достаточно УЗИ почек.
Ведение и лечение
Как лечат инфекции почек (пиелонефрит)?
Врач лечит болезнь на основании своего осмотра. Он или она может начать стандартное лечение пациента курсом антибиотиков до того, как станут доступны результаты лабораторных анализов.Лекарство может измениться после того, как лабораторные тесты выявят точный штамм бактерий.
При эффективном лечении пациент должен чувствовать себя лучше через два-три дня. В противном случае ваш лечащий врач начнет искать дополнительные проблемы. Большинство курсов лечения антибиотиками длится 14 дней, и важно, чтобы пациенты принимали таблетки в соответствии с рекомендациями в течение полных 14 дней, даже если симптомы могут исчезнуть через несколько дней. Исчезновение симптомов не означает, что все бактерии погибают.Некоторые могут остаться, и инфекция может появиться снова.
Также существует опасение, что у оставшихся бактерий может развиться устойчивость к лекарству. По какой-то причине мужчинам сложнее лечить заболевание, и им, возможно, придется принимать лекарства до шести недель. Пациенты с тяжелым заболеванием, у которых наблюдается сильная тошнота и рвота, высокая температура, сильная боль и признаки обезвоживания, могут быть госпитализированы на несколько дней, пока антибиотики вводятся внутривенно.Образцы мочи берутся примерно через шесть недель после лечения и исследуются, чтобы гарантировать искоренение бактериальной инфекции.
Профилактика
Можно ли предотвратить инфекцию почек (пиелонефрит)?
Инфекции почек можно предотвратить, не допуская попадания бактерий в мочевыводящие пути и мочевой пузырь.Инфекции почек часто начинаются с инфекции нижних отделов мочевого пузыря. Предотвращая эти инфекции, вы можете предотвратить инфекции почек.
Есть несколько способов избежать заражения и сохранить здоровье почек. Эти советы могут включать:
- Гидратация: важно пить достаточное количество жидкости (не только воды) каждый день, но нет конкретных рекомендаций, применимых к каждому пациенту. Количество может измениться, если у вас есть определенные заболевания или вы живете в особенно жарком климате.Поговорите со своим врачом о рекомендуемом количестве воды, которое вам нужно каждый день.
- Полное мочеиспускание: когда вам нужно помочиться, полностью опорожните мочевой пузырь. Удерживание в моче может быть вредным и способствовать росту бактерий. Мочеиспускание каждые несколько часов может помочь вывести из организма любые бактерии и защитить его от инфекции.
- Мочеиспускание после полового акта: Мочеиспускание после полового акта помогает удалить любые бактерии, которые могли попасть в организм. И мужчины, и женщины должны делать это для предотвращения инфекций.
- Соблюдайте правила гигиены. Поддержание чистоты помогает защитить свое тело от инфекций. После дефекации протрите его спереди назад, чтобы отогнать бактерии от уретры (отверстия в теле). Это особенно важно для женщин.
Перспективы / Прогноз
Каковы прогнозы при инфекциях почек (пиелонефрите)?
При лечении прогноз почечных инфекций (пиелонефрита) очень положительный.Жизненно важно принимать все прописанные вам лекарства от инфекции. Вы можете почувствовать себя лучше вскоре после начала лечения, но при этом вам все равно нужно будет пройти весь прописанный курс лечения.
Внутривенная и пероральная антимикробная терапия острого пиелонефрита
По сравнению с внутривенным (IV) лечением пероральная антимикробная терапия сокращала время пребывания в стационаре пациентов с острым пиелонефритом, вызванным энтеробактериями, продуцирующими β-лактамазы (ESBL-PE) расширенного спектра действия.Согласно исследованию, опубликованному в Европейском журнале клинической микробиологии и инфекционных заболеваний , .
Это ретроспективное когортное исследование было разработано для определения эффективности пероральных противомикробных препаратов по сравнению со стандартом лечения острого пиелонефрита, вызванного БЛРС-ПЭ, с помощью внутривенных антимикробных препаратов.В когорту исследования вошли 238 пациентов, которые лечились в медицинском центре Samsung в Сеуле, Южная Корея, с января 2014 г. по декабрь 2016 г. Пациенты были разделены на 2 группы: пероральные антимикробные препараты (ОАТ), в которых пациенты получали соответствующие пероральные противомикробные препараты после терапии антибиотиками внутривенно <7 дней и только противомикробными препаратами внутривенно.
Исходные характеристики сравнивались с использованием данных из электронных медицинских карт. Первичной конечной точкой была общая неэффективность лечения, определяемая как микробиологическая и / или клиническая неэффективность.Микробиологическая неудача определялась как результаты посева крови и / или мочи, не становящиеся отрицательными в течение 7 дней, а клиническая неудача определялась как симптомы пациента, которые не исчезали в течение 7 дней или повторялись во время лечения. Успех лечения определялся как пациенты с клиническим выздоровлением от острого пиелонефрита без микробиологического наблюдения. Вторичными конечными точками были продолжительность пребывания в больнице, рецидивы в течение 2 месяцев и 1 года и побочные эффекты, связанные с лечением. Чтобы свести к минимуму систематическую ошибку, использовались сопоставление оценок предрасположенности и многомерное моделирование пропорциональных рисков Кокса.
Наиболее частым возбудителем был Escherichia coli (83,6%, 199/238) во всей когорте. Группа ОАТ включала 60 пациентов, получавших пероральную антимикробную терапию после 4-дневной соответствующей внутривенной терапии в среднем, а группа только внутривенного введения включала 178 пациентов. Эртапенем чаще всего назначали в группе только для внутривенного введения; пероральные фторхинолоны чаще всего использовались в группе ОАТ (76,4% и 58,3% соответственно), за ними следовали триметоприм-сульфаметоксазол и амоксициллин-клавуланат.Продолжительность госпитализации была короче примерно на 4,5 дня в группе ОАТ по сравнению с группой, получавшей только IV (6,15 дней против 10,65 дней; P <0,001). Риск неудачи лечения в группе ОАТ не был статистически выше, чем лечение только внутривенным введением (скорректированное отношение шансов [OR] 0,66; 95% ДИ, 0,18-24,3; P = 0,538). Через 2 месяца рецидив острого пиелонефрита, вызванного инфекцией ESBL-PE, также существенно не отличался между группами (скорректированное отношение рисков [HR] 0,56; 95% ДИ, 0.16-2.00; P = 0,366), и рецидив в течение 1 года также был аналогичен между группами OAT и IV (HR 0,78; 95% ДИ 0,35–1,77; P = 0,519).
Исследователипришли к выводу: «[Пероральные противомикробные препараты] можно использовать для лечения [острого пиелонефрита], вызванного инфекциями ESBL-PE, и сокращения продолжительности пребывания в больнице без неблагоприятных последствий для клинических исходов в качестве стратегии сохранения карбапенема». Кроме того, они подчеркнули, что результаты продемонстрировали, что более половины всех изолятов ESBL-PE из группы IV были чувствительны к пероральным антимикробным агентам, что еще раз доказывает, что пероральное лечение не уступает лечению IV.Исследователи также отметили, что необходимы дополнительные проспективные исследования на более широкой популяции, чтобы гарантировать эффективность и безопасность ОАТ при остром пиелонефрите, вызванном БЛРС-ПЭ.
Артикул
Ким Ш., Лим К. Р., Ли Х. и др. Клиническая эффективность пероральной антимикробной терапии острого пиелонефрита, вызванного энтеробактериями, продуцирующими β-лактамазы расширенного спектра действия [опубликовано в Интернете 13 сентября 2019 г.]. Eur J Clin Microbiol Infect Dis . DOI: 10.1007 / s10096-019-03705-w
| 1. | Shin J, Kim J, Wie SH, Cho YK, Lim SK, Shin SY и др. Устойчивость к фторхинолонам при неосложненном остром пиелонефрите: эпидемиология и клиническое влияние. Microb Drug Resist 2012; 18: 169–175. |
| 2. | Ли SJ, Ли Д.С., Чхве Х.С., Шим Б.С., Ким С.С., Ким М.Э. и др. Устойчивость к противомикробным препаратам при внебольничных инфекциях мочевыводящих путей: результаты Корейской системы мониторинга устойчивости к противомикробным препаратам.Журнал Infect Chemother 2011; 17: 440–446. |
| 3. | Всемирная организация здравоохранения. Отчет об инфекционных заболеваниях 2000 г .: преодоление устойчивости к противомикробным препаратам. Женева: Всемирная организация здравоохранения; 2000 г. |
| 4. | Центры по контролю и профилактике заболеваний. Профилактика возникающих инфекционных заболеваний [Интернет]. Атланта: Центры по контролю и профилактике заболеваний; c1998 [цитируется 2 сентября 2016 г.]. |
| 5. | Picozzi S, Ricci C, Gaeta M, Macchi A, Dinang E, Paola G и др. Действительно ли мы знаем о распространенности кишечной палочки с множественной лекарственной устойчивостью в территориальном и внутрибольничном населении? Урол Энн 2013; 5: 25–29. |
| 6. | Брионгос-Фигеро Л.С., Гомес-Травесо Т., Бачиллер-Луке П., Домингес-Хиль Гонсалес М., Гомес-Ньето А., Паласиос-Мартин Т. и др.Эпидемиология, факторы риска и коморбидность инфекций мочевыводящих путей, вызванных энтеробактериями, продуцирующими бета-лактамазы расширенного спектра (БЛРС). Int J Clin Pract 2012; 66: 891–896. |
| 7. | Лу П.Л., Лю Ю.С., Тох Х.С., Ли Ю.Л., Лю Ю.М., Хо СМ и др. Эпидемиология и профили чувствительности к антимикробным препаратам грамотрицательных бактерий, вызывающих инфекции мочевыводящих путей в Азиатско-Тихоокеанском регионе: результаты исследования по мониторингу тенденций устойчивости к противомикробным препаратам (SMART) за 2009-2010 гг.Int J Antimicrob Agents 2012; 40: S37 – S43. |
| 8. | Акдуман Б., Акдуман Д., Токгёз Х., Эрол Б., Тюркер Т., Айоглу Ф. и др. Длительное применение фторхинолона перед биопсией простаты может увеличить риск сепсиса, вызванного резистентными микроорганизмами. Урология 2011; 78: 250–255. |
| 9. | Picozzi SC, Casellato S, Rossini M, Paola G, Tejada M, Costa E и др.Положительная бета-лактамаза расширенного спектра действия Escherichia coli, вызывающая осложненную инфекцию верхних мочевых путей: уролог должен действовать вовремя. Урол Энн 2014; 6: 107–112. |
| 10. | Бойл Д.П., Zembower TR. Эпидемиология и борьба с новыми лекарственно-устойчивыми грамотрицательными бактериями: β-лактамазы расширенного спектра и другие. Урол Клин Норт Ам 2015; 42: 493–505. |
| 11. | van Nieuwkoop C, van’t Wout JW, Assendelft WJ, Elzevier HW, Leyten EM, Koster T., et al. Продолжительность лечения фебрильной инфекции мочевыводящих путей (исследование FUTIRST): рандомизированное плацебо-контролируемое многоцентровое исследование, сравнивающее короткое (7 дней) лечение антибиотиками с традиционным лечением (14 дней). BMC Infect Dis 2009; 9: 131. |
| 12. | Piddock LJ. Механизмы устойчивости к фторхинолонам: обновление 1994-1998 гг.Наркотики 1999; 58 Дополнение 2: 11–18. |
| 13. | Танака М., Онодера Ю., Учида Ю., Сато К., Хаякава И. Ингибирующая активность хинолонов против ДНК-гиразы и топоизомеразы IV, очищенной от Staphylococcus aureus. Противомикробные агенты Chemother 1997; 41: 2362–2366. |
| 14. | Navia MM, Ruiz J, Ribera A, de Anta MT, Vila J. Анализ механизмов устойчивости к хинолонам в клинических изолятах Citrobacter freundii.Журнал Antimicrob Chemother 1999; 44: 743–748. |
| 15. | Linde HJ, Schmidt M, Fuchs E, Reischl U, Niller HH, Lehn N. Активность шести хинолонов in vitro и механизмы устойчивости у Staphylococcus aureus и коагулазонегативных стафилококков. Противомикробные агенты Chemother 2001; 45: 1553–1557. |
| 16. | Burchall JJ, Elwell LP, Fling ME.Молекулярные механизмы устойчивости к триметоприму. Rev Infect Dis 1982; 4: 246–254. |
| 17. | Park H, Bradrick TD, Howell EE. Мутация глутамина 67 -> гистидина в гомотетрамерной дигидрофолатредуктазе R67 приводит к четырем мутациям на одну пору активного сайта и вызывает существенное ингибирование субстрата и кофактора. Protein Eng 1997; 10: 1415–1424. |
| 18. | Тогда RL. Механизмы устойчивости к триметоприму, сульфаниламидам и триметоприм-сульфаметоксазолу. Rev Infect Dis 1982; 4: 261–269. |
| 19. | Ливермор DM. Устойчивость стафилококков к антибиотикам. Int J Antimicrob Agents 2000; 16 Приложение 1: S3 – S10. |
| 20. | Стэплтон П., Ву П.Дж., Кинг А., Шеннон К., Френч Джи, Филлипс И.Заболеваемость и механизмы устойчивости к комбинации амоксициллина и клавулановой кислоты у Escherichia coli. Антимикробные агенты Chemother 1995; 39: 2478–2483. |
| 21. | Джонс RN. Паттерны устойчивости среди внутрибольничных патогенов: тенденции за последние несколько лет. Сундук 2001; 119 2 Дополнение: 397S – 404S. |
| 22. | Culebras E, Martínez JL.Устойчивость к аминогликозидам, опосредованная бифункциональным ферментом 6′-N-аминогликозидацетилтрансфераза-2 «-O-аминогликозид фосфотрансферазой. Front Biosci 1999; 4: D1 – D8. |
| 23. | Группы изучения устойчивости к аминогликозидам. Наиболее часто встречающиеся механизмы устойчивости к аминогликозидам — объединенные результаты опросов в восьми регионах мира. J Chemother 1995; 7 Suppl 2: 17–30. |
| 24. | Wagenlehner FM, Weidner W, Naber KG. Антибиотики в урологии: новые основы. Urol Clin North Am 2008; 35: 69–79. vi. |
| 25. | Gupta K, Hooton TM, Naber KG, Wullt B, Colgan R, Miller LG и др. Международные клинические рекомендации по лечению острого неосложненного цистита и пиелонефрита у женщин: обновление 2010 г., подготовленное Американским обществом инфекционистов и Европейским обществом микробиологии и инфекционных заболеваний.Clin Infect Dis 2011; 52: e103 – e120. |
| 26. | Макласки К., Кэмерон С., Хаммершмидт Ф., Хантер В.Н. Структура и реакционная способность эпоксидазы гидроксипропилфосфоновой кислоты в биосинтезе фосфомицина по катионо- и флавин-зависимому механизму. Proc Natl Acad Sci U S. A 2005; 102: 14221–14226. |
| 27. | Schito GC. Почему фосфомицин трометамол используется в качестве терапии первой линии при неосложненных ИМП? Int J Antimicrob Agents 2003; 22 Suppl 2: 79–83. |
| 28. | Веве МП, Вагнер Дж. Л., Кенни Р. М., Грюнвальд Дж. Л., Дэвис С. Л.. Сравнение фосфомицина и эртапенема в амбулаторных условиях или при пониженной терапии инфекций мочевыводящих путей с расширенным спектром β-лактамаз. Int J Antimicrob Agents 2016; 48: 56–60. |
| 29. | Ode B, Haidl S, Hoffstedt B, Walder M, Ursing J. Сравнение фосфомицина с ампициллином в лечении острого пиелонефрита.Chemioterapia 1988; 7: 96–100. |
| 30. | Patel SS, Balfour JA, Bryson HM. Фосфомицин трометамин. Обзор его антибактериальной активности, фармакокинетических свойств и терапевтической эффективности в качестве однократного перорального лечения острых неосложненных инфекций нижних мочевых путей. Наркотики 1997; 53: 637–656. |
| 31. | Уоррен Дж. У., Абрутин Э, Хебель Дж. Р., Джонсон Дж., Шеффер А. Дж., Штамм МЫ.Американское общество инфекционных болезней (IDSA). Рекомендации по противомикробной терапии неосложненного острого бактериального цистита и острого пиелонефрита у женщин. Clin Infect Dis 1999; 29: 745–758. |
| 32. | Санчес М., Колвинент Б., Миро О., Хоркахада Дж. П., Морено А., Марко Ф. и др. Краткосрочная эффективность однократной дозы цефтриаксона при начальном лечении острого неосложненного пиелонефрита у женщин. Рандомизированное контролируемое исследование.Emerg Med J 2002; 19: 19–22. |
| 33. | Czaja CA, Scholes D, Hooton TM, Stamm WE. Популяционный эпидемиологический анализ острого пиелонефрита. Clin Infect Dis 2007; 45: 273–280. |
| 34. | Jeon JH, Kim K, Han WD, Song SH, Park KU, Rhee JE и др. Эмпирическое использование ципрофлоксацина при остром неосложненном пиелонефрите, вызванном Escherichia coli, в сообществах, где высока распространенность устойчивости к фторхинолонам.Антимикробные агенты Chemother 2012; 56: 3043–3046. |
| 35. | Хаммонд ML. Эртапенем: карбапенем группы 1 с ярко выраженными антибактериальными и фармакологическими свойствами. J Antimicrob Chemother 2004; 53 Дополнение 2: ii7 – ii9. |
| 36. | Папп-Уоллес К.М., Эндимиани А., Тарасила М.А., Бономо РА. Карбапенемы: прошлое, настоящее и будущее. Антимикробные агенты Chemother 2011; 55: 4943–4960. |
| 37. | Мелетис Г. Устойчивость к карбапенему: обзор проблемы и перспективы на будущее. Ther Adv Infect Dis 2016; 3: 15–21. |
| 38. | Баучер Х.В., Сакулас Г. Перспективы устойчивости к даптомицину с упором на устойчивость к золотистому стафилококку. Clin Infect Dis 2007; 45: 601–608. |
| 39. | Ramaswamy DP, Amodio-Groton M, Scholand SJ. Использование даптомицина в лечении устойчивых к ванкомицину энтерококковых инфекций мочевыводящих путей: серия коротких случаев. БМК Урол 2013; 13:33. |
| 40. | Джонс Р.Н., Джонсон Д.М., Эрвин М.Э. Антимикробная активность in vitro и спектры двух новых фторированных оксазолидинонов U-100592 и U-100766. Противомикробные агенты Chemother 1996; 40: 720-726. |
| 41. | Бетриу С., Редондо М., Палау М.Л., Санчес А., Гомес М., Кулебрас Е. и др. Сравнительная активность линезолида, хинупристин-далфопристина, моксифлоксацина и тровафлоксацина in vitro в отношении стрептококков, чувствительных к эритромицину, и резистентных к ним. Противомикробные агенты Chemother 2000; 44: 1838–1841. |
| 42. | Дикема Д.И., Джонс Р.Н. Оксазолидиноны: обзор. Наркотики 2000; 59: 7–16. |


 ;
;