Лечение эндокринной системы и нарушения обмена веществ в санаториях
Болезни эндокринной системы, расстройства питания и нарушение обмена веществ
Неблагоприятные экологические условия больших городов, стрессы, нехватка времени, нарушение регулярности в питании, плохая наследственность — всё это и многое другое негативно отражается на функциях желез внутренней секреции. Это приводит к развитию эндокринных заболеваний, которые, как правило, имеют долгий и тяжелый характер, влияя на общее самочувствие, настроение больного и даже его внешний вид.
В санаториях проходят лечение при следующих заболеваниях:
— болезни щитовидной железы, связанные с йодной недостаточностью, диффузный (эндемический) зоб, связанный с йодной недостаточностью;
— субклинический гипотиреоз вследствие йодной недостаточности, диффузный (эндемический) зоб с гипотиреозом легкой степени;
— нетоксический диффузный зоб, диффузный эутиреоидный зоб при увеличении железы I-III степени;
— тиреотоксикоз с диффузным зобом, диффузный токсический зоб легкой, средней степени, при увеличении железы I-III степени;
— хронический тиреоидит при увеличении железы I-III степени с эутиреозом и гипотиреозом;
— сахарный диабет инсулинзависимый средней и тяжелой формы при стабильном течении, без наклонности к кетозу;
— сахарный диабет инсулиннезависимый, легкой, средней, тяжелой формы при стабильном течении, без наклонности к кетозу;
— ожирение первичное, экзогенноконституциональное I-III степени, без декомпенсации кровообращения;
— нарушение обмена липопротеидов и другие липидемии, дислипидемия;
— оксалурия;
— гиперурикемия без признаков воспалительного артрита и подагрических узлов;
Противопоказания:
Тиреотоксикоз в тяжелой степени, сахарный диабет в стадии декомпенсации с кетоацидозом, симптомами прекоматозного состояния, а так же при лабильном течении, эндокринное ожирение органического генеза и любые формы ожирения при недостаточности кровообращения, общие противопоказания, узловой зоб.
Лечение эндокринной системы | Санаторное лечение в Калининграде
- Автор: Санаторий “Отрадное”
Особенности лечения
Назначение процедур происходит с учетом индивидуальных противопоказаний, на основе медицинских методик, не менее 5 наименований по основному и 1-2 наименований по сопутствующему заболеванию.
Показания
- Диффузный токсический зоб 1-2 степени в эутиреоидном состоянии или тиреотоксикоз легкой степени, субклинический тиреотоксикоз.
- Хронические воспалительные заболевания щитовидной железы (нетуберкулезной этиологии) при увеличении железы 0-1 степени с эутиреозом, перенесенный подострый тиреоидит, хронический аутоиммунный тиреоидит диффузная форма в эутиреоидном состоянии и с гипотиреозом, в стадии компенсации.
- Йоддефицитные состояния с увеличением щитовидной железы 0-1 степени в состоянии эутиреоза, легкого гипотиреоза.
- Сахарный диабет 1 и 2 типа, легкой и средней тяжести, в состоянии устойчивой компенсации, без наклонности к кетоацидозу.
- Ожирение первичное, экзогенно-конституциональное 1-3 степени без декомпенсации сердечно-сосудистой системы или с недостаточностью кровообращения не выше 1 степени.
- Нарушение обмена липопротеидов (дислипидемия).
- Подагра (нарушение обмена мочевой кислоты).

Противопоказания
- Диффузный токсический зоб с тиреотоксикозом тяжелой степени, тиреотоксическое сердце с нарушением ритма.
- Тяжелый гипотиреоз.
- Злокачественные опухоли эндокринных желез и состояния после оперативного лечения.
- Сахарный диабет тяжелой степени с частыми гипогликемическими комами, кетоацидозом.
- Ожирение с явлениями сердечно-сосудистой недостаточности 2 стадии.
Клиническая эффективность низкодозовой комбинированной терапии бисопрололом с гидрохлоротиази-дом у женщин с артериальной гипертонией и патологией щитовидной железы в постменопаузе | Cтрюк
1. Лебедева М.В. Антигипертензивная терапия у женщин в перименопаузе // Consilium medicum. 2008; 5: 65-68.
2. Ansa V.O., Oyo-Ita A., Essien O.E. Perception of ischaemic heart disease, knowledge of and attitude to reduction of its risk factors. East. Afr.Med J 2007; 84 (7): 318-23.
4. Люсов В.А., Евсиков Е.М., Машукова Ю.М., Шарипов РА Частота эндокринных нарушений и характер гормонального дисбаланса при кризовом течении первичной артериальной гипертензии // Российский кардиологический журнал. 2008; 1: 4-70.
5. Башмакова Н.В., Дерябина Е.Г. Проспективное клиническое исследование влияния динамики индекса массы тела и функционального состояния щитовидной железы на формирование менопаузального метаболического синдрома у женщин после хирургической менопаузы // Акушерство и гинекология.
6. Сметник В.П., Ильина Л.М. Особенности факторов риска сердечно-сосудистых заболеваний у женщин и роль половых гормонов // Вопросы репродукции. 2008; 2: 80-87.
7. Murawski M.M., Bentley J.P. Pharmaceutical therapy-related quality of life: conceptual development. J Soc Adm Pharm 2001;18 (1): 2-14.
8. Стрюк РИ., Длусская И. Г. Адренореактивность и сердечно-сосудистая система. М.: Медицина, 2003; 174 с.
9. Стрюк РИ., Длусская И.Г., Токмачев Ю.К. и др. Прогнозирование и профилактика нейровегетативных гипертонических кризов // Кардиология. 1995; 3: 24-28.
Субтотальная тиреоидэктомия. Гипертиреоз лечение — хирургическая клиника Линия жизни
Субтотальная тиреоидэктомия относится к сложным хирургическим операциям на щитовидной железе. В ходе нее удаляют одну долю полностью с перешейком и частично другую. В клинике «Линия жизни» процедура проводится максимально безопасно благодаря малоинвазивному вмешательству с использованием лапароскопического инструмента.
Показания к операции
В рамках операции проводится лечение диффузного токсического зоба. Это заболевание сопровождается увеличением количества вырабатываемого гормона тироксина. В последствии нарушается работа нервной, сердечно-сосудистой систем, повышается обмен веществ и происходят сбои во всем организме. Сопровождается такими симптомами:
-
увеличение щитовидки;
-
ускоренное сердцебиение;
-
похудание на 10-15 кг;
-
возбуждение;
-
тремор рук;
-
повышение аппетита;
-
потливость.

Как лечится
Сначала в клинике «Линия жизни» по возможности применяют консервативные методы, назначают прием тиреостатических препаратов, йода. Иногда они позволяют достичь состояния стойкой ремиссии. Препараты также назначаются для обеспечения эутиреоза, необходимого перед проведением операции.
Удаление доли щитовидной железы или резекция в нашей клинике полностью безопасна. Мы проводим процедуру тонкими инструментами через небольшие надрезы на шее. Период реабилитации короткий, а осложнения исключены. На теле практически не остается видимых рубцов и шрамов.
Хирургическое лечение гипертиреоза в Иркутске врачами клиники «Линия жизни» осуществляется после досконального обследования пациента, подтверждающего необходимость операции. Мы учтем возраст обследуемого, масштабы увеличения щитовидки, общее состояние здоровья, наличие противопоказаний. При умеренном увеличении железы, возможно, удастся ограничиться консервативными методами.
Лечение радиойодом в Нижнем Новгороде (радиойод, зоб, тиретоксикоз)
Уважаемые коллеги!
Радиойодтерапия (РЙТ) заболеваний с синдромом тиреотоксикоза признана в мире как самый эффективный и безопасный метод лечения.
Мы
проводим радиойодтерапию пациентам с диффузным
токсическим зобом и многоузловым токсическим зобом с
2005 года. За истекшие годы проведено лечение тысяч
пациентов. Нами проводилось динамическое наблюдение за
значительной частью больных как в период пребывания
пациентов в стационаре, так и на протяжении года после
радиойодтерапии с целью анализа эффективности и
безопасности данного вида лечения. Результаты
неоднократно были представлены на различных
эндокринологических конгрессах, конференциях, а
также в ведущих периодических журналах.
Позвольте остановиться на некоторых аспектах ведения больных в период подготовки пациентов к радиойодтерапии и после лечения радиоактивным йодом.
В период подготовки, прежде всего, необходимо исключить йод-содержащие продукты питания и медикаменты, особенно, амиодарон. По нашим наблюдениям, пациенты, получившие кордарон, длительно (до года и более) имеют очень низкий захват йода, нередко всего 1-2% (через 24 часа после приема тестовой дозы йодида натрия I-131), что делает невозможной радиойодтерапию. Необходимо исключить йод-содержащие контрасты. Кроме того, поглощение йода снижается после приема Br-содержащих препаратов. Рекомендуется отмена тироксина за месяц до предстоящего лечения. Ухудшаются результаты лечения при продолжающемся приеме тиреостатиков, особенно пропицила.
Перед предстоящей радиойодтерапией необходимо отменить мерказолил (тирозол) за 5-7 дней. Наиболее безопасна радиойодтерапия у пациентов в состоянии эутиреоза при приеме не более 10мг тиамазола с продолжительностью отмены не более недели до приема I-131. Однако у пациентов пожилого возраста и с сопутствующей кардиологической патологией возможно сокращение сроков отмены тиамазола и даже проведение РЙТ при продолжающемся приеме препарата, что, конечно, увеличивает вероятность повторного лечения, но обеспечивает безопасность процедуры, особенно при сопутствующей коронарной патологии. Более продолжительной должна быть отмена пропицила до 1 мес.
Прием
лечебной дозы радиойода не сопровождается немедленным
ухудшением состояния пациентов. Эффект радиойода
развивается относительно медленно и, по нашим данным,
редко сопровождается умеренным болевым синдромом
вследствие лучевого тиреоидита. Однако, у пациентов,
главным образом, с повышением уровня Т3 и Т4 на момент
приема препарата, может отмечаться дальнейшее увеличение
содержания тиреоидных гормонов, обычно без клинически
значимого изменения состояния на протяжении первой
недели.
Однако, у пациентов,
главным образом, с повышением уровня Т3 и Т4 на момент
приема препарата, может отмечаться дальнейшее увеличение
содержания тиреоидных гормонов, обычно без клинически
значимого изменения состояния на протяжении первой
недели.
К исходу 1 месяца у каждого третьего пациента развивается гипотиреоз, что требует динамического исследования содержания гормонов и своевременного назначения заместительной терапии, особенно у пациентов с офтальмопатией. У каждого третьего сохраняется гипертиреоз, что нередко требует возобновления приема тиреостатиков. В целом в течение первых 3 месяцев тиреоидный статус изменяется быстро, в дальнейшем темпы существенно снижаются. Это требует ежемесячного контроля уровня тиреоидных гормонов на протяжении первых 3 месяцев с уменьшением кратности исследований в последующем. Формирование гипотиреоза в любые сроки имеет хороший прогноз, относительно редко гипотиреоз бывает преходящим.
Результаты лечения оцениваются не ранее 6 мес. нередко 1 года, когда принимается решение о необходимости повторного лечения при персистирующем гипертиреозе. Благоприятным прогностическим признаком является раннее значительное (более чем на 50%) уменьшение объема щитовидной железы после РЙТ.
Уважаемые коллеги! Мы готовы к обсуждению с Вами тактики ведения Ваших пациентов и будем признательны за Ваши наблюдения и отзывы об эффективности проведенного нами лечения.
Ведение пациентов с амиодарон-ассоциированной дисфункцией щитовидной железы. Новости Европейской тиреоидологической ассоциации 2018 г. | Демидова Т.Ю., Кишкович Ю.С., Ладыгина Д.О.
В статье представлены новости Европейской тиреоидологической ассоциации 2018 г. Освещены особенности ведения пациентов с амиодарон-ассоциированной дисфункцией щитовидной железы (гипотиреоз, тиреотоксикоз).
Освещены особенности ведения пациентов с амиодарон-ассоциированной дисфункцией щитовидной железы (гипотиреоз, тиреотоксикоз).
Введение
Амиодарон — это производное бензофурана, йодсодержащий препарат, особенно эффективный в терапии наджелудочковых аритмий [1]. Из-за высокого содержания йода и фармакологических свойств (подавление периферического монодейоденирования тироксина, Т4) препарат вызывает дисфункцию ЩЖ и изменение показателей, свидетельствующее об изменении ее функции. Приблизительно у 15–20% пациентов, получавших лечение амиодароном, развивается тиреотоксикоз (амиодарон-индуцированный тиреотоксикоз, АИТ) или гипотиреоз (амиодарон-индуцированный гипотиреоз, АИГ) [2]. Тип дисфункции ЩЖ частично зависит от приема йода, так, АИГ
более часто встречается в йод-насыщенных областях,
АИТ — в йод-дефицитных [2]. Диагноз, классификация и тактика при амиодарон-индуцированной дисфункции ЩЖ, а именно АИТ, часто сложны [3, 4]. Не обнаружено ни одного специфического предиктора амиодарон-ассоциированной дисфункции ЩЖ [5], хотя женский пол и антитела к антитиреоидной тиреопероксидазе прогнозируют АИГ [6].
Патогенез изменений ЩЖ при лечении амиодароном и тактика лечения ее дисфункции
Как амиодарон влияет на анализы, оценивающие функцию ЩЖ, у эутиреоидных пациентов?
У большинства пациентов, начавших получать амиодарон (обычно 200 мг/сут), отмечается эутиреоз, даже если используются большие дозы (400 мг/сут) [6]. Однако у всех пациентов, получавших лечение амиодароном, наблюдаются ранние (3 мес.) изменения уровней сывороточных тиреоидных гормонов в анализах. Высокое содержание йода в амиодароне повышает концентрацию неорганического йода в плазме крови в 40 раз, выделение йода с мочой — до 15 тыс. мкг за 24 ч. Из-за эффекта Вольфа — Чайкова ЩЖ адаптируется к перегрузке йодом путем подавления органификации йода и снижения уровней гормонов ЩЖ. Последний эффект — основная причина повышения концентрации сывороточного тиреотропного гормона (ТТГ). Кратковременное лечение амиодароном (400 мг/сут в течение 3 нед.) снижает скорость продукции тироксина (Т4) и скорость метаболизма Т4 [6]. Амиодарон также подавляет внутриклеточный перенос Т4 и активность йодтирониндейодиназы 2-го типа в гипофизе, с последующим снижением продукции внутриклеточного трийодтиронина (Т3) и связывания тиреоидного гормона с его родственным рецептором в гипофизе [7]. Однако эти гипофизарные эффекты также проявляются в хронических стадиях в течение длительного лечения амиодароном и, скорее всего, менее важны для изменения уровня ТТГ, чем эффект Вольфа — Чайкова. Позже эффект Вольфа — Чайкова проходит [8], и происходит нормализация сывороточной концентрации Т4 и ТТГ. В эту фазу уровни Т4, свободного Т4 (свT4) и превращенного Т3 (пТ3) повышаются, в то время как уровни сывороточных общего Т3 и свободного Т3 (свT3) снижаются из-за подавления активности печеночной йодидтирониндейодиназы 1-го типа [9, 10].
Кратковременное лечение амиодароном (400 мг/сут в течение 3 нед.) снижает скорость продукции тироксина (Т4) и скорость метаболизма Т4 [6]. Амиодарон также подавляет внутриклеточный перенос Т4 и активность йодтирониндейодиназы 2-го типа в гипофизе, с последующим снижением продукции внутриклеточного трийодтиронина (Т3) и связывания тиреоидного гормона с его родственным рецептором в гипофизе [7]. Однако эти гипофизарные эффекты также проявляются в хронических стадиях в течение длительного лечения амиодароном и, скорее всего, менее важны для изменения уровня ТТГ, чем эффект Вольфа — Чайкова. Позже эффект Вольфа — Чайкова проходит [8], и происходит нормализация сывороточной концентрации Т4 и ТТГ. В эту фазу уровни Т4, свободного Т4 (свT4) и превращенного Т3 (пТ3) повышаются, в то время как уровни сывороточных общего Т3 и свободного Т3 (свT3) снижаются из-за подавления активности печеночной йодидтирониндейодиназы 1-го типа [9, 10]. Повышение концентрации сывороточного пТ3 обычно намного больше, чем понижение концентрации Т3 в сыворотке [11]. Упомянутые выше изменения сывороточных Т4, Т3 и пТ3 наблюдались рано во время лечения амиодароном и сохранялись в течение длительного лечения. После 3-х мес. терапии достигалось устойчивое состояние, при котором уровень сывороточного ТТГ возвращался к исходным значениям [12]. Нормализация сывороточного ТТГ, скорее всего, связана с повышенной скоростью продукции Т4 и уменьшением скорости метаболизма [6, 13]. Изменения скорости выработки Т4 и скорости метаболизма подавляют блокаду образования Т3, таким образом, повышая уровень сывороточного Т3 в низко нормальном диапазоне [13]. С кумулятивной дозой амиодарона уровни сывороточного общего Т4, свТ4 и пТ3 остаются у верхней границы нормы или слегка повышенными, в то время как уровни сывороточного Т3 (биохимически активного гормона) находятся в нормальном диапазоне у нижней границы.
 Такой биохимический профиль пациентов, получающих лечение амиодароном, считается эутиреоидным.
Такой биохимический профиль пациентов, получающих лечение амиодароном, считается эутиреоидным.Лечить ли всех пациентов с АИГ? Надо ли отменять амиодарон у этих пациентов?
Распространенность АИГ у пациентов, получавших лечение амиодароном, может достигать 26% (субклинический гипотиреоз) и 5% (манифестный гипотиреоз) [14]. Хотя АИГ может развиваться у пациентов с нормальной ЩЖ и отсутствием аутоиммунной реакции, он чаще всего развивается у пациентов со скрытым хроническим аутоиммунным тиреоидитом, преобладает у женщин, а также в йод-насыщенных областях [2, 15, 16]. Клинически симптомы АИГ не отличаются от симптомов гипотиреоза другой этиологии, но стоит упомянуть, что тяжелый гипотиреоз может способствовать повышению чувствительности желудочков к жизнеугрожающим аритмиям [17].
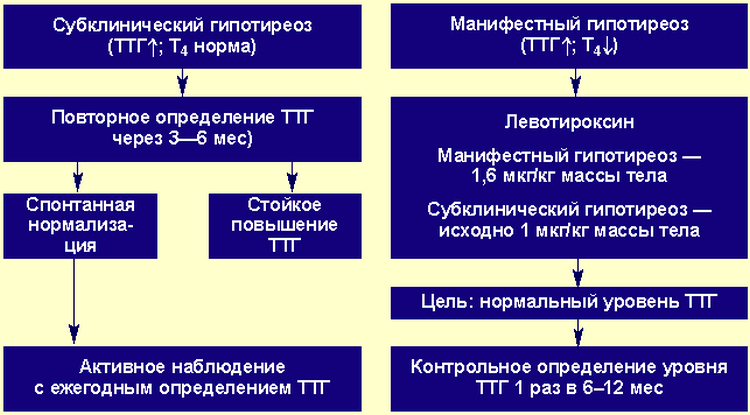
АИГ не требует отмены амиодарона. Лечение левотироксином натрия (ЛН) рекомендовано во всех случаях манифестного гипотиреоза, в то время как этого можно избежать при субклинических формах, особенно у пожилых людей, но необходимо часто оценивать тиреоидный статус для выявления возможного прогрессирования гипотиреоза (рис. 1).
Сколько типов АИТ может быть выделено и каковы диагностические критерии?
АИТ 1-го типа — это форма йод-индуцированного гипертиреоза, обусловленная чрезмерным, бесконтрольным синтезом тиреоидных гормонов автономно функционирующей ЩЖ в ответ на йодную нагрузку, которая обычно развивается при наличии исходно узлов ЩЖ или латентной болезни Грейвса [1, 2, 18]. АИТ 2-го типа —это деструктивный тиреоидит, который развивается при нормальной ЩЖ [1, 2, 18]. Смешанная/недифференцированная форма также устанавливается, когда у пациента присутствуют оба типа. АИТ 2-го типа преобладает в йод-дефицитных областях [1, 2, 18], и это наиболее часто встречающаяся форма АИТ [19]. Диагноз АИТ обычно предусматривает повышение сывороточных уровней cвТ4 и свТ3 и снижение уровня сывороточного ТТГ [20]. Антитиреоидные антитела, так же как и антитела к антитиреоидной тиреопероксидазе, обычно положительные при АИТ 1 и отрицательные при АИТ 2 [1], хотя их наличие необязательно для установления диагноза АИТ 1 [21].

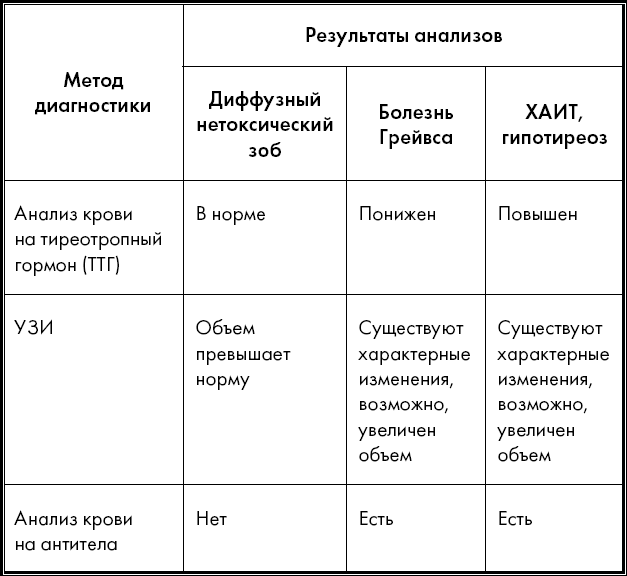
С помощью УЗИ можно быстро оценить объем ЩЖ, узловые образования, паренхиматозные эхогенные структуры и васкуляризацию. В целом большинство данных показывают, что стандартное УЗИ ЩЖ имеет низкое диагностическое значение. УЗИ с эффектом Допплера представляет собой неинвазивную оценку васкуляризации ЩЖ в реальном времени [18], является хорошей помощью в диагностике деструктивной формы АИТ 2 (отсутствие гиперваскуляризации вместе с высокими уровнями гормонов ЩЖ (табл. 1) [22].
Всегда ли АИТ — чрезвычайная ситуация?
АИТ может быть опасным состоянием, т. к. может обострять имеющуюся кардиальную патологию. АИТ ассоциирован с повышением уровня заболеваемости и смертности, особенно у пожилых пациентов с нарушенной функцией левого желудочка [23–25]. Таким образом, в большинстве случаев, а именно у пожилых пациентов, требуются срочное восстановление и поддержание эутиреоза [26]. Пациентам с АИТ должно проводиться срочное лечение в любое время из-за повышенных рисков заболеваемости и смертности, в частности, у пожилых и/или при наличии дисфункции левого желудочка. Тотальная тиреоидэктомия должна быть выполнена без промедления у пациентов с АИТ с ухудшением функции сердца и у тех пациентов, у которых тиреотоксикоз не поддается терапии. Это заключение может быть сделано мультидисциплинарной бригадой в составе эндокринолога, кардиолога, анестезиолога и хирурга с большим опытом.Может ли терапия амиодароном быть продолжена в некоторых случаях АИТ?
Не существует ни единого мнения, ни достоверных данных касательно решения продолжать или прекращать терапию амиодароном у пациентов с АИТ. Это решение должно быть индивидуальным, с учетом стратификации рисков, принятым совместно кардиологами и эндокринологами [1, 27].В рандомизированных клинических исследованиях все 26 пациентов с АИТ 2, получавших лечение тиамазолом (метимазолом) и преднизолоном или преднизолоном и перхлоратом натрия, достигли эутиреоза на 8–14 нед., невзирая на амиодарон [28].
 Похожие результаты получили в небольшом проспективном исследовании 13 больных с АИТ 2 [29]. В Японии изучали 50 пациентов с АИТ 2, которые продолжали получать амиодарон, рецидивирующий АИТ 2 отмечался только у трех пациентов спустя несколько лет после первого эпизода АИТ [30]. С другой стороны, в большом ретроспективном когортном исследовании у 83 пациентов с АИТ 2 преднизолон восстанавливал эутиреоз у большинства независимо от продолжения или отмены
Похожие результаты получили в небольшом проспективном исследовании 13 больных с АИТ 2 [29]. В Японии изучали 50 пациентов с АИТ 2, которые продолжали получать амиодарон, рецидивирующий АИТ 2 отмечался только у трех пациентов спустя несколько лет после первого эпизода АИТ [30]. С другой стороны, в большом ретроспективном когортном исследовании у 83 пациентов с АИТ 2 преднизолон восстанавливал эутиреоз у большинства независимо от продолжения или отмены амиодарона, но продолжающаяся терапия амиодароном повышала процент рецидива тиреотоксикоза, вызывая задержку устойчивого восстановления эутиреоза и более длительное воздействие гормонов ЩЖ на сердце [31]. Если состояние сердца нетяжелое и стабильное, амиодарон можно осторожно отменять, если необходимо, то возможно возобновить после восстановления эутиреоза. Проблема более трудная при АИТ 1 и смешанных/недифференцированных случаях АИТ. Многие эндокринологи предпочитают отменять амиодарон, если это возможно с кардиологической точки зрения [3, 32]. Таким образом, решение, стоит ли продолжать применять амиодарон или отменять, должно приниматься с учетом потенциальной пользы амиодарона при жизнеугрожающих аритмиях, угрозе длительного воздействия избытка гормонов и типа АИТ.
Какова тактика лечения при АИТ 1?
Ввиду преобладающего патогенетического механизма АИТ 1 лучше поддается лечению антитиреоидными препаратами (карбимазол (пролекарство для метимазола), метимазол или пропилтиоурацил), когда медикаментозная терапия целесообразна [12, 33]. В некоторых случаях экстренная или спасительная тиреоидэктомия может быть первоначальным терапевтическим выбором. Йод-насыщенная ЩЖ у пациентов с АИТ малочувствительна к тионамидам, так, с более высокими ежедневными дозами лекарств (40–60 мг метимазола или эквивалентной дозой пропилтиоурацила) требуется более длительный период, чем обычно, для восстановления эутиреоза. Это, очевидно, не идеальная ситуация у пациентов с исходной кардиальной патологией, у которых гипертиреоз должен быть быстро скомпенсирован. Для того чтобы увеличить чувствительность ЩЖ к тионамидам, используется перхлорат калия, который снижает захват йода ЩЖ. Были использованы дозы, не превышающие 1 г/сут, для того, чтобы минимизировать неблагоприятное действие лекарства (особенно на почки и костный мозг). Кроме того, рекомендуется не использовать препарат более чем
Для того чтобы увеличить чувствительность ЩЖ к тионамидам, используется перхлорат калия, который снижает захват йода ЩЖ. Были использованы дозы, не превышающие 1 г/сут, для того, чтобы минимизировать неблагоприятное действие лекарства (особенно на почки и костный мозг). Кроме того, рекомендуется не использовать препарат более чем 4–6 нед. [2]. Перхлорат натрия — альтернативный вариант, т. к. перхлорат калия больше недоступен. Перхлорат натрия доступен в качестве раствора — 21 капля соответствует 300 мг перхлората. Лечение тионамидами может быть продолжено до восстановления эутиреоза, если это допустимо при основном заболевании сердца и сердечно-сосудистой компенсации. После восстановления эутиреоза обычно рекомендуется окончательная терапия гиперфункционирующей ЩЖ [1]. Это позволяет безопасно возобновить и продолжить прием амиодарона, если это необходимо с кардиологической точки зрения. Если прием амиодарона может быть прекращен, радиойодтерапия может быть проведена, когда контаминация йодом окончена, вплоть до 6–12 мес. после прекращения приема амиодарона, нормализации выделения йода с мочой и адекватного уровня поглощения радиоактивного йода. Окончательное лечение АИТ 1 с исходной гиперфункцией ЩЖ не отличается от лечения спонтанного гипертиреоза. При отсутствии доказательств, свидетельствующих о деструктивном тиреотоксикозе, не рекомендуется использование ГК при АИТ 1.
Какова тактика при АИТ 2?
В одном рандомизированном исследовании у 36 пациентов, которые получали амиодарон и метимазол (30 мг/сут), сравнивались прием преднизолона (30 мг/сут) и перхлората натрия (500 мг/сут) или комбинации этих препаратов. При лечении преднизолоном эутиреоз был достигнут у всех пациентов, в то время как 30% пациентов, лечившихся только перхлоратом натрия, нуждались в дополнительном лечении преднизолоном для достижения эутиреоза. Таким образом, преднизолон рассматривается как наиболее эффективный способ лечения этих пациентов [28]. Начальная доза пероральных ГК при АИТ — 2–30 мг/сут преднизолона(или эквивалентная доза других ГК), снижаемая при достижении клинического и/или биохимического эутиреоза.
 В некоторых случаях АИТ 2 может требовать длительного периода лечения. Если АИТ 2 представляет собой критическое состояние, спасающая тиреоидэктомия может быть рассмотрена так же, как и при АИТ 1 или смешанных/недифференцированных формах.
В некоторых случаях АИТ 2 может требовать длительного периода лечения. Если АИТ 2 представляет собой критическое состояние, спасающая тиреоидэктомия может быть рассмотрена так же, как и при АИТ 1 или смешанных/недифференцированных формах.Какова тактика при смешанных/недифференцированных формах АИТ?
Различие между АИТ 1, АИТ 2 и смешанными/недифференцированными формами может быть важным для определения дальнейшей тактики лечения [1, 34].Смешанные/недифференцированные АИТ (даже если не полностью охарактеризованы) встречаются в клинической практике и обусловлены обоими патогенетическими механизмами АИТ 1 (йод-индуцированный гипертиреоз) и АИТ 2 (деструктивный тиреоидит) [1, 34]. Весьма маловероятно, что пациенты с АИТ и морфологически нормальной ЩЖ, отсутствующей васкуляризацией, отрицательными антителами к анти-ТТГ имеют смешанные/недифференцированные формы АИТ. У этих пациентов на основании физикального осмотра, измерения чувствительности антител к анти-ТТГ рецепторам допускают диагноз АИТ 2 и лечение ГК [35]. Различие между АИТ 1 и смешанными/недифференцированными формами АИТ проводить более трудно, обычно это представляет собой диагноз исключения (при наличии узлового зоба). Терапевтический подход в данной ситуации неясен. Если точный диагноз не может быть выставлен, могут быть предложены 2 возможных подхода. В первую очередь начинают с лечения тионамидами (± перхлорат натрия), как и при АИТ 1, при отсутствии биохимического улучшения за относительно короткий период времени (оправданно 4–6 нед.) добавляют ГК с предположением, что в существующей патологии имеет место деструктивный компонент. Альтернативный метод представлен комбинированным лечением (тионамиды и ГК) с самого начала [36]. Проведение тиреоидэктомии обоснованно в случае слабого ответа на комбинированную терапию (рис. 2).
Может ли прием амиодарона быть возобновлен (если необходимо) у пациентов с предшествующим АИТ?
В ретроспективном исследовании, в котором изучалась проблема повторного введения амиодарона при АИТ в анамнезе, из 172 пациентов с АИТ 46 нуждались в повторном курсе амиодарона спустя 2 года в среднем после отмены лекарства. АИТ рецидивировал у 14 из 46 пациентов (30%), у 12 из 46 (26%) развился АИГ, у оставшихся 20 пациентов эутиреоз сохранялся в среднем в течение 6 лет после лечения [37]. У большинства пациентов с рецидивом АИТ (11 из 14) был классифицирован АИТ 1 [38]. Другие неопубликованные исследования, упомянутые в статье Ryana et al. [39], сообщают о рецидиве АИТ или вновь развившемся гипертиреозе после восстановления терапии амиодароном в 9% случаев. Вопрос, применять ли превентивную терапию антитиреоидными препаратами перед возобновлением приема амиодарона, остается без ответа ввиду отсутствия доказательств.
АИТ рецидивировал у 14 из 46 пациентов (30%), у 12 из 46 (26%) развился АИГ, у оставшихся 20 пациентов эутиреоз сохранялся в среднем в течение 6 лет после лечения [37]. У большинства пациентов с рецидивом АИТ (11 из 14) был классифицирован АИТ 1 [38]. Другие неопубликованные исследования, упомянутые в статье Ryana et al. [39], сообщают о рецидиве АИТ или вновь развившемся гипертиреозе после восстановления терапии амиодароном в 9% случаев. Вопрос, применять ли превентивную терапию антитиреоидными препаратами перед возобновлением приема амиодарона, остается без ответа ввиду отсутствия доказательств.Заключение
В то время как АИГ легко лечится, АИТ представляет собой диагностическую и терапевтическую сложность. Большинство пациентов с АИТ 2 (деструктивным тиреоидитом) успешно лечатся ГК, им может не понадобиться отмена амиодарона. Лечение АИТ 1 (смешанных/недифференцированных форм) — намного более сложная задача из-за устойчивости йодонасыщенной железы к антитиреоидным препаратам. С учетом сложности диагностической дифференциации между АИТ 1 и смешанными/недифференцированными формами часто используется комбинированное лечение..
Гипертиреоз и хроническая болезнь почек у кошек
Автор: Гусева В. А. к.в.н., ветеринарный врач диагностического центра «Прайд», ассистент кафедры акушерства и оперативной хирургии ФГБОУ ВО СПБГАВМ.Гипертиреоз у кошек – заболевание, сопровождающееся повышенной выработкой тиреоидных гормонов.
Хроническая болезнь почек (ХБП) – это синдром, который является результатом широкого спектра первичных нарушений нефронов со снижением скорости клубочковой фильтрации (СКФ).
Введение
Такие заболевания кошек, как гипертиреоз и ХБП, являются часто встречающимися и, следовательно, могут протекать одновременно. При этом оба этих заболевания успешно маскируют друг друга, что затрудняет их диагностику и лечение. Известно, что между гормонами щитовидной железы и функцией почек существует взаимодействие, при котором протекают физиологически противоречивые процессы.
Ключевой момент затруднений, связанных с диагностикой и лечением, состоит в том, что указанные заболевания по-разному влияют на метаболические процессы, происходящие в организме. При ХБП происходит снижение скорости клубочковой фильтрации и метаболических процессов в целом, в то время как при гипертиреозе наблюдаются повышение уровня метаболических процессов в организме и стимуляция ренин-ангиотензин-альдостероновой системы (РААС), что, в свою очередь, способствует увеличению сердечного выброса и скорости клубочковой фильтрации соответственно6. Согласно данным гуманной медицины, у людей, больных гипертиреозом, СКФ повышается на 18–25% за счет увеличения почечной вазодилатации и уменьшения вазоконстрикции2.
Таким образом, именно различное влияние гипертиреоза и ХБП на скорость клубочковой фильтрации способствует маскировке одного заболевания другим.
Суть патофизиологических процессов
Стимуляция ренин-ангиотензин-альдостероновой системы, вызванная тиреотоксикозом, усиливает реабсорбцию натрия, приводя к увеличению объема циркулирующей плазмы крови, повышению ударного объема, ЧСС и системного артериального давления, что способствует увеличению скорости клубочковой фильтрации. При повышении СКФ маркеры уремии (креатинин и, возможно, мочевина) быстрее метаболизируются и попадают в референтные интервалы. По этой причине при сочетанном протекании ХБП и гипертиреоза мы можем не распознать наличие болезни почек при первичном обследовании пациента.Возможна и другая ситуация, когда ХБП маскирует гипертиреоз. Данная ситуация связана с тем, что течение различных сопутствующих заболеваний, в том числе и ХБП, может снижать концентрацию общего тироксина в крови. Когда есть выраженная уремия, концентрация общего тироксина может находиться в пределах референтных интервалов, в то время как в действительности происходит избыточная секреция тироксина щитовидной железой. Происходит это потому, что общий тироксин связан с белками плазмы крови и подвержен влиянию не только сопутствующих заболеваний (в том числе и ХБП), но и различных препаратов, что может приводить к ложному снижению его концентрации.
 Для более точной диагностики необходимо определять концентрацию свободного тироксина в крови, который не связан с белками плазмы (в отличие от общего тироксина) и практически не подвержен колебаниям в зависимости от наличия сопутствующих болезней. Однако достоверное определение концентрации свободного тироксина возможно только с помощью метода равновесного диализа, недоступного в России.
Для более точной диагностики необходимо определять концентрацию свободного тироксина в крови, который не связан с белками плазмы (в отличие от общего тироксина) и практически не подвержен колебаниям в зависимости от наличия сопутствующих болезней. Однако достоверное определение концентрации свободного тироксина возможно только с помощью метода равновесного диализа, недоступного в России.При лечении гипертиреоза у кошек может выявляться нарушение почечной функции, поскольку при достижении эутиреоза (как следствие) будет снижаться стимуляция РААС и СКФ. И при проведении повторных лабораторных исследований концентрация общего тироксина начнет снижаться или будет находиться в пределах референтных интервалов, а маркеры уремии могут начать повышаться в том случае, если тиреотоксикоз скрывает сопутствующее течение ХБП.
Также одной из причин затруднения выявления ХБП при гипертиреозе во время первичного обследования является тот факт, что при гипертиреозе снижается масса тела, в том числе и за счет потери мышечной ткани, вследствие чего происходит уменьшение выработки креатинина у больных гипертиреозом кошек без лечения.
По статистическим данным, примерно у 30% кошек при лечении гипертиреоза развивается уремия7.
Однако усиление СКФ при сочетанном протекании гипертиреоза и ХБП оказывает благотворное влияние на функцию почек лишь на первый взгляд. В действительности же тироксин негативно влияет на все системы организма, приводит к интоксикации, потере мышечной массы, полиурии, а также к гипокалиемии и мышечной слабости при длительном течении заболевания. Также системная артериальная гипертензия, вызванная гипертиреозом, может приводить к гиперфильтрации, дальнейшему ухудшению функционального состояния почек и гломерулосклерозу6.
Клинические признаки
Для гипертиреоза характерны следующие клинические признаки: полиурия, полидипсия, полифагия, рвота, повышенная активность, агрессия, вокализация. Также в 10% случаев может встречаться апатичная форма гипертиреоза, которая проявляется угнетением и анорексией3. Иногда у таких кошек может наблюдаться вентрофлексия головы и шеи, что является следствием гипокалиемии или дефицита тиамина. Клинические признаки могут присутствовать все вместе или по отдельности.
Иногда у таких кошек может наблюдаться вентрофлексия головы и шеи, что является следствием гипокалиемии или дефицита тиамина. Клинические признаки могут присутствовать все вместе или по отдельности. ХБП может сопровождаться полиурией, полидипсией, апатией, рвотой и отказом от корма. При этом полиурия/полидипсия является следствием в большей степени развития ХБП, чем гипертиреоза.
Следовательно, клинические признаки являются схожими с признаками, наблюдаемыми при гипертиреозе у кошек, и для проведения диагностики необходимо соблюдение определенного алгоритма действий и лабораторной диагностики2.
Диагностика
Для проведения диагностики необходимо учитывать наличие клинических признаков и проводить лабораторные исследования концентрации общего тироксина, биохимический и общеклинический анализы крови. Но поскольку получить однозначную картину для постановки диагноза удается не всегда, был разработан определенный алгоритм действий. Когда гипертиреоз протекает самостоятельно, без сопутствующих заболеваний с характерными клиническими признаками и сопровождается повышенной концентрацией общего тироксина в крови, его диагностика не составляет труда.Однако в тех случаях, когда клиническая картина несколько стерта и имеются сопутствующие патологии (в особенности ХБП), постановка диагноза «гипертиреоз» может оказаться затруднительной. В связи с этим в 2016 году американской ассоциацией практикующих фелинологов были разработаны рекомендации по диагностике и лечению гипертиреоза у кошек. В данном документе к каждой группе больных кошек рекомендован индивидуальный подход:
Кошки с классическими клиническими признаками гипертиреоза и повышенной концентрацией общего тироксина в крови. В данном случае лечение гипертиреоза следует начать незамедлительно. Далее необходимо достичь состояния эутиреоза и оценивать уровни маркеров уремии (креатинина, мочевины) в крови на фоне проводимого лечения, чтобы не пропустить возможное развитие хронической почечной недостаточности (ХПН).
Кошки с классическими клиническими признаками гипертиреоза и нормальной концентрацией общего тироксина. Необходимо иметь в виду, что представители данной группы могут иметь сопутствующее нетиреоидное заболевание, в частности ХПН, и, соответственно, ложное снижение концентрации общего тироксина. В таком случае рекомендованы лечение нетиреоидного заболевания (если оно диагностировано) и повторная пересдача крови на общий тироксин через 2–4 недели. В случае повышенной концентрации общего тироксина необходимо начать лечение гипертиреоза и продолжать мониторинг функции почек.
Кошки с классическими клиническими признаками гипертиреоза и подтвержденным нетиреоидным заболеванием, например ХПН. Вне зависимости от тяжести течения нетиреоидного заболевания лечение гипертиреоза у кошек рекомендуется начинать незамедлительно, поскольку гипертиреоидизм негативно влияет на все системы организма и может приводить к значительному ухудшению состояния животного.
Кошки с субклиническим гипертиреозом. Если у кошек отсутствуют классические клинические признаки и при этом выявлено повышение концентрации общего тироксина в крови, то рекомендовано провести повторное исследование крови на общий тироксин через 1–2 недели. В случае стойкого повышения концентрации общего тироксина в крови (при отсутствии классических клинических признаков) следует начать лечение гипертиреоза с последующим мониторингом концентрации общего тироксина и уровня маркеров уремии в крови.
Поскольку тироксин эпизодически синтезируется у кошек в течение суток, есть вероятность того, что полученный результат исследования концентрации общего тироксина будет находиться в пределах референтных интервалов при наличии гипертиреоза. Поэтому, если присутствуют типичные клинические признаки, рекомендуется обязательно проводить повторное исследование концентрации общего тироксина в крови, например через 2–4 недели. Алгоритм действий приведен в таблице 1.
Таблица 1.
Клиническая картина и лабораторные показатели Кошки с признаками гипертиреоза и повышенной концентрацией Т4 Кошки с признаками гипертиреоза и нормальной концентрацией Т4 Кошки с признаками гипертиреоза и ХБП Кошки с субклиническим гипертиреозом
Диагностический подход Необходимо начать лечение с последующим мониторингом функции почек Следует исключить нетиреоидное заболевание,
в частности ХБП Необходимо начать лечение гипертиреоза и ХБП согласно рекомендациям IRIS Необходимо пересдать кровь для определения концентрации Т4 через 1–2 недели
Необходимо пересдать кровь для определения концентрации Т4 через 2–4 недели При повышенной концентрации Т4 следует начать лечение гипертиреоза с мониторингом Т4 и маркеров уремии в крови
В случае повышенной концентрации Т4 следует начать лечение гипертиреоза и продолжать лечение почек или мониторинг их функции.
Лечение гипертиреоза при наличии ХБП и мониторинг пациентов
Конкретные рекомендации по лечению гипертиреоза зависят от наличия ХБП и ее стадии. По этой причине необходимо оценить функцию почек одновременно с проведением диагностики гипертиреоза. Важно помнить, что дозу метимазола следует подбирать постепенно, чтобы не привести больную кошку в состояние гипотиреоза, что значительно снизит СКФ и ухудшит функцию почек.На сегодняшний день самым удобным и доступным способом лечения гипертиреоза, особенно когда речь идет о сочетанном течении гипертиреоза и ХБП, остается применение метимазола в таблетированной форме. Этот препарат существует также в виде геля (метимазол гель), но он не всегда доступен на российском рынке, а лечение радиоактивным йодом совсем недоступно.
Специализированная диета не будет являться лечением выбора при сочетании данных патологий и длительном, тяжелом течении гипертиреоза. Однако преимуществом использования диеты является то, что она не будет приводить к развитию каких-либо побочных эффектов4.
При лечении больных гипертиреозом кошек без сопутствующей ХПН на момент первичного обследования назначают метимазол. Дозировка метимазола составляет от 1,25 до 2,5 мг на кошку 2 раза в день. Через 2–3 недели рекомендуется провести повторное исследование крови на концентрацию общего тироксина и маркеры уремии (креатинин, мочевину, фосфор). При достижении эутиреоза рекомендовано оставить выбранную дозу метимазола. В случае сохранения гипертиреоидного состояния на стартовой дозировке метимазола необходимо увеличить дозу на 1,25–2,5 мг 2 раза в день с последующим еженедельным контролем Т4 и маркеров уремии. При достижении эутиреоза оставляют подобранную дозу на том же уровне и проводят повторное мониторирование концентрации общего тироксина и маркеров уремии в крови с периодичностью 1 раз в 3 месяца.
Необходимо иметь в виду, что у неазотемичных кошек при лечении гипертиреоза может развиться азотемия после начала приема метимазола.
Наиболее вероятными кандидатами на развитие азотемии в процессе лечения будут кошки с системной артериальной гипертензией, протеинурией и изостенуричной мочой. Поэтому у неазотемичных кошек так же, как и у азотемичных, необходимо измерять системное артериальное давление, сдавать мочу на общий анализ и проводить оценку уровня протеинурии (соотношение белок/креатинин более 0,4 соответствует протеинурии). Если при достижении эутиреоидного состояния гипертензия и протеинурия сохраняются, они требуют отдельного лечения. Для контроля гипертензии рекомендовано применение атенолола 6,25–12,5 мг 1 раз в день. Для лечения протеинурии необходимо выяснить ее причину. Она может возникнуть из-за инфекции мочевыводящих путей, что требует антибиотикотерапии, либо являться следствием системной артериальной гипертензии. При отсутствии лечения гипертензии и протеинурии время наступления азотемической стадии ХБП сокращается. Микроальбуминурию можно наблюдать при гипертиреозе и ХБП. И, вероятно, такие кошки будут демонстрировать развитие азотемической стадии ХПН в будущем. Также, по некоторым данным, наличие изостенуричной мочи на момент начала лечения гипертиреоза является предиктором развития азотемической стадии ХБП, в том числе и по причине повышенной склонности таких животных к инфекциям мочеполовой системы.
При лечении больных гипертиреозом кошек с азотемической стадией ХПН рекомендован различный подход к лечению в зависимости от стадии заболевания. В любом случае необходимо одновременно начинать лечение и гипертиреоза, и ХБП. Кошек с 1–2-й стадиями ХБП по классификации Международного общества изучения заболеваний почек (англ. International Renal Interest Society; IRIS) рекомендовано лечить от гипертиреоза как пациентов без азотемии. Лечение ХБП необходимо выполнять согласно стадии (1 – креатинин < 140; 2 – креатинин – 140–249) по рекомендациям IRIS. При ХБП 3–4-й стадий (3 – креатинин – 250–439; 4 – креатинин > 440) следует начинать терапию с более низких доз метимазола и подключать активное лечение ХБП также согласно рекомендациям IRIS. При одновременном течении гипертиреоза и ХБП 3–4-й стадий важно помнить о том, что у кошек с умеренной ХБП может быть дефицит эритропоэтина, но анемия может маскироваться гипертиреозом, поскольку для гипертиреоза характерна гемоконцентрация. Развитие же анемии вследствие гипертиреоза является очень редкой ситуацией. Электролитные нарушения, такие как гиперфосфатемия, гипокалиемия и гиперкальциемия, также являются сигналами более поздней стадии ХБП.
Особое внимание необходимо уделить лечению гипертиреоза с помощью тиреоидэктомии. Удаление щитовидной железы показано в случае наличия злокачественного новообразования либо в ситуации, когда пациент благоприятно отвечает на медикаментозное лечение и при этом почечная функция остается стабильной5,8.
Возможные осложнения
К наиболее неблагоприятным последствиям применения метимазола относятся вероятность развития ятрогенного гипотиреоза и, как следствие этого, ухудшение почечной функции. Если в процессе лечения концентрация общего тироксина при последующем мониторинге оказывается ниже референтных интервалов, необходимо незамедлительно снизить дозу метимазола. В случае, если при снижении концентрации общего тироксина маркеры уремии возрастут, некоторые авторы советуют начать лечение L-тироксином. Если у кошки клинически все хорошо и маркеры уремии не ухудшились, следует подождать еще некоторое время, прежде чем принимать решение о приеме L-тироксина.В случае развития ятрогенного гипотиреоза по причине тиреоидэктомии больным гипертиреозом кошкам без ХБП рекомендован периодический контроль концентрации общего тироксина в крови и уровней маркеров уремии без использования L-тироксина. Применение данного препарата в такой ситуации может быть даже противопоказано, поскольку в этом случае не будут осуществляться стимуляция гипофиза для выработки ТТГ и регенерация тканей щитовидной железы. Однако, если у таких кошек развиваются симптомы гипотиреоза, лечение L-тироксином является необходимым.
У кошек с одновременным протеканием гипертиреоза и ХБП в случае развития ятрогенного гипотиреоза лечение L-тироксином однозначно показано, так как с развитием гипотиреоза при отсутствии его коррекции ХБП будет прогрессировать вследствие снижения СКФ.
Из всего вышесказанного можно сделать вывод о том, что диагностика и лечение гипертиреоза при сопутствующем наличии ХБП являются непростой задачей для клинициста и требуют тщательного анализа всех деталей.
Список литературы:
- Игнатенко Н. А. Клиническая картина, диагностика и лечение гипертиреоза у котов. – VetPharma № 1. – 2013.
- Мельник А. А. Дисфункция щитовидной железы и заболевания почек. Нирки № 1. – 2019, с. 68–72.
- Торранс Э. Д. и Муни К. Т. Эндокринология мелких домашних животных. – «Аквариум». – 2006, 311с.
- Тодд Л. Тауэл. Диетотерапия гипертиреоза у кошек. VetPharma № 5. – 2012, с. 51–54.
- Ссылка 1
- Ссылка 2
- Ссылка 3.
- Ссылка 4
Предикторов эутиреоза у пациентов с гипертиреозом, получавших радиоактивный йод 131 I -: ретроспективное исследование | BMC Endocrine Disorders
Vanderpump MP. Эпидемиология заболеваний щитовидной железы. Br Med Bull. 2011; 99: 39–51.
Артикул PubMed Google Scholar
Сингер П.А., Купер Д.С., Леви Э.Г., Ладенсон П.В., Браверман Л.Э., Дэниэлс Г. и др. Руководство по лечению пациентов с гипертиреозом и гипотиреозом . Комитет по стандартам ухода, Американская тироидная ассоциация. ДЖАМА. 1995. 273 (10): 808–12.
CAS Статья PubMed Google Scholar
Берч Х. Б., Бурман К. Д., Купер Д. С.. Обзор клинической практики лечения болезни Грейвса за 2011 год. J Clin Endocrinol Metab. 2012. 97 (12): 4549–58.
CAS Статья PubMed Google Scholar
Вартофски Л., Глинер Д., Соломон Б., Нагатаки С., Лагассе Р., Нагаяма Ю. и др. Различия и сходства в диагностике и лечении болезни Грейвса в Европе, Японии и США. Щитовидная железа. 1991. 1 (2): 129–35.
CAS Статья PubMed Google Scholar
Ли Х.С., Хван Дж. С.. Лечение болезни Грейвса у детей и подростков. Ann Pediatr Endocrinol Metab. 2014. 19 (3): 122–6.
Артикул PubMed PubMed Central Google Scholar
Ван Дж., Цинь Л. Радиойодтерапия в сравнении с антитиреоидными препаратами при болезни Грейвса: метаанализ рандомизированных контролируемых испытаний. Br J Radiol. 2016; 89 (1064): 20160418.
Артикул PubMed PubMed Central Google Scholar
Росс Д.С., Берч Х.Б., Купер Д.С., Гринли М.С., Лаурберг П., Майя А.Л. и др. Рекомендации Американской тироидной ассоциации по диагностике и лечению гипертиреоза и других причин тиреотоксикоза, 2016 г.Щитовидная железа. 2016; 26 (10): 1343–421.
Артикул PubMed Google Scholar
Weetman AP. Лечение радиойодом доброкачественных заболеваний щитовидной железы. Clin Endocrinol. 2007. 66 (6): 757–64.
CAS Статья Google Scholar
Лесли В.Д., Уорд Л., Саламон Е.А., Людвиг С., Роу Р.С., Кауден Е.А. Рандомизированное сравнение доз радиоактивного йода при гипертиреозе Грейвса.J Clin Endocrinol Metab. 2003. 88 (3): 978–83.
CAS Статья PubMed Google Scholar
Ярлов А.Е., Хегедюс Л., Кристенсен Л.О., Найгаард Б., Хансен Дж.М. Стоит ли рассчитывать дозу радиойодтерапии гипертиреоза? Clin Endocrinol. 1995. 43 (3): 325–9.
Артикул Google Scholar
Аллахабадия А., Дайкин Дж., Холдер Р.Л., Шеппард М.С., Гоф, Южная Каролина, Франклин Дж.Возраст и пол позволяют прогнозировать исход лечения гипертиреоза Грейвса. J Clin Endocrinol Metab. 2000. 85 (3): 1038–42.
CAS PubMed Google Scholar
Аллахабадия А., Дайкин Дж., Шеппард М.С., Гоф, Южная Каролина, Франклин Дж. Лечение радиоактивным йодом гипертиреоза — факторы прогноза исхода. J Clin Endocrinol Metab. 2001. 86 (8): 3611–7.
CAS PubMed Google Scholar
Катарги Б., Лепрат Ф., Гайот М., Валли Н., Дукассу Д., Табарин А. Оптимизированная радиойодтерапия болезни Грейвса: анализ доставленной дозы и других возможных факторов, влияющих на результат. Eur J Endocrinol. 1999. 141 (2): 117–21.
CAS Статья PubMed Google Scholar
Howarth D, et al. Определение оптимальной минимальной дозы радиоактивного йода у пациентов с болезнью Грейвса: исследование клинических результатов. Eur J Nucl Med.2001; 28: 1489–95.
CAS Статья PubMed Google Scholar
Манохар К., Миттал Б.Р., Бхойл А., Бхаттачарья А., Датта П., Бхансали А. Факторы, предсказывающие неэффективность лечения пациентов, получавших йод-131 от болезни Грейвса. Мир J Nucl Med. 2013; 12 (2): 57–60.
Артикул PubMed PubMed Central Google Scholar
Лю М., Цзин Д., Ху Дж., Инь С.Факторы прогнозирования результатов индивидуализированного лечения болезни Грейвса радиоактивным йодом ((131) I). Am J Med Sci. 2014; 348 (4): 288–93.
Артикул PubMed Google Scholar
Zaman MU, Fatima N, Zaman U, Sajjad Z, Zaman A, Tahseen R. Прогностическое значение пирамидальной доли, процент поглощения щитовидной железой и возраст для исхода абляции после фиксированной дозы 15 мКи радиоактивного йода-131 в могилах болезнь. Индийский J Nucl Med. 2015; 30 (4): 309–13.
Артикул PubMed PubMed Central Google Scholar
Ceccarelli C, Bencivelli W, Vitti P, Grasso L, Pinchera A. Результат терапии радиоактивным йодом-131 гиперфункции узлов щитовидной железы: ретроспективное исследование за 20 лет. Clin Endocrinol. 2005. 62 (3): 331–5.
CAS Статья Google Scholar
Pfeilschifter J, Elser H, Haufe S, Ziegler R, Georgi P.Влияние переменных до лечения на результат стандартизированной терапии 131I с помощью болезни Грейвса 150. Нуклеармедизин. 1997. 36 (3): 81–6.
CAS Статья PubMed Google Scholar
Льюис А., Аткинсон Б., Белл П., Кортни Н., МакКанс Д., Маллан К. и др. Результат терапии 131I при гипертиреозе с использованием режима фиксированной дозы 550 МБк. Ольстер Мед Дж. 2013; 82 (2): 85–8.
PubMed PubMed Central Google Scholar
Маркович В., Этерович Д. Эхогенность щитовидной железы позволяет прогнозировать исход радиойодтерапии у пациентов с болезнью Грейвса. J Clin Endocrinol Metab. 2007. 92 (9): 3547–52.
CAS Статья PubMed Google Scholar
Блэр А.Л., Лоу, округ Колумбия, Хадден Д.Р., Уивер Дж. А., Монтгомери, округ Колумбия. Долгосрочное наблюдение за пациентами, лечившимися от гипертиреоза низкими дозами радиоактивного йода. Ольстер Мед Дж. 1980; 49 (1): 71–8.
CAS PubMed PubMed Central Google Scholar
Петерс Х., Фишер С., Богнер У., Райнерс С., Шлейзнер Х. Радиойодтерапия гипертиреоза Грейвса: стандартная и расчетная активность йода. Результаты проспективного рандомизированного многоцентрового исследования. Eur J Clin Investig. 1995. 25 (3): 186–93.
CAS Статья Google Scholar
Вальтер М.А., Крист-Крейн М., Эккард Б., Шиндлер С., Ницше ЕС, Мюллер-Бранд Дж. И др. Радиойодтерапия при гипертиреозе: обратная корреляция между уровнем потребления йода до лечения и посттерапевтическим исходом.Eur J Clin Investig. 2004. 34 (5): 365–70.
CAS Статья Google Scholar
Kristoffersen US, Hesse B, Rasmussen AK, Kjaer A. Радиойодтерапия при гипертироидной болезни: худший исход у пациентов с высоким 24-часовым потреблением радиойода. Clin Physiol Funct Imaging. 2006. 26 (3): 167–70.
CAS Статья PubMed Google Scholar
Tamatea JA, Conaglen JV, Elston MS.Ответ на терапию радиоактивным йодом при тиреотоксикозе: несопоставимые результаты для коренного населения. Int J Endocrinol. 2016; 2016: 7863867.
Артикул PubMed PubMed Central Google Scholar
Schneider DF, Sonderman PE, Jones MF, Ojomo KA, Chen H, Jaume JC, et al. Недостаток радиоактивного йода в лечении гипертиреоза. Энн Сург Онкол. 2014. 21 (13): 4174–80.
Артикул PubMed PubMed Central Google Scholar
Boelaert K, Syed AA, Manji N, Sheppard MC, Holder RL, Gough SC, et al. Прогнозирование излечения и риска гипотиреоза у пациентов, получающих 131I по поводу гипертиреоза. Clin Endocrinol. 2009. 70 (1): 129–38.
CAS Статья Google Scholar
Метсо С., Яатинен П., Хухтала Х, Лууккаала Т., Оксала Х, Салми Дж. Долгосрочное последующее исследование лечения гипертиреоза радиоактивным йодом. Clin Endocrinol. 2004. 61 (5): 641–8.
CAS Статья Google Scholar
Erem C, Kandemir N, Hacihasanoglu A, Ersöz HO, Ukinc K, Kocak M. Лечение гипертиреоза радиоактивным йодом: прогностические факторы, влияющие на результат. Эндокринная. 2004. 25 (1): 55–60.
CAS Статья PubMed Google Scholar
Кнапска-Кухарска М., Ошуковская Л., Левински А. Анализ демографических и клинических факторов, влияющих на исход радиойодтерапии у пациентов с гипертиреозом. Arch Med Sci. 2010. 6 (4): 611–6.
Артикул PubMed PubMed Central Google Scholar
Петерс Х., Фишер С., Богнер У., Райнерс С., Шлейзнер Х. Лечение гипертиреоза Грейвса радиоактивным йодом: результаты проспективного рандомизированного исследования. Щитовидная железа. 1997. 7 (2): 247–51.
CAS Статья PubMed Google Scholar
Александр Е.К., Ларсен ПР. Терапия в высоких дозах (131) I для лечения гипертиреоза, вызванного болезнью Грейвса.J Clin Endocrinol Metab. 2002. 87 (3): 1073–7.
CAS PubMed Google Scholar
Ямасита Ю., Ямане К., Тамура Т., Окубо М., Коно Н. Возраст начала связан с исходом радиойодтерапии при болезни Грейвса. Эндокр Дж. 2004; 51 (2): 127–32.
Артикул PubMed Google Scholar
Bonnema SJ, Hegedüs L. Радиойодтерапия при доброкачественных заболеваниях щитовидной железы: эффекты, побочные эффекты и факторы, влияющие на терапевтический результат.Endocr Rev.2012; 33 (6): 920–80.
CAS Статья PubMed Google Scholar
Рейнхардт MJ, Brink I, Joe AY, Von Mallek D, Ezziddin S, Palmedo H, et al. Радиойодтерапия при болезни Грейвса на основе расчетов поглощенной тканью дозы: влияние объема щитовидной железы до лечения на клинический исход. Eur J Nucl Med Mol Imaging. 2002. 29 (9): 1118–24.
CAS Статья PubMed Google Scholar
Чиовато Л., Фиоре Э, Витти П., Рокки Р., Раго Т., Докич Д. и др. Результаты нарушения функции щитовидной железы у пациентов Грейвса, получавших радиоактивный йод: роль тиреотропных и тиреотропинблокирующих антител и индуцированного радиоактивным йодом повреждения щитовидной железы J Clin Endocrinol Metab. 1998. 83 (1): 40–6.
CAS PubMed Google Scholar
Jensen BE, Bonnema SJ, Hegedüs L. Глюкокортикоиды не влияют на эффект радиойодтерапии при болезни Грейвса.Eur J Endocrinol. 2005. 153 (1): 15–21.
CAS Статья PubMed Google Scholar
Сабри О., Зимний М., Шульц Г., Шрекенбергер М., Рейнарц П., Уиллмс К. и др. Степень успеха радиойодтерапии при болезни Грейвса: влияние тиреостатических препаратов. J Clin Endocrinol Metab. 1999. 84 (4): 1229–33.
CAS PubMed Google Scholar
Вальтер М.А., Крист-Крейн М., Шиндлер С., Мюллер-Бранд Дж., Мюллер Б.Результат радиойодтерапии без карбимазола, в течение 3 дней или 3 дня после него: проспективное интервенционное сравнение в трех группах. Eur J Nucl Med Mol Imaging. 2006. 33 (6): 730–7.
CAS Статья PubMed Google Scholar
van Isselt JW, de Klerk JM, van Rijk PP, van Gils AP, Polman LJ, Kamphuis C, et al. Сравнение методов оценки объема щитовидной железы у пациентов с болезнью Грейвса. Eur J Nucl Med Mol Imaging. 2003. 30 (4): 525–31.
Артикул PubMed Google Scholar
Ярлов А.Е., Хегедюс Л., Йёруп Т., Хансен Дж. Э. Точность клинической оценки размеров щитовидной железы. Дэн Мед Булл. 1991. 38 (1): 87–9.
PubMed Google Scholar
Machado C, Tavares P, Monteiro S, Rocha G, Silva F, Oliveira JM, et al. Исход радиойодтерапии у больных гипертиреозом. Endocr Abstr.2017; 49: EP1351. https://doi.org/10.1530/endoabs.49.EP1351.
Артикул Google Scholar
Nygaard B, Hegedüs L, Ulriksen P, Nielsen KG, Hansen JM. Радиойодтерапия при многоузловом токсическом зобе. Arch Intern Med. 1999. 159 (12): 1364–8.
CAS Статья PubMed Google Scholar
Кобе С., Эшнер В., Уайлд М., Ральфф И., Садброк Ф., Шмидт М. и др.Радиойодтерапия доброкачественных заболеваний щитовидной железы: каков эффективный период полувыведения из щитовидной железы и поглощение 131I? Nucl Med Commun. 2010. 31 (3): 201–5.
CAS Статья PubMed Google Scholar
Кобе С., Эшнер В., Садброк Ф., Вебер И., Маркс К., Дитляйн М. и др. Болезнь Грейвса и радиойодтерапия: зависит ли успех абляции от достигнутой дозы выше 200 Гр? Нуклеармедизин. 2008; 47: 13–7.
CAS Статья PubMed Google Scholar
Концентрация гепсидина снижается у пациентов с гипотиреозом и тиреоидитом Хашимото после восстановления эутиреоза
Насколько нам известно, наше исследование является первым проспективным наблюдательным исследованием, в котором сравниваются уровни гепсидина и выбранные гематологические параметры, отражающие гомеостаз Fe у пациентов с гипотиреозом и ГТ при диагностике и после восстановления эутиреоза.Уровень гепсидина регулируется ионами Fe в сыворотке и многочисленными стимулирующими и ингибирующими факторами. В большинстве случаев снижение концентрации Fe (например, гемолиз или кровотечение) вызывает снижение продукции гепсидина. Напротив, состояния острого воспаления, опосредованного IL-6, рака, хронических и аутоиммунных заболеваний, приводят к увеличению уровней гепсидина 12 . Согласно данным производителя, основанным на исследованиях, проведенных на здоровых взрослых людях, нормальный уровень гепсидина составляет 0.3–47,7 (нг / мл). Аналогичные результаты были получены болгарскими и голландскими исследователями и оцениваются в 3,1–37,7 (нг / мл) 15 . Кумар и др. . оценил средний уровень гепсидина в плазме у здоровых детей примерно на уровне 21,9 нг / мл 16 . В нашем исследовании мы стремились оценить концентрацию гепсидина у пациентов с гипотиреозом. Влияние любых других факторов, кроме статуса щитовидной железы, которые потенциально могут повлиять на гомеостаз гепсидина или Fe, было исключено. Средний уровень гепсидина в нашей группе пациентов с гипотиреозом составлял 17.4 (нг / мл) и снизился до 7,7 нг / мл после терапии.
Гормоны щитовидной железы играют важную роль в кроветворении, регулируя экспрессию генов и секрецию ЭПО в почках, что стимулирует пролиферацию предшественников эритроцитов 5,6,17,18 . Дефицит гормона щитовидной железы характеризуется снижением потребности тканей в кислороде. Физиологическая адаптация приводит к снижению секреции ЭПО, уменьшению количества и пролиферативной активности эритроидных клеток 19 и стимулированию накопления мукополисахаридов в костном мозге 20 .Эти процессы обращаются вспять после восстановления эутиреоза 1 .
Наши данные согласуются с текущей моделью, в которой пациенты с гипотиреозом имеют гипопролиферативную анемию с низким уровнем ЭПО, сопровождающимся сокращением объема, но с небольшим влиянием на концентрацию гемоглобина или без него. После коррекции гипотиреоза объем эритрона и плазмы увеличивается. Это может снизить уровень гепсидина за счет увеличения ЭПО, генерирующего эритроидный сигнал (например, эритроферрон), и за счет временного снижения сывороточного железа и накопленных запасов железа, которые используются для производства большего количества гемоглобина.Однако через 12 недель повышенное всасывание железа приведет к корректировке параметров железа, эритрон расширится, и будет достигнуто новое устойчивое состояние с более высоким обменом эритроцитов и более низким содержанием гепсидина. Это может быть отражено наблюдаемым увеличением концентрации RDW-CV, которая является чувствительным маркером гомеостаза Fe 21,22 .
Гипотиреоз также проявляется микседемой и уменьшением объема плазмы, что может привести к относительному завышению значений гемоглобина, скрывающему лежащую в основе анемию 19 .После восстановления эутиреоза и последующего увеличения объема плазмы не может наблюдаться никаких изменений уровня гемоглобина или даже снижения показателей эритроцитов. Таким образом, у пациентов с гипотиреозом повышенная RDW может быть первым признаком дисбаланса железа. В этих ситуациях более ценным индикатором состояния Fe может быть соотношение между стандартным отклонением объемов эритроцитов и MCV, умноженное на 100 (RDW-CV). Это могло бы объяснить наблюдаемые изменения значений RDW-CV при переходе от гипотиреоза к эутиреоидному состоянию в нашем исследовании, в то время как другие показатели эритроцитов остались неизменными.Было обнаружено, что этот параметр положительно коррелирует с ТТГ в здоровой популяции и был предложен Aktas et al . быть маркером гипотиреоза у женщин после исключения пациентов с железодефицитной анемией 21,23 . Клинически RDW в основном используется для выявления микроцитарной анемии 24 . Следовательно, более высокое значение параметра отражает большую степень анизоцитоза. Таким образом, когда происходит снижение RDW-CW, есть свидетельства улучшения баланса железа и лучшего поступления железа, что позволяет формировать эритроциты нормального объема, отражающие более эффективный эритропоэз.В нашем предыдущем исследовании пациентов с сердечной недостаточностью и гипотиреозом, прошедших терапию радиойодом, была выявлена сильная корреляция между уровнями ТТГ и RDW 22 . Более того, было обнаружено, что RDW положительно коррелирует с уровнями ТТГ в здоровой популяции, и это было предложено Aktas et al . быть маркером гипотиреоза у женщин после исключения пациентов с железодефицитной анемией 21,23 . Ю и др. . также сообщили о связи между RDW и TSH в большой когорте эутиреоидных и субклинических пациентов с гипотиреозом, где корреляция была наиболее сильной для TSH выше нормального диапазона 25 .В нашем исследовании пациентов с гипотиреозом уровни RDW-CV были в пределах нормы. Однако после восстановления эутиреоза наблюдалось статистически значимое улучшение, что может отражать снижение анизоцитоза. Между тем, не наблюдалось никаких существенных различий в уровнях Fe, ферритина, гемоглобина, HTC и RBC, что соответствует предыдущим отчетам 26 . Мы не наблюдали значительных изменений в количестве тромбоцитов (PLT) после введения L-тироксина, что противоречит предыдущим данным исследований на мышах, предполагающим, что гормоны щитовидной железы могут подавлять тромбоцитопоэз 27 .Хотя результаты MCV и MCH могут быть несколько неоднозначными, наши результаты совместимы с Horton et al ., Которые наблюдали уменьшение анизоцитоза после приема L-тироксина, несмотря на нормальный исходный уровень и значения MCV после лечения 28 .
Данных о концентрации гепсидина при дисфункции щитовидной железы недостаточно. В двух предыдущих исследованиях сравнивали концентрацию гепсидина у пациентов с гипертиреозом до и после успешного лечения. Первое исследование, проведенное Lehtihet et al ., не смогли продемонстрировать значительных различий в концентрации гепсидина или Fe в сыворотке при гипертиреозе по сравнению с эутиреоидным состоянием, что сопровождалось значительным повышением уровней ферритина 29 . Во втором исследовании Fischili et al . оценивая пациентов с гипертиреозом, вызванным болезнью Грейвса, авторы отметили, что уровни ферритина и гепсидина, измеренные только масс-спектрометрией и только в мужской подгруппе, показали статистически значимое снижение, также без изменений в уровнях Fe, в то время как гепсидин измерялся методом ELISA. не различались между группами 30 .В последнем исследовании нашей команды мы демонстрируем, что подострый тиреоидит связан со значительно более высокой концентрацией гепсидина по сравнению со значениями, полученными после достижения ремиссии болезни 31 . Однако, в отличие от настоящего исследования, у пациентов с подострым тиреоидитом наблюдается системное воспаление, которое генерирует воспалительный сигнал, опосредованный IL-6, который повышает уровень гепсидина. Это отражается в очень высоких уровнях СРБ при постановке диагноза, которые нормализуются во время ремиссии.Однако этот механизм не применялся у субъектов с ГТ, потому что уровень СРБ находился в пределах нормы при постановке диагноза и во время терапии, без каких-либо значительных изменений.
Предыдущие исследования также выявили взаимосвязь между гепсидином и половыми гормонами. Введение тестостерона мужчинам привело к снижению уровней гепсидина, в то время как наблюдалось повышение гемоглобина и гематокрита 32 . Более того, Guo et al . также продемонстрировали, что тестостерон подавляет транскрипцию гепсидина, воздействуя на сигнальный путь BMP / Smad 33 .Точно так же повышение уровня эндогенного эстрогена у женщин до оплодотворения in vitro , по-видимому, вызывает супрессию гепсидина 29 . Ян и др. . продемонстрировали, что 17-β-эстрадиол подавляет экспрессию гена гепсидина (HAMP) in vitro в клетках человека и, следовательно, увеличивает поглощение Fe 34 . Согласно Galesloot et al ., концентрация гепсидина зависит от эстрогенового статуса женщин, она самая низкая у молодых женщин и выше после менопаузы; однако он не зависит от возраста у мужчин 35 .Таким образом, чтобы гарантировать отсутствие влияния статуса эстрогена на концентрацию гепсидина, наша женская подгруппа полностью состояла из женщин пременопаузального возраста с регулярными менструальными кровотечениями.
Сообщалось также о нарушениях функции почек у пациентов с гипотиреозом 36 . В нашем исследовании мы обнаружили, что восстановление эутиреоза было связано со значительным улучшением СКФ и креатинина. Хотя почечные параметры были в пределах нормы как при гипотиреозе, так и при эутиреоидном состоянии, после достижения эутиреоза СКФ и креатинин значительно улучшились.Перспективное наблюдение ден Холландера и др. . также сообщил о подобных результатах 37 .
В большинстве предыдущих исследований сообщалось о положительной корреляции уровней гепсидина и ферритина у детей 38 , пациентов отделения интенсивной терапии 39 и пациентов с респираторными заболеваниями 40 и васкулитом 41 . Наши результаты изучения гипотиреоза и здоровых субъектов согласуются с предыдущими исследованиями. Куниредди и др. .сообщили о положительной корреляции уровней гепсидина и ферритина как в группе здоровых женщин, так и в другой группе, которая включала пациентов с аутоиммунными заболеваниями, такими как системная красная волчанка 42 .
Хотя в нашем исследовании представлены новые результаты, следует упомянуть некоторые ограничения. Поскольку размер выборки был относительно небольшим, наши результаты должны быть подтверждены будущими исследованиями на более крупных популяциях. Мы не сравнивали концентрацию гепсидина со здоровой контрольной группой, поскольку исследование было разработано для использования тех же пациентов в качестве их собственного контроля после успешного восстановления нормальной функции щитовидной железы.Сильными сторонами нашего проекта были строгие критерии включения и тщательный отбор пациентов, что позволило нам добиться ситуации, при которой только тирометаболический статус влиял на показатели гепсидина и эритроцитов у исследуемых пациентов.
В заключение, результаты нашего исследования позволяют предположить, что успешное лечение гипотиреоидных пациентов с ГТ и восстановление эутиреоидного состояния связано со снижением концентрации гепсидина, которое следует наблюдаемой динамике гомеостаза железа.Это отражается в соответствующем улучшении RDW-CV и значительной корреляции между уровнями как гепсидина, так и ферритина, а также гепсидина и fT3.
Восстановление эутиреоза не может улучшить качество жизни
Eustatia-Rutten CFA et al . (2006) Качество жизни при долгосрочном экзогенном субклиническом гипертиреозе и эффекты восстановления эутиреоза, рандомизированное контролируемое исследование. Clin Endocrinol 64 : 284–291
Группа ученых из Нидерландов сообщила об эффектах восстановления эутиреоза у пациентов с субклиническим гипертиреозом в результате длительной терапии, подавляющей ТТГ, после лечения дифференцированного рака щитовидной железы (DTC).
В общей сложности 24 пациента с DTC в анамнезе, которые прошли терапию, подавляющую ТТГ> 10 лет, завершили исследование. Половина этих пациентов продолжала существующую терапию ТТГ (группа с низким ТТГ), в то время как другая половина получала уменьшающиеся дозы левотироксина, тем самым восстанавливая эутиреоз (группа эутиреоидов).Все участники заполнили пять анкет, в которых оценивались различные аспекты качества жизни (КЖ) на исходном уровне и через 6 месяцев. Удивительно, но исходные симптомы гипертиоидизма не отличались от контрольных значений; однако показатели СОМАТОФОРМОВОГО НАРУШЕНИЯ были заметно выше контрольных значений.
Вопреки ожиданиям исследователей улучшения показателей качества жизни через 6 месяцев, большинство результатов для эутиреоидной группы были сопоставимы с их исходными показателями. Единственные существенные изменения произошли в двух анкетах: в одном из пяти параметров утомляемости и в одном из восьми параметров общего самочувствия.
Авторы предупреждают, что их результаты трудно сравнивать с результатами предыдущих исследований. Опыт выживания в DTC может улучшить воспринимаемое качество жизни, уравновешивая любые негативные эффекты субклинического гипертиреоза. Базовые показатели депрессии в обеих группах были значительно лучше, чем у населения в целом; кроме того, оценки симптомов гипертиреоза не превышали таковых в контрольной группе. В целом эти результаты показывают, что взаимосвязь между субклиническим гипертиреозом, симптомами и качеством жизни является сложной.
Об этой статье
Цитируйте эту статью
Sole, K. Восстановление эутиреоза не может улучшить качество жизни. Nat Rev Endocrinol 2, 307 (2006). https://doi.org/10.1038/ncpendmet0184
Ссылка для скачивания
Лечение гипертиреоза у молодых людей
Болезнь Грейвса редко встречается в детстве, но все чаще встречается в подростковом и юношеском возрасте.Существует сильная семейная предрасположенность, но первопричина неизвестна. Стимуляция рецептора тиреотропного гормона (ТТГ) аутоантителами вызывает чрезмерное производство и секрецию тироидных гормонов и диффузное увеличение щитовидной железы. Могут быть вовлечены и другие системы, особенно глаза с проптозом. У детей ранние симптомы гипертиреоза неспецифичны и могут проявляться постепенно; если нет явного зоба, часто подозревается психологическое или поведенческое расстройство.После рассмотрения диагноз легко подтверждается биохимически повышенными концентрациями циркулирующих гормонов щитовидной железы и подавлением ТТГ.
Целью лечения является восстановление и поддержание постоянного эутиреоза как можно безопаснее, быстрее и удобнее. В частности, среди молодежи нет единого мнения о том, как этого лучше всего достичь, и в этой аннотации мы рассмотрим варианты.
Первоначальное руководство
Симптомы гипертиреоза могут вызывать беспокойство и могут быть быстро купированы в значительной степени за счет блокирования периферических эффектов избытка гормонов щитовидной железы.Β-блокирующий агент, такой как пропранолол, 1 мг / кг / день в разделенных дозах, эффективен и полезен для поддержки пациента до тех пор, пока болезнь не станет контролируемой.
Одновременно можно начать прием антитиреоидного препарата. Тионамидные препараты блокируют синтез гормонов щитовидной железы, а также обладают плохо изученным иммунодепрессивным действием при болезни Грейвса.1 Карбимазол более широко используется в Европе, а пропилтиоурацил в Соединенных Штатах; хотя их действия и профили побочных эффектов немного отличаются, на практике они взаимозаменяемы.Карбимазол от 0,5 до 1,0 мг / кг / день или пропилтиоурацил от 5 до 10 мг / кг / день в разделенных дозах позволяет контролировать гипертиреоз болезни Грейвса за четыре-восемь недель.
Если есть срочная необходимость вылечить болезнь как можно скорее, можно безопасно приступить к тиреоидэктомии, но большинство клиницистов предпочитают пробное лечение в надежде, что наступит длительная ремиссия. Это влечет за собой лечение антитиреоидными препаратами от 18 месяцев до двух лет под регулярным наблюдением.Когда циркулирующие гормоны щитовидной железы восстанавливаются до нормального уровня, лечение можно сократить до разовой суточной дозы и титровать с помощью обычных тестов функции щитовидной железы для поддержания эутиреоза. Более удобный подход состоит в том, чтобы продолжать прием антитиреоидного препарата без изменений и добавлять тироксин 100 мкг / м 2 / день по схеме «блокируй и заменяй» 2. Хотя воздействие антитиреоидного препарата в полной дозировке продолжается, требуется меньший мониторинг и эутиреоз сохраняется более надежно.
Как и при любом долгосрочном лечении, многим пациентам и их семьям чрезвычайно трудно помнить о регулярном приеме лекарств. Примерно у 2–5% пациентов появляется сыпь или другие незначительные побочные эффекты при приеме антитиреоидных препаратов (обычно тошнота, головная боль или артралгия). Если симптомы легкие, симптомы обычно преходящие, но если они сохраняются, пациента можно перевести на другой основной агент, поскольку перекрестная чувствительность необычна. Серьезные побочные эффекты возникают редко, особенно у молодых пациентов, но включают нейтропению, агранулоцитоз (который почти всегда обратим) и гепатотоксичность.3 4 Подобные эффекты обычно проявляются в первые несколько месяцев лечения. Их нельзя предсказать путем частого наблюдения, поэтому пациентов и родителей необходимо предупредить о необходимости незамедлительно сообщать о любых эпизодах значительной температуры, боли в горле или других симптомах. Наша практика — запрашивать анализ крови при проверке функции щитовидной железы, но не заказывать анализы в противном случае.
По окончании курса лечения препараты отменяются, и у ребенка наблюдается рецидив гипертиреоза.Рецидив более вероятен у детей, чем у взрослых, а также у детей с низким индексом массы тела и большим зобом на момент обращения. 6 Уровень ремиссии у детей в США, как сообщается, составляет 25% после каждого из повторных двухлетних курсов лечения 7, при этом частота ремиссии составляет около 50–65% во время исследований взрослых5. 8 Из широкого разнообразия биохимических маркеров и динамических тестов, которые были исследованы в надежде найти метод прогнозирования рецидива, ни один не оказался надежным. Хашизуме и его коллеги9 сообщили, что введение тироксина во время и после лечения антитиреоидными препаратами значительно улучшило скорость ремиссии, возможно, за счет снижения презентации антигена, но недавние исследования не подтвердили их выводы.10 11 Рецидив обычно возникает в течение первых нескольких месяцев после отмены лечения, но может быть отсрочен надолго. Пациенты, находящиеся в стадии ремиссии от болезни Грейвса, также подвергаются повышенному риску развития гипотиреоза в будущем, поэтому есть основания для продолжения нечастых проверок функции щитовидной железы.
В случае рецидива есть три варианта: (1) возобновить лечение антитиреоидными препаратами; (2) перейти к тиреоидэктомии; (3) лечить ребенка радиоактивным йодом. Здесь существует трансатлантический разрыв в подходах.В Европе субтотальная или тотальная тиреоидэктомия в целом была единственным вариантом, предлагаемым для окончательного лечения2. Некоторые американские отделения продолжают сообщать об отличных хирургических результатах12, но во многих центрах13–15 лечение радиоактивным йодом является предпочтительным для всех возрастных групп.
Дальнейшее лечение
Если лечение переносится хорошо и регулярное наблюдение с тестированием функции щитовидной железы не является обременительным, некоторые пациенты и их семьи предпочтут возобновить лечение антитиреоидными препаратами.Это может быть следующий полный курс с надеждой на ремиссию в конце — что можно ожидать у 25% тех, кто рецидивировал после первого курса лечения — или на более короткий срок, с окончательным лечением, запланированным на удобный момент.
Тиреоидэктомия
Surgery предоставляет один окончательный терапевтический вариант. В прошлом предпочтение было отдано частичной тиреоидэктомии с целью оставить достаточно ткани щитовидной железы, чтобы ребенок оставался эутиреоидным. Слишком консервативная операция привела к высокому уровню повторного гипертиреоза и слишком радикальной тиреоидэктомии при гипотиреозе; любая из этих проблем может непредсказуемо возникнуть много лет спустя.16-18 Большинство хирургов сейчас стремятся вылечить гипотиреоз у ребенка при первой операции, удалив практически всю железу. Как только подтвердится гипотиреоз, можно начинать заместительную терапию тироксином. Хотя соблюдение режима заместительной терапии остается проблемой, корректировка дозы тироксина в течение многих лет роста и развития является несложной задачей, и никаких дальнейших изменений не требуется, когда пациент полностью вырастет. Во многих регионах Соединенного Королевства в настоящее время ведутся регистры щитовидной железы, и за пациентами могут наблюдать их терапевты без необходимости постоянного осмотра в больнице.
Необходимо непродолжительное пребывание в больнице, и потенциальные проблемы включают дискомфорт во время операции, рубец (который может образовывать келоид), небольшой, но заметный риск общих анестезиологических и хирургических осложнений, особые риски повреждения возвратных гортанных нервов и преходящий или постоянный гипопаратиреоз. Все эти риски снижаются в руках опытных хирургов, специализирующихся на щитовидной железе, но такой опыт сейчас редок, когда гипертиреоз у взрослых обычно лечится радиоактивным йодом.
Радиоактивный йод
Этот изящный метод лечения был впервые использован 50 лет назад и зарекомендовал себя с замечательными показателями безопасности.19 Радиойод можно назначать с целью вывести пациента из состояния эутиреоза или в более высоких дозах с особым намерением удалить железу и принять стойкий гипотиреоз. Корректировка дозы в зависимости от размера и поглощения железы может привести к временному восстановлению эутиреоза, но на каком-то этапе вероятно прогрессирование до гипотиреоза.Поскольку основная цель окончательного лечения — избавить пациента от необходимости длительного наблюдения, 17 20 многие центры в настоящее время приняли политику абляции щитовидной железы и согласились с необходимостью замены тироксина21; это особенно подходит для детей.
Высказывались опасения, что лечение радиойодом может усугубить офтальмопатию Грейвса, и для предотвращения этого осложнения было рекомендовано лечение стероидами. 23 По нашему собственному опыту и опыту других этот эффект не оказался проблемой; Заболевание глаз не следует рассматривать как противопоказание к лечению радиоактивным йодом.23
В прошлом во многих центрах использование радиоактивного йода было ограничено пациентами старше репродуктивного возраста. Сейчас, когда растет уверенность в его безопасности, он используется на протяжении всей взрослой жизни, но по-прежнему часто отказывают детям и подросткам из-за сохраняющихся опасений по поводу возможности долгосрочных побочных эффектов. Эти опасения вполне уместны, но после 50 лет использования радиоактивного йода нет никаких доказательств их обоснованности.
Хорошо известно, что внешнее облучение вызывает рак щитовидной железы24, и канцерогенез также может быть результатом воздействия низких доз 131 I, как это было видно после аварии на Чернобыльской АЭС в бывшем Советском Союзе.25 26 К счастью, риск рака щитовидной железы в будущем может быть устранен путем удаления железы, и это является сильным дополнительным аргументом в пользу использования этого подхода при лечении молодых пациентов27. 28 Нет данных об увеличении заболеваемости лейкемией 29, снижении фертильности или повреждении половых клеток13. 30 после терапевтического радиоактивного йода. В большой группе пациентов, в основном взрослых, которые получили среднюю дозу 506 МБк и наблюдались в среднем в течение 15 лет, общего увеличения заболеваемости раком не наблюдалось, 28 хотя небольшое превышение рака желудка наблюдалось только в этом одном исследовании. .
Хотя вполне вероятно, что сильно отсроченные побочные эффекты радиоактивного йода у молодых людей еще могут проявиться, многие клиницисты в настоящее время рассматривают радиоактивный йод в качестве лечения первого выбора для молодых пациентов с болезнью Грейвса, у которых после медикаментозного лечения рецидивы рецидивируют. Радиойод стал еще более приемлемым вариантом, поскольку стало очевидно, что пожизненная замена тироксина также необходима после операции.
За последние 10 лет мы пролечили радиоактивным йодом восемь молодых пациентов.Им была дана начальная доза 131 I в 300 Мбк с целью удаления железы. Лечение было возобновлено на шесть месяцев, а затем прекращено. У четырех пациентов развился гипотиреоз после однократной дозы радиоактивного йода, но четверым потребовалась вторая доза. У всех появился гипотиреоз в течение двух лет. Побочных эффектов не наблюдалось, в частности, не было ухудшения глазных болезней ни у одного пациента.
После лечения радиоактивным йодом необходимо соблюдать некоторые меры предосторожности. Следует избегать тесного и продолжительного физического контакта с другими людьми в течение трех дней, и мы рекомендуем детям не посещать школу в течение двух недель.31 Для девочек более старшего возраста следует подчеркнуть важность предотвращения беременности в течение как минимум шести месяцев.32
Выводы
После того, как болезнь Грейвса диагностирована, ее можно легко контролировать, но идеальной формы лечения для молодых людей не существует. Подробное обсуждение преимуществ, недостатков и рисков каждой из различных форм лечения важно, чтобы терапевтический план мог учитывать потребности и пожелания пациента и семьи.
Если нет веских причин для поиска быстрого излечения, рекомендуется первоначальное испытание лечения по схеме «блокируй и заменяй» в течение 18–24 месяцев.Для большинства пациентов, у которых наблюдается рецидив после отмены лечения антитиреоидными препаратами, лечение можно возобновить, но следует рассмотреть возможность окончательного лечения. Если доступны отличные хирургические услуги, полная тиреоидэктомия с последующей заменой тироксина является окончательным решением с низким риском. Лечение радиоактивным йодом предлагает простую альтернативу без краткосрочных рисков и с отличными показателями безопасности в долгосрочной перспективе, что оправдывает его использование у молодых пациентов. Имея выбор, многие выберут эту форму лечения, и наш опыт показывает, что доза 131 I в 400 мбк уменьшит количество пациентов, которым требуется вторая доза.Мы рекомендуем подход, при котором удаляется железа и признается необходимость замены тироксина.
Синдром больного эутиреоидом — интегративная медицина, деревня Элк-Гроув,
Патрик Мэсси MD, PhDALT-MED Лечебная и физиотерапия
Elk Grove Village Il и обслуживает район Чикаго
Синдром эутиреоза — это заболевание (не заболевание), при котором у пациента проявляются многие симптомы гипотиреоза — усталость, увеличение веса, бессонница, сухость кожи, депрессия, беспокойство, снижение памяти / концентрации. , низкое либидо, мышечные боли и т. д. — и при этом у вас нормальный или низкий / нормальный уровень тиреотропного гормона (ТТГ), Т3 и Т4.(Видео доктора Мэсси на сайте SES, щелкните здесь)
Синдром эутиреоидного синдрома является результатом большего стресса, чем может выдержать организм, и организм пытается сберечь ресурсы. Тело начинает вырабатывать гормон щитовидной железы (обратный Т3), который отключает его … в спячку.
Большинство врачей не верят, что синдром больного эутиреоидом существует за пределами отделения интенсивной терапии и что он редко встречается среди населения. Однако недавние медицинские исследования показали, что симптомы эутиреоидного синдрома часто обнаруживаются у пациентов со стрессовыми хроническими заболеваниями, такими как рак, диабет и болезни сердца….если вы его ищите. Доктор Мэсси также диагностировал синдром больного эутиреоидом у пациентов с тяжелым хроническим стрессом без других заболеваний. Лечение синдрома больного эутиреоидом может восстановить энергию и жизнеспособность. По определению, пациенты с синдромом больного эутиреоидом также имеют усталость надпочечников.
Традиционной медикаментозной терапии эутиреоидного синдрома не существует. Однако интегративная медицина сочетает в себе лучшее из традиционной медицины, дополнительной и альтернативной медицины… и имеет решение. Синдром больного эутиреоидом — это не болезнь, а терапия — это не пожизненный процесс.Большинство пациентов хорошо себя чувствуют как в краткосрочной, так и в долгосрочной перспективе.
Подход интегративной медицины ALT-MED адаптирован к конкретному пациенту и может включать следующее:
- Тесты для подтверждения эутиреоидного синдрома и утомления надпочечников
- Специальные препараты для лечения щитовидной железы — краткосрочные — при необходимости
- Специальные добавки для улучшения функции надпочечников и стресса
- Витамины для внутривенного введения (нажать)
- Изменения образа жизни
- Энергетическая медицина для снижения стресса и баланса потока энергии (нажмите здесь)
- Иглоукалывание для снятия стресса, увеличения энергии (нажмите здесь)
- Массаж для снятия стресса, увеличения гормонов «релаксации» (нажмите здесь)
Мы можем помочь…позвоните (847) 923-0046
Гипотиреоз — AMBOSS
Резюме
Гипотиреоз — это состояние, при котором щитовидная железа недостаточно активна, что приводит к дефициту тиреоидных гормонов трийодтиронина (Т3) и тироксина (Т4). В редких случаях выработка гормонов может быть достаточной, но гормоны щитовидной железы могут иметь недостаточное периферическое действие. Гипотиреоз может быть врожденным или приобретенным. Если врожденный, это обычно результат дисплазии или аплазии щитовидной железы.Этиология приобретенного гипотиреоза обычно бывает аутоиммунной (тиреоидит Хашимото) или ятрогенной. Патофизиология при гипотиреозе характеризуется в основном снижением скорости основного обмена и генерализованной микседемой. Типичные клинические проявления включают утомляемость, непереносимость холода, увеличение веса и периорбитальный отек. Более серьезные проявления включают микседематозную болезнь сердца и микседематозную кому, которые могут быть фатальными, если их не лечить. У детей с врожденным гипотиреозом часто возникают пупочные грыжи, и без своевременного лечения у них развивается синдром врожденной йодной недостаточности (умственная отсталость, задержка роста).Соответственно, неонатальный скрининг на гипотиреоз через 24–48 часов после рождения является обязательным по закону в большинстве штатов. У взрослых диагноз устанавливается на основании уровня тиреотропного гормона (ТТГ) и свободного Т4 (FT4) в сыворотке крови. Терапия как приобретенного, так и врожденного гипотиреоза состоит из пожизненного лечения левотироксином (L-тироксином) и регулярных осмотров для контроля активности заболевания.
Эпидемиология
Эпидемиологические данные относятся к США, если не указано иное.
Этиология
- Спорадические (∼ 85% случаев) [3]
- Наследственный (около 15% случаев)
Приобретенный гипотиреоз
Патофизиология
Гипоталамус, передняя доля гипофиза и щитовидная железа вместе с их соответствующими гормонами составляют саморегулирующуюся цепь, называемую «гипоталамо-гипофизарная». ось щитовидной железы ».
Последствия гипотиреоза
[5] [6]Клинические особенности
Общие признаки и симптомы
- Симптомы, связанные со снижением метаболизма
- Утомляемость, снижение физической активности
- Непереносимость холода
- Снижение потоотделения
- Выпадение волос, ломкость ногтей и холодная сухая кожа
- Увеличение веса (несмотря на плохой аппетит)
- Запор
- Брадикардия
- Гипотиреоидная миопатия; , миалгия, скованность, судороги
- Признак Вольтмана: замедленное расслабление глубоких сухожильных рефлексов, которое обычно наблюдается у пациентов с гипотиреозом, но также может быть связано с пожилым возрастом, беременностью и сахарным диабетом.
- Синдром защемления (например, синдром запястного канала)
- Симптомы, связанные с генерализованной микседемой
- Симптомы гиперпролактинемии
- Дополнительные симптомы
Пациенты пожилого возраста могут не иметь типичных симптомов гипотиреоза. Вместо этого может показаться, что у них слабоумие или депрессия.
Врожденный гипотиреоз
Дети с врожденным гипотиреозом могут иметь общие признаки и симптомы гипотиреоза в дополнение к тем, которые типичны для новорожденных (см. Ниже).
У большинства детей с врожденным гипотиреозом симптомы отсутствуют во время рождения, поскольку плацента снабжает плод материнским гормоном щитовидной железы. По этой причине неонатальный скрининг жизненно важен, даже если у детей нет симптомов. Необратимых умственных нарушений можно избежать, если начать адекватную терапию на раннем этапе!
Чтобы запомнить характерные проявления синдрома врожденного дефицита йода, подумайте о «7 П»: пузатый, бледный, пухлое, выпирающий пупок, выпирающий язык, плохое развитие мозга и длительная желтуха новорожденных.
Диагностика
Неонатальный скрининг для измерения уровня ТТГ через 24–48 часов после рождения требуется по закону. Повышенный уровень ТТГ указывает на врожденный гипотиреоз.
Приобретенный гипотиреоз
Базовая стратегия диагностики
Первым шагом является определение уровней ТТГ, за которым может следовать измерение уровней FT4 для подтверждения или исключения подозреваемого диагноза.
Обзор изменений уровня гормонов
ТТГ также изменяется при гипертиреозе.Однако при гипертиреозе FT3 и FT4 будут увеличены.
Дополнительные диагностические соображения
[9]Комбинация следующих трех диагностических инструментов может быть полезна для различения различных состояний, влияющих на щитовидную железу, таких как дифференциация экзогенного гипертиреоза от эндогенного.
Исключение других состояний, которые могут имитировать гипотиреоз, может быть полезным в диагностике.
Нормальные уровни ТТГ с большой вероятностью исключают первичный гипотиреоз и гипертиреоз и, следовательно, являются решающим параметром при скрининге обоих состояний.
Дифференциальный диагноз
Синдром эутиреоидной болезни (СЭБ)
- Синонимы: синдром слабого эутиреоида (СЭС), синдром не тиреоидного заболевания (НТИ)
- Этиология: возникает при тяжелом заболевании или тяжелом физическом стрессе (чаще всего у пациентов интенсивной терапии).
- Патофизиология
- Клинические признаки: характерны для основного заболевания, не связанного с щитовидной железой
- Лаборатория
- Синдром низкого уровня Т3: снижение как общего уровня, так и уровня FT3, нормального уровня FT4 и ТТГ и повышенного обратного T3
- Синдром низкого T3 низкого T4: уровни FT4 могут быть низкими при длительном течении болезни (указывает на плохой прогноз)
- Лечение
- Лечить основное заболевание
- Замена гормона щитовидной железы обычно не рекомендуется, поскольку функция щитовидной железы в норме (нет убедительных доказательств того, что заместительная терапия гормоном щитовидной железы полезна для пациентов с ESS)
- Определение: недостаточная чувствительность органов-мишеней к гормонам щитовидной железы.
- Этиология: нарушение метаболизма гормонов щитовидной железы, транспорта или взаимодействия рецепторов в результате генетических мутаций
- Клинические признаки: Возможны симптомы как гипотиреоза, так и гипертиреоза.
- Лабораторные исследования: типично стойкое повышение FT4 и FT3 и отсутствие подавления ТТГ.
- Терапия: нет причинной терапии.
Перечисленные здесь дифференциальные диагнозы не являются исчерпывающими.
Лечение
Замена L-тироксина
[9]- Лекарственные препараты
- L-тироксин (левотироксин, синтетическая форма Т4): периферически превращается в Т3 (биологически активный) и rT3 (биологически неактивный)
- Лиотиронин: синтетическая форма трийодтиронина (Т3).
- Общие принципы
- Пожизненная замена
- Быстрое инициирование
- Показания
- Побочные эффекты
- Взаимодействия
- Регулярное наблюдение с лабораторным контролем функции щитовидной железы (ТТГ); при необходимости корректировка дозировки
| Уровни ТТГ | Метаболизм щитовидной железы | Т4-доза | |||
|---|---|---|---|---|---|
| Высокая | Пониженная | Повышенная | 907 24 Нормальная 907 Низкая | Повышенная | Уменьшенная |
Особые соображения
- Дети с врожденным гипотиреозом. Нормализация уровня гормонов щитовидной железы в течение 2–3 недель жизненно важна для предотвращения повреждения мозга и нарушений развития. [16]
- Беременные женщины с гипотиреозом в анамнезе: доза левотироксина должна быть увеличена, но после родов должна быть снижена до уровня до беременности.
- Пациенты с анорексией: синтетические гормоны щитовидной железы иногда неправильно используются для снижения веса.
- Пожилые пациенты или пациенты с ранее существовавшими сердечно-сосудистыми заболеваниями: начните прием левотироксина с более низкой дозы и постепенно увеличивайте дозу.
- Замена L-тироксина при субклиническом гипотиреозе, если:
- ТТГ ≥ 10 мЕд / л
- ТТГ 7.0–9,9 мЕд / л у бессимптомных пациентов
- ТТГ выше верхней границы нормы до 6,9 мЕд / л у пациентов с симптомами
У беременных с гипотиреозом доза L-тироксина должна быть увеличена в связи с повышенным спросом. Гипотиреоз отрицательно сказывается на развитии нервной системы плода.
Осложнения
Микседема кома
[17]Микседема кома — чрезвычайно редкое состояние, вызванное декомпенсацией существующего дефицита гормонов щитовидной железы и может быть вызвано инфекциями, хирургическим вмешательством или травмой.Кома микседема является потенциально опасным для жизни состоянием и, если ее не лечить, приводит к летальному исходу примерно в 40% случаев. [18]
- Клиническая картина
- Диагноз [19]
- Лечение
При клиническом подозрении на микседемную кому лечение следует начинать, не дожидаясь результатов лабораторных исследований.
Дополнительные осложнения
Мы перечисляем наиболее важные осложнения. Выбор не исчерпывающий.
Ежедневная терапия тироксином по сравнению с альтернативной дневной терапией для поддержания эутиреоза у детей с врожденным гипотиреозом | Международный журнал эндокринологии и метаболизма
Бонгерс-Шоккинг Дж. Дж., Кут Х. М., Вирсма Д., Веркерк PH, де Мюнк Кейзер-Шрама С. М.. Влияние времени и дозы заместительной гормона щитовидной железы на развитие младенцев с врожденным гипотиреозом. J Pediatr. 2000; 136 (3): 292 -7 [DOI] [PubMed]
Фишер Д.А. Клинический обзор 19: Лечение врожденного гипотиреоза. J Clin Endocrinol Metab. 1991; 72 (3): 523 -9 [PubMed]
Haynes Jr RC, Murad F. Тиреоидные и антитиреоидные препараты. 1980;
Сток Джеррольд М., Суркс Мартин I, Оппенгеймер Джек Х. Замещающая доза L-тироксина при гипотиреозе: переоценка. New Engl J Med. 1974; 290 (10): 529 -533
Кек Ф.С., Лоос У. Периферическая ауторегуляция тиромиметической активности у человека. Horm Metab Res. 1988; 20 (2): 110 -4 [DOI] [PubMed]
Bornschein A, Paz-Filho G, Graf H, Carvalho GA. Лечение первичного гипотиреоза еженедельными дозами левотироксина: рандомизированное слепое перекрестное исследование. Arq Bras Endocrinol Metabol. 2012; 56 (4): 250 -8 [PubMed]
Поганка СК, Кук Р.Р., Форд ХК, Fagerstrom JN, Кордвелл Д.П., Рычаг NA, и другие. Лечение гипотиреоза тироксином 1 раз в неделю. J Clin Endocrinol Metab. 1997; 82 (3): 870 -5 [PubMed]
Sekadde CB, Slaunwhite WR, Aceto T, Murray Kl. Прием тироксина 1 раз в неделю. J Clin Endocrinol Metabol. 1974; 39 (4): 759 -764
Ривкиз С.А., Хардин Д.С. Кретинизм после еженедельного приема левотироксина для лечения врожденного гипотиреоза. J Pediatr. 1994; 125 (1): 147 -9 [PubMed]
Тейлор Дж., Уильямс Б.О., Брат Дж., Стотт Диджей, Коннелл Дж.Дозирование два раза в неделю для заместительной терапии тироксином у пожилых пациентов с первичным гипотиреозом. J Int Med Res. 1994; 22 (5): 273 -7 [PubMed]
Vermeire E, Hearnshaw H, Van Royen P, Denekens J. Приверженность пациентов лечению: три десятилетия исследований. Всесторонний обзор. J Clin Pharm Ther. 2001; 26 (5): 331 -42 [PubMed]
Ранган С., Тахрани А.А., Маклеод А.Ф., Мулик П.К.Еженедельное лечение тироксином как стратегия лечения несоблюдения режима лечения. Postgrad Med J. 2007; 83 (984) [DOI] [PubMed]
Азизи Ф. Уровни гамма-глутамилтранспептидазы при заболеваниях щитовидной железы. Arch Intern Med. 1982; 142 (1): 79 -81 [PubMed]
Foldes J, Tarjan G, Banos C, Nemeth J, Varga F, Buki B. Биологические маркеры крови, отражающие эффект гормона щитовидной железы на уровне периферических тканей у пациентов, получающих заместительную терапию левотироксином для лечения гипотиреоза. Acta Med Hung. 1991; 48 (1-2): 33 -43 [PubMed]
Гоу С.М., Колдуэлл Дж., Тофт А.Д., Беккет Дж. Дж. Различные реакции печени на замену тироксина при спонтанном и индуцированном 131I первичном гипотиреозе. Clin Endocrinol (Oxf). 1989; 30 (5): 505 -12 [PubMed]
Стауб JJ, Альтхаус БУ, Энглер Х, Ryff AS, Трабукко П, Марквардт К., и другие. Спектр субклинического и явного гипотиреоза: влияние на тиреотропин, пролактин и тироидный резерв, а также метаболическое воздействие на периферические ткани-мишени. Am J Med. 1992; 92 (6): 631 -42 [PubMed]
Буджак Н, Пахт А, Мандель Х, Янку Т. Тамир А, Сруго I, и другие. Значение изолированного повышения сывороточных аминотрансфераз у младенцев и детей раннего возраста. Arch Dis Child. 2007; 92 (12): 1109 -12 [DOI] [PubMed]
Таргер Г, Монтаньяна М, Сальваньо Г, Могетти П, Зоппини Дж., Muggeo M, и другие. Связь между сывороточным ТТГ, свободным Т4 и активностью сывороточных ферментов печени в большой когорте неотобранных амбулаторных пациентов. Clin Endocrinol (Oxf). 2008; 68 (3): 481 -4 [DOI] [PubMed]
Пеппа М., Бетси Г., Димитриадис Г. Нарушения липидов и кардиометаболический риск у пациентов с явным и субклиническим заболеванием щитовидной железы. J Липиды. 2011; 2011 : 575840 [DOI] [PubMed]
Mosekilde L, Eriksen EF, Charles P. Влияние гормонов щитовидной железы на метаболизм костей и минералов. Endocrinol Metab Clin North Am. 1990; 19 (1): 35 -63 [PubMed]
Фишер Д.А. Важность раннего лечения для оптимизации IQ у младенцев с врожденным гипотиреозом. J Pediatr. 2000; 136 (3): 273 -4 [DOI] [PubMed]
Морреале де Эскобар Г., Обрегон М. Дж., Кальво Р., Эскобар дель Рей Ф. Влияние дефицита йода на метаболизм гормонов щитовидной железы и мозг у плодных крыс: роль материнского переноса тироксина.