Первичный билиарный холангит — симптомы, причины и лечение
Как лечится первичный билиарный холангит?
Лечение болезни
Лекарства от ПБЦ неизлечимо, однако есть лекарства, которые могут помочь замедлить прогрессирование заболевания и облегчить симптомы. Урсодиол (торговые марки Actigall, URSO 250, URSO Forte) — это встречающаяся в природе желчная кислота (урсодезоксихолевая кислота или УДХК), которая помогает перемещать желчь из печени в тонкий кишечник. При достаточно раннем применении Урсодиол может улучшить функцию печени и избавить вас от необходимости или отсрочить потребность в пересадка печени. Люди с ПБЦ должны принимать это лекарство каждый день на всю жизнь.
УДХК эффективна более чем у 50 процентов пациентов, но до 40 процентов пациентов не достигают адекватного снижения щелочной фосфотазы (ЩФ) или билирубина с УДХК, а 5-10 процентов не переносят УДХК.
В мае 2016 года обетихолевая кислота (торговая марка Ocaliva) была одобрена для лечения ПБЦ в комбинации с УДХК у взрослых с неадекватным ответом на УДХК или в качестве единственной терапии у взрослых, не переносящих УДХК. Обетихолевая кислота увеличивает отток желчи от печени и подавляет выработку желчной кислоты в печени, тем самым снижая воздействие на печень токсичных уровней желчных кислот. Побочные эффекты обетихолевой кислоты могут включать усиление зуда и повышение уровня липидов в крови.
Другие альтернативные методы лечения пациентов с неполным ответом на УДХК включают фенофибрат. Также могут быть назначены лекарства для подавления иммунной системы, включая преднизон или азатиоприн, пациентам с ПБЦ с «синдромом перекрытия» с аутоиммунным гепатитом. Трансплантация печени рассматривается, когда медицинское лечение больше не контролирует болезнь. Когда у человека терминальная стадия заболевания печени, для выживания необходима трансплантация печени.
Лечение симптомов
Сильный зуд — один из наиболее частых симптомов ПБЦ. Могут быть полезны безрецептурные антигистаминные препараты, такие как дифенгидрамин (Бенадрил). Могут быть назначены другие агенты, такие как рифампицин, налтрексон, холестирамин и сертралин.
Могут быть полезны безрецептурные антигистаминные препараты, такие как дифенгидрамин (Бенадрил). Могут быть назначены другие агенты, такие как рифампицин, налтрексон, холестирамин и сертралин.
От сухости глаз можно избавиться, используя глазные капли (искусственные слезы).
При сухости во рту можно облегчить сосание леденцов или жевательной резинки, которые увеличивают выделение слюны. Также можно использовать заменители слюны и некоторые лекарства.
Предотвращение осложнений
Часто проводятся анализы крови для выявления дефицита жирорастворимых витаминов. По мере прогрессирования ПБХ некоторым людям необходимо восполнять жирорастворимые витамины, теряемые с жирным стулом, поэтому вам может быть назначена заместительная терапия витаминами A, D, E и K.
Поскольку люди с ПБЦ подвержены более высокому риску остеопороза, обычно назначают кальций и витамин D. На момент постановки диагноза в настоящее время рекомендуется исходная плотность костной ткани.
Поскольку способность печени функционировать со временем снижается, необходимо будет устранить и лечить осложнения, связанные с циррозом. Часто рекомендуется обследование на наличие варикозного расширения вен и рака печени.
Постхолецистэктомический синдром — диагностика и лечение в СПб, цена
Желчнокаменная болезнь (ЖКБ) — одно из наиболее распространенных заболеваний современного человека. Оно занимает третье место после сердечно-сосудистых заболеваний и сахарного диабета. В развитых странах ЖКБ встречается у 10-15% взрослого населения.
На территории России по поводу желчнокаменной болезни каждый год в медицинские учреждения обращаются примерно 1 млн. человек. Число ежегодно выполняемых холецистэктомий в целом по России занимает второе место, уступая лишь числу аппендэктомий. В Москве и других крупных городах проводится около 7000 операций на 100 000 населения в год.
Большинство этих операций в последние годы выполняются с помощью малоинвазивных технологий (хирургия малых доступов, эндовидеохирургия, транслюминальная хирургия). Так как количество операций по поводу ЖКБ постоянно растет, соответственно увеличивается и число больных с различными послеоперационными проблемами. По данным разных авторов, 1-2 из каждых 10 оперированных пациентов после выполнения холецистэктомии продолжают испытывать дискомфорт со стороны желудочно-кишечного тракта, боли, нарушения процесса пищеварения, повторные болевые приступы. Гастроэнтерологи объединяют такие симптомы термином
Терминология и классификация
Термин ПХЭС был введен в 30-е годы ХХ века американскими хирургами и используется до настоящего времени. Он объединяет большую группу патологических состояний в гепатопанкреатодуоденальной зоне, которые существовали до холецистэктомии, сопутствовали холециститу, осложнили его или возникли после операции. Во многом это объединение связано с тем, что при повторном обращении больного с жалобами после перенесенной холецистэктомии редко удается правильно поставить диагноз без многокомпонентного, комплексного обследования. При этом обобщающий термин ПХЭС используется в качестве временного диагноза в процессе обследования больного в соответствии с дифференциально-диагностическим алгоритмом. В дальнейшем, в большинстве случаев, удается выяснить причину жалоб больного и более общий термин уступает место конкретному диагнозу.
Все патологические состояния, которые наблюдаются у пациентов после удаления желчного пузыря, делят на две основные группы в зависимости от причин их возникновения:
- функциональные нарушения,
- органические поражения.
В свою очередь, к органическим относят:
- поражения желчных путей;
- поражения желудочно-кишечного тракта, среди которых следует выделить заболевания печени, поджелудочной железы и 12- двенадцатиперстной кишки;
- заболевания и причины, не связанные с желудочно-кишечным трактом.

Но сам ПХЭС, то есть состояние, возникшее после операции по удалению желчного пузыря, встречается крайне редко. Оно вызвано адаптационной перестройкой желчевыводящей системы в ответ на выключение из нее желчного пузыря — эластичного резервуара, в котором собирается и концентрируется желчь. В остальных случаях имеются заболевания, симулирующие ПХЭС.
Современные гастроэнтерологические исследования свидетельствуют, что у половины больных причиной жалоб служат функциональные нарушения пищеварения. Органические нарушения, которые находят у трети обращающихся, только в 1,5% случаев действительно являются следствием выполненной операции, и лишь 0,5% пациентов с установленным диагнозом ПХЭС требуют повторного оперативного вмешательства. Если установлен диагноз ПХЭС, неизбежно возникают вопросы, связанные с юридической и страховой ответственностью за нарушения, возникшие после оказания медицинской помощи. Поэтому среди многообразия патологических состояний, проходящих под маркой ПХЭС, предложено выделяют две основные группы в зависимости от характера причинно-следственных связей с предшествующей холецистэктомией:
- заболевания, не связанные с перенесенной операцией, — как правило,это диагностические ошибки;
- заболевания, являющиеся непосредственным следствием хирургического вмешательства, то есть операционная ошибка.
К диагностическим ошибкам относят:
- Не выявленные до операции сопутствующие заболевания или заболевания по своей клинической картине похожие на проявления желчнокаменной болезни. Это ситуации, когда произошла диагностическая ошибка и, хотя в результате операции и был убран заполненный конкрементами желчный пузырь, но истинный источник болей устранен не был.
- Заболевания других органов, расположенных в этой же области, которые никак не связаны с оперативным вмешательством, но по возникшим жалобам напоминают рецидив желчнокаменной болезни и после операции беспокоят больного.

К операционным ошибкам относят
- Резидуальный холедохолитиаз (оставленные в желчных протоках камни).
- Папиллостеноз (сужение области впадения желчных протоков в кишку).
- Опухоли желчных протоков и головки поджелудочной железы.
- Повреждения желчных протоков во время операции.
Большинство таких ошибок вызвано неполным дооперационным обследованием и следующим за ним несоответствием объема оперативного вмешательства характеру и стадии основного патологического процесса. Это, прежде всего, проявляется в лечении осложненных форм желчнокаменной болезни, когда выполняется только стандартная холецистэктомия вместо более расширенных вариантов вмешательства. В этом случае имеет место ошибка по формуле “неполный диагноз — недостаточный объем операции”.
И, наконец, самой опасной является группа прямых ятрогенных хирургических осложнений. Симптоматика ПХЭС у пациентов с различными абдоминальными расстройствами появляется в разные периоды после холецистэктомии, а иногда представляет собой продолжение тех же расстройств, которые были до операции и не прекратились после нее. Многообразие симптоматики и разные сроки ее появления определяются теми конкретными причинами, которые лежат в основе этих нарушений.
Причины «постхолецистэктомического синдрома»
1. Наиболее частой причиной ПХЭС являются камни желчевыводящих протоков (холедохолитиаз). Здесь важно отличить истинные рецидивы желчнокаменной болезни, когда конкременты в желчных протоках вновь образуются после выполненной холецистэктомии, и ложные, когда имеются резидуальные (оставшиеся, сохранившиеся) конкременты. Подавляющее большинство камней желчных протоков — это камни, не удаленные во время первой операции. “Забытые” камни составляют от 4 до 12% всех выполняемых холецистэктомий. В последние годы, после широкого внедрения в практическую медицину лапароскопических и эндоскопических технологий, стала изменяться хирургическая тактика лечения пациентов с желчнокаменной болезнью. В наше время холедохолитиаз не является противопоказанием к лапароскопической холецистэктомии и в отношении этой категории больных стандартным подходом считается двухэтапное лечение: эндоскопическая папиллосфинктеротомия и удаление конкремента из холедоха с последующей лапароскопической холецистэктомией. Возможна и обратная последовательность этапов, когда в холедохе выявляется одиночный конкремент небольших размеров, оставляемый для удаления эндоскопическим методом в послеоперационном периоде.
В наше время холедохолитиаз не является противопоказанием к лапароскопической холецистэктомии и в отношении этой категории больных стандартным подходом считается двухэтапное лечение: эндоскопическая папиллосфинктеротомия и удаление конкремента из холедоха с последующей лапароскопической холецистэктомией. Возможна и обратная последовательность этапов, когда в холедохе выявляется одиночный конкремент небольших размеров, оставляемый для удаления эндоскопическим методом в послеоперационном периоде.
2. Изменения большого дуоденального сосочка (БДС) как органического, так и функционального характера. Именно с этим нередко связано появление рецидивов болей после операции, температуры или желтухи, хотя желчный пузырь уже удален.
Причины функциональные. Выполненная холецистэктомия приводит к временному (до 6 месяцев) усилению тонуса сфинктера БДС у 85% больных. Подобное состояние чаще всего связано с одномоментным исчезновением рефлекторного влияния со стороны желчного пузыря на сфинктер. В дальнейшем, при отсутствии патологических изменений в органах гепатодуоденопанкреатической системы, тонус сфинктера нормализуется, восстанавливается нормальный пассаж желчи.
Органическое поражение БДС (стеноз) можно обнаружить почти у четверти больных, оперированных на желчных путях. Чаще он развивается в результате травматических повреждений при прохождении камней или расположении их в ампуле. Сначала появляется отек БДС, а при длительном воздействии и травматизации рубцовые изменения, приводящие к его сужению. Методом выбора для лечения стеноза БДС рубцового характера является эндоскопическая папиллосфинктеротомия.
У 5% пациентов, перенесших удаление желчного пузыря, причиной ПХЭС является недостаточность БДС, приводящая к нарушению запирательной функции и зиянию устья. В основе ее лежат дистрофические изменения стенки 12-перстной кишки с атрофией слизистой оболочки и деформацией клапанного аппарата. Свободное поступление содержимого 12-перстной кишки (рефлюкс) в желчные протоки через зияющий БДС приводит к холангиту и панкреатиту. Клиническая картина складывается из болей в эпигастрии и диспептических расстройств в виде чувства тяжести и вздутия, которые возникают после приема пищи. Фибродуоденоскопия позволяет выявить зияющий БДС. Более ценные сведения могут быть получены при рентгеноскопии желудка и дуоденографии: бариевая взвесь поступает в желчные протоки, иногда видна перерастянутая ампула БДС.
Свободное поступление содержимого 12-перстной кишки (рефлюкс) в желчные протоки через зияющий БДС приводит к холангиту и панкреатиту. Клиническая картина складывается из болей в эпигастрии и диспептических расстройств в виде чувства тяжести и вздутия, которые возникают после приема пищи. Фибродуоденоскопия позволяет выявить зияющий БДС. Более ценные сведения могут быть получены при рентгеноскопии желудка и дуоденографии: бариевая взвесь поступает в желчные протоки, иногда видна перерастянутая ампула БДС.
При выявлении данной патологии лечение начинают с консервативного устранения воспалительных изменений в 12-перстной кишке. Обнаружение органических причин, обуславливающих дуоденостаз и дуоденобилиарный рефлюкс, является показанием к хирургическому лечению.
3. Стриктуры и повреждения желчных протоков. Послеоперационные стриктуры желчных протоков осложняют 1-2%оперативных вмешательств, выполняемых на желчевыводящих путях. Сужение протока возникает либо в результате воспалительных изменений его стенки, либо является следствием находящегося в нем камня. Но иногда оно возникает из-за внешних причин: в результате вовлечения их в рубцовую ткань при язвенной болезни 12-перстной кишки, перихоледохеальном лимфадените или других воспалительных явлениях в этой области. Существует еще одна причина, приводящая к сужению протоков — первичный склерозирующий холангит.
Основными проявлениями рубцовой непроходимости желчевыводящих протоков являются желтуха, холангит, наружный желчный свищ и жалобы, обусловленные развитием вторичного билиарного цирроза печени и портальной гипертензии.
Лечение стриктур протоков может быть только хирургическим. Выбор способа оперативного вмешательства, главным образом, зависит от локализации рубцовой стриктуры, ее протяженности и степени обструкции, выраженности воспалительных изменений. Операция должна обеспечивать полноценную декомпрессию желчевыделительной системы, быть, по возможности, физиологичной, малотравматичной и исключать рецидив заболевания.
4. Холангит является одним из самых серьезных осложнений желчнокаменной болезни. Если желчь плохо выводится, возникает ее застой, и повышается давление в желчевыводящих путях. Это создает условия для восходящего распространения инфекции. В таком случае холецистэктомия удалит лишь один очаг инфекции, а протоки останутся инфицированными.
5. Следующая группа причин ПХЭС — оставленная хирургом «избыточная культя» пузырного протока и “остаточный” желчный пузырь. Специфической симптоматики для этого варианта осложнений нет. Также характерны боль в правом подреберье, повышение температуры, бывает желтуха. Как правило, рецидив болей возникает только тогда, когда оставленная часть желчного пузыря или избыточная культя содержат камни или замазку из сгущенной желчи.
Обнаружить подобные дефекты операции возможно с помощью ультразвукового исследования (УЗИ) органов брюшной полости. Более эффективно и детально представление о проблеме даст выполнение МР-холангиографии. Благодаря этому исследованию можно уточнить длину избыточной культи пузырного протока, а также получить представление о ширине протоков. Появившаяся симптоматика и обнаружение избыточной культи или остаточного желчного пузыря являются показанием к проведению повторной операции и их удалению, потому что в них могут содержаться конкременты, замазкообразные массы, гранулемы, невриномы, которые являются источником воспаления. Однако даже при выявлении избыточной культи пузырного протока необходимо производить тщательное обследование всей гепатопанкреатодуоденальной зоны, чтобы не пропустить другую возможную причину имеющихся жалоб.
6. Опухоли желчных протоков как причина ПХЭС составляют 2,3-4,7%. Они могут быть не обнаружены при проведении первой операции или появиться позднее. Их отличает медленный рост, не резкое нарастание болевой симптоматики. Наиболее информативным для правильной постановки диагноза является МР- холангиография и МСКТ брюшной полости с болюсным контрастированием.
7. Заболевания 12-перстной кишки. Почти всегда у больных с заболеваниями желчевыводящих путей, поджелудочной железы и печени (в 72,5-98,5% случаев) обнаруживают изменения со стороны 12-перстной кишки в виде отека и гиперемии слизистой оболочки, ее атрофии или нарушения моторной функции кишки. После устранения источника воспаления эти расстройства могут уменьшаться, однако в большинстве случаев без адекватного лечения хронический гастрит и дуоденит прогрессируют и создают условия для диагностирования ПХЭС. Клинические проявления заключаются в чувстве тяжести и болях в эпигастральной области, диспептических явлениях.
При рентгенологическом обследовании определяется нарушенная перистальтика с замедлением пассажа бариевой взвеси по кишке или, наоборот, ускоренная эвакуация со спастическими перистальтическими волнами и дуоденогастральным рефлюксом. При фиброгастродуоденоскопии выявляются признаки выраженного гастродуоденита.
Хроническое нарушение дуоденальной проходимости (ХНДП) встречается в 0,45-5,7 % случаев. Его клинические проявления маскируются жалобами, похожими на заболевания других органов. Выраженный болевой синдром, часто приступообразного характера, может быть расценен как проявление холецистита или панкреатита. При декомпенсированной форме дуоденостаза присоединяется обильная с примесью желчи. При фиброгастродуоденоскопии слизистая оболочка желудка и 12-перстной кишки атрофична, имеется дуоденогастральный рефлюкс. Наиболее информативным для выявления данной формы заболевания 12-перстной кишки является ренгенологическое исследование.
Дивертикулы 12-перстной кишки встречаются в 2-3% случаев. Обычно они располагаются на внутренней стенке кишки в средней трети нисходящей части, где мышечный каркас стенки ослаблен в результате проходящих в этой области сосудов и протоков. Клинические симптомы проявляются в виде болей, реже — рвоты. Иногда присоединяется желтуха с явлениями холангита. В диагностике ведущее значение имеет рентгенологическое исследование (дуоденография). При ФГДС уточняют размеры дивертикула, состояние слизистой оболочки и место расположения БДС. Лечение данного заболевания хирургическое.
В диагностике ведущее значение имеет рентгенологическое исследование (дуоденография). При ФГДС уточняют размеры дивертикула, состояние слизистой оболочки и место расположения БДС. Лечение данного заболевания хирургическое.
8. Хронический панкреатит. Хронический панкреатит у больных, перенесших холецистэктомию, встречается довольно часто. Именно при ЖКБ имеется большое количество факторов, приводящих к поражению не только желчевыводящих путей, но и близлежащих органов. У большинства больных снижается внешнесекреторная функция поджелудочной железы, возникает ферментативная недостаточность.
Во всех случаях технически правильно выполненная холецистэктомия способствует улучшению оттока панкреатического сока и частичному восстановлению внешнесекреторной функции железы. В первую очередь восстанавливается секреция трипсина (к 6-му месяцу), тогда как нормализацию показателей активности амилазы можно ожидать только через 2 года. Однако, при далеко зашедшей стадии фиброзных изменений хронический панкреатит начинает проявляться после операции как самостоятельное заболевание с обострениями и ремиссиями.
Обычно боли характеризуются как опоясывающие, сопровождаются расстройствами пищеварения, потому что нарушается внешнесекреторная функция поджелудочной железы, снижается ее ферментативная активность. Позже, в связи с фиброзом ткани железы, могут присоединиться нарушения внутрисекреторной функции инсулярного аппарата. Поэтому при обследовании таких больных, помимо общепринятых биохимических показателей с определением амилазы и липазы, необходимо изучение ферментативной активности панкреатического сока, сахарной кривой и теста на толерантность к глюкозе, а также рентгенологическое исследование желудочно-кишечного тракта и желчных протоков.
9. Прочие причины. Нарушение кишечного всасывания, дисбактериоз и колит могут симулировать рецидив болей после операции. Надо помнить и о гемолитической болезни, протекающей с анемией, желтухой и спленомегалией, о заболеваниях правой половины толстой кишки, правой почки и пояснично-крестцового отдела позвоночника, вызывающих у 15-63% пациентов болевой синдром, не связанный с патологическими изменениями желчевыводящей системы.
Таким образом, необходимо тщательное обследование больных с ПХЭС, включающее помимо общеклинических и биохимических анализов, ультразвукового исследования органов гепатопанкреатодуоденальной зоны, фиброгастродуоденоскопии и рентгеноконтрастного исследования органов желудочно-кишечного тракта, рентгеноконтрастные исследования желчевыводящих путей (КТ, РХПГ или ЧЧХГ) для выяснения истинной причины рецидива болей и выбора адекватной тактики лечения.
Принципы обследования больного с постхолецистэктомическим синдромом
Прежде всего, необходима преемственнность и рациональное взаимодействие амбулаторно-поликлинического, общехирургического и специализированного звеньев оказания медицинской помощи. Все больные после холецистэктомии подлежат диспансерному наблюдению у гастроэнтеролога как для раннего выявления неблагоприятных результатов, так и для проведения профилактических мероприятий: лечебное питание, физкультура, диета растительного характера с ограничением белков и жиров животного происхождения, использование желчегонных средств, снижающих литогенность желчи.
Другим положением является обязательная консультация оперирующего хирурга после завершения реабилитации. При этом оперирующий хирург получает важную информацию о непосредственных и отдаленных результатах хирургического лечения. Для больного это ценно тем, что именно в руках хирурга находится ценная информация о преморбидном статусе, особенностях и деталях самой операции, данных вспомогательных до- и интраоперационных методов исследований.
Еще одним важным условием при обследовании больных с ПХЭС является принцип поиска патологии от наиболее частых причин, к более редким и выполнение исследований от простого к сложному, от неинвазивных, но часто менее информативных методов к более травматичным, но дающим более важную информацию о заболевании.
Вместе с тем, на фоне планируемой программы обследования, включающей многочисленные методы и занимающей, по понятным причинам, длительный период времени, необходимо выделять ситуации, требующие срочного направления больного в стационар. Хирургическая настороженность должна быть тем выше, чем меньше времени прошло с момента операции. Это, прежде всего, относится к болевому синдрому, сопровождаемому желтухой, лихорадкой, ознобом, тошнотой и рвотой, то есть тогда, когда мы можем заподозрить у больного острый холангит.
Хирургическая настороженность должна быть тем выше, чем меньше времени прошло с момента операции. Это, прежде всего, относится к болевому синдрому, сопровождаемому желтухой, лихорадкой, ознобом, тошнотой и рвотой, то есть тогда, когда мы можем заподозрить у больного острый холангит.
Обследование больного с предполагаемым диагнозом постхолецистэктомического синдрома, безусловно следует начинать с УЗИ брюшной полости. Результат исследования позволит исключить выраженные анатомические изменения органов гепатопанкреатобилиарной системы и сделать дальнейшие исследования более целенаправленными.
Что касается КТ, то ее применение в целях выявления холедохолитиаза при отсутствии патологических изменений печени и поджелудочной железы — нерационально и менее информативно. В то же время, возможности КТ трудно переоценить при органических изменениях органов гепатопанкреатодуоденальной зоны. МРТ, особенно выполненная в режиме МР-холангиографии, может дать достаточно важную информацию относительно состояния желчевыводящих путей, а также протоковой системы поджелудочной железы. И все же, несмотря на большие возможности современных диагностических методов, существует группа больных, у которых не удается выявить причину жалоб после перенесенной холецистэктомии.
Лечение
Лечение больных с ПХЭС должно быть комплексным и направлено на устранение тех функциональных или структурных нарушений со стороны печени, желчевыводящих путей, желудочно-кишечного тракта и поджелудочной железы, которые лежат в основе страдания и явились поводом для обращения к врачу. Образ жизни и питание играют существенную роль в развитии ЖКБ. Поэтому диета, режим приема пищи, двигательный режим являются важнейшими условиями реабилитации после операции холецистэктомии.
Назначается диета, которая:
-
1) не должна провоцировать печеночную колику и оказывать вредное влияние на поджелудочную железу;
-
2) должна положительно влиять на желчевыделение и на внешнесекреторную функцию поджелудочной железы;
-
3) способствует снижению литогенных свойств желчи;
-
4) улучшает обменные процессы печени.

Медикаментозная терапия также обычно включает сочетание лекарственных средств разных классов. Основа лечения — это нормализация пассажа желчи по общему печеночному, общему желчному протокам и панкреатического сока по главному панкреатическому протоку. Для устранения имеющей место у большинства больных относительной ферментативной недостаточности, улучшения переваривания жиров обосновано адекватное ферментное сопровождение курса лечения.
Выявление эрозивно-язвенных поражений слизистой оболочки верхних отделов желудочно-кишечного тракта подразумевает проведение антисекреторной терапии, а при диагностике хеликобактериоза — эрадикационной терапии.
Купирование метеоризма может достигаться назначением пеногасителей, комбинированных препаратов, сорбентов, препаратов микрокристаллической целлюлозы. Нередко ЖКБ сопровождается нарушением кишечного биоценоза, приводящего к кишечной диспепсии. В этих случаях целесообразно проведение деконтаминационной терапии. Затем проводится лечение пробиотиками и пребиотиками.
Безусловно, подобное комплексное обследование и лечение правильнее всего проводить в одном учреждении. Наша клиника располагает всеми необходимыми диагностическим возможностями для полноценного обследования, лечения и проведения реабилитационных и профилактических мероприятий.
Холангит, описание заболевания на портале Medihost.ru
Холангит – заболевание органов пищеварения, характеризующееся развитием воспалительных процессов желчного протока, которые могут иметь острый и хронический характер.
Причины холангита
Большинство случаев холангита связаны с проникновением в желчные протоки микроорганизмов – протея, кишечной палочки, энтерококков, стафилококков, в редких случаях микобактерий туберкулеза, бледной спирохеты и др. вирусный гепатит может стать причиной поражения мелких протоков, глистные инвазии – аскаридоз, описторхоз, фасциолез – все эти заболевания также могут вызвать холангит.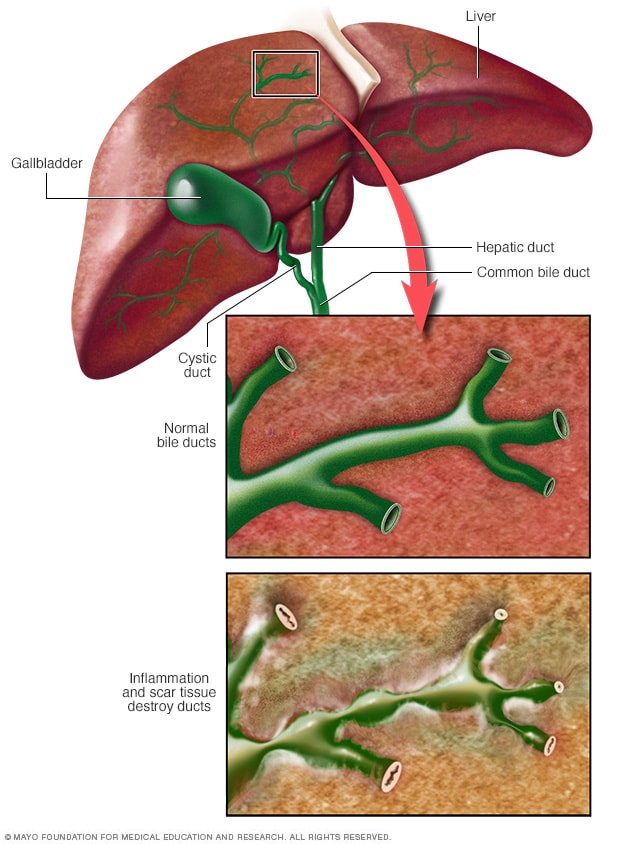
В асептических условиях воспаление может развиваться в результате раздражения желчных протоков и их стенок панкреатическим соком. Также может развиться асептический склерозирующий холангит, причина которого – аутоиммунные процессы, колит (язвенный), васкулиты, болезнь Крона и другие.
Классификация холангита
По течению воспалительных процессов различают острый и хронический холангит. Острый холангит делится на подвиды: дифтерический (образование фибринозных пленок), катаральный (гиперемия и отек стенок желчных протоков), некротический, гнойный (расплавление стенок). Хронический холангит также имеет подвиды – септический, склерозирующий, абсцедирующий, латентный, рецидивирующий.
По локализации воспалительного процесса различают – папиллит (воспаление фатерова сосочка), ангиохолит (протоки внутри и вне печени), холедохит (воспаление общего желчного протока).
Симптомы холангита
При развитии острого холангита характерна триада симптомов (Шарко) – боли в правом подреберье с желтухой, лихорадочный синдром.
Начинается заболевание с повышения температуры до 40 градусов, появляется озноб, повышенная потливость. Пациент жалуется на сильные боли в правом подреберье, которые по характеру напоминают желчную колику. Боли иррадиирует в правое плечо, лопатку, иногда в шею. Состояние больного быстро ухудшается, нарастает синдром интоксикации, слабость, потеря аппетита. Появляется тошнота и рвота, расстройства кишечника в виде диареи. С течением времени появляется иктеричность (желтушность) кожных покровов, слизистых оболочек. Желтуха, как правило, сопровождается сильным зудом, который усиливается в ночное время. Пациент просыпается ночью, расчесывает зудящую кожу, нарушая ее целостность.
В тяжелых случаях возможна потеря сознания, развитие шокового состояния – это пентада Рейнолдса.
При развитии хронического холангита симптомы носят стертый, смазанный характер, однако, со временем симптомы усиливаются. Желтуха развивается поздно, говорит о запущенности воспалительного процесса, боли тупого характера незначительной интнсивности, появляется ощущение распирания в эпигастральной области.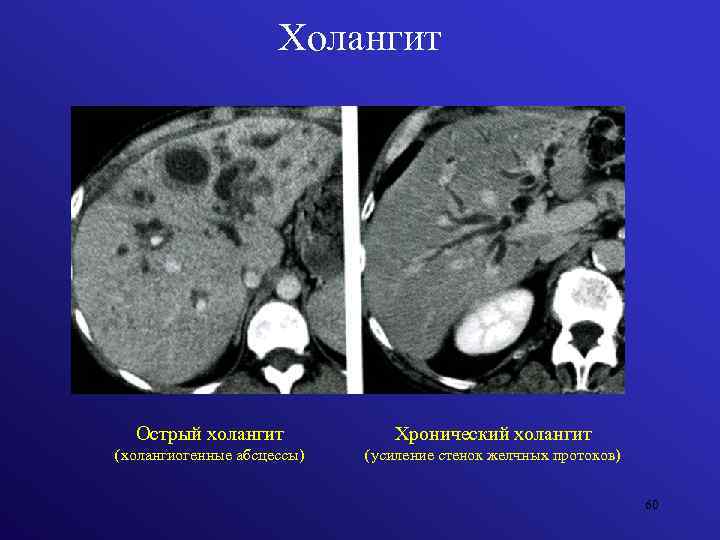
Диагностика
- Биохимический анализ крови – холестаз, повышение билирубина, щелочная фосфатаза также повышена
- Фракционное дуоденальное зондирование, бактериологический посев желчи
- Исследование кала на яйца гельминтов
- УЗИ брюшной полости, печени
- Ультрасонография
- Компьютерная томография
- Панкреатохолангиография
Лечение холангита
- Постельный режим, голодная диета
- Спазмолитические препараты, противовоспалительные, антибактериальная терапия при инфекционном процессе с учетом чувствительности возбудителя, противопаразитарные препараты
- Плазмоферез – в тяжелых случаях
- Индуктотермия, УВЧ, диатермия, электрофорез, грязевые апликации, парафинотерапия, различные вид ванн
- Хирургические вмешательства – стенирование холедоха, дренирование желчных протоков и другие виды оперативных вмешательств
- При склерозирующем холангите показана пересадка донорской печени
Болезни печени и желчного пузыря — признаки и симптомы
Сбои в работе печени, желчного пузыря изучает гепатология. Врачи-гепатологи нашей клиники лечат гепатиты, циррозы, холециститы, опухолевые новообразования, заболевания желчевыводящих путей и многое другое. В клинике выполняется тщательное обследование для установления точного диагноза, а также выявления причин болезни. Далее наши квалифицированные врачи подбирают нужный метод лечения. Мы пользуемся наиновейшим оборудованием. Если вас беспокоят гепатологические проблемы, мы гарантированно поможем вам избавиться от них.
Когда нужно обращаться к гастроэнтерологу?
Болезни печени, желчевыводящих путей, желчного пузыря сопровождаются определенной симптоматикой. Симптомы, при которых нужно обратиться к гепатологу, следующие:
- тошнота
- дискомфорт, тяжесть либо ощущение боли в правом подреберье
- горечь во рту
- снижение аппетита
- пожелтение кожных покровов и склер (белков глаз)
- кожный зуд
- асцит (избыток жидкости в брюшной полости)
- слишком темная моча
- серовато-белый стул
- кровавая рвота.

О каких болезнях могут сигнализировать ваши симптомы
Вышеперечисленные симптомы могут сопровождать разные болезни желчного пузыря, печени, а именно:
- гепатиты: аутоиммунный, гепатит С, вирусный хронический В, С, Д, токсический гепатит, неалкогольный стеатогепатит.
- первичный билиарный цирроз.
- алкогольная болезнь печени.
- цирроз печени любой этиологии.
- наследственный гемохроматоз (избыточное накопление железа).
- первичный склерозирующий холангит.
- желчнокаменная болезнь.
- болезнь Вильсона-Коновалова.
- хронический холецистит.
- жировой гепатоз.
- дискинезия желчевыводящих путей.
Какие методы диагностики вам предложат в клинике?
Иногда опытный гепатолог клиники может предположить имеющийся диагноз сразу, при первом взгляде, поскольку некоторые из симптомов болезней печени видны невооруженным глазом (типичные виды желтухи, сыпь на коже). Но чаще заболевания и печени, и желчного пузыря довольно долго протекают незаметно, проявляясь клинически на поздних стадиях, и тогда помочь уже бывает сложнее.
Поэтому так важно вовремя заметить малозначительные, но необъяснимые симптомы, такие, как утомляемость, плохой аппетит, дискомфортные ощущения в правом подреберье. Не только заметить, но и своевременно прийти в нашу клинику.
Диагностика болезней желчного пузыря и печени начинается с беседы со специалистом о ваших симптомах. Важно также выяснить, какие заболевания вы перенесли.
Врачебный осмотр позволит выявить ряд симптомов. Вам предложат все нужные инструментальные, а также клинические обследования, чтобы точно диагностировать вашу болезнь.
Лабораторные методы исследования таковы:
- биохимия крови
- общие анализы крови, мочи
- серологические реакции
- молекулярно-генетические исследования.
Инструментальные способы диагностики:
Данных обследований часто бывает достаточно для выявления заболеваний печени и пройти их можно у нас в клинике. Для более детального обследования, врач может направить пациента в диагностический центр, для проведения:
Для более детального обследования, врач может направить пациента в диагностический центр, для проведения:
- лучевой диагностики
- фиброэластографии
- компьютерной томографии
- магнитно-резонансной томографии
- рентгенологическго исследовании
- биопсии печени
- инвазивных исследований
- колоноскопии.
Технологии лечения
После обработки всех данных возможны три варианта: врач предпишет вам особую диету; назначит комплексное медикаментозное лечение для устранения возбудителя заболевания; либо назначит еще и дополнительное лечение, учитывающее существование у вас других патологий (болезней сердечно-сосудистой системы, дыхательной, мочевыделительной и проч.)
Острые болезни печени, желчного пузыря вполне излечимы в большинстве случаев, но хронические полностью вылечить практически невозможно. При хронике в нашей клинике врачи добиваются скорейшего купирования обострения, длительной ремиссии, сохранения максимальной функции печени (то есть компенсации печеночной недостаточности), желчного пузыря.
Своевременная диагностика, оперативное начало лечения позволят свести врачебное вмешательство, а также последствия болезни к минимуму. Обращение к гастроэнтерологу нашей клиники гарантирует вам квалифицированные услуги по диагностике и терапии. Вас будут лечить по индивидуальной программе.
Обесцвеченный кал
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу. Цвет кала зависит от количества желчных пигментов (продуктов распада гемоглобина), красящих веществ, содержащихся в продуктах питания и лекарственных препаратах, примесей свежей или свернувшейся крови, продуктов метаболизма микроорганизмов, живущих в кишечнике.
При отсутствии сильно красящих пищевых пигментов цвет кала в норме от светло- до темно-коричневого.
Коричневую окраску придает калу стеркобилин – продукт распада билирубина. Изменение цвета каловых масс от светло-зеленого до желтовато-серого может возникать при различных болезнях.Если билирубин по какой-либо причине не поступает в желудочно-кишечный тракт, то кал будет обесцвечиваться. Такой кал называется ахоличным. Обесцвеченный кал может иметь различную консистенцию, которая определяется количеством потребляемой воды, растительных волокон, тонусом кишечника и другими факторами. Эти факторы учитываются при диагностике заболеваний печени.
Возможные причины
Поражение печеночных и желчных протоков. При нарушении проходимости печеночных протоков развивается холестаз, для которого характерен ахоличный кал. Холестаз может быть вызван закупоркой протоков мелкими камнями (желчнокаменная болезнь), сгустками крови, паразитами (при описторхозе, фасциолезе, клонорхозе), а также может быть следствием врожденных аномалий, рубцовых стенозов, наличием опухолей желчных протоков. Просвет общего желчного протока может быть сужен в связи с опухолевым ростом, из-за воспаления и кист поджелудочной железы, рецидивирующих холангитов, лимфаденита на фоне туберкулеза, саркоидоза или быть следствием хирургического лечения и спаечного процесса. Во всех случаях нарушено поступление желчи из печени.
Симптомами холестаза являются: кожный зуд, желтуха, обесцвечивание кала и потемнение мочи, тяжелое течение проявляется гриппоподобным состоянием (озноб и повышение температуры).
Склерозирующий холангит – патология, которая так же сопровождается обесцвечиванием кала из-за нарушения оттока желчи. При этом заболевании происходит склерозирование желчных протоков (замещение здоровой ткани органа рубцовыми соединительными волокнами) вследствие воспалительных процессов.
Склерозирующий холангит в большинстве случаев сопровождается воспалительными заболеваниями желудочно-кишечного тракта (язвенный колит, болезнь Крона).
Функциональные расстройства желчевыводящих путей. Функциональное нарушение моторики желчевыводящих путей – дискинезия желчных путей – относится к числу наиболее распространенных причин изменения окраски каловых масс. Это связано с сужением (мышечным спазмом) просвета желчных протоков и дуоденального сосочка, регулирующего поступление желчи в кишку.
Спазм может возникать вследствие гормональных расстройств, системных заболеваний, при болевом синдроме, после хирургических вмешательств. В этом случае обесцвечивание кала не будет носить постоянного характера. Стул становится светлым только после спастических приступов, а в период возобновления моторики желчевыводящих путей его цвет возвращается к норме.
Учитывая, что коричневый оттенок кала обусловлен желчными пигментами, любой процесс нарушения их синтеза или поступления в желудочно-кишечный тракт, сопровождается изменением цвета стула. Не всегда обесцвеченный кал свидетельствует о болезни: при чрезмерном потреблении жирной пищи обычного количества желчи не хватает для переработки всех поглощенных жиров, и кал приобретает светлую окраску. При некоторых инфекционных заболеваниях (холера, сальмонеллез, дизентерия), нарушении процессов пищеварения (неадекватность всасывания питательных веществ, синдром раздраженной кишки) усиленная перистальтика кишечника приводит к быстрому продвижению каловых масс, которые не успевают изменить цвет.
При стойком формировании обесцвеченного кала следует подозревать заболевания органов гепатобилиарной системы (печени, желчного пузыря, печеночных и желчных протоков, сфинктера Одди).
Дегенеративно-воспалительные болезни печени (гепатиты различной этиологии, циррозы) влияют на синтез и метаболизм желчных пигментов и билирубина, что часто проявляется неокрашенным калом.
Поражение клеток печени (гепатоцитов). Гепатоциты, вырабатывающие желчь, могут погибать под воздействием многих факторов.
Инфекционную природу заболеваний печени следует рассматривать прежде всего.
При попадании в кровь вирусов гепатита развивается острое инфекционное заболевание, которое проявляется высокой температурой, тошнотой, рвотой, тяжестью и болью в правом подреберье, появляется желтая окраска склер (иктеричность), темнеет моча, а кал обесцвечивается. При заражении вирусами гепатита В, С процесс часто приобретает хронический характер. Инкубационный период гепатита С может достигать шести месяцев, а в острый период заболевания симптомы напоминают респираторную инфекцию. Хронические вирусные гепатиты В и С при отсутствии лечения могут приводить к циррозу и раку печени. Гепатитами может сопровождаться цитомегаловирусная инфекция, заболевания герпесвирусной этиологии, инфекционный мононуклеоз (возбудитель – вирус Эпштейна-Барр).В настоящее время часто диагностируется алкогольный гепатит.
Продукты этилового спирта и его метаболиты оказывают прямое поражающее воздействие на клетки печени.
Хроническое течение алкогольной болезни печени завершается массивным замещением гепатоцитов соединительной тканью с полной потерей их функций. В клинической картине основными становятся жалобы на тяжесть и характерные боли в правом подреберье, которые могут отдавать в руку, лопатку, поясничную область. Развивается желтушность кожных покровов, склер, кал обесцвечивается, моча темнеет, возникают признаки энцефалопатии. На последних стадиях алкогольной болезни развивается цирроз печени, печеночная недостаточность, кровотечение из варикозно-расширенных вен пищевода и т. д.К числу токсинов, оказывающих разрушительное воздействие на клетки печени, относятся растительные яды (некоторые грибы, сок горчака и крестовника) и химические промышленные вещества (фосфор, мышьяк, хлорорганические вещества, фенолы, пестициды). Многие лекарственные средства (противовоспалительные, противовирусные, противотуберкулезные, противосудорожные) изменяют функциональную активность гепатоцитов, что влияет на цвет кала.
Многие лекарственные средства (противовоспалительные, противовирусные, противотуберкулезные, противосудорожные) изменяют функциональную активность гепатоцитов, что влияет на цвет кала.
Клетки печени погибают при кислородном голодании, вызванном недостаточностью кровообращения и дефицитом кислорода в крови. При синдроме печеночно-клеточной недостаточности, возникает нарушение функции гепатоцитов, что сопровождается общей интоксикацией организма.
Диагностика и обследование
При жалобах на обесцвеченный, ахоличный стул диагностика включает физикальные и лабораторные исследования.
Информацию о работе печени и желчного пузыря дают общие анализы крови и мочи; биохимическое исследование крови (аспартатаминотрансфераза, аланинаминотрансфераза, щелочная фосфатаза, билирубин, глюкоза, амилаза и липаза).
Первичный склерозирующий холангит
Авторы: K.N. Lazaridis, N. F. LaRusso, США
Эпидемиология
Около 60% больных первичным склерозирующим холангитом (ПСХ) – лица мужского пола (средний возраст – 41 год). Заболеваемость ПСХ составляет 0-1,3 случая на 100 тыс. населения, распространенность варьирует в пределах от 0 до 16,2 случая на 100 тыс. Результаты исследований, проведенных в Северной Европе, свидетельствуют о неуклонном росте показателей распространенности и заболеваемости ПСХ. В настоящее время окончательно не ясно, с чем связано это повышение: с увеличением грамотности врачей, с улучшением качества диагностики либо с применением современных методов обследования (эндоскопическая ретроградная холангиопанкреатография, ЭРХПГ, магнитно-резонансная холангиопанкреатография, МРХПГ).
Клиника
ПСХ – коварное заболевание: более половины пациентов с указанной патологией не предъявляют никаких жалоб, а подтвердить диагноз даже после получения результатов печеночных проб бывает непросто. Наиболее часто при объективном осмотре обнаруживают гепато- (44% случаев) и спленомегалию (39%). Если течение заболевания сопровождается появлением жалоб, то среди них доминируют абдоминальная боль (20% случаев), зуд (10%), желтуха (6%), усталость (6%). Диагностические критерии ПСХ включают увеличение сывороточной концентрации щелочной фосфатазы (ЩФ), персистирующее более 6 мес, а также холангиографические признаки стриктур билиарного дерева. В случаях, когда течение заболевания сопровождается возникновением стриктур желчных протоков, подтверждаемых данными МРХПГ или ЭРХПГ, необходимо исключить вторичный склерозирующий холангит (ВСХ; табл. 1).
Наиболее часто при объективном осмотре обнаруживают гепато- (44% случаев) и спленомегалию (39%). Если течение заболевания сопровождается появлением жалоб, то среди них доминируют абдоминальная боль (20% случаев), зуд (10%), желтуха (6%), усталость (6%). Диагностические критерии ПСХ включают увеличение сывороточной концентрации щелочной фосфатазы (ЩФ), персистирующее более 6 мес, а также холангиографические признаки стриктур билиарного дерева. В случаях, когда течение заболевания сопровождается возникновением стриктур желчных протоков, подтверждаемых данными МРХПГ или ЭРХПГ, необходимо исключить вторичный склерозирующий холангит (ВСХ; табл. 1).
Проведение биопсии печени не является обязательным, за исключением тех случаев, когда существует подозрение на поражение мелких желчных протоков или имеет место сочетанное течение ПСХ и аутоиммунного гепатита (АИГ). Магнитно-резонансная или транзиторная эластография печени – перспективные неинвазивные методы исследования, в ходе которых оцениваются механические свойства ткани (фиброз), однако их специфическая роль в оценке степени фиброза печени у больных ПСХ еще окончательно не определена.
Выделяют несколько подтипов ПСХ. Классический подтип, при котором в патологический процесс вовлекается все билиарное дерево, диагностируют у 90% больных ПСХ; у 5% пациентов патологический процесс локализуется только в мелких внутрипеченочных желчных протоках. Перекрестный синдром ПСХ и АИГ выявляют у 35% детей с ПСХ и у 5% взрослых с данной патологией.
Клиническая манифестация и характер прогрессирования ПСХ могут отличаться в зависимости от подтипа заболевания (табл. 2). Так, у пациентов с преимущественным поражением мелких внутрипеченочных желчных протоков течение заболевания более благоприятное, чем у лиц с классическим вариантом ПСХ. В то же время в отличие от больных с сочетанием ПСХ и воспалительных заболеваний кишечника (ВЗК) пациенты, у которых ПСХ не сопровождается развитием ВЗК, могут иметь различные подтипы заболевания. Является ли указанная комбинация случайным совпадением или нет, в настоящее время окончательно не ясно, поскольку ВЗК может развиться спустя несколько лет после подтверждения ПСХ или трансплантации печени.
Является ли указанная комбинация случайным совпадением или нет, в настоящее время окончательно не ясно, поскольку ВЗК может развиться спустя несколько лет после подтверждения ПСХ или трансплантации печени.
Примерно у 10% больных ПСХ выявляют высокие сывороточные концентрации IgG4; прогноз для жизни у таких пациентов хуже, чем у лиц с нормальным содержанием этого иммуноглобулина. Таких пациентов не стоить путать с больными, страдающими IgG4-ассоциированным холангитом (системное заболевание, характеризующееся высоким уровнем IgG4 в сыворотке крови и IgG4-положительной лимфоплазматической инфильтрацией различных органов – поджелудочной железы, желчных протоков, резким началом (с появления желтухи), возникновением билиарных стриктур, отвечающих на лечение глюкокортикоидами (преднизолон 40 мг/сут), отсутствием ВЗК). В настоящее время не существует биомаркеров, с помощью которых можно было бы точно прогнозировать характер прогрессирования какого-либо подтипа ПСХ. Однако уровень сывороточной ЩФ в 1,5 раза меньше верхней границы нормы ассоциирован с лучшим прогнозом, чем уровень ЩФ, превышающий эту границу в ≥1,5 раза. В настоящее время до конца не ясно, является ли концентрация ЩФ надежной суррогатной конечной точкой для клинических исследований или же предиктором долгосрочного прогноза при ПСХ.
Как правило, ПСХ прогрессирует медленно, с переменными результатами. По данным одного популяционного исследования, выживаемость пациентов с ПСХ, находившихся на стационарном лечении в 44 нидерландских больницах, была выше, чем средняя выживаемость больных, терапия которых осуществлялась в 3 трансплантационных центрах этой страны (21,3 vs 13,2 года соответственно; р<0,001). Эти данные, вероятно, объясняются направлением в высокоспециализированные учреждения тяжелобольных пациентов, нуждающихся в трансплантации печени.
Бактериальный холангит, являющийся первым клиническим проявлением ПСХ у 6% пациентов, может иметь рецидивирующее течение и плохо поддаваться терапии, в большинстве случаев необходима трансплантация печени. В исследовании, в котором приняли участие 273 пациента (средняя длительность наблюдения составила 76 мес), доминирующая стриктура (сужение внепеченочного протока <1,5 мм) имела место у 40% больных и, по всей видимости, была ассоциирована с развитием неоплазии у 15 из 20% пациентов. Таким образом, обнаружение доминирующей стриктуры должно насторожить медицинский персонал и рассматриваться как повод для дальнейшего углубленного обследования. Дифференцировать доброкачественный и злокачественный характер доминирующей стриктуры достаточно сложно, несмотря на внедрение метода флуоресцентной гибридизации in situ.
В исследовании, в котором приняли участие 273 пациента (средняя длительность наблюдения составила 76 мес), доминирующая стриктура (сужение внепеченочного протока <1,5 мм) имела место у 40% больных и, по всей видимости, была ассоциирована с развитием неоплазии у 15 из 20% пациентов. Таким образом, обнаружение доминирующей стриктуры должно насторожить медицинский персонал и рассматриваться как повод для дальнейшего углубленного обследования. Дифференцировать доброкачественный и злокачественный характер доминирующей стриктуры достаточно сложно, несмотря на внедрение метода флуоресцентной гибридизации in situ.
ПСХ часто сопровождается появлением различных сопутствующих заболеваний. Принимая во внимание тот факт, что ВЗК (чаще диагностируют неспецифический язвенный колит – НЯК, а не болезнь Крона) развиваются у большинства пациентов с ПСХ, колоноскопия является оправданным методом диагностики для всех больных, которым впервые установлен диагноз ПСХ. По данным одного исследования, практически у всех лиц с сочетанным течением ПСХ и ВЗК (НЯК или болезнь Крона) имеет место тотальное поражение толстого кишечника, в единичных случаях диагностируются ретроградный илеит (язвенно-воспалительные изменения в терминальном отделе подвздошной кишки у больных НЯК) и незначительное поражение прямой кишки. Риск развития рака толстого кишечника у пациентов с ПСХ и сопутствующим ВЗК в 4 раза выше, чем у лиц с изолированным течением ВЗК, и в 10 раз превышает таковой в общей популяции.
Патология желчного пузыря (ЖП; конкременты, полипы, рак) часто диагностируется у больных ПСХ. Конкременты ЖП обнаруживают у 25% больных, новообразования – у 6-14% пациентов. Около 60% опухолей ЖП являются аденокарциномами; в одном исследовании показано, что при гистологическом исследовании ЖП, удаленных у больных ПСХ до или во время трансплантации печени, в 37% случаев выявили признаки дисплазии, а в 14% случаев – аденокарциномы. В экономически развитых странах ПСХ является основным фактором риска развития холангиокарциномы: вероятность возникновения этой патологии у пациентов с ПСХ в 400 раз выше, чем в общей популяции. Ежегодный риск развития холангиокарциномы у больных ПСХ составляет 2%, 30-летняя кумулятивная заболеваемость – 20%. Внезапное изменение клинической симптоматики (неожиданное появление желтухи, лихорадки, снижение массы тела) или биохимических показателей (ранее не отмечавшийся рост ЩФ и/или билирубина с прогрессирующим повышением сывороточной концентрации опухолевого маркера СА 19-9 или без такового) является показанием для дополнительного углубленного исследования.
Ежегодный риск развития холангиокарциномы у больных ПСХ составляет 2%, 30-летняя кумулятивная заболеваемость – 20%. Внезапное изменение клинической симптоматики (неожиданное появление желтухи, лихорадки, снижение массы тела) или биохимических показателей (ранее не отмечавшийся рост ЩФ и/или билирубина с прогрессирующим повышением сывороточной концентрации опухолевого маркера СА 19-9 или без такового) является показанием для дополнительного углубленного исследования.
Дополнительные исследования включают ультразвуковое исследование (УЗИ), магнитно-резонансную томографию печени в сочетании с ЭРХПГ. Несмотря на то что достоверные биомаркеры вероятного развития холангиокарциномы у больных ПСХ пока не установлены, многие клиницисты рекомендуют ежегодно проводить УЗИ печени и определять СА 19-9.
Больные ПСХ могут страдать остеопорозом. В одном масштабном исследовании (n=237) примерно 15% пациентов страдали остеопорозом (значения Т-показателя <-2,5). Возраст >54 лет, индекс массы тела ≤24 кг/м2, длительный анамнез ВЗК (≥19 лет) коррелировали с развитием остеопороза.
Патогенез
Наследственность, а также воздействие окружающей среды являются основными этиологическими факторами ПСХ, вовлеченными в патогенез заболевания (рис.).
Согласно существующей гипотезе после воздействия неопределенного фактора внешней среды при наличии генетической предрасположенности создаются условия для персистирующего поражения холангиоцитов (клеток, выстилающих желчные протоки), что приводит к воспалению желчных протоков и инициации фиброзных изменений.
Лечение
Ведение больных ПСХ является сложной задачей: необходимо назначить терапию как для первичной патологии печени, так и для сопутствующих заболеваний, а также предусмотреть последующее лечение вероятных осложнений на терминальной стадии болезни. Пациентов с прогрессирующим течением ПСХ (в том числе больных с рефрактерными симптомами или холангиокарциномой) целесообразнее лечить в условиях высокоспециализированных центров, где используется интегрированный, мультидисциплинарный подход с участием команды специалистов (гепатологов, гастроэнтерологов, эндоскопистов, рентгенологов, хирургов-трансплантологов).
До настоящего времени эффективная медикаментозная терапия ПСХ не разработана, несмотря на большое количество клинических исследований, которые проводились на протяжении нескольких десятилетий. С учетом того, что патогенез ПСХ продолжает изучаться, определить терапевтические цели и подобрать эффективные схемы лечения непросто. Кроме того, ПСХ – достаточно редкое заболевание, гетерогенное по своему характеру, характеризующееся отсутствием надежных биомаркеров. Все это затрудняет проведение должной стратификации пациентов и определение конечных точек, необходимых для адекватного проведения клинических исследований.
Эффективность урсодезоксихолевой кислоты (УДХК) в лечении ПСХ изучалась во многих испытаниях. В одном рандомизированном двойном слепом плацебо-контролированном исследовании у пациентов, получавших УДХК, зафиксировано снижение уровня печеночных ферментов, при этом показатели выживаемости практически не отличались от таковых у больных, принимавших плацебо. По данным другого рандомизированного двойного слепого плацебо-контролированного исследования, риск достижения первичной конечной точки (летальный исход, трансплантация печени, минимальные критерии для трансплантации печени, цирроз, варикозно расширенные вены (ВРВ) пищевода или желудка, холангиокарцинома), был в 2,3 раза выше у пациентов, получавших высокие дозы УДХК (25 мг/кг/сут) по сравнению с соответствующим показателем у больных, принимавших плацебо (р<0,01). Поэтому существующие рекомендации по лечению ПСХ являются противоречивыми: Американская ассоциация по изучению болезней печени (AASLD) не поддерживает применение УДХК, Американская коллегия гастроэнтерологов (ACG) допускает возможность назначения УДХК при условии использования стандартных суточных доз, а Европейская ассоциация по изучению печени (EASL) поощряет применение УДХК в умеренной дозировке (13-15 мг/кг/сут). Учитывая противоречивость рекомендаций, по нашему мнению, следует назначать УДХК в дозе 13-15 мг/кг/сут на протяжении 6 мес под контролем активности печеночных ферментов. Если на протяжении указанного отрезка времени не происходит снижения концентрации ЩФ, предлагаем прекратить терапию и наблюдать за состоянием пациента либо включить больного в клиническое исследование.
Если на протяжении указанного отрезка времени не происходит снижения концентрации ЩФ, предлагаем прекратить терапию и наблюдать за состоянием пациента либо включить больного в клиническое исследование.
В настоящее время продолжает изучаться эффективность новых препаратов в лечении ПСХ. Так, обетихолевая кислота, которая представляет собой полусинтетический аналог хенодезоксихолевой кислоты и является потенциальным лигандом для фарнезоидного Х-рецептора, оказывает выраженное антифибротическое действие. В данный момент проводится клиническое исследование, в котором этот препарат назначается больным ПСХ. Дизайн другого испытания предполагает применение симтузумаба, моноклонального антитела против одного из профибротических белков – лизилоксидазоподобному ферменту (Loxl2). Изучается также эффективность 24-нор-УДХК – синтетической желчной кислоты, способствующей возникновению бикарбонатного холереза, индуцированного желчными кислотами; предполагается, что она может быть полезна пациентам с фиброзом печени.
Уменьшение чувствительности холангиоцитов к потенциально токсичным желчным кислотам может быть достигнуто посредством ингибирования апикального натрийзависимого транспортера желчных кислот в подвздошной кишке. В экспериментальной модели с участием лабораторных животных было показано, что снижение экспрессии печеночного профибротического гена, увеличение экспрессии противовоспалительного и антифибротического генов, а также снижение размеров пула и изменение состава желчных кислот приводят к улучшению гистологической картины печени.
В другом исследовании изучается ВТТ1023 – человеческое моноклональное антитело, которое нацелено на белок сосудистой адгезии 1 типа (молекула адгезии, необходимая для осуществления эффекта возвращения Т-клеток в кишечник). Тестируется гипотеза относительно целесообразности назначения пероральных антибиотиков в качестве дополнительного метода лечения: предполагается, что воздействие на кишечную микробиоту позволит уменьшить интенсивность врожденных иммунных реакций, играющих решающее значение в развитии билиарного воспаления и фиброза. По данным одного небольшого испытания, прием ванкомицина способствовал уменьшению уровня ЩФ к 12-й неделе терапии; в настоящее время продолжается исследование, в рамках которого изучается эффективность этого препарата у детей, больных ПСХ. В стадии планирования находится работа, предполагающая трансплантацию фекальной микробиоты больным ПСХ (интестинальный микробиом может быть вовлечен в патогенез этого заболевания).
По данным одного небольшого испытания, прием ванкомицина способствовал уменьшению уровня ЩФ к 12-й неделе терапии; в настоящее время продолжается исследование, в рамках которого изучается эффективность этого препарата у детей, больных ПСХ. В стадии планирования находится работа, предполагающая трансплантацию фекальной микробиоты больным ПСХ (интестинальный микробиом может быть вовлечен в патогенез этого заболевания).
Лечение осложнений, возникающих на терминальной стадии ПСХ, а также терапия ассоциированных и сопутствующих заболеваний описаны в таблице 3.
Лечение больных с сочетанным течением ПСХ и ВЗК должно назначаться в соответствии с положениями существующих руководств.
Пациентам с ВЗК, перенесшим трансплантацию печени, следует ежегодно проводить колоноскопию с биопсией, учитывая высокий риск развития колоректального рака. Больным, не имеющим сопутствующего ВЗК, колоноскопию необходимо проводить 1 раз в 5 лет, учитывая риск развития поражения кишечника. Рекомендуется ежегодное УЗИ ЖП для обнаружения полипов или других опухолевых образований. С учетом риска возникновения неоплазий пациентам с опухолевым образованием ЖП любого размера должна быть рекомендована холецистэктомия. Показатель 5-летней выживаемости без рецидивов заболевания у лиц с ПСХ и перипортальной холангиокарциномой, перенесших трансплантацию печени после неоадъювантной химио- и лучевой терапии, составляет 65%.
В связи с прогрессирующим течением ПСХ около 40% пациентов будут нуждаться в трансплантации печени. Примечательно, что 6% трансплантаций, проведенных в США с 1988 по 2015 год, были выполнены по такому показанию, как ПСХ. Эти статистические данные заслуживают пристального внимания: с учетом редкости заболевания (1 случай на 10 тыс. населения) они подчеркивают экономическое бремя ПСХ (ежегодно на проведение трансплантации печени при ПСХ в США расходуется 125 млн долларов) и ургентную потребность в назначении эффективной медикаментозной терапии.
Показатели годичной выживаемости после трансплантации печени при ПСХ составляют примерно 85%, 5-летней выживаемости – 72%.
К сожалению, в 25% случаев заболевание может рецидивировать даже после трансплантации печени. Рецидив ПСХ диагностируется на основании данных холангиографии в отсутствие явлений отторжения печени или сосудистой патологии (ишемии) в пересаженном органе. По данным одного исследования, проведение колэктомии при сочетанном течении ПСХ и ВЗК перед трансплантацией печени может снизить вероятность рецидива ПСХ после вмешательства.
ПСХ является заболеванием с окончательно не выясненным патогенезом, эффективная медикаментозная терапия данной патологии еще не разработана. Для лучшего понимания патогенеза ПСХ и разработки новых методов лечения при проведении больших исследований с участием хорошо фенотипированных когорт пациентов, а также при выполнении экспериментальных модельных (животные, органеллы) работ необходимо придерживаться объективных, так называемых -омик-подходов (геномика, эпигеномика, протеомика).
Статья печатается в сокращении.
Lazaridis K. N., LaRusso N. F. Primary Sclerosing Cholangitis. N Engl J Med 2016; 375: 1161-1170.
Перевела с англ. Лада Матвеева
Медична газета «Здоров’я України 21 сторіччя» № 20 (393), жовтень 2016 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
06.04.2021 Гастроентерологія Особливості ведення хворих із НПЗП-індукованою гастропатієюОбговорюються ризики розвитку несприятливих явищ в осіб похилого віку з коморбідною патологією, що виникають на тлі тривалого застосування нестероїдних протизапальних препаратів (НПЗП) з метою купірування больового і запального суглобового синдромів у поєднанні з прийомом препаратів інших лікарських груп (зокрема ацетилсаліцилової кислоти та антитромбоцитарних засобів), які використовуються для лікування супутніх захворювань серцево-судинної системи. …
…
Первичный этап диагностического поиска весьма важен как для врача (поскольку свидетельствует о его квалификации), так и для больного (поскольку определяет время назначения верного оптимального лечения, дальнейшую тактику поведения пациента и, соответственно, качество его жизни). Диагностика всей группы гастроэнтерологических заболеваний представляет определенные трудности в связи с наличием у большинства пациентов диспепсического и болевого синдромов. Исходя из этого, знание особенностей этиологических и патогенетических моментов, клинической картины (особенностей симптоматики, вплоть до так называемых малых симптомов), а также объективных методов исследования является важным в диагностике. …
28.03.2021 Гастроентерологія Гепадоктор: на захисті печінкиЗа останні десятиліття значно збільшився тягар хронічних захворювань печінки, зокрема через поширеність метаболічно-асоційованої жирової хвороби печінки. В усьому світі внаслідок захворювань печінки помирають приблизно 2 млн людей на рік, із них 1,16 млн осіб – від ускладнень цирозу печінки, який посідає 11-е місце серед найбільш частих причин смерті. У західних індустріальних країнах головними причинами розвитку цирозу є надмірне вживання алкоголю та неалкогольна жирова хвороба печінки (НАЖХП), тоді як у багатьох азіатських країнах це гепатит В (S.K. Asrani et al., 2019)….
В усьому світі внаслідок захворювань печінки помирають приблизно 2 млн людей на рік, із них 1,16 млн осіб – від ускладнень цирозу печінки, який посідає 11-е місце серед найбільш частих причин смерті. У західних індустріальних країнах головними причинами розвитку цирозу є надмірне вживання алкоголю та неалкогольна жирова хвороба печінки (НАЖХП), тоді як у багатьох азіатських країнах це гепатит В (S.K. Asrani et al., 2019)….
Запальні захворювання кишечнику (ЗЗК) – група хронічних рецидивуючих захворювань, які виникають унаслідок невідповідності імунної відповіді на кишкові коменсальні мікроорганізми у генетично схильних осіб, що призводить до запальної реакції з формуванням виразок у шлунково-кишковому тракті (ШКТ). В останні роки як патогенетичні механізми розглядають роль мікробіому, підвищеної проникності слизової оболонки кишечнику, оксидативного стресу й епігенетики [1]. До ЗЗК належать такі захворювання, як виразковий коліт (ВК) та хвороба Крона (ХК). …
Внепеченочные проявления первичного склерозирующего холангита | #02/12
Первичный склерозирующий холангит (ПСХ) — это хроническое прогрессирующее холестатическое заболевание печени неясной этиологии, характеризующееся негнойным деструктивным воспалением, облитерирующим склерозом и сегментарной дилятацией внутри- и внепеченочных желчных протоков, приводящее к развитию вторичного билиарного цирроза, портальной гипертензии и печеночной недостаточности [1]. Распространенность ПСХ в разных странах отличается. Так, в Северной Европе она составляет 10 на 100 тысяч населения, а в Азии ПСХ встречается в 10–100 раз реже. Болезнь развивается чаще у мужчин (женщины болеют в 1,5–2 раза реже) [2]. Чаще всего заболевание начинается в возрасте 30–40 лет, хотя известны случаи развития ПСХ в детском и пожилом возрасте [3].
Распространенность ПСХ в разных странах отличается. Так, в Северной Европе она составляет 10 на 100 тысяч населения, а в Азии ПСХ встречается в 10–100 раз реже. Болезнь развивается чаще у мужчин (женщины болеют в 1,5–2 раза реже) [2]. Чаще всего заболевание начинается в возрасте 30–40 лет, хотя известны случаи развития ПСХ в детском и пожилом возрасте [3].
В патогенезе ПСХ важная роль принадлежит нарушению иммунной толерантности. Доказательством этого являются обнаружение широкого спектра аутоантител в сыворотке крови таких больных: обнаружены антитела к ДНК, к гладкой мускулатуре, к билиарному эпителию, к тиреопероксидазе, антимитохондриальные антитела и некоторые другие (описано более 25 видов аутоантител у больных ПСХ), а также частое сочетание ПСХ с другими аутоиммунными заболеваниями, которые могут быть рассмотрены как системные проявления ПСХ [4]. Хронические воспалительные заболевания кишечника обнаруживают у 80–90% больных ПСХ, чаще это язвенный колит, реже встречается болезнь Крона с поражением толстой кишки [2, 3]. Реже ПСХ сочетается с аутоиммунным гепатитом, аутоиммунным тиреоидитом, сахарным диабетом 1-го типа, псориазом (до 10% случаев). Описаны отдельные наблюдения развития ревматоидного артрита, системной склеродермии, системной красной волчанки, склерита, увеита у больных ПСХ [5]. Частое сочетание ПСХ и воспалительных заболеваний кишечника легло в основу предположения о триггерной роли бактериальных антигенов в возникновении ПСХ, однако доказать это не удалось [2]. У родственников больных ПСХ в 11,5 раз повышен риск развития ПСХ, в 3 раза — язвенного колита и в 1,4 раза — болезни Крона [6]. Было сделано предположение о ключевой роли некоторых генов в развитии ПСХ. Были проведены исследования генов HLA-A, HLA-B, HLA-DR, MST1R, NOD2, ATG16L1, однако какого-либо одного гена, специфичного для ПСХ, не было найдено [2].
ПСХ можно заподозрить при наличии у больного синдрома холестаза, не объяснимого другими причинами. Чаще всего больных беспокоит выраженный кожный зуд, желтуха, лихорадка (чаще субфебрильная, при присоединении бактериального холангита — фебрильная), боли в правом подреберье, тошнота, общая слабость, быстрая утомляемость. Нередко (примерно у трети больных) жалобы отсутствуют, и холестаз выявляется случайно при лабораторном исследовании по другому поводу [3]. При лабораторном исследовании выявляют повышение активности гамма-глутамилтранспептидазы и щелочной фосфатазы, гипербилирубинемию (при развитии бактериального холангита уровень билирубина может резко возрастать), гиперлипидемию, повышение скорости оседания эритроцитов, иногда эозинофилию [7]. Диагноз подтверждают при магнитно-резонансной холангиографии или эндоскопической ретроградной холангиопанкреатографии («золотой стандарт»). При этих исследованиях выявляются участки сужения желчных протоков с неравномерными контурами, чередующиеся с нормальными или расширенными участками; мелкие внутрипеченочные протоки видны не все или не видны совсем (симптом «обгорелого дерева») [2]. При биопсии печени можно выявить особую форму ПСХ — мелкопротоковую (поражаются только мелкие внутрипеченочные протоки), а также иногда удается получить участки пораженных крупных протоков [3]. Морфологически ПСХ характеризуется негнойным деструктивным холангитом с облитерацией просветов желчных протоков и склерозом их стенок, выраженным перидуктальным фиброзом (феномен «луковичной шелухи»). Чаще всего (в 75% случаев) поражаются и крупные, и мелкие протоки, хотя встречаются случаи поражения только крупных или только мелких желчных протоков [2].
Нередко (примерно у трети больных) жалобы отсутствуют, и холестаз выявляется случайно при лабораторном исследовании по другому поводу [3]. При лабораторном исследовании выявляют повышение активности гамма-глутамилтранспептидазы и щелочной фосфатазы, гипербилирубинемию (при развитии бактериального холангита уровень билирубина может резко возрастать), гиперлипидемию, повышение скорости оседания эритроцитов, иногда эозинофилию [7]. Диагноз подтверждают при магнитно-резонансной холангиографии или эндоскопической ретроградной холангиопанкреатографии («золотой стандарт»). При этих исследованиях выявляются участки сужения желчных протоков с неравномерными контурами, чередующиеся с нормальными или расширенными участками; мелкие внутрипеченочные протоки видны не все или не видны совсем (симптом «обгорелого дерева») [2]. При биопсии печени можно выявить особую форму ПСХ — мелкопротоковую (поражаются только мелкие внутрипеченочные протоки), а также иногда удается получить участки пораженных крупных протоков [3]. Морфологически ПСХ характеризуется негнойным деструктивным холангитом с облитерацией просветов желчных протоков и склерозом их стенок, выраженным перидуктальным фиброзом (феномен «луковичной шелухи»). Чаще всего (в 75% случаев) поражаются и крупные, и мелкие протоки, хотя встречаются случаи поражения только крупных или только мелких желчных протоков [2].
Препаратом выбора при консервативном лечении ПСХ является урсодезоксихолевая кислота в дозе 20–30 мг/кг/сут (Урсофальк, Урсосан, Урдокса). Урсодезоксихолевая кислота обладает гепатопротективным действием — она образует нетоксичные мицеллы с токсичными желчными кислотами (хенозедоксихолевой, литохолевой), а также включается в состав мембран гепатоцитов и холангиоцитов, увеличивая их стабильность. Это уменьшает степень повреждения клеток печени токсичными желчными кислотами. Урсодезоксихолевая кислота обладает свойствами иммуномодулятора, угнетая экспрессию HLA-антигенов на мембранах гепатоцитов и холангиоцитов. Кроме того, препарат уменьшает литогенность желчи за счет уменьшения абсорбции холестерина в кишечнике, а также стимулирует холерез, что увеличивает выведение желчных кислот через кишечник [2, 3]. При неэффективности монотерапии урсодезоксихолевой кислотой к терапии добавляют фибраты, которые способствуют уменьшению холестаза [2].
Кроме того, препарат уменьшает литогенность желчи за счет уменьшения абсорбции холестерина в кишечнике, а также стимулирует холерез, что увеличивает выведение желчных кислот через кишечник [2, 3]. При неэффективности монотерапии урсодезоксихолевой кислотой к терапии добавляют фибраты, которые способствуют уменьшению холестаза [2].
Получены данные о том, что лактулоза (Дюфалак, Нормазе) в дозе 15–45 мл/сут обладает гепатопротективным действием, которое может реализовываться посредством нескольких механизмов: 1) ингибирование продукции аммиака и других ксенобиотиков; 2) утилизация образовавшегося аммиака; 3) нарушение всасывания и быстрое выведение аммиака с калом [7, 8]. Уменьшение образования аммиака в кишечнике под действием лактулозы связано с уменьшением количества кишечной микрофлоры, продуцирующей уреазу. Утилизация аммиака происходит при помощи бактерий, использующих азотсодержащие соединения в качестве субстрата для синтеза собственных белков; лактулоза способствует увеличению количества этих микроорганизмов в кишечнике. Кроме того, лактулоза способна связывать молекулы аммиака и увеличивать скорость транзита содержимого по кишечнику, что способствует быстрому выведению аммиака из организма. Лактулоза обладает свойствами пребиотика: под ее воздействием в кишечнике увеличивается количество бифидобактерий и уменьшается количество патогенных бактерий, что предотвращает избыточный бактериальный рост и снижает риск проникновения антигенов патогенных бактерий из кишечника в кровь [14]. Недавно в России было проведено исследование, согласно результатам которого при лечении больных с холестазом урсодезоксихолевой кислотой в комбинации с лактулозой (Урсолив) наблюдается большее уменьшение выраженности холестаза, чем при лечении только урсодезоксихолевой кислотой [9].
Таким образом, совместное применение урсодезоксихолевой кислоты и лактулозы приводит к синергизму гепатопротективного эффекта обоих веществ.
При сочетании ПСХ с аутоиммунным гепатитом к лечению добавляют глюкокортикостероиды и/или иммуносупрессанты в дозах, стандартных для лечения аутоиммунного гепатита [9]. С целью устранения зуда в качестве препарата первой линии применяют Холестирамин (4 г/сут), однако не все пациенты хорошо его переносят: наиболее частыми причинами отказа от препарата являются его вкус, вздутие живота, запоры или диарея. При непереносимости Холестирамина применяют Рифампицин (300 мг/сут), Сертралин (75–100 мг/сут), Налтрексон (50 мг/сут). При выраженном зуде может потребоваться альбуминовый диализ или плазмаферез. Нестерпимый зуд, не купирующийся консервативными методами, может являться самостоятельным показанием к трансплантации печени. Длительный холестаз является фактором риска развития остеопороза, поэтому таким пациентам в схему лечения необходимо включать кальций (1500 мг/сут) и витамин D (1000 МЕ/сут). Витамин K назначается при наличии геморрагического синдрома, особенно перед инвазивными диагностическими процедурами [3, 10].
С целью устранения зуда в качестве препарата первой линии применяют Холестирамин (4 г/сут), однако не все пациенты хорошо его переносят: наиболее частыми причинами отказа от препарата являются его вкус, вздутие живота, запоры или диарея. При непереносимости Холестирамина применяют Рифампицин (300 мг/сут), Сертралин (75–100 мг/сут), Налтрексон (50 мг/сут). При выраженном зуде может потребоваться альбуминовый диализ или плазмаферез. Нестерпимый зуд, не купирующийся консервативными методами, может являться самостоятельным показанием к трансплантации печени. Длительный холестаз является фактором риска развития остеопороза, поэтому таким пациентам в схему лечения необходимо включать кальций (1500 мг/сут) и витамин D (1000 МЕ/сут). Витамин K назначается при наличии геморрагического синдрома, особенно перед инвазивными диагностическими процедурами [3, 10].
К хирургическим методам лечения ПСХ относятся установка стентов, резекция пораженных участков желчных протоков, трансплантация печени. Стентирование, баллонная дилятация и резекция пораженных участков протоков лишь временно уменьшают выраженность холестаза, не останавливая прогрессирование ПСХ. Наиболее эффективным хирургическим методом лечения ПСХ является трансплантация печени, которая улучшает выживаемость больных. Однако у 15–20% больных развивается рецидив ПСХ в трансплантате, что ухудшает прогноз таких пациентов [2, 3, 10].
При естественном течении ПСХ часто развивается холангиокарцинома (до 40% больных), повышен риск развития рака поджелудочной железы и колоректального рака, поэтому необходимы как можно более ранние диагностика и лечение этого заболевания [11, 12].
Цель исследования. Изучение распространенности и спектра внепеченочных проявлений первичного склерозирующего холангита.
Материалы и методы. Объектом исследования были 23 больных первичным склерозирующим холангитом, наблюдавшихся в Клинике нефрологии, внутренних и профессиональных заболеваний им. Е. М. Тареева Первого МГМУ им. И. М. Сеченова в период с 1984 по 2010 гг. В группе было 12 мужчин и 11 женщин, средний возраст данной группы составил 36,4 ± 13,7 года, средний возраст начала заболевания 30,6 ± 15 лет, средняя продолжительность заболевания 5,8 ± 5,2 года.
Е. М. Тареева Первого МГМУ им. И. М. Сеченова в период с 1984 по 2010 гг. В группе было 12 мужчин и 11 женщин, средний возраст данной группы составил 36,4 ± 13,7 года, средний возраст начала заболевания 30,6 ± 15 лет, средняя продолжительность заболевания 5,8 ± 5,2 года.
Материалами исследования служили данные из архивных записей в историях болезни и амбулаторных картах. Критерием включения в исследование являлся подтвержденный диагноз ПСХ (морфологически, посредством магнитно-резонансной холангиографии или ретроградной эндоскопической холангиопанкреатографии). Критерием исключения являлось наличие у больного сочетания ПСХ и аутоиммунного гепатита, так как аутоиммунный гепатит также характеризуется широким спектром системных проявлений. Изучалось наличие следующих системных проявлений ПСХ: хронические воспалительные заболевания кишечника (язвенный колит и болезнь Крона), поражение глаз (склерит, кератит), аутоиммунный тиреоидит, синдром Шегрена, геморрагический васкулит.
Результаты и обсуждение. У 16 больных (69,6%) были выявлены внепеченочные проявления ПСХ. Из данных, представленных в табл. 1, видно, что в обследованной группе были выявлены хронические воспалительные заболевания кишечника (язвенный колит и болезнь Крона), синдром Шегрена, геморрагический васкулит, поражение глаз (склерит, кератит), поражение щитовидной железы (аутоиммунный тиреоидит).
У пациентов с сочетанием ПСХ и болезни Крона (5 больных) в 1 случае была поражена только толстая кишка; в 2 случаях — и тонкая, и толстая кишка; в 2 случаях — только тонкая кишка. Отсутствие поражения толстой кишки у двух больных с болезнью Крона при ПСХ указывает на необходимость длительного динамического наблюдения за этими пациентами, так как в дальнейшем у них возможно присоединение поражения толстой кишки.
У 4 больных (17,4%) отмечено сочетание нескольких системных проявлений ПСХ. У 3 больных выявлено два внепеченочных проявления ПСХ (2 случая — язвенный колит в сочетании с аутоиммунным тиреоидитом, 1 случай — язвенный колит в сочетании с геморрагическим васкулитом).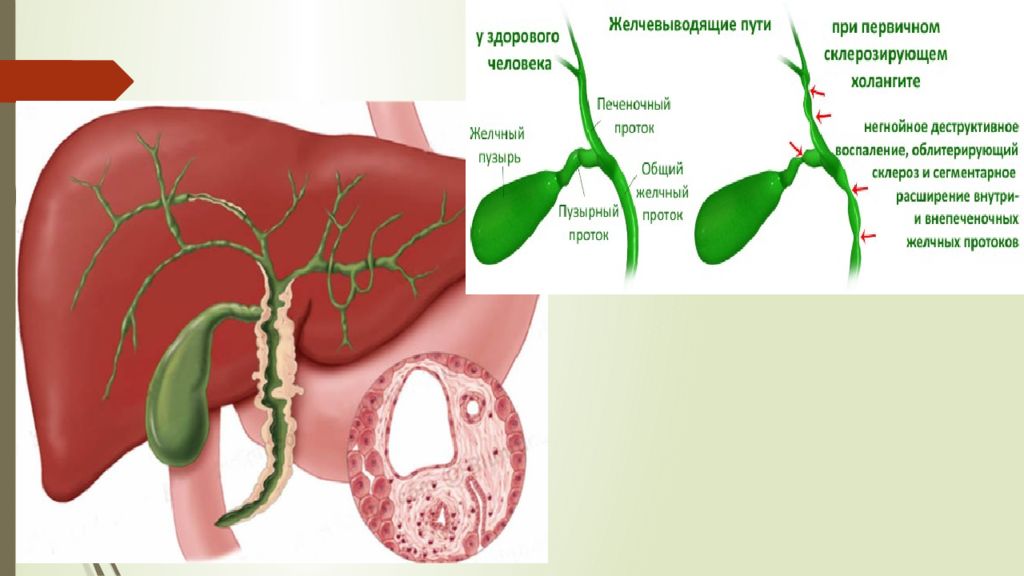 У 1 пациента выявлено три внепеченочных проявления ПСХ — язвенный колит в сочетании с геморрагическим васкулитом и поражением глаз (склерит, кератит).
У 1 пациента выявлено три внепеченочных проявления ПСХ — язвенный колит в сочетании с геморрагическим васкулитом и поражением глаз (склерит, кератит).
В связи с повышенным риском развития онкологических заболеваний у больных ПСХ мы изучили распространенность злокачественных заболеваний в изучаемой группе больных. Онкологические заболевания были выявлены у 3 больных (13%): 1 случай (пациент с ПСХ в сочетании с болезнью Крона) — лимфома с поражением тонкой кишки, выявлена одновременно с подтверждением диагноза ПСХ; 1 случай (больная с ПСХ без системных проявлений) — лимфома с поражением печени, лимфатических узлов ворот печени, забрюшинных лимфатических узлов, выявлена одновременно с подтверждением диагноза ПСХ; 1 случай (пациентка с ПСХ в сочетании с язвенным колитом) — аденокарцинома толстой кишки, выявлена через 13 лет после подтверждения диагноза ПСХ. В связи с частым развитием злокачественных опухолей у больных ПСХ необходима постоянная онкологическая настороженность врачей, работающих с этой категорией больных.
Также мы проанализировали распространенность системных проявлений ПСХ в зависимости от пола больных и возраста первых проявлений ПСХ (табл. 2 и 3).
Как видно из табл. 2, хронические воспалительные заболевания кишечника, поражение глаз и синдром Шегрена встречались чаще у мужчин, а поражение щитовидной железы было зарегистрировано только у женщин. Возможно, меньшая подверженность женщин хроническим воспалительным заболеваниям кишечника связана с большей концентрацией эстрогенов в их крови, чем у мужчин. В эксперименте на мышах (Harnish D. C. et al., 2004) был доказан положительный эффект эстрогенов при лечении хронических воспалительных заболеваний кишечника, однако необходимо дальнейшее исследование этого вопроса [13]. Более частое развитие аутоиммунного тиреоидита у женщин, наиболее вероятно, связано с более низким содержанием тестостерона в их крови, чем у мужчин. В исследовании, проведенном на мышах, Ansar A. S. et al. (1986) доказали положительный эффект тестостерона при лечении аутоиммунного тиреоидита [14].
et al. (1986) доказали положительный эффект тестостерона при лечении аутоиммунного тиреоидита [14].
С целью изучения связи частоты обнаружения системных проявлений ПСХ и возраста начала заболевания мы разделили больных ПСХ на две подгруппы — тех, у кого заболевание началось в детском возрасте (6 человек, возраст начала заболевания от 10 до 17 лет), и тех, у кого первые проявления ПСХ возникли во взрослом состоянии (17 человек, возраст начала заболевания от 20 до 66 лет) (табл. 3).
Из табл. 3 следует, что в группе больных, у которых ПСХ начался в детском возрасте, внепеченочные проявления регистрировались чаще, чем в группе пациентов, заболевших во взрослом состоянии. Причина такого различия распространенности системных проявлений ПСХ в различных возрастных группах в настоящее время неясна, необходимы дальнейшие исследования этого вопроса, в том числе обследование больших групп больных ПСХ.
Выводы
- ПСХ часто сопровождается внепеченочными проявлениями, наиболее распространенные из которых — хронические воспалительные заболевания кишечника.
- У одного больного может встречаться сочетание нескольких системных проявлений ПСХ.
- Поражение кишечника при ПСХ чаще развивается у мужчин, поражение щитовидной железы — у женщин.
- ПСХ, развившийся в детском возрасте, сопровождается системными проявлениями чаще, чем ПСХ, начавшийся у взрослых.
Литература
- Лазебник Л. Б., Рыбак В. С., Ильченко Л. Ю. Первичный склерозирующий холангит // Consilium Medicum. 2003; 6: 28–30.
- Авдеев В. Г. Первичный склерозирующий холангит // Гепатологический форум. 2009; 1: 24–32.
- Karlsen T. H., Schrumpf E., Boberg K. M. Update on primary sclerosing cholangitis // Digestive and Liver Disease. 2010; 42: 390–400.
- Hov J. R., Boberg K. M., Karlsen T. H. Autoantibodies in primary sclerosing cholangitis //World J.
 Gastroenterol. 2008; 14 (24): 3781–3791.
Gastroenterol. 2008; 14 (24): 3781–3791. - Saarinen S., Olerup O., Broome U. Increased frequency of autoimmune diseases in patients with primary sclerosing cholangitis // Am. J. Gastroenterol. 2000; 95: 3195–3199.
- Bergquist A., Montgomery S. M., Bahmanyar S. et al. Increased risk of primary sclerosing cholangitis and ulcerative colitis in first-degree relatives of patients with primary sclerosing cholangitis // Clin. Gastroenterol. Hepatol. 2008; 6 (8): 939–943.
- VanBerge-Henegouwen G. P., Portincasa P., van Erpecum K. J. Effect of lactulose and fiber-rich diets on bile in relation to gallstone diosease: an update // Scand. J. Gastroenterol. Suppl. 1997; 222: 68–71.
- Григорьев П. Я., Яковенко Э. П. Лактулоза в терапии заболеваний органов пищеварения // Российский гастроэнтерологический журнал. 2000; № 2: 71–78.
- Кучмин А. Н., Резван В. В., Евсюков К. Б. и соавт. Исследование клинической эффективности совместного применения урсодезоксихолевой кислоты и лактулозы у больных с гепато-билиарной патологией // Русский медицинский журнал. 2011; Том 19, № 12: 742–747.
- Авдеев В. Г., Бурневич Э. З., Северов М. В. Первичный склерозирующий холангит. В кн.: Практическая гепатология. Под ред. Мухина Н. А. М.: Проект «Мы». 2004. 111–115.
- Duclos-Vallee J. C., Sebagh M. Recurrence of autoimmune disease, primary sclerosing cholangitis, primary biliary cirrhosis, and autoimmune hepatitis after liver transplantation // Liver Transpl. 2009; 15 (Suppl. 2): S25-S34.
- Мухин Н. А., Абдурахманов Д. Т., Лопаткина Т. Н. и соавт. Первичный склерозирующий холангит у молодой женщины // Клиническая гепатология. 2006; 3: 34–39.
- Harnish D. C., Albert L. M., Leathurby Y. et al. Beneficial effects of estrogen treatment in the HLA-B27 transgenic rat model of inflammatory bowel disease // Am.
 J. Physiol. Gastrointest. Liver Physiol. 2004; 286 (1): G118–125.
J. Physiol. Gastrointest. Liver Physiol. 2004; 286 (1): G118–125. - Ansar Ahmed S., Young P. R., Penhale W. J. Beneficial effect of testosterone in the treatment of chronic autoimmune thyroiditis in rats // J. Immunol. 1986; 136 (1): 143–147.
Е. А. Александрова*
Э. З. Бурневич*, кандидат медицинских наук, доцент
Е. А. Арион**
* ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития РФ,
**Клиника нефрологии, внутренних и профессиональных болезней им. Е. М. Тареева, Москва
Контактная информация об авторах для переписки: [email protected]
Холангит | MUSC Health | Чарльстон SC
Что такое холангит?
Холангит относится к воспалению общего желчного протока из-за того, что один или несколько желчных камней выходят из желчного пузыря и застревают, что препятствует оттоку желчи из печени в тонкий кишечник.
Что вызывает холангит?
Камни желчных протоков, а также медицинские процедуры, влияющие на общий желчный проток, являются наиболее значительными факторами развития холангита.
Некоторые причины включают:
- бактериальная инфекция
- Закупорка, вызванная одним или несколькими желчными камнями в желчном дереве
- Блокировка, вызванная непреднамеренно в результате манипуляций во время медицинской процедуры
- опухоль, поразившая желчное дерево
Факторы риска
У человека больше шансов заболеть холангитом, если присутствует какой-либо из этих факторов риска:
- История камней в желчном пузыре
- Склерозирующий холангит, состояние, при котором повреждены протоки, ведущие к печени
- ВИЧ (вирус иммунодефицита человека)
- аномально узкий желчный проток, который может быть врожденным (имеется в виду, что человек родился с этим заболеванием)
Холангит представляет значительный риск для здоровья и даже смерть, если не лечить его вовремя. Это в первую очередь затрагивает людей в возрасте от 50 до 60 лет. Не существует расы или пола, которые подвергаются значительно большему риску развития холангита.
Это в первую очередь затрагивает людей в возрасте от 50 до 60 лет. Не существует расы или пола, которые подвергаются значительно большему риску развития холангита.
Симптомы
Симптомы могут включать:
- Боль в животе в правой верхней области кишечника
- лихорадка и озноб
- табуреты глиняные
- темная моча
- тошнота и рвота
- желтуха (желтый оттенок, появляющийся в глазах и на коже)
Боль может быть периодической, а также может распространяться на спину.Боли могут быть слабыми или интенсивными, в зависимости от тяжести состояния.
Тесты
Поскольку эти симптомы являются общими для ряда состояний, поражающих желчевыводящие пути, ваш врач может назначить несколько тестов, чтобы определить причину ваших симптомов.
- УЗИ, с помощью которого можно определить наличие камней
- ЭРХПГ (эндоскопическая ретроградная холангиопанкреатография)
- MRCP (магнитно-резонансная холангиопанкреатография)
- холангиограмма или чрескожная чреспеченочная холангиограмма
Следующие анализы крови могут проводиться в плановом порядке для определения текущего состояния определенных уровней ферментов в вашем кровотоке:
- Анализы крови, особенно лейкоцитов, так как это показатель инфекции
- Уровень билирубина (пигмент, который содержится в крови и кале человека)
- Ферментные и функциональные пробы печени
Лечение
Важно немедленно заняться лечением холангита, поскольку в результате могут возникнуть осложнения, которые только усугубят состояние.Боль и дискомфорт, испытываемые больным холангитом, могут стать довольно сильными.
- Антибиотики часто используются для остановки инфекции желчных путей.
- ERCP может быть проведена для удаления камней или открытых стриктур, которые могли вызвать холангит.
- Хирургия часто рассматривается у пациентов, которые не реагируют на антибиотики или неинвазивные процедуры, такие как ERCP.

Восстановление
После начала приема антибиотиков человек обычно быстро начинает чувствовать себя лучше.Выздоровление во многом зависит от того, как быстро будет начато лечение, поэтому очень важно как можно скорее проконсультироваться с врачом.
Осложнения
Одним из возможных осложнений является сепсис, состояние, при котором организм сильно реагирует на бактерии. Человеческие системы воспаляются при сепсисе. Артериальное давление падает, органы начинают отключаться. Без немедленной медицинской помощи результатом может быть смерть. Это может произойти очень быстро.
Холангит — это заболевание, требующее активного и быстрого лечения.При появлении нескольких симптомов (перечисленных ранее на этой странице) всегда разумно немедленно обратиться за медицинской помощью.
Первичный билиарный холангит — симптомы, причины и лечение
Как лечится первичный билиарный холангит?
Лечение болезни
Нет лекарства от ПБЦ, однако есть лекарства, которые могут помочь замедлить прогрессирование болезни и облегчить симптомы. Урсодиол (торговые марки Actigall, URSO 250, URSO Forte) — это встречающаяся в природе желчная кислота (урсодезоксихолевая кислота или УДХК), которая помогает перемещать желчь из печени в тонкий кишечник.При достаточно раннем применении Урсодиол может улучшить функцию печени и избавить вас от необходимости или отсрочить необходимость трансплантации печени . Люди с ПБЦ должны принимать это лекарство каждый день на всю жизнь.
УДХК эффективен более чем у 50 процентов пациентов, но до 40 процентов пациентов не достигают адекватного снижения щелочной фосфотазы (ЩФ) или билирубина с УДХК, в то время как 5-10 процентов не переносят УДХК.
В мае 2016 года обетихолевая кислота (торговая марка Ocaliva) была одобрена для лечения ПБЦ в комбинации с УДХК у взрослых с неадекватным ответом на УДХК или в качестве единственной терапии у взрослых, не переносящих УДХК. Обетихолевая кислота увеличивает отток желчи от печени и подавляет выработку желчной кислоты в печени, тем самым снижая воздействие на печень токсичных уровней желчных кислот. Побочные эффекты обетихолевой кислоты могут включать усиление зуда и повышение уровня липидов в крови.
Обетихолевая кислота увеличивает отток желчи от печени и подавляет выработку желчной кислоты в печени, тем самым снижая воздействие на печень токсичных уровней желчных кислот. Побочные эффекты обетихолевой кислоты могут включать усиление зуда и повышение уровня липидов в крови.
Другие альтернативные методы лечения пациентов с неполным ответом на УДХК включают фенофибрат. Также могут быть назначены лекарства для подавления иммунной системы, включая преднизон или азатиоприн, пациентам с ПБЦ с «синдромом перекрытия» с аутоиммунным гепатитом. Трансплантация печени рассматривается, когда лечение более не позволяет контролировать болезнь. Когда у человека терминальная стадия заболевания печени, для выживания необходима трансплантация печени.
Лечение симптомов
Сильный зуд — один из наиболее частых симптомов ПБЦ. Могут быть полезны безрецептурные антигистаминные препараты, такие как дифенгидрамин (Бенадрил). Могут быть назначены другие агенты, такие как рифампицин, налтрексон, холестирамин и сертралин.
Сухость глаз можно уменьшить, используя глазные капли (искусственные слезы).
При сухости во рту можно облегчить сосание леденцов или жевательной резинки, которые увеличивают слюноотделение. Также можно использовать заменители слюны и некоторые лекарства.
Профилактика осложнений
Часто проводятся анализы крови для выявления дефицита жирорастворимых витаминов. По мере прогрессирования ПБХ некоторым людям необходимо восполнять жирорастворимые витамины, теряемые при жирном стуле, поэтому вам может быть назначена заместительная терапия витаминами A, D, E и K.
Поскольку люди с ПБЦ подвержены более высокому риску остеопороза, обычно назначают кальций и витамин D. На момент постановки диагноза в настоящее время рекомендуется исходная плотность костной ткани.
Поскольку способность печени функционировать со временем снижается, необходимо устранять и лечить осложнения, связанные с циррозом. Часто рекомендуется обследование на наличие варикозного расширения вен и рака печени.
Часто рекомендуется обследование на наличие варикозного расширения вен и рака печени.
Первичный склерозирующий холангит: симптомы, причины, лечение
Первичный склерозирующий холангит (ПСХ) — это заболевание, поражающее желчные протоки.Желчь — это пищеварительная жидкость, которую вырабатывает печень. Протоки позволяют ей течь из печени в желчный пузырь и, наконец, в тонкий кишечник. Там он помогает расщеплять жиры из пищи.
При ПСХ воспаляются желчные протоки. Это приводит к образованию рубцов, которые блокируют прохождение желчи через них. В результате он накапливается в вашей печени и повреждает ее клетки. Это также вызывает образование рубцовой ткани в печени.
Со временем рубцовая ткань влияет на способность вашей печени работать должным образом и может привести к циррозу и, в конечном итоге, к печеночной недостаточности.
ЗОП может случиться в любом возрасте. Но это чаще встречается у взрослых, чем у детей, и поражает больше мужчин, чем женщин. Около 70% людей с ПСХ — мужчины.
Симптомы
ПСХ развивается медленно. У вас может быть это в течение многих лет, прежде чем вы заметите какие-либо симптомы. Вот некоторые из признаков:
По мере ухудшения ПСХ ваши желчные протоки могут инфицироваться. Это может вызвать жар, озноб и боль в животе.
Причины
Врачи не уверены, что вызывает ПСХ. Это может быть вирус, бактерии, гены или проблемы с вашей иммунной системой.
Это связано с воспалительным заболеванием кишечника, в первую очередь с язвенным колитом и, реже, с болезнью Крона. Около 75% людей с ПСХ страдают язвенным колитом. Врачи не знают, как и почему связаны эти состояния.
Диагноз
Ваш врач возьмет образец вашей крови, чтобы проверить уровень ферментов вашей печени. Необычный уровень определенных ферментов может быть признаком того, что у вас есть ПСХ.
Чтобы подтвердить это, вам нужно будет пройти визуализационный тест, называемый холангиографией, чтобы ваш врач поближе посмотрел на ваши желчные протоки. Существует несколько различных типов холангиографии:
Существует несколько различных типов холангиографии:
- Магнитно-резонансная холангиопанкреатография (MRCP). Он использует мощные магниты и радиоволны для получения детальных изображений желчных протоков. Часто это первый выбор врача, потому что он безопасен, безболезнен и неинвазивен.
- Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Перед обследованием вы получите успокаивающее средство, чтобы сохранять спокойствие и комфорт. Ваш врач вставит длинную гибкую трубку, называемую эндоскопом, через ваш рот в пищеварительный тракт.Они введут краситель в желчные протоки и сделают рентген. Краситель способствует более четкому отображению желчных протоков.
- Чрескожная чреспеченочная холангиография. Врач вводит иглу в кожу, вставляет тонкую трубку в проток в печени и вводит краситель. Затем они делают рентген.
Лечение
Не было показано лекарств, помогающих с PTC, но исследователи работают над этим. Вы можете спросить своего врача, имеете ли вы право на участие в каких-либо испытаниях лекарственной терапии.Эти тестовые лекарства, которые еще не одобрены для лечения ПСХ, могут помочь с вашими симптомами или помочь контролировать повреждение печени.
Если у вас есть эндоскопическая ретроградная холангиопанкреатография, ваш врач может использовать специальные инструменты через эндоскоп, чтобы открыть заблокированные желчные протоки.
В противном случае цель состоит в том, чтобы облегчить симптомы и контролировать возможные осложнения. Например, ваш врач может прописать лекарства для облегчения зуда, антибиотики для борьбы с инфекцией или витаминные добавки для устранения недостатков.
Если у вас печеночная недостаточность, вам может потребоваться пересадка печени. Большинство людей с ПСХ после этого имеют очень хорошие результаты и качество жизни.
Первичный билиарный холангит — NORD (Национальная организация по редким заболеваниям)
Точная причина ПБХ неизвестна. Возможные иммунологические, аутоиммунные, генетические факторы и / или факторы окружающей среды исследуются в качестве потенциальных причин.
Возможные иммунологические, аутоиммунные, генетические факторы и / или факторы окружающей среды исследуются в качестве потенциальных причин.
Иммунологические отклонения могут быть важным фактором развития ПБЦ.Иммунная система разделена на несколько компонентов, совокупное действие которых отвечает за защиту от различных инфекций. Система Т-клеток (клеточно-опосредованный иммунный ответ) отвечает за борьбу с дрожжами и грибками, некоторыми вирусами и некоторыми бактериями. Система В-клеток (гуморальный иммунный ответ) борется с инфекцией, вызванной другими вирусами и бактериями. Это достигается путем выделения иммунных факторов, называемых антителами (также известных как иммуноглобулины), в жидкую часть крови (сыворотку) и секреты организма (например,г., слюна). У людей с ПБЦ наблюдается необычно пониженное количество циркулирующих Т-клеток в крови и нарушения функции и регуляции Т-клеток (то есть хелперных и супрессорных Т-клеток). Роль аномалий Т-лимфоцитов в развитии симптомов, связанных с ПБЦ, неизвестна.
Аутоиммунитет также может способствовать возникновению ПБЦ. Аутоиммунные расстройства возникают, когда естественная защита организма от вторжения микроорганизмов ошибочно атакует здоровые ткани. Например, антитела обычно напрямую убивают «захватчиков» (например,g., микроорганизмы, токсины и другие посторонние вещества) или покрывают их, чтобы они легче разрушались лейкоцитами. (Лейкоциты [лейкоциты] являются частью системы защиты организма, играя важную роль в защите от инфекции, а также в борьбе с инфекцией, если она возникла.) Однако у некоторых пациентов антитела могут неправильно формироваться против некоторых из них. собственные ткани, вызывающие аутоиммунное заболевание.
Примерно 95 процентов людей с ПБЦ вырабатывают антитела (известные как «аутоантитела»), которые действуют на определенные митохондрии организма (митохондриальные аутоантигены, напр.g., компонент E2 комплекса пируватдегидрогеназы [PDC-E2], компонент E2 комплекса дегидрогеназы 2-оксокислот с разветвленной цепью [BCOADC-E2]).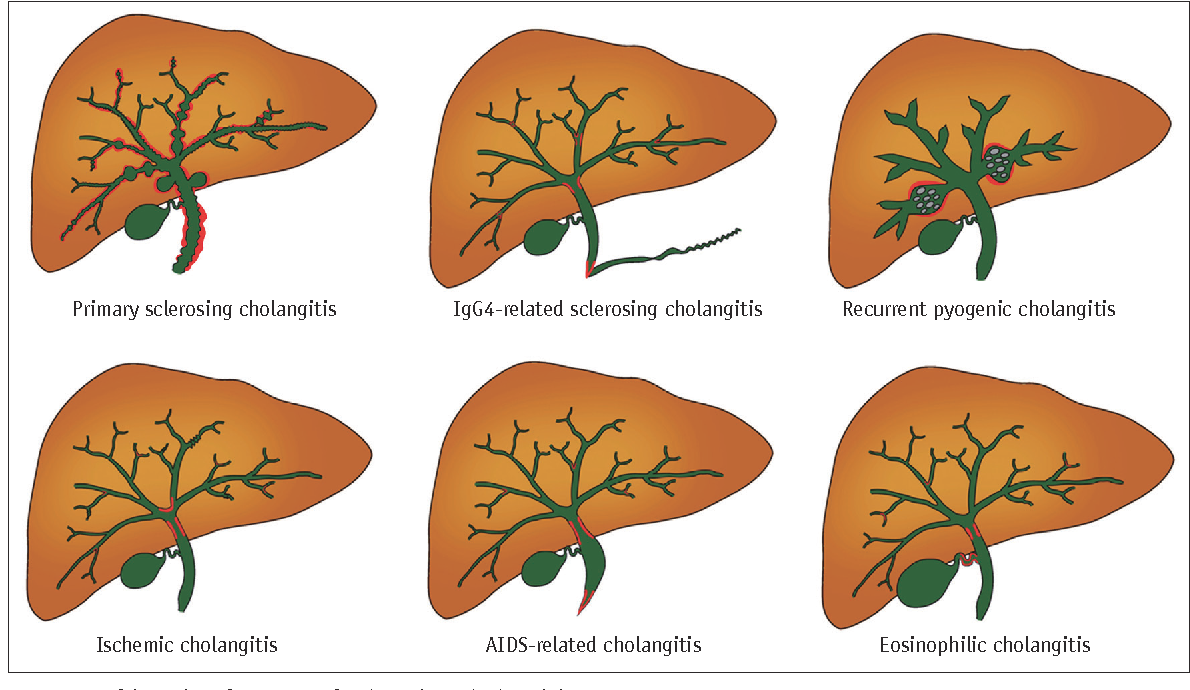 Митохондрии обнаруживаются сотнями внутри клеток тела и несут в себе схемы для производства энергии. Они имеют свои собственные генетические инструкции (мтДНК) и расположены вне ядра клетки (цитоплазмы). Роль антимитохондриальных антител в потенциальном возникновении симптомов, связанных с ПБЦ, до конца не изучена.
Митохондрии обнаруживаются сотнями внутри клеток тела и несут в себе схемы для производства энергии. Они имеют свои собственные генетические инструкции (мтДНК) и расположены вне ядра клетки (цитоплазмы). Роль антимитохондриальных антител в потенциальном возникновении симптомов, связанных с ПБЦ, до конца не изучена.
Кроме того, у некоторых людей с ПБЦ специализированные лабораторные тесты, проведенные на жидкой части крови (сыворотке), показали присутствие определенных антител, обычно вырабатываемых в ответ на определенные вирусы (например,g., ретровирусные антигены). Антигены — это вещества, такие как микроорганизмы, токсины или другие чужеродные вещества, которые могут запускать выработку определенных антител как часть иммунного ответа. Это говорит о том, что у людей с ПБЦ определенные антитела могут ошибочно реагировать на один или несколько собственных белков организма, которые очень похожи на фрагменты белков из определенных вторгшихся вирусов (т. Е. Иммунная система не может различить «имитирующие» белки. на поверхности определенных вирусов и собственных белков организма).С другой стороны, такие результаты могут служить доказательством того, что ПБЦ может быть вызван, по крайней мере частично, предыдущей бактериальной или вирусной инфекцией, обнаружение, которое было продемонстрировано при других аутоиммунных заболеваниях.
Поскольку в медицинской литературе сообщалось о ряде семейных случаев ПБЦ, также есть подозрения, что определенные генетические факторы могут играть определенную роль в развитии ПБХ. Факторы окружающей среды или другие факторы могут вызывать симптомы у людей с генетической предрасположенностью к заболеванию.
Необходимы дальнейшие исследования для определения потенциальной роли, которую иммунологические, аутоиммунные, генетические, экологические и / или другие факторы могут играть в возникновении ПБЦ.
Холангит. Что такое холангит? Заболевание желчного пузыря
Введение
[1] Острый обструктивный холангит был определен Рейнольдсом и Дарганом в 1959 году как синдром, состоящий из летаргии или спутанности сознания и шока, а также вызванных лихорадкой, желтухой и болью в животе. путем непроходимости желчных путей.Эти пять симптомов были названы пентадой Рейнольдса.
путем непроходимости желчных путей.Эти пять симптомов были названы пентадой Рейнольдса.
Острый холецистит — острое воспалительное заболевание желчного пузыря, часто вызываемое желчными камнями; однако также задействованы многие факторы (например, ишемия, нарушения моторики, химическое повреждение, инфекции, вызванные микроорганизмами, простейшими и паразитами, заболевание коллагеном и аллергические реакции).
Термин «печеночная лихорадка» впервые был использован Шарко в его отчете, опубликованном в 1887 году. Перемежающаяся лихорадка, сопровождающаяся ознобом, болью в правом верхнем квадранте живота и желтухой, была установлена как триада Шарко.
Желчь обычно стерильна; однако, если общий желчный проток (CBD) заблокирован, отток желчи уменьшается (застой желчных протоков), и может возникнуть инфекция. Инфекция также может течь ретроградно вверх по CBD в результате острого холецистита или таких инструментов, как эндоскопическая ретроградная холангиопанкреатография (ERCP).
Наиболее распространены в Великобритании виды Klebsiella , Escherichia coli , Enterobacter spp., Энтерококки и стрептококки.Может быть задействовано более одного организма. За пределами Великобритании холангит может быть вызван аскаридой и печеночной двуусткой [2] .
NB : первичный склерозирующий холангит — это этиологически не связанное идиопатическое заболевание, которому посвящена отдельная статья.
Эпидемиология
[1]- До 9% пациентов, госпитализированных с желчнокаменной болезнью, страдают острым холангитом [3] .
- Примерно у 1% пациентов развивается холангит после ERCP [4] .
- Структура расового распределения в некоторой степени повторяет расы, среди которых высока распространенность желчных камней, то есть светлокожие люди североевропейского происхождения, выходцы из Латинской Америки, коренные американцы и индейцы пима.

- Соотношение мужчин и женщин одинаковое.
- Средний возраст обращения 50-60 лет.
- Злокачественные заболевания (опухоли желчных протоков, опухоли желчного пузыря, ампулярные опухоли, опухоли поджелудочной железы и опухоли двенадцатиперстной кишки) составляют 10-30% случаев острого холангита.
Этиология
[5, 6]- Закупорка желчного пузыря или желчного протока из-за камней.
- ERCP.
- Опухоли — рак поджелудочной железы, холангиокарцинома, ампулярный рак, опухоли или метастазы ворот печени.
- Стриктура или стеноз желчного протока.
- Холедохоцеле (киста или дивертикул CBD).
- СПИД-холангиопатия.
- Паразитарная инфекция — аскариды, печеночная двуустка.
Презентация
- 50–70% пациентов имеют классическую триаду Шарко, состоящую из желтухи, лихорадки и боли в правом подреберье.
- У пожилых пациентов боль в животе может быть плохо локализована.
- Острый холангит классифицируется по степени тяжести от I (легкая), II (умеренная) и III (тяжелая) степени. Тяжелый острый холангит — это острый холангит, связанный, по крайней мере, с одной из сердечно-сосудистой, неврологической, респираторной, почечной, печеночной и / или гематологической дисфункцией [1] .
- 10-20% пациентов также имеют дополнительные признаки гипотонии из-за септического шока и спутанности сознания — пентада Рейнольдса.
- Пациент также может сообщать об ахолическом (замазанном) стуле и зуде.
- История желчных камней, камней CBD, недавняя холецистэктомия, ERCP или другие инвазивные процедуры, ВИЧ или СПИД могут помочь в постановке диагноза.
- У некоторых пациентов возникает несколько приступов, обычно связанных с нелеченными камнями желчных путей (рецидивирующий пиогенный холангит).
- Физические признаки могут включать жар, болезненность в правом верхнем квадранте, желтуху, изменения психического статуса, гипотонию и тахикардию.
 Перитонизм — необычный признак и должен стимулировать поиск альтернативного диагноза.
Перитонизм — необычный признак и должен стимулировать поиск альтернативного диагноза.
Диагностические критерии острого холангита
[1]- A. Системное воспаление:
- A-1. Лихорадка и / или дрожащий озноб — температура> 38 ° C.
- А-2. Лабораторные данные: свидетельство воспалительной реакции — аномальное количество лейкоцитов, повышение уровня С-реактивного белка в сыворотке и другие изменения, указывающие на воспаление.
- Б.Холестаз:
- В-1. Желтуха.
- Б-2. Лабораторные данные: аномальные LFT — повышенные уровни сывороточной ЩФ, γGTP (GGT), AST и ALT.
- C. Изображение:
- C-1. Расширение желчевыводящих путей.
- С-2. Доказательства этиологии при визуализации (стриктура, камень, стент и т. Д.).
Предполагаемый диагноз: один пункт в A + один пункт в B или C.
Определенный диагноз: один пункт в A, один пункт в B и один пункт в C.
Дифференциальный диагноз
Исследования
Кровь тесты
- FBC: количество лейкоцитов обычно повышено.
- Воспалительные маркеры: могут быть повышены СОЭ и СРБ.
- LFT: обычно демонстрируют структуру механической желтухи.
- Функциональные пробы почек и электролиты: ассоциированная почечная дисфункция.
- Посев крови.
- Уровень амилазы может быть повышен, что часто указывает на поражение нижней части общего желчного протока.
- Если желчная жидкость доступна (например, произошел дренаж желчных путей в результате вмешательства), образец следует отправить на посев.
Визуализация
[1] При подозрении на острый холангит диагностическая оценка включает рентгенологическое исследование брюшной полости (почек, мочеточников и мочевого пузыря) и УЗИ брюшной полости.Лучшим методом диагностики острого холангита является динамическая КТ с контрастированием, за которой следует МРТ. Магнитно-резонансная холангиопанкреатография (MRCP) также может быть необходима для обнаружения некальцинированных желчных камней.
Магнитно-резонансная холангиопанкреатография (MRCP) также может быть необходима для обнаружения некальцинированных желчных камней.
Лечение
[1]Начальное лечение состоит из инфузионной реанимации, коррекции коагулопатии и назначения антибиотиков широкого спектра действия.
- Пациентам с септическим шоком может потребоваться реанимация, и должное внимание следует уделять оксигенации и коррекции дисбаланса жидкости и электролитов.Следует следить за жизненно важными показателями.
- Парентеральные антибиотики следует вводить после посева крови. Выбранные препараты должны быть эффективными против анаэробов и грамотрицательных организмов.
Большинство пациентов с острым холангитом реагируют на терапию антибиотиками, но в конечном итоге для лечения основной обструкции требуется эндоскопический дренаж желчных путей [5] .
- Действующие руководящие принципы рекомендуют лечение в зависимости от степени тяжести. Оценивая клиническую картину, результаты анализа крови и визуализацию в соответствии с критериями, изложенными в рекомендациях 2007 г. (и обновленных в 2013 г.), можно классифицировать степень тяжести состояния следующим образом:
- Стадия I — легкая
- Стадия II — умеренная
- Стадия III — тяжелая
- Токийские руководящие принципы 2013 г., кроме того, признали, что определение степени тяжести по критериям может создать некоторые трудности в реальности.Они посоветовали выполнить экстренный дренаж желчных путей в любое время, когда состояние становится тяжелым, на что указывает развитие:
- Шок (снижение артериального давления).
- Нарушение сознания.
- Острая травма легких.
- Острое повреждение почек.
- Повреждение печени.
- Диссеминированная внутрисосудистая коагуляция (ДВС).
- Лечение сепсиса следует начинать в соответствии с действующими руководящими принципами.

- Ведение в зависимости от степени тяжести:
- Этап 1 — антимикробная терапия, чрескожное, эндоскопическое или оперативное вмешательство для пациентов, не ответивших на лечение, в зависимости от этиологии.
- 2 этап — раннее чрескожное или эндоскопическое дренирование с помощью Т-образной трубки. При остром холангите рекомендуется эндоскопический дренаж желчевыводящих путей. После стабилизации состояния пациента потребуется более радикальное хирургическое вмешательство в зависимости от этиологии.
- Этап 3 — лечение органной недостаточности (дыхательной / кровеносной) с помощью искусственной вентиляции легких, вазопрессоров и т. Д. Неотложное чрескожное или эндоскопическое дренирование или, в тяжелых случаях, декомпрессия желчного протока с помощью Т-образной трубки. После улучшения клинической картины потребуется окончательное лечение.
Осложнения
- У пациентов с тяжелым сепсисом могут развиться абсцессы печени и печеночная недостаточность, бактериемия и грамотрицательный сепсис.
- Тяжелый острый холангит может вызвать септический шок, острое повреждение почек и сердечно-сосудистую, неврологическую, респираторную, почечную, печеночную и / или гематологическую дисфункцию.
- У пациентов, получавших чрескожное или эндоскопическое дренирование, может развиться внутрибрюшное или чрескожное кровотечение, сепсис, свищи и утечка желчи.
Прогноз
[7]Сообщается, что уровень смертности составляет от 17% до 40%, в зависимости от сопутствующих медицинских проблем и возраста. Раннее эндоскопическое дренирование после стабилизации состояния пациента значительно улучшает прогноз. Отсутствие ответа на консервативную терапию и лежащая в основе злокачественная этиология являются неблагоприятными факторами.
Первичный склерозирующий холангит (ПСХ) | Сидарс-Синай
Не то, что вы ищете?Что такое первичный склерозирующий холангит?
Первичный склерозирующий холангит (ПСХ) — редкое заболевание, поражающее желчные протоки. В
слово склерозирование означает рубцевание. При ПСХ ваши желчные протоки покрываются рубцами. Они медленно
сужайтесь, пока желчь не вернется в печень и не начнет ее повреждать.
В
слово склерозирование означает рубцевание. При ПСХ ваши желчные протоки покрываются рубцами. Они медленно
сужайтесь, пока желчь не вернется в печень и не начнет ее повреждать.
желчь — важный пищеварительный сок, необходимый для расщепления жиров. Это тоже необходимо к усваивают жирорастворимые витамины A, D, E и K. Желчь, которая вырабатывается в вашей печени, проходит по протокам от печени к желчному пузырю и тонкому кишечнику.PSC повреждает желчные протоки как внутри, так и снаружи печени.
Что вызывает PSC?
Никто не знает точной причины PSC. Это может начаться в любом возрасте. Поставщики медицинских услуг часто диагностируют его в возрасте от 30 до 40 лет. ПСХ чаще встречается у мужчин.
Некоторые из возможных причин включают:
- Гены. Наличие члена семьи с PSC увеличивает ваш риск.
- Микробы. Бактерии и вирусы могут играть роль в запуске ПСХ.
- Воспалительное заболевание кишечника. Многие люди с ПСХ также страдают язвенной болезнью. колит, воспалительное заболевание кишечника.
- Проблемы иммунной системы. Ваша иммунная система — это система защиты вашего тела. Аномальная иммунная система может играть роль в PSC.
Каковы симптомы ПСХ?
Симптомы ПСХ развиваются медленно. У вас может быть ПСХ в течение многих лет без каких-либо симптомов.
Как только симптомы развиваются, они могут появляться и исчезать.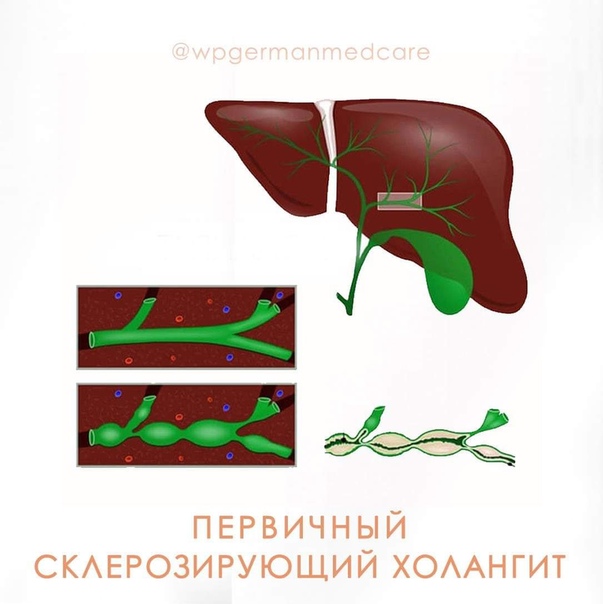 Но со временем они часто ухудшаются. Желчь
который возвращается в вашу печень, может со временем вызвать тип рубцевания печени, известный как
цирроз.Это приводит к печеночной недостаточности. Симптомы ПСХ включают:
Но со временем они часто ухудшаются. Желчь
который возвращается в вашу печень, может со временем вызвать тип рубцевания печени, известный как
цирроз.Это приводит к печеночной недостаточности. Симптомы ПСХ включают:
- Зудящая кожа
- Экстрим усталость (утомляемость)
- Живот боль
- Пожелтение кожи и глаз, называемое желтухой
- Озноб и жар из-за инфекции желчных протоков
Как диагностируется ПСХ?
Ваш поставщик медицинских услуг может подумать, что у вас ПСХ, если обычный анализ крови показывает отклонения от нормы. печень ферменты.Эти ферменты увеличиваются при повреждении печени. Визуализирующее исследование желчь протоки, скорее всего, подтвердят диагноз. Тесты могут включать:
- Эндоскопический ретроградная холангиопанкреатография (ЭРХПГ). В этой процедуре ваш провайдер вводит краситель в желчные протоки с помощью эндоскопа. Это длинная тонкая трубка с а крошечная камера и свет на одном конце.Прицел вводится через рот и опускается в тонкую кишку. Ваш врач сделает рентгеновские снимки после того, как краситель будет нанесен. введен. Он или она может открыть заблокированные желчные протоки во время этой процедуры.
- чрескожный
чреспеченочная холангиография. В этом исследовании ваш лечащий врач вводит
покрасьте желчные протоки с помощью длинной иглы, вставленной в кожу.
 Ваш
провайдер делает рентген после инъекции красителя.
Ваш
провайдер делает рентген после инъекции красителя. - Магнитный резонансная холангиопанкреатография (MRCP). В этом исследовании используется компьютер и радиоволны, чтобы сделать изображения ваших желчных протоков. Если ваш лечащий врач использует краситель, он или она вводит его в ваш кровеносный сосуд. Это основной тест, используемый для диагностики PSC.
- Внешний или внутреннее УЗИ (эндоскопическое УЗИ, ЭУЗИ). В этих исследованиях используется ультразвуковые волны для получения изображений желчных протоков и дренажной системы, а также желчный пузырь и печень.
- Печень биопсия. В ходе этого теста берется образец ткани печени. Затем проверяется под микроскопом. Иногда необходимо провести оценку других подобных заболеваний.
- Анализы крови. Они могут помочь диагностировать заболевание желчных протоков. Они также могут оценить уровень витамина дефицит.
Как лечится ПСХ?
Не существует известного лечения для остановки или замедления ПСХ. Ваш лечащий врач может
лечите симптомы лекарствами, чтобы уменьшить зуд и вылечить инфекцию. Он или она может
также
иногда открывайте протоки в печени, если они заблокированы.Вам может понадобиться взять
витаминные добавки. ПСХ прогрессирует медленно. Но примерно через 10-15 лет
Это
может привести к печеночной недостаточности.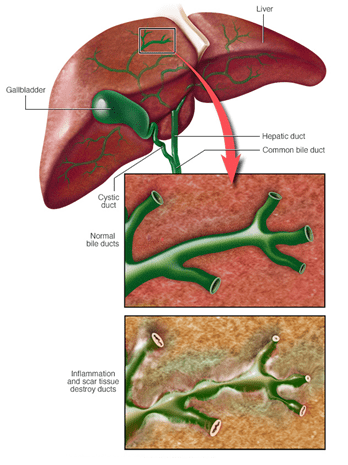 Многие люди с печеночной недостаточностью хорошо реагируют на печень.
трансплантационная хирургия.
Многие люди с печеночной недостаточностью хорошо реагируют на печень.
трансплантационная хирургия.
Хрупкие кости (остеопороз) также очень часто встречаются при ПСХ. Вам понадобится наблюдали за плотностью костей. Также нужно будет следить за уровнем витаминов. Если у тебя есть воспалительное заболевание кишечника (ВЗК), вам следует ежегодно проходить колоноскопию.Даже если ты у вас нет ВЗК, при постановке диагноза ПСХ следует провести колоноскопию, чтобы оценить колит. Люди с ПСХ также подвержены риску рака желчных протоков. печень, желчный пузырь и толстая кишка. Ваш лечащий врач может обсудить скрининговые тесты. с участием ты.
Жизнь с PSC
Узнайте как можно больше о своем заболевании и работайте со своим лечащим врачом, чтобы управлять состоянием.Не употребляйте алкоголь. Придерживайтесь здоровой диеты. Сообщите своему врачу поставщика медицинских услуг о любых лекарствах, которые вы принимаете. Это включает в себя внебиржевые и рецептурные лекарства, витамины, травы и пищевые добавки.
Ключевые моменты о первичной склерозирующий холангит
- Первичный склерозирующий холангит — редкое заболевание, поражающее желчные протоки.
- Симптомы развиваются медленно. Они могут включать зуд кожи, усталость, боль в животе, желтый кожа или озноб и жар, если есть инфекция.
- Хрупкие кости (остеопороз) также очень часто встречаются при ПСХ. Ты потребуется следить за плотностью костей.
- Есть
нет известного лекарства.
 Но лекарства могут облегчить симптомы.
Но лекарства могут облегчить симптомы. - Если Возникает печеночная недостаточность, вы можете быть кандидатом на пересадку печени.
Следующие шаги
подсказок чтобы помочь вам получить максимальную пользу от визита к врачу:
- Знайте причину вашего визита и то, что вы хотите случаться.
- Перед визитом запишите желаемые вопросы ответил.
- Возьмите с собой кого-нибудь, кто поможет вам задать вопросы и запомнить что вам говорит ваш провайдер.
- При посещении запишите название нового диагноза и любые новые лекарства, методы лечения или тесты. Также запишите все новые инструкции в свой провайдер дает вам.
- Знайте, почему прописано новое лекарство или лечение и как это поможет вам. Также знайте, каковы побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему рекомендуется тест или процедура и какие результаты могут означать.
- Знайте, чего ожидать, если вы не примете лекарство или тест или процедура.
- Если у вас назначена повторная встреча, запишите дату, время и цель этого визита.
Первичный склерозирующий холангит | Заболевание печени | Система здравоохранения Генри Форда
В Центре болезней печени Генри Форда мы имеем обширный опыт лечения редких состояний, таких как первичный склерозирующий холангит и связанные с ним осложнения.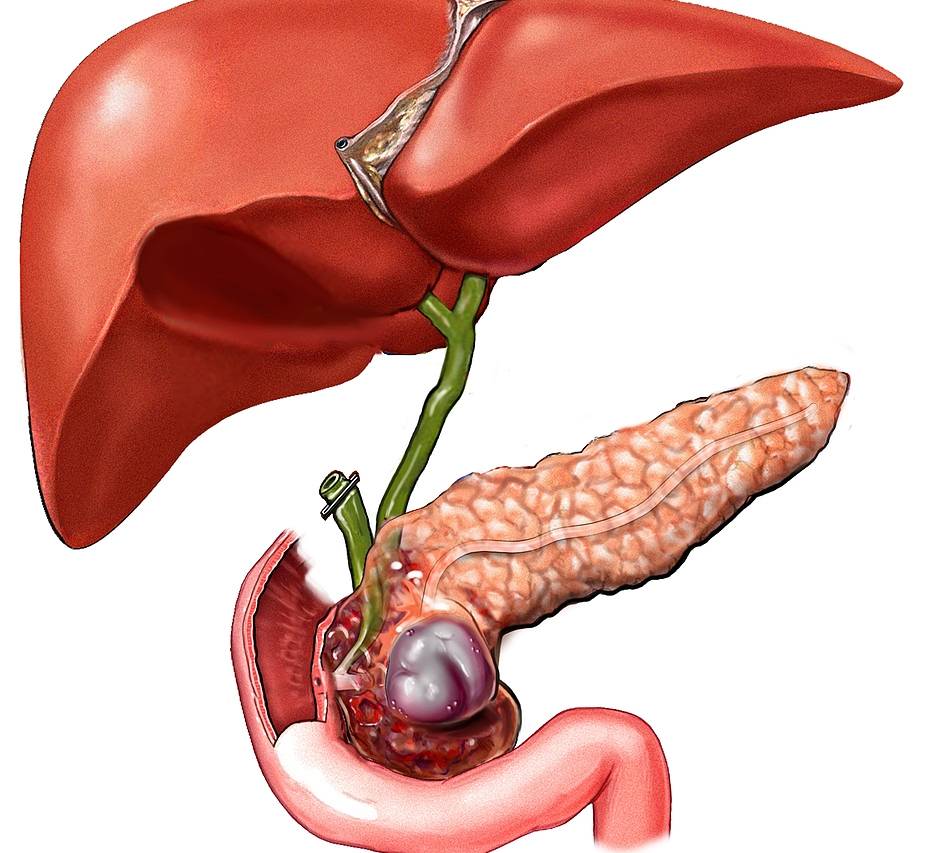 Наша многопрофильная команда специализируется на предоставлении всестороннего ухода и поддержки, в которых вы нуждаетесь во время лечения и за его пределами.
Наша многопрофильная команда специализируется на предоставлении всестороннего ухода и поддержки, в которых вы нуждаетесь во время лечения и за его пределами.
Что такое первичный склерозирующий холангит (ПСХ)?
Первичный склерозирующий холангит (ПСХ) — это заболевание, вызванное воспалением и рубцеванием желчных протоков — трубок, по которым пищеварительная жидкость из печени в тонкий кишечник. По мере образования рубцов желчные протоки сужаются и затвердевают. ПСХ прогрессирует медленно, часто с годами, и может привести к печеночной недостаточности и, в некоторых случаях, к раку желчных протоков.
Причины и факторы риска первичного склерозирующего холангита (ПСХ)
Исследователи еще не знают, что вызывает первичный склерозирующий холангит (ПСХ). Однако факторы риска ПСХ включают:
- Воспалительное заболевание кишечника в анамнезе : включает язвенный колит или болезнь Крона
- Возраст : ПСХ обычно появляется у молодых людей, но может развиться в любом возрасте
- Пол : ПСХ чаще встречается у мужчин, чем у женщин
Симптомы первичного склерозирующего холангита
Симптомы прогрессирующего первичного склерозирующего холангита (ПСХ) могут включать:
- Необъяснимая усталость
- Зуд
- Боль в животе
- Лихорадка
- Озноб
- Ночная одежда
- Увеличенная печень
- Похудание
- Желтуха (пожелтение кожи и глаз)
Как диагностируется первичный склерозирующий холангит (ПСХ)?
Первичный склерозирующий холангит можно диагностировать до появления симптомов с помощью анализов крови и визуализации.В компании Henry Ford мы предлагаем комплексные расширенные диагностические тесты. Мы прилагаем все усилия, чтобы выбрать для вас наименее инвазивные и наиболее эффективные варианты. Наши диагностические тесты PSC включают:
- Функциональные пробы печени : Анализы крови, которые проверяют, насколько хорошо ваша печень функционирует
- MRCP (магнитно-резонансная холангиопанкреатография) : диагностический инструмент, который создает подробные изображения печени и желчных протоков с помощью магнитного поля и радиоволн
- ЭРХПГ (эндоскопическая ретроградная холангиопанкреатография) : минимально инвазивная процедура, при которой ваш врач вводит эндоскоп (тонкую трубку с подсветкой) вам в горло и использует контрастный краситель и рентгеновское изображение для просмотра желчных протоков.
 Узнайте больше об эндоскопии в Центре болезней печени Генри Форда.
Узнайте больше об эндоскопии в Центре болезней печени Генри Форда. - Биопсия печени : Процедура забора образца ткани печени для анализа
Узнайте больше о передовых методах диагностики и диагностики в больнице Генри Форда.
Лечение первичного склерозирующего холангита (ПСХ) в больнице Генри Форда
Мы предлагаем полный спектр лечения первичного склерозирующего холангита и связанных с ним состояний, включая язвенный колит, заболевания щитовидной железы и костей.Как крупный справочный центр для пациентов с ПСХ, мы обладаем опытом, необходимым для оказания комплексной индивидуальной помощи даже в самых сложных ситуациях. Наши процедуры включают:
- Лекарства для уменьшения симптомов
- Антибиотики для лечения инфекций, вызванных закупоркой желчных протоков
- Эндоскопия : Мы предлагаем современные, минимально инвазивные эндоскопические процедуры, такие как ERCP. В этом году наши опытные гастроэнтерологи поставили перед собой цель выполнить большинство ERCP в регионе.Они готовы к вызову 24 часа в сутки и 365 дней в году, чтобы помочь в экстренных случаях.
- Трансплантация печени : Являясь одной из ведущих программ трансплантации печени в стране, наши пациенты могут рассчитывать на более короткие сроки ожидания донорской печени и самые высокие показатели выживаемости пациентов в течение одного и трех лет в Мичигане. В нашу команду трансплантологов входят опытные гастроэнтерологи, специализирующиеся на осложнениях желчных протоков до и после трансплантации с использованием ERCP.
- Исследования и клинические испытания : Мы предлагаем многообещающие варианты лечения, которых нет больше нигде.
Узнайте больше о наших методах лечения заболеваний печени в компании Henry Ford.
.





 Gastroenterol. 2008; 14 (24): 3781–3791.
Gastroenterol. 2008; 14 (24): 3781–3791. J. Physiol. Gastrointest. Liver Physiol. 2004; 286 (1): G118–125.
J. Physiol. Gastrointest. Liver Physiol. 2004; 286 (1): G118–125.
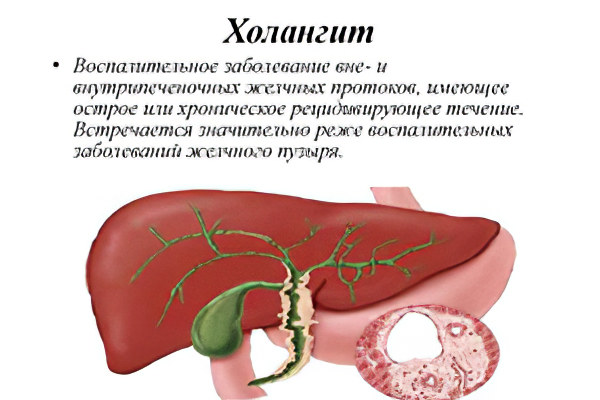
 Перитонизм — необычный признак и должен стимулировать поиск альтернативного диагноза.
Перитонизм — необычный признак и должен стимулировать поиск альтернативного диагноза.
 Ваш
провайдер делает рентген после инъекции красителя.
Ваш
провайдер делает рентген после инъекции красителя.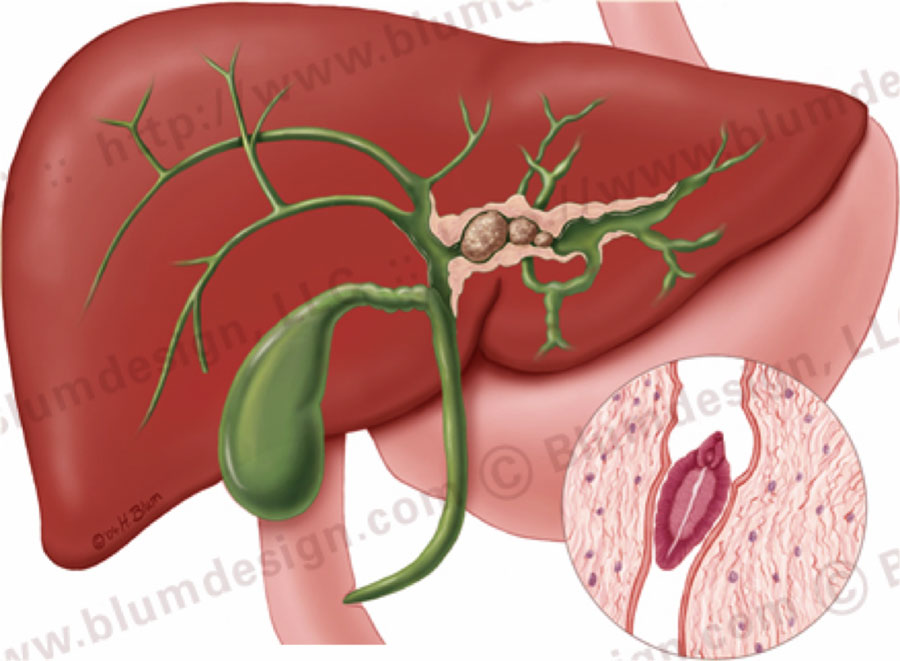 Но лекарства могут облегчить симптомы.
Но лекарства могут облегчить симптомы. Узнайте больше об эндоскопии в Центре болезней печени Генри Форда.
Узнайте больше об эндоскопии в Центре болезней печени Генри Форда.