Безоперационные методы лечения геморроя
Геморрой — одно из самых «популярных» заболеваний человечества. Вспомним строчки А. С. Пушкина из «Евгения Онегина»: «Больных теснится бледный рой: кто жертва чести боевой, кто почечуя, кто Киприды…». Практически каждый человек хоть раз в жизни сталкивается с этой болезнью, и возникает проблема: как лечить, чем лечить и как быстрее стать здоровым и активным человеком, полным жизненных сил. Тем более что современный ритм жизни не позволяет надолго «выходить из строя». Таблетки помогают на короткое время, операция — процесс малоприятный, и его откладывают до последнего, стараясь избежать длительного и неприятного восстановительного послеоперационного периода.
Действительно, раньше единственным действенным методом лечения геморроя было хирургическое вмешательство. Теперь с появлением радикальных безоперационных методик ситуация в корне изменилась. Это как раз те методики, которые используются чаще и лучше всего, если конечно болезнь не находится в стадии, когда возможна лишь операция.
- Высокая эффективность, сопоставимая с результатами хирургического удаления геморроидальных узлов
- Минимальный риск осложнений
- Лечение проводится амбулаторно. Привычный ритм жизни пациента не меняется. После манипуляции не требуется больничный лист и сохраняется трудоспособность.
- Процедуры более комфортны, чем операция, нет тяжелого и длительного восстановительного периода
- Пациент быстро и безболезненно избавляется от геморроя и возвращается к нормальной жизни в максимально короткие сроки с хорошими ближайшими и отдаленными результатами.
На сегодняшний момент существует несколько наиболее распространенных и эффективных безоперационных методик лечения геморроя – инфракрасная фотокоагуляция, склеротерапия и перевязка (легирование) геморроидальных узлов латексными кольцами. Остановимся на каждом из них.
Инфракрасная фотокоагуляция
Стала применяться с 1989 года. При помощи аппарата — фотокоагулятора через световод происходит тепловое прижигание сосудов геморроидального узла. Следствием этого является уменьшение кровотока, сокращение узла в размерах и его фиксация к стенке кишки. Генерируемое аппаратом излучение абсолютно безопасно, по спектру и интенсивности соответствует обычной лампе накаливания. Во время процедуры пациент испытывает ощущение тепла в области манипуляции. Показанием являются лишь небольшие кровоточащие геморроидальные узлы на ранних стадиях геморроя. Склеротерапия. Применяется с начала прошлого века. Суть процедуры заключается во введении в просвет геморроидального узла с помощью шприца специального препарата – склерозанта, который вызывает замещение сосудистых полостей соединительной тканью – как бы «пломбирует» геморроидальный узел, прекращая по нему кровоток. Тем самым, исчезают кровотечения, выпадавшие до этого узлы уменьшаются и подтягиваются в анальный канал. Процедура полностью безболезненна.
При помощи аппарата — фотокоагулятора через световод происходит тепловое прижигание сосудов геморроидального узла. Следствием этого является уменьшение кровотока, сокращение узла в размерах и его фиксация к стенке кишки. Генерируемое аппаратом излучение абсолютно безопасно, по спектру и интенсивности соответствует обычной лампе накаливания. Во время процедуры пациент испытывает ощущение тепла в области манипуляции. Показанием являются лишь небольшие кровоточащие геморроидальные узлы на ранних стадиях геморроя. Склеротерапия. Применяется с начала прошлого века. Суть процедуры заключается во введении в просвет геморроидального узла с помощью шприца специального препарата – склерозанта, который вызывает замещение сосудистых полостей соединительной тканью – как бы «пломбирует» геморроидальный узел, прекращая по нему кровоток. Тем самым, исчезают кровотечения, выпадавшие до этого узлы уменьшаются и подтягиваются в анальный канал. Процедура полностью безболезненна.
Лигирование геморроидальных узлов
Используется с 1963 года.---buasir.jpg) На основание геморроидального узла с помощью специального устройства накладывается эластичное резиновое кольцо, нарушающее его кровоснабжение. В результате геморроидальный узел через 7-10 суток самостоятельно отторгается. Метод несколько более болезнен, чем предыдущие. Показанием для этого метода являются крупные выпадающие внутренние геморроидальные узлы в поздних стадиях геморроя.
На основание геморроидального узла с помощью специального устройства накладывается эластичное резиновое кольцо, нарушающее его кровоснабжение. В результате геморроидальный узел через 7-10 суток самостоятельно отторгается. Метод несколько более болезнен, чем предыдущие. Показанием для этого метода являются крупные выпадающие внутренние геморроидальные узлы в поздних стадиях геморроя.
Другие методы (криотерапия, перевязка питающих артерий под контролем ультразвука, электрокоагуляция) используются мало в силу своей низкой эффективности, неизученности отдаленных результатов, либо чреваты осложнениями.
Хирургическое лечение
В запущенных случаях – когда узлы все чаще выпадают и практически не вправляются – пациент попадает уже на операционный стол. Хирургическое удаление геморроидальных узлов избавляет от геморроя навсегда. Правда, приходить в себя после операции нужно достаточно долго – около 1,5-2 месяцев. И это достаточно болезненно.
Принципиально новый подход операции при геморрое был разработан итальянцем Антонио Лонго в 1993 году и получил его имя. Во время операции сами геморроидальные узлы не иссекаются, удаляется только небольшой участок слизистой прямой кишки выше них. В результате геморроидальные узлы как бы подтягиваются кверху в прямую кишку, меньше выпадают и резко уменьшаются в объеме за счет уменьшения притока крови, что приводит к их запустеванию и зарастанию соединительной тканью. На сегодня это лучший и оптимальный способ хирургического лечения геморроя. Обычно операция по методу Лонго длится 15-25 минут, в то время как классическое удаление геморроидальных узлов не менее 40 минут. Через 3-4 дня после операции можно уже отправляться на работу, а через неделю заниматься спортом. Среди недостатков метода можно отметить недостаточную изученность отдаленных результатов. Кроме того, пусть непродолжительная, но госпитализация в стационар все же необходима.
Итак, подведем итоги. Нужно помнить: отсутствие ярко выраженных болевых ощущений еще не означает, что болезни нет. Поэтому необходимо обязательно проходить периодические профилактические осмотры. Если проблема все же существует, то необходимо точно поставить диагноз, естественно не самостоятельно. И, главное – чем раньше начато лечение, тем менее болезненно и обременительно оно будет. Ведь любую болезнь проще и лучше предотвратить или «захватить» на ранней стадии, чем доводить себя до критического состояния, когда от болезни может избавить только малоприятная операция.
Нужно помнить: отсутствие ярко выраженных болевых ощущений еще не означает, что болезни нет. Поэтому необходимо обязательно проходить периодические профилактические осмотры. Если проблема все же существует, то необходимо точно поставить диагноз, естественно не самостоятельно. И, главное – чем раньше начато лечение, тем менее болезненно и обременительно оно будет. Ведь любую болезнь проще и лучше предотвратить или «захватить» на ранней стадии, чем доводить себя до критического состояния, когда от болезни может избавить только малоприятная операция.
Какой путь выбрать, и какому методу лечения геморроя в итоге отдать предпочтение — операции или малотравматичному лечению – решать больному.
Михаил Дмитриевич Крылов —
врач-колопроктолог Скандинавского медицинского центра,
кандидат медицинских наук, член Ассоциации колопроктологов России
Острый тромбоз наружных геморроидальных узлов
Что такое острый тромбоз наружного геморроидального узла (перианальный венозный тромбоз, острый наружный геморрой)?
Острый тромбоз — это внезапно возникающее заболевание, обусловленное возникновением тромбов в венозных сплетениях наружных геморроидальных узлов, которые располагаются у выхода из анального канала (рис.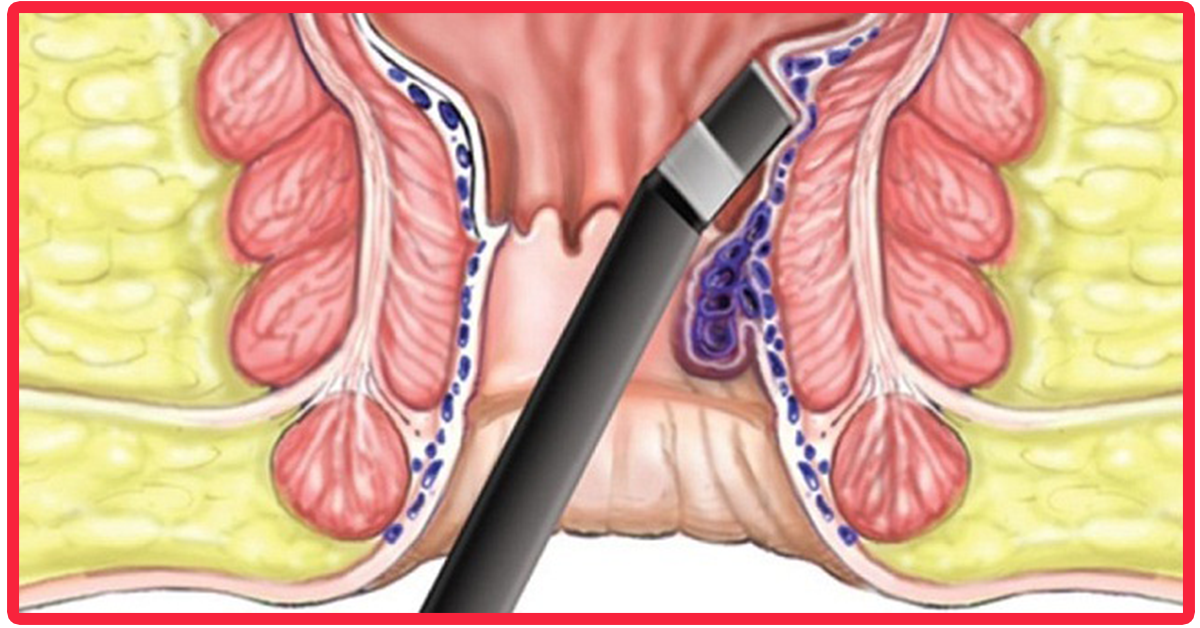
Рис.1. Неосложненный тромбоз наружного узла
Рис. 2. Острый тромбоз наружного геморроидального узла с некрозом участка кожи над ним.
Что такое наружные геморроидальные узлы? Немного анатомии
Наружные геморроидальные узлы (сплетения) – это образования, расположенные под кожей на границе анального канала и перианальной (вокруг анального отверстия) кожи. Они представляют собой венозные сплетения (рис.3). Обычно они никак себя не проявляются, не видны и не определяются на ощупь. По мере хронического прогрессирования ухудшения состояния
Они представляют собой венозные сплетения (рис.3). Обычно они никак себя не проявляются, не видны и не определяются на ощупь. По мере хронического прогрессирования ухудшения состояния
внутренних геморроидальных узлов в наружных происходят изменения, ведущие к их увеличению и потери связи с мышечным кольцом анального канала. Однако наиболее значительные изменения в наружных узлах наступают при возникновении в них тромба.
Рис. 3. Схема анального канала, на выходе из которого располагаются наружные геморроидальные узлы (номер 7 на схеме).
Как проявляется острый тромбоз наружного геморроидального узла?
Пациенты с острым тромбозом наружного геморроидального узла жалуются на появление
выпячивания, «шишки» (новообразования) и/или боль различной интенсивности в области заднего прохода. Размер «шишки» может быть от нескольких милиметров до нескольких сантиметров и зачастую сопровождаться отеком окружающих тканей (вплоть до всей окружности анального канала).
Для оценки степени боли используют специальную визуально-аналоговую шкалу, в которой можно самостоятельно определить выраженность боли. Ведь именно это является ключевым моментом при выборе метода лечения. Хирургическое лечение будет наиболее эффективным при выраженности боли 7 и более баллов, тогда как при боли до 4 баллов – оптимальным можно считать консервативный метод лечения.
Рис. Визуально-аналоговая шкала для оценки боли.
Болевые ощущения обычно усиливаются во время дефекации (опорожнения кишечника) и/или при сидении. Боль и отек могут быть очень выраженными, даже невыносимыми в течение нескольких дней. Интенсивность боли зависит от размеров тромба и его расположения по отношению к мышцам анального сфинктера. В целом, проявления заболевания могут сохраняться несколько недель, в исключительных случаях и дольше. Иногда происходит самостоятельная эвакуация тромба из геморроидального узла. Этому предшествует некроз (разрушение) кожи над тромбом, и тромб как бы «выпадает» из узла. Внешне это сопровождается ощущением «лопнушего» шарика, выделением небольшого количества крови. Обычно, после эвакуации тромба резко уменьшаются болевые ощущения и чувство дискомфорта в области заднего прохода постепенно уменьшаются. Однако, не всегда некроз слизистой над тромбом заканчивается лишь эвакуацией тромба, некроз может продолжить распространение на сам геморроидальный узел и окружающие ткани, вот почему это состояние требует консультации специалиста. После стихания острого тромбоза у пациента чаще всего остаются так называемые «кожный бахромки» — избыток кожи там, где был тромбоз. Они не требуют медицинского лечения, но могут доставлять косметический дисфкомфорт.
Иногда происходит самостоятельная эвакуация тромба из геморроидального узла. Этому предшествует некроз (разрушение) кожи над тромбом, и тромб как бы «выпадает» из узла. Внешне это сопровождается ощущением «лопнушего» шарика, выделением небольшого количества крови. Обычно, после эвакуации тромба резко уменьшаются болевые ощущения и чувство дискомфорта в области заднего прохода постепенно уменьшаются. Однако, не всегда некроз слизистой над тромбом заканчивается лишь эвакуацией тромба, некроз может продолжить распространение на сам геморроидальный узел и окружающие ткани, вот почему это состояние требует консультации специалиста. После стихания острого тромбоза у пациента чаще всего остаются так называемые «кожный бахромки» — избыток кожи там, где был тромбоз. Они не требуют медицинского лечения, но могут доставлять косметический дисфкомфорт.
Из-за чего возникает острый тромбоз наружного геморроидального узла?
В основе возникновения тромбоза чаще лежит переполнение вен наружных геморроидальных сплетений кровью с последующим замедлением тока крови в этих сосудах и возникновением тромбов. Тромбоз на фоне венозного полнокровия чаще всего развивается после резкого или длительного напряжения. Классическими примерами такого перенапряжения являются поднятие тяжестей, натуживание при запорах или поносах, а также родах. Хронический застой крови в органах таза (к которым относится и анальный канал) возникает при длительном сидении, избыточной массе тела, недостаточной физической активности.
Тромбоз на фоне венозного полнокровия чаще всего развивается после резкого или длительного напряжения. Классическими примерами такого перенапряжения являются поднятие тяжестей, натуживание при запорах или поносах, а также родах. Хронический застой крови в органах таза (к которым относится и анальный канал) возникает при длительном сидении, избыточной массе тела, недостаточной физической активности.
Как отличить острый тромбоз наружного геморроидального узла от других заболеваний?
Обычно для диагностики острого тромбоза достаточно осмотреть пациента и узнать, как развивалось заболевание и какие жалобы беспокоят. При осмотре можно увидеть увеличенный в размерах (иногда до нескольких сантиметров) чаще темно-красного цвета узел расположенный к наружи от ануса, возможно с очагом некроза в центре. При пальпации (ощупывании) в первые несколько дней можно четко определить тромб в узле, при осмотре в более поздние сроки тромб уже не так просто определить, он начинается постепенно «растворяться» и частично замещаться рубцовой тканью.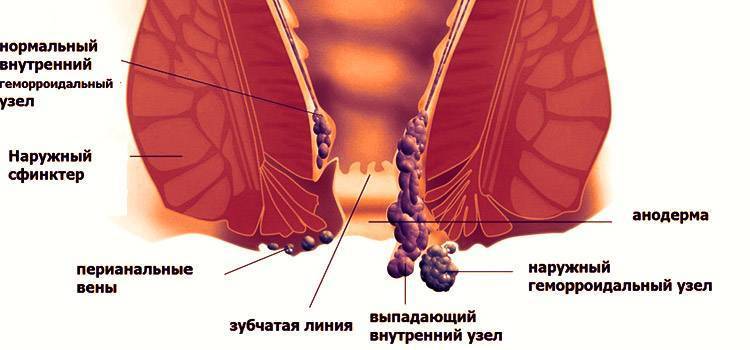 Тромбоз наружного геморроидального узла нужно отличать от
Тромбоз наружного геморроидального узла нужно отличать от
ущемления выпавшего внутреннего геморроидального узла. В этой ситуации происходит выпадение внутреннего геморроидального узла, в норме расположенного внутри анального канала, сдавление его ножки, в которой проходят питающие его сосуды и нарушение кровоснабжения (ишемия) с отмираем ткани узла (рис. 4 и 5). Для специалиста отличить эти состояния не составляет особого труда, самостоятельно же пациенту понять какой именно узел доставляет ему дискомфорт достаточно сложно. Важно отличать эти заболевания, так как лечение их значительно различается. При ущемлении внутреннего геморроидального узла, как правило, требуется срочное оперативное лечение.
Рис. 4. Ущемленный выпавший внутренний геморроидальный узел с явлениями некроза ткани узла.
Рис.5. Схематичное изображение ущемления внутреннего выпавшего геморроидального узла.
Острая (обострение хронической) анальная трещина – сопровождается таким же как при тромбозе болевым синдромом, но значительно более выраженным в момент опорожнения кишечника. При этом заболевании возникает разрыв слизистой анального канала. Появление острой трещины часто сопряжено с рефлекторным «защитным» спазмом сфинктерного аппарата, который затрудняет заживление раны. Консервативное и оперативное лечение заболеваний различно.
При этом заболевании возникает разрыв слизистой анального канала. Появление острой трещины часто сопряжено с рефлекторным «защитным» спазмом сфинктерного аппарата, который затрудняет заживление раны. Консервативное и оперативное лечение заболеваний различно.
Острый парапроктит – сходство с острым тромбозом заключается в появлении объемного образования в области заднего прохода, выраженным болевым синдромом. Парапроктит – это инфекционно-воспалительное заболевание с формированием абсцесса (гнойника) в параректальной области. Заболевание сопровождается повышением температуры тела, общими симптомами интоксикации. Объемное образование в области анального канала гораздо больше и болезненнее, чем при тромбозе. Часто имеется выделение гноя на кожу или в просвет прямой кишки. Для точной диагностики применяется УЗ-исследование. Заболевание крайне опасно развитием хронических гнойных свищей перианальной области при отсутствии адекватного и своевременного лечения.
Всегда ли нужно лечить острый тромбоз наружного геморроидального узла?
Выбор метода лечения этого заболевания один из самых спорных вопросов общей проктологии./102891261-56a5043a5f9b58b7d0da90be.jpg) Как и геморрой – острый тромбоз не превращается в рак, не вызывает смертельно опасных осложнений, но может значительно влиять на качество жизни пациента, зачастую болевой синдром описывается как «невыносимый», с которым жить «просто невозможно».
Как и геморрой – острый тромбоз не превращается в рак, не вызывает смертельно опасных осложнений, но может значительно влиять на качество жизни пациента, зачастую болевой синдром описывается как «невыносимый», с которым жить «просто невозможно».
В нашей Клинике принят пациент-ориентированный подход к выбору метода лечения острого тромбоза наружных геморроидальных узлов: врач вместе с пациентом определяют, насколько выражены симптомы, как сильно страдает качество жизни пациента с учетов его трудовой занятости и выбирают метод лечения.
Острый тромбоз наружного геморроидального узла можно лечить оперативно (выполнять операцию), консервативно (принимать таблетки и использовать местно мази и/или свечи) или вовсе не лечить, а выбрать выжидательную тактику. Исследования и практический опыт показывают, что оперативное лечение позволяет в более короткие сроки избавиться от проявлений заболевания, консервативное лечение также позволяется избавиться от проявлений заболевания, но за гораздо более длительное время. Отсутствие какого либо лечения, также заканчивается выздоровлением, сроки которого лишь незначительно отличаются от сроков при интенсивном консервативном лечении. Определяющим в выборе метода лечения является выбор пациента и его оценка выраженности болевого синдрома, поэтому, мнение пациента имеет решающее значение для выбора тактики. Если пациент оценивает боль как невыносимую, или же ему надо срочно вернуться к работе, улететь в другой город или страну – разумнее выбрать оперативное лечение в объеме удаления геморроидального узла или же эвакуации тромба из узла. Хирургическое лечение, обычно, приводит к более быстрому облегчению неприятных симптомов. Если болевой синдром позволяет пациенту полноценно жить в этом состоянии или пациент неготов к хирургическому вмешательству – возможно проведение консервативного лечения, направленного на уменьшение болевого синдрома и ускорение процесса организации и рассасывания тромба.
Отсутствие какого либо лечения, также заканчивается выздоровлением, сроки которого лишь незначительно отличаются от сроков при интенсивном консервативном лечении. Определяющим в выборе метода лечения является выбор пациента и его оценка выраженности болевого синдрома, поэтому, мнение пациента имеет решающее значение для выбора тактики. Если пациент оценивает боль как невыносимую, или же ему надо срочно вернуться к работе, улететь в другой город или страну – разумнее выбрать оперативное лечение в объеме удаления геморроидального узла или же эвакуации тромба из узла. Хирургическое лечение, обычно, приводит к более быстрому облегчению неприятных симптомов. Если болевой синдром позволяет пациенту полноценно жить в этом состоянии или пациент неготов к хирургическому вмешательству – возможно проведение консервативного лечения, направленного на уменьшение болевого синдрома и ускорение процесса организации и рассасывания тромба.
Как лечить острый тромбоз наружного геморроидального узла?
Возможности оперативного лечения
Существуют две основные операции для лечения острого тромбоза наружного геморроидального узла: удаление всего узла или только тромба из него. Первая операция называется экономная (частичная) геморроидэктомия (удаление только наружного геморроидального узла), вторая – тромбэктомия. Обе операции эффективны с точки зрения ликвидации болевого синдрома в течение 2-3 суток после их выполнения, однако после операции по эвакуации тромба чаще бывает рецидив (повторное возникновение тромба).
Первая операция называется экономная (частичная) геморроидэктомия (удаление только наружного геморроидального узла), вторая – тромбэктомия. Обе операции эффективны с точки зрения ликвидации болевого синдрома в течение 2-3 суток после их выполнения, однако после операции по эвакуации тромба чаще бывает рецидив (повторное возникновение тромба).
Экономная (частичная) геморроидэктомия тромбированного узла представляет собой рассечение кожи вокруг узла, его выделение и удаление вместе с тромбом. Операция может быть выполнена под местной анестезией.
После удаления геморроидального узла образуется небольшая раневая поверхность, которая может вызвать болевые ощущения, особенно во время дефекации. Но обычно боль гораздо менее выражена, чем при наличии тромбированнного узла, и лишь иногда требует приема таблетированных обезболивающих средств.
Тромбэктомия выполняется через разрез кожи над тромбом, после чего тромб удаляется и может быть наложено 1-2 шва на место разреза.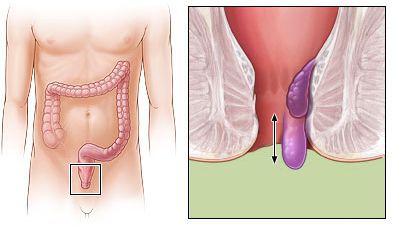 Это вмешательство практически всегда выполняется под местной анестезией.
Это вмешательство практически всегда выполняется под местной анестезией.
Консервативное лечение
Консервативное лечение (таблетки и местные средства – мази и свечи) направленно в основном на купирование болевого синдрома, вызванного тромбом, уменьшение отека и воспаления геморроидального узла, нормализацию частоты и качества стула. В аптеках представлено большое количество средств для лечения геморроидальной болезни, но все они примерно равны по эффективности и могут применяться для лечения острого тромбоза наружного геморроидального узла. Местные средства (мази и свечи) в основном обладают обезболивающим, противоспалительным действием. Топические средства с антикоагулянтным действием в лечении острого тромбоза эффективны только для временной профилактики возникновения новых тромбов или же при наличии в составе препарата обезболивающего компонента – для обезболивания. Таблетки используются также для обезболивания (нестероидные противовоспалительные, парацетамол) и нормализации венозного кровотока в малом тазу (в области прямой кишки), например флавоноиды. Кроме того, консервативное лечение проводится и после операции для устранения возможных послеоперационных симптомов. Схему консервативного лечения может определить только специалист, причем комбинацию препаратов лучше подбирать в каждом конкретном случае в зависимости от особенностей каждого пациента.
Кроме того, консервативное лечение проводится и после операции для устранения возможных послеоперационных симптомов. Схему консервативного лечения может определить только специалист, причем комбинацию препаратов лучше подбирать в каждом конкретном случае в зависимости от особенностей каждого пациента.
Нужно ли готовится к операции?
В большинстве случаев возможно выполнение операции в амбулаторных условиях под местной анестезией, т.е. не требуется госпитализация в стационар для лечения. Однако, части пациентов все же лучше выполнить операцию в операционной, для этого вам потребуются стандартные анализы и обследования необходимые для госпитализации. Особой подготовки кишечника для операции не требуется.
Что будет после операции?
Обычно пациенты чувствуют резкое облегчение после операции и отмечают уменьшение болевого синдрома (рис.6). Иногда требуется продолжение минимальной обезболивающей терапии. Основной задачей пациента в послеоперационном периоде становится нормализация стула: мягкий стул вызывает гораздо меньше болезненных ощущений при опорожнении кишечника, чем плотный. Как правило, к своей обычной жизни пациенты возвращаются на 2-3 сутки после операции, иногда и на следующий же день.
Как правило, к своей обычной жизни пациенты возвращаются на 2-3 сутки после операции, иногда и на следующий же день.
a) б)
Рис. 6. Вид области ануса до (а) и сразу после удаления наружного геморроидального узла (б). До операции уровень боли оценивался пациентом как 8 из 10, сразу после операции 4 из 10.
Существуют ли способы профилактики рецидивов/повторов заболевания?
Профилактика рецидивов заболевания основана на исключении возможных причин возникновения тромбоза. Среди них плотный стул, запоры или поносы, «чтение в туалете», недостаточная или наоборот чрезмерная физическая активность (тяжелая атлетика, фитнес), длительная сидячая работа. К сожалению, однозначных методов профилактики возникновения острого тромбоза наружного геморроидального узла не существует, мы можем лишь уменьшить вероятность его возникновения, но не полностью ее исключить., Тем не менее, нужно отметить, что при консервативном лечении вероятность возникновения повторна заболевания выше, чем после выполнения операции.
Что делать беременным и родильницам/роженицам с острым тромбозом?
По статистике около четверти беременных и почти половина родильниц сталкиваются с различными проявлениями геморроидальной болезни, наиболее мучительным из которых является острый тромбоз. Обычно родильницы и особенно беременные в ответ на свои жалобы доктору слышат предложение потерпеть. Такой подход продиктован тем, что существует множество противопоказаний к применению подавляющего большинства лекарственных средств у беременных, а хирургическое вмешательство расценивается медицинским сообществом, как фактор который может спровоцировать роды или остановить процесс кормления грудью. На практике это означает, что не зависимо от выраженности болевого синдрома, иногда очень значительного, женщины вынуждены оставаться без сколько-нибудь эффективного лечения. Боль из-за тромбоза в свою очередь может ухудшить психологическое состояние беременных или родильниц и привести к не желательным последствиям при родах (преждевременные роды) или в период грудного вскармливания (отказ от кормления грудью). Наша клиника является сторонником персонализированного подхода в лечении острого тромбоза у таких женщин. Если острый тромбоз категорически мешает пациентке жить, его следует активно лечить с использованием всего арсенала средств, применяемых у обычных пациентов, но с учетом противопоказаний для лекарственных препаратов. У беременных во II и III триместрах возможно выполнение операции по удалению тромбированного узла (рис.7), равно как и у родильниц и рожениц (рис.8). При беременности есть некоторые ограничения по препаратам местного и общего обезболивания, которые можно применять. Конкретные лекарственные средства следует выбирать совместно как колопроктологом, так и акушером, чтобы не нанести вред плоду или новорожденному. Специалисты нашей Клиники имеют опыт лечения как беременных так и родильниц с проявлениями острого тромбоза геморроидального узла с очень хорошими результатами, отзывы о которых наши пациента оставляют на нашем сайте в том числе.
Наша клиника является сторонником персонализированного подхода в лечении острого тромбоза у таких женщин. Если острый тромбоз категорически мешает пациентке жить, его следует активно лечить с использованием всего арсенала средств, применяемых у обычных пациентов, но с учетом противопоказаний для лекарственных препаратов. У беременных во II и III триместрах возможно выполнение операции по удалению тромбированного узла (рис.7), равно как и у родильниц и рожениц (рис.8). При беременности есть некоторые ограничения по препаратам местного и общего обезболивания, которые можно применять. Конкретные лекарственные средства следует выбирать совместно как колопроктологом, так и акушером, чтобы не нанести вред плоду или новорожденному. Специалисты нашей Клиники имеют опыт лечения как беременных так и родильниц с проявлениями острого тромбоза геморроидального узла с очень хорошими результатами, отзывы о которых наши пациента оставляют на нашем сайте в том числе.
а) б)
Рис. 7. Острый тромбоз наружного геморроидального узла у беременной 38 недель.
7. Острый тромбоз наружного геморроидального узла у беременной 38 недель.
До операции болевой синдром оценивался на 8 из 10, сразу после операции 3 из 10.
а)внешний вид тромбированного наружного геморроидального узла с некрозом, б) внешний вид после удаления тромбированного узла.
а) б)
Рис. 8. а) острый тромбоз наружного геморроидального узла с выраженным отеком у пациентки на 5 сутки после родов, б) состояние пациентки на 7 сутки после операции. На первые сутки после операции снижение болевого синдрома с 9 до 4 из 10.
О лечении других проявлений геморроидальной болезни у беременных и родильниц вы можете прочесть в разделе Геморрой у беременных.
Что делать, если вы прошли курс консервативного лечения тромбоза
Обилие средств для консервативного лечения тромбоза и зачастую настроенность врача на использование этой методики приводит к тому, что большая часть тромбозов лечатся консервативно. В нашу Клинику обращаются пациенты на разных этапах проведения курса консервативной терапии. Часто это ситуация, когда сразу после возникновения тромба была начата консервативная терапия, произошло некоторое облегчение состояния, уменьшился болевой синдром, но остается «шишка» в области заднего прохода, некоторые болевые ощущения. Иногда приходят вполне здоровые люди, которые пережили эпизод острого тромбоза несколько месяцев или лет назад и сейчас их беспокоит наличие кожных «бахромок», избытка кожи в области заднего прохода, которые остаются после разрешения острого состояния. Они могут препятствовать качественно осуществлять гигиену этой области, влиять на интимную жизнь. Что делать в этой ситуации? И снова главным для врачей нашей Клиники будет мнение пациента. Если вы хотите избавиться от проявления острого тромбоза, даже если уже проведено консервативное лечение, прошло много времени – это можно сделать оперативным путем.
В нашу Клинику обращаются пациенты на разных этапах проведения курса консервативной терапии. Часто это ситуация, когда сразу после возникновения тромба была начата консервативная терапия, произошло некоторое облегчение состояния, уменьшился болевой синдром, но остается «шишка» в области заднего прохода, некоторые болевые ощущения. Иногда приходят вполне здоровые люди, которые пережили эпизод острого тромбоза несколько месяцев или лет назад и сейчас их беспокоит наличие кожных «бахромок», избытка кожи в области заднего прохода, которые остаются после разрешения острого состояния. Они могут препятствовать качественно осуществлять гигиену этой области, влиять на интимную жизнь. Что делать в этой ситуации? И снова главным для врачей нашей Клиники будет мнение пациента. Если вы хотите избавиться от проявления острого тромбоза, даже если уже проведено консервативное лечение, прошло много времени – это можно сделать оперативным путем.
Можно ли провести профилактику тромбоза?
К сожалению, однозначной рекомендации, соблюдение которой позволило бы с высокой вероятностью предупредить тромбоз не существует. Нормализация стула, «отсутствие библиотеки в туалете», отказ от занятий тяжелой атлетикой – снижают риск возникновения острого тромбоза, но не гарантируют полностью, что вновь не возникнет тромбоз в одном из наружных геморроидальных узлов.
Нормализация стула, «отсутствие библиотеки в туалете», отказ от занятий тяжелой атлетикой – снижают риск возникновения острого тромбоза, но не гарантируют полностью, что вновь не возникнет тромбоз в одном из наружных геморроидальных узлов.
Чем руководствоваться при выборе врача и лечебного учреждения
Если вы находитесь в поиске лечебного учреждения, куда обратиться для консультации и лечения острого перианального тромбоза, то нужно обратить внимание на несколько факторов.
- Наличие у учреждения именно проктологической, а не только общехирургичсекой или онкоколопроктологической специализации.
- Владением сотрудниками Клиники информации о всех возможных способах лечения острого перианального тромбоза
- Возможность выполнения в Клинике малых колопроктологическитх операций в условиях стационара
- Возможность выполнения оперативного лечения в Клинике у «особых» групп пациентов – беременных, пациентов старшей возрастной группы
Современные технологии в лечении хронического геммороя
Гончаров Д. Ю. к.м.н.
Ю. к.м.н.Геморрой является одним из широко распространенных заболеваний взрослого населения индустриально развитых стран. Установлено, что у людей старше 40 лет симптомы геморроя обнаруживаются в 60-70 % случаев. На долю геморроя, в структуре колопроктологических заболеваний, приходится около 40%.
В последние годы в повседневную практику колопроктологов уже прочно внедрились малоинвазивные способы лечения геморроя. Преимущества этих методов перед хирургическими вмешательствами, заключаются в возможности их применения в амбулаторных условиях, без потери трудоспособности; высокой эффективности, при начальных стадиях заболевания; небольшом числе осложнений.
Наиболее часто используемыми малоинвазивными методами являются:
- аппаратное лигирование геморроидальных узлов латексными кольцами,
- склеротерапия,
- инфракрасная фотокоагуляция геморроидальных узлов,
- шовное лигирование геморроидальных артерий под контролем допплерометрии,
- электрокоагуляция геморроидальных узлов.

Показанием к проведению малоинвазивных хирургических вмешательств является неосложненный внутренний геморрой I — III стадии.
При выборе способа лечения больных геморроем, целесообразно пользоваться классификацией, которая подразделяет хронический геморрой на IV стадии.
- I ст. Выделение алой крови из заднего прохода без выпадения геморроидальных узлов.
- II ст. Выпадение геморроидальных узлов с самостоятельным вправлением их в анальный канал (с кровотечением или без кровотечения).
- III ст. Периодическое выпадение геморроидальных узлов и необходимость их ручного вправления в анальный канал (с кровотечением или без кровотечения).
- IV ст. Постоянное выпадение геморроидальных узлов вместе со слизистой оболочкой прямой кишки, невозможность их вправления в анальный канал при помощи ручного пособия (с кровотечением или без кровотечения).
К противопоказаниям относятся: сочетание геморроя с анальной трещиной, свищем прямой кишки, воспалительные заболевания анального канала и промежности, острый геморрой.
Лигирование геморроидальных узлов латексными кольцами является наиболее часто применяемой методикой (32-82%), а склеротерапия, в связи частым развитием осложнений (11-47%), используется все реже. Остальные методы малоинвазивного лечения применяются менее чем в 5% случаев.
Лигирование геморроидальных узлов латексными кольцами
Впервые разработал и использовал инструмент для наложения циркулярной латексной лигатуры на ножку геморроидального узла Blaisdell в 1954г. В последующем, были разработаны другие, более совершенные модели лигаторов.
Применение данного метода показано при внутреннем геморрое II, иногда III ст. Противопоказаниями для выполнения лигирования геморроидальных узлов являются: сочетание внутреннего геморроя с анальной трещиной и свищем прямой кишки; острый геморрой; воспалительные заболевания анального канала; лечение антикоагулянтами.
Непосредственно лигирование (пережатие) геморроидальных узлов происходит с помощью латексного кольца с внутренним диаметром 1 мм, которое обладает хорошей эластичностью и обеспечивает равномерное, постоянное сдавление тканей. Отторжение геморроидального узла вместе с лигатурой происходит через 5 — 9 дней после манипуляции. В этот период, как правило, возникает незначительное выделение алой крови из анального канала, которое не требует назначения медикаментозных средств, так как оно купируется самостоятельно. На месте отторгнутого геморроидального узла образуется соединительнотканный рубец.
Отторжение геморроидального узла вместе с лигатурой происходит через 5 — 9 дней после манипуляции. В этот период, как правило, возникает незначительное выделение алой крови из анального канала, которое не требует назначения медикаментозных средств, так как оно купируется самостоятельно. На месте отторгнутого геморроидального узла образуется соединительнотканный рубец.
Существует две основные методики лигирования геморроидальных узлов. Первая основана на втягивании кавернозной ткани во втулку механического лигатора при помощи специального мягкого зажима, после чего на ножку геморроидального узла сбрасывается с инструмента одна или две лигатуры. Кольцо должно пережимать только ножку узла, не захватывая тканей, расположенных ниже аноректальной линии.
Суть второй методики заключается в применении вакуумного лигатора, который подсоединяется к отсосу. Рабочая часть инструмента должна плотно прижиматься к геморроидальному узлу. После включения отсоса, в цилиндре прибора создается отрицательное давление, и узел постепенно втягивается в муфту лигатора. При достижении давления 0,7 — 0,8 атмосферы, на ножку геморроидального узла сбрасывается с инструмента два латексных кольца.
При достижении давления 0,7 — 0,8 атмосферы, на ножку геморроидального узла сбрасывается с инструмента два латексных кольца.
Во время первого сеанса проводится лигирование одного-, двух геморроидальных узлов. Следующий этап лечения назначается не раньше, чем через 15 дней.
При правильном соблюдении методики, больной не должен испытывать выраженную боль. После манипуляции может появиться незначительная болезненность, ощущение давления, чувство инородного тела в прямой кишке, тенезмы, которые могут сохраняться в течение 1 — 2 дней. Эти ощущения купируются приемом ненаркотических анальгетиков.
Осложнениями лигирования геморроидальных узлов являются: болевой синдром (отмечается при условии неправильного выполнения манипуляции), тромбоз наружных геморроидальных узлов (возникает у 2-3% пациентов), кровотечение (наблюдается у 1% больных). Эффективность методики составляет более 80%.
Склеротерапия
Впервые склеротерапию, как метод лечения геморроя, применил И. И. Карпинский (Россия) в 1870 г., используя для этих целей персульфат железа и фенол. Однако часто развивающиеся осложнения, после такой склерозирующей терапии, привели к ограничению использования этого метода. С появлением новых склерозирующих препаратов, аноскопов, специальных игл, вновь возрос интерес к этой методике.
И. Карпинский (Россия) в 1870 г., используя для этих целей персульфат железа и фенол. Однако часто развивающиеся осложнения, после такой склерозирующей терапии, привели к ограничению использования этого метода. С появлением новых склерозирующих препаратов, аноскопов, специальных игл, вновь возрос интерес к этой методике.
В Российской Федерации разрешены к применению препараты группы детергентов. К ним относятся: полидоканол-этоксисклерол, тромбовар, фибровейн, морруат натрия, тетрадецилсульфат натрия. Детергенты являются наиболее эффективными и безопасными флебосклерозирующими химическими веществами. В основе механизма действия данной группы препаратов лежит способность вызывать коагуляцию белков эндотелия и десквамацию эпителия. Детергенты оказывают местное воздействие на сосудистую ткань и не приводят к системному тромбообразованию.
Показанием для проведения склеротерапии является внутренний геморрой I-II стадии; продолжающееся кровотечение из геморроидальных узлов.
К противопоказаниям данного метода относятся: наружный геморрой, парапроктит, тромбоз геморроидальных узлов, изъязвление слизистой, анальная трещина.
Суть методики склерозирования заключается во введении препарата в толщу геморроидального узла, с помощью специально изогнутой иглы с ограничителем. В зависимости от величины геморроидального узла, вводят от 0,5 до 2.0 мл детергента.
В первый день после процедуры возникает реакция тканей на химическую коагуляцию и может развиться болевой синдром. Выраженная болевая реакция может быть связана с введением препарата не в толщу геморроидального узла, а в мышечный слой кишки, а так же с введением концентрированного склерозирующего препарата, в большем объеме. При этом может возникнуть тромбоз и некроз слизистой геморроидального узла.
С целью предотвращения развития болевого синдрома и воспалительного процесса целесообразно за один сеанс проводить склерозирование не более двух геморроидальных узлов. Повторный этап лечения назначают не раньше, чем через 2 недели. При контрольном осмотре на 12-14 день после процедуры, в анальном канале определяется плоский, округлый безболезненный склерозированный участок кавернозной ткани с неизмененной слизистой.
Склеротерапия геморроидальных узлов наиболее эффективна при I стадии геморроя. При увеличении стадийности заболевания, уменьшается количество хороших результатов и возрастает число рецидивов. Склерозирующая терапия не позволяет достичь радикального излечения больных от проявлений геморроидальной болезни, а хорошие отдаленные результаты лечения наблюдаются лишь у 20 % больных.
Инфракрасная фотокоагуляция
С началом применения в медицине ультрафиолетового и инфракрасного излучений, А. Neiger в 1978 г. предложил методику инфракрасной фотокоагуляции геморроидальных узлов. Метод отличается своей простотой и коротким временем воздействия. Применяется при начальных стадиях внутреннего геморроя, а так же для остановки геморроидального кровотечения. Противопоказаниями являются наружный геморрой, тромбоз внутренних геморроидальных узлов, сочетание с парапроктитом и с анальной трещиной.
Принцип действия фотокоагулятора заключается в том, что инфракрасный световой поток фокусируется и по световоду направляется в кавернозную ткань. Наконечник световода пропускает инфракрасный свет, который, проникая в геморроидальный узел, преобразуется в тепловую энергию. Вследствие этого происходит коагуляция подслизистых структур с развитием некробиотических процессов в эндотелии сосудов, что приводит к уменьшению кровенаполнения кавернозной ткани. Глубина некроза зависит от длительности воздействия.
Методика проводится следующим образом. Через аноскоп установленный в анальный канал вводится тубус фотокоагулятора. Наконечником прижимается слизисто-подслизистый слой к мышечному и производится фотокоагуляция. Такое воздействие осуществляется в 3-4 точках, у ножки геморроидального узла, с оставлением промежутков между зонами коагуляции. При этом на слизистой образуется дефект диаметром 4-5 мм с зоной локального коагуляционного некроза, глубина которого распространяется не более чем на 5 мм. Через неделю после фотокоагуляции на месте воздействия образуется струп, который постепенно замещается соединительной тканью с образованием рубца.
За один этап целесообразно проводить коагуляцию не более двух геморроидальных узлов. Повторная процедура проводится через 2 недели. Возможны повторные курсы фотокоагуляции.
Наблюдение за пациентами и анализ результатов лечения показал, что данный метод наиболее целесообразно применять при I стадии хронического геморроя, а так же для остановки геморроидального кровотечения.
Криохирургическое лечение
Одним из малоинвазивных методов лечения геморроя является холодовая деструкция. Криотерапия основана на быстром замораживании геморроидальных узлов жидким азотом. Недостатками данного метода являются: выраженный, неконтролируемый отек перианальных тканей, чувство дискомфорта в анальном канале, болевой синдром, мокнущая рана, а так же длительные сроки выздоровления. Эти проявления отмечаются более чем у 50% пациентов.Ограниченное применение этого метода обусловлено так же сложностью контроля границы распространения криовоздействия, опасностью глубокого некроза тканей, возможностью развития кровотечения. В связи с этим,криотерапия, как метод лечения геморроя, в последние годы практически не используется.
Шовное лигирование геморроидальных артерий под контролемультразвуковой допплерометрии
Сравнительно новой малоинвазивной методикой, пока не получившей широкого распространения на нашем рынке услуг, являетсяшовное лигирование геморроидальных артерий под контролем ультразвуковой допплерометрии. Этот способ привлекает простотой выполнения и целенаправленным воздействием на этиологический фактор развития геморроя.
Метод основан на идентификации геморроидальных артерий, при помощи ультразвуковой (УЗ) допплерометрии, с последующим прошиванием и лигированием их обычной нитью. Данный метод был разработан и предложен японским хирургом Morigana R. (1996 г.)
Для диагностической допплерометрии используется ультразвуковой хирургический аппарат с преобразователем звука и аноскоп с вмонтированным в него ультразвуковым датчиком. После установления этого датчика над геморроидальной артерией на аппарате раздается световой и звуковой сигнал. Через инцизуру в аноскопе, над внутренним геморроидальным узлом производится прошивание и лигирование дистальной ветви геморроидальной артерии восьмиобразным швом. Критерием правильной перевязки артерии, является исчезновение звукового и светового сигналов. Таким же образом лигируются геморроидальные артерии по всей окружности прямой кишки. Это приводит к прерыванию избыточного кровоснабжения внутренних геморроидальных узлов и фиксации их в анальном канале. Эта методика наиболее эффективна при I-III стадиях геморроя.
Противопоказаниями являются наружный геморрой, тромбоз геморроидальных узлов, воспалительные заболевания анального канала, сочетание с парапроктитом и анальной трещиной.
К незначительному числу осложнений можно отнести кратковременную задержку мочеиспускания, чувство дискомфорта в области анального канала в течение 2-3 дней после процедуры. Однако следует помнить, что при чрезмерном затягивании лигатуры возможно прорезывание геморроидальной артерии с развитием массивного артериального кровотечения. Для профилактики отсроченного артериального кровотечения, целесообразно за один сеанс проводить прошивание не более 2 геморроидальных артерий. Последующие сеансы проводятся через 2 недели после первой процедуры. Шовное лигирование геморроидальных артерий под контролем УЗ допплерометрии возможно является перспективным малоинвазивным методом лечения геморроя. Однако, для оценки эффективности этого метода, как и других методик, необходимо изучение отдаленных результатов лечения.
Электрокоагуляция геморроидальных узлов
Одной из современных малоинвазивных методик является электрокоагуляция геморроидальных узлов. Впервые этот способ лечения больных геморроем предложил A.Gain в 1939 году. В литературе сообщается о коагуляции геморроидальных узлов различными аппаратами типа AKM, Bicap, Ultroid, WD-II. Все эти приборы основаны на принципе диатермического воздействия электрического тока, путем проведения его через проводник к слизисто-подслизистым структурам. Путем теплового и химического воздействия на кавернозную ткань происходит некроз её, с последующим фиброзом и образованием рубцовой соединительной ткани.
Методика манипуляции достаточно простая. В зависимости от типа используемого аппарата, производится аппликационная электрокоагуляция слизистой оболочки около ножки геморроидального узла (аппарат Bicap), по типу метода фотокоагуляции. При использовании аппарата WD-II, входящим в комплект двухточечным электродом прокалывается слизистая оболочка ножки геморроидального узла на глубину 0,5 см и при активизации прибора постепенно происходит электрокоагуляция кавернозной ткани. Сила тока регулируется индивидуально. Недостатком метода при использовании этого аппарата, является долгое время экспозиции электрода в одном геморроидальном узле (10-15 мин). За этот период лечения устает как пациент, находящийся в соответствующей позиции, так и врач, проводящий процедуру. Поэтому за один сеанс, возможно, коагулировать лишь один геморроидальный узел.
Показаниями для проведения данной методики является внутренний геморрой I — II стадии, а противопоказаниями — острый геморрой, парапроктит, анальная трещина.
По мнению отечественных и зарубежных исследователей, лечение геморроя методом электрокоагуляции позволяет получить хорошие результаты только у пациентов с I — II стадией геморроя.
В заключение этого раздела, следует сказать, что накопленный личный опыт использования различных малоинвазивных методик, наблюдение за пациентами и анализ отдаленных результатов лечения таких больных показал, что эти методики наиболее эффективны при начальных стадиях геморроя. При IV и III стадиях заболевания целесообразно использовать оперативный метод лечения. Малоинвазивные методики при поздних стадиях геморроя могут быть применены для остановки геморроидального кровотечения, что может быть первым этапом дальнейшего радикального лечения таких больных, а так же у пожилых, соматически отягощенных пациентов с паллиативной целью. По нашему мнению не более 10-15 % пациентов с диагнозом хронический геморрой могут быть радикально вылечены, используя малоинвазивные методы. Однако сочетание различных способов позволяет расширить показания к их применению. Безусловно, положительной стороной малоинвазивных методик является простота применения, небольшое число осложнений, малая травматичность, хорошая переносимость процедуры, возможность их использования в амбулаторных условиях, что экономически выгодно в современных условиях страховой медицины.
Хирургическое лечение
В настоящее время в России все-таки самым распространенным методом лечения геморроя является геморроидэктомия. Большинство колопроктологов и хирургов в нашей стране применяют методику, направленную на иссечение основных коллекторов кавернозной ткани, предложенную Milligan E., и Morgan G. в 1937 г. Эта операция применяется в двух модификациях. Часть врачей применяют закрытую геморроидэктомию, когда после иссечения геморроидального узла, прошивания и перевязки сосудистой ножки, слизистая оболочка ушивается наглухо. Другие колопроктологии используют открытую методику, не восстанавливая целостность слизистой оболочки прямой кишки, с оставлением цельной кожно-слизистой полоски тканей между иссеченными геморроидальными узлами. Каждая модификация имеет свои преимущества и недостатки. В связи с развитием новых технологий и разработкой современных аппаратов, их стали использовать при выполнении геморроидэктомии, с целью уменьшения числа послеоперационных осложнений и сокращения сроков реабилитации пациентов после выполнения операции. Наиболее часто применяют ультразвуковой гармонический скальпель, электротермическую систему LigaSure, радиоволновой скальпель. В последние годы распространение получил метод циркулярной резекции участка слизисто-подслизистого слоя дистального отдела прямой кишки с помощью циркулярного сшивающего аппарата (метод Лонго).
Ультразвуковой гармонический скальпель
Данный метод в нашей стране начал применяться в практике хирургического лечения геморроя сравнительно недавно, но сразу привлек внимание. Принцип действия гармонического скальпеля отличается от других электрохирургических аппаратов тем, что основан на высокой частоте колебания рабочего лезвия в продольном направлении. Это позволяет одновременно коагулировать и рассекать ткани за счет механического разрезания, кавитации и температурного воздействия. Установка позволяет надежно коагулировать сосуды до 5 мм в диаметре. Важно отметить, что при этом происходит строго направленное воздействие на ткани, а глубина термического повреждения прилежащих структур не превышает 1,5мм, что выгодно отличает этот прибор от электрокоагуляторов.
При выполнении геморроидэктомии с использованием ультразвукового скальпеля, первым этапом производится рассечение перианальной кожи с помощью электрокоагулятора и отделение наружного геморроидального узла от волокон подкожной порции наружного сфинктера. Затем, используя режим коагуляции и резания, единым блоком иссекаются наружный и внутренний геморроидальные узлы. Обработка сосудистой ножки производится только в режиме коагуляции. Аналогичным способом удаляются оставшиеся геморроидальные узлы. Раны не ушивают, а оставляют открытыми.
Надежная коагуляция и практически бескровная эксцизия геморроидальных узлов, позволяет сократить время оперативного вмешательства. Неглубокое термическое повреждение тканей приводит к уменьшению болевой реакции в послеоперационном периоде. Все это положительно сказывается на частоте дизурических расстройств и сокращает сроки послеоперационной реабилитации пациентов.
Аппаратно контролируемая биполярная электрокоагуляция
Разработанная для биполярной электрокоагуляции и пересечения сосудов, электротермическая система LigaSure, осуществляет контролируемую подачу энергии на бранши зажима. В результате этого в тканях происходит денатурация коллагена и эластина с образованием зоны коагуляционного некроза. Кроме этого зажимом механически сдавливают ткани, к которым дозировано подается электрический ток. Прочность зоны воздействия, состоящей из частично денатурированного протеина, сравнима с прочностью прошитой ткани. В связи с этим, нет необходимости в выделении и дополнительном лигировании сосудистой ножки геморроидального узла. Весь процесс занимает около 5 секунд. Аппарат позволяет коагулировать сосуды до 7мм в диаметре. Глубина термического воздействия на ткани, согласно характеристикам составляет 2мм.
Электротермическая система LigaSure позволяет проводить геморроидэктомию практически бескровно, не используя шовный материал. При этом значительно сокращается время операции. Однако у некоторых пациентов, в ближайшем послеоперационном периоде развивается достаточно интенсивная болевая реакция, что может быть связано с глубоким термическим воздействием на ткани анального канала. В связи с этим, этот аппарат, по нашему мнению, наиболее целесообразно применять при геморроидэктомии крупных геморроидальных узлов.
Радиоволновой скальпель
Некоторые исследователи предлагают использовать для геморроидэктомии радиоволновой скальпель, который хорошо зарекомендовал себя в косметической хирургии.
Прибор излучает радиоволну, которая вызывает в тканях образование тепла, под воздействием которого происходит распад клеточных структур и происходит разделения тканей. В связи с этим аппарат обладает хорошими диссекционными свойствами. Тепловое повреждение тканей минимальное, что создает оптимальные условия для заживления ран. Однако гемостатические свойства радиоволнового скальпеля низкие, особенно в присутствии биологических жидкостей, что не позволяет использовать только этот аппарат (без электрокоагулятора) для выполнения геморроидэктомии.
Операция Лонго
Эта операция отличается от других методов оперативного лечения больных геморроем тем, что геморроидальные узлы не удаляются. За счет циркулярного иссечения участка слизистой оболочки дистального отдела прямой кишки, при помощи циркулярного сшивающего аппарата, происходит проксимальное подтягивание геморроидальных узлов и фиксация их в анальном канале. При этом происходит пересечение терминальных ветвей геморроидальных артерий, что приводит к значительному снижению кровенаполнения кавернозных сплетений. Все это обуславливает купирование клинических проявлений геморроя, после этой операции. Метод предложил в 1998г. итальянский хирург A. Longo.
Показаниями для данного вида оперативного вмешательства является геморрой III-IV ст. с выпадением узлов, но без выраженного наружного компонента, а так же рецидив заболевания. Противопоказанием — воспалительные заболевания анального канала и промежности, свищ прямой кишки, выпадение только одного геморроидального узла.
Преимуществом аппаратной геморроидопексии является малая травматичность и небольшая продолжительность операции, невыраженный послеоперационный болевой синдром, короткие сроки реабилитации пациентов. Однако следует упомянуть, что у некоторых больных, в послеоперационном периоде была отмечена интенсивная геморрагия, потребовавшая повторной операции.
Несмотря на широкую распространенность данной методики за рубежом, в России эта операция выполняется сравнительно редко. Сдерживающими факторами является высокая стоимость аппарата и отсутствие данных об отдаленных результатах лечения. Безусловно, необходимо иметь сведения о том, что происходит с оставшимися геморроидальными узлами в отдаленные сроки наблюдения. Остается не ясным, происходит ли реваскуляризация оставшейся кавернозной ткани через несколько лет, надежная ли фиксация геморроидальных узлов в анальном канале, не произойдет ли возврат клинических проявлений болезни в отдаленные сроки наблюдения.
Итак, современные возможности хирургического лечения больных хроническим геморроем значительны. Арсенал методов воздействия на это распространенное заболевание велик. Нельзя приспосабливать имеющийся в клинике какой-либо один способ лечения, ко всем стадиям геморроя. Нужно умело определять показания к лечению и, в зависимости от стадии заболевания, выбирать наиболее подходящий способ. Следует помнить, что малоинвазивные методы лечения, на которые охотно соглашаются пациенты, тем более применяемые в амбулаторных условиях, наиболее эффективны при начальных стадиях геморроя. При увеличении стадийности заболевания, а так же при сочетании геморроя с другими заболеваниями анального канала и параректальной клетчатки, показано хирургическое лечение.
Лечение геморроя в Москве – цены на диагностику в клиниках МЕДСИ
Что такое геморрой
При геморрое в области заднего прохода образуются узлы, из-за которых человек испытывает дискомфорт и боль. Это происходит из-за того, что сосуды нижних отделов прямой кишки теряют тонус и эластичность: происходит их варикозное расширение.
Причины возникновения
Основная причина геморроя – генетическая предрасположенность. Склонность к заболеванию переходит по наследству от родителей к детям.
Возможны и другие причины.
- Сидячий образ жизни (недостаточная подвижность, некоторые профессии: кассир, водитель и др.)
- Беременность, роды, использование оральных контрацептивов
- Злоупотребление острой, жирной, сладкой пищей, кофе и алкогольными напитками, а также недостаток в рационе пищевых волокон, овощей и фруктов
- Частое использование клизм и слабительных препаратов
- Анальные половые контакты
- Некоторые виды спорта: мотоцикл, велогонки, верховая езда
- Хронический кашель и другие заболевания, при которых повышается давление в брюшной полости
Проявления геморроя
Первые симптомы – дискомфорт, ощущение тяжести в заднем проходе. По мере развития заболевания присоединяются жжение, зуд и боль при дефекации, кровотечения.
При отсутствии лечения геморрой прогрессирует, появляются анальные трещины, выпадают узлы. Со временем они начинают выпадать не только при дефекации, но и при малейшей физической нагрузке.
Выпавшие узлы нередко тромбируются и воспаляются, что может приводить к дополнительному дискомфорту. Мучительный анальный зуд, периодически сопровождающий геморрой, приводит к расчесыванию, травматизации кожи.
Иногда пациенты предъявляют жалобы на слизистые выделения из прямой кишки и даже недержание стула.
Стадии развития геморроя
Первая стадия – «внутренний геморрой». Проявления заболевания минимальны: дискомфорт в области промежности, усиливающийся при дефекации. К сожалению, пациенты редко обращаются к врачу на этой стадии, хотя это наиболее подходящий момент для эффективного и быстрого лечения.
Вторая стадия характеризуется зудом и жжением в области ануса, а также выраженной болезненностью во время дефекации. Может наблюдаться выпадение геморроидальных узлов.
Третья стадия – «наружный геморрой», при котором узлы выпадают даже без дефекации и не втягиваются назад.
Четвертая стадия – геморрой с осложнениями, когда в крупных узлах происходит тромбоз, ущемление, пациента могут беспокоить длительные кровотечения.
Диагностика
Диагноз ставит проктолог. Жалоб, осмотра и пальцевого исследования прямой кишки, как правило, достаточно для постановки диагноза. Чтобы его уточнить, особенно при внутреннем геморрое, иногда требуется ректороманоскопия или аноскопия.
Лечение
На начальных стадиях заболевания возможно медикаментозное лечение обезболивающими, противовоспалительными и тромболитическими средствами.
Если от лекарств эффекта нет или болезнь находится на стадиях III–IV, используются инвазивные техники, в том числе хирургические. Основные применяемые методы:
- Фотокоагуляция – локальное воздействие на узлы интенсивным пучком инфракрасного излучения. В итоге они лишаются притока крови, запустевают и уменьшаются в размерах
- Склеротерапия – введение в геморроидальный узел вещества, которое вызывает уплотнение (склероз) питающих его сосудов. Сосуды закрываются, и в него больше не поступает кровь. Узел постепенно уменьшается и исчезает
- Дезартеризация – прошивание сосудов, кровоснабжающих узлы. Обескровленные узлы быстро отмирают
- Латексное лигирование – перетяжка основания узла при помощи специального латексного кольца. Узел изолируется от притока крови и отторгается самостоятельно в течение двух недель
- Резекция слизистой по методу Лонго – удаление участка слизистой прямой кишки выше геморроидального узла с последующим ушиванием. Таким образом узел подтягивается вверх и лишается кровоснабжения
- Геморроидэктомия – хирургическое удаление геморроидального узла
У наших пациентов мы предпочитаем использовать малоинвазивные техники, несущие минимум дискомфорта и не требующие длительного восстановления. Среди наиболее эффективных методов лечения – дезартеризация HAL-RAR.
Дезартеризация HAL-RAR может применяться при II, III и даже IV стадии геморроя. Так как это вмешательство не является хирургической операцией, подготовка к нему минимальна. Лечение длится 20-30 минут. С помощью специального устройства (аноскоп с ультразвуковым датчиком) перевязываются артерии, питающие узлы. Слизистая оболочка выше узла закрепляется в постоянном положении, что препятствует его выпадению. Пациента выписывают через 1-2 дня после операции. Реабилитация после процедуры занимает менее недели, а риск рецидива заболевания минимален.
Современные концепции патогенеза и лечения геморроя
В.Л. РИВКИН, д.м.н., профессор, хирург-проктолог, Многопрофильная клиника ЦЭЛТ, МоскваВ патогенезе геморроя основную роль играет тромбоз особых, кавернозных вен (телец) прямой кишки, заполняющихся артериальной кровью. В зоне трех концевых разветвлений прямокишечной артерии, на участках анального канала, проецирующихся на отметки циферблата, соответствующие 3, 7 и 11 часам, из кавернозных вен формируются три основных внутренних геморроидальных узла с их наружными разветвлениями. Геморрой можно делить на бессимптомную стадию, острую форму, кровоточащий геморрой без выпадения узлов и хронический кровоточащий геморрой с выпадением узлов. Традиционное консервативное лечение геморроя ныне дополнено склерозирующими инъекциями и трансанальным лигированием внутренних узлов. Радикальное хирургическое лечение состоит в иссечении трех внутренних узлов одним блоком с соответствующими наружными узлами. Лечение геморроя должно проводиться только после колоноскопии, чтобы не пропустить опухоли толстой кишки, случаи которых в последние годы резко участились, особенно у пожилых людей, часто страдающих геморроем.
Геморрой известен с глубокой древности, название болезни традиционно переводится как кровотечение из прямой кишки во время дефекации (от лат. hemo – кровь и rrhoe – вытекать), хотя клиника болезни намного разнообразнее и шире. Самые различные теории возникновения геморроя (варикоз вен прямой кишки, прямокишечная гемангиома и др.), история методов его лечения многократно описаны, особенно после выделения проктологии как отдельной медицинской специальности (R. Blanchard, 1938; А.Н. Рыжих, 1956; А.М. Аминев, 1973), но только в ХХ в. изучены и объяснены, наконец, настоящие морфологические основы болезни (Миллиган с соавт., 1937). Геморрой долго считался следствием эктазии обычных вен прямой кишки, но оказалось, что в основе его лежит скопление (узлы, piles, от латинского pila – шарик) особых, т.н. кавернозных вен (телец) прямой кишки, имеющих множественные артериовенозные анастомозы (Stelzner, Staubezand, 1962) и заполняющихся артериальной кровью. Анатомическая основа формирования кавернозных телец прямой кишки, геморроидальных узлов – концевые разветвления прямокишечной артерии на правой боковой, левой передне-боковой и левой заднебоковой стенках анального канала, т. е. в проекции 3, 7 и 11 часов по циферблату (при положении тела на спине). В указанных участках анального канала, в подслизистом слое образуются группы кавернозных вен, связанных между собой анастомозами и коллатералями, в т. ч. прямыми артериовенозными соустьями («улитковые артерии», гломусные анастомозы).
Такие же кавернозные образования есть у человека и в других органах – в носу, в мочеточниках, в половых органах, и причины их появления и локализации пока специально не изучались. Кавернозные тельца прямой кишки тромбированы, заполнены кровью постоянно, вне акта дефекации, и сообщаются с обычными венами слизистой оболочки прямой кишки. При самых малых травмах, например, плотными каловыми массами при запорах, при натуживаниях во время родов и т. п. наружная оболочка тромбированного внутреннего геморроидального узла разрывается и возникает артери-альное кровотечение алыми каплями или напряженной алой струйкой, обычно во время или сразу после дефекации. Кровотечение, как правило, самостоятельно останавливается и в большинстве случаев не анемизирует больных. Изучение газового состава и коагуляционной активности крови из геморроидальных узлов, проведенное названными выше Stelzner, Staubezand и другими исследователями, подтверждает, что эта кровь близка по составу к артериальной. Отметим, что, несмотря на приведенную научно обоснованную концепцию этиологии геморроя, до сих пор в некоторых солидных по объему изданиях, например «Colorectal Surgery» (3-е изд., пер. 2009 г.), геморрой почему-то отнесен к «малой проктологии», и этиология его, по мнению авторов, «связана с недостатком в диете пищевых волокон и с растяжением при дефекации». Если это не издержки перевода, то такая трактовка и неверна, и ничего не объясняет. Вероятно, имеются в виду упорные запоры с последующим ослаблением функции анального держания, но это не этиология, а только одна из возможных причин выпадения узлов, которые образуются отнюдь не из-за запоров.
Вторая проблема – первичность воспаления или тромбофлебита при геморрое. Ис-следования свидетельствуют, что острый геморроидальный тромбофлебит вторичен. В его основе лежит воспаление, обусловленное повреждением (изъязвлением) слизистой оболочки анального канала при резком нарушении кровообращения в зонах с патогенной кишечной флорой. Что касается опасности эмболии при остром геморроидальном тромбозе, то это практически исключено, т. к. просветы кавернозных вен очень маленькие, меньше размеров самых мелких тромбов (Л.Л. Капуллер, 1984). Таким образом, ныне патогенез геморроя – как острого болевого приступа, так и хронического его течения с постоянными кровотечениями подробно изучен и принят к сведению большинством специалистов. Дальнейшие исследования могут касаться только отдельных звеньев этого механизма.
При профилактических проктологических обследованиях довольно часто, в основ-ном у пожилых мужчин и много рожавших женщин, при пальцевом ректальном исследовании на стенках анального канала обнаруживаются безболезненные подвижные участки – формирующиеся внутренние геморроидальные узлы, как правило, не кровоточащие и не выпадающие. Этот бессимптомный геморрой, «предболезнь», в лечении не нуждается, у таких лиц следует проводить борьбу с запорами и предупреждать их о возможности кровотечений во время дефекации.
Клинически наиболее часто геморрой начинается с острого приступа – болей, вы-падения и ущемления узлов, чему обычно способствует задержка стула с натуживанием при дефекации. При наружном осмотре в таких случаях определяются плотные, болезнен-ные при дотрагивании, синюшные узлы по всей окружности ануса. Пальцевое (и тем бо-лее инструментальное) исследование и, особенно, попытки вправления таких узлов пред-принимать в это время не следует, ничего, кроме боли, это не дает. Необходим комплекс мер – теплые лежачие ванны, препарат Детралекс и свечи, которых выпускается множест-во. По нашему личному опыту, лучше других действуют свечи Ультрапрокт. Этот комби-нированный препарат, содержащий противовоспалительный компонент флуокортолон и местный анестетик цинхокаин, обеспечивает комплексный эффект – противовоспалительный, противозудный, противоаллергический, антигистаминный и местноанестезирующий. Входящий в состав цинхокаин является местным анестетиком амидного типа, тропный к эпителию прямой кишки. Глюкокортикостероид флуокортолон обеспечивает быстрое начало действия, приводит к уменьшению воспалительного экссудата и продукции цитокинов, торможению миграции макрофагов, уменьшению процессов инфильтрации и грануляции. При местном применении флуокортолон способствует улучшению микроциркуляции, уменьшению отечности и зуда, ускоряет регенерацию СО прямой кишки. В инструкциях к свечам подробно описан способ их применения, но многолетняя практика позволяет дать дополнительные советы: кончик свечи следует смазать любым маслом, вводить свечу неглубоко, в анальный канал, и в течение хотя бы минуты удерживать ее снаружи.
Важный патогенетический фактор острого геморроя – спазм анального сфинктера, возникающий при болевом синдроме и препятствующий самостоятельному вправлению узлов. Ванны и свечи помогают снятию спазма, но в выраженных случаях приходится прибегать к дозированной задней сфинктеротомии, применяемой при анальной трещине и некоторых формах парапроктита (В. Ан, В. Ривкин, 2003). Консервативное лечение, исключение из еды соленых и кислых блюд, разжижение стула (фитолакс, чернослив и другие натуральные фруктовые препараты) в течение в среднем одной недели приводят к почти полному исчезновению симптомов, но больного надо предупредить о возможности рецидивов воспаления и кардинально решать вопрос о дальнейшем лечении. Если после острого приступа, в холодном периоде, пальцевое исследование не обнаруживает выраженных внутренних узлов, если описанное консервативное лечение оказалось эффектив-ным, то можно считать острый эпизод геморроя единичным, эксклюзивным и каких-то конкретных лечебных мер не принимать. Но острый геморрой возникает при уже сформировавшихся внутренних узлах, и болезнь склонна к рецидивам или к переходу в хроническую стадию, о чем надо больного предупредить.
Второй вариант – кровоточащий геморрой без выпадения узлов. При пальцевом ректальном исследовании определяются слегка болезненные, мягкие, подвижные участки в типичных местах, на перчатке нередки следы крови. Ригидная аноскопия или ректоско-пия, ранее широко применявшиеся в таких случаях, неадекватны, ибо никаких новых данных о локализации и состоянии геморроидальных узлов при этом не определяется, а для диагностики сопутствующей патологии толстой кишки, прежде всего опухолей, необходима тотальная фиброколоноскопия (в последние годы все чаще полипы и рак толстой кишки определяются в правых отделах ободочной кишки, недоступных при ректоскопии). Лечение кровоточащего геморроя без выпадения узлов проводят регулированием стула, свечами и т. п.; такое лечение паллиативно, ибо субстрат болезни остается и узлы со временем только увеличиваются. Это привело к поискам более эффективных методов лечения этих многочисленных больных, и ныне, особенно за рубежом, широко применяются две эффективные амбулаторные методики, почему-то плохо воспринимаемые отечественными проктологами. Первый метод – склеротерапия внутренних узлов. После обычной пальцевой дивульсии ануса через операционный аноскоп с подсветом в ручке шприцом с длинной иглой в верхний полюс каждого узла (напомним, их обычно всего три) вводят 1,5–2 мл склерозирующего раствора (тромбовар, этоксисклерол). За один сеанс склерозируют все три узла. Лечение безболезненно, ибо пункция узлов проводится выше зубчатой линии анального канала, где слизистая оболочка не имеет чувствительных нервных окончаний. Эффект наступает быстро, кровотечения надолго прекращаются. Склеротерапия применяется только в хронической стадии геморроя, вне обострения болезни и только при невыпадающих узлах. Вторая методика при этом варианте болезни – трансанальное лигирование ножек внутренних геморроидальных узлов специальными резиновыми (латексными) кольцами (шайбами). С помощью специального миниатюрного инструмента, вводимого через операционный аноскоп, верхушку узла захватывают цапками, втягивают в цилиндр и на ножку узла нажатием кнопки накидывают тугое резиновое кольцо. Узел перестает снабжаться кровью и через день-два вместе с кольцом-шайбой безболезненно выделяется при стуле. Эти методы подробно описаны (O’Regan, 1995), и наш собственный опыт применения этих двух новых «полуконсервативных» амбулаторных методов лечения геморроя свидетельствует об их эффективности (В. Ривкин с соавт., 2012). Удивительно, но до сих пор наши хирурги и даже проктологи длительно, годами лечат таких больных консервативно, меняют разные свечи и препараты, не обращая внимания на начинающуюся анемию. Ни склеротерапия, ни трансанальное лигирование узлов почему-то в широкую практику не входят, тогда как за рубежом эти методики превалируют и их эффективность постоянно подтверждается.
Третий вариант, наиболее практически важный – геморрой с выпадением узлов. В большинстве случаев формируется, как сказано выше, три основных внутренних узла, а впечатление о большем числе узлов складывается из визуального наблюдения дистальных частей (верхушек) этих трех узлов, которые выглядят как отдельные образования (рис. 1). У таких больных узлы обычно легко вправляются, но при самом легком натуживании вновь выпадают. При пальцевом ректальном исследовании, обычно почти безболезнен-ном, удается определить типичную локализацию оснований (ножек) трех основных узлов. Если исследование болезненно и сфинктер заднего прохода спазмирован, то речь идет чаще всего о сочетании геморроя с анальной трещиной: на задней стенке анального канала определяется линейный плотноватый болезненный рубец. Такое сочетание очень часто, оно объясняется повторными воспалительными обострениями геморроя. Так же часто и по этой же причине хронический геморрой сочетается с воспалением стенок прямой (проктит) или прямой и сигмовидной кишки (проктосигмоидит). На фоне хро-нического геморроя при колоноскопии в толстой кишке, намного выше самих геморроидальных узлов, у пожилых людей нередко впервые выявляются полипы и ранние формы рака. Это совершенно с геморроем не связано, геморроидальные узлы не озлокачествляются (кроме, может быть, очень редких случаев анальной меланомы), но колоноскопия у этих, в основном пожилых, людей сама по себе необходима, это в настоящее время очень действенный путь своевременной диагностики опухолей толстой кишки.
Радикальное лечение хронического кровоточащего геморроя с выпадением узлов оперативное. Наиболее эффективной является, на наш взгляд, операция, разработанная названными выше английскими хирургами (Миллиган с соавт.) еще в 1930-х гг. После перевязки сосудистой ножки границы внутреннего узла очерчивают скальпелем и иссе-кают ножницами «снаружи внутрь» со всеми наружными узлами. В конце операции остаются три открытых перианальных раны (в форме, как образно описали авторы, «лопастей резинового вентилятора»). В нашей модификации при этой операции дно этих трех ран принято ушивать (рис. 2), что способствует, во-первых, их более быстрому заживлению и, во-вторых, частично суживает линейными рубцами задний проход, что способствует его лучшей герметизации. До сих пор многие хирурги, считающие лечение геморроя своей компетенцией, оперируют больных старым, отжившим методом простой перевязки наружных узлов, что приводит часто к серьезным осложнениям, например, к стойкой стриктуре ануса, когда между удаленными наружными узлами не остается необходимой широкой кожно-слизистой полоски тканей. Нам приходилось лечить таких больных, и в одном случае развилась полная рубцовая стриктура заднего прохода, и дело кончилось наложением временной колостомы с последующей сложной анальной пластикой. Несмотря на полностью обоснованную и эффективную методику Миллигана с соавт., постоянно предлагаются всё новые и новые методы, подробно описанные Л.А. Благодарным (1999), и возникает ощущение искусственной, только ради пресловутой новизны, разработки и попыток внедрения «новых» методик, иногда совершенно неадекватных, как, к примеру, опасная и сложная операция Уайтхеда и сверхрадикальная резекция анального канала (операция Лонго). Огромный мировой опыт операции Миллигана с соавт. однозначно свидетельствует в ее пользу и незаменимость. Возможны лишь незначительные мелкие усовершенствования, например, суживание трех перианальных ран (рис. 2д).
Радикальная операция при геморрое должна быть четко обоснована; выше уже сказано, что у пожилых больных с сопутствующей серьезной сердечно-сосудистой и другой органопатологией консервативное лечение диетой, свечами, разжижением стула дает длительный благоприятный эффект. У многих пожилых людей хронический кровоточащий геморрой сочетается со стойкой гипертонией, и небольшие, не анемизирующие геморроидальные кровотечения, может быть, для них небесполезны.
Еще раз подчеркнем: начинать лечить, тем более оперировать, геморрой без пред-варительной колоноскопии нельзя. Обращаем внимание врачей любой специальности на то, что кровотечения из заднего прохода, особенно не связанные с дефекацией, требуют безотлагательной колоноскопии. В последние годы во всем мире резко участились случаи опухолей толстой кишки, полипов и рака, а рак прямой и сигмовидной кишки выходит на первое-второе место в онкологической патологии. Опухоли толстой кишки, особенно бессимптомные полипы-аденомы (факультативный предрак), обнаруживаются более чем у 15% людей старше 50 лет (Н. Якутин с соавт., 2002). В России рак толстой кишки диагностируют поздно, на неоперабельных стадиях (Н.Ю. Залит с соавт., 2003), и при анализе выясняется, что многих таких больных долго, иногда в течение недель и месяцев, лечили по поводу геморроя без предварительного обследования толстой кишки. Геморрой у них был, но была и опухоль толстой кишки, диагностика которой запаздывала из-за длительного лечения геморроя. В наше время, когда в каждом городе доступна кишечная гибкая фиброэндоскопия, лечение ректальных кровотечений без проведения колоноскопии является не просто ошибкой, а врачебным преступлением. Полипы и рак толстой кишки часты у пожилых людей, в т. ч. у страдающих геморроем, и длительное лечение геморроя ослабляет внимание врача, оттягивает сроки необходимой колоноскопии.
Литература
1. Blanchard R. Romance of Proctology. London, 1938.
2. Рыжих А.Н. Хирургия прямой кишки. М., 1956.
3. Аминев А.М. Руковоство по проктологии. Т. 2. Куйбышев, 1973.
4. Milligan E., Morgan S., Jones L., Officer R. Anatomy of the anal canal and the operative treatment of hemorrhoids // Lancet. 1937. №2. Р. 1119–1123.
5. R. Phillips (ed.) Colorectal Surgery. Колоректальная хирургия / пер. с англ. М.: ГЭОТАР, 2009. Гл. 14. С. 262–268.
6. Stelzner F., Staubesand J. Das Corpus Cavernosom Recti. // Archiv. Klin. Chir. 1962. №299. Р. 302–312.
7. Капуллер Л.Л. Геморрой // Морфологические основы болез-ней желудка и кишечника. М., 1998. С. 123–128.
8. Ан В.К., Ривкин В.Л. Неотложная проктология. М., 2003.
9. O’Regan P.J. Disposable device and minimally invasive technique for rubber band ligation of hemorrhoids // Dis. Colon. Rectum. 1999. №42. Р. 623–625.
10. Ривкин В.Л., Капуллер Л.Л., Белоусова Е.А. Колопроктология. М., 2011. С. 77–98.
11. Благодарный Л.А. Клинико-патогенетическое обоснование современных способов лечения геморроя. Дис. … д-ра мед. наук. М., 1999.
12. Якутин Н.А. [и др.] Диагностика предраковых заболеваний и начальных форм рака толстой кишки на догоспитальном этапе // Проблемы колопроктологии: сб. М., 2002. С. 502–507.
13. Залит Н.Ю. [и др.] Проблема рака ободочной кишки на рубеже третьего тысячелетия // Акт. вопросы колопроктологии: сб. Самара, 2003. С. 233–235.
Лечение геморроя методом лигирования латексными кольцами. Полезно знать
29.12.2011В настоящее время все более широкое распространение среди колопроктологов получает достаточно простой и эффективный амбулаторный метод лечения внутреннего геморроя — лигирование геморроидальных узлов латексными кольцами.
В свое время зарубежом было разработано специальное устройство, при помощи которого на ножку геморроидального узла набрасывают циркулярную лигатуру из специальной латексной резины. После сдавливания ножки и прекращения притока крови к узлу он отторгается вместе с лигатурой на 11 — 14 день после манипуляции. В результате постепенного прорезывания тканей эластичной лигатурой после его отторжения образуется культя, покрытая соединительной тканью.
Лигирование геморроидальных узлов выполняется пациентам с второй-третьей стадией геморроя. При первой стадии в связи с невыраженностью геморроидальных узлов эта процедура не проводится. В некоторых случаях процедуру можно проводить при четвертой стадии заболевания, то есть при постоянно выпадающих геморроидальных узлах, но с четко выраженными границами, без выраженных наружных геморроидальных узлов.При отсутствии четких границ между наружными и внутренними геморроидальными узлами проведение лигирования считается нецелесообразным. Отсутствие границ между наружными и внутренними геморроидальными узлами, как это бывает при комбинированном геморрое, затрудняет и ограничивает наложение латексных лигатур.Противопоказанием для лигирования внутренних геморроидальных узлов являются воспалительные заболевания: трещина анального канала, хронический парапроктит, проктит в фазе воспаления.
Методика лигирования геморроидальных узлов латексными кольцами
В нашем центре используется методика вакуумного лигирования. Суть методики заключается в следующем. Через аноскоп к геморроидальному узлу, выступающему в просвет аноскопа, подводят специальный вакуумный лигатор, подсоединенный к отсосу для создания отрицательного давления. Ножной педалью включают отсос и большим пальцем правой руки закрывают отверстие в лигаторе для создания отрицательного давления в головке инструмента. За счет отрицательного давления геморроидальный узел втягивается внутрь головки. При достижении отрицательного давления 0,7-0,8 атмосферы при помощи спускового механизма для большей надежности сбрасывают два латексных кольца на геморроидальный узел и отпускают большой палец с отверстия на лигаторе, выравнивая внешнее давление и давление в головке. Затем удаляют лигатор из просвета кишки. Удаление лигатора без выравнивания давления чревато отрывом геморроидального узла и кровотечением.
В методике применяются эластичные кольца, изготовленные из натурального каучука (латекс), с наружным диаметром 5 мм и внутренним — 1 мм. Особенностью латексного кольца является хорошая эластичность и постепенное сдавливание тканей с поэтапным пересечением ножки геморроидального узла в течение 12-14 дней.
Методика вакуумного лигирования более проста и удобна, чем методика механического лигирования. В частности при использовании вакуумного лигатора отпадает необходимость в использовании ассистента во время проведения манипуляции. Помимо этого, методику вакуумного лигирования применяют не только в случаях с четко ограниченной ножкой геморроидального узла, но и при циркулярном внутреннем геморрое, когда достаточно сложно определить ножку узла. При технически правильном выполнении процедуры эластичная лигатура пережимает ножку узла и находится на 5-7 мм выше зубчатой линии.
Процедура лигирования внутреннего геморроя у одного пациента, как правило, проводится за три (чаще всего) и более сеансов. Лучше всего производить за один сеанс лигирование одного геморроидального узла.Иногда может возникнуть необходимость в проведении дополнительных (повторных) лигирований в случае достаточно крупных геморроидальных узлов, размер которых не позволяет за один раз полностью захватить узел головкой вакуумного лигатора, в данном случае повторное лигирование геморроидального узла следует проводить не ранее чем через месяц.
Результаты лигирования геморроидальных узлов латексными кольцами
Лигирование геморроидальных узлов латексными кольцами позволяет избежать геморроидэктомии примерно у 80% больных геморроем.Все процедуры проводятся амбулаторно, без ограничения трудоспособности. В подавляющем большинстве случаев применение данной методики при 2-й и 3-й стадии заболевания позволяет добиться хороших результатов — прекращения выделения крови и выпадения геморроидальных узлов.При 4-й стадии методику лигирование латексными кольцами целесообразно применять лишь у больных с четкими границами выпадающих узлов.В течение первых двух дней после лигирования большинство больных отмечают чувство инородного тела в анальном канале и невыраженный болевой синдром, который купируется ненаркотическими анальгетиками. Эти явления не считают осложнениями, они связаны с пережатием ножки геморроидального узла и не требуют специального лечения.
Возможные осложнения:
Болевой синдром.
Тромбоз наружных геморроидальных узлов.
Ректальное кровотечение.
В некоторых случаях после проведения сеанса лигирования у пациента может возникнуть болевой синдром. В большинстве случаев сильный болевой синдром возникает после одновременного лигирования трех геморроидальных узлов и из-за наложения лигатуры на ножку геморроидального узла на уровне гребешковой линии, т.е. в области заднего прохода, снабженной болевыми рецепторами. Для исключения возникновения сильно выраженного болевого синдрома необходимо строго соблюдать правило поэтапного лигирования геморроидальных узлов с интервалом между процедурами не менее 7 дней.
В некоторых случаях после проведения сеанса лигирования у пациента может возникнуть тромбоз наружных геморроидальных узлов. Возникновение этого осложнения, как правило, связано с тем; что эта процедура проводится у больных со смешанной формой геморроя, при отсутствии границ между наружными и внутренними узлами. С тромбозом геморроидальных узлов в большинстве случаев удается справиться консервативными мероприятиями.При наличии таких заболеваний, как анальная трещина и хронический парапроктит, до их излечения следует отказаться от применения процедуры лигирования.
Примерно в одном случае из ста после лигирования возможно ректальное кровотечение, требующее экстренных мероприятий. Чаще всего, такое кровотечение возникает из-за неточного выбора показаний к процедуре лигирования (выполнение лигирования при невыраженных геморроидальных узлах, после которого массы геморроидального узла может оказаться недостаточно для удержания лигатуры — во время натуживания она может соскочить) или из-за несоблюдения пациентом врачебных рекомендаций по ограничению физических нагрузок, нормализации опорожнения кишечника, питанию и гигиене.Кровотечение также может произойти после стула в первый день после процедуры. Поэтому перед процедурой необходимо проводить подготовку толстой кишки с такой же тщательностью, как и для геморроидэктомии, а больных предупреждать о нежелательности стула в первый день после манипуляции.Результаты лечения позволяют считать лигирование латексными кольцами эффективным и радикальным методом лечения геморроя.
вернуться к списку…
Современные методы лечения геморроя | #03/08
Этиология
Геморрой (от греческого haimorrois) дословно означает «кровотечение». Это заболевание, известное с незапамятных времен, до сих пор объясняется неоднозначно, а подчас и противоречиво, что полностью отражает уровень наших знаний о нем. Большинством исследователей признано, что источниками кровотечения являются кавернозные образования, которые в нормальных условиях формируются в процессе внутриутробного развития.
Первая группа геморроидальных образований, поражение которых приводит к образованию наружного геморроя, расположена на выходе из анального канала, в подкожной клетчатке.
Вторая группа кавернозных образований, расположенная в подслизистом слое прямой кишки, выше зубчатой линии, является источником развития внутреннего геморроя.
Между наружными и внутренними кавернозными образованиями существуют анастомозы, функциональное назначение которых не вполне ясно хотя бы потому, что при повышении внутрибрюшного давления тромбируются, как правило, наружные, а не внутренние узлы. Наряду с наружным и внутренним сфинктером, кавернозные сплетения являются частью запирательного аппарата прямой кишки. Их способность увеличиваться в объеме за счет наполнения кровью позволяет осуществлять идеальную герметизацию кишки. Косвенным доказательством этого предположения служит упорядоченное расположение геморроидальных образований по окружности кишки; оно соответствует 3, 7 и 11 часам. К сожалению, этот тонкий механизм весьма уязвим и причин тому много. Непосредственной причиной возникновения геморроя является нарушение кровенаполнения кавернозных вен, которое может быть вызвано усилением артериального кровотока, но чаще замедлением венозного оттока. Расширенная вена образует «мешок с кровью», который и называется геморроидальным узлом. За последние годы много внимания было уделено изучению состояния связочного аппарата подслизистого слоя прямой кишки, нарушение которого приводит к выпадению внутренних геморроидальных узлов. Поэтому, с точки зрения современной патофизиологии, оба варианта развития заболевания должны рассматриваться не только как равноценные, но, возможно, как взаимодополняющие.
Распространенность. Данные о распространенности геморроя весьма противоречивы, так, в России этот показатель колеблется в пределах 130–145 случаев на 1000 взрослого населения [1]. Статистические данные, приводимые зарубежными исследователями, составляют всего около 4,4% [2, 3]. Противоречивость показателей, вероятнее всего, обусловлена разницей между заболеваемостью и обращаемостью, что косвенно подтверждают данные осмотров жителей США, констатировавшие, что 80% лиц, имевшие геморроидальные узлы, не предъявляли жалоб [4].
Классификация геморроя. Классификация предложена Государственным научным центром колопроктологии [1]. В нее включены симптомы заболевания, его клинические проявления и анатомические изменения. По течению заболевания различаются хронический и острый виды геморроя. По форме — внутренний, наружный, комбинированный. Хроническое течение для внутреннего геморроя подразделяют на 4 стадии. Следует подчеркнуть, что клинические симптомы заболевания соответствуют морфологическим изменениям, происходящим в продольной мышце, фиксирующей кавернозные образования в подслизистом слое прямой кишки.
В первой стадии: клинически отмечаются кровотечения и дискомфорт, геморроидальные узлы не выпадают из анального канала, сосудистый рисунок слизистой оболочки усилен, анатомически — изменения в продольной мышце незначительные.
Во второй — кровотечения, выпадение узлов, зуд, слизистые выделения; выпадающие узлы самостоятельно вправляются в анальный канал; гистологически в фиброзно-мышечном каркасе невыраженная дистрофия, число эластичных волокон преобладает.
В третьей — кровотечения, выпадение узлов, анальный зуд, слизистые выделения. Выпавшие геморроидальные узлы требуют ручного пособия для вправления их в анальный канал; при этом морфологические изменения мышечной ткани свидетельствуют об утрате эластичности, что доказывает преобладание процессов дистрофии.
В четвертой — кровотечения, зуд, дискомфорт, недержание анального сфинктера, выраженный болевой синдром; постоянное выпадение и невозможность ручного вправления геморроидальных узлов в анальный канал; что соответствует полной дистрофии фиброзно-мышечного каркаса, удерживающего узлы в анальном канале.
Осложнения геморроя. Наиболее частым осложнением геморроя является тромбоз геморроидальных узлов. Как правило, поражение возникает в наружных узлах и весьма часто тромбоз является первой манифестацией заболевания. К провоцирующим моментам развития тромбоза чаще относятся беременность, роды, длительные авиаперелеты, подъем больших тяжестей, острые нарушения стула. Если пациенты обращаются за помощью в первые 2 дня от начала заболевания, визуально легко выявляется увеличенный синюшный (на ранней стадии) геморроидальный узел, сверху покрытый кожей и частично слизистой. Чаще появление узла сопровождается болями, особенно интенсивными в случае поражения двух и более узлов. Если размер узла значительный (как правило, более 2 см) при выраженном напряжении ткани слизистой, на ней появляется участок некроза, после отторжения последнего развивается кровотечение, иногда могут частично отойти части тромба и размеры выпавшего образования могут значительно уменьшиться. Кожная часть узла становится отечной и гиперемированной. Клинически, как правило, в этом случае, пациент отмечает уменьшение болей. Пальцевое исследование необходимо начинать с осмотра противоположной от тромбированного узла стенки анального канала, что позволяет сделать исследование более щадящим. При пальцевом исследовании можно обнаружить признаки тромбоза внутреннего геморроидального узла. Осмотр анального канала с помощью инструментов проводят только проктологи.
К более редким осложнениям относится образование гематомы при резком повышении давления и повреждение стенки венозного сосуда. В случае выпадения внутреннего геморроидального узла возможно его ущемление. При возникновении некроза внутреннего узла возможны массивные кровотечения, поэтому больного следует показать специалисту-проктологу. В случае ущемления нескольких выпавших узлов или возникновения нарушений стула возможно присоединение гнойного процесса в параректальной клетчатке.
Дифференциальная диагностика
Клинические проявления геморроя не отличаются специфичностью симптомов. При остром геморрое или его осложнениях — это острый парапроктит, анальная трещина, криптит, выпадение прямой кишки. В случае хронического геморроя в первую очередь следует исключать развитие опухоли прямой кишки или анального канала. Особенную настороженность в плане онкологических заболеваний представляет собой группа больных, длительно страдающих геморроем, обратившихся по поводу участившихся кровотечений или по поводу неустойчивого стула. В случае любого обращения больного с геморроем к терапевту или врачу общей практики необходимо направить его на консультацию к специалисту-проктологу.
Консервативное лечение
Выбор способа лечения, как правило, определяется стадией заболевания или характером развившихся осложнений.
Специальной диеты для больных с геморроем не требуется за исключением некоторых случаев. При тромбозе геморроидальных узлов рекомендуется белково-растительная диета с высоким содержанием клетчатки и исключением жареных и острых блюд, специй, алкоголя. У пациентов с сопутствующими заболеваниями толстой кишки (синдром раздраженной толстой кишки, дивертикулярная болезнь или неспецифические колиты) диета должна быть направлена на нормализацию стула. В случае тромбоза геморроидальных узлов, сопровождающегося запором, больным следует назначать микроклизмы для очистки кишечника. Больным, ведущим сидячий образ жизни, вне обострения необходимо рекомендовать занятия спортом, за исключением тяжелой атлетики и велоспорта. Особое внимание больных следует обратить на выполнение гигиенических мероприятий. В острый период заболевания следует рекомендовать принимать прохладный душ 2–3 раза в сутки и обязательно после стула, при этом необходимо промывать не только кожу промежности и анальное отверстие, но и сам анальный канал. В тех случаях, когда водные процедуры недоступны, следует рекомендовать применение специальных влажных гигиенических салфеток.
Препараты системного действия. В консервативном лечении геморроя одна из ведущих ролей принадлежит препаратам, содержащим биофлаваноиды (диосмин и гесперидин). Использование последних в лечении геморроя традиционно, однако с созданием современных биотехнологий удалось получить Детралекс — микронизированный препарат, что сделало его более биодоступным и увеличило эффективность лечения примерно на 30%. Биофлаваноиды обладают несколькими свойствами: прежде всего они способны повышать венозный тонус, усиливать лимфатический дренаж, уменьшать ломкость сосудов и улучшать микроциркуляцию. В первую очередь перечисленные качества делают необходимым применение Детралекса при возникновении тромбоза геморроидальных узлов. Препарат назначается по 2 таблетки 3 раза в день первые четыре дня, далее по 1 таблетке 4 раза до 7 дней. Кроме того, Детралекс способен уменьшать и предотвращать развитие геморроидальных кровотечений и обострение геморроя. С профилактической целью препарат рекомендуется принимать до 6 месяцев по 2 таблетки в сутки. Использование микронизированных биофлаваноидов (источником которых являются естественные источники, например, косточки красного винограда) возможно даже в период беременности, правда, не длительное время (до 7 дней). Препарат хорошо переносится, крайне редко дает аллергические реакции. К настоящему времени успешно используется препарат «Флебодия 600», обладающий пролонгированным эффектом, что позволяет принимать его один раз в день. У больных с тромбозом геморроидальных узлов, сопровождающимся выраженным болевым синдромом, возможно применение нестероидных противовоспалительных препаратов и анальгетиков, однако оценить эффективность их воздействия крайне трудно, поэтому вопрос о их назначении следует решать индивидуально в каждом конкретном случае.
Местная терапия. Местное лечение назначают в целях снятия воспаления и анальгезии. Среди препаратов первой группы можно рекомендовать мазь «Постеризан форте» (или свечи аналогичного названия). Препарат содержит в себе суспензию культуры кишечной палочки и гидрокортизон. Метаболиты кишечной палочки способны усиливать местные иммунные реакции, сопровождающиеся освобождением цитокинов, особенно интралейкина-1. Кроме того, суспензия культуры бактерий вызывает образование специфического иммуноглобулина А, который образует нежную пленку на слизистой кишечника, выполняющую роль местного защитного барьера. Гидрокортизон, являющийся второй составляющей препарата, способствует скорейшему подавлению воспаления и ускоряет процессы регенерации тканей, индуцируемых суспензией культуры кишечной палочки. Препарат назначается ректально 2 раза в день, в случае тяжелого воспалительного процесса, например, у больных с неспецифическими колитами кратность введения можно увеличить с учетом частоты стула. Максимальная продолжительность лечения не превышает трех недель. При необходимости продолжать терапию возможно использование свечей или мази «Постеризан», содержащих исключительно суспензию культуры бактерий.
Среди препаратов, обладающих комплексным воздействием, следует рекомендовать свечи «Релиф адванс». В состав входит 10%-ный бензокаин, обладающий быстрым анальгезирующим эффектом, кроме того, масло печени акулы, содержащее жирорастворимые витамины, свободные жирные кислоты, сквален и алкилглицерол, являющиеся мощными репарантами, что позволяет рекомендовать их даже для применения в послеоперационном периоде у больных, перенесших вмешательство по поводу геморроя. Кратность введения 3–5 раз в сутки. Препарат обладает высокой эффективностью, хорошо переносим и редко дает побочные реакции.
Хирургическое лечение геморроя
Наружный геморрой. Помимо консервативного лечения тромбированного геморроя в первые 24–48 часов, до момента присоединения воспалительных изменений кожной части узла возможно проведение хирургического вмешательства. Обычно оно выполняется под местной анестезией и заключается в удалении гематомы или тромботических масс, хотя существует мнение о необходимости удаления всего узла вместе с пораженной веной [5]. Такая тактика оправдана при наличии одного (реже двух) узлов больших размеров или при выраженном болевом синдроме. К сожалению, подобные операции удается выполнить не часто, ибо основная масса больных обращается к врачу уже при наличии выраженного воспаления, которое резко усиливает существовавший до этого момента болевой синдром. Хирургическое удаление больших наружных узлов оправдано в случае затруднений, возникающих с гигиеной, при упорном анальном зуде или после перенесенного ранее тромбоза, хотя в последние годы многие пациенты обращаются к проктологу по эстетическим соображениям.
Внутренний геморрой. В настоящее время имеется достаточно большой выбор малоинвазивных пособий, применяемых, в основном, при изолированном внутреннем геморрое I–II стадии. Правда, иногда показания к их применению могут быть расширены, в основном у лиц пожилого и старческого возраста с тяжелыми сопутствующими заболеваниями. К малоинвазивным вмешательствам относятся: инфракрасная фотокоагуляция, лигирование латексными кольцами и, наконец, трансанальное лигирование под контролем доплерометрии. Первые два из перечисленных методик давно применяются в клинической практике, и их сильные и слабые стороны хорошо известны, поэтому подробнее мы остановимся на последнем методе.
Лигирование геморроидальных артерий под доплерометрическим контролем. Суть метода основывается на том, что при доплерометрическом исследовании обнаруживаются дистальные ветви верхней геморроидальной артерии, кровоснабжающие внутренние геморроидальные узлы. Необходимое оборудование — электронный блок и анаскоп с доплеровским датчиком. Метод может быть использован при I–III стадии заболевания. Проведение процедуры возможно в условиях стационара в течение одного дня. Процедура длится 20–40 минут, не требуется общего обезболивания, ограничения на физическую нагрузку около двух недель. Временной нетрудоспособности для пациентов не требуется. Отсутствуют проблемы со стулом в раннем послеоперационном периоде.
Операция Лонго. Выпадение слизистой анального канала с внутренними геморроидальными сплетениями, обусловленное повреждением мышечного и связочного аппарата последних, сопровождается нарушением их кровоснабжения и изменением анатомических отношений между наружными и внутренними узлами. Эта предпосылка послужила основой для создания операции Лонго, предусматривающей подтяжку выпавшей слизистой, восстановление анатомического положения геморроидальных сплетений и нормализацию их кровотока. Метод Лонго используется в клинической практике с 1993 г., в нашей стране последние 5 лет. Вмешательство производится одноразовым набором инструментов. Операция показана при II–IV стадиях геморроя. На наш взгляд, преимущества этой процедуры наиболее убедительны при циркулярном выпадении узлов. Операция может выполняться под проводниковой или местной анестезией.
Достоинства метода; длительность операции 10–20 минут, срок госпитализации не превышает одних суток, болевой синдром хорошо купируется без применения наркотических анальгетиков, отпадает необходимость в перевязках, больной может выйти на работу через 5–10 дней.
Биполярная коагуляция геморроидальных узлов аппаратом LigaSure. Современной альтернативой классической геморроидэктомии является метод биполярной коагуляции геморроидальных узлов, успешно используемый в III–IV стадии заболевания. В основу метода положен принцип биполярной коагуляции модернизированным генератором, снабженным блоком обратной связи, позволяющим дифференцировать ткани. При этом не возникает привычного ожога ткани, а происходит ее сваривание за счет полимеризации собственного коллагена и вместо обычного струпа рана покрывается коллагеновой пленкой. Вмешательство может быть проведено под спинальной или перидуральной анестезией. Методика проведения вмешательства проста. Гарантированная методом надежность полимеризации позволяет коагулировать сосуды до 7 мм в диаметре. Продолжительность операции около 20 минут. Длительность послеоперационного лечения определяется величиной раневых дефектов анального канала. Болевой синдром в послеоперационном периоде выражен менее, чем при традиционной операции.
Литература
-
Воробьев Г. И., Шелыгин Ю. А., Благодарный Л. А. Геморрой. М.: Из-во ООО «Митра-Пресс», 2002. 192 с.
-
Johanson J. F., Sonnenberg A. The prevalence of hemmhoroids and chronic constipation // Gastroenterology. 1990, 98; 380–386.
-
Bayer I., Myslovaty B., Picovsky B. M. Rubber Band ligation of hemorrhoids: covenient and economic treatment // J. Clin. Gastroentrrol. 1966; 23: 50–52.
-
Haas P. A., Haas G. P., Schmaltz S., Fox T.A. Jr. The prevalence of hemorrhoids // Dis. Colon Rectum. 1983; 29: 435–439.
-
Corman M. I. Colon and Rectum surgery, 3 rd ed.Philadelphia, Pa:JB Lippincott. 1993: 54–115.
К. Е. Маят, кандидат медицинских наук
Европейский медицинский центр, Москва
Диагностика и лечение красных глаз в первичной медико-санитарной помощи
1. Петерсен I, Hayward AC. Назначение антибактериальных препаратов в первичной медико-санитарной помощи. J Antimicrob Chemother . 2007; 60 (приложение 1): i43–47 ….
2. Хёвдинг Г. Острый бактериальный конъюнктивит. Акта офтальмол . 2008. 86 (1): 5–17.
3. Вирбелауэр К. Устранение эффекта красных глаз для терапевта. Ам Дж. Мед . 2006. 119 (4): 302–306.
4. Leibowitz HM. Красный глаз. N Engl J Med . 2000. 343 (5): 345–351.
5. Галор А, Jeng BH. Красный глаз для терапевта: когда лечить, когда обращаться. Клив Клин Дж. Мед . 2008. 75 (2): 137–144.
6. Ритвельд Р.П., тер Рит G, Bindels PJ, и другие. Прогнозирование бактериальной причины инфекционного конъюнктивита. BMJ . 2004. 329 (7459): 206–210.
7.Роза PW, Харден А, Brueggemann AB, и другие. Лечение хлорамфениколом острого инфекционного конъюнктивита у детей в первичной медико-санитарной помощи. Ланцет . 2005. 366 (9479): 37–43.
8. Ритвельд Р.П., ван Верт ХК, тер Рит G, и другие. Диагностическое влияние признаков и симптомов острого инфекционного конъюнктивита. BMJ . 2003; 327 (7418): 789.
9. Everitt HA, Маленький PS, Смит П.В.Рандомизированное контролируемое исследование стратегий ведения острого инфекционного конъюнктивита в общей практике [опубликованные поправки опубликованы в BMJ. 2006, 333 (7566): 468]. BMJ . 2006; 333 (7563): 321.
10. Вагнера Р.С., Акино М. Воспаление глаз у детей. Immunol Allergy Clin North Am . 2008. 28 (1): 169–188.
11. Бузнач Н., Даган Р, Гринберг Д. Клинико-бактериальная характеристика острого бактериального конъюнктивита у детей в эпоху устойчивости к антибиотикам. Pediatr Infect Dis J . 2005. 24 (9): 823–828.
12. Морроу GL, Abbott RL. Конъюнктивит. Ам Фам Врач . 1998. 57 (4): 735–746.
13. Азар М.Дж., Дхаливал DK, Бауэр К.С., и другие. Возможные последствия рукопожатия пациентам с эпидемическим кератоконъюнктивитом. Ам Дж. Офтальмол . 1996. 121 (6): 711–712.
14. Фэй А. Заболевания зрительной системы.В: Goldman L, Ausillo D, eds. Сесил Медицина. 23-е изд. Филадельфия, Пенсильвания: Сондерс; 2007.
15. Американская академия офтальмологии. Предпочтительные образцы практики. Конъюнктивит. Сентябрь 2008 г. http://one.aao.org/CE/PracticeGuidelines/PPP.aspx. По состоянию на 3 сентября 2009 г.
16. Sheikh A, Гурвиц Б. Антибиотики в сравнении с плацебо при остром бактериальном конъюнктивите. Кокрановская база данных Syst Rev . 2006 (2): CD001211.
17. Шейх А, Гурвиц Б.Актуальные антибиотики при остром бактериальном конъюнктивите. Br J Gen Pract . 2005. 55 (521): 962–964.
18. Шейх А, Гурвиц Б. Актуальные антибиотики при остром бактериальном конъюнктивите: систематический обзор. Br J Gen Pract . 2001. 51 (467): 473–477.
19. Викстрём К. Острый бактериальный конъюнктивит: польза и риск при лечении антибиотиками. Акта офтальмол . 2008. 86 (1): 2–4.
20.Блок SL, Хедрик Дж, Тайлер Р, и другие. Повышение бактериальной резистентности при остром конъюнктивите у детей. Противомикробные агенты Chemother . 2000. 44 (6): 1650–1654.
21. Goldstein MH, Ковальский Р.П., Гордон Ю.Дж. Возникающая резистентность к фторхинолонам при бактериальном кератите. Офтальмология . 1999. 106 (7): 1313–1318.
22. Литл П, Гулд C, Уильямсон I, и другие.Повторная посещаемость и осложнения в рандомизированном исследовании стратегии назначения лекарств от боли в горле. BMJ . 1997. 315 (7104): 350–352.
23. Сравнение офтальмологической мази на основе сульфата триметоприма-полимиксина B и офтальмологической мази с хлорамфениколом при лечении бактериального конъюнктивита J Antimicrob Chemother . 1989. 23 (2): 261–266.
24. Эмили А, Фсадни М, Гамба Г. Метаанализ шести клинических исследований фазы III, сравнивающих ломефлоксацин 0.3% глазные капли два раза в день до пяти стандартных антибиотиков у пациентов с острым бактериальным конъюнктивитом. Офтальмол Грэфес Арч Клин Эксперт . 1999. 237 (9): 705–713.
25. Лор Дж. А., Остин Р.Д., Гроссман М, и другие. Сравнение трех местных противомикробных препаратов при остром бактериальном конъюнктивите. Pediatr Infect Dis J . 1988. 7 (9): 626–629.
26. Процко Э., Bowman L, Абельсон М, и другие.Фаза 3: сравнение безопасности 1,0% азитромицина в полимерных мукоадгезивных глазных каплях и 0,3% тобрамицина глазных капель при бактериальном конъюнктивите. Инвест офтальмол Vis Sci . 2007. 48 (8): 3425–3429.
27. Белоры Л, Friedlaender MH. Аллергический конъюнктивит. Immunol Allergy Clin North Am . 2008. 28 (1): 43–58.
28. Гране Д. Аллергический риноконъюнктивит и дифференциальная диагностика красных глаз. Allergy Asthma Proc .2008. 29 (6): 565–574.
29. Шаумберг Д.А., Салливан Д.А., Беринг Дж. Э., и другие. Распространенность синдрома сухого глаза среди женщин в США. Ам Дж. Офтальмол . 2003. 136 (2): 318–326.
30. Джексон В.Б. Блефарит: современные стратегии диагностики и лечения. Банка Офтальмол . 2008. 43 (2): 170–179.
31. Томлинсон А, Ханал С, Рамаеш К., и другие. Осмолярность слезной пленки: определение референта для диагностики синдрома сухого глаза. Инвест офтальмол Vis Sci . 2006. 47 (10): 4309–4315.
32. Американская академия офтальмологии. Предпочтительные образцы практики. Синдром сухого глаза. http://one.aao.org/CE/PracticeGuidelines/PPP.aspx. Проверено 3 сентября 2009 г.
33. Американская академия офтальмологии. Предпочтительный образец практики. Блефарит. http://one.aao.org/CE/PracticeGuidelines/PPP.aspx. По состоянию на 3 сентября 2009 г.
34. Tullo A. Патогенез и лечение кератита, вызванного вирусом простого герпеса. Глаз . 2003. 17 (8): 919–922.
35. Тернер А, Рабиу М. Патч от истирания роговицы. Кокрановская база данных Syst Rev . 2006 (2): CD004764.
36. Williams CP, Браунинг AC, Сон TJ, и другие. Рандомизированное двойное слепое испытание местного применения кеторолака в сравнении с искусственными слезами для лечения эписклерита. Глаз . 2005. 19 (7): 739–742.
Симптомы и лечение голосового кровотечения
Что такое голосовое кровотечение?
Голосовое кровотечение — это кровь, которая просочилась в голосовую связку из поврежденного кровеносного сосуда.
Голосовые связки называются «складками», потому что это не просто струны или связки ткани. Они многослойны и содержат внутри очень тонкие кровеносные сосуды. Когда голос используется с силой, тонкие кровеносные сосуды голосовой связки могут разорваться, и кровь попадет в голосовую связку. Принудительное голосовое использование может включать:
- пение агрессивных стилей (например, госпел, рок и т. Д.)
- пение неправильно (то есть плохая техника, нездоровье)
- пение в плохой среде (т.е., плохое усиление, плохие мониторы, шумная обстановка и т. д.)
- прочистка горла
- кашель
- крик
Через короткое время утечка прекращается, но кровь остается в голосовых связках.
Представьте, что происходит, когда вы падаете и приземляетесь на колени. Сила этого удара значительна, но не обязательно приводит к разрыву штанов. Однако ваши колени получили травму. Они становятся темно-пурпурными в течение суток после травмы.Через неделю, когда тело заживает синяк, эта область становится желтой, а затем возвращается к норме. В этом случае ваши штаны похожи на подкладку голосовых связок. Они поглощают часть ударов и не рвутся, но нежная ткань под ними все равно повреждается. Образуется синяк. Таким образом, голосовое кровотечение похоже на ушиб голосовой связки.
Симптомы голосового кровотечения
Симптомы голосового кровотечения различаются в зависимости от ваших требований к голосу.
Если вы являетесь профессиональным пользователем голосовой связи (т.е., кто-то, кто использует свой голос для своей жизни, например певец, актер, закадровый голос и т. д.), вы, возможно, заметите:
- Слушание двух высот одновременно
- Слышание трепета в вашем голосе
- Охриплость вашего голоса (может быть легкой или сильной)
- Снижение диапазона (больше не удается легко брать высокие ноты)
- Неспособность петь тихо
- Неспособность сохранять устойчивую высоту звука
- Боль в шее
- Наиболее значимым симптомом является острая потеря голоса или голосового диапазона .Певцы часто описывают это как «занавес», внезапно закрывающий их голос. Редко, если вообще возможно, получить доступ к полному диапазону голоса с кровотечением без каких-либо манипуляций.
Кровоизлияние — это ушиб голосовой связки. Следовательно, за пределами голосовой связки крови нет. Кровь застряла внутри. Когда это происходит впервые, голосовая связка становится красной. Голосовые связки обычно должны быть белыми; однако, когда кровь впервые попадает в голосовую связку, она окрашивает ее в красный цвет. Со временем, по мере заживления кровоизлияния, организм снова впитает кровь в пуповине, и цвет изменится на желтоватый, а затем вернется к своему нормальному белому цвету.При стробоскопии пуповина будет казаться жесткой и может совсем не вибрировать. В более легких случаях он может слабо вибрировать.
Самопроверка
Спойте пяти нотную шкалу в середине своего диапазона как можно тише. Если это не очень просто (даже без разминки), если качество не идеальное, если ваш голос трескается или если вы намеренно понижаете ноты, у вас может быть кровоизлияние или другое повреждение голоса.
Если вы любитель озвучивания (т.д., врач, учитель, юрист и т. д.), возможно вы заметите:
- Дискомфорт, боль или ощущение стеснения в горле
- Охриплость в голосе
Вы, , не заметите крови в слюне и не откашляетесь кровью.
Как узнать, есть ли у меня кровотечение?
Единственный способ узнать, вызваны ли ваши симптомы кровотечением, — это проверить голосовые связки. Это требует использования видеостробоскопии ларингологом.
Обычный ЛОР обычно не может увидеть полип с традиционным прицелом. Это связано с тем, что оборудование, доступное большинству обычных ЛОР, недостаточно сложное, чтобы внимательно рассмотреть голосовые связки и их вибрацию.
Осложнения вокального кровотечения
Кровоизлияния могут быть осложнены, особенно если диагноз поставлен слишком поздно. Осложнения включают:
- Постоянная охриплость
- Рубцы
- Болезненное звучание / использование голоса
- Потеря голосового диапазона
Ранняя диагностика — ключ к предотвращению этих осложнений.Это означает, особенно для певца, что нужно пройти оценку , как только вы охрипте .
Певцы ошибочно полагают, что охрипнуть после долгого выступления или репетиции — это нормально. — это ненормально, — хрипеть в такие моменты; охриплость голоса — признак того, что что-то не так. Оценка в настоящее время имеет решающее значение для обеспечения обратимости.
К сожалению, люди часто игнорируют охриплость, потому что, когда они отдыхают, она проходит. Однако сейчас самое время прийти.Проходящая охриплость обычно означает, что проблема с голосом обратима. Когда вы обнаружите, что охриплость никогда не проходит, это может означать, что уже слишком поздно, и у вас необратимая проблема с голосом, которая может потребовать хирургического вмешательства.
Правда и мифы
Я слышу противоречивые сведения о кровоизлияниях. Что правда?
Миф: Кровоизлияние означает конец моей карьеры.
Правда: Совсем наоборот! При ранней диагностике кровотечения полностью обратимы и не могут оставить необратимых повреждений.Ранняя диагностика также помогает предотвратить будущие кровотечения.
Миф: Кровоизлияния требуют хирургического вмешательства.
Правда: Кровоизлияния редко требуют хирургического вмешательства. При повторных кровотечениях может потребоваться безопасная процедура, чтобы снизить риск кровотечения в будущем.
Миф: Кровоизлияния невозможно предотвратить.
Правда: Кровоизлияние возникает после злоупотребления голосом, обычно при пении во время болезни или необходимости толкаться по какой-либо причине.Если пройти обследование до того, как у вас возникнут проблемы, вы сможете обнаружить проблемы с гигиеной голоса или кровеносные сосуды, которые подвержены риску кровотечения. Затем вы можете принять меры для предотвращения кровотечения.
Лечение голосового кровотечения
Лечение наиболее эффективно, когда кровотечение обнаружено на ранней стадии и правильно диагностировано.
Это может показаться простым, но без видеостробоскопии сделать это намного сложнее.
Как справиться с кровоизлиянием в голосовую связку?Лучшее лечение — точный диагноз.Любой певец или голосовой пользователь, который замечает резкое изменение голоса, должен немедленно обратиться за помощью к ларингологу. В редких случаях серьезное кровотечение требует неотложной операции, чтобы гарантировать, что голос не будет поврежден навсегда. Однако чаще всего для полного разрешения кровотечения требуются лекарства и отдых для голоса.
Если голосовая пауза не будет остановлена или если диагноз отложен, пациент рискует необратимо повредить голос.
Однако необходимо обследовать пациента, чтобы определить , почему проблема возникла, чтобы помочь предотвратить ее повторение .
В отделении голоса Института головы и шеи Осборна (OHNI) мы понимаем, что ваш голос — это ваше средство к существованию. Мы делаем все возможное, чтобы предотвратить плохие результаты голосовой связи. Ваша оценка в OHNI включает:
- Полный анамнез
- Полный медицинский осмотр головы и шеи
- Ларингоскопия
- Видеостробоскопия
- Планирование лечения — обычно это включает голосовую терапию с квалифицированным терапевтом, имеющим опыт лечения голосовых нарушений
Это комплексное обследование дает вам лучший план лечения, который поможет вам избежать проблем в будущем.
Могу ли я просто обратиться к своему постоянному врачу?К сожалению, немногие люди обучены правильно диагностировать и лечить нарушения голоса. Большинство врачей просто назначают певцам стероидные таблетки. Это на самом деле усугубит кровотечение. Каждый раз, когда вы охрипте, вы потенциально наносите необратимый ущерб, который не может увидеть обычный врач.
Только ларинголог может точно диагностировать и лечить вас, а также помочь предотвратить более серьезную проблему.
О чем я должен спросить своего врача, когда я его посещаю, чтобы убедиться, что я получаю правильное лечение?Пациенту очень сложно отличить квалифицированного врача по голосу от человека, который называет себя врачом по голосу, просто потому, что его стена покрыта фотографиями головы артистов. Большинство певцов полагаются на молву, которая может не привести к истинному ларингологу.
Чтобы убедиться, что вы получаете лечение, которого заслуживаете, вам следует задать своему врачу-терапевту следующие вопросы:
- Вы сертифицированы по ЛОР?
- Имеете ли вы стажировку в области ларингологии / профессионального голоса?
- Вы выполняете видеостробоскопию?
- Выполняете ли вы обследование своих пациентов? *
- Когда требуется операция, проводите ли вы операцию самостоятельно или к участию в ней привлекаются другие врачи или врачи-стажеры? *
- Принимаете ли вы страховку? Покрываются ли ваши услуги страховкой?
* Часто ларингологи находятся в учреждениях, где большую часть услуг выполняют пациенты или стажеры (стажеры).
Оплачивает ли страховка посещение ларинголога?Если ларинголог принимает страховку, ваше посещение обычно покрывается. Ларингоскопия со стробоскопией также обычно закрывается. Лучше всего попросить у вашего врача разъяснения по вопросам страхования.
Цереброваскулярные заболевания — Классификация, симптомы, диагностика и лечение
| Цереброваскулярные заболевания | Американская ассоциация неврологических хирургов |
Слово цереброваскулярное состоит из двух частей: «цереброваскулярный», обозначающий большую часть мозга, и «сосудистый», обозначающий артерии и вены.Вместе слово цереброваскулярное относится к кровотоку в головном мозге. Термин цереброваскулярное заболевание включает все нарушения, при которых область мозга временно или постоянно поражена ишемией или кровотечением, и один или несколько церебральных кровеносных сосудов вовлечены в патологический процесс. Цереброваскулярное заболевание включает инсульт, стеноз сонной артерии, стеноз позвонков и внутричерепной стеноз, аневризмы и сосудистые мальформации.
Ограничение кровотока может быть вызвано сужением сосудов (стенозом), образованием сгустков (тромбоз), закупоркой (эмболией) или разрывом кровеносных сосудов (кровотечением).Отсутствие достаточного кровотока (ишемия) влияет на ткани мозга и может вызвать инсульт.
Приток крови к мозгу
Сердце перекачивает кровь в мозг через две группы артерий: сонные артерии и позвоночные артерии. Сонные артерии расположены в передней части шеи, и это то, что вы чувствуете, когда измеряете пульс прямо под челюстью. Сонные артерии разделяются на внешнюю и внутреннюю артерии в верхней части шеи, при этом наружные сонные артерии снабжают кровью лицо, а внутренние сонные артерии идут в череп.Внутри черепа внутренние сонные артерии разветвляются на две большие артерии — переднюю мозговую и среднюю мозговые артерии и несколько меньших артерий — глазную, заднюю соединительную и переднюю хориоидальную артерии. Эти артерии снабжают кровью передние две трети головного мозга.
Позвоночные артерии проходят вдоль позвоночника и не прощупываются снаружи. Позвоночные артерии соединяются, образуя единую базилярную артерию возле ствола головного мозга, которая расположена у основания черепа.Вертебробазилярная система посылает множество мелких ветвей в ствол головного мозга и разветвляется, образуя заднюю мозжечковую и заднюю менингеальную артерии, которые кровоснабжают заднюю треть мозга. Яремная и другие вены выводят кровь из мозга.
Поскольку мозг полагается только на два набора основных артерий для кровоснабжения, очень важно, чтобы эти артерии были здоровыми. Часто основной причиной ишемического инсульта является закупорка сонных артерий жировыми отложениями, называемыми бляшками.Во время геморрагического инсульта происходит разрыв артерии на поверхности мозга или на его поверхности, что приводит к кровотечению и повреждению головного мозга или вокруг него.
Какими бы ни были основное заболевание и причина, крайне важно как можно скорее восстановить нормальный кровоток и кислород в мозгу. Без кислорода и важных питательных веществ пораженные клетки мозга либо повреждаются, либо умирают в течение нескольких минут. Когда клетки мозга умирают, они не могут восстанавливаться, что может привести к разрушительным повреждениям, иногда приводящим к физическим, когнитивным и умственным нарушениям.
Статистика цереброваскулярных заболеваний
- По оценкам, в 2003 г. произошло 157 803 смертельных случая, связанных с цереброваскулярными заболеваниями; 138 397 из них были у людей в возрасте 65 лет и старше.
- Цереброваскулярное заболевание является наиболее распространенным неврологическим событием, угрожающим жизни, в США. Внутричерепной атеросклероз является причиной примерно 40 000 таких приступов в год, что составляет 10 процентов всех ишемических инсультов.
- Инсульт — третья по значимости причина смерти в США.Из более чем 700 000 человек, пострадавших каждый год, около 500 000 из них — первые нападения, а 200 000 — повторные. Около 25 процентов людей, выздоравливающих после первого инсульта, перенесут еще один инсульт в течение пяти лет.
- Инсульт является основной причиной серьезной хронической инвалидности, и в настоящее время в живых осталось около 5,4 миллиона человек, перенесших инсульт. По оценкам Американской кардиологической ассоциации, в 2003 г. в США инсульт стоил около 51,2 млрд долларов прямых и косвенных затрат.С. в одиночку.
- Согласно последним статистическим данным Американской кардиологической ассоциации, инсульт перенесли 5 400 000 человек.
- Ежегодно около 30 000 человек в США страдают разрывом церебральной аневризмы, а у 6 процентов может быть неразорвавшаяся аневризма.
- Артериовенозные мальформации (АВМ) присутствуют примерно у 1 процента населения в целом. Риск кровотечения из АВМ составляет 4 процента в год с 15-процентной вероятностью инсульта или смерти при каждом кровотечении.
Цереброваскулярные диагностические тесты
Большинство цереброваскулярных проблем можно выявить с помощью диагностических визуализационных тестов. Эти тесты позволяют нейрохирургам просматривать артерии и сосуды в головном мозге и вокруг него, а также саму ткань мозга.
Церебральная ангиография (также называемая вертебральной ангиограммой, каротидной ангиограммой): Артерии обычно не видны на рентгеновском снимке, поэтому используется контрастный краситель. Пациенту вводят местный анестетик, прокалывают артерию, обычно в ноге, и вводят иглу в артерию.Катетер (длинная узкая гибкая трубка) вводится через иглу в артерию. Затем он продвигается через основные сосуды брюшной полости и груди до тех пор, пока не будет должным образом помещен в артерии шеи. Эта процедура контролируется флюороскопом (специальным рентгеновским аппаратом, проецирующим изображение на телеэкран). Затем через катетер в область шеи вводят контрастный краситель и делают рентгеновские снимки.
Дуплекс сонной артерии (также называемый ультразвуком сонной артерии) : В этой процедуре ультразвук используется для выявления бляшек, сгустков крови или других проблем с кровотоком в сонных артериях.Водорастворимый гель наносится на кожу в том месте, где должен быть помещен датчик (портативное устройство, которое направляет высокочастотные звуковые волны на исследуемые артерии). Гель помогает передавать звук на поверхность кожи. Включают ультразвук и получают изображения сонных артерий и формы пульсовой волны. Нет известных рисков, и этот тест неинвазивен и безболезнен.
Компьютерная томография (компьютерная томография или компьютерная томография) : диагностическое изображение, созданное после считывания компьютером рентгеновских снимков.В некоторых случаях через вену вводят лекарство, чтобы выделить структуры мозга. Плотность костей, крови и головного мозга очень разная, и их легко различить на компьютерной томографии. КТ — полезный диагностический тест для геморрагических инсультов, потому что кровь легко увидеть. Однако повреждения от ишемического инсульта могут не быть обнаружены на компьютерной томографии в течение нескольких часов или дней, а отдельные артерии в головном мозге не видны. КТА (КТ-ангиография) позволяет врачам видеть кровеносные сосуды головы и шеи и все чаще используется вместо инвазивной ангиограммы.
Допплерография : водорастворимый гель наносится на датчик (ручное устройство, которое направляет высокочастотные звуковые волны на исследуемую артерию или вену) и кожу над венами проверяемой конечности. Если венозная система в норме, на допплере издается «свистящий» звук. Оцениваются как поверхностная, так и глубокая венозная система. Нет известных рисков, и этот тест неинвазивен и безболезнен.
Электроэнцефалограмма (ЭЭГ) : диагностический тест с использованием небольших металлических дисков (электродов), помещаемых на кожу головы человека для регистрации электрических импульсов.Эти электрические сигналы распечатываются в виде мозговых волн.
Люмбальная пункция (спинномозговая пункция) : инвазивный диагностический тест, при котором игла удаляет образец спинномозговой жидкости из пространства, окружающего спинной мозг. Этот тест может быть полезен при обнаружении кровотечения, вызванного кровоизлиянием в мозг.
Магнитно-резонансная томография (МРТ) : диагностический тест, позволяющий получать трехмерные изображения структур тела с использованием магнитных полей и компьютерных технологий.Он может четко отображать различные типы нервной ткани и четкие изображения ствола и задней части мозга. МРТ головного мозга может помочь определить, есть ли признаки предшествующих мини-инсультов. Этот тест является неинвазивным, хотя некоторые пациенты могут испытывать клаустрофобию в тепловизоре.
Магнитно-резонансная ангиограмма (МРА) : Это неинвазивное исследование, которое проводится с помощью магнитно-резонансного томографа (МРТ). Магнитные изображения собираются компьютером для получения изображения артерий головы и шеи.MRA показывает настоящие кровеносные сосуды в шее и головном мозге и может помочь обнаружить закупорку и аневризмы.
Ход
Инсульт — это резкое прерывание постоянного притока крови к мозгу, которое вызывает потерю неврологической функции. Прерывание кровотока может быть вызвано закупоркой, ведущей к более частому ишемическому инсульту, или кровотечением в головном мозге, приводящим к более смертельному геморрагическому инсульту. Ишемический инсульт составляет примерно 80 процентов всех случаев инсульта.Инсульт может возникнуть внезапно, иногда без предупреждения или без предупреждения, и результаты могут быть катастрофическими.
Симптомы инсульта
Предупреждающие знаки могут включать некоторые или все из следующих симптомов, которые обычно возникают внезапно:
- Головокружение, тошнота или рвота
- Необычно сильная головная боль
- Замешательство, дезориентация или потеря памяти
- Онемение, слабость в руке, ноге или лице, особенно с одной стороны
- Ненормальная или невнятная речь
- Затруднения с пониманием
- Потеря зрения или трудности со зрением
- Потеря равновесия, координации или способности ходить
Типы инсульта и лечение
Ишемический инсульт
Ишемический инсульт — это, безусловно, самый распространенный тип инсульта, на который приходится подавляющее большинство инсультов.Существует два типа ишемического инсульта: тромботический и эмболический. Тромботический инсульт возникает, когда сгусток крови, называемый тромбом, блокирует артерию, ведущую к мозгу, и останавливает кровоток. Эмболический инсульт возникает, когда кусок бляшки или тромба перемещается с исходного места и блокирует артерию ниже по течению. Переместившийся материал называется эмболом. Какая часть мозга повреждена или поражена, зависит от того, насколько далеко ниже по течению артерии происходит закупорка.
В большинстве случаев сонные или позвоночные артерии не закупориваются полностью, и в мозг течет небольшой поток крови.Снижение притока крови к мозгу лишает клетки питательных веществ и быстро приводит к нарушению работы клеток. Поскольку часть мозга перестает функционировать, возникают симптомы инсульта. Во время инсульта есть центральная область, где кровь почти полностью отсекается, и клетки умирают в течение пяти минут. Однако существует гораздо большая область, известная как ишемическая полутень, которая окружает ядро мертвых клеток. Ишемическая полутень состоит из клеток, которые повреждены и не могут функционировать, но все еще живы.Эти клетки называются холостыми, и они могут выжить в этом состоянии около трех часов.
Ишемический инсульт лечится путем устранения препятствия и восстановления притока крови к мозгу. Одним из методов лечения ишемического инсульта является одобренный FDA препарат активатор тканевого плазминогена (tPA), который для достижения наилучшего эффекта необходимо вводить в течение трех часов с момента появления симптомов. К сожалению, лишь от 3 до 5 процентов тех, кто перенес инсульт, вовремя попадают в больницу, чтобы им было назначено это лечение.Это лекарство связано с риском увеличения внутричерепного кровоизлияния и не используется при геморрагическом инсульте. Для пациентов, выходящих за пределы трехчасового временного окна, возможен внутриртериальный тромболизис лекарственными средствами или механическими устройствами. Каротидная эндартерэктомия и / или стентирование шейных и внутричерепных сосудов в некоторых случаях может помочь уменьшить повторный инсульт.
Merci Retriever, недавно одобренный FDA, представляет собой устройство в форме штопора, используемое для удаления сгустков крови из артерий пациентов, перенесших инсульт.В паху пациента делается небольшой разрез, в который вводится небольшой катетер, пока он не достигнет артерий на шее. На шее небольшой катетер внутри большего катетера проводится по артериям, пока не достигнет сгустка мозга. Merci Retriever, прямая проволока внутри небольшого катетера выходит за пределы сгустка и автоматически свертывается в форму штопора. Он втягивается обратно в сгусток, штопор вращается и захватывает сгусток. Баллон надувается в артерии шеи, перекрывая кровоток, поэтому устройство может безопасно вытащить сгусток из мозга.Сгусток удаляется через катетер шприцем.
Геморрагический инсульт
Геморрагический инсульт может быть вызван гипертонией, разрывом аневризмы или сосудистой мальформацией или осложнением приема антикоагулянтных препаратов. Внутримозговое кровоизлияние возникает при кровотечении непосредственно в ткани головного мозга, который часто образует сгусток внутри мозга. Субарахноидальное кровоизлияние возникает, когда кровотечение заполняет пространство спинномозговой жидкости вокруг головного мозга.Оба условия очень серьезные.
Геморрагический инсульт обычно требует хирургического вмешательства для снятия внутричерепного (внутри черепа) давления, вызванного кровотечением. Хирургическое лечение геморрагического инсульта, вызванного аневризмой или дефектом кровеносного сосуда, может предотвратить дополнительные инсульты. Хирургическое вмешательство может быть выполнено для закрытия дефектного кровеносного сосуда и перенаправления кровотока к другим сосудам, которые снабжают кровью тот же участок мозга.
Эндоваскулярное лечение включает в себя введение длинной тонкой гибкой трубки (катетера) в главную артерию, обычно в бедре, направление ее к аневризме или дефектному кровеносному сосуду и введение крошечных платиновых спиралей (называемых стентами) в кровеносный сосуд через катетер.Стенты поддерживают кровеносный сосуд, чтобы предотвратить дальнейшее повреждение и дополнительные удары.
Восстановление и реабилитация — важные аспекты лечения инсульта. В некоторых случаях неповрежденные участки мозга могут выполнять функции, утраченные при инсульте. Реабилитация включает физиотерапию, логопедию и трудотерапию.
Независимо от того, какой тип инсульта перенес, крайне важно, чтобы пострадавшие получали неотложную медицинскую помощь как можно скорее для достижения наилучшего результата.Изучая признаки и симптомы инсульта и обращаясь к факторам риска превентивно, можно предотвратить разрушительные последствия этого заболевания.
Транзиторная ишемическая атака (ТИА)
ТИА — это временное цереброваскулярное событие, не оставляющее необратимых повреждений. Скорее всего, артерия, ведущая к мозгу, временно заблокирована, вызывая симптомы, похожие на инсульт, но закупорка смещается до того, как произойдет какое-либо необратимое повреждение.
Симптомы ТИА могут быть похожи на инсульт, но быстро проходят.На самом деле симптомы могут быть настолько расплывчатыми и мимолетными, что люди просто «отмахиваются» от них, особенно если они длятся всего несколько минут. Симптомы ТИА включают:
- Внезапное онемение или слабость лица, руки или ноги, особенно одной стороны тела
- Внезапное замешательство, проблемы с речью или пониманием
- Внезапное ухудшение зрения одним или обоими глазами
- Внезапное нарушение ходьбы, головокружение, потеря равновесия или координации
- Внезапная сильная головная боль без известной причины
Хотя лечения самой TIA не существует, важно, чтобы источник TIA был идентифицирован и надлежащим образом обработан до того, как произойдет другая атака.Если вы испытываете симптомы ТИА, обратитесь за неотложной медицинской помощью и немедленно сообщите об этом своему лечащему врачу. Около 30 процентов всех людей, перенесших серьезный инсульт, перенесли предшествующую ТИА, а 10 процентов всех жертв ТИА переносят инсульт в течение двух недель. Чем быстрее вы обратитесь за медицинской помощью, тем быстрее можно будет поставить диагноз и начать курс лечения. Раннее вмешательство необходимо для эффективной профилактики серьезного инсульта. Варианты лечения пациентов с ТИА направлены на лечение болезни сонной артерии или сердечных заболеваний.
Факторы риска
Хотя инсульт чаще встречается у пожилых людей, он может возникнуть в любом возрасте. Профилактика инсульта может помочь уменьшить инвалидность и смертность, вызванные этим заболеванием. Контролируемые или излечимые факторы риска инсульта включают:
- Курение: Уменьшите риск, бросив курить. Риск может быть увеличен еще больше при использовании некоторых форм оральных контрацептивов и курильщике. Недавно появились доказательства того, что длительное воздействие пассивного курения может увеличить риск инсульта.
- Высокое кровяное давление: Артериальное давление 140/90 мм рт. Ст. Или выше является наиболее важным фактором риска инсульта. Контроль артериального давления имеет решающее значение для предотвращения инсульта.
- Заболевание сонной или другой артерии: Сонные артерии шеи снабжают кровью головной мозг. Сонная артерия, суженная жировыми отложениями из-за атеросклероза (скопление бляшек на стенках артерии), может быть заблокирована сгустком крови.
- История транзиторных ишемических атак (ТИА).
- Диабет: очень важно контролировать уровень сахара в крови, артериальное давление и уровень холестерина.Диабет, особенно без лечения, повышает риск инсульта и имеет множество других серьезных последствий для здоровья.
- Высокий уровень холестерина в крови: высокий уровень общего холестерина в крови (240 мг / дл или выше) является основным фактором риска сердечных заболеваний, повышающих риск инсульта.
- Отсутствие физической активности и ожирение: Отсутствие физической активности, ожирение или и то, и другое могут увеличить риск высокого кровяного давления, высокого уровня холестерина в крови, диабета, сердечных заболеваний и инсульта.
- Недавние исследования показывают, что у людей, получающих заместительную гормональную терапию (ЗГТ), в целом риск инсульта, в частности ишемического инсульта, повышается на 29 процентов.
К неконтролируемым факторам риска относятся:
- Возраст: инсульты страдают люди любого возраста, включая детей. Но чем вы старше, тем выше риск инсульта.
- Пол: Инсульт чаще встречается у мужчин, чем у женщин.
- Наследственность и раса: риск инсульта выше, если инсульт перенес один из родителей, дедушка или бабушка, сестра или брат. Чернокожие имеют гораздо более высокий риск смерти от инсульта, чем европейцы, отчасти потому, что они более склонны к высокому кровяному давлению, диабету и ожирению.
- Предыдущий инсульт или сердечный приступ: Те, у кого был инсульт, подвергаются гораздо более высокому риску повторного инсульта. Те, у кого был сердечный приступ, также подвержены более высокому риску инсульта.
Стеноз сонной артерии
Сонные артерии снабжают мозг богатой кислородом кровью. Зубной налет образуется, когда внутренние сонные артерии блокируются накоплением жира и холестерина. Этот процесс называется атеросклерозом. Сильная закупорка называется стенозом сонной артерии.Стеноз сонной артерии может вызвать ТИА.
Стеноз сонной артерии часто протекает бессимптомно. Врач может обнаружить это по ненормальному звуку, называемому шумом (BROO’e), при прослушивании сонных артерий с помощью стетоскопа. Пациенты обычно сначала проходят тщательный медицинский осмотр. Это обследование может выявить специфические неврологические, моторные и сенсорные нарушения, которые могут дать ключ к пониманию как степени, так и локализации закупорки. Если врач подозревает стеноз, будут рекомендованы такие диагностические тесты, как ультразвуковая допплерография, дуплексная сонная артерия или церебральная ангиография.
Лечение
Лечение зависит от степени сужения и состояния пациента. Многим людям с артериями, суженными менее чем на 50 процентов, назначают лекарства, помогающие снизить риск ишемического инсульта. К ним относятся гипотензивные средства для контроля высокого кровяного давления, лекарства для снижения уровня холестерина и антикоагулянты для разжижения крови и предотвращения ее свертывания.
Хирургия
Каротидная эндартерэктомия — это процедура, при которой нейрохирург делает разрез в сонной артерии и удаляет бляшку с помощью инструмента для рассечения.Удаление налета достигается за счет расширения прохода, что помогает восстановить нормальный кровоток. Артерия будет зашита швом или трансплантатом. Вся процедура обычно занимает около двух часов. Пациент может испытывать боль возле разреза на шее и некоторые затруднения при глотании в течение первых нескольких дней после операции. Большинство пациентов могут вернуться домой через один-два дня и вернуться к работе, как правило, в течение месяца. Избегайте вождения и ограничьте физические нагрузки в течение нескольких недель после операции.
Каротидная ангиопластика и стентирование
Альтернативная новая форма лечения, каротидная ангиопластика и стентирование, дает определенные надежды для пациентов, которые могут подвергаться слишком высокому риску, чтобы подвергнуться хирургическому вмешательству. Стентирование сонной артерии — это процедура, при которой крошечная тонкая трубка с металлической сеткой вставляется внутрь сонной артерии, чтобы увеличить поток крови, заблокированный бляшками. Стент вводится после процедуры, называемой ангиопластикой, при которой врач вводит катетер с баллоном в закупоренную артерию.Баллон надувается и прижимается к бляшке, сглаживая ее и повторно открывая артерию. Стент действует как каркас, предотвращая схлопывание артерии или ее повторное закрытие после завершения процедуры.
Аневризмы головного мозга
Церебральная (или краниальная) аневризма — это область, в которой кровеносный сосуд в головном мозге ослабевает, что приводит к выпячиванию или расширению части стенки сосуда. Обычно аневризмы развиваются в месте разветвления кровеносного сосуда, потому что «вилка» структурно более уязвима.Расстройство может быть результатом врожденных дефектов или других состояний, таких как высокое кровяное давление, атеросклероз (накопление жировых отложений в артериях) или травма головы.
Аневризмы встречаются во всех возрастных группах, но заболеваемость неуклонно растет среди людей в возрасте 25 лет и старше, наиболее распространена среди людей в возрасте от 50 до 60 лет и примерно в три раза чаще среди женщин. Исход для пациентов, получавших лечение до разрыва аневризмы, намного лучше, чем для пациентов, получавших лечение после, поэтому очень важна необходимость адекватной оценки пациентов с подозрением на аневризму головного мозга.
Неразрывные аневризмы головного мозга могут быть обнаружены неинвазивными методами, включая МРА и каротидную ангиограмму. Разрыв можно обнаружить с помощью компьютерной томографии или люмбальной пункции. Если эти тесты предполагают наличие аневризмы, может быть проведена формальная церебральная ангиография.
Люди, страдающие разрывом аневризмы головного мозга, могут иметь некоторые или все эти предупреждающие признаки: локализованная головная боль, тошнота и рвота, ригидность шеи, нечеткость или двоение в глазах, чувствительность к свету (светобоязнь) или потеря чувствительности.У многих людей с неразорвавшимися аневризмами головного мозга симптомы отсутствуют. Другие могут испытывать некоторые или все из следующих симптомов, которые могут быть возможными признаками аневризмы: паралич черепных нервов, расширенные зрачки, двоение в глазах, боль над и за глазом и локализованная головная боль.
При разрыве аневризм головного мозга они обычно вызывают кровотечение в головном мозге, что приводит к субарахноидальному кровоизлиянию. Кровь также может просачиваться в спинномозговую жидкость (CSF) или области, окружающие мозг, и вызывать внутричерепную гематому (сгусток крови).Кровь может раздражать, повреждать или разрушать близлежащие клетки мозга. Это может вызвать проблемы с функциями тела или умственными способностями. В более серьезных случаях кровотечение может вызвать повреждение головного мозга, паралич или кому. Разрыв аневризмы головного мозга заканчивается смертельным исходом примерно в 50% случаев.
Хирургия
Операция по «зажиманию» аневризмы выполняется путем трепанации черепа (хирургического вскрытия черепа) и изоляции аневризмы от кровотока с помощью одного или нескольких зажимов, что позволяет ей сдуваться.Хирургическое лечение аневризм головного мозга невозможно, если они расположены в недоступных частях головного мозга. Ангиография используется для визуализации закрытия аневризмы и сохранения нормального кровотока в головном мозге.
Менее инвазивный метод, не требующий операции, называемый эндоваскулярной терапией, использует микрокатетеры для доставки спиралей к участку увеличенного кровеносного сосуда, который закупоривает (закрывает) аневризму изнутри кровеносного сосуда. В процедуре, называемой намоткой с помощью баллона, используется крошечный баллонный катетер, который помогает удерживать спираль на месте.Процедура, называемая комбинированным стентом и намоткой, использует небольшую гибкую цилиндрическую сетчатую трубку, которая обеспечивает основу для намотки. Аневризмы можно лечить эндоваскулярными методами, когда риск хирургического вмешательства слишком высок.
Хотя лучший метод фиксации аневризмы должен применяться в индивидуальном порядке, в целом пациентов с разрывом церебральной аневризмы следует лечить как можно скорее. Хирургические риски и исходы зависят от того, разорвалась ли аневризма, размера и расположения аневризмы, возраста пациента и общего состояния здоровья.
Послеоперационные осложнения могут включать спазм сосудов и гидроцефалию. Спазм сосудов — это внезапное сужение кровеносного сосуда, которое снижает кровоток. Гидроцефалия — это состояние, при котором избыток спинномозговой жидкости (ЦСЖ) накапливается в желудочках (полостях, содержащих жидкость) головного мозга и может повышать давление в голове.
Сосудистые мальформации
Термин «сосудистая мальформация» относится к аномальному соединению артерии, вены или того и другого.К ним относятся аномалии нормальных вен или артерий, ведущих непосредственно к венам. Сосудистые мальформации образуются по мере развития кровеносных сосудов головного мозга во время беременности, но прямая причина неизвестна.
Артериовенозные мальформации (АВМ)
АВМ представляет собой клубок аномальных и плохо сформированных кровеносных сосудов (артерий и вен) с более высокой скоростью кровотечения, чем нормальные сосуды. АВМ могут возникать в любом месте тела, но АВМ головного мозга представляют значительный риск при кровотечении.АВМ твердой мозговой оболочки возникают в покрытии головного мозга и представляют собой приобретенное заболевание, которое может быть вызвано травмой.
АВМ обычно диагностируются с помощью МРТ и ангиографии. АВМ могут раздражать окружающий мозг и вызывать судороги или головные боли. При отсутствии лечения АВМ могут увеличиваться и разрываться, вызывая внутримозговое или субарахноидальное кровоизлияние и необратимое повреждение головного мозга. Каждый год около четырех из 100 человек с АВМ испытывают кровотечение. Предотвращение разрыва сосудистых мальформаций — одна из основных причин, по которой при АВМ рекомендуется раннее нейрохирургическое лечение.
План лечения разработан таким образом, чтобы предложить наименьший риск, но при этом наибольший шанс стереть поражение. Доступны три типа лечения: прямое удаление с использованием микрохирургических методов, стереотаксическая радиохирургия и эмболизация с использованием нейроэндоваскулярных методов. Хотя микрохирургическое лечение дает возможность немедленного удаления АВМ, некоторые АВМ лучше всего лечить с помощью комбинации методов лечения.
Стереотаксическая радиохирургия — это минимально инвазивное лечение, при котором используется компьютерное управление для концентрации излучения на деформированных сосудах головного мозга.Это излучение вызывает закрытие аномальных сосудов. К сожалению, стереотаксическая радиохирургия обычно ограничивается очагами диаметром менее 3,5 см и может занять до двух лет, чтобы полностью стереть поражение.
Эмболизация использует нейроэндоваскулярные методы для введения крошечных катетеров в мелкие церебральные сосуды головного мозга, которые питают АВМ. Как только катетер достигает сердцевины АВМ, можно вводить жидкий клей или частицы для закупорки частей АВМ или ее питающих артерий.Нейроэндоваскулярная терапия может сделать последующее хирургическое удаление АВМ более безопасным или уменьшить размер АВМ до объема, в котором радиохирургия обеспечивает более высокую эффективность.
Болезнь Моямоя
Болезнь Моямоя — прогрессирующее заболевание сонных артерий и их основных ветвей, которое может привести к необратимой закупорке. Название происходит от японского слова «клуб дыма» из-за появления образовавшихся повреждений. Фактически, это поражает людей японского происхождения гораздо чаще, чем остальную часть населения.Это заболевание, которое обычно поражает детей и взрослых в третьем-четвертом десятилетии жизни. У детей с этим заболеванием могут быть инсульты, ТИА, медленно прогрессирующее снижение когнитивных функций, судороги или непроизвольные движения конечностей. Взрослые чаще испытывают внутричерепные кровоизлияния в результате заболевания.
Есть несколько операций, которые были разработаны для этого состояния, но в настоящее время наиболее популярными являются EDAS, EMS, STA-MCA и множественные заусенцы.
Процедура EDAS (энцефалодуроартериосинангиоз) требует рассечения артерии скальпа на несколько дюймов и затем создания небольшого временного отверстия в черепе непосредственно под артерией.Затем артерию пришивают к поверхности мозга и заменяют кость.
В хирургии EMS (энцефаломиосинангиоза) височная мышца, которая находится в области виска на лбу, рассекается и через отверстие в черепе помещается на поверхность мозга.
Другие операции включают STA-MCA (поверхностная височная артерия-средняя мозговая артерия), при которой артерия скальпа пришивается непосредственно к поверхностной артерии головного мозга, а также процедуру, при которой в черепе помещают несколько небольших отверстий (заусенцев), чтобы допускают рост новых сосудов в головном мозге из кожи головы.
Венозные ангиомы
Пациенты с венозными ангиомами могут иметь головные боли или судороги, хотя эти симптомы могут не иметь отношения к ангиомам. Чаще эти поражения протекают бессимптомно и выявляются при обследовании пациентов на предмет других состояний. Они редко кровоточат, поэтому лечение обычно не требуется. Они затрагивают примерно 2 процента населения в целом.
Вена мальформации Галена (ВГМ)
Гораздо более редким пороком развития является VGM, который иногда обнаруживается при пренатальном тестировании или при сердечной недостаточности у младенцев.Возникающий во время эмбрионального развития, VGM представляет собой аномальную связь между артериями и глубокими дренирующими венами головного мозга. В нормальных условиях эти артерии и вены связаны капиллярами, которые замедляют кровоток через мозг, обеспечивая необходимый обмен кислорода и питательных веществ.
VGM имеет более толстую стенку, чем AVM, и маловероятен разрыв и кровотечение. Однако, поскольку VGM не имеет капилляров, кровь может течь очень быстро, вызывая чрезмерную нагрузку на сердце, что может привести к сердечной недостаточности.Очень важно, чтобы дети, страдающие этим заболеванием, были оценены и диагностированы экспертами, чтобы были приняты соответствующие меры лечения. Эмболизация — это предпочтительный метод лечения пациентов с ВГМ.
Глоссарий
Аневризма — Аномальное, похожее на баллон выпуклость стенки артерии.
Ангиограмма — исследование, которое показывает кровеносные сосуды, ведущие к головному мозгу и в нем, путем введения красителя или контрастного вещества через катетер, помещенный в артерию ноги.
Ангиография — Рентгенография кровеносных сосудов с использованием инъекции материала, непрозрачного для рентгеновских лучей, для лучшего определения сосудов.
Антикоагулянт — Любое лекарство, препятствующее свертыванию крови; разжижитель крови.
Антигипертензивное средство — Любое лекарство или другое средство для снижения артериального давления.
Арахноид — Средний слой оболочек, покрывающих головной и спинной мозг.
Артериовенозный — Относится как к артериям, так и к венам.
Артерия — кровеносный сосуд, по которому кровь идет от сердца к телу.
Атеросклероз — заболевание, которое приводит к накоплению жира и холестерина внутри кровеносных сосудов, так называемых бляшках.
Мозговая атака — Другое название инсульта.
Bruit — Звук, издаваемый в кровеносных сосудах в результате турбулентности, возможно, из-за накопления зубного налета или повреждения сосудов.
Сонная артерия — Основная артерия на правой и левой стороне шеи, снабжающая кровью головной мозг.
Церебральная эмболия — сгусток крови из одной части тела, который переносится кровотоком в мозг, где он блокирует артерию.
Кровоизлияние в мозг — Кровоизлияние в мозг в результате разрыва кровеносного сосуда, аневризмы или травмы головы.
Инфаркт мозга — Инсульт, вызванный прерыванием или блокированием кровотока в головном мозге; также называется ишемическим инсультом.
Церебральный тромбоз — Образование сгустка крови в артерии, которая снабжает кровью часть головного мозга.
Цереброваскулярные сосуды — Относится к головному мозгу и кровеносным сосудам, которые его снабжают.
Цереброваскулярная окклюзия — Закупорка или закрытие кровеносного сосуда в головном мозге.
Эндартерэктомия — Удаление жировых или холестериновых бляшек и кальцинированных отложений с внутренней стенки артерии.
Эндоваскулярный — Относится к хирургической процедуре, при которой катетер, содержащий лекарства или миниатюрные инструменты, вводится через кожу в кровеносный сосуд для лечения сосудистого заболевания.
Гидроцефалия — состояние, при котором избыток спинномозговой жидкости (CSF) накапливается в желудочках (полостях, содержащих жидкость) головного мозга и может повышать давление в голове.
Ишемия — Неадекватное кровообращение, как правило, из-за закупорки артерии.
Ишемический инсульт — Инсульт, вызванный прерыванием или блокированием кровотока в головном мозге.
Яремные вены — Вены, по которым кровь идет от головы к сердцу.
Зубной налет — Отложение жировых (и других) веществ во внутренней выстилке стенки артерии, которое обычно приводит к атеросклерозу.
Стент — Устройство из расширяемой металлической сетки, которое помещается (с помощью баллонного катетера) в месте сужения артерии.Затем стент расширяют и оставляют на месте, чтобы артерия оставалась открытой.
Субарахноидальное кровоизлияние — Кровь в или кровотечение в пространстве под паутинной оболочкой, чаще всего в результате травмы или разрыва аневризмы.
Транзиторная ишемическая атака (ТИА) — Временное нарушение кровоснабжения определенной области головного мозга; также называется мини-инсультом. Обычно это длится всего несколько минут и не вызывает необратимых повреждений или инвалидности.
Вазоспазм — Спазм кровеносных сосудов, уменьшающий их диаметр.
AANS не поддерживает какие-либо виды лечения, процедуры, продукты или врачей, упомянутые в этих информационных бюллетенях о пациентах. Эта информация предоставляется в качестве образовательной услуги и не предназначена для использования в качестве медицинской консультации. Любой, кому нужен конкретный нейрохирургический совет или помощь, должен проконсультироваться со своим нейрохирургом или найти его в своем районе с помощью онлайн-инструмента AANS «Найди сертифицированного нейрохирурга».
Информация о болезни, вызванной вирусом Эбола, для врачей в медицинских учреждениях США | Клиницистам | Эбола (болезнь, вызванная вирусом Эбола) | Геморрагическая лихорадка Эбола
Ansumana R, Jacobsen KH, Sahr F, Idris M, Bangura H, Boie-Jalloh M et al. Эбола во Фритауне, Сьерра-Леоне — тематическое исследование с участием 581 пациента. N Engl J Med . 2015 5 февраля; 372 (6): 587–8.
Bah EI, Lamah MC, Fletcher T., Jacob ST, Brett-Major DM, Sall AA et al. Клиническая картина пациентов с болезнью, вызванной вирусом Эбола, в Конакри, Гвинея. N Engl J Med. 2015, 1 января; 372 (1): 40–7.
Baize S, Pannetier D, Oestereich L, Rieger T, Koivogui L, Magassouba N et al. Появление заирской болезни, вызванной вирусом Эбола, в Гвинее. N Engl J Med. 9 октября 2014 г .; 371 (15): 1418–25.
Brett-Major DM, Jacob ST, Jacquerioz FA, Risi GF, Fischer WA 2nd, Kato Y et al. Бенг готов лечить пациентов с болезнью, вызванной вирусом Эбола. Am J Trop Med Hyg. 2015 4 февраля; 92 (2): 233–7.
Чертов Д.С., Кляйне С., Эдвардс Дж. К., Скаини Р., Джулиани Р., Спречер А.Болезнь, вызванная вирусом Эбола, в Западной Африке — клинические проявления и лечение. N Engl J Med. 27 ноября 2014 г .; 371 (22): 2054–7.
Чертов Д.С., Нат А., Суффредини А.Ф., Даннер Р.Л., Рейх Д.С., Бишоп Р.Дж., Чайлдс Р.В., Араи А.Е., Палмор Т.Н., Лейн ХК, Фаучи А.С., Дэйви Р.Т. Тяжелый менингоэнцефалит в случае заболевания, вызванного вирусом Эбола: отчет о болезни. Энн Интерн Мед. . 2016 г. 5 апреля. Doi: 10.7326 / M15–3066. [Epub перед печатью]
Feldmann H, Geisbert TW. Геморрагическая лихорадка Эбола. Ланцет. 5 марта 2011 г .; 377 (9768): 849–62.
Фицпатрик Г., Фогт Ф., Мой Гбабай О. Б., Декру Т., Кин М., Де Клерк Х. и др. Вклад вирусной нагрузки Эболы при поступлении и других характеристик пациентов в смертность в Центре ведения пациентов с Эболой «Врачи без границ», Кайлахун, Сьерра-Леоне, июнь – октябрь 2014 г. J Infect Dis . 2015 г., 1 декабря; 212 (11): 1752–8.
Флореску Д.Ф., Калил А.С., Хьюлетт А.Л., Шух А.Дж., Штрохер Ю., Уеки Т.М. и др. Введение бринцидофовира и плазмы выздоравливающих у пациента с болезнью, вызванной вирусом Эбола. Clin Infect Dis . 2015 15 сентября; 61 (6): 969–73.
Фаулер Р.А., Флетчер Т., Фишер В.А. 2-й, Ламонтань Ф., Джейкоб С., Бретт-Майор Д. и др. Уход за тяжелобольными пациентами с болезнью, вызванной вирусом Эбола: перспективы из Западной Африки. Am J Respir Crit Care Med. , 1 октября 2014 г .; 190 (7): 733–7.
Хант Л., Гупта-Райт А., Симмс В., Тамба Ф., Нотт В., Тамба К. и др. Клинические проявления, биохимические и гематологические параметры и их связь с исходом у пациентов с болезнью, вызванной вирусом Эбола: наблюдательное когортное исследование. Ланцет Infect Dis . 2015 ноя; 15 (11): 1292–9.
Джейкобс М., Ааронс Э., Бхагани С., Бьюкенен Р., Кропли И., Хопкинс С. и др. Постконтактная профилактика болезни, вызванной вирусом Эбола, с помощью экспериментальных противовирусных агентов: серия случаев медицинских работников. Ланцет Infect Dis . 2015 ноя; 15 (11): 1300–4.
Johnson DW, Sullivan JN, Piquette CA, Hewlett AL, Bailey KL, Smith PW et al. Извлеченные уроки: управление интенсивной терапией пациентов с лихорадкой Эбола в США.Crit Care Med. 2015 июн; 43 (6): 1157–64.
Кортепетер М.Г., Бауш Д.Г., Брей М. Основные клинические и лабораторные характеристики филовирусной геморрагической лихорадки. J Infect Dis. , ноябрь 2011 г .; 204 Прил. 3: S810–6.
Kraft CS, Hewlett AL, Koepsell S, Winkler AM, Kratochvil CJ, Larson L, et al. Использование TKM-100802 и плазмы выздоравливающих у 2 пациентов с болезнью, вызванной вирусом Эбола, в США. Clin Infect Dis . 2015 15 августа; 61 (4): 496–502.
Kreuels B, Wichmann D, Emmerich P, Schmidt-Chanasit J, de Heer G, Kluge S, et al.Случай тяжелой инфекции, вызванной вирусом Эбола, осложненной грамотрицательной септицемией. N Engl J Med. , 18 декабря 2014 г .; 371 (25): 2394–2401.
Lai L, Davey R, Beck A, Xu Y, Suffredini AF, Palmore T. wt al. Экстренная постконтактная вакцинация вакциной против вируса Эбола везикулярного стоматита после укола иглой. ДЖАМА. 2015 24–31 марта; 313 (12): 1249–55.
Liddell AM, Davey RT Jr, Mehta AK, Varkey JB, Kraft CS, Tseggay GK et al. Характеристики и клиническое ведение кластера из 3 пациентов с заболеванием, вызванным вирусом Эбола, включая первые случаи домашнего заражения в Соединенных Штатах. Энн Интерн Мед. . 2015 21 июля; 163 (2): 81–90.
Lyon GM, Mehta AK, Varkey JB, Brantly K, Plyler L, McElroy AK et al. Клиническая помощь двум пациентам с болезнью, вызванной вирусом Эбола, в США. N Engl J Med. , 18 декабря 2014 г .; 371 (25): 2402–2409.
Mora-Rillo M, Arsuaga M, Ramírez-Olivencia G, de la Calle F, Borobia AM, Sánchez-Seco P et al. Синдром острого респираторного дистресс-синдрома после использования плазмы выздоравливающих: лечение пациента с болезнью, вызванной вирусом Эбола, заразившейся в Мадриде, Испания. Ланцет Респир Мед . 2015 июл; 3 (7): 554–62.
Парра Дж. М., Сальмерон О. Дж., Веласко М. Первый случай заболевания, вызванного вирусом Эбола, за пределами Африки. N Engl J Med. , 18 декабря 2014 г .; 371 (25): 2439–40.
Qin E, Bi J, Zhao M, Wang Y, Guo T, Yan T et al. Клинические особенности пациентов с болезнью, вызванной вирусом Эбола, в Сьерра-Леоне. Clin Infect Dis . 2015 15 августа; 61 (4): 491–5.
Sagui E, Janvier F, Baize S, Foissaud V, Koulibaly F, Savini H et al. Тяжелая инфекция вирусом Эбола с энцефалопатией: доказательства прямого заражения вирусом. Clin Infect Dis . 2015 15 ноября; 61 (10): 1627–8.
Schibler M, Vetter P, Cherpillod P, Petty TJ, Cordey S, Vieille G et al. Клинические особенности и вирусная кинетика у быстро излечившегося пациента с болезнью, вызванной вирусом Эбола: отчет о случае. Ланцет Infect Dis . 2015 Сен; 15 (9): 1034–40.
Schieffelin JS, Shaffer JG, Goba A, Gbakie M, Gire SK, Colubri A et al. Клинические заболевания и исходы у пациентов с Эболой в Сьерра-Леоне. N Engl J Med. , 27 ноября; 371 (22): 2092–100.
Sueblinvong V, Johnson DW, Weinstein GL, Connor MJ Jr, Crozier I, Liddell AM et al. Критическая помощь при полиорганной недостаточности, вторичной по отношению к болезни, вызванной вирусом Эбола, в США. Crit Care Med . 2015 октябрь; 43 (10): 2066–75.
Uyeki TM, Mehta AK, Davey RT Jr, Liddell AM, Wolf T, Vetter P et al. Клиническое ведение болезни, вызванной вирусом Эбола, в США и Европе. N Engl J Med . 2016 18 февраля; 374 (7): 636–46.
Группа реагирования ВОЗ на Эболу, Агуа-Агум Дж., Арияраджа А., Блейк И.М., Кори А., Доннелли, Калифорния, Доригатти И. и др.Болезнь, вызванная вирусом Эбола, среди детей в Западной Африке. N Engl J Med . 2015 26 марта; 372 (13): 1274–7.
Группа реагирования ВОЗ на Эболу. Болезнь, вызванная вирусом Эбола, в Западной Африке — первые девять месяцев эпидемии и перспективные прогнозы. N Engl J Med. , 16 октября 2014 г .; 371 (16): 1481–95.
Группа реагирования ВОЗ на Эболу. Эпидемия Эболы в Западной Африке через год — замедление, но пока не под контролем. N Engl J Med . 2015 5 февраля; 372 (6): 584–7.
Wong KK, Davey RT Jr, Hewlett AL, Kraft CS, Mehta AK, Mulligan MJ, Beck A, Dorman W, Kratochvil CJ, Lai L, Palmore TN, Rogers S, Smith PW, Suffredini AF, Wolcott M, Ströher U, Uyeki TM.Использование постконтактной профилактики после профессионального заражения Заирским эболавирусом. Clin Infect Dis . 2016 26 апреля. Pii: ciw256. [Epub перед печатью]
Кошачий бокавирус-1, связанный со вспышками геморрагического энтерита у домашних кошек: потенциальное первое свидетельство патологической роли, вирусного тропизма и естественной генетической рекомбинации
Животные и образцы препаратов
Всего 17 домашних кошек ( Felis catus ) из три разных независимых домохозяйства (10, четыре и три кошки из домохозяйств A, B и C соответственно), расположенные в столичном городе Бангкок, Таиланд, показали аналогичное острое начало депрессии, за которым последовала кровавая диарея, кровохарканье и судороги.Начало клинической картины было очевидным в течение 24 часов после распознавания депрессии животного. Первоначальные диагностические тесты были выполнены на всех кошках, включая гематологию, биохимические профили сыворотки и исследование кала, во время их посещения больницы. Антиген FPLV, вируса лейкемии кошек (FeLV) и коронавируса кошек (FCoV), а также антитела вируса иммунодефицита кошек (FIV) были проверены на предмет наличия коммерческих тест-наборов (Rapid Anigen, Bionote, Южная Корея). Общая токсикология, включая отравление варфарином и фосфорорганическими соединениями, обнаружение в моче и фекалиях, а также бактериальные культуры из носовых и / или фекальных мазков, проводилась рандомизированным кошкам.Во время поддерживающего лечения у всех кошек собирали мазки из кала для дальнейшего исследования. Все протоколы экспериментов были одобрены Комитетом по уходу и использованию животных Университета Чулалонгкорн (№ 1631002). Все процедуры были выполнены в соответствии с соответствующими инструкциями и правилами. Владельцы собак дали письменное согласие на сбор образцов и публикацию данных.
Позже всего 13 из этих кошек умерли (10, две и одна из домохозяйств A, B и C соответственно).С разрешения владельцев три из 13 умирающих кошек (по одной из каждого дома) были отправлены на вскрытие в отделение патологии факультета ветеринарных наук Университета Чулалонгкорн. Отобранные образцы тканей, включая мозг, легкие, сердце, желудок, тонкий и толстый кишечник, печень, селезенку, лимфатические узлы и почки, были собраны, зафиксированы в 10% нейтральном забуференном формалине и отправлены на стандартную гистопатологию плюс периодическая кислота-Шифф. (PAS) и окрашивание альциановым синим. Результаты микроскопии были оценены сертифицированным ветеринарным патологом (TK).Более того, свежие ткани, включая мозг, трахею, легкие, тимус, подчелюстные и брыжеечные лимфатические узлы, печень и кишечник, собирали для дальнейшего молекулярного анализа. Фекальные мазки от всех 17 кошек и свежие ткани от трех вскрытых кошек были отдельно гомогенизированы, и общая вирусная РНК / ДНК была экстрагирована с использованием набора для экстракции вирусных нуклеиновых кислот II (Geneaid, Тайбэй, Тайвань). Качество и количество экстрагированной РНК / ДНК определяли по оптической плотности в соотношении A260 / 280 с использованием спектрофотометра (NanoDrop, Thermo Scientific ™, США).Пан-респираторные и кишечные вирусологические ПЦР-панели, включая обнаружение вируса герпеса 38 , парамиксовируса 39 , парвовируса 40 , коронавируса 41 и BoV 1 , были выполнены в отобранных образцах свежих тканей (легкие, лимфатические узлы). , и кишечник) от трех вскрытых кошек. Праймеры для ПЦР, специфичные для панкалицивирусов; прямой (CV2429F): 5’GAACTACCCGCCAAT3 ‘и обратный (CV2550R): 5’AGCACRYCATATGCGGC3’ были разработаны на основе выравнивания последовательностей ORF1 различных калицивирусов и затем выполнены в тех же образцах.
Для установления распространенности FBoV-1 у здоровых кошек и кошек без FPLV с диареей, образцы фекалий от двадцати здоровых и пятнадцати образцов фекалий от кошек без FPLV, находящихся в том же районе (Бангкок, Таиланд), где возникли вспышки. были включены для обнаружения FBoV-1.
Геномная идентификация и характеристика штаммов FBoV-1 и FPLV
Для первоначальной идентификации FBoV положительные образцы ПЦР pan-BoV затем секвенировали для подтверждения и классификации происхождения BoV.Анализ секвенирования подтвердил достоверность положительных образцов ПЦР pan-BoV и, следовательно, присутствие FBoV-1. Чтобы повысить чувствительность обнаружения FBoV-1 и исследовать присутствие генома FBoV-1 в других органах трех умирающих кошек и установить вспышку заболевания у соседних кошек, экстрагированная общая вирусная РНК / ДНК, полученная из селективных свежих образцы тканей трех вскрытых кошек, фекальные мазки от всех кошек с FPLV, кошек без FPLV и здоровых кошек тестировали с помощью FBoV-1-NS1-специфической ПЦР с использованием праймеров, как описано ранее 1 .
Кроме того, вырожденные наборы праймеров, специфичные для генома FBoV-1, были разработаны путем выравнивания различных штаммов FBoV-1, доступных из базы данных NCBI GenBank, чтобы позволить амплификацию ПЦР и коммерческое секвенирование для получения полного кодирующего генома тайских штаммов FBoV-1 (Дополнительная таблица S1). Вкратце, общая вирусная РНК / ДНК, полученная из лимфатических узлов трех вскрытых кошек, была индивидуально амплифицирована с использованием набора Qiagen OneStep RT-PCR (Qiagen GmbH, Hilden, Германия) с комбинацией обратной транскриптазы и ДНК-полимеразы и специфических праймеров.Ампликоны были получены термоциклированием при 50 ° C в течение 30 минут, 94 ° C в течение 15 минут, а затем 40 циклов при 94 ° C в течение 30 секунд, 50 ° C в течение 30 секунд и 72 ° C в течение 1 минуты, перед окончанием 72 ° C. ° C в течение 7 мин. Продукты ПЦР визуализировали при электрофорезе в 1% (мас. / Мас.) Агарозном геле и дополнительно очищали с использованием набора для экстракции из геля ДНК Monarch (New England Biolab, Франкфурт, Германия) перед коммерческим секвенированием по Сэнгеру (Macrogen Inc, Сеул, Южная Корея). Полные кодирующие последовательности изолятов FBoV-1, полученные от трех вскрытых кошек, были депонированы в GenBank (номера доступа MN127776-MN127778).
Кроме того, праймеры, специфичные для гена VP1 / 2 FPLV, были извлечены из предыдущей публикации 40 , а праймеры для генов NS1 и NP1 FPLV (дополнительная таблица S2) были сконструированы путем выравнивания доступных геномов FPLV в GenBank с амплифицировать полный кодирующий геном полученных штаммов FPLV в этом исследовании. Вкратце, общая РНК / ДНК, выделенная из образцов кишечника трех вскрытых кошек, и образцы фекалий, полученные от здоровых кошек с симптомами, были индивидуально амплифицированы с использованием набора Qiagen OneStep RT-PCR и амплифицированы и секвенированы, как указано выше для FBoV-1, за исключением для термоциклического отжига (55 ° C в течение 2 минут) и удлинения (72 ° C в течение 2 минут).Полные кодирующие последовательности тайских штаммов FPLV были депонированы в GenBank (номера доступа MN127779-MN127781).
Секвенирование и филогенетический анализ FBoV-1 и FPLV
Полные кодирующие последовательности генома тайских штаммов FBoV-1 были сопоставлены с опубликованными последовательностями FBoV-1 с использованием MAFFT версии 7 (http://mafft.cbrc.jp / alignment / server /) и программное обеспечение MEGA7. Выравнивания выходных последовательностей затем использовали в качестве шаблона для построения филогенетического дерева. Филограмма была построена с использованием метода максимального правдоподобия (ML) с моделью TN93 + G, которая была выбрана с использованием алгоритма модели поиска наилучшего соответствия в Mega7 в соответствии с байесовским информационным критерием.Дерево было протестировано с 1000 повторениями начальной загрузки. Последовательности попарных расстояний между геномами FBoV-1 были рассчитаны с использованием модели максимального сложного правдоподобия, а их эволюционное расстояние проанализировано в MEGA7. Выходные парные нуклеотидные расстояния были сгенерированы и визуализированы на попарной тепловой карте с использованием веб-сервера Heatmapper (http://www.heatmapper.ca/) 42 . Вариабельность предсказанных (транслированных in silico) аминокислотных последовательностей генов NS1, VP1 / 2 и NP1 штаммов FBoV-1 была проанализирована с помощью индекса разнообразия Симпсона с использованием онлайн-программного обеспечения Protein Variability Server (http: // imed.med.ucm.es/PVS/).
Для геномов FPLV, полученных от пораженных кошек, был проведен филогенетический анализ с использованием тех же критериев для геномов FBoV-1, указанных выше. Филогенетическое дерево ML геномов FPLV было построено с использованием общей обратимой модели и загружено с 1000 повторов.
Генетическая рекомбинация в штамме тайского FBoV-1 и штаммах FPLV
Потенциальная генетическая рекомбинация в полученном тайском штамме FBoV-1 была заподозрена на основании филогенетического анализа, и поэтому была исследована на предмет использования пакета интегрированной программы обнаружения рекомбинации 4 (RDP4) v .Программное обеспечение Beta 4.94 43 . Для анализа систематически использовался ряд методов обнаружения рекомбинации, включая Bootscan, Chimera, GeneConv, MaxChi, RDP, SiScan и 3Seq, с допустимым пороговым значением p 0,01. Поправка Бонферрони была установлена по умолчанию. Выравнивание каждой обнаруженной последовательности FBoV-1 с последовательностями, доступными в GenBank, использовали в качестве матрицы для анализа генетической рекомбинации. Любое потенциальное событие рекомбинации, которое было обнаружено по крайней мере четырьмя методами, считалось потенциальным рекомбинантным 44,45 .Основные и второстепенные родители потенциального рекомбинанта, обнаруженного в RDP, были дополнительно проанализированы с использованием графика сходства и анализа загрузочного сканирования в программном пакете SimPlot v. 3.5.1 46 . Рекомбинантный геном, полученный в результате анализа RDP, использовали в качестве запрашиваемой последовательности. Рекомбинационный анализ проводился с размером окна 200 п.н. и размером шага 20 п.н. Точки излома рекомбинации были идентифицированы и проанализированы с помощью модели параметра Кимуры-2 (K2P) для анализа загрузочного сканирования и модели GapStrip для графика сходства.Затем была построена филогения обнаруженной области рекомбинации, чтобы подтвердить предложенную рекомбинацию. Критерии и процедура построения филогенетического дерева ML выполнялись, как описано в анализе полного кодирующего генома. Для полного анализа другие тайские штаммы FBoV и все тайские штаммы FPLV, полученные в этом исследовании, также были проверены на потенциальную рекомбинацию с использованием подхода, аналогичного описанному выше для FBoV-1.
Тканевое распределение нуклеиновых кислот FBoV-1
Распределение FBoV-1 и, следовательно, вирусный тропизм оценивали с помощью ISH, чтобы подтвердить присутствие вирусной ДНК в фиксированных формалином образцах, залитых парафином (FFPE) из трех вскрытых. кошки.Исследованные ткани включали мозг, легкие, сердце, язык, желудок, тонкий и толстый кишечник, печень, селезенку и лимфатические узлы. ДНК-зонд, покрывающий 133 п.н. гена NS1 FBoV-1, получали с использованием набора для синтеза зонда PCR DIG (Roche Diagnostics, Базель, Швейцария) в соответствии с инструкциями производителя. Реакцию ПЦР проводили в тех же условиях термоциклирования, описанных ранее, с использованием описанных праймеров NS1 1 , за исключением использования олигонуклеотидов, меченных дигоксигенином (DIG), вместо немеченых олигонуклеотидов.Валидацию гибридизационного зонда проводили с помощью разрешения по размеру на 1,5% (мас. / Об.) Электрофореза в агарозном геле и с использованием контрольной ДНК для иммуномечения Нозерн-блотом (не показано). ISH с хромогенной ДНК выполняли, как ранее сообщалось 47 , с незначительной модификацией. Вкратце, каждое предметное стекло FFPE толщиной 4 мкм депарафинизировали, регидратировали и затем промывали фосфатно-солевым буфером (PBS). После этого слайды обрабатывали протеиназой К (200 мкг / мл; VWR, Radnor, США) в предварительно нагретом PBS при 37 ° C в течение 15 мин.Затем предметные стекла трижды промывали в PBS по 5 мин каждое. Чтобы удалить эндогенную щелочную фосфатазу, на каждое предметное стекло наносили холодную 20% (об. / Об.) Уксусную кислоту на 20 секунд, и эти предметные стекла пропитывали PBD 3 раза по 5 минут каждое, затем сушили при комнатной температуре. После этого все слайды предварительно гибридизовали в буфере для гибридизации [50% (об. / Об.) Формамида, 6-кратного SSC, 5-кратного раствора Денхардта, 100 мкг / мл ДНК и 0,5% (мас. / Об.) Додецилсульфата натрия] при 37 ° C в течение 45 мин. Тем временем поставить на лед. На каждое предметное стекло наносили 50 мкл гибридизационного буфера, содержащего зонды для FBoV-1, тогда как гибридизационный буфер, содержащий DIG-меченный зонд кошачьего герпесвируса, помещали на каждое предметное стекло отрицательного контроля.Затем предметные стекла переносили в увлажненную камеру и дополнительно инкубировали при 37 ° C в течение ночи. Затем предметные стекла пропитывали серией цитрата стандартного физиологического раствора, включая 2X SSC при pH 7,0–7,4 и 1X SSC при 37 ° C в течение 5 минут каждого и 0,5X SSC при 37 ° C в течение 30 минут. Для блокирования неспецифического связывания все слайды заливали смесью блокирующих растворов, состоящей из 1 мл блокирующего раствора и 9 мл буфера малеиновой кислоты (DIG Wash and Block Buffer Set, Roche, Базель, Швейцария), затем инкубировали при комнатной температуре в течение 60 мин. .Затем предметные стекла промывали 20 мМ трис-буферным физиологическим раствором (TBS) при 37 ° C в течение 5 минут. После неспецифического блокирования 100 мкл Fab-фрагментов анти-DIG-AP (Roche, Базель, Швейцария) (1: 200 в 1X блокирующем растворе) помещали на каждое слайд, и слайды инкубировали во влажной камере в течение 60 мин при комнатной температуре. температуры, затем трижды промывали TBS по 5 мин каждый и помещали в буфер для обнаружения (DIG Wash and Block Buffer Set, Roche, Базель, Швейцария) на 5 мин. Жидкий перманентный красный (LPR) (Dako, Glostrup, Дания) наносили в темной комнате при комнатной температуре в течение 30 мин.Затем предметные стекла контрастировали гематоксилином, дегидратировали и накладывали покровные стекла.
Срезы головного мозга, легких, печени, лимфатических узлов и кишечника от кат. 1 с неродственным зондоспецифическим гликопротеином В при инкубации кошачьего герпесвируса использовали в качестве отрицательного контроля, а ткани мозга, легких и лимфатического узла, полученные от кошки, отрицательной по FBoV-1, служили дополнительными отрицательными контролями.
Окрашивание на FPLV с помощью иммуногистохимии (IHC)
Все ткани FFPE от трех вскрытых кошек подвергали анализу IHC с использованием метода 1.Мышиное моноклональное антитело против парвовируса собак B.450 (Abcam AB59832, Кембридж, Великобритания) в качестве первичного антитела. Вкратце, после депарафинизации и регидратации срезы тканей предварительно обрабатывали 0,1% (мас. / Об.) Трипсином при 37 ° C в течение 25 минут с последующим блокированием активности эндогенной пероксидазы с помощью 5% (мас. / Об.) Обезжиренного молока при 37 ° C в течение 40 минут. мин. После трехкратной промывки PBS срезы инкубировали с первичным антителом (разведение 1: 200) при 4 ° C в течение ночи с последующим обнаружением с использованием системы обнаружения Dako REAL EnVision (Dako, Glostrup, Дания) при комнатной температуре в течение 45 минут.После трехкратного промывания PBS наблюдали положительную реакцию антиген-антитело путем мечения DAB и контрастного окрашивания гематоксилином Майера. FPLV-положительная ткань кишечника от ПЦР-положительной FPLV-инфицированной кошки служила положительным контролем. Образцы, обработанные дистиллированной водой (DW) вместо первичных антител, и образцы, не инфицированные FPLV, служили отрицательными контролями.
Заявление об этике
Все экспериментальные протоколы были одобрены Комитетом по уходу и использованию животных Университета Чулалонгкорн (No.1631002). Все процедуры были выполнены в соответствии с соответствующими инструкциями и правилами. Владельцы кошек дали письменное согласие на сбор проб и публикацию данных.
Признаки и симптомы макроглобулинемии Вальденстрема
Иногда макроглобулинемия Вальденстрема (WM) не вызывает никаких симптомов при первом обнаружении. Вместо этого он обнаруживается, когда у человека сдают анализы крови по какой-либо другой причине. Найденную таким образом WM иногда называют бессимптомной или тлеющей WM.
Когда WM действительно вызывает симптомы, некоторые из них могут быть такими же, как при других типах неходжкинской лимфомы (НХЛ). Например, потеря веса, лихорадка, ночная потливость и увеличение лимфатических узлов наблюдаются при многих типах НХЛ.
Другие симптомы WM вызваны большим количеством аномальных антител IgM (M-белок), вырабатываемых раковыми клетками:
- При синдроме гипервязкости слишком большое количество М-белка в крови может привести к тому, что она станет слишком «густой».(Это не та толщина, которую можно лечить препаратами, известными как разжижители крови.) Когда кровь становится слишком густой, у нее возникают проблемы с перемещением по кровеносным сосудам. Это может вызвать такие проблемы, как плохое кровообращение в головном мозге, что может привести к таким симптомам, как инсульт.
- Если белок M сгущает кровь только в более прохладных частях тела (например, в кончике носа, ушах, пальцах рук и ног), он называется криоглобулином . Криоглобулины могут вызывать боль или другие проблемы в этих областях, если человек подвергается воздействию более низких температур.
- Состояние, называемое амилоидозом , может возникать, когда часть антитела IgM (называемая легкой цепью) накапливается в таких органах, как сердце и почки. Это скопление может привести к проблемам с сердцем и почками.
Не у всех людей с WM развиваются повышенная вязкость, криоглобулины или амилоидоз.
Общие симптомы WM
Слабость: Это один из наиболее частых симптомов WM. Это может быть вызвано анемией (слишком мало эритроцитов), которая может произойти, когда WM-клетки вытесняют нормальные клетки костного мозга.Некоторые люди также чувствуют слабость, когда кровь сгущается из-за накопления аномального белка.
Потеря аппетита: Некоторые люди с WM теряют аппетит.
Лихорадка, пот, потеря веса: WM, как и другие лимфомы, может вызывать лихорадку (без инфекции), сильную ночную потливость и потерю веса (без всяких попыток). Это так называемые симптомы B.
Невропатия: У некоторых людей с WM аномальные антитела могут атаковать и повреждать нервы вне мозга.Это может привести к онемению или болезненному ощущению «иголок» в ступнях и ногах, что называется невропатией.
Менее распространенные признаки и симптомы WM
Увеличенные лимфатические узлы: Обычно они появляются в виде шишек под кожей вокруг шеи, в паху или в подмышечных впадинах. Увеличенные лимфатические узлы обычно составляют 2,5-5 см в диаметре. Они реже встречаются при WM, чем при большинстве других лимфом.
Вздутие живота (живота): WM может иногда увеличивать селезенку или печень, из-за чего живот выглядит опухшим.В верхней части живота печень находится справа, а селезенка — слева. Когда селезенка становится больше, она может давить на желудок, что заставляет людей чувствовать сытость, когда они едят даже небольшое количество.
Симптомы системы кровообращения: При синдроме гипервязкости загустевшая кровь вызывает нарушение мозгового кровообращения, что приводит к таким проблемам, как головная боль, спутанность сознания и головокружение. Он также может вызывать симптомы, подобные тем, которые наблюдаются при инсульте, включая невнятную речь и слабость на одной стороне тела.Пациентам с этими симптомами следует немедленно обратиться к врачу.
Аномальное кровотечение: Высокий уровень аномальных антител может повредить кровеносные сосуды, что может привести к таким проблемам, как кровотечение из носа и кровоточивость десен.
Проблемы со зрением: Кровотечение вокруг мелких кровеносных сосудов внутри глаз или нарушение кровообращения в этих сосудах, вызванное сгущением крови, может привести к нечеткому зрению или слепым пятнам.
Проблемы с почками: Высокий уровень белка М может повредить почки напрямую или в результате развития амилоидоза.Когда почки плохо работают, в крови остается избыток соли, жидкости и продуктов жизнедеятельности организма. Это может вызвать такие симптомы, как слабость, затрудненное дыхание и скопление жидкости в тканях тела.
Проблемы с сердцем: Высокий уровень белка М может повредить ткань сердца напрямую или в результате развития амилоидоза, при котором белок накапливается в сердечной мышце. Это ослабляет сердце, влияя на его способность перекачивать кровь. Кроме того, поскольку кровь людей с WM толще, чем обычно, их сердцам приходится усерднее работать, чтобы перекачивать кровь по всему телу.Это напряжение может истощить сердечную мышцу, что приведет к состоянию, называемому застойной сердечной недостаточностью . Симптомы могут включать учащенное сердцебиение, чувство усталости и слабости, кашель, одышку, быстрое увеличение веса и отеки в ступнях и ногах.
Инфекции: Высокий уровень аномальных антител в WM может замедлить нормальную продукцию антител в организме. Это затрудняет борьбу с инфекциями.
Пищеварительные симптомы: У некоторых людей с WM накопление белка М в кишечнике может привести к таким проблемам, как диарея, плохое всасывание витаминов или желудочно-кишечное кровотечение (проявляющееся кровью в стуле или темным стулом).
Чувствительность к холоду: У людей с криоглобулинами воздействие низких температур может вызвать боль, зуд, синеватый оттенок или даже язвы на кончике носа, ушах, пальцах рук или ног из-за снижения притока крови к ним. области.
Совместное кровообращение множественных заболеваний геморрагической лихорадки с отчетливыми клиническими характеристиками в Даньдуне, Китай
Abstract
Геморрагические лихорадки (HF), вызываемые вирусами и бактериями, являются серьезной проблемой общественного здравоохранения в Китае и характеризуются различными клиническими проявлениями, так что часто бывает трудно достичь точного диагноза и лечения.Причины сердечной недостаточности у 85 пациентов, госпитализированных в больницу Даньдун, Китай, в период с 2011 по 2012 гг., Были определены с помощью серологических тестов и ПЦР. Из них у 34 пациентов была диагностирована геморрагическая лихорадка Хуайяншань (HYSHF), у 34 — геморрагическая лихорадка с почечным синдромом (HFRS), у одного — мышиный тиф и у одного — сыпной тиф. Этиологические агенты не могли быть определены у оставшихся 15 пациентов. Филогенетический анализ восстановленных бактериальных и вирусных последовательностей показал, что возбудители инфекции были тесно связаны с теми, которые описаны в других географических регионах.Поскольку эти заболевания не имеют отличительных клинических признаков на ранней стадии, только 13 пациентам был первоначально поставлен точный диагноз. Отличительные клинические признаки HFRS и HYSHF развивались по мере прогрессирования заболевания. Увеличенные лимфатические узлы, кашель, мокрота и диарея чаще встречались у пациентов с HYSHF, в то время как больше случаев HFRS представляло головную боль, боль в горле, олигурию, перкуторную боль в области почек и петехии. Кроме того, у пациентов с HYSHF наблюдались значительно более низкие уровни лейкоцитов (WBC), более высокие уровни креатинин-киназы (CK) и аланинаминотрансферазы (ALT), в то время как у пациентов с HFRS наблюдалось повышение уровня азота мочевины крови (BUN) и креатинина (CREA). .Эти клинические особенности помогут поставить точный диагноз как HYSHF, так и HFRS. В целом, наши данные показывают сложность патогенов, вызывающих сердечную недостаточность, в одной китайской больнице и подчеркивают необходимость точной ранней диагностики и лучшего понимания их отличительных клинических особенностей.
Образец цитирования: Chen Z-H, Qin X-C, Song R, Shen Y, Chen X-P, Wang W и др. (2014) Совместное кровообращение множественных заболеваний геморрагической лихорадки с отчетливыми клиническими характеристиками в Даньдуне, Китай.PLoS ONE 9 (2): e89896. https://doi.org/10.1371/journal.pone.0089896
Редактор: Дэниел Г. Бауш, Тулейнская школа общественного здравоохранения и тропической медицины, Соединенные Штаты Америки
Поступила: 30 августа 2013 г .; Одобрена: 29 января 2014 г .; Опубликовано: 27 февраля 2014 г.
Авторские права: © 2014 Chen et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Финансирование: Это исследование было поддержано Национальным фондом естественных наук Китая (гранты 812
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Введение
Заболевания, известные под собирательным термином «геморрагическая лихорадка (HF)», являются важными человеческими инфекциями, часто с высокой смертностью и с такими известными примерами, как геморрагическая лихорадка денге, геморрагическая лихорадка Эбола и геморрагическая лихорадка с почечным синдромом (HFRS). Клинически эти заболевания часто характеризуются сильной лихорадкой и коагулопатией. Некоторые HFs демонстрируют четкий набор клинических стадий, например HFRS с отчетливыми почечными симптомами [1]. Этиологические исследования определили несколько вирусов в качестве возбудителей, особенно РНК-вирусы из семейств Arenaviridae , Bunyaviridae , Filoviridae и Flaviviridae [2], [3]. Rickettsiales бактерии, такие как Rickettsia typhi , Orientia tsutsugamushi и Anaplasma phagocytophilums , также могут вызывать HF [4]. Однако клинические проявления и тяжесть приливов значительно различаются: от чрезвычайно высокой смертности при геморрагической лихорадке Эбола до бессимптомных при многих вирусных инфекциях денге [3], а тяжелая лихорадка и коагулопатия также присутствуют при таких заболеваниях, как лептоспироз и малярия. На сегодняшний день нет коммерческих наборов для диагностики большинства HF.Следовательно, трудно точно диагностировать заболевания сердечной недостаточности только на основании клинических проявлений. Как следствие, очевидно, что лучшее понимание клинических характеристик заболеваний сердечной недостаточности, вызываемых различными патогенами, является ключевым моментом в улучшении диагностики и лечения.
Известно, что в Китае несколько патогенов вызывают сердечную недостаточность. Действительно, Китай является одним из наиболее важных эндемичных регионов по ГЛПС (вызываемому хантавирусами) во всем мире: в период 1970–2007 гг. Было зарегистрировано более 1,5 миллиона случаев заболевания и 44 475 смертей [5].Более 10 хантавирусов были идентифицированы у летучих мышей, грызунов и землероек, взятых из Китая [5] — [8]. Случаи ГЛПС в основном вызываются вирусом Хантаан (HTNV) и вирусом Сеула (SEOV), передаваемым грызунами [5]. Недавно было обнаружено, что вирус Gou (GOUV), также переносимый грызунами, вызывает HFRS [9]. ВЧ, вызванные другими вирусами (например, вирусом Крымско-Конго геморрагической лихорадки (CCHFV), вирусом денге) и бактериями (например, Rickettsiales , Leptospira ), также являются эндемичными в Китае [10] — [14]. Однако из-за отсутствия коммерческой специфической диагностики для большинства патогенов HF (особенно бактерий Rickettsiales ), многие случаи HF в Китае диагностируются полностью с использованием клинических критериев и, следовательно, часто диагностируются неправильно.Кроме того, другие HF могут быть вызваны еще нераспознанными патогенами.
В 2009 г. новое заболевание сердечной недостаточности (геморрагическая лихорадка Хуайяншань, HYSHF, также известное как тяжелая лихорадка с синдромом тромбоцитопении) со смертностью 15% было зарегистрировано в районе Хуайяншань Китая [15] — [17]. Заболевание было вызвано новым вирусом (Huaiyangshan virus, HYSV), передаваемым клещами, наиболее близким к вирусам рода Phlebovirus (семейство Bunyaviuridae ) [15].Хотя в нескольких статьях описываются клинические проявления и прогрессирование HYSHF [15] — [19], ни в одном исследовании не сравнивались клинические характеристики HYSHF с таковыми других HF в Китае. Недавно в США было зарегистрировано заболевание с аналогичными симптомами, вызываемое HYSV-подобным вирусом [20]. Лучшее понимание клинического течения HYSHF и других HF может быть полезным для точной диагностики и лечения этих разрушительных заболеваний.
Город Даньдун с населением около 2 453 000 человек (включая городские и сельские районы) расположен в южной части провинции Ляонин, граничащей с Северной Кореей (Рисунок S1).В провинции Ляонин Даньдун серьезно пострадал от HFRS [21], хотя полный спектр HF и вызывающих их вирусов и бактерий, присутствующих в популяции, неизвестен. Чтобы лучше понять HF в Даньдуне, с целью улучшения клинической диагностики и лечения, мы проанализировали 85 пациентов, поступивших в инфекционную больницу Даньдун в 2011–2012 гг., Страдающих тяжелой лихорадкой и / или кровотечением. Исследовались этиологические агенты, клинические проявления, распределение симптомов и терапевтические реакции этих пациентов.Кроме того, мы сравнили различия в клинических характеристиках HYSHF и HFRS и изучили молекулярную эпидемиологию этих патогенов.
Материалы и методы
Заявление об этике
Это исследование было рассмотрено и одобрено комитетами по этике инфекционной больницы Даньдун и больницы Дитан в Пекине. Сбор образцов человеческой сыворотки от пациентов с сердечной недостаточностью был также одобрен этическими комитетами инфекционной больницы Даньдун и больницы Дитан в Пекине в соответствии с правилами медицинских исследований Министерства здравоохранения Китая.Подписанное индивидуальное письменное информированное согласие было получено от каждого из 84 взрослых пациентов при заборе образцов крови. На одного пациента четырехлетнего возраста письменное согласие было предоставлено его родителями.
Определения случаев и клинические данные
Мы набирали пациентов на два года (с января 2011 года по декабрь 2012 года) из инфекционной больницы Даньдун в городе Даньдун, провинция Ляонин, Китай. Пациенты были набраны на основе результатов клинического анализа.
Определение случая включало любого человека любого возраста, госпитализированного с острым началом лихорадки (> 37.5 ° C), тромбоцитопения (<100 × 10 9 / л) и / или геморрагические проявления. Заболевания были первоначально диагностированы в соответствии с национальными клиническими и лабораторными критериями, перечисленными Министерством здравоохранения Китая для HYSHF, HFRS, мышиного тифа, сыпного тифа и других родственных заболеваний (Таблица S1). Как правило, врачи ставили первичный диагноз в соответствии со своим клиническим опытом, когда пациенты попадали в больницу. Они поставили свои клинические диагнозы, сочетая клинические презентации с биохимическими параметрами, и окончательные диагнозы для HFRS на основе лабораторных тестов, когда были доступны соответствующие специфические реагенты.
Лабораторная диагностика была основана на наличии специфических антител иммуноглобулина M (IgM) или четырехкратном увеличении титра антител IgG, или после выделения и характеристики конкретных последовательностей вирусного и бактериального генома (см. Ниже) в Департаменте зоонозов Национальный институт по контролю и профилактике инфекционных заболеваний, Центр контроля заболеваний Китая в Пекине.
Демографические и клинические данные, история приема лекарств / лечения и описание клинического течения, включая время до обращения за медицинской помощью, клинические симптомы, такие как лихорадка, головная боль, миалгия, тошнота, недомогание, кровотечение, легочная и печеночная дисфункция, почечная дисфункция и неврологические заболевания. вовлеченности, были собраны и оценены.
Лабораторные исследования
Во время госпитализации у каждого пациента были взяты образцы крови на 1-й день и при последующем наблюдении во время госпитализации. Подсчет и дифференциация клеток крови обычно проверялась лабораторией клинической диагностики инфекционной больницы Даньдун. Посевы крови на анаэробы и аэробы повторяли трижды для обнаружения бактериальных агентов. Уровни аланинтрансаминазы (ALT), аспартаттрансаминазы (AST), лактатдегидрогеназы (LDH) и креатинфосфатазы (CK) в плазме у отдельных пациентов, тромбиновое время (TT) и другие биохимические параметры были впервые оценены лабораторией клинической диагностики. из инфекционной больницы Даньдун, а затем подтверждено в биохимической лаборатории больницы Дитан в Пекине.
Серологический анализ
Образцы крови, собранные у пациентов с подозрением на ГЛПС, сначала были протестированы в больнице инфекционных болезней Даньдун на предмет антител, специфичных к хантавирусу (HV), с помощью непрямого иммунофлуоресцентного анализа (IFA), как описано ранее [22]. Все сыворотки пациентов были протестированы в отделении зоонозов Национального института по контролю и профилактике инфекционных заболеваний Китайского центра контроля заболеваний в Пекине на предмет специфических антител IgM и IgG против HYSV, HV (включая HTNV и SEOV), R.typhi, R. prowazekii, O. tsutsugamushi, A. phagocytophilum и E . chaffeensis с помощью IFA, как описано ранее [12], [15], [22]. Клетки, инфицированные HYSV, HTNV и SEOV, наносили на предметные стекла, сушили на воздухе и фиксировали ацетоном. Эти слайд-антигены использовали для обнаружения HYSV и HV, тогда как антигены для обнаружения R. typhi, R. prowazekii, O. tsutsugamushi, A. phagocytophilum и E. chaffeensis были приобретены либо у Focus Diagnostics (Cypress, Калифорния, США) или Fuller Laboratories (Фуллертон, Калифорния, США).Для обнаружения бактерий Leptospira были проведены тесты микроскопической агглютинации (MAT) с использованием батареи антисывороток против китайских эталонных штаммов, принадлежащих к 15 сероварам в 15 серогруппах [23].
ПЦР и секвенирование
РНК и ДНКэкстрагировали из всех образцов крови с использованием набора QIAamp MinElute Virus Spin Kit (Qiagen, Валенсия, Калифорния, США). Для выявления HYSV, HV, вируса болезней Кисанурского леса, вируса омской геморрагической лихорадки, вируса крымско-конголезской геморрагической лихорадки вирусная РНК в образцах крови отдельных пациентов выделялась методом обратной транскрипции (ОТ) -ПЦР, как описано ранее [15]. [22], [24] — [26].
ДНКRickettsiale была обнаружена с помощью ПЦР, как описано ранее, с использованием праймеров EHR16SD и rp1588 (5′-ACRGCTACCTTGTTACGACT-3 ‘) для начальной ПЦР и праймеров EHR16SD и 16SR871 (5′-AGCACTCATCGTTTACAGCG-3’ для второго раунда амплификации). [27], [28], в результате чего был получен фрагмент 345 нуклеотидов гена 16S рРНК (16S рДНК) бактерий Rickettsiales . ДНК Leptospira также была обнаружена с помощью ПЦР, как описано ранее [29].
продуктов ПЦР очищали в геле и подвергали секвенированию с помощью анализатора последовательности ДНК 3730 (Applied Biosystems, США).
Филогенетический анализ
Все вирусные и бактериальные последовательности были выровнены и отредактированы с помощью программы ClustalW (DNASTAR, Inc., Мэдисон, Висконсин). Филогенетические деревья оценивались с использованием байесовского метода, реализованного в MrBayes 3.1, и метода максимального правдоподобия (ML), доступного на веб-сервере RAxML Blackbox [30], [31], в рамках наиболее подходящей модели нуклеотида GTR + I + Γ 4 подстановка установлена с помощью jModeltest [32]. Для байесовского анализа мы использовали три горячих и одну холодную цепь Маркова Монте-Карло (MCMC), выборку каждые 100 поколений и 25% сжигания.Эффективный размер выборки (ESS) всех параметров был больше 200, что свидетельствует о сходимости параметров. Топологическая поддержка оценивалась с помощью апостериорных вероятностей узлов для байесовских деревьев и значений поддержки начальной загрузки для деревьев ML соответственно.
В дополнение к последовательностям, полученным в этом исследовании, мы использовали сравнительные вирусные и бактериальные последовательности, полученные из GenBank (www.ncbi.nlm.nih.gov/Genbank) для филогенетических анализов (Таблица S2).
Статистический анализ
Статистический анализ был выполнен с использованием SPSS (версия 16).Сравнение лабораторных параметров HYSHF и HFRS проводилось с использованием критерия хи-квадрат или точного критерия Фишера, при этом значение p <0,05 считалось статистически значимым.
Результаты
Демографические характеристики и клиническая эпидемиология
Демографические характеристики 85 пациентов с сердечной недостаточностью описаны в таблице 1. Примечательно, что случаи HYSHF наблюдались с июля по октябрь, случаи HFRS наблюдались зимой, а неустановленные инфекции наблюдались летом, осенью и зимой (Рисунок S2).Все случаи произошли в сельской местности, и все пациенты были сельскохозяйственными рабочими. Пациенты включали 59 мужчин и 26 женщин в возрасте от 12 до 89 лет (в среднем 54 года).
Лабораторные диагностики и клинические диагнозы
В период с января 2011 года по декабрь 2012 года в инфекционной больнице Даньдун было проведено проспективное обследование 85 пациентов с подозрением на симптомы сердечной недостаточности. Согласно серологическим тестам и генетическому анализу, 34 пациента пострадали от HYSHF, 34 — от HFRS, один — от мышиного сыпного тифа и один — от сыпного тифа, что было первым случаем заболевания человека, зарегистрированным на северо-востоке Китая (Таблица 2).
Хотя только семь случаев HFRS были распознаны по клиническим симптомам на ранней стадии (Таблица 3), 31 случай HFRS (91,18%) был точно диагностирован на момент выписки на основании лабораторных тестов, проведенных в инфекционной больнице Даньдун (в качестве реагентов). для диагностики HTNV и SEOV теперь доступны в Китае). Однако, поскольку диагностические реагенты для агентов HYSV и Rickettsiales не были доступны в инфекционной больнице Даньдун, только шесть (17,6%) случаев HYSHF были точно диагностированы в соответствии с клиническими критериями (Таблица 3), а остальные 28 случаев были ошибочно диагностированы как HFRS или риккетсиоз, или называемые «неустановленными инфекциями».Более того, мышиный сыпной тиф и скрабовый сыпной тиф были ошибочно диагностированы как сепсис и HFRS, соответственно. Четырнадцать из 15 неустановленных инфекций (93,33%), которые не могли быть идентифицированы с помощью лабораторных тестов, были клинически ошибочно диагностированы как HYSHF, HFRS, неспецифическая вирусная инфекция или брюшной тиф.
Филогенетический анализ вирусных и бактериальных последовательностей
Последовательности генома HYSV и HV были успешно амплифицированы из образцов сыворотки крови пациентов. Эти последовательности были обозначены как «последовательности DandongHu» (таблица S2).Кроме того, последовательности 16S рДНК были выделены из O. tsutsugamushi -положительного образца сыворотки. К сожалению, наши попытки амплифицировать последовательности генома других патогенов не увенчались успехом (таблица 2).
Частичные последовательности сегментов S или L были извлечены из 30 образцов сыворотки, собранных у пациентов с HYSHF. Генетический анализ показал, что эти последовательности были очень тесно связаны друг с другом (95,9–100% и 96,8–100% идентичности последовательностей в частичных последовательностях сегментов S и L соответственно), а некоторые были тесно связаны с последовательностями, полученными от людей, находящихся в Горный район Хуайяншань Китая в 2010 г. (94.2–99,5% и 96,0–99,5%) [15], [33]. Действительно, в филогенном дереве S последовательности из Даньдуна были разделены на три линии, которые сгруппировались с последовательностями, полученными от людей и клещей в других частях Китая (рисунки 1a и 1b) [15], [17], [18], [ 33].
Рис. 1. Филогенетические отношения между вирусом Хуайяншань (HYSV) и вариантами хантавируса, обнаруженными у людей в Китае и за его пределами.
Байесовские деревья были выведены с использованием (a) частичных последовательностей S и (b) частичных L-сегментов HYSV, (c) частичных S и (d) частичных M последовательностей HV и (e) гена ДНК 16S Риккетсиал .Цифры над или под ветвями указывают вероятности апостериорных узлов и значения поддержки начальной загрузки. Вероятность заднего узла выше 0,7 или значение бутстрапа 70% считались сильной поддержкой для конкретного узла. Синий цвет представляет последовательности HYSV, HV или O. tsutsugamushi , выделенные из человеческих образцов, собранных в Даньдуне. Масштабные полосы указывают количество нуклеотидных замен на сайт. Для получения более подробной информации о вирусах и бактериях, использованных в этом исследовании, см. Таблицу S2.
https://doi.org/10.1371/journal.pone.0089896.g001
Полные (или частичные) последовательности сегментов S или M были амплифицированы из 24 образцов сыворотки от пациентов с HFRS. Интересно, что большинство этих последовательностей были очень тесно связаны друг с другом, с 93,6–100% идентичностей в сегменте S и 96,7-99,5% идентичностей в сегменте M, и образовывали монофилетическую группу на филогенетических деревьях (рисунки 1c и 1d). . Эти последовательности также были тесно связаны с последовательностями (YaluRiver13, HQ611981), полученными из A.agrarius отобран в соседнем районе Даньдун. Кроме того, последовательности (Dandong-Hu-92) сформировали другую группу в деревьях S и M и имели тесную связь с последовательностями (CGHu1), выделенными от пациента с HFRS (34) и от мышей Apodemus (Bao14, CJAp93 ) (35, 36). Кроме того, все эти последовательности были расположены близко к последовательностям, полученным от человека и мышей Apodemus из Северо-Восточного Китая и Дальнего Востока Азии (86,8–96,6 и 87,3–95% идентичности) [34] — [38], некоторые из которых ( Ходжо, Ли, Мааджи-2) были связаны с тяжелыми случаями ГЛПС [1].
Наконец, последовательности 16S рДНК, полученные от одного пациента с сыпным тифом в этом исследовании, были тесно связаны с соответствующими последовательностями штаммов, обнаруженных как внутри, так и за пределами Китая, с 97–100% идентичностью нуклеотидов (рис. 1e) [39], [39]. 40].
Клинические характеристики HYSHF, HFRS и инфекций, вызванных неизвестным агентом (ами)
Заболевание началось внезапно с высокой температуры, головной боли и миалгии, тошноты, рвоты и диареи, а также множества других неспецифических признаков и симптомов (Таблица 4).Однако в течение нескольких дней у некоторых пациентов наблюдались дефекты коагуляции и легкие геморрагические симптомы, такие как кожная сыпь, петехии и гематурия. Примечательно, что увеличенные лимфатические узлы наблюдались только в случаях HYSHF (44,12%).
Две трети пациентов с ГЛПС имели геморрагические проявления. Хотя количество пациентов с HYSHF с проявлениями кровотечения было относительно низким (Таблица 4), обширная пурпура в руке (Рисунок 2a) и ягодице (Рисунок 2b) или кровотечение из желудочно-кишечного тракта наблюдались только у пациентов с HYSHF.У большего количества пациентов с HYSHF наблюдались кашель, мокрота, диарея и увеличение лимфатических узлов (p <0,05 или p <0,001), в то время как у большего числа пациентов с HFRS наблюдались головная боль, боль в горле, болезненность почечного угла и олигурия (p <0,05 или p <0,001). Кроме того, синдромы нервной системы встречались у пациентов с HYSHF, но не у пациентов с HFRS.
На ранней стадии (2-3 дня) от начала у большинства пациентов наблюдались значительные изменения в количестве клеток крови (таблица 5). Примечательно, что количество лейкоцитов (WBC), включая нейтрофилы, лимфоциты, моноциты и эозинофилы, резко снизилось у большинства пациентов с HYSHF.Однако количество лейкоцитов, включая моноциты, увеличилось у большинства пациентов с HFRS, тогда как количество лейкоцитов и лимфоцитов уменьшилось почти в половине неизвестных инфекций. У большинства пациентов с HYSHF наблюдалось большее повышение уровня КФК. Высокие уровни АЛТ, АСТ, ЛДГ и ГБДГ наблюдались в большинстве случаев HYSHF, HFRS и неизвестных инфекций, но более высокая доля пациентов с HYSHF демонстрировала повышенные уровни АЛТ, TBA и ADA, чем пациенты с HFRS (Таблица 5). Тромбоцитопения встречалась в большинстве случаев HYSV, HV и неизвестных инфекций. Длительный TT также наблюдался у большинства пациентов с HYSHF и более чем у половины пациентов с HFRS.В соответствии с нарушением функции почек у большинства пациентов с ГЛПС отмечалось повышение уровня азота мочевины в крови (АМК) и креатинина.
Изменения температуры, лейкоцитов и биохимических показателей
Чтобы лучше понять клиническое течение приливов, мы дополнительно сравнили изменения температуры, клеток крови и биохимических параметров во время прогрессирования (с 1 по 15 день во время госпитализации) (рис. 3). За период наблюдения обе относительно высокие температуры (0.25–0,96 ° C) и более длительная высокая температура наблюдалась у пациентов с HYSHF по сравнению с пациентами с HFRS (Рисунок 3, Таблица S3). Уровни лейкоцитов у пациентов с HYSHF резко снизились в течение 3-5 дней после начала заболевания (рис. 3), в то время как уровни лейкоцитов у пациентов с HFRS значительно повысились по сравнению с нормальным уровнем в течение 3-5 дней. Примечательно, что уровни лейкоцитов были нормальными в пациенты с неустановленными инфекциями в этот период. Для HFRS и неустановленной инфекции (инфекций) количество тромбоцитов было ниже нормального в течение 2–9 дней и даже до 11 дня для пациентов с HYSHF.
Рис. 3. Динамические профили температуры, количества лейкоцитов (WBC) и тромбоцитов (PLT) у пациентов с HYSHF (красная линия), HFRS (зеленая линия) или неопределенными инфекциями (синяя линия).
Более подробная информация представлена в таблице S3.
https://doi.org/10.1371/journal.pone.0089896.g003
Мы также проанализировали изменения биохимических параметров для HYSHF, HFRS и неопределенных инфекций (Рисунок 4). Повышение уровней ALT, AST и GGT, которые являются основным показателем поражения печени, наблюдались при HYSHF, HFRS и инфекциях неустановленной причины.Примечательно, что повышение (особенно AST) было больше у пациентов с HYSHF, чем у пациентов с HFRS в течение 5–14 дней, что позволяет предположить, что повреждение печени может быть более серьезным при HYSHF, чем при HFRS. Хотя высокие уровни LDH, CK и HBDH были обнаружены у пациентов с HFRS и с инфекциями неустановленной этиологии, резкое увеличение наблюдалось у пациентов с HYSHF во время прогрессирования заболевания (Рисунок 4, Таблица S4). В соответствии с поражением почек у пациентов с HFRS, уровни BUN и CREA были значительно выше, чем обычно, в течение 3-15 дней у пациентов с HFRS (рис. 4).Инфекции неизвестной этиологии также показали более высокий уровень BUN и CREA в течение 6-11 дней после начала.
Рис. 4. Изменения аланинаминотрансферазы (ALT), аспартатаминотрансферазы (AST), гамма-глутамилтрансферазы (GGT), креатинкиназы (CK), лактатдегидрогеназы (LDH), гидроксигутиратдегидрогеназы (HBDH), азота мочевины крови. и уровни креатинина (CREA) у пациентов с HYSHF, HFRS и неустановленными инфекциями.
Цветовая кодировка такая же, как на рисунке 3.Более подробная информация представлена в таблице S4.
https://doi.org/10.1371/journal.pone.0089896.g004
Лечение и исходы
Было реализовано несколько стратегий лечения пациентов с подозрением на сердечную недостаточность. Во-первых, поскольку большинство пациентов находились в критическом состоянии из-за потери крови и биологических жидкостей, всем пациентам была назначена поддерживающая терапия (включая обеспечение электролитами и глюкозой) для поддержания правильного баланса биологических жидкостей и электролитов, а также для поддержания функций организма. .Во-вторых, поскольку рибавирин в настоящее время рекомендуется для профилактики и лечения вирусных заболеваний, таких как HFRS, CCHF, лихорадка Ласса [2], всем пациентам с HFRS, диагностированным врачами инфекционной больницы Даньдун (всего 23, или 67,6% от общего числа лабораторно подтвержденных) 34 случая) лечили внутривенным введением 0,6 г рибавирина один раз в день. Шесть пациентов с подозрением на HYSHF и девять с подозрением на другие вирусные инфекции также получали препарат. В-третьих, антибиотики, такие как доксициклин, использовались для лечения тех пациентов, которым изначально был поставлен диагноз риккетсиоз, и для предотвращения вторичных бактериальных инфекций, поскольку у некоторых пациентов развивалась нейтропения и лимфопения.Наконец, при необходимости применялись антибиотики широкого спектра действия, гранулоцитарный колониестимулирующий фактор (G-CSF) и другие поддерживающие меры. Несмотря на все эти меры, пять пациентов умерли; два от HYSHF, два от HFRS и один от еще не установленной инфекции. При поступлении у всех этих пяти пациентов были клинически диагностированы неустановленные инфекции. Примечательно, что из этих пяти смертей два пациента с HFRS и один с HYSHF не получили внутривенное введение рибавирина.
Обсуждение
Геморрагические лихорадки представляют собой разнообразную группу серьезных заболеваний человека, вызываемых РНК-вирусами и различными бактериями Rickettsiales [2] — [4].В этом исследовании мы наблюдали инфекции HYSV, HV, R. typhi и O. tsutsugamushi в городе Даньдун, провинция Ляонин, северный Китай. Интересно, что этиологический агент не удалось идентифицировать у 15 пациентов с сердечной недостаточностью. Следовательно, эти данные раскрывают сложность патогенов, вызывающих HF, а также предполагают возможное присутствие неизвестных патогенов человека в этом географическом регионе. Таким образом, очевидно, что необходимы дополнительные исследования для создания соответствующих диагностических тестов.
В настоящее время нет коммерческих наборов для диагностики HF, а специфическая диагностика доступна только в специализированных лабораториях [2]. Почти во всех больницах Китая отсутствуют специфические реагенты для диагностики HF, за исключением HFRS, что, несомненно, способствует высокому количеству ошибочных диагнозов, наблюдаемых здесь. Более того, отсутствие отчетливых клинических признаков и симптомов на ранней стадии заболевания увеличивает вероятность ошибочного диагноза даже при ГЛПС [41]. Кроме того, могут существовать более легкие или бессимптомные случаи, которые могут быть пропущены дозорным эпиднадзором.Таким образом, истинное количество случаев HYSHF может быть в несколько раз выше, чем зарегистрированное. Таким образом, наши данные подчеркивают острую потребность в диагностических реагентах, в то время как лучшее понимание клинических особенностей каждого заболевания при сердечной недостаточности также может улучшить их диагностику.
Мы сравнили эпидемиологические характеристики возникающих HYSHF с HFRS в той же популяции, используя соответствующий набор, лабораторную диагностику и последующее наблюдение. В соответствии с ранними сообщениями [15], все случаи HYSHF произошли с июня по сентябрь, в то время как все случаи HYSHF, вызванные HTNV, регистрировались зимой, как и в предыдущих отчетах [9], [42].Эти данные предполагают, что поведение человека летом, вероятно, увеличивает риск заражения клещами [33], в то время как холодные условия зимой увеличивают заражение домов грызунами [42]. Следовательно, сезонность заболевания может дать некоторые полезные указания для постановки диагноза. Из-за благоприятных экологических условий и низкого социально-экономического статуса в сельской местности фермеры часто становились основными жертвами зоонозов, включая ГЛПС, кустарниковый тиф и лептоспироз [5], [9], [10], [14], [43]. Таким образом, наши данные убедительно подтверждают необходимость бдительности для предотвращения распространения HV, HYSV от животных в сельских районах Китая.
Как и другие хантавирусы (например, PUUV) [44], [45], HTNV демонстрирует высокое генетическое разнообразие с присутствием по крайней мере девяти линий [34]. Кроме того, он показывает заметную географическую кластеризацию генетических вариантов, особенно в горных регионах [34]. В этом исследовании последовательности сегментов S и M, полученные от 24 пациентов с HFRS, были разделены на две группы и имели тесную филогенетическую связь с вирусами, полученными от пациентов с HFRS и мышей Apodemus из Дальневосточной Азии [1], [34] — [40], что указывает на то, что человеческая инфекция связана с распространением HTNV.Хотя последовательности HYSV, полученные в этом исследовании, были очень тесно связаны друг с другом, их можно разделить на три линии в деревьях S и L (рис. 1ab) [33], что свидетельствует об относительно высоком генетическом разнообразии HYSV в Даньдуне. Интересно, что эти последовательности также имели тесную связь с последовательностями, полученными от клещей и людей, взятых из провинций Аньхой, Хубэй, Цзянсу и Шаньдун, с отсутствием географической структуры, которая может отражать недавнее появление и распространение этого вируса.
Тяжесть и клинические проявления вирусных заболеваний сердечной недостаточности были связаны с задействованными этиологическими агентами [3]. Среди известных этиологических агентов HFRS, HTNV и вирус Добрава-Белграда (DOBV) могут вызывать тяжелую форму HFRS с уровнем летальности до 15% [5], [41], [43], [45], в то время как SEOV обычно вызывает более легкую форму HFRS с уровнем смертности около 1% [5], [41]. Напротив, PUUV вызывает только легкое заболевание, известное как эпидемическая нефропатия (NE), с уровнем смертности <0.3% в Европе [43], [46]. Серологические тесты и ПЦР показали, что из вирусов, вызывающих HFRS в Dandong, почти все принадлежали к HTNV, за исключением одного пациента, инфицированного SEOV, и клинические проявления были аналогичны таковым для HFRS, вызванного HTNV, как описано ранее [1], с двумя пациенты умирают. Филогенетический анализ вирусных последовательностей показал, что варианты HTNV, описанные в этом исследовании, были тесно связаны с вариантами (CGHu1, Hojo, Lee, Maaji-2), вызывающими тяжелую HFRS в Китае и других частях Дальневосточной Азии [1], [34].Очевидно, что необходимы дополнительные усилия для предотвращения тяжелой формы HFRS, вызванной HTNV, в этом регионе Китая.
Подобно HFRS и другим вирусным заболеваниям HF [1], [3], начало HYSHF характеризуется недомоганием, анорексией, ознобом, головной болью, миалгиями и лихорадкой [15], [16]. Через несколько дней после начала у пациентов развиваются конституциональные, желудочно-кишечные, сердечно-сосудистые и неврологические признаки и симптомы. Мы сравнили клинические признаки и биохимические показатели, а также их динамику у пациентов с HYSHF и HFRS.Очевидно, что температура у пациентов с HYSHF была относительно выше и оставалась высокой дольше, чем у пациентов с HFRS. Более серьезные кровотечения также наблюдались у пациентов с HYSHF, но не у пациентов с HFRS. Кроме того, пациенты с HYSHF имели более серьезное повреждение печени, чем HFRS, что проявлялось в резком повышении ALT. Эксперименты с использованием животных моделей выявили более крупные некротические области и большую инфильтрацию мононуклеарных клеток в печени мышей, инфицированных HYSV, чем мышей, инфицированных HTNV [47].В целом, эти данные подтверждают определение «Хуайяншаньская геморрагическая лихорадка» для нового заболевания с высокой лихорадкой и геморрагическими проявлениями, о котором впервые было сообщено в регионе Хуайяншань Китая [15] и которое клинически сопоставимо с HFRS.
В настоящее время лечение вирусной сердечной недостаточности, включая HYSHF, включает использование специфических противовирусных препаратов и общих поддерживающих мер [2], [19], [48]. В этом исследовании все пациенты с подозрением на вирусную сердечную недостаточность (38 случаев) получали поддерживающую терапию при необходимости и лечились рибавирином внутривенно.Кроме того, антибиотики, включая доксициклин, использовались для предотвращения вторичных бактериальных инфекций. Несмотря на эти меры, два пациента с HYSHF и два пациента с HFRS умерли. Таким образом, существует острая необходимость в разработке эффективных клинических протоколов для пациентов с HF вирусного происхождения, особенно для HFRS и HYSHF в Китае.
В заключение, HYSV и HV распространены у людей в Даньдуне. Сообщалось также о сыпном и кустарниковом сыпном тифе. Важно отметить, что этиологические агенты HF не могут быть определены во всех случаях.Таким образом, эти данные подчеркивают сложность патогенов, вызывающих сердечную недостаточность у человека. Более того, большинство клинических симптомов HYSHF были сравнимы с таковыми при HFRS, а их отличительные клинические признаки не развивались до более позднего прогрессирования заболевания.
Вклад авторов
Задумал и спроектировал эксперименты: YZZ ZHC. Проведены эксперименты: XCQ XPC WW JSZ JRH MHL. Проанализированы данные: YZZ RS XCQ WW JX XWL AP. Предоставленные реагенты / материалы / инструменты для анализа: ZHC RS YS YXZ XHZ DWL XKF DT.Написал бумагу: YZZ AP ECH.
Список литературы
- 1. Lee JS, Lähdevirta J, Koster F, Levy H (1999) Клинические проявления и лечение HFRS и HPS. В: Руководство по геморрагической лихорадке с почечным синдромом и хантавирусным легочным синдромом. Сеул: Сотрудничающий центр ВОЗ по справочным материалам и исследованиям вирусов (хантавирусы), Институт наук о жизни Асан.
- 2. Ипполито Дж., Фельдманн Х., Ланини С., Вайро Ф., Ди Каро А. и др. (2012) Вирусные геморрагические лихорадки: повышение уровня лечения.BMC Med 10: 31.
- 3. Паесслер С., Уокер Д.Х. (2013) Патогенез вирусных геморрагических лихорадок. Анну Рев Патол 8: 411–440.
- 4. Рауль Д., Парола П. (2007) Риккетсиозные болезни. Нью-Йорк: Informa Healthcare USA, Inc.
- 5. Zhang YZ, Zou Y, Fu ZF, Plyusnin A (2010) Хантавирусные инфекции у людей и животных, Китай. Emerg Infect Dis 16: 1195–1203.
- 6. Guo WP, Lin XD, Wang W, Zhang XH, Chen Y и др. (2011) Новый подтип вируса Thottapalayam, переносимый азиатской домашней бурозубкой ( Suncus murinus ) в Китае.Infect Genet Evol 11: 1862–1867.
- 7. Lin XD, Wang W, Guo WP, Zhang XH, Xing JG и др. (2012) Межвидовая передача в видообразовании известных в настоящее время хантавирусов, ассоциированных с муринами. J Virol 86: 11171–11182.
- 8. Guo WP, Lin XD, Wang W, Tian JH, Cong ML и др. (2013) Филогения и происхождение хантавирусов, обитающих у летучих мышей, насекомоядных и грызунов. PLoS Pathog 9: e1003159.
- 9. Wang W, Wang MR, Lin XD, Guo WP, Li MH и др.(2013) Продолжающееся распространение хантавирусов Hantaan и Gou от грызунов связано с геморрагической лихорадкой с почечным синдромом (HFRS) в Китае. PLoS Negl Trop Dis 7: e2484.
- 10. Fan MY, Walker DH, Yu SR, Liu QH (1987) Эпидемиология и экология риккетсиозных заболеваний в Китайской Народной Республике. Rev Infect Dis 9: 823–840.
- 11. Дай Х, Мухтар, Фен Ч., Сан С.Р., Тай ХР и др. (2006) География и распространение Крымско-Конго геморрагической лихорадки в Таримском бассейне.Чжунхуа Лю Син Бин Сюэ За Чжи 27: 1048–1052.
- 12. Zhang L, Liu Y, Ni D, Li Q, Yu Y и др. (2008) Нозокомиальная передача гранулоцитарного анаплазмоза человека в Китае. JAMA 300: 2263–2270.
- 13. Гао X, Nasci R, Liang G (2010) Забытые арбовирусные инфекции в материковом Китае. PLoS Negl Trop Dis 4: e624.
- 14. Zhang C, Wang H, Yan J (2012) Распространенность лептоспироза в китайском населении за последние два десятилетия. Микробы заражают 14: 317–323.
- 15. Zhang YZ, Zhou DJ, Xiong Y, Chen XP, He YW и др. (2011) Геморрагическая лихорадка, вызванная новым клещевым вирусом Bunyavirus в Хуайяншане, Китай. Чжунхуа Лю Син Бин Сюэ За Чжи 32: 209–220.
- 16. Ю XJ, Liang MF, Zhang SY, Liu Y, Li JD и др. (2011) Лихорадка с тромбоцитопенией, связанная с новым буньявирусом в Китае. N Engl J Med 364: 1523–1532.
- 17. Zhang YZ, He YW, Dai YA, Xiong Y, Zheng H и др. (2012) Геморрагическая лихорадка, вызванная новым буньявирусом в Китае: патогенез и корреляты летального исхода.Clin Infect Dis 54: 527–533.
- 18. Сюй Б, Лю Л., Хуанг Х, Ма Х, Чжан И и др. (2011) Метагеномный анализ синдрома лихорадки, тромбоцитопении и лейкопении (FTLS) в провинции Хэнань, Китай: открытие нового буньявируса. PLoS Pathog 7 (11): e1002369.
- 19. Gai ZT, Zhang Y, Liang MF, Jin C, Zhang S и др. (2012) Клинический прогресс и факторы риска смерти у пациентов с тяжелой лихорадкой и синдромом тромбоцитопении. J Infect Dis 206: 1095–1102.
- 20.Макмаллан Л.К., Фолк С.М., Келли А.Дж., Макнил А., Голдсмит С.С. и др. (2012) Новый флебовирус, связанный с тяжелым лихорадочным заболеванием в Миссури. N Engl J Med 367: 834–841.
- 21. Wu W, Guo J, Guan P, Sun Y, Zhou B (2011) Кластеры пространственного, временного и пространственно-временного распределения геморрагической лихорадки с почечным синдромом в провинции Ляонин, Северо-Восточный Китай. BMC Infect Dis 11: 229.
- 22. Чжан Ю.З., Донг Х, Ли Х, Ма Ц., Сюн Х.П. и др. (2009) Сеульский вирус и хантавирусная болезнь, Шэньян, Китайская Народная Республика.Emerg Infect Dis 15: 200–206.
- 23. Zhang YZ, Nie YX, Li XW, Zhang Y, Dai FL и др. (2006) Стандартизация MAT для выявления антител к лептоспирозу и международное тестирование достоверности результатов MAT. Эпиднадзор за заболеваниями 21: 229–231.
- 24. Zou Y, Hu J, Wang ZX, Wang DM, Yu C и др. (2008) Генетическая характеристика хантавирусов, выделенных из Гуйчжоу, Китай: доказательства распространения и реассортации в природе. J Med Virol 80: 1033–1041.
- 25. Maher-Sturgess SL, Forrester NL, Wayper PJ, Gould EA, Hall RA и др. (2008) Универсальные праймеры, амплифицирующие РНК всех трех подгрупп флавивирусов. Вирол J 5: 16.
- 26. Burt FJ, Leman PA, Smith JF, Swanepoel R (1998) Использование обратной транскрипционно-полимеразной цепной реакции для обнаружения вирусной нуклеиновой кислоты в диагностике крымско-конголезской геморрагической лихорадки. Дж. Вирол Методы 70: 129–137.
- 27. Parola P, Roux V, Camicas JL, Baradji I., Brouqui P, et al.(2000) Обнаружение эрлихий у африканских клещей с помощью полимеразной цепной реакции. Trans R Soc Trop Med Hyg 94: 707–708.
- 28. Weisburg WG, Barns SM, Pelletier DA, Lane DL (1991) амплификация 16S рибосомной ДНК для филогенетического исследования. J Bacteriol 173: 697–703.
- 29. Zhang CC, Li XW, Cui ZG, Jiang XG (2009) Применение анализа тандемных повторов с переменным числом множественных локусов (MLVA) для молекулярного типирования lcterohaemorrhagiae серогруппы Leptospira interrogans.Chin J Microbiol Immunol 13: 1144–1147.
- 30. Ronquist F, Huelsenbeck JP (2003) MrBayes 3: байесовский филогенетический вывод в смешанных моделях. Биоинформатика 19: 1572–1574.
- 31. Стаматакис А., Гувер П., Ружмонт Дж. (2008) Алгоритм быстрой загрузки для веб-серверов RAxML. Syst Biol 57: 758–771.
- 32. Посада Д. (2008) jModelTest: усреднение филогенетической модели. Mol Biol Evol 25: 1253–1256.
- 33. Zhang YZ, Zhou DJ, Qin XC, Tian JH, Xiong Y и др.(2012) Экология, генетическое разнообразие и филогения вируса Хуайяншань в Китае. J Virol 86: 2864–2868.
- 34. Zou Y, Hu J, Wang ZX, Wang DM, Li MH и др. (2008) Молекулярное разнообразие и филогения вируса Хантаан в Гуйчжоу, Китай: свидетельства того, что Гуйчжоу является радиационным центром нынешнего вируса Хантаан. J Gen Virol 89: 1987–1997.
- 35. Ван Х., Йошимацу К., Эбихара Х., Огино М., Араки К. и др. (2000) Генетическое разнообразие хантавирусов, выделенных в Китае, и характеристика новых хантавирусов, выделенных из Niviventer confucianus и Rattus rattus .Вирусология 278: 332–345.
- 36. Zhang YZ, Zou Y, Yao LS, Hu GW, Du ZS и др. (2007) Выделение и характеристика хантавируса, переносимого Apodemus peninsulae в Цзилине, Китай. J Gen Virol 88: 1295–1301.
- 37. Карива Х., Йошикава К., Таникава Й., Сето Т., Санада Т. и др. (2012) Выделение и характеристика хантавирусов на Дальнем Востоке России и этиология геморрагической лихорадки с почечным синдромом в этом регионе. Am J Trop Med Hyg 86: 545–553.
- 38. Lee HW, Lee PW, Johnson KM (1978) Выделение этиологического агента корейской геморрагической лихорадки. J Infect Dis 137: 298–308.
- 39. Kelly DJ, Fuerst PA, Ching WM, Richards AL (2009) Скраб-сыпной тиф: географическое распределение фенотипических и генотипических вариантов Orientia tsutsugamushi . Clin Infect Dis 48: S203–330.
- 40. Охаши Н., Фукухара М., Шимада М., Тамура А. (1995) Филогенетическое положение Rickettsia tsutsugamushi и взаимосвязь между его антигенными вариантами путем анализа последовательностей гена 16S рРНК.FEMS Microbiol Lett 125: 299–304.
- 41. Zhang X, Chen HY, Zhu LY, Zeng LL, Wang F и др. (2011) Сравнение вирусных инфекций Хантаана и Сеула среди пациентов с геморрагической лихорадкой с почечным синдромом (HFRS) в Хэйлунцзяне, Китай. Scand J Infect Dis 43: 632–641.
- 42. Chen HX, Qiu FX, Dong BJ, Ji SZ, Li YT и др. (1986) Эпидемиологические исследования геморрагической лихорадки с почечным синдромом в Китае. J Infect Dis 154: 394–398.
- 43. Вапалахти О, Мустонен Дж., Лундквист А., Хенттонен Х., Плюснин А. и др.(2003) Хантавирусные инфекции в Европе. Lancet Infect Dis 3: 653–361.
- 44. Сиронен Т., Вахери А., Плюснин А. (2001) Молекулярная эволюция хантавируса Пуумала. J Virol 75: 11803–11810.
- 45. Jonsson CB, Figueiredo LT, Vapalahti O (2010) Глобальный взгляд на экологию, эпидемиологию и болезни хантавирусов. Clin Microbiol Rev 23: 412–441.
- 46. Hjertqvist M, Klein SL, Ahlm C, Klingstrom J (2010) Характер смертности от геморрагической лихорадки с почечным синдромом, вызванным вирусом Пуумала.

