Диета при дисбактериозе. Бифилакт БИОТА
Другие статьи из рубрики «Болезни пищеварительной системы»:
Дисбактериоз: понятие, виды, тактика лечения. Бифилакт БИОТА
Хронический дисбактериоз кишечника, признаки и симптомы. Бифилакт БИОТА
Хронический дисбактериоз, от чего возникает, симптомы и причины. Бифилакт биота
Диета во время дисбактериоза, продукты для взрослых и детей. Бифилакт БИОТА
Повышение температуры во время дисбактериоза. Бифилакт БИОТА
Сыпь при дисбактериозе: причины и симптомы у детей и взрослых. Бифилакт БИОТА
Основные причины развития дисбактериоза. Бифилакт БИОТА
Перечень лекарств от дисбактериоза. Бифилакт БИОТА
Возникновение дисбактериоза после антибиотиков. Бифилакт БИОТА
Диета при дисбактериозе. Бифилакт БИОТА
Какой врач лечит дисбактериоз кишечника: симптомы, причины заболевания. Бифилакт БИОТА
Грибковое поражение пищеварительной системы
Запор и его лечение, причины, профилактика.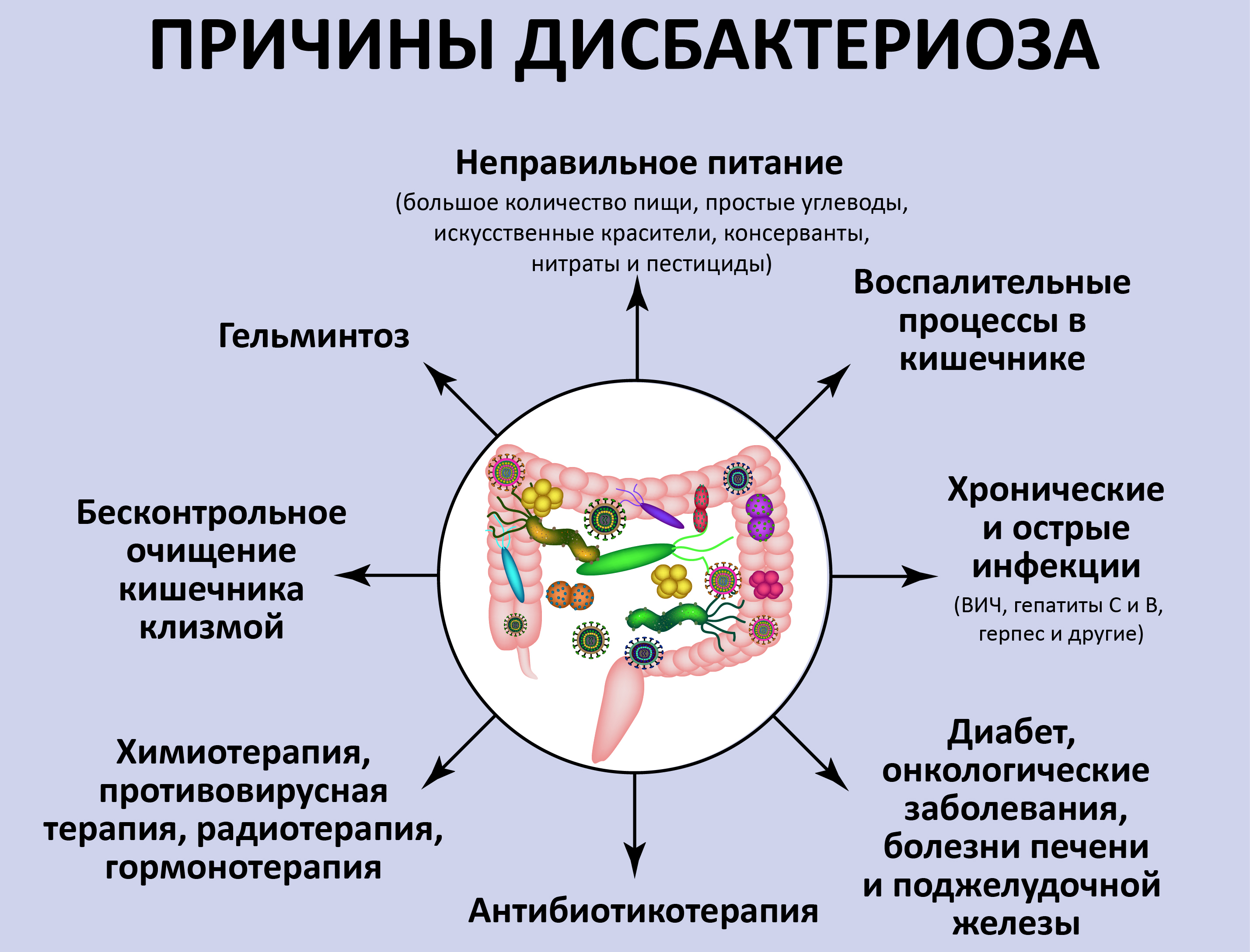
Средства от запора. Таблетки, прибиотики, слабительные. Бифилакт БИОТА
Эффективные домашние средства от запора. Бифилакт БИОТА
Что есть во время запора. Бифилакт БИОТА
Запор у пожилых, основные причины, терапия. Бифилакт БИОТА
Запор у взрослого человека, причины возникновения и лечение. Бифилакт БИОТА
Что делать при возникновении запора. Несколько действенных советов. Бифилакт БИОТА
Как в домашних условиях делать клизму, во время запора. Бифилакт БИОТА
Лактазная недостаточность. Бифилакт БИОТА
Вздутие кишечника: лечение вздутия кишечника. Бифилакт БИОТА
Причины вздутия живота и появления запора. Бифилакт БИОТА
Бифилакт БИОТА для лечения печени
Бифилакт БИОТА для лечения желудка
Синдром раздраженного кишечника. Бифилакт БИОТА
Колит: симптомы и лечение. Бифилакт БИОТА
Энтероколит: симптомы и лечение энттороколита. Бифилакт БИОТА
Бифилакт БИОТА для лечения кишечника
Микрофлоракишечника является системой, которая включает в себя слизистые оболочки пищеварительного тракта, бактерии, вирусы, грибы и частицы пищи, играющие одну из важных ролей в пищеварении. Микрофлора помогает кишечнику расщепить пищу, подвергшуюся обработке пищеварительным соком, учувствует в обмене желчных кислот и расщеплении клетчатки, образует аминокислоты и витамины, отвечает за всасывание полезных веществ и витаминов. При нарушение баланса полезных и болезнетворных бактерий развивается дисбактериоз, требующийлечения. По причине того, что дисбактериоз не имеет ярко выраженной клинической картины, диагностирование болезни на ранней стадии является затруднительным. После определения причины возникновения дисбиоза в первую очередь врач назначает лечение в виде диеты.
Микрофлора помогает кишечнику расщепить пищу, подвергшуюся обработке пищеварительным соком, учувствует в обмене желчных кислот и расщеплении клетчатки, образует аминокислоты и витамины, отвечает за всасывание полезных веществ и витаминов. При нарушение баланса полезных и болезнетворных бактерий развивается дисбактериоз, требующийлечения. По причине того, что дисбактериоз не имеет ярко выраженной клинической картины, диагностирование болезни на ранней стадии является затруднительным. После определения причины возникновения дисбиоза в первую очередь врач назначает лечение в виде диеты.
Диета при дисбактериозе
Диета при дисбактериозе кишечника основывается на питании, показанном при болезнях, являющиеся причиной нарушения микрофлорыкишечника. Если заболевание спровоцировано приемом антибактериальных препаратов, слабительных или гормональных средств, то необходимо их исключить. Чаще всего дисбактериоз кишечникаразвивается через несколько дней после начала лечения антибиотиками.
Питание при дисбактериозедолжно быть полноценным по калорийности и содержанию полезных веществ. Одновременно диета требует исключения и ограничения употребления некоторых продуктов, негативно влияющих на микрофлору – газированные напитки, шоколад, фрукты и овощи, консервированные продукты, сгущенка, жирные сорта мяса, макароны и вермишель из нетвердых сортов, мясные и рыбные консервы.
В диету должны быть включены пребиотические продукты, помогающие стимулировать выработку полезных бактерий и угнетать патогенные, к ним относятся некоторые сорта фруктов и овощей (желательно термически обработанные), пшеничные изделия, натуральные соки и морсы.
Лечение дисбактериоза диетой
Питание при дисбактериозе должно быть сбалансированным, требуется убрать продукты, способные вызвать газообразование в кишечнике, питаться необходимо дробно не менее 5 раз в день.
исключить продукты, включающие красители и консерванты;
исключить газированные и спиртные напитки, кофе;
исключить фаст-фуд и полуфабрикаты;
включить в диету продукты, содержащие бифидо- и лактобактерии: бифидок, кефир, айран;
в качестве обработки продуктов использовать отваривание и тушение;
не запивать пищу чаем или водой, должно пройти не менее получаса;
убрать из рациона кондитерские изделия и сахар;
при вздутии живота и метеоризме убрать продукты, способствующие брожению;
исключить острую и жирную пищу, негативно сказывающуюся на моторике кишечника и усугубляющие процесс размножения вредных микроорганизмов.

Во время лечения диетой при дисбактериозе кишечника продукты должны проходить термическую обработку, в сыром виде разрешено употреблять только огурцы. Желательно продукты тушить или готовить на пару. Основой лечения диетой должнабыть слизистая и пресная пища. В период облегчения состояния разрешено готовить еду с добавлением небольшого количества соли.
Причины развития дисбактериоза
На сегодняшний день до сих пор не выявлены точные причины развития дисбактериоза, но существуют факторы, которые могут спровоцировать нарушение микрофлоры кишечника:
заболевания вирусной этиологии;
наличие инфекции в кишечнике;
прием противовоспалительных и гормональных нестероидных медикаментов;
поражение организма паразитами;
аллергические реакции;
оперативное вмешательство;
болезни, связанные с пищеварительной системой;
заболевания нервной системы, частые стрессовые ситуации;
неправильное и несбалансированное питание;
прием антибактериальных препаратов.

Для того чтобы избежать в дальнейшем развития дисбактериоза, необходимо вовремя лечить инфекционные и воспалительные заболевания, вести здоровый образ жизни и правильно питаться. Также нельзя забывать об укреплении иммунитета, что позволит снизить риск развитии заболевания.
Основа диеты при дисбактериозе кишечника у взрослых
Диета при дисбактериозе является одним из главных этапов нормализации микрофлоры. Если соблюдать все правила и рекомендации специалиста, то есть шанс избавиться от заболевания без применения медикаментозных препаратов. Полезные вещества и витамины будут поступать в организм из основного меню.
Основа питания при дисбактериозе включает в себя не только отказ от запрещенных продуктов и употребления полезных, но и соблюдении режима питания и правил приготовления. Питание должно быть дробным не менее 5 раз вдень, пища должна быть разнообразной и полноценной. Для того чтобы выбор продуктов не был затруднительным, для своего рационаможно взять за основу следующего меню:
Варианты для завтрака: куриные тефтели, приготовленные на пару, пюре без добавления молока и масла, манная каша, творог, овсяная каша, картофельное пюре с тунцом на пару, каша из пшена с добавлением плавленого сыра.
 Через 30 минут после завтрака можно выпить цикорий, чай или компот.
Через 30 минут после завтрака можно выпить цикорий, чай или компот.Варианты для первого перекуса: банан, яблоко, запеченное в духовке, йогурт без добавок, ягоды, творожная масса.
Варианты для обедов: бульон из нежирных сортов мяса, супы из круп и макарон. В качестве второго блюда можно приготовить филе рыбы на пару с картофельным пюре, биточки из постного мяса и свекольный салат, овощное рагу. Через полчаса разрешено выпить отвар из шиповника, компот или чай.
Варианты для второго перекуса: компот или чай с вафлей или зефиром, сок с сухариком, чай с галетными печеньями.
Варианты ужина: отварное мясо с омлетом на пару, пюре из тыквы и котлета из рыбы, тефтели, приготовленные на пару с отварным рисом, сладкий чай, натуральный йогурт. Ужин должен быть самым легким приемом пищи.
На ночь рекомендуется выпить ½ стакана киселя, что послужит дополнительной защитой для стенок кишечника.
Диета при дисбактериозе кишечника является одной из главных составляющих при лечении заболевания.
Запрещенные и допустимые к приему продукты
Во время диеты при дисбактериозекишечниканеобходимо правильно подобрать продукты, которые разделяются на запретные и разрешенные.
К запретным продуктам относятся:
приправы: перец, горчица, уксус;
консервированные продукты;
крепкие и слабоалкогольные напитки, вина и газировки способствуют развитию бродильных процессов, что активизирует размножение патогенных микроорганизмов;
капуста, шпинат, щавель, редиска и другие овощи провоцируют повышенное газообразование;
сыр, сгущенка, мороженое и сухое молоко затрудняют пищеварение;
отварные грибы и бульоны нагружают пищеварительную систему, поскольку продукт является трудно перевариваемым;
сосиски, колбасные изделия;
жирные сорта рыбы и мяса;
сдобные продукты, сладости, кондитерские изделия способствуют размножению бактерий и оказывают негативное воздействие на иммунную систему.

Список продуктов является поверхностным, поскольку меню подбирается индивидуально для каждого больного, отталкиваясь от причин возникновения заболевания, а также клинической картины. Например, если дисбактериоз сопровождается диареей, то из рациона следует убрать фрукты и овощи в сыром виде.
После исключения продуктов, необходимо самостоятельно или с помощью специалиста составить меню из разрешенных продуктов. Такая еда должны быть преимущественно из слизистых и постных блюд, содержащая минимальное количество соли и исключающая использование специй. К таким продуктам относятся:
натуральный кисель;
ягоды: земляника, брусника и малина;
мед;
небольшое количество сахара;
кефир и натуральный творог;
запеченные фрукты и отварные овощи;
паровые тефтели из постных сортов рыбы и мяса;
небольшое количество зелени: петрушка, укроп;
очищенные от кожуры огурцы;
бульоны из нежирных сортов рыбы и мяса;
отварной рис или рисовый суп.

Придерживаясь списку допустимых продуктов можно без применения лекарственных средств нормализовать микрофлору кишечника, а для исключения обострения необходимо такой рацион взять за основу.
Еда: питание с последствиями | Хронический гастрит — Кишечный дисбактериоз
Заболевания органов пищеварительной системы во многом связаны с особенностями пищевого поведения. Отсутствие режима питания, неадекватные диеты, агрессивная пища, голодание наряду с перееданием — все это приводит к неблагоприятным последствиям. В группе особого риска пациенты с осложненным гастроэнтерологическим анамнезом, лица, употребляющие алкогольные напитки, курильщики. К лечению расстройств пищевого поведения подключаются психотерапевты, гастроэнтерологи, терапевты, диетологи.
Под агрессивной пищей понимают консервацию, копчености, пряности, соленья, маринады. В этот список входят промышленные соусы, сдоба, жирное мясо, фастфуд и другие. Неправильное питание и неумеренность в еде приводят к заболеваниям органов ЖКТ, снижению функции желудка и кишечника, общесоматические расстройства.
Хронический гастрит
Хронический гастрит развивается, преимущественно, при отсутствии пищевой дисциплины. Половина населения планеты страдают от гастрита. Важное клиническое значение имеет кислотность желудочного сока и уровень его секреции. При пониженной секреции патология сопровождается снижением аппетита, горечью во рту, позывами к рвоте сразу после приема пищи (чаще всего после переедания). При повышенной секреции болезнь характеризуется болью и дискомфортом в эпигастрии, тошнотой, болевым синдромом в области поджелудочной железы.
Лечение комплексное, включает коррекцию образа жизни, питания. С целью симптоматической терапии назначают антацидные, обволакивающие препараты, обезболивающие. Важно не заниматься самолечением, а пройти обследовать и подобрать индивидуальную схему терапии с учетом клинического анамнеза больного.
Гастрит часто осложняется язвенной болезнью, профузными кровотечениями или геморрагическим шоком при эрозивном поражении. При флегмонозном гастрите есть вероятность перфорации стенок органа, деформации желудка, образования свищевых ходов. При недостатке фактора Касла у 90% всех больных хроническим гастритом развивается мегалобластная анемия. При длительном течении патологического процесса есть риск озлокачествления слизистого эпителия и образования аденокарциномы.
При недостатке фактора Касла у 90% всех больных хроническим гастритом развивается мегалобластная анемия. При длительном течении патологического процесса есть риск озлокачествления слизистого эпителия и образования аденокарциномы.
Кишечный дисбактериоз
Дисбактериоз кишечника или кишечный симбиоз — патологическое состояние микрофлоры кишечника, обусловленное с нарушением видового состава бактерий. При дисбактериозе условно-патогенная микрофлора меняет численный состав в сторону патогенной, что сопровождается диареей, метеоризмом, отделением зловонных газов, снижением аппетита, зудом в анусе из-за частых дефекаций. Нередко при дисбактериозе в каловых массах появляется скрытая кровь (выявляется лабораторно), кровяные прожилки, которые можно рассмотреть. Появление симптома требует срочной коррекции, чтобы исключить развитие более серьезных осложнений.
С целью лечения назначают бифидобактерии, кисломолочные продукты, лактобактерии. Спустя 1-2 недели стул восстанавливается, состояние нормализуется. Коррегируют и питание. Легкие формы дисбактериоза можно вылечить питанием: кисломолочными продуктами, сбалансированным рационом, обогащением питания клетчаткой, свежими овощами, фруктами.
Коррегируют и питание. Легкие формы дисбактериоза можно вылечить питанием: кисломолочными продуктами, сбалансированным рационом, обогащением питания клетчаткой, свежими овощами, фруктами.
Аллергические реакции
Аллергией на пищу страдают более 12% взрослых и почти 35-40% детей. Увеличение статистики связано с ухудшением экологической ситуации, употреблением в пищу консервации, красителей, стабилизаторов, эмульгаторов. Аллергические реакции встречаются при употреблении промышленных продуктов питания. При отягощенном аллергоанамнезе следует уделить внимание качеству и видовому составу пищи. Чаще всего аллергия развивается на клубнику, томаты, цитрусовые, цельное молоко, какао и шоколад.
Чтобы справиться с возникновением аллергических проявлений, рекомендуется иметь под рукой антигистаминные препараты, а при тяжелейшем течении аллергореакции и гормональные препараты.
Головные боли
Частые головные боли, в том числе мигренеподобные, развиваются в результате негативного воздействия пищи. Одним из провокаторов головной боли является тирамин, который содержится в сырах и кисломолочной продукции, слабосоленой, соленой и маринованной рыбе, шоколаде, копченом мясе, колбасных продуктов.
Одним из провокаторов головной боли является тирамин, который содержится в сырах и кисломолочной продукции, слабосоленой, соленой и маринованной рыбе, шоколаде, копченом мясе, колбасных продуктов.
Вызвать головную боль может и глютамат натрия — усилитель вкуса, который входит в соевый соус и блюда китайской, японской кухни. Если головные боли возникают сразу или через некоторое время после приема пищи, то можно подозревать некоторые пищевые ингредиенты.
Появление признаков пищевых расстройств и симптомов заболеваний органов ЖКТ требует обращения к доктору гастроэнтерологу. В нашей клинике А2МЕД в Симферополе пациенты могут пройти полный комплекс обследований, получить консультацию опытного диетолога. Коррекция рациона и навык правильного выбора еды для всей семьи — залог здоровья на долгие годы.
Кишечная инфекция у детей
Кишечная инфекция у детей – группа инфекционных заболеваний различной этиологии, протекающих с преимущественным поражением пищеварительного тракта, токсической реакцией и обезвоживанием организма.
У детей кишечная инфекция проявляется повышением температуры тела, вялостью, отсутствием аппетита, болями в животе, рвотой, диареей. Диагностика кишечной инфекции у детей основана на клинико-лабораторных данных (анамнезе, симптоматике, выделении возбудителя в испражнениях, обнаружении специфических антител в крови). При кишечной инфекции у детей назначаются антимикробные препараты, бактериофаги, энтеросорбенты; в период лечения важно соблюдение диеты и проведение регидратации.
Кишечная инфекция у детей – острые бактериальные и вирусные инфекционные заболевания, сопровождающиеся кишечным синдромом, интоксикацией и дегидратацией. В структуре инфекционной заболеваемости в педиатриикишечные инфекции у детей занимают второе место после ОРВИ. Восприимчивость к кишечной инфекции у детей в 2,5-3 раза выше, чем у взрослых. Около половины случаев кишечной инфекции у детей приходится на ранний возраст (до 3 лет). Кишечная инфекция у ребенка раннего возраста протекает тяжелее, может сопровождаться гипотрофией, развитием дисбактериоза и ферментативной недостаточности, снижением иммунитета._575.gif) Частое повторение эпизодов инфекции вызывает нарушение физического и нервно-психического развития детей.
Частое повторение эпизодов инфекции вызывает нарушение физического и нервно-психического развития детей.
Причины кишечной инфекции у детей
Спектр возбудителей кишечных инфекций у детей крайне широк. Наиболее часто патогенами выступают грамотрицательные энтеробактерии (шигеллы, сальмонеллы, кампилобактеры, эшерихии, иерсинии) и условно-патогенная флора (клебсиеллы, клостридии, протей, стафилококки и др.). Кроме этого, встречаются кишечные инфекции, вызываемые вирусными возбудителями (ротавирусами, энтеровирусами, аденовирусами), простейшими (лямблиями, амебами, кокцидиями), грибами. Общими свойствами всех возбудителей, обусловливающих развитие клинических проявлений, являются энтеропатогенность, способность к синтезу эндо- и экзотоксинов.
Заражение детей кишечными инфекциями происходит посредством фекально-орального механизма алиментарным (через пищу), водным, контактно-бытовым путями (через посуду, грязные руки, игрушки, предметы обихода и т. д.). У ослабленных детей с низкой иммунологической реактивностью возможно эндогенное инфицирование условно-патогенными бактериями. Источником ОКИ может выступать носитель, больной со стертой или манифестной формой заболевания, домашние животные. В развитии кишечной инфекции у детей большую роль играет нарушение правил приготовления и хранения пищи, допуск на детские кухни лиц-носителей инфекции, больных тонзиллитом, фурункулезом, стрептодермией и пр.
Источником ОКИ может выступать носитель, больной со стертой или манифестной формой заболевания, домашние животные. В развитии кишечной инфекции у детей большую роль играет нарушение правил приготовления и хранения пищи, допуск на детские кухни лиц-носителей инфекции, больных тонзиллитом, фурункулезом, стрептодермией и пр.
Наиболее часто регистрируются спорадические случаи кишечной инфекции у детей, хотя при пищевом или водном пути инфицирования возможны групповые и даже эпидемические вспышки. Подъем заболеваемости некоторыми кишечными инфекциями у детей имеет сезонную зависимость: так, дизентерия чаще возникает летом и осенью, ротавирусная инфекция — зимой.
Распространенность кишечных инфекций среди детей обусловлена эпидемиологическими особенностями (высокой распространенностью и контагиозностью возбудителей, их высокой устойчивостью к факторам внешней среды), анатомо-физиологическими особенностями пищеварительной системы ребенка (низкой кислотностью желудочного сока), несовершенством защитных механизмов (низкой концентрацией IgA). Заболеваемости детей острой кишечной инфекцией способствует нарушение нормальной микробиоты кишечника, несоблюдение правил личной гигиены, плохие санитарно-гигиенические условия жизни.
Заболеваемости детей острой кишечной инфекцией способствует нарушение нормальной микробиоты кишечника, несоблюдение правил личной гигиены, плохие санитарно-гигиенические условия жизни.
Классификация кишечной инфекции у детей
По клинико-этиологическому принципу среди кишечных инфекций, наиболее часто регистрируемых в детской популяции, выделяют шигеллез (дизентерию), сальмонеллез, коли-инфекцию (эшерихиозы), иерсиниоз, кампилобактериоз, криптоспоридиоз, ротавирусную инфекцию, стафилококковую кишечную инфекцию и др.
По тяжести и особенностям симптоматики течение кишечной инфекции у детей может быть типичным (легким, средней тяжести, тяжелым) и атипичным (стертым, гипертоксическим). Выраженность клиники оценивается по степени поражения ЖКТ, обезвоживания и интоксикации.
Характер местных проявлений при кишечной инфекции у детей зависит от поражения того или иного отдела ЖКТ, в связи с чем выделяют гастриты, энтериты, колиты, гастроэнтериты, гастроэнтероколиты, энтероколиты. Кроме локализованных форм, у грудных и ослабленных детей могут развиваться генерализованные формы инфекции с распространением возбудителя за пределы пищеварительного тракта.
Кроме локализованных форм, у грудных и ослабленных детей могут развиваться генерализованные формы инфекции с распространением возбудителя за пределы пищеварительного тракта.
В течении кишечной инфекции у детей выделяют острую (до 1,5 месяцев), затяжную (свыше 1,5 месяцев) и хроническую (свыше 5-6 месяцев) фазы.
Дизентерия у детейПосле непродолжительного инкубационного периода (1-7 суток) остро повышается температура (до 39-40° C), нарастает слабость и разбитость, снижается аппетит, возможна рвота. На фоне лихорадки отмечается головная боль, ознобы, иногда – бред, судороги, потеря сознания. Кишечная инфекция у детей сопровождается схваткообразными болями в животе с локализацией в левой подвздошной области, явлениями дистального колита (болезненностью и спазмом сигмовидной кишки, тенезмами с выпадением прямой кишки), симптомами сфинктерита. Частота дефекации может варьировать от 4-6 до 15-20 раз за сутки. При дизентерии стул жидкий, содержащий примеси мутной слизи и крови. При тяжелых формах дизентерии возможно развитие геморрагического синдрома, вплоть до кишечного кровотечения.
При тяжелых формах дизентерии возможно развитие геморрагического синдрома, вплоть до кишечного кровотечения.
У детей раннего возраста при кишечной инфекции общая интоксикация преобладает над колитическим синдромом, чаще возникают нарушения гемодинамики, электролитного и белкового обмена. Наиболее легко у детей протекает кишечная инфекция, вызванная шигеллами Зоне; тяжелее — шигеллами Флекснера и Григорьеза-Шига.
Сальмонеллез у детейНаиболее часто (в 90% случаев) развивается желудочно-кишечная форма сальмонеллеза, протекающая по типу гастрита, гастроэнтерита, гастроэнтероколита. Характерно подострое начало, фебрильный подъем температуры, адинамия, рвота, гепатоспленомегалия. Стул при сальмонеллезе жидкий, обильный, каловый, цвета «болотной тины», с примесями слизи и крови. Обычно данная форма кишечной инфекции заканчивается выздоровлением, однако у грудных детей возможен летальный исход вследствие тяжелого кишечного токсикоза.
Гриппоподобная (респираторная) форма кишечной инфекции встречается у 4-5% детей. При данной форме сальмонеллы обнаруживаются в посеве материала из зева. Ее течение характеризуется фебрильной температурой, головной болью, артралгией и миалгией, явлениями ринита, фарингита, конъюнктивита. Со стороны сердечно-сосудистой системы отмечаются тахикардия и артериальная гипотония.
При данной форме сальмонеллы обнаруживаются в посеве материала из зева. Ее течение характеризуется фебрильной температурой, головной болью, артралгией и миалгией, явлениями ринита, фарингита, конъюнктивита. Со стороны сердечно-сосудистой системы отмечаются тахикардия и артериальная гипотония.
На тифоподобную форму сальмонеллеза у детей приходится 2% клинических случаев. Она протекает с длительным периодом лихорадки (до 3-4-х недель), выраженной интоксикацией, нарушением функции сердечно-сосудистой системы (тахикардией, брадикардией).
Септическая форма кишечной инфекции обычно развивается у детей первых месяцев жизни, имеющих неблагоприятный преморбидный фон. На ее долю приходится около 2-3% случаев сальмонеллеза у детей. Заболевание протекает крайне тяжело, сопровождается септицемией или септикопиемией, нарушением всех видов обмена, развитием тяжелых осложнений (пневмонии, паренхиматозного гепатита, отоантрита, менингита, остеомиелита).
Эшерихиозы у детейДанная группа кишечных инфекций у детей крайне обширна и включает коли-инфекци, вызываемые энтеропатогенными, энтеротоксигенными, энтероинвазивными, энтерогеморрагическими эшерихиями.
Кишечная инфекция у детей, вызванная эшерихиями, протекает с субфебрильной или фебрильной температурой, слабостью, вялостью, снижением аппетита, упорной рвотой или срыгиваниями, метеоризмом. Характерна водянистая диарея (обильный, брызжущий стул желтого цвета с примесью слизи), быстро приводящая к дегидратации и развитию эксикоза. При эшерихиозе, вызываемом энтерогеморрагическими эшерихиями, диарея носит кровавый характер.
Вследствие обезвоживания у ребенка возникает сухость кожи и слизистых оболочек, снижается тургор и эластичность тканей, западает большой родничок и глазные яблоки, снижается диурез по типу олигурии или анурии.
Ротавирусная инфекция у детейОбычно протекает по типу острого гастроэнтерита или энтерита. Инкубационный период в среднем длится 1-3 дня. Все симптомы кишечной инфекции у детей разворачиваются в течение одних суток, при этом поражение ЖКТ сочетается с катаральными явлениями.
Респираторный синдром характеризуется гиперемией зева, ринитом, першением в горле, покашливанием. Одновременно с поражением носоглотки развиваются признаки гастроэнтерита: жидкий (водянистый, пенистый) стул с частотой дефекаций от 4-5 до 15 раз в сутки, рвотой, температурной реакцией, общей интоксикацией. Длительность течения кишечной инфекции у детей – 4-7 дней.
Одновременно с поражением носоглотки развиваются признаки гастроэнтерита: жидкий (водянистый, пенистый) стул с частотой дефекаций от 4-5 до 15 раз в сутки, рвотой, температурной реакцией, общей интоксикацией. Длительность течения кишечной инфекции у детей – 4-7 дней.
Различают первичную стафилококковую кишечную инфекцию у детей, связанную с употреблением пищи, обсемененной стафилококком, и вторичную, обусловленную распространением возбудителя из других очагов.
Течение кишечной инфекции у детей характеризуется тяжелым эксикозом и токсикозом, рвотой, учащением стула до 10-15 раз в день. Стул жидкий, водянистый, зеленоватого цвета, с небольшой примесью слизи. При вторичной стафилококковой инфекции у детей кишечные симптомы развиваются на фоне ведущего заболевания: гнойного отита, пневмонии, стафилодермии, ангины и пр. В этом случае заболевание может принимать длительное волнообразное течение.
Диагностика кишечной инфекции у детей
На основании осмотра, эпидемиологических и клинических данных педиатр (детский инфекционист) может лишь предположить вероятность кишечной инфекции у детей, однако этиологическая расшифровка возможна только на основании лабораторных данных.
Главную роль в подтверждении диагноза кишечной инфекции у детей играет бактериологическое исследование испражнений, которое следует проводить как можно ранее, до начала этиотропной терапии. При генерализованной форме кишечной инфекции у детей проводится посев крови на стерильность, бактериологическое исследование мочи, ликвора.
Определенную диагностическую ценность представляют серологические методы (РПГА, ИФА, РСК), позволяющие выявлять наличие Ат к возбудителю в крови больного с 5-х суток от начала болезни. Исследование копрограммы позволяет уточнить локализацию процесса в ЖКТ.
При кишечной инфекции у детей требуется исключить острый аппендицит, панкреатит, лактазную недостаточность, дискинезию желчевыводящих путей и др. патологию. С этой целью проводятся консультации детского хирурга и детского гастроэнтеролога.
Лечение кишечной инфекции у детей
Комплексное лечение кишечных инфекций у детей предполагает организацию лечебного питания; проведение оральной регидратации, этиотропной, патогенетической и симптоматической терапии.
Диета детей с кишечной инфекцией требует уменьшения объема питания, увеличения кратности кормлений, использования смесей, обогащенных защитными факторами, употребление протертой легкоусвояемой пищи. Важной составляющей терапии кишечных инфекций у детей является оральная регидратация глюкозо-солевыми растворами, обильное питье. Она проводится до прекращения потерь жидкости. При невозможности перорального питания и употребления жидкости назначается инфузионая терапия: внутривенно вводятся растворы глюкозы, Рингера, альбумина и др.
Этиотропная терапия кишечных инфекций у детей проводится антибиотиками и кишечными антисептиками (канамицин, гентамицин, полимиксин, фуразолидон, налидиксовая кислота), энтеросорбентами. Показан прием специфических бактериофагов и лактоглобулинов (сальмонеллезного, дизентерийного, колипротейного, клебсиеллезного и др.), а также иммуноглобулинов (антиротавирусного и др.). Патогенетическая терапия предполагает назначение ферментов, антигистаминных препаратов; симптоматическое лечение включает прием жаропонижающих, спазмолитиков. В период реконвалесценции необходима коррекция дисбактериоза, прием витаминов и адаптогенов.
В период реконвалесценции необходима коррекция дисбактериоза, прием витаминов и адаптогенов.
Прогноз и профилактика кишечной инфекции у детей
Раннее выявление и адекватная терапия обеспечивают полное выздоровление детей после кишечной инфекции. Иммунитет после ОКИ нестойкий. При тяжелых формах кишечной инфекции у детей возможно развитие гиповолемического шока, ДВС-синдрома, отека легких, острой почечной недостаточности, острой сердечной недостаточности, инфекционно-токсического шока.
В основе профилактики кишечных инфекций у детей – соблюдение санитарно-гигиенических норм: правильное хранение и термическая обработка продуктов, защита воды от загрязнения, изоляция больных, проведение дезинфекции игрушек и посуды в детских учреждениях, привитие детям навыков личной гигиены. При уходе за грудным ребенком мама не должна пренебрегать обработкой молочных желез перед кормлением, обработкой сосок и бутылочек, мытьем рук после пеленания и подмывания ребенка.
Дети, контактировавшие с больным кишечной инфекцией, подлежат бактериологическому обследованию и наблюдению в течение 7 дней.
Особенности питания при акне — рекомендации от МЦ РОШ
В середине прошлого века ученые пришли к выводу, что нет связи между формированием акне и диетой. Данное мнение поддерживалось дерматологами на протяжении последующих десятилетий. Однако сами пациенты отмечали связь между пищевым поведением и проявлениеми акне. В данной статье представлены современные доказательства взаимосвязи между патогенезом акне и употреблением в пищу углеводов, молочных продуктов, омега-3 жирных кислот, антиоксидантов, цинка, витамина А, Е и С.
Что может быть причиной акне?
Для начала нужно сказать что такое акне. Акне (угревая сыпь) – это воспалительное заболевание кожи, вызываемое изменениями сальных желез и их выводных протоков с вовлечением в процесс волосяных фолликулов.
Существует множество самых различных причин появления высыпаний и все они кроются внутри человеческого организма, так как состояние кожи напрямую зависит от здоровья и работоспособности внутренних органов.
К причинам развития угревой сыпи относится и гормональный дисбаланс, и нервный стресс, и нарушения иммунной системы, и некоторые гинекологические заболевания, и прием каких либо лекарственных препаратов и БАДов и в том числе неправильное питание и как следствие заболевания желудочно-кишечного тракта!
Поэтому перед лечением акне очень важно провести комплексную диагностику всего организма!
Болезни ЖКТ – частая причина акне
Очень часто акне провоцируют заболевания желудочно-кишечного тракта. Уже давно установлено, что качество кожи напрямую зависит от качества питания человека. И если пищевой рацион насыщен углеводами, а аминокислот и жиров в нем мало, возникает повышенная секреция сальных желез.
Также при неправильном питании идет большая нагрузка на печень. Печени становится тяжело выполнять все свои функции по детоксикации организма и часть усилий берет на себя кожа, так как кожа также является органом выведения! Таким образом, заболевания органов пищеварительной системы очень часто проявляются на лице. Достаточно часто у пациентов с угревой сыпью диагностируют гастрит, дисбактериоз кишечника и другие заболевания желудочно-кишечного тракта.
Достаточно часто у пациентов с угревой сыпью диагностируют гастрит, дисбактериоз кишечника и другие заболевания желудочно-кишечного тракта.
Диета при акне – неотъемлемая часть лечения
Чтобы избавиться от акне, нужно снизить жирность кожных покровов, и способствовать сужению сальных желез. Для этого потребуется использование косметических и медикаментозных средств и процедур в обязательном сочетании с правильным питанием. Диета при угревой сыпи во многом направлена на сокращение употребления жиров, сахара, а также на увеличение потребления клетчатки, что приводит к нормализации пищеварения и значительному улучшению состоянии кожи лица и тела. Кроме того, правильно подобранные продукты и регулярность питания улучшают состояние иммунной системы, что помогает естественной борьбе организма с воспалениями кожи и с другими заболеваниями.
От каких продуктов нужно отказаться при лечении акне?
Всем известно, что курение и употребление алкоголя вызывают интоксикацию организма и способствуют ухудшению состояния кожи.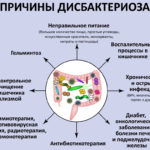 Но и некоторые обычные продукты питания могут вызывать у некоторых людей явление интоксикации.
Но и некоторые обычные продукты питания могут вызывать у некоторых людей явление интоксикации.
Диета при акне подразумевает под собой отказ от всех продуктов, повышающих уровень глюкозы и холестерина в крови, а также от тех блюд, которые могут усиливать работу сальных и потовых желез. Итак, рекомендуется исключить из рациона:
- сладости;
- молоко;
- алкогольные напитки;
- фастфуд и полуфабрикаты;
- газированные напитки, крепкий чай, кофе;
- острые пряности и специи;
- кетчупы и соусы;
- жирные сорта мяса и рыбы, копчености из них;
- жареный картофель;
- мучные и крахмалосодержащие сладости;
- хлебобулочные изделия.
При потреблении этих продуктов в крови возрастает количество токсинов, которые организм будет стремиться вывести наружу.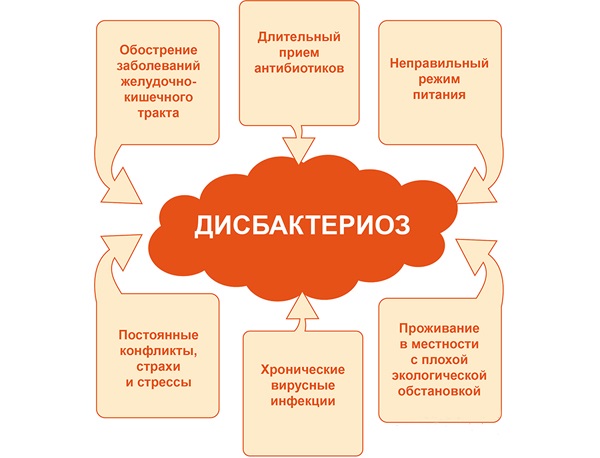 В том числе и посредством пор на коже лица и тела, что будет способствовать развитию угревой болезни.
В том числе и посредством пор на коже лица и тела, что будет способствовать развитию угревой болезни.
Существует ряд исследований, установивших, что в регионах, где в пище преобладают растительные продукты с минимальным содержанием животных жиров, уровень заболевания акне ниже чем в среднем по миру. Эти, а также многие другие показатели позволили сделать вывод об эффективности диеты при угревой сыпи на лице и теле.
Сахар и рафинированные продукты – главные враги вашей кожи
Исследования показали, что тяжесть проявления акне связана с употреблением пищи с большим содержанием сахара. Используемый с 1981 года в медицине глекимический индекс является установленной количественной единицей измерения потребляемой пищи, отражает скорость ее расщепления, а так же изменяющийся уровень глюкозы и инсулина в плазме крови. К продуктам с низким гликемическим индексом относятся овощи и зерновые, а высокий гликемический индекс характерен для более рафинированных углеводов, таких как белые макароны, каши, чипсы, выпечка или продукты приготовленные из белой муки.
Поэтому первое, что рекомендуется, это отказаться от чрезмерного употребления сладостей. Доказано, что сахар и рафинированные продукты способствуют накоплению инсулина, а также инсулиноподобного фактора роста. Это приводит к избыточному количеству андрогенов (мужских гормонов), отчего повышается выработка кожного сала, которое закупоривает поры и при присоединении бактерий, появляется угревая сыпь.
Лучшей клинической иллюстрацией гиперинсулинэмии и сопутствующей эндокринологической патологии, приводящих к акне, является синдром поликистозных яичников у взрослых женщин. Это состояние характеризуется гиперинсулинэмией, инсулинорезистентностью, гиперандрогенией, приводящими гиперандрогенизму, при котором развиваются такие симптомы как гирсутизм и акне. Когда гиперинсулинэмия подвергается лечению. Симптомы становятся менее выраженными, это говорит о том, что гиперандрогенизм и гиперинсулинэмия связаны между собой. Более того, когда пациенты придерживались диеты с низким гликемическим индексом, уровень андрогенов у них нормализовался.
Таким образом результаты, полученные во всех работах и исследованиях ученых всего мира, подтверждают, что низкая углеводная нагрузка может улучшить состояние кожи при акне.
Молочные продукты усиливают выработку кожного сала
Коровье молоко обладает повышенным содержанием лактозы — молочного сахара, что также приводит к повышению уровня сахара и инсулина в крови, что способствует стимуляции продукции кожного сала и гиперкератинизации себорейных зон. А некоторые авторы, исследовавшие связи между употреблением молочной продукции и проявлениями акне сделали вывод, что тяжесть акне зависит не только от употребления молочных продуктов, но и от их видов.
Глютен – помеха в работе кишечника
В зерновых культурах, таких как пшеница, рожь, овес, ячмень и продуктах производимых на их основе, т.е. мука и мучные изделия, каши, макароны, кондитерские изделия и другие продукты питания содержится глютен, который образует клейковину, мешающую правильной работе кишечника.
Кофе способствует возникновению акне
Отдельно хочется сказать про кофе. Кофе стимулирует выработку гормона кортизола, являющегося гормоном стресса (еще его называют гормон «разрушитель») и оказывающего пагубное воздействие на работу печени, также кофе резко повышает содержание глюкозы (сахара) в крови. Поэтому неоправданное повышение уровня кортизола в большинстве случаев приводит к появлению акне и при лечении угревой сыпи от кофе лучше отказаться.
Какие продукты помогут в борьбе с акне?
Вода – источник здоровья вашей кожи
При любой диете крайне важно соблюдать питьевой режим. Вода является важнейшим источником жизни на земле и здоровья каждого из нас. Вода принимает прямое участие в метаболизме веществ с целью снизить пагубное воздействие токсинов на организм. Вода ускоряет выведение шлаков из организма. Что, в свою очередь, способствует борьбе с акне. Минеральная вода утилизирует токсины, помогая коже восстановиться на клеточном уровне. Вода также способствует усвоению питательных веществ, полученных с пищей, и как следствие улучшению качества кожи и ее увлажненности.
Вода также способствует усвоению питательных веществ, полученных с пищей, и как следствие улучшению качества кожи и ее увлажненности.
Витамины С, А, В и Е – помощники в борьбе с акне
Чтобы повысить способность кожи к регенерации, и наладить работу иммунной системы, необходимо чтобы пищевой рацион был богат различными витаминами и микроэлементами.
Для повышения уровня коллагена в крови, который отвечает за упругость кожи и способность ее к регенерации, в питании должны присутствовать продукты с высоким содержанием витамина С. Такие как смородина, сладкий перец, брокколи, цветная капуста, квашенная белокочанная капуста. Очень часто у больных акне наблюдается дефицит витаминов А и Е, которые также в свою очередь отвечают за эластичность и здоровье кожи. Продукты с высоким содержанием данных витаминов такие как орехи, морковь, шпинат, тыква, овощи и фрукты зеленого и оранжевого цвета, также должны присутствовать в рационе питания при акне.
Витамины С, А и Е также являются мощными антиоксидантами. И как показали исследования, у некоторых пациентов с акне установлен низкий уровень антиоксидантов, поэтому у них снижена способность к устранению свободных радикалов, которые способствуют проявлению акне.
И как показали исследования, у некоторых пациентов с акне установлен низкий уровень антиоксидантов, поэтому у них снижена способность к устранению свободных радикалов, которые способствуют проявлению акне.
Для хорошего состояния кожи очень важен витамин В, который содержится в капусте, гречневой крупе, бобовых, печени.
Антиоксиданты – надежная защита кожи
В научных экспериментах продолжают исследовать роль флавоноидов с антиоксидантными свойствами. Например, ученым удалось установить, что эпигалокатехин-3-галлат – антиоксидант, обнаруженный в зеленом чае, способствует снижению продукции кожного сала. Цветок Impatiens balsamina (Недотрога бальзаминовая, или Бальзамин садовый), который используют в восточной медицине, содержит флавоноиды камферон и кверцетин, обладающие бактерицидным действием в отношении Propionibacterium acnes. Такие же свойства проявляет хорошо известный фитоалексин ресвератрол, который содержится в шкурке красного винограда, орехах, шелковице, ели, эвкалипте.
При акне включайте в рацион продукты, богатые селеном и цинком
Большую роль играет соотношение цинка и селена в организме. Эти микроэлементы принимают участие в строение клеточных мембран, обладают заживляющим эффектом. Цинк является необходимым элементом для правильного развития и функционирования кожи, он обладает бактериостатическим действием в отношении Propionibacterium acnes. У пациентов с акне отмечено снижение содержания цинка. Исследования показали, что употребление цинка пациентами с тяжелыми формами акне улучшило состояние их кожи. Большое количество цинка сосредоточено в бобовых, морепродуктах, тыквенных семечках, орехах. Максимальное количество селена сосредоточено в бразильском орехе.
Омега-кислоты необходимы для здоровья кожи
Также в рацион при лечении акне необходимо включать рыбу. Предпочтение лучше отдавать морским видам рыб, богатым омега-кислотами.
Доказано, что важны и омега-кислоты, которые можно найти в семенах льна. Полиненасыщенные жирные кислоты омега-3 и омега-6 могут влиять на воспалительные реакции при формировании акне. Жирная пища в типичных развитых странах состоит преимущественно из омега-6 жирных кислот, а в неразвитых странах она включает большое количество омега-3 жирных кислот, содержащихся в рыбе, дичи, овощах. Соотношение омега-6 и омега-3 жирных кислот в пище рекомендуемое экспертами 2:1.
Полиненасыщенные жирные кислоты омега-3 и омега-6 могут влиять на воспалительные реакции при формировании акне. Жирная пища в типичных развитых странах состоит преимущественно из омега-6 жирных кислот, а в неразвитых странах она включает большое количество омега-3 жирных кислот, содержащихся в рыбе, дичи, овощах. Соотношение омега-6 и омега-3 жирных кислот в пище рекомендуемое экспертами 2:1.
Да данный момент существует очень мало исследований, в которых установлена корреляция между потреблением омега-3 и омега-6 жирных кислот и развитием акне. В эпидемиологическом исследовании, проведенном в 1961 году, была установлена связь между употреблением большого количества рыбы (источника омега-3 жирных кислот) и уменьшением проявлений акне. В более поздней работе (2008 года) было показано, что употребление в пищу добавки омега-3 способствовало снижению тяжести акне и уменьшению случаев проявления воспалительных элеиентов, а также улучшению состояния пациента.
Сырые овощи – лучший источник клетчатки
Важной составляющей в диете при акне является клетчатка. Клетчатка помогает вывести из организма токсины и другие вредные вещества. Продукты с высоким содержанием клетчатки всем известны – это овощи в сыром виде, фрукты, орехи, семена льна, гречка.
Клетчатка помогает вывести из организма токсины и другие вредные вещества. Продукты с высоким содержанием клетчатки всем известны – это овощи в сыром виде, фрукты, орехи, семена льна, гречка.
Киноа – «золотое зерно» для лечения акне
Отдельно хотелось бы рассказать про очень интересный, уникальный продукт, богатый клетчаткой, но пока малоизвестный – это зерна киноа. Киноа даже называют «золотым зерном» из-за его уникальных свойств, но его сложно назвать злаком, ближайшие родственники киноа — это шпинат и свекла. Листья и молодые побег киноа также употребляют в пищу, как овощи. В киноа отсутствует глютен, что также очень важно при лечении акне. В состав киноа входит большое количество уникального полезного растительного белка, причем аминокислотный состав белков очень сбалансированный. Лизин, который также входит в состав киноа, помогает скорейшему заживлению тканей, благодаря чему ускоряется процесс восстановления кожного покрова, что очень ценно при лечении акне и различных других повреждениях кожи . По содержанию фосфора киноа сравним с многими видами рыбы.
По содержанию фосфора киноа сравним с многими видами рыбы.
Кроме того, продукт богат фитиновой кислотой, которая способствует снижению уровня холестерина, в связи с чем снижается выработка кожного сала. Много в киноа и различных минералов: магния, калия, железа, кальция, цинка и витаминов группы В и Е, которые насыщают и питают клетки кожи, что способствует улучшению качества кожи и волос.
Употреблять киноа можно как в виде каш, так и в супах и салатах. Благодаря своему составу, киноа, прежде всего, мощное общеукрепляющее средство, которое придает энергии, сил и здоровья в нашей активной жизни. А внутреннее здоровье — это залог внешней красоты!
Правильного питания следует придерживаться, как во время лечения акне, для ускорения получения результата, так и на постоянной основе, для поддержания кожи в здоровом, сияющем, чистом состоянии.
Гастроэнтерит: причины, симптомы, лечение, профилактика
Гастроэнтерит – заболевание желудочно-кишечного тракта, которое выражается воспалительными процессами в кишечнике и желудке. Гастроэнтерит может быть как острым, так и приобретать хроническую форму.
Гастроэнтерит может быть как острым, так и приобретать хроническую форму.
Острый гастроэнтерит
Острый гастроэнтерит – воспаление желудка или кишечника, вызванное, зачастую, неправильным режимом питания или попаданием в кишечный тракт различного вида вирусов и инфекционных возбудителей.
Слишком частое переедание или частое питание всухомятку, а также нерегулярный рацион также может стать причиной воспаления желудка. Симптомы заболевания проявляют себя резко, болевые ощущения при этом носят характер схваток. Основные симптомы острого гастроэнтерита – сильная боль в животе, или в районе пупка, тошнота, рвотные позывы, общая слабость всего организма, учащенное сердцебиение, бледность кожи, нарушение аппетита, чувство головокружения.
В особо тяжелых случаях с больным могут случаться обмороки. При остром гастроэнтерите наблюдается изменение стула – выделения становятся похожими на слизь. При проявлении болезни еще один визуальный симптом – заострение черт лица. При возникновении первых симптомом острого гастроэнтерита больному необходимо оказать первую помощь – промыть желудок теплой водой с добавлением марганцовки или с добавлением соды. После промывания желудка необходимо обратиться к доктору и провести комплексное обследование желудочно – кишечного тракта и выявить возбудителя гастроэнтерита.
При возникновении первых симптомом острого гастроэнтерита больному необходимо оказать первую помощь – промыть желудок теплой водой с добавлением марганцовки или с добавлением соды. После промывания желудка необходимо обратиться к доктору и провести комплексное обследование желудочно – кишечного тракта и выявить возбудителя гастроэнтерита.
Причины гастроэнтерита
Гастроэнтерит делится на несколько видов в зависимости от того, что стало возбудителем заболевания. Бактериальный гастроэнтерит – провоцируется кишечными возбудителями, бактериями, сальмонеллой или стафилококками, которые попадают в пищевод с некачественной пищей или при ослабленном иммунитете. Вирусный гастроэнтерит – возбудителем является ротавирус – кишечная вирусная бактерия.
Попадание ротавируса вызывается проблемой грязных рук, несоблюдением гигиены до еды и во время приема пищи, некачественной, немытой пищей, плохо приготовленной едой, или употребление сырой еды, например морепродуктов. Хронический гастроэнтерит в основном появляется как следствие невылеченного острого гастроэнтерита, или на фоне онкологических заболеваний. Гастроэнтерит так же можно отнести к «профессиональным» заболеваниям.
Хронический гастроэнтерит в основном появляется как следствие невылеченного острого гастроэнтерита, или на фоне онкологических заболеваний. Гастроэнтерит так же можно отнести к «профессиональным» заболеваниям.
Симптомы гастроэнтерита
Основные симптомы гастроэнтерита — тошнота, рвота и изменения в стуле, в более тяжелых случаях воспаления стул может сопровождаться кровяными выделениями. Довольно часто у больного наблюдается жар, сильные головные боли, боли в животе, особенно в области пупка. При возникновении вирусного гастроэнтерита у больного наблюдается сильное повышение температуры тела. Боли в животе сопровождаются его сильным вздутием.
Основные симптомы гастроэнтерита проявляют себя уже через сутки — двое после заражения. Если у больного началось сильное головокружение и глубокие обмороки необходимо незамедлительно обращаться за помощью к врачу, так как такие симптомы свидетельствуют о запущенности заболевания и неспособности организма противостоять болезни. В особо тяжелых случаях наблюдаются судороги по телу.
В особо тяжелых случаях наблюдаются судороги по телу.
Гастроэнтерит у детей
Гастроэнтерит у детей является распространённым заболевание, но в особо тяжелых и запущенных случаях может стать причиной летального исхода. Гастроэнтерит у детей может быть как следствие дисбактериоза, перенесенного гриппа, попадания ротавируса в организм. Симптоматика гастроэнтерита у детей – тошнота при приеме пищи, вздутие живота, колики, нарушение сна, повышенная температура, понос. При возникновении первых признаков гастроэнтерита у ребенка, необходимо принять меры по предостережению обезвоживания организма – давать пить как можно больше воды.
Если через сутки после обнаружения заболевания рвота не прекращается – немедленно обращайтесь к врачу. При обнаружении гастроэнтерита ребенку необходимо придерживаться диеты для нормализации работы желудка. Она включает в себя несладкие пюре из овощей или фруктов, запеченные яблоки, отварное нежирное мясо, постные супы, рыба. Такой режим питания соблюдается на протяжении недели, после чего можно возвращаться к привычному рациону. При лечении гастроэнтерита у детей необходимо исключить употребление молочных продуктов на две недели.
Такой режим питания соблюдается на протяжении недели, после чего можно возвращаться к привычному рациону. При лечении гастроэнтерита у детей необходимо исключить употребление молочных продуктов на две недели.
Лечение гастроэнтерита
При проявлении первых признаков заболевания больному необходимо воздержаться от употребления пищи на несколько часов для нормализации работы кишечника. Пейте как можно больше жидкости – вода или легкие соки без мякоти. После того, как чувство тошноты пропадает, можно съесть немного отварного риса, сухарик или банан. При лечении гастроэнтерита антибиотики не принимаются. При наличии сильных болей, необходимо сделать промывание желудка слабым раствором марганцовки или соды.
Диета при гастроэнтерите включает в себе нежирную отварную рыбу и мясо, постные супы, каши, овощи, и как можно больше жидкости – вода, соки. Больному запрещено употребление молочных продуктов, фруктов. Диеты необходимо придерживаться 3-4 дня, после чего снова возвращаться на прежний режим питания.
В течение трех дней (3-5 июня 2015 года) в приемное отделение ГБУЗ ЯНАО «Губкинская городская больница» обратились 7 горожан с диагнозом острый гастроэнтерит, еще 6 пациентов доставлены сотрудниками отделения скорой помощи; из них: 1 — госпитализирован в отделение реанимации и анестезиологии, 7 — в инфекционное отделение в состоянии средней степени тяжести, остальные — отказались от госпитализации. Возрастной диапазон пациентов — от 12 лет до 61 года. В данный период состояние всех пациентов стабильное.
Аллергическое поражение желудочно-кишечного тракта у ребенка
Аллергическое поражение желудочно-кишечного тракта у ребенка
Вовлечение желудочно-кишечного тракта в аллергический процесс происходит столь часто, что его можно считать обязательным. Да это и не удивительно. Кишечник является очень важным иммунным органом, он буквально пронизан иммунными клетками, местами собирающимися в большие скопления. Кишечник служит входными воротами для проникновения в организм самых различных экзогенных аллергенов (пищевых, химических, лекарственных, паразитарных и др. ). В стенке кишок могут наблюдаться фиксированные в них антитела и поступившие различным путем в организм (ингаляционным, подкожным, внутривенным) антигены вызывают иммунологический процесс, в результате чего возникают разнообразные функциональные поражения кишок. Иными словами, кишки могут быть «шоковым» органом, в котором развивается реакция антиген — антитело при сенсибилизации организма парентеральным путем.
). В стенке кишок могут наблюдаться фиксированные в них антитела и поступившие различным путем в организм (ингаляционным, подкожным, внутривенным) антигены вызывают иммунологический процесс, в результате чего возникают разнообразные функциональные поражения кишок. Иными словами, кишки могут быть «шоковым» органом, в котором развивается реакция антиген — антитело при сенсибилизации организма парентеральным путем.
Так, при сывороточной болезни, бронхиальной астме, поллинозе, крапивнице, отеке Квинке, лекарственной аллергии наблюдаются нарушения функций кишок аллергического характера. С другой стороны, воспалительные и атрофические изменения в слизистой оболочке кишок повышают вероятность всасывания пищевых и лекарственных антигенов и благоприятствуют вторичной сенсибилизации организма. При этом может играть роль снижение продукции секреторного IgA, препятствующего в норме проникновению через кишечную стенку экзоантигенов. Аллергическое поражение кишок чаще всего возникает при пищевой и лекарственной аллергии, а также на почве сенсибилизации к аутомикрофлоре.
Аллергические энтеро- и колопатии могут развиваться вторично на почве дисбактериоза, хронических энтеритов, колитов, холециститов за счет сенсибилизации к аутомикрофлоре, тканевым антигенам, а особенно часто к пищевым антигенам и различным пищевым добавкам (консерванты, красители, антибактериальные вещества и др.).
Следовательно, кишечные дисфункции в одних случаях являются следствием и проявлением общего аллергоза, в других — аллергический компонент может быть существенным патогенетическим фактором хронического патологического процесса в органе самой различной этиологии.
На характер складывающегося заболевания влияют, в основном, три условия — возраст ребенка, отдел желудочно-кишечного тракта, который становится главным «плацдармом» для аллергической реакции, и глубина вовлечения слизистой оболочки в патологический процесс. Зависимость от возраста, в целом, можно охарактеризовать так: чем меньше ребенок, тем острее он реагирует на аллерген и тем обширнее площадь вовлечения слизистой оболочки.
Проявление аллергического поражения желудочно-кишечного тракта у ребенка.
У ребенка первых месяцев жизни употребление пищевого аллергена может вызвать обильную многократную рвоту и одновременно частый жидкий стул. Это очень напоминает симптомы острого отравления или кишечной инфекции.
В возрасте старше года, особенно после 5-6 лет, симптомы не столь остры и более отчетливо привязаны к определенному «этажу» желудочно-кишечного тракта — желудку, двенадцатиперстной, тонкой или толстой кишке. Одними из первых признаков формирующегося аллергического воспаления могут быть пищевые «капризы».
Более половины больных реагируют на употребление аллергена рвотой. Ее приближение вы заметите по изменению настроения и поведения ребенка: он хнычет, капризничает, отказывается от дальнейшего приема пищи. Рвота возникает во время еды или в пределах часа после нее. Нередко она сопровождается кишечными коликами. Маленький ребенок внезапно начинает пронзительно кричать, сучит ножками. Поглаживая его животик, вы ощутите, как он напряжен. Колики — это проявление своеобразной «моторной бури», вызываемой острой аллергической реакцией. Нередко они многократно повторяются в течение дня и приурочены к определенным часам.
Поглаживая его животик, вы ощутите, как он напряжен. Колики — это проявление своеобразной «моторной бури», вызываемой острой аллергической реакцией. Нередко они многократно повторяются в течение дня и приурочены к определенным часам.
У детей дошкольного и школьного возраста боль не обязательно возникает приступами. Она может быть тупой, продолжительной и не так явно связана с употреблением аллергенной пищи. После трех лет появляется тенденция к более узкой локализации болезненности живота, хотя сам ребенок еще не может показать это место. При вопросе «где у тебя болит?» он обычно кладет руку на пупок.
В некоторых случаях клиническая картина напоминает острый аппендицит, непроходимость кишок, тромбоз мезентериальных сосудов. Коликообразная боль в животе и болезненность при пальпации, повышение температуры тела, рвота, задержка стула или, наоборот, понос, а также тахикардия, падение АД, лейкоцитоз в крови позволяют заподозрить брюшную катастрофу. Однако быстрый эффект от приема антиаллергических средств, наличие общих аллергических симптомов (крапивница, отек Квинке, бронхоспазм, мигрень и др. ) и благополучный в большинстве случаев исход помогают поставить правильный диагноз. Алиментарная аллергическая реакция может повторяться у одного и того же больного при приеме непереносимого продукта.
) и благополучный в большинстве случаев исход помогают поставить правильный диагноз. Алиментарная аллергическая реакция может повторяться у одного и того же больного при приеме непереносимого продукта.
У многих матерей вырабатывается полезная привычка рассматривать стул своего ребенка. Основную тревогу у них может вызвать наличие слизи, иногда в значительном количестве, или прожилок крови. Такие отклонения характерны для аллергического воспаления толстой кишки. В дальнейшем на этой основе формируются серьезные хронические заболевания кишечника.
Расстройства стула — обычный признак желудочно-кишечной аллергии. Оно нарушает сложившуюся периодичность походов на горшок или ритм «грязный-чистый». У казалось бы здорового ребенка на привычной диете вдруг начинается понос, который через несколько дней сменяется запором. Такие «срывы» со временем принимают определенную регулярность. Это нарушение даже при относительно хорошем самочувствии ребенка далеко не безобидно. Оно свидетельствует о серьезных и уже далеко зашедших проблемах с кишечником.
Оно свидетельствует о серьезных и уже далеко зашедших проблемах с кишечником.
Все дело в том, насколько глубоко поражена стенка кишечника или желудка. Если срок заболевания еще короток и аллергическое воспаление захватило только поверхностные слои слизистой оболочки, — это приводит к нарушению процессов переваривания и усвоения пищи. При вовлечении более глубоких слоев возможно утолщение стенки и сужение просвета кишки. Тут уж не миновать тяжелых хронических запоров и мучительных болей в животе. Если такое сужение формируется в верхних отделах желудочно-кишечного тракта, то создаются условия для заброса кислого желудочного сока в пищевод, особенно при длительном нахождении ребенка в горизонтальном положении, например, во время ночного сна. Такие забросы могут вызвать рефлекторный спазм бронхов и приступ удушья. Почти всем современным родителям знаком специальный медицинский термин дисбактериоз. Это не что иное, как нарушение внутрикишечной экологии.
Обычно оно возникает после кишечных инфекций или длительного приема антибиотиков, но и аллергическое воспаление так же закономерно разрушает полноценное состояние естественной микробной флоры. Многие микробы, безвредные в здоровом организме, получают при пищевой аллергии возможность интенсивно размножаться и распространяться из мест своего обычного обитания в стерильные органы, вызывая болезненные процессы.
Многие микробы, безвредные в здоровом организме, получают при пищевой аллергии возможность интенсивно размножаться и распространяться из мест своего обычного обитания в стерильные органы, вызывая болезненные процессы.
Аллергия, избирая своим плацдармом желудочно-кишечный тракт, расставляет много хитрых «ловушек», в которые попадаются как родители, так и врачи. Одна из них связана с тем, что все симптомы аллергии точно такие же, как и при других заболеваниях желудка и кишечника. Но это еще не все. Аллергическое воспаление приводит к таким серьезным тканевым нарушениям, что они оформляются в самостоятельные заболевания. Эти болезни (гастрит, гастродуоденит, ферментативная недостаточность, язвенная болезнь и др.) традиционно лечат у гастроэнтеролога.
Но все свое коварство аллергия проявляет у детей, уже страдающих хроническими заболеваниями желудочно-кишечного тракта. Ее скрытая «работа» приводит к тому, что традиционные методы лечения оказываются мало эффективными или, как это ни парадоксально, вызывают ухудшение состояния.
Вот почему все дети с аллергическими заболеваниями, имеющие желудочно-кишечные симптомы, должны проходить углубленное обследование как у аллерголога, так и у гастроэнтеролога.
Как нужно обследовать ребенка?
Специальное аллергологическое исследование с применением кожных проб с соответствующим антигеном, выявление специфических антител в сыворотке крови и сенсибилизации лимфоцитов к тому или иному аллергену позволяют установить истинную природу заболевания.
В кале иногда находят повышенное количество слизи, лейкоцитов, эозинофильных гранулоцитов. Слизистая оболочка кишки при эндоскопии может быть гиперемирована, отечна. При гистоморфо-логическом исследовании выявляют клеточную, преимущественно лимфоцитарную, эозинофильную или плазмоклеточную инфильтрацию, увеличение слизеобразующих бокаловидных клеток, иногда расширение капилляров, отек, геморрагии. В легких случаях биопсия кишок патологии не обнаруживает.
В период обострения может измениться характер электроколо-графической кривой: учащается ритм сокращений, тонические волны и участки повышения моторной функции чередуются с явлениями спазма и атонии.
Электроколограмма приобретает вид «раздраженной кишки» после приема продукта-аллергена. Рентгенологическое исследование вне периода обострения патологии не выявляет. После провокации продуктом, который, возможно, оказывает аллергизирующее воздействие, усиливается перистальтика желудка и кишок, ускоряется пассаж бария, образуются спастические перетяжки, скапливаются газы.
Дифференцировать аллергические электроколопатии необходимо от инфекционных, паразитарных, опухолевых заболеваний кишок, от острого аппендицита, тромбоза брыжеечных сосудов.
Лечение.
Рекомендуются диета, медикаментозные средства, физические факторы, лекарственные растения, минеральные воды. В зависимости от превалирования клинических симптомов (боль в животе, понос, запор) дифференцируется диета и фармакотерапия.
При запоре первостепенное значение имеет соответствующая диета, содержащая достаточное количество растительной клетчатки и других продуктов, усиливающих перистальтику. Обычно назначают диету № 3 по Певзнеру.
Обычно назначают диету № 3 по Певзнеру.
В рацион питания можно включать разнообразные напитки, газированные, в холодном виде; хлеб ржаной или содержащий отруби, хрустящие хлебцы с отрубями; молочнокислые продукты однодневные (кефир, ацидофильное молоко, простокваша), сметану, творог, сливки; сливочное, растительное масло; мясо и рыбу в любом виде; супы в большом количестве овощные и фруктовые, желательно в холодном виде, можно мясные, рыбные.
Крупы и мучные изделия: гречневая, ячневая, перловая, рассыпчатые каши, чечевица. Яйца вкрутую. Овощи и фрукты в большом количестве сырые, особенно морковь, чернослив, квашеная капуста, абрикосы.
Сладкие блюда: в большом количестве мед, компоты, варенье. Закуски и соусы разнообразные.
Исключаются кисели, крепкий чай, какао, шоколад, слизистые супы, протертые каши, сдобное тесто, ограничиваются блюда и напитки в горячем виде.
При поносе пищевые вещества должны минимально раздражать слизистую оболочку кишок. Из диеты исключают все продукты, стимулирующие опорожнение кишок, вводят вещества, уменьшающие перистальтику. Этим требованиям удовлетворяет диета № 4.
Из диеты исключают все продукты, стимулирующие опорожнение кишок, вводят вещества, уменьшающие перистальтику. Этим требованиям удовлетворяет диета № 4.
При назначении ее больные должны соблюдать постельный режим, пищу принимать 5—6 раз в день небольшими порциями. Химический состав диеты: белка 75 г, жира 50 г, углеводов 250—300 г, 8374—9211 Дж (калорий — 2000—2200). Поваренную соль ограничивают.
В рацион питания можно включать крепкий горячий чай, кофе, какао на воде, отвар из черники, белые сухари, сухое, несдобное печенье; молочные продукты: кефир и простоквашу трехдневную, свежий творог в протертом виде; масло сливочное в небольшом количестве; яйца и яичные блюда в ограниченном количестве; некрепкий куриный бульон, слизистые супы на воде с небольшим количеством масла, рисовый или овсяный отвар.
Мясо можно употреблять в ограниченном количестве в виде паровых котлет, кнелей и фрикаделек, в которые вместо хлеба рекомендуется добавлять рис с протертым чесноком, куры и рыбу нежирных сортов в отварном рубленом виде.
Крупы и мучные блюда: протертая каша на воде, паровой пудинг из протертой крупы.
Сладкое: кисель или желе, можно из сушеных фруктов, сахар и сахаристые вещества в ограниченном количестве.
Из рациона исключают пряности, острые и соленые приправы и блюда, овощи, фрукты, черный хлеб, молоко и свежие кислые молочные продукты, жирные сорта мяса и рыбы, холодные напитки и блюда, сдобное тесто и пироги.
Наряду с указанными общими принципами диетотерапии при составлении пищевого рациона больных необходимо исключить продукты-аллергены. Для этого на основании данных аллергологического анамнеза, кожных проб и серологических реакций выявляют продукты, которые могут быть аллергенами у данного больного. Часто наблюдается поливалентная аллергия, поэтому необходимо, по возможности, полностью прекратить контакт с соответствующими медикаментами, растениями, пылевыми, эпидермальными или другими антигенами.
Большое значение имеет исключение паразитарной инвазии как аллергизирующего фактора, для чего необходимо исследовать дуоденальное содержимое и кал на простейшие и яйца глист.
Неспецифическую сенсибилизацию проводят с помощью антигистаминных препаратов (димедрол по 0,03—0,05 г, тавегил по 0,01 г 2 раза в день, фенкарол или бикарфен по 0,025 г 3—4 раза в сутки, перитол по 0,04 г или диазолин по 0,05—0,1—0,2 г 1—2 раза в сутки). В более тяжелых случаях можно назначать глюкокортикостероидные препараты внутрь, внутримышечно, внутривенно или ректально.
При сочетании аллергической энтеропатии и аллергического колита целесообразна специфическая микробная гипосенсибилизация восходящими дозами аллергенов кишечной палочки, протея, стрептококка, стафилококка в зависимости от характера выявленной сенсибилизации.
Большое значение имеют седативная и психотерапия, ферментативные препараты (фестал, панзинорм, мексаза, панкреатин, панфермент, холензим и др.), ограничение, как правило, антибиотиков и других антибактериальных средств.
Лечение аллергического ринита
В первую очередь терапия предусматривает проведение комплекса элиминационных мероприятий по устранению контакта с аллергенами. К элиминационным мероприятиям относятся меры по снижению концентрации аэроаллергенов в жилых помещениях за счет регулярной уборки, устранению домашних животных, птиц, тараканов, очагов плесени, пищевых продуктов и лекарственных средств, уменьшению контакта с пыльцевыми аллергенами в период цветения, устранению пассивного курения.
К элиминационным мероприятиям относятся меры по снижению концентрации аэроаллергенов в жилых помещениях за счет регулярной уборки, устранению домашних животных, птиц, тараканов, очагов плесени, пищевых продуктов и лекарственных средств, уменьшению контакта с пыльцевыми аллергенами в период цветения, устранению пассивного курения.
С целью элиминации аллергенов используют промывание носовой полости с различными солевыми растворами. Однако очень важно, чтобы эти препараты не только хорошо вымывали частицы, но и увлажняли слизистую оболочку, оказывали терапевтическое, противоотечное воздействие, а по своим физико-химическим свойствам и составу были близки к назальному секрету человека.
Промывающий раствор обязательно должен быть в компактной упаковке, снабженной распылителем для удобного и быстрого использования.
Для удаления пыльцы ребенку слегка запрокидывают голову и делают по два впрыска в каждую ноздрю. Затем ребенка просят тщательно высморкаться. Процедуру следует повторить 2–4 раза для смягчения и увлажнения слизистой носа.
Препарат для промывания полости носа (например, «Хьюмер» «Аква Марис», «Ризосин», «Физиомер») рекомендуется хранить в аптечке. Родителям можно советовать снабжать им ребенка перед посещением детское учреждение.
Быстрое и своевременное промывание полости носа с помощью противоотечных препаратов приводит к эффективному удалению причинных аллергенов из полости носа, тем самым не позволяя им проникать в организм ребенка и запускать механизм аллергии. В настоящее время подобную элиминационную терапию принято рассматривать как первый этап лечения аллергического ринита.
Фармакотерапия аллергических ринитов направлена на устранение симптомов заболевания, воспаления в слизистой оболочке носа и предупреждения его возникновения необратимых изменений в виде утолщения слизистой оболочки носовых раковин и включает назначение.
С этой целью используются препараты применяемые внутрь, так и топические (местно действующие) препараты следующие лекарственные препараты.
Антигистаминные препараты.
При аллергических реакциях иммунная система объявляет ложную тревогу и на обычные вещества, такие как пыльца растений, домашняя пыль. Получив сигнал различные иммунные клетки выделяют сильные вещества – медиаторы, хранящиеся в специальных гранулах в клетках и в организме развивается бурная реакция и обострение заболевания. Одним из важных медиаторов, который вызывает симптомы аллергии – спазм бронхов, чихание, кашель, слезотечение, зуд, секрецию слюнных и бронхиальных желез — является гистамин. Действие гистамина связано с его влиянием на специфические рецепторы, расположенные на поверхности клеток различных органов и тканей. Так как эти рецепторы широко распространены в организме ( в коже, легких, слизистой желудочно-кишечного тракта), то и действие гистамина проявляется очень быстро и разнообразно. Препятствовать действию гистамина могут препараты, которые блокируют гистаминовые рецепторы, т.е. временно закрывают их и не дают соединиться с ними гистамину. Эти препараты называются антигистаминами. Они блокируют только гистаминовые рецепторы, т.е. действуют селективно, выборочно.
Они блокируют только гистаминовые рецепторы, т.е. действуют селективно, выборочно.
В терапии детей предпочтение отдается антигистаминным препаратам второго поколения. Антигистамины применяются для быстрой ликвидации аллергических проявлений при симптоматическом лечении сезонной сенной лихорадки, аллергического ринита и конъюнктивита, атопических дерматитах. “Старые” антигистамины сегодня применяются редко, так как созданы препараты, второго и третьего поколения, которые имеют высокий клинический эффект и редко побочные проявления. У маленьких детей применяют зиртек, кларитин, кетотифен. У детей старшего возраста и подростков — телфаст, кестин, кларитин, симплекс. Местные антигистаминные препараты (вибрацил, левокабастин, азеластин) назначается в виде капель в нос или назального спрея.
Кромоны
В терапии аллергического ринита, как и в случае лечения бронхиальной астмы, применяется профилактическое лечение кромогликатом натрия (кромолин, ломузол, кромоглин). Этот препарат эффективен при лечении легкого и среднетяжелого аллергического ринита. В случае регулярных сезонных обострений препараты кромогликата натрия следует назначать за 1-2 недели до предполагаемого обострения. Эффект при лечении кромогликатами в виде назальных или глазных капель наступает через несколько дней. Курс лечения продолжается от нескольких дней до 2-3 месяцев.
Этот препарат эффективен при лечении легкого и среднетяжелого аллергического ринита. В случае регулярных сезонных обострений препараты кромогликата натрия следует назначать за 1-2 недели до предполагаемого обострения. Эффект при лечении кромогликатами в виде назальных или глазных капель наступает через несколько дней. Курс лечения продолжается от нескольких дней до 2-3 месяцев.
Для больных аллергическим конъюнктивитом, проявляющимся воспалением слизистых оболочек глаза (покраснением, отеком, зудом, слезотечением) кромогликат выпускается в виде глазных капель (Оптикром, Хай-кром).
Антихолинергические препараты
Из лекарственных средств этой группы наиболее широко используется ипратропиум бромид. Он способствует уменьшению отделяемого (ринореи) и отека слизистой оболочки носа.
Назальные кортикостероидные препараты беклометазон (альдецин) и флютиказон (фликсоназе) обладают выраженным противовоспалительным эффектом. Эти лекарственные средства назначают при тяжелом и среднетяжелом течении аллергических ринитов, при отсутствии эффекта от антигистаминные средств и кромонов. В среднем, достаточно месячного курса лечения назальными стероидами. Доза определяется врачом, частота введения — 1-2 раза в день. В случае хронического течения аллергического круглогодичного ринита после курса топических стероидов, целесообразно продолжить лечение назальными кромонами.
В среднем, достаточно месячного курса лечения назальными стероидами. Доза определяется врачом, частота введения — 1-2 раза в день. В случае хронического течения аллергического круглогодичного ринита после курса топических стероидов, целесообразно продолжить лечение назальными кромонами.
Для лечения сочетанной тяжелой бронхиальной астмы и аллергического ринита будет целесообразно использовать одну и ту же группу топических кортикостероидов, например беклометазон в виде дозирующего аэрозоля и в виде назального спрея. Применение назальных стероидов в этом случае приводит не только к восстановлению носового дыхание, но и к более быстрому купированию бронхиальной обструкции. Кроме того, купирование аллергического воспаления в носовой полости оказывает положительное лечебное воздействие на течение аллергического конънктивита. Необходимо учитывать общую дозу назначаемых глюкокортикостероидов.
Деконгестанты — это сосудосуживающие средства для восстановление носового дыхания. Применяют их в виде капель и назальных аэрозолей. Их действие носит исключительно симптоматический характер. Ограничением к использованию препаратов этой группы являются побочные эффекты. Одно из них – развитие, так называемого, “медикаментозного” ринита при длительном применении.
Применяют их в виде капель и назальных аэрозолей. Их действие носит исключительно симптоматический характер. Ограничением к использованию препаратов этой группы являются побочные эффекты. Одно из них – развитие, так называемого, “медикаментозного” ринита при длительном применении.
Специфическая иммунотерапия — метод лечения, направленный на снижение чувствительности организма к аллергенам. Проведение этого вида терапии показано пациентам, страдающих аллергическим ринитом, с четко установленными аллергенами, при наличии определенных показаний и отсутствии противопоказаний, определяемых аллергологом.
🧬 Анализ на «дисбактериоз»: пожалуйста, хватит
Прилетели как-то на Землю инопланетяне. Посмотрели: ледники тают, озоновые дыры растут, панды не размножаются. Стали думать, отчего это все. Спустились в московский район Бирюлево. Взяли сотню человек, раздели, пощупали, допросили. Сделали вывод: озоновые дыры — из-за брюнетов (много их попалось), панды не размножаются из-за мужиков — их на летающей тарелке оказалось больше половины. Ну, а глобальное потепление — из-за рубля: у всех жителей Бирюлево в карманах оказалась эта валюта. Улетели инопланетяне к себе домой и по результатам исследования напечатали своими зелеными щупальцами десять кандидатских диссертаций.
Ну, а глобальное потепление — из-за рубля: у всех жителей Бирюлево в карманах оказалась эта валюта. Улетели инопланетяне к себе домой и по результатам исследования напечатали своими зелеными щупальцами десять кандидатских диссертаций.
Вот как-то так и проводится «анализ на дисбактериоз». Поговорим об этом диагнозе с гастроэнтерологом GMS Clinic Головенко Алексеем.
Что не так с этим исследованием? Его же так часто назначают врачи!
- Давайте оговоримся: его назначают врачи только в странах бывшего СССР. За пределами этих государств простой посев стула для выявления дисбаланса микрофлоры не выполняется. Вы не найдете указаний на необходимость этого исследования ни в руководстве WGO по синдрому раздраженного кишечника, ни в рекомендациях ACG (Американской коллегии гастроэнтерологов) по острой диарее, ни в стандарте AAFP (Американской ассоциации семейных врачей) по наблюдению новорожденных с коликами. Ну и, естественно, никакого диагноза «дисбактериоз» нет ни в Международной классификации болезней, ни в хотя бы одном (!) нерусскоязычном учебнике.
 8 в грамме стула. Ссылок на литературу в стандарте полно, но, что подозрительно, среди них нет ни одной зарубежной публикации. Ну а сами статьи и учебники не описывают, как именно сравнивали микрофлору здоровых и больных людей, то есть как именно был сделан вывод о нормальном содержании той или иной бактерии.
8 в грамме стула. Ссылок на литературу в стандарте полно, но, что подозрительно, среди них нет ни одной зарубежной публикации. Ну а сами статьи и учебники не описывают, как именно сравнивали микрофлору здоровых и больных людей, то есть как именно был сделан вывод о нормальном содержании той или иной бактерии. - Бактерии, обнаруживаемые в стуле (который формируется в толстой кишке) — это совсем не те же бактерии, что обитают в ротовой полости или тонкой кишке. Кроме того, бактерии в стуле (то есть в просвете кишки) — это совсем не бактерии, обитающие в слизи, защищающей кишечную стенку. Вообще, через наш пищеварительный тракт «пролетает» безумное количество чужеродных бактерий, грибов и вирусов. К счастью, большая их часть не могут подобраться к кишечной стенке: обитающая там пристеночная микрофлора конкурирует с «пришельцами». Мы называем это явление колонизационной резистентностью, и именно ему мы обязаны тем, что первая же проглоченная со стаканом московской воды условно-патогенная бактерия не вызывает у нас понос.

- Состав и соотношение кишечных бактерий у каждого человека свои. Изучив (не посевом кала, конечно, а сложнейшими генетическими методами) состав бактерий в стуле, можно, например, угадать принадлежит ли образец жителю Нью-Йорка или побережья Амазонки. Ну, или в каком регионе отдельной страны (например, Дании). проживает человек, отправивший на анализ свои фекалии. В общем, истинный состав кишечной микрофлоры — наши «отпечатки пальцев», и предполагать некую общую норму, а уж тем более судить о «нормальности» флоры всего по 20 видам из 1000 — смешно.
- То, будут ли размножаться бактерии на питательной среде, зависит не только от того, какие бактерии в стуле живут, но и от того, как стул собрали (с унитаза, со стерильной бумаги), как хранили (в холодильнике, у батареи, у окна), как быстро доставили в лабораторию. Много ли людей, которым рекомендовали анализ на дисбактериоз читали вот эту инструкцию, согласно которой кал нужно собрать в стерильную посуду, поместить в холодильник и нести в лабораторию не в руках, а в термосе с кубиком льда? Впрочем, даже при совершении этих действий результат анализа на дисбактериоз интерпретировать нормальный врач не может.
 А значит, не должен и пытаться это сделать.
А значит, не должен и пытаться это сделать.
В питательной среде появились колонии бактерий. К счастью для нас, действительно опасная Сальмонелла растет в питательной среде. Большая часть кишечных бактерий, увы, нет.
Так что, нет такого понятия — «дисбактериоз»?
Конечно, есть. Например, псевдомембранозный колит — тяжелое воспаление толстой кишки после антибиотика — самый настоящий дисбактериоз: погибли конкуренты, и поэтому размножается Clostridium difficile. Только для того, чтобы это лечить, совершенно не нужно констатировать очевидное — состав бактерий в кишке изменился. Достаточно подтвердить инфекцию (выявить токсины C.difficile) и назначить лечение.
Кишечная микрофлора, вне сомнения, влияет на все процессы в нашем организме. Пересадив стул от мыши с ожирением мышке с нормальным весом, у последней мы вызываем ожирение. Состав кишечных бактерий принципиально разный у людей с тревожностью и депрессией. Ну, а добавление пробиотика Bacteroides fragilis мышам, у которых искусственно вызвали аутизм, улучшает их социальные навыки. Прочитайте популярную книгу «Смотри, что у тебя внутри» известного микробиолога Роба Найта: наши знания о микрофлоре колоссальны, но применять их на практике (то есть для лечения болезней) мы пока только начинаем.
Ну, а добавление пробиотика Bacteroides fragilis мышам, у которых искусственно вызвали аутизм, улучшает их социальные навыки. Прочитайте популярную книгу «Смотри, что у тебя внутри» известного микробиолога Роба Найта: наши знания о микрофлоре колоссальны, но применять их на практике (то есть для лечения болезней) мы пока только начинаем.
Состав бактерий можно и нужно изучать. Этому посвящено амбициозное международное исследование Human Microbiome Project с бюджетом $115 млн. Естественно, никакие «посевы стула» при этом не используются. Для анализа микробных «джунглей» кишечника используются методы метагеномики. Они позволяют описать, сколько уникальных последовательностей ДНК присутствует у конкретного человека, какие группы бактерий преобладают, а какие отсутствуют. К слову, когда такие технологии (например, секвенирование 16S-рРНК появились, выяснилось, что 75% видов, обнаруживаемых при генетическом анализе того же кала, вообще не известны науке.
Стоп. То есть делать посев стула вообще нет смысла?
Я этого не говорил. Мы обязательно выполняем посев стула, если хотим выявить рост по-настоящему вредных бактерий. Например, у человека с кровавой диареей мы пытаемся найти Сальмонеллу или Шигеллу, Кампилобактерию или особую разновидность кишечной палочки. Здесь посев кала жизненно необходим, ведь так мы сможем назначить лечение антибиотиком — убить конкретного возбудителя.
Грамотный врач выполняет диагностический тест только тогда, когда его результат может изменить лечение. Если и при «дефиците» лактобактерий, и при «избытке» кишечной палочки будет назначено одно и то же лекарство или диета, анализ является пустой тратой денег.
Полноценное исследование собственной микрофлоры уже можно сделать на коммерческой основе в США и Европе. Стоит «удовольствие» около 100 евро, и в результате генетического анализа микрофлоры вы получите заключение (например, вот такое) о преобладающих в вашем пищеварительном тракте бактериях. Проблема в том, что и эти результаты невозможно применить на практике. Потому что:
Проблема в том, что и эти результаты невозможно применить на практике. Потому что:
пока у нас НЕТ способа, избирательно менять состав кишечных бактерий.
Предположим, мы однозначно установили, что у человека имеется дефицит какой-то конкретной микроорганизмы (например, лактобактерий). Мы можем:
- Дать пробиотик (то есть конкретную живую бактерию) и надеяться, что она останется жить в кишечнике.
- Дать пребиотик (то есть «корм» для бактерии) и надеяться, что это усилит рост именно нужной нам бактерии.
- Дать антибиотик (яд для бактерии) и надеяться, что погибнет именно чрезмерно размножившаяся бактерия.
- Пересадить человеку чужую микрофлору — сделать трансплантацию фекальной микробиоты (ввести разбавленный стул здорового человека больному человеку).
Очевидно, избирательным действием можно считать только назначение пробиотика. Максимальная доза лучшего коммерческого пробиотика — это 10 млрд. жизнеспособных бактерий в дозе препарата. В кишечнике обитает около 100 триллионов бактерий. То есть, на каждую бактерию «из аптеки» приходится 10 тысяч бактерий, уже «проживающих» в кишке. Маловероятно, что это ничтожное количество бактерий сможет преодолеть колонизационную резистентность и «заселить» кишку. Кроме того, механизм действия пробиотиков (когда они работают) может вообще быть связан с не с самими бактериями: у трансгенных мышей, предрасположенных в воспалению кишечника это самое воспаление удалось остановить, применяя не «живой» пробиотик, а вообще ДНК и некоторые белки, выделенные из «убитого» температурой препарата.
жизнеспособных бактерий в дозе препарата. В кишечнике обитает около 100 триллионов бактерий. То есть, на каждую бактерию «из аптеки» приходится 10 тысяч бактерий, уже «проживающих» в кишке. Маловероятно, что это ничтожное количество бактерий сможет преодолеть колонизационную резистентность и «заселить» кишку. Кроме того, механизм действия пробиотиков (когда они работают) может вообще быть связан с не с самими бактериями: у трансгенных мышей, предрасположенных в воспалению кишечника это самое воспаление удалось остановить, применяя не «живой» пробиотик, а вообще ДНК и некоторые белки, выделенные из «убитого» температурой препарата.
Ну, а главное: одно дело — теория и лабораторные исследования, другое дело — клинические испытания (то есть изучение эффекта препаратов у людей). Разберем три типовых для России ситуации, когда человеку предлагают сдать «анализ кала на дисбактериоз»:
Колики у новорожденного
Мама жалуется, что ребенок много плачет. К слову, любой ребенок в первые три месяца жизни кричит от 117 до 133 минут в сутки (мета-анализ). Наличие или отсутствие колик (беспричинный крик более 3 часов за день хотя бы 3 дня в неделю), в целом, не влияет на риск задержки развития ребенка. В одном исследовании, простая беседа с родителями о «безопасности» колик уменьшала продолжительность плача с 2,6 до 0,8 часов в день. Дети — эмпаты.
К слову, любой ребенок в первые три месяца жизни кричит от 117 до 133 минут в сутки (мета-анализ). Наличие или отсутствие колик (беспричинный крик более 3 часов за день хотя бы 3 дня в неделю), в целом, не влияет на риск задержки развития ребенка. В одном исследовании, простая беседа с родителями о «безопасности» колик уменьшала продолжительность плача с 2,6 до 0,8 часов в день. Дети — эмпаты.
Чаще бывает не так. Выполняется анализ кала на дисбактериоз, там, естественно (норма-то взята с «потолка»), обнаруживаются «отклонения». Назначается пробиотик. И часто ведь помогает: еще бы, ведь частота колик неумолимо снижается с возрастом ребенка. При этом уверенности в том, что пробиотики вообще эффективны при коликах, у нас нет. Многочисленные мета-анализы, посвященные лечению и профилактике этого состояния, не смогли однозначно подтвердить эффективность пробиотиков. Возможно, какое-то полезное действие оказывает пробиотик Lactobacillus reuteri. Вот только для того, чтобы назначить этот препарат, анализ кала на «дисбактериоз» нам совершенно не нужен.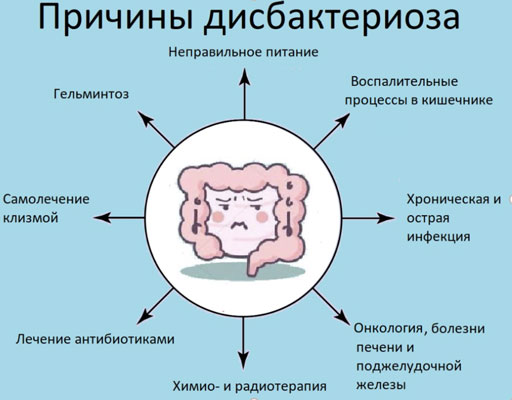
Атопический дерматит у ребенка
Все уверены, что проблемы с кожей — от «живота». Будь это так, наверное, атопический дерматит прекрасно лечился бы пробиотиками. Но этот подход не слишком эффективен. Последний мета-анализ свидетельствует: применение пробиотиков (главным образом, Lactobacillus rhamnosus GG) несколько уменьшает выраженность экземы, но эффект этот весьма символический, а дополнительная терапия пробиотиком не позволяет сократить частоту применения местных стероидов, которые (вместе с увлажнением кожи) остаются основой лечения атопического дерматита. И вновь: назначить этот пробиотик мы можем вне зависимости от «результатов» «анализа на дисбактериоз».
Вздутие и спазмы в животе у взрослого
Вздутие живота чаще всего является проявлением избыточного бактериального роста в тонкой кишке (СИБРа), при котором помогает не пробиотик, а антибиотик, например, рифаксимин. Это состояние диагностируется при помощи специального дыхательного теста. Нередко постоянное вздутие живота является следствием внешнесекреторной недостаточности поджелудочной железы: дефицит ферментов в стуле можно выявить при помощи теста на фекальную эластазу, назначив при снижении постоянную терапию ферментами. Но чаще всего ощущение «вздутия» связано с повышенной чувствительностью кишки (висцеральной гиперчувствительностью), которая развивается у людей с синдромом раздраженного кишечника. Как вы уже догадались, для того, чтобы оценить количество бактерий в тонкой кишке, функцию поджелудочной железы или чувствительность кишки к растяжению, изучать 20 бактерий в кале бессмысленно. Да и эффективность пробиотиков при синдроме раздраженного кишечника вызывает сомнения.
Нередко постоянное вздутие живота является следствием внешнесекреторной недостаточности поджелудочной железы: дефицит ферментов в стуле можно выявить при помощи теста на фекальную эластазу, назначив при снижении постоянную терапию ферментами. Но чаще всего ощущение «вздутия» связано с повышенной чувствительностью кишки (висцеральной гиперчувствительностью), которая развивается у людей с синдромом раздраженного кишечника. Как вы уже догадались, для того, чтобы оценить количество бактерий в тонкой кишке, функцию поджелудочной железы или чувствительность кишки к растяжению, изучать 20 бактерий в кале бессмысленно. Да и эффективность пробиотиков при синдроме раздраженного кишечника вызывает сомнения.
Так нужно хоть в какой-то ситуации сдавать «кал на дисбактериоз»?
Нет. Никогда. Ни при каких обстоятельствах. Мы не лечим вздутие живота, изучая линии на ладони. Мы не лечим сыпь, глядя в хрустальный шар. Мы не делаем бессмысленный анализ на дисбактериоз, чтобы назначить лечение.
Мы ждем, когда доказательная медицина предложит нам эффективные препараты и практические способы понять, что не так с нашими бактериями.
Жду вместе с вами!
Источник: deti.mail.ru
(PDF) Дисбиоз кишечной микробиоты, вызванный диетой, и его влияние на иммунитет и заболевания
Nutrients 2012, 4 1113
86. Vijay-Kumar, M .; Aitken, J.D .; Carvalho, F.A .; Kumar, M.V .; Aitken, J.D .; Carvalho, F.A .;
Cullender, T.C .; Mwangi, S .; Srinivasan, S .; Sitaraman, S.V .; и другие. Метаболический синдром и
измененная микробиота кишечника у мышей, лишенных толл-подобных рецепторов 5. Science 2010, 328, 228–231.
87. Amar, J .; Chabo, C .; Вагет, А.; Klopp, P .; Vachoux, C .; Бермудес-Хумаран, Л.Г .; Смирнова, Н .;
Berge, M .; Sulpice, T .; Lahtinen, S .; и другие. Прилипание к слизистой оболочке кишечника и транслокация
комменсальных бактерий при раннем начале диабета 2 типа: молекулярные механизмы и лечение пробиотиками
. EMBO Mol. Med. 2011, 3, 559–572.
EMBO Mol. Med. 2011, 3, 559–572.
88. Cani, P.D .; Дельзенн Н.М. Кишечный микробиом как терапевтическая мишень. Pharmacol. Ther. 2011,
130, 202–212.
89. Парнелл, Дж.А .; Реймер, Р.А. Модуляция пребиотических волокон микробиоты кишечника улучшает факторы риска
ожирения и метаболического синдрома. Кишечные микробы 2012, 3, 29–34.
90. Ley, R.E. Ожирение и микробиом человека. Curr. Мнение. Гастроэнтерол. 2010, 26, 5–11.
91. Pozzilli, P .; Синьор, А .; Уильямс, A.J .; Билс, П. Кивните колонии мышей по всему миру
— Последние факты и цифры. Иммунол. Сегодня 1993, 14, 193–196.
92. Roesch, L.F .; Лорка, Г.L .; Casella, G .; Giongo, A .; Наранхо, А .; Pionzio, A.M .; Li, N .; Mai, V .;
Wasserfall, C.H .; Schatz, D .; и другие. Независимая от культуры идентификация кишечных бактерий коррелировала
ис началом диабета в модели на крысах. ISME J. 2009, 3, 536–548.
93. Wen, L .; Ley, R.E .; Волчков П.Ю . ; Stranges, P.B .; Аванесян, Л .; Stonebraker, A.C .; Hu, C .;
; Stranges, P.B .; Аванесян, Л .; Stonebraker, A.C .; Hu, C .;
Wong, F.S .; Szot, G.L .; Bluestone, J.A .; и другие. Врожденный иммунитет и микробиота кишечника
в развитии диабета 1 типа.Природа 2008, 455, 1109–1113.
94. Giongo, A .; Gano, K.A .; Crabb, D.B .; Mukherjee, N .; Novelo, L.L .; Casella, G .; Дрю, J.C .;
Ilonen, J .; Книп, М .; Hyoty, H .; и другие. К определению аутоиммунного микробиома для диабета 1 типа
. ISME J. 2011, 5, 82–91.
95. Sapone, A .; de Magistris, L .; Pietzak, M .; Clemente, M.G .; Трипати, А .; Cucca, F .; Lampis, R .;
Крышак, Д .; Carteni, M .; Generoso, M .; и другие. Повышенная регуляция зонулина связана с увеличением проницаемости кишечника на
у субъектов с диабетом 1 типа и их родственников.Диабет 2006, 55,
1443–1449.
96. Lee, A.S .; Гибсон, Д.Л .; Zhang, Y .; Sham, H.P .; Vallance, B.A .; Дутц, Дж. П. Нарушение кишечного барьера
кишечным бактериальным патогеном ускоряет инсулит у мышей nod. Диабетология 2010, 53,
Диабетология 2010, 53,
741–748.
97. Bosi, E .; Molteni, L .; Radaelli, M.G .; Folini, L .; Fermo, I .; Bazzigaluppi, E .; Piemonti, L .;
Пасторе, М.Р .; Парони, Р. Повышенная кишечная проницаемость предшествует клиническому началу диабета 1 типа
.Диабетология 2006, 49, 2824–2827.
98. Ватт, т .; Берти, I .; Sapone, A .; Герардуцци, Т .; Не, Т .; Zielke, R .; Фазано, А. Роль зонулина, модулятора плотного соединения кишечника
в патогенезе диабета I типа у крыс BB
, склонных к диабету. Proc. Natl. Акад. Sci. USA 2005, 102, 2916–2921.
99. Kriegel, M.A .; Сефик, Э .; Hill, J.A .; Wu, H.J .; Benoist, C .; Mathis, D. Естественно передающиеся
сегментированных нитчатых бактерий разделяются с защитой от диабета у мышей, не страдающих ожирением.
Proc. Natl. Акад. Sci. USA 2011, 108, 11548–11553.
100. Alam, C .; Bittoun, E .; Bhagwat, D .; Valkonen, S .; Саари, А .; Jaakkola, U .; Eerola, E .; Huovinen, P . ;
;
Hanninen, A. Влияние стерильной среды на иммунную регуляцию кишечника и прогрессирование диабета
у мышей с диабетом без ожирения (nod). Диабетология 2011, 54, 1398–1406.
Еда для лечения дырявого кишечника
Апрель 2020 Выпуск
Еда для лечения дырявого кишечника
Сара Томсен Феррейра, MS, MPH, RD, CDN, IFNCP, CHWC
Диетолог сегодняшнего дня
Vol.22, № 4, стр. 38
Исследование диетических вмешательств для поддержания здоровой барьерной функции кишечника
Исследования, проведенные за последние 30 лет, связали плохую функцию кишечного барьера с пищеварительными и аутоиммунными расстройствами. Параллельно с повышенным интересом к микробиому как модулятора здоровья и болезней, роль барьерной функции кишечника (кишечника) в поддержании иммунитета и здоровья пищеварительной системы вышла на первый план.
С акцентом на механизмы, с помощью которых плохая функция кишечного барьера может вызывать клинические и субклинические симптомы, в этой статье рассматривается потенциальная роль режима питания, конкретных питательных веществ и пробиотических добавок в поддержании барьерной функции кишечника.
Анатомия барьерной функции
Кишечный тракт с площадью поверхности 200 м2 действует как полупроницаемый физический барьер, позволяющий абсорбировать питательные вещества и жидкости, удерживая патогены и пищевые белки на расстоянии.1 Стенка кишечника состоит из столбцов из эпителиальные клетки удерживаются вместе сильно разветвленными сетчатыми структурами, называемыми плотными соединениями. Плотные соединения включают белки клаудин-2, окклюдин и цингулин, которые образуют каналы для избирательной диффузии питательных веществ и воды.В поврежденной эпителиальной клеточной стенке может развиваться неограниченный путь, позволяющий соединениям, таким как белки и бактерии, проходить через них практически любого размера2,3
Над эпителиальной клеточной стенкой должен лежать другой уровень барьерной защиты: толстый слой слизи, состоящий из двух частей, содержащий антимикробные молекулы (называемые муцином), секретируемые бокаловидными клетками. 1 Когда он полностью функционирует, внешний слой этого толстого слизистого покрытия содержит иммуноглобулины и другие вещества. белки, которые связывают бактерии, чтобы предотвратить контакт с внутренним слоем.
1 Когда он полностью функционирует, внешний слой этого толстого слизистого покрытия содержит иммуноглобулины и другие вещества. белки, которые связывают бактерии, чтобы предотвратить контакт с внутренним слоем.
Поскольку бокаловидные клетки выделяют дополнительный муцин для обновления обоих слоев, связанные бактерии во внешнем слое изгоняются через перистальтику. Если какой-либо слой истощен или поврежден, бактерии могут достичь эпителиальных клеток и вызвать клеточное воспаление.4 Было обнаружено, что люди с воспалительным заболеванием кишечника (ВЗК) имеют дефекты гликозилирования и более высокие уровни сульфида от сульфатредуцирующих бактерий, что может уменьшить дисульфид. связь между муцинами, ослабляющая барьерную функцию.5
За стенкой эпителиальных клеток лежит богатая лимфоидами сеть, содержащая до 70% иммунных клеток организма, также известная как лимфоидная ткань, ассоциированная с кишечником.6 Таким образом, эпителиальные клетки действуют как медиаторы между активностью иммунной системы и внешними воздействиями (включая пищевые антигены), жестко регулирующие баланс между толерантностью и иммунитетом. 7
7
Таким образом, полностью функциональный барьер кишечника требует адекватного производства слизи, достаточных уровней иммуноглобулинов в слизи и должным образом регулируемых плотных контактов.
Измерение барьерной функции кишечника
В клинических исследованиях используются различные методы для измерения степени кишечной проницаемости. Трансэпителиальное / трансэндотелиальное электрическое сопротивление (TEER) используется для измерения динамики плотного соединения. Отношение лактулозы к рамнозе (L: R) (или двойной анализ проницаемости сахаров) широко используется для оценки степени прохождения больших и малых частиц через эпителиальную выстилку 8,9
Некоторые пищевые сахара, включая лактулозу и L-рамнозу, проходят через эпителиальную выстилку и могут быть измерены в моче.Поскольку лактулоза представляет собой большую молекулу, а рамноза — небольшую молекулу, их соотношение и количество каждой из них, измеренное в моче, действуют как индикаторы степени проницаемости. Еще одним маркером проницаемости являются уровни белков, связывающих жирные кислоты кишечника, которые обнаруживаются в энтероцитах и высвобождаются в кровоток при повреждении кишечника.9,10
Еще одним маркером проницаемости являются уровни белков, связывающих жирные кислоты кишечника, которые обнаруживаются в энтероцитах и высвобождаются в кровоток при повреждении кишечника.9,10
Зонулин, белок, вырабатываемый в кишечнике, уровни циркуляции которого можно измерить в крови, также использовался в качестве косвенного биомаркера кишечной проницаемости.Высвобождение сывороточного зонулина, которое может быть вызвано дисбактериозом или глиадином у генетически предрасположенных людей, независимо может ослабить прочность плотных контактов.11,12 Болезненные состояния, при которых зонулин влияет на людей, включают аутоиммунные состояния, такие как целиакия, диабет 1 типа. , ревматоидный артрит, рассеянный склероз, экспериментальный аутоиммунный энцефаломиелит и анкилозирующий спондилит; метаболические нарушения, такие как ожирение, инсулинорезистентность, диабет 2 типа и синдром поликистозных яичников; и кишечные заболевания, включая синдром раздраженного кишечника (СРК) и нечувствительность к глютену, не связанном с целиаком. 12,13
12,13
В исследовании 100 пациентов с IBS — 50% с IBS-C (IBS с запором) и 50% с IBS-D (IBS с диареей) — уровни зонулина в сыворотке были сопоставимы с уровнями, обнаруженными при активной целиакии. , повышение уровня зонулина коррелировало с учащением еженедельного стула14
Механизмы дисрегуляции барьерной функции
Нарушение функции кишечного барьера может вызвать или усугубить дисфункцию как при кишечных, так и внекишечных заболеваниях из-за высвобождения воспалительных молекул и последующего повреждения желудочно-кишечного тракта (ЖКТ).
Заболевания, которые были связаны с повышенной проницаемостью кишечника, включают язвы желудка, инфекционную диарею, СРК, ВЗК, целиакию, пищевую аллергию, инфекции (например, респираторные), острое воспаление (например, сепсис, синдром системного воспалительного ответа), аутоиммунные заболевания ( например, рассеянный склероз, системная красная волчанка) и нарушения обмена веществ (например, неалкогольный стеатогепатит, сердечно-сосудистые заболевания) 7,15-17
Если нарушение функции кишечного барьера позволяет микробам взаимодействовать с собственной пластинкой, контакт может вызвать высвобождение чрезмерного количества провоспалительных цитокинов, включая интерферон гамма, фактор некроза опухоли альфа (TNF-альфа), интерлейкин (IL) 1 бета и IL-13. .Поскольку обильное высвобождение этих цитокинов вызывает повышенное повреждение кишечной ткани и рубцевание, это может привести к самовоспроизводящемуся циклу плохой барьерной функции, увеличению провоспалительных цитокинов и повреждению кишечника. Например, повреждение желудочно-кишечного тракта, вызванное цитокинами, было зарегистрировано в IBD.18
.Поскольку обильное высвобождение этих цитокинов вызывает повышенное повреждение кишечной ткани и рубцевание, это может привести к самовоспроизводящемуся циклу плохой барьерной функции, увеличению провоспалительных цитокинов и повреждению кишечника. Например, повреждение желудочно-кишечного тракта, вызванное цитокинами, было зарегистрировано в IBD.18
Клиническая значимость на практике
GI Health
Маркеры повышенной проницаемости неоднократно измерялись в контексте заболевания желудочно-кишечного тракта.Например, в группе из 33 детей с язвенным колитом, у которых оценивалась частота рецидивов в течение одного года, исследование проницаемости тонкой кишки было аномальным у 77,8% тех, у кого возник рецидив, по сравнению с только 8,3% тех, у кого болезнь оставалась бессимптомной19
Целиакия
Целиакия долгое время ассоциировалась с аномальной структурой плотного соединения и повышенной кишечной проницаемостью.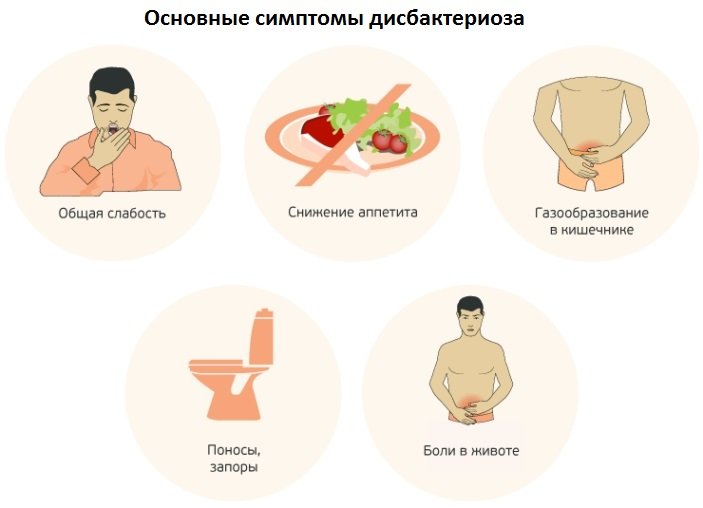 Интересно, что фармацевтический пептид и регулятор плотных контактов, называемый ларазотида ацетатом, в настоящее время находится на стадии 3 испытаний в качестве дополнительного лечения для пациентов с глютеновой болезнью, у которых сохраняются симптомы на безглютеновой диете.20,21
Интересно, что фармацевтический пептид и регулятор плотных контактов, называемый ларазотида ацетатом, в настоящее время находится на стадии 3 испытаний в качестве дополнительного лечения для пациентов с глютеновой болезнью, у которых сохраняются симптомы на безглютеновой диете.20,21
Инфекционный гастроэнтерит
Стойкие желудочно-кишечные симптомы, вызванные известной или предполагаемой инфекцией, также должны побуждать к оценке кишечной проницаемости. В исследовании, проведенном с участием 21 человека с инфекционным гастроэнтеритом из Campylobacter jejuni , кишечная проницаемость, оцениваемая по повышенному соотношению экскреции лактулозы и маннита, оставалась повышенной в течение 12 недель. У тех, у кого симптомы сохранялись через 12 месяцев после первоначальной инфекции, продолжалось резкое увеличение количества воспалительных клеток, особенно Т-лимфоцитов и макрофагов, что потенциально указывает на стойкую иммунную дисрегуляцию.22
Режимы питания и питательные вещества: ключевые участники барьерной функции
Следующие избранные питательные вещества жизненно важны для правильной барьерной функции. Поскольку различные провоспалительные цитокины и медиаторы, включая NF-каппа-B и липополисахарид, могут увеличивать проницаемость эпителиальных плотных соединений, диетические вмешательства, направленные на ослабление или устранение непропорциональной воспалительной реакции, также могут помочь поддерживать здоровый уровень проницаемости.
Поскольку различные провоспалительные цитокины и медиаторы, включая NF-каппа-B и липополисахарид, могут увеличивать проницаемость эпителиальных плотных соединений, диетические вмешательства, направленные на ослабление или устранение непропорциональной воспалительной реакции, также могут помочь поддерживать здоровый уровень проницаемости.
Пищевые волокна и роль бутирата
Ферментируемые пищевые волокна являются предпочтительным топливом для микробиоты в толстом кишечнике.В отсутствие адекватных источников ферментируемых углеводов микробиота кишечника расщепляет гликопротеины слизи в качестве вторичного источника топлива, разрушая защитный слизистый барьер. Ухудшение слизистой оболочки толстой кишки, в свою очередь, является фактором риска развития колита и патогенных инфекций23
В ответ на адекватное количество выбранных форм ферментируемой клетчатки определенные бактерии в микробиоме (например, Fecalibacterium prausnitzii , Roseburia Кишечник ) могут продуцировать короткоцепочечные жирные кислоты, включая бутират. 24 Бутират поддерживает функцию плотного барьера за счет влияния на белки плотных контактов и, как было показано, ингибирует активацию инфламмасомы NLRP3, индуцированную липополисахаридом. 24,25
24 Бутират поддерживает функцию плотного барьера за счет влияния на белки плотных контактов и, как было показано, ингибирует активацию инфламмасомы NLRP3, индуцированную липополисахаридом. 24,25
Цельные зерна и отруби из пшеницы, ржи и овса, богатые арабарабиноксиланом, стимулируют выработку бутирата, в то время как целлюлоза, ксилан и пектин вызывают низкий уровень бутирата26.
В исследовании 18 пожилых людей, страдающих диареей или запором, бета-глюкан из овса значительно снижал кишечную проницаемость у субъектов с симптомами желудочно-кишечного тракта.24 Вместе диета с высоким содержанием клетчатки и добавление бутирата натрия увеличивали количество белков плотных контактов в экспериментальной модели аутоиммунного гепатита27
В небольшой группе из 10 пациентов с болезнью Крона лечение F prausnitzii и смесью шести бактерий, продуцирующих бутират, значительно увеличило синтез бутирата и улучшило целостность эпителиального барьера in vitro. может объяснить положительное влияние средиземноморской диеты на симптомы ревматоидного артрита, аутоиммунная патология которого может усугубляться повышенной кишечной проницаемостью. 29
29
Витамин D
Дефицит витамина D связан с дисфункцией барьера, в то время как достаточный уровень витамина D может помочь восстановить функцию белков плотного соединения zonula occludens-1 (ZO-1) и клаудина-2.30. связан с более низкой активностью заболевания и длительной ремиссией при болезни Крона, что может быть связано с более низкими циркулирующими воспалительными маркерами и повышенным поддержанием чрезмерной кишечной проницаемости.31
Витамин A
Было показано, что витамин A усиливает белок плотных контактов маркеры, включая ZO-1, окклюдин и клаудин-1, и защищают от индуцированной липополисахаридом проницаемости кишечного эпителия.32
Цинк
Депривация цинка может вызвать нарушение эпителиального барьера из-за разрушения белков плотных контактов в клетках монослоя како-2.33 Более того, даже незначительный дефицит цинка может усилить пагубное влияние алкоголя на эпителиальный барьер. 34
34
In В исследовании с участием восьми здоровых спортсменов прием добавки карнозина цинка в дозе 37,5 мг два раза в день был связан с 70% снижением значений проницаемости, вызванной физической нагрузкой, после 14 дней лечения.35
Куркумин
Куркумин, противовоспалительное, биологически активное соединение, обнаруженное в куркуме, может быть особенно актуальным в качестве модулятора барьера во время острого инфекционного или вызванного физической нагрузкой барьерного стресса. Спортсмены, подвергшиеся повреждению желудочно-кишечного барьера, вызванному тепловым стрессом, из-за тренировок в жару получали 500 мг куркумина в день в течение трех дней. Уровни белков, связывающих жирные кислоты кишечника, измеряли до и после тренировки.
У тех, кто не получал куркумин, уровень белка, связывающего жирные кислоты кишечника, повышался на 87% до и после тренировки, в то время как уровень в группе куркумина увеличился только на 58%.36 Куркумин также защищает от дефицита барьера, вызываемого C jejuni 37.
Зеленый чай или EGCG
В модели ВЗК на мышах обработка EGCG (эпигаллокатехин галлат), полифенолом, обнаруженным в растениях, улучшала кишечную проницаемость, а также подавляла провоспалительные цитокины, включая IL-6, хемоаттрактантный белок-1 моноцитов. и TNF-альфа. 38
Омега-3 полиненасыщенные жирные кислоты
Когда потребление омега-3 является адекватным и пропорционально потреблению омега-6, омега-3 вырабатывают специальные провоспалительные медиаторы, известные как резолвины, протектины и марезины.Когда острое воспаление возникает в ответ на травму, теперь известно, что для предотвращения хронического воспаления необходимо активное рассасывание и очистка клеточного мусора. Специализированные провоспалительные медиаторы играют центральную роль в разрешении острого воспаления, включая ослабление цитокиновых ответов слизистых оболочек.39 Специализированные провоспалительные медиаторы также могут ослаблять передачу сигналов эндотоксинов (например, липополисахаридов) 40
Глютамин
Глютамин — это условно незаменимая аминокислота, которая потенциально может быть истощена в условиях метаболического стресса, таких как изнурительные упражнения, травмы, сепсис и ВЗК. 41-43
41-43
В одной из моделей экспериментальной гиперпроницаемости in vitro применение глутамина уменьшало гиперпроницаемость на 19% и 39% в соответствующих клеточных линиях.44 В другом исследовании после того, как активные самцы завершили 60-минутный пробег, наблюдалось значительное увеличение L: Соотношение R во всех испытаниях сравнивалось с измерениями в состоянии покоя перед пробежкой. Когда глютамин потреблялся в дозе 0,9 г / кг массы тела перед тренировкой в тех же условиях, наблюдалось умеренное снижение соотношения L: R после тренировки.45 Уменьшение отношения L: R также наблюдалось у пациентов с болезнью Крона с аномальными значениями проницаемости, которым давали 0,5 г / кг идеальной массы тела орального глютамина в течение двух месяцев 46
Диеты с высоким содержанием жиров
Было неоднократно показано, что диеты с высоким содержанием жиров являются факторами риска кишечной проницаемости, отчасти потому, что они влияют на развитие провоспалительной микробиоты кишечника. Однако эта часто упоминаемая связь, вероятно, связана с типами жиров и смягчающими диетическими факторами.
Однако эта часто упоминаемая связь, вероятно, связана с типами жиров и смягчающими диетическими факторами.
Еда с высоким содержанием насыщенных жиров может спровоцировать высвобождение липополисахаридов47; однако в одном исследовании после того, как 20 человек следовали средиземноморской диете (40% жира с акцентом на мононенасыщенные жиры и <10% насыщенных жиров) в течение 16 недель, увеличения кишечной проницаемости не наблюдалось.48
Полифенолы
Полифенолы могут играть роль в защите от диеты с высоким содержанием жиров. В модели на животных исследователи кормили мышей жирной (сало) диетой в течение 15 недель.Диета вызвала инсулинорезистентность и была связана с повышенной проницаемостью кишечника, снижением экспрессии белков плотного соединения подвздошной кишки и эндотоксемией. Однако добавление диетического (-) — эпикатехина в дозе от 2 до 20 мг / кг массы тела смягчало все эти побочные эффекты.49
Другими соединениями или полифенолами, заслуживающими внимания, являются кверцетин, мирицетин и кемпферол, которые, как было показано, участвуют в регуляции кишечного барьера, способствуя более высокой экспрессии белков плотных контактов, включая клаудин-1. 29
29
Диеты с высоким содержанием сахара
Глюкоза и фруктоза транспортируются к эпителию кишечника посредством облегченной диффузии, где эти сахара абсорбируются через мембраны с помощью транспортеров SGLT1 и GLUT2. Для повышения уровня облегченной диффузии форма плотных контактов может измениться, чтобы приспособиться к увеличенному прохождению абсорбированных сахаров. Эти изменения могут способствовать снижению защитных сил кишечника.
Перейра и его коллеги изучали влияние абсорбции сахара на модели совместного культивирования человека in vitro, в которой изучались определенные эпителиальные клетки вне человеческого тела.Когда клетки подвергались воздействию высоких концентраций сахара, сниженные уровни фактора защиты слизистой оболочки (кишечная щелочная фосфатаза) наблюдались в экспонированных клетках.50 В модели на мышах гипергликемия приводила к дисфункции кишечного барьера, но только у мышей, у которых был переносчик GLUT2. .51
Употребление алкоголя
Дозозависимое потребление алкоголя может влиять на здоровье слизистой оболочки кишечника двумя способами: снижая уровень окклюдина в толстой кишке и вызывая дисбиотическую микробиоту, вызванную алкоголем, что коррелирует с высоким уровнем эндотоксина. 52
52
В ходе исследования на крысах исследователи обнаружили, что повышенная проницаемость кишечника, окислительное повреждение кишечника и эндотоксемия наблюдались через две недели при ежедневном потреблении алкоголя.53 Всего одна неделя умеренного потребления красного вина среди 21 человека с неактивным ВЗК была связана с значительное снижение кальпротектина в стуле и значительное увеличение кишечной проницаемости 54
Глиадин
Глиадин, класс белков, обнаруженных в пшенице, ячмене и ржи, может запускать высвобождение зонулина путем связывания с рецептором CXCR3, который сверхэкспрессируется на апикальной поверхности энтероцитов у пациентов с глютеновой болезнью.12 Высвобождение зонулина также наблюдалось при нечувствительности к глютену без глютена.55
Используя TEER, Холлон и его коллеги проанализировали кишечную проницаемость эксплантатов биопсии двенадцатиперстной кишки при целиакии (как активной, так и в стадии ремиссии). Они также проанализировали проницаемость для нечувствительности к глютену без глютена и контрольной группы без глютена. После воздействия глиадина увеличение проницаемости наблюдалось во всех группах, с наибольшим увеличением у пациентов с активной глютеновой болезнью и нечувствительностью к глютену, не связанным с целиаком.56,57
После воздействия глиадина увеличение проницаемости наблюдалось во всех группах, с наибольшим увеличением у пациентов с активной глютеновой болезнью и нечувствительностью к глютену, не связанным с целиаком.56,57
Могут ли помочь пробиотики?
Точно так же, как некоторые питательные вещества и режимы питания могут способствовать правильному функционированию барьерной стенки, также можно выбирать виды пробиотиков, уменьшая медиаторы воспаления или усиливая защитный слой слизи.
В рандомизированном двойном слепом плацебо-контролируемом исследовании на людях с ожирением экскреция сукралозы была снижена как при приеме Bifidobacterium lactis BB-12, так и при добавлении пребиотиков с галактоолигосахаридами, что указывает на улучшение проницаемости толстой кишки.58 Среди 11 физически активных мужчин, получавших многовидовые пробиотики (Ecologic Performance или OMNi-BiOTiC POWER) в течение 14 недель, уровни зонулина после интенсивной езды на велосипеде снизились. 59 Однако в другом исследовании с использованием Ecologic Barrier, которое содержит восемь различных штаммов пробиотиков, исследователи не заметили никакой разницы. по проницаемости кишечника 60
59 Однако в другом исследовании с использованием Ecologic Barrier, которое содержит восемь различных штаммов пробиотиков, исследователи не заметили никакой разницы. по проницаемости кишечника 60
В недавнем обзоре Ван и его коллег обсуждались следующие дополнительные виды бактерий как потенциально поддерживающие барьерную функцию: Lactobacillus plantarum , Lactobacillus casei , Lactobacillus brevis , Bifidobacterium infantis , Lactobacillus Gantobacillus , r. plantarum МБ452.61 В группе из 30 пациентов с СРК-Д, получавших ферментированное молоко ( Streptococcus thermophilus , Lactobacillus bulgaricus , Lactobacillus acidophilus и Bifidobacterium longum ) в течение четырех недель, проницаемость малой чаши кишечника снизилась, но не уменьшилась. значительно по сравнению с исходным уровнем 62
Как и в случае с любыми другими проблемами или состояниями, пробиотические штаммы следует выбирать с учетом их конкретных преимуществ, поскольку не все пробиотические штаммы будут эффективны для улучшения барьерной функции.
Рекомендации по консультированию
Диетологи, которые консультируют клиентов и пациентов, у которых могут быть различные расстройства пищеварения, связанные с плохой барьерной функцией кишечника, могут помочь им интегрировать факторы питания и образа жизни, которые могут поддерживать здоровый микробиом. Рекомендуем клиентам сделать следующее:
• Придерживайтесь средиземноморской диеты, богатой полифенолами и безглютеновой.
• Сведите к минимуму употребление алкоголя.
• Обеспечьте частое употребление разнообразных ферментируемых источников углеводов.
• Оценка бактерий, продуцирующих бутират; при необходимости рассмотрите возможность добавления бутирата.
• Измерьте статус EPA и DHA; подумайте о добавлении рыбьего жира или специализированных провоспалительных медиаторов.
• Измерьте и исправьте статус витамина D.
• Обеспечьте адекватное потребление ретинола или бета-каротина; если вы сильно полагаетесь на бета-каротин, подумайте об оценке генетической способности превращать бета-каротин в ретинол.
• Рассмотрите возможность приема добавок карнозина цинка и / или глютамина.
• Рассмотрите возможность использования куркумы в продуктах питания, напитках и закусках или добавлении куркуминоидов в системы доставки фосфолипидов для повышения биодоступности.
— Сара Томсен Феррейра, MS, MPH, RD, CDN, IFNCP, CHWC, является менеджером по лечебному питанию в Клиническом центре функциональной медицины Кливленда в Огайо. Она также ведет подкаст Nourished Brain , в котором рассказывается о еде, настроении, здоровье мозга, психологии питания и искусстве преднамеренного приема пищи.Дополнительную информацию можно получить по телефону sarahferreirard.com .
Список литературы
1. Мартини Э., Круг С.М., Зигмунд Б., Нейрат М.Ф., Беккер С. Исправьте свои препятствия: эпителиальный барьер и его связь с иммунитетом слизистой оболочки при воспалительном заболевании кишечника. Cell Mol Gastroenterol Hepatol . 2017; 4 (1): 33-46.
2017; 4 (1): 33-46.
2. Günzel D, Yu AS. Клаудин и модуляция проницаемости плотных стыков. Physiol Ред. .2013; 93 (2): 525-569.
3. France MM, Turner JR. Краткий обзор слизистого барьера. J Cell Sci . 2017; 130 (2): 307-314.
4. Hansson GC, Johansson ME. Внутренний из двух слоев слизи, зависящей от Muc2 в толстой кишке, лишен бактерий. Кишечные микробы . 2010; 1 (1): 51-54.
5. Эйссеннаггер Н., ван дер Меер Р., ван Мил SWC. Сульфид как разрушитель слизистого барьера при воспалительном заболевании кишечника? Trends Mol Med .2016; 22 (3): 190-199.
6. Альберт-Байо М., Паракуэльос I, Гонсалес-Кастро А.М. и др. Тучные клетки слизистой оболочки кишечника: ключевые модуляторы барьерной функции и гомеостаза. Ячейки . 2019; 8 (2): E135.
7. Абдельхамид Л., Луо XM. Ретиноевая кислота, повышенная кишечная проницаемость и аутоиммунные заболевания. Питательные вещества . 2018; 10 (8): E1016.
Питательные вещества . 2018; 10 (8): E1016.
8. Бьярнасон И., Макферсон А., Холландер Д. Кишечная проницаемость: обзор. Гастроэнтерология .1995; 108 (5): 1566-1581.
9. Wells JM, Brummer RJ, Derrien M, et al. Гомеостаз кишечного барьера и потенциальные биомаркеры. Am J Physiol Gastrointest Liver Physiol . 2017; 312 (3): G171-G193.
10. Лау Э., Маркес С., Пестана Д. и др. Роль I-FABP как биомаркера дисфункции кишечного барьера, обусловленной изменениями кишечной микробиоты при ожирении. Нутр Метаб (Лондон) . 2016; 13:31.
11. Сринивасан Б., Колли А.Р., Эш М.Б., Абачи Х.Э., Шулер М.Л., Хикман Дж. Дж.Методы измерения TEER для модельных систем барьеров in vitro. Дж. Лаборатория Автомат . 2015; 20 (2): 107-126.
12. Sturgeon C, Fasano A. Зонулин, регулятор эпителиальных и эндотелиальных барьерных функций, и его участие в хронических воспалительных заболеваниях. Тканевые барьеры . 2016; 4 (4): e1251384.
Тканевые барьеры . 2016; 4 (4): e1251384.
13. Ciccia F, Guggino G, Rizzo A, et al. Дисбиоз и повышенная регуляция зонулина изменяют эпителиальный и сосудистый барьеры кишечника у пациентов с анкилозирующим спондилитом. Энн Рум Дис . 2017; 76 (6): 1123-1132.
14. Сингх П., Сильвестр Дж., Чен Х и др. Зонулин в сыворотке повышен при СРК и коррелирует с частотой стула при СРК-Д. United European Gastroenterol J . 2019; 7 (5): 709-715.
15. Bischoff SC, Barbara G, Buurman W, et al. Кишечная проницаемость — новая цель для профилактики и лечения заболеваний. БМК Гастроэнтерол . 2014; 14: 189.
16. Люеттиг Дж., Розенталь Р., Бармейер С., Шульцке Дж. Д..Клаудин-2 как медиатор непроницаемого кишечного барьера при воспалении кишечника. Тканевые барьеры . 2015; 3 (1-2): e977176.
17. Блэр С.А., Кейн С.В., Клейбург Д. Р., Тернер-младший. Экспрессия и активность киназы легкой цепи эпителиального миозина повышаются при воспалительном заболевании кишечника. Лаб Инвест . 2006; 86 (2): 191-201.
Р., Тернер-младший. Экспрессия и активность киназы легкой цепи эпителиального миозина повышаются при воспалительном заболевании кишечника. Лаб Инвест . 2006; 86 (2): 191-201.
18. Фридрих М., Похин М., Паури Ф. Цитокиновые сети в патофизиологии воспалительных заболеваний кишечника. Иммунитет . 2019; 50 (4): 992-1006.
19. Miele E, Pascarella F, Quaglietta L, et al. Изменение кишечной проницаемости является предиктором раннего рецидива у детей со стероид-зависимым язвенным колитом. Алимент Фармакол Тер . 2007; 25 (8): 933-939.
20. Первый пациент получил дозу в первом в истории клиническом испытании фазы 3 по поводу целиакии. Веб-сайт Фонда целиакии. https://celiac.org/about-the-foundation/featured-news/2019/08/first-patient-dosed-in-first-ever-phase-3-clinical-trial-for-celiac-disease/.Опубликовано 15 августа 2019 г.
21. Кастильо, NE, Theethira TG, Leffler DA. Настоящее и будущее в диагностике и лечении целиакии. Гастроэнтерол Реп (Oxf) . 2015; 3 (1): 3-11.
Гастроэнтерол Реп (Oxf) . 2015; 3 (1): 3-11.
22. Spiller RC, Jenkins D, Thornley JP, et al. Увеличение энтероэндокринных клеток слизистой оболочки прямой кишки, Т-лимфоцитов и повышенная проницаемость кишечника после острого энтерита, вызванного кампилобактером, и постдизентерийного синдрома раздраженного кишечника. Кишка .2000; 47 (6): 804-811.
23. Десаи М.С., Сикатц А.М., Коропаткин Н.М. и др. Микробиота кишечника, лишенная пищевых волокон, разрушает слизистый барьер толстой кишки и повышает восприимчивость к патогенам. Ячейка . 2016; 167 (5): 1339-1353.e21.
24. Бах Кнудсен KE, Lærke HN, Hedemann MS, et al. Влияние регулируемого диетой производства бутирата на функцию кишечного барьера и воспаление. Питательные вещества . 2018; 10 (10): E1499.
25. Плёгер С., Штумпфф Ф., Пеннер Г.Б. и др.Микробный бутират и его роль в барьерной функции желудочно-кишечного тракта. Ann N Y Acad Sci . 2012; 1258: 52-59.
Ann N Y Acad Sci . 2012; 1258: 52-59.
26. Feng Y, Wang Y, Wang P, Huang Y, Wang F. Короткоцепочечные жирные кислоты проявляют стимулирующее и защитное действие на барьерную функцию кишечника за счет ингибирования NLRP3 инфламмасомы и аутофагии. Cell Physiol Biochem . 2018; 49 (1): 190-205.
27. Hu ED, Chen DZ, Wu JL, et al. Диета с высоким содержанием клетчатки и бутират натрия ослабляют экспериментальный аутоиммунный гепатит за счет регуляции иммунных регуляторных клеток и кишечного барьера. Клеточный иммунол . 2018; 328: 24-32.
28. Geirnaert A, Calatayud M, Grootaert C, et al. Бактерии, продуцирующие бутират, добавленные in vitro к микробиоте пациентов с болезнью Крона, увеличивают продукцию бутирата и улучшают целостность кишечного эпителиального барьера. Научный представитель . 2017; 7 (1): 11450.
29. Guerreiro CS, Calado Â, Sousa J, Fonseca JE. Диета, микробиота и проницаемость кишечника — неизвестная триада при ревматоидном артрите. Фронт Мед (Лозанна) . 2018; 5: 349.
Диета, микробиота и проницаемость кишечника — неизвестная триада при ревматоидном артрите. Фронт Мед (Лозанна) . 2018; 5: 349.
30. Ли К., Лау Е., Чусилп С. и др. Защитные эффекты витамина D от повреждения эпителия кишечника. Педиатр Хирург Инт . 2019; 35 (12): 1395-1401.
31. Рафтери Т., Мартино А.Р., Грейлер С.Л. и др. Влияние добавок витамина D на кишечную проницаемость, кателицидин и маркеры болезни при болезни Крона: результаты рандомизированного двойного слепого плацебо-контролируемого исследования. United European Gastroenterol J . 2015; 3 (3): 294-302.
32. He C, Deng J, Hu X и др. Витамин А подавляет действие ЛПС на барьерную функцию кишечного эпителия и белки плотных контактов. Продовольственная функция . 2019; 10 (2): 1235-1242.
33. Miyoshi Y, Tanabe S, Suzuki T. Клеточный цинк необходим для поддержания кишечного эпителиального барьера посредством регуляции экспрессии клаудина-3 и окклюдина. Am J Physiol Gastrointest Liver Physiol .2016; 311 (1): G105-G116.
Am J Physiol Gastrointest Liver Physiol .2016; 311 (1): G105-G116.
34. Чжун В., Макклейн С.Дж., Кейв М., Кан Ю.Дж., Чжоу З. Роль дефицита цинка в вызванной алкоголем дисфункции кишечного барьера. Am J Physiol Gastrointest Liver Physiol . 2010; 298 (5): G625-G633.
35. Гуо С., Нигхот М., Аль-Сади Р., Алхмуд Т., Нигхот П., Ма Т.Ю. Липополисахаридная регуляция проницаемости плотных контактов кишечника опосредуется активацией пути передачи сигнала TLR4 FAK и MyD88. Дж Иммунол .2015; 195 (10): 4999-5010.
36. Шимански М.С., Гиллум Т.Л., Гулд Л.М., Морин Д.С., Куеннен М.Р. Кратковременное диетическое добавление куркумина снижает повреждение желудочно-кишечного барьера и реакцию физиологического напряжения во время теплового стресса при физической нагрузке. J Appl Physiol (1985) . 2018; 124 (2): 330-340.
37. Лобо де Са Ф. Д., Буткевич Э., Наттрамиларасу П. К. и др. Куркумин смягчает иммунно-индуцированную дисфункцию эпителиального барьера, вызванную Campylobacter jejuni. Int J Mol Sci .2019; 20 (19): E4830.
К. и др. Куркумин смягчает иммунно-индуцированную дисфункцию эпителиального барьера, вызванную Campylobacter jejuni. Int J Mol Sci .2019; 20 (19): E4830.
38. Du Y, Ding H, Vanarsa K, et al. Низкая доза эпигаллокатехина галлата облегчает экспериментальный колит, подавляя воспалительные клетки и цитокины и улучшая кишечную проницаемость. Питательные вещества . 2019; 11 (8): E1743.
39. Ван RX, Colgan SP. Особые действия про-разрешающего медиатора (SPM) в регуляции воспаления желудочно-кишечного тракта и иммунных реакций слизистой оболочки кишечника. Мол Аспект Мед . 2017; 58: 93-101.
40. Серхан К.Н., Чанг Н., Ван Дайк Т.Э. Устранение воспаления: двойные противовоспалительные и липидные медиаторы, способствующие разрешению. Нат Рев Иммунол . 2008; 8 (5): 349-361.
41. Ван Б., Ву Г., Чжоу З. и др. Глютамин и кишечная барьерная функция. Аминокислоты . 2015; 47 (10): 2143-2154.
2015; 47 (10): 2143-2154.
42. Кастелл Л.М., Ньюсхолм Е.А. Связь между глутамином и иммунодепрессией, наблюдаемой при физических упражнениях. Аминокислоты .2001; 20 (1): 49-61.
43. Li N, Neu J. Депривация глутамина изменяет плотные контакты кишечника посредством пути, опосредованного PI3-K / Akt в клетках Caco-2. J Nutr . 2009; 139 (4): 710-714.
44. Vermeulen MA, de Jong J, Vaessen MJ, van Leeuwen PA, Houdijk AP. Глутамат снижает экспериментальную кишечную проницаемость и способствует поддержанию целостности кишечника глутамином. Мир Дж. Гастроэнтерол . 2011; 17 (12): 1569-1573.
45.Пью Дж. Н., Сейдж С., Хатсон М. и др. Добавка глутамина снижает маркеры кишечной проницаемости во время бега в жару в зависимости от дозы. Eur J Appl Physiol . 2017; 117 (12): 2569-2577.
46. Бенджамин Дж., Махария Г., Ахуджа В. и др. Глютамин и сывороточный белок улучшают проницаемость и морфологию кишечника у пациентов с болезнью Крона: рандомизированное контролируемое исследование. Dig Dis Sci . 2012; 57 (4): 1000-1012.
Dig Dis Sci . 2012; 57 (4): 1000-1012.
47.Лайт Дж. М., Габлер Н. К., Холлис Дж. Х. Постпрандиальный сывороточный эндотоксин у здоровых людей модулируется диетическим жиром в рандомизированном контролируемом перекрестном исследовании. Липиды Здоровье Dis . 2016; 15 (1): 186.
48. Биолато М., Манка Ф, Марроне Дж. И др. Кишечная проницаемость после средиземноморской диеты и диеты с низким содержанием жиров при неалкогольной жировой болезни печени. Мир Дж. Гастроэнтерол . 2019; 25 (4): 509-520.
49. Cremonini E, Wang Z, Bettaieb A, et al.(-) — Эпикатехин защищает кишечный барьер от пермеабилизации, вызванной диетой с высоким содержанием жиров: последствия для стеатоза и инсулинорезистентности. Редокс Биол . 2018; 14: 588-599.
50. Перейра М. Т., Малик М., Ностро Дж. А., Малер Г. Дж., Массельман Л. П.. Влияние пищевых добавок на проницаемость кишечника как у дрозофилы, так и у совместных культур клеток человека. Dis Модель Mech . 2018; 11 (12): dmm034520.
Dis Модель Mech . 2018; 11 (12): dmm034520.
51. Thaiss CA, Levy M, Grosheva I, et al.Гипергликемия вызывает дисфункцию кишечного барьера и риск кишечной инфекции. Наука . 2018; 359 (6382): 1376-1383.
52. Mir H, Meena AS, Chaudhry KK, et al. Дефицит окклюдина способствует индуцированному этанолом разрушению эпителиальных соединений толстой кишки, дисфункции кишечного барьера и повреждению печени у мышей. Biochim Biophys Acta . 2016; 1860 (4): 765-774.
53. Кешаварзян А., Фархади А., Форсайт CB и др. Доказательства того, что хроническое воздействие алкоголя способствует окислительному стрессу кишечника, повышенной проницаемости кишечника и эндотоксемии до развития алкогольного стеатогепатита у крыс. J Hepatol . 2009; 50 (3): 538-547.
54. Swanson GR, Tieu V, Shaikh M, Forsyth C, Keshavarzian A. Безопасно ли умеренное потребление красного вина при неактивном воспалительном заболевании кишечника? Пищеварение . 2011; 84 (3): 238-244.
2011; 84 (3): 238-244.
55. Драго С., Эль-Асмар Р., Ди Пьерро М. и др. Глиадин, зонулин и проницаемость кишечника: воздействие на слизистую оболочку кишечника и линии кишечных клеток при целиакии и без целиакии. Сканд Дж Гастроэнтерол .2006; 41 (4): 408-419.
56. Холлон Дж., Пуппа Э.Л., Гринвальд Б., Голдберг Э., Геррерио А., Фазано А. Влияние глиадина на проницаемость эксплантатов кишечной биопсии от пациентов с глютеновой болезнью и пациентов с нечувствительностью к глютену без целиакии. Питательные вещества . 2015; 7 (3): 1565-1576.
57. Leccioli V, Oliveri M, Romeo M, Berretta M, Rossi P. Новое предложение о патогенетическом механизме нецелиакии / неаллергической чувствительности к глютену / пшенице: собирая воедино головоломку последних научных данных. Питательные вещества . 2017; 9 (11): E1203.
58. Krumbeck JA, Rasmussen HE, Hutkins RW, et al. Пробиотические штаммы Bifidobacterium и галактоолигосахариды улучшают барьерную функцию кишечника у взрослых с ожирением, но не проявляют синергизма при совместном использовании в качестве синбиотиков. Микробиом . 2018; 6 (1): 121.
Микробиом . 2018; 6 (1): 121.
59. Лампрехт М., Богнер С., Шиппингер Г. и др. Прием пробиотиков влияет на маркеры кишечного барьера, окисления и воспаления у тренированных мужчин; рандомизированное двойное слепое плацебо-контролируемое исследование. J Int Soc Sports Nutr . 2012; 9 (1): 45.
60. Wilms E, Gerritsen J, Smidt H, et al. Влияние добавок синбиотика Ecologic® 825 / FOS P6 на функцию кишечного барьера у здоровых людей: рандомизированное контролируемое исследование. PLoS One . 2016; 11 (12): e0167775.
61. Хорват А., Лебер Б., Шмербок Б. и др. Рандомизированное клиническое испытание: влияние многовидового пробиотика по сравнению с плацебо на врожденную иммунную функцию, бактериальную транслокацию и проницаемость кишечника у пациентов с циррозом. Алимент Фармакол Тер . 2016; 44 (9): 926-935.
62. Цзэн Дж., Ли YQ, Цзо XL, Чжэнь Ю.Б., Ян Дж. , Лю Ч. Клинические испытания: влияние активных молочнокислых бактерий на барьерную функцию слизистой оболочки у пациентов с синдромом раздраженного кишечника с преобладанием диареи. Алимент Фармакол Тер . 2008; 28 (8): 994-1002.
, Лю Ч. Клинические испытания: влияние активных молочнокислых бактерий на барьерную функцию слизистой оболочки у пациентов с синдромом раздраженного кишечника с преобладанием диареи. Алимент Фармакол Тер . 2008; 28 (8): 994-1002.
Что есть для лучшего управления
Термин «дырявый кишечник» может сбивать с толку и даже вызывать споры. Название иногда используется для описания конкретного заболевания, связанного с кишечной проницаемостью.Однако этот термин также используется для описания так называемого «синдрома дырявого кишечника». Хотя это популярно в альтернативной медицине, медики не признают синдром дырявого кишечника заболеванием или действительным диагнозом.
Если ваш врач использует термин «дырявый кишечник», чтобы помочь вам понять заболевание, он, скорее всего, имеет в виду повышенную проницаемость кишечника. Однако этот контекст отличается от теоретического «синдрома дырявого кишечника».
Если ваш врач подозревает, что у вас повышенная проницаемость кишечника из-за хронического заболевания пищеварительной системы, изменение диеты может быть частью вашего плана лечения. Многие люди с воспалительным заболеванием кишечника обнаруживают, что то, что они едят, может существенно повлиять на их симптомы.
Многие люди с воспалительным заболеванием кишечника обнаруживают, что то, что они едят, может существенно повлиять на их симптомы.
Специфической диеты «дырявого кишечника», рекомендованной медицинскими работниками, не существует. Некоторые общие диетические рекомендации могут помочь вам справиться с основным заболеванием, которое его вызвало.
Транг Доан / ПекселсПреимущества
«Синдром дырявого кишечника» не является признанным заболеванием. Тем не менее, те, кто предполагал, что это способствует ухудшению здоровья, часто предлагают диетические меры в качестве средства «лечения», но эти методы лечения не основаны на доказательствах.
Тем не менее, повышенная проницаемость кишечника, вызванная воспалительным заболеванием желудочно-кишечного тракта, может выиграть от определенных диетических изменений. Например, исследования показали, что когда люди с глютеновой болезнью перестают есть глютен, это может помочь восстановить слизистый барьер их кишечной стенки.
Люди с болезнью Крона могут уменьшить обострения болезни, соблюдая диету, которая не увеличивает воспаление кишечника и способствует заживлению пищеварительной системы. Независимо от того, действуют ли эти изменения конкретно на проницаемость кишечника или нет, было показано, что они помогают улучшить симптомы желудочно-кишечных расстройств.
Одна из основных задач вашего кишечника — поглощать воду и питательные вещества из того, что вы едите. В то же время ваш кишечник обеспечивает защитный барьер, не позволяющий бактериям и побочным продуктам попадать в кровоток. Процесс регулируется размером щелей (стыков) в стенке кишечника.
Если промежутки становятся слишком большими, ваш кишечник не может хорошо всасывать, и этот защитный барьер оказывается под угрозой. Если ненужные вещества из кишечника попадают в кровоток, это может вызвать проблемы во всем организме.
Исследователи изучают роль специфического белка, называемого зонулином, который, как известно, помогает регулировать размер промежутков. Исследование все еще относительно новое, поскольку белок был открыт только в 2000 году. Несколько исследований связали повышенный уровень зонулина с такие состояния, как глютеновая болезнь и диабет 1 типа, подразумевая, что они могут играть роль в аутоиммунных реакциях.
Исследование все еще относительно новое, поскольку белок был открыт только в 2000 году. Несколько исследований связали повышенный уровень зонулина с такие состояния, как глютеновая болезнь и диабет 1 типа, подразумевая, что они могут играть роль в аутоиммунных реакциях.
Люди с определенными желудочно-кишечными заболеваниями чаще испытывают повышенную кишечную проницаемость.Воспалительные заболевания кишечника, такие как болезнь Крона и язвенный колит, повреждают слизистую оболочку кишечника, что может привести к ослаблению соединений.
Недостаточно доказательств, подтверждающих утверждения о том, что «дырявый кишечник» — это синдром сам по себе. Исследования не подтвердили утверждения о том, что негерметичный кишечник вызывает другие заболевания (включая психическое здоровье и неврологические состояния, такие как аутизм).
Сторонники «синдрома дырявого кишечника» утверждают, что он вызывает «мозговой туман», неясное воспаление и множество других симптомов. Однако большинство медицинских работников опровергают идею о том, что повышенная кишечная проницаемость может вызывать симптомы.
Однако большинство медицинских работников опровергают идею о том, что повышенная кишечная проницаемость может вызывать симптомы.
Исследователи также не уверены, что повышенная кишечная проницаемость представляет собой медицинскую проблему. Если да, то не ясно, как это следует лечить и нужно ли вообще лечить.
Исследование 2013 года показало, что повышенная проницаемость иногда может быть полезной. Например, если она позволяет кишечнику поглощать больше воды и питательных веществ для удовлетворения потребностей организма.
Как это работает
План питания для уменьшения желудочно-кишечных симптомов и улучшения здоровья пищеварительной системы может основываться на диетах, используемых для лечения ВЗК, синдрома раздраженного кишечника и пищевой аллергии.
Диетические соображения для людей с диабетом 1 типа также могут быть полезны, поскольку исследования показали, что изменение проницаемости кишечника может быть связано с этим состоянием.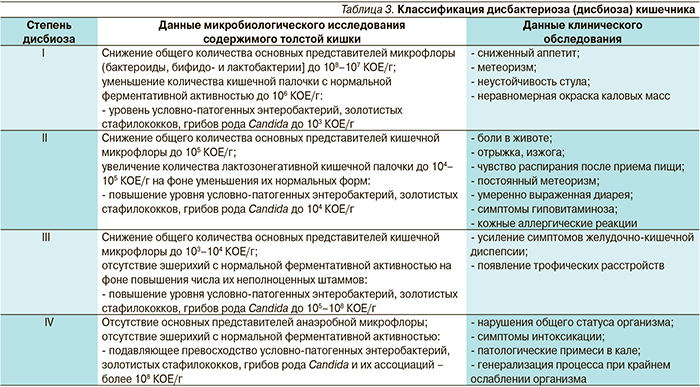
Каждый может получить пользу от сбалансированной и питательной диеты, но то, что вы выбираете, имеет еще большее значение, если ваше пищеварение не функционирует оптимально. Когда вы разрабатываете диету с дырявым кишечником, сосредоточьтесь на продуктах, которые обеспечивают энергию и питание, не напрягая пищеварительную систему.
Продолжительность
Если вы используете диету с повышенной кишечной проницаемостью для лечения расстройства пищеварения, внесение постоянных изменений может помочь вам лучше справиться с симптомами.Соблюдение определенной диеты, исключающей «провоцирующие» продукты, может помочь предотвратить обострение симптомов.
С другой стороны, вы можете решить, что вам нужно следовать определенному плану питания только при появлении симптомов. Это обеспечивает кратковременное облегчение и дает вашему телу время на восстановление.
Что есть
Вы можете начать с общих рекомендаций и адаптировать свой конкретный план питания в соответствии со своими вкусами, потребностями и предпочтениями. Возможно, вам будет полезно поработать с врачом, диетологом или диетологом.
Возможно, вам будет полезно поработать с врачом, диетологом или диетологом.
Если у вас расстройство пищеварения, ваш врач может дать конкретные рекомендации или дать вам правила относительно того, что вы можете есть в рамках лечения. Вы должны внимательно следовать их инструкциям и поговорить с ними, прежде чем вносить какие-либо изменения в свой рацион.
Совместимые продуктыФрукты и овощи (приготовленные, если недопустимо сырые)
Куриная грудка или грудка индейки без кожи, нежирная свинина
Жирная рыба (лосось, тунец, сельдь)
Супы, костный бульон
кисломолочные продукты и заменители молока (в зависимости от переносимости)
Обезжиренный сыр
Тофу, темпе, заменители мяса
Паста (избегайте безглютеновых версий, приготовленных из фасоли / бобовых / кукурузы, если вызывает симптомы)
Орехи и гладкая ореховая паста
Хлеб на закваске, зерна без глютена, цельнозерновые в соответствии с допуском
Горячие каши, крупы, овсяные пакеты без добавления сахара
Нежирный йогурт без добавления сахара
Лен, чиа, другие семена (при переносе)
Ферментированные продукты, богатые пробиотиками (йогурт, чайный гриб, кефир)
Вода, кокосовая вода, фруктовый сок без сахара, горячий или холодный чай
Фасоль, бобовые, кукуруза, крестоцветные овощи
Сырые фрукты и овощи с кожурой и семенами (при наличии симптомов)
Отруби, хлопья или мюсли с орехами / фруктами, сухофруктами
Жирные, жирные, острые или жареные продукты
Обед, мясные полуфабрикаты (хот-доги, колбаса)
Полножирные молочные продукты
Пирожные, торты, печенье, конфеты, шоколад
Заменители сахара, такие как ксилит и сорбитол
Цельнозерновой хлеб, макароны, крекеры (при наличии симптомов)
Крутые жирные куски мяса
Коричневый, мультизерновой или дикий рис, рисовый плов (при наличии симптомов)
Обработанные закуски и десерты, рафинированные углеводы и сахар
Сода, энергетические напитки
Кофе и чай с кофеином (переносимые)
Спирт
Фрукты и овощи: Сырые фрукты и овощи богаты клетчаткой, что может быть проблемой для вас, если у вас заболевание пищеварения. Если у вас есть симптомы при употреблении их в сыром виде, попробуйте очистить, измельчить и приготовить фрукты и овощи, чтобы улучшить их усвояемость.
Если у вас есть симптомы при употреблении их в сыром виде, попробуйте очистить, измельчить и приготовить фрукты и овощи, чтобы улучшить их усвояемость.
Такие овощи, как картофель, легко размягчаются, они универсальны по консистенции и вкусу. Фрукты с низким содержанием клетчатки можно добавлять в соковыжималку или делать пюре для смузи.
Вы можете ограничить или избегать фруктов и овощей с высоким содержанием клетчатки, таких как кукуруза, брокколи и чернослив, которые, как известно, вызывают газообразование.
Зерна: Выбор цельного зерна вместо очищенных зерен обычно является более здоровым вариантом, но если вам трудно переваривать клетчатку, это не всегда может быть самым удобным вариантом.
Если у вас есть симптомы пищеварения, выбор мягких углеводов, которые легко перевариваются, успокаивает и дает вашему пищеварению шанс восстановиться. Белый рис вместо коричневого — один из вариантов, как и простой хлеб на закваске для тостов, а не мультизерновой или пшеничный.
Горячие хлопья, крупы и овсяные хлопья без добавления сахара — это основные продукты для завтрака, которые легко переваривать и готовить. Просто следите за добавками, такими как орехи и сухофрукты, которые могут быть триггерами пищи, если у вас есть определенные проблемы с пищеварением.
Молочные продукты: Некоторые люди с расстройствами пищеварения считают, что молочные продукты, как правило, ухудшают их симптомы, даже если у них нет строгой непереносимости лактозы. Вы можете поэкспериментировать с молочными заменителями молока, сыра и йогурта. Йогурт особенно полезен, если вы пытаетесь улучшить свое пищеварение, поскольку он является богатым источником пробиотиков. Некоторые теории предполагают, что сбалансированная микрофлора кишечника может помочь улучшить проницаемость кишечника.
Белок: Нежирный белок, такой как куриная грудка или грудка индейки без кожи, легко приготовить и переварить.Жирная рыба, такая как лосось, — еще один вариант приготовления, который хорошо подходит для диеты с дырявым кишечником. Только не пережаривайте мясо, так как это может затруднить пережевывание (и переваривание) волокон.
Только не пережаривайте мясо, так как это может затруднить пережевывание (и переваривание) волокон.
Яйца — еще один источник белка, который можно готовить различными способами и который хорошо сочетается с другими питательными продуктами. Сами по себе яйца также содержат много белка для небольшой порции.
Если вы не едите продукты животного происхождения, то тофу и темпе — универсальные альтернативы. Фасоль и бобовые являются важным источником белка для растительной диеты, но они с большей вероятностью, чем другие источники, вызывают газообразование.
Точно так же некоторые люди с расстройствами пищеварения обнаруживают, что высокое содержание жиров в орехах и ореховой пасте затрудняет переваривание этих источников белка. Вы можете поэкспериментировать с небольшими порциями определенных орехов и гладкого сливочного масла, чтобы увидеть, какие из них вам подходят.
Независимо от того, готовите ли вы мясо или заменители мяса, избегайте или ограничивайте использование жирных или потенциально раздражающих масел, сливочного масла и специй.
Десерты: Большинство основных ингредиентов десертов содержат много жира и сахара, что означает, что печенье, торты, выпечка, а также молочные десерты могут вызывать раздражение.
Если вы пытаетесь сократить потребление сахара, имейте в виду, что популярные заменители сахара, такие как сорбит и ксилит, вызывают у некоторых людей расстройство пищеварения. Скорее всего, вы найдете эти ингредиенты в жевательной резинке и леденцах с маркировкой «без сахара».
Некоторые сторонники «синдрома дырявого кишечника» рекомендуют избегать дрожжей, которые, по их мнению, приводят к их чрезмерному разрастанию. Однако тип дрожжей, используемых в выпечке или пивоварении, отличается от дрожжей Candida albicans , которые связаны с дрожжами. инфекции и избыточный бактериальный рост тонкой кишки (СИБР).
Напитки: Правильная гидратация важна для здоровья пищеварительной системы в целом, особенно если кишечная проницаемость не работает должным образом. Некоторые люди считают кофеин из кофе и чая раздражающим и предпочитают избегать употребления этих напитков или ограничивать их употребление. Газированные напитки, такие как сельтерская вода, могут быть нормальными, если они не вызывают дискомфортное газообразование.
Некоторые люди считают кофеин из кофе и чая раздражающим и предпочитают избегать употребления этих напитков или ограничивать их употребление. Газированные напитки, такие как сельтерская вода, могут быть нормальными, если они не вызывают дискомфортное газообразование.
Исследования показали, что алкоголь может увеличить кишечную проницаемость. Вы можете ограничить употребление алкогольных напитков или полностью отказаться от них.
По большей части придерживайтесь воды. Вы можете украсить его нарезанными фруктами и веточками мяты или имбиря, успокаивающими пищеварение. Горячие напитки, такие как костный бульон, — еще один питательный и успокаивающий вариант.
Ваш врач может порекомендовать напитки, заменяющие электролиты, если у вас диарея. Если вам также трудно получить правильное питание, они могут порекомендовать жидкие пищевые или калорийные добавки.
Рекомендуемое время
Некоторые люди с заболеваниями пищеварительной системы считают, что регулярное питание помогает контролировать их симптомы. Возможно, вы почувствуете себя лучше, если будете есть небольшими порциями чаще в течение дня, чем три раза в день.
Возможно, вы почувствуете себя лучше, если будете есть небольшими порциями чаще в течение дня, чем три раза в день.
Если у вашего кишечника проблемы с проницаемостью, возможно, он поглощает слишком много или недостаточно жидкости. Возможно, вам придется соответствующим образом скорректировать ежедневное потребление жидкости.
Если вы чувствуете себя слишком сытым, старайтесь есть и пить в разное время.
Советы по приготовлению
Есть несколько способов изменить еду, которую вы едите, приготовив ее.Можно отрегулировать их текстуру и консистенцию, не делая их менее питательными.
Людям с желудочно-кишечными заболеваниями иногда легче переваривать продукты с высоким содержанием клетчатки, например свежие овощи, если они размягчены путем варки или варки. Вы также можете попробовать бланшировать овощи (опустить их в кипящую воду на минуту или две). Это немного сложнее, но может быть полезно для предварительной подготовки ингредиентов, если вы планируете заморозить еду.
Другие продукты, богатые клетчаткой, также можно запечь или даже приготовить в микроволновой печи.Например, хрустящее яблоко с кожицей может быть трудно перевариваемым, но если вы очистите его и размягчите мякоть с помощью некоторого тепла, у вас будет вкусное яблочное пюре.
Вам следует избегать стилей приготовления, которые затрудняют переваривание пищи, например жарки на масле и сливочном масле. Вы также можете ограничить или избегать употребления специй и подсластителей, которые могут усугубить расстройство пищеварения у некоторых людей.
Ферментация — еще один популярный способ приготовления пищи и увеличения содержания в ней пробиотиков. Исследования показывают, что ферментированная еда и напитки могут уравновесить «хорошие» кишечные бактерии, которые, в свою очередь, могут помочь регулировать проницаемость кишечника.Взаимодействие с другими людьми
Однако некоторые люди считают, что чайный гриб, кимчи, квашеная капуста и другие ферментированные продукты вызывают дискомфорт при пищеварении. Если эти варианты вам не подходят, попробуйте йогурт или пробиотические добавки.
Если эти варианты вам не подходят, попробуйте йогурт или пробиотические добавки.
Модификации
Вы можете скорректировать диету с повышенной проницаемостью кишечника с учетом особых диетических потребностей, пищевой аллергии и других заболеваний.
Некоторые изменения могут быть только временными, например, удовлетворение повышенных потребностей в питании во время беременности или возможность восстановления вашего тела после болезни или операции.
Если вам нужно внести значительные или долгосрочные изменения, проконсультируйтесь с врачом или диетологом, чтобы убедиться, что вы по-прежнему получаете необходимое питание.
Соображения
Вы можете не осознавать этого до тех пор, пока вам не понадобится внести в него изменения, но ваша диета может заключаться не только в том, что, когда и сколько вы едите. Ваша роль дома, в школе или на работе может повлиять на то, насколько легко или сложно соблюдать диету. Точно так же ваша социальная деятельность и образ жизни также влияют на ваш выбор.
Разрабатывая диету с повышенной кишечной проницаемостью, учитывайте эти факторы наряду с изменениями, которые вы хотите внести. Понимание того, как каждый аспект вашей жизни повлияет на вашу диету и на нее повлияет, даст вам возможность найти рабочий распорядок и придерживаться его.
General Nutrition
Если диета с повышенной кишечной проницаемостью не является слишком строгой, она может быть питательной и удовлетворительной. Если вы сильно ограничите то, что вы едите, или исключите целые группы продуктов, вы можете почувствовать дефицит питательных веществ и мотивации.
Если у вас возникнет дефицит основных витаминов и минералов, ваш врач может посоветовать вам попробовать добавить жидкие пищевые добавки к вашей диете с дырявым кишечником. Они также могут попросить вас пересмотреть свой рацион, чтобы вы могли получать адекватное питание из того, что вы едите.
Безопасность
Если она питательна и содержит достаточно калорий, диета с повышенной кишечной проницаемостью (или диета при любом заболевании, связанном с кишечником) может быть безопасной и удовлетворительной.
Некоторые рекомендации по диете с повышенной кишечной проницаемостью могут быть для вас небезопасными.Вам нужно будет поговорить со своим врачом, прежде чем полностью исключить что-то из своего рациона.
Сильно ограничивающая диета вряд ли обеспечит адекватное питание и энергию. Эти диеты следует использовать только на краткосрочной основе и / или под наблюдением врача.
Вы можете увидеть специальные продукты, диеты и добавки, рекламируемые при «синдроме дырявого кишечника». Эти продукты и планы не проверялись медицинскими специалистами или регулирующими органами. Недостаточно исследований, чтобы узнать, безопасны ли они и эффективны.
Гибкость
Вы сможете настроить диету с повышенной кишечной проницаемостью в соответствии со своими потребностями в питании и личными вкусами. Как это часто бывает с людьми с расстройствами пищеварения, вам, возможно, придется отказаться от «триггерных продуктов», некоторые из которых могут оказаться любимыми.
Если вы разочарованы его ограничениями или чувствуете, что ваша диета не дает вам возможности есть в обществе, поговорите со своим врачом, диетологом или диетологом. Они могут помочь вам понять, как изменить свой рацион или научиться справляться с этими ситуациями.
Побочные эффекты
Вы можете заметить изменения в пищеварении каждый раз, когда меняете то, как или что вы едите. Нередко бывает временное расстройство, пока ваше тело приспосабливается. Например, если вы измените количество клетчатки в своем рационе, вы, скорее всего, заметите прямое влияние на свой кишечник.
Обычно эти изменения «выравниваются», когда ваше тело привыкает к диете. Однако, если этого не произойдет или ситуация ухудшится, возможно, вам придется пересмотреть изменение. Если у вас возник запор, для его устранения может быть достаточно пить больше воды или добавлять пищевые волокна.
Если у вас развивается диарея, которая не проходит через несколько дней, посоветуйтесь с врачом. Симптом может быть признаком другой проблемы со здоровьем, а продолжительная диарея может вызвать обезвоживание.
Симптом может быть признаком другой проблемы со здоровьем, а продолжительная диарея может вызвать обезвоживание.
Диетические ограничения
Возможно, вы уже едите определенным образом, чтобы справиться с проблемами со здоровьем, например, избегайте глютена, если у вас глютеновая болезнь. У вас также могут быть личные предпочтения в отношении диеты, например, отказ от мяса.
Ваши личные потребности и предпочтения могут хорошо вписаться в диету с дырявым кишечником, но вы можете столкнуться с некоторыми проблемами.Например, если вы ищете продукты без пшеницы, вы заметите, что многие макаронные изделия без глютена сделаны из фасоли, бобовых и кукурузы. Если у вас расстройство пищеварения, эти ингредиенты могут вызвать усиление симптомов.
Вегетарианцы и веганы могут захотеть обратить пристальное внимание на то, как они готовят и готовят фрукты и овощи, которые являются одним из основных продуктов растительной диеты. Например, сырые фрукты и овощи можно очистить, нарезать кубиками и приготовить, чтобы облегчить их переваривание.
Слово от Verywell
«Дырявый кишечник» может быть запутанной и спорной темой.Большинство врачей не признают «синдром дырявого кишечника» действительным медицинским диагнозом. Однако повышенная кишечная проницаемость (которую можно назвать «дырявой кишкой») — известное следствие некоторых состояний пищеварения. Если ваш кишечник поврежден, стенки могут больше не обеспечивать прочный и абсорбирующий барьер. Люди с хроническими желудочно-кишечными заболеваниями часто обнаруживают, что изменение рациона помогает справиться с симптомами. Соблюдение определенных диетических рекомендаций также может помочь пищеварительной системе отдохнуть и восстановиться.Если у вас такое заболевание, как целиакия, избегайте продуктов, вызывающих воспаление в кишечнике, чтобы предотвратить дальнейшее повреждение. Независимо от того, есть ли у них проблемы с пищеварением, многие люди чувствуют себя лучше, когда избегают сладкой, жирной, обработанной пищи и сосредотачиваются на питательной и сбалансированной диете.
Влияние микобиомной диеты на кишечные грибковые и бактериальные сообщества здоровых взрослых
Исследовательская статья — (2020) Том 8, Выпуск 1
Ghannoum M 1, 2 * , Smith C 3 , Adamson E 4 , Isham N 1 , Salem I 1 и Retuerto M 1 * Переписка: Ганнум М., Западный резервный университет Кейса, Кливленд, США, Тел .: 2168448580, Факс: 2168441076, Эл. Почта:Информация об авторе »
Абстрактные
Введение: Это исследование было проведено для оценки эффективности микобиомной диеты (представленной в книге «Общий баланс кишечника») на микробиом кишечника человека в целом и микобиом кишечника (грибковое сообщество) в частности.Включенных субъектов оценивали на предмет улучшения здоровья, желудочно-кишечных симптомов и потери веса, а также субъективных отчетов об изменениях энергии, усталости и сна.
Метод: Десять здоровых добровольцев (шесть мужчин и четыре женщины в возрасте от 30 до 70 лет) были включены в этот 28-дневный протокол. Участники заполняли дневник питания, отмечая ежедневные и еженедельные необходимые продукты, а также отмечая испражнения, вес и любые осложнения, связанные с пищеварением. Образцы фекалий собирали в начале и в конце исследования, при этом профили микобиома и бактериома секвенировали с использованием ITS и 16S областей соответственно.
Результаты: Микобиомная диета оказалась очень успешной в снижении количества патогенных видов Candida . В течение двух недель количество грибов Candida и уменьшилось на 72,4%; C. albicans , в частности, уменьшилось в 1,42 раза, в то время как C. tropicalis не было обнаружено через 4 недели. Субъекты значительно повысили уровень полезных бактерий, в частности Faecalibacterium prausnitzii , Bifidobacterium , Roseburia , Lactobacillus и Bacteroides . Кроме того, значительно снизилось количество патогенных бактерий, включая Escherichia coli , Bacteroides fragilis и Clostridium . Изменения в структуре микробиома сопровождались улучшением пищеварительных симптомов, потерей веса, меньшей утомляемостью, повышением энергии, улучшением сна и уменьшением тяги к пустой калорийной пище.
Кроме того, значительно снизилось количество патогенных бактерий, включая Escherichia coli , Bacteroides fragilis и Clostridium . Изменения в структуре микробиома сопровождались улучшением пищеварительных симптомов, потерей веса, меньшей утомляемостью, повышением энергии, улучшением сна и уменьшением тяги к пустой калорийной пище.
Заключение: Наши данные показали, что соблюдение микобиомной диеты в течение 4 недель привело к положительным сдвигам в сообществах грибкового и бактериального микробиома одновременно с положительным улучшением симптомов желудочно-кишечного тракта и общего состояния здоровья.
Ключевые слова
Микобиомная диета; Здоровье кишечника; Candida виды
Введение
Последние достижения в технологии секвенирования ДНК позволили охарактеризовать микробиом человека, совокупность микробных сообществ, состоящих из бактерий, грибов и вирусов. Исследования показали, что каждый человек имеет уникальный микробный профиль кишечника, на который влияет образ жизни, а также различные врожденные факторы и факторы окружающей среды. В частности, было показано, что диета играет центральную роль во влиянии на микробный состав кишечника, изменяя баланс между полезными и вредными уровнями микроорганизмов.Типичная западная диета включает высокий процент жиров, простых / рафинированных сахаров, соли и животного белка с низким процентным содержанием клетчатки [1]. Такой режим питания может привести к дисбактериозу или дисбалансу микробиоты, что приводит к ожирению и может повысить риск развития таких широкомасштабных состояний, как диабет, артрит, воспалительное заболевание кишечника (ВЗК), болезни сердца и даже рак [2] .
В частности, было показано, что диета играет центральную роль во влиянии на микробный состав кишечника, изменяя баланс между полезными и вредными уровнями микроорганизмов.Типичная западная диета включает высокий процент жиров, простых / рафинированных сахаров, соли и животного белка с низким процентным содержанием клетчатки [1]. Такой режим питания может привести к дисбактериозу или дисбалансу микробиоты, что приводит к ожирению и может повысить риск развития таких широкомасштабных состояний, как диабет, артрит, воспалительное заболевание кишечника (ВЗК), болезни сердца и даже рак [2] .
Недавние исследования показали, что восстановление баланса и поддержание бактериального и грибкового сообществ кишечной микробиоты является предпосылкой для оптимального здоровья желудочно-кишечного тракта и общего самочувствия.Для достижения этой цели мы разработали микобиомную диету (см. Общий баланс кишечника) с целью обеспечения общего баланса кишечника бактериальных и грибковых сообществ [3-6]. Микобиомная диета включает лучшие элементы палео, низкоуглеводной, вегетарианской и средиземноморской диет, избегая при этом аспектов каждой из этих диет, которые, как было специально доказано, увеличивают количество патогенных грибов в кишечнике человека. Он позволяет избежать часто высокого потребления сахара в вегетарианской диете, что может привести к увеличению роста Candida в кишечнике [7], при этом полностью используются пребиотические волокна овощей, которые улучшают баланс полезных бактерий.Кроме того, микобиомная диета избегает типичной для низкоуглеводной диеты сильной зависимости от красного мяса, которое является фактором развития нескольких хронических заболеваний, включая колоректальный рак [8], при этом используются многие благоприятные для грибов аспекты морепродуктов. Кроме того, он заимствует всю философию естественного питания палео-стиля, но не избегает богатых клетчаткой и питательными веществами бобовых, которые являются отличным источником пищи (в частности, клетчаткой и устойчивым крахмалом) для полезных членов микробиома.
Микобиомная диета включает лучшие элементы палео, низкоуглеводной, вегетарианской и средиземноморской диет, избегая при этом аспектов каждой из этих диет, которые, как было специально доказано, увеличивают количество патогенных грибов в кишечнике человека. Он позволяет избежать часто высокого потребления сахара в вегетарианской диете, что может привести к увеличению роста Candida в кишечнике [7], при этом полностью используются пребиотические волокна овощей, которые улучшают баланс полезных бактерий.Кроме того, микобиомная диета избегает типичной для низкоуглеводной диеты сильной зависимости от красного мяса, которое является фактором развития нескольких хронических заболеваний, включая колоректальный рак [8], при этом используются многие благоприятные для грибов аспекты морепродуктов. Кроме того, он заимствует всю философию естественного питания палео-стиля, но не избегает богатых клетчаткой и питательными веществами бобовых, которые являются отличным источником пищи (в частности, клетчаткой и устойчивым крахмалом) для полезных членов микробиома. Кроме того, микобиомная диета избегает чрезмерного использования в средиземноморской диете сложных углеводов и злаков, которые увеличивают распространенность и изобилие вредных грибов, а также его склонность к алкоголю, что, как было доказано, снижает микробное разнообразие [9].
Кроме того, микобиомная диета избегает чрезмерного использования в средиземноморской диете сложных углеводов и злаков, которые увеличивают распространенность и изобилие вредных грибов, а также его склонность к алкоголю, что, как было доказано, снижает микробное разнообразие [9].
Это исследование было проведено для оценки эффективности микобиомной диеты на микробиом кишечника человека в целом и микобиом кишечника (грибковое сообщество) в частности. Кроме того, исследование зафиксировало влияние диеты на желудочно-кишечные симптомы и субъективные маркеры, включая потерю веса, усталость, энергию, сон и тягу к пустой калорийной пище.
Дизайн исследования
Десять здоровых добровольцев (шесть мужчин и четыре женщины в возрасте от 30 до 70 лет) получили информированное согласие и были включены в исследование. Участники заполняли дневник питания, отмечая ежедневные и еженедельные необходимые продукты, а также отмечая испражнения, вес и любые осложнения, связанные с пищеварением. Общие правила исследования были следующие:
Общие правила исследования были следующие:
1. Ешьте в основном цельную пищу. Запрещается обрабатывать пищевые продукты или упакованные продукты, содержащие более трех ингредиентов.
2. Включайте «хороший» белок в каждый прием пищи и закуски (нежирное или растительное, без обработанного или вяленого мяса).
3. Включайте «хороший» источник жира в каждый прием пищи и закуски (одобренные масла или жирные продукты, в основном содержащие мононенасыщенные и полиненасыщенные жиры с низким содержанием насыщенных жиров).
4. Включайте в каждый прием пищи продукты, богатые клетчаткой и / или устойчивым крахмалом (цельнозерновые, бобовые и крахмалистые овощи), но не употребляйте более одной порции этих продуктов за один прием пищи.Распределяйте эти продукты в течение дня на меньшие порции, чтобы избежать избытка углеводов в любом приеме пищи, которые потенциально могут увеличить численность видов Candida .
5. Не меняйте упражнения, сон, режим приема добавок или привычки управления стрессом в ходе этого исследования.
образцов фекалий, при этом профили микобиома и бактериома были секвенированы с использованием ITS и 16S областей соответственно. ДНК бактерий и грибов выделяли и очищали с использованием набора для экстракции ДНК QiaAmpFast (Qiagen).Качество и чистоту выделенной геномной ДНК подтверждали с помощью прибора NanoDrop 2000 (Fisher Scientific). Концентрацию ДНК определяли количественно с помощью прибора Qubit 2.0 с применением анализа Qubit dsDNA HS (Life Technologies) и нормализовали до 100 нг на образец. После денатурации библиотеку ампликонов генерировали с помощью разрезанных продуктов ПЦР с использованием наборов Ion plus Fragment Library (<350 п.н.) и кодировали штрих-кодом с помощью адаптера штрих-кода Ion Xpress ™, лигированного с адаптерами A и P1. Библиотеки со штрих-кодами были сконцентрированы, объединены и секвенированы в системе Ion Torrent PGM с использованием набора Ion Sequencing 400 bp Hi-Q View Kit (Life Technologies, США). Для классификации на уровне видов использовалась справочная база данных Greengene (версия 13.8), а таксоны, присвоенные с использованием метода nBlast, с пороговой достоверностью 90%.
Для классификации на уровне видов использовалась справочная база данных Greengene (версия 13.8), а таксоны, присвоенные с использованием метода nBlast, с пороговой достоверностью 90%.
Результаты
Соблюдение диеты микобиома привело к изменениям в структуре микобиома на разных таксономических уровнях
Рисунок 1 суммирует профиль микобиома (грибок в кишечнике) субъектов до и после соблюдения диеты на основе микобиома. Анализ показал, что в течение двух недель после начала диеты микобиомов снижение на 72.Отмечено 4% численности представителей рода Candida . Более того, C. albicans снизилось на 142%, в то время как C. tropicalis больше не обнаруживалось ни в каких образцах участников, собранных через 4 недели.
Рисунок 1. Профили полезных и патогенных грибов до и
после начала диеты на микобиоме, показывая увеличение
полезные грибы (Pichia kluyveri и Galactomyces geotrichum ) и
снижение патогенных видов Candida (в частности, C. albicans и C. tropicalis ).
albicans и C. tropicalis ).
Помимо снижения численности патогенного Candida , мы также отметили увеличение количества полезных видов грибов к 4-й неделе. Например, Galactomyces geotrichum и Pichia kluyveri увеличились на 58,4% и 45,1% соответственно.
Соблюдение диеты микобиома привело к изменению структуры бактериома на разных таксономических уровнях
На рис. 2 показано количество основных бактериальных типов, обнаруженных в микробиоте кишечника людей, включенных в исследование, до и после соблюдения диеты на основе микобиома.Исходно бактериальный тип состоял в основном из Firmicutes, Bacteroidetes и Proteobacteria. Следует отметить, что уровень протеобактерий был повышен в этих исходных образцах (маркер потенциального дисбактериоза и воспаления при повышении) [10]. Снижение относительной численности наблюдалось уже через 2 недели после начала микобиомной диеты. Анализ образцов кала после 4 недель употребления диеты показал снижение в 1,7 раза численности провоспалительных протеобактерий (уровень снизился с 38 до 38%). От 6% до 23,3%). Это снижение, в свою очередь, привело к благоприятной более высокой относительной численности двух других бактериальных типов ( Firmicutes и Bacteroidetes ).
От 6% до 23,3%). Это снижение, в свою очередь, привело к благоприятной более высокой относительной численности двух других бактериальных типов ( Firmicutes и Bacteroidetes ).
Рис. 2. Профили полезных и патогенных бактерий до и после начала диеты на микобиоме наблюдается увеличение полезные бактерии ( Faecalibacterium prausnitzii, Bifidobacterium adolescentis, Roseburia и Lactobacillus ), а также снижение провоспалительного Протеобактерии ( E.coli, Clostridium и Bacteroides fragilis ).
Как и большинство населения в США, субъекты нашего исследования вошли в испытание с высоким уровнем провоспалительных протеобактерий (при опросе почти тысячи субъектов без основных заболеваний мы обнаружили, что 63% этих участников имели высокий уровень провоспалительных протеобактерий). уровень этого типа (данные не показаны). Анализ бактериальных профилей на уровне родов / видов показал увеличение количества бактерий, которые считаются полезными, включая Faecalibacterium prausnitzii, Bifidobacterium adolescentis, Roseburia, Lactobacillus и Bacteroides ( Рисунок 2 ).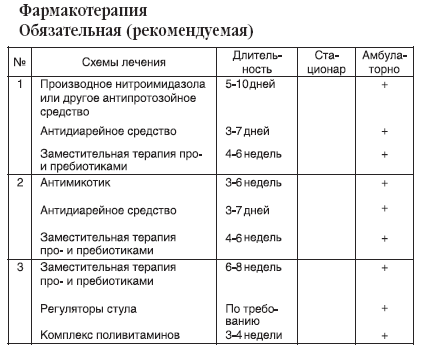 В этом отношении F. prausnitzii и B. adolescentis имели прирост на 35,8% и 61,6% соответственно. Кроме того, количество родов Lactobacillus и Roseburia увеличилось на 77,6% и 57,5% соответственно. Напротив, количество известных бактериальных патогенов, включая Escherichia coli, B. fragilis, и Clostridium , снизилось. Эти популяции уменьшились на 74%, 45,3% и 55,5% у E. coli , B. fragilis и Clostridium , соответственно, к 4 неделе.
В этом отношении F. prausnitzii и B. adolescentis имели прирост на 35,8% и 61,6% соответственно. Кроме того, количество родов Lactobacillus и Roseburia увеличилось на 77,6% и 57,5% соответственно. Напротив, количество известных бактериальных патогенов, включая Escherichia coli, B. fragilis, и Clostridium , снизилось. Эти популяции уменьшились на 74%, 45,3% и 55,5% у E. coli , B. fragilis и Clostridium , соответственно, к 4 неделе.
Соблюдение микобиомной диеты привело к субъективным улучшениям желудочно-кишечных симптомов и других показателей здоровья участников
Перед началом исследования 60% участников сообщили о проблемах со здоровьем, особенно желудочно-кишечных симптомах. У 30% был СИБР (избыточный бактериальный рост в тонком кишечнике, который возникает, когда бактерии, которые обычно растут в других частях кишечника, начинают расти в тонком кишечнике), а у 10% — целиакия. Многие сообщали о проблемах с газами, вздутием живота, запорами, изжогой и диареей.Другие сообщенные проблемы включали усталость, низкий уровень энергии, тягу к сахару, хлебу или соленым углеводам, а также нарушения сна, особенно при пробуждении посреди ночи.
Многие сообщали о проблемах с газами, вздутием живота, запорами, изжогой и диареей.Другие сообщенные проблемы включали усталость, низкий уровень энергии, тягу к сахару, хлебу или соленым углеводам, а также нарушения сна, особенно при пробуждении посреди ночи.
В конце исследования все участники с симптомами желудочно-кишечного тракта сообщили об умеренных или значительных улучшениях. В связи с этим все участники, которые хотели похудеть, действительно похудели (от двух до 10 фунтов). Тридцать процентов участников сообщили об умеренном или значительном улучшении утомляемости и повышении уровня энергии, а 30% сообщили о лучшем сне, меньшем бодрствовании ночью и уменьшении приливов.Кроме того, 60% участников решили продолжить диету с микобиомами после испытания. Из 40%, которые вернулись к своей прежней диете, у всех, кроме одного (чья диета уже была очень похожа на диету микобиома), ухудшились симптомы. После рецидива симптомов некоторые решили снова вернуться к микобиомной диете или вернуться к определенным аспектам диеты, которые, по их мнению, были полезными.
Обсуждение
Микобиомная диета восстанавливает баланс грибкового сообщества в кишечнике
Наше исследование показало, что соблюдение диеты с микобиомом привело к изменениям как грибковых, так и бактериальных сообществ.Уменьшение численности патогенных грибов (например, C. albicans и C. tropicalis ) обнадеживает, поскольку известно, что эти дрожжи связаны с множеством заболеваний, таких как воспалительные заболевания кишечника (ВЗК) и болезнь Крона. болезнь [11,12]. Candida избыточное представительство в кишечнике сопровождается увеличением воспаленной ткани кишечника и может также препятствовать восстановлению полезных бактерий, таких как Lactobacillus , от нарушения кишечного бактериома.Кроме того, присутствие C. tropicalis в условиях ВЗК приводит к большей тяжести симптомов ВЗК и выработке провоспалительных цитокинов [13,14].
Помимо снижения уровня патогенов, соблюдение микобиомной диеты привело к одновременному увеличению числа полезных грибов, в частности, Pichia kluyveri и Galactomyces geotrichum . В 2014 году наша группа провела анализ взаимодействий в микробиоме ВИЧ-инфицированных пациентов, который привел к обнаружению антагонистических отношений между Pichia (непатогенными дрожжами, которые используются в Европе в качестве агента биоконтроля для защиты сельскохозяйственных культур от грибковый рост) и Candida [15].Мы отметили, что снижение уровня Pichia совпало с увеличением колонизации Candida и наоборот. В ходе дальнейшего тестирования мы обнаружили, что Pichia высвобождает ингибирующую молекулу, которая была способна ограничивать рост Candida , а также других грибковых патогенов, таких как Fusarium и Aspergillus . Более того, клетки Pichia или среда, в которой они были выращены, приводили к значительному ингибированию образования биопленок с помощью Candida .Наконец, мы смогли вылечить инфекцию, вызванную C. albicans , с использованием фильтрата Pichia. Эти данные свидетельствуют о том, что повышение уровня Pichia за счет соблюдения диеты с микобиомами поможет держать под контролем Candida и может объяснить улучшение симптомов, отмеченное у наших добровольцев.
Galactomyces geotrichum — еще один полезный гриб, количество которого увеличивалось у участников, соблюдающих микобиомную диету. В нашем исследовании, сравнивающем микобиом кишечника пациентов с болезнью Крона (БК) и их родственниками, не являющимися родственниками Крона (NCDR), мы показали, что C.tropicalis был обычен в группе CD (10%), тогда как Saccharomyces cerevisiae и G. geotrichum (27% и 8% соответственно) были наиболее распространенными в группе NCDR [16]. Недавнее исследование показало, что G. geotrichum прочно связывается с молочнокислыми бактериями, что предполагает потенциальную роль в поддержании симбиотической микробиоты в здоровом кишечнике [17]. Еще одно преимущество, приписываемое G. geotrichum , — это его способность продуцировать пептиды, которые могут ингибировать фермент, превращающий ангиотензин I, который отвечает за регуляцию артериального давления у людей.В совокупности это говорит о том, что увеличение численности этого вида грибов в результате соблюдения диеты микобиома может помочь в улучшении общего баланса микробиома кишечника.
Микобиомная диета восстанавливает баланс бактериального сообщества в кишечнике
Участники испытания микобиомной диеты испытали сдвиг в бактериоме с уменьшением количества вредных бактерий ( Proteobacteria, Escherichia coli, Bacteroides fragilis и Clostridium ), что сопровождалось увеличением числа полезных бактерий ( Faecalibacterium prausnitzii, Roseburst. Lactobacillus, Bacteroides и Bifidobacteria ).
Ряд исследований подтверждают концепцию, согласно которой переизбыток Proteobacteria в желудочно-кишечном тракте отражает дисбактериоз или нестабильную структуру микробиома кишечника. Было высказано предположение, что нарушение гомеостаза хозяином или другими факторами окружающей среды (например, диета с низким содержанием клетчатки и острое или хроническое воспаление) может вызвать дисбактериоз, а сопутствующее увеличение численности протеобактерий может привести к воспалительным симптомам или инвазии. патогенами. В связи с этим дисбактериоз ВЗК характеризуется увеличением количества протеобактерий с соответствующим снижением представленности Firmicutes [18].Исследования на животных показывают, что микробный дисбаланс при ВЗК связан с чрезмерной представленностью патогенных таксонов Proteobacterial , таких как Enterobacteriaceae (например, E. coli ), и снижением защитных видов Firmicutes , таких как F . prausnitzii [19].
Другие исследования также продемонстрировали снижение разнообразия Firmicutes , при этом у пациентов с ВЗК было обнаружено меньшее количество составляющих видов по сравнению с контрольной группой [20].Изменения в двух доминирующих типах, Firmicutes, и Bacteroidetes, сочетаются с увеличением численности представителей филума Proteobacteria , которые, как все чаще обнаруживают, играют ключевую роль в ВЗК [21]. Исследования показали сдвиг в сторону увеличения количества видов, принадлежащих к этому типу, что предполагает роль агрессора в инициировании хронического воспаления у пациентов с ВЗК. В частности, при БК подвздошной кишки зарегистрировано повышенное количество E. coli , включая патогенные варианты [22].
E. coli — патогенная бактерия, которая, как было показано, играет важную роль в индукции хронического воспаления кишечника у восприимчивых хозяев, где она может дифференцированно вызывать воспалительные реакции клеток Th2 и Th27 [23]. Наша команда также показала, что этот организм повышен у пациентов с болезнью Крона. Кроме того, мы продемонстрировали, что E. coli кооперируется с C. tropicalis и Serratia marcescens с образованием биопленок in vivo у животных с ВЗК [24].Кроме того, было показано, что E. coli взаимодействует с B. fragilis (другая патогенная бактерия, уменьшенная с помощью микобиомной диеты), образуя биопленки в желудочно-кишечном тракте, которые могут привести к раку толстой кишки. Эти исследования начинают показывать потенциальную роль микробиоты толстой кишки в развитии рака [25].
Исследования, связывающие увеличение численности E. coli , показали, что более высокое потребление закусок и нездоровой пищи приводит к увеличению количества E.coli подсчитывает и подавляет полезные лактобациллы и продуцирующие бутират Firmicutes члена (например, F. prausnitzii ). Эти изменения представляют собой потенциально опасную среду воспалительной кишечной микробиоты для хозяина [9]. Напротив, длительная диета, богатая полисахаридами (с высоким содержанием клетчатки и резистентного крахмала), была связана с меньшим количеством представителей таксонов Enterobacteriaceae ( Shigella и Escherichia ).
Недавние исследования показывают, что некоторые виды Bacteroides полезны, обеспечивая разложение сложных полисахаридов, производство антибактериальных молекул (например,, дефенсины), а также развитие иммунной толерантности и, как следствие, предотвращение аллергии [26]. Другие опубликованные отчеты предполагают, что определенные виды Bacteroides играют роль в предотвращении инфекций, вызванных C. difficile [27,28]. В кишечнике Bacteroides участвуют в ферментации углеводов, что приводит к образованию летучих жирных кислот (например, короткоцепочечных жирных кислот, SCFA). Эти жирные кислоты реабсорбируются хозяином через толстый кишечник и используются в качестве источника энергии, тем самым обеспечивая значительную часть суточной потребности в энергии [29].Кроме того, Bacteroides способствует выживанию других кишечных бактерий, которым не хватает сахара, использующего ферменты.
Некоторые предыдущие исследования показали, что Bacteroides spp ., Особенно B. vulgatus и B. fragilis , могут играть роль в патогенезе язвенного колита (ЯК) [30-32]. Кроме того, энтеротоксигенный B. fragilis (ETBF) был замешан в ВЗК, при этом распространенность гена энтеротоксина, как сообщается, выше в смывах просвета пациентов с диареей по сравнению с контрольной группой без диареи.Было высказано предположение, что колонизация штаммами ETBF может привести к острому / хроническому воспалению кишечника [33]. Кроме того, было показано, что B. fragilis отвечает за большую долю бактериальной массы у пациентов с ВЗК по сравнению с контрольной группой [34].
Род Clostridium был связан с рядом проблем с желудочно-кишечным трактом, особенно с диареей, запором, рвотой и тошнотой, характерными для синдрома раздраженного кишечника (СРК) [35,36]. Удар С.difficile в системе здравоохранения широко распространена и становится все более заметной. Например, количество госпитализаций по причине C. difficile увеличилось на 237% с 2000 г., при этом предполагаемая внутрибольничная летальность составляет 4% [37,38].
Примечательно, что недавние исследования начинают показывать, что пробиотики полезны для лечения желудочно-кишечных расстройств, связанных с Clostridium, включая диарею. Например, было показано, что S. boulardii предотвращает или сокращает продолжительность диареи, связанной с антибиотиками, и предотвращает дальнейшее рецидивирование C.difficile -ассоциированная диарея [39].
Род Roseburia состоит из грамположительных анаэробных бактерий, включающих 5 видов, включая Roseburia Кишечник , R. hominis , R. inulinivorans , R. faecis и R. cecicola . Это комменсальные бактерии, продуцирующие SCFA, особенно бутират, которые обладают противовоспалительным действием и помогают поддерживать иммунитет. Исследования показали, что диета на основе животных снижает уровень видов Firmicutes , включая Roseburia , которые метаболизируют полисахариды пищевых растений [40,41].Кроме того, испытания на людях, оценивающие влияние диет для похудения с низким содержанием общих углеводов, также показали снижение уровней SCFA в кале (например, бутирата), что коррелирует с уменьшением количества бактерий, продуцирующих бутират, таких как Roseburia [42,43]. В связи с этим, даже несмотря на то, что диета с микобиомом содержит мало рафинированных углеводов, мы не наблюдали снижения уровня Roseburia , а скорее его повышение, что указывает на то, что микобиомная диета может быть более полезной, чем диеты, специально разработанные для похудения. из-за включения резистентных крахмалов [44].
F. prausnitzii является продуцентом бутирата и продемонстрировал противовоспалительное действие на моделях колита у мышей in vitro и in vivo . Уменьшение количества видов Firmicutes F. prausnitzii хорошо документировано у пациентов с CD, особенно с подвздошной CD. Напротив, высокие уровни F. prausnitzii обнаруживаются у здоровых людей [45]. Например, в нашем исследовании болезни Крона мы показали, что численность F.prausnitzii была выше у здоровых родственников по сравнению с пациентами с болезнью Крона [11]. Следовательно, модуляция уровней F. prausnitzii может иметь профилактическое или терапевтическое значение.
Заключение
Наше исследование показало, что соблюдение микобиомной диеты привело к сдвигам в бактериальных и грибковых сообществах кишечника участников, с увеличением количества полезных грибов и бактерий и, соответственно, уменьшением количества вредных микроорганизмов. В целом, этот сдвиг был связан с улучшением симптомов со стороны желудочно-кишечного тракта, потерей веса, меньшей утомляемостью, большей энергией, улучшением сна и уменьшением тяги к пустой калорийной пище.
Ссылки
- Сингх Р.К., Чанг Х.В., Ян Д., Ли К.М., Укмак Д., Вонг К. и др. Влияние диеты на микробиом кишечника и последствия для здоровья человека. J из Translational Med. 2017; 15:73.
- Кордайн Л., Итон С.Б., Себастьян А., Манн Н., Линдеберг С., Уоткинс Б.А. и др. Истоки и эволюция западной диеты: значение для здоровья в 21 веке. Американский журнал Clinic Nutri. 2005; 81: 341-354.
- Келли Д., Кинг Т., Аминов Р. Важность микробной колонизации кишечника в раннем возрасте для развития иммунитета.Mut Res / Fundamental и Mol Mech мутагенеза. 2007; 622: 58-69.
- Vrieze A, de Groot PF, Kootte RS, Knaapen M, Van Nood E, Nieuwdorp M. Пересадка фекалий: безопасная и устойчивая клиническая терапия для восстановления баланса кишечных микробов при заболеваниях человека? Best Practice & Res Clinic Gastro. 2013; 27: 127-137.
- Shoaib A, Dachang W, Xin Y. Определение роли пробиотика в восстановлении баланса кишечных микробов с помощью молекулярных и культурных методов. Gene и Mol Res: GMR.2015; 14: 1526-1537.
- Ганнум М. Общий баланс кишечника. Countryman Press. Нью-Йорк, штат Нью-Йорк. 2019.
- Вейг М., Вернер Э., Фрош М., Каспер Х. Ограниченное влияние пищевых добавок с рафинированными углеводами на колонизацию желудочно-кишечного тракта здоровых субъектов Candida albicans . Американский журнал Clin Nutri. 1999; 69: 1170-1173.
- Larsson SC, Orsini N. Потребление красного мяса и мясных продуктов, а также общая смертность: метаанализ. Американский журнал эпидемиологии.2013; 179: 282-289.
- Мицу Э.К., Какали А., Антонопулу С., Маунтзурис К.С., Яннакулия М., Панайотакос Д.Б. и др. Приверженность средиземноморской диете связана с микробиотой кишечника и характеристиками желудочно-кишечного тракта у взрослого населения. Британский журнал питания. 2017; 117: 1645-1655.
- Rizzatti G, Lopetuso LR, Gibiino G, Binda C, Gasbarrini A. Протеобактерии: общий фактор болезней человека. Bio Med Res Int. 2017.
- Ганноум М. Микобиом: постоянно игнорируемое постоянное грибковое сообщество играет решающую роль в здоровье и болезнях человека.Ученый. 2016.
- Sokol H, Leducq V, Aschard H, Pham HP, Jegou S, Landman C и др. Дисбактериоз грибковой микробиоты при ВЗК. Кишечник. 2017; 66: 1039-1048.
- Enaud R, Vandenborght LE, Coron N, Bazin T, Prevel R, Schaeverbeke T. и др. Микобиом: компонент, которым пренебрегают, в системе микробиота-кишечник-мозг. Микроорганизмы. 2018; 6:22.
- Mukherjee PK, Sendid B. Hoarau G2, Colombel JF, Poulain D, Ghannoum MA. Микобиота при желудочно-кишечных заболеваниях. Нат Рев Гастроэнтерол Гепатол.2015; 12: 77-87.
- Мукерджи П.К., Чандра Дж., Ретуэрто М., Сикаруоди М., Браун Р.Э., Юревич Р. и др. Анализ микобиома полости рта у ВИЧ-инфицированных пациентов: идентификация Pichia как антагониста условно-патогенных грибов. PLOS Патогены. 2014; 10: e1003996.
- Hoarau G, Mukherjee PK, Gower-Rousseau C, Hager C., Chandra J, Retuerto MA, et al. Взаимодействие бактериома и микобиома подчеркивает микробный дисбиоз при семейной болезни Крона. MBio. 2016; 7: e01250-e012516.
- Тан Х, Ван Х, Ю Х, Пяо Ц, Лю Дж, Ху Ю.Galactomyces geotrichum, выделенный из водного кефира: взаимодействие с лактобациллами кефира. Итальянский J. Food Sci. 2016; 28: 287-297.
- Нагалингам Н.А., Линч С.В. Роль микробиоты в воспалительных заболеваниях кишечника. Воспалительные заболевания кишечника. 2012; 18: 968-984.
- Wu GD, Lewis JD. Анализ микробиома кишечника человека и его связь с заболеванием. Clin Gastroenterol Hepatol. 2013; 11.
- Manichanh C, Rigottier-Gois L, Bonnaud E, Gloux K, Pelletier E, Frangeul L, et al.Уменьшение разнообразия фекальной микробиоты при болезни Крона, выявленное с помощью метагеномного подхода. Кишечник. 2006; 55: 205-211.
- Mukhopadhya I, Thomson JM, Hansen R, Berry SH, El-Omar EM, Hold GL. Обнаружение Campylobacter concisus и других видов Campylobacter в биоптатах толстой кишки взрослых с язвенным колитом. PLOS One. 2011; 6: e21490.
- Лупп С., Робертсон М.Л., Викхэм М.Э., Секиров И., Чемпион О.Л., Гейнор ЕС и др. Воспаление, опосредованное хозяином, нарушает микробиоту кишечника и способствует чрезмерному росту энтеробактерий.Клеточный хозяин и микроб. 2007; 2: 119-129.
- Eun CS, Mishima Y, Wohlgemuth S, Liu B., Bower M, Carroll IM, et al. Индукция бактериального антиген-специфического колита упрощенным консорциумом микробиоты человека у мышей гнотобиотического интерлейкина-10 — / -. Инфекция и иммунитет. 2014; 82: 2239-2246.
- Hager CL, Ghannoum MA. Микобиом: роль в здоровье и болезнях, а также в качестве потенциальной пробиотической мишени при желудочно-кишечных заболеваниях. Dig Liver Dis. 2017; 49 (11): 1171-1176.
- Dejea CM, Wick EC, Hechenbleikner EM, White JR, Welch M, Rossetti BR et al.Организация микробиоты — отличительная черта проксимального колоректального рака. Proc Natl Acad Sc USA. 2014; 111 (51): 18321-18326.
- Wexler HM. Bacteroides: хорошее, плохое и непритязательное. Clin Microbiol Rev.2007; 20 (4): 593-621.
- Хопкинс М, Макфарлейн GT. Неперевариваемые олигосахариды повышают устойчивость бактерий к колонизации против Clostridium difficile in vitro. Appl Environ Microbiol. 2003; 69 (4): 1920-1927.
- Хопкинс MJ, Macfarlane GT. Изменения в преобладающих популяциях бактерий в фекалиях человека с возрастом и при инфекции Clostridium difficile.J Med Microbiol. 2002; 51 (5): 448-454.
- Hooper LV, Midtvedt T, Gordon JI. Как взаимодействие хозяина и микроба формирует питательную среду кишечника млекопитающих. Annu Rev Nutr. 2002; 22: 283-307.
- Poxton IR, Brown R, Sawyerr A, Ferguson A. Бактериальная флора слизистой оболочки толстой кишки человека. J Med Microbiol. 1997; 46 (1): 85-91.
- Rath HC, Herfarth HH, Ikeda JS, Grenther WB, Hamm Jr TE, Balish E et al. Нормальные просветные бактерии, особенно виды Bacteroides, опосредуют хронический колит, гастрит и артрит у трансгенных крыс с HLA-B27 / β2-микроглобулином человека.J Clin Invest. 1996; 98 (4): 945-953.
- Matsuda H, Fujiyama Y, Andoh A, Ushijima T., Kajinami T., Bamba T. Характеристика антител к бактериальной флоре, связанной со слизистой оболочкой прямой кишки, у пациентов с язвенным колитом. J Gastroenterol Hepatol. 2000; 15 (1): 61-68.
- Wu S, Powell J, Mathioudakis N, Kane S, Fernandez E, Sears CL. Энтеротоксин Bacteroides fragilis индуцирует секрецию интерлейкина-8 эпителиальными клетками кишечника через митоген-активируемые протеинкиназы и регулируемый тирозинкиназой путь ядерного фактора-B.Заражение иммунной. 2004; 72 (10): 5832-5839.
- Swidsinski A, Weber J, Loening-Baucke V, Hale LP, Lochs H. Пространственная организация и состав флоры слизистой оболочки у пациентов с воспалительным заболеванием кишечника. J Clin Microbiol. 2005; 43 (7): 3380-3389.
- Джеффри И.Б., О’Тул П.В. Взаимодействие диеты и микробиоты и их значение для здорового образа жизни. Питательные вещества. 2013; 5 (1): 234-52.
- Франкавилла Р., Калассо М., Калаче Л., Сирагуса С., Ндагижимана М., Вернокки П. и др. Влияние лактозы на микробиоту кишечника и метаболом младенцев с аллергией на коровье молоко.Pediatr Allergy Immunol. 2012; 23 (5): 420-427.
- Peery AF, Dellon ES, Lund J, Crockett SD, Mcgowan CE, Bulseiwicz WJ et al. Бремя желудочно-кишечных заболеваний в США: обновление 2012 г. Гастроэнтерол. 2012; 143 (5): 1179-1187.
- Zuo T, Wong SH, Cheung CP, Lam K, Lui R, Cheung K et al. Грибковый дисбиоз кишечника коррелирует со сниженной эффективностью трансплантации фекальной микробиоты при инфекции Clostridium difficile. Nat Commun. 2018; 9 (1): 3663.
- Marteau PR, de Vrese M, Cellier CJ, Schrezenmeir J.Защита от желудочно-кишечных заболеваний с помощью пробиотиков. Am J Clin Nutr. 2001; 73 (2) 430-436.
- Дэвид Л.А., Морис К.Ф., Кармоди Р.Н., Гутенберг Д.Б., Баттон Д.Е., Вулф Б.Э. и др. Диета быстро и воспроизводимо изменяет микробиом кишечника человека. Природа. 2014; 505 (7484): 559-563.
- О’Киф С.Дж., Ли СП, Лахти Л., Оу Дж., Карбонеро Ф., Мохаммед К. и др. 2015. Жир, клетчатка и риск рака у афроамериканцев и сельских жителей Африки. Nature Commun. 2015; 6: 6342.
- Duncan SH, Belenguer A, Holtrop G, Johnstone AM, Flint HJ, et al.Снижение потребления углеводов с пищей у людей с ожирением приводит к снижению концентрации бутирата и бутират-продуцирующих бактерий в кале. Appl Environ Microbiol. 2007; 73 (4): 1073-1078.
- Рассел В., Грац С.В., Дункан С.Х., Холтроп Дж., Инс Дж., Скобби Л. и др. 2011 г. Диеты для похудения с высоким содержанием белка и низким содержанием углеводов способствуют формированию профиля метаболитов, который может быть вредным для здоровья толстой кишки. Am J Clin Nutr. 2011; 93 (5): 1062-1072.
- Maier TV, Lucio M, Lee LH, VerBerkmoes NC, Brislawn CJ, Bernhardt J et al.Влияние диетического резистентного крахмала на микробиом кишечника человека, метапротеом и метаболом. MBio. 2017.8 (5): e01343-17.
- Микель С., Мартин Р., Росси О., Бермудес-Хумаран Л.Г., Шатель Дж. М., Сокол Х и др. Faecalibacterium prausnitzii и здоровье кишечника человека. Curr Op Microbiol. 2013; 16 (3): 255-261.
Информация об авторе
Ghannoum M 1, 2 * , Smith C 3 , Adamson E 4 , Isham N 1 , Salem I 1 и Retuerto M 1 1 Университет Кейс Вестерн Резерв, Кливленд, США2 Университетские больницы Кливлендский медицинский центр, Кливленд, США
3 Терапевт по питанию, Гранд-Джанкшен, Колорадо, США
4 Eve Ink Books, Айова-Сити, США
Образец цитирования: Ghannoum M, Smith C, Adamson E, Isham N, Salem I, Retuerto M (2020) Влияние микобиомной диеты на кишечные грибковые и бактериальные сообщества здоровых взрослых.J Пробное здоровье. 8: 215. DOI: 10.35248 / 2329-8901.20.8.215
Дата получения: 8 декабря 2019/ Дата принятия: 2 января 2020 г./ Дата публикации: 10 янв.2020 г.
Авторские права: © 2020 Ghannoum M, et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Лечение синдрома раздраженного кишечника у детей
Хуан Р. Малагелада 1 * , Каролина Малагелада 1
1 Отдел исследования пищеварительной системы, Университетская клиника Валь-д’Эброн, Центр биомедицинских исследований и красных энфермедадес Hepáticas y Digestivas (Ciberehd), Медицинский факультет Автономного университета Барселоны, Барселона, Испания
СРК — это клиническое состояние, включающее частые (≥4 дней в месяц) и хронические (> 2 месяцев) боли в животе и нарушение стула.Вздутие живота — распространенный и очень раздражающий сопутствующий симптом. Диагноз устанавливается путем применения критериев симптомов, выявленных с помощью ряда медицинских экспертных групп (процесс I, II, III и IV «ROME»). Диагностические критерии очень похожи для детей и взрослых 1 . Что касается нарушений опорожнения кишечника, то у детей чаще встречается паттерн с преобладанием запора, чем с преобладанием диареи или смешанный, чередующийся паттерн запор / диарея 2-4 .Сдвиги модели во времени довольно обычны 3 .
К настоящему времени выявленные механизмы заболевания СРК многочисленны, разнообразны и не всегда полностью изучены. Патофизиологические особенности СРК, подтвержденные убедительными научными данными, включают висцеральную гиперчувствительность, нарушение моторики желудочно-кишечного тракта, воспаление кишечника, триггеры питания, дисбактериоз кишечника и нарушения оси кишечник-мозг. Таким образом, согласно недавнему обзору 5 , СРК патогенетически является гетерогенным.Семейная агрегация часто заметна, но неясно, является ли причиной этого генетическое или экологическое влияние, в том числе повышенное осознание ощущений в животе.
СРК довольно часто встречается как у детей, так и у взрослых. Хорошо проведенное, хотя и относительно более старое исследование показало, что 14% учащихся средних школ и 6% учащихся средних школ в США страдают от симптомов, соответствующих IBS 6 . Последние данные в целом подтверждают очень высокую распространенность СРК у детей 2, 4, 7 и, следовательно, высокое экономическое бремя 8 .В клинической практике диагноз СРК нередко применяется довольно свободно, поскольку СРК определяется исключительно по относительно сложной формуле симптома без поддающегося проверке биологического маркера. Поэтому клиницисты иногда наносят ярлык IBS на любого пациента без признаков «определенного» органического заболевания, который жалуется на неострую боль в животе в сочетании с измененным типом опорожнения кишечника. Как указано Quigley & Shanahan 9 , такое заболевание, как СРК, которое определяется исключительно критериями симптомов, может создавать иллюзию понимания и приравнивать жалобы к «болезни».Этот аспект может быть особенно актуален для детей, у которых симптомы могут проявляться расплывчато и непоследовательно. У этой возрастной группы пациентов также может быть трудно определить реальную «интенсивность жалоб». Важны стрессовые события, влияющие на ребенка и семью, а также отношения и факторы окружающей среды 10, 11 .
Разумное и тщательно взвешенное применение диагностических тестов в порядке. Сначала следует попытаться поставить «положительный» диагноз СРК, основанный на критериях симптомов, а не «исключающий» диагноз СРК, как это традиционно делается, потому что последний предполагает гораздо более высокие ятрогенные риски и / или экономическое бремя.Тем не менее, некоторые базовые методы оценки могут быть оправданы, если есть сомнения, если давление со стороны семьи является значительным, если быстрое решение не достигается применением терапевтических мер первой линии и, конечно, если наблюдаются тревожные клинические признаки. Первые широко применяемые диагностические обследования включают анализ крови, проверку стула на наличие паразитов или крови, ультразвуковое исследование брюшной полости и эндоскопическое обследование желудочно-кишечного тракта.
Клиницисты, обследующие ребенка с абдоминальными симптомами, также должны обращать внимание на внекишечные проявления и сопутствующие заболевания, такие как усталость, головные боли, мочевые и скелетно-мышечные симптомы и т. Д., Как показали исследования СРК у взрослых 12 .Совпадение этих различных симптоматических проявлений у одного и того же человека предполагает, что участие ЦНС искажает и объединяет периферические входы, что приводит к концепции центральных сенсибилизирующих расстройств, которые могут включать СРК. Действительно, у детей с хроническими симптомами пищеварения наблюдается преувеличенная реакция ствола мозга на окружающие стимулы, а неадекватное поведение родителей, по-видимому, усугубляет симптомы 13 . И наоборот, кажущееся спонтанное разрешение СРК не редкость 14 .
Ярлык СРК в современном гиперкоммуникационном обществе может также включать концептуальные элементы «мема», распространяющегося путем заражения среди клиницистов, родственников или опекунов детей 15 . Сами симптомы могут быть потенциально усилены окружением ребенка и даже медицинским персоналом, стремящимся установить диагноз у ребенка с необъяснимыми в противном случае жалобами на брюшную полость. Этот механизм может объяснить растущую распространенность диагноза СРК в западных обществах как у детей, так и у взрослых.
При рассмотрении лечения СРК может быть полезно попытаться выяснить патогенетический механизм или, по крайней мере, преобладающее патофизиологическое нарушение, действующее у отдельных пациентов, поскольку подход, основанный на механизме, вероятно, повышает терапевтическую эффективность 5 .
Диета может выступать как индуктор симптомов, так и терапевтическая возможность. Само собой разумеется, что не все дети одинаково переносят несколько компонентов нормальной диеты.Специфическая пищевая аллергия может проявляться клинически очевидным образом, что не оставляет сомнений в их патогенетической роли. Однако более тонкие формы иммунных взаимодействий между питательными веществами и клетками могут лежать в основе симптомов, подобных СРК 16, 17 . Задача состоит в том, чтобы установить определенную ответственность за определенные продукты питания за возникновение симптомов, когда простое наблюдение дает только двусмысленные ответы. В настоящее время доступен ряд коммерческих тестов под названием «тесты на пищевую непереносимость».К ним относятся аллерген-специфическая реакция IgG на различные продукты питания, электродермальные тесты, сублингвальные или внутрикожные тесты, цитотоксические тесты и другие. Хотя некоторые из этих тестов вызвали интерес у врачей и, в частности, у широкой общественности, они не получили твердого научного одобрения, и есть сомнения относительно того, действительно ли результаты тестов отражают клинически значимую непереносимость. Кроме того, растет беспокойство по поводу того, что необоснованные и радикальные ограничения в диете могут привести к дисбалансу питания, включая накопление токсичных веществ металлических элементов (т.е. ртуть) в крови и тканях 18 .
Неаллергическая пищевая непереносимость в основном связана с ограниченной способностью кишечника переваривать и усваивать сахар и другие обычные пищевые компоненты. Истинная непереносимость лактозы в основном связана с низкой доступностью лактазы в кишечнике, но клинически проявляется только при относительно больших нагрузках лактозы, поэтому предупрежденных пациентов легко ее избежать. 19 . Фруктоза, моносахарид, присутствующий во многих обработанных пищевых продуктах, имеет относительно низкий порог абсорбции в тонком кишечнике человека, и, следовательно, диета, богатая фруктозой, может вызывать кишечные симптомы у восприимчивых людей за счет стимуляции перистальтики кишечника 20 .Психологические факторы могут влиять на симптоматическую реакцию на мальабсорбцию сахара, поскольку это было хорошо задокументировано для лактозы 21 . Таким образом, субъективная оценка симптомов представляет собой потенциальное искажающее клиническое влияние, которое необходимо принимать во внимание.
Механизмы абдоминальных симптомов, развивающихся в контексте мальабсорбции питательных веществ, включают увеличение количества выделений из тонкой кишки, попадающих в толстую кишку 22 . В свою очередь, эти молекулы ферментируются бактериями толстой кишки, увеличивая выработку газа в толстой кишке и вырабатывая осмотические стимуляторы и стимуляторы моторики, которые вызывают выделения из толстой кишки и спазматическую деятельность кишечника.В дополнение к лактозе и фруктозе в нормальном рационе есть много не полностью усвояемых углеводов, которые при определенных обстоятельствах могут также вызывать перегрузку толстой кишки ферментируемыми субстратами, генерирующими газ, что плохо переносится пациентами с СРК. К ним относятся группа, известная как FODMAP (фруктаны, галакто-сахариды и полиолы, включая сорбит, маннит и ксилит), которые естественным образом присутствуют во многих фруктах и овощах, а также в таких добавках, как искусственные подсластители (рис. 1).Накоплены существенные доказательства того, что диета, ограничивающая компоненты FODMAP, облегчает симптомы СРК. Респондеры, по-видимому, содержат больше видов сахаролитических бактерий в своем микробиоме 23 . К сожалению, долгосрочное соблюдение этой и других строго ограничительных диет обременительно для многих пациентов. Кроме того, было высказано предположение, что обычные и разумные ограничения в диете могут быть столь же эффективными, как и строгая диета FODMAP, хотя этот вопрос все еще является предметом обсуждения 24 .Последний подход может заключаться в отказе от молочных продуктов, жирной пищи, напитков с искусственными подсластителями или напитков, содержащих кофеин.
По этой теме есть два аспекта, которые имеют отношение к патогенезу и лечению СРК. Во-первых, существует проблема постинфекционного СРК, хорошо задокументированная эпидемиологическими исследованиями у людей, как детей, так и взрослых, 25 , ранее пострадавших от инфекционного гастроэнтерита. Примерно у 10% (цифры различаются) таких людей впоследствии развиваются симптомы, совместимые с СРК 26 .Лямблиоз также представляет собой признанный фактор риска 27, 28 . Молодой возраст, психологические расстройства, предшествующие антибиотики и другие факторы, по-видимому, предрасполагают к постинфекционному гастроэнтериту. СРК-подобный синдром 29 . Патогенетические факторы включают активацию иммунных клеток слизистой оболочки и пролиферацию иммунных клеток, которые могут усиливать периферическую сенсорную передачу сигналов и приводить к висцеральной гиперчувствительности 30 . Примечательно, что некоторые формы инфекционного гастроэнтерита в детстве, например, вызванные видами Salmonella, увеличивают вероятность развития СРК во взрослом возрасте 31 .
Второй аспект микробного воздействия на патогенез СРК связан с нарушениями микробиома. С этой целью необходимо учитывать две ситуации: чрезмерная микробная транслокация в тонкий кишечник (избыточный бактериальный рост в тонкой кишке — SIBO-) и изменения в экологии микробиома. Доказательства SIBO получены в основном из анализа дыхательных тестов. К сожалению, быстрый транзит тестового субстрата по тонкой кишке может вызвать ранний пик сигнала из-за раннего поступления субстрата в толстую кишку, что может быть ошибочно интерпретировано как внутрипросветная ферментация тонкой кишки 32 .Изменения в микробиоме толстой кишки также вовлечены в патогенез СРК. В самом деле, некоторые виды микробиома человека могут влиять на функцию кишечника и даже потенциально изменять взаимодействие кишечника с мозгом. Например, было замечено, что F. prausnitzii может модулировать гиперчувствительность толстой кишки, а Lactobacillus reuterii участвует в регуляции транзита толстой кишки 33 . Изменения микробиоты, наблюдаемые при постинфекционном СРК, включают повышенное присутствие типа Bacteroidetes, который напоминает состав микробиоты, наблюдаемый при СРК с преобладанием диареи 34 .Однако для прояснения этих аспектов потребуются дальнейшие исследования, поскольку текущие данные являются предварительными и все еще не могут быть приняты как окончательные.
Усилия по восстановлению микробной экологии включают применение антибиотиков, пребиотиков и пробиотиков. Антибиотики были предложены для лечения предполагаемого СИБР, а также для «исправления» состава микробиома. В этом отношении предпочтение отдается рифаксимину на основании его неабсорбируемости и эмпирических данных об эффективности. У взрослых относительно высокие дозы от 800 до 1650 мг / день в течение 10-14 дней, по-видимому, улучшают общую симптоматику СРК и вздутие живота, связанное с СРК.Данные у детей предполагают, что рифаксимин может быть особенно полезным у пациентов с положительным результатом дыхательного теста на лактулозу 35, 36 . Клинически благоприятный модулирующий эффект рифаксимина в отличие от ранее испытанных и бесполезных антибиотиков широкого спектра действия интригует. Это может быть связано с более высокими внутрипросветными концентрациями в кишечнике, достигаемыми с помощью рифаксимина из-за его неабсорбируемости 37 . Дополнительным фактором может быть предполагаемое специфическое действие рифаксимина на бактериальную вирулентность и бактериальную метаболическую активность.В свою очередь, они могут уменьшить висцеральную гиперчувствительность и уменьшить гипералгезию.
Пробиотики в настоящее время пользуются большой популярностью среди пациентов и многих врачей из-за интуитивной привлекательности предполагаемого механизма действия и присущей им безопасности (хотя по этому последнему вопросу были высказаны некоторые сомнения). Однако, хотя экспериментальные данные иногда подтверждали их противовоспалительное, антиноцицептивное и даже модифицирующее действие на поведение и настроение мозга, результаты клинических исследований остаются двусмысленными, а иногда и противоречивыми.Как указали Шанахан и Куигли, 38 , существует множество мягких заявлений о пробиотиках, включая непроверенные этикетки, пробелы между результатами исследований и заявлениями на рынке. Также неудовлетворены утверждения на этикетке о количестве и типах жизнеспособных микробов, а также о спецификациях на полке относительно выживаемости упакованных микробных продуктов. Хотя некоторые пробиотики прошли хорошо спланированные и надежные испытания с положительными результатами, сообщалось о других безуспешных испытаниях. У детей Francavilla et al. 39 показали положительный ответ на Lactobacillus GG, а другие исследователи также на Lactobacillus reuterii, VSL # 3, Bifidobacterium infantis, brevis и longum 40 .Ясно, что только дальнейшие качественные исследования могут подтвердить реальную ценность пробиотиков в терапии СРК.
Пребиотики — это пищевые продукты, которые способствуют размножению видов бактерий, потенциально уменьшающих воспаление слизистой оболочки. У пребиотиков есть теоретический недостаток, заключающийся в том, что они могут способствовать образованию газа посредством внутрипросветной ферментации. Однако недавние данные предполагают, что это может быть временным явлением, которое задерживает, но не устраняет их в остальном благоприятные эффекты 41 .
Воспалительная основа симптомов типа СРК подтверждена прямыми доказательствами измененной иммунной активности слизистых оболочек, наличия инфильтратов иммунных клеток слизистой оболочки, пролиферации тучных клеток в непосредственной близости от нервных окончаний, повышенной проницаемости апикального соединения и других признаков 16, 17, 42 .Эти воспалительные реакции могут быть результатом постинфекционной, аллергической или идиопатической кишечной реакции. Клинические данные о том, что симптоматика СРК развивается у лиц с атопией, с астматическими, кожными или другими тканевыми иммунными воспалительными реакциями или без них. Также сообщалось об индуцированной микробами иммунной активности слизистой оболочки, связанной с конкретными видами бактерий в кишечнике 43 .
Несмотря на соблазнительный экспериментальный фон, введение противовоспалительных агентов для облегчения клинических проявлений СРК пока не имело большого клинического успеха.Кортикостероиды, месалазин и другие противовоспалительные средства не показали особой эффективности 44 . Только стабилизатор тучных клеток кетотифен, по-видимому, дал предварительные положительные результаты 45 .
Теоретическая модель «двух мозгов», которая предполагает, что центральный мозг работает вместе с кишечным мозгом, чтобы контролировать и регулировать функцию кишечника, остается не полностью определенной и лишь частично подтвержденной экспериментальными данными. Однако это мощная концепция и потенциально полезная в клиническом ведении, поскольку она обеспечивает основу для фармакологического вмешательства по центрально-периферической оси 46 .Важным дополнительным элементом, который следует учитывать, является тесное и хорошо налаженное взаимодействие между нервной и иммунной системами в кишечнике 47 .
При функциональных состояниях, таких как СРК, боль — это субъективное переживание, которое, даже если возникает из-за ноцицептивных раздражителей в кишечнике, формируется механизмами, действующими в различных слоях вдоль оси мозг-кишечник. Усиление и искажение афферентных сигналов из-за воспаления, сенсибилизации и других местных факторов приводит к нарушению передачи болевых сигналов.Кроме того, нарушение модуляции боли по нисходящей линии дополнительно усиливает входные сигналы в центральные цепи для восприятия и модуляции боли. Между эмоциями и когнитивной модуляцией боли существует ключевая связь, которая подчеркивает сильное влияние стресса и тревоги на восприятие висцеральных сигналов. Следовательно, боль в животе, являющаяся признаком СРК, вероятно, является результатом комбинации нарушенной периферической передачи сигналов и нарушенной модуляции эмоциональной боли 48 .
Лечение боли при СРК смещается в сторону агентов, которые модулируют висцеральную гиперчувствительность, проявляя свои действия, все еще плохо изученные, на различных участках оси кишечник-мозг.В связи с этим было указано, что интенсивность и рефрактерность боли, проявляемой пациентами, могут указывать на преобладающий механизм ноцицепции. Вообще говоря, более интенсивные и непрекращающиеся уровни боли указывают на большее вовлечение мозга, чем абдоминальные механизмы 48 . Следовательно, в тяжелых случаях существует большая потребность в использовании нейрофармакологических агентов, действующих на центральном уровне. В этом отношении блокаторы ГАМК и антидепрессанты, особенно те, которые обладают ингибирующим действием на обратный захват норадреналина, кажутся особенно эффективными.Классические трициклические антидепрессанты, такие как амитриптилин, нортриптилин и дезипрамин, которые включают множественные целевые механизмы, также могут быть полезны, хотя они, как правило, связаны с более неприятными побочными эффектами, такими как сонливость, антихолинергические системные эффекты и гипотензия. Важно титрование дозы. Некоторые классы антидепрессантов действуют на определенные рецепторы, что делает их особенно полезными при определенных жалобах. Например, сродство миртазапина к h2-рецепторам можно использовать для коррекции бессонницы и увеличения веса.Среди ингибиторов ГАМК прегабалин оказывает сильное подавляющее действие на генерализованную тревогу и ноцицепцию, что может быть весьма полезным 49 .
Практическую ценность нейрофармакологических агентов для лечения боли нельзя легко отделить от их воздействия на основное тревожное / депрессивное расстройство. Однако относительно низкие дозы этих препаратов, которые обычно используются для лечения СРК, обычно ниже, чем обычные для лечения психических состояний, если только психопатологический компонент не требует полного использования психотропов.
Психологические подходы, включая поведенческую терапию, были с энтузиазмом предложены как немедикаментозный подход к коррекции эмоционального компонента расстройств функционального типа. К ним относятся психотерапия для облегчения вызванной стрессом тревоги, такая как когнитивно-поведенческая терапия и психодинамическая терапия. Гипнотерапия, проводимая хорошо обученным терапевтом, может помочь ребенку погрузиться в состояние транса. Сообщается, что эти официально проводимые психологические методы лечения достигли значительного успеха и все чаще применяются сегодня.Однако клиницисты должны знать о высокой частоте ответа на плацебо, наблюдаемой в большинстве контролируемых исследований СРК и связанных состояний (30–70%). Кроме того, более структурированные психотерапевтические подходы требуют много времени, а их долгосрочная эффективность остается недоказанной.
На периферическом уровне препараты, воздействующие на моторную и / или секреторную функцию, уже давно используются для облегчения боли, а также для уменьшения характерного характера дефекации при СРК, будь то запор и / или диарея, которые могут, препятствуя упорядоченному движению, вызывать боль. .В эту группу средств входят классические спазмолитики, антидиарейные и слабительные средства различных типов. Санкционированное временем использование таких агентов, свидетельствующее об их популярности, не предполагает доказанной клинической эффективности. В частности, классические спазмолитики с антихолинергическим действием (следовательно, с неприятными побочными эффектами) и неантихолинергические спазмолитики (в первую очередь блокаторы кальциевых каналов), такие как мебеверин и отилония бромид, хотя и широко используются, имеют лишь слабые научные доказательства их клинической эффективности.
Обычно используются обычные противодиарейные средства, такие как лоперамид, но при диарее, связанной с СРК, их трудно модулировать, и они проявляют склонность к ускорению запора, что беспокоит пациента, который обычно ожидает более стабильного регулирующего действия на дефекацию 7 .
Диарея при СРК также может быть вызвана или усугублена мальабсорбцией желчных кислот с перетеканием в толстую кишку, где эти молекулы, особенно в их неконъюгированной форме (как побочные продукты бактериального гидролиза), раздражают слизистую оболочку толстой кишки и вызывают отток воды 50 .Избыточное выделение желчных кислот может быть результатом либо аномально ускоренного транзита по тонкому кишечнику, либо нарушения слизистой оболочки подвздошной кишки со снижением реабсорбции желчных кислот подвздошной кишки или перепроизводства печенью. Независимо от конкретного задействованного механизма пероральные секвестранты желчных кислот, действующие внутримышечно, такие как холестирамин и более приятный на вкус продукт колесевелам, могут помочь контролировать диарею 51 . Тщательное титрование доз этих агентов необходимо для предотвращения неоправданного перехода к запорам и вздутию живота.
Элюксадолин представляет собой комплексный активатор опиодных рецепторов, который оказался полезным в качестве противодиарейного и антиноцицептивного средства при СРК-D 52 . Его эффекты более тонкие, чем у традиционного противодиарейного средства лоперамида, но он показал тревожную, хотя и необычную, склонность к панкреатиту, хотя в основном у пациентов с холецистэктомией.
Терапевтический эффект обычных слабительных средств у детей сложно изменить. Растворы ПЭГ являются предпочтительным агентом.Появляются новые потенциально полезные агенты. Линаклотид, агонист энтеросолюбильной гуанилатциклазы, и любипростон, аналог простагландина E, способствуют выведению воды в кишечник. Кроме того, они обладают предполагаемым антиноцицептивным действием, что делает их пригодными для лечения СРК-З. К сожалению, хотя и весьма полезен для взрослых, ни один из этих двух агентов пока не одобрен для терапевтических целей у детей (и даже сообщалось о некоторых отрицательных эффектах любипростона в этой молодой возрастной группе) 53 .
Семейное окружение может положительно или отрицательно влиять на проявление детьми симптомов СРК. Похоже, что парентеральное отношение, моделирование симптомов, методы совладания с психологическими особенностями и подверженность семье стрессу могут потенциально влиять на сообщения детей о желудочно-кишечных и не желудочно-кишечных симптомах 54 . Таким образом, привлечение родителей и, возможно, других членов семьи, чтобы помочь изменить поведение ребенка при болезни и влияние симптомов на повседневную деятельность, имеет некоторую теоретическую основу.Однако исследований, подтверждающих терапевтическую пользу вмешательства через родственников, еще предстоит провести.
- Камиллери М., Ди Лоренцо С. Ось мозга и кишечника: от базового понимания до лечения СРК и связанных с ним расстройств. J Pediatr Gastroenterol Nutr. 2012; 54: 446-53.
- Self MM, Czyzewski DI, Chumpitazi BP, et al. Подтипы синдрома раздраженного кишечника у детей и подростков. Clin Gastroenterol Hepatol. 2014; 12: 1468-73.
- Giannetti E, de’Angelis G, Turco R, et al.Подтипы синдрома раздраженного кишечника у детей: распространенность при постановке диагноза и при последующем наблюдении. J Pediatr. 2014; 164: 1099-1103 e1.
- Saps M, Velasco-Benitez CA, Bloom PJJ, et al. Проспективное исследование желудочно-кишечных симптомов у школьников Южной Америки. J Pediatr Gastroenterol Nutr. 2018; 66: 391-394.
- Малагелада Дж. Р., Малагелада С. Механизм-ориентированная терапия синдрома раздраженного кишечника. Достижения в терапии. 2016; 33: 877-893.
- Hyams JS, Burke G, Davis PM, et al.Боль в животе и синдром раздраженного кишечника у подростков: исследование на уровне сообщества. J Pediatr. 1996; 129: 220-6.
- Sandhu BK, Paul SP. Синдром раздраженного кишечника у детей: патогенез, диагностика и доказательное лечение. Мир Дж. Гастроэнтерол. 2014; 20: 6013-23.
- Hoekman DR, Rutten JM, Vlieger AM, et al. Годовые затраты на лечение детского синдрома раздраженного кишечника, функциональной боли в животе и синдрома функциональной боли в животе. J Pediatr. 2015; 167: 1103-8 e2.
- Куигли Э.М., Шанахан Ф. Язык медицины: слова как слуги и негодяи. Clin Med (Лондон). 2009; 9: 131-135.
- Philips EM, Peeters B, Teeuw AH, et al. Стрессовые жизненные события у детей с функциональными нарушениями дефекации. J Pediatr Gastroenterol Nutr. 2015; 61: 384-92.
- Chogle A, Mintjens S, Saps M. Педиатрический IBS: обзор патофизиологии, диагностики и лечения. Pediatr Ann. 2014; 43: e76-82.
- Чанг Л., Берман С., Майер Е.А. и др.Ответы мозга на висцеральные и соматические раздражители у пациентов с синдромом раздраженного кишечника с фибромиалгией и без нее. Am J Gastroenterol. 2003; 98: 1354-61.
- Сейно С., Ватанабе С., Ито Н. и др. Повышенная слуховая реакция ствола мозга и стиль родительской связи у детей с желудочно-кишечными симптомами. PLoS One. 2012; 7: e32913.
- Giannetti E, Maglione M, Sciorio E, et al. Вырастают ли дети из-за синдрома раздраженного кишечника. J Pediatr. 2017; 183: 122-126.e1.
- Росс SE. «Мемы» как возбудители психосоматических заболеваний. Ann Intern Med. 1999; 131: 867-71.
- Matricon J, Meleine M, Gelot A и др. Обзорная статья: Связь между активацией иммунной системы, кишечной проницаемостью и синдромом раздраженного кишечника. Алимент Pharmacol Ther. 2012; 36: 1009-31.
- Cremon C, Gargano L, Morselli-Labate AM и др. Иммунная активация слизистой оболочки при синдроме раздраженного кишечника: гендерная зависимость и связь с пищеварительными симптомами.Am J Gastroenterol. 2009; 104: 392-400.
- Элли Л., Росси В., Конте Д. и др. Повышенный уровень ртути у пациентов с целиакией после безглютеновой схемы. Гастроэнтерол Рес Прак. 2015; 2015: 953042.
- Итан Ю., Джонс Б.Л., Инграм С.Дж. и др. Мировая корреляция фенотипа и генотипов персистенции лактазы. BMC Evol Biol. 2010; 10: 36.
- Мэдсен Дж. Л., Линнет Дж., Румессен Дж. Дж. Влияние неабсорбированных количеств смеси фруктозы и сорбита на транзит через тонкий кишечник у здоровых добровольцев.Dig Dis Sci. 2006; 51: 147-53.
- Casellas F, Aparici A, Casaus M и др. Субъективное восприятие непереносимости лактозы не всегда указывает на мальабсорбцию лактозы. Clin Gastroenterol Hepatol. 2010; 8: 581-6.
- Мюррей К., Уилкинсон-Смит В., Хоад С. и др. Различное влияние FODMAP (ферментируемых олиго-, ди-, моносахаридов и полиолов) на содержимое тонкого и толстого кишечника у здоровых людей, показанное с помощью МРТ. Am J Gastroenterol. 2014; 109: 110-9.
- Chumpitazi BP, Cope JL, Hollister EB, et al.Рандомизированное клиническое исследование: биомаркеры кишечного микробиома связаны с клинической реакцией на диету с низким содержанием FODMAP у детей с синдромом раздраженного кишечника. Алимент Pharmacol Ther. 2015; 42: 418-27.
- Бон Л., Стёрсруд С., Лильебо Т. и др. Диета с низким содержанием FODMAP снижает симптомы синдрома раздраженного кишечника, а также традиционные диетические рекомендации: рандомизированное контролируемое исследование. Гастроэнтерология. 2015; 149: 1399-1407.e2.
- Табане М., Симунович М., Ахтар-Данеш Н. и др.Вспышка острого бактериального гастроэнтерита связана с учащением случаев синдрома раздраженного кишечника у детей. Am J Gastroenterol. 2010; 105: 933-9.
- Даунс И.А., Арониадис О.К., Келли Л. и др. Постинфекционный синдром раздраженного кишечника: связь между гастроэнтеритом, воспалением, микробиомом и функциональными заболеваниями. J Clin Gastroenterol. 2017; 51: 869-877.
- Ханевик К., Диздар В., Лангеланд Н. и др. Развитие функциональных желудочно-кишечных расстройств после инфицирования Giardia lamblia.BMC Gastroenterol. 2009; 9: 27.
- Nakao JH, Collier SA, Gargano JW. Лямблиоз и последующий синдром раздраженного кишечника: продольное когортное исследование с использованием данных медицинского страхования. J Infect Dis. 2017; 215: 798-805.
- Schwille-Kiuntke J, Enck P, Zendler C, et al. Постинфекционный синдром раздраженного кишечника: наблюдение за группой пациентов с подтвержденными случаями бактериальной инфекции Salmonella или Campylobacter. Нейрогастроэнтерол Мотил. 2011; 23: e479-88.
- Spreadbury I, Ochoa-Cortes F, Ibeakanma C, et al.Сопутствующий психологический стресс и инфекционный колит являются ключом к поддержанию усиленной периферической сенсорной сигнализации. Нейрогастроэнтерол Мотил. 2015; 27: 347-55.
- Cremon C, Stanghellini V, Pallotti F и др. Сальмонеллезный гастроэнтерит в детстве является фактором риска развития синдрома раздраженного кишечника во взрослом возрасте. Гастроэнтерология. 2014; 147: 69-77.
- Yu D, Cheeseman F, Vanner S. Комбинированная оро-цекальная сцинтиграфия и водородный дыхательный тест на лактулозу демонстрируют, что дыхательный тест выявляет проходимость через рот и слепую кишку, а не избыточный бактериальный рост в тонком кишечнике у пациентов с СРК.Кишечник. 2011; 60: 334-40.
- Микель С., Мартин Р., Лашермес А. и др. Антиноцицептивный эффект Faecalibacterium prausnitzii на невоспалительных моделях, подобных СРК. Sci Rep.2016; 6: 19399.
- Яланка-Туовинен Дж., Салоярви Дж., Салонен А. и др. Состав фекальной микробиоты и перекрестный диалог между хозяином и микробом после гастроэнтерита и постинфекционного синдрома раздраженного кишечника. Кишечник. 2014; 63: 1737-45.
- Scarpellini E, Giorgio V, Gabrielli M, et al. Лечение рифаксимином избыточного бактериального роста в тонком кишечнике у детей с синдромом раздраженного кишечника.Eur Rev Med Pharmacol Sci. 2013; 17: 1314-20.
- Коллинз Б.С., Лин Х.С. Двойное слепое плацебо-контролируемое исследование избыточного бактериального роста в тонком кишечнике у детей с хронической болью в животе. J Pediatr Gastroenterol Nutr. 2011; 52: 382-6.
- Jiang ZD, Ke S, Palazzini E, et al. Активность и концентрация рифаксимина в фекалиях in vitro после перорального приема. Антимикробные агенты Chemother. 2000; 44: 2205-6.
- Шанахан Ф, Куигли ЭМ.Манипуляции с микробиотой для лечения IBS и IBD-проблем и противоречий. Гастроэнтерология. 2014; 146: 1554-63.
- Francavilla R, Miniello V, Magista AM и др. Рандомизированное контролируемое исследование Lactobacillus GG у детей с функциональной болью в животе. Педиатрия. 2010; 126: e1445-52.
- Джаннетти Э, Стаяно А. Пробиотики при синдроме раздраженного кишечника: клинические данные у детей. J Pediatr Gastroenterol Nutr. 2016; 63 Приложение 1: S25-6.
- Huaman JW, Mego M, Manichanh C и др.Эффекты пребиотиков по сравнению с диетой с низким содержанием фуд-карт у пациентов с функциональным расстройством кишечника. Гастроэнтерология. 2018; 28 июня [Epub перед печатью]
- О’Мэлли Д. Иммуномодуляция кишечной нервной функции при синдроме раздраженного кишечника. Мир Дж. Гастроэнтерол. 2015; 21: 7362-6.
- Пауэлл Н., Уокер М.М., Талли, штат Нью-Джерси. Иммунная система слизистых оболочек: главный регулятор двунаправленных сообщений кишечника и мозга. Нат Рев Гастроэнтерол Гепатол. 2017; 14: 143-159.
- Торнблом Х., Симрен М.В поисках модифицирующего болезнь лечения синдрома раздраженного кишечника. Кишечник. 2016; 65: 2-3.
- Klooker TK, Braak B, Koopman KE и др. Кетотифен, стабилизатор тучных клеток, снижает висцеральную гиперчувствительность и улучшает кишечные симптомы у пациентов с синдромом раздраженного кишечника. Кишечник. 2010; 59: 1213-21.
- Колоски Н.А., Джонс М., Калантар Дж. И др. Путь между мозгом и кишечником при функциональных желудочно-кишечных расстройствах является двунаправленным: 12-летнее проспективное популяционное исследование.Кишечник. 2012; 61: 1284-90.
- Ghia JE, Blennerhassett P, Collins SM. Нарушение парасимпатической функции увеличивает восприимчивость к воспалительному заболеванию кишечника на мышиной модели депрессии. J Clin Invest. 2008; 118: 2209-18.
- Дроссман Д.А. Redux: вырастают ли маленькие брюхопухи, чтобы стать большими. Clin Gastroenterol Hepatol. 2014; 12: 2033-6.
- Сапс М., Миранда А. Фармакология желудочно-кишечного тракта. Handb Exp Pharmacol. 2017; 239: 147-176.
- Баджор А., Торнблом Х., Рудлинг М. и др.Повышенное воздействие желчных кислот толстой кишки: важный фактор для симптомов и лечения СРК. Кишечник. 2015; 64: 84-92.
- Camilleri M, Acosta A, Busciglio I, et al. Влияние колесевелама на фекальные желчные кислоты и функции кишечника при синдроме раздраженного кишечника с преобладанием диареи. Алимент Pharmacol Ther. 2015; 41: 438-48.
- Уэйд П.Р., Палмер Дж. М., МакКенни С. и др. Модуляция желудочно-кишечной функции MuDelta, смешанный агонист µ-опиоидных рецепторов / антагонист µ-опиоидных рецепторов.Br J Pharmacol. 2012; 167: 1111-25.
- Hyman PE, Di Lorenzo C, Prestridge LL, et al. Любипростон для лечения функциональных запоров у детей. J Pediatr Gastroenterol Nutr. 2014; 58: 283-91.
- ван Тилбург М.А., Леви Р.Л., Уокер Л.С. и др. Психосоциальные механизмы передачи соматических симптомов от родителей детям. Мир Дж. Гастроэнтерол. 2015; 21: 5532-41.
SIBO: сопутствующие заболевания, SIFO и диагностика
Здоровый микробиом кишечника необходим для оптимальной иммунной функции и благополучия.Чрезмерный рост микробов в тонкой кишке связан с рядом проблем со здоровьем и может быть вызван многими факторами. В частности, избыточный бактериальный рост в тонком кишечнике (СИБР) представляет собой состояние, которое проявляется рядом пагубных желудочно-кишечных (ЖКТ) и не связанных с ЖКТ симптомов и связано с различными сопутствующими заболеваниями. Восстановление баланса кишечной флоры с помощью индивидуализированных вмешательств и индивидуальных методов лечения, учитывающих факторы образа жизни и потребности в питании, может значительно улучшить здоровье.
В этом видео преподаватель IFM Томас Султ, доктор медицинских наук, IFMCP обсуждает лечебное питание и изменяемые планы питания, которые могут быть подходящими для пациентов с SIBO.
Сопутствующие заболевания SIBO
Результаты исследований подтвердили связь между СИБР и такими заболеваниями, как синдром раздраженного кишечника (СРК), воспалительное заболевание кишечника (ВЗК), нарушения моторики, хронический панкреатит, цирроз печени и различные синдромы иммунодефицита. 1,2 Специфично для СРК, в систематическом обзоре и метаанализе 2020 г. было изучено 25 исследований «случай-контроль» с участием в общей сложности 3192 пациентов с СРК и 3 320 человек контрольной группы, и было обнаружено, что распространенность СИБР у пациентов с СРК значительно увеличилась. 3
Кроме того, более мелкие исследования показали, что SIBO чаще встречается в популяциях с активной инфекцией H. pylori 4 и повреждением спинного мозга с тромбозом глубоких вен, 5 , а также связан с детским ожирением, 6 папулопустулезная розацеа, 7 и неалкогольная жировая болезнь печени (НАЖБП) чаще, чем в контрольной группе. В небольшом исследовании детей с ожирением и СИБР исследователи обнаружили повышенный риск развития НАЖБП. 8 В исследовании сделан вывод о том, что взаимосвязь между дисбактериозом кишечника и диетой может влиять на ось кишечник-печень. 8 Интересно отметить, что исследователи обнаружили более низкую распространенность СИБР у пациентов с диабетом 1 типа и предположили, что это может быть связано с вмешательством в питание при лечении заболевания. 9
С учетом грибкового компонента
В здоровом желудочно-кишечном тракте бактериальные и грибковые организмы больше всего колонизируют толстую кишку, тогда как эти микробные сообщества появляются в меньшей степени в тонкой кишке.Как и в случае SIBO, чрезмерный рост грибков в тонком кишечнике (SIFO) может привести к различным системным симптомам, таким как мигрень, усталость, депрессия, вздутие живота и т. Д. 10 Также, как и SIBO, нарушение моторики кишечника и снижение количества кислоты в желудке в результате использования PPI являются потенциальными факторами риска, особенно для SIFO. 1,11-13
В то время как лечение SIBO может включать антибиотики и пробиотики, противогрибковая терапия 1,14 может быть эффективной для улучшения симптомов SIFO. 13 Диетические модификации также могут быть полезны при обоих состояниях. В пилотном исследовании оценивалась эффективность диетического вмешательства в сочетании с противогрибковыми препаратами для пациентов с хронической формой кишечного разрастания Candida . 15 Через десять дней после диеты и контрольной группы, получавшей противогрибковое лечение, обе показали удовлетворительный противогрибковый и симптоматический эффект без статистически значимой разницы; однако при втором обследовании через три месяца группа вмешательства по диете показала значительно более высокий процент пациентов без симптомов (85%) по сравнению с контрольной группой (42.5%). 15
Клинический диагноз и первопричина
SIBO может быть сложной задачей для диагностики, а при наложении симптомов SIFO также может быть фактором дисбаланса желудочно-кишечного тракта и важным фактором, который следует учитывать при выявлении основных причин и выборе оптимальных стратегий лечения. Недавняя литература предполагает, что не существует золотого стандарта для диагностики СИБР. 16 Согласно клиническим рекомендациям Американского колледжа гастроэнтерологии 2020, аспират и посев тонкой кишки часто считаются подходящими для диагностики SIBO, а также для использования дыхательного теста у пациентов с СРК; тем не менее, в руководстве признаются продолжающиеся усилия по переоценке критериев диагностики SIBO и оптимальных методов диагностического тестирования. 1
Для потенциальных диагнозов SIBO и SIFO важно выявление и лечение основных состояний, вызывающих микробный дисбаланс в тонком кишечнике, а восстановление популяций кишечной флоры может значительно улучшить здоровье и облегчить ряд симптомов. 17,18 Структура 5R IFM решает ряд проблем со здоровьем GI, включая SIBO и SIFO, и использует определенные шаги — удаление, замена, повторная инокуляция, ремонт и ребалансировка — чтобы помочь восстановить естественный баланс в системе GI.Подходы функциональной медицины для улучшения здоровья кишечника могут включать в себя диетические вмешательства, которые снижают ферментацию углеводов в кишечнике, чтобы помочь справиться с бактериальным и грибковым разрастанием, или элиминационную диету, которая удаляет триггерные продукты, чтобы потенциально уменьшить воспаление и улучшить симптомы.
Присоединяйтесь к IFM в модуле расширенной практики GI (APM), чтобы изучить клинически полезные методы, такие как концепция 5R для решения всех типов желудочно-кишечных проблем. В дополнение к последним исследованиям вы также узнаете о том, как разработать индивидуальные протоколы лечения с использованием образа жизни, диеты, нутрицевтиков, фармацевтических препаратов и растений, которые помогут восстановить здоровье кишечника.
Статьи по теме
Основы 5R для здоровья кишечника
Управление SIBO с помощью диетических вмешательств
Создание новой, более здоровой нормы с Винсентом Педре, MD, IFMCP, и Робертом Раунтри, MD
Список литературы
- Pimentel M, Saad RJ, Long MD, Rao SSC. Клинические рекомендации ACG: избыточный бактериальный рост в тонком кишечнике. Ам Дж. Гастроэнтерол . 2020; 115 (2): 165-178. DOI: 10.14309 / ajg.0000000000000501
- Ли А.А., Бейкер Дж. Р., Вамстекер Э. Дж., Саад Р., ДиМаньо М. Дж.Избыточный бактериальный рост в тонком кишечнике часто встречается при хроническом панкреатите и связан с диабетом, серьезностью хронического панкреатита, низким уровнем цинка и употреблением опиатов. Ам Дж. Гастроэнтерол . 2019; 114 (7): 1163-1171. DOI: 10.14309 / ajg.0000000000000200
- Шах А., Талли, штат Нью-Джерси, Джонс М. и др. Избыточный бактериальный рост тонкой кишки при синдроме раздраженного кишечника: систематический обзор и метаанализ исследований случай-контроль. Ам Дж. Гастроэнтерол . 2020; 115 (2): 190-201. DOI: 10.14309 / ajg.0000000000000504
- Enko D, Kriegshäuser G. Функциональные (13) дыхательные тесты на C-мочевину и глюкозу, водород / метан показывают значительную связь избыточного бактериального роста в тонком кишечнике у людей с активной инфекцией Helicobacter pylori . Клин Биохим . 2017; 50 (1-2): 46-49. DOI: 10.1016 / j.clinbiochem.2016.08.017
- Cheng X, Zhang L, Xie NC, Xu HL, Lian YJ. Связь между избыточным бактериальным ростом в тонкой кишке и тромбозом глубоких вен у пациентов с повреждениями спинного мозга. J Тромб Haemost . 2017; 15 (2): 304-311. DOI: 10.1111 / jth.13583
- Guercio Nuzio S, Di Stasi M, Pierri L, et al. Множественные аномалии оси кишечник-печень у детей с ожирением с поражением печени и без него . Педиатр ожирения . 2017; 12 (6): 446-452. DOI: 10.1111 / ijpo.12164
- Agnoletti AF, DE Col E, Parodi A, et al. Этиопатогенез розацеа: проспективное исследование с трехлетним наблюдением. G Итал Дерматол Венереол . 2017; 152 (5): 418-423. DOI: 10.23736 / S0392-0488.16.05315-3
- Белей О., Олариу Л., Добреску А., Марковичи Т., Марджинян О. Взаимосвязь между неалкогольной жировой болезнью печени и избыточным бактериальным ростом тонкой кишки среди детей и подростков с избыточным весом и ожирением. J Педиатр Метаб эндокринола . 2017; 30 (11): 1161-1168. DOI: 10.1515 / jpem-2017-0252
- Адамска А., Новак М., Пилациски С. и др. Избыточный бактериальный рост в тонком кишечнике у взрослых пациентов с диабетом 1 типа: его распространенность и связь с метаболическим контролем и наличием хронических осложнений заболевания. Pol Arch Med Wewn . 2016; 126 (9): 628-634. DOI: 10.20452 / pamw.3501
- Сингх Р., Маллин Г.Е. Синдром истощения и недоедание, вызванные чрезмерным ростом грибков в тонкой кишке: отчет о болезни и обзор литературы. Интегр Мед (Энсинитас) . 2017; 16 (3): 48-51.
- Su T, Lai S, Lee A, He X, Chen S. Мета-анализ: ингибиторы протонной помпы умеренно повышают риск избыточного бактериального роста в тонком кишечнике. Дж Гастроэнтерол . 2018; 53 (1): 27-36. DOI: 10.1007 / s00535-017-1371-9
- Джейкобс К., Косс Адам Э, Атталури А., Валестин Дж., Рао С.С. Нарушение моторики и использование ингибиторов протонной помпы являются независимыми факторами риска избыточного бактериального и / или грибкового роста в тонком кишечнике. Алимент Фармакол Тер . 2013; 37 (11): 1103-1111. DOI: 10.1111 / apt.12304
- Erdogan A, Rao SSC. Грибковое разрастание тонкой кишки. Курр Гастроэнтерол Реп . 2015; 17 (4): 16. DOI: 10.1007 / s11894-015-0436-2
- Авелар Родригес Д., Райан П. М., Торо Монхарас Е. М., Рамирес Майанс Дж. А., Куигли Е. М..Избыточный бактериальный рост в тонкой кишке у детей: современный обзор. Передний педиатр . 2019; 7: 363. DOI: 10.3389 / fped.2019.00363
- Оташевич С., Момилович С., Петрович М., Радулови О., Стоянович Н.М., Арси-Арсеньевич В. Модификация диеты и лечение кишечного разрастания Candida — пилотное исследование. J Mycol Med . 2018; 28 (4): 623-627. DOI: 10.1016 / j.mycmed.2018.08.002
- Adike A, DiBaise JK. Разрастание бактерий в тонком кишечнике: последствия для питания, диагностика и лечение. Гастроэнтерол Клин Норт Ам . 2018; 47 (1): 193-208. DOI: 10.1016 / j.gtc.2017.09.008
- Левентогианнис К., Гколфакис П., Спитакис Г. и др. Влияние препарата четырех пробиотиков на симптомы у пациентов с синдромом раздраженного кишечника: связь с избыточным бактериальным ростом кишечника. Пробиотики, антимикробные белки . 2019; 11 (2): 627-634. DOI: 10.1007 / s12602-018-9401-3
- Krajicek EJ, Hansel SL. Разрастание бактерий в тонком кишечнике: обзор первичной медико-санитарной помощи. Mayo Clin Proc . 2016; 91 (12): 1828-1833. DOI: 10.1016 / j.mayocp.2016.07.025
Диета, дети и расстройства аутистического спектра, часть 1: Кишечник
Для взрослых самой большой (но не единственной!) Причиной перехода на Палео является, вероятно, потеря веса. Но среди взрослых, соблюдающих палеодиету для своих детей, расстройства аутистического спектра (РАС) являются одной из самых распространенных проблем.
Многие родители сначала начинают с безглютеновой диеты (или без глютена и казеина), а затем оттуда открывают для себя Палео.Другие сразу же вмешиваются. Но в любом случае, , многие люди сообщают о резком улучшении симптомов у своих детей, когда они пробуют какой-либо вид палео или даже очень слабо цельнопищевую диету без глютена .
Итак, что могло вызвать это улучшение? Есть некоторые интересные связи между диетой и РАС, и их обсуждает множество исследований, но это также очень эмоционально заряженная тема, и важно не выходить за рамки исследований, направленных на поиск «причины» или «лечения».”
Эта статья не объясняет «причины аутизма». Расстройства аутистического спектра очень сложны, и их нельзя связать с одним отрывком. Это также не замена настоящего врача, терапевта или консультанта, и никогда не предназначалось для этого. Это просто пост, в котором представлена интересная информация об одном очень специфическом факторе, который может способствовать возникновению симптомов РАС сложным образом, который еще никто полностью не понимает.
Тем не менее, с этой кристальной ясностью взаимодействие диеты и симптомов РАС является абсолютно захватывающим и потенциально очень важным, хотя многие исследования все еще находятся на стадии грызунов.Итак, в Части 1 мы рассмотрим только кишечник (как и почти любое другое хроническое заболевание, РАС тесно связаны со здоровьем кишечника), а Часть 2 будет охватывать все остальное (дефицит питательных веществ, вызванный селективностью питания, Омега-3). жиры, холестерин…).
ДМПП связаны с дисфункцией кишечникаОгромное количество детей с РАС имеют различные проблемы с желудочно-кишечным трактом, от видимых (диарея, рвота) до невидимых (боль, нарушение всасывания питательных веществ, кислотный рефлюкс).И что еще более интересно, исследователи в этом исследовании обнаружили сильную корреляцию между тяжестью симптомов желудочно-кишечного тракта и тяжестью симптомов РАС.
Эти проблемы могут проявляться так же, как и у любого другого человека, или как поведенческие проблемы, которые кажутся совершенно не связанными друг с другом, включая нарушение сна, раздражительность, оппозиционное поведение или членовредительство. К сожалению, если поведенческие симптомы являются единственным очевидным признаком, основная проблема кишечника часто может остаться недиагностированной , потому что это не очевидный скачок от «проблем со сном» к «кишечной флоре».”
Кишечные симптомы обычно указывают на какую-то основную проблему — диарея и вздутие живота не появляются сами по себе. Итак, вот два обычных подозреваемых: дисбиоз кишечной флоры и кишечная проницаемость («дырявый кишечник»).
Дисбактериоз кишечной флорыОдной из основных первопричин кишечных симптомов является дисбактериоз кишечника: совершенно очевидно, что ребенок с аутизмом имеет измененный паттерн кишечной флоры. Различные исследования показали, что…
- У аутичных детей больше некоторых видов, например.грамм. desulfovibrio, чем у нейротипичных детей с такими же проблемами ЖКТ. Фактически, есть пара видов, которые, кажется, встречаются почти исключительно при аутизме.
- У аутичных детей меньше других видов, например бифидобактерии.
- Отношение Bacteroidetes к Firmicutes также ниже у аутичных детей (если эти имена кажутся знакомыми, вероятно, потому, что вы узнали их по исследованиям ожирения: оба этих вида также очень важны в исследованиях кишечной флоры и веса).
Неясно, как именно эти изменения кишечной флоры могут влиять на симптомы РАС, но мы знаем, что кишечник и мозг тесно связаны, и доказательства (например) того, что лечение антибиотиками может модулировать симптомы РАС, говорят об этом. Принимая во внимание, что мы до сих пор почти не знаем, как вообще выглядит «здоровый» микробиом, способность диеты изменять флору кишечника может быть одной из причин, почему она влияет на симптомы РАС.
Кишечная проницаемость («дырявый кишечник»)Другой частой причиной кишечных симптомов является кишечная проницаемость.Название «дырявый кишечник» звучит как полная чушь, но на самом деле это серьезное заболевание: в основном это означает, что стенка кишечника не работает должным образом как барьер между вашим телом и остальным миром; это пропускает в кровь вещи, которых там быть не должно. Это может быть вызвано проблемами кишечной флоры, а также раздражителями кишечника в рационе, различными инфекциями, лекарствами и другими факторами образа жизни. (Если вы хотите узнать больше, вот обзор)
Есть некоторые свидетельства того, что у детей с РАС повышенная проницаемость кишечника, чем у остальной части населения, что может быть еще одной причиной их симптомов.Например, в этом исследовании исследователи измерили кишечную проницаемость у пациентов с аутизмом и их родственников и сравнили ее со здоровыми неродственными контрольными субъектами. У 37% пациентов с РАС была необычная кишечная проницаемость, по сравнению с 21% родственников и всего 5% контрольной группы. Авторы исследования также обсуждают некоторые потенциальные способы, которыми кишечная проницаемость может способствовать развитию симптомов РАС, от иммунной дисфункции до взаимоотношений кишечника и мозга.
С другой стороны, другие исследования не обнаружили никакой взаимосвязи — надеюсь, возросший интерес к здоровью кишечника в последние несколько лет в конечном итоге приведет к большему количеству исследований с более крупными размерами выборки, чтобы мы могли получить лучшее представление.
Улучшает ли улучшение здоровья кишечника симптомы РАС?Итак, если основная дисфункция кишечника является обычным явлением при РАС, может ли лечение кишечных проблем помочь улучшить симптомы? К сожалению, неясно, действительно ли лечение патологии кишечника улучшит симптомы РАС. . Существующие исследования обнадеживают и интересны, но не окончательны.
ПробиотикиПервое, что приходит на ум при дисбактериозе кишечника, — это, как правило, пробиотики.Эти исследователи давали детям с аутизмом пробиотическую добавку, содержащую штаммы лактобацилл, бифидумбактерий и стрептококков. Добавки помогли нормализовать кишечную флору и уровень воспаления, но исследователи не отметили, повлияло ли это на их поведение.
У мышей лечение пробиотиками определенно помогает улучшить коммуникативное, сенсомоторное и тревожное поведение. У крыс введение побочного продукта бактериальной ферментации (продуцируемого некоторыми видами бактерий, количество которых повышено у аутичных детей) может вызвать симптомы аутизма даже без изменения фактической микрофлоры кишечника.Это говорит о том, что изменение кишечной флоры может фактически улучшить симптомы РАС. Но человеческий ребенок не мыши и не крысы — как говорится в этом исследовании,
«Может ли использование пробиотиков детьми с аутизмом привести к улучшению поведения, необходимо установить в хорошо контролируемых испытаниях с достаточным размером групп».
Непонятно, влияет ли пробиотическая терапия на симптомы РАС у людей так же, как у животных. Другая многообещающая теория, которая является всего лишь теорией, заключается в том, что улучшение при дисбактериозе кишечника может помочь улучшить выбор продуктов питания, что может улучшить общее состояние здоровья за счет устранения дефицита питательных веществ.Дети с аутизмом часто имеют крайне ограниченный выбор продуктов, которые они готовы есть. Типичный образец — это предпочтение мясной нездоровой пищи и сильное отвращение к фруктам, овощам и белкам.
Возможно, это на самом деле симптом дисбактериоза кишечника: у детей проблемы с перевариванием грубых кормов, что вызывает у них болезненные газы и вздутие живота, поэтому они отказываются от богатой клетчаткой растительной пищи, чтобы избежать боли. Лечение дисбактериоза кишечника может быть одним из способов решения этой проблемы и улучшения здоровья за счет общего улучшения качества питания ребенка.
Интересно, что антибиотики часто вызывают временное улучшение симптомов РАС, что может указывать на некоторый бактериальный рост, который лучше всего лечить с помощью комбинации антибиотиков и пробиотиков. Флора кишечника сложна!
Элиминационные диетыС точки зрения палео, «дырявый кишечник» сразу поднимает вопрос о пищевых раздражителях кишечника. И, к счастью, на самом деле есть некоторые исследования безглютеновых и казеиновых диет при РАС, поскольку они являются очень популярной домашней терапией.
В этом исследовании использовалась безглютеновая и казеиновая диета, и не было обнаружено значительных различий в поведении, но проблема в том, что даже исследователи отметили, что дети не были полностью безглютеновыми в течение безглютенового периода : несколько родителей и учителей сообщили, что крадут еду у других детей. Кроме того, чтобы участники не знали, на какой диете они на самом деле сидят, исследователи заменили глютен-содержащий мусор на безглютеновый мусор, что не совсем идеально для здоровья кишечника.
В других исследованиях, таких как это, пациенты с аутизмом, которые сидели на безглютеновой и без казеиновой диете, имели меньшую проницаемость кишечника, но здесь пациенты знали, что они соблюдают диету, поэтому невозможно исключить эффект плацебо.
Другими словами: это сложно, и разработать хорошие исследования очень сложно. Удаление раздражителей кишечника вряд ли кому-то повредит, но, в частности, трудно измерить, улучшит ли оно симптомы РАС.
Подводя итогиОдин из способов, которым диета может повлиять на симптомы расстройств аутистического спектра, — это улучшение здоровья кишечника.Совершенно очевидно, что дети с РАС часто страдают той или иной патологией кишечника, но гораздо менее ясно, улучшит ли их симптомы улучшение здоровья кишечника, и если да, то какие стратегии питания наиболее эффективны.
С другой стороны, можно с уверенностью сказать, что простые шаги по улучшению здоровья кишечника, вероятно, будут полезны для всех, независимо от того, имеют ли они какие-либо преимущества конкретно для симптомов РАС или нет. Даже если он «только» улучшает усвоение питательных веществ и снимает дискомфорт в желудочно-кишечном тракте, совершенно не влияя на поведение, от этого все равно нечего упускать.
Хотите знать, каким образом диета может влиять на РАС? Ознакомьтесь со второй частью этой серии статей, в которой рассказывается обо всем, кроме кишечника.



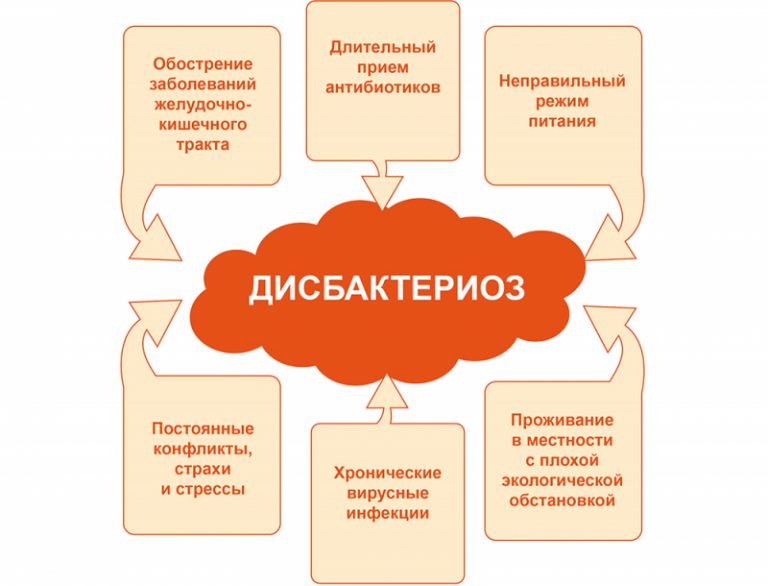 Через 30 минут после завтрака можно выпить цикорий, чай или компот.
Через 30 минут после завтрака можно выпить цикорий, чай или компот.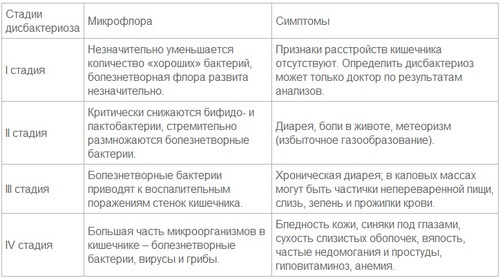


 8 в грамме стула. Ссылок на литературу в стандарте полно, но, что подозрительно, среди них нет ни одной зарубежной публикации. Ну а сами статьи и учебники не описывают, как именно сравнивали микрофлору здоровых и больных людей, то есть как именно был сделан вывод о нормальном содержании той или иной бактерии.
8 в грамме стула. Ссылок на литературу в стандарте полно, но, что подозрительно, среди них нет ни одной зарубежной публикации. Ну а сами статьи и учебники не описывают, как именно сравнивали микрофлору здоровых и больных людей, то есть как именно был сделан вывод о нормальном содержании той или иной бактерии.