Нейрогенный мочевой пузырь( гиперактивный мочевой пузыря, нейрогенная дисфункция нижних мочевых путей)
Причины заболевания
Заболевание характеризуется разнообразными формами нарушений резервуарной (способность накапливать мочу), эвакуаторной (способность выводить мочу) и вентильной (способность удерживать мочу в пузыре) функций мочевого пузыря вследствие поражения нервной системы на разных уровнях — от коры головного мозга до интрамурального аппарата (система внутристеночных нервов мочевого пузыря). Встречается в любом возрасте, так как поражения нервной системы могут быть и приобретенными, и врожденными.
Причинами могут служить разнообразные по характеру факторы.
У взрослых это могут быть различные травмы, воспалительные мозговые заболевания, нарушенное кровообращение, дегенеративные мозговые заболевания, сдавления нервов или спинномозговых корешков, дегенеративно-дистрофические изменения позвоночника.
У детей такими факторами могут служить несоответствие между развитием уровней регуляции мочеиспускательной системы и темпами созревания, нарушенный уровень обменных процессов, пороки развития поясничного и крестцового отелов, постродовые травмы.
Причины
- Заболевания головного мозга (например, опухоли, травмы, кровоизлияния, болезнь Паркинсона, инсульты, слабоумие).
- Заболевания спинного мозга (например, опухоли, травмы, заболевания позвоночника, межпозвоночные грыжи).
- Поражение периферической (нервы, идущие от спинного мозга) нервной системы (например, при сахарном диабете, интоксикациях, при нарушении формирования оболочки нерва).
- ВИЧ-инфекция.
Симптомы и протекание заболевания
Типичным проявлением нарушений мочеиспускания при локализации демиелинизирующих поражений выше центра мочеиспускания, расположенного в мосту головного мозга, является гиперрефлексия детрузора. Учащенное мочеиспускание через короткие промежутки времени, императивное недержание мочи, странгурия являются типичными симптомами гиперрефлексии детрузора. Возникая в любой период времени и зачастую в неудобном месте, указанные симптомы приносят значительное беспокойство больным. Механизм возникновения этих симптомов заключается в снижении или утрате произвольного контроля над актом мочеиспускания и снижении адаптационной способности детрузора. При этом рефлекторная дуга, включающая расположенный в крестцовой области центр и центр мочеиспускания в области моста головного мозга, остается нетронутой. Иными словами, при гиперрефлексии детрузора, несмотря на сохранение самостоятельного акта мочеиспускания, накопление достаточного количества мочи в мочевом пузыре становится невозможным.
При поражении надкрестцовой области больные могут испытывать недостаток супраспинального подавления автономных сокращений мочевого пузыря, что сопровождается гиперрефлексией детрузора вплоть до императивного недержания мочи, как и в случае церебральных нарушений. В то же время спинальные повреждения имеют и свои характерные особенности в виде поражения ретикулоспинальных путей, идущих от моста мозга и участвующих в синергической интеграции активности уретрального сфинктера и детрузора. Помимо непроизвольных сокращений детрузора, одновременно отмечается сокращение поперечнополосатого сфинктера уретры, что вызывает задержку мочеиспускания и сопровождается повышением внутрипузырного давления. Указанное состояние получило название детрузорно-сфинктерной диссинергии.
Клинические проявления надкрестцового поражения спинного мозга складываются из ирритативных (учащенное, императивное мочеиспускание, порой до императивного недержания мочи, в сочетании со странгурией) и обструктивных (прерывание струи мочи нередко до полной задержки мочеиспускания, что может сопровождаться болью в нижних отделах живота и промежности) симптомов. Для детрузорно-сфинктерной диссинергии характерно неполное опорожнение мочевого пузыря с появлением остаточной мочи, что повышает возможность развития воспалительных осложнений мочевого пузыря и верхних мочевых путей, а также уролитиаза. Ко всему прочему, при данном уровне поражения могут отмечаться неполное расслабление поперечнополосатого сфинктера и его паралич, что проявляется тяжелой формой недержания мочи (сфинктерное недержание).
Поражение крестцовой области вызывает утрату рефлекторного сокращения детрузора (детрузорная арефлексия) и потерю сократительной способности поперечнополосатого сфинктера уретры. В данной ситуации больные предъявляют жалобы на отсутствие позывов к акту мочеиспускания. При отсутствии нормального опорожнения мочевого пузыря в дальнейшем у больных развивается недержание мочи вследствие переполнения мочевого пузыря. Другим вариантом нарушения мочеиспускания при крестцовых повреждениях является снижение сократительной способности детрузора, что вызывает нарушение опорожнения мочевого пузыря и проявляется затрудненным мочеиспусканием вялой струей с ощущением неполного опорожнения мочевого пузыря. Все перечисленные выше симптомы со стороны нижних мочевых путей могут приводить к различным нарушениям верхних мочевых путей — пузырно-мочеточниковому рефлюксу, расширению мочеточников и лоханок, пиелонефриту и хронической почечной недостаточности.
Ввиду того, что денервация мочевого пузыря, на каком бы уровне она ни происходила, приводит к резко выраженным трофическим нарушениям, течение болезни часто осложняется интерстициальным циститом, вызывающим склерозирование и сморщивание мочевого пузыря (микроцист). Это тяжелое осложнение усугубляет опасность для почек и в ряде случаев требует специальных хирургических вмешательств для увеличения емкости мочевого пузыря.
Лучшие государственные клиники Израиля
Лучшие частные клиники Израиля
Лечение заболевания
Лечение нейрогенных дисфункций мочевого пузыря продолжает оставаться сложной и во многом еще нерешенной задачей. Болезнь затрагивает сложнейшие механизмы взаимоотношений детрузорно-сфинктерных систем, нарушает все три функции пузыря — накопление, удержание и изгнание мочи.
До недавнего времени даже не ставилась задача дать схему лечения, основанную на патогенетических принципах и подходах. Оно и сейчас имеет выраженную симптоматическую направленность.
Можно выделить три основных направления симптоматического лечения:
- медикаментозное;
- электростимуляция;
- паллиативно-симптоматические операции.
Однако основным видом лечения урологических нарушений у больных с нейрогенными дисфункциями мочевого пузыря является использование фармакологических средств. Оно зависит от нарушений уродинамики нижних мочевых путей, приводящих к затруднениям в накоплении мочи в мочевом пузыре или опорожнении мочевого пузыря.
К медикаментозным препаратам для лечения нейрогенных дисфункций мочевого пузыря относят:
- антихолинергические препараты — блокируют мускариновые холинорецепторы в мочевом пузыре, за счет чего достигается уменьшение сократимости детрузора в условиях его гиперрефлексии;
- миотропные спазмолитические релаксанты;
- -адреноблокаторы — снижают тонус внутреннего сфинктера;
- бета-адреноблокаторы — повышают тонус детрузора и внутрипузырное давление, способствуя тем самым изгнанию мочи;
- а-адреностимуляторы — повышают тонус сфинктеров и уретральное сопротивление, способствуя тем самым удержанию мочи;
- антагонисты ионов кальция; простагландины Е2 и F2а;
- внутрипузырное введение препаратов, обладающих нейро-токсическим воздействием.
В последнее время отмечают положительный эффект при применении низкоинтенсивного лазерного облучения (гелий-неоновый лазер).
Однако, ни медикаментозное лечение и стимуляция, ни симптоматические операции не дают удовлетворительных стойких результатов. Поэтому в последние 20 лет предприняты настойчивые попытки разработки методов лечения, основанных на патогенетических принципах восстановления иннервации мочевого пузыря. Разнообразие форм нейрогенных дисфункций не позволяет успешно решать все вопросы патогенетической терапии с помощью одного метода. Весь комплекс патогенетической терапии необходимо применять как можно раньше, до того как наступят вторичные осложнения в других органах и системах, а также дегенерация местных нервно-мышечных структур.
Лечение нейрогенного мочевого пузыря
- Мочеиспускание за счет напряжения брюшного пресса, либо за счет надавливания на низ живота.
- Формирование мочеиспускания за счет стимуляции кожи в области спины (так называемый триггерный механизм мочеиспускания).
- Лечебная физкультура — укрепления мышц тазового дна.
- Терапия, основанная на принципе обратной биологической связи, когда больной с помощью специальных устройств самостоятельно мочится в определенный момент.
- Индивидуальная лекарственная терапия с учетом гипо/гиперактивности (повышенного или пониженного тонуса) мочевого пузыря — применяют препараты либо расслабляющие замыкательный аппарат мочевого пузыря, либо увиливающее тонус стенки мочевого пузыря, иногда используется их совместное применение.
- Препараты, влияющие на работу нервной системы.
- Физиотерапевтическое лечение (например: электростимуляция области промежности, крестца, внутрипузырная электростимуляция, ультразвуковое воздействие, электросон, регионарная гипертермия (нагревание) мочевого пузыря, электрофорез лекарственных средств).
- Интерметтирующая катетеризация мочевого пузыря — когда больной самостоятельно, несколько раз в день вводит катетер (стерильную трубочку) в мочевой пузырь и опорожняет его.
Хирургическое лечение напрямую зависит от формы нейрогенного мочевого пузыря. Хирургическое эндоскопическое вмешательство при гипотонии нейрогенного мочевого пузыря заключается в трансуретральной воронкообразной резекции шейки мочевого пузыря, обеспечивающей в дальнейшем возможность опорожнения пузыря слабым нажатием снаружи. При гиперрефлекторном мочевом пузыре (со спастикой тазового дна и детрузорно-сфинктерной диссинергией) проводят надрез наружного сфинктера, что снижает напор мочеиспускания, а в последующем — гиперреактивность детрузора, увеличивая вместимость пузыря.
Также при нейрогенном мочевом пузыре возможно проведение оперативного увеличения мочевого пузыря (с использованием пластики тканей), ликвидация пузырно-мочеточникового рефлюкса, постановка цистостомического дренажа для опорожнения мочевого пузыря.
Патогенетическое лечение синдрома нейрогенного мочевого пузыря позволяет уменьшить риск повреждения мочевыделительных органов и необходимость оперативного вмешательства в будущем.Сообщите мне цены
Диагностика заболевания
Диагностирование нейрогенного мочевого пузыря, которое проводит врач — невролог, важны наряду с клинической картиной и результаты лабораторных и инструментальных исследований.
Проводится анализ и оценка нарушения процесса мочеиспускания, с помощью специальных таблиц и шкал, врач так же проводит оценку функциональности органов таза при осмотре больного.
Обязательно проводят рентгеноскопию верхних мочевыводящих путей, уретры и самого мочевого пузыря (рентген делается с применением специальных растворов), цистометрию (то есть, определяют давление в мочевом пузыре), и электромиографию поперечнополосатой мускулатуры околоуретральной области.
В дополнение для уточнения диагноза могут проводиться такие исследования: магнитно-резонансная и компьютерная томографии, иммунологические исследования, вирусологические исследования, бактериологические и биохимические анализы, электронейромиография.
Цены
| Заболевание | Ориентировочная цена, $ |
|---|---|
| Цены на обследование и лечение при раке яичка | 3 730 — 39 940 |
| Цены на вапоризацию аденомы простаты «зеленым лазером» | 16 050 |
| Цены на диагностику и лечение импотенции | 1 320 — 50 000 |
| Цены на диагностику мочеполовой системы у мужчин | 5 630 |
| Цены на лечение рака яичка | 15 410 |
| Цены на лечение мочекаменной болезни | 11 760 — 16 180 |
| Цены на лечение рака мочевого пузыря | 21 280 — 59 930 |
| Цены на диагностику простатита | 2 720 |
| Цены на диагностику мужского бесплодия | 6 300 |
| Цены на лечение рака предстательной железы | 23 490 — 66 010 |
| Заболевание | Ориентировочная цена, $ |
|---|---|
| Цены на диагностику мигрени | 7 060 — 8 260 |
| Цены на диагностику детской эпилепсии | 3 100 — 4 900 |
| Цены на шунтирование мозга при гидроцефалии | 33 180 |
| Цены на лечение болезни Паркинсона | 58 600 |
| Цены на лечение мигрени | 9 680 |
| Цены на диагностику бокового амиотрофического склероза | 6 550 |
| Цены на диагностику эпилепсии | 3 520 |
| Цены на реабилитацию после инсульта | 78 300 — 82 170 |
| Цены на лечение детской эпилепсии | 3 750 — 5 450 |
| Цены на лечение рассеянного склероза | 4 990 — 17 300 |
Видеоматериалы по теме
 Рассчитать стоимость лечения
Рассчитать стоимость леченияМатериалы по теме
israel-clinics.guru
Нейрогенная дисфункция мочевого пузыря: признаки, осложнения — Онлайн-диагностика
Медучреждения, в которые можно обратитьсяОбщее описание
Нейрогенная дисфункция мочевого пузыря (НДМП) — это многообразные патологические изменения резервуарной и эвакуаторной функций мочевого пузыря, являющиеся следствием дизрегуляции мочеиспускания различного происхождения и разного уровня иннервации. Частота патологии — до 10%.
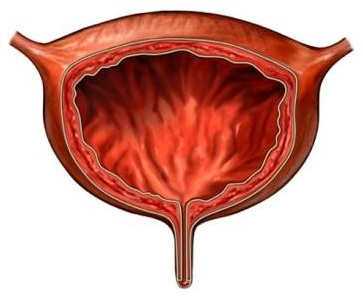 Известны следующие причины:
Известны следующие причины:
- Недостаточная функция супраспинального торможения спинальных центров регуляции мочеиспускания дезонтогенетического генеза;
- Миелодисплазия;
- Асинхронное развитие регуляторных систем акта мочеиспускания;
- Нарушение функционирования вегетативной системы;
- Нарушения в нейроэндокринной регуляции;
- Дизрегуляция рецепторной чувствительности;
- Изменение биоэнергетики детрузора.
Мочевой пузырь является норморефлекторным, когда мочеиспускание происходит при нормальном возрастном объеме мочевого пузыря, гипорефлекторным, когда объем превышает возрастную норму, и гиперрефлекторным, когда объем меньше возрастной нормы.
НДМП сопровождается вторичным хроническим циститом (до 80%), пиелоненефритом (60%), часто осложняется двусторонним ПМР, который может привести к уретерогидронефрозу, рефлюкс-нефропатии, артериальной гипертензии и хронической почечной недостаточности.
Симптомы нейрогенной дисфункции мочевого пузыря
Клинически гиперрефлекторный вариант проявляется поллакиурией, императивными позывами на мочеиспускание. Гипорефлекторный вариант характеризуется редкими мочеиспусканиями, ослаблением или отсутствием позыва на мочеиспускание, увеличенным объемом мочи при мочевыделении, инконтиненцией. Характер адаптации детрузора к возрастающему объему мочи позволяет выделить адаптированный и неадаптированный мочевой пузырь. Адаптация детрузора рассматривается как нормальная при несущественном увеличении внутрипузырного давления в фазу накопления. Нарушением адаптации считается непроизвольное сокращение детрузора при заполнении мочевого пузыря, ведущее к увеличению внутрипузырного давления выше 15 см водного столба. Есть и еще одна разновидность НДПМ, симптомы которой появляются при занятии больным вертикального положения, это так называемый постуральный мочевой пузырь. Чаще встречаются гиперрефлекторная (50%), гипорефлекторная (5%), постуральная (25-30%), неадаптированная (60-70%) НДМП.
Диагностика нейрогенной дисфункции мочевого пузыря
С диагностической целью проводится регистрация ритма спонтанных мочеиспусканий на протяжении 1-2 суток, сонография мочевого пузыря, урофлоуметрия с целью детекции объема и скорости мочеиспускания, цистоманометрия при естественном наполнении мочевого пузыря, ретроградная цистометрия в вертикальном и горизонтальном положении пациента, непрерывная профилометрия уретры. По показаниям проводят электромиографию мышц тазового дна и анального сфинктера, миелографию, КТ либо МРТ позвоночника.
Лечение нейрогенной дисфункции мочевого пузыря
Лечение гиперрефлекторного неадаптированного мочевого пузыря направлено на увеличение эффективного объема мочевого пузыря и купирование незаторможенных сокращений детрузора в фазу накопления. С этой целью применяются антихолинергические средства. При нестабильности детрузора наиболее эффективен «Дриптан» («Оксибутин»), который назначается детям старше 5 лет при индивидуальном подборе дозы. Применяются антагонисты мускариновых рецепторов, ингибиторы простагландинов. С целью улучшения функционального состояния ЦНС показаны «Пикамилон» по 0,02 2-3 раза в день, «Пантогам». Для усиления действия медикаментов рекомендуется физиотерапия: теплолечение на мочевой пузырь, электрофорез с холинолитиками и спазмолитиками.
Лечение гипорефлекторного мочевого пузыря заключается, прежде всего, в обеспечении регулярного и эффективного опорожнения мочевого пузыря (принудительные мочеиспускания не реже одного раза в 2-3 часа). Из медиментозных средств наиболее эффективны М-холиномиметики. При гипорефлекторном мочевом пузыре происходит гипоксия и метаболические изменения в стенке мочевого пузыря, поэтому в лечение включаются цитохром С, гипербарическая оксигенация, коферментные формы витаминов группы B. Параллельно проводят физиотерапию: СМТ, ДДТ в ритме синкопа по стимулирующей методике, лазер на область мочевого пузыря или спинальные центры мочеиспускания, рефлексотерапия. При отсутствии эффекта от консервативной терапии в течение длительного времени, низкого градиента пузырно-уретрального давления возможно проведение хирургического лечения, заключающиегося в восстановлении гладкомышечного сфинктера уретры и создании или укреплении наружного жома из поперечнополосатой мускулатуры.
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.

- Оксибутинина гидрохлорид (Дриптан) — препарат, снижающий тонус гладкой мускулатуры мочевыводящих путей. Режим дозирования: взрослым препарат назначают внутрь по 5 мг 2-3 раза/сут. Детям и лицам пожилого возраста рекомендованная доза составляет 5 мг 2 раза/сут.
- Пантогам (ноотропный препарат с противосудорожным действием). Режим дозирования: принимается перорально по 0,025 мг 4 раза в день на протяжении 2-3 месяцев.
- Дистигмина бромид (Убретид) — препарат, улучшающий нервно-мышечную передачу, повышает тонус мочевого пузыря. Режим дозирования: для приема внутрь — 5-10 мг 1 раз/сут.; в/м — 500 мкг 1 раз/сут. Длительность применения устанавливают индивидуально.
- Неостигмина метилсульфат (Прозерин) — препарат, улучшающий нервно-мышечную передачу, повышает тонус мочевого пузыря. Режим дозирования: внутрь взрослым — по 10-15 мг 2-3 раза/сут.; п/к — 1-2 мг 1-2 раза/сут. Внутрь детям до 10 лет — по 1 мг/сут. на 1 год жизни; для детей старше 10 лет максимальная доза составляет 10 мг. П/к доза рассчитывается по 50 мкг на 1 год жизни, но не более 375 мкг на одну инъекцию. Максимальные дозы: для взрослых при приеме внутрь разовая доза составляет 15 мг, суточная — 50 мг; при п/к введении разовая доза — 2 мг, суточная — 6 мг.
- Пикамилон (ноотропный препарат, снижает гипоксию детрузора). Режим дозирования: принимать внутрь из расчета 5 мг/кг 2-3 раза в сутки на протяжении 1 месяца.
Рекомендации при нейрогенной дисфункции мочевого пузыря
Рекомендуются консультации педиатра, невролога, уролога.
Заболеваемость (на 100 000 человек)
| Мужчины | Женщины | |||||||||||||
| Возраст, лет | 0-1 | 1-3 | 3-14 | 14-25 | 25-40 | 40-60 | 60 + | 0-1 | 1-3 | 3-14 | 14-25 | 25-40 | 40-60 | 60 + |
| Кол-во заболевших | 0.1 | 0.5 | 1.5 | 6 | 6 | 6 | 7 | 0.1 | 0.5 | 1.5 | 6 | 6 | 6 | 7 |
Что нужно пройти при подозрении на заболевание
- 1. Компьютерная томография (КТ) или Магнитно-резонансная томография (МРТ)
Симптомы
online-diagnos.ru
Нейрогенный мочевой пузырь у женщин, мужчин: лечение, симптомы
При поражении участков нервной системы, которые отвечают за мочеиспускательный процесс, диагностируют нейрогенный мочевой пузырь. Нейромышечный недуг диагностируют у пациентов разных возрастных категорий, ведь поражение нервной системы проявляется как врожденный дефект или бывает приобретенным со временем под влиянием различных факторов. Для диагностики нейромышечного недуга применяют такие методы, как УЗИ, урография, анализы, рентгенография и т. д. В качестве лечения недуга применяют медикаментозную терапию, народные методы, а в более осложненных случаях проводят операцию. Для успешного лечебного воздействия необходимо своевременное обращение пациента к врачу, когда у человека начинают проявляться первые признаки. Как проявляется недуг и какие факторы влияют на его развитие?
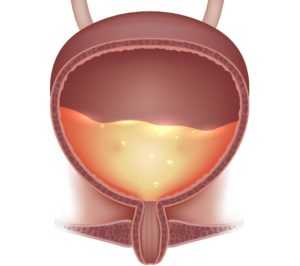
Общие сведения о заболевании у женщин и мужчин
Нейрогенные расстройства мочеиспускания довольно распространены в урологической практике. При патологии больному не удается произвести мочеиспускательный акт, который развивается на рефлекторном уровне. Этому препятствует поражение участков нервной системы, отвечающих за регулирование процессов выделения урины. Подобные расстройства влияют на социальные моменты в жизни пациента, потому что существенно ограничивается как физическая, так и психическая активность больного, и ему труднее адаптироваться в обществе.
По статистике, болезнь развивается у мужчин и женщин с одинаковой частотой, и может привести к нарушению половых функций, сбоям в работе пищеварительной системе. Одновременно с недугом у больного возможно проявление миофасциального синдрома, а также венозного застоя в тазовой области. Также у пациента нередко на фоне болезни развиваются вторичные воспалительные процессы в системе мочевыделения. К таким осложнениям относят хронический цистит, пиелонефрит, почечную недостаточность в хронической форме, вследствие чего пациент останется инвалидом на всю оставшуюся жизнь.
Вернуться к оглавлениюКлассификация нейрогенной дисфункции мочевого пузыря
 Недержание мочи, особенно ночью, может быть симптомом начальной стадии болезни.
Недержание мочи, особенно ночью, может быть симптомом начальной стадии болезни.Нейрогенная дисфункция мочевого пузыря имеет несколько классификаций. В зависимости от степени тяжести недуга выделяют 3 стадии: легкую, среднюю и тяжелую. На легкой стадии человеку трудно сдерживать мочу при напряжении, у него появляется ночной энурез. На средней стадии появляются застои мочи, а мочеиспускательный акт происходит крайне редко. Во время тяжелой стадии человеку не удается сдерживать мочу, появляются запоры, а также в мочевых путях распространяется инфекция. На практике больше ориентируются на классификацию, распределяющую недуг в зависимости от характера течения на 3 вида: гипорефлекторный, арефлекторный и гиперрефлекторный мочевой пузырь.
Вернуться к оглавлениюГипоактивный мочевой пузырь
Гипорефлекторный мочевой пузырь проявляется из-за плохого функционирования нервной системы, проявляясь в крестцовой зоне. Данному типу свойственно то, что мышцы перестают сокращаться должным образом, поэтому мочеиспускания на рефлекторном уровне не происходит. Вследствие скопления большого количества жидкости мочевой пузырь начинает увеличиваться в размере, что сопровождается болевыми ощущениями. Из-за этого происходят сбои в функционировании сфинктера и человеку не удается сдерживать урину. Гипоактивный мочевой пузырь проявляется без болей, но впоследствии у взрослых и детей расслабляются сфинктеры.
Вернуться к оглавлениюСпастический или гиперактивный мочевой пузырь
Гиперактивный тип нейрогенного мочевого пузыря могут спровоцировать заболевания головного мозга.Недуг имеет второе название — спастический мочевой пузырь. Гиперрефлекторный мочевой пузырь проявляется при сбоях нервной системы в надмостовой области головного мозга, при этом повышается активность мышц мочевого пузыря. Вследствие этого органу не удается удержать имеющуюся урину и при попадании жидкости в пузырь происходит ее выпускание. Нейрогенный гиперактивный мочевой пузырь может сопровождаться развитием цистита, вследствие чего сморщивается мочевой пузырь и проявляется его склероз. Для лечения данной формы используют только хирургический способ, так как требуется расширение размера органа.
Вернуться к оглавлениюАрефлекторный мочевой пузырь
При наличии арефлекторного мочевого пузыря человеку не удается осознанно произвести мочеиспускательный акт при первых позывах. При этом в мочевом пузыре скапливается большое количество жидкости, заполняющей максимальный объем органа. После этого наблюдается недержание мочи и урина выделяется в любое время. Такой тип недуга может привести к появлению хронических задержек урины, а при отсутствии лечения возникнут осложнения, среди которых мочекаменный недуг, цистит и т. д.
Вернуться к оглавлениюПричины развития заболевания
Существует 2 группы факторов, провоцирующих развитие недуга: функциональные, органические. Функциональный фактор включает в себя стрессовые ситуации или сильное эмоциональное потрясение, при этом последствия проявляются из-за длительных эмоциональных всплесков. В группу органических факторов входит травмирование головного или спинного мозга, что вызывает дистрофию суставов.
 Очень часто, поражения спинного мозга вызывают нарушения мочеиспускания.
Очень часто, поражения спинного мозга вызывают нарушения мочеиспускания.Кроме этого, заболевание возникает на фоне патологий сфинктера, развивающихся вследствие воспалительных процессов и травм мочевого пузыря. Нейромышечная болезнь может быть связана с врожденными патологиями спинного мозга, в том числе и с травмами, полученными в процессе рождения. У маленьких пациентов нервно-мышечная дисфункция мочевого пузыря развивается из-за нарушенных физических и психических показателей, спинномозговой грыжи, опухолей и врожденных дефектов. Нейрогенные нарушения мочеиспускания у зрелых пациентов развиваются из-за таких причин, как:
- наличие патологий головного мозга, среди которых выделяют рассеянный склероз, нарушенное мозговое кровообращение и синдром Паркинсона;
- развитие недугов спинного мозга, к которым относят грыжу Шморля, остеохондроз, осложнения после операций на органах мочевыделительной системы, дистрофия, поражающая мелкие позвоночные суставы;
- патологии, поражающие рецепторы мочевого пузыря;
- проявление ВИЧ-инфицирования.
Какие проявляются симптомы у мужчин и женщин?
Гиперактивный нейрогенный мочевой пузырь полностью исключает возможность накопления мочи.В зависимости от формы, в которой проявляется заболевание, развиваются разные признаки. Гипотонические сбои функции мочевого пузыря проявляются тем, что у человека переполненный жидкость орган, но у него не получается произвести мочеиспускательный акт. Чтобы урина вышла из пузыря, пациенту приходится тужиться, а в некоторых случаях жидкость выходит самопроизвольно.
Гипертоническая форма мочевого пузыря отличается частыми мочеиспускательными актами, во время которых выделяется небольшой объем жидкости. При этом позывы могут быть достаточно сильными, из-за чего у пациента происходит недержание урины. В ночное время наблюдается энурез, в процессе которого выходит суточный объем жидкости. У пациентов наблюдается тонкая и прерывистая струя, а после акта мочеиспускания остается ощущение, что не вся жидкость вышла. При выделении урины больного тревожат болевые ощущения, а перед этим повышается уровень потоотделения и поднимаются показатели давления.
Какой бы вид недуга ни был диагностирован, у больного появляется психическое расстройство. Наблюдается невозможность к адаптации в окружающей среде, появляющееся из-за плохих запахов. Это ведет к тому, что развивается эмоциональное сотрясение, которое ухудшает ход болезни. В медицинской практике были случаи, когда пациенты пытались покончить жизнь самоубийством. В избегание такого при первых симптомах нужно обратиться за медицинской помощью.
Вернуться к оглавлениюВозможные осложнения и последствия
Нейрогенный мочевой пузырь у женщин и мужчин нередко сопровождается осложнениями, которые опасны для жизни человека. Прежде всего, это психические расстройства, которые могут привести к суицидальному исходу больного. В качестве осложнения выступает недержание урины, не относящееся к признакам заболевания, и проявляющееся при гипертоническом виде.
Гипотония мочевого пузыря у женщин и мужчин заканчивается застоем жидкости, вследствие чего наблюдается рефлюкс урины в мочеточниковые каналы. Из-за этого нарушается функционирование почек, а затем кровь заражается токсинами мочи. Переполненный мочевой пузырь может привести к разрыву стенок органа и в результате диагностируют перитонит. При таком осложнении заражается кровь, что приводит к летальному исходу.
Вернуться к оглавлениюДиагностические мероприятия
 Неврологические обследования проводят только после того, как была исключена возможность инфекционного заболевания.
Неврологические обследования проводят только после того, как была исключена возможность инфекционного заболевания.Для постановки точного диагноза, прежде всего, составляют анамнез пациента, во время которого определяются жалобы человека, наличие у него сопутствующих заболеваний. Далее исследуется наследственный фактор с целью определения подобных недугов у родственников. После этого пациенту назначают анализы крови и мочи, чтобы определить химические и физические свойства, исследовать обменные процессы, наличие инфекции и т. д. С помощью УЗИ пузыря и почек оценивается состояние органа, его внешние показатели, а также исследуется то, сколько жидкости остается после мочеиспускательного акта.
Диагностика, включающая проведение МРТ, дает возможность оценить реальное состояние головного и спинного мозга, выявить наличие дистрофии суставов. При проведении цистоуретроскопии исследуется мочевой пузырь, его стенки. С помощью рентгенологического обследования выявляют аномалии в структуре пузыря. Нейрогенный мочевой пузырь диагностируют при проведении комплексного уродинамического обследования, при котором определяется функционирование мочевыводящих каналов. Для комплексного исследования пациент должен посетить невролога или психотерапевта, ведь симптомы проявляются не только на физическом, но и на психическом уровнях.
Вернуться к оглавлениюЛечение мочевого пузыря: основные методы
Медикаментозная терапия
Медикаментозное лечение нейрогенного мочевого пузыря у мужчин и женщин включает в себя прием альфа-аденоблокаторов, понижающих тонус сфинктера («Фентоламин», «Тропафен»). Для повышения давления внутри пузыря применяют бета-адреноблокаторы, среди которых «Индерал». С помощью альфа-адреностимуляторов происходит стимуляция тонуса сфинктера и исчезает недержание мочи (например, «Эфедрин»). Медикаментозная терапия дает результат лишь при легких стадиях недуга, а эффект от нее кратковременный.
Вернуться к оглавлениюФизиотерапевтические методы
Подобрать наиболее подходящий физиотерапевтический метод может только врач. При гиперрефлекторном виде прибегают к использованию способов физиотерапии, которые обладают симпатомиметическим и спазмолитическим воздействием. Пациентам с гипорефлекторной формой назначают миостимулирующие способы. Чтобы понизить напряжение при мочевыделении, проводят ультразвуковую терапию, лекарственные электрофорезы спазмолитиков и холинолитиков. Для стимулирования мышечного функционирования назначают электрофорез с прозерином и диадинамотерапию.
Вернуться к оглавлениюПроведение лечебной физкультуры
Вылечить нейромышечную дисфункцию мочевого пузыря можно с помощью упражнений, с помощью которых укрепляются мышцы таза и нормализуется тонус мочевого пузыря. Упражнения проводятся в кабинете ЛФК, где пациент под присмотром специалистов правильно выполняет элементы лечебной гимнастики. Но лечебной физкультурой можно заниматься как в домашних условиях, так и на работе. Эффективными считаются упражнения Кегеля, которые назначают пациенткам. Они укрепляют мускулатуру как мочевыделительной системы, так и зоны влагалища.
Вернуться к оглавлениюГомеопатия
Для того, чтобы лечить нейрогенный мочевой пузырь, применяется гомеопатия, подкрепляющая действие медикаментов и лечебной физкультуры. Гомеопатические препараты направлены на лечение ранних стадий заболевания, но не отличаются эффективностью при тяжелой стадии и осложнениях. Для лечения пациентам назначают ««Петрозелинум» или «Урилан».
Вернуться к оглавлениюПсихотерапевтический метод
Выйти из депрессии и вернутся к обычной жизни поможет психотерапия.Основной лечебный комплекс всегда сопровождается психотерапией, так как необходимо улучшить психологическое здоровье пациента. При проведении сеансов психотерапии у людей повышается самооценка, которая была понижена из-за депрессивных состояний. Пациенту предлагают вести специальный дневник, в котором регистрируется количество посещений туалета.
Вернуться к оглавлениюХирургическое лечение
Если не удалось вылечить неврологический недуг консервативными методами лечения, пациенту назначают операцию, которая лечит эффективно недуг. Для лечения нейромышечной болезни любой формы проводят пластику тканей, целью которой является увеличение объема мочевого пузыря. Также пациентам устанавливают цитоскопический дренаж, вследствие чего орган опорожняется без препятствий.
Вернуться к оглавлениюПитание и образ жизни пациента
В процессе лечения пациент находится в больнице, чтобы врачи контролировали его состояние и вносили коррективы. Если нервный недуг развивается на фоне травм головного или спинного мозга, человек постоянно находится в лежачем состоянии. Также пациенту назначают специальное диетическое меню, при котором исключается соленая, кислая, копченная и жирная пища. Запрещено употребление газированных напитков, крепкого кофе и чая. Исключение из рациона вредной пищи подкрепляет основные лечебные способы и расслабляет напряженные участи, а, значит, у пациента будет полный контроль над мочеиспусканием.
Вернуться к оглавлениюЛечение народными средствами
Нейрогенный мочевой пузырь не поддается лечению народными средствами. Но для того, чтобы успокоить нервную систему, используют специальные отвары из трав. Эффективным средством является ромашковый отвар, подкрепляющий воздействие основных лечебных методов и успокаивающий нервы пациента. Кроме этого, отвар борется с возможным скоплением инфекции.
Вернуться к оглавлениюПрогноз и профилактика развития недуга
Если пациент обратился за помощью к врачу при первых же признаках и был назначен лечебный комплекс, то прогноз благоприятный и пациенту удастся избавиться от недуга в ближайшие сроки, будет достигнут полный контроль над актом мочеиспускания. В случаях, когда недуг был выявлен в детстве, то в процессе развития ребенка симптомы исчезают. При отсутствии лечения у человека развиваются осложнения, которые могут привести к летальному исходу.
Профилактические мероприятия направляются не на нейрогенный мочевой пузырь, а на причины его возникновения. Во избежание развития недуга пациент не должен допускать переохлаждение организма, также нужно избегать травм позвоночника и области таза. В частности, это касается людей, занимающихся спортом. Также необходимо избегать стрессовых ситуаций, которые влияют на состояние организма.
etopochki.ru
Нейрогенный мочевой пузырь | Описание заболевания
Нейрогенный мочевой пузырь — это патология, при которой из-за травмы центральной нервной системы нарушается функционирование мочевыделительной системы у женщин и мужчин. Проявляется это в виде задержки и недержания мочи.
Что вызывает нейрогенный мочевой пузырь
Сбой функционирования мочевого пузыря вызывается травмами ЦНС на фоне ранее перенесенных хронических и вирусных заболеваний.
Факторы риска
Различают следующие причины нейрогенного мочевого пузыря:
- органические — стрессы и сильные эмоциональные потрясения;
- функциональные — травмы ЦНС и мочевого пузыря вследствие операций, перелома позвоночника, опухолевых процессов, инсульта.
Симптомы и клиническая картина при нейрогенном мочевом пузыре
В зависимости от вида травмы ЦНС различают 2 вида симптомов нейрогенного мочевого пузыря.
- Гипертонический. Характеризуется незначительным количеством выделяемой мочи при частых позывах, болезненным гипертонусом органа.
- Гипотонический. Для него характерно переполнение мочевого пузыря и невозможность мочеиспускания.
Учитывая то, что любой вид данной патологии для пациента становится тяжелым потрясением, признаки нейрогенного мочевого пузыря дополняются психическим расстройством.
Какой врач лечит нейрогенный мочевой пузырь
У взрослых нейрогенный мочевой пузырь лечит врач-уролог. У детей — терапевт и педиатр. Могут понадобиться консультации невролога и психолога.
Диагностика нейрогенного мочевого пузыря
Для правильной диагностики нейрогенного мочевого пузыря важное значение имеет ежедневный учет больным объема выделяемой урины и частоты мочеиспусканий. Первичный диагноз ставится врачом-урологом после осмотра пациента. Для его подтверждения назначаются инструментальные исследования и анализы на нейрогенный мочевой пузырь.
Методы диагностики
Проводятся следующие диагностические мероприятия:
- цистоскопия, МРТ, экскреторная урография, УЗИ мочевыделительной системы, урофлоуметрия, профилометрия;
- неврологические исследования спинного и головного мозга: МРТ, КТ, электроэнцефалография, рентгенография;
- дифференциальная диагностика;
- лабораторные исследования: анализ крови и мочи (общий и биохимический), анализ мочи на инфекции, по Зимницкому, по Нечипоренко.
Схема лечения нейрогенного мочевого пузыря
Как лечить нейрогенный мочевой пузырь, решают совместно уролог и невролог с учетом анамнестических сведений, результатов диагностических исследований и возрастных особенностей больного. Самолечение исключено.
Основные методы лечения и противопоказания
Лечение нейрогенного мочевого пузыря комплексное и проводится медикаментозными, немедикаментозными и хирургическими средствами.
- Медикаментозная терапия предусматривает применение антидепрессантов, адреноблокаторов, антагонистов кальция, внутрипузырные инъекции Капсаицина, Резинфератоксина.
- Немедикаментозная терапия представлена лечебной физкультурой, психотерапией, сбалансированным питанием.
- Хирургическое вмешательство проводится при необходимости установки цистостомического дренажа, увеличения вместительности мочевого пузыря, эвакуации мочи.
Повышению эффективности лечения способствует физиотерапия: сеансы электростимуляции, лазеротерапии, тепловые аппликации.
Возможные осложнения
Несвоевременная диагностика и запоздалое лечение чреваты следующими осложнениями нейрогенного мочевого пузыря: психическими расстройствами, застоем мочи, нарушением работы почек, уремией с последующим заражением крови токсинами. Невозможность сходить в туалет при переполненном мочевом пузыре приводит к разрыву мочевого пузыря и заражению крови.
Меры профилактики нейрогенного мочевого пузыря
Профилактика нейрогенного мочевого пузыря подразумевает полноценное питание с исключением острых и жирных блюд, отказ от курения и употребления алкоголя, предупреждение переохлаждения, своевременное выполнение всех предписаний врача.
meds.ru
Медикаментозное лечение гиперактивного мочевого пузыря | Мазо Е.Б., Кривобородов Г.Г.
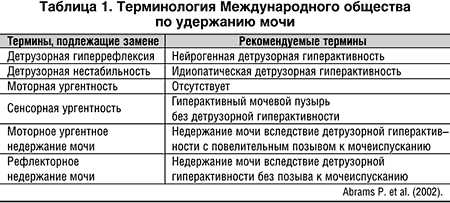
Термины и распространенность Гиперактивный мочевой пузырь (ГМП) – клинический синдром, с симптомами учащенного и ургентного мочеиспускания с (или без) ургентным недержанием мочи и ноктурией (мочеиспускание в период от засыпания до пробуждения). В основе ГМП лежит гиперактивность детрузора нейрогенного или идиопатического характера. Нейрогенная детрузорная гиперактивность является следствием неврологических заболеваний. Идиопатическая детрузорная гиперактивность обозначает, что причина непроизвольных сокращений детрузора не известна. Когда учащенное, ургентное мочеиспускание не сопровождается детрузорной гиперактивностью при отсутствии других причин этих симптомов используют термин ГМП без детрузорной гиперактивности [5]. Таким образом, термин ГМП является общим для обозначения всех приведенных нарушений акта мочеиспускания. При этом термин ГМП не претендует на замену хорошо известной терминологии Международного общества по удержанию мочи, которую использует узкий круг урологов. На рисунке 1 и в таблице 1 представлены уродинамические и клинические термины при учащенном и ургентном мочеиспускании.
Гиперактивный мочевой пузырь (ГМП) – клинический синдром, с симптомами учащенного и ургентного мочеиспускания с (или без) ургентным недержанием мочи и ноктурией (мочеиспускание в период от засыпания до пробуждения). В основе ГМП лежит гиперактивность детрузора нейрогенного или идиопатического характера. является следствием неврологических заболеваний. обозначает, что причина непроизвольных сокращений детрузора не известна. Когда учащенное, ургентное мочеиспускание не сопровождается детрузорной гиперактивностью при отсутствии других причин этих симптомов используют термин [5]. Таким образом, термин ГМП является общим для обозначения всех приведенных нарушений акта мочеиспускания. При этом термин ГМП не претендует на замену хорошо известной терминологии Международного общества по удержанию мочи, которую использует узкий круг урологов. На рисунке 1 и в таблице 1 представлены уродинамические и клинические термины при учащенном и ургентном мочеиспускании.

Рис. 1. Клинические и уродинамические термины для обозначения учащенного и ургентного мочеиспускания
Несмотря на тот факт, что ГМП чаще отмечают в пожилом возрасте, достаточно часто симптомы ГМП встречаются и в других возрастных группах. По нашим данным, наибольшее количество больных отмечено в возрасте старше 40 лет, при этом у мужчин старше 60 лет четко прослеживается тенденция к увеличению заболеваемости, в то время как у женщин, напротив, к снижению [2]. Приведенные данные наглядно демонстрируют, что ГМП – весьма распространенный клинический синдром, встречающийся в различных возрастных группах и приводящий к физической и социальной дезадаптации таких больных.
Клинически у больных ГМП чаще имеет место идиопатическая детрузорная гиперактивность, реже нейрогенная и еще реже ГМП без детрузорной гиперактивности (по нашим данным, у 64%, 23,5% и 12,5% соответственно). Если идиопатическая детрузорная гиперактивность наблюдается в 2 раза чаще, а ГМП без детрузорной гиперактивности в 6 раз чаще у женщин, то нейрогенная детрузорная гиперактивность имеет место практически одинаково часто как у женщин, так и у мужчин [2].
Этиология и патогенез
Достоверно установлено, что ГМП может являться следствием нейрогенных и ненейрогенных поражений. Первые – это нарушения на уровне супраспинальных центров нервной системы и проводящих путей спинного мозга, вторые – следствие возрастных изменений детрузора, инфравезикальной обструкции и анатомических изменений положения уретры и мочевого пузыря.
Известны некоторые морфологические изменения детрузора при его гиперактивности. Так, у большинства больных ГМП выявляют снижение плотности холинергических нервных волокон, которые, в свою очередь, имеют повышенную чувствительность к ацетилхолину. Эти изменения определяют, как «постсинаптическая холинергическая денервация детрузора» [12]. Кроме того, с помощью электронной микроскопии удалось установить нарушения нормальных межклеточных соединений в детрузоре ГМП в виде протрузии межклеточных соединений и выпячивания клеточной мембраны одного миоцита в другой соседний миоцит с сближением межклеточных границ – «плотное соединение двух параллельных плоскостей смежных миоцитов» [11,18]. На основании этих, как считают, характерных для ГМП морфологических изменений Brading и Turner в 1994 предложили теорию патогенеза развития детрузорной гиперактивности, в основе которой лежит повышенная возбудимость миоцитов, находящихся в тесной связи друг с другом в местах денервации [9,10].
Полагают, что причиной денервации, помимо нервных нарушений, может являться гипоксия детрузора по причине возрастных ишемических изменений или вследствие инфравезикальной обструкции. В последнем случае это подтверждается наличием ГМП у 40–60% мужчин с доброкачественной гиперплазией простаты [8]. Таким образом, патогенез детрузорной гиперактивности при ГМП представляют следующим образом: гипоксия, возникающая в детрузоре вследствие возрастного артериолосклероза или в результате ИВО, приводящей к гипертрофии и инфильтрации соединительной ткани детрузора, приводят к денервации детрузора (выявляют в биоптатах детрузора при всех видах детрузорной гиперактивности), вследствие чего в миоцитах происходят структурные изменения (тесным контактом между миоцитами c повышенной нервной возбудимостью и проводимостью), как компенсаторная реакция на дефицит нервной регуляции. В этом случае любое спонтанное или спровоцированное растяжением стенки мочевого пузыря (период накопления мочи) сокращение отдельных миоцитов в виде «цепной реакции» приводит к непроизвольным сокращениям всего детрузора. Предложенная теория развития детрузорной гиперактивности при ГМП является в настоящее время ведущей.
Клиническое течение и тактика обследования
Учащенное дневное и ночное мочеиспускание, как преобладающие симптомы ГМП, мы наблюдали примерно в 2 раза чаще без ургентного мочеиспускания и в 3 раза чаще без ургентного недержания мочи, которое, несомненно, наиболее тяжелое проявление ГМП, поскольку вызывает несравнимо значительные страдания больных. Особенностью течения ГМП является динамика его симптомов. В период 3–х лет наблюдения почти у трети больных ургентное недержание мочи спонтанно регрессирует без лечения и вновь рецидивирует в разные сроки. Наиболее стойким симптомом является учащенное мочеиспускание, которое нередко достигает такого числа, что делает больных абсолютно нетрудоспособными и толкает их на необдуманные решения.
Всем больным с учащенным и ургентным мочеиспусканием помимо сбора анамнеза и физикального обследования проводят оценку частоты мочеиспусканий (на основании 72 ч дневника мочеиспусканий), исследование осадка мочи и посев мочи на стерильность, ультразвуковое сканирование почек, мочевого пузыря, простаты, с определением остаточной мочи. Результаты дневника мочеиспусканий имеют наиболее важное значение: оценив их, можно во многом предположить ГМП и на основании этого быстро решить вопрос о начале лечения и его методах. ГМП имеет право на диагноз при условии наличия не менее 8 мочеиспусканий и/или не менее 2 эпизодов ургентного недержания мочи в течение суток. Важно, что результаты такого первичного обследования, которое проводят на поликлиническом этапе, нередко позволяют выявить заболевания, которые сопровождаются симптомами учащенного и ургентного мочеиспускания, но не имеют отношения к ГМП.
При выявлении ГМП можно сразу начинать лечение для улучшения качества жизни больного путем купирования учащенного и ургентного мочеиспускания. В случае неэффективности лечения или по желанию больного для уточнения формы ГМП (идиопатическая или нейрогенная детрузорная гиперактивность, ГМП без детрузорной гиперактивности) проводят цистометрию и специальные тесты с холодной водой и лидокаином, которые позволяют заподозрить неврологические нарушения, лежащие в основе развития детрузорной гиперактивности. Во всех случаях при выявлении детрузорной гиперактивности показано детальное неврологическое обследование.
Лечение
Лечение больных ГМП направлено прежде всего на восстановление утраченного контроля за накопительной способностью мочевого пузыря. При всех формах ГМП основным методом лечения является медикаментозный. Антихолинергические средства (М–холиноблокаторы) являются стандартными препаратами такого лечения. Эти препараты используют как в качестве монотерапии, так и в комплексе с другими лекарственными препаратами (табл. 2). Ниже мы сообщим, какие антихолинергические препараты целесообразно применять в современном лечении симптомов ГМП. Как правило, прием медикаментов сочетают с поведенческой терапией, биологической обратной связью или нейромодуляцией. Механизм действия антихолинергических препаратов заключается в блокаде постсинаптических (М2, М3) мускариновых холинорецепторов детрузора. Это уменьшает или предупреждает действие ацетилхолина на детрузор, снижая его гиперактивность. У человека известны пять видов мускариновых рецепторов, из них в детрузоре содержатся два – М2 и М3. Последние составляют только 20% всех мускариновых рецепторов мочевого пузыря, но именно они отвечают за сократительную активность детрузора. Местонахождение М2 – сердце, задний мозг, гладкие мышцы, калиевые каналы; М3 – гладкие мышцы, железы в том числе слюнные, мозг. Клеточный ответ стимуляции М2 – отрицательный, изотропный, снижение пресинаптического выделения трансмиттеров; М3 – сокращение гладких мышц, секреция желез, снижение пресинаптического выделения трансмиттеров. Доказано, что активация М2 рецепторов приводит к ингибированию симпатической активности детрузора, что увеличивает его сократительную активность. Таким образом, блокада М2 холинорецепторов имеет существенное значение наряду с блокадой М3 в подавлении детрузорной гиперактивности. Полагают, что М2 холинорецепторы в большей степени ответственны за развитие детрузорной гиперактивности при неврологических заболеваниях и у больных пожилого возраста. М–рецепторы – основная мишень медикаментозного лечения ГМП. Препаратами выбора остаются М3 антихолинергические медикаменты, среди которых особую роль играют высокоселективные. По химической структуре антихолинергические препараты делятся на вторичные, третичные (оксибутинин гидрохлорид, толтеродина тартрат) и четвертичные (троспиум хлорид) амины. С практической точки зрения это деление позволяет предполагать развитие побочных эффектов в зависимости от химической структуры препарата. В частности, считают, что четвертичные амины по сравнению с вторичными и третичными в меньшей степени проникают через гематоэнцефалический барьер и, следовательно, имеют меньшую вероятность развития побочных эффектов со стороны центральной нервной системы. Эта точка зрения пока не в полной мере находит свое подтверждение в клинической практике, поскольку развитие побочных эффектов определяется и другими особенностями антихолинергических препаратов (органоспецифичность, фармакокинетика препарата, метаболиты препарата, тип блокируемых рецепторов).
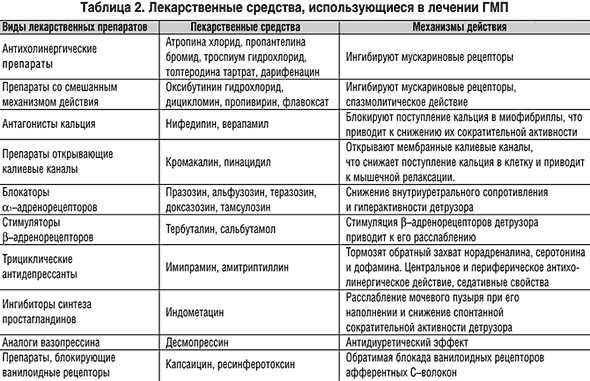
Значительным шагом вперед является синтез нового антихолинергического препарата – толтеродина, предложенного специально для лечения ГМП. Толтеродин – смешанный антагонист М2 и М3 холинорецепторов, обладающий отчетливой органной специфичностью действия в отношении детрузора. В отличие от оксибутинина, который имеет выраженную селективность по отношению к М1 и М3 рецепторам, толтеродин демонстрирует практически одинаковую чувствительность к разным подтипам М–рецепторов. Наш опыт применения немедленно освобождающейся формы толтеродина в дозе 2 мг 2 раза в день у 43 больных с идиопатической детрузорной гиперактивностью свидетельствует о его высокой эффективности. Через 12 недель применения число мочеиспусканий в сутки в среднем снизилось с 13,5±2,2 (9–24) до 7,9±1,6 (6–17), а эпизодов ургентного недержания мочи с 3,6±1,7 (1–6) до 2,0±1,8 (0–3). Немедленно освобождающаяся форма толтеродина относительно хорошо переносится, о чем говорят данные клинических испытаний, в рамках которых 6– и 12–месячные курсы лечения закончили 82% и 70% больных соответственно, что свидетельствует о том, что эффективность терапии сохраняется в течение длительного времени. Частота побочных эффектов при применении немедленно освобождающейся формы толтеродина практически не отличается от группы плацебо, за исключением сухости во рту, которая отмечается у 39% больных, принимавших толтеродин, и у 16% группы плацебо [6]. Наши данные также свидетельствуют о хорошей эффективности и переносимости немедленно освобождающейся формы толтеродина (4 мг) на протяжении 6 мес. лечения у 16 больных с нейрогенной детрузорной гиперактивностью. Отмечено снижение среднего числа суточных мочеиспусканий на 5,7/сут эпизодов ургентного недержания мочи на 2,7/сут и увеличение среднеэффективного объема мочевого пузыря на 104,5.
Клинические исследования показывают, что антихолинергические препараты приводят к снижению частоты симптомов ГМП в течение 1–2 недель лечения, а максимальный эффект достигается к 5–8 неделям. В то же время лечение предполагает длительные курсы. Несмотря на это в большинстве случаев монотерапии антихолинергическими средствами после их отмены наблюдается рецидив симптомов ГМП, что делает необходимым постоянный их прием с целью поддержания адекватного терапевтического эффекта.
Применение антихолинергических препаратов, в частности, толтеродина требует тщательного наблюдения и осторожности, особенно у больных с нейрогенной детрузорной гиперактивностью. Дело в том, что при длительном бесконтрольном применении этих лекарственных препаратов у больных может возникнуть нарушение сократительной активности детрузора, с развитием хронической задержки мочи, уретрогидронефроза и хронической почечной недостаточности. Для своевременного контроля за возможными побочными эффектами необходимо оценивать количество остаточной мочи. Мы рекомендуем в первые три месяца после назначения антихолинергических препаратов определять количество остаточной мочи не реже чем 1 раз в две недели, а в последующем с периодичностью 1 раз в месяц. Больные должны быть предупреждены о возможности такого осложнения и немедленно сообщить врачу в случае ощущения неполного опорожнения мочевого пузыря.
Известно, что наряду с препаратами за развитие побочных эффектов отвечают их метаболиты, концентрация которых в крови и их сродство к М – холинорецепторам превышает нередко таковые исходных препаратов. Например, метаболизм оксибутинина приводит к формированию N–дезитил оксибутинина, а толтеродина – к активному метаболиту – 5–гидроксиметильное производное. Эти данные явились основанием для использования других, отличных от пероральных форм, антихолинергических препаратов. В частности, используют внутрипузырное введение оксибутинина или ректальные свечи. Проникновение препарата непосредственно в кровь, минуя печень, при таких формах введения не сопровождается образованием метаболитов, что снижает количество побочных эффектов. С 1999 г. стали применять медленноосвобождающуюся форму оксибутинина на основе осмотической системы доставки OROS, которая обеспечивает пролонгированное высвобождение препарата и постоянную его концентрацию в плазме крови на протяжении 24 ч. Клинические исследования показывают, что медленно освобождающаяся форма оксибутинина имеет эффективность в отношении снижения симптомов ургентного мочеиспускания, сравнимую с немедленно освобождающейся формой с меньшим числом побочных эффектов (25% по сравнению с 46%). Считают, что поэтому 60% больных ГМП продолжают прием медленно освобождающейся формы оксибутинина на протяжении 12 мес. в дозе 15 мг в сутки [7].
В настоящее время проводят изучение эффективности и переносимости S–формы оксибутинина, а также исследуются трансдермальная (OXYtrol patch) и внутрипузырная (UROS) формы применения оксибутинина.
Медленно освобождающаяся форма толтеродина представляет собой множество маленьких бусинок, состоящих из полистерина. Активное вещество находится на поверхности бусинок и покрыто специальной капсулой. Освобождение препарата происходит при разрушении капсулы кислым содержимым желудка. Такая система доставки обеспечивает постоянный уровень препарата в крови на протяжении 24 ч. Медленно освобождающаяся форма толтеродина отличается более значимым снижением эпизодов ургентного недержания мочи и лучшей переносимостью по сравнению с немедленно освобождающейся формой. Больные, получавшие медленно освобождающийся толтеродин, имели на 23% меньше случаев сухости во рту [19].
Учитывая незначительное количество побочных эффектов при использовании медленно освобождающихся форм антихолинергических препаратов, в последнее время в литературе обсуждается вопрос увеличения их дозы при лечении больных ГМП. Это связано с тем обстоятельством, что большинство больных имеют положительный эффект при использовании стандартной дозы антихолинергических препаратов и только некоторые из них избавляются полностью от симптомов ГМП. В то же время, несмотря на хорошую переносимость, обычно врачи не увеличивают дозу препаратов для полного исчезновения симптомов ГМП. Клинические исследования и практика показывают, что значительное число пациентов с успешными результатами терапии антихолинергическими препаратами в дальнейшем могут иметь клинические улучшения симптомов при увеличении дозы этих препаратов [16].
Отдельно стоит вопрос о возможности применения антихолинергических препаратов у больных с ГМП и инфравезикальной обструкцией. Несмотря на то, что антихолинергические средства уменьшают учащенное и ургентное мочеиспускание, врачи опасаются использовать их у больных с сопутствующей инфравезикальной обструкцией из–за риска развития острой задержки мочи. Этот вопрос изучался только в двух рандомизированных контролируемых исследованиях. Эти исследования показали, что немедленно освобождающаяся форма толтеродина в качестве монотерапии или в комбинации с тамсулозином (a1–адреноблокатор) безопасна в отношении возможного развития острой задержки мочи и обеспечивает улучшение качества жизни у больных с гиперактивностью детрузора в сочетании с легкой и среднетяжелой степенью инфравезикальной обструкции и умеренным количеством остаточной мочи [4,8].
Мы использовали немедленно освобождающуюся форму толтеродина (2 мг 2 раза в сутки) у 12 больных ГМП в сочетании с доброкачественной гиперплазией простаты [1]. У 2 больных в первые 3 недели лечения отмечено появление остаточной мочи в объеме до 100 мл, что явилось показанием к прекращению лечения. У 10 больных через 12 недель лечения средний балл I–PSS снизился с 17,2 до 11,7 за счет ирритативных симптомов, средний балл качества жизни снизился с 5,2 до 3,1. Число мочеиспусканий по данным дневника мочеиспусканий снизилось с 14,6 до 9,2. Максимальная скорость потока мочи не только не уменьшилась, но даже незначительно увеличилась с 12,3 до 13,4, что, вероятно, связано с увеличением накопительной способности мочевого пузыря. Не вызывает сомнения тот факт, что для уточнения возможности применения антихолинергических препаратов у больных ГМП и инфравезикальной обструкцией необходимы дальнейшие исследования.
Имеются отдельные сообщения разрозненного характера о применении других лекарственных средств у больных ГМП. В частности, сообщают об использовании трициклических антидепрессантов, антагонистов ионов кальция, блокаторов a1–адренорецепторов, ингибиторов синтеза простагландинов, аналогов вазопрессина, стимуляторов b-адренорецепторов и препаратов, открывающих калиевые каналы. Однако вследствие малого числа наблюдений точная оценка результатов их применения в лечении ГМП в настоящее время не представляется возможной. Обычно эти препараты используют в сочетании с антихолинергическими препаратами.
В последнее время сообщают об успешном применении в лечении больных ГМП капсаицина и ресиниферотоксина [17]. Эти вещества в виде раствора вводят в мочевой пузырь. Капсаицин и ресиниферотоксин являются препаратами со специфическим механизмом действия, который заключается в обратимом блокировании ванилоидных рецепторов афферентных С–волокон мочевого пузыря. Эти препараты сегодня используют главным образом у больных с нейрогенной детрузорной гиперактивностью при отсутствии эффекта от традиционных лекарственных средств.
Мы апробировали новый метод медикаментозного лечения ГМП, который во всем мире считается весьма перспективным. Метод заключается в последовательном введении в различные отделы детрузора суммарно 200–300 единиц ботулинического токсина типа А. Механизм действия токсина заключается в блокировании выброса ацетилхолина из пресинаптической мембраны в нервно–мышечном синапсе, что приводит к снижению сократительной активности детрузора. В большинстве случаев прежняя мышечная активность восстанавливается через 3–6 мес. после введения токсина, но нередко это может произойти через год и более. Наши результаты применения ботулинического токсина типа А у 3 больных с нейрогенной детрузорной гиперактивностью свидетельствуют об увеличении емкости мочевого пузыря, что клинически проявляется снижением числа мочеиспусканий и эпизодов ургентного недержания мочи. Однако пока нет достаточных данных, чтобы с большой определенностью характеризовать эффективность этого метода лечения.
Таким образом, данные литературы и наш собственный опыт свидетельствуют, что среди медикаментозных методов лечения антихолинергические препараты занимают ведущее место в терапии ГМП и позволяют получить хороший результат у значительного числа больных. Совершенствование способов и форм введения антихолинергических препаратов при сохранении терапевтической эффективности позволяет снизить количество побочных эффектов. Можно надеяться, что по мере расширения знаний в отношении патофизиологических процессов, лежащих в основе развития детрузорной гиперактивности, появятся принципиально новые мишени фармакологического лечения.
Литература:
www.rmj.ru
Нейрогенный мочевой пузырь — Лечение
Нарушение накопления мочи в мочевом пузыре
Нарушение накопления мочи в мочевом пузыре вследствие неврологических заболеваний и повреждений выражается в нейрогенной детрузорной гиперактивности (одна из форм гиперактивного мочевого пузыря). Подходы к лечению гиперактивного мочевого пузыря подробно изложены в соответствующей главе данного руководства.
[9], [10], [11], [12], [13], [14], [15], [16], [17], [18], [19]
Нарушение опорожнения мочевого пузыря
Детрузорно-сфинктерная диссинергия, нарушение сократительной активности детрузора и нарушение адекватного расслабления сфинктеров приводят к нарушению опорожнения мочевого пузыря.
Интермиттирующая аутокатетеризация мочевого пузыря, предложенная Лапидесом в 1972 году, до настоящего времени является лучшим методом лечения больных с нарушением опорожнения мочевого пузыря вследствие неврологических заболеваний. Однако у пациентов с нарушением функции рук (не могут осуществлять периодическую самокатетеризацию), а также у больных, которые по тем или иным причинам отказываются от данного вида опорожнения мочевого пузыря, применяют другие методы.
Гладкие мышцы шейки мочевого пузыря и проксимального отдела мочеиспускательного канала контролируются тоническими симпатическими стимулами посредством альфа-адренорецепторов. Блокада альфа-адренорецепторов может улучшить опорожнение мочевого пузыря. Несмотря на то что альфа-адреноблокаторы (тамсулозин, альфузазин, доксазозин и другие) с успехом применяют при лечении больных с аденомой простаты, они не нашли широкого применения при функциональных нарушениях опорожнения мочевого пузыря. Тем не менее, большинство авторов считают целесообразным использовать альфа-адреноблокаторы при лёгких формах нарушения функции опорожнения мочевого пузыря.
При детрузорно-сфинктерной диссинергии, сопровождающейся высоким детрузорном давлением (более 40 см вод.ст.), во время мочеиспускания очень важно выбрать адекватный метод опорожнения мочевого пузыря.
Медикаментозное лечение нейрогенного мочевого пузыря включает бензодиазепины и миорелаксанты центрального действия. Наиболее часто применяют миорелаксанты центрального действия. Они снижают возбуждение моторных нейронов и интернейронов и способны ингибировать передачу нервного импульса в спинном мозге, уменьшая спастичность поперечно-полосатых мышц. Однако при использовании этих препаратов даже в максимально допустимых дозах положительный эффект отмечают только у 20% больных.
Медикаментозное лечение нейрогенного мочевого пузыря (метоклопрамид) также не имеет существенного значения при лечении пациентов со снижением или отсутствием сократительной активности детрузора. Часть больных со снижением или отсутствием сократительной активности детрузора и с паралитическим состоянием поперечно-полосатого сфинктера мочеиспускательного канала может опорожнять мочевой пузырь, искусственно увеличивая внутриабдоминальное давление пальцевой компрессией нижних отделов живота (приём Креда). При спастическом состоянии наружного сфинктера мочеиспускательного канала приёма Креда не приводит к адекватному опорожнению мочевого пузыря.
При невозможности проведения или отказе больного от аутокатетеризации, а также при неэффективности медикаментозного лечения, больным как с детрузорно-сфинктерной диссинергией, так и с нарушением сократительной активности детрузора в сочетании со спастическим состоянием наружного сфинктера мочеиспускательного канала, для устранения обструкции в зоне указанного сфинктера назначают оперативные методы лечения. В частности, применяют инъекцию ботулинического нейротоксина типа А в область поперечно-полосатого сфинктера мочеиспускательного канала. ТУР шейки мочевого пузыря, инцизию поперечно-полосатого сфинктера мочеиспускательного канала и имплантацию специальных стентов в зону наружного сфинктера мочеиспускательного канала.
100 ЕД ботулинического нейротоксина типа А разводят в 8 мл стерильного 0,9% раствора натрия хлорида. Препарат вводят в наружный сфинктер мочеиспускательного канала. У мужчин препарат вводят трансуретрально в четырёх точках на 3,6,9 и 12 ч по условному циферблату, а у женщин — парауретрально в двух точках слева и справа от мочеиспускательного канала. Хемоденервация наружного сфинктера мочеиспускательного канала снижает внутриуретральное сопротивление, тем самым, улучшая опорожнение мочевого пузыря, а в ряде случаев восстанавливая самостоятельное мочеиспускание.
ТУР шейки мочевого пузыря применяют при обструкции шейки мочевого пузыря и проксимального отдела мочеиспускательного канала, установленной по результатам видеоуродинамического исследования. Шейку мочевого пузыря рассекают через все слои на 5 и/или 7 ч по условному циферблату (у мужчин — от основания мочевого пузыря до семенного бугорка).
Инцизию поперечно-полосатого сфинктера мочеиспускательного канала (сфинктеротомия) выполняют холодным ножом или при помощи лазера на 12 ч по условному циферблату. Положительные результаты отмечают у 70% больных. Возможные осложнения: кровотечения, импотенция, мочевые затёки.
Лечение нейрогенного мочевого пузыря требует также применения постоянных металлических стентов. Стенты устанавливают трансуретрально таким образом, чтобы шинировать только поперечно-полосатый сфинктер мочеиспускательного канала. В таком положении гладкомышечные волокна шейки мочевого пузыря обеспечивают удержание мочи. Из осложнений наиболее часто происходят спонтанные миграции стента и инкрустации стента солями.
Электростимуляцию передних сакральных корешков также используют в лечении неврологических больных с нарушением функции опорожнения мочевого пузыря. Методика впервые была предложена Бриндли. Применяют у больных с полным повреждением спинного мозга. Электростимуляция передних корешков сакрального отдела спинного мозга одновременно стимулирует автономные волокна детрузора и соматические волокна наружного сфинктера мочеиспускательного канала и тазовой диафрагмы. Вследствие того, что поперечно-полосатые мышечные волокна не способны к длительному тоническому сокращению, происходит снижение внутриуретрального давления, а сокращение гладкомышечных волокон детрузора способствует мочеиспусканию.
В особых случаях тяжёлого течения нейрогенной дисфункции нижних мочевыводящих путей и выраженной инвалидизации больного отведение мочи из мочевого пузыря осуществляют путём установки постоянного уретрального катетера или надлобковой цистостомии.
Лечение сфинктерного недержания мочи при нарушении иннервации поперечно-полосатого сфинктера уретры осуществляют оперативным вмешательством. У женщин применяют уретральный слинг и искусственный сфинктер, у мужчин — искусственный сфинктер.
Таким образом, проявления нарушений акта мочеиспускания у пациентов с нейрогенной дисфункцией нижних мочевыводящих путей достаточно разнообразны. Во всех случаях необходимо проведение комплексного УДИ для уточнения функционального состояния мочевого пузыря и его сфинктеров. К сожалению, современное лечение нейрогенного мочевого пузыря у подавляющего большинства пациентов не позволяют полностью восстановить нормальную функцию нижних мочевыводящих путей, и тогда лечение заключается в выборе адекватного и подходящего для конкретного больного метода опорожнения мочевого пузыря.
[20], [21], [22]
ilive.com.ua
Нейрогенный мочевой пузырь у женщин и мужчин: симптомы, лечение, профилактика
Термин нейрогенный мочевой пузырь употребляется для описания группы функциональных нарушений, возникающих вследствие поражения органов центральной и перифиричечкой нервной системы. Заболевание характеризуется частичной или полной утратой контроля за мочеиспусканием, а выраженность симптоматики зависит от локализации и этиологии поражения ЦНС.
Основные причины и классификация заболевания
 Многочисленность факторов, влияющих на дисфункцию мочевого пузыря, затрудняют верификацию диагноза и на сегодняшний день врачебное сообщество не выработало однозначной системы классификации заболевания. Однако достоверно известно, что НМП (нейрогенный мочевой пузырь) не является самостоятельной патологией, а образуется вследствие врожденных или перенесенных заболеваний. В этиологии нейрогенной дисфункции МП (мочевого пузыря) решающее значение имеет распространённость и степень поражения нервной системы, а в основе заболевания лежит рассинхронизация сокращения детрузора с раскрытием мочеиспускательного канала. Условно, причины нейрогенного мочевого пузыря, объединяют в несколько групп:
Многочисленность факторов, влияющих на дисфункцию мочевого пузыря, затрудняют верификацию диагноза и на сегодняшний день врачебное сообщество не выработало однозначной системы классификации заболевания. Однако достоверно известно, что НМП (нейрогенный мочевой пузырь) не является самостоятельной патологией, а образуется вследствие врожденных или перенесенных заболеваний. В этиологии нейрогенной дисфункции МП (мочевого пузыря) решающее значение имеет распространённость и степень поражения нервной системы, а в основе заболевания лежит рассинхронизация сокращения детрузора с раскрытием мочеиспускательного канала. Условно, причины нейрогенного мочевого пузыря, объединяют в несколько групп:
- Врожденное слабоумие, онкологические, инфекционные и воспалительные процессы спинного и головного мозга: энцефалит, невриты различной этиологии, поствакцинальные нарушения, болезнь Паркинсона и Альцгеймера.
- Поражения периферических нервов и мышц накопительного органа вследствие интоксикации и травм, после хирургических вмешательств и инсультов.
- Врожденные дефекты мочеиспускательного тракта и ЦНС.
- Дегенеративные изменения хрящей позвоночного столба – остеохондроз и спинномозговые грыжи;
- Вирус иммунодефицита – ВИЧ.
В некоторых случаях синдром НМП является следствием хронического цистита, мочекаменной болезни и эмоционального потрясения. Нейрогенный мочевой пузырь у женщин встречается в равной степени по отношению к пациентам мужского пола. Возникновение дисфункции в детском возрасте обусловлено родовыми травмами, врожденными патологиями ЦНС и урогенитальной сферы, а также нестабильностью гормонального фона и нарушением обменных процессов в период полового созревания.
Клиническая картина разных форм заболевания
 В зависимости от функциональной активности выделяют гиперактивный и гипоактивный мочевой пузырь. Клиническая картина и характер развития патологических состояний имеет существенные различия. Врачи выделяют 3 степени степени тяжести нарушений нейрогенной функции мочевого пузыря:
В зависимости от функциональной активности выделяют гиперактивный и гипоактивный мочевой пузырь. Клиническая картина и характер развития патологических состояний имеет существенные различия. Врачи выделяют 3 степени степени тяжести нарушений нейрогенной функции мочевого пузыря:
- Легкая – сопровождается дизурией, недержанием при напряжении мышц брюшного пресса, энурезом в ночное время;
- Среднюю отличают редкие позывы к опорожнению, застои мочи;
- Тяжелая степень характеризуется запорами, недержанием, мочекаменной болезнью, хроническими воспалительными процессами урогенитальных органов, невротическими состояниями и общей слабостью.
Симптомы нейрогенного мочевого пузыря зависят от степени тяжести поражения ЦНС и могут носить как эпизодический, так и постоянный характер.
Гипоактивный мочевой пузырь
Типичными проявлениями дисфункции являются снижение сократительной активности накопительного органа. Из-за гипотонии детрузора и сфинктера становится невозможным создание необходимых параметров внутрипузырного давления, что ведет к задержке и вялому процессу выведения жидкости, образованию большого количества остаточной мочи и дискомфортным ощущениям неполного опорожнения. Результатом гипотонии является формирование перерастянутого мочевого пузыря с гипертрофией стенок и уменьшением объема органа. Подобная трансформация приводит к неконтролируемому выведению мочи малыми дозами(каплями), склерозированию и сморщиванию накопительного органа.
Гиперактивный мочевой пузырь
Недержание мочи, непреодолимые (императивные) позывы к опорожнению органа, и ночная дизурия характеризуют гиперактивный мочевой пузырь. Спазмированный детрузор способствует образованию повышенного пузырного давления при небольшом объеме жидкости, что и вызывает императивные позывы. Синдром гиперактивного мочевого пузыря обычно сопровождается гипертензией, потливостью, а при тяжелых неврологических нарушениях может возникать неконтролируемое выделение большого объема урины при малейшем напряжении стенок брюшного пресса.
Важно! Нейрогенный гиперактивный пузырь снижает качество жизни, существенно ограничивает круг общения и физическую активность. На фоне заболевания возникают серьезные осложнения: гипертензия, воспаление почек, циститы и дистрофические изменения органов урогенитальной сферы.
Можно констатировать, что нейрогенная дисфункция мочевого пузыря приводит к атонии стенок органа и развитию выраженных нарушений оттока мочи. Серьезным осложнением может стать обратный заброс урины по восходящему типу, что приводит к образованию конкрементов и воспалению почек. В большинстве случаев дисфункция мочевого пузыря сопровождается расстройствами психики и социальной дезадаптацией.
Диагностика НМП
 Установление причины и формы патологии требует кропотливой работы не только от лечащего врача, но и от пациента. Важным аспектом является ведение дневника, где указывается время, число и количество выведенной жидкости, ощущения после акта мочеиспускания. Диагностика нейрогенного мочевого пузыря состоит из нескольких этапов, включающих в себя следующие виды обследования:
Установление причины и формы патологии требует кропотливой работы не только от лечащего врача, но и от пациента. Важным аспектом является ведение дневника, где указывается время, число и количество выведенной жидкости, ощущения после акта мочеиспускания. Диагностика нейрогенного мочевого пузыря состоит из нескольких этапов, включающих в себя следующие виды обследования:
- анамнестический опрос с анализом объективных жалоб, наследственных факторов, установление хронических и перенесенных заболеваний;
- выявление неврологической патологии и исключение органических поражений;
- анализы мочи по Зимницкому и Нечипоренко;
- посев на бактериальную флору;
- УЗИ органов мочеполового тракта;
- клинический и биохимический анализ крови;
- урофлоуметрия – определяет мышечную активность детрузора и скорость потока выделяемой жидкости;
- цистометрия наполненного мочевого пузыря с оценкой емкости и чувствительности, внутрипузырного и внутрибрюшного давления;
- профилометрия – уродинамическое исследование уретрального давления.
По показаниям могут быть назначены дополнительные, более информативные виды диагностики: надлобковая пункция, цистоскопия, ректроманоскопия, рентгенконтрастные методы, МРТ. В большинстве случаев целесообразны консультации узких специалистов: невролога, психотерапевта, проктолога, гинеколога, нефролога. При невозможности установления точного диагноза говорят о неясной этиологии и идиопатическом характере патологии.
Лечение нейрогенного мочевого пузыря
 Терапия заболевания требует комплексного подхода, особо важное значение имеет диагностика нейрогенного мочевого пузыря, направленная на выявление причины и типа дисфункции органа. Обычно, терапевтическая схема включает в себя:
Терапия заболевания требует комплексного подхода, особо важное значение имеет диагностика нейрогенного мочевого пузыря, направленная на выявление причины и типа дисфункции органа. Обычно, терапевтическая схема включает в себя:
- медикаментозное лечение;
- психотерапию;
- периодическую катетеризацию и применение физиотерапевтических методик;
- обучение пациентов контролю за мочеиспусканием при помощи специальных упражнений;
- сакральную электростимуляцию с имплантацией электродов;
- чрескожные лекарственные блокады;
- малоинвазивные хирургические вмешательства.
Для снижения гипертонуса мочевого пузыря используются антихолинергические средства, блокирующие нервные импульсы: Оксибутинин, Дарифенацин, Толтеродин. Препараты отличаются отсутствием привыкания при длительном применении и обладают выраженным эффектом при минимальных негативных последствиях. Некоторым категориям пациентов назначаются блокаторы кальциевых каналов Нифедипин и Пантогам. В случае скопления мочи проводится катетеризация и внутрипузырные инсталляции растворами анестезирующих и антиоксидантных препаратов. Дополнительно к медикаментозному лечению больным с гиперфункцией мочевого пузыря могут быть назначены физиотерапевтические процедуры. Рекомендуются упражнения, направленные на тренировку мышц брюшного пресса и тазового дна, что в перспективе позволяет компенсировать часть утраченных функций сфинктера мочевыводящих путей. При состояниях, сопровождающихся задержкой мочи и снижением тонуса детрузора, проводится периодическая катетеризация и курсовая электростимуляция накопительного органа. Рефлекторная деятельность восстанавливается курсовым приемом холиномиметиков и препаратов усиливающих работу гладкой мускулатуры: Цитохром, Рибофлавин, Бетанехол, Ацеклидин. Во многих случаях при нарушении функций мочевого пузыря в схему лечения включаются фитопрепраты: Цистон, Цистениум, Канефрон, Монурель. У женщин в период менопаузы целесообразно проведение заместительной гормональной терапии. При выявлении воспалительного процесса назначаются антибактериальные, антисептические и иммуномодулирующие лекарственные средства. Для устранения детрузорно-сфинктерной диссенергии применяются перспективные методики по введению препаратов ботулотоксина в стенку или сфинктер накопительного органа. Благодаря высокой эффективности широкое применение получила нейромодуляция, в зависимости от характера нарушений, направленная на активацию или торможение функций накопительного органа. Мероприятие считается успешным при уменьшении признаков нарушений более, чем на 50%. Разработаны и активно применяются в медицинской практике малоинвазивные хирургические методики, улучшающие функции мочевого пузыря.
Рекомендации и профилактика
Успех лечения связан с коррекцией поведенческих привычек и питания. Во время болезни следует придерживаться бессолевой диеты и исключить из рациона пряностй, копчености, консервации, дрожжевую выпечку и алкоголь. План лечения больных с травматическими повреждениями головного и спинного мозга требует постельного режима, если пациент способен передвигаться или причины патологии носят другую этиологию, то рекомендуется лечение в стационаре. Реабилитация и профилактика заболевания заключается в ежедневном выполнении упражнений по укреплению мышц тазового дна, соблюдении правил гигиены и лечебных рекомендаций. Частые обмывания наружных половых органов отварами трав или теплой водой со специальными гигиеническими средствами предотвращают инфицирование мочевых путей. Для лечения нейрогенного мочевого пузыря, вызванного психологическими расстройствами, необходимым условием выздоровления и предупреждения рецидивов является длительное наблюдение и реабилитация у врача-психотерапевта. Во всех случаях хороший эффект дает санаторно-курортное лечение с употреблением минеральной воды, проведением грязелечения в виде тампонов и аппликаций на область мочевого пузыря.
Профилактика заболевания заключается в своевременном купировании воспалительных процессов в органах мочевыводящей системы, предупреждении травматизации, переохлаждения и нервных стрессов.
pochkimed.ru
