Лечение миомы матки без операции: лекарственные препараты
О симптомах и признаках миомы матки читайте в нашей отдельной статье. В данной работе мы расскажем о лечении патологии с помощью консервативной терапии. Выбор метода избавления от миомы матки определяется тяжестью симптомов, возрастом пациентки, величиной и количеством узлов. Если патологические признаки наличия новообразования отсутствуют, некоторые специалисты выбирают выжидательную тактику. Другие врачи настаивают на том, что медикаментозное лечение миомы матки требуется даже в случае обнаружения микроочагов разрастания мягких тканей.
Сегодня специалисты не спешат обращаться к хирургическим техникам при маточной опухоли, для начала применяя лекарственные средства. Нередко лейомиома или фибромиома рассасывается самостоятельно под влиянием терапии гормонами или подвергается обратному развитию во время менопаузы.
Выбор препаратов, схемы и долговременности лечения прямо связаны с результатами диагностики, возрастом, тяжестью симптомов, намерением пациентки родить в неотдаленном будущем.
Лечение миомы матки без операции показано при следующих условиях:
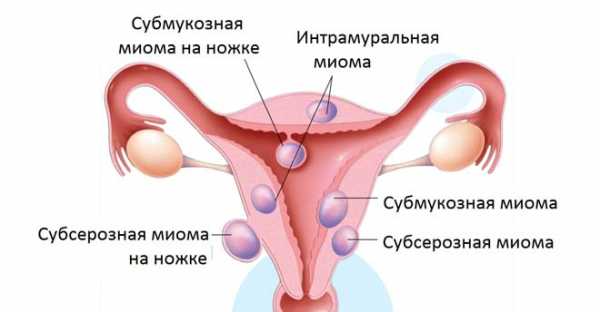
- У пациентки диагностирован интрамуральный или субсерозный тип опухоли без подозрений на онкологию.
- Размеры узла находятся в пределах 30 мм при незначительном увеличении органа.
- Патология протекает без выраженных тягостных признаков.
- В будущем планируется беременность.
- Необходимо затормозить рост образования или уменьшить его размеры перед применением оперативного вмешательства.
Цель гормональной терапии при миоме – снизить действие половых гормонов (эстрадиола и прогестерона), которые стимулируют рост клеток в миоматозных тканях, затормозить разрастание опухоли или уменьшить ее размеры. Это достигается временным угнетением работы яичников с целью наступления обратимой псевдоменопаузы.
Использование лекарственной терапии как первого этапа органосохраняющего лечения способствует уменьшению как тягостных проявлений у пациентки, так и снижению риска операционных и послеоперационных осложнений.
Долговременность применения фармакологических средств — от 3 до 7 месяцев. Неэффективность медикаментозного лечения миомы матки отмечают у 10 – 15 пациенток из 100 при наличии у них показаний для гормонотерапии.
Самостоятельный прием гормонов не только бесполезен, но крайне опасен. Только специалист может проанализировать состояние гормонального статуса девушки и соотношение между разными видами гормонов, рассчитать нужную дозу лекарства от миомы матки, разработать схему применения в определенные дни месячного цикла. Врач учтет переносимость того или иного средства и проконтролирует его лечебный эффект, добиваясь уменьшения опухоли и ослабления всех симптомов.
Рассмотрим подробнее лекарства, которые назначают при консервативном лечении миомы матки.
Гестагены, прогестагены
Данные средства подавляют продукцию эстрогена в яичниках, но в менее выраженной степени по сравнению с блокаторами гормонов (а-ГнРГ).
 Базовые препараты: Утрожестан, Норколут, Примолют-нор (норэтистерон), Дюфастон (дидрогестерон), 17-ОПК (17-оксипрогестерона капронат) в ампулах. Они положительно влияют как на репродуктивную систему, так и на функцию надпочечников по выработке стероидных гормонов. Практически в 100% устанавливался стабильный месячный цикл. Уменьшение объема миомы матки в процессе терапии отмечается в 42 – 46%. Но у части пациенток происходило разрастание опухоли.
Базовые препараты: Утрожестан, Норколут, Примолют-нор (норэтистерон), Дюфастон (дидрогестерон), 17-ОПК (17-оксипрогестерона капронат) в ампулах. Они положительно влияют как на репродуктивную систему, так и на функцию надпочечников по выработке стероидных гормонов. Практически в 100% устанавливался стабильный месячный цикл. Уменьшение объема миомы матки в процессе терапии отмечается в 42 – 46%. Но у части пациенток происходило разрастание опухоли.
Используют такие медикаменты чаще при сочетании маленьких единичных узлов, гиперплазии (разрастании) эндометрия и расстройства месячного цикла.
Антигестагены
Одни из наиболее результативных медикаментов с минимальным перечнем побочных реакций. Блокируют действие прогестерона и являются средством для срочного прерывания беременности (до 9 недель). Первый препарат этого ряда Мифепристон (Гинестрил) показывает достоверное снижение роста опухолевых структур и устранение симптомов, также как и более поздние медикаменты-антипрогестагены: Онапристон, Пенкрофтон (миропристон) и одно из последних средств – Эсмия (улипристал).
Их назначают:
- пациенткам со значительным размером лейомиомы в матке;
- для подготовки к операции женщин с выраженной анемией;
- в качестве основного метода терапии в фазе женщин 45 – 55 лет с тягостными патологическими проявлениями;
- для лечения молодых девушек с условием индивидуального подбора повышенных суточных доз.
На фоне консервативного лечения миомы матки с помощью антигестагенов, почти у 80 – 90 % пациенток значимо снижается объем миоматозных узлов и интенсивность кровопотери при менструациях. Почти половина женщин, получавших Эсмию, избежали хирургического вмешательства.
Аналоги гонадотропин-рилизинг гормонов (аГнРГ)
К группе аналогов ГнРг относят агонисты и антагонисты гонадотропин-рилизинг гормона. Использование медпрепаратов этой группы ведет к угнетению продукции гонадотропинов в гипофизе, вызывая антиэстрогенный эффект, и запускает процесс наступления временной и обратимой медикаментозной менопаузы, на фоне которой происходит существенное уменьшение аномальных узлов.
Назначаются данные лекарства от миомы матки в виде подкожных уколов по индивидуальной схеме и рассчитанных дозах с целью:
- устранения клинических признаков миомы и уменьшения ее размера;
- длительной терапии при наличии противопоказаний к любому хирургическому вмешательству, включая малоинвазивное;
- избежать операции по удалению миомы матки у женщин, планирующих зачатие;
- уменьшения объема миоматозного узла в стадии подготовки к операции — предварительный прием аГнРг существенно облегчает любой вид вмешательства, включая гистерэктомию и миомэктомию.
 В группу аГнРг включены: Трипторелин (Декапептил, Диферелин), Гозерелин (Золадекс), Нафарелин (Синарел), Бусерелин, Лейпрорелин (Люкрин), Цетротид (Цетротерикс), Ганиреликс.
В группу аГнРг включены: Трипторелин (Декапептил, Диферелин), Гозерелин (Золадекс), Нафарелин (Синарел), Бусерелин, Лейпрорелин (Люкрин), Цетротид (Цетротерикс), Ганиреликс.
При лечении миомы матки с помощью аГнРг, к 3 – 4 месяцу наблюдается уменьшение опухоли более чем на 50%. Но в 6 – 18 % случаев использование этого вида средств не показывает положительных результатов. Более того, иногда после существенного уменьшения объема узла (до 70 – 80%) при продлении терапии наблюдается вторичное разрастание тканей. Поэтому чаще аГнРг назначают не в качестве длительной терапии, а перед операцией.
Отрицательным фактором использования аГнРг является развитие депрессивных состояний, приливы, снижение сексуального влечения, разрушение костной ткани из-за деминерализации.
Чтобы минимизировать выраженность нежелательных эффектов, специалисты практикуют различные режимы лечения, меняя схемы применения: прерывистый режим, схема с включением рассчитанных доз эстрогенов.
Вы используете народные средства лечения?
ДаНет
Комбинированные оральные контрацептивы (противозачаточные) при миоме матки
Женщинам 35 – 45 лет с миомой, кистой яичника, дисфункцией яичников и обильными маточными кровотечениями, кратковременно (на 3 – 4 месяца) назначают курс противозачаточных таблеток — КОК с комбинацией этинилэстрадиола и таких гестагенных соединений, как дезогестрел (Мерсилон, Новинет, Марвелон ), норгестрел (Овидон, Ригевидон), гестоден (Логест, Линдинет), Жанин, Ярина.
Терапия КОК ведет к ослаблению кровотечений, болей, но уменьшение объема новообразования можно ожидать, только если его диаметр не превышает 15 мм.
Каждая группа лекарств и каждый медикамент из группы имеет свою специфику применения и противопоказания, и только специалист может подобрать лечебное средство наиболее эффективное и безопасное для конкретной пациентки. Самостоятельное назначение гормональных препаратов способно вызвать активный рост опухоли, нарушить функцию эндокринных желез, остеопороз, а также жизнеугрожающее состояние – тромбоэмболию – закупорку сосудов тромбами из-за повышения густоты крови. Поэтому прием тех или иных противозачаточных таблеток от миомы матки должен назначать только квалифицированный специалист.
Заместительная гормональная терапия (ЗГТ)
 Влияние на миому матки заместительного гормонального лечения при климаксе остается спорным. В этот период у большинства женщин рост доброкачественного образования прекращается самостоятельно, поэтому требуется осторожный подход к гормональной терапии. Так, в постменопаузе у части женщин прием эстрогенных лекарств может спровоцировать появление миомы в теле матки. Из рекомендованных средств выделяют прогестагены Трисеквенс и Клиогест, обладающие свойством подавлять аномальное разрастание тканей в репродуктивных органах. Грамотный подбор фармпрепаратов снимает тягостные симптомы климакса, снижает риск разрушения костной ткани и поражения сердечно-сосудистой системы.
Влияние на миому матки заместительного гормонального лечения при климаксе остается спорным. В этот период у большинства женщин рост доброкачественного образования прекращается самостоятельно, поэтому требуется осторожный подход к гормональной терапии. Так, в постменопаузе у части женщин прием эстрогенных лекарств может спровоцировать появление миомы в теле матки. Из рекомендованных средств выделяют прогестагены Трисеквенс и Клиогест, обладающие свойством подавлять аномальное разрастание тканей в репродуктивных органах. Грамотный подбор фармпрепаратов снимает тягостные симптомы климакса, снижает риск разрушения костной ткани и поражения сердечно-сосудистой системы.
Другие средства
Для уменьшения интенсивности месячных кровотечений врач может назначить кровоостанавливающие медицинские средства: Транексам, Аскорутин, Этамзилат с обязательным отслеживанием показателей свертываемости крови, чтобы не допустить тромбозов глубоких вен.
Домашняя медицина
К народным средствам и методам лечения миомы матки грамотные медики относятся отрицательно, считая, что время, потраченное на домашние рецепты, только затягивает начало проведения адекватного лечения, особенно при размере миомы больше 2 – 3 см.
Осторожное одобрение получают только сборы с красной щеткой, календулой, боровой маткой, донником, медуницей, шалфеем, хвощом, но только после обсуждения схемы применения с врачом и учетом противопоказаний для этих трав. Многие природные вещества и растения могут только усугубить течение болезни, вызвать аллергию и отравление.
Лечение миомы матки без операции возможно только при своевременном обращении к гинекологу и диагностировании болезни. Именно поэтому необходимо при первых же признаках заболевания обращаться в медицинский центр.
ikista.ru
Современные методы лечения миомы матки: медикаментозное, хирургическое или ЭМА
В современной гинекологии есть несколько методов лечения миомы матки. Они делятся на три типа:
- медикаментозные
- хирургические
- эмболизация маточных артерий

Медикаментозное лечение миомы матки
В настоящее время для медикаментозного лечения миомы матки используется только один фармацевтический препарат Эсмия. Это негормональное средство, которое блокирует рецепторы прогестерона — основного гормона, который способствует росту миоматозных узлов. Под воздействием этого препарата миоматозные узлы уменьшаются. К сожалению, это происходит не всегда.
Эффективность препарата зависит от того, насколько много прогестероновых рецепторов содержится непосредственно в миоматозном узле. В зависимости от этого результаты лечения могут быть различны – от практически полного отсутствия эффекта до ярко выраженного эффекта.
Медикаментозное лечение данного заболевания рекомендуется в тех случаях, когда эмболизация маточных артерий будет избыточным методом – например, в молодом возрасте при маленьких миоматозных узлах. Если у 20-летней пациентки узлы не превышают 1,5 – 3 см и заболевание протекает бессимптомно, то изначально медикаментозного лечения препаратом Эсмия, который позволяет на раннем этапе заболевания уменьшить эти узлы до минимума, будет вполне достаточно. Со временем медикаментозное лечение можно будет повторить при необходимости.
Иногда для лечения данного заболевания применяются также другие лекарственные препараты, но в современной гинекологической практике они считаются менее эффективными, чем любые другие методы лечения.
Хирургическое лечение миомы матки
Хирургическое удаление миоматозных узлов производится с помощью миомэктомии или гистерорезектоскопии.
Эти методы рекомендуются в тех случаях, если пациентка планирует беременность в ближайшее время и миоматозные узлы могут помешать зачатию или благополучному вынашиванию плода.
Но в этом случае необходимо оценить, насколько этот метод лечения может быть травмирующим для матки – в каждом случае это решается индивидуально.
Данные хирургические методы лечения применимы, если:
- миоматозный узел расположен снаружи матки
- миоматозный узел расположен внутри полости матки и его удобно полностью срезать с помощью гистерорезектоскопии
Гистерэктомия (хирургическое удаление матки) назначается только в исключительных случаях:
- при гигантских матках (более 20 – 22 недель беременности)
- при наличии множества миоматозных узлов (кроме тех гигантских миоматозных узлов, при которых показана миомэктомия)
- при наличии сопутствующей пограничной патологии эндометрия, шейки матки или яичников.
Эмболизация маточных артерий
ЭМА позволяет окончательно решить проблему миоматозных узлов, так как у этого метода нет рецидивов, которые возникают при хирургическом лечении, и при таком методе практически не бывает осложнений.
Если заболевание протекает с выраженными симптомами (обильные кровотечения, боли и т.п.), то эмболизация маточных артерий позволяет полностью решить эту проблему.
- при симптомной миоме у пациентки, которая не планирует беременность в ближайшее время, но в будущем собирается иметь детей
- при симптомной миоме у пациентки, которая уже закончила свой репродуктивный период
- если женщина планирует беременность в ближайшее время, при этом миома является множественной или миоматозные узлы располагаются в разных локализациях, поэтому хирургический метод лечения может нанести матке выраженный дефект в виде глубоких множественных рубцов

При эмболизации миоматозные узлы не удаляются. Эмболы перекрывают сосуды, питающие узлы, и миома усыхает, так же как виноград становится изюмом.
Другие методы лечения миомы матки
Несмотря на то, что иногда врачи предлагают женщинам некоторые другие методы лечения этого заболевания, в настоящее время они считаются неэффективными. К таким методам относится Мирена, ФУЗ-абляция.
Доказано, что гормональная спираль Мирена не оказывает никакого действия на миоматозные узлы и не является способом лечения миомы матки.
Такой метод как ФУЗ-абляция изначально обещал хорошие результаты, но у него есть серьезные недостатки. Во-первых, существует очень много условий для реализации этого метода (т.е. его применение возможно только в определенных случаях), а во-вторых, при таком методе лечения очень часто возникают рецидивы.
Позвоните и запишитесь на приём:+7 (495) 221-21-47Проконсультируйтесь по e-mailБАДы (индинол, эпигалат) и средства народной медицины не являются методами лечения миомы матки, так как они не оказывают на данное заболевания никакого доказанного лечебного эффекта.
www.mioma.ru
как вылечить миоматозные узлы без удаления, где лечить миому в Москве
08 февраль 2018 7887 0Миома матки представляет собой достаточно распространенное заболевание, которое диагностируется, в среднем, у 40% женщин. Большинство из пациенток долгие годы не придают значения тазовым болям, обильным менструациям и не могут забеременеть, прибегая лишь к симптоматическому лечению. В итоге длительное отсутствие адекватной терапии приводит к необходимости проведения гистерэктомии – калечащей операции по удалению матки. Однако любой женщине необходимо понимать, что в наше время существует несколько методов, как избавиться от миомы без операции и предотвратить возникновение новых миоматозных узлов.
Обращаем ваше внимание, что данный текст готовился без поддержки нашего Экспертного совета.
Точные причины возникновения миомы матки до сих пор досконально не изучены. По одной из версий развитие данного заболевания связано с гормональным дисбалансом – при нарушении соотношения в организме прогестерона и эстрогена. В менопаузальный период у женщин уменьшается выработка этих гормонов, поэтому в это время зачастую происходит уменьшение миомы и неприятные симптомы, беспокоившие их ранее, исчезают.
Как правило, миома матки длительное время протекает бессимптомно, либо имеет слабо выраженную симптоматику. Появление неприятных симптомов связано с кровотечениями или сдавлением внутренних органов.
У некоторой части пациенток миома матки проявляется следующими симптомами:
- ощущением сдавления или переполненности в животе;
- болями в области поясницы;
- длинными и обильными менструациями;
- болевыми ощущениями во время полового акта;
- частыми позывами к мочеиспусканию.
Обильные кровотечения во время менструаций могут привести к развитию анемии, которая сопровождается ухудшением общего состояния: появлением усталости и слабости. Кроме того, миома матки может осложняться бесплодием или проблемами во время наступившей беременности — стать причиной преждевременных родов или выкидышей.
Первичный диагноз «миома матки» врач может установить на основании результатов анализа симптомов заболевания и гинекологического осмотра. Для уточнения диагноза могут быть назначены дополнительные методы исследования, самым распространенным из которых является УЗИ, с помощью которого определяют размеры и локализацию миоматозного узла. Анемия и другие проблемы со здоровьем выявляются с помощью клинических лабораторных анализов.
Довольно часто женщинам с миомой матки назначается динамическое наблюдение с регулярным проведением ультразвукового исследования, которое позволяет определить состояние миоматозных узлов. Курс терапии чаще всего назначается при наличии четырех факторов:
- с учетом возраста пациентки – в постменопаузальном периоде миоматозные узлы прекращают свой рост, тем самым избавляя женщину от дискомфортных ощущений;
- при симптомах, которые снижают качество жизни женщины. К ним относят анемию, нарушение мочеиспускания, связанное со сдавлением мочевого пузыря;
- при росте миоматозного узла, зафиксированном с помощью нескольких последовательных ультразвуковых исследований;
- при наличии у пациентки планов на беременность.
Узнать подробнее, как проявляется миома, как лечить без операции данное заболевание можно, записавшись на консультацию ведущих специалистов.
Наиболее эффективными методами лечения миомы матки на сегодняшний день считаются три: хирургическое вмешательство, эмболизация маточных артерий (ЭМА) и медикаментозное лечение миомы матки без операции с применением препаратов группы блокаторов рецепторов прогестерона.
Хирургическое лечение миомы матки
Для проведения миомэктомии – удаления миомы матки хирургическим способом используется классический метод (посредством выполнения разреза) и лапароскопический. Лапароскопия предполагает удаление миоматозного узла через влагалище специальным эндоскопическим инструментом (резектоскопом), на одном из концов которого имеется петля.
Данная операция имеет свои преимущества и недостатки. К преимуществам относят возможность удаления доброкачественной опухоли. К недостаткам – довольно существенные риски, которые сопровождают любое хирургическое вмешательство и наркоз.
По данным статистических исследований, рецидивы после миомэктомии возникают более, чем в 10% случаев в год. Для снижения вероятности их возникновения пациенткам необходимо проведение гормональной терапии.
Кроме того, хирургическое удаление миомы не является оптимальным решением для пациенток, планирующих беременность в ближайшем будущем или в отдаленной перспективе. После миомэктомии нередко отмечается развитие негативных последствий, например, спаечного процесса в малом тазу, осложняющегося трубно-перитонеальным бесплодием – нарушением проходимости маточных труб и, как следствие, невозможностью попадания оплодотворенной яйцеклетки в матку.
При миоме матки огромных размеров чаще всего рекомендуется проведение гистерэктомии, в ходе которой приходится удалять матку, так как лечить миому матки без операции в этом случае не имеет смысла. Подобное хирургическое вмешательство позволяет избежать серьезных проблем, возникающих на фоне миомы.
Миома: лечение без операции посредством эмболизации маточных артерий (ЭМА)
Процедура эмболизации маточных артерий (ЭМА) предполагает введение эмболизирующего препарата непосредственно в сосуды, которые питают миому матки. Частицы, входящие в состав данного препарата, обеспечивают перекрытие кровотока в сосудах миомы, благодаря чему в патологически разросшиеся ткани не поступает кислород, необходимый для их питания. В результате происходит гибель миоматозного узла, замещение его соединительной тканью и уменьшение размеров.
Эмболизация маточных артерий не является новой процедурой. Для лечения миомы матки в европейских клиниках её применяют уже несколько десятилетий.
К основным преимуществам ЭМА относят:
- высокую эффективность – практически полное отсутствие рецидивов после ЭМА, отсутствие необходимости в применении дополнительных методов лечения;
- нормализация менструального цикла, устранение проблем с мочеиспусканием, связанных со сдавлением мочевого пузыря миоматозным узлом;
- абсолютная безопасность метода ЭМА – отсутствие рисков, связанных с хирургическим вмешательством. Для проведения ЭМА не требуется применение наркоза, продолжительность самой процедуры, как правило, не превышает 15-20 минут. Из стационара пациентка может выписаться уже на 2-3 сутки после ЭМА, период реабилитации длится от 5 до 7 дней.
Показания к эмболизации маточных артерий:
- обильные менструации, признаки сдавления органов малого таза, частые мочеиспускания – полное исчезновение данных симптомов отмечается уже через полтора месяца после ЭМА;
- рост миоматозных узлов, зафиксированный согласно результатам ультразвукового исследования (не реже одного раза в три-шесть месяцев), даже при отсутствии симптомов миомы матки и планирования беременности;
- множественные миоматозные узла средних и больших размеров, независимо от их направления роста и локализации.
Учитывая вышесказанное, можно сделать вывод о том, что удаление миомы матки без операции с помощью ЭМА может проводиться как при единичных, так и при множественных миоматозных узлах, при любой их локализации.
Основанием для проведения подобного вмешательства является улучшение качества жизни женщины и устранение беспокоящих её проблем.
Выполнить процедуру ЭМА можно в одной из современных клиник, с современными рентгенографическими операционными, оснащенными ангиографами, их список представлен на нашем сайте.
Уточнить информацию о стоимости ЭМА, узнать детали выполнения проведения эмболизации маточных артерий и записаться к лучшему специалисту можно связавшись с нашим координатором.
Как вылечить миому матки без операции с помощью медикаментозной терапии
На сегодняшний день медикаментозное лечение миомы без операции предполагает применение блокаторов рецепторов прогестерона – улипристала ацетата. Наивысшую эффективность препарат показывает при приеме в два-три цикла (не более четырех), с соблюдением перерывов в два месяца. Динамику лечения оценивают с помощью ультразвукового исследования. Более чем в 50% случаев миоматозные узлы при этом регрессируют. Еще одним преимуществом подобной медикаментозной терапии является хорошая переносимость препарата. Однако имеются и некоторые недостатки метода:
- непостоянство сохранения результата и невозможность предсказать рецидив заболевания;
- отсутствие данных о реакции на препарат различных миоматозных узлов: у одних может отмечаться уменьшение, у других – постоянство размера.
Чаще всего медикаментозную терапию назначают пациенткам молодого возраста при первично выявленных мелких узлах размеров до 3см.
Однако нужно знать, что гормональные препараты обладают временным или профилактическим эффектом. Тем более при поиске способов, как уменьшить миому без операции, не стоит обращаться к всевозможным БАДам, фитопрепаратам и гомеопатическим средствам. Самолечение может не просто бесполезным, но и довольно опасным, так как за это время миоматозный узел может вырасти, что потребует более сложных методов лечения и удаление миомы без операции будет невозможным. Женщинам с миомой матки требуется серьезное наблюдение квалифицированных специалистов.
www.mioma.ru
Новый метод консервативного лечения миомы матки | #03/17
Миома матки — одно из наиболее часто встречающихся доброкачественных новообразований в большинстве стран мира. Распространенность данного заболевания различается в различных исследованиях, что зависит от изучаемой популяции женщин и применяемых методов обследования [1]. У 30–35% пациенток миома выявляется в репродуктивном возрасте, и у трети из них сопровождается такими клиническими проявлениями, как аномальные маточные кровотечения, дисменорея, анемия, тазовые боли, диспареуния, бесплодие, осложненное течение беременности [2–4].
Как правило, у подавляющего большинства пациенток сохраняется репродуктивная функция, за исключением субмукозной формы заболевания, но взаимосвязь между миомой матки и бесплодием увеличивается с возрастом. Принимая во внимание тенденцию к позднему планированию беременности и увеличение частоты встречаемости миомы матки среди женщин репродуктивного возраста, актуальность проблемы лечения данного заболевания значительно возрастает и принимает социальную значимость. Так, в России в 2012 г. почти каждый третий ребенок был рожден женщиной старше 35 лет. Вот почему следует придерживаться тактики преимущественно органосохраняющих операций при незначительных размерах миомы матки, особенно у женщин, не реализовавших свои репродуктивные планы [5].
Согласно данным ряда исследователей, миома матки заметно чаще других причин оказывается поводом для гистерэктомии. При этом во многих ситуациях к радикальному хирургическому лечению прибегают не только для удаления гигантских форм миомы, но и в случае множественной локализации узлов, даже если размеры каждого образования невелики, причем соотношение органоуносящих к органосохраняющим операциям как 95:5. Сторонники радикальных методов лечения считают, что после органосберегающих операций сохраняется риск рецидивов (15–45%) [6–9].
Однако органоуносящие операции не могут явиться методом выбора для женщин, не реализовавших репродуктивную функцию, что заставляет врачей искать другие методы лечения.
При выборе того или иного метода лечения пациентки с миомой матки учитываются следующие факторы: кровотечение, анемия с низким уровнем гемоглобина, железа и/или ферритина, проблемы с мочеиспусканием или дефекацией, тазовые боли, фертильность, возраст пациентки и ожидаемый период до наступления менопаузы. Выбор метода лечения зависит от возраста пациентки, размеров и локализации миоматозных узлов, динамики роста, их количества, желания сохранить фертильность [10–16].
Варианты лечения пациенток с миомой матки включают терапевтическое, хирургическое и радиологическое вмешательство. Большую популярность в последнее десятилетие получили новые малоинвазивные технологии — эмболизация маточных артерий и фокальная ультразвуковая аблация миоматозных узлов. Эти высокотехнологичные хирургические вмешательства, безусловно, предпочтительнее, чем гистерэктомия, поскольку позволяют сохранить и орган, и его функцию, но их внедрение в широкую практику существенно ограничено ввиду высокой стоимости оборудования и недостатка квалифицированных кадров.
Консервативные методы лечения применяются, если пациентка хочет сохранить фертильность либо она находится в пременопаузальном периоде, а размеры миомы матки невелики, либо при наличии противопоказаний к оперативному вмешательству.
Медикаментозная консервативная терапия миомы матки должна быть направлена на замедление роста миоматозного узла, инволюцию миомы матки и устранение симптомов, например, менометроррагии и анемии [17].
В настоящее время увеличивается актуальность медикаментозного лечения миомы матки, а также предоперационной подготовки больных.
Основными преимуществами новых алгоритмов терапии миомы матки являются: увеличение интервала времени для подготовки пациентки к операции, более выраженное уменьшение размеров миомы, что позволяет провести органосохраняющую операцию менее травматично, возможность «выиграть» время у женщин с приближающейся менопаузой до наступления естественного менопаузального регресса миомы матки, снижение риска осложнений при оперативном вмешательстве. Однако в настоящее время все чаще ставится вопрос о возможном отказе от хирургического лечения в пользу консервативной терапии [18–20].
Для консервативной терапии миомы матки используются различные гормональные препараты. Так, прогестины в качестве самостоятельного лечения могут вызывать прорывные кровотечения и обладают неоднозначным ответом в плане стабилизации миоматозных узлов [21, 22]. Широко назначаемые для предоперационной подготовки агонисты гонадотропин-рилизинг гормонов (аГнРГ) приостанавливают рост, как правило, миоматозных узлов небольших размеров, создавая искусственную менопаузу. В то же время последующее выполнение органосохраняющей операции становится затруднительным из-за потери псевдокапсулы миоматозного узла, и из миомэктомии операция превращается в миометрэктомию, поскольку выделение миоматозного узла напоминает «очищение от кожуры засохшего апельсина». Необходимо учитывать побочные проявления аГнР, которые возможно назначать лишь короткими курсами (не более 6 месяцев): приливы, депрессии, снижение либидо, вагиниты, снижение минеральной плотности костной ткани, проявляющееся болями в костях. Данные проявления снижают качество жизни и как следствие комплаентность, что ограничивает назначение аГнРГ [23, 24].
Большое значение в лечении миоматозных узлов небольших размеров (до 1–1,5 см) в сочетании с аденомиозом и гиперпластическими процессами эндометрия уделяется введению левоноргестрел-выделяющей системы Мирена, которая позволяет достичь контроля над меноррагиями. Однако введение данной системы нередко сопровождается нерегулярными кровотечениями, экспульсией и практически отсутствием влияния на крупные миоматозные узлы, невозможностью использования при деформации полости матки субмукозными узлами или узлами с выраженным центрипетальным ростом [25–27].
Полученные результаты гормональной терапии пациенток с миомой матки показали, что они пока не заняли достойного места в схемах лечения этого новообразования, в том числе в рамках дооперационной подготовки.
Миома матки — не только эстроген-, но и прогестеронзависимое заболевание, которое развивается, как правило, у женщин с овуляторным менструальным циклом [28–30]. Полученные знания о патогенетических механизмах роста миомы матки в последние годы привели к применению антипрогестагенов (АП) и селективных модуляторов прогестерона (СМРП). В 2012 г. Европейская комиссия одобрила препарат, относящийся к классу СМРП — улипристала ацетат в дозе 5 мг для применения в качестве предоперационной терапии миомы матки у пациенток старше 18 лет с умеренными или тяжелыми симптомами (2 курса по 3 месяца) [28–30]. Улипристала ацетат (Эсмия) — селективный модулятор прогестероновых рецепторов, обладает смешанными агонистическими/антагонистическими свойствами, оказывает антипролиферативный, антифиброзный эффекты, индуцирует апоптоз в клетках миоматозного узла, не влияя на здоровый миометрий [17, 31, 32]. Селективно блокируя влияние прогестерона в гипофизе, улипристала ацетат (УПА) уменьшает секрецию лютеинизирующего и частично фолликулостимулирующего гормонов, приводя к ановуляции, при этом концентрация эстрадиола характерна для середины фолликулярной фазы, что позволяет избежать симптомов гипоэстрогении [29]. Развивается гипофизарно-индуцируемая аменорея. Влияние на другие гормоны (тиреотропный, адренокортикотропный, пролактин) отсутствует. СМРП обладают фармакодинамическим эффектом относительно эндометрия, в том числе антипролиферативным эффектом, который может способствовать индукции аменореи. Улипристала ацетат оказывает прямое действие на эндометрий: вызывает аменорею или уменьшает интенсивность кровотечений уже к 6–10 дню применения, а также снижает выраженность болей, беспокоящих большинство пациенток с миомой.
Когда прием препарата прекращают, менструальный цикл обычно восстанавливается в течение 4 недель. Прямое действие на эндометрий приводит к специфичным для этого класса препаратов изменениям в слизистой оболочке, связанным с модулятором рецепторов прогестерона (Progesterone Receptor Modulator Associated Endometrial Changes, PAEC). Указанные изменения гистологически представлены неактивным и слабо пролиферирующим эпителием с асимметрией роста стромы и эпителия, выраженным кистозным расширением желез со смешанными эстрогенными (митотическими) и прогестагенными (секреторными) воздействиями на эпителий матки. Подобную картину ошибочно можно принять за гиперплазию эндометрия, однако процессы обратимы и исчезают после прекращения лечения; во время терапии в коррекции данного состояния нет необходимости [33–35].
Стоит отметить и отсутствие трудностей при выполнении миомэктомии и энуклеации миоматозных узлов. В отличие от аГнРГ, препараты с улипристала ацетатом не вызывают дефицита эстрогенов и не трансформируют псевдокапсулу миомы.
Немаловажным преимуществом СМПР можно считать отсутствие влияний на надпочечники, функции печени и систему гемостаза, что очень важно для пациенток с сопутствующими соматическими заболеваниями.
Многочисленные благоприятные влияния улипристала ацетата в качестве модулятора прогестероновых рецепторов были продемонстрированы в клинических исследованиях длительной цикловой терапии PEARL I, II, III [33–35]. Авторами показано, что уже после первого курса лечения улипристала ацетатом аменорея наблюдалась через 4 дня от начала лечения (79%), а уменьшение узлов миомы в среднем составило 45%. Коррекция анемии достигается у 94% пациенток — уровень гемоглобина выше 120 г/л.
Повторные назначения 3-месячных курсов терапии улипристала ацетатом позволяют эффективно контролировать кровотечение и уменьшить размеры миомы у пациенток.
Гистологические исследования показали отсутствие гиперпластических процессов на фоне повторных курсов приема УПА, а также при применении норэтистерона ацетата или плацебо.
В настоящее время идет накопление российского опыта [1, 17, 18, 25]. по использованию УПА в качестве подготовки для хирургического лечения симптомной миомы матки.
Таким образом, улипристала ацетат — новая инновационная стратегия органосберегающей терапии миомы матки с возможностью проведения консервативного лечения при небольших размерах миоматозных узлов. Улипристала ацетат, обладающий высокоизбирательным действием на рецепторы тканей-мишеней, позволяет не только отсрочить оперативное вмешательство, но и, в некоторых случаях, вовсе его избежать. После лечения улипристала ацетатом эффект более выражен и сохраняется длительнее, чем после применения других фармакологических схем, предложенных для терапии миомы ранее [37].
Литература
- Тихомиров А. Л. Новые возможности патогенетической терапии миомы матки // Гинекология. 2013. Т. 15, № 3. С. 36–38.
- Levy B. S. Management of uterine fibroids // Acta Obstet Gynecol Scand. 2008; 87 (8): 812–823.
- Practice Committee of American Society for Reproductive Medicine in collaboration with Society of Reproductive Sur geons // Myomas and reproductive function. Fertil Steril. 2008; 90: 5. Suppl: S125-S130.
- Somigliana E., Vercellini P., Daguati R., Pasin R., De Giorgi O., Crosignani P. G. Fibroids and female reproduction: a critical analysis of the evidence // Hum Reprod Update. 2007; 13: 465–476.
- Laughlin S. K., Schroeder J. C., Baird D. D. New directions in the epidemiology of uterine fibroids // Semin Reprod Med. 2010; 28: 204–217.
- Arici A., Sozen I. Transforming growth factor-beta3 is expressed at high levels in leiomyoma where it stimulates fibronectin expression and cell proliferation // Fertil Steril. 2000; 73: 1006–1011.
- Chavez N. F., Stewart E. A. Medical treatment of uterine fibroids // Clin Obstet Gynecol. 2001; 44: 372–384.
- Luo X., Ding L., Xu J., Chegini N. Gene expression profiling of leiomyoma and myometrial smooth muscle cells in response to transforming growth factor-beta // Endocrinology. 2005; 146: 1097–1018.
- Martin Chaves E. B., Brum I. S., Stoll J., Capp E., Corleta H. E. Insulin-like growth factor 1 receptor mRNA expression and autophosphorylation in human myometrium and leiomyoma // Gynecol Obstet Invest. 2004; 57: 210–213.
- Fields K. R., Neinstein L. S. Uterine myomas in adolescents: case reports and a review of the literature // J Pediatr Adolesc Gynecol. 1996; 9: 195–198.
- Cramer S. F., Patel A. The frequency of uterine leiomyomas // Am J Clin Pathol. 1990; 94: 435–438.
- Ross R. K., Pike M. C., Vessey M. P., Bull D., Yeates D., Casagrande J. T. Risk factors for uterine fibroids: reduced risk associated with oral contraceptives // Br Med J (Clin Res Ed). 1986; 293: 359–362.
- Lumbiganon P., Rugpao S., Phandhu-Fung S., Laopaiboon M., Vudhikamraksa N., Werawatakul Y. Protective effect of depotmedroxyprogesterone acetate on surgically treated uterine leiomyomas: a multicenter case-control study // Br J Obstet Gynaecol. 1996; 103: 909–914.
- Marshall L. M., Spiegelman D., Goldman M. B. et al. A prospective study of reproductive factors and oral contraceptive use in relation to the risk of uterine leiomyomata // Fertil Steril. 1998; 70: 432–439.
- Parazzini F., Negri E., La Vecchia C., Chatenoud L., Ricci E., Guarnerio P. Reproductive factors and risk of uterine fibroids // Epidemiology. 1996; 7: 440–442.
- Burbank F. Childbirth and myoma treatment by uterine artery occlusion: do they share a common biology? // J Am Assoc Gynecol Laparosc. 2004; 11: 138–152.
- Радзинский В. Е., Архипова М. П. Миома матки: проблемы и перспективы начала века // Медицинский совет. 2014. С. 2–4.
- Адамян Л. В., Козаченко А. В., Ревазова З. В. Новые подходы к медикаментозному лечению симптомной миомы матки // Пробл. репродукции. 2013. № 3. С. 21–23.
- Stewart E. A. Uterine fibroids and evidence-based medicine — not an oxymoron // N. Engl. J. Med. 2012. Vol. 366. P. 471–473.
- Zimmermann A., Bernuit D., Gerlinger C. et al. Prevalence, symptoms and management of uterine fibroids: an international internet-based survey of 21,746 women // BMC Women’s Health. 2012. Vol. 12. P. 6. DOI: 10.1186/14726874-12-6.
- Yin P. et al. Transcription factor KLF11 integrates progesterone receptor signaling and proliferation in uterine leiomyoma cells // Canser. Res. 2010. Feb 15. Vol. 70 (4). P. 1722–1730.
- Kim J. J., Sefton E. C. The role of progesterone signaling in the pathogenesis of uterine leiomyoma // Mol Cell Endocrinol. 2011, June 6 (Epub ahead of print).
- Lethaby A., Vollenhoven B., Sowter M. Pre-operative GnRH analogue therapy before hysterectomy or myomectomy for uterine fibroids // Cochrane Database Syst Rev. 2001; CD000547.
- Campo S., Garcea N. Laparoscopic myomectomy in premenopausal women with and without preoperative treatment using gonadotrophin-releasing hormone analogues // Hum Reprod. 1999; 14: 44–48.
- Тихомиров А. Л., Леденкова А. А. Доброкачественные гиперплазии матки и внутриматочная левоноргестрел-релизинг система // Гинекология. 2012. № 3. С. 62–64.
- Zapata L. B., Whiteman M. K., Tepper N. K., Jamieson D. J., Marchbanks P. A., Curtis K. M. Intrauterine device use among women with uterine fibroids: a systematic review // Contraception. 2010; 82: 41–55.
- Sayed G. H., Zakhera M. S., El-Nashar S. A., Shaaban M. M. A randomized clinical trial of a levonorgestrel-releasing intrauterine system and a low-dose combined oral contraceptive for fibroidrelated menorrhagia // Int J Gynaecol Obstet. 2011; 112: 126–130.
- Адамян Л. В., Зайратьянц О. В., Тихомиров А. Л. и др. Антипролиферативное и проапоптотическое действие селективного модулятора рецепторов прогестерона улипристала на лейомиомц матки in vivo // Пробл. репродукции. 2014. № 3. С. 25–28.
- Коренная В. В., Подзолкова Н. М. Улипристал ацетат в лечении миомы матки // Гинекология. 2013. № 15, № 6. С. 58–61.
- Ishikawa H., Ishi K., Serna V. A., Kakazu R. Progesterone is essential for maintenance and growth of uterine leiomyoma // Endocrinology. 2010. Vol. 151, № 6. P. 2433–2442.
- Тихомиров А. Л., Казенашев В. В. Улипристал ацетат — новые возможности в лечении лейомиомы матки // Акуш. и гин. 2013. № 9. С. 97–100.
- Yoshida S., Ohara N., Xu Q. et al. Cell type specifications of progesterone receptor modulators in the regulation of uterine leiomyoma growth // Semin. Reprod. Med. 2010. Vol. 28. P. 260–273.
- Donnez J. With the advent of selective progesterone receptor modulators, what is the place of myoma surgery in current practice? // Fertility and Sterility. 2014.
- Donnez J., Tatarchuk T. F., Bouchard P., Puscasiu L., Zakharenko N. F., Ivanova T., Ugocsai G., Mara M., Jilla M. P., Bestel E., Terrill P., Osterloh I., Loumaye E. PEARL I Study Group. Ulipristal acetate versus placebo for fibroid treatment before surgery // N. Engl. J. Med. 2012. Feb 2. Vol. 366 (5). P. 409–420. DOI: 10.1056/NEJMoa1103182.
- Donnez J., Tomaszewski J., Vázquez F. et al. PEARL II Study Group. Ulipristal acetate versus leuprolide acetate for uterine fibroids // N. Engl. J. Med. 2012. Feb 2. Vol. 366 (5). P. 421–432. DOI: 10.1056/NEJMoa1103180. PMID 22296076.
- Erekson E., Yip S., Martin D. et al. // Female Pelvic Med Reconstr Surg. 2012; 18 (5): 274–280.
- Радзинский В. Е., Тотчиев Г. Ф. Миома матки: курс на органосохранение. Информационный бюллетень. М., 2014. 25 с.
А. З. Хашукоева1, доктор медицинских наук, профессор
Т. Н. Сухова
Р. А. Рзаева
Г. Г. Мосешвили
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
1 Контактная информация: [email protected]
Купить номер с этой статьей в pdf
www.lvrach.ru
