Эпштейна-Барр вирусная инфекция у детей: совершенствование программы диагностики и лечения | Симованьян
1. Боковой А.Г., Егоров А.И. Герпесвирусные инфекции у детей и родителей. — М.: Центр стратегической конъюнктуры, 2014. — 256 с. Bokovoj A.G., Egorov A.I. Gerpesvirusnye infekcii u detej i roditelej [Herpesvirus infections in children and parents] — M.: Centr strategicheskoj konjunktury, 2014. — 256 s. (In Russ.)
2. Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека. — СПб.: Спецлит, 2013. 670 с. Isakov V.A., Arhipova E.I., Isakov D.V. Gerpesvirusnye infekcii cheloveka. [Human herpesvirus infections]. — SPb.: Speclit, 2013. 670 s. (In Russ.)
3. Барычева Л.Ю. Голубева М.В., Волкова А.В. Факторы и механизмы иммуносупрессии при Эпштейна-Барр вирусной инфекции // Детские инфекции. 2014. №2. С. 28—33. Barycheva L.Ju. Golubeva M.V., Volkova A.V. Faktory i mehanizmy immunosupressii pri Jepshtejna-Barr virusnoj infekcii [Factors and mechanisms of immunosuppression by Epstein-Barr virus infection] // Detskie Infekcii. 2014. №2. S. 28—33. (In Russ.)
4. Кудин А.П. Эта «безобидная» вирус Эпштейна-Барра инфекция. Часть 1. Характеристика возбудителя. Реакция иммунной системы на вирус // Медицинские новости. 2006. №7. http: //www.mednovosti.by. Kudin A.P. Jeta «bezobidnaja» virus Jepshtejna-Barra infekcija. Chast 1. Harakteristika vozbuditelja. Reakcija immunnoj sistemy na virus [This «harmless» Epstein-Barr virus infection. Part 1. Characteristics of the pathogen. The reaction of the immune system to the virus] // Medicinskie Novosti. 2006. №7. http://www.mednovosti.by. (In Russ.)
5. Human herpesviruses / Ed. by A. Arvin, G. Campadelli-Fiume, E. Mocarski et al. Cambrige, Cambrige University Press, 2007. http //www.ncbi.nlm.nih.gov / books / NBK 47376.
Human herpesviruses / Ed. by A. Arvin, G. Campadelli-Fiume, E. Mocarski et al. Cambrige, Cambrige University Press, 2007. http //www.ncbi.nlm.nih.gov / books / NBK 47376.
6. Raab-Traub N. Novel mechanisms of EBV induced oncogenesis // Curr. Opin. Virol. 2012. Vol. 2, N 4. P. 453—458.
9. Денисенко В.Б., Симованьян Э.Н., Саухат С.Р., Колпаков Д.С. и др. Эпштейна-Барр вирусная инфекция у детей с ВИЧ-инфекцией // Материалы X Конгресса детских инфекционистов России «Актуальные вопросы инфекционной патологии и вакцинопрофилактики». — М., 2011. С. 31. Denisenko V.B., Simovanyan E.N., Sauhat S.R., Kolpakov D.S. i dr. Jepshtejna-Barr virusnaja infekcija u detej s VICH-infekciej [EpsteinBarr virus infection in children with HIV infection] // Materialy X Kongressa detskih infekcionistov Rossii «Aktualnye voprosy infekcionnoj patologii i vakcinoprofilaktiki» [Materials of X Congress of Russian childrens infectionists «Actual problems of infectious disease and vaccine prevention»].
10. Tracy S.I., Kakalacheva K., Lunemann J.D., Luzuriaga K. et al. Persistence of Epstein-Barr virus in self-reactive memory B cells // J. Virol. 2012. Vol. 88, N 22. P. 12330—12340.
11. Харламова Ф.С., Егорова Н.Ю., Гусева Л.Н. Вирусы семейства герпеса и иммунитет // Детские инфекции. 2006. №3. С. 3—9. Harlamova F.S., Egorova N.Ju., Guseva L.N. Virusy semejstva gerpesa i immunitet [Viruses herpes family and immunity] // Detskie Infekcii. 2006. №3. S. 3—9. (In Russ.)
12. Хмилевская С.А. Эпштейна-Барр вирусный мононуклеоз у детей: клинико-патогенетические аспекты, критерии диагностики, тактика терапии и диспансеризации различных вариантов течения заболевания: Автореф. дис. … докт. мед. наук. — Саратов, 2010. 50 с. Hmilevskaja S.A. Jepshtejna-Barr virusnyj mononukleoz u detej: kliniko-patogeneticheskie aspekty, kriterii diagnostiki, taktika terapii i dispanserizacii razlichnyh variantov techenija zabolevanija [Epstein-Barr virus mononucleosis in children: clinical and pathogenetic aspects, criteria for diagnosis, therapy tactics and medical examination of the different variants of the disease]: Avtoreferat dissertacii na soiskanie uchenoj stepeni doktora medicinskih nauk [Abstract of dissertation for the degree of Doctor of Medical Sciences]. — Saratov, 2010. 50 s. (In Russ.)
14. Julish E.I. Persistirujushhie infekcii i chelovek. Strategija vzaimootnoshenij [Persistent infection and people. The strategy of mutual relations] // Zdorovie Rebenka. 2009. №4. S. 114—122. (In Russ.)
2009. №4. S. 114—122. (In Russ.)
15. Малашенкова И.К., Дидковский Н.А., Сарсания Ж.Ш., Жарова Е.Н. и др. Клинические формы хронической Эпштейна-Барр вирусной инфекции: вопросы диагностики и лечения // Лечащий врач. 2003. №9. С. 32—38. Malashenkova I.K., Didkovskij N.A., Sarsanija Zh.Sh., Zharova E.N. i dr. Klinicheskie formy hronicheskoj Jepshtejna-Barr virusnoj infekcii: voprosy diagnostiki i lechenija [The clinical forms of chronic Epstein-Barr virus infection: diagnosis and treatment issues] // Lechashhij Vrach. 2003. №9. S. 32—38. (In Russ.)
16. Савенкова М.С., Савенков М.П., Абрамова Н.А., Красева Г.Н. Правильно ли мы выбираем имуномодуляторы для лечения часто болеющих детей? // Педиатрия. Приложение к журналу Consilium Medicum. 2014. №1. С. 96—99. Savenkova M.S., Savenkov M.P., Abramova N.A., Kraseva G.N. Pravil’no li my vybiraem imunomoduljatory dlja lechenija chastj bolejushhih detej? [Do we choose to treat imunomodulyatory for frequently ill children?] // Pediatrija. Prilozhenie k zhurnalu Consilium Medicum. 2014. №1. S. 96—99. (In Russ.)
17. Гусева Л.Н., Егорова Н.Ю., Гусева Н.А., Фомичева Е.А. и др. Лечение Эпштейна-Барр вирусного мононуклеоза у детей на современном этапе // Детские инфекции. 2010. №3. С. 57—60. Guseva L.N., Egorova N.Ju., Guseva N.A., Fomicheva E.A. i dr. Lechenie Jepshtejna-Barr virusnogo mononukleoza u detej na sovremennom jetape [Treatment of Epstein-Barr virus mononucleosis in children at the modern stage] // Detskie Infekcii. 2010. №3. S. 57—60. (In Russ.)
18. Oertel S.H., Riess H. Antiviral treatment of Epstein-Barr virus associated lymphoproliferations // Recent. Results Cancer. 2002. Vol. 159. P. 89—95.
19. Булгакова В.А. Противовирусная терапия острых респираторных инфекций у детей // Здоровье ребенка. 2014. №2. С. 78—84. Bulgakova V.A. Protivovirusnaja terapija ostryh respiratornyh infektcij u detej [Antiviral therapy of acute respiratory infections in children] // Zdorov’e Rebenka. 2014. №2. S. 78—84. (In Russ.)
Булгакова В.А. Противовирусная терапия острых респираторных инфекций у детей // Здоровье ребенка. 2014. №2. С. 78—84. Bulgakova V.A. Protivovirusnaja terapija ostryh respiratornyh infektcij u detej [Antiviral therapy of acute respiratory infections in children] // Zdorov’e Rebenka. 2014. №2. S. 78—84. (In Russ.)
20. Осидак Л.В., Зарубаев В.В., Образцова Е.В., Эрман Е.С. и др. Изопринозин в терапии ОРВИ у часто болеющих детей // Детские инфекции. 2008. №4. С. 35—41. Osidak L.V., Zarubaev V.V., Obrazcova E.V., Jerman E.S. i dr. Izoprinozin v terapii ORVI u chasto bolejushhih detej [Isoprinosine in the treatment of acute respiratory infections in frequently ill children] // Detskie Infekcii. 2008; 4: 35—41. (In Russ.)
21. Малиновская В.В., Деленян Н.В., Ариненко Р.Ю., Мешкова Е.Н. Виферон: комплексный противовирусный препарат для взрослых и детей. — М., 2006. 56 с. Malinovskaja V.V., Delenjan N.V., Arinenko R.Ju., Meshkova E.N. Viferon: kompleksnyj protivovirusnyj preparat dlja vzroslyh i detej. [Viferon: complex antiviral drug for adults and children]. — M., 2006. 56 s. (In Russ.)
совершенствование программы диагностики и лечения – тема научной статьи по клинической медицине читайте бесплатно текст научно-исследовательской работы в электронной библиотеке КиберЛенинка
Оригинальные статьи
Эпштейна-Барр вирусная инфекция у детей: совершенствование программы диагностики и лечения
Э. Н. Симованьян, В. Б. Денисенко, А. В. Григорян, М. А. Ким, Л. Ф. Бовтало, Л. В. Белугина
Ростовский государственный медицинский университет, Россия
Широкое распространение, тяжелое течение, частое развитие хронических форм, неблагоприятные последствия Эпштей-на-Барр вирусной инфекции для здоровья детей, трудности диагностики и терапии диктуют необходимость совершенствования лечебно-диагностической программы при данном заболевании. Обследованы 286 больных с острой и хронической Эпштей-на-Барр вирусной инфекцией. Установлено, что для своевременной диагностики заболевания необходим комплексный анализ данных анамнеза, клинической симптоматики, включающей проявления острого и хронического мононуклеозоподобного синдрома в сочетании с полиорганной патологией, а также результаты лабораторного обследования (иммуноферментный анализ, полимеразная цепная реакция, иммунный статус). Ключевые слова: Эпштейна-Барр вирусная инфекция, дети
Обследованы 286 больных с острой и хронической Эпштей-на-Барр вирусной инфекцией. Установлено, что для своевременной диагностики заболевания необходим комплексный анализ данных анамнеза, клинической симптоматики, включающей проявления острого и хронического мононуклеозоподобного синдрома в сочетании с полиорганной патологией, а также результаты лабораторного обследования (иммуноферментный анализ, полимеразная цепная реакция, иммунный статус). Ключевые слова: Эпштейна-Барр вирусная инфекция, дети
Epstein-Barr Virus Infection in Children: Improving the Diagnosis and Treatment Program
E. N. Simovanyan, V. B. Denisenko, A. V Grigoryan, M. A. Kim, L. F. Bovtalo, L. V. Belugina
Rostov-on-Don State Medical University, Russian Federation
Widespread, severe course, frequent development of chronic forms, adverse effects of the Epstein-Barr virus infection to the health of children, the difficulties of diagnosis and therapy dictate the need to improve the diagnostic and treatment programs in this disease. A total of 286 patients with acute and chronic Epstein-Barr virus infection. It was established, that for the timely diagnosis of the disease requires a comprehensive analysis of anamnesis, clinical symptoms, including symptoms of acute and chronic mononucleosis syndrome in combination with multiorgan pathology, and the results of laboratory examination (enzyme immunoassay, polymerase chain reaction, immune status). Keywords: Epstein-Barr virus infection, children
Контактная информация: Симованьян Эмма Никитична — д.м.н., профессор, заведующая кафедрой детских инфекционных болезней Ростовского государственного медицинского университета; 344022 г. Ростов-на-Дону, пер. Нахичеванский, 29; (863) 232-73-58; detinfrostov@gmail. com Simovanyan Emma Nikitichna, MD, Professor, Head of the Department of Pediatric Infectious Diseases at Rostov-on-Don State Medical University; Russia, 344022, Rostov-on-Don, Nakhichevansky, 29; tel: (863) 232-73-58; e-mail: [email protected]
com Simovanyan Emma Nikitichna, MD, Professor, Head of the Department of Pediatric Infectious Diseases at Rostov-on-Don State Medical University; Russia, 344022, Rostov-on-Don, Nakhichevansky, 29; tel: (863) 232-73-58; e-mail: [email protected]
УДК 616.9:578.825.1 1
Проблема Эпштейна-Барр вирусной инфекции (ЭБВИ) является одной из наиболее актуальных в современной педиатрии и детской инфектологии. Ее значимость определяется высокой распространенностью ЭБВИ в популяции детского населения нашей страны, неблагоприятными последствиями для здоровья ребенка, индукцией аутоиммунной, онкологической, соматической патологии, отсутствием эффективных методов лечения и реабилитации [1, 2] .
Вирус Эпштейна-Барр (ВЭБ) является ДНК-содержа-щим герпесвирусом [2—4]. Основными клетками-мишенями служат В-лимфоциты и эпителий ротоглотки. В-лимфо-циты имеют на своей мембране CD21-рецептор, с которым связывается вирус. Кроме того, ВЭБ поражает другие иммунокомпетентные клетки (Т-лимфоциты, естественные киллерные клетки, нейтрофилы, макрофаги), а также клетки протоков слюнных желез, шейки матки, желудочно-кишечного тракта (ЖКТ), эндотелий сосудов, гладкомышечные клетки. ВЭБ пожизненно персистирует в организме человека. В настоящее время описаны два типа поражения клеток — продуктивная (цитолитическая) и непродуктивная (латентная) инфекции (табл. 1). В последние годы доказана иммуносупрессивная активность возбудителя, индукция ряда злокачественных опухолей, аутоиммунных и соматических заболеваний [5, 6].
ЭБВИ характеризуется широким эпидемическим распространением — ежегодно антитела к ВЭБ появляются у 10—15% детей и подростков [7, 8]. Причем, в отличие от экономически развитых стран, в Российской Федерации
распространенность ЭБВИ начинает быстро увеличиваться уже со второго полугодия жизни. Более половины детей инфицированы вирусом к 3—4 годам жизни, 80— 90% — к периоду совершеннолетия. Распространению ВЭБ способствует разнообразие путей передачи вируса — контактно-бытовой (особенно при поцелуях), воздушно-капельный, половой, парентеральный, вертикальный пути. Неблагоприятную роль играет длительное, иногда пожизненное выделение вируса. Так, у 70—90% лиц, перенесших первичную ЭБВИ, в течение последующих полутора лет вирус продолжают обнаруживать в слюне. Кроме того, у 80—90% людей с латентной формой ЭБВИ регистрируют эпизоды выделения вируса со слюной, а у каждого четвертого из них ВЭБ обнаруживают постоянно. При им-муносупрессии число лиц, постоянно выделяющих вирус, возрастает. Так, проведенное нами обследование 58 детей с ВИЧ-инфекцией, показало, что клинико-лаборатор-ные маркеры ЭБВИ имели место у 72,4% больных [9]. Из их числа у 76,2% пациентов методом полимеразной цепной реакции (ПЦР) в режиме реального времени в слизи ротоглотки выделяли ВЭБ в титре от 59 до 7 061 112 коп./мл (в среднем 329 065 ± 22 260 коп./мл).
Более половины детей инфицированы вирусом к 3—4 годам жизни, 80— 90% — к периоду совершеннолетия. Распространению ВЭБ способствует разнообразие путей передачи вируса — контактно-бытовой (особенно при поцелуях), воздушно-капельный, половой, парентеральный, вертикальный пути. Неблагоприятную роль играет длительное, иногда пожизненное выделение вируса. Так, у 70—90% лиц, перенесших первичную ЭБВИ, в течение последующих полутора лет вирус продолжают обнаруживать в слюне. Кроме того, у 80—90% людей с латентной формой ЭБВИ регистрируют эпизоды выделения вируса со слюной, а у каждого четвертого из них ВЭБ обнаруживают постоянно. При им-муносупрессии число лиц, постоянно выделяющих вирус, возрастает. Так, проведенное нами обследование 58 детей с ВИЧ-инфекцией, показало, что клинико-лаборатор-ные маркеры ЭБВИ имели место у 72,4% больных [9]. Из их числа у 76,2% пациентов методом полимеразной цепной реакции (ПЦР) в режиме реального времени в слизи ротоглотки выделяли ВЭБ в титре от 59 до 7 061 112 коп./мл (в среднем 329 065 ± 22 260 коп./мл).
В последние годы получены новые данные о патогенезе ЭБВИ. Доказано, что стратегия ВЭБ заключается в репликации в клетках-мишенях, сопровождающейся выделением зрелых вирусных частиц во внешнюю среду, с последующей пожизненной персистенцией возбудителя в В-лимфоцитах [5, 7, 10]. При этом создается пул «клеток-резервуаров» для реактивации вируса в условиях им-
Таблица 1. Характеристика продуктивной и непродуктивной форм ЭБВИ
Характеристики Продуктивная (цитолитическая) инфекция Непродуктивная (латентная) инфекция
Клетки-мишени Все клетки-мишени Только В-лимфоциты
ДНКВЭБ Линейная Замкнута в эписому
Количество экспрессированных генов 100 3 — 10
Репликация ВЭБ Быстрая, с образованием вирионов Медленная, синхронно делению клетки
Экспрессия иммуногенных антигенов Экспрессируются Не экспрессируются
Разрушение инфицированной клетки За счет выхода вирионов, иммунного цитолиза Не происходит
муносупрессии. В связи с этим ВЭБ реализует сложные механизмы подавления ответных реакций иммунной системы и, с другой стороны, формирования латентной инфекции.
В связи с этим ВЭБ реализует сложные механизмы подавления ответных реакций иммунной системы и, с другой стороны, формирования латентной инфекции.
Установлено, что при первичном заражении ВЭБ поражает, прежде всего, В-лимфоциты и эпителий ротоглотки [5, 7]. В этих клетках развивается продуктивная (цито-литическая) инфекция, которая сопровождается образованием новых вирионов и разрушением пораженных клеток. В составе инфицированных В-лимфоцитов и в свободном виде ВЭБ диссеминирует по организму, что ведет к поражению лимфоидных органов. Контакт вирусных антигенов с клетками иммунной системы приводит к запуску иммунного ответа [3, 5, 11]. Ведущую роль в элиминации ВЭБ-инфицированных клеток играет иммунный ответ по клеточному типу с участием специфических цитотоксиче-ских CD8-лимфоцитов. Причем, именно с ответными реакциями иммунной системы связано появление клинической симптоматики инфекционного мононуклеоза — общеинфекционного, лимфопролиферативного синдромов, тонзиллита, аденоидита, изменений в гемограмме.
ВЭБ вступает в сложные взаимодействия с иммунной системой, что, в конечном итоге, приводит к формированию вторичного иммунодефицитного состояния (ИДС) и обеспечивает ускользание вируса от защитных реакций [3, 7, 11]. Происходит поражение, прежде всего, основных клеток-мишеней — В-лимфоцитов. Особенностью им-мунопатогенеза ЭБВИ является не гибель инфицированных В-клеток, а, наоборот, приобретение ими способности к неконтролируемой пролиферации за счет угнетения апоптоза (иммортализации). Кроме того, развивается по-ликлональная активация В-лимфоцитов, которая ведет к гиперпродукции гетерофильных антител к эритроцитам барана, лошади, быка, аминопенициллинам, а также аутоантител. При этом нарушается выработка защитных антител, что связано с блокадой вирусом CD21 -рецептора В-лимфоцитов (в норме связывается с C3d-компонентом комплемента), а также с угнетением экспрессии HLA-анти-гена I класса вирусным антигеном EBNA-1, в результате чего нарушается распознавание антигенов Т-хелперами 2-го типа (^2) и регуляция синтеза иммуноглобулинов.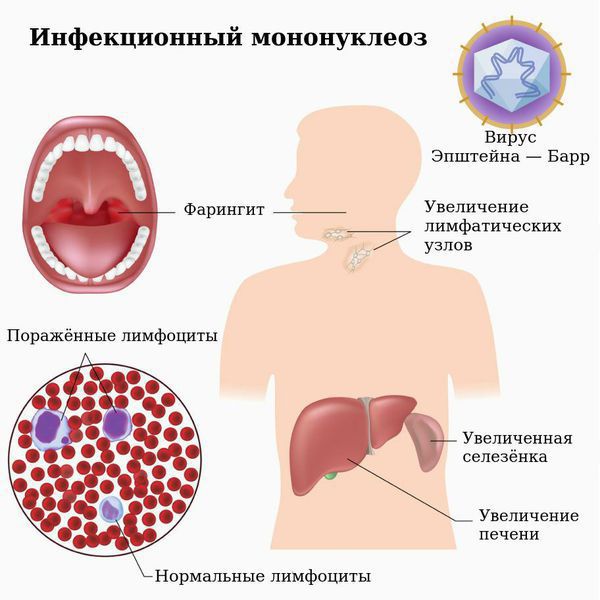 2-типа.
2-типа.
При ЭБВИ возникают изменения со стороны факторов врожденной резистентности, прежде всего, системы ИФН [3, 11 ]. Наблюдается не только снижение выработки ИФН-у и ИФН-а, но и уменьшение экспрессии рецепторов к ИФН-у на клеточной мембране, а также передачи сигнала от них в клетку. Нарушение функциональной активности естественных киллерных клеток, макрофагов, нейтрофилов обусловлено как прямым инфицированием этих клеток, так и развитием вторичных иммунопатологических процессов.
Формирование вторичного ИДС обеспечивает пожизненную персистенцию возбудителя с периодической реактивацией и, с другой стороны, является причиной формирования микст-инфекции [12]. Достаточно часто присоединяются инфекции, вызванные респираторными вирусами, герпесвирусами, условно-патогенными бактериями, хламидиями, микоплазмами, грибами, что ведет к негладкому течению заболевания и может служить причиной летального исхода. Кроме того, развитие вторичного ИДС в условиях незрелости иммунной системы у детей раннего возраста приводит к тому, что клиника типичного инфекционного мононуклеоза развивается редко. При этом у почти половины пациентов (40%) первичная ЭБВИ протекает под маской острого респираторного заболевания (ОРЗ) — фаринготонзиллита [4].
Важный этап патогенеза ЭБВИ — переход в латентную инфекцию [1, 2, 4, 10]. Эта форма развивается только в ВЭБ-инфицированных В-лимфоцитах. При этом вирусная
ДНК замкнута в виде кольца (эписомы), экспрессируется не более десяти генов. При этом вирус становится недоступным для защитных реакций иммунной системы.
Следует отметить, что на этапе латентной инфекции возможна злокачественная трансформация инфицированных клеток. В онкогенезе играет роль не только сам ВЭБ, но и наследственные, географические факторы, состояние иммунной системы. ВЭБ-ассоциированные опухоли поражают лимфоидную ткань, эпителий и гладкую мускулатуру [2, 4—6]. Их подразделяют на несколько видов: лимфомы — В-клеточные (эндемическая лимфома Беркитта, диффузная лимфома, ходжкинские лимфомы), Т-N K-клеточные; карциномы — назофарингеальная карцинома, карцинома желудка; саркомы.
ВЭБ-ассоциированные опухоли поражают лимфоидную ткань, эпителий и гладкую мускулатуру [2, 4—6]. Их подразделяют на несколько видов: лимфомы — В-клеточные (эндемическая лимфома Беркитта, диффузная лимфома, ходжкинские лимфомы), Т-N K-клеточные; карциномы — назофарингеальная карцинома, карцинома желудка; саркомы.
На этапе латентной инфекции возможно формирование вторичного ИДС, приводящего к реактивации вируса [13]. Причины, способствующие переходу из латентной в цитолитическую инфекцию, многообразны [2, 3, 5]. К ним относятся неадекватный иммунный ответ по клеточному и гуморальному типам, нарушение функциональной активности факторов врожденной резистентности, защитных свойств апоптоза, прямое действие ВЭБ на клетки-мишени (высокая вирусная нагрузка, экспрессия генов LPM-1, EBN1-1 и др.), инфицирование лимфоцитов (CD3, CD4, CD16), угнетение апоптоза ВЭБ-инфицированных клеток, действие суперантигена вируса.
В результате реактивации вируса заболевание приобретает хроническое течение [14]. Формирование глубокого вторичного ИДС ведет к частому присоединению интеркур-рентных инфекций, что является причиной перехода ребенка в группу часто болеющих детей (ЧБД) [15].
В настоящее время получены убедительные данные о роли ВЭБ в патогенезе аутоиммунных заболеваний (системной красной волчанки, ревматоидного артрита), рассеянного склероза, васкулитов, гемофагоцитарного синдрома [1, 2, 4, 5]. Хронический воспалительный процесс, индуцированный ВЭБ, приводит к структурным и метаболическим нарушениям пораженных тканей, что является причиной возникновения разнообразной соматической патологии [5, 12—14]. Важную роль в ее формировании играет индукция апоптоза клеток [13, 14].
Особенности возбудителя, эпидемиологии и патогенеза заболевания определяют многообразие клинических форм с учетом сроков от момента инфицирования.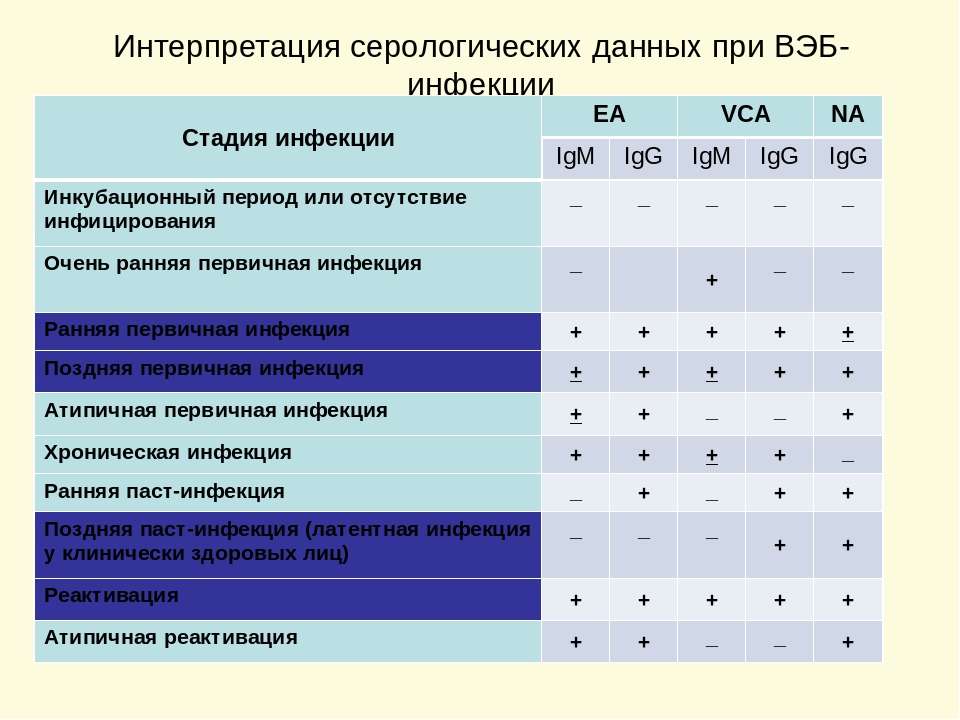
I. 0—6 месяцев после инфицирования
Типичная форма — острый инфекционный мононукле-оз (первичный)
Атипичная форма — ОРЗ, стертая, бессимптомная, генерализованная
Латентная форма
II. Более 6 месяцев после инфицирования
Типичная форма — хронический инфекционный моно-нуклеоз (первичный, вторичный), острый инфекционный мононуклеоз (вторичный)
Атипичная форма — хроническая стертая, бессимптомная формы, активная ЭБВИ с тяжелой полиорганной патологией, гемофагоцитарный синдром и др.
Латентная форма
III. Отдаленный период
Опухоли
Аутоиммунная патология
Неблагоприятное течение ЭБВИ с формированием полиорганной патологии, ИДС, присоединением микст-инфекций, переход в хроническую форму, индукция онкологической и аутоиммунной патологии диктуют необходимость своевременной диагностики острой и хронической ЭБВИ, в т.ч. в форме микст-инфекции, назначения комплексной терапии с использованием препаратов, воздействующих на различные этапы жизненного цикла ВЭБ, проведения этапной реабилитации пациентов.
Что касается проблемы лечения, то в настоящее время существуют различные подходы к этиотропной терапии ЭБВИ. Используют монотерапию аномальными нукле-озидами (ацикловиром и др.), препаратами интерферона (ИФН), индукторами ИФН [2, 16]. Ряд авторов ставит под сомнение необходимость противовирусной терапии при данном заболевании, а для купирования клинических симптомов, с учетом роли иммунной системы в их генезе, рекомендуют иммунодепрессанты (глюкокортикоиды) [5, 17]. В связи с этим требует уточнения ряд вопросов, касающихся лечения ЭБВИ. Во-первых, представляется целесообразным эффективное подавление репликации ВЭБ в цитолитическую стадию инфекции (первичная, реактивированная ЭБВИ, активная форма ХЭБВИ), что позволит уменьшить количество ВЭБ-инфицированных В-лимфо-цитов и, тем самым, сузить «плацдарм» для последующей реактивации вируса. Во-вторых, недостаточная эффективность монотерапии аномальными нуклеозидами из-за сниженной активности клеточной тимидинкиназы диктуют необходимость разработки новых схем лечения с включением не менее двух препаратов, воздействующих на различные этапы жизненного цикла ВЭБ. В-третьих, низкая эффективность коротких курсов противовирусной терапии определяют целесообразность длительного этапного лечения с учетом способности клетки к выработке эндогенного ИФН. В-четвертых, значимая роль иммунной системы в элиминации ВЭБ-инфицированных клеток на этапе цитолитической инфекции, а также контроле за вирусом на этапе латентной инфекции свидетельствуют о необходимости включения в схемы лечения препаратов с иммунокорригирующей активностью. И, наконец, в-пятых, с учетом формирования полиорганной патологии в комплексное лечение больных ЭБВИ следует следует включать также средства патогенетической терапии.
В связи с этим требует уточнения ряд вопросов, касающихся лечения ЭБВИ. Во-первых, представляется целесообразным эффективное подавление репликации ВЭБ в цитолитическую стадию инфекции (первичная, реактивированная ЭБВИ, активная форма ХЭБВИ), что позволит уменьшить количество ВЭБ-инфицированных В-лимфо-цитов и, тем самым, сузить «плацдарм» для последующей реактивации вируса. Во-вторых, недостаточная эффективность монотерапии аномальными нуклеозидами из-за сниженной активности клеточной тимидинкиназы диктуют необходимость разработки новых схем лечения с включением не менее двух препаратов, воздействующих на различные этапы жизненного цикла ВЭБ. В-третьих, низкая эффективность коротких курсов противовирусной терапии определяют целесообразность длительного этапного лечения с учетом способности клетки к выработке эндогенного ИФН. В-четвертых, значимая роль иммунной системы в элиминации ВЭБ-инфицированных клеток на этапе цитолитической инфекции, а также контроле за вирусом на этапе латентной инфекции свидетельствуют о необходимости включения в схемы лечения препаратов с иммунокорригирующей активностью. И, наконец, в-пятых, с учетом формирования полиорганной патологии в комплексное лечение больных ЭБВИ следует следует включать также средства патогенетической терапии.
Целью лечения является уменьшение последствий ЭБВИ для организма ребенка, задачами — подавление репликации ВЭБ и ассоциантов, коррекция иммунного статуса, лечение полиорганной патологии.
Показания к назначению противовирусной терапии
■ Цитолитическая инфекция, высокая вирусная нагрузка в плазме крови, слизи ротоглотки, клетках крови (при использовании ПЦР в режиме реального времени).
■ Нарушения иммунного статуса.
■ Симптомы поражения жизненно важных внутренних органов.
При выборе этиотропного препарата необходимо учитывать механизм его противовирусной активности на этапах внеклеточного вириона, адсорбции и проникнове-
Таблица 2. Механизм противовирусного действия лекарственных препаратов
ния ВЭБ в клетку, синтеза вирусных белков, сборки и выхода зрелых вирионов (табл. 2).
В схемы лечения целесообразно включать препараты с комплексной этиотропной и патогенетической активностью. В этом плане предпочтительным представляется использование инозина пранобекс, обладающего противовирусной, иммуномодулирующей и цитопротективной активностью. Препарат подавляет репликацию ДНК- и РНК-содержащих вирусов за счет модификации стерео-химической структуры рибосом путем встраивания в них инозин-оротовой кислоты, что ведет к нарушению присоединения адениловой кислоты к вирусной РНК [2, 18]. Кроме того, инозин пранобекс повышает противовирусную резистентность клеток [19]. Препарат обладает им-мунокорригирующей активностью — модулирует иммунный ответ по клеточному типу за счет усиления диффе-ренцировки Т-хелперов и цитотоксических CD8-лимфо-цитов, продукции цитокинов (ИЛ-1, ИЛ-2, ИФНу), улучшения функциональной активности естественных киллер-ных клеток, макрофагов и нейтрофилов [2, 18]. Инозин пранобекс способствует дифференцировке В-лимфоци-тов в плазматические клетки, увеличивает продукцию антител, влияет на интерфероновый статус. Инозин пранобекс обладает цитопротективной активностью [18]. Известно, что инозин входит в состав пуриновых коэнзимов, АТФ, циклических нуклеотидов, в связи с чем препарат улучшает обменные процессы в пораженных вирусом клетках, оказывает противовоспалительное и антигипок-сическое действие.
Целью нашего исследования явилось совершенствование диагностики, лечения и реабилитации детей с острой и хронической ЭБВИ.
Обследованы следующие группы пациентов — 118 больных в возрасте от 1 до 14 лет с острым инфекционным мононуклеозом (первичная ЭБВИ — у 79 человек, реактивация ЭБВИ — у 39 человек), 168 детей в возрасте от 3 до 14 лет с ХЭБВИ (моно-инфекция — у 70 человек, микст-инфекции с хламидиозом — у 98 человек). В работе использован комплекс клинических, инструментальных, серологических, молекулярно-генетических, иммунологических и статистических методов.
С учетом важности эпидемиологических критериев диагностики исследован преморбидный фон пациентов. У всех детей с острым инфекционным мононуклеозом заболевание развивалось на неблагоприятном преморбид-ном фоне. Так, отягощенный акушерский анамнез имел место у 34,7% матерей, перинатальное поражение ЦНС — у 27,1% детей, частые ОРЗ — у 37,3%, хроническая ЛОР-патология — у 16,9%, сопутствующие герпесвирус-ные инфекции — у 69,5%, атопический дерматит — у 16,9%. Следует отметить, что дети с реактивацией ЭБВИ чаще имели возраст младше семи лет жизни по сравнению с больными с первичной ЭБВИ (76,9% и 53,2%, соответственно; P < 0,05). В этой группе у матерей чаще регистрировали отягощенный акушерский анамнез (51,3% и 26,5%, соответственно; P < 0,05), у детей — частые ОРЗ (51,3% и 30,4%, соответственно; P < 0,05), ЛОР-патологию (30,8% и 13,9%, соответственно; P < 0,05).
Клинически острый инфекционный мононуклеоз характеризовался острым началом — у 83,1% пациентов, лихорадкой — у всех больных, в том числе фебрильного характера — у 75,4% (табл. 3). Генерализованная лим-фаденопатия (ГЛАП) с преимущественным увеличением шейной группы выявлена у 1 00% детей. У всех пациентов при фарингоскопии обнаружен тонзиллит (катаральный — у 20,3%, лакунарный — у 50,8%, некротический — у 28,8%). У 67,8% больных имела место симптоматика аденоидита — затруднение носового дыхания при отсутствии выделений из носа, гнусавый оттенок голоса, храпящее дыхание во сне. У подавляющего большинства детей (89,8%) выявлена гепатомегалия. Край печени выступал на 1—5 см ниже реберной дуги по срединно-ключич-ной линии. Спленомегалия обнаружена у 48,3% пациентов. Край селезенки пальпировался на 1—3 см ниже реберной дуги. У 23,7% больных на 4—7 день болезни на коже появилась полиморфная розеолезная, пятнистая или пятнисто-папулезная сыпь без четкой локализации. Типичные изменения в гемограмме в виде лейкоцитоза, лимфоцитоза, моноцитоза, атипичных мононуклеаров выявлены у 64,4% пациентов. Негладкое течение инфекционного мононуклеоза с развитием осложнений имело место у 14,4% больных. К наиболее частым осложнениям относились гепатит (6,8%) и синусит (5,1%), к более редким — па-ратонзиллярный абсцесс (1,7%) и лимфаденит (0,8%).
У подавляющего большинства детей (89,8%) выявлена гепатомегалия. Край печени выступал на 1—5 см ниже реберной дуги по срединно-ключич-ной линии. Спленомегалия обнаружена у 48,3% пациентов. Край селезенки пальпировался на 1—3 см ниже реберной дуги. У 23,7% больных на 4—7 день болезни на коже появилась полиморфная розеолезная, пятнистая или пятнисто-папулезная сыпь без четкой локализации. Типичные изменения в гемограмме в виде лейкоцитоза, лимфоцитоза, моноцитоза, атипичных мононуклеаров выявлены у 64,4% пациентов. Негладкое течение инфекционного мононуклеоза с развитием осложнений имело место у 14,4% больных. К наиболее частым осложнениям относились гепатит (6,8%) и синусит (5,1%), к более редким — па-ратонзиллярный абсцесс (1,7%) и лимфаденит (0,8%).
Моно-инфекция ВЭБ диагностирована у 66,1 % детей, смешанная инфекция — у 33,9%. Из 40 пациентов со смешанной инфекцией клинико-лабораторные признаки активной формы герпесвирусных инфекций, вызванных вирусом простого герпеса 1-го и 2 типов, цитомегалови-русом, вирусом герпеса человека 6-го типа, выявлена у 42,5%, хламидийно-микоплазменной инфекции — у 25%, герпесвирусной и хламидийно-микоплазменной инфекции — у 32,5%. При бактериологическом обследовании мазков из ротоглотки у 41,5% пациентов выделены Streptococcus viridans, у 11,9% — Candida albicans, у 8,5% — Staphylococcus epidermidis, у 6,8% — Streptococcus pyogenes, у 3,4% — Klebsiella pneumoniae, у 41,5% — ассоциация различных бактерий.
Клиника острого инфекционного мононуклеоза при первичной и реактивированной формах ЭБВИ характе-
Этап жизненного цикла ВЭБ Группы препаратов
Внеклеточные вирионы В/в иммуноглобулины Цитокины Иммуномодуляторы
Адсорбция, проникновение в клетку Антиоксиданты Арбидол
Синтез ДНК Аномальные нуклеозиды
Синтез вирусных белков Инозин пранобекс ИФН, индукторы ИФН
Сборка вириона Антиоксиданты
Выход вирионов Антиоксиданты ИФН, индукторы ИФН
Таблица 3. Симптоматика острого инфекционного мононуклеоза с учетом формы заболевания
Показатели Первичная, ЭБВИ, n = 79 Реактивация, ЭБВИ, n = 39 Все больные, n = 118
n % n % n %
Острое начало 71 89,9 27 69,3* 98 83,1
Лихорадка 79 100 39 100 118 100
ГЛАП 79 100 39 100 118 100
Тонзиллит 79 100 39 100 118 100
Аденоидит 48 60,8 32 82,1* 80 67,8
Гепатомегалия 72 91,1 34 87,2 106 89,8
Спленомегалия 37 46,8 20 51,3 57 48,3
Экзантема 27 34,2 1 2,6* 28 23,7
Атипичные мононуклеары 13 16,4 3 7,7* 16 13,6
Осложнения 7 8,9 10 25,7* 17 14,4
Микст-инфекция 12 15,2 28 71,8* 40 33,9
* — достоверность различий показателей между группами больных с первичной и реактивированной ЭБВИ (р < 0,05)
ризовалась одинаковым набором симптомов. Однако, при первичной ЭБВИ чаще имели место острое начало заболевания, экзантема и атипичные мононуклеары в гемограмме, при реактивировации ЭБВИ — аденоидит, смешанные инфекции и осложнения.
При серологическом обследовании методом иммуно-ферментного анализа (ИФА) у 82,3% больных с первичной ЭБВИ обнаружены IgM к VCA-антигену ВЭБ, у 54,4% — IgG к EA- антигену вируса. У всех пациентов с реактивированной ЭБВИ выявлены IgM и IgG к VCA-, IgG к EA-, IgG к EBNA-антигенам ВЭБ, индекс авидности IgG более 50%.
При исследовании состояния иммунного статуса пациентов с первичной ЭБВИ обнаружены признаки активации иммунной системы в виде увеличения количества Т-лимфоцитов (CD3), цитотоксических CD8-лимфоцитов, маркеров поздних этапов активации иммунокомпетент-ных клеток (HLA-DR), повышение числа В-лимфоцитов (CD20), продукции IgA, IgM, IgG, активация кислород-зависимого метаболизма нейтрофилов по данным теста восстановления нитро-синего тетразолия (НСТ). Вместе с тем, имели место признаки угнетения иммунной системы — отсутствие увеличения Т-хелперов (CD4), снижение коэффициента CD4/CD8, уменьшение маркеров ранних этапов активации иммунокомпетентных клеток (CD25), повышение готовности к апоптозу (CD95), нарушение элиминации циркулирующих иммунных комплексов (ЦИК), снижение коэффициента стимуляции НСТ-теста (К ст. НСТ), количества естественных киллерных клеток (CD16).
При реактивации ЭБВИ признаки угнетения иммунной системы были более выраженными и заключались в снижении CD3-, CD4-лимфоцитов, умеренном увеличении числа CD8-клеток, значительном уменьшении коэффициента CD4/CD8. Более существенные изменение выявляли со стороны маркеров активации иммунокомпетентных клеток в виде умеренного повышения HLA-DR-позитивных лимфоцитов и уменьшения готовности к апоптозу (CD95). Сдвиги со стороны В-клеточного звена также были более выраженными и включали уменьшение содержания CD20-лимфоцитов, умеренное повышение продукции
IgA, IgG, значительное повышение содержания ЦИК. Особенностями показателей, характеризующих факторы врожденной резистентности, являлись выраженная редукция адаптационных возможностей кислород-зависимого метаболизма нейтрофилов (К ст. НСТ) и увеличение количества CD16-лимфоцитов.
Нами обследованы 168 детей с ХЭБВИ, в том числе в форме моно-инфекции — 70 человек (41,7%), микст-инфекции с хламидиозом — 98 пациентов (58,3%). Анализ преморбидного фона выявил наличие групп риска у всех пациентов. Достаточно часто регистрировалась патология беременности и родов у матерей, в том числе гестоз — у 25,6% женщин, угроза прерывания беременности — у 41,1%, хроническая внутриутробная гипоксия плода — у 38,7%, анемия — у 24,4%, стремительные роды — у 20,2%, преждевременные роды — у 11,9%, оперативные вмешательства — у 10,7% женщин. У обследованных детей имела место высокая частота фоновых состояний в периоде новорожденности. Так, у 13,1% пациентов диагностирована асфиксия, у 35,1% — затянувшаяся желтуха в периоде новорожденности. У 64,3% больных выявлены признаки перинатального поражения ЦНС, у 20,2% — врожденные пороки развития. Острые кишечные инфекции перенесли 36,3% пациентов. Клинически манифестные формы инфекции простого герпеса имели место у 1 1,3% детей, ветряная оспа — у 27,4%. Следует отметить, что лишь 36,3% детей в анамнезе имели указания на перенесенный острый инфекционный мононуклеоз. У 11,3% больных выявлены различные аллергические заболевания.
У больных с микст-ХЭБВИ имела место более высокая частота групп риска по сравнению с моно-ХЭБВИ, в том числе указаний в анамнезе на хроническую внутриутробную гипоксию плода во время беременности у матери (50% и 22,9%, соответственно; Р < 0,05), затяжную желтуху в периоде новорожденности (45,9% и 20%, соответственно; Р < 0,05), перинатальное поражение ЦНС (73,5% и 51,4%, соответственно; Р < 0,05), перенесенные острые кишечные инфекции (49% и 7,1%, соответ-
Таблица 4. Клиническая симптоматика хронической Эпштейна-Барр вирусной инфекции с учетом формы заболевания
Показатели Моно-ХЭБВИ, п = 70 Микст-ХЭБВИ, п = 98 Все больные, п = 168
П % П % п %
Интоксикационный синдром 53 75,7 77 78,6 130 77,4
Лимфопролиферативный синдром: 70 100 98 100 168 100
ГЛАП 70 100 98 100 168 100
Гипертрофия небных миндалин, в т.ч. 70 100 98 100 168 100
1 степени 39 55,7 50 51 89 53
2—3 степени 31 44,3 48 49 79 47
Гипертрофия глоточной миндалины, в т.ч. 49 70 72 73,4 121 72
1 степени 28 40 22 24,4* 50 29,8
2—3 степени 21 30 50 51* 71 42,2
Гепатомегалия 42 60 78 79,6* 120 71,4
Спленомегалия 30 42,9 64 65,3* 94 55,9
Респираторный синдром: 70 100 98 100 168 100
Ринофарингит 15 21,4 34 34,7* 49 29,2
Фаринготонзиллит 55 78,6 64 65,3* 119 70,8
Аденоидит 32 45,7 40 40,8 72 42,9
О. бронхит, о. обструктивный бронхит 9 12,9 49 50* 58 34,5
О.пневмония ? ? 10 10,2* 10 5,9
Церебральный синдром: 36 51,4 54 55,1 90 53,6
гипертензионно-гидроцефальный синдром 18 25,7 44 44,9* 62 36,9
синдром дефицита внимания с гиперактивностью 21 30 20 20,4 41 24,4
судорожный синдром 13 18,6 18 18,4 31 18,5
Вегето-висцеральный синдром 28 40 22 22,4* 50 29,8
Гастроинтестинальный синдром: 39 55,7 58 59,2 97 57,7
Аномалии развития ЖКТ 16 22,9 38 38,8* 54 32,1
Хронический гастрит 37 52,9 23 23,5* 60 35,7
Дискинезия желчевыводящих путей 15 21,4 18 18,4 33 19,6
Артралгический синдром 24 34,3 33 33,7 57 33,9
Кардиальный синдром 28 40 31 31,6 59 35,1
* — достоверность различий показателей у больных с моно- и микст-ХЭБВИ (р < 0,05)
ственно; Р < 0,05) и ветряную оспу (36,7% и 14,3%, соответственно; Р < 0,05).
Следует особо отметить значимость ХЭБВИ в формировании группы ЧБД, к которой относились все обследованные пациенты. Эпизоды ОРЗ возникали с частотой 8,3 ± ±0,3 раз в год и продолжались в среднем 1 1,9 ± 0,2 дней. Острые ринофаригиты развились 29,2% пациентов, фаринготонзиллиты — у 72%, аденоидиты — у 42,9%, бронхиты — у 38,1%, пневмонии — у 7,7%. Пациенты чаще относились к смешанному типу ЧБД (55,3%), реже — к соматическому (17,3%) и оториноларингологи-ческому типам (27,4%). Причем, у пациентов с микст-ХЭБВИ частота эпизодов ОРЗ (9,4 ± 0,3 раз в год) была более высокой, чем при моно-инфекции (7,2 ± 0,2 раз в год; P < 0,05), с более высокой частотой развивались острые ринофарингиты (34,7% и 21,4%, соответственно; Р < 0,05), бронхиты (50% и 19,9%, соответственно; Р < < 0,05), реже регистрировался острый фаринготонзиллит (67,7% и 78,6%, соответственно; Р < 0,05). В этой группе чаще диагностирован смешанный тип ЧБД (64,3% и 42,8% соответственно; P < 0,05).
При изучении клиники ХЭБВИ установлено, что у 77,4% больных имела место симптоматика интоксикационного синдрома — вялость, слабость, адинамия, снижение аппетита, субфебрилитет (табл. 4). У всех больных выявлен лимфопролиферативный синдром, который включал ГЛАП — у 100%, гипертрофию небных миндалин — у 100% (в том числе 1 степени — у 53%, 2—3 степени — у 47%), гипертрофию глоточной миндалины — у 72% (в том числе 1 степени — у 29,8%, 2—3 степени — у 42,2%), ге-патомегалию — у 71,4%, спленомегалию — у 55,9%. Край печени выступал на 1—3 см ниже края реберной дуги, край селезенки — на 0,5—2 см. Кроме того, клиническая картина ХЭБВИ включала разнообразную полиорганную патологию. У всех больных выявлено поражение респираторного тракта, в том числе острый ринофа-рингит — у 29,2%, фаринготонзиллит — у 70,8%, аденоидит — у 43%, острый бронхит, острый обструктив-ный бронхит — у 35,7%, острая сегментарная пневмония — у 5,9% детей. Церебральный синдром имел место у 53,6% пациентов и включал гипертензионно-гидроце-фальный синдром — у 36,9%, синдром дефицита внима-
ния с гиперактивностью — у 24,4%, судорожный синдром — у 18,5%, вегето-висцеральный синдром — у 29,8%. К симптоматике гастроинтестинального синдрома (57,7% больных) относились аномалии развития ЖКТ — у 32,1%, хронический гастрит — у 35,7%, дискинезия желчевыво-дящих путей — у 19,6% детей. Артралгический синдром выявлен у 33,9% пациентов, кардиальный синдром (боли в области сердца, сердцебиение, нарушение ритма) — у 35,1% детей. Осложнения имели место у 38,1% больных, в том числе отиты — у 19,6%, синуситы — у 1 6,7%, патология мочевыделительной системы (пиелонефрит, цистит) — у 13,1%, анемия — у 5,9%, дисбактериоз кишечника — у 5,9% пациентов.
У больных микст-ХЭБВИ с более высокой частотой, чем при моно-инфекции, регистрировались гипертрофия глоточной миндалины 2—3 степени, гепатомегалия, спле-номегалия, острый ринофарингит, простой бронхит, об-структивный бронхит, пневмония, гипертензионно-гидро-цефальный синдром, аномалии ЖКТ, осложнения. Особенностью симптоматики моно-ХЭБВИ являлась более высокая частота острого фаринготонзиллита, вегето-вис-церального синдрома и хронического гастрита.
При серологическом обследовании у всех детей обнаружены маркеры ХЭБВИ в стадии типичной и атипичной реактивации, в том числе IgM к VCA — у 100%, IgG к EA — у 89,3%, IgG к EBNA — у 100% больных. У пациентов с микст-ХЭБВИ выявлены серологические показатели активной формы хламидийной инфекции: антитела класса IgA — у 15,5%, IgM — у 13,1%, IgG — у 43,5% детей. При обследовании методом ПЦР у всех больных обнаружена ДНК ВЭБ, в том числе в плазме крови — у 61,9%, в слизи ротоглотки — у 75% детей.
При исследовании микробного пейзажа верхних дыхательных путей у 32,1% пациентов выделен Streptococcus pyogenes, у 29,2%, — Streptococcus viridans, у 17,3% — Staphylococcus aureus, у 5,4% — Staphylococcus epider-midis, у 3% — Pseudomonas aeruginosa, у 1,2% — Klebsiella pneumoniae, у 1,2% — Escherichia coli. При сопоставлении клинической симптоматики с учетом микробного пейзажа установлено, что у пациентов с выделением Streptococcus pyogenes чаще, чем у остальных пациентов, регистрировались синдром пленчатой ангины (90,7% и 72,8%, соответственно; Р < 0,05), гипертрофия небных и глоточной миндалин 3 степени (76,9% и 34,2%, соответственно; Р < 0,05), аденоидит (59,2% и 35,1%, соответственно; Р < 0,05), осложнения (59,3% и 28,1%, соответственно; Р < 0,05).
При исследовании иммунного статуса у пациентов с моно- и микст-ХЭБВИ выявлены однонаправленные изменения. Следует отметить более выраженные признаки активации иммунной системы при смешанной инфекции — более существенное увеличение CD8-лимфоцитов, HLA-DR-позитивных клеток, гиперпродукция IgA. Однако, у этих пациентов имели место также более существенные показатели угнетения иммунной системы — значительное снижение коэффициента CD4/CD8, нарушение элиминации ЦИК.
Диагностика ЭБВИ, таким образом, независимо от формы заболевания, должна проводиться с учетом дан-
ных эпидемического анамнеза, клинической картины и результатов лабораторного обследования. Важное значение имеет анализ групп риска в антенатальном и пост-натальном периодах, особенно указаний на повторные ОРЗ в анамнезе (группа ЧБД). Следует учитывать, что симптоматика острого инфекционного мононуклеоза (сочетание лихорадки, ГЛАП, тонзиллита, аденоидита, гепа-томегалии, спленомегалии, полиморфной сыпи, изменений в гемограмме) может быть результатом как первичной ЭБВИ, так и реактивации инфекционного процесса. Необходимо учитывать, что острый инфекционный моно-нуклеоз в качестве проявления первичной ЭБВИ чаще встречается у детей старше семи лет жизни, характеризуется острым началом заболевания, появлением сыпи и изменений в гемограмме. При реактивации ЭБВИ чаще выявляют анамнестические группы риска, с более высокой частотой развиваются аденоидит, смешанные инфекции и осложнения.
При диагностике ХЭБВИ также следует учитывать факторы риска, а также наличие у больного симптоматики хронического инфекционного мононуклеоза (синдрома хронической интоксикации, ГЛАП, гипертрофии небных и глоточной миндалин, гепатомегалии, спленомегалии) в сочетании с полиорганной патологией — поражением респираторного тракта, ЦНС, ЖКТ, опорно-двигательного аппарата. Причем, у большинства пациентов заболевание протекает в форме микст-инфекции в сочетании с различными ассоциантами, что накладывает отпечаток на клиническую симптоматику. В частности, у больных ХЭБВИ в сочетании с хламидийной инфекцией с более высокой частотой обнаруживают анамнестические группы риска, проявления лимфопролиферативного синдрома, поражение нижних отделов респираторного тракта, патологию ЦНС, ЖКТ, осложнения.
При выявлении анамнестических и клинических признаков ЭБВИ пациенты нуждаются в углубленном лабораторном обследовании. Методом ИФА определяют 1дМ и IgG к УСА-, IgG к ЕА-, IgG к EBNA-антигенам ВЭБ, индекс авидности IgG. С помощью метода ПЦР исследуют кровь и мазки из ротоглотки (предпочтительно исследовать титр вируса в плазме крови, лимфоцитах и слизи из ротоглотки методом ПЦР в режиме реального времени). В план обследования следует включать исследование иммунного статуса, с помощью которого выявляют признаки активации (чаще при первичной ЭБВИ, микст-ХЭБВИ) и/или угнетения иммунного ответа по клеточному, гуморальному типам, нарушение факторов врожденной резистентности (чаще при реактивации ЭБВИ, моно-ХЭБВИ).
Нами изучена эффективность включения инозина пра-нобекс в комплексную терапию острой и хронической ЭБВИ у детей. Препарат применяли по следующей схеме: детям старше трех лет с массой тела 15—20 кг в дозе 50 мг/кг/сут в 3—4 приема внутрь в течение 10 дней. Проводили три десятидневных курса с интервалом 10 дней.
Комплексная этиотропная терапия ЭБВИ включала следующие этапы.
Стартовая терапия (10 дней) — инозин пранобекс + ре-комбинантный ИФНа2Ь (ВИФЕРОН®) в полной дозе [20].
Поддерживающая терапия (4—8 недель) — повторные курсы инозина пранобекс + рекомбинантный ИФНа2Ь в поддерживающей дозе.
Закрепляющая терапия (с 5—9 недели) — индукторы ИФН.
В комплекс патогенетической терапии включали следующие группы препаратов:
Иммунокорригирующие препараты (на этапе закрепляющей этиотропной терапии),
Витаминно-минеральные комплексы, антиоксиданты, Пробиотики и пребиотики, Препараты метаболической реабилитации, Энтеросорбенты.
Препараты церебральной поддержки, ферменты, ге-патопротекторы и др. — по показаниям.
Для оценки эффективности комплексной терапии острой ЭБВИ методом случайной выборки больные были распределены на две группы, оказавшиеся сопоставимыми по клинико-лабораторным показателям. Пациенты первой группы (39 человек) получали инозин пранобекс в сочетании с рекомбинантным ИФН-а2Ь, дети второй группы (40 человек) — монотерапию рекомбинантным ИФН-а2Ь. Пациентов обследовали до начала лечение и через три месяца. У детей, получавших инозин прано-бекс, в моменту окончания исследования с меньшей частотой, по сравнению с контрольной группой, обнаруживали симптомы интоксикации (10,3% и 30%, соответственно; P < 0,05), ГЛАП (17,9% и 40%, соответственно; P < 0,05), тонзиллит (10,3% и 30%, соответственно; P < 0,05), аденоидит (5,1% и 22,5%, соответственно; P < 0,05), ге-патомегалию (7,7% и 27,5%, соответственно; P < 0,05), спленомегалию (0% и 15%, соответственно; P < 0,05), а также серологические маркеры активности ВЭБ — IgM к VCA- (0% и 15%, соответственно; P < 0,05) и IgG EA-ан-тигенам ВЭБ (19,3% и 45%, соответственно; P < 0,05). Назначение комплексной противовирусной терапии способствовало модуляции иммунного ответа по клеточному типу, о чем свидетельствовало увеличение CD3-, CD4-, CD8-, CD 16- и HLA-DR-лимфоцитов. Нормализовалась готовность иммунокомпетентных клеток к апоптозу (CD95). Отмечались положительные сдвиги со стороны В-клеточного звена — восстановление количества CD20-клеток, стимуляция выработки IgA, переключение синтеза антител с IgM на IgG, снижение содержания ЦИК. Повышалась интенсивность кислород-зависимого метаболизма нейтрофилов (НСТ сп.), происходило восстановление его адаптационных возможностей (К с. НСТ).
Эффективность комплексной терапии исследована также у 50 больных моно-ХЭБВИ, которые методом случайной выборки были распределены на две сопоставимые по клинико-лабораторым показателям на момент начала лечения группы. В первую группу вошли 24 ребенка, получавших инозин пранобекс в сочетании с рекомбинантным ИФН-а2Ь, во вторую группу — 26 человек, которым назначали только рекомбинантный ИФН-а2Ь. Сопоставляли клинико-лабораторные данные до начала лечения и через 12 месяцев. Установлено, что на фоне лечения инозином пранобекс к моменту окончания исследования реже регистрировали симптомы интоксикации
(8,3% и 42%, соответственно; P < 0,05), ГЛАП (12,5% и 62,5%, соответственно; P < 0,05), гипертрофию небных миндалин (75% и 100%, соответственно; P < 0,05), глоточной миндалины (41,6% и 70,8%, соответственно; P < 0,05), гепатомегалию (37,5% и 62,5%, соответственно; P < 0,05), спленомегалию (8,3% и 41,7%, соответственно; P < 0,05), фаринготонзиллит (25% и 75%, соответственно; P < 0,05), аденоидит (12,5% и 33,3%, соответственно; P < 0,05), осложнения (4,2% и 29,2%, соответственно; P < 0,05). Следует отметить, что назначение инозина пранобекс способствовало более существенному уменьшению частоты ОРЗ (3,2 ± 0,3 раз в год и 5,6 ± 0,4 раз в год, соответственно; P < 0,05) и их продолжительности (4,6 ± 0,3 дней и 8,8 ± 0,3 дней, соответственно; P < 0,05). ЕА-антигенам ВЭБ (8,3% и 45,8%, соответственно; P < 0,05). Использование инозина пранобекс приводило к нормализации показателей Т-клеточного звена (CD3, CD4) и активации иммунокомпетентных клеток (HLA-DR, CD95). Со стороны В-клеточного звена имело место восстановление количества CD20-лимфоцитов и продукции 1дМ, со стороны факторов врожденной резистентности — нормализация адаптационных возможностей кислород-зависимого метаболизма нейтрофилов (К ст. НСТ) и числа CD16-лимфоцитов.
Таким образом, оптимизация лечения ЭБВИ у детей заключается в использовании инозина пранобекс в сочетании со средствами патогенетической терапии, что способствует положительной динамике клинико-иммунологи-ческих и серологических показателей и является следствием противовирусной и иммунокорригирующей активности препарата.
Больные ЭБВИ нуждаются в длительном диспансерном наблюдении, реализации комплекса реабилитационных мероприятий под контролем клинико-лабораторных показателей. Диспансерное наблюдение должно проводиться педиатром и инфекционистом с привлечением, по показаниям, других специалистов. Ориентировочная кратность контроля клинических, лабораторных (гемограмма, биохимический анализ крови, ИФА, ПЦР, имму-нограмма), инструментальных данных (УЗИ, ЭКГ, доппле-рометрия и др.) — один раз в три месяца, по показаниям — чаще. Реабилитационная терапия должна включать поддерживающие курсы противовирусных препаратов, патогенетическую терапию (иммунокорригирующие препараты, витаминно-минеральный комплексы, пробиотики, пребиотики, препараты метаболической реабилитации, энтеросорбенты и др.). Диспансерное наблюдение продолжают до шести месяцев стойкой ремиссии.
Выводы
1. Широкое эпидемическое распространение, имму-нодепрессивная активность возбудителя, неблагоприятные последствия ЭБВИ для организма ребенка диктуют необходимость совершенствования диагностики и лечения заболевания.
2. Для своевременной диагностики ЭБВИ необходим комплексный анализ данных анамнеза, клинической симптоматики, включающей проявления острого и хрони-
ческого мононуклеозоподобного синдрома в сочетании с полиорганной патологией, а также результаты лабораторного обследования (ИФА, ПЦР, иммунограмма).
3. Больные ЭБВИ нуждаются в проведении комплексного лечения и этапной реабилитации с использованием препарата с противовирусной и иммуномодулирующей активностью инозина пранобекс, средств сопроводительной терапии под контролем клинико-лабораторных показателей.
Литература/References:
1. Боковой А.Г., Егоров А.И. Герпесвирусные инфекции у детей и родителей. — М.: Центр стратегической конъюнктуры, 2014. — 256 с.
Bokovoj A.G., Egorov A.I. Gerpesvirusnye infekcii u detej i roditelej [Herpesvirus infections in children and parents] — M.: Centr strate-gicheskoj konjunktury, 2014. — 256 s. (In Russ.)
2. Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека. — СПб.: Спецлит, 201 3. 670 с.
Isakov V.A., Arhipova E.I., Isakov D.V. Gerpesvirusnye infekcii cheloveka. [Human herpesvirus infections]. — SPb.: Speclit, 2013. 670 s. (In Russ.)
3. Барычева Л.Ю. Голубева М.В., Волкова А.В. Факторы и механизмы иммуносупрессии при Эпштейна-Барр вирусной инфекции // Детские инфекции. 2014. №2. С. 28—33. Barycheva L.Ju. Golubeva M.V., Volkova A.V. Faktory i mehanizmy immunosupressii pri Jepshtejna-Barr virusnoj infekcii [Factors and mechanisms of immunosuppression by Epstein-Barr virus infection] // Detskie Infekcii. 2014. №2. S. 28—33. (In Russ.)
4. Кудин А.П. Эта «безобидная» вирус Эпштейна-Барра инфекция. Часть 1. Характеристика возбудителя. Реакция иммунной системы на вирус // Медицинские новости. 2006. №7. http: // www.mednovosti.by.
Kudin A.P. Jeta «bezobidnaja» virus Jepshtejna-Barra infekcija. Chast 1. Harakteristika vozbuditelja. Reakcija immunnoj sistemy na virus [This «harmless» Epstein-Barr virus infection. Part 1. Characteristics of the pathogen. The reaction of the immune system to the virus] // Medicinskie Novosti. 2006. №7. http: // www.mednovos-ti.by. (In Russ.)
5. Human herpesviruses / Ed. by A. Arvin, G. Campadelli-Fiume, E. Mocarski et al. Cambrige, Cambrige University Press, 2007. http // www.ncbi.nlm.nih.gov / books / NBK 47376.
6. Raab-Traub N. Novel mechanisms of EBV induced oncogenesis // Curr. Opin. Virol. 2012. Vol. 2, N 4. P. 453—458.
7. Бабаченко И.В., Кветная А.С., Мельник О.В., Левина А.С. Патогенез формирования частых респираторных заболеваний у детей с Эпштейна-Барр вирусной и цитомегаловирусной инфекцией // Журнал инфектологии. 2011. №4. С. 67—42. Babachenko I.V., Kvetnaja A.S., Melnik O.V., Levina A.S. Patogen-ez formirovanija chastyh respiratornyh zabolevanij u detej s Jepsht-ejna-Barr virusnoj i citomegalovirusnoj infekciej [The pathogenesis of the formation of frequent respiratory infections in children with Epstein-Barr virus and cytomegalovirus infections] // Zhurnal Infek-tologii. 2011. №4. S. 67—42. (In Russ.)
8. Полтавцева Т.В., Каражас Н.В., Калугина М.Ю., Мамедова Е.А. и др. Диагностика герпесвирусной инфекции у детей раннего возраста // Детские инфекции. 2012. №2. С. 51—53. Poltavceva T.V., Karazhas N.V., Kalugina M.Ju., Mamedova E.A. i dr. Diagnostika gerpesvirusnoj infekcii u detej rannego vozrasta [Diagnosis of herpesvirus infection in young children] // Detskie In-fekcii. 2012. №2. S. 51—53. (In Russ.)
9. Денисенко В.Б., Симованьян Э.Н., Саухат С.Р., Колпаков Д.С. и др. Эпштейна-Барр вирусная инфекция у детей с ВИЧ-инфекцией // Материалы X Конгресса детских инфекционистов России «Актуальные вопросы инфекционной патологии и вакцинопро-филактики». — М., 2011. С. 31.
Denisenko V.B., Simovanyan E.N., Sauhat S.R., Kolpakov D.S. i dr. Jepshtejna-Barr virusnaja infekcija u detej s VICH-infekciej [Epstein-
Barr virus infection in children with HIV infection] // Materialy X Kongressa detskih infekcionistov Rossii «Aktualnye voprosy infek-cionnoj patologii i vakcinoprofilaktiki» [Materials of X Congress of Russian childrens infectionists «Actual problems of infectious disease and vaccine prevention»]. — M., 2011. S. 31. (In Russ.)
10. Tracy S.I., Kakalacheva K., Lunemann J.D., Luzuriaga K. et al. Persistence of Epstein-Barr virus in self-reactive memory B cells // J. Virol. 2012. Vol. 88, N 22. P. 12330—12340.
11. Харламова Ф.С., Егорова Н.Ю., Гусева Л.Н. Вирусы семейства герпеса и иммунитет // Детские инфекции. 2006. №3. С. 3—9. Harlamova F.S., Egorova N.Ju., Guseva L.N. Virusy semejstva ger-pesa i immunitet [Viruses herpes family and immunity] // Detskie Infekcii. 2006. №3. S. 3—9. (In Russ.)
12. Хмилевская С.А. Эпштейна-Барр вирусный мононуклеоз у детей: клинико-патогенетические аспекты, критерии диагностики, тактика терапии и диспансеризации различных вариантов течения заболевания: Автореф. дис. … докт. мед. наук. — Саратов, 2010. 50 с.
Hmilevskaja S.A. Jepshtejna-Barr virusnyj mononukleoz u detej: kliniko-patogeneticheskie aspekty, kriterii diagnostiki, taktika terapii i dispanserizacii razlichnyh variantov techenija zabolevanija [Epstein-Barr virus mononucleosis in children: clinical and pathoge-netic aspects, criteria for diagnosis, therapy tactics and medical examination of the different variants of the disease]: Avtoreferat dis-sertacii na soiskanie uchenoj stepeni doktora medicinskih nauk [Abstract of dissertation for the degree of Doctor of Medical Sciences]. — Saratov, 2010. 50 s. (In Russ.) 1 3. Юлиш Е.И. Персистирующие инфекции и человек. Стратегия взаимоотношений // Здоровье ребенка. 2009. №4. С. 1 14— 122.
Julish E.I. Persistirujushhie infekcii i chelovek. Strategija vzaimoot-noshenij [Persistent infection and people. The strategy of mutual relations] // Zdorovie Rebenka. 2009. №4. S. 1 14—122. (In Russ.)
14. Малашенкова И.К., Дидковский Н.А., Сарсания Ж.Ш., Жарова Е.Н. и др. Клинические формы хронической Эпштейна-Барр вирусной инфекции: вопросы диагностики и лечения // Лечащий врач. 2003. №9. С. 32—38.
Malashenkova I.K., Didkovskij N.A., Sarsanija Zh.Sh., Zharova E.N. i dr. Klinicheskie formy hronicheskoj Jepshtejna-Barr virusnoj infekcii: voprosy diagnostiki i lechenija [The clinical forms of chronic Epstein-Barr virus infection: diagnosis and treatment issues] / / Le-chashhij Vrach. 2003. №9. S. 32—38. (In Russ.)
15. Савенкова М.С., Савенков М.П., Абрамова Н.А., Красева Г.Н. Правильно ли мы выбираем имуномодуляторы для лечения часто болеющих детей? // Педиатрия. Приложение к журналу Consilium Medicum. 2014. №1. С. 96—99.
Savenkova M.S., Savenkov M.P., Abramova N.A., Kraseva G.N. Pravil’no li my vybiraem imunomoduljatory dlja lechenija chastj bolejushhih detej? [Do we choose to treat imunomodulyatory for frequently ill children?] // Pediatrija. Prilozhenie k zhurnalu Consilium Medicum. 2014. №1. S. 96—99. (In Russ.)
16. Гусева Л.Н., Егорова Н.Ю., Гусева Н.А., Фомичева Е.А. и др. Лечение Эпштейна-Барр вирусного мононуклеоза у детей на современном этапе // Детские инфекции. 2010. №3. С. 57— 60.
Guseva L.N., Egorova N.Ju., Guseva N.A., Fomicheva E.A. i dr. Lechenie Jepshtejna-Barr virusnogo mononukleoza u detej na sovremennom jetape [Treatment of Epstein-Barr virus mononucleosis in children at the modern stage] // Detskie Infekcii. 2010. №3. S. 57—60. (In Russ.)
17. Oertel S.H., Riess H. Antiviral treatment of Epstein-Barr virus associated lymphoproliferations // Recent. Results Cancer. 2002. Vol. 159. P. 89—95.
18. Булгакова В.А. Противовирусная терапия острых респираторных инфекций у детей // Здоровье ребенка. 2014. №2. С. 78—84.
Bulgakova V.A. Protivovirusnaja terapija ostryh respiratornyh infekt-cij u detej [Antiviral therapy of acute respiratory infections in children] // Zdorov’e Rebenka. 2014. №2. S. 78—84. (In Russ.)
Эпштейн—Барр вирусная инфекция у детей
SOVREMENNAYA PEDIATRIYA.2015.4(68):103-110; doi 10.15574/SP.2015.68.103
Эпштейн—Барр вирусная инфекция у детей
Волоха А. П.
Национальная медицинская академия последипломного образования имени П.Л. Шупика, г. Киев, Украина
Вирус Эпштейн—Барр (EBV) — чрезвычайно распространенный в популяции вирус, возбудитель инфекционного мононуклеоза, персистирует бессимптомно на протяжении всей жизни у инфицированных лиц. В отличие от других герпесвирусов, реактивация EBV не имеет существенного значения в клинической практике, за исключением иммуноскомпрометированных пациентов (Х-сцепленный лимфопролиферативный синдром, иммуносупрессия после трансплантации), у которых развиваются лимфопролиферативные заболевания. Вирус Эпштейн—Барр ассоциируется с развитием злокачественных опухолей. Первичная EBV-инфекция обычно бессимптомная у детей раннего возраста, в старшем возрасте протекает с классическими симптомами: лихорадка, фарингит, лимфаденопатия. Выздоровление полное через несколько недель после начала заболевания. Основой лечения EBV-индуцированного инфекционного мононуклеоза является симптоматическая терапия. Назначение противовирусных препаратов и кортикостероидов в лечении первичной EBV-инфекции остается дискутабельным и в целом не рекомендуется.
Ключевые слова: вирус Эпштейн—Барр, инфекционный мононуклеоз, дети.
Литература:
1. Candy B, Hotopf M. 2006. Steroids for symptom control in infectious mononucleosis. Cochrane Database Syst Rev. 3: CD004402. http://dx.doi.org/10.1002/14651858.cd004402.pub2
2. Carbone A, Gloghini A, Dotti G. 2008. EBV-Associated lymphoproliferative disorders: classification and treatment. The Oncologist. 13: 577—585. http://dx.doi.org/10.1634/theoncologist.2008-0036; PMid:18515742
3. Centers for Disease Control and Prevention, National Center for Infectious Diseases. Epstein—Barr virus and infectious mononucleosis. Updated May 16, 2006. http://www.cdc.gov/ncidod/diseases/ebv.htm. Accessed December 20, 2011.
4. Ebell MH. 2004. Epstein—Barr virus infectious mononucleosis. Am Fam Physician. 70(7): 1279—1287. PMid:15508538
5. Hellwig T, Jude K, Meyer B. 2013. Management options for infectious mononucleosis. US Pharmacist. 38(5): 38—41.
6. Macsween KF, Higgins CD, McAulay KA et al. 2010. Infectious mononucleosis in university students in the United Kingdom: evaluation of the clinical features and consequences of the disease. Clinical Infectious Diseases. 50: 699—706. http://dx.doi.org/10.1086/650456; PMid:20121570
7. Johanssen EC, Kaye KM. 2010. Epstein—Barr virus (Infectious mononucleosis, Epstein—Barr virus_associated malignant diseases, and other diseases). Douglas and Bennett’s Principles and Practice of Infectious Diseases. Mandell GL, Bennett JE, Dolin R Mandell. 7th Ed. Churchill Livingstone Elsevier: 1989—2010.
8. Junker AK. 2005. Epstein—Barr virus. Pediatrics in review. 26(3): 79—85. http://dx.doi.org/10.1542/pir.26-3-79; PMid:15743754
9. Katz BZ. 2008. Epstein—Barr virus (mononucleosis and lymphoproliferative disorders). Principles and Practice of Pediatric Infectious Diseases. Long SS, Pickering LK, Prober CG. Churchill Livingstone: 1036—1044.
10. Luzuriaga K, Sullivan JL. 2010. Infectious mononucleosis. N Engl J Med. 362;7: 1993-2000. http://dx.doi.org/10.1056/NEJMcp1001116; PMid:20505178
11. Odumade OA. 2011. Progress and problems in understanding and managing primary Epstein—Barr virus infections. Clin Microbiology review. 24(1): 193—209. http://dx.doi.org/10.1128/CMR.00044-10; PMid:21233512 PMCid:PMC3021204
12. Paschale M, Clerici P. 2012. Serological diagnosis of Epstein—Barr virus infection: Problems and solutions. World J Virol. 1(1): 31—43. http://dx.doi.org/10.5501/wjv.v1.i1.31; PMid:24175209 PMCid:PMC3782265
13. Rezaei N, Hedayat M, Aghamohammadi A, Nichols KE. 2011. Primary immunodeficiency diseases associated with increased susceptibility to viral infections and malignancies. J Allergy Clin Immunol. 127: 1329—41. http://dx.doi.org/10.1016/j.jaci.2011.02.047; PMid:21514636
14. Kimura H, Morishima T, Kanegane H et al. 2003. Prognostic factors for chronic active Epstein—Barr Virus infection. The Journal of Infectious Diseases. 187: 527—33. http://dx.doi.org/10.1086/367988; PMid:12599068
15. Sumaya CV. 2009. Epstein—Barr virus. Textbook of Pediatric Infectious Diseases. RD Feigin, JD Cherry. 4th Ed. Philadelphia, W.B. Saunders: 1751—1762.
16. Valachis A, Kofteridis DP. 2012. Mononucleosis and Epstein—Barr virus infection: treatment and medication. Virus Adaptation and Treatment. 4: 23—28.
17. Williams H, Crawford DH. 2006. Epstein—Barr virus: the impact of scientific advances on clinical practice. Blood. 107: 862—869. http://dx.doi.org/10.1182/blood-2005-07-2702; PMid:16234359
Какого ребенка считать часто болеющим, и чем ему грозит вирус Эпштейна-Барр?
Буквально каждая вторая современная мама, словно мантру, заучила формулировку «часто болеющий ребенок», но что это значит, известно не всем. Почему он часто болеет, чем это грозит, и что за странные анализы назначают врачи? Такие вопросы нередко рождаются в головах испуганных родителей.
Пролить свет истины на эту тему пресс-службе Интернет-Портала NEDUGAMNET.RU помогла Ксения Борисовна Степанова, к.м.н., врач-инфекционист, заведующий клиникой ФБУН «Тюменский научно-исследовательский институт краевой инфекционной патологии».
Для начала Ксения Борисовна рассказала о том, в каких случаях можно с уверенностью сказать, что ребенок болеет слишком часто.
«Если ребенок возрастом до 3 лет болеет 5-6 раз – это норма, для ребенка 5-14 в норме болеть не более 4 раз в год. Однако это справедливо лишь для случаев, когда дети болеют без осложнений.
Когда болеют пять раз легкими простудами, это одна ситуация, которая не так страшна, чем когда ребенок за год все 4 раза подхватывал тяжелые инфекционные заболевания, а итогом стали осложнения: гайморит, аденоиды, менингит и т.д. В последнем случае вероятность иммунодефицита очень высока», – пояснила врач-инфекционист.
Также она уточнила, что причина частых заболеваний у ребенка кроется в неадекватном иммунном ответе на внедрение инфекционного агента. Причиной такого неадекватного ответа иммунной системы могут быть как паразиты, так и хронические вирусные инфекции, в том числе вирус Эпштейна-Барр.
Анализ на выявление этого вируса в организме могут назначить часто болеющему ребенку, что нередко пугает родителей.
«Эпштейна-Барр (ВЭБ) – вирус герпеса, который впервые был обнаружен у больного с онкопатологией (лимфома Беркитта) 35 лет назад. Может стать причиной как острых инфекционных заболеваний (например, инфекционного мононуклеоза, так и хронического течения данной инфекции. Также ВЭБ может приводить к ряду онкологических и аутоиммунных заболеваний.
ВЭБ может пожизненно находится в организме человека, поражая b-лимфоциты иммунной системы, которые в основном находятся в миндалинах. По этой причине во внешнюю среду вирус выделяется чаще всего со слюной.
Врожденная Эпштейна-Барр-вирусная инфекция, пожалуй, дает самые серьезные осложнения – ребенок изначально рождается с различными патологиями: с гепатитом С, энцефалитом, различными повреждениями кожного покрова. Хотя такие случаи редки в медицинской практике.
Самое типичное проявление вируса Эпштейна-Барр – это инфекционный мононуклеоз, острое инфекционное заболевание, которое протекает с выраженной интоксикацией, с поражением лимфатических узлов, возможным увеличением печени, селезенки и даже развитием в тяжелых случаях острого гепатита.
Хроническая Эпштейна-Барр-вирусная инфекция характеризуется длительным рецидивирующим течением и наличием признаков вирусной активности (боли в мышцах, суставах, высыпания, затрудненное дыхание, боли в горле, головные боли, часто наблюдается субфебрильная температура).
У лиц с выраженной иммунной недостаточностью могут возникнуть генерализованные формы ВЭБ-инфекции с развитием менингита и энцефалита, а также миокардита. Для ВЭБ-инфекции характерно развитие анемии и панцитопении (снижается уровень лейкоцитов и тромбоцитов).
Диагностика ВЭБ-инфекции достаточно сложна и трудоемка, диагноз может поставить только врач-инфекционист после проведения анализов – исследования крови или мочи (ИФА и ПЦР)», – пояснила Ксения Борисовна.
Она отметила, что есть несколько категорий пациентов среди детского населения, которым рекомендовано сдавать анализ на выявление вируса:
· пациенты с частыми респираторными заболеваниями, с любыми иммунодефицитными состояниями;
· дети с долговременной температурой субфебрильного характера либо жалобами на беспричинное повышение температуры тела;
· дети с увеличенными лимфоузлами;
· пациенты с отклонениями в общем анализе крови;
· пациенты, у которых обнаруживаются неустановленные заболевания печени;
· все пациенты с диагнозом ВИЧ;
· все, кто перенес пересадку органов или переливания крови и ее компонентов.
«У этого вируса нет сезонности, он распространен повсеместно, передается воздушно-капельным путем. Также вирус Эпштейна-Барр называют «болезнью поцелуев» или «студенческой болезнью», потому как этим заболеванием можно заразиться в том числе контактно-бытовым путем, через слюну.
Лечение требуется как острой инфекции, так и хронической, но в определенной стадии заболевания. Подход к лечению строго индивидуальный с подбором противовирусной терапии. Учитывается возраст пациента, длительность течения заболевания и клиническая картина. Иногда при хронической ВЭБ-инфекции пациент вынужден наблюдаться у специалистов длительное время и даже пожизненно», – рассказала врач-инфекционист Ксения Борисовна Степанова.
Информация подготовлена по материалам сайта http://www.nedugamnet.ru
Ссылка на интервью: http://nedugamnet.ru/kakogo-rebenka-schitat-chasto-boleyushchim-i-chem-emu-grozit-virus-epshteyna-barrЭффективность применения инозина пранобекс у часто болеющих детей с хронической Эпштейна–Барр вирусной инфекцией: результаты рандомизированного исследования | Симованьян
1. Альбицкий В.Ю., Баранов А.А., Камаев И.А., Огнева М.Л. Часто болеющие дети. Н. Новгород: НГМА. 2003. 180 с.
2. Намазова Л.С., Ботвиньева В.В., Торшхоева Р.М. и др. Лечение и профилактика острых респираторных инфекций у часто болеющих детей, проживающих в мегаполисах. Детские инфекции. 2007; 2: 49–52.
3. Самсыгина Г.А., Коваль Г.С. Часто болеющие дети: проблемы диагностики, патогенеза и терапии. Лечащий врач. 2009; 1: 10–15.
4. Нестерова И.В. Проблемы лечения вирусно-бактериальных респираторных инфекций у часто и длительно болеющих иммунокомпрометированных детей. Лечащий врач. 2009; 6: 26–29.
5. Учайкин В.Ф. Рецидивирующие респираторные инфекции у детей: применение иммуномодуляторов для лечения и профилактики. Педиатрия. 2009; 1: 127–132.
6. Иванова В.В., Шилова И.В., Симованьян Э.Н. и др. Новые данные об инфекционном мононуклеозе у детей. Российский вестник перинатологии и педиатрии. 2006; 6: 44–51.
7. Бабаченко И.В., Левина А.С., Седенко О.В. и др. Эффективность различных методов этиологической диагностики у часто болеющих детей с хронической Эпштейна–Барр и цитомегаловирусной инфекциями. Здоровье. Медицинская экология. Наука. 2009; 2: 13–15.
8. Сарычев А.М. Особенности клинических проявлений и иммунопатогенеза хронической Эпштейна–Барр вирусной инфекции. Автореф. дис. … канд. мед. наук. Ростов–на–Дону. 2004. 26 с.
9. Боковой А.Г. Герпесвирусные инфекции у детей. М.: Макс–Пресс. 2008. 144 с.
10. Краснова Е.И., Васюнин А.В. Инфекционный мононуклеоз у детей: Руководство. Новосибирск. 2007. 95 с.
11. Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека. СПб.: Спецлит. 2006. 303 с.
12. Бадальянц Э.Е. Клинико-иммунологическая характеристика респираторных инфекций у часто болеющих детей и эффективность иммунокорригирующей терапии. Автореф. дис. … канд. мед. наук. Ростов–на–Дону. 2009. 24 с.
13. Булгакова В.А., Балаболкин И.И., Ханова Н.И. и др. Применение изопринозина (инозин пранобекс) для профилактики и лечения респираторных инфекций у детей. М. 2010. 19 с.
14. Осидак Л.В., Зарубаев В.В., Образцова Е.В. и др. Изопринозин в терапии ОРВИ у часто болеющих детей. Детские инфекции. 2008; 4: 35–41.
15. Эрман Е.С. Оценка клинико-эпидемической эффективности новых средств для профилактики гриппа и ОРИ другой этиологии у часто болеющих детей. Автореф. дис. …канд. мед. наук. М. 2009. 24 с.
Клинические формы вирусной инфекции Эпштейна — Барр | Понежева Ж.Б., Гришаева А.А., Попова Т.И.
В статье приведены современные представления об особенностях иммунопатогенеза, диагностики и терапии вирусной инфекции Эпштейна — Барр в зависимости от фазы заболевания и клинических форм. Представлены клинические примеры острой и хронической инфекции
АктуальностьОдной из актуальных проблем современной медицины является высокая заболеваемость герпесвирусными инфекциями, которые достаточно широко распространены в человеческой популяции. Сложная по сравнению с другими ДНК-содержащими вирусами структура генома вирусов семейства герпеса обусловливает основные различия в их репликативном цикле. Гены, кодирующие структурные белки, составляют у герпесвирусов всего лишь 15% ДНК, большую же часть генома составляют участки, ответственные за синтез регуляторных протеинов и ферментов, и именно эта особенность позволяет им реализовывать совершенно уникальную программу, включающую возможность латентного, персистентного и реактивированного состояния в инфицированном организме [1].
Особое место среди герпесвирусов занимает Эпштейна — Барр вирус (ЭБВ), которым инфицировано 95% населения и, как и все герпесвирусы, он способен поражать практически все органы и системы организма, вызывая латентную, острую и хроническую формы инфекции, склонные к реактивации в условиях иммуносупрессии. Активная пролиферация вируса во всех органах и системах, имеющих лимфоидную ткань, приводит к структурным изменениям, оказывающим неблагоприятное воздействие на организм в целом. Доказана ключевая роль ЭБВ в развитии таких заболеваний, как острый, хронический мононуклеоз, интерстициальный пневмонит, миокардит, гепатит, опухоли лимфоидной и эпителиальной тканей, гемофагоцитарный лимфогистиоцитоз, лейкоплакия языка и посттрансплантационные лимфопролиферативные осложнения.
Проявления ЭБВИНаиболее известным и изученным проявлением Эпштейна — Барр вирусной инфекции (ЭБВИ) является инфекционный мононуклеоз (ИМ). В настоящее время неясны иммунопатологические основы индивидуальных различий течения ИМ и его исходов. Клинические проявления, диагностика и лечение ИМ представлены в таблице 1.
Метаанализ 5 рандомизированных плацебо-контролируемых испытаний с участием 339 больных показал отсутствие эффекта от ацикловира у больных ИМ ЭБВ этиологии [5].
ЭБВ обладает множественными механизмами иммуносупрессии и ускользания от иммунного ответа в организме человека, что может приводить к формированию хронической ЭБВИ (ХЭБВИ) [6], в ходе которой иммунологические нарушения усугубляются, подавляется продукция интерферонов, блокируются механизмы апоптоза, что формирует вторичный иммунодефицит, способствующий развитию аутоиммунных и опухолевых процессов у генетически предрасположенных лиц.
Клинические формы ХЭБВИ представлены в таблице 2.
Накоплено немало данных об этиологической роли ЭБВ в формировании синдрома хронической усталости, развитии системных васкулитов, специфического колита, имеются данные о триггерной роли ЭБВ в развитии рассеянного склероза и системной красной волчанки [15, 16].
Описаны такие кожные проявления ХЭБВИ, как гиперчувствительность к укусам комаров и световая оспа (Hydroa vacciniforme, HV) (см. табл. 2). Световая оспа — заболевание, характеризующееся развитием поэтапной полиморфной некротической сыпи на участках кожи, подверженных солнечному облучению. Заболевание зачастую носит семейный характер, однако у ряда пациентов при гистохимическом анализе поражений кожи имеет место инфильтрация Т-клетками, экспрессирующими малую РНК, кодируемую ЭБВ. Совпадение наличия ХЭБВИ и световой оспы (HV) может перерасти в развитие злокачественной лимфомы, которая была включена в классификацию ВОЗ 2008 г. как HV-подобная лимфома [14].
Активная ЭБВИ (см. табл. 2) может служить триггером для развития идиопатической тромбоцитопенической пурпуры [17] — аутоиммунного гематологического заболевания, в основе которого лежит тромбоцитопения с развитием геморрагического синдрома. Характерными признаками данного заболевания являются множественные, полиморфные кровоизлияния в кожный покров и слизистые оболочки, а также кровотечения различной локализации (нос, десны и др.).
Гемофагоцитарный лимфогистиоцитоз (ГЛГ) — одно из наиболее опасных, жизнеугрожающих осложнений ЭБВИ, основными симптомами которого являются: лихорадка, рефрактерная к антимикробной терапии, геморрагический и отечный синдромы, желтуха, экзантема, гепатоспленомегалия, симптомы поражения центральной нервной системы (возбудимость, угнетение сознания, судороги, менингеальные знаки) [18]. Развитие ГЛГ сопряжено с расстройством иммунной регуляции в результате бесконтрольной активации и пролиферации макрофагов и Т-клеток, что проявляется избыточной продукцией цитокинов, воспалением и повреждением тканей. Выделяют первичный ГЛГ, характеризующийся наличием семейного анамнеза и определенного генетического дефекта, и вторичный ГЛГ, ассоциированный с инфекцией, аутоиммунными и онкологическими заболеваниями, а также иммунодефицитным состоянием [19].
Доказана ключевая роль ЭБВ в развитии лимфопролиферативных заболеваний. Одной из ключевых лимфом, ассоциированных с ВЭБ, считается лимфома Беркитта [20]. Клиническими проявлениями лимфом служат увеличение лимфатических узлов, спленомегалия, цитопения, лихорадка. Считается, что наличие латентной ЭБВИ в эпителии носоглотки является ранней стадией патогенеза недифференцированной назофарингеальной карциномы [21].
Критерии и методы диагностики ЭБВИДиагностика ЭБВИ сложна и не всегда возможна в рутинной практике клинициста. Критериями диагностики ИМ ЭБВ-этиологии являются клинико-лабораторные данные (см. табл. 1). При этом оценка результатов серологического обследования имеет некоторые особенности. Так, не всегда первоначальная продукция IgM к VCA предшествует выработке антител класса IgG к VCA, возможно одновременное появление или полное отсутствие их выработки при иммуносупрессии у пациента с ЭБВИ. Может наблюдаться длительная (более 3–4 мес.) персистенция IgM к VCA (паст-инфекция). Наличие IgG к ранним антигенам (EA) не всегда свидетельствует о ранней стадии инфекции, они могут выявляться у 70% больных острым ИМ и у большинства здоровых доноров, а также при реактивации ЭБВИ [22, 23].
Методом ПЦР определяют ДНК ЭБВ в крови или другом биологическом материале (слюна, мазки из ротоглотки), а при необходимости и в биоптатах печени, лимфоузлов, слизистой кишечника и т. д.), но качественный анализ не позволяет в клинической практике отличить здоровое носительство от активной репликации вируса. В связи с этим некоторые исследователи указывают на необходимость использования количественного варианта ПЦР [3, 22, 23], при этом определение в пробе 10 копий ДНК ЭБВ (1000 ГЭ/мл в 1 мл образца) характеризуется как здоровое носительство, а выявление 100 и более копий (10000 ГЭ/мл в 1 мл образца) указывает на активную фазу ЭБВИ.
Критериями диагностики ХЭБВИ являются признаки инфицирования более 6 мес.: лихорадка, лимфаденопатия и спленомегалия (мононуклеозоподобный синдром), выраженное повышение титров антител к антигену вирусного капсида ЭБВ (VCA ≥ 1:5120) или ранним антигенам (EA ≥1:640), обнаружение ДНК ЭБВ в крови, ДНК, мРНК или белков вируса в пораженных тканях в отсутствие другой причины иммуносупрессии [23, 24]. Важно помнить о возможном отсутствии IgM при нарастании титров IgG к вирусным белкам.
Дополнительную информацию о течении инфекции можно получить с помощью иммуноблота. Иммуноблоттинг — это высокоспецифичный и высокочувствительный референтный метод, с помощью которого определяют широкий спектр вирусспецифических белков (р125, р65, р42, р41, р40, p33, р22), характеризующих определенную фазу заболевания. Так, выявление белка VCA 125 указывает на раннюю фазу инфекции; о поздней фазе течения инфекции свидетельствует обнаружение VCA 22, который выявляется одиночно или совместно с EBNA 1 (p-79), он длительно присутствует у перенесших заболевание и убедительно свидетельствует о перенесенной инфекции. Отмечается частое присутствие IgM p-45 и IgM p-79 при активном процессе [3]. Но, к сожалению, эти методы не совсем доступны в амбулаторной практике.
Таким образом, для постановки диагноза ЭБВИ, особенно ХЭБВИ, помимо проведения общеклинического обследования, необходимы серологические исследования специфических противовирусных антител, количественное определение ДНК вируса в различном биологическом материале и определение индекса авидности в динамике.
Принципы лечения ЭБВИЛечение любой формы ЭБВИ, а особенно ХЭБВИ, составляет большую проблему для современной медицины. До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ЭБВ, также нет патогенетически обоснованной схемы лечения больных ЭБВИ, а данные отечественных исследователей об эффективности терапии не имеют достаточной доказательной базы и все указания носят рекомендательный характер [1, 24–26].
Ведущее место среди этиотропных препаратов в терапии герпесвирусных инфекций занимают ациклические аналоги гуанозина (уровень доказательности А), препараты интерферонов и иммуноглобулинов, которые являются важной дополнительной составляющей лечения (уровень доказательности В). Чувствительность различных герпесвирусов к ацикловиру можно расположить в порядке убывания следующим образом: ВПГ-1, ВПГ-2, ВГ-3 > ЭБВ, ЦМВ-5 > ВГЧ-6, ВГЧ-7, ВГЧ-8.
Доказательная база свидетельствует, что ацикловир наиболее эффективен при инфекциях, вызванных альфа-герпесвирусами (ВПГ-1, 2, ВГ-3), имеет ограниченную эффективность при ЭБВИ и назначается только в случаях тяжелого ИМ с высокой вирусной нагрузкой. Однако он практически неэффективен при инфекциях, вызванных ВГЧ-6, 7, 8. Различная чувствительность к ацикловиру обусловлена разным содержанием вирусной тимидинкиназы у герпесвирусов. В отличие от ацикловира, к валацикловиру чувствительны все вирусы герпеса и наиболее высокая чувствительность — у альфа-подсемейства [26].
Лечение больных ИМ проводят в амбулаторных условиях, госпитализируют лиц с длительной лихорадкой, выраженным синдромом интоксикации, тяжелым тонзиллитом, гепатитом, желтухой, анемией, обструкцией дыхательных путей и при развитии осложнений [24, 26]. Базисная терапия ИМ (см. табл. 1) включает охранительный режим, симптоматическую терапию: адекватную регидратацию (обильное питье), полоскание горла антисептиками и по необходимости жаропонижающие средства. Применение антибиотиков необходимо только в случаях наслоения бактериальной инфекции с явлениями лакунарной или некротической ангины, при этом препаратами выбора будут цефалоспорины 2–3-го поколения, макролиды, карбапенемы [1, 26].
Противовирусные препараты неэффективны при латентном течении ХЭБВИ [25, 26], т. к. они ингибируют ДНК-полимеразу и репликацию литической фазы вируса в инфицированных клетках, которые экспрессируют вирусную ДНК-полимеразу. При ХЭБВИ в инфицированных клетках вирус находится в латентной фазе, экспрессируя латентные белки, для синтеза которых не требуется ДНК-полимераза [2, 23, 27].
По поводу назначения глюкокортикостероидов (ГКС) мнения также расходятся. Они рекомендуются больным с тяжелым течением ИМ, обструкцией дыхательных путей, неврологическими гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [27, 28]. При латентной ЭБВИ ГКС приводят к реактивации инфекции с литической репликацией ЭБВ через индуцирование раннего гена BZLF1 и литического трансактивирующего белка ZEBRA. Интересными представляются исследования по применению моноклональных антител к СD20 (ритуксимаб) у пациентов с иммунной тромбоцитопенической пурпурой [26]. Иммуносупрессивные препараты дают кратковременный положительный эффект в виде уменьшения симптомов ХЭБВИ без долгосрочной ремиссии и могут быть назначены при начальной фазе гемофагоцитарного лимфогистиоцитоза, который часто осложняет ХЭБВИ [18, 19]. Положительные результаты в лечении ХЭБВИ достигнуты при применении трансплантации гемопоэтических стволовых клеток. Начинать данную терапию рекомендовано в начале заболевания ввиду ее тяжелой переносимости [27, 28].
На основании изучения фармакодинамики и собственного обширного клинического опыта многие исследователи считают препараты α-интерферонов (уровень доказательности D) средством выбора в лечении тяжелых форм ЭБВИ и при нейроинфекциях как дополнение к специфическим препаратам, особенно показаны детям первых 3 лет жизни и подросткам. Эти препараты тормозят репликацию вирусов за счет разрушения вирусной мРНК, модулируют иммунный ответ, стимулируют выработку цитокинов, повышают функциональную активность макрофагов, нейтрофилов и стабилизируют клеточные мембраны. Так, в многочисленных работах [28–33] показана эффективность α-интерферона при инфекционном мононуклеозе у детей по сравнению с контрольной группой, при активации хронического мононуклеоза с интермиттирующей лихорадкой, цитопенией, дисфункцией печени, гепатоспленомегалией, аномальными титрами специфических антител и положительным геномом вируса у больного ХЭБВИ, при посттрансплантационном лимфопролиферативном синдроме, ассоциированном с ВЭБ, а также у больных ХЭБВИ при общем вариабельном иммунодефиците.
Препараты β-интерферонов снижают проницаемость гематоэнцефалического барьера и могут иметь определенные преимущества при рассеянном склерозе, ассоциированном с ЭБВ, с ремиттирующим течением, но доказательная база у таких препаратов значительно меньше, чем у α-интерферонов [32, 33].
Есть несколько исследований, указывающих на эффективность препаратов рекомбинантного γ-интерферона при ЭБВИ, которые оказывают ограниченное прямое противовирусное воздействие. Их клинический эффект опосредован усилением клеточного иммунитета, контролирующего эндогенный вирус. Терапевтический эффект этой группы препаратов продемонстрировали при тяжелой активной ХЭБВИ [34–38], рецидивирующей назофарингеальной карциноме, тяжелом лимфопролиферативном синдроме, вызванном ЭБВ. Учитывая синергическое действие, их можно применять как дополнение к терапии α-интерферонами [35, 37]. Показано, что противовирусный и иммуномодулирующий эффекты α-интерферонов частично опосредованы вторичной индукцией синтеза γ-интерферона Т-лимфоцитами [23, 36, 37]. Индукторы интерферонов имеют низкую доказательную базу при ЭБВИ, несмотря на широкое применение в клинической практике в странах постсоветского пространства.
Ряд авторов рекомендуют комплексную терапию ЭБВИ с введением препаратов иммуноглобулинов класса G. В отличие от интерферонов препараты иммуноглобулинов действуют преимущественно на внеклеточный вирус в виде вирионов. Этиотропный эффект иммуноглобулинов выражается в вируцидном и вирустатическом действии препарата и развитии антителозависимой комплемент-опосредованной цитотоксичности. Убедительно доказана их эффективность при первичной или вторичной гипоиммуноглобулинемии, а также в качестве базисной терапии при аутоиммунных осложнениях (синдром Гийена — Барре, тромбоцитопеническая пурпура, синдром Кавасаки, хроническая демиелинизирующая полинейропатия и системная красная волчанка) [36, 37]. В контролируемом нерандомизированном исследовании продемонстрирована эффективность комбинированной иммунотерапии при ЭБВИ, проявляющейся гипертрофией лимфоидных органов лимфоглоточного кольца, при реактивированной ЭБВИ с различными органными поражениями и при трудно поддающихся лечению формах болезни [37, 39], а также в профилактике виремии при ХЭБВИ. Многие исследователи [26, 38, 39] считают целесообразным применение специфического иммуноглобулина в комплексной терапии для профилактики ЭБВ-ассоциированного лимфопролиферативного синдрома у реципиентов солидных органов, при гемофагоцитарном синдроме, ассоциированном с ЭБВ, указывая на необходимость дальнейших исследований. Некоторым пациентам необходимо хирургическое лечение: удаление селезенки иногда выполняют при ИМ ЭБВ-этиологии при угрозе разрыва или начавшемся внутреннем кровотечении; возможна трахеостомия у больных с тяжелым ИМ при наличии фарингеальной обструкции и асфиксии.
В клинической практике диагностика и ведение пациентов с ЭБВИ всегда сложны и неодназначны. Приводим два клинических случая.
Клинические наблюденияСлучай 1. Пациентка Ю., 26 лет, доставлена в инфекционную клиническую больницу № 2 (ИКБ № 2) с жалобами на повышение температуры тела, слабость, появление одышки, ощущение сердцебиения при физической нагрузке.
Из анамнеза известно, что заболела 15 дней назад, когда появились повышение температуры тела до 39,0 °С, боль в горле, слабость, возникновение одышки при физической нагрузке. В последующие дни сохранялась повышенная температура тела, появились тяжесть в правом подреберье, потемнение мочи. Обследована амбулаторно: в клиническом анализе крови обнаружены лимфомоноцитоз, атипичные мононуклеары, снижение уровня гемоглобина до 73 г/л. Была госпитализирована в ИКБ № 2 с диагнозом: «Инфекционный мононуклеоз. Анемия тяжелой степени».
При поступлении состояние пациентки средней тяжести. Температура тела 38,0 °С. Выраженная слабость. Кожные покровы бледные, сыпи, геморрагий, кровоточивости нет. Склеры инъецированы, отмечается краевая иктеричность. Слизистая ротоглотки слабо гиперемирована, миндалины увеличены до II степени, имеются гнойные наложения в лакунах. Пальпируются подчелюстные, шейные до 1–1,5 см лимфатические узлы, плотные, безболезненные. Дыхание через нос свободное. Выделений из носа нет. В легких дыхание ослабленное. Хрипы не выслушиваются. ЧДД 20 в минуту. Тоны сердца приглушены, ритмичные. На верхушке сердца выслушивается систолический шум. ЧСС 80 в минуту. АД 110/70 мм рт. ст. Язык влажный, обложен белым налетом Живот при пальпации мягкий, чувствительный в правом подреберье. Перистальтика выслушивается. Перитонеальных знаков нет. Печень выступает из-под края реберной дуги на 4 см, плотная, чувствительная при пальпации. Пальпируется увеличенная селезенка, плотная, безболезненная. Симптом поколачивания по поясничной области отрицательный с обеих сторон. Физиологические отправления не нарушены. Очаговых и менингеальных знаков нет. Больной назначена терапия цефтриаксоном 2,0 г × 2 р./сут внутривенно, полоскание ротоглотки раствором фурациллина, внутривенно дезинтоксикационная терапия 5% раствором глюкозы с аскорбиновой кислотой, инъекции диклофенака при повышении температуры.
При обследовании: в общем анализе крови отмечается снижение количества эритроцитов до 1,96×1012/л, гемоглобина до 64 г/л, лейкоцитоз 17,5×109/л, лимфоцитоз 82%, среди лимфоцитов обнаружено 18 атипичных мононуклеаров. В биохимическом анализе крови отмечается умеренное повышение печеночных трансаминаз (АЛТ 106,3 ЕД/л; АСТ 165,4 ЕД/л). Содержание сывороточного железа в норме. При ПЦР-исследовании крови обнаружена ДНК ЭБВ, в реакции ИФА на антитела к VCA — IgМ положительные, IgG отрицательные.
Выполнено УЗИ органов брюшной полости: выявлены диффузные изменения в паренхиме печени и паренхиме поджелудочной железы, значительное увеличение и диффузные изменения в паренхиме селезенки.
Больная консультирована гематологом, заключение: картина крови соответствует лейкемоидной реакции по лимфоцитарному типу на фоне инфекционного мононуклеоза ЭБВ-этиологии. Рекомендована терапия эпоэтином бета, фолиевой кислотой, витамином В12. Больной выполнена 1 инъекция эпоэтина бета (2 тыс. Ед подкожно), далее ввиду возникновения у пациентки выраженного болевого синдрома и категорического отказа пациентки инъекции прекращены.
На 11-й день пребывания пациентки в стационаре отсутствует положительная динамика от проводимого лечения: в общем анализе крови сохраняется снижение эритроцитов до 1,84×1012/л, гемоглобина до 62 г/л, в биохимическом анализе крови отмечается повышенный уровень печеночных трансаминаз (АЛТ 110,4 ЕД/л; АСТ 160,1 ЕД/л). Больной назначена терапия ганцикловиром по 250 мг 2 р./сут внутривенно.
На 17-й день пребывания в стационаре пациентка пожаловалась на появление болей в животе, в связи с чем выполнено повторное УЗИ органов брюшной полости, выявлена зона инфаркта селезенки небольших размеров в нижнем полюсе. Больная консультирована хирургом, рекомендовано наблюдение в динамике.
В дальнейшем на фоне проводимой терапии отмечается положительная динамика в виде нормализации температуры тела, регресса явлений тонзиллита. В общем анализе крови обращает на себя внимание повышение гемоглобина до 96 г/л, эритроцитов до 3,01×1012/л, нормализация уровня лейкоцитов.
На 21-й день госпитализации больная выписана под наблюдение инфекциониста и гематолога по месту жительства.
Случай 2. Пациент Ж., 25 лет, поступил в ИКБ № 2 с жалобами на повышение температуры тела до 37,7 °С, сухой кашель.
Из анамнеза известно, что заболел 10.03.2019: слабость, головокружение, повышение температуры тела до фебрильных цифр. 11.03.2019: повышение температуры тела до 38,5 °С. Лечился самостоятельно: принимал тилорон, азитромицин без эффекта. 14.03.2019: осмотрен терапевтом на дому, выставлен диагноз ОРВИ, назначен осельтамивир. 15.03.2019: симптомы сохранялись, появился однократный жидкий стул без патологических примесей, насморк, сухой кашель. 19.03.2019 обследован амбулаторно: выполнена обзорная рентгенография грудной клетки — без патологических изменений, в общем анализе крови отмечается небольшой лейкоцитоз (11×109/л), остальные показатели в норме. Назначен левофлоксацин без эффекта. 21.03.2019 госпитализирован в ИКБ № 2 службой скорой помощи с диагнозом «лихорадка неясной этиологии».
При осмотре состояние пациента средней степени тяжести. Температура тела 37,7 °С. Кожные покровы физиологической окраски, умеренной влажности, сыпи нет. Слизистая ротоглотки гиперемирована, фолликулы на задней стенке глотки, миндалины не увеличены, свободны от наложений. При пальпации: периферические лимфатические узлы не увеличены. Периферических отеков нет. Дыхание через нос свободное. Выделений из носа нет. В легких дыхание жесткое, проводится во все отделы, хрипы не выслушиваются, ЧДД 18 в минуту. Тоны сердца ясные, ритмичные, ЧСС 78 в минуту, АД 100/60 мм рт. ст. Живот при пальпации мягкий, безболезненный во всех отделах. Перистальтика активна. Перитонеальных знаков нет. Печень выступает из-под края реберной дуги на 2 см, селезенка не увеличена, безболезненны. Симптом поколачивания по поясничной области сомнителен с обеих сторон. Со слов больного, стул оформлен, обесцвечен. Мочеиспускание не нарушено. Моча темная. Очаговых и менингеальных знаков нет.
При обследовании: в общем анализе крови отмечается лейкоцитоз 10×109/л, лимфоцитоз 74%, среди лимфоцитов обнаружено 17 атипичных мононуклеаров, остальные показатели в норме. В биохимическом анализе крови отмечается умеренное повышение печеночных трансаминаз (АЛТ 61 ЕД/л; АСТ 60,4 ЕД/л). В ПЦР-исследовании крови и мазка из ротоглотки ДНК ВЭБ не обнаружена, при ИФА на антитела к VCA — реакция на IgМ и IgG положительная.
По данным УЗИ органов брюшной полости и почек отмечаются увеличение и диффузные изменения в паренхиме печени, увеличение и диффузные изменения в паренхиме селезенки, умеренные диффузные изменения в паренхиме почек.
Назначен цефотаксим по 2 г 2 р./сут внутримышечно, полоскание ротоглотки раствором хлоргексидина, цетиризин, комплекс лактобактерий ацидофильных и кефирных грибков. На 3-й день пребывания в стационаре в связи с сохраняющейся лихорадкой произведена замена антимикробной терапии на ципрофлоксацин 400 мг 2 р./сут внутривенно.
На 5-й день пребывания больного в стационаре отмечена положительная динамика в виде исчезновения лихорадки, и на 9-й день больной выписан из стационара под наблюдение врача-инфекциониста по месту жительства.
ЗаключениеВажность проблемы изучения ЭБВИ обусловлена высокой распространенностью, специфической тропностью возбудителя к иммунокомпетентным клеткам, трудностями ранней и дифференциальной диагностики, особенностями клинического течения инфекции, отсутствием специфической профилактики и эффективной этиотропной терапии.
Учитывая разнообразие клинических форм ЭБВИ, высокий риск онкопатологии, формирование иммунодефицитов различной степени выраженности, в генезе которых ЭБВ играет ключевую роль, особое значение следует придавать своевременной диагностике и адекватной тактике ведения, т. к. они определяют исход заболевания. Необходимо более детальное и углубленное изучение иммунопатогенеза различных стадий ЭБВИ для определения критериев прогноза течения заболевания, выявления иммунологических нарушений и иммуногенетических факторов предрасположенности к ЭБВ-ассоциированным осложнениям, а также для оптимизации терапии.
Лечение больных с любой формой ЭБВИ должно быть комплексным, с учетом клинических проявлений, тяжести течения, периода болезни, что на практике бывает крайне трудно реализовать. Залогом же успешного лечения ХЭБВИ являются своевременная диагностика, правильный и строго индивидуальный подход как к этиотропной, так и к патогенетической терапии с последующим персонифицированным ведением конкретного больного на всех этапах (стационар, поликлиника). Необходимо наблюдение у инфекциониста, гематолога, иммунолога.
.
Дифференциально-диагностические аспекты инфекционного мононуклеоза Эпштейна-Барр вирусной этиологии у детей с позиции длительности инфицирования
УДК 616.0
DOI: 10.22138/2500-0918-2017-14-2-171-181
М. В. Антонова, Э. А. Кашуба, Т. Г. Дроздова, О. А. Любимцева,
Л. В. Ханипова, Н. В. Огошкова, Ю. С. Чехова
Тюменский государственный медицинский университет, г. Тюмень, Российская Федерация
Резюме. В настоящее время в мире отмечается рост заболеваемости Эпштейна-Барр вирусной инфекцией. Особое внимание ученых привлекает проблема длительной персистенции вируса с вероятностью формирования хронического процесса. Цель исследования — определить возможности дифференциальной диагностики первичной Эпштейна-Барр вирусной инфекции и ее реактивации, протекающих с клиническими проявлениями инфекционного мононуклеоза. Материалы и методы. В исследование были включены 152 ребенка с клиническими проявлениями инфекционного мононуклеоза и серологически подтвержденной активностью Эпштейна-Барр вируса. Комплексное исследование включало в себя динамическое клиническое наблюдение, анализ результатов лабораторных методов исследования (общий анализ крови, общий анализ мочи, биохимический анализ крови), расчет лейкоцитарного индекса интоксикации, серологическое исследование крови методом ИФА. Результаты. В 1/3 случаев клинические проявления инфекционного мононуклеоза были связаны с реактивацией вируса. Клиническая картина заболевания при этом характеризовалась меньшей выраженностью и продолжительностью основных симптомокомплексов, таких как тонзиллит, аденоидит, лимфаденопатия и гепатоспленомегалия. В качестве гематологических «маркеров» реактивации были определены высокое СОЭ, нейтрофилез, небольшое количество атипичных мононуклеаров (до 5%), высокий лейкоцитарный индекс интоксикации и нормальные биохимические показатели. Корреляционный анализ выявил появление при реактивации большого количества связей клинических симптомов с индексами позитивности антител различных классов, что, по нашему мнению, может указывать на иммунопатологический тип воспалительной реакции. С практической точки зрения оптическая плотность антител к различным антигенам Эпштейна-Барр вируса может служить прогностическим критерием тяжести и длительности течения заболевания. Заключение. Диспансерное наблюдение за детьми, перенесшими манифестную реактивацию Эпштейна-Барр вируса, должно быть более продолжительным, включающим периодическое отслеживание результатов общего, биохимического анализов крови, ИФА и количественной ПЦР крови.
Ключевые слова: инфекционный мононуклеоз, Эпштейна-Барр вирусная инфекция, дети, длительная персистенция
Дата поступления 31.05.2017
Образец для цитирования:
Антонова М.В., Кашуба Э.А., Дроздова Т.Г., Любимцева О.А., Ханипова Л.В., Огошкова Н.В., Чехова Ю.С. Дифференциально-диагностические аспекты инфекционного мононуклеоза Эпштейна-Барр вирусной этиологии у детей с позиции длительности инфицирования. Вестник уральской медицинской академической науки. 2017, Том 14, №2, с. 171–181 DOI: 10.22138/2500-0918-2017-14-2-171-181
ЛИТЕРАТУРА
1. Шарипова Е.В., Бабаченко И.В. Герпес-вирусные инфекции и инфекционный мононуклеоз (обзор литературы). Журнал инфектологии. 2013; 2: 5-12.
2. Исаков В.А., Архипова Е.И., Исаков Д.В. Герпеcвирусные инфекции человека. СПб: СпецЛит, 2013, 670 с.
3. Львов Н.Д., Дудукина Е.А. Ключевые вопросы диагностики Эпштейна-Барр вирусной инфекции. Инфекционные болезни: новости, мнения, обучение. 2013; 3: 24-32.
4. Хмилевская С.А. Эпштейна-Барр вирусный мононуклеоз: клинико-динамические особенности различных вариантов инфекции. Саратовский научно-медицинский журнал. 2010; 6 (3): 570-574.
5. Антонова М.В., Любимцева О.А., Кашуба Э.А., Дроздова Т.Г., Бертрам Л.И., Молокова О.М., Мясунова Е.Ю. Клиническая картина инфекционного мононуклеоза Эпштейн-Барр вирусной этиологии в возрастном аспекте. Академический журнал Западной Сибири. 2014; 5(54): 65-66.
6. Бертрам Л.И., Кашуба Э.А., Дроздова Т.Г., Лобацевич В.Ю., Перетягин А.Н. Роль аллергии в формировании кожных проявлений при некоторых инфекционных заболеваниях у детей. Медицинская наука и образование Урала. 2006; 7(4): 47-49.
7. Симованьян Э.Н. и др. Хроническая инфекция вируса Эпштейна-Барр у детей: современные аспекты диагностики и лечения. Consilsum Medicum. 2006; 8(2): 2-8.
8. Figueira-Silva C.M., Pereira F.E.L. Prevalence of Epstein-Barr virus antibodies in healthy children and adolescents in Vitoria, State of Espirito Santo, Brazil. Revista da Sociedade Brasileira de Medicina Tropical. 2004; 37(5): 409-412.
9. Masakhwe C. et al. Frequency of Epstein-Barr Virus in Patients Presenting with Acute Febrile Illness in Kenya. PloS one. 2016; 11(5): e0155308.
10. Бертрам Л.И., Кашуба Э.А., Дроздова Т.Г., Огошкова Н.В., Герасименко С.М., Князева Е.Ф., Любимцева О.А., Черемных Л.Г., Лобацевич В.Ю., Кечерукова Л.М., Смирнягина Р.Н. Иммунопатогенез основных клинических проявлений при заболеваниях, сопровождающихся мононуклеозоподобным синдромом. Медицинская наука и образование Урала. 2006; 7(2): 23-28.
11. Голева О.В., Мурина Е.А., Осипова З.А. Серологические маркеры реактивации вируса Эпштейна–Барр у детей с вирусными энцефалитами. Журнал инфектологии. 2015; 7(1): 70-74.
12. Bolis V. et al. Atypical manifestations of Epstein–Barr virus in children: a diagnostic challenge. Jornal de pediatria. 2016; 92(2): 113-121.
13. Калинина Н.М., Дрыгина Л.Б., Горейко Т.В. Современные представления об иммунопатогенезе инфекции, вызванной вирусом Эпштейна-Барр. Инфекция и иммунитет. 2011; 1(2): 121-130.
14. Крамарев С.А., Выговская О.В. Опыт использования препарата флавозид при Эпштейна-Барр вирусной инфекции у детей. Современная педиатрия. 2011; 39(5): 1-6.
15. Малашенкова И.К. и др. Клинические формы хронической Эпштейна-Барр вирусной инфекции: вопросы диагностики и лечения. Лечащий врач. 2003; 9: С. 32-38.
16. Кальф-Калиф Я.Я. О лейкоцитарном индексе интоксикации и его практическом значении. Врачебное дело. 1941; 1: 31-40.
17. Ильин В.П. Корреляционный анализ количественных данных в медико-биологических исследованиях. Бюллетень Восточно-Сибирского научного центра Сибирского отделения Российской академии медицинских наук. 2013; 4(92): 125-130.
18. Тимченко В.Н. и др. Клинико-лабораторные критерии тяжести и принципы терапии острого инфекционного мононуклеоза Эпштейна-Барр вирусной этиологии у детей. Педиатр. 2015; 6(4): 147-153.
19. Блохина Е.Б. Роль латентной инфекции, вызванной вирусом Эпштейна-Барр, в развитии лимфопролиферативных заболеваний. Вопросы гематологии, онкологии и иммунопатологии в педиатрии. 2003; 2(3): 65-70.
20. Выговская О.В. и др. Инфекционный мононуклеоз Эпштейна-Барр вирусной этиологии у детей: вопросы этиологии, патогенеза, иммуногенеза, лечения. Практикуючий лікар. 2012; 4: 29-34.
21. Свинцова Т.А. и др. Значение показателей иммунного ответа у больных с ВЭБ-инфекционным мононуклеозом в прогнозировании течения и эффективности противовирусной и иммунокорригирующей терапии. Эпидемиология и инфекционные болезни. 2013; 1: 7-14.
22. Летаева О.В., Филимонкова Н.Н., Чигвинцева Е.А. Выявленные патогенетические особенности красного плоского лишая и оптимизация терапии. Вестник уральской медицинской академической науки.2009; 3(26): 41-43.
23. Смирнов А.В., Чуелов С.Б., Россина А.Л. Современное представление о гепатитах, вызванных вирусами семейства герпеса. Детские инфекции. 2008; 7(3): 3-16.
24. Canovic P., Gajovic O., Todorovic Z., Mijailovic Z. Epstein-Barr virus hepatitis associated with icterus — a case report. Med. Pregl. 2006; 59: 179-182.
25. Дрыганова М.Б., Мартынова Г.П., Куртасова Л.М. Инфекционный мононуклеоз, вызванный вирусом Эпштейна-Барр у детей: клинико-иммунологические параллели. Сибирское медицинское обозрение. 2010; 63(3): 16-28.
26. Crum N.F. Epstein Barr virus hepatitis: case series and review. Southern medical journal. 2006; 99(5): 544-548.
27. Симованьян Э.Н. и др. Эпштейна-Барр вирусная инфекция у детей: современные подходы к диагностике и лечению. Лечащий врач. 2007; 7: 36-41.
28. Нагоев Б.С., Камбачокова З.А. Состояние клеточного иммунитета у больных герпесвирусными инфекциями. Вестник новых медицинских технологий. 2011; 18(3): 325-327.
29. Пирогова З. И., Рябчук Ф. Н. Клинико-лабораторная характеристика персистирующих форм герпес-вирусной инфекции у детей. Лечащий врач. 2011; 8: 62-65.
30. Шано В.П., Кучер Е.А. Синдром эндогенной интоксикации. Острые и неотложные состояния в практике врача. 2011; 1(25): 35-41.
Авторы
Антонова Мария Владимировна
Аспирант кафедры инфекционных болезней с курсом детских инфекций
[email protected]
Кашуба Эдуард Алексеевич
доктор медицинских наук, профессор, заведующий кафедрой инфекционных болезней с курсом детских инфекций [email protected]
Дроздова Татьяна Георгиевна
кандидат медицинских наук, доцент кафедры инфекционных болезней с курсом детских инфекций
[email protected]
Любимцева Оксана Анатольевна
кандидат медицинских наук, доцент кафедры инфекционных болезней с курсом детских инфекций
[email protected]
Ханипова Людмила Вячеславовна
кандидат медицинских наук, доцент кафедры инфекционных болезней с курсом детских инфекций
[email protected]
Огошкова Наталья Владимировна
кандидат медицинских наук, доцент кафедры инфекционных болезней с курсом детских инфекций
[email protected]
Чехова Юлия Сергеевна
ассистент кафедры инфекционных болезней с курсом детских инфекций
[email protected]
ФГБОУ ВО «Тюменский государственный медицинский университет Минздрава РФ
Российская Федерация,625023 г. Тюмень, ул. Одесская, 54
Это произведение доступно по лицензии Creative Commons «Attribution-NonCommercial» («Атрибуция — Некоммерческое использование») 4.0 Всемирная.
Мононуклеоз
Мононуклеоз, также известный как «мононуклеоз», обычно вызывается микробом, который называется вирусом Эпштейна-Барра. Другие вирусы, такие как ЦМВ и ВИЧ, и другие инфекции, такие как токсоплазмоз, также могут вызывать мононуклеоз. Хотя мононуклеоз наиболее известен тем, что вызывает опухание желез и усталость, он может принимать разные формы. Большинство детей с моно выздоравливают без каких-либо проблем. Но болезнь может пройти долго. В некоторых случаях моно может вызвать проблемы с печенью, селезенкой или сердцем.Поэтому важно, чтобы моно был диагностирован и за ребенком внимательно наблюдали.
Причины мононуклеозаMono может легко передаваться через слюну инфицированного человека:
- Пить и есть после них
- Совместное использование соломинки, чашки, зубных щеток и столовых приборов
- Поцелуи и близкий контакт
- Обращение с игрушками с детьми слюни
У детей общие симптомы включают:
- Усталость, слабость
- Лихорадка
- Боль в горле
- Болезненные или увеличенные лимфатические узлы на шее или подмышках
- Опухшие миндалины ,00
- Сыпь
- Боль в мышцах или скованность
- Головная боль
- Потеря аппетита, тошнота
- Тупая боль в области живота
- Увеличенные печень и селезенка
- Головные боли
- Пухлые глаза
- Светочувствительность
Мононуклеоз может быть диагностирован с помощью простого анализа крови, выполненного вашим врачом.
Лечение мононуклеозаПоскольку это вирусная инфекция, антибиотики не излечивают моно. Лечащий врач вашего ребенка может прописать лекарства, которые помогут облегчить боль или дискомфорт вашего ребенка. Лучшее лечение моно — отдых. Ребенку с моно также следует пить много жидкости. Чтобы помочь вашему ребенку почувствовать себя лучше и быстрее выздороветь:
- Убедитесь, что ребенок много отдыхает.
- Держите ребенка в тепле.
- Давайте ребенку много жидкости, например воды или яблочного сока.
- Не позволяйте никому курить рядом с ребенком.
- Убедитесь, что ваш ребенок в течение месяца избегает контактных видов спорта и подъема тяжестей, чтобы не повредить селезенку. Во время этой болезни может увеличиваться селезенка. Обсудите с лечащим врачом вашего ребенка, когда он или она сможет вернуться к нормальной деятельности.
- Лечите у ребенка жар, боль в горле или мышечные боли с помощью детского ацетаминофена или ибупрофена. Никогда не давайте ребенку аспирин.
Симптомы обычно длятся несколько недель, но иногда могут длиться от 1 до 2 месяцев или дольше.Даже после того, как симптомы исчезнут, ваш ребенок может некоторое время чувствовать усталость или слабость.
Предотвращение распространения мононуклеозаПока вы ухаживаете за ребенком с моно:
- Часто мойте руки теплой водой с мылом, особенно до и после ухода за больным ребенком.
- Следите за своим здоровьем и здоровьем других членов семьи
- Ограничьте контакт больного ребенка с другими детьми.
- Посуду и столовые приборы, используемые больным ребенком, следует мыть отдельно в очень горячей мыльной воде.Или пропустите их в посудомоечной машине.
Немедленно позвоните поставщику медицинских услуг, если ваш ребенок в остальном здоров:
- Младенец младше 3 месяцев с ректальной температурой 100,4 ° F (38 ° C) или выше
- Является ли ребенок любого возраста, у которого повторяется температура 104 ° F (40 ° C) или выше
- Имеет лихорадку, которая держится более 24 часов у ребенка в возрасте до 2 лет или в течение 3 дней у ребенка в возрасте 2 лет и старше
- Был припадок, вызванный лихорадкой
- Испытывает затрудненное или учащенное дыхание.
- Не успокаивается, проявляет признаки раздражительности или беспокойства.
- Кажется необычно сонным, вялым или безразличным.
- Имеет проблемы с едой, питьем или глотанием.
- Прекращает дыхание даже на мгновение.
- Показывает признаки сильной боли в груди, шее или животе.
Вирус Эпштейна-Барра | Американская академия педиатрии
Цели
После прочтения этой статьи читатели смогут:
Изложите эпидемиологию первичной инфекции, вызванной вирусом Эпштейна-Барра (ВЭБ).
Опишите и объясните физиологические основы клинических проявлений инфекционного мононуклеоза.
Опишите и объясните физиологическую основу распространенных осложнений инфекционного мононуклеоза.
Перечислите диагностические тесты, которые помогут отличить острую первичную ВЭБ-инфекцию от отдаленной.
Просмотрите лимфопролиферативные заболевания и злокачественные новообразования, связанные с ВЭБ.
Введение
EBV был первоначально идентифицирован в 1964 году в опухолевой ткани пациента, у которого была африканская лимфома Беркитта (BL), быстрорастущее, обычно смертельное, злокачественное новообразование B-лимфоцита.Когда лаборант, работавший с этим новым вирусом, заболел мононуклеозом и превратился в сероконверсию в ВЭБ, связь между ВЭБ и мононуклеозом стала очевидной. Вскоре после этого сероэпидемиологические исследования показали, что ВЭБ инфицирует практически все население мира, обычно как субклиническое или незначительное заболевание в детстве. Десять лет спустя сообщения о семейном Х-сцепленном заболевании фатального инфекционного мононуклеоза подчеркнули важность иммуногенетических факторов в лечении ВЭБ-инфекции.Теперь, спустя почти 40 лет после своего открытия, ВЭБ продолжает увлекать клиницистов, вирусологов, онкологов, генетиков и иммунологов, пытающихся понять этот очень успешный патоген человека.
Эпидемиология
ВЭБ — повсеместно распространенный во всем мире патоген, постоянно являющийся укрытием практически для всех взрослых, независимо от географического положения. После первичного заражения вирус латентно заражает циркулирующие В-клетки и незаметно выделяется в слюну и генитальные выделения. Разговорный термин «болезнь поцелуев» означает пероральный путь заражения большинства людей.Распространение связано с тесным личным контактом, поэтому неудивительно, что возраст первого заражения зависит от условий жизни. Заражение происходит в более раннем возрасте при плохой гигиене и стесненных условиях проживания; Уровень инфицирования в…
Атипичные проявления вируса Эпштейна – Барра у детей: диагностическая проблема
Резюме
Цель
Уточнить частоту и патофизиологические механизмы редких проявлений инфекции вируса Эпштейна – Барра.
Источники
Оригинальные исследования, опубликованные на английском языке в период с 1985 по 2015 год, были отобраны с помощью компьютерного поиска литературы (PubMed и Scopus). При компьютерном поиске использовались комбинации ключевых слов, относящиеся к «инфекциям ВЭБ» и «атипичным проявлениям».
Сводка результатов
Вирус Эпштейна – Барра — это вирус герпеса, который вызывает скрытую инфекцию на протяжении всей жизни почти у каждого взрослого человека. Первичная инфекция поражает в основном детей и проявляется клиническим синдромом инфекционного мононуклеоза.Однако инфекция вирусом Эпштейна – Барра может проявлять множество редких, атипичных и угрожающих проявлений. Это может вызвать вторичные инфекции и различные осложнения со стороны дыхательной, сердечно-сосудистой, мочеполовой, желудочно-кишечной и нервной систем. Вирус Эпштейна – Барра также играет важную роль в патогенезе аутоиммунных заболеваний, аллергии и новообразований, главным представителем которых является лимфома Беркитта. Механизмы этих проявлений до сих пор не выяснены. Таким образом, основные предположения — это прямая вирусная инвазия и хронический иммунный ответ из-за реактивации латентного состояния вируса или даже различных мутаций ДНК.
Выводы
Врачи должны с осторожностью относиться к необычным проявлениям вирусной инфекции и рассматривать ВЭБ в качестве возбудителя, когда они сталкиваются с аналогичными клиническими картинами.
Resumo
Objetivo
Esclarecimento da frequência e dos mecanismos patofisiológicos das manifestações raras dafecção por vírus de Epstein – Barr.
Fontes
Estudos de pesquisas originais publicados em inglês entre 1985 и 2015 foram selectionados por meio de uma busca na literatura assistida por computador (Pubmed e Scopus).As buscas no computador utilizaram combinações de palavras-chave relacionadas a «influencções por VEB» e «manifestação atípica».
Resumo dos achados
O vírus de Epstein – Barr é um herpesvírus responseável por uma influencção latente vitalícia em quase todo vulto. Первичная инфекционная инфекция и основная инфекция, вызванная вирусом мононуклеоза. Contudo, инфекция, вызванная вирусом Эпштейна – Барра, представляет собой различные манифестации, характерные для жизни и альт-риско.Ela pode causar influencções secundárias e diversas осложнениям душевой системы респираторной, сердечно-сосудистой, мочеполовой, желудочно-кишечной и нервной. O vírus de Epstein – Barr também desempenha um papel знаменательно на патогенезе деяний, аллергиях и аутоиммунных новообразованиях, com o linfoma de Burkitt sendo o main submitante das últimas. Os mecanismos dessas manifestações ainda não foram resolvidos. Портанто, как правило, требует, чтобы вирусное направление было инвазировано и реагировало на скрытое обнаружение вируса или различных изменений в ДНК.
Выводы
Os médicos devem tomar cuidado sobre apresentações incuns de вирусная инфекция и рассмотрение VEB um agent causador quando encontrarem situações clínicas semelhantes.
Ключевые слова
Вирус Эпштейна – Барра
Инфекционный мононуклеоз
Детский
Осложнения
Палаврас-чав
Вирус де Эпштейн – Барр
Мононуклеоза
000 статей0000002 Mononucleose 9ç300000030003000300030003000300030003000300030003000300030003000300030003 Просмотреть аннотациюCopyright © 2016 Sociedade Brasileira de Pediatria.Опубликовано Elsevier Editora Ltda.
Рекомендуемые статьи
Цитирующие статьи
Мононуклеоз (мононуклеоз): симптомы, лечение и диагностика
Обзор
Что такое мононуклеоз (моно)?
Мононуклеоз — это болезнь, которая обычно поражает подростков и молодых людей, но может поражать и детей.Болезнь вызывают вирусы, чаще всего вирус Эпштейна-Барра (ВЭБ), и некоторые инфекции. Моно иногда называют «болезнью поцелуев», потому что она легко распространяется через жидкости организма, такие как слюна.
Для большинства людей моно не является серьезным заболеванием, и его состояние улучшается без лечения. Тем не менее крайняя усталость, ломота в теле и другие симптомы могут мешать учебе, работе и повседневной жизни. С моно вы можете чувствовать себя плохо в течение месяца.
Насколько распространен мононуклеоз (моно)?
Вирус Эпштейна-Барра (EBV), вызывающий моно, чрезвычайно распространен.Около 90% американцев инфицированы им к 35 годам. Не у всех, у кого есть вирус, развиваются моносимптомы — некоторые люди только переносят вирус.
Кто может заболеть мононуклеозом (моно)?
Часто бывает два пика, когда люди заражаются ВЭБ: дети младшего школьного возраста и снова в подростковом / молодом возрасте. Маленькие дети часто протекают бессимптомно, тогда как подростки и люди в возрасте от 20 лет чаще заболевают моно. Примерно каждый четвертый человек в этой возрастной группе, заболевший ВЭБ, заболевает моно, но любой может заразиться, независимо от его возраста.
Является ли моно инфекция, передающаяся половым путем?
Эпштейн-Барр — это вирус герпеса. Он отличается от вируса простого герпеса (ВПГ), вызывающего генитальный и оральный герпес. Оба вируса могут передаваться половым путем. Тем не менее, ВЭБ с большей вероятностью распространяется другими способами, такими как разделение напитков или поцелуи.
Заразен ли мононуклеоз (моно)?
Вирусы, вызывающие моно, очень заразны. Вы можете заразиться ими при контакте с жидкостями организма инфицированного человека, включая слюну.Эти вирусы распространяются через:
Можно ли заболеть мононуклеозом (моно) более одного раза?
Вирус Эпштейна-Барра остается в вашем организме в неактивной форме даже после исчезновения моносимптомов. Но большинство людей развивают моно только один раз.
Если ВЭБ реактивируется, симптомы возникают редко. Однако вы можете неосознанно передать реактивированный вирус другим. А у людей с ослабленной иммунной системой моносимптомы могут развиваться более одного раза.
Симптомы и причины
Что вызывает мононуклеоз (моно)?
Более 90% моно случаев вызваны вирусом Эпштейна-Барра.Другие вирусы и определенные инфекции также могут вызывать болезнь. Симптомы могут развиться из-за:
Каковы симптомы мононуклеоза (моно)?
Симптомы мононуклеоза могут быть легкими или тяжелыми. Они имеют тенденцию появляться постепенно. Если вы заболели моно, это, вероятно, произойдет через четыре-шесть недель после того, как вы войдете в контакт с EBV. Эти симптомы могут длиться четыре недели и дольше:
Диагностика и тесты
Как диагностируется мононуклеоз (моно)?
Ваш лечащий врач оценит ваши симптомы, чтобы поставить диагноз.Они особенно проверит увеличение лимфатических узлов на шее и признаки увеличения селезенки или печени.
Анализы крови обнаруживают антитела, вырабатываемые вашим организмом для борьбы с вирусом Эпштейна-Барра. Ваш врач может также проверить наличие большого количества лейкоцитов (лимфоцитов), которые указывают на инфекцию.
Ведение и лечение
Как лечить или лечить мононуклеоз (моно)?
Не существует вакцины или лекарства от моно.Антибиотики для борьбы с бактериальной инфекцией и противовирусные препараты для уничтожения других вирусов не работают против моно. Вместо этого лечение направлено на то, чтобы помочь вам почувствовать себя лучше за счет облегчения симптомов. Ваша помощь может включать:
- Отдых: Моно очень утомляет. Сон помогает организму бороться с инфекциями.
- Гидратация: Пейте много жидкости, чтобы предотвратить обезвоживание.
- Обезболивающие: Нестероидные противовоспалительные препараты (НПВП) снимают жар, воспаление, головные боли и боли в мышцах.Эти препараты включают ибупрофен (Адвил®) и напроксен (Алеве®). Также действует ацетаминофен (Тайленол®).
- Пустышки от боли в горле: Можно полоскать горло соленой водой и использовать леденцы для горла.
- Избегание занятий спортом: Физическая активность может оказать слишком сильное давление на увеличенную селезенку, увеличивая риск ее разрыва. Вам следует избегать контактных видов спорта и физических упражнений во время болезни и в течение четырех недель после нее.
Каковы осложнения мононуклеоза (моно)?
Моно-симптомы имеют тенденцию постепенно улучшаться примерно через четыре недели.Чувство усталости может сохраняться месяцами. Некоторые люди пропускают школу или работу, когда выздоравливают.
Увеличенная селезенка, которая разрывается (разрывается) — самая большая проблема при моно у ранее здоровых людей. Эта железа в верхнем левом углу живота (живота) помогает фильтровать кровь. Если у вас лопнет селезенка, она может кровоточить в брюшную полость. Внутреннее кровотечение из разрыва селезенки может быть опасным для жизни и требует неотложной операции. Ваш лечащий врач может посоветовать вам избегать интенсивных упражнений, контактных видов спорта и тяжелой атлетики, пока вы не почувствуете себя лучше.
Профилактика
Как предотвратить мононуклеоз (моно)?
Нет вакцины против моно. Лучший способ предотвратить заражение вирусами, вызывающими моно, — это соблюдение правил гигиены. Не делитесь едой, напитками или биологическими жидкостями с людьми, у которых есть моно или какие-либо признаки вирусного заболевания, такие как лихорадка, кашель, боль в горле или усталость.
Как мононуклеоз (моно) влияет на беременность?
Будущие мамы, у которых развивается моно от ВЭБ, обычно беременны здоровыми. Позвоните своему врачу, если у вас поднялась температура, которая может увеличить риск выкидыша и преждевременных родов. Хотя существует небольшая вероятность передачи вируса Эпштейна-Барра ребенку во время беременности или после родов во время грудного вскармливания, у большинства детей моносимптомы не развиваются. Если моно был вызван ЦМВ-инфекцией во время беременности, есть вероятность, что ваш ребенок может быть поражен, и вам следует обсудить это со своим акушером.
Перспективы / Прогноз
Каков прогноз (перспективы) для людей с мононуклеозом (моно)?
Моносимптомы могут быть серьезными. Они могут временно повлиять на вашу способность вести активный образ жизни. К счастью, эти симптомы постепенно улучшаются при лечении в домашних условиях.
Вы можете испытывать постоянную усталость в течение нескольких месяцев. Вам нужно будет защитить свое здоровье, достаточно отдыхая и пить в это время. Вам также следует избегать физических нагрузок, чтобы предотвратить разрыв селезенки.
Жить с
Когда мне следует позвонить врачу?
Вам следует позвонить своему врачу, если у вас есть моно, и вы испытываете:
- Затрудненное дыхание или глотание.
- Головокружение или обморок.
- Сильная мышечная слабость рук или ног.
- Сильные боли в теле.
- Постоянная высокая температура.
- Сильные головные боли.
- Острая боль в левом верхнем углу живота.
Какие вопросы я должен задать своему врачу?
Если у вас моно, вы можете спросить своего врача:
- Каковы лучшие методы лечения моносимптомов?
- Как долго я заразен?
- Какие шаги я могу предпринять, чтобы не заразить других этим вирусом?
- Сколько времени потребуется на восстановление после моно?
- Когда я смогу вернуться на работу или в школу?
- Когда я смогу вернуться к упражнениям и физической активности?
- Могу ли я снова получить моно?
- Стоит ли обращать внимание на признаки осложнений?
Записка из клиники Кливленда
В большинстве случаев мононуклеоз (моно) не вызывает серьезных проблем.Однако такие симптомы, как крайняя усталость, боль в горле и ломота в теле, могут мешать учебе, работе и жизни. Ваш лечащий врач может дать рекомендации по поиску облегчения. Отдых и лекарства, отпускаемые без рецепта, часто являются лучшим способом облегчить симптомы. Также важно избегать физических нагрузок, которые могут привести к разрыву увеличенной селезенки.
Вирус Эпштейна-Барра — симптомы, причины, лечение
Вирус Эпштейна-Барра, также называемый EBV, является чрезвычайно распространенным вирусом, который в то или иное время заражает большинство людей в течение их жизни.Инфекция вирусом Эпштейна-Барра обычно вызывает легкое простудное или гриппоподобное заболевание, но в некоторых случаях симптомы инфекции могут отсутствовать.
У подростков и молодых людей вирус Эпштейна-Барра может вызывать более серьезное заболевание — мононуклеоз. Инфекция вируса Эпштейна-Барра также была связана с развитием некоторых редких видов рака, включая лимфому Беркитта и карциному носоглотки.
Вирус Эпштейна-Барра очень заразен и передается от человека к человеку через интимный контакт со слюной человека, инфицированного вирусом Эпштейна-Барра.По данным Центров по контролю и профилактике заболеваний, до 95% всех взрослых в какой-то момент своей жизни были инфицированы вирусом Эпштейна-Барра.
Лечение большинства вирусных заболеваний начинается с предотвращения распространения болезни с соблюдением элементарных гигиенических мер. Однако контролировать распространение вируса Эпштейна-Барра чрезвычайно сложно, потому что он очень распространен и потому что можно распространять вирус Эпштейна-Барра, даже если человек не выглядит больным.Многие здоровые люди, перенесшие вирусную инфекцию Эпштейна-Барра, продолжают переносить вирус в своей слюне, что означает, что они могут передавать его другим на протяжении всей своей жизни. Тем не менее, избегание контакта со слюной другого человека за счет отказа от использования стаканов или зубных щеток по-прежнему является хорошей общей мерой профилактики заболеваний.
В настоящее время не существует специального лекарства от инфекции вируса Эпштейна-Барра. Лечение включает в себя меры по облегчению симптомов и поддержанию максимальной силы организма до тех пор, пока болезнь не пойдет своим чередом.Это включает в себя отдых, лекарства для облегчения боли в теле и лихорадку, а также обильное питье. Люди с хорошим здоровьем, как правило, могут вылечиться от инфекции вируса Эпштейна-Барра дома с помощью поддерживающей терапии, такой как отдых, питье и обезболивающие.
Кортикостероиды могут быть назначены в некоторых случаях мононуклеоза. Антибиотики неэффективны против вируса Эпштейна-Барра, но могут быть назначены при развитии вторичной бактериальной инфекции, например бактериального тонзиллита.
Серьезные или опасные для жизни осложнения, такие как энцефалит, разрыв селезенки или гепатит, могут развиваться в некоторых случаях инфекции вируса Эпштейна-Барра или мононуклеоза, который часто вызывается вирусом Эпштейна-Барра.
Немедленно обратитесь за медицинской помощью , если у вас или вашего ребенка есть симптомы мононуклеоза, такие как сильная усталость, увеличение лимфатических узлов или заболевание, похожее на простуду или грипп, которое не проходит. Немедленно обратитесь за медицинской помощью (позвоните по номеру 911) , если у вас или у кого-то из ваших близких есть опасные для жизни симптомы, такие как одышка, судороги, спутанность сознания или бред, или изменение бдительности или сознания.
Мононуклеоз — Диагностика и лечение
Диагноз
Физический осмотр
Ваш врач может заподозрить мононуклеоз на основании ваших признаков и симптомов, их продолжительности и физического осмотра.Он или она будет искать такие признаки, как увеличение лимфатических узлов, миндалин, печени или селезенки, и рассматривать, как эти признаки соотносятся с симптомами, которые вы описываете.
Анализы крови
- Тесты на антитела. Если есть необходимость в дополнительном подтверждении, может быть проведен моноспотный тест для проверки вашей крови на антитела к вирусу Эпштейна-Барра. Этот скрининговый тест дает результаты в течение дня. Но он может не обнаружить инфекцию в течение первой недели болезни.Другой тест на антитела требует более длительного времени для получения результата, но может выявить болезнь даже в течение первой недели появления симптомов.
- Количество лейкоцитов. Ваш врач может использовать другие анализы крови, чтобы определить повышенное количество лейкоцитов (лимфоцитов) или лимфоцитов аномального вида. Эти анализы крови не подтвердят мононуклеоз, но могут предположить, что это возможно.
Лечение
Специфической терапии для лечения инфекционного мононуклеоза не существует.Антибиотики не действуют против вирусных инфекций, таких как моно. Лечение в основном включает в себя заботу о себе, например, достаточный отдых, здоровое питание и употребление большого количества жидкости. Вы можете принимать безрецептурные обезболивающие для лечения лихорадки или боли в горле.
Лекарства
Лечение вторичных инфекций и других осложнений. Стрептококковая (стрептококковая) инфекция иногда сопровождается болью в горле при мононуклеозе.У вас также может развиться инфекция носовых пазух или миндалин (тонзиллит). Если это так, вам может потребоваться лечение антибиотиками от этих сопутствующих бактериальных инфекций.
Сильное сужение дыхательных путей можно лечить кортикостероидами.
- Риск появления сыпи при приеме некоторых лекарств. Амоксициллин и другие антибиотики, в том числе на основе пенициллина, не рекомендуются людям с мононуклеозом. Фактически, у некоторых людей с мононуклеозом, принимающих один из этих препаратов, может появиться сыпь.Однако сыпь не обязательно означает, что у них аллергия на антибиотик. При необходимости доступны другие антибиотики, которые с меньшей вероятностью вызывают сыпь, для лечения инфекций, которые могут сочетаться с мононуклеозом.
Образ жизни и домашние средства
Помимо большого количества отдыха, эти шаги могут помочь облегчить симптомы мононуклеоза:
- Пейте много воды и фруктовых соков. Жидкости помогают снять жар, боль в горле и предотвратить обезвоживание.
Примите безрецептурное обезболивающее. При необходимости используйте болеутоляющие, такие как ацетаминофен (Тайленол и др.) Или ибупрофен (Адвил, Мотрин IB и др.). Эти лекарства не обладают противовирусными свойствами. Принимайте их только для снятия боли или жара.
Соблюдайте осторожность при назначении аспирина детям или подросткам. Хотя аспирин одобрен для использования у детей старше 3 лет, детям и подросткам, выздоравливающим после ветрянки или гриппоподобных симптомов, никогда не следует принимать аспирин.Это связано с тем, что аспирин был связан с синдромом Рея, редким, но потенциально опасным для жизни заболеванием у таких детей.
- Полоскать горло соленой водой. Делайте это несколько раз в день, чтобы облегчить боль в горле. Смешайте 1/4 чайной ложки (1,5 грамма) соли с 8 унциями (237 миллилитрами) теплой воды.
Подождите, чтобы вернуться к спорту и другим занятиям
Большинство признаков и симптомов мононуклеоза исчезают в течение нескольких недель, но может пройти два-три месяца, прежде чем вы почувствуете себя полностью нормальным.Чем больше вы отдыхаете, тем скорее вы поправитесь. Слишком раннее возвращение к своему обычному графику может увеличить риск рецидива.
Чтобы избежать риска разрыва селезенки, врач может посоветовать вам подождать около месяца, прежде чем вернуться к активной деятельности, поднятию тяжестей, грубым занятиям или контактным видам спорта. Разрыв селезенки приводит к сильному кровотечению и требует неотложной медицинской помощи.
Спросите своего врача о том, когда вам безопасно вернуться к обычному уровню активности.Ваш врач может порекомендовать программу постепенных упражнений, чтобы помочь вам восстановить силы по мере выздоровления.
Как справиться и поддержать
Мононуклеоз может длиться несколько недель, и вы будете оставаться дома на время выздоровления. Будьте терпеливы со своим телом, поскольку оно борется с инфекцией.
Для молодых людей мононуклеоз будет означать пропущенные занятия — занятия, групповые занятия и вечеринки. Без сомнения, вам нужно немного расслабиться. Учащимся необходимо сообщить своим школам, что они выздоравливают от мононуклеоза, и, возможно, потребуется особое внимание, чтобы не отставать от своей работы.
Если у вас мононуклеоз, вам не обязательно помещать в карантин. Многие люди уже имеют иммунитет к вирусу Эпштейна-Барра из-за контакта с ним в детстве. Но старайтесь не ходить в школу и не заниматься другими делами, пока не почувствуете себя лучше.
Обратитесь за помощью к друзьям и семье, когда вы выздоравливаете от мононуклеоза. Студенты колледжа также должны обращаться к сотрудникам медицинского центра студенческого городка за помощью или лечением, если это необходимо.
Подготовка к приему
Если вы подозреваете, что у вас мононуклеоз, обратитесь к семейному врачу.Вот некоторая информация, которая поможет вам подготовиться к приему и узнать, чего ожидать от врача.
Что вы можете сделать
- Запишите все симптомы, которые вы испытываете, включая те, которые могут показаться не связанными с причиной, по которой вы записались на прием.
- Запишите ключевую личную информацию, отметив любые серьезные стрессы, недавние изменения в жизни, ваш распорядок дня, включая привычки сна, или контакты с кем-либо, кто болен мононуклеозом.
- Составьте список всех лекарств, витаминов и пищевых добавок, которые вы принимаете.
- Запишите вопросы, которые вы можете задать своему врачу.
Подготовка списка вопросов поможет вам максимально эффективно проводить время с врачом. При мононуклеозе врачу следует задать следующие основные вопросы:
- Каковы наиболее вероятные причины моих симптомов или состояния?
- Каковы другие возможные причины моих симптомов или состояния, кроме наиболее вероятной?
- Какие тесты мне нужны?
- У меня другие проблемы со здоровьем.Как мне лучше всего управлять ими вместе?
- Есть ли ограничения, которым я должен следовать?
- Должен ли я оставаться дома и не ходить на работу или в школу? Как долго я должен оставаться дома?
- Когда я смогу вернуться к активной деятельности и контактным видам спорта?
- Есть ли лекарства, которых мне следует избегать?
- Есть ли брошюры или другие печатные материалы, которые я могу взять с собой? Какие сайты вы рекомендуете?
Не стесняйтесь задавать другие вопросы.
Чего ожидать от врача
Ваш врач может задать вам ряд вопросов, в том числе:
- Когда у вас появились симптомы?
- Были ли вы контактировали с кем-нибудь с мононуклеозом?
- Ваши симптомы были постоянными или случайными?
- Насколько серьезны ваши симптомы?
- Что может улучшить ваши симптомы?
- Что может ухудшить ваши симптомы?
Декабрь22, 2020
Отчет о случае и ведение вирусного энцефалита Эпштейна-Барра
Вирус Эпштейна-Барра (ВЭБ) обычно вызывает легкие, бессимптомные и самостоятельно купирующиеся инфекции у детей и взрослых; однако иногда это может приводить к тяжелым состояниям, таким как неврологические заболевания, злокачественные заболевания, печеночная недостаточность и миокардит. Неврологические расстройства, связанные с вирусом Эпштейна-Барра, включают менингит, энцефалит и краниальный или периферический неврит, которые чаще всего наблюдаются у пациентов с ослабленным иммунитетом.Терапевтические методы лечения тяжелого поражения органов, связанного с ВЭБ, включая проявления центральной нервной системы, все еще не определены. Здесь мы описываем семилетнего мальчика с ВЭБ-энцефалитом, у которого наблюдалась длительная лихорадка, экссудативный фарингит, снижение сознания и ригидность шеи. Магнитно-резонансная томография черепа показала усиление контраста в двусторонней корке островка и правом гипоталамусе. Диагноз был поставлен путем амплификации ДНК ВЭБ в образцах крови и спинномозговой жидкости.Он был выписан на терапию ацикловиром без каких-либо последствий.
1. Введение
Инфекция, вызванная вирусом Эпштейна-Барра (ВЭБ), часто встречается у детей и обычно проходит спонтанно [1]. Наиболее частые клинические проявления ВЭБ-инфекции включают инфекционный мононуклеоз, длительную лихорадку, лимфаденопатию, экссудативный тонзиллофарингит, средний отит и диарею [1, 2]. Хотя это крайне редко, ВЭБ может также вызывать поражение центральной нервной системы (ЦНС), такое как демиелинизирующее заболевание, острый энцефалит, менингит, менингоэнцефалит, миелит, полирадикулит, полирадикуломиелит, паралич черепных или периферических нервов и острая мозжечковая атаксия [1, 3, 4] .Кроме того, тяжелые поражения органов, связанные с ВЭБ, обычно наблюдаются у пациентов с ослабленным иммунитетом [5].
Вирус Эпштейна-Барра (EBV) был обнаружен как возбудитель в 2–5% случаев вирусных энцефалитов и менингитов [1, 6]. При ВЭБ-энцефалите пациенты могут иметь лихорадку, головную боль, ригидность шеи, изменение психического статуса, раздражительность, летаргию и, в редких случаях, коматозное состояние [1, 6, 7]. Вирус Эпштейна-Барра следует рассматривать как возможный возбудитель для любого ребенка с острым энцефалитом, поскольку клинические данные о EBV-энцефалите обычно неспецифичны [1].При диагностике ВЭБ-энцефалита могут быть полезны тесты на антитела к ВЭБ и нуклеиновые кислоты в крови или спинномозговой жидкости, а также исследования изображений черепа.
Здесь мы описываем случай 7-летнего мальчика с ВЭБ-энцефалитом с поражением серого вещества, двусторонней коры островка и гипоталамуса, который был выписан с терапией ацикловиром без каких-либо последствий.
2. История болезни
В отделение неотложной помощи поступил 7-летний мальчик с пониженным сознанием, бессвязной речью, галлюцинациями и продолжительной лихорадкой.У него были жалобы на тошноту, рвоту и диарею в течение 10 дней, и он получал пероральные антибиотики от фарингита. При физикальном обследовании выявлен экссудативный фарингит и скованность шеи. Результаты лабораторных анализов были следующими: гемоглобин: 12,5 г / дл, количество лейкоцитов: 11,3 × 10 9 / л, скорость оседания эритроцитов: 78 мм / ч и C-реактивный белок: 4 г / дл (0– 5). Трансаминазы печени были в пределах нормы. Выполнена люмбальная пункция. Давление открытия спинномозговой жидкости (ЦСЖ) составляло 100 мм / ч 2 О.Прямое микроскопическое исследование показало 80 эритроцитов / мм 3 и 20 лейкоцитов / мм 3 . Уровень белка в спинномозговой жидкости составлял 59 мг / дл, а уровень глюкозы в спинномозговой жидкости составлял 50 г / дл (одновременный уровень глюкозы в сыворотке: 130 г / дл). При первоначальной оценке анализ полимеразной цепной реакции (ПЦР) ЦСЖ на вирус простого герпеса типов 1 и 2 и энтеровирусы был отрицательным. Терапия ванкомицином, цефтриаксоном и ацикловиром была начата эмпирически на основании предварительного диагноза менингоэнцефалита.Магнитно-резонансная томография (МРТ) показала усиление контраста в задней части двусторонней коры островка, правом гипоталамусе и нижней левой лобной части коры головного мозга, что соответствует энцефалиту (рисунки 1 (а) и 1 (b)). Его уровень сознания ухудшился, и его оценка комы в Глазго снизилась с 15 до 12 в течение первых шести часов после госпитализации. Он не реагировал на словесные команды, и в его правой руке наблюдались тремор в состоянии покоя, ригидность и гипертонус. Электроэнцефалография (ЭЭГ) аномалий не показала.На третий день госпитализации была проведена повторная люмбальная пункция для изучения других редких вирусных причин энцефалита, аутоиммунных заболеваний и подострого склерозирующего панэнцефалита, поскольку клинического улучшения не было достигнуто. Количественная полимеразная цепная реакция (ПЦР) крови в реальном времени дала положительный результат на ВЭБ ниже 1500 копий / мл. Количественная ПЦР ЦСЖ в реальном времени дала положительный результат на ВЭБ на уровне 1600 копий / мл. Цитомегаловирус, вирус простого герпеса типов 1 и 2, пареховирус, эховирус и Mycobacterium tuberculosis ПЦР-анализы дали отрицательные результаты в спинномозговой жидкости.Между тем, серологический анализ вируса EBV в сыворотке позволял предположить первичную инфекцию, тогда как IgM к противовирусному капсидному антигену (VCA) EBV был положительным, а IgG к анти-VCA EBV отрицательным. Серологические тесты на энцефалит Западного Нила, вирусный энцефалит Японии, боррелиоз Лайма и корь были отрицательными в спинномозговой жидкости. Ванкомицин и цефтриаксон были отменены, а терапия ацикловиром была продолжена. На пятый день приема повысился уровень сознания. Терапия ацикловиром проводилась в течение 14 дней. Его обследовали на иммунодефицит; однако значительного иммунодефицита обнаружено не было.Его симптомы полностью исчезли, и он был выписан без каких-либо последствий.
На втором месяце наблюдения результаты МРТ черепа показали улучшение со значительным снижением контрастности, локализованной в коре головного мозга и лобной доле, и исчезновением поражений гипоталамуса (рис. 2). Результаты его физикального обследования были нормальными, жалоб не предъявлялось.
3. Обсуждение
Энцефалит, который представляет собой гистопатологическое определение воспаления паренхимы головного мозга, является тяжелым и смертельным заболеванием центральной нервной системы [8].Однако ВЭБ редко вызывает энцефалит, особенно у пациентов с ослабленным иммунитетом. В этой статье мы описываем случай ВЭБ-энцефалита у иммунокомпетентного ребенка с типичными симптомами вирусного энцефалита, такими как лихорадка, головная боль и изменение психического статуса.
Патогенез ВЭБ-энцефалита до сих пор неясен. Неврологические осложнения обычно возникают одновременно с типичными проявлениями инфекционного мононуклеоза; однако они также могут присутствовать на этапе разрешения инфекции.Возможные механизмы описаны как прямая вирусная инвазия в паренхиму головного мозга, инфильтрация цитотоксических Т-лимфоцитов в нервную ткань и отложение комплекса антитело-антиген в нервных структурах.
Кроме того, EBV может вызывать поражение ЦНС, такое как демиелинизирующее заболевание, острый энцефалит, менингит, миелит, полирадикулит, полирадикуломиелит и паралич черепных нервов [3, 4]. Сумайя [1] продемонстрировал, что ВЭБ был возбудителем в 3,6% случаев из 2357 пациентов, проживающих в Нью-Йорке, у которых был диагностирован менингит или энцефалит [9].
Хотя конкретное лечение ВЭБ-энцефалита является спорным, предыдущие сообщения предполагали, что терапия ацикловиром и кортикостероидами может быть разумной [10]. Хотя в нескольких отчетах было продемонстрировано, что противовирусные средства, включая ацикловир, валганцикловир, ганцикловир и цидофовир, обладают in vitro активностью против литической фазы инфекций EBV, противовирусные средства не одобрены для лечения инфекций EBV [9]. Ацикловир может снизить репликацию вируса и распространение вируса из носоглотки; однако его клинические преимущества еще предстоит выяснить [11].В этом случае терапия ацикловиром проводилась в течение 14 дней.
Хотя прогноз ВЭБ-энцефалита обычно хороший в большинстве случаев (85%), у некоторых пациентов он может быть фатальным [12, 13]. У нашего пациента терапия ацикловиром была начата эмпирически, а затем продолжалась для купирования тяжелых неврологических симптомов даже после того, как был поставлен диагноз ВЭБ. В некоторых сообщениях предлагалось использовать противовирусные препараты при тяжелой инфекции ВЭБ, что может быть полезным [14]. В исследовании с участием 45 пациентов с тяжелыми проявлениями ВЭБ-инфекции, включая поражение ЦНС и периферической нервной системы, тромбоцитопению, апластическую анемию, острую почечную недостаточность и миокардит, пациенты получали противовирусную терапию; Из них 39 имели благоприятный исход, шесть пациентов умерли [14].В этом исследовании ацикловир был наиболее часто назначаемой схемой противовирусной терапии в качестве монотерапии у 35 пациентов [14]. В другом исследовании Bathoorn et al. [15] сообщили, что все пациенты, получавшие ацикловир, полностью выздоровели, за исключением трех пациентов, которые не получали противовирусное лечение и имели стойкие симптомы; у одного из них было злокачественное новообразование, связанное с ВЭБ. В нашем случае мы продолжили противовирусную терапию ацикловиром, основываясь на большом количестве клинических опытов с этим агентом в литературе.
Кроме того, МРТ черепа является одним из наиболее полезных методов диагностики энцефалита.Он вызывает широкий спектр неврологических проявлений, связанных с ВЭБ, от небольшого локального усиления контраста до диффузных изменений интенсивности сигнала в белом или сером веществе и атрофии головного мозга [4, 16, 17]. В некоторых случаях результаты визуализации ЦНС могут быть ничем не примечательными. В большинстве случаев ВЭБ-энцефалита результаты МРТ преходящи и обычно разрешаются в течение короткого периода времени или через несколько месяцев [7, 18].
В заключение, ВЭБ-энцефалит может наблюдаться у иммунокомпетентных пациентов или пациентов с ослабленным иммунитетом, как у детей, так и у взрослых.Может быть полезна терапия ацикловиром; однако необходимы дальнейшие исследования для установления стандартного терапевтического подхода к лечению этой популяции пациентов.
Согласие
Письменное информированное согласие было получено от нашего пациента на публикацию этого описания случая и любых сопутствующих изображений.
