Дополнительное пероральное введение цинка для лечения диареи у детей
В странах с низким и средним уровнем дохода миллионы детей ежегодно страдают от тяжелой диареи и многие умирают от дегидратации (обезвоживания). Было показано, что приём жидкости через рот (с использованием раствора для пероральной регидратации) спасает жизни детей, но не оказывает влияния на продолжительность страдания детей от диареи. Дополнительное введение цинка может помочь уменьшить продолжительность и тяжесть диареи, и, следовательно, приносит дополнительную пользу по отношению к пероральным регидратационным растворам в снижении детской смертности.
Что такое пероральный цинк и как он может сократить продолжительность и тяжесть диареи
Цинк обычно применяют в виде сульфата цинка, ацетата цинка или глюконата цинка, все они являются водорастворимыми соединениями. Всемирная организация здравоохранения (ВОЗ) и Детский Фонд Организации Объединенных Наций (ЮНИСЕФ) рекомендует детям с диареей от 10 мг до 20 мг цинка в сутки.
Какие доказательства представлены в этом обзоре
Тридцать три клинических испытания, которые включали 10841 ребёнка, соответствовали критериям включения этого обзора.
Мы не знаем, влияет ли лечение цинком на смертность или число госпитализированных детей среди детей с острой диареей ( очень низкая уверенность в доказательствах). У детей старше 6 месяцев дополнительное введение цинка может сокращать среднюю продолжительность диареи примерно на половину суток (низкая уверенность в доказательствах) и, вероятно, уменьшает число детей, у которых диарея сохраняется на седьмые сутки ( умеренная уверенность в доказательствах).
Среди детей с сохраняющейся диареей дополнительное введение цинка, вероятно, сокращает среднюю продолжительность диареи примерно на 16 часов (умеренная уверенность в доказательствах) но, вероятно, увеличивает риск развития рвоты ( умеренная уверенность в доказательствах).
В районах с высокой распространенностью дефицита цинка или недостаточности питания цинк может быть полезным у детей в возрасте шести месяцев или старше. Имеющиеся в настоящее время доказательства не поддерживают использование дополнительного введения цинка у детей младше 6 месяцев, хорошо питающихся детей и в условиях, где дети имеют низкий риск дефицита цинка.
Имеющиеся в настоящее время доказательства не поддерживают использование дополнительного введения цинка у детей младше 6 месяцев, хорошо питающихся детей и в условиях, где дети имеют низкий риск дефицита цинка.
актуальность проблемы и новые возможности терапии – тема научной статьи по клинической медицине читайте бесплатно текст научно-исследовательской работы в электронной библиотеке КиберЛенинка
В ПОМОЩЬ ПРАКТИКУЮЩЕМУ ВРАЧУ
Острая диарея у взрослых: актуальность проблемы и новые возможности терапии
Ющук Н.Д., ФГБОУ ВО «Московский государственный медико-стоматологический
Андреев Д Н университет им. А.И. Евдокимова» Минздрава России
Кучерявый Ю.А.
В настоящее время острая диарея (ОД) представляет одну из ведущих проблем здравоохранения как в развитых, так и в развивающихся странах.
Лечение ОД основано на проведении патогенетической, регидратационной и симптоматической терапии, направленной на восстановление патофизиологических механизмов. Рацекадотрил — это новый анти-диарейный препарат симптоматического действия, оказывающий непосредственное супрессивное влияние на процессы гиперсекреции воды и электролитов в кишечнике, индуцированные патогенным влиянием вирусов и бактериальных токсинов. Эффективность рацекадотрила в лечении ОД у взрослых была продемонстрирована в ряде рандомизированных контролируемых клинических исследований и в нескольких метаанализах.
Терапия ОД рацекадотрилом четко показала выраженное превосходство над плацебо в отношении регрессии продолжительности диареи, а также количества и массы неоформленного стула.
Ключевые слова:
острая диарея, острые кишечные инфекции, симптоматическая терапия, лоперамид, рацекадотрил, Гидрасек
Инфекционные болезни: новости, мнения, обучение. 2017. № 4. С. 99-107.
Acute diarrhea in adults: urgency of the problem and new
Yushchuk N.D., Andreev D.N., A.I. Yevdokimov Moscow State University of Medicine and Dentistry
Kucheryavyy Yu. A. of the Ministry of Healthcare of the Russian Federation
A. of the Ministry of Healthcare of the Russian Federation
To date, acute diarrhea (AD) in adult population is one of the leading health problems in both developed and developing countries. Each year there are approximately 2.2 billion cases of AD worldwide. The AD-associated dehydration is a leading cause of mortality in this cohort of patients resulting in 1.3-2.5 million deaths each year. The management of AD is based on the pathogenetic treatment, rehydration therapy and symptomatic treatment aiming at restoring of pathophysiologic mechanisms. Racecadotril is a new symptomatic antidiarrheal drug exerting a direct suppressive effect on the intestinal water and electrolyte hypersecretion caused by pathogenic effects of viruses and bacterial toxins. The efficacy of racecadotril
 Treatment with racecadotril was characterized by its clear superiority over placebo in terms of regression of diarrhea duration and amount and weight of loose stool. Compared to reference therapy (loperamide), there were no significant differences in treatment effectiveness. However, it was found that treatment with racecadotril was associated with lower rates of constipation. A pharmacoeco-nomic evaluation revealed superiority of racecadotril over loperamide.
Treatment with racecadotril was characterized by its clear superiority over placebo in terms of regression of diarrhea duration and amount and weight of loose stool. Compared to reference therapy (loperamide), there were no significant differences in treatment effectiveness. However, it was found that treatment with racecadotril was associated with lower rates of constipation. A pharmacoeco-nomic evaluation revealed superiority of racecadotril over loperamide.acute diarrhea, acute intestinal infections, symptomatic therapy, loperamide, racecadotril, Hidrasec
Infectious Diseases: News, Opinions, Training. 2017; (4): 99-107.
Received: 21.04.2017. Accepted: 05.06.2017.
Согласно современным представлениям, острая диарея (ОД) — это учащенное опорожнение кишечника (3 раза в сутки и более) в виде жидкого или неоформленного стула продолжительностью до 14 сут [1, 2].
По разным данным, ежегодно в мире регистрируют от 1,7 до 2,7 млрд случаев ОД [6, 7]. В США доля случаев ОД в общей структуре госпитализаций среди взрослого населения составляет около 1,5% [8]. В России, по данным Роспотреб-надзора, в 2016 г. показатель заболеваемости ОКИ, ассоциированными с ОД, составил около 800 тыс. человек [9]. ОД приводит к миллионам смертей ежегодно, что особенно четко прослеживается в развивающихся странах [10]. По различным экспертным оценкам, ежегодно от диареи умирают 1,3-2,5 млн человек [11, 12], 85% случаев приходится на пациентов старше 65 лет [13]. Согласно данным Росстата, с 2015 по 2016 г. ОКИ стали причиной смерти более 600 человек [14]. В целом, ежегодно около 0,05% случаев ОД завершаюся летальным исходом [11].
Согласно данным Росстата, с 2015 по 2016 г. ОКИ стали причиной смерти более 600 человек [14]. В целом, ежегодно около 0,05% случаев ОД завершаюся летальным исходом [11].
ОКИ, ассоциированные с развитием ОД, имеют высокую социально-экономическую значимость и являются актуальной проблемой здравоохранения во всем мире в связи с высокой заболеваемостью, смертностью и объективными трудностями диагностики [15]. Данную группу инфекций объединяет развитие ОД с более чем 30 клиническими формами, причем возбудителями могут быть бактерии, вирусы и простейшие микроорганизмы [16]. В большинстве случаев ОД инфекционного генеза у взрослых обусловлена вирусами или патогенными бактериями [8]. В развитых странах в этиологической структуре ОД преобладают вирусные агенты, в то время как в развивающихся — бактериальные [17]. В большинстве случаев заражение происходит через конта-минированную воду или пищу [17]. Около 75-78% составляют ОКИ и пищевые токсикоинфекции с неустановленным возбудителем, что ограничивает возможности этиотропной
терапии [18]. ОД является результатом воздействия вирусов или бактериальных токсинов на энтероциты, что, с одной стороны, приводит к гиперсекреции воды в тонкой кишке, а с другой — к сниженной реабсорбции жидкости [19].
ОД является результатом воздействия вирусов или бактериальных токсинов на энтероциты, что, с одной стороны, приводит к гиперсекреции воды в тонкой кишке, а с другой — к сниженной реабсорбции жидкости [19].
Общие принципы лечения
С учетом того что дегидратация является ведущим синдромом при ОКИ и наиболее частой причиной смерти при ОД, она остается наиболее важным компонентом патогенетической терапии. Активное применение пероральной и парентеральной регидратации привело к серьезному снижению числа смертей от ОД, особенно в развитых странах [1, 20]. Несмотря на то что ОД вирусной этиологии имеет тенденцию к самоизлечению, она является патологическим состоянием, существенно снижающим качество жизни пациента и оказывающим негативное влияние на экономическую и социальную сферу страны, повышая частоту краткосрочной нетрудоспособности населения [21]. Более того, даже в индустриально развитых странах у взрослых пациентов диарея может приводить к смерти из-за органной недостаточности, развивающейся вторично вследствие дегидратации, особенно в пожилом возрасте [22]. Так, в США более половины смертей, ассоциированных с ОД, приходятся на пациентов пожилого возраста [13, 23].
Так, в США более половины смертей, ассоциированных с ОД, приходятся на пациентов пожилого возраста [13, 23].
Среди симптоматических препаратов в клинической практике пациентам с ОД нередко назначают терапию анти-диарейными препаратами в комбинации с пероральной регидратацией. Данная тактика позволяет ускорить регрессию симптоматики заболевания и снизить потребность в повторных курсах корригирующей регидратационной терапии [24]. Наиболее часто в общемировой клинической практике для этих целей используется лоперамид — агонист периферических |_1-опиодных рецепторов, локализующихся в энтеральной нервной системе (преимущественно в межмышечных нервных сплетениях кишечника) [25, 26]. Однако, несмотря на доказанную эффективность в лечении диарей, применение лоперамида имеет ряд ограничений. Учитывая механизм его действия, использование данного препарата при лечении ОД может привести к вторичному запору [27]. В этом случае элиминация патогенов из организма может задерживаться, что крайне нежелательно при ОКИ [28].
По этой причине Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration, FDA) считает, что лопе-рамид противопоказан пациентам с бактериальным энтероколитом, вызванным инвазивными микроорганизмами, включая роды Salmonella, Shigelb и Campylobacter, а также пациентам с псевдомембранозным колитом, для лечения которого используются антибиотики широкого спектра действия [29]. Помимо этого, лоперамид имеет значительный потенциал для межлекарственного взаимодействия, поскольку он метаболизируется изоферментами цитохрома P450 — 2C8 и 3А4. Соответственно совместное применение лекарственных препаратов, ингибирующих данные изоферменты, может значительно повысить концентрацию лоперамида в плазме крови [30]. Более того, отмечен ограниченный центральный эффект лоперамида, который во многом обусловлен тем, что он является субстратом для P-гликопротеина. Таким образом, ингибиторы P-гликопротеина могут повысить не только уровень лоперамида в плазме крови [30], но и его доступ к головному мозгу [31].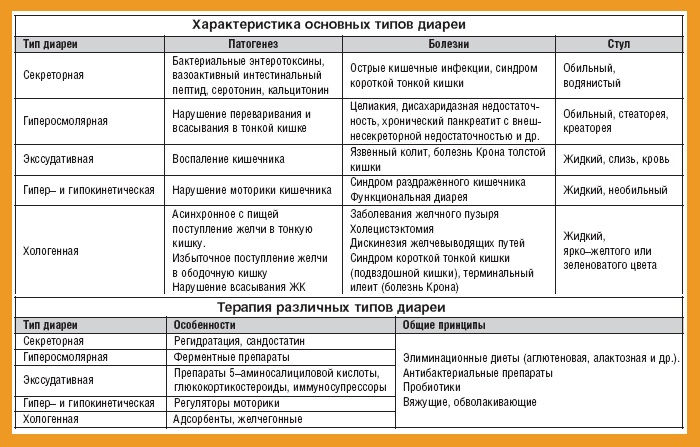 Основываясь на этом взаимодействии препаратов, а также на случаях передозировки и злоупотребления, FDA недавно предупредило о риске возникновения серьезных кардиологических проблем при приеме лоперамида [31, 32].
Основываясь на этом взаимодействии препаратов, а также на случаях передозировки и злоупотребления, FDA недавно предупредило о риске возникновения серьезных кардиологических проблем при приеме лоперамида [31, 32].
Помимо лоперамида, для симптоматического лечения ОД у взрослых используют пробиотические препараты (в частности, Lactobacillus rhamnosus GG и Saccharomyces boulardii) и диоктаэдрический смектит. Некоторые пробиотики доказали свою эффективность в рамках профилактики псев-домембранозного колита, однако количество плацебо-контролируемых исследований среди взрослых с ОД инфекционного генеза ограничено [33]. Согласно последним рекомендациям Американской коллегии гастроэнтерологов (ACG, 2016 г.), не рекомендуется использовать пробиотики для лечения ОД, за исключением случаев антибиотикоассоцииро-ванной диареи [1]. В свою очередь эффективность диокта-эдрического смектита подтверждена у взрослых пациентов с хроническим течением функциональной диареи, включая синдром раздраженного кишечника [34, 35].
Новые возможности симптоматической терапии
С 2017 г. в России зарегистрирован антидиарейный препарат принципиально другого механизма действия -рацекадотрил (Гидрасек), оказывающий непосредственное супрессирующее влияние на процессы гиперсекреции воды и электролитов в кишечнике, индуцированные патогенным влиянием вирусов и бактериальных токсинов [19, 36]. Рацекадотрил предназначен для симптоматической терапии ОД у взрослых в сочетании с регидратацион-ной терапией в тех случаях, когда это необходимо, а также совместно с антибиотиками он может применяться в качестве дополнительной терапии бактериальной ОД. Рацекадо-трил зарегистрирован во Франции в качестве средства для лечения ОД у взрослых с 1992 г., в настоящее время этот лекарственный препарат применяется в 92 странах мира.
Эффективность рацекадотрила при лечении ОД у взрослых (независимо от причины и степени ее тяжести) установлена в рамках 15 рандомизированных исследований, 10 из которых были двойными слепыми.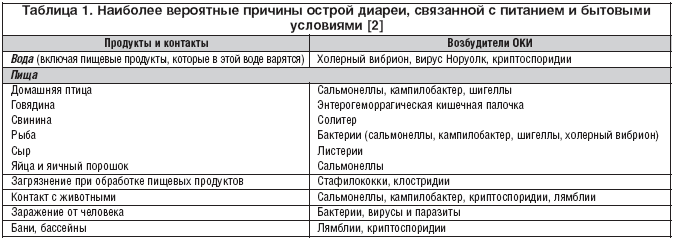 Клинические результаты проявления фармакодинамических свойств — это отсутствие вторичных запоров, быстрое исчезновение боли и вздутия живота [37].
Клинические результаты проявления фармакодинамических свойств — это отсутствие вторичных запоров, быстрое исчезновение боли и вздутия живота [37].
Попадая в кровь, рацекадотрил под действием неспецифических эстераз быстро трансформируется в свою активную форму — тиорфан, который оказывает непосредственное ингибирующее действие на фермент энкефалиназу [36]. Энкефалиновые нейротрансмиттеры играют важную роль в контроле секреции желудочно-кишечного тракта. Действие энкефалина обычно прекращается под влиянием энкефали-назы. Тиорфан, активный метаболит рацекадотрила, является ингибитором данного фермента, он повышает концентрацию энкефалина путем его защиты от ферментативной деградации [19]. При этом формируются повышенные си-наптические концентрации энкефалина, которые действуют на 5-опиоидные рецепторы, расположенные на клеточной поверхности энтероцитов [38]. Активация этих рецепторов снижает активность аденилатциклазы, которая катализирует превращение АТФ в циклическую форму АМФ (цАМФ). ), осуществляющего транспорт ионов хлора через мембрану клетки (см. рисунок). Снижение секреции ионов хлора в просвет кишечника идет параллельно снижению экскреции жидкости и других ионов [36, 38]. Таким образом, рацекадотрил оказывает антисекреторный эффект в кишечнике, уменьшая гиперсекрецию воды и электроли-
), осуществляющего транспорт ионов хлора через мембрану клетки (см. рисунок). Снижение секреции ионов хлора в просвет кишечника идет параллельно снижению экскреции жидкости и других ионов [36, 38]. Таким образом, рацекадотрил оказывает антисекреторный эффект в кишечнике, уменьшая гиперсекрецию воды и электроли-
Токсины вирусов и бактерий
Na+ K+
h3O
{+-»- Аденилатциклаза
Gi
J
Энкефалин
Энкефалиназа Рацекадотрил
Механизм действия рацекадотрила
Cl
Обзор ключевых рандомизированных исследований применения рацекадотрила у взрослых пациентов с острой диареей
Автор, год Дизайн Количество пациентов в группах Лечение Результаты (первичная конечная точка)
Сравнение с плацебо
Ваитег Двойное слепое 95/98 Рацекадотрил: 200 мг, затем 100 мг Продолжительность диареи:
и соавт. , рандомизированное после каждого неоформленного стула, 3,4±0,1 сут
, рандомизированное после каждого неоформленного стула, 3,4±0,1 сут
1992 [40] плацебо- в течение 10 сут или до выздоровления
контролируемое Плацебо Продолжительность диареи: 4,4±0,2 сут
Натна Двойное слепое 32/38 Рацекадотрил: 100 мг 3 раза в сутки Масса стула на 1-е сутки —
и соавт., рандомизированное в течение 6 сут или до выздоровления 355±35г
1999 [41] плацебо-контролируемое Плацебо Масса стула на 1-е сутки -499±46г
Сравнение с лоперамидом
Двойное слепое 37/32 Рацекадотрил: 200 мг на начальном Задержка в разрешении
и соавт., рандомизированное этапе, затем 200 мг через 12 ч, затем диареи — 2,2±0,2 сут
1993 [44] исследование с активным контролем 100 мг 3 раза в сутки в течение 7 сут или до выздоровления
Лоперамид: 2,66 мг на начальном Задержка в разрешении
этапе, затем 2,66 мг через 12 ч. диареи — 2,3±0,2 сут
диареи — 2,3±0,2 сут
В последующем 1,33 мг 3 раза в сутки
в течение 7 сут или до выздоровления
Уе1е! Двойное слепое 77/70 Рацекадотрил: 100 мг 3 раза в сутки Количество дефекаций
и соавт., рандомизированное в течение 7 сут или до выздоровления с жидким стулом до
1999 [45] исследование выздоровления — 3,5±0,5
с активным контролем Лоперамид: 2 мг после каждого жидкого стула Количество дефекаций с жидким стулом до выздоровления — 2,9±0,4
Ргас1о Простое слепое 473/471 Рацекадотрил: 100 мг 3 раза в сутки Продолжительность диареи —
и соавт., рандомизированное до выздоровления 55 ч (95% ДИ 50-65)
2002 [46] исследование Лоперамид: 2 мг 3 раза в сутки до выздоровления Продолжительность диареи -55 ч (95% ДИ 48-66)
ваПеШ Двойное слепое 30/31 Рацекадотрил: 100 мг 3 раза в сутки Продолжительность диареи —
и соавт. , рандомизированное до выздоровления 36±4 ч
, рандомизированное до выздоровления 36±4 ч
2010 [47] исследование Лоперамид: 4 мг, далее 2 мг после Продолжительность диареи —
с активным контролем каждого неоформленного стула до выздоровления 63±6 ч
Сравнение с Saccharomyces Ьои1агсШ
Могаев Е. Простое слепое 175/161 Рацекадотрил: 100 мг 3 раза в сутки Продолжительность диареи —
и соавт., рандомизированное до выздоровления 64 ч
2001 [48] исследование Saccharomyces Ьои!агСИ: 100 мг 2 раза в сутки до выздоровления Продолжительность диареи -77 ч
ДИ — доверительный интервал.
тов, не влияя на базальную секрецию. При этом рацекадо-трил не влияет на моторику кишечника и скорость кишечного транзита.
При этом рацекадо-трил не влияет на моторику кишечника и скорость кишечного транзита.
Доказательная база рацекадотрила
К настоящему времени эффективность рацекадотрила в лечении ОД у взрослых была продемонстрирована в ряде рандомизированных контролируемых клинических исследований и в нескольких метаанализах (см. таблицу) [39-48]. Терапия данным препаратом характеризовалась четко выраженным превосходством над плацебо в отноше-
нии регрессии продолжительности диареи, а также количества и массы неоформленного стула. Так, в первом пла-цебо-контролируемом исследовании препарата Р. Ваитег и соавт. [40] показали, что продолжительность диареи в группе рацекадотрила была меньше (лечение продолжалось 4,4±0,2 сут в группе плацебо и 3,4±0,1 сут в группе рацекадотрила, р=0,001), а в конце исследования неоформленный стул наблюдался у 23,5% пациентов, получавших плацебо, и только у 7,4% пациентов, получавших рацекадотрил (р<0,002). Аналогичным образом такие проявления, как жжение в анальной области, боль в животе, тошнота, анорек-сия, боль при пальпации живота и вздутие живота, в группе
Аналогичным образом такие проявления, как жжение в анальной области, боль в животе, тошнота, анорек-сия, боль при пальпации живота и вздутие живота, в группе
Гидрасек
(Рацекадотрил)
Инновационная терапия для быстрой остановки диареи
БЫСТРЫЙ ЭФФЕКТ
• Начинает работать через 30 мин2
• Останавливает диарею с первых суток терапии3
УНИКАЛЬНЫЙ МЕХАНИЗМ ДЕЙСТВИЯ9
• Останавливает патологическое образование жидкости2 в кишечнике
• Снижает потери воды электролитов7
БЕЗОПАСНЕЕ ЛОПЕРАМИДА
• Без запоров и вздутия2
• В сравнении с лоперамидом частота побочных эффектов до 5 раз ниже4
МИРОВОМ зарегистрирован в
опыт 92
странах мира (в т. ч. с ОТС статусом)1
ч. с ОТС статусом)1
включен в мировые стандарты терапии острой диареи5-6-8
125
МЛН
пациентов получили лечение
1 капсула 3 раза в день
RUHID172591 от 29.06.2017 г.
Гидрасек
Регистрационный номер: ЛП-004150
Международное непатентованное наименование: рацекадотрил Лекарственная форма: капсулы, 100 мг
Фармакотерапевтическая группа: противодиарейное средство
Фармакодинамика. Рацекадотрил является кишечным антисекреторным веществом. Оно уменьшает кишечную гиперсекрецию воды и электролитов, вызываемую энтеротоксином холеры или воспалением, и не влияет на базальную секрецию кишечника. Рацекадотрил оказывает быстрое противодиарейное действие, не изменяя время прохождения кишечного содержимого через кишечник. Рацекадотрил не вызывает вздутия живота. В клинических исследованиях частота возникновения вторичных запоров при приеме рацекадотрила была сравнима с плацебо*. Показания к применению. Симптоматическое лечение острой диареи у взрослых. Противопоказания. Гиперчувствительность к действующему веществу или любому другому компоненту препарата. Врожденная непереносимость галактозы, недостаточность лактазы, синдром глюкозо-галактозной мальабсорбции (в связи с тем, что препарат содержит лактозу). Беременность и период грудного вскармливания. Детский возраст до 18 лет (из-за высокого содержания действующего вещества). Применение при беременности и в период грудного вскармливания. В связи с отсутствием соответствующих данных не следует применять препарат Гидрасек во время беременности и в период грудного вскармливания*.
Оно уменьшает кишечную гиперсекрецию воды и электролитов, вызываемую энтеротоксином холеры или воспалением, и не влияет на базальную секрецию кишечника. Рацекадотрил оказывает быстрое противодиарейное действие, не изменяя время прохождения кишечного содержимого через кишечник. Рацекадотрил не вызывает вздутия живота. В клинических исследованиях частота возникновения вторичных запоров при приеме рацекадотрила была сравнима с плацебо*. Показания к применению. Симптоматическое лечение острой диареи у взрослых. Противопоказания. Гиперчувствительность к действующему веществу или любому другому компоненту препарата. Врожденная непереносимость галактозы, недостаточность лактазы, синдром глюкозо-галактозной мальабсорбции (в связи с тем, что препарат содержит лактозу). Беременность и период грудного вскармливания. Детский возраст до 18 лет (из-за высокого содержания действующего вещества). Применение при беременности и в период грудного вскармливания. В связи с отсутствием соответствующих данных не следует применять препарат Гидрасек во время беременности и в период грудного вскармливания*._575.gif) Способ применения и дозы. Для приема внутрь. Первую капсулу в начале лечения принимают независимо от времени суток. Далее — одну капсулу три раза в день перед едой. Лечение необходимо продолжать до нормализации стула (появления нормального кала до двух раз), но не более 7 дней. Не рекомендуется применять рацекадотрил длительное время. Коррекция дозы препарата для пациентов пожилого возраста не требуется. Побочное действие. Сообщения о следующих нежелательных реакциях были отмечены при приеме рацекадотрила чаще, чем при приеме плацебо, или были получены в период постмаркетингового применения. Нарушения со стороны нервной системы: часто (г 1/100, < 1/10) головная боль. Нарушения со стороны кожи и подкожных тканей: нечасто (а 1/1000, < 1/100) кожная сыпь, эритема. Частота неизвестна (для оценки частоты случаев имеющихся данных недостаточно): полиморфная эритема, отек языка, отек лица, отек губ, отек век, ангионевротический отек, крапивница, узловатая эритема, папулезная сыпь, пруриго, кожный зуд, токсический дерматит.
Способ применения и дозы. Для приема внутрь. Первую капсулу в начале лечения принимают независимо от времени суток. Далее — одну капсулу три раза в день перед едой. Лечение необходимо продолжать до нормализации стула (появления нормального кала до двух раз), но не более 7 дней. Не рекомендуется применять рацекадотрил длительное время. Коррекция дозы препарата для пациентов пожилого возраста не требуется. Побочное действие. Сообщения о следующих нежелательных реакциях были отмечены при приеме рацекадотрила чаще, чем при приеме плацебо, или были получены в период постмаркетингового применения. Нарушения со стороны нервной системы: часто (г 1/100, < 1/10) головная боль. Нарушения со стороны кожи и подкожных тканей: нечасто (а 1/1000, < 1/100) кожная сыпь, эритема. Частота неизвестна (для оценки частоты случаев имеющихся данных недостаточно): полиморфная эритема, отек языка, отек лица, отек губ, отек век, ангионевротический отек, крапивница, узловатая эритема, папулезная сыпь, пруриго, кожный зуд, токсический дерматит. Передозировка. В настоящее время известны единичные случаи передозировки без побочных эффектов. У взрослых прием однократной дозы препарата более 2 г, эквивалентной 20-кратной терапевтической дозе, неблагоприятных эффектов не вызывал. Взаимодействие с другими лекарственными препаратами. В настоящее время данные о взаимодействии с другими препаратами отсутствуют*. Особые указания. Применение препарата Гидрасек не освобождает от проведения пероральной регидратации в тех случаях, когда она необходима. Монотерапия рацекадотрилом при наличии кровянистых или гнойных выделений в стуле и высокой температуре противопоказана. В качестве дополнительной терапии острой бактериальной диареи рацекадотрил может применяться совместно с антибиотиками. Не рекомендуется применять рацекадотрил при антибиотик-ассоциированной диарее и хронической диарее. С осторожностью следует применять пациентам с почечной и печеночной недостаточностью. Биодоступность может быть снижена при многократной рвоте*. Влияние на способность к управлению автомобилем и другими механизмами.
Передозировка. В настоящее время известны единичные случаи передозировки без побочных эффектов. У взрослых прием однократной дозы препарата более 2 г, эквивалентной 20-кратной терапевтической дозе, неблагоприятных эффектов не вызывал. Взаимодействие с другими лекарственными препаратами. В настоящее время данные о взаимодействии с другими препаратами отсутствуют*. Особые указания. Применение препарата Гидрасек не освобождает от проведения пероральной регидратации в тех случаях, когда она необходима. Монотерапия рацекадотрилом при наличии кровянистых или гнойных выделений в стуле и высокой температуре противопоказана. В качестве дополнительной терапии острой бактериальной диареи рацекадотрил может применяться совместно с антибиотиками. Не рекомендуется применять рацекадотрил при антибиотик-ассоциированной диарее и хронической диарее. С осторожностью следует применять пациентам с почечной и печеночной недостаточностью. Биодоступность может быть снижена при многократной рвоте*. Влияние на способность к управлению автомобилем и другими механизмами. Применение препарата Гидрасек не влияет или оказывает незначительное влияние на способность к управлению автомобилем и механизмами. Срок годности. 3 года*. Условия отпуска. Отпускают по рецепту. * Полная информация по препарату представлена в инструкции по медицинскому применению. СИП от 23.03.2017 на основании ИМП от 21.02.2017.
Применение препарата Гидрасек не влияет или оказывает незначительное влияние на способность к управлению автомобилем и механизмами. Срок годности. 3 года*. Условия отпуска. Отпускают по рецепту. * Полная информация по препарату представлена в инструкции по медицинскому применению. СИП от 23.03.2017 на основании ИМП от 21.02.2017.
1. Внутренние данные ООО «Эбботт Лэбораториз» о количестве стран, в которых в настоящий момент зарегистрирован рацекадотрил.
2. Инструкция по медицинскому применению препарата Гидрасек (рацекадотрил), капсулы 100 мг, от 21.02.2017.
3. Vetel J.M., Berard Н„ Fretault N., Lecomte J.M. Comparison of racecadotril and loperamide in adults with acute diarrhea. Aliment Pharmacol Ther. 1999; 13Suppl 6: 21-26.
4. Gallelli L., Colosimo M., Tolotta G.A. et al. Prospective randomized double-blind trial of racecadotril compared with loperamide in elderly people with gastroenteritis living in nursing homes. Eur J Clin Pharmacol. 2010; 66(2): 137-144.
Prospective randomized double-blind trial of racecadotril compared with loperamide in elderly people with gastroenteritis living in nursing homes. Eur J Clin Pharmacol. 2010; 66(2): 137-144.
5. Alfredo Guarino et al. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition/European Society for Pediatric Infectious Diseases Evidence-Based Guidelines for the Management of Acute Gastroenteritis in Children in Europe: Update 2014.
6. Глобальные практические рекомендации Всемирной гастроэнтерологической организации. Острая диарея у взрослых и детей: глобальная перспектива. World Gastroenterology Organisation, 2012.
7. Hinterleitner T.A., Petritsch W., Dimsity G., Berard H., Lecomte J.M., Krejs G.J. Acetorphan prevents cholera-toxin induced water and electrolyte secretion in the human jejunum. Eur J Gastroenterol Hepatol. 1997; 9: 887-891.
1997; 9: 887-891.
8. Riddle M.S. et al. ACG Clinical Guideline: Diagnosis, Treatment, and Prevention of Acute Diarrheal Infections in Adults. Am J Gastroenterol. 2016; 111: 602-622.
9. Lecomte J.M. An overview of clinical studies with racecadotril in adults. Int J Antimicrob Agents. 2000; 14(1): 81-87. Регистрационное удостоверение ЛП-004150
Информация предназначена для медицинских и фармацевтических работников.
ООО «Эбботт Лэбораториз»
125171, Москва, Ленинградское шоссе, д. 16а, стр. 1, бизнес-центр «Метрополис» Тел.: 8 (495) 258-42-80 www.abbott-russia.ru
R Abbott
„
Гидрасек
плацебо встречались чаще, чем в группе рацекадотрила [40]./82/82.jpg) В другом плацебо-контролируемом исследовании H. Hamza и соавт. [41] продемонстрировали, что масса стула на 1-й день лечения в группе рацекадотрила была значительно меньше, чем в группе плацебо (355+35 и 499±46 г, p=0,025), как и количество дефекаций с жидким стулом (4,3+0,4 и 5,4+0,4, p=0,027). На 4-е сутки лечения признаки и симптомы в обеих группах были сравнимы, за исключением вздутия живота, которое в группе рацекадотрила встречалось реже (5,6%), чем в группе плацебо (18,2%) [41].
В другом плацебо-контролируемом исследовании H. Hamza и соавт. [41] продемонстрировали, что масса стула на 1-й день лечения в группе рацекадотрила была значительно меньше, чем в группе плацебо (355+35 и 499±46 г, p=0,025), как и количество дефекаций с жидким стулом (4,3+0,4 и 5,4+0,4, p=0,027). На 4-е сутки лечения признаки и симптомы в обеих группах были сравнимы, за исключением вздутия живота, которое в группе рацекадотрила встречалось реже (5,6%), чем в группе плацебо (18,2%) [41].
Согласно результатам метаанализа, опубликованного в 2014 г., терапия рацекадотрилом значительно эффективнее плацебо при разрешении диареи у взрослых [отношение рисков (ОР) = 1,65 [1,38; 1,97], p<0,00001] [39]. В другом метаанализе, построенном на многоуровневых моделях оценки индивидуальных данных пациентов, было показано, что по сравнению с плацебо минимальная эффективная доза рацекадотрила (100 мг) вызывала увеличение доли выздоровевших пациентов на 80% в любой момент времени [ОР=1,8 [1,3, 2,5], p<0,001], доли ответивших на лечение, т. е. выздоровевших в течение 3 сут, — на 60% (p<0,001), уменьшение боли в животе и тошноты — на 47% и снижение общего количества дней нетрудоспособности — на 33% (p<0,001) [43].
е. выздоровевших в течение 3 сут, — на 60% (p<0,001), уменьшение боли в животе и тошноты — на 47% и снижение общего количества дней нетрудоспособности — на 33% (p<0,001) [43].
По сравнению с эталонной терапией (лоперамидом) значительных различий по параметрам эффективности в рандомизированных исследованиях не наблюдалось, однако было отмечено, что при приеме рацекадотрила вторичные запоры развивались реже [39, 44-47]. Так, в двойном слепом рандомизированном исследовании J. Roge и соавт. [44] эффективность рацекадотрила и лоперамида была признана эквивалентной. Частота разрешения диареи на 2-е сутки составила 59,3% в группе рацекадотрила и 50,0% в группе лоперамида. Тем не менее частота продолжительности вздутия живота более 1 дня в группе рацекадотрила была значительно ниже (27%), чем в группе лоперамида (50%, p<0,05). При этом частота развития запора после разрешения диареи у пациентов, получавших рацекадотрил, была значительно ниже, чем у пациентов, получавших лоперамид (8,1 и 31,3%, p<0,02) [44]. В исследовании J.M. VeteL и соавт. [45] также не выявлено статистически значимых различий в отношении первичных и вторичных характеристик эффективности (количество дефекаций с жидким стулом, продолжительность диареи, частота ассоциированных симптомов) между группами рацекадотрила и лоперамида. Однако частота развития вторичного запора на фоне терапии была выше в группе лоперамида (18,7 против 9,8%). При этом тяжелые запоры наблюдали только у пациентов, получавших лоперамид [45]. В более крупном многонациональном сравнительном исследовании (473 пациента в группе рацекадотрила, 471 пациент в группе лоперамида) отмечено, что у пациентов, получавших лоперамид, статистически значимо повышена частота запоров по сравнению с пациентами, получавшими рацекадотрил (25 и 16% соответственно, p=0,001) [46].
В исследовании J.M. VeteL и соавт. [45] также не выявлено статистически значимых различий в отношении первичных и вторичных характеристик эффективности (количество дефекаций с жидким стулом, продолжительность диареи, частота ассоциированных симптомов) между группами рацекадотрила и лоперамида. Однако частота развития вторичного запора на фоне терапии была выше в группе лоперамида (18,7 против 9,8%). При этом тяжелые запоры наблюдали только у пациентов, получавших лоперамид [45]. В более крупном многонациональном сравнительном исследовании (473 пациента в группе рацекадотрила, 471 пациент в группе лоперамида) отмечено, что у пациентов, получавших лоперамид, статистически значимо повышена частота запоров по сравнению с пациентами, получавшими рацекадотрил (25 и 16% соответственно, p=0,001) [46].
Согласно данным метаанализа, обобщившего результаты 12 клинических исследований, при сравнении эффективности рацекадотрила и лоперамида продолжительность диареи была эквивалентна [0Р=1,08 [0,95; 1,22], р=0,24]. При этом
При этом
частота развития запора на фоне терапии рацекадотрилом была сопоставима с плацебо [ОР=0,95 [0,24; 3,68], р=0,97] и значительно ниже по сравнению с лоперамидом [ОР=0,34 [0,22; 0,51], р<0,0001] [42].
Отдельно стоит отметить, что рацекадотрил показал свою эффективность и безопасность у пожилых пациентов (73 года — 96 лет) с ОД. Так, по результатам двойного слепого рандомизированного исследования L. GaLLeLLi и соавт. [47], у пациентов, получавших рацекадотрил, продолжительность диареи была значительно меньше, чем у пациентов, получавших лоперамид (36 и 63 ч соответственно, р<0,01). Кроме того, в группе рацекадотрила были значительно ниже такие показатели, как продолжительность боли в животе (14 и 28 ч соответственно, р<0,01) и общая масса жидкого стула до выздоровления (120 и 150 г на 1 кг массы тела соответственно, р<0,01). Нежелательные явления регистрировались у 12% пациентов, получавших рацекадотрил, и у 60% пациентов группы лоперамида. Тошнота чаще встречалась в группе лоперамида, а не в группе рацекадотрила (20 и 10% соответственно), это было характерно и для запоров (60 и 15% соответственно). Побочные явления и отсутствие эффекта от применения лоперамида ведут к значительному повышению непосредственных затрат на лечение. Фактически при анализе затрат в когорте пациентов с назначенным лечением стоимость терапии лоперамидом была в 2 раза выше по сравнению с затратами на лечение рацекадотрилом [47].
Тошнота чаще встречалась в группе лоперамида, а не в группе рацекадотрила (20 и 10% соответственно), это было характерно и для запоров (60 и 15% соответственно). Побочные явления и отсутствие эффекта от применения лоперамида ведут к значительному повышению непосредственных затрат на лечение. Фактически при анализе затрат в когорте пациентов с назначенным лечением стоимость терапии лоперамидом была в 2 раза выше по сравнению с затратами на лечение рацекадотрилом [47].
Эффективность рацекадотрила по сравнению с пробио-тическим препаратом, содержащим БассЬаготусез Ьои1агСИ, в рамках лечения ОД у взрослых сравнивали в слепом исследовании, проведенном в Бразилии [48]. Эффективность лечения в обеих группах была сопоставима, однако время выздоровления (64 против 77 ч) и число дефекаций в течение суток до момента выздоровления (52 против 76 среди тех, у кого оно на момент начала исследования было 3-5 раз, и 70 против 87 среди у тех, у кого в начале исследования данное число превышало 8) были значительно меньше в группе рацекадотрила, чем в группе лечения пробиотиком. При анализе методом Каплана-Мейера расчетная вероятность выздоровления на 2-е сутки составила 42% для рацекадотрила по сравнению с 21% для БассЬаготусез Ьои1агСИ. Соответствующие показатели для 3-х суток составили 67 и 55%. Частота нежелательных явлений — 6,8% в группе рацекадотрила и 7,1% в группе пациентов, принимавших БассЬаготусез Ьои1огСИ [48].
При анализе методом Каплана-Мейера расчетная вероятность выздоровления на 2-е сутки составила 42% для рацекадотрила по сравнению с 21% для БассЬаготусез Ьои1агСИ. Соответствующие показатели для 3-х суток составили 67 и 55%. Частота нежелательных явлений — 6,8% в группе рацекадотрила и 7,1% в группе пациентов, принимавших БассЬаготусез Ьои1огСИ [48].
Заключение
Вышеизложенное позволяет сделать вывод, что рацекадотрил является новым симптоматическим антидиарейным препаратом, оказывающим непосредственное супрессивное влияние на процессы гиперсекреции воды и электролитов в кишечнике, индуцированные патогенным влиянием вирусов и бактериальных токсинов. Эффективность рацекадотрила в лечении ОД у взрослых пациентов была продемонстрирована в ряде рандомизированных контролируемых клинических исследований и в нескольких метаанализах. Терапия данным препаратом характеризовалась четко выраженным превосходством над плацебо в отношении регрессии продолжительности диареи, а также количества и массы неоформленного
стула. По сравнению с эталонной терапией (лоперамид) значительных различий по параметрам эффективности не отмечено, однако было установлено, что при приеме рацека-дотрила запоры развиваются реже, что важно с учетом патофизиологических механизмов развития ОКИ. По сравнению с пробиотиком БассЬаготусез Ьои1огСИ рацекадотрил показал несколько большую эффективность, но сходную переноси-
По сравнению с эталонной терапией (лоперамид) значительных различий по параметрам эффективности не отмечено, однако было установлено, что при приеме рацека-дотрила запоры развиваются реже, что важно с учетом патофизиологических механизмов развития ОКИ. По сравнению с пробиотиком БассЬаготусез Ьои1огСИ рацекадотрил показал несколько большую эффективность, но сходную переноси-
мость. Таким образом, внедрение в клиническую практику рацекадотрила в качестве симптоматической терапии с доказанным противодиарейным эффектом и принципиально отличным от других антидиарейных препаратов антисекреторным механизмом действия позволяет диверсифицировать схемы лечения и открывает новые перспективы ведения этой непростой группы пациентов.
СВЕДЕНИЯ ОБ АВТОРАХ
Ющук Николай Дмитриевич — академик РАН, доктор медицинских наук, профессор, заведующий кафедрой инфекционных болезней и эпидемиологии, президент ФГБОУ ВО «Московский государственный медико-стоматологический университет им.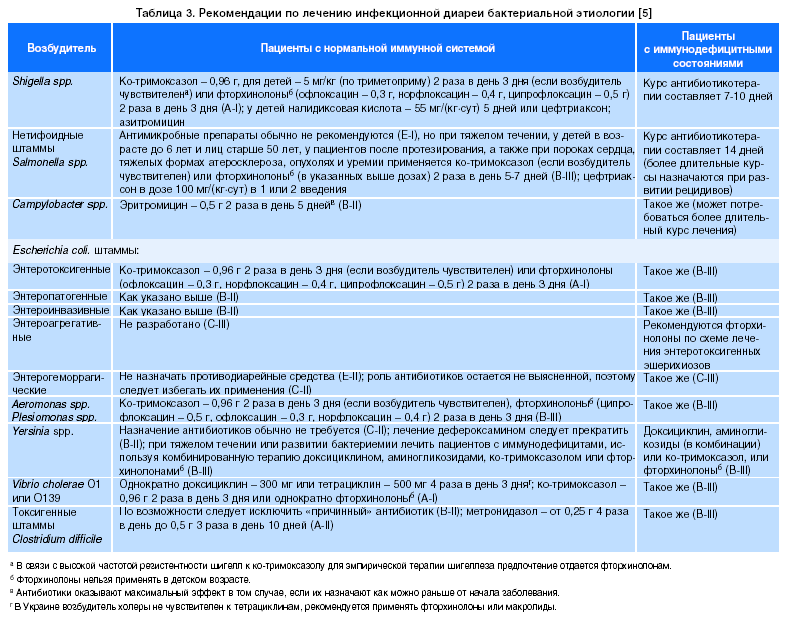 А.И. Евдокимова» Минздрава России, член Правления Национального научного общества инфекционистов, председатель Учебно-методической комиссии по инфекционным болезням Координационного совета по области образования «Здравоохранение и медицинские науки» E-mail: [email protected]
А.И. Евдокимова» Минздрава России, член Правления Национального научного общества инфекционистов, председатель Учебно-методической комиссии по инфекционным болезням Координационного совета по области образования «Здравоохранение и медицинские науки» E-mail: [email protected]
Андреев Дмитрий Николаевич — кандидат медицинских наук, ассистент кафедры пропедевтики внутренних болезней и гастроэнтерологии ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России E-mail: [email protected]
Кучерявый Юрий Александрович — кандидат медицинских наук, доцент кафедры пропедевтики внутренних болезней и гастроэнтерологии ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России
ЛИТЕРАТУРА
1. Riddle M.S., DuPont H.L., Connor B.A. ACG Clinical Guideline: diagnosis, treatment, and prevention of acute diarrheal infections in adults // Am. J. Gastroenterol. 2016. Vol. 111, N 5. P. 602-622.
Riddle M.S., DuPont H.L., Connor B.A. ACG Clinical Guideline: diagnosis, treatment, and prevention of acute diarrheal infections in adults // Am. J. Gastroenterol. 2016. Vol. 111, N 5. P. 602-622.
2. Guarino A., ALbano F., Ashkenazi S. et aL. European Society for Pae-diatric Gastroenterology, HepatoLogy, and Nutrition/European Society for Paediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe // J. Pediatr. Gastroenterol. Nutr. 2008. Vol. 46, suppL. 2. P. S81-S122.
3. BaLdi F., Bianco M.A., Nardone G., PiLotto A. et aL. Focus on acute diar-rhoeaL disease // World J. Gastroenterol. 2009. VoL. 15, N 27. P. 3341-3348.
4. Manatsathit S., Dupont H.L., Farthing M. et aL. Guideline for the management of acute diarrhea in adults // J. Gastroenterol. HepatoL. 2002. VoL. 17, suppL. P. S54-S71.
17, suppL. P. S54-S71.
5. Кожухова Е.А., Андреева Н.В., Иващенко В.Д. Этапный анализ результатов выявления возбудителей острых диарей для верификации диагноза у взрослых пациентов // Инфекция и иммунитет. 2016. № 4. С. 379-383.
6. DiarrhoeaL disease. Fact sheet No.°330. WorLd HeaLth Organization, ApriL 2013. URL: http://www.who.int/mediacentre/factsheets/fs330/en/
7. Vos T., Barber R.M., BeLL B. et aL. GLobaL, regional, and nationaL incidence, prevaLence, and years Lived with disabiLity for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic anaLysis for the GLobaL Burden of Disease Study 2013 // Lancet. 2015. VoL. 386, N 9995. P. 743-800.
8. Soffer E.E. Diarrhea // CeciL EssentiaLs of Medicine. 5th ed. / eds T.E. AndreoLi, C.C.J. Carpenter, R. Griggs, J. LoscaLzo. PhiLadeLphia, PA : W.B. Saunders, 2001. P. 316-320.
Griggs, J. LoscaLzo. PhiLadeLphia, PA : W.B. Saunders, 2001. P. 316-320.
9. Федеральная служба государственной статистики. Заболеваемость населения отдельными инфекционными заболеваниями в 2016 году (данные Роспотребнадзора). URL: http://www.gks.ru/bgd/regL/ b17_01/IssWWW.exe/Stg/d01/3-3.doc
10. Lamberti L.M., Fischer Walker C.L., Black R.E. Systematic review of diarrhea duration and severity in children and adults in low- and middle-income countries // BMC Public Health. 2012. Vol. 12. P. 276.
11. Naghavi M., Wang H., Lozano R. et al. Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013 // Lancet. 2015. Vol. 385, N 9963. P. 117-171.
12. Kosek M. , Bern C., Guerrant R.L. The global burden of diarrhoeal disease, as estimated from studies published between 1992 and 2000 // Bull. World Health Organ. 2003. Vol. 81, N 3. P. 197-204.
, Bern C., Guerrant R.L. The global burden of diarrhoeal disease, as estimated from studies published between 1992 and 2000 // Bull. World Health Organ. 2003. Vol. 81, N 3. P. 197-204.
13. Gangarosa R.E., Glass R.I., Lew J.F., Boring J.R. Hospitalizations involving gastroenteritis in the United States, 1985 the special burden of the disease among the elderly // Am. J. Epidemiol. 1992. Vol. 135. P. 281-290.
14. Федеральная служба государственной статистики. Сведения о смертности населения по причинам смерти по Российской Федерации (за январь — декабрь 2016 года). URL: http://gks.ru/free_doc/2016/ demo/t3_3.xls
15. Thielman N.M., Guerrant R.L. Clinical practice. Acute infectious diarrhea // N. Engl. J. Med. 2004. Vol. 350. P. 38-47.
16. Ющук Н.Д., Мартынов Ю.В., Кулагина М.Г. Острые кишечные инфекции. 2-е изд. М., 2012. 402 с.
2-е изд. М., 2012. 402 с.
17. Farthing M.J. Diarrhoea: a significant worldwide problem // Int. J. Antimicrob. Agents. 2000. Vol. 14, N 1. P. 65-69.
18. Гюлазян Н.М. Клинико-патогенетическое значение бактериальных токсинов в развитии особенностей течения острых кишечных диарей : автореф. дис. … д-ра мед. наук. М., 2009. 45 с.
19. Farthing M.J. Antisecretory drugs for diarrheal disease // Dig. Dis. 2006. Vol. 24, N 1-2. P. 47-58.
20. Victora C.G., Bryce J., Fontaine O., Monasch R. Reducing deaths from diarrhoea through oral rehydration therapy // Bull. World Health Organ. 2000. Vol. 78, N 10. P. 1246-1255.
21. Garthright W.E., Archer D.L., Kvenberg J.E. Estimates of incidence and costs of intestinal infectious diseases in the United States // Public Health Rep. 1988. Vol. 103, N 2. P. 107-115.
1988. Vol. 103, N 2. P. 107-115.
22. Lew J.F., Glass R.I., Gangarosa R.E., Cohen I.P. et al. Diarrheal deaths in the United States, 1979 through 1987. A special problem for the elderly // JAMA. 1991. Vol. 265, N 24. P. 3280-3284.
23. Bennett R.G., Greenough W.B. 3rd. Approach to acute diarrhea in the elderly // Gastroenterol. Clin. North Am. 1993. Vol. 22, N 3. P. 517-533.
24. Sur D., Bhattacharya S.K. Acute diarrhoeal diseases — an approach to management // J. Indian Med. Assoc. 2006. Vol. 104, N 5. P. 220223.
25. Федеральное руководство по использованию лекарственных средств (формулярная система). Вып. XVIII. М. : Видокс, 2017. 848 с.
26. Schiller L.R., Santa Ana C.A., Morawski S.G., Fordtran J.S. Mechanism of the antidiarrheal effect of loperamide // Gastroenterology. 1984. Vol. 86, N 6. P. 1475-1480.
1984. Vol. 86, N 6. P. 1475-1480.
27. Douma J.A., Smulders Y.M. Loperamide for acute infectious diarrhoea // Ned. Tijdschr. Geneeskd. 2015. Vol. 159. Article ID A9132.
28. Nelson J.M., Griffin P.M., Jones T.F., Smith K.E. et al. Antimicrobial and antimotility agent use in persons with shiga toxin-producing Escherichia coli 0157 infection in FoodNet Sites // Clin. Infect. Dis. 2011. Vol. 52, N 9. P. 1130-1132.
29. U.S. Food and Drug Administration. Loperamide, 2015. URL: http://www.drugs.com/pro/loperamide.html.
30. Rang H.P., Dale M.M., Ritter J.M., Flower R.J. et al. Rang and Dale’s Pharmacology. London : Elsevier; Churchill Livingstone, 2012.
31. Kreisl W.C., Liow J.S., Kimura N., Seneca N. et al. P-glycoprotein function at the blood-brain barrier in humans can be quantified with the substrate radiotracer 11 C-N-desmethyl-loperamide // J. Nucl. Med. 2010. Vol. 51, N 4. P. 559-566. doi: 10.2967/jnumed.109.070151.
Nucl. Med. 2010. Vol. 51, N 4. P. 559-566. doi: 10.2967/jnumed.109.070151.
32. U.S. Food and Drug Administration. FDA Drug Safety Communication: FDA Warns about Serious Heart Problems with High Doses of the Antidiarrheal Medicine Loperamide (Imodium), Including from Abuse and Misuse, 2016. URL: http://www.fda.gov/Drugs/DrugSafety/ ucm504617.htm
33. Sebastian Domingo J.J. Review of the role of probiotics in gastrointestinal diseases in adults // Gastroenterol. Hepatol. 2017. Vol. 40, N 6. P. 417-429.
34. Chang F.Y., Lu C.L., Chen C.Y., Luo J.C. Efficacy of dioctahedral smectite in treating patients of diarrhea-predominant irritable bowel syndrome // J. Gastroenterol. Hepatol. 2007. Vol. 22, N 12. P. 2266-2272.
REFERENCES
1. Riddle M.S., DuPont H.L., Connor B.A. ACG Clinical Guideline: diagnosis, treatment, and prevention of acute diarrheal infections in adults. Am J Gastroenterol. 2016; 111 (5): 602-22.
Riddle M.S., DuPont H.L., Connor B.A. ACG Clinical Guideline: diagnosis, treatment, and prevention of acute diarrheal infections in adults. Am J Gastroenterol. 2016; 111 (5): 602-22.
2. Guarino A., Albano F., Ashkenazi S., et al. European Society for Pae-diatric Gastroenterology, Hepatology, and Nutrition/European Society for Paediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe. J Pediatr Gastroenterol Nutr. 2008; 46 (suppl. 2): S81-122.
3. Baldi F., Bianco M.A., Nardone G., Pilotto A., et al. Focus on acute diarrhoeal disease. World J Gastroenterol. 2009; 15 (27): 3341-8.
4. Manatsathit S., Dupont H.L., Farthing M., et al. Guideline for the management of acute diarrhea in adults. J Gastroenterol Hepatol. 2002; 17 (suppl.): S54-71.
35. Yao-Zong Y., Shi-Rong L., Delvaux M. Comparative efficacy of dioctahedral smectite (Smecta) and a probiotic preparation in chronic functional diarrhea // Dig. Liver Dis. 2004. Vol. 36, N 12. P. 824-828.
Yao-Zong Y., Shi-Rong L., Delvaux M. Comparative efficacy of dioctahedral smectite (Smecta) and a probiotic preparation in chronic functional diarrhea // Dig. Liver Dis. 2004. Vol. 36, N 12. P. 824-828.
36. Matheson A.J., Noble S. Racecadotril // Drugs. 2000. Vol. 59, N 4. P. 829-835.
37. Schwartz J.C. Racecadotril: a new approach to the treatment of diarrhoea // Int. J. Antimicrob. Agents. 2000. Vol. 14, N 1. P. 75-79.
38. Racecadotril. Abbott scientific brochure (data on file).
39. Fischbach W., Andresen V., Eberlin M., Mueck T. et al. A comprehensive comparison of the efficacy and tolerability of racecadotril with other treatments of acute diarrhea in adults // Front. Med. (Lausanne). 2016. Vol. 3. P. 44.
40. Baumer P. , Dorval E.D., Bertrand J., Vetel J.M. et al. Effects of ace-torphan, an enkephalinase inhibitor, on experimental and acute diarrhea // Gut. 1992. Vol. 33. P. 753-758.
, Dorval E.D., Bertrand J., Vetel J.M. et al. Effects of ace-torphan, an enkephalinase inhibitor, on experimental and acute diarrhea // Gut. 1992. Vol. 33. P. 753-758.
41. Hamza H., Ben K.H., Baumer P., Berard H. et al. Racecadotril versus placebo in the treatment of acute diarrhea in adults // Aliment. Pharmacol. Ther. 1999. Vol. 13, suppl. 6. P. 15-19.
42. Vetel J.M., Hamza H., Coffin B., Lehert P. Racecadotril efficacy in the symptomatic treatment of adult acute diarrhoea: a systematic review and meta-analysis // Int. J. Clin. Med. 2014. Vol. 5. P. 361-375.
43. Coffin B., Hamza H., Vetel J.M., Lehert P. Racecadotril in the treatment of acute diarrhoea in adults. An individual patient data based metaanalysis // Int. J. Clin. Med. 2014. Vol. 5. P. 345-360.
44. Roge J., Baumer P. , Berard H., Schwartz J.C. et al. The enkephalinase inhibitor, acetorphan, in acute diarrhoea. A double-blind, controlled clinical trial versus loperamide // Scand. J. Gastroenterol. 1993. Vol. 28. P. 352-354.
, Berard H., Schwartz J.C. et al. The enkephalinase inhibitor, acetorphan, in acute diarrhoea. A double-blind, controlled clinical trial versus loperamide // Scand. J. Gastroenterol. 1993. Vol. 28. P. 352-354.
45. Vetel J.M., Berard H., Fretault N., Lecomte J.M. Comparison of racecadotril and loperamide in adults with acute diarrhoea // Aliment. Pharmacol. Ther. 1999. Vol. 13, suppl. 6. P. 21-26.
46. Prado D. A multinational comparison of racecadotril and loperamide in the treatment of acute watery diarrhoea in adults // Scand. J. Gastroenterol. 2002. Vol. 37, N 6. P. 656-661.
47. Gallelli L., Colosimo M., Tolotta G.A. et al. Prospective randomized double-blind trial of racecadotril compared with loperamide in elderly people with gastroenteritis living in nursing homes // Eur. J. Clin. Pharmacol. 2010. Vol. 66. P. 137-144.
48. Moraes E., Chinzon D., Coleho L.G., Fernandes T.F. et al. A multicentric, randomised, investigator-blinded, parallel group study to assess the efficacy, safety and tolerability of racecadotril versus Saccharomyces boulardii in the treatment of acute diarrhea in adults // Rev. Bras. Med. 2001. Vol. 58, N 1-2. P. 65-74.
Moraes E., Chinzon D., Coleho L.G., Fernandes T.F. et al. A multicentric, randomised, investigator-blinded, parallel group study to assess the efficacy, safety and tolerability of racecadotril versus Saccharomyces boulardii in the treatment of acute diarrhea in adults // Rev. Bras. Med. 2001. Vol. 58, N 1-2. P. 65-74.
5. Kozhukhova E.A., Andreeva N.V., Ivashchenko V.D. Open ended results of acute diarrhea agent detection to verify diagnosis in adult cases. Infektsiya i immunitet [Infection and Immunity]. 2016; (4): 379-83. (in Russian)
6. Diarrhoeal disease. Fact sheet No.°330. World Health Organization, April 2013. URL: http://www.who.int/mediacentre/factsheets/fs330/en/
7. Vos T., Barber R.M., Bell B. et al. Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet. 2015; 386 (9995): 743-800.
Lancet. 2015; 386 (9995): 743-800.
8. Soffer E.E. Diarrhea. Cecil Essentials of Medicine. 5th ed. Eds T.E. Andreoli, C.C.J. Carpenter, R. Griggs, J. Loscalzo. Philadelphia, PA: W.B. Saunders; 2001: 316-20.
9. Federal Service of State Statistics. Morbidity of the population by certain infectious diseases in 2016 (data from Rospotrebnadzor). URL: http:// www.gks.ru/bgd/reg1/b17_01/IssWWW.exe/Stg/d01/3-3.doc (in Russian)
10. Lamberti L.M., Fischer Walker C.L., Black R.E. Systematic review of diarrhea duration and severity in children and adults in low- and middle-income countries. BMC Public Health. 2012; 12: 276.
11. Naghavi M., Wang H., Lozano R., et al. Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet. 2015; 385 (9963): 117-71.
Lancet. 2015; 385 (9963): 117-71.
12. Kosek M., Bern C., Guerrant R.L. The global burden of diarrhoeal disease, as estimated from studies published between 1992 and 2000. Bull World Health Organ. 2003; 81 (3): 197-204.
13. Gangarosa R.E., Glass R.I., Lew J.F., Boring J.R. Hospitalizations involving gastroenteritis in the United States, 1985 the special burden of the disease among the elderly. Am J Epidemiol. 1992; 135: 281-90.
14. Federal Service of State Statistics. Data on the death rate of the population for reasons of death in the Russian Federation (January-December 2016). URL: http://gks.ru/free_doc/2016/demo/t3_3.xls. (in Russian)
15. Thielman N.M., Guerrant R.L. Clinical practice. Acute infectious diarrhea. N Engl J Med. 2004; 350: 38-47.
16. Yushchuk N.D., Martynov Yu.V., Kulagina M.G. Ostrye kishechnye infektsii [Acute Intestinal Infections]. 2nd. Moscow; 2012: 402 p. (in Russian)
Yushchuk N.D., Martynov Yu.V., Kulagina M.G. Ostrye kishechnye infektsii [Acute Intestinal Infections]. 2nd. Moscow; 2012: 402 p. (in Russian)
17. Farthing M.J. Diarrhoea: a significant worldwide problem. Int J Antimicrob. Agents. 2000; 14 (1): 65-9.
18. Gyulazyan N.M. Clinical and pathogenetic significance of bacterial toxins in the development of the characteristics of the course of acute intestinal diarrhea: Abstract of Diss. Moscow; 2009: 45 p. (in Russian)
19. Farthing M.J. Antisecretory drugs for diarrheal disease. Dig Dis. 2006; 24 (1-2): 47-58.
20. Victora C.G., Bryce J., Fontaine O., Monasch R. Reducing deaths from diarrhoea through oral rehydration therapy. Bull World Health Organ. 2000; 78 (10): 1246-55.
21. Garthright W. E., Archer D.L., Kvenberg J.E. Estimates of incidence and costs of intestinal infectious diseases in the United States. Public Health Rep. 1988; 103 (2): 107-15.
E., Archer D.L., Kvenberg J.E. Estimates of incidence and costs of intestinal infectious diseases in the United States. Public Health Rep. 1988; 103 (2): 107-15.
22. Lew J.F., Glass R.I., Gangarosa R.E., Cohen I.P., et al. Diarrheal deaths in the United States, 1979 through 1987. A special problem for the elderly. JAMA. 1991; 265 (24): 3280-4.
23. Bennett R.G., Greenough W.B. 3rd. Approach to acute diarrhea in the elderly. Gastroenterol Clin North Am. 1993; 22 (3): 517-33.
24. Sur D., Bhattacharya S.K. Acute diarrhoeal diseases — an approach to management. J Indian Med Assoc. 2006; 104 (5): 220-3.
25. Federal Guidelines for the Use of Medicines (Formulary System). Is. XVIII. Moscow : Vidoks; 2017: 848 p. (in Russian)
26. Schiller L. R., Santa Ana C.A., Morawski S.G., Fordtran J.S. Mechanism of the antidiarrheal effect of loperamide. Gastroenterology. 1984; 86 (6): 1475-80.
R., Santa Ana C.A., Morawski S.G., Fordtran J.S. Mechanism of the antidiarrheal effect of loperamide. Gastroenterology. 1984; 86 (6): 1475-80.
27. Douma J.A., Smulders Y.M. Loperamide for acute infectious diarrhea. Ned Tijdschr Geneeskd. 2015; 159: ID A9132.
28. Nelson J.M., Griffin P.M., Jones T.F., Smith K.E., et al. Antimicrobial and antimotility agent use in persons with shiga toxin-producing Escherichia coli O157 infection in FoodNet Sites. Clin Infect Dis. 2011; 52 (9): 1130-2.
29. U.S. Food and Drug Administration. Loperamide, 2015. URL: http://www.drugs.com/pro/loperamide.html.
30. Rang H.P., Dale M.M., Ritter J.M., Flower R.J., et al. Rang and Dale’s Pharmacology. London : Elsevier; Churchill Livingstone; 2012.
31. Kreisl W.C., Liow J.S., Kimura N., Seneca N., et al. P-glycoprotein function at the blood-brain barrier in humans can be quantified with the substrate radiotracer 11 C-N-desmethyl-loperamide. J Nucl Med. 2010; 51 (4): 559-66. doi: 10.2967/jnumed.109.070151.
Kreisl W.C., Liow J.S., Kimura N., Seneca N., et al. P-glycoprotein function at the blood-brain barrier in humans can be quantified with the substrate radiotracer 11 C-N-desmethyl-loperamide. J Nucl Med. 2010; 51 (4): 559-66. doi: 10.2967/jnumed.109.070151.
32. U.S. Food and Drug Administration. FDA Drug Safety Communication: FDA Warns about Serious Heart Problems with High Doses of the Antidiarrheal Medicine Loperamide (Imodium), Including from Abuse and Misuse, 2016. URL: http://www.fda.gov/Drugs/DrugSafety/ucm504617. htm
33. Sebastian Domingo J.J. Review of the role of probiotics in gastrointestinal diseases in adults. Gastroenterol Hepatol. 2017; 40 (6): 417-29.
34. Chang F.Y., Lu C.L., Chen C.Y., Luo J.C. Efficacy of dioctahedral smectite in treating patients of diarrhea-predominant irritable bowel syndrome. J Gastroenterol Hepatol. 2007; 22 (12): 2266-72.
2007; 22 (12): 2266-72.
35. Yao-Zong Y., Shi-Rong L., Delvaux M. Comparative efficacy of dioctahedral smectite (Smecta) and a probiotic preparation in chronic functional diarrhea. Dig Liver Dis. 2004; 36 (12): 824-8.
36. Matheson A.J., Noble S. Racecadotril. Drugs. 2000; 59 (4): 829-35.
37. Schwartz J.C. Racecadotril: a new approach to the treatment of diarrhea. Int J Antimicrob. Agents. 2000; 14 (1): 75-9.
38. Racecadotril. Abbott scientific brochure (data on file).
39. Fischbach W., Andresen V., Eberlin M., Mueck T., et al. A comprehensive comparison of the efficacy and tolerability of racecadotril with other treatments of acute diarrhea in adults. Front Med (Lausanne). 2016; 3: 44.
40. Baumer P., Dorval E.D., Bertrand J., Vetel J.M. et al. Effects of ace-torphan, an enkephalinase inhibitor, on experimental and acute diarrhea. Gut. 1992; 33: 753-8.
Baumer P., Dorval E.D., Bertrand J., Vetel J.M. et al. Effects of ace-torphan, an enkephalinase inhibitor, on experimental and acute diarrhea. Gut. 1992; 33: 753-8.
41. Hamza H., Ben K.H., Baumer P., Berard H., et al. Racecadotril versus placebo in the treatment of acute diarrhea in adults. Aliment Pharmacol Ther. 1999; 13 (suppl. 6): 15-9.
42. Vetel J.M., Hamza H., Coffin B., Lehert P. Racecadotril efficacy in the symptomatic treatment of adult acute diarrhoea: a systematic review and meta-analysis. Int J Clin Med. 2014; 5: 361-75.
43. Coffin B., Hamza H., Vetel J.M., Lehert P. Racecadotril in the treatment of acute diarrhoea in adults. An individual patient data based metaanalysis. Int J Clin Med. 2014; 5: 345-60.
44. Roge J., Baumer P., Berard H., Schwartz J.C., et al. The enkephali-nase inhibitor, acetorphan, in acute diarrhoea. A double-blind, controlled clinical trial versus loperamide. Scand J Gastroenterol. 1993; 28: 352-4.
A double-blind, controlled clinical trial versus loperamide. Scand J Gastroenterol. 1993; 28: 352-4.
45. Vetel J.M., Berard H., Fretault N., Lecomte J.M. Comparison of racecadotril and loperamide in adults with acute diarrhea. Aliment Pharmacol Ther. 1999; 13 (suppl. 6): 21-6.
46. Prado D. A multinational comparison of racecadotril and loperamide in the treatment of acute watery diarrhoea in adults. Scand J Gas-troenterol. 2002; 37 (6): 656-61.
47. Gallelli L., Colosimo M., Tolotta G.A., et al. Prospective randomized double-blind trial of racecadotril compared with loperamide in elderly people with gastroenteritis living in nursing homes. Eur J Clin Pharmacol. 2010; 66: 137-44.
48. Moraes E., Chinzon D., Coleho L.G., Fernandes T.F., et al. A multicentric, randomised, investigator-blinded, parallel group study to assess the efficacy, safety and tolerability of racecadotril versus Saccharomyces boulardii in the treatment of acute diarrhea in adults. Rev Bras Med. 2001; 58 (1-2): 65-74.
Rev Bras Med. 2001; 58 (1-2): 65-74.
Лечение диареи у детей: диета, профилактика
От диареи не застрахован никто. Но есть правила, которые позволяют уменьшить риск заболевания:
Регулярно с мылом мыть руки, особенно после посещения общественных мест и перед едой
Тщательно мыть сырые овощи и фрукты перед употреблением, желательно с использованием мыла и щетки
Правильная кулинарная обработка продуктов
Соблюдение правил хранения продуктов. Ни в коем случае не хранить сырые и готовые продукты вместе
Употреблять в пищу только свежие продукты, обращать внимание на сроки их годности, состав и производителя
Следить за чистотой посуды
Избегать употребления сырой воды
Не употреблять незнакомую или подозрительную пищу
Питаться в проверенных местах
Избегать контакта с людьми, страдающими кишечными расстройствами
Соблюдайте эти правила, научите им детей и будьте здоровы!
АНТИБИОТИК-АССОЦИИРОВАННАЯ ДИАРЕЯ У ДЕТЕЙ: ПРИНЦИПЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ | Черников
1. Запруднов А. М., Мазанкова Л. Н. Микробная флора кишечника и пробиотики. М.: Педиатрия. 1999. 48 с.
Запруднов А. М., Мазанкова Л. Н. Микробная флора кишечника и пробиотики. М.: Педиатрия. 1999. 48 с.
2. Микрофлора пищеварительного тракта / под ред. А. И. Хавкина. М.: Фонд социальной педиатрии. 2006. 416 с.
3. Дисбактериоз кишечника: пути решения проблемы / под ред.В. А. Алешкина, С. С. Афанасьева. Москва. 2004. 24 с.
4. Минушкин О. Н., Ардатская М. Д., Зверков И. В. и соавт. Дисбактериоз кишечника (понятие, диагностика, принципы лечебной коррекции). Современные возможности пребиотической терапии. Москва. 2010. 50 с.
5. Хавкин А. И. Нарушения микроэкологии кишечника. Принципы коррекции. Методические рекомендации. Москва. 2004. 40 с.
6. Кучумова С. Ю., Полуэктова Е. А., Шептулин А. А. и соавт.Физиологическое значение кишечной микрофлоры. Consilium
Кучумова С. Ю., Полуэктова Е. А., Шептулин А. А. и соавт.Физиологическое значение кишечной микрофлоры. Consilium
7. medicum. 2011; 2: 75–78.
8. Урсова Н. И. Нарушения микрофлоры и дисфункции билиарного тракта у детей / под ред. проф. Г. В. Римарчук. Москва.
9. 218 с.
10. Авдеева Т. Г., Рябухин Ю. В., Парменова Л. П. и др. Детская гастроэнтерология. М.: ГЭОТАР-Медиа. 2011. 192 с.
11. Тец В. В. Справочник по клинической микробиологии. Санкт-Петербург. 1994. 211 с.
12. Мухина Ю. Г. Диагностика и коррекция дисбактериоза у детей. Русский медицинский журнал. 1999; 7 (11): 487–494.
Русский медицинский журнал. 1999; 7 (11): 487–494.
13. Сурков А. Н. Тактика лечения острых кишечных инфекций у детей. Вопросы современной педиатрии. 2011; 10 (6): 141–147.
14. Урсова Н. И., Римарчук Г. В., Щеплягина Л. А., Савицкая К. И. Современные методы коррекции дисбиоза кишечника у детей. Учебное пособие. М.: МОНИКИ. 2000. 48 с.
15. Болезни кишечника у детей / под общей редакцией А. М. Запруднова. М.: Анахарсис. 2009. 280 с.
16. Детская гастроэнтерология: руководство для врачей / под ред. проф. Н. П. Шабалова. М.: МЕДпресс-информ. 2011. 736 с.
17. McFarland L. V. Antibiotic-associated diarrhea: epidemiology, trends and treatment. Future Microbiol. 2008; 3 (5): 563–578.
Future Microbiol. 2008; 3 (5): 563–578.
18. Wistrom J., Norrby S. R., Myhre E. B. et al. Frequency of antibioticassociated diarrhoea in 2462 antibiotic-treated hospitalized patients: a prospective study. J. Antimicrob. Chemother. 2001; 47 (1): 43–50.
19. LaRosa M., Bottaro G., Gulino N. et al. Prevention of antibiotic-associated diarrhea with Lactobacillus sporogens and fructooligosaccharides in children: a multi-centric double-blind vs. placebo study. Minerva Pediatr. 2003; 55: 447–452.
20. McFarland L. V. Meta-analysis of probiotics for the prevention of antibiotic associated diarrhea and the treatment of Clostridium difficile disease. Am. J. Gastroenterol. 2006; 101 (4): 812–822.
21. Ардатская М. Д., Дубинин А. В., Минушкин О. Н. Дисбактериоз кишечника: современные аспекты изучения проблемы, принципы диагностики и лечения. Терапевтический архив. 2001; 2: 67–72.
Ардатская М. Д., Дубинин А. В., Минушкин О. Н. Дисбактериоз кишечника: современные аспекты изучения проблемы, принципы диагностики и лечения. Терапевтический архив. 2001; 2: 67–72.
22. Максимов В. А., Далидович К. К., Чернышев А. Л., Мельников В. Л. Диагностические тесты при заболеваниях орга- нов пищеварения. Пенза: Информационно-издательский ПГУ. 2005. 228 с.
23. Римарчук Г. В., Щеплягина Л. А., Круглова И. В. и соавт. Нарушение микрофлоры кишечника у детей (клиническое значе- ние, диагностика, факторы риска, новые технологии в лечении). Лекция для врачей. Москва. 2009. 32 с.
24. Казначеева Л. Ф., Ишкова Н. С., Казначеев К. С. и соавт. Методы коррекции дисбиотических нарушений кишечника у детей/под ред. Л. Ф. Казначеевой. Новосибирск. 2006. 48 с.
25. Kale-Pradhan P. B., Jassal H. K., Wilhelm S. M. Role of Lactobacillus in the prevention of antibiotic-associated diarrhea: a metaanalysis. Pharmacotherapy. 2010; 30 (2): 119–126.
Kale-Pradhan P. B., Jassal H. K., Wilhelm S. M. Role of Lactobacillus in the prevention of antibiotic-associated diarrhea: a metaanalysis. Pharmacotherapy. 2010; 30 (2): 119–126.
26. Bergogne-Berezin E. Treatment and prevention of antibiotic associated diarrhea. Int. J. Antimicrob. Agents. 2000; 16 (4): 521–526.
27. Doron S. I., Hibberd P. L., Gorbach S. L. Probiotics for prevention of antibiotic-associated diarrhea. J. Clin. Gastroenterol. 2008; 42 (Suppl 2): S58–63.
28. Szajewska H., Ruszczynski M., Radzikowski A. Probiotics in the prevention of antibiotic-associated diarrhea in children: a metaanalysis of randomized controlled trials. J. Pediatr. 2006; 149 (3): 367–372.
29..gif) Шендеров Б. А. Медицинская микробная экология и функ- циональное питание. М.: ГРАНТЪ. 1998. 288 с.
Шендеров Б. А. Медицинская микробная экология и функ- циональное питание. М.: ГРАНТЪ. 1998. 288 с.
30. Бельмер С. В., Гасилина Т. В., Хавкин А. И., Эйберман А. С. Функ циональные нарушения органов пищеварения у детей. Рекомендации и комментарии. Москва. 2006. 44 с.
31. Сурков А. Н. Современные технологии в лечении и профи- лактике антибиотик-ассоциированной диареи у детей. Вопросы современной педиатрии. 2011; 10 (5): 146–151.
32. Татьянина О. Ф. Современные антибактериальные препара- ты: новые возможности в профилактике дисбиотических наруше- ний. Вопросы современной педиатрии. 2011; 10 (6): 77–82.
33. Богданов М. Б., Черненькая Т. В. Алгоритмы и организация антибиотикотерапии. Руководство для врачей. М.: Издательский дом «Видар-М». 2004. 223 с.
Руководство для врачей. М.: Издательский дом «Видар-М». 2004. 223 с.
34. Таточенко В. К. Антибиотико- и химиотерапия инфекций у детей. М.: ИПК Континент-пресс. 2008. 256 с.
35. Горелов А. В., Усенко Д. В., Плоскирева А. А. Роль пробиотиков в профилактике диареи, ассоциированной с приемом анти- биотиков. Consilium medicum. 2001; 4: 27–30.__
Ротавирусная инфекция, лечение | H-Clinic
11.12.2019
Ротавирусная инфекция – это острая вирусная инфекция желудочно-кишечного тракта, которая клинически проявляется в виде гастроэнтерита и может сопровождаться поражением органов дыхания, в связи с чем ее так же называют кишечным гриппом. Ротавирус поражает и детей, и взрослых, однако у взрослых заболевание чаще протекает в легкой форме или бессимптомно. Основными клиническими проявлениями болезни у взрослых являются тошнота, потеря аппетита и спазматическая боль в животе. При этом, наличие диареи у взрослого пациента не так опасно, как у детей. У детей и людей пожилого возраста ротавирусный гастроэнтерит может привести к значительной степени обезвоживания вплоть до летального исхода.
Основными клиническими проявлениями болезни у взрослых являются тошнота, потеря аппетита и спазматическая боль в животе. При этом, наличие диареи у взрослого пациента не так опасно, как у детей. У детей и людей пожилого возраста ротавирусный гастроэнтерит может привести к значительной степени обезвоживания вплоть до летального исхода.
Во всем мире ротавирус вызывает около 125 млн случаев детской диареи ежегодно и является самой главной причиной обезвоживания. Более 2 млн детей ежегодно госпитализируются из-за ротавирусного гастроэнтерита и около 500тыс. умирают от этой болезни.
По оценочным данным, практически каждый ребенок в мире инфицируется ротавирусом в возрасте от 3 до 5 лет. В странах с низким доходом средний возраст заболеваемости детей – от 6 до 9 месяцев и 80% ротавирусных инфекций развиваются в возрасте до года. В странах с высоким доходом заболеваемость немного отсрочена – от 2 до 5 лет и 65% заболевают в возрасте до года.
Диагностикой и лечением больных с ротавирусными гастроэнтеритами занимается врач-инфекционист. Но при появлении первых симптомов заболевания люди обычно обращаются к семейному врачу, к педиатру — в случае заболевания ребенка или вызывают скорую помощь. Важно своевременно распознать признаки обезвоживания, особенно у детей младшего возраста и незамедлительно начать адекватное лечение.
Но при появлении первых симптомов заболевания люди обычно обращаются к семейному врачу, к педиатру — в случае заболевания ребенка или вызывают скорую помощь. Важно своевременно распознать признаки обезвоживания, особенно у детей младшего возраста и незамедлительно начать адекватное лечение.
До семидесятых годов двадцатого века причина кишечных инфекций устанавливалась лишь в 30% случаев. В 1973 году Рут Бишоп с коллегами выделили и, с помощью электронной микроскопии, описали вирусные частицы из тканей кишечника у детей с клиническим гастроэнтеритом. Их назвали ротавирусами – за характерный внешний вид, напоминающий колесо (rota по латыни – колесо).
Возбудитель ротавирусного гастроэнтерита – вирус из отряда Rotavirus, семейства Reoviridae.
Вирион представляет из себя 2-цепочечную фрагментированную РНК из 11 фрагментов, которая содержится внутри 3-слойного капсида.
Благодаря трехслойной оболочке, вирус устойчив в окружающей среде. Он может сохранять жизнеспособность до нескольких часов на руках, а на сухих твердых поверхностях до нескольких недель и даже месяцев, если не применялись дезинфицирующие средства.
Он может сохранять жизнеспособность до нескольких часов на руках, а на сухих твердых поверхностях до нескольких недель и даже месяцев, если не применялись дезинфицирующие средства.
Ротавирус попадает в организм через рот и размножение вируса происходит в тонком кишечнике, что в свою очередь приводит к нарушению всасывания натрия, глюкозы, воды, снижению активности лактазы, щелочной фосфатазы и сахаразы, и в результате к возникновению изотонической диареи, обезвоживанию, дисбалансу электролитов и метаболическому ацидозу.
Иммунный ответ изучен не полностью. Важную роль в иммунной защите организма, а так же в восстановлении после заболевания играют антитела, циркулирующие в плазме и в слизистых оболочках, выработанные в ответ на внедрение вируса.
Ребенок, переболевший ротавирусным гастроэнтеритом, не имеет пожизненно стойкого иммунитета и повторное заражение возможно в любом возрасте. С каждым последующим инфицированием иммунная защита выше, а клинические проявления заболевания все более легкие.
Вирус очень заразен, легко передается от человека к человеку, распространяется в семьях, детских садах и больницах. Распространять вирус могут как взрослые и дети с клиническими проявлениями, так и с бессимптомным течением заболевания. Наибольший риск для заражения ротавирусом имеют дети от 4 до 24 месяцев. Взрослые могут заразиться при уходе за инфицированным ребенком.
Резервуаром инфекции является желудочно-кишечный тракт больного. Механизм передачи – фекально-оральный, реализация передачи происходит, если:
• не соблюдаются гигиенические нормы и правила (частота и качество) мытья рук;
• человек касается рта после прикосновения к предмету (подгузник, игрушка), загрязненному зараженным калом;
• употребляют пищу или питьевую воду, загрязненную вирусом (редко).
Наибольшее количество вируса в биоматериале обнаруживается за 2 дня до проявления симптомов болезни и сохраняется до 10 дней после их исчезновения.
Стоит отметить, что лица с иммунодефицитом могут распространять вирус намного дольше, так как в их кале вирус может обнаруживаться до 30 дней после выздоровления.
В основном заболеваемость сезонная – в осенне-зимний период. Инкубационный период развития заболевания достаточно короткий – менее 48 часов.
Клинические проявления варьируют, в зависимости от того, первое это инфицирование или повторное. Таким образом, течение заболевания может быть бессимптомным, может ограничиваться умеренным диарейным синдромом, а может проявляться тяжелой диареей, приводящей к обезвоживанию, сопровождающейся лихорадкой и рвотой. Наиболее тяжелое течение заболевания отмечается при первичном инфицировании детей первых 6 месяцев жизни. У трети детей с ротавирусной инфекцией заболевание сопровождается высокой лихорадкой до 39С.
При опросе заболевшие нередко упоминают о недавнем контакте с больным человеком.
Наиболее распространенные симптомы:
• снижение аппетита, тошнота, рвота
• лихорадка
• водянистый стул без крови, диарея может привести к развитию обезвоживания
• боли в животе
При физикальном осмотре не выявляется примечательных симптомов, за исключением симптомов, которые могут быть связаны с развитием обезвоживания: заторможенность, снижение диуреза, отсутствие слез при плаче, сухая холодная кожа, сухие слизистые ротовой полости, впалые глаза или родничок, выраженная жажда.
Гастроинтестинальные симптомы (рвота и диарея) разрешаются в течение 3-7 дней. У людей с иммунодефицитными состояниями заболевание может приобретать тяжелый персистирующий характер с дальнейшим развитием полиорганных поражений.
Клинические проявления заболевания достаточно неспецифичны, поэтому для подтверждения диагноза требуется проведение лабораторного тестирования.
Лабораторная диагностика ротавирусной инфекции основана на выявлении специфических антигенов вируса в образцах кала.
Основным методом, который используется в этих целях, является ИФА (иммуноферментный анализ) – применение специализированных коммерческих тест-систем, которые позволяют обнаружить антигены в исследуемом материале в среднем в течение 5 дней от начала заболевания.
Так же могут быть использованы электронная микроскопия, ПЦР-методика. У 2/3 всех детей с гастроэнтеритами ротавирусной этиологии тяжелого течения антиген ротавируса может быть обнаружен в плазме крови на 3-7 день от начала заболевания, но сейчас в рутинной практике применяется только исследование образцов кала.
Специфического лечения ротавирусного гастроэнтерита не существует. При этом следует отметить, что показана регидратационная, симптоматическая терапия и противопоказана антибактериальная, так как антибактериальные препараты бесполезны в борьбе с вирусами, но могут способствовать дальнейшему прогрессированию дисбактериоза кишечника и в результате ухудшению состояния больного.
Основа терапии это адекватное восполнение водного и электролитного баланса – в основном, за счёт оральной регидратации – с этой целью можно использовать препарат «Регидрон» — 1пакетик развести в 1литре холодной кипяченной воды, принимать дробно по 5-100мл каждые3-5минут в течение 3-5 часов. Препарат противопоказан при гиперчувствительности и сахарном диабете, почечной недостаточности, стоимость упаковки 20 пакетиков – 370-400р. Можно применять и домашние методы приготовления регидратационных растворов — воду с добавлением соли (из расчета 1 чайная ложка поваренной соли на 1 литр воды), иногда и с добавлением соды и сахара.
Противорвотные препараты применяются ограниченно и только по назначению лечащего врача. Противодиарейные препараты могут применяться при затяжных эпизодах диареи, также строго по назначению доктора.
Жаропонижающие препараты могут применяться при лихорадке выше 38,5С (до этих цифр сбивать температуру не рекомендуется, если ребенок нормально ее переносит, так как повышение температуры тела указывает на активную борьбу организма с инфекцией – во время лихорадки активизируется продукция антител, ускоряется процесс фагоцитоза и т.д.) – это такие препараты как «Панадол», «Нурофен», «Цефекон» — по назначению врача.
При тяжелом течении заболевания и наличии признаков обезвоживания показана госпитализация в стационар и внутривенная регидратационнаяинфузионная терапия.
Диета при заболевании взрослых предполагает исключение молочных продуктов, кофеин-содержащих напитков, жирной и жареной, а также консервированной пищи.
После купирования острого периода, когда ребенок отказывается от еды и важна лишь адекватная регидратация, детям рекомендованы: смеси на основе сои, диетическая мягкая еда – каши на безлактозном молоке или воде, перетертые овощные супы, нежирное мясо, вареные или тушенные овощи, печеные яблоки, кисель, отвары из шиповника, компоты из сухофруктов.
Если есть заболевшие в детском саду – необходимо разделять детей с симптомами от детей без симптомов, ухаживающий персонал должен быть разным для обеих групп.
Желательно использовать спирт-содержащие средства для рук – санитайзеры или салфетки.
Соблюдение правил гигиены и мытья рук – важный фактор профилактики передачи ротавирусной инфекции, но этого не всегда достаточно. В настоящее время одним из основных методов специфической профилактики ротавирусных гастроэнтеритов является вакцинация. После внедрения вакцин заболеваемость ротавирусом существенно снизилась не только среди детей младше 5 лет, но и среди лиц старшего возраста.
Вакцины вызывают выработку иммунной защиты, так как состоят из микроорганизмов и клеточных компонентов, которые стимулируют выработку антител с определенными защитными свойствами.
В феврале 2006 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (UnitedStatesFoodandDrugAdministration, FDA) одобрило вакцину RotaTeq.
RotaTeq – пятивалентная вакцина, которая содержит 5 штаммов ротавируса (G1-4 и А) и белок Р1А (генотип Р). Режим вакцинации — 3 отдельные дозы в виде оральных капель вводятся в возрасте 2, 4, 6месяцев.
В 2008 году одобрили Rotarix (другая оральная вакцина) – защищает от гастроэнтерита, вызванного G1, G3, G4, G9 штаммов и назначается 2 дозы в возрасте от 6 до 24 недель.
Клинические испытания показали, что каждая вакцина предотвращает 74-78% всех гастроэнтеритов, вызванных ротавирусом, и практически все госпитализации по причине ротавирусных гастроэнтеритов. Минимальный рекомендуемый возраст вакцинации – 6 недель. Минимальный промежуток между дозами 4недели, максимальный — 8месяцев. Полный курс вакцинации рекомендуется завершить к возрасту 16 недель жизни и обязательно завершить к 24 неделям (6 месяцев).
Минимальный рекомендуемый возраст вакцинации – 6 недель. Минимальный промежуток между дозами 4недели, максимальный — 8месяцев. Полный курс вакцинации рекомендуется завершить к возрасту 16 недель жизни и обязательно завершить к 24 неделям (6 месяцев).
Грудное вскармливание может продолжаться в обычной режиме до и после вакцинации против ротавируса.
В России в настоящее время зарегистрирована и разрешена к использованию вакцина RV5 («РотаТек»). Всемирная организация здравоохранения рекомендует внедрить вакцинацию от ротавирусной инфекции в Национальный календарь профилактических прививок и рассматривать этот метод профилактики, как приоритетный. Такая работа (вакцинация грудных детей в поликлиниках) уже проводится в некоторых регионах нашей страны.
Автор: врач Университетской клиники H-Clinic Коновалова Анастасия Александровна
Медицинский редактор: руководитель Университетской клиники, к.м.н., врач-инфекционист Коннов Данила Сергеевич
Возврат к списку
Низкие дозы цинка спасли детей от рвоты при лечении диареи
The Simpsons / Fox, 1989–2020
Ученые выяснили, что низкие дозы цинка при диарее у детей так же эффективны, как и высокие, но при этом не вызывают рвоту. Как сообщается в журнале New England Journal of Medicine, при приеме цинка в дозах 5 и 10 миллиграммов продолжительность диареи, частота жидкого стула в день и концентрация цинка в плазме крови сравнимы с показателями при приеме 20 миллиграммов цинка, однако частота рвоты — основного побочного эффекта препаратов цинка — снижается почти на 30 и 20 процентов соответственно.
Как сообщается в журнале New England Journal of Medicine, при приеме цинка в дозах 5 и 10 миллиграммов продолжительность диареи, частота жидкого стула в день и концентрация цинка в плазме крови сравнимы с показателями при приеме 20 миллиграммов цинка, однако частота рвоты — основного побочного эффекта препаратов цинка — снижается почти на 30 и 20 процентов соответственно.
Многие исследования показывают, что прием препаратов цинка приводит к снижению продолжительности диареи, числа ее приступов и риска последующего заболевания. Опираясь на эти данные, ВОЗ включила в свои рекомендации по лечению диареи у детей препараты цинка. Так, при возникновении у ребенка тяжелой диареи организация рекомендует принимать 20 миллиграммов цинка в день в течение 10–14 дней. Эта доза существенно превышает рекомендуемую диетическую норму цинка в младенчестве и раннем детстве (от 2 до 5 миллиграммов в сутки). Доза, рекомендованная ВОЗ, рассчитана из того положения, что увеличение потери цинка во время диареи и недостаточность его поступления при обычной диете негативно сказывается на работе иммунной системы и желудочно-кишечной тракта..gif)
Однако пероральный прием препаратов цинка может вызвать рвоту из-за сильного металлического вкуса и раздражающего действия на желудок. Поэтому более низкие дозы цинка, при условии, что они так же эффективны, как и рекомендуемые ВОЗ 20 миллиграммов, могли бы избавить пациентов от этого неприятного побочного эффекта. Уша Дхингра (Usha Dhingra) с коллегами из Центра кинетики общественного здоровья Нью-Дели и Бостонского детского госпиталя провела рандомизированное двойное слепое исследование в Индии и Танзании, в котором сравнили эффект от приема 5 и 10 миллиграммов цинка с эффектом от приема рекомендуемой ВОЗ дозы — 20 миллиграммов. Ученые предположили, что более низкие дозы цинка смогут оставаться эффективными при лечении диареи, но снизят частоту побочных эффектов — в первую очередь, рвоты.
В исследовании приняли участие 4,5 тысячи детей в возрасте от шести месяцев до пяти лет. Их разделили поровну на три группы, каждая из которых получала 5, 10 или 20 миллиграммов цинка. Процент детей, у которых на фоне приема цинка наблюдалась диарея (три и более жидких стула в день) длительностью более пяти дней, был примерно одинаковым в трех группах: 7,2 процента в группе 5 миллиграммов, 7,7 процента в группе 10 миллиграммов и 6,5 процента в группе 20 миллиграммов (разница оказалась статистически незначимой). Однако у детей, принимавших 5 миллиграммов цинка, относительный риск возникновения рвоты в течение 30 минут после приема был на 29 процентов ниже, чем у детей в группе 20 миллиграммов (p < 0,001), а у детей в группе 10 миллиграммов — на 19 процентов (p < 0,01).
Процент детей, у которых на фоне приема цинка наблюдалась диарея (три и более жидких стула в день) длительностью более пяти дней, был примерно одинаковым в трех группах: 7,2 процента в группе 5 миллиграммов, 7,7 процента в группе 10 миллиграммов и 6,5 процента в группе 20 миллиграммов (разница оказалась статистически незначимой). Однако у детей, принимавших 5 миллиграммов цинка, относительный риск возникновения рвоты в течение 30 минут после приема был на 29 процентов ниже, чем у детей в группе 20 миллиграммов (p < 0,001), а у детей в группе 10 миллиграммов — на 19 процентов (p < 0,01).
Таким образом, низкие дозы цинка — 5 и 10 миллиграммов — не уступают стандартной дозе цинка (20 миллиграммов) по влиянию на продолжительность диареи и частоте жидкого стула у детей. Однако частота рвоты при приеме низких доз цинка оказалась ниже, чем при приеме стандартной дозы — 13,7 процента в группе 5 миллиграммов и 15,6 процента в группе 10 миллиграммов, когда в группе 20 миллиграммов частота рвоты составила 19,3 процента. При этом концентрация цинка в плазме крови оставалась в пределах нормы.
При этом концентрация цинка в плазме крови оставалась в пределах нормы.
По словам авторов, это исследование заполняет пробелы в эмпирических знаниях об эффектах разных доз цинка и их эффективности при лечении диареи у детей. В будущем это позволит назначать дозы препарата с максимальным лечебным эффектом и минимальными рисками развития побочных эффектов.
Впрочем, цинк важен не только как лекарство — этот металл выполняет немало важных функций и в здоровом организме. Так, недавно мы рассказывали, что KRAB-белки с цинковыми пальцами — фрагментами особой формы, позволяющей связывать ионы цинка — регулируют развитие головного мозга приматов в эмбриональном периоде.
Вячеслав Гоменюк
Антибиотик-ассоциированные диареи у детей: как выявить, что делать и как лечить? | Захарова
1. Kazanowski M, Smolarek S, Kinnarney F, Grze-bieniak Z. Clostridium difficile: epidemiology, diagnostic and therapeutic possibilities — a systematic rewiew. Tech Coloproctol. 2014. 18: 223-232.
Kazanowski M, Smolarek S, Kinnarney F, Grze-bieniak Z. Clostridium difficile: epidemiology, diagnostic and therapeutic possibilities — a systematic rewiew. Tech Coloproctol. 2014. 18: 223-232.
2. Goossens H, Ferech M, Vander Stichele R, Elseviers M. ESAC Project Group. Outpatient antibiotic use in Europe and association with resistance: a cross-national database study. Lancet. 2005. 365: 579-87.
3. Таточенко В.К., Антибиотико- и химиотерапия инфекций у детей. Москва, 2008.
4. Van Boeckel TP, Gandra S, Ashok A et al. Global antibiotic consumption 2000 to 2010: an analysis of national pharmaceutical sales data. Lancet Infect Dis. 2014. 14: 742-50.
5. Ткаченко Е.И., Рязанцев С. В., Орешко Л.С., Карпов А.А. Антибактериальная терапия инфекций верхних дыхательных путей: защита индигенной микрофлоры. Российская оториноларингология. 2012. 6(61): 190-195.
В., Орешко Л.С., Карпов А.А. Антибактериальная терапия инфекций верхних дыхательных путей: защита индигенной микрофлоры. Российская оториноларингология. 2012. 6(61): 190-195.
6. ВОЗ: Лечение диареи, 2006.
7. Guarino А, Albano F, Ashkenazi S et al. European society for paediatric gastroenterology, hepatol-ogy, and nutrition/european society for paediat-ric infectious diseases evidence-based guidelines for the management of acute gastroenteritis in children in europe: executive summary. Journal of Pediatric Gastroenterology and Nutrition. 2008. Vol. 46. 5: 619-621. View at Scopus.
8. Еженедельный эпидемиологический бюллетень. 1 февраля 2013 г., 88-й год №5. 2013, 88.
9. Захарова И. Н., Дмитриева Ю.А. Антибиотикоассоциированные диареи: лечение и профилактика. Consilium medicum. Педиатрия. 2009. 2: 7-10.
Н., Дмитриева Ю.А. Антибиотикоассоциированные диареи: лечение и профилактика. Consilium medicum. Педиатрия. 2009. 2: 7-10.
10. Bartlett JG. Antibiotic-associated pseudomem-branous colitis due to toxin producing clostrid-ia. N. Engl.J.Med. 1978. 298: 531.
11. Hempel S, Newberry SJ, Maher AR, Wang Z, Miles JNV, Shanman R, Johnsen B, Shekelle PG. Probiotics for the Prevention and Treatment of Antibiotic-Associated Diarrhea. JAMA. 2012. 307(18): 1959-1969.
12. Hogenauer C, Hammer HF, Krejs GJ, Reisinger EC. Mechanisms and management of antibiotic-associated diarrhea. Clin Infect Dis. 1998. 27: 702-710.
13. Захарова И.Н., Мазанкова Л.Н. и соавт. Антибиотик-ассоциированные диареи у детей: проблема и решение. М., 2011. 48 с.
М., 2011. 48 с.
14. McFarland LV Diarrhea acquired in the hospital. Gastroenterol Clin North Am. 1993 22: 563-77.
15. Заплатников А.Л., Захарова И.Н., Коровина Н.А. Clostridium difficile-инфекция у детей. РМЖ. 2004. 5: 373-377.
16. Mitchell DK, Van R, Mason EH at al. Prospective study of toxigenic Clostridium difficilе children given amoxicillin/clavulanate for otitis media. Pediatr. Inf. Dis. J. 1996. 15: 514-519.
17. Lupse M, Flonta M, Cioara A, Filipescu I, Todor N. Predictors of First Recurrence in Clostridium difficile-Associated Disease. A Study of 306 Patients Hospitalized in a Romanian Tertiary Referral Center. J Gastrointestin Liver Dis, December 2013. 22. 4: 397-403.
18. Zilberberg et al. Risk factors for recurrent Clostridium difficile infection (CDI) hospitaliza-tion among hospitalized patients with an initial CDI episode: a retrospective cohort study. BMC Infectious Diseases. 2014. 14: 306. http:// www.biomedcentral.com/1471-2334/14/306.
19. Alam S, Muchatad M., Antibiotic associated diarrhea in children. Indian Pediatr. 2009 Jun. 46(6): 491-6.
20. Малов В.А. Инфекция Clostridium Difficile: современное состояние проблемы. Фарматека. 2010. 4.
21. Hedge Dennis D, Strain Joe D, Heins Jodi R, Farver Debra K. New advances in the treatment of Clostridium difficile infection (CDI). Therapeutics and Clinical Risk Management. 2008. 4(5).
22. Lowy I, Molrine DC, Leav BA, Blair BM, Baxter R, Gerding DN, Nichol G, Thomas WD, Leney M, Sloan S, Hay CA, Ambrosino DM. Treatment with Monoclonal Antibodies against Clostridium difficile Toxins. N Engl J Med. 2010. 362: 197-205. Copyright © 2010 Massachusetts Medical Society.
Lowy I, Molrine DC, Leav BA, Blair BM, Baxter R, Gerding DN, Nichol G, Thomas WD, Leney M, Sloan S, Hay CA, Ambrosino DM. Treatment with Monoclonal Antibodies against Clostridium difficile Toxins. N Engl J Med. 2010. 362: 197-205. Copyright © 2010 Massachusetts Medical Society.
23. Massey V et al. Clinical usefulness of components of the Triage immunoassay, enzyme immunoassay for toxins A and B, and cytotoxin B tissue culture assay for the diagnosis of Clostridium difficile diarrhea. Am J Clin Pathol. 2003. 119: 45-9.
24. Nyc O, Pituch H, Matejkova J, Obuch-Woszczatynski P, Kuijper EJ. Clostridium difficile PCR ribotype 176 in the Czech Republic and Poland. Lancet. 2011. Apr 23. 377(9775): 1407,
25. Warren CA, Guerrant RL. Pathogenic C. difficile is here (and everywhere) to stay. Lancet. 2011. jan 1. 377(9759): 8-9.
Lancet. 2011. jan 1. 377(9759): 8-9.
26. Nylund CM, Goudie A, Garza JM, Fairbrother G, Cohen MB. Clostridium difficile infection in hospitalized children in the United States. Arch Pediatr Adolesc Med. 2011. 165: 451-457. (PMID: 21199971 DOI: 10.1001/archpediatrics.2010.282).
27. Учайкин В.Ф. Руководство по инфекционным заболеваниям у детей. М.: Гэотар Медицина, 1998. 492-494.
28. Maha Barakat, yZeinab El-Kady, zMohamed Mostafa, yNaglaa Ibrahim, and yHamdy Ghazaly. Antibiotic-associated Bloody Diarrhea in Infants: Clinical, Endoscopic, and Histopatho-logic Profiles. JPGN. January 2011. 52. 1.
29. Joanne Donovan, MD, PhD. 18th European Congress of Clinical Microbiology and Infectious Diseases: Abstract O464. Presented April 22, 2008.
Presented April 22, 2008.
30. Киргизов К.И, Шульга С.Ю., Пристанскова Е.А., Константинова В.В., Герасимова Ю.В., Сидорова Н.В., Благонравова О.Л., Федорова Н.И., Скоробогатова Е.В. Энтероколит, связанный с Clostridium difficile, в детской гематологии-онкологии — решенная проблема? Обзор литературы и собственный опыт. Российский журнал детской гематологии и онкологии. 2014. 1: 25-31.
31. Лобзин Ю.В., Захаренко С.М., Иванов Г.А. Современные представления об инфекции Clostridium difficile. Клиническая микробиология и антимикробная химиотерапия. 2002. 4. 3: 200-232.
32. Bauer MP, Notermans DW, van Benthem BH, Brazier JS, Wilcox MH, Rupnik M, Monnet DL, van Dissel JT, Kuijper EJ. ECDIS Study Group (2011) Clostridium difficile infection in Europe: a hospital-based survey. Lancet. 2011. 377: 63-73.
33. Wilcox MH. Updated guidance on the management and treatment of Clostridium difficile infection. Crown Copyright 2013 Published May 2013.
34. Bryan F Curtin, Yousef Zarbalian, Mark H Flasar, Erik von Rosenvinge. Clostridium difficile -associated disease: Adherence with current guidelines at a tertiary medical center. World J Gastroenterol. 2013. December. 14. 19(46): 8647-8651. ISSN 1007-9327 (print) ISSN 22192840 (online).
35. Cohen SH, Gerding DN, Johnson S, Kelly CP, Loo VG, McDonald LC, Pepin J, Wilcox MH; Society for Healthcare Epidemiology of America; Infectious Diseases Society of America (2010) Clinical practice guidelines for Clostridium difficile infection in adults: 2010 update by the Society for Healthcare Epidemiology of America (SHEA) and the Infectious Disases Society of America (IDSA). Infect Contr Hosp Epidem. 2010. 5:431-455.
36. Elliott B, Reed R, Chang BJ, Riley TV. Bacteremia with a large clostridial toxin-negative, binary toxin-positive strain of Clostridium difficile. J. Anaerobe. 2009. 15: 249-251.
37. Minino A, Xu J and Kochanek K. (2010) Deaths: preliminary data for 2008. National Vital Statistics Report 59. Hyattsville, MD: National Center for Health Statistics. Available at: http:// www.cdc.gov/ nchs/data/nvsr/nvsr59/ nvsr59_02.pdf.
38. Wistrom J, Norrby SR, Myhre EB, Eriksson S, Granstrom G, Lagergren L, Englund G, Nord CE, Svenungsson B. Frequency of antibiotic-associated diarrhea in 2462 antibiotic-treated hospitalized patients: a prospective study. Journal of Antimicrobial Chemotherapy. 2001. 47: 43-50.
39. Vaishnavi C, Bhassin D, Kochhar R, Singh K. Clostridium difficile toxin and faecal lactofer-rin assays in adult patients. Microbes Infect. 2000. 2: 1827-1830.
40. Hogenauer C, Langner C, Krause R, Gerstgrasser N, Krejs GJ, Hinterleitner TA. Antibiotic-associated segmental hemorrhagic colitis: clinical features, and influence of Klebsiella oxyto-ca in its patogenesis. Abstracts of 12 UEGW, Gut. 2004. 53 (Suppl VI), A135.
41. Шевяков М.А. Антибиотик-ассоциированная диарея и кандидоз кишечника: возможности лечения и профилактики. Антибиотики и химиотерапия. 2004. 49. 10: 26-29.
42. Krause R, Krejs G, Wenisch C, Reisinger E. Elevated fecal Candida counts in patients with antibiotic-associated diarrhea. Clin Diagn Lab Immunol. 2003. 10(1): 167-8.
43. Larson HE, Prise AB, Honour P et al. Pseudomembranous colitis: present of clostrid-ial toxin. Lancet. 1977: 1312-1314.
44. Schwartz et al. Severe clinical outcome is uncommon in Clostridium difficile infection in children: a retrospective cohort study. BMC Pediatrics, 2014. 14: 28.
45. Johnson S et al. Interruption of recurrent Clostridium difficile-associated diarrhea episodes by serial therapy with vancomycin and rifaximin. Clin Infect Dis. 2007. Mar 15. 44(6): 846-8. Epub 2007 Feb 2.
46. Малов В.А. Антибиотик-ассоцированные поражения кишечника. Врач. 2000. 10: 16-19.
47. Friedman ND, Pollard J, Stupart D, Knight DR, Khajehnoori M, Davey EK, Parry L, Riley TV Prevalence of Clostridium difficile colonization among healthcare workers. BMC Infectious Diseases. 2013. 13: 459. Page 2 of 5http://www. biomedcentral.com/1471-2334/13/459.
48. Ковалева Е.П., Семина Н.А., Семененко Т.А., Галкин В.В. Справочник госпитального эпидемиолога. М.: Хризостом, 1999. 136-139.
49. Edward O’Rourke. Harvard University — Harvard Medical School. Nospital epidemiology. 2014.
50. Poutanen SM, Simor AE. Clostridium difficile-associated diarrhea in adults. CMAJ. 2004. 171: 51-8.
51. Barakat M, El-Kady Z, Mostafa M, Ibrahim N, Ghazaly H. Antibiotic-associated Bloody Diarrhea in Infants: Clinical, Endoscopic, and Histopatho-logic Profiles. JPGN. 52, 1, January 2011.
52. Ковалева Е.П., Семина Н.А., Семененко Т.А., Галкин В.В. Справочник госпитального эпидемиолога. М.: Хризостом, 1999. 136-139.
53. Hsu J, Abad C, Dinh M, Safdar Nasia. Prevention of Endemic Healthcare-Associated Clostridium difficile Infection: Reviewing the Evidence. Am J Gastroenterol. 2010. 105: 2327-2339. doi: 10.1038/ ajg.2010.254; published online 6 July 2010.
54. Tatochenko V.K. Antibiotic and chemotherapy of infections in children. Moscow, 2008.
55. Tkachenko E.I., Ryazantsev S.V., Oreshko L.S., Karpov A.A. Antibacterial therapy of upper respiratory infections: protection of indigenous microflora. Rossiyskaya Otorinolaringologiya. 2012. 6(61): 190-195.
56. WHO. Treatment of diarrhea, 2006.
57. Weekly Epidemiological Record. February 1, 2013, year 88, №5. 2013, 88.
58. Zakharova I.N., Dmitrieva Y.A. Antibiotic-associated diarrhea: treatment and prevention. Consilium medicum. Pediatriya. 2009. 2: 7-10.
59. Zakharova I.N., Mazankova L.N. et al. Antibiotic-associated diarrhea in children: problem and solutions. М., 2011. 48 p.
60. Zaplatnikov A.L., Zakharova I.N., Korovina N.A. Clostridium difficile infection in children. RMZ. 2004. 5: 373-377.
61. Malov V.A. Clostridium Difficile Infection: current situation. Pharmateka. 2010. 4.
62. Uchaikin V.F. Guidance on infectious diseases in children. М.: Geotar Medicine, 1998. 492-494.
63. Kirgizov K.I., Shulga S.Y,, Pristanskova E.A., Konstantinova V.V., Gerasimova Y.V., Sidorova N.V., Blagonravova O.L., Fedorova N.I., Skorobogatova E.V. Enterocolitis associated with Clostridium difficile in pediatric hematology-oncology — a problem solved? Review of literature and own experience. Rossiyskiy Zhurnal Detskoy Gematologii i Onkologii. 2014. 1: 25-31.
64. Lobzin Yu.V., Zakharenko S.M., Ivanov G.A. Modern ideas about Clostridium difficile infection. Klinicheskaya Mikrobiologiya i Antimikrobnaya Terapiya. 2002. 4. 3: 200-232.
65. Sheviakov M.A. Antibiotic-associated diarrhea and intestinal candidiasis: treatment and prevention options. Antibiotiki i Khimioterapiya. 2004. 49. 10: 26-29.
66. Malov V.A. Antibiotic-associated bowel lesions. Vrach. 2000. 10: 16-19.
67. Kovaleva E.P., Semina N.A., Semenenko T.A., Galkin V.V. Reference Guide of Hospital Epidemiologist. М.: Khrizostom, 1999. 136-139.
68. Kovaleva E.P., Semina N.A., Semenenko T.A., Galkin V.V. Reference Guide of Hospital Epidemiologist. М.: Khrizostom, 1999. 136-139.
Россия: диарея у путешественников | IAMAT
Описание
Термин «диарея путешественников» используется для описания желудочно-кишечных инфекций, поражающих путешественников, вызванных употреблением в пищу бактерий, вирусов и простейших. Эти микроорганизмы встречаются во всем мире и обычно передаются от человека к человеку фекально-оральным путем — инфицированный человек, который не соблюдает надлежащую гигиену рук или тела, передает инфекцию другому человеку при работе с пищей и водой.Диарея путешественников — одна из самых распространенных болезней путешественников.
Риск
Диарея у путешественников может возникнуть, когда:
Употребление сырого, недостаточно приготовленного, немытого или неправильно обработанного мяса, продуктов из птицы, молочных продуктов, фруктов, овощей, моллюсков и морепродуктов.
Пить зараженную воду или напитки.
Случайное проглатывание фекалий, яиц простейших или вирусов путем прикосновения к рту грязными или неправильно вымытыми руками.
Еда в ресторанах, буфетах или у уличных торговцев, где не соблюдаются правила обращения с пищевыми продуктами и гигиены.
Профилактика
Золотое правило профилактики желудочно-кишечных инфекций: Варите, варите, очищайте от кожуры или забудьте об этом! Однако важно не только , что вы едите, но также важно учитывать , где вы едите. Не всегда легко узнать, соблюдает ли ресторан или продавец продуктов питания надлежащие правила обращения с пищевыми продуктами и соблюдение гигиены (например, отделение сырых продуктов от приготовленных, правильная чистка разделочных досок и посуды, мытье рук и правильное охлаждение продуктов).Избегайте ресторанов и поставщиков продуктов питания, которые кажутся нечистыми или у которых мало клиентов. Будьте осторожны с продуктами, которые хранились непокрытыми, неправильно охлаждались или долго выделялись, например, буфеты.
Если вы не уверены в качестве воды из-под крана, доведите ее до кипения. Кипячение воды уничтожает патогены, которые могут вызвать диарею путешественников и другие желудочно-кишечные инфекции. Если вы не можете вскипятить воду, выберите вместо нее очищенную или бутилированную воду.
Риск диареи путешественников также можно свести к минимуму, соблюдая правила гигиены. Обязательно мойте руки теплой водой с мылом не менее 20 секунд, особенно перед приготовлением или едой и после посещения туалета. Если нет воды и мыла, используйте дезинфицирующее средство для рук на спиртовой основе, которое содержит не менее 60% спирта.
Борьба с диареей путешественников
При первых признаках диареи выпейте раствор для пероральной регидратации (ПРС), смесь соли и сахара, предназначенную для восстановления электролитов и лечения обезвоживания.Средства против моторики, такие как лоперамид, также могут использоваться для уменьшения симптомов, но они не лечат желудочно-кишечную инфекцию. Диарея путешественников, как правило, является самоизлечивающейся инфекцией (она проходит сама собой), но если она не проходит и усиливается через 2 или 3 дня, вы можете рассмотреть возможность лечения антибиотиком.
Если вы принимаете лекарства от высокого кровяного давления, следите за признаками обезвоживания, поскольку это может очень быстро стать неотложной проблемой.
Прежде чем отправиться в путь, проконсультируйтесь с врачом по поводу лучших вариантов лечения диареи.Путешественники, у которых уже есть проблемы со здоровьем и которые более восприимчивы к желудочно-кишечным инфекциям, могут рассмотреть возможность приема профилактических лекарств.
Дополнительную информацию о предотвращении диареи путешественников можно найти по телефону:
. Безопасность пищевых продуктов и воды
Как предотвратить диарею путешественников
Как предотвратить болезнь с помощью мытья рук
Инфографика
Последнее обновление информации: 16 апреля 2020 г.
Источники Источники- Веларде Дж. Дж., Левин М. М., Натаро Дж. П., Escherichia coli Diarrhea.В: McGill, A; Райан, Э; Хилл, Д; Соломон, Т., ред. Тропическая медицина Хантера и новые инфекционные болезни. 9 -е изд. Нью-Йорк: Сондерс Эльзевир; 2013: 442-447.
- Вулф MS. Диарея путешественника. В: Jong, E; Стивенс, Д., ред. Инфекционные болезни Неттера. Нью-Йорк: Сондерс Эльзевир; 2012: 390-393.
- Вирк А. Амебиаз, лямблиоз и другие кишечные протозойные инфекции. В: Jong, E; Сэнфорд, С. ред. Руководство по путешествиям и тропической медицине, 4 th ed.Уолтем, Эльзевьер; 2008: 448-466.
- Центры по контролю и профилактике заболеваний: Желтая книга, диарея путешественников
- Консультативный комитет по тропической медицине и путешествиям, PHAC: Заявление о диарее путешественников
Распространенность диареи, ассоциированной с Clostridium Difficile, у госпитализированных пациентов (результаты российского проспективного многоцентрового исследования)
Использование антибиотиков доказанный фактор риска диареи.По данным McFarland, CDAD встречается у 5–39% пациентов [1]. Исследование Бартлетта и Гилберта, опубликованное в 1990-х годах, показало, что диарея развивается у 5–10% пациентов, получавших ампициллин; 10–25%, амоксициллин / клавуланат; 15–20%, цефиксим; 2–5% — цефалоспорины, фторхинолоны, азитромицин, кларитромицин, эритромицин и тетрациклин [2, 3].
C. difficile преобладает среди инфекционных причин ААД [1,2,3,4]. Роль C. difficile в развитии CDAD и псевдомембранозного колита была установлена в 1978 году.В большинстве случаев развитие патологических состояний было связано с применением клиндамицина [4]. Другие патогены AAD включают Clostridium perfringens [14], Staphylococcus aureus [15], Klebsiella oxytoca [16] и, возможно, Candida albicans [17].
C. difficile способна продуцировать энтеротоксин (токсин A) и цитотоксин (токсин B), которые нарушают функцию и повреждают слизистые оболочки и, следовательно, играют ведущую роль в патогенезе инфекционных заболеваний [18, 19].Качественные и количественные параметры продукции токсинов связаны с тяжестью заболевания [20, 21]. Штаммы C. difficile , не продуцирующие токсины, способны к колонизации, но обычно не повреждают слизистые оболочки желудочно-кишечного тракта [22].
Инфекционные заболевания, вызванные C. difficile , имеют различные проявления: от легкой формы заболевания с незначительными симптомами до фульминантного течения псевдомембранозного колита (токсический мегаколон, перфорация кишечника) [6, 23,24,25,26] .Рецидив наблюдается примерно у 10–25% пациентов через 30 дней после успешного лечения [27, 28]. Согласно европейскому исследованию, атрибутивная смертность составила 2% у пациентов с диареей, развившейся через ≥ 3 дней после их пребывания в больнице, или у пациентов с подозрением на инфекцию C. difficile . Еще в 7% случаев инфекция сыграла значительную роль в летальном исходе [6].
Немногочисленные российские данные о распространенности CDAD у пациентов с AAD, полученные в одноцентровых исследованиях, заметно различаются.Например, 28,7% (154/563) и 51,5% (67/130) случаев были зарегистрированы в больницах общего профиля [10, 11]. Сообщалось об увеличении распространенности CDAD среди онкологических больных с 15,6% (7/45) в 2011 г. до 24,2% (57/236) в 2013 г. [12]. Высокая распространенность CDAD наблюдалась у пациентов-гастроэнтерологов — 39,1% (93/238) [13].
Настоящее исследование было проведено из-за недостатка информации о распространенности CDAD в Российской Федерации и отсутствия соответствующих российских многоцентровых исследований. По результатам проведенных экспресс-тестов ХДД диагностирована у 21.7% пациентов с ААД, что соответствует международным данным (15–25%) [29]. Исследование также продемонстрировало выраженные различия в распространенности CDAD между различными стационарными учреждениями (от 0 до 44,3%) и между группами пациентов по типу помощи (хирургия, 26,2%; терапия, 17,6%; интенсивная терапия, 17,8%), и по специальности (септическая хирургия — 39,2%; общая медицина — 27,2%; онкогематология — 17,2%; гастроэнтерология — 15,0%; онкология — 11,3%; трансплантация — 6,8%). Эти различия могут отражать местные характеристики эпидемиологии CDAD.В частности, исследователи из центра с самой высокой распространенностью CDAD (44,3%) также сообщили об особенно тяжелом контингенте пациентов и вспышке заболевания во время исследования.
Процент пациентов с GDH-положительными результатами экспресс-теста, но отрицательными результатами на токсины, составил 16,8%, в то время как общий процент GDH-положительных пациентов составил 38,6%. Таким образом, около 39% пациентов с ААД, участвовавших в исследовании, были колонизированы C. difficile , тогда как около половины C.difficile , случаи колонизации сопровождались выработкой токсинов и началом инфекции.
Пациенты в возрасте ≥ 65 лет демонстрировали более высокую распространенность CDAD (26,7–42,9%) по сравнению с пациентами <65 лет (14,1–7,2%). Это было ожидаемо, поскольку пожилой возраст (≥ 65 лет) является одним из известных факторов риска развития CDAD [30].
Результаты этого исследования и ранее опубликованных российских эпидемиологических исследований свидетельствуют о том, что CDAD является частым осложнением, возникающим в российских больницах.Это делает более актуальным тщательное обследование пациента с необъяснимой диареей, когда он проходит лечение антибиотиками или в течение 30 дней после такого лечения. Существенные различия в распространенности CDAD между больницами и отделениями больниц могут быть связаны со специфическими характеристиками госпитализированных пациентов, факторами экологического риска C. difficile -ассоциированного заболевания и местными подходами к мониторингу нозокомиальных инфекций.
Ограничения исследования
В исследовании участвовали только крупные стационарные лечебные учреждения в городах России с высокой плотностью населения (Москва и Санкт-Петербург).Это ограничивает возможность экстраполяции данных на уровне страны.
Выраженные различия в уровнях распространенности CDAD между исследовательскими центрами повлияли на точность оценки первичных конечных точек: 95% ДИ, скорректированный для дизайна исследования, оказался шире, чем 95% ДИ, основанный на простой модели случайной выборки, которая была используется для расчета размера выборки в процессе планирования исследования.
Экспресс-тест, использованный в исследовании, имеет известные ограничения по чувствительности и специфичности, снижающие точность диагностики CDAD.В частности, отрицательные результаты этого лабораторного теста не исключили полностью CDAD.
Диарея путешественников | Свободный стул в поездках
Что такое диарея путешественников?
Диарея путешественника (иногда называемая «животом Дели») — это диарея, которая развивается во время или вскоре после поездки за границу. Диарея определяется как «жидкий или водянистый стул (фекалии), обычно не реже трех раз в сутки».
Что вызывает диарею путешественников?
Диарея путешественника вызвана употреблением пищи или питьевой водой, содержащей определенные микробы (микробы) или их яды (токсины).Типы микробов, которые могут быть причиной, включают:
- Бактерии: это наиболее распространенные микробы, вызывающие диарею путешественников. Распространенными типами участвующих бактерий являются:
- Escherichia coli
- Campylobacter
- Salmonella
- Shigella
- Вирусы: это следующие по распространенности вирусы, в частности норовирус и ротавирус.
- Паразиты: это менее распространенные причины. Лямблии, криптоспоридиум и Entamoeba histolytica являются примерами паразитов, которые могут вызывать диарею путешественников.
Часто точная причина диареи путешественников не обнаруживается, и исследования показали, что у многих людей не выявляется конкретный микроб, несмотря на исследования (например, образец стула (фекалий)).
См. Отдельные брошюры под названием E. Coli (VTEC O157), Campylobacter, Salmonella, Cryptosporidium, Amoebiasis (информация о дизентерии), Shigella и Giardia для получения более подробной информации о каждом из упомянутых выше микробов.
Примечание : эта брошюра посвящена диарее путешественников в целом и способам ее предотвращения.
Все ли путешественники в группе риска?
Диарея путешественников чаще всего поражает людей, путешествующих из развитой страны, такой как Великобритания, в менее развитую страну, где санитарные и гигиенические меры могут не соответствовать тем же стандартам. Это может затронуть от 2 до 6 из 10 путешественников.
Существуют разные риски в зависимости от того, куда вы отправляетесь:
Зоны повышенного риска : Южная и Юго-Восточная Азия, Центральная Америка, Западная и Северная Африка, Южная Америка, Восточная Африка.
Зоны среднего риска : Россия, Китай, Карибский бассейн, Южная Африка.
Зоны низкого риска : Северная Америка, Западная Европа, Австралия и Новая Зеландия.
Иногда вспышки диареи могут возникать у путешественников, остановившихся в одной гостинице, или, например, у тех, кто останавливается на круизном лайнере. Люди, путешествующие в более отдаленные районы (например, туристы и туристы), также могут иметь ограниченный доступ к медицинской помощи, если они действительно заболеют. Люди, путешествующие с рюкзаком, чаще заболевают, чем люди в командировках, останавливающиеся в отелях.
Каковы симптомы диареи путешественника?
По определению, диарея является основным симптомом. Он может быть водянистым и иногда содержать кровь. Другие симптомы могут включать:
- Спастические боли в животе (животе).
- Чувство тошноты (тошнота).
- Заболевание (рвота).
- Высокая температура (лихорадка).
Симптомы у большинства людей обычно легкие и длятся от 3 до 4 дней, но могут длиться дольше. Симптомы могут быть более серьезными у очень молодых, пожилых людей и людей с другими проблемами со здоровьем.Те, чья иммунная система не работает так хорошо, как обычно, чаще всего заболевают. Например, люди с ВИЧ-инфекцией, проходящие химиотерапию, длительное лечение стероидами и т. Д.
Несмотря на то, что симптомы обычно довольно легкие, они часто могут означать, что ваш маршрут или командировка прервана или может потребоваться быть измененным.
Нужно ли мне расследование?
Диарея путешественников обычно диагностируется по типичным симптомам.Как упоминалось выше, у большинства людей симптомы легкие, и им не нужно обращаться за медицинской помощью. Однако в некоторых случаях требуется консультация врача (см. Ниже).
Если вы все же обратитесь к врачу, он может предложить сдать образец вашего стула (фекалий). Он будет отправлен в лабораторию для поиска микробов, которые могут вызывать ваши симптомы. Иногда могут потребоваться анализы крови или другие анализы, если у вас наблюдаются более серьезные симптомы или развиваются какие-либо осложнения.
Когда мне следует обратиться за медицинской помощью?
Как упоминалось выше, у большинства людей, страдающих диареей путешественников, симптомы относительно легкие, и они могут справиться с ними самостоятельно, отдыхая и следя за тем, чтобы они пили много жидкости.Однако вам следует обратиться за медицинской помощью в любом из следующих случаев или при появлении других симптомов, которые вас беспокоят:
- Если у вас высокая температура (жар).
- Если у вас кровь в стуле (фекалиях).
- Если трудно получить достаточно жидкости из-за серьезных симптомов: частый или очень водянистый стул или неоднократные тошноты (рвота).
- Если диарея длится более 3 или 4 дней.
- Если вы сами начали лечение антибиотиками, и диарея не проходит в течение трех дней после начала лечения.
- Если вы пожилой человек или у вас есть проблемы со здоровьем, например диабет, воспалительное заболевание кишечника или заболевание почек.
- Если у вас ослабленная иммунная система, например, из-за химиотерапевтического лечения, длительного лечения стероидами или ВИЧ-инфекции.
- Если вы беременны.
- Если заболевший ребенок младше 6 месяцев.
- Если у вас возникнут какие-либо из перечисленных ниже симптомов, указывающих на недостаток жидкости в организме (обезвоживание).Если пострадал ваш ребенок, для детей есть отдельный список.
Симптомы обезвоживания у взрослых
К ним относятся:
- Усталость.
- Головокружение или дурноту.
- Головная боль.
- Мышечные судороги.
- Запавшие глаза.
- Меньше мочи.
- Сухость во рту и языке.
- Слабость.
- Становится раздражительным.
Симптомы тяжелого обезвоживания у взрослых
К ним относятся:
- Глубокая потеря энергии или энтузиазма (апатия).
- Слабость.
- Путаница.
- Учащенное сердцебиение
- Вырабатывается очень мало мочи.
- Кома, которая может наступить.
Примечание : сильное обезвоживание требует неотложной медицинской помощи.
Симптомы обезвоживания у детей
К ним относятся:
- Небольшое количество мочи.
- Сухость во рту.
- Сухой язык и губы.
- Меньше слез при слезах.
- Запавшие глаза.
- Слабость.
- Быть раздражительным.
- Отсутствие энергии (вялость).
Симптомы тяжелого обезвоживания у детей
К ним относятся:
- Сонливость.
- Кожа бледная или в пятнах.
- Холодные руки или ноги.
- Очень мало мокрых подгузников.
- Быстрое (но часто поверхностное) дыхание.
Примечание : сильное обезвоживание требует неотложной медицинской помощи.
Обезвоживание более вероятно у:
- Младенцы в возрасте до 1 года (особенно в возрасте до 6 месяцев). Это связано с тем, что младенцам не нужно терять много жидкости, чтобы терять значительную часть общей жидкости организма.
- Младенцы в возрасте до 1 года с низким весом при рождении, которые не достигли своего веса.
- Ребенок на грудном вскармливании, которого перестали кормить грудью во время болезни.
- Любой младенец или ребенок, который мало пьет во время кишечной инфекции (гастроэнтерита).
- Любой младенец или ребенок с сильной диареей и рвотой. (Например, если у них было пять или более диарейных стула и / или их рвало два или более раз за предыдущие 24 часа.)
Как лечится диарея путешественника у взрослых?
В большинстве случаев диарея путешественников не требует специального лечения. Самая важная вещь — пить много жидкости, чтобы избежать ее нехватки (обезвоживания).
Восполнение жидкости
- В качестве ориентировочного руководства выпивайте не менее 200 мл после каждого водянистого стула (приступ диареи).
- Эта дополнительная жидкость добавляется к тому, что вы обычно пьете. Например, взрослый человек обычно выпивает около двух литров в день, но в жарких странах больше. Вышеуказанные «200 мл после каждого водянистого стула» добавляются к обычному количеству, которое вы бы выпили.
- Если вы заболели (рвота), подождите 5-10 минут и затем снова начните пить, но медленнее. Например, делайте глоток каждые 2-3 минуты, но убедитесь, что ваше общее потребление соответствует описанному выше.
- Вам нужно будет пить еще больше, если вы обезвожены.Врач посоветует, сколько пить, если вы обезвожены.
Примечание : если вы подозреваете, что у вас обезвоживание, вам следует обратиться за медицинской помощью.
Для большинства взрослых в качестве жидкости для поддержания гидратации следует использовать в основном воду. Однако это должна быть безопасная питьевая вода — например, бутилированная или кипяченая и очищенная вода. Лучше не употреблять напитки, содержащие много сахара, такие как кола или поп, поскольку они иногда могут усугубить диарею. Также следует избегать алкоголя.
Можно также использовать напитки для регидратации. Они сделаны из пакетиков, которые вы можете купить в аптеке, и, возможно, их стоит положить в аптечку первой помощи, когда вы путешествуете. Вы добавляете содержимое пакетика в воду. Напитки для регидратации обеспечивают хороший баланс воды, солей и сахара. Они не останавливают и не уменьшают диарею. Однако небольшое количество сахара и соли способствует лучшему всасыванию (усвоению) воды из кишечника в организм. Смеси соли и сахара домашнего приготовления используются в развивающихся странах, если напитки для регидратации недоступны; однако их нужно делать осторожно, так как слишком много соли может быть опасно.Напитки для регидратации дешевы, легко доступны в Великобритании и являются лучшим лечением. Обратите внимание, что для восстановления пакетиков соли для пероральной регидратации следует использовать безопасную питьевую воду.
Существует также «антисекреторное» лекарство (называемое рацекадотрилом), предназначенное для лечения регидратации. Он уменьшает количество воды, попадающей в кишечник во время эпизода диареи. Его можно применять детям старше 3 месяцев и взрослым. Однако в настоящее время это не рекомендуется в Великобритании при диарее путешественников.
Противодиарейные препараты
Противодиарейные лекарства обычно не требуются. Однако, возможно, вы захотите сократить количество походов в туалет. Это может быть необходимо, если вы путешествуете. Перед поездкой вы можете купить в аптеке противодиарейные лекарства. Самый безопасный и эффективный — лоперамид. Сначала доза для взрослых составляет две капсулы. Затем следует по одной капсуле после каждого прохождения диареи, максимум до восьми капсул за 24 часа.Он работает, замедляя деятельность вашего кишечника.
Альтернативой является Пепто-Бисмол®, который можно приобрести в аптеке без рецепта. Однако некоторым людям не следует принимать Пепто-Бисмол®. К ним относятся люди с аллергией на аспирин, люди, получающие антикоагулянтное лечение, такое как варфарин, люди с проблемами почек или люди с подагрой. Беременным или кормящим женщинам также не следует принимать Пепто-Бисмол®. Внимательно прочтите брошюру или спросите своего врача или фармацевта перед поездкой, безопасно ли вам принимать Пепто-Бисмол®.
Не следует принимать лоперамид или Пепто-Бисмол® дольше двух дней. Вы также не должны использовать противодиарейные лекарства, если у вас высокая температура (жар) или кровавый понос.
Ешьте как можно более нормально
Раньше рекомендовали какое-то время «голодать», если у вас диарея. Однако теперь по возможности рекомендуется есть небольшими легкими блюдами. Руководствуйтесь своим аппетитом. Вы можете не чувствовать аппетита, и большинство взрослых могут обходиться без еды в течение нескольких дней. Ешьте, как только сможете, но не бросайте пить.Если вы все же захотите поесть, избегайте жирной, острой или тяжелой пищи. Простые продукты, такие как хлеб и рис, — это хорошие продукты, которые стоит попробовать.
Антибиотики
Большинство людей, страдающих диареей путешественников, не нуждаются в лечении антибиотиками. Однако иногда рекомендуется лечение антибиотиками. Это может быть связано с тем, что конкретный микроб (микроб) был идентифицирован после анализа образца стула (фекалий).
Некоторым группам людей может быть рекомендовано брать с собой некоторые антибиотики «на всякий случай» во время путешествий, чтобы вы могли начать принимать их, если у вас появятся симптомы.Всемирная организация здравоохранения рекомендует рассмотреть возможность применения антибиотиков «на всякий случай» для тех, кто находится в местах, где медицинская помощь недостаточна или недоступна. Его следует начинать, если испражнения становятся «очень частыми, очень водянистыми, содержат кровь или длятся более трех дней». Обычно в качестве антибиотиков используют ципрофлоксацин, азитромицин или рифаксимин. Если вам посоветовали взять с собой в отпуск антибиотик «на всякий случай», ваш врач должен будет выписать его по частному рецепту.(Таким же образом выдаются таблетки от малярии или некоторые туристические вакцины. Они не могут быть прописаны в NHS.)
Как лечится диарея путешественников у детей?
Жидкости для предотвращения обезвоживания
Вы должны поощрять вашего ребенка пить много жидкости. Цель — предотвратить недостаток жидкости в организме (обезвоживание). Жидкость, потерянную при рвоте и / или диарее, необходимо восполнить. Ваш ребенок должен продолжать свою обычную диету и пить обычные напитки.Кроме того, их также следует поощрять пить больше жидкости. Однако избегайте фруктовых соков и газированных напитков, так как они могут усугубить диарею.
Дети младше 6 месяцев подвержены повышенному риску обезвоживания. Вам следует обратиться за медицинской помощью, если у них разовьется острая диарея. Следует поощрять кормление грудью или из бутылочки как обычно. Вы можете обнаружить, что потребность вашего ребенка в корме увеличивается. Вам также могут посоветовать давать дополнительные жидкости (воду или напитки для регидратации) между кормлениями.
Перед поездкой разумно подумать о покупке саше для пероральной регидратации для детей. Они могут обеспечить идеальный баланс воды, солей и сахара и могут использоваться для восполнения жидкости. Помните, что, как упоминалось выше, для восстановления пакетиков необходима безопасная вода.
Если у вашего ребенка рвота, подождите 5-10 минут, а затем снова начните давать напитки, но более медленно (например, по ложке каждые 2-3 минуты). Использование шприца может помочь детям младшего возраста, которые не могут делать глотки.
Примечание : если вы подозреваете, что у вашего ребенка обезвоживание или обезвоживание, вам следует срочно обратиться за медицинской помощью.
Жидкости для лечения обезвоживания
Если у вашего ребенка умеренное обезвоживание, его можно лечить, дав ему напитки для регидратации. Врач посоветует, сколько давать. Это может зависеть от возраста и веса вашего ребенка. Если вы кормите грудью, продолжайте это в течение этого времени. Важно, чтобы ваш ребенок получил регидратацию до того, как он будет есть твердую пищу.
Иногда ребенку может потребоваться госпитализация для лечения, если он обезвожен. Лечение в больнице обычно включает введение раствора для регидратации через специальный зонд, называемый «назогастральный зонд». Эта трубка проходит через нос вашего ребенка, спускается вниз по горлу и прямо в желудок. Альтернативное лечение — это жидкости, вводимые непосредственно в вену (внутривенные жидкости).
Ешьте как можно более нормально после лечения любого обезвоживания
Коррекция любого обезвоживания является первоочередной задачей.Однако, если ваш ребенок не обезвожен (в большинстве случаев) или после того, как обезвоживание было устранено, посоветуйте ему придерживаться обычной диеты. Не «морите» ребенка инфекционной диареей. Раньше это советовали, но теперь известно, что это неверно. Итак:
- Дети, находящиеся на грудном вскармливании, должны продолжать получать грудное вскармливание, если они будут его брать. Обычно это будет в дополнение к напиткам для дополнительной регидратации (описанным выше).
- Детей, находящихся на искусственном вскармливании, следует кормить обычным полноценным кормом, если они будут его есть.Опять же, это обычно будет в дополнение к дополнительным напиткам для регидратации (описанным выше).
- Дети постарше — время от времени предлагайте им немного еды. Однако, если он или она не хочет есть, это нормально. Напитки являются наиболее важным фактором, и еда может подождать, пока не вернется аппетит.
Лекарство
Ни лоперамид, ни Пепто-Бисмол® не рекомендуются детям с диареей. Есть опасения, что лоперамид может вызвать непроходимость кишечника (кишечную непроходимость) у детей с диареей.Pepto-Bismol® содержит салицилат, который не следует применять детям в возрасте до 16 лет из-за возможной связи между салицилатами и синдромом Рея (редкая проблема, вызывающая воспаление головного мозга и печеночную недостаточность).
Как и для взрослых, рацекадотрил — это вариант, предназначенный для лечения регидратации. Его можно применять детям старше 3 месяцев. Однако в настоящее время это не рекомендуется в Великобритании при диарее путешественников.
Большинство детей с диареей путешественников не нуждаются в лечении антибиотиками.Однако по тем же причинам, которые описаны выше для взрослых, в некоторых случаях может быть рекомендовано лечение антибиотиками.
Есть ли осложнения?
Большинство людей болеют в легкой форме, и осложнения диареи путешественников возникают редко. Однако если возникают осложнения, они могут включать следующее:
- Солевой (электролитный) дисбаланс и недостаток жидкости в организме (обезвоживание) . Это наиболее частое осложнение. Это происходит, если соли и вода, которые теряются с калом (фекалиями) или когда вы заболели (рвота), не восполняются употреблением достаточного количества жидкости.Если вам удастся пить много жидкости, то обезвоживание маловероятно или, скорее всего, будет умеренным и скоро восстановится после питья. Сильное обезвоживание может привести к падению артериального давления. Это может привести к снижению притока крови к жизненно важным органам. Если обезвоживание не лечить, ваши почки могут быть повреждены. Некоторым людям, страдающим сильным обезвоживанием, необходимо «капать» жидкость прямо в вену. Для этого требуется госпитализация. Люди пожилого возраста или беременные более подвержены риску обезвоживания.
- Реактивные осложнения . В редких случаях другие части вашего тела могут «реагировать» на инфекцию кишечника. Это может вызвать такие симптомы, как воспаление суставов (артрит), воспаление кожи и воспаление глаз (конъюнктивит или увеит). Реактивные осложнения возникают нечасто, если у вас есть вирус, вызывающий диарею путешественника.
- Распространение инфекции на другие части вашего тела , такие как кости, суставы или мозговые оболочки, окружающие головной и спинной мозг.Это редко. Если это действительно происходит, это более вероятно, если диарея вызвана инфекцией сальмонеллы.
- Стойкие диарейные синдромы могут развиваться редко:
- Синдром раздраженного кишечника иногда вызывается приступом диареи путешественника.
- Непереносимость лактозы иногда может возникать в течение определенного периода времени после диареи путешественника. Это явление известно как «вторичная» или «приобретенная» непереносимость лактозы. Эпизод диареи может повредить слизистую оболочку кишечника (кишечника).Это приводит к недостатку вещества (фермента), называемого лактазой, которое необходимо для того, чтобы помочь вашему организму переваривать молочный сахар лактозу. Непереносимость лактозы приводит к вздутию живота, болям в животе (животу), ветру и водянистому стулу после употребления молока. Состояние улучшается, когда инфекция проходит и слизистая оболочка кишечника заживает. Чаще встречается у детей.
- Гемолитико-уремический синдром — еще одно возможное осложнение. Это редко и обычно связано с диареей путешественников, вызванной определенным типом E.coli инфекция. Это серьезное заболевание, при котором наблюдается анемия, низкий уровень тромбоцитов в крови и повреждение почек. Чаще встречается у детей. Если распознать и лечить, большинство людей выздоравливают хорошо.
- Синдром Гийена-Барре в редких случаях может быть вызван инфекцией кампилобактерия, одной из причин диареи путешественников. Это состояние, которое поражает нервы по всему телу и конечностям, вызывая слабость и сенсорные проблемы. См. Дополнительную информацию в отдельной брошюре «Синдром Гийена-Барре».
- Снижение эффективности некоторых лекарственных средств . Во время эпизода диареи путешественника некоторые лекарства, которые вы принимаете по другим причинам или причинам, могут быть не такими эффективными. Это потому, что диарея и / или тошнота (рвота) означают, что меньшее количество лекарств попадает (всасывается) в ваш организм. Примеры таких лекарств — лекарства от эпилепсии, диабета и контрацепции. Поговорите со своим врачом или практикующей медсестрой перед поездкой, если вы не уверены, что делать, если вы принимаете другие лекарства и у вас развивается диарея.
Каковы перспективы (прогноз)?
Как упоминалось выше, симптомы обычно кратковременны, и болезнь обычно легкая, и большинство людей полностью выздоравливает в течение нескольких дней. Однако у некоторых людей, страдающих диареей путешественников, развивается стойкая (хроническая) диарея, которая может длиться один месяц и более. Также возможен второй приступ диареи путешественника во время той же поездки. Один раз, похоже, не защитит вас от заражения в будущем.
Как избежать диареи путешественников?
- Избегайте сырого мяса, моллюсков и яиц.Избегайте салатов и очищенных фруктов.
- Будьте осторожны с тем, что вы пьете. Не пейте воду из-под крана, даже кубики льда.
- Регулярно мойте руки, особенно перед приготовлением пищи или приемом пищи.
- Будьте осторожны при плавании. Загрязненная вода может вызвать диарею путешественника.
Регулярное мытье рук
Вы должны всегда мыть руки и тщательно их сушить; научите детей мыть и сушить свои:
- После посещения туалета (и после смены подгузников или помощи старшему ребенку в посещении туалета).
- Перед приготовлением или прикосновением к еде или напиткам.
- Перед едой.
Некоторые антибактериальные гели для рук можно брать с собой в поездку, если мыло и горячая вода недоступны.
Будьте осторожны с тем, что вы едите и пьете
Путешествуя в районы с плохими санитарными условиями, вам следует избегать еды или питьевой воды, которые могут содержать микробы (микробы) или их яды (токсины). Избегайте:
- Водопроводная вода.
- Фруктовые соки у уличных торговцев.
- Мороженое (если оно не было изготовлено из безопасной воды).
- Кубики льда.
- Моллюски (например, мидии, устрицы, моллюски) и сырые морепродукты.
- Яйца.
- Салаты.
- Сырое или недоваренное мясо.
- Плод с уже очищенной кожурой или с поврежденной кожицей.
- Пища, содержащая сырые или сырые яйца, например майонез или соусы.
- Молоко непастеризованное.
Вода в бутылках и газированные напитки в запечатанных бутылках или банках, чай, кофе и алкоголь считаются безопасными для употребления.Однако избегайте кубиков льда и не бутилированной воды в алкогольных напитках. Пища должна быть тщательно приготовлена и при подаче быть очень горячей. Вы также должны быть осторожны при употреблении еды с рынков, уличных торговцев или буфетов, если не уверены, хранилась ли она горячей или охлажденной. Свежий хлеб обычно безопасен, как и консервы или продукты в запечатанных пакетах.
Будьте осторожны при плавании
Купание в загрязненной воде также может привести к диарее путешественников. Старайтесь не глотать воду во время плавания; учите детей делать то же самое.
Получите во время поездки медицинский совет перед поездкой
Всегда заблаговременно до поездки обязательно посещайте приемный врач или туристическую клинику для получения консультации по вопросам здоровья. Кроме того, веб-сайт Fit for Travel (см. Раздел «Дополнительная литература и ссылки» ниже) предоставляет информацию о здоровье путешественников и конкретную информацию для разных стран. Сюда входит информация о любых требуемых прививках, советы о еде, воде и мерах личной гигиены и т. Д.Вакцины, предотвращающей диарею путешественников в целом, не существует. Однако есть и другие вакцины, которые могут вам понадобиться во время путешествия, например, против гепатита А, брюшного тифа и т. Д. В зависимости от того, где вы путешествуете, вам также может потребоваться принимать таблетки от малярии.
Прием антибиотиков для предотвращения диареи путешественников (профилактика антибиотиками) обычно не рекомендуется. Это связано с тем, что для большинства людей диарея путешественников носит умеренный характер и проходит самостоятельно. Кроме того, антибиотики не защищают от небактериальных причин диареи путешественников, таких как вирусы и паразиты.Антибиотики могут иметь побочные эффекты, и их ненужное использование может привести к проблемам с устойчивостью к лекарствам.
Тем не менее, есть несколько случаев, когда может быть рекомендована профилактика антибиотиками. Иногда людям из группы очень высокого риска назначают курс антибиотиков на всю поездку, чтобы предотвратить диарею путешественников. В таких случаях обычно используют ципрофлоксацин. Это только для людей, которые с большой вероятностью могут серьезно заболеть, отправляясь в путешествие с очень высоким риском.Например:
- Людям с нарушенной иммунной системой. (Например, люди с ВИЧ-инфекцией и те, кто получает химиотерапию или лекарства, влияющие на иммунную систему.)
- Люди, у которых более высока вероятность развития кишечных осложнений. Сюда входят люди с проблемами кишечника. (Например, болезнь Крона, язвенный колит, илеостомия или колостома и т. Д.)
- Люди с другими проблемами со здоровьем, такими как серповидноклеточная анемия или диабет 1 типа.
Пробиотики в некоторой степени влияют на диарею путешественников и могут сократить приступ примерно на один день. Пока неизвестно, какой тип пробиотика и в какой дозе, поэтому нет рекомендаций по использованию пробиотиков для предотвращения диареи путешественников.
Больничный эпиднадзор за ротавирусом и другими вирусными возбудителями диареи у детей и взрослых в России, 2005–2007 | Журнал инфекционных болезней
Абстрактные
В течение двухлетнего периода 2005–2007 гг. Мы провели наблюдение за ротавирусами группы А и другими кишечными возбудителями среди пациентов, госпитализированных с острым гастроэнтеритом в 8 различных городах Российской Федерации.Образцы фекалий были собраны у 3208 детей (в том числе 2848 детей в возрасте до 5 лет) и 1354 взрослых, госпитализированных в больницы Москвы, Санкт-Петербурга, Челябинска, Нижнего Новгорода, Тюмени, Хабаровска, Махачкалы и Якутска. Полимеразная цепная реакция была проведена для обнаружения ротавирусов групп А и С, норовирусов геногрупп I и II, астровирусов, саповирусов и кишечных аденовирусов (группа F). Ротавирус группы А был наиболее частым вирусным патогеном, выявляемым среди детей в возрасте до 5 лет (43.6%), за ним следует норовирус (12,5%), тогда как норовирус был патогеном, наиболее часто обнаруживаемым у взрослых (11,9%). Генотипы P и G были определены для 515 образцов ротавируса, и наиболее распространенными генотипами были G1P [8] (44,9%), G4P [8] (40,0%), G2P [4] (8,5%) и G3P [8] ( 6,6%). Данное исследование является первым многоцентровым исследованием ротавирусов в Российской Федерации и документирует серьезное бремя болезней, вызываемых этим патогеном, которые вскоре можно будет предотвратить с помощью вакцинации
.Хотя ротавирусная инфекция считается наиболее частой причиной острого детского гастроэнтерита во всем мире [1–3], во многих странах отсутствуют важные данные о местной распространенности заболевания, необходимые для принятия решений.Ротавирусные инфекции являются универсальными, поражая большинство детей в течение первых нескольких лет жизни, но бремя тяжелой ротавирусной болезни представляет собой особую проблему в странах с низким и средним уровнем доходов, где доступ к медицинской помощи может быть ограничен и где могут возникнуть кишечные инфекции. фатальный [4, 5]. Разработка новых вакцин для предотвращения ротавируса требует оценки местного бремени ротавирусной болезни, чтобы каждая страна могла оценить полезность вакцин в своих собственных условиях.Чтобы помочь таким исследованиям, Всемирная организация здравоохранения (ВОЗ) опубликовала общий протокол для изучения распространенности ротавируса среди детей с тяжелой диареей, которые поступают в дозорные больницы, чтобы дать представление о бремени тяжелого заболевания [6]
В 2005 году Центральный научно-исследовательский институт эпидемиологии (ЦНИИЭ) в Москве начал расследование эпидемиологии ротавируса и других вирусных агентов гастроэнтерита среди пациентов, госпитализированных в 8 разных городах Российской Федерации.Поскольку у нас был доступ к платформе молекулярной диагностики, разработанной в CRIE, мы расширили рекомендованные ВОЗ алгоритмы для эпиднадзора за ротавирусами, включили пациентов всех возрастов и проверили их фекальные образцы на ротавирус и 5 дополнительных вирусных патогенов. В этой статье обобщены данные по выявлению различных вирусных патогенов и подробно рассматривается конкретная роль ротавируса в гастроэнтерите, приводящем к госпитализации как детей, так и взрослых
Методы
Дизайн исследования В исследование были включены пациенты с острым гастроэнтеритом, определяемым по ≥3 более жидкому, чем обычно, стулу и / или рвоте в течение 24 часов до госпитализации, которые были госпитализированы в инфекционные больницы в 8 различных городах Российской Федерации. : Москва, С.-Петербург, Челябинск, Нижний Новгород, Тюмень, Хабаровск, Махачкала, Якутск. Для всех пациентов была собрана единая эпидемиологическая и клиническая информация. Образцы фекалий собирали в день поступления, разводили в фосфатно-солевом буфере, содержащем 20% глицерина, и хранили при температуре от -15 ° C до -20 ° C не более 30-40 дней. Впоследствии замороженные образцы были доставлены в лабораторию CRIE в Москве и были протестированы на ряд кишечных вирусных патогенов
Лабораторная диагностика ротавирусной инфекции Лаборатория CRIE разработала платформу на основе полимеразной цепной реакции (ПЦР). тесты для обнаружения различных кишечных вирусов, которые были коммерциализированы в Российской Федерации и продаются в виде наборов под торговой маркой AmpliSens.Набор AmpliSens Rotavirus-290 использовался для обнаружения ротавируса, и предыдущие сравнения этого набора с Premier Rotaclone (Meridian Diagnostics) продемонстрировали очень высокое соответствие как чувствительности, так и специфичности (> 96%) (данные не показаны) [7]. Образцы, собранные в Москве и Челябинске в 2005–2006 гг., Были протестированы с помощью стандартной ПЦР на ротавирус группы А, геногруппы норовируса I и II, астровирус и аденовирус. Образцы, полученные в других городах в течение этого интервала, и все образцы, собранные с 2007 года, были исследованы с использованием набора AmpliSens OKI screen PCR (CRIE) для множественного обнаружения ротавируса группы A, норовируса геногруппы II, астровируса и аденовируса группы F с использованием флуоресцентного обнаружения в формат конечной точки со специфическими зондами TaqMan для маяков.Отрицательные образцы были протестированы на ротавирус группы С и саповирусы [8, 9]. Все образцы были также протестированы на наличие бактериальных патогенов ( видов Shigella , энтероинвазивных видов Escherichia coli, Salmonella и термофильных видов Campylobacter) с использованием тест-систем AmpliSens (данные не показаны)
Ротавирусы группы A были охарактеризованы как: определить наиболее распространенные генотипы P (P [4] и P [8]) и генотипы G (G1, G2, G3 и G4) с помощью ПЦР с множественным флуоресцентным определением конечной точки.Для ПЦР мы использовали набор обратных праймеров: 2T1, 1-T1, 9T4, 9T2 и 9T3P, описанных в других источниках [10, 11] (таблица 1). Прямые праймеры и специфические зонды TaqMan были разработаны с помощью программного обеспечения Sarani (Strand Genomics), при этом некоторые зонды содержат модифицированные нуклеотиды для улучшения их аналитических характеристик. Области сегментов генома VP4 и VP7 различных типов ротавирусов P и G были клонированы в фаги MS2, и эти клоны были использованы в качестве положительных контролей для типирования ротавируса
.Таблица 1
Последовательности праймеров и зондов, используемых для обнаружения и типирования штаммов ротавирусов
Таблица 1
Последовательности праймеров и зондов, используемых для обнаружения и типирования штаммов ротавирусов
Результаты
В 2005–2007 гг. Были исследованы образцы кала 3208 детей в возрасте до 14 лет (включая 2848 детей в возрасте до 5 лет) и 1354 взрослых, госпитализированных по поводу гастроэнтерита (Таблица 2).Среди детей в возрасте до 5 лет и всех детей в возрасте до 14 лет ротавирус был наиболее частым патогеном, выявляемым у 43,6% и 41,0% соответственно. Из ротавирус-положительных детей в возрасте до 5 лет и детей в возрасте до 14 лет у 33,3% и 30,5%, соответственно, ротавирус был идентифицирован как единственный патоген, а у 10,3% и 9,5%, соответственно, ротавирус был обнаружен вместе с 1 из другие патогены, которые могут быть обнаружены тест-системами, использованными в этом исследовании. Ротавирус также был обнаружен у 8.2% взрослых страдают острой диареей, в том числе 6,6% с ротавирусом в качестве единственного патогена и 1,6% с ротавирусом, смешанным с другими патогенами. Норовирус был вторым по частоте вирусным патогеном у детей в возрасте до 5 лет (12,5%) и был наиболее частым вирусным патогеном у взрослых (11,9%)
Таблица 2
Показатели выявления вирусных патогенов, выделенных у детей и взрослых, госпитализированных по поводу гастроэнтерита в Российской Федерации, 2005–2007 гг.
Таблица 2
Показатели выявления вирусных патогенов, выделенных от детей и взрослых, госпитализированных по поводу гастроэнтерита в России Federation, 2005–2007
Из детей в возрасте до 5 лет с ротавирусной диареей 12% были в возрасте до 6 месяцев, 43% — в возрасте до 1 года и 74% — в возрасте до 2 лет (Таблица 3).Скорость выявления ротавируса была наибольшей у детей в возрасте от 7 месяцев до 2 лет, но младенцы младшего возраста и дети старшего возраста также могли иметь ротавирус в качестве обнаруживаемого патогена. Пиковыми сезонами госпитализации пациентов с ротавирусной инфекцией были зима и весна, с декабря по май (Рисунок 1). В этом исследовании не наблюдалось значительной разницы в сезонности ротавирусной инфекции между разными городами (Рисунок 2)
Таблица 3
Возрастное распределение ротавирусных инфекций группы А у детей в возрасте <5 лет, госпитализированных по поводу гастроэнтерита в Российской Федерации, 2005–2007
Таблица 3
Возрастное распределение ротавирусных инфекций группы А у детей в возрасте <5 лет Кто госпитализирован по поводу гастроэнтерита в Российской Федерации, 2005–2007 гг.
Рисунок 1
Сезонность ротавирусных инфекций среди детей, госпитализированных в 8 разных городах Российской Федерации, 2005–2007 гг.
Рисунок 1
Сезонность ротавирусных инфекций среди детей, госпитализированных в 8 разных городах Российской Федерации, 2005–2007 гг.
Рисунок 2
Круглогодичная сезонность ротавирусных инфекций среди детей, госпитализированных в Российской Федерации, по городам, в 2005–2007 гг.
Рисунок 2
Круглогодичная сезонность ротавирусных инфекций среди детей, госпитализированных в Российской Федерации, по городам , в 2005–2007 гг.
В 2005–2007 гг. G1P [8] был наиболее часто обнаруживаемым типом штаммов (44.9%), затем идут G4P [8] (40,0%), G3P [8] (6,6%) и G2P [4] (8,5%). Между городами и годами наблюдались значительные различия между типами штаммов (таблица 4)
Таблица 4
Распределение генотипа ротавируса среди детей в возрасте до 5 лет в нескольких городах Российской Федерации, 2005–2007 гг.
Таблица 4
Распределение генотипа ротавируса среди детей в возрасте до 5 лет в нескольких городах Российской Федерации, 2005– 2007
Обсуждение
Это исследование предоставляет данные о роли ротавируса группы А как у детей, так и у взрослых с тяжелым гастроэнтеритом, которым потребовалась госпитализация в 8 медицинских учреждениях в Российской Федерации.Общий уровень выявления ротавируса группы А среди детей в возрасте до 5 лет составил 43,6%, что сопоставимо с показателями, обнаруженными в исследованиях, проведенных во многих других странах Европы, Америки и Азии [3]. Однако, поскольку в этом исследовании также рассматривались различные вирусные кишечные патогены, примерно четверть всех детей в возрасте <5 лет с ротавирусной инфекцией были инфицированы другим патогеном. Это поднимает интересные вопросы о том, действительно ли ротавирус был этиологическим агентом болезни у этих пациентов и каков был вклад других патогенов.Хотя другие надзорные исследования, в которых изучается только ротавирус, могут завышать сведения о ротавирусе как о предполагаемой причине диареи, исследования вакцины неоднократно обнаруживали, что вакцина против ротавируса снижает частоту диареи у детей в большей степени, чем можно отнести только к ротавирусу [12]. Использование этой диагностической платформы для обнаружения множественных вирусных агентов на основе ПЦР могло бы пролить новый свет на вопрос о том, когда патоген является истинным возбудителем болезни
Некоторые особенности, выявленные в этом исследовании, заслуживают особого внимания.Во-первых, относительно высокие показатели выявления ротавирусов, обнаруженные в 8 городах, аналогичны показателям предыдущих пилотных исследований в Москве в 2005–2007 гг. (740 [45,9%] из 1613 детей в возрасте до 5 лет) (А. Мухина, личное сообщение ). Во-вторых, возрастное распределение детей с ротавирусной инфекцией показало, что 42% детей были в возрасте до 1 года, что соответствует показателям в США и других промышленно развитых странах [5]. В-третьих, ротавирус по-прежнему имеет отчетливую сезонность зимой и весной.Наконец, у большинства штаммов ротавирусов были общие серотипы. Однако необычные типы были выявлены другими авторами; таким образом, потребуется долгосрочный мониторинг для выявления новых штаммов, которые могут возникнуть [13–16]. Особое внимание к этому вопросу требуется на территориях с активным применением ротавирусных вакцин.
В этом исследовании также изучалась ротавирусная инфекция у взрослых и рассматривались множественные вирусные патогены. Примечательно, что, несмотря на общее мнение о том, что взрослые имеют хороший иммунитет к ротавирусной болезни, у многих взрослых с диареей ротавирус был обнаружен в образцах кала.Это говорит о том, что ротавирус является проблемой как у взрослых, так и у детей, или что у этих пациентов могут быть коинфекции, а ротавирус не способствует развитию болезни. Исследование, проведенное в Японии, показало, что ротавирус был выделен 14% из 693 взрослых пациентов с гастроэнтеритом, обратившихся в отделения неотложной помощи, и 5% пациентов без диареи [17]. Предыдущие исследования продемонстрировали присутствие ротавируса в нескольких группах риска взрослых [18] — пожилых людей, родителей и опекунов маленьких детей, лиц с ослабленным иммунитетом и путешественников, — но у нас не было достаточно информации, чтобы выяснить, были ли какие-либо из этих факторов риска чаще встречается в исследуемой популяции.Мы обнаружили, что норовирус был вторым по частоте вирусным возбудителем гастроэнтерита среди детей и наиболее распространенным возбудителем среди взрослых. Усилия по разработке методов профилактики норовирусной инфекции, возможно, должны получить более высокий приоритет, потому что важность этого патогена всегда недооценивалась из-за отсутствия чувствительных диагностических методов для его обнаружения. Это исследование демонстрирует дополнительную ценность использования широкой панели диагностических тестов для понимания этиологии кишечных инфекций и определения приоритетности их важности на национальном уровне.
В заключение, это исследование заложило основу для рассмотрения необходимости будущих вмешательств с ротавирусами. вакцины, чтобы более полно изучить роль ротавируса у взрослых и провести более тщательный поиск всего спектра возбудителей диареи, чтобы мы могли разработать меры вмешательства, направленные на наиболее распространенные и наиболее важные
Ссылки
1« и др.Эпидемиология ротавирусной диареи в Соединенных Штатах: эпиднадзор и оценка бремени болезней
,J Infect Dis
,1996
, vol.174
Дополнение 1
(стр.S5
—11
) 2,,,,.Ротавирусные и ротавирусные вакцины
,Adv Exp Med Biol
,2006
, vol.582
(стр.45
—54
) 3,,,.Ротавирус и тяжелая детская диарея
,Emerg Infect Dis
,2006
, vol.12
(стр.304
—6
) 4« и др.Заболевания и смертность детей от ротавирусной инфекции в мире
,Emerg Infect Dis
,2003
, vol.9
(стр.565
—72
) 5« и др.Госпитализации и смерти от диареи и ротавируса среди детей младше 5 лет в США, 1993–2003 гг.
,J Infect Dis
,2007
, vol.195
(стр.1117
—25
) 6Всемирная организация здравоохранения
.Общий протокол для (i) эпиднадзора на базе больниц для оценки бремени ротавирусного гастроэнтерита у детей и (ii) обследования на уровне общины по использованию медицинских услуг при гастроэнтерите у детей
,Версия полевых испытаний
,2002
Женева
Всемирная организация здравоохранения
7,,, et al.Сравнительная оценка эффективности различных тест-систем для диагностики ротавирусной инфекции у детей в Новосибирске
,CERIS Новосибирск
,2005
(стр.241
—3
) 8« и др.Исследования этиологии острых кишечных инфекций у детей, поступивших в инфекционные отделения московских больниц
,Infect Dis
,2004
, vol.2
(стр.85
—92
) 9«Абрамичева Н.Ю
и др.Сезонная и возрастная структура заболеваемости острыми кишечными инфекциями в Российской Федерации
,Тер Арх
,2007
, т.79
(стр.10
—6
) 10« и др.Идентификация гена ротавируса группы А 4 типов с помощью полимеразной цепной реакции
,J Clin Microbiol
,1992
, vol.30
(стр.1365
—73
) 11« и др.Амплификация с помощью полимеразной цепной реакции и типирование нуклеиновой кислоты ротавируса из образцов кала
,J Clin Microbiol
,1990
, vol.28
(стр.276
—82
) 12,,, et al.Безопасность и эффективность аттенуированной вакцины против тяжелого ротавирусного гастроэнтерита
,N Engl J Med
,2006
, vol.354
(стр.11
—22
) 13« и др.Оценка эпидемического потенциала нового штамма ротавируса, связанного с новым серотипом G9, который вызвал вспышку в США впервые в сезоне 1995–1996 гг.
,J Clin Microbiol
,2004
, vol.42
(стр.1434
—8
) 14« и др.Характеристика нового ротавируса P [25], G11 человека группы A
,J Clin Microbiol
,2005
, vol.43
(стр.3208
—12
) 15« и др.Первое обнаружение ротавирусов G12 у новорожденных с неонатальной ротавирусной инфекцией во Всеиндийском институте медицинских наук, Нью-Дели, Индия
,J Clin Microbiol
,2007
, vol.45
(стр.3824
—7
) 16,.Появление штаммов ротавируса G12 в Дели, Индия, в 2000-2007 гг.
,J Clin Microbiol
,2008
, vol.46
(стр.1343
—8
) 17« и др.Зимняя сезонность и ротавирусная диарея у взрослых
,Ланцет
,2001
, т.357
стр.1950
18,.Ротавирусная инфекция у взрослых
,Lancet Infect Dis
,2004
, vol.4
(стр.91
—9
)© 2009 Американского общества инфекционистов
глобальная перспектива Рекомендации по клинической практике
Клинические проявления и диагностика
Хотя могут быть клинические подсказки, окончательный этиологический диагноз клинически невозможен (см. Таблицы ниже).
Таблица: Эпизоды диареи можно разделить на три категории
| Категория | Клиническое проявление |
|---|---|
| Острая диарея | Присутствие воды в течение трех или более часов аномально в течение 24 часов |
| Дизентерия | Наличие видимой крови в стуле |
| Постоянная диарея | Острый начальный эпизод диареи продолжительностью более 14 дней |
Таблица острых симптомов — связь с основными причинами Энтерогеморрагическая Escherichia coli (E.coli) (EHEC)
| Симптомы | Причины острой диареи |
|---|---|
| Лихорадка |
|
| Стул с кровью |
|
Клинические особенности инфекции отобранными диарейными патогенами см. в таблице 4 исходного руководящего документа.
Клиническая оценка
Первоначальная клиническая оценка пациента (см. Таблицу «Медицинское обследование при диарее» ниже) должна быть сосредоточена на:
- Оценка тяжести заболевания и степени (степени) обезвоживания (см. Таблицу «Оценка обезвоживания с использованием« метода Дакки »» ниже)
- Определение вероятных причин на основе истории болезни и клинических данных, включая характеристики стула
Таблица: Медицинское обследование при диарее
| История болезни | Физикальное обследование |
|---|---|
| Масса корпуса Педиатрические данные : Доказательства сопутствующих проблем у детей |
Таблица: Оценка обезвоживания с использованием «метода Дакки»
| Оценка | Plan A | Plan B | Plan C | ||
|---|---|---|---|---|---|
| Нормальное | Раздражающий / менее активный * | Вялый / коматозный * 925 | Нормальный | Затонувший | — |
| Нормальный | Сухой | — | ||
24 | | Необычная жажда24 | |||
| Нормальный | Низкий объем * | Отсутствует / неисчислимо * | ||
| Нормальный | Пониженный * | 20 | 909Некоторое обезвоживание.Имеются как минимум два знака, включая как минимум один ключевой знак (*) | Тяжелое обезвоживание. Присутствуют признаки «некоторого обезвоживания» плюс хотя бы один ключевой признак (*) |
| Лечение | Предотвращение обезвоживания | Регидратация с помощью раствора ПРС, если нет возможности пить | Регидратация с помощью внутривенных жидкостей и ПРС | ||
| Периодически проверяйте | Частая переоценка | Более частая переоценка |
* Ключевые признаки
ПРС, соли для пероральной регидратации
Лабораторное обследование
При остром энтерите и колролите, поддержание адекватного внутрисосудистого объема и устранение нарушения электролита над установлением вызывающего агента.Наличие видимой крови у пациентов с лихорадкой обычно указывает на инфекцию, вызванную инвазивными патогенами, такими как Shigella , Campylobacter jejuni , Salmonella или Entamoeba histolytica . Посев кала обычно не требуется для иммунокомпетентных пациентов с водянистой диареей, но может быть необходимо для выявления Vibrio cholerae , когда есть клиническое и / или эпидемиологическое подозрение на холеру, особенно в первые дни вспышек / эпидемий (также для определить чувствительность к противомикробным препаратам) и определить возбудителя дизентерии.
Эпидемиологические ключи к инфекционной диарее можно найти, оценив инкубационный период, историю недавних поездок в связи с региональной распространенностью различных патогенов, необычными пищевыми продуктами или обстоятельствами питания, профессиональными рисками, недавним применением противомикробных препаратов, помещением в учреждения и вирусом иммунодефицита человека ( ВИЧ) риски заражения.
Расходы на анализ стула и посевы можно снизить за счет улучшения отбора и тестирования образцов, представленных на основе интерпретации информации о случае, такой как история болезни, клинические аспекты, визуальный осмотр стула и предполагаемый инкубационный период для.См. Таблицы 7-9 в исходном руководящем документе для получения информации о подробностях истории болезни пациента и причинах острой диареи, инкубационном периоде и вероятных причинах диареи, а также подробных сведениях о пациенте и анализе на наличие бактерий, которые следует учитывать соответственно.
Скрининг обычно касается неинвазивных анализов кала. Некоторые лабораторные исследования могут быть важны, когда основной диагноз неясен или возможны другие диагнозы, кроме острого гастроэнтерита. Там, где это применимо, можно рассмотреть возможность проведения быстрых диагностических тестов (ДЭТ) для быстрого тестирования на холеру у постели пациента.
Педиатрические данные . Выявление патогенных бактерий, вирусов или паразитов в образце стула ребенка с диареей не во всех случаях указывает на то, что они являются причиной заболевания.
Измерение электролитов сыворотки может потребоваться у некоторых детей с более длительной диареей с умеренным или тяжелым обезвоживанием, особенно с атипичным анамнезом или находками. Гипернатремическое обезвоживание чаще встречается у детей с хорошим питанием и детей, инфицированных ротавирусом, и проявляется раздражительностью, повышенной жаждой, несоразмерной клинической дегидратации, и ощущением рыхлости кожи.Это требует особых методов регидратации.
Факторы прогноза и дифференциальный диагноз у детей
Таблица: Факторы прогноза у детей
| Фактор | Примечания | |
|---|---|---|
| Недоедание Приблизительно 25 | стран составляют 25 | детей в развивающихся странах сильно недовес. |
| Дефицит цинка |
| |
| Стойкая диарея |
| |
| Иммуносупрессия |
|
ВИЧ, вирус иммунодефицита человека
Дифференциальный диагноз острой диареи у детей:
- Пневмония — может возникать вместе с диареей в развивающихся странах. Менингит
Комплексное ведение детских болезней (ИВБДВ)
В развивающихся странах большая доля детской заболеваемости и смертности вызвана пятью состояниями: острыми респираторными инфекциями, диареей, корью, малярией и недоеданием.Стратегия ИВБДВ была разработана для улучшения общего состояния здоровья детей с признаками и симптомами более чем одного заболевания. В таких случаях может потребоваться более одного диагноза и, возможно, придется сочетать методы лечения состояний. Уход должен быть сосредоточен на ребенке в целом, а не только на отдельных заболеваниях или состояниях, влияющих на ребенка, в то время как другие факторы, влияющие на качество ухода за детьми, такие как наличие лекарств, организация системы здравоохранения, направление к специалистам пути и услуги, а также поведение сообщества — лучше всего решать с помощью комплексной стратегии.
Стратегия ИВБДВ включает ряд мероприятий по профилактике и лечению основных детских болезней как в медицинских учреждениях, так и дома. Он включает многие элементы программы борьбы с диарейными и острыми респираторными инфекциями, а также связанные с детьми аспекты борьбы с малярией, программы питания, иммунизации и основных лекарственных средств (Всемирная организация здравоохранения [ВОЗ], Бангладеш; см. Http: // www. who.int/countries/bgd/en/).
Варианты лечения и профилактики
Регидратация у взрослых и детей
Пероральная регидратационная терапия (ОРТ) — это пероральное введение соответствующих растворов для предотвращения или коррекции диарейного обезвоживания.ОРТ — это экономически эффективное лечение острого гастроэнтерита, также в развитых странах.
Соли для пероральной регидратации (ORS), используемые в ORT, содержат определенные количества важных солей, которые теряются с калом при диарее. Новый ПРС с более низкой осмолярностью (рекомендованный ВОЗ и Международным фондом чрезвычайных ситуаций для детей Организации Объединенных Наций [ЮНИСЕФ]) снижает концентрацию натрия и глюкозы и ассоциируется с меньшей рвотой, меньшим выделением стула, меньшей вероятностью гипернатриемии и уменьшением потребности во внутривенном введении. инфузии по сравнению со стандартным ПРС (см. Таблицу 11 в исходном руководящем документе).Этот состав рекомендуется независимо от возраста и типа диареи, включая холеру.
ОРТ состоит из:
- Регидратация — вода и электролиты вводятся для возмещения потерь.
- Поддерживающая жидкостная терапия для лечения текущих потерь после достижения регидратации (наряду с соответствующим питанием).
ORT противопоказан при начальном лечении тяжелого обезвоживания, а также у детей с паралитической кишечной непроходимостью, частой и стойкой рвотой (более четырех эпизодов в час) и болезненными состояниями полости рта, такими как молочница средней и тяжелой степени (кандидоз полости рта).Однако назогастральное введение раствора ПРС потенциально может спасти жизнь, когда внутривенная регидратация невозможна и пациента транспортируют в учреждение, где может быть назначена такая терапия.
ПРС на рисовой основе превосходит стандартные ПРС для взрослых и детей, больных холерой, и может использоваться для лечения таких пациентов везде, где его приготовление удобно. Он не превосходит стандартный ПРС при лечении детей с острой диареей, не связанной с холерой, особенно когда пища дается вскоре после регидратации, что рекомендуется для предотвращения недоедания.
Дополнительная терапия цинком, поливитамины и минералы у детей
Дефицит цинка широко распространен среди детей в развивающихся странах. Рутинная терапия цинком в качестве дополнения к ОРТ полезна для умеренного уменьшения тяжести, но, что более важно, для уменьшения эпизодов диареи у детей в развивающихся странах. Всем детям с диареей рекомендуется принимать 20 мг цинка в день в течение 10 дней. Младенцы в возрасте 2 месяцев и младше должны получать 10 мг в день в течение 10 дней.
Добавка с сульфатом цинка в рекомендуемых дозах снижает частоту диареи в течение следующих 3 месяцев и снижает неслучайную смертность на 50%. Это более важно при лечении диареи у детей с недостаточным питанием и постоянной диареи. ВОЗ и ЮНИСЕФ рекомендуют рутинную терапию цинком для детей с диареей, независимо от типа.
Все дети с постоянной диареей должны получать дополнительные поливитамины и минералы, включая магний, каждый день в течение 2 недель.Часто подходят местные коммерческие препараты; Таблетки, которые можно измельчить и давать во время еды, являются наименее дорогостоящими. Они должны обеспечивать как можно более широкий спектр витаминов и минералов, включая как минимум две рекомендуемые суточные нормы (РСН) фолиевой кислоты, витамина А, цинка, магния и меди. (См. Таблицу 12 в исходном руководящем документе по RDA для 1-летнего ребенка.)
Диета
Практика воздержания от еды более 4 часов неуместна — нормальное кормление следует продолжать для тех, у кого нет Признаки обезвоживания, и прием пищи следует начинать сразу после коррекции некоторого (умеренного) и тяжелого обезвоживания, которое обычно занимает 2–4 часа, с помощью ОРТ или внутривенной регидратации.
Педиатрические данные . Младенцы и дети, находящиеся на грудном вскармливании, должны продолжать получать пищу даже во время фазы регидратации. Однако для обезвоженных детей и взрослых, не находящихся на грудном вскармливании, регидратация является первоочередной задачей, и ее можно выполнить за 2–4 часа.
Примечания ниже относятся как к взрослым, так и к детям, если возраст не указан.
Предоставьте:
- Соответствующая возрасту диета — независимо от жидкости, используемой для ОРТ / поддерживающей терапии
- Частые небольшие приемы пищи в течение дня (шесть приемов пищи в день), особенно для младенцев и маленьких детей
- Энергия и микроэлементы богатая, смешанная пища (зерновые, яйца, мясо, фрукты и овощи)
- Повышение калорийности, допустимое после эпизода диареи
- Педиатрические данные .Младенцам требуется более частое грудное вскармливание или кормление из бутылочки — специальные смеси или разведения не нужны. Дети старшего возраста и взрослые должны получать обычную еду и напитки. Детям, особенно маленьким детям, следует дать еще один прием пищи после того, как у них исчезнет диарея, для наверстывающего роста.
Избегайте:
- Консервированные фруктовые соки — они гиперосмолярны и могут усугубить диарею.
Пробиотики — это живые микроорганизмы, такие как Lactobacillus GG (ATCC 53103), оказывающие благотворное влияние на здоровье человека.Однако эффекты зависят от штамма и требуют проверки для каждого штамма в исследованиях на людях. Экстраполяция результатов даже для близкородственных штаммов невозможна, и сообщалось о значительно различных эффектах. Использование пробиотиков может быть неприемлемым в условиях ограниченных ресурсов, в основном в развивающихся странах. Обратитесь к исходному руководству для получения дополнительной информации об использовании пробиотиков для лечения острой диареи.
Педиатрические данные .Контролируемые клинические интервенционные исследования и метаанализы подтверждают использование конкретных пробиотических штаммов и продуктов для лечения и профилактики ротавирусной диареи у младенцев.
Неспецифическое противодиарейное лечение
Ни один из перечисленных ниже препаратов не устраняет основные причины диареи (потеря воды, электролитов и питательных веществ). Противорвотные средства обычно не нужны при лечении острой диареи, а некоторые, обладающие седативным эффектом, могут затруднить ПРТ.
Педиатрические данные . В целом противодиарейные препараты не имеют практической пользы для детей с острой или стойкой диареей.
Препараты против моторики
Лоперамид (4–6 мг / день) является препаратом выбора для взрослых:
- Следует использовать в основном при легкой и умеренной диарее путешественников (без клинических признаков инвазивной диареи)
- Подавляет кишечник перистальтика и обладает мягкими антисекреторными свойствами.
- Следует избегать при кровавой или подозреваемой воспалительной диарее (пациенты с лихорадкой).
- Сильная боль в животе также указывает на воспалительную диарею (это противопоказание для использования лоперамида).
- Педиатрические данные . Не рекомендуется для детей — было продемонстрировано увеличение степени тяжести заболевания и осложнений, особенно у детей с инвазивной диареей.
Антисекреторные агенты
Рацекадотрил — ингибитор энкефалиназы (неопиат) с антисекреторной активностью:
- Не применяется у взрослых, больных холерой
- Педиатрические данные . Было обнаружено, что он полезен для детей, страдающих диареей, и теперь лицензирован во многих странах мира для использования у детей.
Адсорбенты
Каолин-пектин, активированный уголь, аттапульгит:
- Недостаточные доказательства эффективности при острой диарее у взрослых, увеличивают затраты и поэтому не должны использоваться.
Противомикробные препараты у взрослых и детей
Информацию об антимикробных средствах для лечения конкретных причин диареи см. В Таблице 15 исходного руководящего документа.
Важные примечания
- Все дозы, указанные в таблице 15, предназначены для перорального приема.
- Выбор противомикробного препарата должен основываться на характеристиках чувствительности штаммов патогенов в данной местности / регионе.
- Противомикробные препараты надежно полезны, и их регулярное использование рекомендуется при лечении тяжелых (клинически распознаваемых):
- Холера, шигеллез, брюшной тиф и паратиф
- Дизентерийные проявления кампилобактериоза и нетифоидного сальмонеллеза, когда они вызывают персистирующий понос у хозяина иммунный статус нарушен по любой причине, такой как тяжелое недоедание, хроническое заболевание печени или лимфопролиферативные нарушения.
- Инвазивный кишечный амебиаз.
- Симптоматический лямблиоз (анорексия и похудание, стойкая диарея, задержка развития).
- Рассмотреть возможность лечения антимикробными препаратами для:
- Shigella , Salmonella , Campylobacter (дизентерийная форма) или паразитарных инфекций
- Нетифоидный сальмонеллез среди групп риска (недоедание, младенцы и пожилые люди, пациенты с ослабленным иммунитетом, пациенты с заболеваниями печени и лимфопролиферативными расстройствами), а также при дизентерии
- Умеренная / тяжелая диарея путешественников или диарея с лихорадкой и / или с кровяным стулом
- Противомикробные препараты также показаны при сопутствующих проблемах со здоровьем, таких как пневмония
- Amebae .Непатогенные амебы чаще обнаруживаются при микроскопии кала и подвергаются неправильному лечению. Присутствие проглоченных эритроцитов при микроскопии кала амебы (гематофага) указывает на инвазивность и необходимость лечения; также при дизентерийном проявлении и отсутствии других инвазивных патогенов. Лечение амебиаза в идеале должно включать дилоксанид фуроат после приема метронидазола, чтобы избавиться от кист, которые могут остаться после лечения метронидазолом; нитазоксанид является альтернативой.
- Азитромицин широко доступен и отличается удобством однократного дозирования. Для лечения большинства типов распространенных бактериальных инфекций рекомендуемая доза азитромицина составляет 250 или 500 мг один раз в сутки в течение 3-5 дней. Дозировка для детей : доза азитромицина для детей может варьироваться (в зависимости от массы тела) от 10 мг до 20 мг на килограмм массы тела в день, один раз в день в течение 3 дней.
- Кампилобактер . Устойчивый к хинолонам Campylobacter присутствует в нескольких районах Юго-Восточной Азии (например,g., Таиланд) и азитромицин является подходящим вариантом в таких ситуациях.
- Холера . Обычная антимикробная терапия рекомендуется для лечения тяжелой (клинически распознаваемой) холеры. Фактический выбор противомикробного препарата будет зависеть от недавней восприимчивости патогена в конкретных странах; при отсутствии такой информации единственным выходом являются отчеты о восприимчивости из соседних стран.
- Эритромицин сегодня практически не используется при диарее.
- Нитазоксанид — эффективное противопротозойное средство при лечении диареи, вызванной паразитами, такими как Giardia Кишечник , Entamoeba histolytica и Cryptosporidium parvum .
- Диарея путешественников . Существуют убедительные доказательства того, что для взрослых с острой диареей однократная терапия некоторыми новыми хинолонами, такими как ципрофлоксацин, сокращает продолжительность острой диареи путешественника. Однако это по-прежнему вызывает споры; использование должно быть ограничено лицами из группы высокого риска или теми, кому необходимо оставаться здоровым во время коротких визитов в зону высокого риска. Противомикробные препараты следует рассматривать как препараты выбора для эмпирического лечения диареи путешественников. и внебольничной секреторной диареи, когда патоген известен (см. Таблицу 15 в исходном руководящем документе).
Педиатрические данные :
- Если лекарства не доступны в жидкой форме для детей младшего возраста, может потребоваться использовать таблетки и оценить дозы, указанные в Таблице 15 (см. Исходное руководство).
- Рассмотрите возможность лечения антимикробными препаратами для:
- Когда Shigella , Salmonella , Campylobacter (дизентерийная форма) являются единственным патогеном, выделенным от детей с постоянной диареей
- Нетифоидный сальмонеллез для лечения младенцев
- Альтернативные препараты для лечения холестерина. у детей — триметоприм / сульфаметоксазол (TMP / SMX; 5 мг / кг TMP + 25 мг / кг SMX, каждые 12 часов в течение 3 дней) и норфлоксацин.
Профилактика диареи с помощью вакцин
- Salmonella typhi : две вакцины против брюшного тифа (с ограниченной экономической эффективностью) в настоящее время одобрены для клинического использования.
- Организмы Shigella : в полевых испытаниях было показано, что три вакцины обладают иммуногенными и защитными свойствами. Парентеральные вакцины могут быть полезны для путешественников и военнослужащих, но нецелесообразны для использования в развивающихся странах. Более многообещающей является однократная живая аттенуированная вакцина, которая в настоящее время разрабатывается в нескольких лабораториях.
- V. cholerae : текущая цена и необходимость многократных доз (как минимум двух) и более короткой защитной эффективности являются ограничениями. Вероятно, скоро появится новая, более дешевая вакцина на убитых клетках; Оральные вакцины против холеры все еще исследуются, и их использование рекомендуется только в сложных чрезвычайных ситуациях, таких как эпидемии. Их использование в эндемичных районах остается спорным. При диарее путешественника пероральная вакцина против холеры рекомендуется только тем, кто работает в лагерях беженцев или лагерях помощи, поскольку риск холеры для обычного путешественника очень низок.
- Энтеротоксигенная вакцина E. coli (ETEC): наиболее продвинутая кандидатная вакцина ETEC состоит из состава убитых цельных клеток плюс субъединица B рекомбинантного холерного токсина. В настоящее время нет вакцин для защиты от инфекции E. coli , продуцирующей токсин шига.
Педиатрические данные :
- Salmonella typhi : в настоящее время вакцина не подходит для рутинного использования у детей в развивающихся странах.
- Ротавирус: в 1998 году ротавирусная вакцина RotaShield (Wyeth) была лицензирована в США для плановой иммунизации младенцев. В 1999 году производство вакцины было остановлено после того, как вакцина была причинно связана с инвагинацией кишечника у младенцев. Другие ротавирусные вакцины находятся в стадии разработки, и предварительные испытания многообещающи. В настоящее время одобрены две вакцины: живая оральная вакцина RotaTeq, производимая Merck для детей, и Rotarix от GSK.
- Иммунизация против кори может существенно снизить заболеваемость и тяжесть диарейных заболеваний.Каждый младенец должен быть вакцинирован против кори в рекомендованном возрасте.
Клиническая практика
Подход к взрослым с острой диареей
- Выполните первоначальную оценку.
- Управляйте обезвоживанием.
- Предотвратите обезвоживание у пациентов без признаков обезвоживания, используя домашние жидкости или раствор ПРС.
- Регидратация пациентов с некоторым обезвоживанием с использованием ПРС и правильное обезвоживание пациента с тяжелым обезвоживанием с помощью соответствующей внутривенной жидкости.
- Поддерживайте гидратацию с помощью раствора ПРС.
- Лечение симптомов (при необходимости рассмотрите возможность применения субсалицилата висмута или лоперамида в случае недизентерийной диареи путешественника).
- Стратифицировать последующее ведение:
- Эпидемиологические ключи: еда, антибиотики, сексуальная активность, путешествия, уход за детьми в дневное время, другие болезни, вспышки, время года.
- Клинические признаки: кровавый понос, боль в животе, дизентерия, истощение, воспаление кала.
- Возьмите образец кала для анализа:
- При тяжелой, кровянистой, воспалительной или постоянной диарее и в начале вспышки / эпидемии.
- Подумайте о противомикробной терапии конкретных патогенов.
- Сообщить в органы здравоохранения.
- При вспышках сохранять чашки с культурами и изоляты; замораживайте пробы фекалий и пробы пищи или воды при температуре –70 ° C.
- Подлежит уведомлению в США: холера, криптоспоридиоз, лямблиоз, сальмонеллез, шигеллез и инфекция, вызывающая токсин шига E. coli (STEC).
Подход к детям с острой диареей
В 2002 году ВОЗ и ЮНИСЕФ пересмотрели свои рекомендации по рутинному использованию гипоосмолярных ПРС, а в 2004 году рекомендовали рутинное использование цинка в качестве дополнения к ОРТ для лечения детской диареи. независимо от этиологии.С тех пор более 40 стран мира приняли эти рекомендации. В странах, где были введены и новые ПРС, и цинк, уровень использования ПРС резко возрос. Принципы надлежащего лечения детей с диареей и обезвоживанием:
- Никаких ненужных лабораторных анализов или лекарств.
- Используйте ПРТ для регидратации:
- Выполните ПРТ быстро, в течение 3–4 часов.
- Обычная дополнительная терапия цинком для детей в возрасте 5 лет и младше.
- Когда обезвоживание устранено, быстрое повторное питание:
- Нормальная пища или неограниченная диета, соответствующая возрасту.
- Продолжить грудное вскармливание.
- Ввести дополнительную ПРС на случай продолжающихся потерь от диареи.
Таблица: Лечение детей в зависимости от степени обезвоживания
| Степень обезвоживания | Отсутствие или минимальное обезвоживание | Легкое или умеренное обезвоживание | Тяжелое обезвоживание | ПРС 50–100 мл / кг массы тела в течение 3–4 часов. Если рвота не проходит, пациент (ребенок или взрослый) не будет принимать ПРС и, скорее всего, потребуется внутривенное введение жидкости. | Регидратация раствором лактата Рингера (100 мг / кг) внутривенно в течение 4–6 часов. Затем введите ПРС для поддержания гидратации до выздоровления пациента. |
|---|---|---|---|
| Возмещение потерь | <10 кг массы тела: 50–100 мл ПРС на каждый эпизод диарейного стула или рвоты | ||
| Питание | Продолжайте грудное вскармливание или соответствующую возрасту нормальную диету. | Продолжать грудное вскармливание или возобновить соответствующую возрасту нормальную диету после начальной гидратации | |
ПРС, соли для пероральной регидратации
Предупреждения
- Опасно лечить пациентов с тяжелой диарейной дегидратацией с использованием 5% декстрозы с 1 / 4 физиологического раствора, и риск смерти очень высок. При диарейном обезвоживании теряется не только вода, но и ряд электролитов; важные из них — натрий, калий и бикарбонат.
- Потеря натрия больше при холере, чем при диарее с ETEC (60–110 ммоль / л), за которой следует ротавирусная диарея (около 20–40 ммоль / л) — три основные причины тяжелой дегидратирующей диареи.
- Попытки исправить обезвоживание с помощью растворов с более низким содержанием натрия (например, 38,5 ммоль / л в 1/4 физиологического раствора с 5% декстрозой) могут привести к внезапной и тяжелой гипонатриемии с высоким риском смерти.
- Лактат Рингера является подходящим решением для лечения тяжелого обезвоживания, но физиологический раствор может спасти жизнь, независимо от возраста, когда лактат Рингера недоступен.В таких случаях ПРС следует начинать, как только пациенты (взрослые и дети) научатся пить, чтобы восполнить потери бикарбоната и калия с диарейным стулом, особенно у детей.
- При острой кровавой диарее (дизентерии) у детей основными принципами терапевтического подхода являются:
- Лечение обезвоживания
- Микроскопия кала для оценки потребности в антимикробной терапии. Демонстрация инвазивных форм E. histolytica и вегетативной Giardia Кишечника у пациента с симптомами может обеспечить прямой диагноз, а наличие воспалительных клеток укажет на инвазивную диарею и введение соответствующего противомикробного агента после отправки образца кала для культуры, где это возможно.
- Частые приемы пищи небольшими порциями с повышенным потреблением белка
Алгоритм терапевтического подхода к острой кровавой диарее у детей см. На Рисунке 1 в исходном руководящем документе.
Домашнее лечение острой диареи у взрослых и детей
Легкие и неосложненные случаи недизентерийной диареи как у взрослых, так и у детей можно лечить в домашних условиях, независимо от этиологического агента, используя домашнюю жидкость или ПРС, в зависимости от ситуации.Родители / опекуны детей должны быть обучены распознаванию признаков обезвоживания и тому, когда следует отправлять детей в медицинское учреждение для лечения. Раннее вмешательство и введение домашних жидкостей / ПРС снижает обезвоживание, недоедание и другие осложнения и приводит к меньшему количеству посещений клиники и потенциально меньшему количеству госпитализаций и смертей.
Самолечение безопасно для здоровых взрослых людей. Снимает дискомфорт и социальную дисфункцию. Нет никаких доказательств того, что это продлевает болезнь.Однако это может не подходить для развивающихся стран, где диарея, требующая специальных вмешательств, более распространена, и люди могут быть некомпетентными в оценке своего состояния.
Принципы самолечения:
- Поддерживайте адекватное потребление жидкости.
- Потребление твердой пищи у взрослых следует руководствоваться аппетитом; небольшие, но более частые приемы пищи для детей.
- Противодиарейный препарат с лоперамидом (гибкая доза в зависимости от жидкого кишечника) может уменьшить диарею и сократить продолжительность.
- Противомикробные препараты отпускаются по рецепту только при диарее жителей или для включения в дорожные наборы (добавьте лоперамид).
Там, где это возможно, следует рекомендовать семьям в местах с высокой распространенностью диарейных заболеваний хранить несколько пакетов с ПРС и таблеток цинка, если в семье есть дети в возрасте до пяти лет, чтобы начать домашнюю терапию, как только начнется диарея.
См. Исходное руководство по рецепту домашнего приготовления жидкости для рта.
Противодиарейные средства . Среди сотен безрецептурных препаратов, рекламируемых как противодиарейные средства, только лоперамид и субсалицилат висмута имеют достаточные доказательства эффективности и безопасности.
Семейные знания . Семейные знания о диарее должны быть усилены в таких областях, как профилактика, питание, использование ОРТ / ПРС, добавление цинка, а также когда и куда обращаться за помощью.
Показания для медицинской консультации или стационарного лечения: :
- Отчет опекуна о признаках, связанных с обезвоживанием
- Изменение психического статуса
- История преждевременных родов, хронических заболеваний или сопутствующих заболеваний
- Молодой возраст (< 6 месяцев или вес <8 кг)
- Лихорадка ≥38 ° C для младенцев <3 месяцев или ≥39 ° C для детей в возрасте 3–36 месяцев
- Видимая кровь в стуле
- Диарея с сильным выбросом, в том числе частая и длительная объемы
- Постоянная рвота, сильное обезвоживание, стойкая лихорадка
- Неоптимальный ответ на ОРТ или неспособность опекуна назначить ОРТ
- Нет улучшения в течение 48 часов — симптомы усиливаются, и общее состояние ухудшается
- Отсутствие мочи в предыдущие 12 часов
Каскады
Каскад — это иерархический набор диагностических или терапевтических методов для Это та же болезнь, согласно имеющимся ресурсам.
Таблица: Каскад для острой, тяжелой, водянистой диареи — холероподобной, с сильным обезвоживанием
| Ресурсы: от высоких к низким |
|---|
Уровень 1 антибиотики + внутривенные антибиотики диагностические тесты: микроскопия кала / посев На основании анализов: тетрациклин, фторхинолон |
Уровень 2 Внутривенные жидкости + антибиотики Эмпирические: тетрациклин, фторхинолон 3,09 |
Уровень 4 Назогастральный зонд ПРС — при стойкой рвоте |
Уровень 5 9000 909 9000 909 909 909 909 90Жидкость ротовой полости домашнего приготовления: соль, с угар и чистая вода |
ПРС, соли для пероральной регидратации; ОРТ, пероральная регидратационная терапия
Предостережения
- Если имеются возможности для направления к специалистам, пациентов с тяжелым обезвоживанием (с риском острой почечной недостаточности или смерти) следует направлять в ближайшее медицинское учреждение с внутривенным введением жидкости (уровни 5 и 6 не могут заменить необходимость направления в случае тяжелого обезвоживания).
- Уровни 5 и 6 должны рассматриваться как временные меры и лучше, чем полное отсутствие лечения, если нет доступных средств для внутривенного введения.
- При внутривенной терапии необходимо убедиться, что используются одноразовые стерильные шприцы, иглы и капельницы, чтобы избежать риска гепатита B и C.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) выпустило предупреждение о том, что фторхинолоны потенциально могут вызвать серьезное повреждение нервов.
Примечания
- Назогастральная терапия требует квалифицированного персонала.
- Часто внутривенное введение жидкости более доступно, чем кормление через назогастральный зонд. ( Осторожно, : существует риск заражения зараженным оборудованием для внутривенной инфузии.)
Педиатрические данные
- Назогастральное кормление не очень подходит для здоровых и активных детей старшего возраста, но подходит для недоедающих, летаргических детей .
- Назогастральное введение (ПРС и диета) особенно полезно у детей с длительным тяжелым истощением (анорексия).
Таблица: Каскад для острой, легкой / умеренной, водянистой диареи с легким / умеренным обезвоживанием
| Ресурсы: от высоких к низким |
|---|
Уровень 1 Внутривенные жидкости + ORT |
Уровень 2 Назогастральный зонд ORS — при стойкой рвоте |
Уровень 3 ORT | Home made жидкость: соль, сахар и чистая вода |
ПРС, соли для пероральной регидратации; ОРТ, пероральная регидратационная терапия
Каскад при острой кровянистой диарее с легким / умеренным обезвоживанием
| Ресурсы: от высоких к низким |
|---|
Уровень 1 Диагностические тесты ORT: микроскопия кала / посев Рассмотреть причины: S.dysenteriae , E. histolytica , Бактериальный колит тяжелой степени |
Уровень 2 ОРТ + антибиотики Эмпирические антибиотики при умеренном / тяжелом заболевании |
900 900 900 |
Уровень 4 Самодельная ротовая жидкость: соль, сахар и чистая вода |
ОРТ, пероральная регидратационная терапия
One Minute Consult | Кого из взрослых с острой диареей следует обследовать?
Какие взрослые с острой диареей
следует оценивать? Что такое
лучший диагностический подход?
Октябрь 2004 г. | Том 71 | Номер 10 | Страницы 778-785
| THOMAS HELTON, DO Кафедра общей внутренней медицины Отделение медицины Фонд Кливлендской клиники | ДЭВИД Д.К. РОЛСТОН,
MD Клинический директор, A91 Кафедра общей внутренней медицины Фонд Кливлендской клиники |
Вернуться к индексу одноминутной консультации
Доказательств для ответа на этот вопрос немного. По общему мнению, тем не менее, необходимо обследовать пациента с любым из следующего:
- Лихорадка (температура > 38,5 ° C; 101.3 ° F)
- Дизентерия (проезд крови и слизи в стуле)
- Симптомы обезвоживания, особенно постуральное головокружение, снижение диуреза и чрезмерное жажда
- Ухудшение диареи через 48 часов
- Шесть и более табуретов через 24 часа
- Пожилой возраст (> 70 лет)
- Взломанный иммунитет система
- Возраст старше 50 с сильными болями в животе. 1-3
Если ничего из этого не в настоящее время, никакая дальнейшая оценка, кроме краткой истории, обычно не проводится необходимо. 4 Гидратация внутрь и лоперамид, отпускаемый без рецепта обычно хватает.
Остальная часть статьи посвящена экономичному подходу к оценке. острой диареи.
Определение и классификация
Диарея определяется как масса стула более 200 г / день, которая лучше всего определяется по сбору стула за 72 часа. 5
Учитывая сложность и непрактичность получения такой информации,
более полезное определение — увеличение частоты стула с
снижение согласованности по сравнению с исходной картиной пациента.
Другой часто
Используемое и практическое определение — три и более стула за 24 часа.
Диарея, которая длилась менее 14 дней, называется острой, а хроническая диарея длится более 1 месяца.Диарея, которая длится 14 дней и проходит в течение 1 месяца, как правило, считается стойким острая диарея. 1,2
Социально-экономическое воздействие
Диарея является обычным явлением: оценочная частота возникновения острой диареи у взрослых
в США — около 99 миллионов случаев в год. это
также дорого: около 50% пациентов ограничивают свою повседневную деятельность
минимум на 1 полный день, что приведет к потере примерно 20 миллиардов долларов
продуктивность для тех, кто не обращается за помощью к врачу.Примерно
250 000 пациентов госпитализированы, медицинские расходы оцениваются в 560 долларов.
миллион. Объединение госпитализированных пациентов и обращающихся за медицинской помощью
уход, но не госпитализированы, общие затраты для общества больше, чем
23 миллиарда долларов ежегодно. 2,6
Оценка
Заказывая посев кала, сообщите в лабораторию, какой организм вы подозреваете.
Врачи первичного звена
и гастроэнтерологи часто сталкиваются с этой проблемой в офисе и
действительно по телефону и необходимо решить, нужно ли пациенту
дальнейшая оценка.При первой встрече врач
следует спросить о нескольких важных симптомах, чтобы определить, требуется ли дальнейшая оценка
необходимо (РИСУНОК 1).
Если эти симптомы отсутствуют, вероятно, в госпитализации нет необходимости. Пациентов без этих симптомов обычно можно лечить пероральным препаратом . гидратация и лекарства, отпускаемые без рецепта, такие как лоперамид, каолин или висмут субсалицилат для облегчения симптомов.Обычно рекомендуется лоперамид для большинства случаев острой диареи, потому что это безопасно и эффективно. 2,7,8
На данный момент есть мало данных в поддержку отказа от приема антидиарейных препаратов при отсутствии лихорадки выше 101,3 ° F или стул с кровью. 9,10
История и физический экспертиза
После принятия решения о проведении медицинского осмотра врач сталкивается с дилеммой выбора подходящей оценки. история может дать ключ к разгадке конкретного патогена, ответственного за болезнь (ТАБЛИЦА 1) . 3,6
Спросите о:
- Путешествие
- Сексуальные практики
- Использование антибиотиков за 2 месяца
- Прочие лекарства (например, слабительные, антациды, дигоксин, иммунодепрессанты)
- Больные контакты
- Групповые собрания после чего другие участники также заболели аналогичным заболеванием
- Недавние операции или процедуры
- Недавние блюда
- Источник воды
- Домашние животные (особенно черепахи)
- Начало и продолжительность болезни
Медицинское обследование помогает определить степень обезвоживания, но редко помогает определить этиология диареи.Он должен включать:
- Общий вид и психическое состояние
- Знаки жизнедеятельности, в том числе ортостатические изменения артериального давления и частоты пульса, а также температуры
- Абдоминальное обследование
- Табурет для оккультизма кровь
- Тургор кожи и влажность слизистой оболочки (считается ценным для детей, но менее надежен у взрослых, особенно пожилых). 1,3,6
Характеристика кожные поражения в редких случаях могут указывать на конкретную причину диареи из-за основных системных заболеваний, 10,11 например:
- мигрирующий некролитический эритема — глюкагономы
- «Щепотка» пурпура — амилоидоз
- Генерализованная гиперпигментация — Болезнь Аддисона
- Герпетиформный дерматит — литник чревный
- Пигментная крапивница, сохраняющаяся макулярная телеангиэктазия и диффузная кожная мастоцитоз — мастоцитоз
- Карциноидный промывочный и венозная телеангиэктазия — карциноидный синдром
- Розовые пятна —
брюшной тиф.
Диагностические исследования
Посев стула. В обычных посевах кала вырастает патогенный организм в 1,5–5,6% случаев по цене от 950 до 1200 долларов за положительный результат. 2,12
Посев кала, вероятно, следует заказывать только в том случае, если у пациента высокая температура. и кровавый понос, или с ослабленным иммунитетом, или как часть исследования проект при расследовании вспышки диареи.
Подозрение на диарею путешественника также может быть показанием для посева кала.
но многие эксперты считают, что в этой ситуации уместны эмпирические антибиотики,
поскольку эти препараты могут сократить продолжительность болезни на 2–3 дня.Кроме того,
посев кала может иметь мало значения, если пациент отвечает на эмпирические
терапия. 13
У госпитализированных пациентов посев кала падает до нуля на третий день госпитализации. Если заказан посев кала, он важно сообщить лаборатории, какой организм подозревается.
«Обычные культуры» обнаруживают Shigella, Salmonella ,
и видов Campylobacter, .Специальные питательные среды и условия
необходимы для видов Aeromonas, Yersinia и Vibrio и Escherichia coli O157: H7. 4 Предварительная вероятность
почти полностью основан на ключах истории и врачебных
знание эпидемиологии острой диареи.
Исследование стула на яйца и паразиты обычно не показано и это следует делать только в следующих ситуациях:
- Пациенты с история недавних путешествий в Африку, Южную и Юго-Восточную Азию, Россию, Дальний Восток и горные районы Северной Америки, где инфекции Giardia , Cryptosporidium и Cyclospora являются эндемичными
- Гомосексуалисты, которые с ослабленным иммунитетом (подвержены риску заражения Giardia и Entamoeba histolytica инфекций)
- Эпидемиологические исследования для массовых очагов вышеупомянутых паразитов
- Дизентерия с мало лейкоцитов. 11,12
Если у пациента недавно был госпитализирован или получал антибиотики, посев кала анализ стула на яйцеклетки и паразитов не требуется, хотя отправка стул для тестирования на токсин Clostridium difficile оправдан.
В дополнение к вышеупомянутым причинам низкого выхода культур стула, также важно понимать, что вирусы — частая причина диареи. и не обнаруживаются обычными культурами стула.
Анализ фекальных лейкоцитов может помочь в принятии решения о заказе
каловые культуры. Положительный тест на лейкоциты в кале предполагает воспалительный процесс.
причина острой диареи (хотя чувствительность этого теста относительно
низкий) и в
соответствующие клинические условия могут способствовать получению культур кала. 3,14
Эндоскопия обычно не имеет значения при оценке острого понос.Однако это может помочь определить причину диареи. и потенциально может изменить план лечения, если ишемический колит или воспалительный заболевание кишечника находится в дифференциальном диагнозе. Еще одна ситуация, при которой эндоскопия может иметь значение, если у пациента ослаблен иммунитет и, возможно, он цитомегаловирусный колит. 6,10
Прочие испытания
В зависимости от клинической тяжести заболевания, другие тесты, которые следует рассмотреть:
- Рентгенография на пленке брюшной полости — для оценки возможности колита, токсического мегаколон, или кишечная непроходимость
- Основной метаболический панель — для оценки функции почек и электролитного статуса, если у пациента наблюдается умеренное или сильное обезвоживание
- Полная кровь подсчет клеток — хотя редко помогает в определении причины диарея, это может указывать на инвазивный организм, если есть лейкоцитоз с бандемией.Также может быть полезно оценить нейтропению, если: анамнез и физические данные указывают на то, что пациент может подвергаться риску. 15
Список литературы
- Browning S. Офисное ведение общих аноректальных проблем: запор, диарея, и синдром раздраженного кишечника. Первичная помощь 1999; 26: 125-126.
- DuPont HL. Руководство по острой инфекционной диарее у взрослых. Параметры практики Комитет Американского колледжа гастроэнтерологии.Am J Gastroenterol 1997; 92: 1962-1975.
- Park S, Джаннелла Р. Обращение к взрослому пациенту с острой диареей. Гастроэнтерол Clin North Am 1993; 22: 483-497.
- R Olston DDK. Острый диарея у взрослых. В: Эдмундов Э.Д., редактор. Двадцать общих проблем в гастроэнтерологии. Нью-Йорк, Макгроу-Хилл, 2002: 159-176.
- Ачкар Э. Что это практический подход к амбулаторной оценке диареи у ранее здоровый пациент среднего возраста? Cleve Clin J Med 2001; 68: 104.
- Лницкий А. Клиническая оценка и лечение острой инфекционной диареи у взрослых.
Гастроэнтерол Клин Норт Ам
2001; 30: 599-609. - Scheidler MD, Джаннелла РА. Практическое ведение острой диареи. Hosp Pract (Office Ed) 2001; 36 (7): 49-56.
- W входной канал Д., Филлипс С., Льюис Дж. И др. Рекомендации для взрослых по самолечению при лечении острых понос. Aliment Pharmacol Ther 2001; 15: 773-782.
- Cimolai N, Carter Дж., Моррисон Б. и др. Факторы риска прогрессирования кишечной палочки O157: энтерит H7 до гемолитико-уремического синдрома. J Pediatr 1990; 116: 589-592.
- Шиллер Л. Успехи гастроэнтерологии: диарея.Med Clin North Am 2000; 84: 1259-1271.
- Фитцпатрик
ТБ, Джонсон Р.А., Вольф К. и др. . В Cooke D, Englis M, Morriss J,
редакторы. Цветовой атлас и синопсис
г. Клиническая дерматология, 4-е изд. Нью-Йорк, McGraw-Hill, 2001: 334 424 490 514. - Тильман Н, Геррант Р. Острая инфекционная диарея. N Engl J Med 2004; 350: 38-47.
- Геррант Р, Гилдер Т. Практическое руководство по ведению инфекционной диареи. Clin Infect Dis 2001; 32: 331-350.
- Gore J, Суравич C. Тяжелая острая диарея. Gastroenterol Clin North Am 2003; 32: 1249-1267.
- Беннетт Р.Г.,
Greenough WB. Подход к острой диарее у пожилых людей. Гастроэнтерол
Clin North Am 1993; 22: 517-533.
Вернуться к индексу одноминутной консультации
Лямблии (см. Хроническая диарея) — Консультант по инфекционным заболеваниям
ОБЗОР: Что необходимо знать каждому врачу
Название и классификация паразита
Giardia lamblia — жгутиковые кишечные простейшие паразиты (также известные как Giardia duodenalis или Giardia Кишечник)
Какое лечение лучше всего?
Соединения 5-нитроимидазола (например,(например, метронидазол, тинидазол, орнидазол, секнидазол) являются предпочтительными противоинфекционными средствами для лечения лямблий. Из них метронидазол широко используется в клинической практике более 40 лет и до сих пор остается наиболее широко применяемым во всем мире.
В клинических испытаниях метронидазола использовался ряд различных режимов дозирования, включая прием дважды и трижды в день (обычно 250 мг / доза) в течение 5-10 дней; короткими курсами 1-3 дня или ежедневной однократной терапией.
В испытаниях пациентов, получавших лечение в течение 5–10 дней, сообщалось о показателях излечения от 60 до 100% как у взрослых, так и у детей, при средней эффективности примерно 90%.
Побочные эффекты, по-видимому, зависят от дозы и обычно проходят самостоятельно; они включают металлический привкус, тошноту, головную боль, головокружение и лейкопению. Гепатотоксичность — редкий побочный эффект. Следует предупредить пациентов о воздержании от употребления алкоголя при приеме метронидазола.
Тинидазол — альтернатива метронидазолу. В нескольких исследованиях оценивалась эффективность разовой дозы тинидазола, 2 г для взрослых и 50 мг / кг для детей. Эффективность однократной дозы тинидазола колеблется от 72 до 100% со средней эффективностью около 89%.
Агенты первой линии включают:
Прочие 5-нитроимидазолы (например, секнидазол, орнидазол)
Орнидазол является альтернативой метронидазолу или тинидазолу.Несколько исследований продемонстрировали эффективность 90-100% после однократного приема 1 или 2 г у взрослых пациентов.
Секнидазол — еще одна альтернатива. Клинические испытания с применением однократной дозы продемонстрировали эффективность от 80 до 98%.
Оба препарата переносятся достаточно хорошо, с побочными эффектами, в том числе тошнотой, рвотой и болями в животе. Сообщалось о трех случаях гепатита с ассоциированным холангитом при применении орнидазола, все из которых улучшились после прекращения приема препарата.
Доступность этих агентов более ограничена, чем метронидазол или тинидазол.
Бензимидазолы
Два члена класса бензимидазолов, альбендазол и мебендазол, были изучены как in vitro, так и in vivo при лечении Giardia lamblia.
Альбендазол и мебендазол обладают широким спектром эффективности против гельминтов и некоторых простейших. Они минимально всасываются из кишечника и относительно хорошо переносятся.
Тестирование этих соединений in vitro в 1990-х годах показало, что они обладают in vitro активностью против лямблий, равной или большей, чем у нитроимидазолов.
Показатели излечения у детей с лямблиозом 78-86% наблюдаются при 3-5-дневном курсе мебендазола.
Исследование, проведенное в Мексике, продемонстрировало аналогичную эффективность мебендазола (80,4%) по сравнению с нитазоксанидом (78%) при лечении лямблиоза у детей.
Испытание, сравнивающее трехдневный курс мебендазола с однократной дозой секнидазола у детей на Кубе, продемонстрировало эффективность лечения 78,1 и 79,4% соответственно. Разница не была статистически значимой, и обе схемы лечения хорошо переносились.
Исследование детей с лямбдазолом на Кубе продемонстрировало эффективность 64% при однодневном курсе мебендазола по сравнению с 82% эффективностью при однократном приеме тинидазола, что позволяет предположить, что однодневный прием мебендазола уступает однократному применению тинидазола.
Было также показано, что альбендазол является эффективным альтернативным средством лечения лямблиоза и обычно предпочтительнее мебендазола из-за более благоприятной фармакокинетики.
Хотя в исследованиях с использованием чего-либо, от однократной дозы альбендазола до 5-дневного курса с показателями излечения от 35 до 96% были продемонстрированы расходящиеся результаты, клинические испытания с использованием 5-дневного курса альбендазола дали показатели излечения 78-90 %.Одно испытание продемонстрировало аналогичную эффективность 5-дневного курса альбендазола (90,4%) по сравнению с 7-дневным курсом метронидазола (90,4%), что свидетельствует о том, что альбендазол является жизнеспособной альтернативой метронидазолу в лечении лямбдазола у детей. .
Мета-анализ эффективности альбендазола по сравнению с метронидазолом показал, что альбендазол при однократном приеме 400 мг / день в течение 5 дней был столь же эффективен, как и метронидазол, при лечении лямблиоза.
Учитывая безопасность, эффективность и дешевизну альбендазола, а также его широкий спектр действия против гельминтов, этот препарат можно использовать в качестве альтернативы метронидазолу, особенно в регионах, в которых часто встречается коинфекция лямблиозом и гельминтами.
Побочные эффекты бензимидазолов возникают нечасто, но включают тошноту, рвоту, диарею и боль в эпигастрии.
Бензимидазолы могут быть особенно полезны в районах, где часто возникают инфекции, вызванные лямблиями и гельминтами, передаваемыми через почву.
Нитазоксанид
Как in vitro, так и клинические исследования продемонстрировали эффективность нитазоксанида при лечении лямблиоза. В Руководстве по лечению «Лекарства от паразитарных инфекций» 2010 года, опубликованном в Medical Letter, рекомендуется трехдневный курс приема нитазоксанида в качестве одной из альтернатив лечения лямблиоза первой линии.
Нитазоксанид продемонстрировал свою эффективность у детей и взрослых с инфекцией Giardia lamblia с эффективностью 70-90%.
В одном исследовании было показано, что 3-дневный курс нитазоксанида столь же эффективен, как и метронидазол, с показателями излечения 85 и 80% соответственно. Сообщалось также, что нитазоксанид эффективен при лечении лямблий у ВИЧ-инфицированных пациентов с клиническими неудачами при приеме метронидазола и альбендазола.
В исследовании детей на Кубе было показано, что однократная доза тинидазола дает значительно более высокий процент излечения, чем трехдневный курс нитазоксанида (90.5% с тинидазолом против 78,4% с нитазоксанидом).
Нитазоксанид обычно хорошо переносится с небольшими побочными эффектами (зарегистрированные побочные эффекты включают боль в животе, диарею, рвоту и головную боль).
Альтернативные агенты включают
Хинакрин
Хинакрин — препарат, эффективный против лямблий еще в 1937 году. Клиническая эффективность достигала 90% в некоторых исследованиях, в которых использовался 5-10-дневный курс.
Побочные эффекты включают головную боль, тошноту, рвоту и горечь. Сообщается также о других побочных эффектах: гемолиз у пациентов с дефицитом глюкозо-6-фосфатдегидрогеназы (G6PD), токсический психоз и обострение псориаза. Он противопоказан во время беременности из-за его возможной связи со спинальной расщелиной и агенезом почек. Его доступность и клиническое применение при лямблиозе в настоящее время относительно ограничены.
Фуразолидон
Фуразолидон показал свою эффективность in vitro и in vivo и используется с 1960-х годов.
В клинических исследованиях было показано, что фуразолидон менее эффективен, чем метронидазол и хинакрин. При использовании в течение 7-10 дней эффективность до 85%. Курсы продолжительностью менее 5 дней имеют существенно сниженную эффективность.
Общие побочные эффекты включают тошноту, рвоту, диарею и гемолиз у пациентов с дефицитом G6PD.
Рекомендуемая дозировка составляет 100 мг внутрь 4 раза в день в течение 7-10 дней (6 мг / кг / день для детей).
Парамомицин
Парамомицин — аминогликозид относительно широкого спектра действия, действующий против многих простейших, гельминтов и некоторых бактерий.
Парамомицин плохо всасывается и по этой причине достигает высоких концентраций в кишечнике.
Клинически эффективность парамомицина считается ниже, чем у других антигиардиальных соединений; Сообщалось о показателях излечения 55-91%.
Рекомендуемая дозировка составляет 25-35 мг / кг / сут перорально в 3 приема в течение 5-10 дней.
Людям, которые не переносят одно средство или не реагируют на него, следует попробовать другой препарат. При резистентных инфекциях может быть успешной комбинация двух разных классов агентов (например,(например, тинидизазол плюс альбендазол или тинидазол плюс паромомицин или хинакрин плюс метронидазол или нитазоксанид плюс один из этих агентов). Однако надежных данных о сравнительной эффективности различных вариантов комбинации нет, и доказательства их успеха находятся на уровне отчетов / серий случаев.
Каковы клинические проявления заражения этим организмом?
Бессимптомная инфекция
Бессимптомный лямблиоз — хорошо известное явление, и исследования, посвященные вспышкам лямблиоза, показали, что уровень бессимптомной инфекции достигает 76%.Бессимптомное выделение кист может длиться 6 месяцев и более, а бессимптомные прохождения кисты потенциально являются источником инфекции для их семьи, а также для сообщества. Лечение бессимптомных людей — вопрос, который остается спорным. Исследования показали, что в гиперэндемичных регионах частота повторного инфицирования достигает 35% через 3 месяца после лечения. Американская академия педиатрии не рекомендует лечение бессимптомных детей. Однако при определенных обстоятельствах, особенно при подозрении на повторное заражение внутри домохозяйства, это может быть разумным.
Острый лямблиоз
Симптомы обычно развиваются после инкубационного периода продолжительностью 1-2 недели и могут длиться 2-4 недели. Симптомы острого лямблиоза, о которых сообщалось в исследованиях вспышек лямблий, включают:
Диарея (внезапное начало; сначала может быть водянистым; 70-100%)
Недомогание (70-85%)
Тошнота (70-75%)
Жирный стул с неприятным запахом (стеаторея; 55-70%)
Метеоризм (35-75%)
Дискомфорт, спазмы или боль в животе (30-80%)
Похудание (40-65%)
Вздутие живота (40-45%)
Рвота (15-30%)
Лихорадка (10-20%)
Хроническая инфекция
Хроническому лямблиозу может предшествовать или не предшествовать острая фаза заболевания.Хотя большинство хронических инфекций возникает у пациентов с нормальным иммунитетом, определенные группы пациентов, в том числе с общим вариабельным иммунодефицитом (ОВИН) и Х-сцепленной агаммаглобулинемией Брутона (XLA), более склонны к хроническому лямблиозу. Удивительно, но симптомы лямблиоза у ВИЧ-инфицированных похожи на симптомы лямблиоза у ВИЧ-отрицательных лиц и не более серьезны, чем симптомы лямблиоза у ВИЧ-отрицательных лиц, при этом бессимптомная инфекция обычно возникает при наличии ВИЧ.
Симптомы хронического лямблиоза могут включать:
Прерывистые или периодические эпизоды диареи
Стеаторея
Похудание
Мальабсорбция
Недоедание
Неспособность процветать
недомогание
Усталость
Даже когда инфекция протекает бессимптомно, хронический лямблиоз может приводить к нарушению всасывания жиров, сахаров, углеводов и витаминов, что приводит к дефициту лактазы и дефициту витамина A, витамина B12 и фолиевой кислоты.
Приобретенная непереносимость лактозы часто возникает после заражения лямблиями и встречается у 40% пациентов; Клинически это проявляется обострением кишечных симптомов после употребления молочных продуктов.
Было показано, что инфицирование Giardia lamblia в раннем детстве связано с плохой когнитивной функцией, задержкой развития и задержкой роста.
Физические данные неспецифичны, но могут включать:
Похудание
Обезвоживание
Недоедание
Задержка роста (дети)
Отставание (дети)
Болезнь в животе
Имитируют ли другие заболевания его проявления?
Другие болезни, имитирующие лямблии, включают:
Какие лабораторные исследования следует заказать и что вы ожидаете найти?
Результаты, подтверждающие диагноз
Идентификация цист или трофозоитов Giardia lamblia с помощью световой микроскопии на свежих и концентрированных образцах стула является золотым стандартом диагностики для выявления инфекции Giardia.
Однако микроскопия трудоемка, требует много времени и недостаточно чувствительна при исследовании единичных стула. Когда три образца кала исследуются с помощью микроскопии, чувствительность и специфичность очень высоки (99 и 97% соответственно).
- Выявление
лямблий можно значительно улучшить с помощью «тройного теста на фекалии», который сочетает в себе многократный отбор проб (в течение 3 дней подряд), фиксатор, метод концентрации и простой в использовании стойкий краситель.
Микроскопическое исследование биопсии тонкой кишки или аспирата двенадцатиперстной кишки может выявить цисты или трофозоиты Giardia lamblia; однако для этого требуется инвазивный тест (эндоскопия).
За последние 15 лет был достигнут прогресс в разработке и валидации неморфологических диагностических тестов на антигены лямблий и ДНК паразитов. Коммерческие наборы, в которых используются иммуноферментные анализы (ELISA), иммунохроматографические анализы и прямые иммунофлуоресцентные анализы (DFA), обычно используются во многих лабораториях.
DFA (или прямое флуоресцентное антитело) используют меченные флуоресцеином антитела, направленные против антигенов клеточной стенки цист лямблий, и позволяют визуализировать интактных паразитов. Сообщается, что эти тесты имеют чувствительность 96–100% и специфичность 99,8–100%.
- Сообщается, что
ELISA или иммуноферментный анализ (EIA), который обнаруживает антигены Giardia lamblia, имеет чувствительность 88–100% и специфичность 97–100.
Обнаружение антигена с помощью иммунохроматографического анализа образцов стула имеет чувствительность от 58 до 100%, в зависимости от марки используемой тест-полоски, и специфичность 97–100%.
- Методы
на основе ПЦР обладают превосходной специфичностью и чувствительностью по сравнению с обнаружением антигена и повышенной чувствительностью по сравнению с микроскопией. Однако в клинической практике это широко не используется в качестве диагностического инструмента.
Многие коммерчески доступные тесты могут обнаруживать как Giardia, так и Cryptosporidium.
Иммуноанализы часто проводятся для выявления лямблий, но они не должны заменять микроскопию, так как существует множество патогенов, которые могут имитировать лямблии, которые требуют микроскопического исследования
Факторы, которые, возможно, способствуют вариации клинических проявлений, включают вирулентность штамма Giardia, количество проглоченных цист, возраст хозяина и состояние иммунной системы хозяина во время инфекции.
Взаимодействия между хозяином и микробами, которые регулируют патогенез инфекции Giardia, все еще не полностью изучены, и симптомы могут присутствовать при отсутствии каких-либо значительных морфологических повреждений слизистой оболочки кишечника.
Исследования с использованием моделей in vivo и in vitro продемонстрировали, что Giardia lamblia вызывает мальабсорбцию глюкозы, натрия и воды, а также снижает активность дисахаридазы. Нарушение всасывания и нарушение пищеварения возникают из-за диффузного укорочения эпителиальных микроворсинок.Другие изменения слизистой оболочки включают гиперплазию крипт и увеличение количества интраэпителиальных лимфоцитов.
Энтероцитарное повреждение, как было показано на моделях мышей (мыши), опосредовано активированными Т-лимфоцитами хозяина. Потеря площади поверхности щеточной каймы кишечника, снижение активности дисахаридаз и увеличение соотношения крипта / ворсинка, по-видимому, опосредуются CD8 + Т-клетками, тогда как клетки CD4 + и CD8 +, по-видимому, опосредуют приток интраэпителиальных лимфоцитов.
Какие визуализационные исследования будут полезны при постановке или исключении диагноза лямблии?
Визуализация не помогает в диагностике лямблиоза; однако это может помочь исключить другие заболевания, такие как воспалительное заболевание кишечника.
Какие общие осложнения связаны с этой инфекцией, и существуют ли дополнительные методы лечения, которые могут помочь облегчить эти осложнения?
Лямблиоз вызывает целый ряд хронических заболеваний желудочно-кишечного тракта, включая пищевую аллергию, синдром раздраженного кишечника и воспалительные заболевания кишечника. Механизмы, с помощью которых инфекция Giardia может инициировать или обострять эти состояния, не совсем понятны.
Сообщалось о случаях явлений гиперчувствительности, включая макулопапулезную сыпь, зуд, крапивницу, увеит, реактивный артрит и аптозные язвы; однако это редкость.
Хронический лямблиоз может привести к нарушению всасывания жиров, сахаров, углеводов и витаминов, что приводит к дефициту лактазы и дефициту витамина A, витамина B12 и фолиевой кислоты. Временная непереносимость лактозы часто встречается после заражения лямблиями.
Было показано, что инфицирование Giardia lamblia в раннем детстве связано с плохой когнитивной функцией, задержкой развития и задержкой роста.
Каков жизненный цикл паразита и как жизненный цикл объясняет инфицирование человека?
Жизненный цикл паразита (см. Рисунок 1)
Лямблии имеют две морфологические формы: цисты и трофозоиты, обе из которых можно найти в фекалиях инфицированных пациентов
Киста является инфекционной формой и относительно устойчивой к окружающей среде — при благоприятных условиях температуры и влажности, таких как вода при 4-10 ° C, цисты могут оставаться жизнеспособными в течение нескольких месяцев.
Заражение происходит при попадании цист в загрязненную воду, пищу или фекально-оральным путем (через руки или фомиты).
Проглатывание всего 10 кист может привести к лямблиозу.
После проглатывания кисты эксцистанция, продуцирующая по два трофозоита из каждой кисты, происходит в проксимальном отделе тонкой кишки в результате воздействия кислого pH желудочного сока и ферментов поджелудочной железы химотрипсина и трипсина.
Трофозоиты представляют собой грушевидные, двуядерные, многожгутиковые формы паразита, которые размножаются в криптах двенадцатиперстной кишки и верхней части тощей кишки и воспроизводятся бесполым путем путем двойного деления.
Адгезивный диск на вентральной поверхности трофозоита облегчает прикрепление к поверхности слизистой оболочки двенадцатиперстной кишки и тощей кишки.
При благоприятных условиях трофозоиты могут локализоваться в других местах, таких как желчный пузырь, мочевыводящие пути, слизистая оболочка желудка, слизистая оболочка толстой и подвздошной кишки и поджелудочная железа.
Трофозоиты, которые не прикрепляются к тонкой кишке, проходят по направлению к толстой кишке и подвергаются энцистации в подвздошной кишке, возможно, в результате воздействия солей желчных кислот или холестеринового голодания.В конечном итоге они переходят в цисты с фекалиями.
Кисты — самая распространенная форма лямблий, обнаруживаемая в недиарейных фекалиях.
При диарее трофозоиты также могут быть обнаружены в стуле.
Лямблии могут передаваться при приеме внутрь зараженной воды или пищи, фекально-оральным путем (через фомиты или от человека к человеку), через передачу от животного к человеку или через оральный или анальный половой контакт.
Значительные сезонные колебания были показаны в ряде исследований по эпиднадзору в Канаде и США, с пиком случаев заболевания летом и ранней осенью.
Эти сезонные колебания могут быть сбиты с толку тем фактом, что этот период совпадает с увеличением активности на свежем воздухе в этих странах, таких как плавание в бассейнах, аквапарках, озерах и реках.
Условия окружающей среды, которые обеспечивают предрасположенность к лямблии, включают:
Контакт с пресной водой для отдыха
Плохая санитария
Высокая интра- / перидомициллярная концентрация домашних животных
Контакт с животными
Ясли
Распространенность инфекции лямблий
Лямблиоз встречается во всем мире и особенно часто встречается в районах с плохими санитарными условиями и недостаточным количеством водоочистных сооружений.
Сообщается, что распространенность Giardia lamblia у детей в развивающихся странах составляет 3–38%.
В развитых странах Giardia lamblia поражает около 2% взрослых и 6-8% детей и является причиной частых вспышек диареи, передаваемых через воду.
Группы повышенного риска заражения лямблиями включают младенцев и детей младшего возраста, особенно находящихся в детских учреждениях; международные усыновленные; путешественники в эндемичные по болезням районы; находящиеся в тесном контакте с инфицированными; лицам, проглатывающим загрязненную воду для отдыха; туристы; туристы; охотники; лица, контактирующие с инфицированными животными; и мужчины, практикующие секс с мужчинами (МСМ).
Австралийское исследование показало, что вероятность заражения лямблиозом у МСМ в два-три раза выше, чем у населения в целом (1,5%), причем этот показатель выше у ВИЧ-положительных МСМ (4,5%) по сравнению с ВИЧ-отрицательными мужчинами (3%). .
Исследование эквадорских детей показало, что наиболее надежным прогностическим фактором риска лямблий была высокая перидомициллярная концентрация домашних животных; проживание в таком домохозяйстве увеличивало риск заражения лямблиями в два-пять раз.
Данные эпиднадзора в США показывают, что заболеваемость лямблиозом остается относительно стабильной.Ограниченные данные эпиднадзора доступны из развивающихся стран.
Giardia была включена в Инициативу Всемирной организации здравоохранения (ВОЗ) по забытым болезням с 2004 года. Частью этой инициативы было введение новых руководящих принципов по качеству питьевой воды в надежде предотвратить передачу этого и других заболеваний через воду.
Проблемы инфекционного контроля
Противоинфекционная профилактика не рекомендуется.
Вакцины нет
Цисты лямблий относительно устойчивы к хлорированию и дезинфекции ультрафиолетом.
Кипяток очень эффективен для инактивации цист лямблий.
Фильтрация с размером пор меньше или равным 2 мкм очень эффективна.
Кисты могут пережить замораживание даже через несколько дней.
В местах с повышенным риском фекально-оральной передачи, например в детских садах, следует часто мыть руки.
Загрязненные подгузники следует утилизировать надлежащим образом.
Рисунок 1.
Жизненный цикл лямблий (с веб-сайта CDC)
Как этот организм вызывает болезнь?
КАКИЕ ДОКАЗАТЕЛЬСТВА для конкретных рекомендаций по ведению и лечению?
Abboud, P, Lemee, V, Gargala, G.«Успешное лечение метронидазол- и альбендазолрезистентного лямблиоза с помощью нитазоксанида у пациента с синдромом приобретенного иммунодефицита». Clin Infect Dis. т. 32. 2001. pp. 1792-4.
Красная книга 2006: отчет Комитета по инфекционным болезням. 2006.
Андерсон, В., Курран, М. «Нитазоксанид: обзор его использования при лечении желудочно-кишечных инфекций». Наркотики. т. 67. 2007. pp. 1947-67.
Бейли, Дж., Эррамусп, Дж.«Лечение нитазоксанидом лямблиоза и криптоспоридиоза у детей». Annals of Pharmacother. т. 38. 2004. С. 634-640.
Беркман, Д. «Влияние задержки роста, диарейных заболеваний и паразитарных инфекций в младенчестве на познавательные способности в позднем детстве: последующее исследование». Ланцет. т. 359. 2002. С. 564–71.
Buret, AG. «Патофизиология кишечных инфекций, вызываемых Giardia duodenalius». Паразит. т. 15. 2008. С. 261
.Calderaro, A, Gorrini, C, Монтеккини, S.«Оценка анализа полимеразной цепной реакции в реальном времени для лабораторной диагностики лямблиоза». Diag Microbiol Infect Dis. т. 66. 2010. С. 261-7.
Каньете, Р., Эскобедо, А., Гонсалес, М., Альмиралл, П. «Рандомизированное клиническое исследование пятидневной терапии мебендазолом по сравнению с хинакрином при лечении симптоматического лямблиоза у детей». World J Gastroenterol. т. 12. 2006. С. 6366-70.
Cañete, R, Escobedo, A, Gonzalez, M, Almirall, P, Cantelar, N.«Рандомизированное контролируемое открытое исследование одного дня мебендазола в сравнении с однократной дозой тинидазола при лечении лямблиоза у детей». Curr Med Res Op. т. 22. 2006. С. 2131-6.
«Лабораторная идентификация паразитов и проблема общественного здравоохранения». 12 марта 2012г.
Крафт, Дж., Мерфи, Т., Нельсон, Дж. «Фуразолидон и хинакрин: сравнительное исследование терапии лямблиоза у детей». Am J Dis Child. т. 135. 1981. С. 164-6.
de Boer, R, Ott, A, Kesztyu, B, Kooistra-Smid, A. «Улучшенное обнаружение пяти основных желудочно-кишечных патогенов с использованием подхода молекулярного скрининга». J Clin Microbiol. т. 48. 2010. С. 4140-6.
Эдлинд, Т., Ханг, Т., Чакраборти, П. «Активность противоглистных бензимидазолов против Giardia duodenalis in vitro». J Infect Dis. т. 162. 1990. pp. 1408-11.
Эскобедо, А., Альварес, Г., Гонсалес, М. «Лечение лямблиоза у детей: однократная доза тинидазола по сравнению с 3-дневным приемом нитазоксанида». Ann Trop Med Parasitol. т. 102. 2008. С. 199-207.
Эскобедо, А., Канете, Р., Гонсалес, М., Пареха, А., Цимерман, С., Альмиралл, П. «Рандомизированное испытание, сравнивающее мебендазол и секнидазол для лечения лямблиоза». Ann Trop Med Parasitol. т. 97. 2003. С. 499-504.
Эскобедо, А., Цимерман, С. «Лямблиоз: обзор фармакотерапии». Exp Opin Pharmacother. т. 8. 2007. С. 1885–902.
Faubert, G. «Иммунный ответ на Giardia duodenalis». Clin Microbiol Rev. vol. 13. 2000. С. 35-54.
Гарсия, Л., Симидзу, Р. «Оценка девяти наборов иммуноанализа (иммуноферментный анализ и прямая флуоресценция) для обнаружения Giardia lamblia и Cryptosporidium parvum в образцах кала человека». J Clin Microbiol. т. 35. 1997. pp. 1526-9.
Гарсия, Л., Шимицу, Р., Новак, С., Кэрролл, М., Чан, Ф. «Коммерческий анализ для обнаружения антигенов Giardia lamblia и Cryptosporidium parvum в образцах кала человека с помощью быстрой твердофазной качественной иммунохроматографии». J Clin Microbiol. т. 41. 2003. С. 209–12.
Гарднер, Т., Хилл, Д. «Лечение лямблиоза». Обзоры клинической микробиологии. т. 14. 2001. С. 114–28.
Хансен, К., Картрайт, К. «Использование иммуноферментного анализа не устраняет необходимости анализировать несколько образцов стула для чувствительного обнаружения лямблий». J Clin Microbiol. т. 39. 2001. С. 474
.Хлавса, М., Уотсон, Дж., Бич, М. «Эпиднадзор за лямблиозом — США, 1998–2002 годы». Сводки эпиднадзора за MMWR CDC. т. 54. 2005. С. 9-16.
Джонстон, С., Баллард, М., Бич, М., Кузер, Л., Уилкинс, П. «Оценка трех коммерческих тестов для обнаружения лямблий и криптоспоридий в образцах фекалий». J Clin Microbiol. т. 41. 2003. С. 623-6.
Лопес, С., Дайкс, А., Джуранек, Д. «Лямблиоз, передающийся через воду: вспышка болезни в масштабах всего сообщества и высокий уровень бессимптомных инфекций». Am J Epidemiol. т.112. 1980. pp. 4
.Мохамед, З., Хассан, Х., Хассан, С., Рахман, З. «Лямблиоз в Малайзии: обзор клинических проявлений и диагностики». Int Med J. vol. 15. 2008. С. 337–41.
Ортега, Ю., Адам, Р. «Лямблии: обзор и обновление». Clin Infect Dis. т. 25. 1997. С. 545-50.
Ортис, Дж., Аюб, А., Гаргала, Дж., Чегне, Н., Фавеннек, Л. «Рандомизированное клиническое исследование нитазоксанида по сравнению с метронидазолом в лечении симптоматического лямблиоза у детей из Северного Перу». Aliment Pharmacol Ther. т. 15. 2001. С. 1409-15.
Остер, Н., Гериг-Фейстель, Х., Юнг, Х., Каммер, Дж., Маклин, Дж., Ланцер, М. «Оценка иммунохроматографического теста CORIS Giardia-Strip для быстрой диагностики лямблий». Eur J Clin Microbiol Infect Dis. т. 25. 2006. С. 112-5.
Regnath, T, Klemm, T., Ignatius, R. «Быстрое и точное обнаружение Giardia lamblia и Cryptosporidium spp. антигенов в образцах кала человека с помощью новых коммерчески доступных качественных иммунохроматографических анализов ». Eur J Clin Microbiol Infect Dis. т. 25. 2006. С. 807-9.
Rendtorff, RC. «Экспериментальная передача кишечных простейших паразитов человека II. Цисты лямблий в капсулах ». Am J Hygiene. т. 59. 1954. С. 209-20.
Родригес-Гарсиа, Р., Родригес-Гусман, Л., Крус дель Кастильо, А. «Эффективность и безопасность мебендазола по сравнению с нитазоксанидом при лечении лямблии лямблии у детей [Eficacia y seguridad de mebendazole contra nitazoxanide en el tratamiento de en niños] ». Рев Гастроэнтерол Мекс. т. 64. 1999. pp. 122-6.
Саджади, С., Альборзи, А., Мостовфи, Х. «Сравнительное клиническое испытание мебендазола и метронидазола при лямблиозе у детей». J Trop Pediatr. т. 47. 2001. С. 176-8.
Саффар, М., Каффари, Дж., Халилиан, А., Косарян, М. «Быстрое повторное инфицирование Giardia lamblia после лечения в гиперэндемичной зоне: аргументы против лечения». Eastern Mediterranean Health J. vol. 11. 2005. С. 1-2.
Schunk, M, Jelinek, T, Wetzel, K, Nothdurft, HD. «Обнаружение Giardia lamblia и Entamoeba histolytica в образцах стула с помощью двух иммуноферментных анализов». Eur J Clin Microbiol Infect Dis. т. 20. 2001. С. 389–91.
Солаймани-Мохаммади, С., Генкингер, Дж., Лоффредо, К., Сингер, С. «Мета-анализ эффективности альбендазола по сравнению с метронидазолом в качестве лечения инфекций, вызванных Giardia duodenalis». PLoS Negl Trop Dis. т. 4. 2010.стр. e682
Старк, Д., Баррат, Дж., Ван Хал, С., Марриотт, Д., Харкнесс, Дж., Эллис, Дж. «Клиническое значение кишечных простейших в популяции людей с подавленным иммунитетом». Clin Microbiol Rev. vol. 22. 2009. С. 634-50.
Старк, Д., Фотедар, Р., ван Хал, С., Биб, Н., Марриотт, Д., Эллис, Дж., Харкнесс, Дж. «Распространенность кишечных простейших у мужчин, инфицированных вирусом иммунодефицита (ВИЧ), и ВИЧ-отрицательных мужчин, которые заниматься сексом с мужчинами из Сиднея, Австралия ». Am J Trop Med Hyg. т. 76. 2007. С. 549-52.
тен Хоув, Р., ван Эсбрук, М., Вервурт, Т., ван ден Энде, Дж., Ван Лисхаут, Л., Вервей, Дж. «Молекулярная диагностика кишечных паразитов у возвращающихся путешественников». Eur J Clin Microbiol Infect Dis. т. 28. 2009. С. 1045-105. (В этом исследовании были собраны образцы стула у пациентов, посещавших туристическую клинику в Бельгии в течение 13 месяцев. Общее количество случаев Giardia lamblia среди 2591 участника исследования составило 156. Из них 95 случаев имели положительный результат микроскопии, 121 — положительный результат ELISA и 149 положительных результатов ПЦР в реальном времени, что свидетельствует о том, что ПЦР является наиболее чувствительным методом диагностики лямблиоза.)
«Лекарства от паразитарных инфекций: рекомендации по лечению». 2010.
van Gool, T, Weijts, R, Lommerse, E. «Тройной тест фекалий: эффективный инструмент для обнаружения кишечных паразитов в повседневной клинической практике». Eur J Clin. Microbiol Infect Dis. т. 22. 2003. С. 284–90.
Weitzel, T, Dittrich, S, Möhl, I, Adusu, E, Jelinek, T. «Оценка семи коммерческих тестов на определение антигенов лямблии и криптоспоридии в образцах стула». Clin Microbiol Inf. т. 12. 2006. С. 656-9.
Вулф, М. «Лямблиоз». Clin Microbiol Rev. vol. 5. 1992. С. 93–100.
Ерели, К., Балчиоглу, И., Эртан, П., Лимонку, Э, Онаг, А. «Альбендазол как альтернативное терапевтическое средство для лечения лямблиоза у детей в Турции». Clin Microbiol Infect. т. 10. 2004. С. 527–9.
Циммерман, СК, Нидхэм, Калифорния. «Сравнение обычных методов концентрации стула и консервированных мазков с прямым иммунофлуоресцентным анализом Merifluor Cryptosporidium / Giardia и микропланшетным анализом ProSpecT Giardia EZ для выявления Giardia lamblia».
