Гиперплазия эндометрия – симптомы и лечение
Матка женщины состоит из двух слоев: внутренний базальный слой и наружный функциональный. Именно наружный слой реагирует на гормональные изменения цикла и отторгается ежемесячно с менструацией. В случае гормональных нарушений происходит разрастание функционального эндометрия, что является патологией, и при отсутствии лечения существует риск возникновения атипичных клеток, что относится к предраковым заболеваниям.
Основная причина чрезмерного разрастания эндометрия – это повышенная выработка эстрогенов и недостаток прогестерона. Чаще всего, данная патология диагностируется у женщин в предменопаузе и у девочек- подростков. Оба состояния связаны с гормональной перестройкой организма. Для гиперплазии эндометрия характерен ановуляторный цикл – отсутствие овуляции.
Что может спровоцировать гиперплазию эндометрия?
Дефицит прогестерона и излишняя выработка эстрогена происходят вследствие следующих причин:
- синдром поликистозных яичников или дисфункция яичников
- нарушение работы системы гипофиз-гипоталамус
- проблемы с поджелудочной железой, в том числе сахарный диабет
- заболевания коры надпочечников
- гипертония
- ожирение
- заболевания щитовидной железы
- опухоли яичников
- Воспалительные заболевания органов малого таза
- Миома матки
- Аденомиоз
- Аборты и диагностические выскабливания
- Длительный прием гормональных препаратов
- Наследственный фактор
Какие симптомы характерны для гиперплазии эндометрия?
- Задержка менструации и длительные мажущие выделения после нее
- Обильные менструации
- Отсутствие овуляции и как следствие – невозможность забеременеть
Все эти симптомы могут сопровождать миому матки или даже выкидыш на раннем сроке, поэтому необходимо сделать УЗИ малого таза, чтобы определить причину нециклических выделений.
Способы диагностики гиперплазии эндометрия
Узи органов малого таза влагалищным датчиком определяет толщину эндометрия. Толщина эндометрия меняется на протяжении всего цикла, в период перед месячными фиксируется самое высокое значение. Для диагностики следует проводить УЗИ в первой половине цикла, обычно на 7-10 день. Толщина свыше 15 мм дает повод заподозрить патологию и направить пациентку на гистероскопию – внутреннее обследование матки гистероскопом (специальным оптическим прибором), сопровождающееся диагностическим выскабливанием эндометрия и исследование полученного материала для типирования гиперплазии. Так УЗИ дает лишь 68 процентов информативности при гиперплазии, а для гистероскопии это значение достигает 94 процентов.
Аспирационная биопсия – еще один метод диагностики, когда кусочек эндометрия, взятый из полости матки, направляется на гистологическое исследование.
В некоторых случаях гинеколог может направить пациентку на анализ крови на гормоны: эстроген и прогестерон, гормоны щитовидной железы и надпочечников.
Лечение гиперплазии.
Самым эффективным способом лечения гиперплазии эндометрия является раздельное диагностическое выскабливание. Проводится в условиях стационара, обычно под наркозом. Затем полученный эндометрий отправляется на гистологию, и в зависимости от полученного результата исследования назначается гормональное лечение.
Гормонотерапия нужна для подавления разрастания эндометрия и регулирования гормонального фона. Гормональное лечение зависит от возраста пациентки. Так женщинам до 35 лет назначают комбинированные оральные контрацептивы.
Лечение гестагенами – еще один способ гормонотерапии, подходит для лечения гиперплазии эндометрия любого типа. Спираль Мирена – это один из таких вариантов. Но существует и таблетированная форма – это назначение препаратов Утрожестан или Дюфастон.
Не следует пренебрегать гормональной терапией, так как процент рецидивов высок (полипы могут возникнуть вновь после их удаления и не один раз), а обильные кровотечения осложняются анемией.
Чернышева Наталья Александровна
Новая технология противорецидивной гормональной терапии гиперпластических процессов эндометрия у женщин позднего репродуктивного возраста | #11/12
Проблема лечения женщин с гиперпластическими процессами в эндометрии (ГПЭ) в течение многих десятилетий остается актуальной, так как они имеют важное медико-биологическое и социально-экономическое значение, являясь наиболее частой причиной маточных кровотечений в позднем репродуктивном и перименопаузальном периодах. Несмотря на широкое распространение данной патологии, существующие методы консервативной терапии недостаточно эффективны [1]. Неослабевающий интерес к данной проблеме определяется наклонностью гиперплазии эндометрия к длительному, рецидивирующему течению, отсутствием специфических, патогномоничных симптомов, сложностью дифференциальной диагностики. Гиперплазия эндометрия относится к числу пролиферативных процессов, которые при длительном течении без лечения могут служить фоном для развития злокачественных поражений слизистой оболочки матки.
Патогенез ГПЭ характеризуется сложным взаимодействием общих системных процессов и локальных изменений в эндометрии. В свете современных концепций в основе развития ГПЭ лежит гормональный дисбаланс, который выражается абсолютной или относительной гиперэстрогенемией [4–6]. Эндометрий является самой чувствительной тканью-мишенью половых гормонов. Исследования последних лет показали, что ведущую роль в развитии ГПЭ играет чувствительность слизистой оболочки матки к стероидным гормонам [2, 7–9].
Резервом повышения эффективности терапии ГПЭ является индивидуальный выбор препаратов. Для осуществления персонализованного подбора гормональной терапии мы предложили использовать силу связывания препарата с рецепторами прогестерона из ткани эндометрия конкретной пациентки. Данное предположение основано на тезисе, что сила связывания лиганда с рецептором определяет эффект от лечения, то есть чем выше связывание гестагенов с прогестерон-связывающими участками, тем лучший эффект ожидается от лечения.
С целью проверки данной гипотезы на кафедре молекулярной фармакологии и радиобиологии им. академика П. В. Сергеева ГБОУ ВПО РНИМУ им. Н. И. Пирогова совместно с МОНИИАГ было проведено исследование специфического связывания рецепторов прогестерона с синтетическими гестагенами у женщин позднего репродуктивного возраста с гиперпластическими процессами эндометрия. Проведенные в отделении гинекологической эндокринологии исследования показали, что выбор гестагена с учетом индивидуальной чувствительности эндометрия к препарату позволил значительно снизить частоту рецидивов железистой гиперплазии эндометрия [4, 5, 7]. По результатам исследования была разработана новая медицинская технология и получен патент на изобретение «Способ гестагенотерапии гиперпластических процессов эндометрия» [11].
Материал и методы исследования
В исследование вошли 164 женщины позднего репродуктивного возраста. Критериями включения в исследование явились: наличие ГПЭ (простой железистой гиперплазии и/или железистых полипов эндометрия), отсутствие тяжелой соматической патологии и выраженных метаболических нарушений, препятствующих проведению противорецидивной гормональной терапии.
Клинические методы исследования включали общее стандартное гинекологическое обследование женщин: осмотр шейки матки в зеркалах, влагалищное бимануальное исследование, трансвагинальное ультразвуковое сканирование органов малого таза (на 5–8 день менструального цикла), мазок на флору и ЗППП. Ультразвуковое сканирование органов малого таза у пациенток позднего репродуктивного возраста проводилось на базе НКО МОНИИАГ, аппаратом Siemens Sequoia 512 с использованием вагинального датчика от 6 до 8 мГц, в режиме двухмерной визуализации.
Ткань эндометрия для определения цитозольных рецепторов половых стероидов получали во время выскабливания стенок полости матки при использовании серийного аппарата Circon Acmi на базе эндоскопического отделения МОНИИАГ или путем эндорам-биопсии.
Уровень рецепторов прогестерона и специфическое связывание стандартных гестагенов с прогестерон-связывающими участками определяли в цитозоле биоптатов эндометрия по методу [12].
Цитозольную фракцию получали стандартным методом с помощью ультрацентрифугирования (105 000 g, ультрацентрифуга UP-65 M, 60’). Уровень рецепторов прогестерона (РП) и специфическое связывание гестагенов с прогестерон-связывающими участками определяли в цитозоле биоптатов эндометрия радиолигандным методом [13].
Уровень рецепторов прогестерона (РП) и специфическое связывание гестагенов с прогестерон-связывающими участками определяли в цитозоле биоптатов эндометрия радиолигандным методом [13].
Белок определяли методом Лоури.
Статистическую обработку материала проводили на персональном компьютере, в работе использовалась программа GraphPad Prism 5.0 и стандартные методы статистического анализа.
Результаты и обсуждение
Из 136 обследованных пациенток с ГПЭ 73 (54%) были с рецидивирующим течением (в анамнезе от 1 до 6 раздельных диагностических выскабливаний (РДВ) слизистой стенок матки и цервикального канала), у остальных 63 женщин (46%) гиперплазия эндометрия была выявлена впервые.
В контрольную группу вошли 28 женщин (без измененного эндометрия), в группу с ГПЭ вошли 73 пациентки, при гистологическом исследовании у 51 (37,5%) пациентки были диагностированы железистые полипы эндометрия, а у 85 — простая железистая гиперплазия эндометрия.
У пациенток с ГПЭ в 112 случаях (82%) были гормонзависимые заболевания гениталий (миома матки и/или эндометриоз различной локализации), 58% обследуемых женщин имели избыточную массу тела (ИМТ ≥ 25).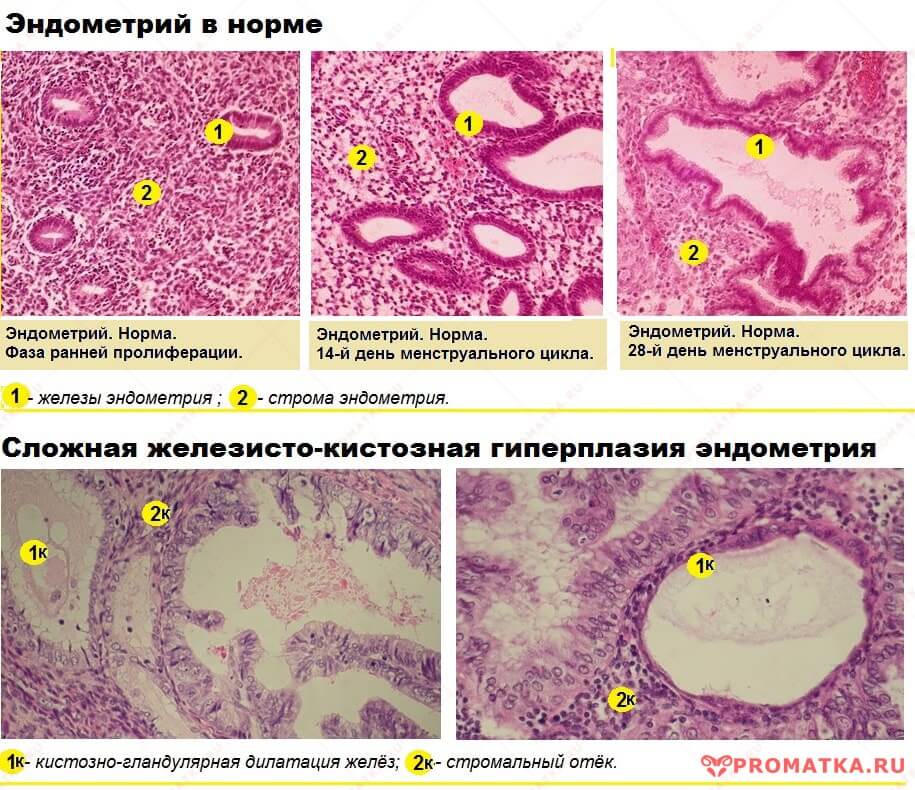
37 (27,2%) пациенткам с ГЭ проводили гистероскопию с РДВ во II фазу менструального цикла в условиях МОНИИАГ. 99 (73%) женщинам РДВ с или без гистероскопии было проведено по месту жительства.
Уровень РП в эндометрии изменялся в зависимости от нозологической формы гиперплазии. Так, при полипах эндометрия средняя величина этого параметра снизилась в 1,4 раза по сравнению с нормой и составила в среднем 16,9 ± 3,7 фмоль/мг белка, а при железистой гиперплазии эндометрия — в 1,2 раза и равнялась 19,2 ± 5,6 фмоль/мг белка (р ≤ 0,05).
В качестве тестируемых гестагенов использовались: медроксипрогестерона ацетат, норэтистерон, дидрогестерон. Приведенные гестагены выбраны по принципу различий структуры и наличия доступных лекарственных форм. Уровень рецепторов прогестерона в цитозоле эндометрия, как и сила специфического связывания с гестагенами, варьировали в широких пределах. При этом усредненные данные показали, что наибольшую силу связывания продемонстрировал медроксипрогестерона ацетат (64,6 ± 7,2 при полипах эндометрия и 73,8 ± 5,2 при гиперплазии (р ≤ 0,001)), наименьшую — норэтистерон (52,7 ± 4,1 при полипах эндометрия и 60,3 ± 2,6 при гиперплазии (р ≤ 0,001)).
При исследовании были выделены следующие группы: контрольная группа (I группа) — 28 пациенток; женщины с рецидивирующим течением ГПЭ, которым была назначена гормональная противорецидивная терапия по методу слепой выборки (II группа) — 41 пациентка; женщины с рецидивирующим течением ГПЭ, которым назначалась гормональная противорецидивная терапия с учетом результатов связывающей активности гестагенов с прогестерон-связывающими участками (III группа) — 32 пациентки.
II группе была назначена гормональная противорецидивная терапия с использованием препаратов, в состав которых входят тестируемые гестагены. Эффективность терапии пациенток данной группы (отсутствие рецидивов в течение 6 месяцев по окончании лечения) сравнивали с результатами индивидуального тестирования аффинитета рецепторов прогестерона, полученных из эндометрия пациенток до начала лечения.
III группе была назначена гормональная терапия с учетом результатов связывающей активности гестагенов с прогестерон-связывающими участками цитозоля эндометрия конкретной пациентки.
Все пациентки, имеющие рецидивирующее течение заболевания, получали:
- дигидрогестерон по 10 мг 2 раза в сутки, с 5 по 25 день цикла в течение 6 месяцев;
- норэтистерон — по 1 таблетке 2 раза в сутки, с 5 по 25 день цикла в течение 6 месяцев;
- медроксипрогестерона ацетат — 1 инъекция в/м через 28 дней в течение 3 месяцев.
Оценка эффективности гормональной терапии проводилась по клиническим симптомам, а также по результатам трансвагинального ультразвукового сканирования органов малого таза на 3-м и 6-м месяцах гормональной терапии. Ультразвуковое исследование проводили на 4–8 день менструального цикла, толщина эндометрия считалась нормальной при значениях 0,3–0,6 см, если же она превышала данные значения, то проводилась гистероскопия для уточнения диагноза.
В результате клинико-лабораторного исследования показано, что во II группе частота рецидивов составила 17,1%, в то время как в III группе частота рецидивов составила 6,3%.
Сравнительный анализ противорецидивной эффективности синтетических гестагенов в проведенном исследовании показал, что количество рецидивов при использовании норэтистерона было максимально и составило 18 через 3 месяца во II группе, тогда как при терапии медроксипрогестерона ацетатом рецидивов обнаружено не было через 3 и 6 месяцев.
Выводы
Таким образом, нами рекомендуется алгоритм проведения персонализированной противорецидивной гормональной терапии по схеме, представленной на рис. 2.
Медико-социальная эффективность
Снижение частоты рецидивов гиперпластических процессов эндометрия у женщин позднего репродуктивного возраста ведет к:
- улучшению качества жизни женщин;
- возможности реализации репродуктивной функции;
- снижению загруженности хирургических коек в стационаре;
- снижению материальных затрат на лечение больных в стационаре;
- уменьшению количества дней нетрудоспособности в году.

Таким образом, предложенная медицинская технология представляет собой подбор индивидуальной гормональной терапии гиперпластических процессов эндометрия на основании индивидуальной оценки связывающих свойств рецепторов прогестерона эндометрия.
Работа выполнена в рамках программы развития НИУ ГБОУ ВПО РНИМУ им Н. И. Пирогова, 2010–2019, приоритетное направление развития ПНР-2, персонализированная медицина.
Литература
- Вихляева Е. М. Руководство по эндокринной гинекологии. М., 2006, с. 424–487.
- Мгдесян К. К. Клиническое значение определения рецепторов стероидных гормонов в прогнозировании эффективности гормонотерапии гиперпластических процессов эндометрия. Автореферат дис. … канд. мед. наук. М., 2002; 24.
- Commeely O. M., Lydon J. P., De Mayo F., O’Malley B. W. Reproductive functions of the progesterone receptor // J. Sooc. Gynec. Invest. 2000; 7 (1): 25–32.
- Гаспарян Н.
 Д., Карева Е. Н., Горенкова О. С. и др. Оптимизация гормональной противорецидивной терапии гиперпластических процессов в эндометрии у женщин позднего репродуктивного возраста // Рос. вестн. акуш.-гин. 2007; № 5: 31–35.
Д., Карева Е. Н., Горенкова О. С. и др. Оптимизация гормональной противорецидивной терапии гиперпластических процессов в эндометрии у женщин позднего репродуктивного возраста // Рос. вестн. акуш.-гин. 2007; № 5: 31–35. - Горенкова О. С. Дифференцированный подход к гестагенотерапии гиперпластических процессов эндометрия у женщин позднего репродуктивного возраста. Автореферат дис. … канд. мед. наук. М., 2005; 24.
- Сметник В. П., Тумилович Л. Г. Неоперативная гинекология. М.: Медицинское информационное агентство, 2000; 592.
- Краснопольский В. И., Гаспарян Н. Д., Карева Е. Н. и др. Рецепция половых стероидов при гиперпластических процессах в эндометрии у женщин позднего репродуктивного возраста // Рос. вестн. акуш.-гин. 2005; № 2: 7–9.
- Сергеев П. В., Шимановский Н. Л., Петров В. И. Рецепторы физиологически активных веществ. Москва–Волгоград, 1999; 400.
- Стрижова Н. В., Сергеев П.
 В., Лысенко О. Н. и др. Роль половых гормонов и их рецепторного аппарата при выборе методов лечения у пациенток с гиперпластическими процессами эндометрия в сочетании с миомой матки // Акуш. и гин. 1998; № 3: 30–33.
В., Лысенко О. Н. и др. Роль половых гормонов и их рецепторного аппарата при выборе методов лечения у пациенток с гиперпластическими процессами эндометрия в сочетании с миомой матки // Акуш. и гин. 1998; № 3: 30–33. - Perez-Medina T., Bajo J., Folgueira G. et al. Atypical endometrial hyperplasia treatment with progestagens and gonadotropin-releasing hormone analogues: long-term follow-up. Madrid, spain. Gynec. Oncol. 1999; 73 (2): 299-23-04.
- Сергеев П. В., Краснопольский В. И., Гаспарян Н. Д. и др. Способ гестагенотерапии гиперпластических процессов эндометрия. Патент на изобретение № 2312354 от 10 декабря 2007.
- Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. Под ред. В. П. Фисенко. М.: ИИА Ремедиум, 2000; 327.
- Бассалык Л. С. Рецепторы стероидных гормонов. М., 1987.
В. И. Краснопольский*, доктор медицинских наук, профессор, член-корреспондент РАМН
Н. Д. Гаспарян*, доктор медицинских наук, профессор
Д. Гаспарян*, доктор медицинских наук, профессор
Л. С. Логутова*, доктор медициинских наук, профессор
Е. Н. Карева**, доктор медицинских наук, профессор
О. С. Горенкова*, кандидат медицинских наук
Д. А. Тихонов**
*ГБУЗ Московской области МОНИИАГ,
**ГБОУ ВПО РНИМУ им. Н. И. Пирогова, Москва
Контактная информация об авторах для переписки: [email protected]
Современные аспекты профилактики и лечения гиперпластических процессов эндометрия в перименопаузе
Современные аспекты профилактики и лечения гиперпластических процессов эндометрия в перименопаузе
Профессор, д.м.н. И.Б. Манухин, профессор, д.м.н. А.Л. Тихомиров,
С.М. Шаркова, А.А. Кочарян
Гиперпластические процессы эндометрия являются распространённой гинекологической патологией, частота которой существенно увеличивается к периоду возрастных гормональных перестроек в перименопаузальном возрасте. Имея неодинаковую степень развития, гиперпластические процессы нередко становятся благоприятным фоном для возникновения предрака, а затем и рака эндометрия, что в течении многих десятилетий представляет важную медико — социальную проблему.
Имея неодинаковую степень развития, гиперпластические процессы нередко становятся благоприятным фоном для возникновения предрака, а затем и рака эндометрия, что в течении многих десятилетий представляет важную медико — социальную проблему.
В настоящее время всё более актуальной становится проблема сохранения здоровья женщины перименопаузального возраста, что связано с увеличением средней продолжительности жизни, возрастающей доли женщин старшей возрастной группы среди населения.
Ещё 50 — 60 лет назад только 28% женщин доживали до возраста менопаузы и лишь 5% из них достигали возраста 75 лет. В настоящее время 95% женщин достигает периода перименопаузы, а 55% из них достигает 75 летнего возраста [3 7 12].
Современная демографическая ситуация в стране и мире такова, что 90% женщин проводят в постменопаузальном периоде треть своей жизни. К 2007 году 12% населения мира составляют лица старше 65 лет [3 7 12].
Термин перименопауза — означает период жизни женщины от первого нарушения регулярности менструального цикла до наступления аменореи.
Этот период характеризуется появлением биологических, клинических и эндокринных признаков прекращения менструаций. Паталогические маточные кровотечения среди женщин перименопаузального возраста составляют от 2 до 5% от всех гинекологических больных и являются достаточно распространенным симптомом, который наблюдается при различных патологических процессах эндометрия:
— гиперпластические процессы эндометрия,
— миома матки, аденомиоз,
— гормонально-активные опухоли яичников и их различное сочетание [4 9,10,].
У большинства женщин период перименопаузы (климактерический период) приходится на возраст 45 -50 лет. Кровотечения в этом возрасте именуются климактерическими, что подчеркивает их связь с возрастными изменениями в репродуктивной системе.
Особая роль в гормональной перестройке отведена гипоталямусу, с началом перименопаузы появляется лабильность менструального цикла, нарушение фазности менструаций, что обусловливает нарушение длинной обратной связи как на уровне гипофиза, так и гипоталямуса. Наиболее стабильная корреляция между ФСГ и ЛГ установленная в репродуктивном периоде, в перименопаузе отсутствует.
Наиболее стабильная корреляция между ФСГ и ЛГ установленная в репродуктивном периоде, в перименопаузе отсутствует.
Со стороны функции яичников в период перименопаузы происходит снижение эстрогенов и прогестерона [4 .9, 10, 11, 13, 14].
Ряд авторов сообщает об отсутствии достоверных статистических различий содержания в крови пролактина, тестостерона и эстрадиола у здоровых женщин, как в репродуктивном периоде, так и в период перименопаузы [7 .12].
Продукция половых стероидных гормонов у женщин тесно связана с ростом фолликулов и гаметогенезом.
Гонадотропная функция гипофиза при физиологическом течении периода перименопаузы является разнонаправленной: уровень ФСГ и ЛГ повышается, а уровень пролактина снижается, что можно рассматривать как универсальную реакцию на резкое снижение функции яичников. При сравнении уровня содержания в крови гормонов: на 7 — 9 день цикла у женщин в перименопаузе ЛГ в три раза, а ФСГ в девять раз выше уровня содержания в крови здоровых женщин репродуктивного возраста, в соответствующие дни менструального цикла [13,14, 15].
Эстрадиол, обнаруживаемый в крови у женщин в перименопаузе, является в основном продуктом экстрагландулярного превращения андрогенов в эстрогены, что имеет важное значение для поддержания нормального гомеостаза.
Ароматизирующие фементные системы, способные превращать андростендион и тестостерон в эстрадиол, обнаруживаются главным образом в жировой ткани.
Ароматизация андростендиона происходит в стромальных и сосудистых клетках жировой клетчатки, а сами жировые клетки (адипоциты) активно захватывают его из плазмы и являются депо половых гормонов [4. 9,10].
Гиперпластические процессы, развивающиеся у женщин в период перименопаузы, имеют неодинаковую степень развития, иногда приобретают характер предракового заболевания.
Согласно классификации ВОЗ (Женева 1984 г .), выделяют три основных вида гиперпластических процессов в эндометрии:
— эндометриальные полипы;
— эндометриальная гиперплазия;
— атиптческая гиперплазия эндометрия.
В отечественных материалах обычно используется морфологическая классификация Б. И.Железнова ( 1973 г .), которая выделяет:
И.Железнова ( 1973 г .), которая выделяет:
— железистую гиперплазию эндометрия;
— железисто — кистозную гиперплазию эндометрия;
— атиптческую гиперплазию эндометрия (диффузные аденоматозные изменения, очаговый аденоматоз и аденоматозные полипы).
Каждое из этих заболеваний может стать причиной кровянистых выделений у женщин в период перименопаузы.
Частота озлокачествления гиперпластических процессов эндометрия колеблется в достаточно широких пределах (0,25 — 50%) и определяется морфологическими особенностями заболевания, длительностью его рецидивирования, а также возрастом пациентки [1. 4,8].
В литературе данная проблема широко обсуждалась, детально освещены вопросы этиологии и патогенеза, диагностики и лечения гиперпластических процессов Несмотря на появление новых направлений в ведении больных с гиперпластическими процессами эндометрия в различных современных периодах , вопросы лечения данной патологии остаются одними из наиболее актуальных вопросов гинекологии, и ещё далеки от окончательного решения. Это обусловлено прежде всего сложным и неоднородным пато- и морфогенезом заболевания и индивидуальной чувствительностью организма к различным лечебным воздействиям [1. 4,].
Это обусловлено прежде всего сложным и неоднородным пато- и морфогенезом заболевания и индивидуальной чувствительностью организма к различным лечебным воздействиям [1. 4,].
Остается недостаточно изученной зависимость различных морфологических форм гиперпластических процессов эндометрия от нейро — эндокринных нарушений организма, таких, как позднее наступление менопаузы, клинический и субклинический сахарный диабет, ожирение, бесплодие, гипертоническая болезнь [8].
Разработка морфологических критериев индивидуальной чувствительности доброкачественных гиперпластических процессов и предрака эндометрия имеет важное практическое значение для оптимизации способа лечения, определения показаний к гормонотерапии, а следовательно и повышения эффективности профилактики развития и лечения предрака, рака эндометрия [1. 4,].
Практически все авторы едины в мнении, что изменение гормональных взаимоотношений играет роль в развитии пролиферативных процессов в эндометрии. Эндометрий, как «ткань мишень», испытывающий на себе влияние половых гормонов, чрезвычайно чувствителен к действию эстрогенов, оказывающих эффект на его структуру и функцию.
Эстрогены — основной фактор, вызывающий пролиферацию эндометрия, которая при отсутствии достаточного влияния прогестерона, прогрессирует в железистую и атиптческую гиперплазию.
К нарушению взаимоотношений между прогестероном и эстрогенами и к возникновению относительной гиперэстрогенемии приводит – ановуляция.
В перименопаузе в крови повышается уровень ФСГ и ЛГ, что оказывает стимулирующее действие на функцию яичников, которые отвечают повышенной продукцией эстрогенов, не компенсированных действием прогестерона. Следствием этого является нередкое сочетание гиперпластических процессов эндометрия с миомой матки и эндометриозом у женщин указанной возрастной группы [4. 7. 8. 13].
Доказано, что характер пролиферации эндометрия, обусловлен не только уровнем содержания в крови и соотношением гормонов, но и способностью эндометрия к их связыванию, — то есть количеством и качеством специфических рецепторов.
Можно полагать, что генетически обусловленный дефицит рецепторов прогестерона и рецепторов эстрадиола, либо нарушение этой рецепторной системы под влиянием различных патогенетических факторов являются одной из причин неэффективности гормонального лечения.
Между тем, в настоящее время не существует методик, позволяющих в клинических условиях осуществлять полноценную коррекцию нарушений рецепторного аппарата эндометрия. В клинической практике широко исследуется изучение фоновых и предраковых состояний эндометрия [3.7.12.].
Известно, что длительная пролиферация клеток эндометрия независимо от причины вызвавшую пролиферацию, облегчает реализацию онкогенного фактора [1.].
За последние 20 лет в России заболеваемость раком эндометрия (тела матки) выросла в два раза [7].
Это связано не только с увеличением средней продолжительности жизни, но и с нарастанием в популяции обменно — эндокринных заболеваний, таких как ановуляция, бесплодие, ожирение, гипертоническая болезнь, сахарный диабет [4].
Рост заболеваний раком тела матки требует не только усовершенствования методов лечения больных, но и в первую очередь усовершенствование возможной профилактики и лечения патологических заболеваний эндометрия на этапе его доброкачественных изменений.
Риск малигнизации в случае железисто — кистозной гиперплазии эндометрия (ЖГЭ) и полипов эндометрия составляет 1 — 2%, что позволяет отнести их скорее к фоновым заболеваниям нежеле к предраковым. В то же время у 55,9% больных раком эндометрия в перименопаузе обнаруживались полипы и железистая гиперплазия эндометрия [1.].
На основании только морфологических исследований невозможно составить прогноз риска развития ракового процесса, должен быть оценен фон, на котором возник пролиферативный процесс в эндометрии, то есть нейро — эндокринно — обменные нарушения в организме женщин, их возраст, гинекологический анамнез, клиническое течение, рецидивирование гиперплазии [1.].
Рецидивирующая гиперплазия эндометрия у женщин перименопаузального возраста, развивающаяся часто на фоне ожирения и гипертонической болезни, может быть отнесена к предраку.
В связи с известной зависимостью физиологической трансформации эндометрия от состояния гормональной регуляции, назначение гормональных препаратов для профилактики и лечения гиперпластических процессов эндометрия (ГПЭ) в перименопаузальном периоде считается патогенетически обоснованным.
В настоящее время здоровье, качество жизни и общий жизненный прогноз у женщин в период климактерия определяется прежде всего адекватностью и современностью лечебно — профилактических мероприятий, среди которых гормональная терапия играет большую роль [7].
Однако при отрицательном отношении пациенток к приёму гормональных препаратов в период климактерия, не стоит забывать и о возможности применении препаратов содержащих в своем составе фитогормоны и фитоэстрогены с целью возможной профилактики развития многих заболеваний развивающихся в этом возрастном периоде. «Данные препараты устраняют также раннюю вазомоторную и психоэмоциональную симптоматику, метаболические нарушения, явления остеопороза, сердечно — сосудистых заболеваний и других заболеваний, развивающихся в климактерии.» [7]
Лечебная тактика при гиперпластических процессах зависит от патоморфологической характеристики эндометрия, возраста, этиологии и патогенеза заболевания, сопутствующей генитальной и экстрагенитальной патологии.
Основным методом лечения гиперпластических процессов эндометрия в период перименопаузы, после оценки патоморфологического исследования, сопутствующей гинекологической и соматической патологии, является гормонотерапия с оказанием антиэстрогенного влияния на слизистую оболочку полости матки, с использованием препаратов, обладающих прогестероновой активностью — синтетические прогестины, «чистые» гестагены. Применяют их укороченными курсами, общей продолжительностью лечения 6 месяцев .
Назначению гормональных препаратов предшествует гистологическое исследование эндометрия, полученного в результате РДВ.
Использование в терапии препаратов прогестероноподобного действия (дюфастон, ЛРС «Мирена», норколут, прогестерон 1% и др.) обосновывается биологическими эффектами прогестерона.
Прогестерон предотвращает эстрогениндуцированное клеточное деление, и тем самым создает условия, при которых пролифирирующий эндометрий превращается в секреторный. Сущность биологического действия прогестерона проявляется в антиэстрогенном эффекте, который осуществляется двумя механизмами:
1 — уменьшение количества цитозольных рецепторов эстрадиола путем ингибирования их синтеза;
2 — прогестерон индуцирует 17в — гидроксистероиддегидрогеназу, которая превращает эстрадиол в менее активный эстрон.
Следует заметить, что реализация действия прогестерона и прогестероноподобных веществ на местном уровне возможна лишь при наличии достаточного количества рецепторов прогестерона. Гормональное лечение гиперпластических процессов эндометрия, проявляющихся маточными кровотечениями, проводится с целью достижения нескольких эффектов, которые связаны между собой:
1) остановка кровотечения;
2) прекращение патологической пролиферации эндометрия;
3) нормализация взаимоотношений в гипоталямо — гипофизарно — яичниковой системе.
Для достижения стойкого клинического эффекта лечение синтетическими прогестинами рекомендуется продолжать 6 — 12 месяцев [11.12].
Влияние гормонов на клетки реализуется посредством взаимодействия со специфическими рецепторами. Количество рецепторов зависит от концентрации соответствующего гормона и от количества стероидов других классов [9.10.].
Эстрогены стимулируют пролиферацию клеток эндометрия, развитие секреторного аппарата клеток и синтез рецепторов к эстрогенам и прогестерону [15].
В тканях мишенях эстрогены увеличивают концентрацию собственных рецепторов и цитоплазматических рецепторов к прогестерону и андрогенам. Прогестерон блокирует этот механизм, снижая, таким образом, количество рецепторов к эстрогенам.
Кроме этого, прогестерон ускоряет оборот ранее синтезированных рецепторов.
Рецептор прогестерона состоит из А и В субъединиц, в соотношении 1:1. Прогестерон обладает высоким сродством к своему рецептору. Эстрадиол, кортизол и тестостерон имеют незначительное сродство к прогестероновым рецепторам. Прогестерон не имеет сродства к рецепторам эстрогенов, но некоторые прогестины и их метаболиты взаимодействуют с эстрагеновыми рецепторами [15].
Эдометрий способен к стероидогенезу, вырабатывая на местном уровне эстрадиол и сульфат эстрона, пролактин, простагландины, андрогены, маркерные протеины. Кроме того он вырабатывает факторы роста — эпидермальный фактор роста, инсулиноподобный фактор роста (ИПФР) — 1 и 2, трансформирующие факторы роста 1-а и 1-в и их рецепторы [13, 16].
ИПФР — 1 и ИПФР — 2 структурно относятся к инсулину. Считается, что ИПФР, действуя через аутокринные и паракринные механизмы вызывает пролиферацию и дифференцировку клеток. В крови ИПФР находится в связи с белком — переносчиком, известно 6 белковых переносчиков (ИПФРСП). Наибольший интерес представляет ИПФРСП — 1, который синтезируется и секретируется в эндометрии во вторую фазу менструального цикла и прогестерон индуцирует его синтез.
Морфологические изменения эндометрия в секреторной фазе характеризуются отёком стромы, атрофией желез, децидуализацией стромы вплоть до полной атрофии функционального слоя и отсутствие митозов [16]. Наблюдается инфильтрация тканей лимфоцитами, плазматическими клетками и макрофагами, иногда возникает некроз стромы. Выявлены выраженные изменения со стороны сосудов эндометрия, заключающиеся в утолщении стенок артериол, тромбозе капилляров и уменьшении количества спиралевидных артерий.
Так, например, в результате проведенных исследований, посвященных влиянию левоноргестрела (производного 19 — нортестостерона), входящего в ЛРС, было выявлено значительное снижение эстрогеновых и прогестероновых рецепторов эндометрия [13, 14, 15].
Кроме того, в 1998г. Н.О.С ritchley и соавт. опубликовали исследования по изучению содержания прогестероновых и эстрогеновых рецепторов, А и В субъединиц и простагландин — дегидрогеназы в эндометрии на фоне применения ЛРС.
Полученные данные свидетельствуют о значительном снижении количества эстрогеновых, а также А и В субъединиц прогестероновых рецепторов.
При этом наблюдается более выраженная супрессия В субъединицы рецепторов к прогестерону. Кроме того, совместно с ингибированием прогестероновых рецепторов было выявлено значительное снижение уровня простагландин — дегидрогеназы. А также выявлено подавление синтеза, индуцированных эстрогенами и прогестероном ростовых факторов [15].
В противоположность этому зарегистрировано стимулирующее действие левоноргестрела, входящего в ЛРС на образование циклооксигеназы — 2, рецепторов к пролактину и белка, связывающего ИПФР — 1 и ИПФРСП – 1 [15].
Гестагеновому влиянию на ИПФР(1,2) и ИПФРСП — 1 посвящены многочислен-ные исследования, наибольший интерес из которых представляет работа Rutanen .
В ряде исследований были получены результаты, свидетельствующие о супресорном действии левоноргестрела на ИПФР- 1, одновременно с ингибирующим действием на ИПФРСП — 1 и ИПФР — 2.
Значимость данных исследований была обусловлена определяющей ролью ИПФР — как медиатора эстрогенового влияния на эндометрий. Кроме того, ИПФРСП — 1 является маркером прогестинового влияния на эндометрий, которое выражается в дециадулизации стромы и подавлении роста эндометрия.
Таким образом, ингибирование ИПФР — 1, по всей вероятности является одним из возможных молекулярных механизмов антипролиферативного действия левоноргестрела, входящего в состав ЛРС, на гиперплазированный эндометрий у женщин в период перименопаузы [14, 15].
Для оказания антиэстрогенного влияния на эндометрий, применяют также эстроген-гестагенные препараты (нон-овлон, ановлар и др.). К их применению существуют относительные противопоказания: хронический холецистит или панкреатит, тромбофлебиты, варикозное расширение вен и др. [4., 13].
[4., 13].
Помимо гестагенов, эстраген-гестагенных препаратов, в настоящее время, для лечения гиперпластических процессов эндометрия у больных в период климактерия применяют антигонадотропины — даназол — производные 17а — этилтестостерона по 400-600 мг. ежедневно, гестринон или неместран — производные 19 — норстероидов по 2,5мг. 2 раза в неделю в непрерывном режиме в течении 6 месяцев. Эти препараты обладают выраженным антигонадотропным эффектом, способствуют подавлению функции яичников и, как следствие, вызывают гипоплазию и атрофию эндометрия, что наиболее актуально в позднем периоде климактерия [10.].
Сохраняется значимость включения гестагенов, норстероидов для лечения гиперпластических процессов в перименопаузальном возрасте, вследствие их эффективности и безопасности при кратковременных курсах лечения. При этом в каждом конкретном случае только врач, ориентируясь на индивидуальный статус пациентки, обязан четко определить целевые указания, которые должны быть решены при назначении конкретных гормональных препаратов, динамично отслеживая эффективность и безопасность гормонотерапии, в том числе гибко корректируя возникающие проблемы. (А.Н.Караченцев, Г.А.Мельниченко, 2003г.).
(А.Н.Караченцев, Г.А.Мельниченко, 2003г.).
Из вышеизложенного следует, что выбор метода профилактики и лечения патологических процессов эндометрия осуществляется с учетом клинико — анамнестических данных, сопутствующей соматической патологии, наличия противопоказаний для проведения традиционной гормонотерапиии, нередко отрицательное отношение пациенток к приему гормональных препаратов, а также органосохраняющее направление в современной медицине, обусловливает необходимость разработки новых подходов к профилактике развития и лечения гиперпластических процессов эндометрия.
synlab: Гиперплазия эндометрия
К гиперпластическим процессам эндометрия относят различные варианты гиперплазии эндометрия и полипы эндометрия.
Гиперпластические процессы эндометрия возможны в любом возрасте, но их частота значительно возрастает к периоду перименопаузы. Гиперпластические процессы эндометрия, по данным большинства ученых, относят к предшественникам рака эндометрия. Простая гиперплазия эндометрия без атипии переходит в рак в 1% случаев, полиповидная форма без атипии — в 3 раза чаще. Простая атипическая гиперплазия эндометрия без лечения прогрессирует в рак у 8% больных, сложная атипическая гиперплазия — у 29% больных.
Простая гиперплазия эндометрия без атипии переходит в рак в 1% случаев, полиповидная форма без атипии — в 3 раза чаще. Простая атипическая гиперплазия эндометрия без лечения прогрессирует в рак у 8% больных, сложная атипическая гиперплазия — у 29% больных.
Наиболее частый вид гиперпластического процесса эндометрия — полипы, встречающиеся у гинекологических больных с частотой до 25%. Чаще полипы эндометрия выявляют в пре- и постменопаузе. Полипы эндометрия озлокачествляются примерно в 2–3% наблюдений.
Согласно гистологической классификации ВОЗ (1975) выделяют 3 основных вида ГПЭ: эндометриальные полипы, эндометриальная гиперплазия, атипическая гиперплазия эндометрия.
Причины развития гиперпластических процессов эндометрия:
Эндометрий является органом-мишенью для половых гормонов из-за присутствия в нем специфических рецепторов. Ведущее место в патогенезе ГПЭ отводится относительной или абсолютной гиперэстрогении, отсутствии антиэстрогенного влияния прогестерона или недостаточном влиянии.
Причины гиперэстрогении: ановуляция; гиперпластические процессы в яичниках или гормонопродуцирующие опухоли яичников; нарушение гонадотропной функции гипофиза; гиперплазия коры надпочечников; неправильное использование гормональных препаратов (эстрогены, антиэстрогены).
Однако ГПЭ могут развиваться и при ненарушенных гормональных соотношениях. В развитии таких патологических процессов ведущая роль отводится нарушениям тканевой рецепции. Инфекционно-воспалительные изменения в эндометрии могут приводить к развитию ГПЭ у 30% больных.
В патогенезе ГПЭ большое место занимают также обменно-эндокринные нарушения: изменения жирового обмена, метаболизма половых гормонов при патологии гепатобилиарной системы и желудочно-кишечного тракта, иммунитета, функции щитовидной железы. Хорошо известен факт частого сочетания гиперплазии и рака эндометрия с ожирением, гипертонической болезнью, диабетом, изменением функции печени.
Нередко наблюдается сочетание патологии эндометрия с пролиферативными изменениями в молочной железе с миомой матки, что указывает на общность патологических процессов.
Симптомы гиперпластических процессов эндометрия:
- маточные кровотечения, чаще ациклические
- контактные кровяные выделения (при половом акте)
- при больших полипах эндометрия могут быть схваткообразные боли внизу живота
бесплодие, как правило, первичное (чаще из-за отсутствия овуляции)
Иногда полипы эндометрия остаются бессимптомными, особенно в постменопаузе, что крайне опасно.
Основные методы диагностики ГПЭ — трансвагинальное УЗИ и гистероскопия. Однако окончательный диагноз с указанием вида ГПЭ устанавливают после гистологического исследования соскоба эндометрия.
Трансвагинальное ультразвуковое сканирование. УЗИ с трансвагинальным сканированием высокоинформативно, неинвазивно, безвредно для пациентки. Информативность метода варьирует в зависимости от вида патологии эндометрия и возраста женщины. Точность диагностики ГПЭ при УЗИ составляет 60-70%. Информативность трансвагинального УЗИ при полипах эндометрия составляет 80-98%
Гистероскопия. Информативность гистероскопии в диагностике ГПЭ составляет 63-97%. Гистероскопия необходима как перед выскабливанием слизистой матки, для верификации характера и локализации патологии, так и после него для контроля за тщательностью проведенной операции.
Информативность гистероскопии в диагностике ГПЭ составляет 63-97%. Гистероскопия необходима как перед выскабливанием слизистой матки, для верификации характера и локализации патологии, так и после него для контроля за тщательностью проведенной операции.
Лечение ГПЭ зависит от патоморфологической характеристики эндометрия, возраста пациентки, причин заболевания, сопутствующей гинекологической и экстрагенитальной патологии.
Терапия в различные возрастные периоды складывается из:
— остановки кровотечения;
— восстановления менструальной функции в репродуктивном периоде или
— восстановление стойкой менопаузы в более старшем возрасте;
— профилактики рецидива гиперпластического процесса.
Ведение пациенток репродуктивного возраста с ГПЭ. Традиционным методом лечения ГПЭ является гормональная терапия. В репродуктивном возрасте она преследует цель как профилактики рецидива ГПЭ, так и восстановления овуляторного менструального цикла.
Контроль эффективности лечения осуществляется путем аспирационной биопсии эндометрия (пайпель-биопсии) и УЗИ через 3, 6 и 12 мес.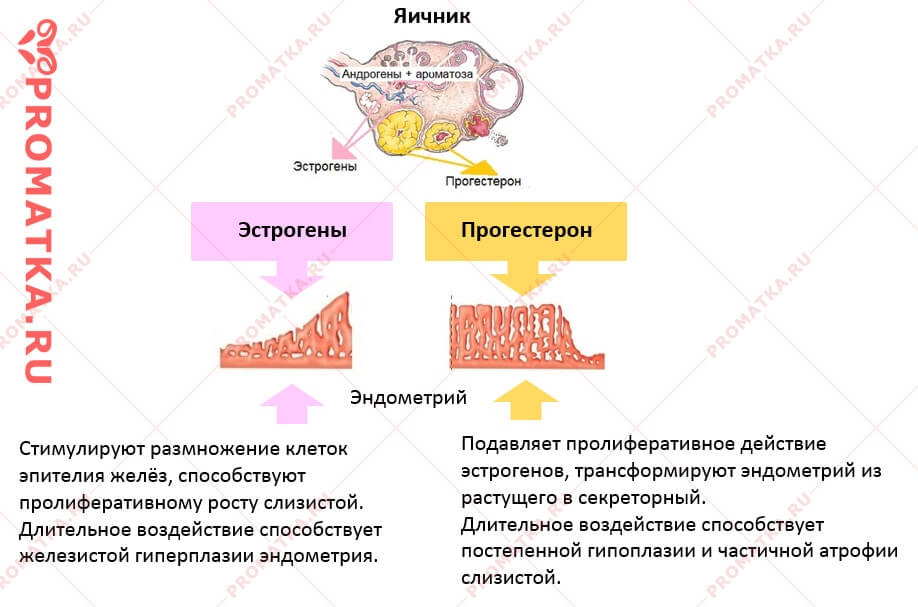 В сомнительных случаях или при подозрении на патологический процесс эндометрия целесообразно проводить гистероскопию с раздельным диагностическим выскабливанием слизистой оболочки матки.
В сомнительных случаях или при подозрении на патологический процесс эндометрия целесообразно проводить гистероскопию с раздельным диагностическим выскабливанием слизистой оболочки матки.
Врачи-гинекологи СИНЛАБ помогут провести необходимое Вам лабораторное и инструментальное обследование и лечение.
Гиперплазия эндометрия — ПроМедицина Уфа
Гиперплазия эндометрия — это доброкачественное разрастание внутреннего слоя матки — эндометрия, приводящее к утолщению и увеличению его объема. В основе заболевания лежит усиленное размножение и в некоторых случаях изменение структуры клеток, в результате чего увеличивается и объем самой матки.Чаще всего гиперплазия эндометрия вызывается нарушением гормонального фона, развивается на фоне патологий липидного и углеводного обмена веществ, различных гинекологических заболеваний, а также некоторых экстрагенитальных нарушений.В основную группу риска входят женщины, страдающие мастопатией, миомой матки, поликистозом яичников, эндометриозом, а также нарушением жирового обмена, гипертонией, болезнями печени, при которых нарушается распад гормонов, а также повышенным уровнем сахара в крови.
Его проявления: длительная задержка менструации, после которой возникает обильное кровотечение, кровянистые выделения в середине цикла. Но часто гиперплазия не вызывает никаких симптомов и обнаруживается случайно во время УЗИ.
Основная опасность в том, что хотя гипертрофия эндометрия является доброкачественным образованием, но она может переродиться в злокачественную раковую опухоль.
Причины
Нарушение гормонального фона. Причинами развития этого состояния чаще всего становятся гормональные нарушения. В анализах выявляется большое количество эстрогенов и дефицит прогестерона. Это бывает у женщин с мастопатией, миомой матки, поликистозом яичников, эндометриозом. Некоторые оральные контрацептивны при неправильном употреблении тоже могут плохо повлиять на гормональный фон.
Нарушение обменных процессов. Причиной могут стать нарушения жирового и углеводного обмена, ожирение. Дело в том, что жировая ткань умеет вырабатывать эстрогены. Некоторые общие заболевания тоже повышают риск гиперплазии. Это сахарный диабет, хронические болезни печени, гипертония.
Это сахарный диабет, хронические болезни печени, гипертония.
Болезни эндокринных желез: надпочечников, поджелудочной и щитовидной желез вызывают сбой работы яичников или самого эндометрия. Это может привести к усиленному росту клеток.
Возрастные изменения в половых органах вызывают гиперплазию эндометрия. Он становится более чувствительным к действию гормонов. Эта патология возникает у 60% женщин в период климакса и после него. Она часто вызывает сильные кровотечения и появление опухолей. Также высок риск развития болезни у девочек-подростков в период полового созревания.
Воспаления матки и других половых органов вызывают гиперплазию. Она может стать последствием инфекций, передающихся половым путем, внутриматочных контрацептивов (спиралей). Воспаление приводит к тому, что в тканях матки собирается много иммунных клеток. Они заставляют клетки эндометрия активно делиться.
Выскабливание и частые аборты, а также врожденные дефекты развития матки – это тоже факторы, которые вызывают разрастание эндометрия. Они приводят к тому, что рецепторы эндометрия становятся нечувствительными к действию прогестерона. Поэтому клетки продолжают размножаться, даже если гормоны в норме.
Они приводят к тому, что рецепторы эндометрия становятся нечувствительными к действию прогестерона. Поэтому клетки продолжают размножаться, даже если гормоны в норме.
Нарушение работы иммунной системы. Существует версия, что причиной гиперплазии эндометрия может быть неправильная работа иммунных клеток. Они по ошибке атакуют слизистый слой матки, и это вызывает неправильное деление его клеток.
Генетика. Существует и наследственная предрасположенность к гиперплазии. Если болезнь была у мамы, то и ее дочери могут иметь такие проблемы.
Симптомы
Проявления гиперплазии эндометрия: обильные, длительные, частые менструации, нерегулярный менструальный цикл или маточные кровотечения. При гиперплазии эндометрия могут быть скудные кровяные выделения до или после менструации, а также в середине цикла или постоянные в течение нескольких недель. Но наиболее частый симптом гиперплазии эндометрия – это внезапное маточное кровотечение после длительного отсутствия менструаций, особенно у женщин в период менопаузы.
Диагностика
Помимо консультации гинеколога, при подозрении на гиперплазию эндометрия очень важно провести УЗИ (обязательно вагинальным датчиком), которое позволяет оценить состояние внутреннего слоя матки (насколько он изменен и утолщен) и яичников (есть ли опухоль или киста). Далее возможны два варианта: гинеколог либо сразу направляет пациентку для гистероскопии (осмотр полости матки с увеличением с помощью прибора гистероскопа) и выскабливания матки, либо сначала проведет биопсию эндометрия. Биопсия эндометрия проводится специальной маленькой одноразовой вакуумной кюреткой (похожей на стержень шариковой ручки). Процедура биопсии эндометрия безопасна, безболезненна, для нее не нужна госпитализация, она занимает несколько минут и очень информативна. На основании гистологического исследования ткани эндометрия, полученной при биопсии или выскабливании, ставится диагноз «гиперплазия эндометрия» с указанием ее вида, что важно для лечения и прогноза.
Лечение
Лечение эндометриоза у женщин может быть консервативным, оперативным и комбинированным.
Консервативное лечение эндометриоза у женщин включает лекарственную терапию. В основе медикаментозного лечения лежит гормональная терапия. В качестве средств симптоматической терапии используют седативные средства, витамины групп В и С, спазмолитики, противовоспалительные средства.
К сожалению, не всегда можно вылечить эндометриоз консервативным путем. Лекарственные препараты помогут снять боль и вылечить легкие формы заболевания, но против полипов, спаек и кист они бессильны. Так как лечить эндометриоз консервативными методами удается не всегда, назначается оперативное вмешательство. Самым распространенным методом хирургического лечения является лапароскопия, при помощи которой можно удалить, кисты, спайки, очаги разрастания эндометрия, но при этом сохранить репродуктивные органы.
При совмещении таких методов как лапароскопия и гормональное лечение, эндометриоз лечится наиболее эффективно.
Лечение полипа эндометрия в матке
Бережно поможем вылечить полип эндометрия в ЦТА!
Основной принцип, которого придерживаются все врачи нашего центра — не навреди. Главное отличие лечения полипа эндометрия в нашем Центре, — мы не сразу госпитализируем для выскабливания, а наблюдаем.
Главное отличие лечения полипа эндометрия в нашем Центре, — мы не сразу госпитализируем для выскабливания, а наблюдаем.
Оставьте свой номер телефона.
Вам перезвонит администратор клиники.
Оставить заявку
Полип эндометрия — это образование «+ ткань». При классическом медицинском подходе, обнаружение полипа в эндометрии (цервикальном канале) — это показание к выскабливанию. Всегда ли это оправдано и эффективно? Не всегда. Иногда это погрешности УЗИ осмотра, и за полип принимают тень, складку и т.п. (тогда по результатам гистологии, на которую обязательно отправляют удаленную ткань, полип не обнаруживается). Иногда удаленный полип через год отрастает вновь на том же месте — и это может повторяться не один, не два, а множество раз.
Подход Территории Здоровья
Обнаружив подозрение на полип, мы делаем контрольное УЗИ через 1 месяц – в первой фазе цикла, на 5-6 день. Делаем «пайпель–тест», который абсолютно безопасно и безболезненно, без наркоза, позволит нам получить слизистую оболочку (эндометрий) полости матки и сделать его гистологическое исследование.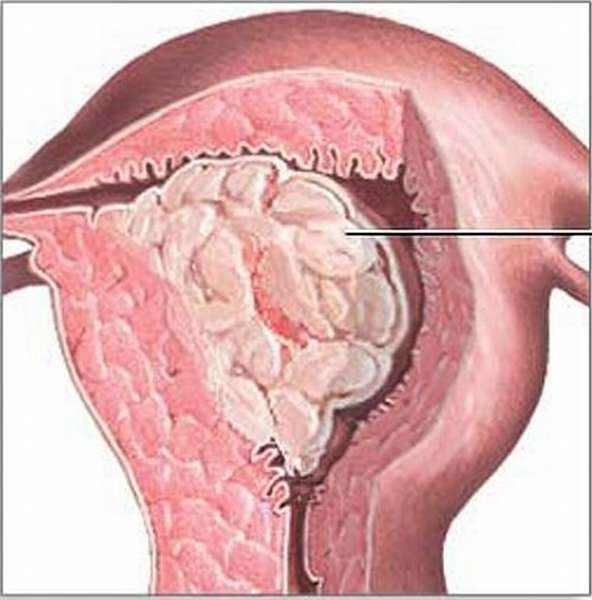 Если, действительно, полип эндометрия подтверждается, то наблюдаем его еще в течение 3 месяцев (за динамикой роста).
Если, действительно, полип эндометрия подтверждается, то наблюдаем его еще в течение 3 месяцев (за динамикой роста).
При активном разрастании полипа, наличии «клиники» (аномальные кровотечения, мажущие кровянистые выделения перед и после менструации, нарушение менструального цикла) — направляем на раздельное диагностическое выскабливание под контролем гистероскопии (осмотр полости матки с помощью специального оптического прибора) — это нужно, чтобы увидеть слизистую полости матки воочию, если есть полип – удалить его, коагулировать его ложе. Только тогда есть гарантия, что полип не вырастет вновь.
«Очень часто по классической схеме лечения полипа эндометрия, после удаления рекомендуют гормональную терапию, а мы рекомендуем… беременность (естественный способ отключить яичники, изменить функциональные процессы в эндометрии). Полипы опасны тем, что могут перерождаться — озлокачествляться. Потому любой врач с таким диагнозом у пациентки имеет онконастороженность. Но если при внимательном наблюдении за полипом его рост не обнаруживается, онкомаркеры не повышены, и нет клинической картины, то, скорее всего, трогать его не придется», — Г. В. Овсянникова, заведующая акушерско-гинекологическим отделением Территории Здоровья.
В. Овсянникова, заведующая акушерско-гинекологическим отделением Территории Здоровья.
Лечение полипов матки гомеопатией
Удаление полипа помогает лишь на время забыть о проблеме. Зачастую новообразования в области матки появляются снова, так как оперативное лечение устраняет только внешние проявления болезни, а не ее причину. Лечение полипов матки гомеопатией помогает избежать рецидивов заболевания. Эта методика комплексно воздействует на организм, устраняя основную причину – дисбаланс гормонов.
Если вам не удается справиться с болезнью при помощи традиционной медицины, обратитесь за консультацией к врачу-гомеопату нашей клиники.Почему лечение полипов матки гомеопатией эффективно
Грамотный специалист подбирает схему терапии индивидуально, учитывая жалобы пациентки и результаты обследований. Из-за натурального состава препаратов побочные эффекты практически исключены. При индивидуальной непереносимости каких-либо компонентов врач корректирует лечение. Программа терапии подбирается так, чтобы одновременно воздействовать на следующие аспекты заболевания:
Программа терапии подбирается так, чтобы одновременно воздействовать на следующие аспекты заболевания:
- Улучшение гормонального фона, сбои которого являются частой причиной новообразований.
- Снижение и профилактика воспалительных процессов, которые также способны приводить к возникновению полипа.
- Восстановление психического состояния, снижение нервозности. Постоянные стрессы и сильные переживания разрушающе действуют на женское здоровье.
Основное преимущество методики – в том, что она не отравляет организм химией, а помогает иммунным силам самостоятельно справиться с болезнью. Восстанавливая системы и органы естественным путем, гомеопатия не только избавляет от полипов без операции, но и предотвращает их появление в будущем.
ИГХ Рецепторы к эстрогенам и прогестерону (иммуногистохимическое исследование)
Метод определенияГистологическое исследование биоптатов слизистой тела матки, биоптатов молочной железы (с окрашиванием гематоксилином-эозином). Иммуногистохимическое исследование экспрессии рецепторов эстрогена и прогестерона с применением моноклональных антител к эстрогенам и прогестерону (пероксидазный и авидин-биотиновый методы).
Иммуногистохимическое исследование экспрессии рецепторов эстрогена и прогестерона с применением моноклональных антител к эстрогенам и прогестерону (пероксидазный и авидин-биотиновый методы).
Исследуемый материал Смотрите в описании
Доступен выезд на дом
Онлайн-регистрацияКомплексное исследование биоптатов. Включает морфологическое описание рецепторов к эстрогенам (ЭР) и прогестерону (ПР) и оценку их экспрессии.
Рецепторы к эстрогенам (ЭР) и прогестерону (ПР) относятся к внутриклеточным рецепторам стероидных гормонов. Они присутствуют в различных тканях-мишенях, в том числе в молочных железах и матке, где участвуют в механизмах гормональной индукции синтеза матричной РНК, белков, высвобождении цитокинов и факторов роста.
ЭР и ПР вовлечены в механизмы развития и метастазирования опухолей. Исследование экспрессии ЭР и ПР входит в стандарт обследования больных раком молочной железы, так как позволяет определить гормональную чувствительность опухоли, уточнить прогноз заболевания и потенциальный эффект гормонального лечения.
Исследование ЭР и ПР также используют в диагностике и прогнозе развития следующих патологических состояний: нарушения женской репродуктивной функции, бесплодие, гиперплазия эндометрия, злокачественные заболевания тела матки.
Опухоли молочной железы
Рак молочной железы – самое распространенное онкологическое заболевание у женщин (частота встречаемости в течение жизни у женщин в возрасте от 13 до 90 лет – 1:9-1:13). Большинство этих опухолей гормонально зависимы, эстрогены и прогестерон стимулируют их рост и метастазирование. Данные гормоны также способствуют развитию некоторых видов рака молочной железы.
Исследование экспрессии ЭР и ПР в биоптате опухоли в настоящее время рекомендовано проводить всем больным раком молочной железы для определения гормональной чувствительности опухоли, уточнения прогноза заболевания и потенциального эффекта гормонального лечения.
Опухоли с высоким содержанием ЭР и ПР, как правило, высокодифференцированные, с низкой пролиферативной активностью и минимально агрессивным течением, они хорошо отвечают на гормональную терапию и обычно имеют хороший прогноз. Эффективность гормональной терапии составляет около 50% при опухолях, экспрессирующих рецепторы к эстрогенам (ЭР+), и доходит до 75% при опухолях, экспрессирующих рецепторы как к эстрогенам, так и к прогестерону (ЭР+/ПР+).
Если опухолевые клетки экспрессируют мало рецепторов к эстрогенам (ЭР-), гормональная терапия обычно неэффективна. Исключение составляют варианты, когда клетки опухоли экспрессируют рецепторы к прогестерону (ЭР-/ПР+) – гормональная терапия эффективна у 10% таких больных.
Несмотря на то, что изредка резистентность к гормональной терапии наблюдается даже у пациентов с ЭР+/ПР+ опухолями, в настоящее время исследование ЭР и ПР в опухолевой ткани входит в «золотой стандарт диагностики» при раке молочной железы наряду с определением герцепт-статуса (HER-2, рецептор 2-го типа человеческого эпидермального фактора роста) и пролиферативной активности.
Частота встречаемости рецепторов к эстрогенам и прогестерону в клетках опухоли рака молочной железы:
- Около 75% всех раковых опухолей молочной железы эстроген-позитивны (ЭР+).
- Около 65% эстроген-позитивных опухолей имеют также рецепторы к прогестерону (ЭР+/ПР+).
- Около 25% всех раковых опухолей молочной железы эстроген-прогестерон-негативны (ЭР-/ПР-), либо их гормональный статус неизвестен.
- Около 10% всех раковых опухолей молочной железы эстроген-позитивны и при этом прогестерон-негативны (ЭР+/ПР-).
- Около 5% всех раковых опухолей молочной железы эстроген-негативны и при этом прогестерон-позитивны (ЭР-/ПР+).
Бесплодие
Стероидная рецепция эндометрия при бесплодии существенно меняется. Получены достоверные данные о снижении количества прогестерон-позитивных стромальных клеток, повышенной экспрессии α-эстрогенов в железистых и стромальных клетках как при первичном, так и при вторичном бесплодии. Исследование ЭР и ПР позволяет №525 ИГХ Рецепторы к эстрогенам и прогестерону (иммуногистохимическое исследование) оценить потенциальную способность эндометрия к нидации плодного яйца.
Исследование ЭР и ПР позволяет №525 ИГХ Рецепторы к эстрогенам и прогестерону (иммуногистохимическое исследование) оценить потенциальную способность эндометрия к нидации плодного яйца.
Не менее важна оценка состояния эндометрия перед назначением высоких доз гормональных препаратов в программах ЭКО. С одной стороны, гормональные препараты оказывают существенное влияние на систему рецепторов, с другой – нарушения в рецепторном аппарате могут привести к недостаточной восприимчивости эндометрия к экзогенному гормональному воздействию.
Восприимчивость эндометрия к воздействию эндогенных гормонов и гормональных препаратов можно определить с помощью соответствующих иммуногистохимических маркеров.
Гиперплазия эндометрия
Уровень экспрессии ЭР и ПР при простой железистой гиперплазии эндометрия без атипии не зависит ни от возраста женщины, ни от наличия неопухолевой гинекологической патологии (хронического эндометрита, полипов эндометрия, фолликулярных кист яичников). Это позволяет сделать вывод, что женщин постменопаузального возраста следует лечить консервативно.
Это позволяет сделать вывод, что женщин постменопаузального возраста следует лечить консервативно.
Вне зависимости от возраста простая железистая гиперплазия эндометрия с кистозными изменениями желез характеризуется снижением экспрессии ЭР в эпителии кист по сравнению с экспрессией ЭР в неизмененных железах.
Рак тела матки
Эндометриальные карциномы – гетерогенная группа опухолей, состоящая из разных нозологических форм, характеризующихся различным клиническим течением и выживаемостью больных (ВОЗ, Histological Typing Tumors of Female Genital Organs, 2003). Однако даже при одной и той же нозологической форме, например, при наиболее частой разновидности рака тела матки – эндометриоидной аденокарциноме – применяемые методы лечения оказываются неэффективными у каждой пятой больной. Биологическое поведение опухоли, обусловленный им вариант клинического течения и прогноз заболевания остаются недостаточно предсказуемыми даже для больных с одной и той же формой рака тела матки.
Гормонально-рецепторный статус – важнейшая характеристика, определяющая клиническое течение заболевания и выживаемость больных эндометриоидным раком тела матки. Известно, что неопухолевая гинекологическая патология (хронический эндометрит, полип эндометрия, наличие фолликулярных кист яичника) не влияет на рецепторный статус эндометрия.
В опухолях эндометрия экспрессия рецепторов зависит от степени дифференцировки опухолевой ткани. Снижение дифференцировки клеток злокачественных опухолей приводит к снижению экспрессии рецепторов половых стероидов. В низкодифференцированных опухолях количество ЭР+ и ПР+ клеток достоверно меньше, чем в высокодифференцированных опухолях. Та же закономерность существует в отношении ПР+ клеток в опухолях с умеренной степенью дифференцировки по сравнению с высокодифференцированными карциномами.
Материал для исследования:
биоптат слизистой тела матки, биоптат опухоли молочной железы, фиксированный в 10%-м растворе формалина, забуференного по Лилли.
Литература
- Волченко Н.Н., Франк Г.А. Комплекс морфологических и прогностических факторов при раке молочной железы: Пособие для врачей. — М., 2000.
- Иммуногистохимические методы, руководство (пер. с англ. под ред. Г.А. Франка и П.Г. Малькова) // М., 2011 – 224 с.
- Пожарисский К.М., Самсонова ЕА, Тен В.П., Максимова Н.А., Урманчеева А.Ф. Иммуногистохимический профиль эндометриоидной аденокарциномы тела матки: ER, PR, HER2, Ki-67 и их прогностическое значение //Архив патологии. — 2005. -Вып. 2.- с.13-17.
- Самсонова Е.А.. Максимова Н.А., Урманчеева А.Ф., Пожарисский К.М. Экспрессия рецепторов эстрогенов, прогестерона и онкобелка HER2 как показатели клинического течения и исхода эндометриоидной аденокарциномы тела матки (иммуногистохимическое исследование) //Вопр. онкол. — 2004. — Т. 50, № 2. — С. 196-201.
- Almasri N.M., Al Hamad M. Immunohistochemical evaluation of human epidermal growth factor receptor 2 and estrogen and progesterone receptors in breast carcinoma//Breast Cancer Res.
 -2005.-Vol.7 (5).-P.598-604.
-2005.-Vol.7 (5).-P.598-604. - WHO Classification of Tumors of the Braest. WHO, Lyon, 20
Гормональная терапия рака эндометрия
В этом виде лечения для лечения рака используются гормоны или препараты, блокирующие гормоны. Это не то же самое, что гормональная терапия, применяемая для облегчения симптомов менопаузы (гормональная терапия менопаузы). Его чаще всего используют для лечения рака эндометрия на поздней стадии (стадия III или IV) или рецидива после лечения (рецидив). Гормональная терапия часто применяется вместе с химиотерапией.
Гормональное лечение рака эндометрия может включать:
- Прогестины (это основное гормональное лечение.)
- Тамоксифен
- Агонисты высвобождающего гормона лютеинизирующего гормона (агонисты LHRH)
- Ингибиторы ароматазы (ИИ)
В настоящее время не установлено, что ни один вид гормонального лечения является лучшим при раке эндометрия.
Прогестины
В основном гормональном лечении рака эндометрия используется прогестерон или подобные ему препараты (так называемые прогестины ). 2 наиболее часто используемых прогестина:
- Медроксипрогестерона ацетат ( Provera ® ), который можно вводить в виде инъекции или в виде таблеток
- Мегестрола ацетат ( Megace ® ) в виде таблеток или жидкости
Эти препараты замедляют рост клеток рака эндометрия.Было обнаружено, что они полезны при лечении женщин с раком эндометрия, которые хотят иметь возможность забеременеть в будущем, и это область исследовательского интереса.
Побочные эффекты могут включать:
- Приливы
- Ночные поты
- Увеличение веса (от задержки жидкости и повышенного аппетита)
- Обострение депрессии
- Повышение уровня сахара в крови у женщин с диабетом
- Серьезные тромбы (редко)
Иногда гиперплазию эндометрия и ранний рак эндометрия можно лечить с помощью внутриматочной спирали (ВМС), содержащей прогестин, называемый левоноргестрелом. Это можно комбинировать с другим гормональным препаратом, таким как ацетат медроксипрогестерона или агонистом рилизинг-гормона лютеинизирующего гормона. (См. Ниже.)
Это можно комбинировать с другим гормональным препаратом, таким как ацетат медроксипрогестерона или агонистом рилизинг-гормона лютеинизирующего гормона. (См. Ниже.)
Тамоксифен
Тамоксифен — это антиэстрогеновый препарат, который часто используется для лечения рака груди. Его также можно использовать для лечения запущенного или рецидивирующего рака эндометрия. Чередование прогестерон и тамоксифен — это вариант, который, кажется, работает хорошо и лучше переносится, чем один прогестерон.
Целью терапии тамоксифеном является удержание эстрогенов в организме женщины от ускорения роста раковых клеток.Хотя тамоксифен может удерживать эстроген от «подпитки» раковых клеток, он действует как слабый эстроген в других частях тела. Это не вызывает потери костной массы, но может вызвать приливы жара и сухость влагалища. Женщины, принимающие тамоксифен, также подвержены более высокому риску образования серьезных тромбов в ногах.
Агонисты рилизинг-гормона лютеинизирующего гормона
Большинству женщин с раком эндометрия в ходе лечения удалили яичники. Некоторые женщины могли пройти курс лечения лучевой терапией, из-за которой их яичники неактивны.Это помогает предотвратить выработку эстрогена в организме, а также может замедлить рост рака.
Агонисты высвобождающего гормона лютеинизирующего гормона (агонисты LHRH) — это препараты, снижающие уровень эстрогена у женщин, у которых все еще есть рабочие яичники. Эти препараты «выключают» яичники у женщин в пременопаузе, поэтому они не вырабатывают эстроген.
Гозерелин (Золадекс ® ) и лейпролид (Лупрон ® ) — это препараты, которые могут использоваться для лечения рака эндометрия.Их делают в виде укола каждые 1–3 месяца. Эти препараты также называются агонистами гонадотропин-рилизинг гормона (GNRH) .
Побочные эффекты могут включать любые симптомы менопаузы, такие как приливы и сухость влагалища. Они также могут вызывать боли в мышцах и суставах. При длительном приеме (годы) эти препараты могут ослабить кости, что иногда приводит к остеопорозу.
Ингибиторы ароматазы
Даже после того, как яичники удалены (или не работают), эстроген все еще вырабатывается в жировой ткани.Это становится основным источником эстрогена в организме. Препараты, называемые ингибиторами ароматазы, могут остановить производство этого эстрогена и еще больше снизить уровень эстрогена. Примеры ингибиторов ароматазы включают летрозол (Фемара ® ), анастрозол (Аримидекс ® ) и экземестан (Аромазин ® ). Эти препараты чаще всего используются для лечения рака груди, но могут быть полезны и при лечении рака эндометрия. Чаще всего они используются для лечения женщин, которым нельзя сделать операцию, но врачи ищут другие способы применения этих препаратов.
Побочные эффекты могут включать головные боли, боли в суставах и мышцах, а также приливы. При длительном приеме (годы) эти препараты могут ослабить кости, что иногда приводит к остеопорозу. Эти препараты все еще изучаются на предмет того, как лучше всего использовать их для лечения рака эндометрия.
Гиперплазия эндометрия — Ассоциированные специалисты по женскому здоровью
E Гиперплазия эндометрия — это состояние, которое возникает, когда слизистая оболочка матки (эндометрий) слишком разрастается.Это доброкачественное (не рак) заболевание. Однако в некоторых случаях это может привести к раку матки. Некоторые женщины подвержены более высокому риску гиперплазии. Если вы находитесь в группе риска или ваш врач диагностировал гиперплазию, эта брошюра расскажет вам больше о:
|
| Гиперплазию эндометрия можно лечить, и женщины из группы риска могут принять меры для защиты от нее. |
Кто находится в опасности?
Гиперплазия эндометрия чаще встречается у некоторых женщин. Наибольшему риску подвержены женщины, которые:
|
Наиболее частым признаком гиперплазии является аномальное вагинальное кровотечение.
| Эндометрий Эндометрий — это слизистая оболочка матки. Эта подкладка растет и утолщается каждый месяц, чтобы подготовить матку к беременности. Если беременность не наступает, во время менструации подкладка сбрасывается. Женские гормоны — эстроген и прогестерон — контролируют изменения слизистой оболочки матки. Эстроген накапливает слизистую оболочку матки. Прогестерон поддерживает и контролирует этот рост.В середине цикла (примерно на 14 день) происходит овуляция (из яичника выходит яйцеклетка). Если яйцеклетка не оплодотворена, уровень гормонов падает. Эта капля вызывает нормальный, регулярный менструальный цикл. Поскольку женщины близки к менопаузе, их организм вырабатывает меньшее количество этих гормонов. После менопаузы, когда у женщины больше нет менструаций, вырабатывается очень мало этих гормонов. Некоторые женщины принимают заместительную гормональную терапию для замены обоих гормонов или принимают только эстроген.Это помогает облегчить симптомы менопаузы. Эстроген без достаточного количества прогестерона может вызвать утолщение слизистой оболочки матки. Это называется гиперплазией эндометрия. В некоторых случаях гиперплазии эндометрия клетки слизистой оболочки становятся ненормальными. Это называется атипичной гиперплазией. Это состояние может привести к раку матки. |
Тесты
Если у вас наблюдается ненормальное кровотечение наряду с любым из других факторов риска, вам может потребоваться обследование на гиперплазию эндометрия.Может потребоваться один или несколько тестов.
УЗИ
Ваш врач может посоветовать вам пройти вагинальное УЗИ . Для этого теста вам во влагалище вводится небольшое устройство. В матку может попасть жидкость. Ультразвук использует звуковые волны для изображения слизистой оболочки матки.
Биопсия
Гиперплазию эндометрия также можно обнаружить при биопсии эндометрия. Биопсия эндометрия может быть сделана в кабинете врача.Ваш врач вставляет узкую трубку внутрь матки, чтобы взять образец клеток. Во время теста вы можете почувствовать спазмы. Клетки будут отправлены в лабораторию и проверены под микроскопом. Результаты биопсии эндометрия могут выявить рак матки.
Дилатация и кюретаж
Для дилатации и выскабливания (D&C) отверстие матки растягивается (расширяется). Специальное устройство, называемое кюреткой, используется для осторожного отделения и удаления образца слизистой оболочки матки.Затем эта ткань изучается в лаборатории на предмет рака.
Для облегчения боли вам могут сделать анестезию. Это можно сделать в поликлинике, кабинете врача или больнице. D&C может выполняться с помощью других процедур, таких как гистероскопия .
Гистероскопия
Для гистероскопии ваш врач вводит в матку тонкое устройство, напоминающее телескоп, чтобы найти участки слизистой оболочки, которые могут быть аномальными.Затем он или она удаляет клетки из этих областей и отправляет образец в лабораторию для тестирования.
Лечение
В большинстве случаев гиперплазию эндометрия можно лечить с помощью лекарств, которые представляют собой форму гормона прогестерона. Прием прогестерона приведет к потере подкладки и предотвратит ее повторное накопление. Это часто вызывает вагинальное кровотечение.
Вы и ваш врач подберете форму прогестерона и дозу, которая вам подойдет. Сколько и как долго вы принимаете прогестерон, зависит от вашего состояния.После приема прогестерона слизистую оболочку матки можно снова проверить с помощью биопсии эндометрия.
Если проблема не исчезнет, можно использовать дополнительное лечение (например, другие лекарства или хирургическое вмешательство). Гистерэктомия (операция по удалению матки) может быть вариантом, если вы пополнили свою семью и ваша биопсия показала клетки, которые могут стать раком (атипичная гиперплазия). Если вы хотите иметь детей, можно обсудить и другие варианты.
Защита от гиперплазии эндометрия
Женщины могут предпринять шаги для снижения риска гиперплазии эндометрия.Это может защитить женщин с определенными факторами риска, а также помочь предотвратить его повторение.
- Если вы принимаете эстроген после менопаузы, вам необходимо принять форму прогестерона, чтобы снизить риск гиперплазии эндометрия и рака матки.
- Если у вас нет месячных, вам может потребоваться прием прогестерона, чтобы предотвратить чрезмерный рост слизистой оболочки матки. Противозачаточные таблетки (оральные контрацептивы) содержат эстроген вместе с прогестероном.Они могут помочь защитить от гиперплазии эндометрия у женщин, у которых нерегулярные месячные.
- Если у вас избыточный вес, может помочь похудание.
Наконец…
В большинстве случаев гиперплазия эндометрия поддается лечению. Во время лечения проконсультируйтесь с врачом, чтобы предотвратить дальнейшие проблемы. Женщины из группы риска могут принять меры для защиты от гиперплазии эндометрия.
Глоссарий
Диабет: Состояние, при котором уровень сахара в крови слишком высок.
Расширение и кюретаж (D&C): Процедура, при которой шейка матки открывается и ткань осторожно соскабливается или отсасывается изнутри матки.
Биопсия эндометрия: Тест, в котором небольшое количество ткани, выстилающей матку, удаляется и исследуется под микроскопом.
Эстроген: Женский гормон, вырабатываемый яичниками, который стимулирует рост слизистой оболочки матки.
Гормональная заместительная терапия: Лечение, при котором эстроген и часто прогестин используются для облегчения симптомов, вызванных низким уровнем гормонов, вырабатываемых организмом.
Гормоны: Вещества, вырабатываемые организмом для контроля функций различных органов.
Гистероскопия: Хирургическая процедура, при которой тонкий светопропускающий телескоп, гистероскоп, используется для осмотра матки изнутри или проведения операции.
Менопауза: Процесс в жизни женщины, когда перестают функционировать яичники и прекращаются менструации.
Синдром поликистозных яичников (СПКЯ): Состояние, при котором повышенное содержание андрогенов приводит к сохранению множественных маленьких кист на яичниках.
Прогестерон: Женский гормон, который вырабатывается в яичниках и вызывает рост слизистой оболочки матки. Когда прогестерон снижается, наступает менструация.
Ультразвук: Тест, в котором звуковые волны используются для исследования внутренних структур. Во время беременности его можно использовать для обследования плода.
Матка: Мышечный орган, расположенный в тазу женщины, который содержит и питает развивающийся плод во время беременности.
Гиперплазия эндометрия
Вопрос
Какова оптимальная доза и схема лечения гиперплазии эндометрия с использованием различных прогестинов? Является ли использование депо медроксипрогестерона хорошим вариантом лечения?
Ответ эксперта
Скотт Г.Чуднов, MD
Для ответа на этот вопрос требуется небольшая справочная информация. Гиперплазия эндометрия обычно считается предвестником рака эндометрия. Доказано, что присутствие беспрепятственного эстрогена, которое, например, может быть результатом терапии экзогенными эстрогенами, ановуляторных циклов, синдрома поликистозных яичников (СПКЯ) или ожирения, увеличивает вероятность развития гиперплазии эндометрия и рака. Некоторые редкие, но опасные состояния могут генерировать беспрепятственный эстроген, включая опухоли гранулезных клеток и яичниковые теомы, а также андрогенсекретирующие опухоли коры головного мозга.Эти условия должны быть исключены, если есть подозрение у пациентов с гиперплазией эндометрия (например, наличие придаточного образования на УЗИ у пациента с аномальным кровотечением).
Пациенты с гиперплазией эндометрия обычно имеют патологическое кровотечение; это может быть меноррагия, метроррагия, менометоррагия или постменопаузальное кровотечение. Следует исключить рак эндометрия, особенно у пациентов старше 35 лет, которые обращаются с этими состояниями.Наиболее распространенный метод, используемый для диагностики гиперплазии и рака, — это аспирация эндометрия с помощью пипетки, также известная как биопсия эндометрия. Это простая процедура для выполнения в офисе с минимальным дискомфортом для пациента и относительно высокой чувствительностью и специфичностью. Другие методы включают измерение эхо-сигнала эндометрия у женщин в постменопаузе и гистероскопию с направленной биопсией эндометрия. Хотя в литературе существует много споров относительно оптимального метода оценки эндометрия, любой из вышеперечисленных методов — по отдельности или в комбинации — представляет собой подходящие диагностические методы.
Важным моментом при лечении гиперплазии является классификация имеющегося типа гиперплазии. Гиперплазия эндометрия определяется как разрастание желез неправильного размера и формы с увеличением соотношения железы / строма. В общем, существует 4 типа гиперплазии: простая, сложная, простая с атипией и сложная с атипией ( Таблица 1 ). Основным соображением в этой классификации является риск, который каждая гиперплазия представляет для прогрессирования рака эндометрия (хорошая легочная пневмония, чтобы помнить приблизительные риски: «пенни, никель, десять центов, четверть» для 1%, 5%, 10% и 25%. соответственно).Первичным дифференцирующим фактором является наличие цитологической атипии, которая значительно увеличивает вероятность прогрессирования рака. Следовательно, лечение этих случаев обычно требует более агрессивной терапии.
Таблица 1. Классификация гиперплазии эндометрия
| Тип | Описание | Риск прогрессирования рака эндометрия |
|---|---|---|
| Простой | Расширенные железы, которые могут содержать некоторые выпячивания и обильную строму эндометрия | ~ 1% |
| Комплекс | Железы переполнены очень маленькой стромой эндометрия, очень сложным узором желез и выходящими образованиями | ~ 3% -5% |
| Простой с атипией | То же, что указано выше, но также содержит цитологическую атипию.Это относится к гиперхромным, увеличенным эпителиальным клеткам с повышенным соотношением ядер к цитоплазматическим. | ~ 8% -10% |
| Комплекс с атипией | ~ 25% -30% |
Несмотря на очень высокий уровень спонтанного регресса (80% в случаях без атипии и более 50% в комплексе с атипией), лечение должно быть назначено, так как некоторые пациенты, тем не менее, прогрессируют до рака. Двумя основными соображениями при лечении гиперплазии эндометрия являются класс и желание будущего деторождения.Как правило, лечение с использованием прогестеронового агента лучше всего подходит для пациентов с гиперплазией — простой или сложной — у которых нет атипии. При атипии идеальным лечением является гистерэктомия, учитывая высокую скорость потенциального прогрессирования рака.
При гиперплазии без атипии циклическая терапия прогестинами рекомендуется женщинам, не ищущим контрацепции. Женщинам, желающим использовать противозачаточные средства, особенно молодым женщинам, можно применять оральные противозачаточные таблетки, которые обеспечивают комбинированный эффект контроля цикла и контрацепции.Если используются оральные противозачаточные таблетки, вероятно, лучше использовать монофазный препарат. Женщинам, для которых контрацепция не является проблемой, следует начинать терапию циклическими прогестиновыми агентами. Обычно мы используем 10 мг медроксипрогестерона ацетата в течение 10–14 дней в месяц в течение 3–6 месяцев. Пациентов обычно берут повторно через это время, и если у них нормальная биопсия и нет симптомов, мы прекращаем терапию. Если гиперплазия стойкая, назначают непрерывную терапию прогестином в дозе 20 мг / день в течение 3–6 месяцев.При желании с самого начала можно использовать лечение непрерывными дозами. Аналогичным образом можно использовать другие пероральные препараты (, таблица 2, ).
Таблица 2. Обычно используемые агенты, содержащие только прогестерон
| Общее имя | Общие торговые наименования | Обычная дозировка |
|---|---|---|
| Прогестерон | Crinone; Прогестасерт; Прометриум | 200 мг PO |
| Медроксипрогестерона ацетат | Provera; Депо-Провера | 10-20 мг PO 150 мг IM |
| мегестрола ацетат | Мегас | 40-320 мг PO |
| Левоноргестрел | Мирена ИУС | 1 внутриматочная каждые 5 лет |
Помимо вышеупомянутых схем, другие системы доставки прогестерона могут помочь в лечении гиперплазии эндометрия.Препарат депо для инъекций медроксипрогестерона ацетата ( Depo-Provera ) можно вводить в стандартной дозе, используемой для контрацепции — 150 мг каждые 12 недель. Дополнительно внутриматочная система левоноргестрела ( Мирена ) эффективна в течение 5 лет. Преимущества, которые предлагают эти методы, заключаются в уменьшенной дозировке (например, после введения Mirena пациенту не нужно принимать дополнительные лекарства) и контрацептивных преимуществах, которые они предоставляют.
Для пациентов с клеточной атипией общая рекомендация — выполнить гистерэктомию.Если гистерэктомия не является жизнеспособным вариантом (например, пациент молодой и желает в будущем вынашивать ребенка или пациент — очень плохой кандидат на хирургическое вмешательство), то можно использовать непрерывную терапию высокими дозами прогестина. Обычно мы принимаем 20 мг медроксипрогестерона ацетата в день. Другой вариант — от 40 до 160 мг мегестрола ацетата в день в течение 6 месяцев. Очень важно, чтобы эти пациенты получали повторную биопсию каждые 6 месяцев из-за высокого риска рецидива.
Список лекарств для профилактики гиперплазии эндометрия (9 в сравнении)
О гиперплазии эндометрия, профилактика
Профилактика гиперплазии эндометрия, аномального разрастания клеток эндометрия.
Лекарства, применяемые при гиперплазии эндометрия, профилактика
Следующий список лекарств так или иначе связаны с этим состоянием или используются для его лечения.
| Название препарата | Рейтинг | Отзывы | Мероприятия & квест; | Rx / OTC | Беременность | CSA | Спирт |
|---|---|---|---|---|---|---|---|
| медроксипрогестерон | 5.2 | 7 отзывов | Rx | Икс | N | ||
Общее название: медроксипрогестерон системный Бренды: Провера, Депо-Провера, depo-subQ Provera 104 Класс препарата: гормоны / противоопухолевые препараты, контрацептивы, прогестины Потребителям: дозировка, взаимодействия, побочные эффекты Для профессионалов: Факты о наркотиках от А до Я, Монография AHFS DI, Информация о назначении | |||||||
| Прометриум | 0.0 | 1 отзыв | Rx / OTC | B | N | ||
Общее название: прогестерон системный Класс препарата: прогестины Потребителям: дозировка, взаимодействия, побочные эффекты Для профессионалов: Прописная информация | |||||||
| Провера | 3.3 | 5 отзывов | Rx | Икс | N | ||
Общее название: медроксипрогестерон системный Класс препарата: гормоны / противоопухолевые препараты, контрацептивы, прогестины Потребителям: дозировка, взаимодействия, побочные эффекты Для профессионалов: Прописная информация | |||||||
| прогестерон | 8.5 | 3 отзыва | Rx / OTC | B | N | ||
Общее название: прогестерон системный Бренды: Прометриум, Эндометрин, Кринон, Первый прогестерон MC10 …показать все Класс препарата: прогестины Потребителям: дозировка, взаимодействия, побочные эффекты Для профессионалов: Факты о лекарствах от А до Я, Монография AHFS DI, Монографии по натуральным продуктам, Информация о назначении | |||||||
| Депо-Провера | 9.0 | 1 отзыв | Rx | Икс | N | ||
Общее название: медроксипрогестерон системный Класс препарата: гормоны / противоопухолевые препараты, контрацептивы, прогестины Потребителям: дозировка, взаимодействия, побочные эффекты Для профессионалов: Прописная информация | |||||||
| Эндометрин | Показатель | Добавить отзыв | Rx / OTC | B | N | ||
Общее название: прогестерон системный Класс препарата: прогестины Потребителям: дозировка, взаимодействия, побочные эффекты Для профессионалов: Прописная информация | |||||||
| Crinone | Показатель | Добавить отзыв | Rx / OTC | B | N | ||
Общее название: прогестерон системный Класс препарата: прогестины Потребителям: дозировка, взаимодействия, побочные эффекты | |||||||
| Первый прогестерон MC10 | Показатель | Добавить отзыв | Rx / OTC | B | N | ||
Общее название: прогестерон системный Класс препарата: прогестины Потребителям: дозировка, взаимодействия, побочные эффекты | |||||||
| depo-subQ Provera 104 | Показатель | Добавить отзыв | Rx | Икс | N | ||
Общее название: медроксипрогестерон системный Класс препарата: гормоны / противоопухолевые препараты, контрацептивы, прогестины Потребителям: дозировка, взаимодействия, побочные эффекты Для профессионалов: Прописная информация | |||||||
Легенда
| Рейтинг | Для оценки пользователей спрашивали, насколько эффективным они нашли лекарство с учетом положительных / побочных эффектов и простоты использования (1 = неэффективно, 10 = наиболее эффективно). |
|---|---|
| Активность | Активность основана на недавней активности посетителей сайта по отношению к другим лекарствам в списке. |
| Rx | Только по рецепту. |
| ОТС | Без рецепта. |
| Rx / OTC | По рецепту или без рецепта. |
| Не по назначению | Это лекарство не может быть одобрено FDA для лечения этого состояния. |
| Категория беременности | |
|---|---|
| A | Адекватные и хорошо контролируемые исследования не смогли продемонстрировать риск для плода в первом триместре беременности (и нет доказательств риска в более поздних триместрах). |
| B | Исследования репродукции животных не смогли продемонстрировать риск для плода, и нет адекватных и хорошо контролируемых исследований у беременных женщин. |
| С | Исследования репродукции животных показали неблагоприятное воздействие на плод, и нет адекватных и хорошо контролируемых исследований на людях, но потенциальные преимущества могут оправдывать использование у беременных женщин, несмотря на потенциальные риски. |
| Д | Имеются положительные доказательства риска для плода у человека, основанные на данных о побочных реакциях, полученных из исследовательского или маркетингового опыта или исследований на людях, но потенциальные преимущества могут потребовать применения у беременных женщин, несмотря на потенциальные риски. |
| X | Исследования на животных или людях продемонстрировали аномалии развития плода и / или есть положительные доказательства риска для плода у человека, основанные на данных о побочных реакциях из исследовательского или маркетингового опыта, и риски, связанные с использованием у беременных женщин, явно перевешивают потенциальную пользу. |
| N | FDA не классифицировало препарат. |
| Закон о контролируемых веществах (CSA) Приложение | |
|---|---|
| N | Не подпадает под действие Закона о контролируемых веществах. |
| 1 | Имеет высокий потенциал для злоупотреблений. В настоящее время не применяется в медицинских целях в США. Нет общепринятых правил безопасности для использования под медицинским наблюдением. |
| 2 | Имеет высокий потенциал для злоупотреблений. В настоящее время разрешено медицинское использование для лечения в Соединенных Штатах или в настоящее время принятое медицинское использование с серьезными ограничениями. Жестокое обращение может привести к серьезной психологической или физической зависимости. |
| 3 | Имеет меньшую вероятность злоупотребления, чем те, которые указаны в таблицах 1 и 2. В настоящее время разрешено медицинское использование для лечения в США. Злоупотребление может привести к умеренной или низкой физической зависимости или высокой психологической зависимости. |
| 4 | Имеет низкий потенциал злоупотребления по сравнению с теми, которые указаны в списке 3. В настоящее время он признан в медицине для лечения в США. Злоупотребление может привести к ограниченной физической или психологической зависимости по сравнению с теми, которые указаны в таблице 3. |
| 5 | Имеет низкий потенциал злоупотребления по сравнению с теми, которые указаны в таблице 4. В настоящее время разрешено медицинское использование для лечения в Соединенных Штатах. Жестокое обращение может привести к ограниченной физической или психологической зависимости по сравнению с теми, которые указаны в таблице 4. |
| Спирт | |
|---|---|
| X | Взаимодействует с алкоголем. |
Дополнительная информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности за медицинское обслуживание
Риски, типы и методы лечения гиперплазии эндометрия
Гиперплазия эндометрия — это аномалия слизистой оболочки матки или эндометрия. В этом состоянии могут наблюдаться симптомы аномального маточного кровотечения, которое возникает в результате гормонального дисбаланса. Диагностическое обследование может показать, есть ли у вас атипичные клетки, что будет определять курс лечения.
ericsphotography / Getty ImagesЭндометрий
Ваш эндометрий — это то, что накапливается и выпадает каждый месяц в ответ на регулярные циклические гормональные изменения.Это основной компонент ежемесячных менструаций. Утолщение или разрастание слизистой оболочки матки в течение первой половины менструального цикла — это совершенно нормально.
Ваши яичники обычно производят эстроген и прогестерон в ответ на стимулирующие гормоны мозга. Это организованное и своевременное изменение и баланс эстрогена и прогестерона — вот что заставляет менструацию приходить регулярно, примерно каждые 28 дней.
Если наблюдается дисбаланс гормональной стимуляции эндометрия, может возникнуть нарушение.Это ненормальное изменение представляет собой нерегулярное утолщение эндометрия и называется гиперплазией эндометрия.
Симптомы гиперплазии эндометрия
Симптомы аномального маточного кровотечения, такие как:
- Менструальное кровотечение более сильное, чем обычно
- Кровотечение между менструациями
- Кровотечение в постменопаузе
Аномальное маточное кровотечение является наиболее частым признаком того, что у вас может быть гиперплазия эндометрия. Важно обратиться к врачу, чтобы обсудить эти изменения в вашем кровотечении.Затем ваш врач может решить, необходимы ли дальнейшие исследования и оценка.
Причины
Гиперплазия эндометрия вызвана гормональным дисбалансом, а именно относительным избытком эстрогена по сравнению с прогестероном. Эстроген — это гормон, который отвечает за нормальное утолщение эндометрия в течение первой половины менструального цикла.
Когда ваш эндометрий сбалансирован правильным количеством прогестерона, он нарастает, но затем истончается, не допуская чрезмерного ненормального роста.При относительном избытке эстрогена подкладка чрезмерно стимулируется и продолжает утолщаться. Со временем на этой утолщенной подкладке начинают развиваться аномальные изменения.
Факторы риска
Состояния, вызывающие избыток эстрогена, которые могут привести к гиперплазии эндометрия, включают:
Ожирение
Жировая ткань превращает другие гормоны в эстроген. Это приводит к дополнительному эстрогену, который стимулирует слизистую оболочку матки в дополнение к нормальному циклическому эстрогену, вырабатываемому вашими яичниками.Если ваш ИМТ превышает 35, у вас значительно повышается риск развития гиперплазии эндометрия по сравнению с вами при идеальной массе тела.
ановуляция
Может быть несколько причин, по которым у вас может не произойти овуляция. Если вы не овулируете, ваш яичник не будет увеличивать выработку прогестерона. Повышение уровня прогестерона необходимо для того, чтобы слизистая оболочка матки потеряла сознание. Другими словами, у вас не будет менструации.
В некоторых типах ановуляторных циклов это отсутствие резкого увеличения прогестерона приводит к относительному избытку эстрогена.Этот несбалансированный эстроген приводит к аномальному утолщению эндометрия. В конце концов, у вас будет ненормальное маточное кровотечение.
Типичные образцы кровотечений при этом типе ановуляции включают нерегулярные и обильные менструации или кровотечения между менструациями. К распространенным причинам этого типа гормонального дисбаланса относятся:
Экзогенные гормоны
Очевидно, что прием заместительной эстрогена увеличит уровень эстрогена по сравнению с уровнем прогестерона.Вот почему, если у вас все еще есть матка, вам нужно принять прогестин в какой-либо форме (прогестерон), чтобы предотвратить чрезмерную стимуляцию эндометрия при приеме эстрогена.
Другой гормональный препарат, который может вызвать аномальное утолщение эндометрия, — это Тамоксифен. Тамоксифен — это препарат, который называется селективным модулятором рецепторов эстрогена или SERM. СЭРМы — это препараты, которые по-разному воздействуют на чувствительные к эстрогену части вашего тела.
Тамоксифен часто используется при лечении гормонально-чувствительного рака груди, поскольку он противодействует воздействию эстрогена в ткани груди.Однако тамоксифен стимулирует рецепторы эстрогена в слизистой оболочке матки, поэтому он действует как эстроген и может вызывать гиперплазию эндометрия.
Если вы принимаете заместительную гормональную терапию или тамоксифен и у вас развивается аномальное маточное кровотечение, очень важно, чтобы вы обратились к врачу и прошли обследование.
Эстроген-продуцирующие опухоли яичников
Гормонопродуцирующие опухоли — не очень частая причина гиперплазии эндометрия. Однако есть определенные (обычно доброкачественные) опухоли яичников, которые производят избыток эстрогена.
Диагностика
Когда вы обратитесь к врачу по поводу аномального маточного кровотечения, вам, скорее всего, сделают биопсию слизистой оболочки матки. Ваш врач может порекомендовать либо офисную биопсию эндометрия, либо небольшую хирургическую процедуру, называемую гистероскопией с кюретажем или забором эндометрия.
Биопсия эндометрия
Это очень распространенная гинекологическая процедура в офисе. В целом переносится очень хорошо. Ожидание и беспокойство по поводу процедуры часто намного хуже, чем сама биопсия.
Если вам нужно сделать биопсию эндометрия, рекомендуется принять 600 мг ибупрофена и немного перекусить примерно за час до процедуры. Вы можете взять с собой небольшой теплый компресс или пластырь, чтобы уменьшить спазмы во время и после процедуры. Ваш врач может даже дать вам один во время биопсии.
Подготовка к биопсии такая же, как и для обычного мазка Папаниколау. После установки расширителя врач очистит шейку матки мягким антисептиком.Скорее всего, ваш врач затем поместит зажим, чтобы удерживать шейку матки на месте, пока вводится небольшой аспиратор.
Вероятно, вы испытаете некоторый дискомфорт. Вы не почувствуете ничего острого, но у вас будут спазмы. Дискомфорт может варьироваться от легких периодических спазмов до сильных спазмов, подобных ранним схваткам.
Хорошая новость заключается в том, что процедура довольно быстрая и обычно длится менее одной минуты. Прием ибупрофена перед процедурой и использование теплого компресса во время процедуры определенно помогает минимизировать боль.
Гистероскопия
Ваш врач может предложить вам пройти гистероскопию и забор эндометрия вместо биопсии эндометрия. Это хирургическая процедура в тот же день, и в некоторых гинекологических практиках ее также проводят в офисе, а не в операционной.
Преимущество гистероскопии заключается в том, что она позволяет вашему врачу непосредственно наблюдать за слизистой оболочкой матки, гарантируя, что все области эндометрия взяты надлежащим образом. В некоторых ситуациях врач может предложить эту несколько более инвазивную процедуру.
Гиперплазию эндометрия нельзя диагностировать с помощью анализа крови или УЗИ. Однако возможно, что ваш врач может порекомендовать определенные анализы крови, чтобы исключить другие причины аномального маточного кровотечения.
Также возможно, что ваш врач может назначить трансвагинальное УЗИ органов малого таза, чтобы помочь в диагностике причины аномального маточного кровотечения.
Гиперплазия эндометрия может быть диагностирована только после взятия пробы эндометрия и его оценки под микроскопом патологом.
Типы
Когда патолог смотрит на образец вашего эндометрия под микроскопом, он обращает особое внимание на изменения в двух компонентах вашего эндометрия, железах и поддерживающей ткани, называемой стромой.
Гиперплазия эндометрия диагностируется, когда желез относительно стромы больше, чем в нормальном пролиферативном или циклическом эндометрии.
Затем патолог прокомментирует, есть ли в этом аномально утолщенном эндометрии атипичные клетки, что приводит к двум классификациям гиперплазии эндометрия:
- Гиперплазия без атипии
- Атипичная гиперплазия
Гиперплазия эндометрия не является раком эндометрия, но считается предраковым состоянием.Фактически, в некоторых случаях значительной атипичной гиперплазии уже может присутствовать рак эндометрия на очень ранней стадии.
Лечение
Очень важно внимательно следить за любой гиперплазией эндометрия или лечить ее. Курс лечения будет зависеть от того, есть ли атипия.
Гиперплазия эндометрия без атипии
Когда нет атипичных клеток, вероятность того, что гиперплазия эндометрия в конечном итоге перерастет в рак эндометрия, очень мала.Данные свидетельствуют о том, что только около 5% женщин с гиперплазией эндометрия без атипии разовьется рак эндометрия. Также вероятно, что этот тип гиперплазии эндометрия пройдет сам по себе со временем.
Целевые факторы риска
Первая линия лечения — это поиск факторов риска, которые можно изменить. Например, если у вас значительно избыточный вес или вы страдаете ожирением, потеря веса поможет уменьшить избыток эстрогена, производимого жировыми клетками.Это позволит слизистой оболочке матки восстановиться.
Точно так же, если вы принимаете заместительную гормональную терапию, вашему врачу может потребоваться скорректировать дозу или порекомендовать вам прекратить ее использование.
Прогестерон
Ваш врач может порекомендовать использовать прогестиновые препараты, чтобы противодействовать загущающему эффекту избытка эстрогена на эндометрий. Причины, по которым ваш врач может предложить вам лечение прогестероном, включают:
- Наблюдение и изменение образа жизни не помогло
- У вас аномальное маточное кровотечение
- Вам нужен самый быстрый результат
Для лечения гиперплазии эндометрия без атипии предлагаются два типа прогестерона: пероральный прогестерон или прогестерон-содержащая ВМС.Имеются данные в пользу использования левоноргестрела ВМС (Мирена).
Если ваш ИМТ превышает 35, более вероятно, что лечение прогестероном не будет эффективным, если вы также не похудеете. Вам следует обсудить со своим врачом, какой вид лечения прогестероном лучше всего подходит для вас.
Независимо от того, выберете ли вы наблюдение или лечение прогестероном, вам необходимо будет тщательно контролировать интервальный забор эндометрия, чтобы гарантировать, что гиперплазия эндометрия исчезла и не вернется.
Гистерэктомия
Эксперты говорят, что гистерэктомию не следует предлагать как вариант лечения первой линии при гиперплазии эндометрия без атипии из-за общей эффективности лечения прогестероном и низкого риска развития рака эндометрия.
Однако эксперты сходятся во мнении, что есть определенные ситуации, в которых гистерэктомия может быть наиболее подходящим вариантом лечения для женщин, у которых закончились роды. Ваш врач может порекомендовать гистерэктомию, если:
- Во время последующего наблюдения у вас развивается атипичная гиперплазия
- Гиперплазия не улучшается после 12 месяцев лечения прогестероном
- У вас значительное аномальное кровотечение
- У вас снова развивается гиперплазия эндометрия после успешного лечения
- Вы не хотите пройти повторную биопсию эндометрия, необходимую при лечении прогестероном.
Гиперплазия эндометрия с атипией
Риск развития рака эндометрия гораздо выше, если у вас гиперплазия с атипией. Руководство немного более агрессивно из-за повышенного риска. Фактически, эксперты рекомендуют гистерэктомию в качестве лечения первой линии при атипичной гиперплазии у женщин, у которых закончились роды.
Если вам поставили диагноз атипичной гиперплазии и вы все еще планируете попытаться забеременеть, вас, скорее всего, будут лечить прогестероном, предпочтительно левоноргестреловой ВМС.
У вас будет более частый забор эндометрия, чтобы гарантировать адекватное лечение атипичной гиперплазии. Ваш врач, скорее всего, порекомендует вам обратиться к специалисту по фертильности и завершить вынашивание ребенка как можно скорее.
Скорее всего, ваш врач порекомендует вам сделать гистерэктомию после того, как вы закончите рожать, из-за высокой вероятности рецидива атипичной гиперплазии эндометрия.
Заместительная гормональная терапия и эндометрий
Заместительная гормональная терапия (ЗГТ) используется для лечения вазомоторных симптомов и состояний, таких как атрофический вагинит, у женщин в перименопаузе и постменопаузе, и ее долгосрочное применение также играет роль в снижении заболеваемости остеопорозом и ишемией. порок сердца у женщин в постменопаузе.По оценкам, не менее 20 миллионов женщин в развитых странах используют ЗГТ. 1 Современные препараты ЗГТ содержат эстроген и прогестаген: прогестаген необходим для защиты от риска гиперплазии эндометрия 2 — 5 и карциномы 6 — 10 , вызванной длительным беспрепятственным лечением эстрогенами. Этот риск более подробно обсуждается ниже. Обычно используются две схемы: последовательный (циклический) и непрерывный комбинированный.Последовательная ЗГТ может проводиться ежемесячно или трижды. Ежемесячная последовательная ЗГТ включает непрерывный прием эстрогена с добавлением прогестагена в течение 10–14 дней / цикл или календарный месяц, вызывая ежемесячное кровотечение отмены. 11 При трехмесячной последовательной ЗГТ прогестаген вводится ежеквартально в течение 10–14 дней, вызывая ежеквартальное кровотечение отмены. Непрерывная комбинированная ЗГТ предполагает непрерывное использование обоих агентов: стимулирующие рост эффекты эстрогена противопоставляются прогестагену, что приводит к атрофическому эндометрию. 12 , 13 Это преимущество состоит в том, что исключает кровотечение отмены, связанное с последовательной ЗГТ, которое может быть основной причиной несоблюдения режима лечения. 14 — 17 Женщина, перенесшая гистерэктомию, может принимать эстроген без прогестагена. Имплант эстрогена — один из вариантов, альтернативой являются таблетки, пластыри или гелевые препараты. Однако женщине, у которой была выполнена аблация эндометрия, необходим прогестаген, поскольку часть ткани эндометрия, возможно, не была разрушена процедурой.
Гистологическая оценка эндометрия — важная часть продолжающегося наблюдения за пациентами, принимающими ЗГТ, и гистопатолог должен быть знаком с внешним видом эндометрия у пациента, принимающего ЗГТ. В этом обзоре мы обсуждаем влияние ЗГТ на эндометрий и рассматриваем те проявления, с которыми может столкнуться гистопатолог, получающий образцы биопсии эндометрия от пациентов, получающих ЗГТ.
Образцы «Pipelle» и диагностические трудности с биопсией эндометрия
Многие образцы биопсии эндометрия у женщин, получающих ЗГТ, будут получены с помощью пробоотборника Pipelle TM в амбулаторных условиях.Этот метод часто приводит к очень маленькому количеству ткани для гистологического анализа (до 59% биопсий в одном исследовании 18 ). Количество эндометриальной ткани, необходимое для постановки диагноза гистопатологу, привыкшему видеть образцы биопсии этого типа, намного меньше, чем требуется тем, кто не привык к такой биопсии. Во многих случаях может быть достаточно нескольких коротких полосок эпителия эндометриального типа или одной или двух желез эндометриального типа. Вместо того, чтобы отклонять такие образцы как «неадекватные для гистологического диагноза», может быть полезно сделать такой комментарий, как «есть несколько полос явно неактивного эпителия эндометриального типа, но нет признаков, указывающих на гиперплазию или неоплазию».Тем не менее будет значительное количество экземпляров, которые действительно невозможно оценить. Они делятся на четыре категории: ткань не идентифицирована, ткань неадекватна для диагностики, эндометрий не идентифицирован и эндометрий неадекватен для диагностики. Данные показывают, что большинство пациентов, у которых биопсия дает минимальное количество ткани, имеют тонкий нормальный эндометрий с толщиной эндометрия не более 7 мм при гистероскопическом или ультразвуковом исследовании. Таким образом, гистопатолог может быть уверен в том, что там, где в полость эндометрия было введено небольшое количество ткани эндометрия или не было получено никакого материала, вероятность наличия важной патологии эндометрия очень мала. 19
Другие трудности, с которыми можно столкнуться при взятии проб по Пипелле, включают интерпретацию очаговых изменений извилистости желез и скученности поврежденных фрагментов эндометрия, которые являются предметом значительных артефактов биопсии. Это особенно верно в контексте секреторного эндометрия. Диагностика цитологической атипии слабой степени также может быть очень сложной. Несмотря на это, метод пипелля показал такую же точность, как обычная дилатация и кюретаж, в диагностике патологии эндометрия у женщин в пременопаузе и постменопаузе. 20 — 22
Гистология эндометрия у женщин на последовательной ЗГТ
Образцы эндометрия у женщин, получающих последовательную ЗГТ, могут показывать секреторные, пролиферативные или неактивные паттерны. Большинство образцов демонстрируют слабую секреторную активность, характеризующуюся только вакуолизацией цитоплазмы. Эти образцы обычно берутся во время прогестагенной фазы режима ЗГТ. Примерно 15% образцов демонстрируют пролиферативную активность, характеризуемую присутствием эпителиальных митотических фигур.Из них примерно половина принимается во время фазы прогестагена, а половина — во время фазы приема только эстрогена. Женщины, получающие прогестерон в течение девяти или более дней / цикла, демонстрируют значительно более низкую степень пролиферативной активности. 18 Небольшая часть (7–8%) покажет неактивный эндометрий. 23 , 24 Можно различать неактивный и атрофический эндометрий: все атрофические эндометрии неактивны, но неактивный эндометрий может не быть атрофическим.Атрофия эндометрия реже встречается у пациентов, получающих последовательную ЗГТ, чем у пациентов, получающих непрерывную комбинированную ЗГТ. С практической точки зрения различие между атрофическим и неактивным эндометрием не имеет клинического значения. Гиперплазия эндометрия также может возникать при последовательной ЗГТ, и ее распространенность обсуждается ниже.
Корреляция между типом кровотечений и гистологией эндометрия у пациентов, получающих последовательную ЗГТ
В клинической практике начало кровотечения в день или после 11 дня прогестероновой фазы часто рассматривается как подтверждение нормального эндометрия 25 и, наоборот, нерегулярное кровотечение часто рассматривается как признак патологии эндометрия.Однако реакция эндометрия на последовательную ЗГТ сильно различается, и классические гистологические критерии, используемые для физиологического датирования эндометрия в отношении кровотечения, не могут использоваться в контексте эндометрия, подвергнутого воздействию ЗГТ. 26 Многоцентровое исследование в Великобритании показало, что у большинства женщин кровотечение начинается примерно на 13 день после начала приема прогестагена, и что нет корреляции между гистологией эндометрия и временем начала кровотечения. 23 , 27 Что касается гиперплазии эндометрия, было обнаружено, что 37 из 65 женщин со сложной гиперплазией и четыре из восьми с атипией имели регулярные кровотечения после 11 дня. 23 Другое недавнее исследование характера кровотечений у женщин, получающих последовательную ЗГТ, обнаружило тенденцию к более позднему кровотечению отмены с секреторным эндометрием и более раннему кровотечению с неактивным или атрофическим эндометрием, но со слишком большим совпадением, чтобы это могло иметь клиническое значение. 28 Следовательно, невозможно предсказать гистологию эндометрия на основе характера кровотечений, а образцы кровотечений не могут идентифицировать те редкие случаи, когда последовательная ЗГТ не может защитить эндометрий от развития гиперплазии.Точно так же неожиданное кровотечение не обязательно указывает на патологию эндометрия.
Непрерывная комбинированная ЗГТ и эндометрий
Исследования показали, что непрерывная комбинированная ЗГТ вызывает атрофический эндометрий и устраняет кровотечение у большинства женщин в постменопаузе в течение 6–12 месяцев. 16 , 29 — 32 Известно, что постоянное присутствие прогестагена в режиме непрерывной комбинированной ЗГТ вызывает подавление рецепторов эстрогена и прогестагена, что, в свою очередь, снижает чувствительность к гормональной стимуляции. 33 Кроме того, прогестоген индуцирует 17-β-дегидрогеназу, которая превращает эстрадиол в менее активный эстрон, тем самым уменьшая эстрогенный стимул. 34 Неизвестно, какой из этих механизмов преобладает в развитии атрофии эндометрия у женщин в постменопаузе, получающих непрерывную комбинированную ЗГТ.
Ранние данные о непрерывной комбинированной ЗГТ также предполагали, что она может трансформировать гиперпластический эндометрий в состояние атрофии. Staland сообщил о 22 женщинах с гиперплазией эндометрия, у которых после шести месяцев лечения непрерывной комбинированной ЗГТ был обнаружен атрофический эндометрий. 35
В недавнем многоцентровом исследовании в Великобритании, которое является крупнейшим на сегодняшний день сообщением о гистологии эндометрия у женщин в постменопаузе, принимающих непрерывную комбинированную ЗГТ, образцы биопсии эндометрия оценивались после девяти месяцев непрерывной комбинированной ЗГТ в двух группах женщин: тех, кто ранее получал последовательную ЗГТ. ЗГТ и те, кто ранее не получал ЗГТ. 23 Женщинам с гиперплазией эндометрия без атипии было разрешено продолжить участие в исследовании и получать исследуемые препараты.В исследовании не сообщалось о случаях гиперплазии эндометрия: это подтверждает результаты предыдущих исследований с использованием непрерывной комбинированной ЗГТ. 5 , 32 , 36 — 38 Все женщины со сложной гиперплазией на последовательной ЗГТ вернулись к нормальному паттерну эндометрия после продолжительной комбинированной ЗГТ. Это подтверждает более ранние выводы Сталенда. 35 Случаев злокачественного новообразования эндометрия не зарегистрировано.
Биопсии после лечения в этом исследовании были «не поддающимися оценке» у 46% женщин, ранее не получавших лечения, и у 37% женщин, которые ранее получали последовательную ЗГТ.Это в целом подтверждает предыдущие исследования, которые показали, что более 50% биоптатов у женщин в постменопаузе, получающих непрерывную комбинированную ЗГТ, не поддаются оценке. 16 , 17 , 31 , 39 , 40 Те биопсии после лечения, которые можно было оценить, показали схожие черты в обеих группах: примерно половина показала атрофию, а половина — секреторные изменения низкой степени. Последние в основном проявлялись разной степенью вакуолизации цитоплазмы, что предположительно отражает одновременную стимуляцию эндометрия эстрогеном и прогестагеном по аналогии с ранней лютеиновой фазой.Псевдодецидуальные или менструальные изменения были редкими, и только 1,8% женщин, ранее не получавших лечения, и 2,3% женщин, ранее получавших последовательную ЗГТ, демонстрировали пролиферативную активность. И снова эти результаты подтверждают результаты предыдущего исследования, в котором пролиферативная активность была обнаружена у 3,6% женщин, принимавших прогестоген ежедневно в течение 24 месяцев. 38 Одним из возможных объяснений наличия пролиферативной активности в этих нескольких случаях является то, что относительная доза прогестагена могла быть недостаточной для полного подавления эстрогенной стимуляции эндометрия.С другой стороны, эндогенные факторы, такие как ожирение, могут способствовать стойкой стимуляции эндометрия, несмотря на непрерывную комбинированную ЗГТ.
Следовательно, значение этого исследования 23 состоит в том, что непрерывная комбинированная ЗГТ не связана с повышенным риском гиперплазии эндометрия или злокачественных новообразований и действительно может нормализовать эндометрий, демонстрирующий сложную гиперплазию до лечения. Это, в свою очередь, означает, что непрерывная комбинированная ЗГТ обеспечивает надежную степень безопасности эндометрия и подходит в качестве режима для длительного использования у женщин в постменопаузе.
ЗГТ и полипы эндометрия
Полипы эндометрия относительно часто встречаются у женщин, получающих ЗГТ. 41 — 43 Большинство из них возникает у женщин, получающих последовательную ЗГТ, и проявляет сходные черты с полипами эндометрия, обнаруживаемыми в общей женской популяции. Однако в одном исследовании сообщалось о более высокой распространенности гиперплазии полипов эндометрия у женщин, получающих ЗГТ, чем в контрольной группе: 41 , это говорит о том, что в случаях полипов у женщин, получающих ЗГТ, требуется тщательная гистологическая оценка.Гиперплазия полипов, ассоциированных с ЗГТ, встречается не так часто, как гиперплазия полипов, ассоциированных с тамоксифеном, а другие особенности, характерные для полипов, ассоциированных с тамоксифеном, такие как метаплазия и стромальный фиброз, реже наблюдаются у полипов от женщин, получающих ЗГТ. 42
Полипы эндометрия реже встречаются у женщин, получающих непрерывную комбинированную ЗГТ, но были зарегистрированы. 19 В редких случаях у женщин, сообщающих о прорывном кровотечении после достижения длительной аменореи на непрерывной комбинированной ЗГТ, обнаруживается полип эндометрия. 44 Однако такие случаи всегда требуют биопсии и гистологического исследования, поскольку аденокарцинома также может возникнуть. 44
ЗГТ и гиперплазия и неоплазия эндометрия
Прежде чем обсуждать ЗГТ и риск рака эндометрия, следует помнить о двух важных моментах. Во-первых, было ясно показано, что поражение эндометрия, связанное со значительным риском карциномы, является атипичной гиперплазией. 45 , 46 Морфологическим признаком предрака эндометрия является цитологическая атипия, хотя теперь признано, что поражение также имеет характерные архитектурные особенности, которые приравниваются к моноклональности. 47 Существует общепринятое мнение, что атипичная гиперплазия — это неопластический процесс, весьма отличный от истинной гиперплазии. Следовательно, рекомендуется использовать термин «внутриэпителиальная неоплазия эндометрия» или EIN. 48 В отличие от атипичной гиперплазии, можно утверждать, что истинная гиперплазия эндометрия представляет собой физиологический ответ эндометрия на избыток эстрогена и, следовательно, имеет низкий риск неопластической трансформации. Гистологические изменения, связанные с текущими диагнозами простой и сложной гиперплазии, просто отражают различные паттерны гиперпластической реакции эндометрия на избыток эстрогена, тогда как для развития предрака требуются другие, еще не идентифицированные, кофакторы.
Во-вторых, женщины в постменопаузе, которые представляют основную группу пациентов, принимающих ЗГТ, в силу своего возраста имеют фоновую распространенность (хотя и низкую) предрака и рака эндометрия, что необходимо учитывать при оценке рисков ЗГТ. В исследовании 801 бессимптомной женщины Archer и соавт. обнаружили распространенность гиперплазии эндометрия 5,2% и атипичной гиперплазии 0,6% с одним случаем рака эндометрия. 49 Korhonen et al оценили образцы биопсии эндометрия от 2964 женщин в перименопаузе и постменопаузе, которые были кандидатами на ЗГТ, и обнаружили 68.7% из них являются атрофическими, 23,5% пролиферативными, 0,5% секреторными и 0,6% гиперпластическими 50 ; 0,07% имели аденокарциному, а 6,6% не имели ткани для классификации. Авторы пришли к выводу, что низкий уровень карциномы эндометрия указывает на то, что биопсия не нужна перед началом ЗГТ у бессимптомных женщин.
НЕОБХОДИМЫЙ ЛЕЧЕНИЕ ЭСТРОГЕНАМИ
Связь между эндогенным гиперэстрогеном и гиперплазией эндометрия была зарегистрирована в 1940-х и 1950-х годах до введения лечения экзогенными эстрогенами. 51 — 53 Связь между лечением экзогенными эстрогенами и карциномой эндометрия была задокументирована в 1970-х годах и с тех пор неоднократно подтверждалась. 54 — 65 Сообщенный коэффициент риска карциномы эндометрия у женщин, принимающих эстроген в неограниченном количестве, варьировался от 2,3 65 до 10. 62 Риск увеличивается с увеличением суточной дозы и продолжительности лечения. 52 , 59 — 62 Риск сохраняется в течение многих лет после прекращения лечения эстрогенами. 56 , 61 , 64 Риск карциномы эндометрия, связанный с эстрогенами, выше у худых женщин, чем у женщин с избыточным весом, что означает, что экзогенные эстрогены оказывают аддитивное (а не мультипликативное) влияние на канцерогенез эндометрия, и предполагают существование верхнего порога риска или наличия некоторого ограничивающего фактора (например, рецепторов половых гормонов), который препятствует продолжающейся эффективности комбинированного эстрогенного стимула ожирения и экзогенного эстрогена сверх определенного уровня. 66 Данные также предполагают, что риск рака эндометрия снижается среди женщин, которые использовали оральные контрацептивы. 63 , 66 Может оказаться, что использование оральных контрацептивов снижает восприимчивость эндометрия к гормональному канцерогенезу.
Исследования неоднократно показывали, что существует связь между безальтернативным лечением эстрогенами и гиперплазией эндометрия, 2 — 5 , 67 , 68 , а некоторые показали связь между дозой эстрогена. и распространенность гиперплазии. 2 — 4 «Исследование постменопаузального эстроген / прогестинового вмешательства (PEPI)» было большим проспективным, рандомизированным, двойным слепым исследованием, которое показало, что женщины, получавшие только эстроген (конъюгированный конский эстроген 0,625 мг), были значительно с большей вероятностью разовьется простая (27,7%), сложная (22,7%) или атипичная гиперплазия (11,7%), чем у пациентов, получавших плацебо (простая 0,8%, сложная 0,8%, атипичная 0%; p <0,001). 67 Это исследование продемонстрировало необходимость в базовых и ежегодных образцах биопсии эндометрия при использовании высоких доз эстрогена без сопротивления, такого как этот.
ПОСЛЕДОВАТЕЛЬНАЯ HRT
Хорошо известно, что добавление прогестагена к схеме ЗГТ существенно снижает риск рака эндометрия. 3 , 5 , 7 , 8 , 67 , 69 Хотя в некоторых исследованиях не сообщалось о существенных различиях в частоте рака эндометрия среди женщин, принимающих комбинированная ЗГТ по сравнению с женщинами, не принимающими ЗГТ, 6 — 8 , 64 Недавние исследования показали, что циклическое добавление прогестагена к ЗГТ не устраняет полностью риск.Beresford и др. обнаружили, что относительный риск рака эндометрия у женщин, использующих последовательный комбинированный режим эстрогена и не менее 10 дней прогестагена, составил 1,3 (доверительный интервал (ДИ) от 0,8 до 2,2), увеличиваясь до 2,5 (ДИ, 1,1. до 5,5) при пяти или более годах использования по сравнению с отношением шансов 1,0 для женщин, которые никогда не принимали гормоны. 9 Это исследование также показало, что менее 10 дней прогестагена на цикл дают относительный риск 3,1 (ДИ от 1,17 до 5,7), а при использовании в течение пяти и более лет относительный риск равен 3.7 (CI от 1,7 до 8,2). Weiderpass и др. обнаружили, что у женщин, получавших последовательный комбинированный режим эстрогена и прогестагена менее 16 дней в течение пяти или более лет, относительный риск карциномы составлял 1,6 по сравнению с контрольной группой. 70 Pike et al. не обнаружили значительного увеличения риска карциномы у женщин, получающих комбинированную и последовательную ЗГТ, последнюю с 10 или более днями прогестагена / цикл; однако у женщин, получающих последовательную ЗГТ с прогестагеном менее 10 дней / цикл, был обнаружен повышенный риск карциномы такой же степени, что и у женщин, принимающих эстроген без сопротивления. 10
Исследование PEPI показало, что у женщин, получающих последовательную ЗГТ, наблюдалась тенденция к развитию гиперплазии (простая 3,4%, сложная 1,7%, атипичная 0%), но цифры были небольшими, а различия между схемами не были значительными. 67 В исследовании PEPI также сообщается, что из 36 женщин, у которых во время исследования развилась гиперплазия, вызванная эстрогеном, у 34 нормализовалось состояние после прекращения приема эстрогена и введения прогестагена.
В многоцентровом исследовании Великобритании данные биопсии эндометрия были получены для женщин, получавших последовательную ЗГТ в течение средней продолжительности 2 раза.5 лет (диапазон от 1 до 6 лет). 23 Сложная гиперплазия обнаружена у 5,4%, атипическая гиперплазия — у 0,7%. Возможно, что эти цифры, которые выше, чем сообщалось ранее, могут отражать продолжительность исследования, в котором средняя продолжительность лечения была больше, чем в предыдущих исследованиях. Случаев рака эндометрия не было. Большинство (76,8%) биопсий, показывающих гиперплазию, были взяты во время фазы прогестагена цикла лечения, тогда как 17,8% были взяты во время лечения только эстрогеном.Не было значительных различий в распространенности гиперплазии между схемами, содержащими 10 или 12 дней прогестагена. Было обнаружено, что гиперплазия значительно чаще встречается при схемах, содержащих левоноргестрел, чем при схемах, содержащих ацетат норэтистерона (7,3% против 4,2%). Гиперплазия также более распространена при более низких дозах прогестагена, чем при лечении более высокими дозами. Эти результаты предполагают, что риск гиперплазии эндометрия может быть увеличен у женщин, получавших последовательную ЗГТ, содержащую более низкие дозы прогестагена.
В целом аналогичные результаты были получены в более недавнем исследовании, в котором сравнивали длительный цикл (три месяца) последовательного режима ЗГТ с месячным циклом, при котором прогестаген вводился в течение 10 дней в каждом цикле: была более высокая частота гиперплазии и по одному случаю каждого атипичной гиперплазии и карциномы в группе длительного цикла по сравнению с группой месячного цикла. Кроме того, в группе с длительным циклом кровотечения была более нерегулярная и, соответственно, более высокий процент выбываний. 71
КОМБИНИРОВАННАЯ НЕПРЕРЫВНАЯ HRT
О карциноме эндометрия редко сообщалось у женщин, принимавших непрерывные комбинированные схемы ЗГТ. 44 , 72 — 75 Однако в большинстве случаев у женщин в анамнезе был беспрепятственный прием эстрогена или последовательная ЗГТ с менее чем 10-дневным приемом гестагена или факторы риска, такие как семейный анамнез карцинома эндометрия. 44 , 72 Как обсуждалось выше, крупнейшее на сегодняшний день исследование гистологии эндометрия у женщин в постменопаузе, получавших непрерывную комбинированную ЗГТ, не показало случаев гиперплазии эндометрия или злокачественных новообразований с атрофическим эндометрием, индуцированным более чем у двух третей женщин во время девятимесячный период лечения. 23 Все женщины со сложной гиперплазией на последовательной ЗГТ, завершившие исследование, вернулись к негиперпластическому типу эндометрия.
За три года исследования PEPI не было зарегистрировано случаев сложной гиперплазии у женщин, получавших непрерывную комбинированную ЗГТ, по сравнению с 1,7% из 118 женщин, получавших последовательную ЗГТ, и 0,8% из 119 женщин, получавших плацебо. 67 Еще одно недавнее исследование непрерывной комбинированной ЗГТ в течение двухлетнего периода не выявило случаев гиперплазии эндометрия, 38 , подтверждающих результаты более ранних исследований. 5 , 32 , 36 , 37
Выводы
Большинство биопсий эндометрия, взятых у женщин на последовательной ЗГТ, показывают слабые секреторные функции, а меньшинство — пролиферативный или неактивный эндометрий.
Многие (до 50%) биопсии женщин, получающих непрерывную комбинированную ЗГТ, содержат минимальное количество ткани для исследования. Примерно 50% более значительных биопсий показывают атрофию эндометрия и примерно 50% показывают слабые секреторные особенности.
Если взят образец из полости матки, биопсия с минимальным содержанием ткани эндометрия или без нее у женщины в постменопаузе, получающей ЗГТ, является подтверждением отсутствия клинически значимой патологии эндометрия.
Нет корреляции между кровотечением при ЗГТ и гистологией эндометрия.
Эстроген без противодействия вызывает гиперплазию эндометрия примерно у 20% женщин после одного года лечения. Относительный риск карциномы составляет два-три.
Сочетание прогестагена с эстрогеном существенно снижает риск атипичной гиперплазии эндометрия и аденокарциномы.
Последовательная ЗГТ связана с низким риском гиперплазии эндометрия и атипичной гиперплазии (примерно 1% для атипичной гиперплазии). Режимы, содержащие прогестаген менее 10 дней или более низкие дозы прогестагена, могут повышать риск гиперплазии, атипичной гиперплазии и аденокарциномы.
Непрерывная комбинированная ЗГТ не связана с развитием гиперплазии эндометрия или злокачественных новообразований.
Вероятность того, что гистопатолог обнаружит клинически значимую патологию в биопсии эндометрия у женщины, принимающей ЗГТ, невысока и, скорее всего, будет проявлением ранее существовавшего заболевания.
Каталожные номера
- ↵
Берал В., Бэнкс Э., Ривз Г., и др. . Использование ЗГТ и последующий риск рака. J. Epidemiol Biostat 1999; 4: 191–210.
- ↵
Whitehead MI, King RJB, McQueen J, и др. .Гистология и биохимия эндометрия у женщин в климактерическом периоде во время терапии эстрогенами и прогестагенами. JR Soc Med 1979; 72: 322–7.
- ↵
Paterson MEL, Wade-Evans T, Sturdee DW, и др. . Заболевания эндометрия после лечения эстрогенами и прогестагенами в климактерическом периоде. BMJ 1980; 280: 822–4.
- ↵
Гельфанд М.М., Ференци А. Проспективное 1-летнее исследование эстрогена и прогестина у женщин в постменопаузе: влияние на эндометрий.Акушер Гинекол 1989; 74: 398–402.
- ↵
Woodruff JD, Pickar JH, для исследовательской группы по менопаузе. Частота гиперплазии эндометрия у женщин в постменопаузе, принимающих конъюгированные эстрогены (премарин) с медроксипрогестерона ацетатом или только конъюгированные эстрогены. Am J Obstet Gynecol 1994; 170: 1213–23.
- ↵
Hammond CB, Jelovsek FR, Lee KL, и др. . Эффекты длительной заместительной терапии эстрогенами.II. Неоплазия. Am J Obstet Gynecol 1979; 133: 537–47.
- ↵
Перссон И., Адами Х.О., Бергквист Л., и др. . Риск рака эндометрия после лечения только эстрогенами или в сочетании с прогестагенами: результаты проспективного исследования. BMJ 1989; 298: 147–51.
- ↵
Войт Л.Ф., Вайс Н.С., Чу Дж., и др. . Прогестагенные добавки экзогенных эстрогенов и риск рака эндометрия.Ланцет 1991; 338: 274–7.
- ↵
Beresford SAA, Weiss NS, Voight LF, и др. . Риск рака эндометрия по отношению к эстрогену в сочетании с циклической прогестагенной терапией у женщин в постменопаузе. Lancet 1997; 349: 458–61.
- ↵
Pike MC, Петерс РК, Козен В., и др. . Заместительная эстроген-прогестиновая терапия и рак эндометрия. J Natl Cancer Inst 1997; 89: 1110–16.
- ↵
Уайтхед М.И., Хиллард Т.С., Крук Д. Роль и использование прогестагенов. Obstet Gynecol 1990; 75: 59S – 76S.
- ↵
Боярышник RJS, Споварт К., Уолш Д., и др. . Состояние эндометрия у женщин, находящихся на длительной непрерывной комбинированной заместительной гормональной терапии. Br J Obstet Gynaecol 1991; 98: 939–42.
- ↵
Hillard TC, Siddle NC, Whitehead MI.Непрерывная комбинированная конъюгированная эстроген-прогестагенная терапия лошадей: влияние медроксипрогестерона ацетата и норэтиндрона на характер кровотечений и гистологический диагноз эндометрия. Am J Obstet Gynecol 1992; 167: 1–7.
- ↵
Барентсен Р., Гроеневельд Ф. П., Бареман Ф. П., и др. . Мнение женщин о кровотечении отмены при заместительной гормональной терапии. Eur J Obstet Gynecol Reprod Biol 1993; 51: 203–7.
Хан РГ.Соображения относительно соответствия заместительной терапии эстрогенами: кровотечение отмены и другие факторы. Am J Obstet Gynecol 1989; 161: 1854–8.
- ↵
Равникар В.А. Препятствия на пути к длительной заместительной гормональной терапии: почему женщины не соблюдают терапию? Европейский журнал менопаузы 1996; 3 (приложение 2): 90–3.
- ↵
Рис М. О менструальных кровотечениях при заместительной гормональной терапии. Ланцет 1994; 343: 250.
- ↵
Мойер Д.Л., де Линьер Б., Дригес П., и др. . Профилактика гиперплазии эндометрия прогестероном при длительной замене эстрадиола: влияние характера кровотечения и секреторных изменений. Fertil Steril 1993; 59: 992–7.
- ↵
Пьегса К., Колдер А., Дэвис Дж. А., и др. . Состояние эндометрия у женщин в постменопаузе, получающих длительную непрерывную комбинированную заместительную гормональную терапию (Клиофем).Сравнительное исследование биопсии эндометрия, амбулаторной гистероскопии и трансвагинального УЗИ. Eur J Obstet Gynecol Reprod Biol 1997; 72: 175–80.
- ↵
Стовалл Т.Г., Photopulos GJ, Постон В.М., и др. . Отбор образцов пипелля у пациентов с известной карциномой эндометрия. Obstet Gynecol 1991; 77: 954–6.
Fothergill DJ, Brown VA, Hill AS. Гистологический забор эндометрия: сравнение формального кюретажа и пробоотборника Pipelle.Br J Obstet Gynaecol 1992; 99: 779–80.
- ↵
Батул Т., Реджинальд П. В., Хьюз Дж. Х. Амбулаторная биопсия эндометрия Пипелле при исследовании кровотечения в постменопаузе. Br J Obstet Gynaecol 1994; 101: 545–6.
- ↵
Стурди Д.В., Ульрих Л.Г., Барлоу Д.Х., и др. . Ответ эндометрия на последовательную и непрерывную комбинированную заместительную терапию эстрогенами и прогестагенами. Br J Obstet Gynaecol 2000; 107: 1392–400.
- ↵
Archer DF, Pickar JH, Bottiglioni F. Характер кровотечения у женщин в постменопаузе, принимающих непрерывные комбинированные или последовательные схемы конъюгированных эстрогенов с медроксипрогестерона ацетатом. Obstet Gynecol 1994; 83: 686–92.
- ↵
Padwick ML, Pryse-Davies J, Whitehead MI. Простой метод определения оптимальной дозы прогестина у женщин в постменопаузе, получающих эстрогены.N Engl J Med 1986; 315: 930–4.
- ↵
Хабиба М.А., Белл С.К., Аль-Аззави Ф. Реакции эндометрия на заместительную гормональную терапию: гистологические особенности по сравнению с таковыми эндометрия в поздней лютеиновой фазе. Hum Reprod 1998; 13: 1674–82.
- ↵
Стерди Д.В., Барлоу Д.Х., Ульрих Л.Г., и др. . Является ли время кровотечения отмены критерием безопасности для эндометрия при последовательной заместительной эстроген-прогестагенной терапии? Ланцет 1994; 344: 979–82.
- ↵
Burch D, Bieshuevel E, Smith S, et al. Можно ли сделать вывод о защите эндометрия по структуре кровотечений при комбинированной циклической заместительной гормональной терапии. Maturitas 2000; 34: 155–60.
- ↵
Obel EB, Munk-Jensen N, Svenstrup B, и др. . Двухлетнее двойное слепое контролируемое исследование клинического эффекта комбинированной и последовательной заместительной терапии в постменопаузе и метаболизма стероидов во время лечения.Maturitas 1993; 16: 13–21.
Mattsson LÅ, Culberg G, Samsioe G. Оценка непрерывного режима эстроген-прогестагена при климактерических жалобах. Maturitas 1982; 4: 95–102.
- ↵
Sporrong T, Hellgren M, Samsioe G, и др. . Сравнение четырех непрерывно вводимых комбинаций прогестагенов и эстрадиола при климактерических жалобах. Br J Obstet Gynaecol 1988; 95: 1042–8.
- ↵
Staland B. Непрерывное лечение комбинацией эстрогена и гестагена — способ избежать стимуляции эндометрия. Клинический опыт применения Kliogest ™ . Acta Obstet Gynaecol Scand Suppl 1985; 130: 29–35.
- ↵
King RJB, Уайтхед М.И., Кэмпбелл С., и др. . Биохимические исследования эндометрия у женщин в постменопаузе, получающих заместительную гормональную терапию.Postgrad Med J 1978; 54: 65–8.
- ↵
Каспер РФ. Регулирование рецепторов эстроген-прогестагена в эндометрии. Int J Fertil Menopausal Stud 1996; 23: 31–9.
- ↵
Staland B. Постоянное лечение натуральными эстрогенами и прогестагенами. Способ избежать стимуляции эндометрия. Maturitas 1981; 3: 145–56.
- ↵
Udoff L, Langenberg P, Adashi EY.Комбинированная непрерывная заместительная гормональная терапия: критический обзор. Obstet Gynecol 1995; 86: 306–16.
- ↵
Stadberg E, Mattson LÅ, Uvebrant M. 17 β-эстрадиол и норэтистерона ацетат в низких дозах в качестве непрерывной комбинированной заместительной гормональной терапии. Maturitas 1996; 23: 31–9.
- ↵
Nand SL, Webster MA, Baber R, и др. , для исследовательской группы Огена / Провера. Характер кровотечения и изменения эндометрия при продолжительной комбинированной заместительной гормональной терапии.Obstet Gynecol 1998; 91: 678–84.
- ↵
Weinstein L, Bewtra C, Gallagher C. Оценка непрерывного комбинированного режима низких доз эстрогена и прогестина для лечения пациентов в менопаузе. Am J Obstet Gynecol 1990; 162: 1534–42.
- ↵
Spowart KJM, Walsh DJ, Hawthorn RJS, и др. . Гистероскопическая оценка эффектов непрерывного комбинированного режима эстроген-прогестагена на эндометрий женщин в постменопаузе.Гинекологическая эндоскопия 1992; 1: 33–5.
- ↵
Орвието Р., Бар-Хава I, Дикер Д., и др. . Полипы эндометрия при климаксе: характеристика и значение. Acta Obstet Gynecol Scand 1999; 78: 883–6.
- ↵
Кеннеди М.М., Бейгри К.Ф., Манек С. Тамоксифен и эндометрий: обзор 102 случаев и сравнение с патологией эндометрия, связанной и не связанной с ЗГТ. Int J Gynecol Pathol 1999; 18: 130–7.
- ↵
Майя Х., младший, Барбоза И.С., Маркес Д., и др. . Гистероскопия и трансвагинальная сонография у женщин в менопаузе, получающих заместительную гормональную терапию. J Am Assoc Gynecol Laparosc 1996; 4: 13–18.
- ↵
Кожа AT, Savvas M, шип JW. Гистология эндометрия и характер кровотечений после 8 лет непрерывной комбинированной терапии эстрогенами и прогестагенами у женщин в постменопаузе. Obstet Gynecol 1991; 78; 1008–10.
- ↵
Курман Р.Дж. Поведение при гиперплазии эндометрия. Долгосрочное исследование «нелеченой» гиперплазии у 170 пациентов. Рак 1985; 56: 403–12.
- ↵
Ференци А., Гельфанд М. Биологическое значение цитологической атипии при гиперплазии эндометрия, обработанной прогестагеном. Am J Obstet Gynecol 1989; 160: 126–31.
- ↵
Mutter GL, Baak JPA, Crum CP, и др. .Диагностика предрака эндометрия с помощью гистопатологии, клонального анализа и компьютерной морфометрии. Дж. Патол, 2000; 190: 462–9.
- ↵
Mutter GL. Внутриэпителиальная неоплазия эндометрия (ЭИН): внесет ли порядок в хаос? Коллективная группа эндометрия. Гинеколь Онкол 2000; 76: 287–90.
- ↵
Арчер Д.Ф., Макинтайр-Селтман К., Уилборн В.В., и др. . Морфология эндометрия у бессимптомных женщин в постменопаузе.Am J Obstet Gynecol 1991; 165: 317–22.
- ↵
Корхонен МО, Саймонс Дж. П., Хайд Б.М., и др. . Гистологическая классификация и патологические данные образцов биопсии эндометрия, полученных от 2964 женщин в перименопаузе и постменопаузе, получающих непрерывное гормональное лечение в качестве заместительной терапии (исследование CHART2). Am J Obstet Gynecol 1997; 176: 377–80.
- ↵
Gusberg SB. Предшественники карциномы тела.Эстрогены и аденоматозная гиперплазия. Am J Obstet Gynecol 1947; 54: 905–27.
- ↵
Mansell H, Hertig AT. Гранулезно-тека-клеточные опухоли и карцинома эндометрия: исследование их взаимосвязи и обзор 80 случаев. Obstet Gynecol 1955; 6: 385–94.
- ↵
Джексон Р.Л., Докерти, МБ. Синдром Штейна Левенталя: анализ 43 случаев с особым упором на связь с карциномой эндометрия.Am J Obstet Gynecol 1957; 73: 161–73.
- ↵
Смит, округ Колумбия, Прентис Р., Томпсон Д. Д., и другие, . Ассоциация экзогенного эстрогена и карциномы эндометрия. N Engl J Med 1975; 293: 1164–7.
Ziel HK, Finkle WD. Повышенный риск рака эндометрия среди пользователей конъюгированных эстрогенов. N Engl J Med 1975; 293: 1167–70.
- ↵
Mack TM, Pike MC, Henderson BE, и др. .Эстрогены и рак эндометрия в пенсионном сообществе. N Engl J Med 1976; 294: 1262–1267.
Weiss NS, Szekely DR, Austin DF. Рост заболеваемости раком эндометрия в США. N Engl J Med 1976; 294: 1259–62.
Antunes CMF, Stolley, Rosenheim NB, и др. . Рак эндометрия и использование эстрогенов. Отчет о большом исследовании методом случай-контроль. N Engl J Med 1979; 300: 9–13.
- ↵
Шапиро С., Кауфман Д.В., Слоан Д., и др. . Недавнее и прошлое использование конъюгированных эстрогенов в отношении аденокарциномы эндометрия. N Engl J Med 1980; 303: 485–9.
Spengler RF, Clarke RA, Woolever CA, и др. . Экзогенные эстрогены и рак эндометрия: исследование случай-контроль и оценка потенциальных предубеждений. Am J Epidemiol 1981; 114: 497–506.
- ↵
Шапиро С., Келли Дж. П., Розенберг Л., и др. . Риск локализованного и широко распространенного рака эндометрия в связи с недавним или прекращенным использованием конъюгированных эстрогенов. N Engl J Med 1985; 313: 969–72.
- ↵
Паганини-Хилл А, Росс РК, Хендерсон Б.Е. Рак эндометрия и схемы заместительной терапии эстрогенами. Br J Cancer 1989; 59: 445–7.
- ↵
Rubin GL, Peterson HB, Lee NC, и др. .Заместительная терапия эстрогенами и риск рака эндометрия: остаются противоречиями. Am J Obstet Gynecol 1990; 162: 148–54.
- ↵
Бринтон Л.А., Гувер Р.Н. и совместная группа по раку эндометрия. Заместительная терапия эстрогенами и риск рака эндометрия: нерешенные вопросы. Obstet Gynecol 1993; 81: 265–71.
- ↵
Гради Д., Гебрестсадик Т., Керликовске К., и др. .Заместительная гормональная терапия и риск рака эндометрия: метаанализ. Obstet Gynecol 1995; 85: 304–13.
- ↵
Леви Ф, Ла Веккья С, Гули С, и др. . Заместительная терапия эстрогенами и риск рака эндометрия: оценка роли ковариат. Eur J Cancer 1993; 29A: 1445–9.
- ↵
Группа разработчиков исследования PEPI 1996. Влияние заместительной гормональной терапии на гистологию эндометрия у женщин в постменопаузе.Исследование постменопаузальных эстроген-прогестиновых вмешательств (PEPI). JAMA 1996; 275: 370–5.
- ↵
Кушинг К.Л., Вайс Н.С., Войт Л.Ф., и др. . Риск рака эндометрия в связи с использованием низких доз эстрогенов без сопротивления. Obstet Gynecol 1998; 91: 35–9.
- ↵
Persson I, Yuen J, Bergkvist L, и др. . Заболеваемость раком и смертность у женщин, получающих заместительную терапию эстрогенами и эстроген-прогестинами — долгосрочное наблюдение в шведской когорте.Int J Cancer 1996; 67: 327–32.
- ↵
Weiderpass E, Adami HO, Baron JA, et al. Риск рака эндометрия после замещения эстрогенов с прогестинами и без них. J Natl Cancer Inst 1999; 91: 1131–7.
- ↵
Бьярнасон К., Церин А., Линдгрен Р., и др. . Побочные эффекты на эндометрий при заместительной гормональной терапии длительного цикла. Скандинавская группа по изучению длинного цикла.Maturitas 1999; 32: 161–70.
- ↵
МакГонигл К.Ф., Карлан Б.А., Барбуто Д.А., и др. . Развитие рака эндометрия у женщин, получающих заместительную терапию эстрогенами и прогестиновыми гормонами. Gynecol Oncol 1994; 55: 126–32.
Дёрен М., Шнайдер HPG. Долгосрочное соблюдение режима непрерывной комбинированной заместительной терапии эстрогенами и прогестагенами у женщин в постменопаузе. Maturitas 1996; 25: 99–105.
Comerci JT, Fields AL, Runowicz CD, и др. . Непрерывная заместительная гормональная терапия низкими дозами и риск рака эндометрия. Гинеколь Онкол 1997; 64: 425–30.
- ↵
Ульрих LG. Накопленные знания по аспектам безопасности Kliogest ™ . Br J Obstet Gynaecol 1996; 103: 99–103.
Гиперплазия эндометрия | Симптомы, причины и лечение
После постановки диагноза гиперплазия эндометрия важно найти врача, который обсудит все доступные вам варианты.
Врачи Центра инновационной гинекологической помощи ® (CIGC ® ) являются специалистами в области малоинвазивной гинекологической хирургии. Пациентам с диагнозом гиперплазия без атипии, которым требуется нехирургическое лечение, предлагаются лучшие доступные медицинские решения. С ними обращаются так же тщательно и целенаправленно, как и с пациентами с диагнозом гиперплазия с атипией, которым требуется хирургическое вмешательство.
Врачи CIGC — это специалисты по лапароскопической хирургии, посвятившие свою карьеру минимально инвазивному уходу за гинекологами.Кроме того, наша приверженность гинекологической хирургии означает, что мы работали с большим количеством случаев, более трудными случаями и использовали передовые методы и процедуры, полученные во время обширных учебных занятий. Мы стремимся выполнять даже самые сложные операции с низким уровнем осложнений.
Если вам действительно требуется гистерэктомия по поводу гиперплазии эндометрия, вы должны знать, что уход за гинекологами — единственное лекарство, которое практикуют хирургические специалисты CIGC. Мы сотрудничаем с OBGYN, чтобы обеспечить пациентам наилучший уход.Увеличение хирургического объема важно для развития и поддержания хирургического опыта.
Хирурги CIGC не проводят открытую гистерэктомию пациентам с гиперплазией эндометрия. Известно, что открытые операции болезненны, сопряжены с относительно высоким риском осложнений и имеют длительный период восстановления. Хирурги CIGC также не проводят роботизированные операции. Операции, в которых процедура выполняется с помощью робототехники, чрезвычайно дороги и имеют высокий риск осложнений.
Специалисты, не являющиеся акушерами-гинекологами
Ваш акушер-гинеколог может быть хорошим врачом, но акушер-терапевт — это универсал, а не хирург.Большая часть практики акушерства посвящена акушерской помощи, поэтому ваш врач не набирает достаточно пациентов или практики, чтобы изучить лучшие хирургические методы. В среднем акушер-гинеколог выполняет от 10 до 15 гистерэктомий в год, в то время как наши хирурги в среднем 400 в год. Поскольку для развития и поддержания хирургического опыта необходим тяжелый объем операции, легко понять, почему вам следует обратиться к хирургу CIGC для операции по поводу гиперплазии эндометрия.
В CIGC наши хирурги по лечению гиперплазии эндометрия выполняют большее количество случаев, рассматривают более широкий спектр типов случаев и проходят комплексное обучение передовым лапароскопическим методам.Независимо от того, переносите ли вы радикальную операцию или консервативную операцию по поводу гиперплазии эндометрия, когда вы ее делаете в CIGC, вы знаете, что работаете со специалистами, которые сосредоточены только на этом типе процедуры.
Используя передовую технику DualPortGYN ® , процедуры CIGC оставляют вам минимальные косметические рубцы, более короткий период восстановления, составляющий всего несколько дней, и более низкий риск осложнений.


 Д., Карева Е. Н., Горенкова О. С. и др. Оптимизация гормональной противорецидивной терапии гиперпластических процессов в эндометрии у женщин позднего репродуктивного возраста // Рос. вестн. акуш.-гин. 2007; № 5: 31–35.
Д., Карева Е. Н., Горенкова О. С. и др. Оптимизация гормональной противорецидивной терапии гиперпластических процессов в эндометрии у женщин позднего репродуктивного возраста // Рос. вестн. акуш.-гин. 2007; № 5: 31–35. В., Лысенко О. Н. и др. Роль половых гормонов и их рецепторного аппарата при выборе методов лечения у пациенток с гиперпластическими процессами эндометрия в сочетании с миомой матки // Акуш. и гин. 1998; № 3: 30–33.
В., Лысенко О. Н. и др. Роль половых гормонов и их рецепторного аппарата при выборе методов лечения у пациенток с гиперпластическими процессами эндометрия в сочетании с миомой матки // Акуш. и гин. 1998; № 3: 30–33. -2005.-Vol.7 (5).-P.598-604.
-2005.-Vol.7 (5).-P.598-604.