Клиническая больница | Гиперплазия эндометрия
Гиперпластические процессы эндометрияГиперплазия – увеличение числа клеток в какой-либо ткани (за исключением опухолевой) или органе, в результате чего увеличивается объем данного анатомического образования или органа.
Гистологически (по клеточному составу) выделяются несколько типов:
- железистая гиперплазия эндометрия
- железисто-кистозная гиперплазия
- атипическая гиперплазия эндометрия (синоним – аденоматоз, аденоматозная гиперплазия)
- полипы эндометрия
По мнению большинства авторов, первые два типа гиперплазии не являются предраковым заболеванием. Третий тип – атипическая гиперплазия, является предраковым заболеванием. При её наличии угроза перерождения в злокачественную опухоль (рак эндометрия) при отсутствии терапии составляет от 1 до 14% и наиболее часто наблюдается в период менопаузы ( прекращения менструальной функции по возрасту).
Предраковые гиперпластические процессы переходят в рак эндометрия примерно у 10% больных (по данным разных авторов, от 2 до 50%), они нередко длительно персистируют, иногда подвергаются обратному развитию. Однако с учетом реальной угрозы перехода процесса в рак эндометрия необходимо внимательнейшее отношение врача к больным с аденоматозом эндометрия и аденоматозными полипами.
Существуют мнения о возможности считать предраком эндометрия железистую гиперплазию и гиперпластические процессы, которые возникают вновь (рецидивируют) после выскабливания эндометрия или не поддаются гормонотерапии. Риск малигнизации (озлокачествления) гиперпластических процессов возрастает при метаболических нарушениях, обусловленных экстрагенитальным заболеванием (ожирение, нарушение углеводного и липидного обмена, расстройства функций гепатобилиарной системы и желудочно-кишечного тракта), сопутствующим развитию патологии эндометрия.
Локальная, ограниченная форма гиперплазии эндометрия называется полипом эндометрия. Гистологически они так же подразделяются на несколько видов в зависимости от клеток, которые преобладают в их строении: железистые; железисто-фиброзные и фиброзные полипы.
Гистологически они так же подразделяются на несколько видов в зависимости от клеток, которые преобладают в их строении: железистые; железисто-фиброзные и фиброзные полипы.
Причина и механизм развития заболевания
Факторами риска возникновения данной патологии являются:
- Возникновению гиперпластических процессов в эндометрии способствуют наследственная отягощенность (миома матки, рак половых органов и молочной железы, гипертоническая болезнь и другие заболевания), повреждающие воздействия в период внутриутробной жизни, заболевания в период полового созревания и сопряженные с ними расстройства менструальной и впоследствии репродуктивной функции. У женщин зрелого возраста появлению гиперпластических процессов часто предшествуют гинекологические заболевания, оперативные вмешательства на половых органах.
- Гиперпластическим процессам эндометрия нередко сопутствуют ожирение, гипертоническая болезнь, гипергликемия (указанная триада признаков особенно часто сочетается с атипическими и гиперпластическими процессами, признанными как предрак эндометрия), миома матки, мастопатия, эидометриоз, являющиеся в значительной мере гормонально-зависимыми заболеваниями, а также расстройства функций печени, ответственной за метаболизм гормонов.

Клиническая картина
В клинической картине патологии чаще всего отмечаются следующие симптомы
- Маточные кровотечения, возникающие после задержки очередной менструации. Они могут быть как продолжительными по длительности с умеренной кровопотерей, так и короткими по времени, но обильными.
- Кровянистые межменструальные выделения.
- Первичное или вторичное бесплодие, в основе которого лежит процесс отсутствия формирования нормальной яйцеклетки.
- Самым частым, почти постоянным симптомом полипов эндометрия являются нарушения менструального цикла. При полипах на фоне нормального функционирующего эндометрия у женщин репродуктивного возраста отмечаются скудные межменструальные и предменструальные сукровичные выделения при сохраненном менструальном цикле, а также увеличение менструальной кровопотери.

- У женщин репродуктивного возраста железисто-фиброзные и фиброзные полипы могут явиться причиной меноррагий. При ановуляторных циклах и наличии полипов железистого строения на фоне гиперпластических процессов эндометрия отмечаются метроррагии, причиной которых являются скорее не полипы, а дистрофические, некротические изменения в эндометрии и гормональные нарушения. Подобные клинические проявления более характерны для женщин пременопаузального возраста (после 45 лет).
Диагностика
- УЗИ с применением трансвагинального датчика;
- С целью диагностики широко используют диагностическое выскабливание слизистой оболочки тела матки и последующее гистологическое исследование полученного материала.
Выскабливание эндометрия рекомендуется производить накануне ожидаемой менструации или в самом начале появления кровянистых выделений. При этом необходимо удалить всю слизистую оболочку, включая область дна матки и маточных трубных углов, где нередко располагаются очаги аденоматоза и полипы.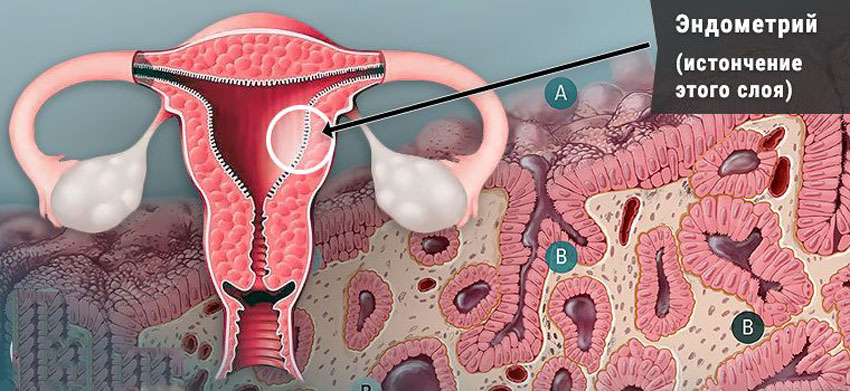 С этой целью выскабливание эндометрия производят под контролем гистероскопии. Удаленную слизистую оболочку направляют на гистологическое исследование.
С этой целью выскабливание эндометрия производят под контролем гистероскопии. Удаленную слизистую оболочку направляют на гистологическое исследование.
Наиболее информативным методом является гистероскопия, которая позволяет не только диагностировать полипы эндометрия с высокой степенью точности, но и прицельно их удалять, проводить контроль за ложем полипа после его удаления. При гистероскопии полипы имеют продолговатую или округлую форму, бледно-розовую, желтоватую или темно-багровую (нарушение кровообращения) окраску. Полипы бывают единичными или множественными, нередко располагаются в области дна или трубных углов матки и в отличие от неподвижных миоматозных узлов колеблются в струе промывной жидкости.
Для клиницистов представляют интерес так называемые рецидивирующие полипы эндометрия. С внедрением контрольной гистероскопии после выскабливания и удаления полипов сложилось твердое убеждение, что «рецидивом» являются неудаленные части полипов.

Следует особо отметить, что раздельное (отдельно – цервикальный канал, отдельно – полость матки) выскабливание слизистой матки является первым этапом лечения гиперпластического процесса эндометрия. Он позволяет получить образец ткани эндометрия и поставить точный диагноз: какая именно гиперплазия, нет ли предраковых изменений. От этого зависит дальнейшее лечение. Убрать измененный эндометрий можно только механически.
Лечение
Лечение гиперпластических процессов эндометрия проводится с учетом многочисленных факторов – возраста больной, причин гиперплазии и характера этой патологии, клинических проявлений, противопоказаний к тому или иному методу лечения, переносимости лечебных препаратов, сопутствующих экстрагенитальных и гинекологических заболеваний. Основное лечение – гормональное (подбирается индивидуально). При назначении гормонотерапии требуется соблюдение определенных условий и строгого учета противопоказаний. Через 3 и 6 месяцев показано контрольное УЗИ. При гиперплазии, связанной с поликистозом яичников, первым этапом лечения является клиновидная резекция гонад.
При недостаточном клиническом эффекте резекции яичников (контроль – биопсия и гистологическое исследование эндометрия) проводят гормонотерапию согласно установкам, принятым в отношении разных видов гиперпластических процессов эндометрия.
Хирургические методы предпочтительны при рецидивирующей железисто-кистозной гиперплазии, развившейся на фоне заболеваний желез внутренней секреции (диабет, предиабет и др.), ожирения, гипертонической болезни, заболеваний печени и вен. Хирургическое лечение показано при предраке (аденоматоз, аденоматозные полипы) эндометрия, особенно при сочетании указанной патологии эндометрия с аденомиозом и миомой матки, патологическими процессами в яичниках.
Гормональной терапии не подлежат больные с фиброзными полипами.
Женщинам репродуктивного и особенно пременопаузального возраста, у которых выявлены железистые и железисто-фиброзные полипы на фоне гиперпластических процессов эндометрия, показано удаление полипа с последующей гормональной терапией.
При аденоматозных полипах у женщин пременопаузального возраста с обменно-эндокринными нарушениями альтернативой является удаление матки с тщательной ревизией яичников (гиперплазия тела ткани, наличие гормонально-активных опухолей). Аденоматозные полипы у женщин в постменопаузе являются показанием к удалению матки с придатками.
Гиперплазия эндометрия матки: лечение и диагностика в Одессе
Под гиперплазией матки принято понимать чрезмерное разрастание ее слизистой оболочки. Сбой в этой части организма обусловлен гормональными нарушениями. Слизистая оболочка теряет способность к уменьшению после окончания цикла и приобретает гипертрофированный вид. Симптомы заболевания — нарушения менструального цикла, мажущие выделения и обильные месячные.
Однако часто болезнь протекает без ярко выраженных симптомов. Проблема разрастания эндометрия матки актуальна для 50% женщин от 30 до 39 лет.
Доверьте лечение гиперплазии эндометрия настоящим профессионалам«Тихое», но опасное заболевание требует высокого профессионализма доктора и передовых методов диагностики. Все это вы найдете в медицинском доме Odrex, где вам предложат:
Все это вы найдете в медицинском доме Odrex, где вам предложат:
- Высокоточную диагностику с применением гистероскопа Karl Storz без наркоза и боли;
- Оперативное составление плана индивидуального лечения;
- Работающие методы лечения.
Диагностика гиперплазии эндометрия в Odrex
Первый и обязательный шаг в диагностике гиперплазии – осмотр женщины врачом-гинекологом. В ходе осмотра врач назначит нужные лабораторные и инструментальные исследования.
Сегодня во врачебной практике применяются высокоэффективные и щадящие методы диагностики:
- УЗИ органов малого таза – распространенный метод. Современные аппараты помогают увидеть и измерить толщину слоя слизистой оболочки с точностью до десятых миллиметра. При этом сама по себе, не подтвержденная другими исследованиями, картина УЗИ – это не диагноз. Делать УЗИ нужно или в середине цикла или сразу по окончании месячных.
- МРТ органов малого таза обеспечивает наглядную визуализацию, благодаря четкому контрасту мягких тканей.
 Незаменимый инструмент для выявления опухолевых заболеваний. Магнитный резонанс точно диагностирует спаечный процессв малом тазу, что невозможно сделать только с помощью ультразвукового исследования.
Незаменимый инструмент для выявления опухолевых заболеваний. Магнитный резонанс точно диагностирует спаечный процессв малом тазу, что невозможно сделать только с помощью ультразвукового исследования. - Гистероскопия – наиболее информативный метод, обеспечивающий точные и достоверные результаты. На вооружении нашей клиники немецкая оптическая система Karl Storz, которая выполнит прицельную биопсию в том месте, где расположен очаг разрастания клеток. При необходимости производится срезание патологической ткани. Занимает процедура менее часа и требует госпитализации на полдня. Срок гистологического исследования – от 2 до 14 дней.
- Лабораторные анализы на определение уровня гормонов в крови, надпочечниках и щитовидной железе.
Подозрение на гиперплазию появляется, когда толщина эндометрия больше 15-16 мм (по данным УЗИ или МРТ органов малого таза).
Как лечить гиперпластический процесс?
На лечение гиперплазии эндометрия влияет много факторов. Среди них решающее значение имеет вид гиперплазии эндометрия:
- Простая железистая гиперплазия характеризуется избыточным разрастанием ткани эндометрия.

- Аденоматозная или комплексная гиперплазия, при которой внутри эндометрия образуются не характерные для него структуры. Встречается примерно у трех из ста женщин.
- Железисто кистозная гиперплазия эндометрия. Сопровождается образованиями кистозного характера и провоцирует увеличение объема матки.
- Очаговая гиперплазия (полипы эндометрия). Патологические образования, состоящие из тела и ножки.
- ААтипическая гиперплазия эндометрия — самая опасная разновидность, которая часто приводит к злокачественным образованиям. Принято выделять очаговую и диффузную разновидности. Иногда к этой форме приводит неправильно подобранная терапия железистой гиперплазии.
Главный принцип лечения основан на удалении участка патологической слизистой. С этой целью в медицине были разработаны следующие методы:
- Гистероскопическая резекция (срезание) эндометрия и удаление полипов — обязательный первый этап лечения. К достоинствам такого лечения относится малая травматичность, экономичность (благодаря сокращению времени нахождения в клинике), сохранение репродуктивной функции и уменьшение длительности вмешательства.

- Гормональная терапия, которая заключается в приеме препаратов, нормализующих выработку эстрогена и прогестерона. Существуют препараты общего и местного воздействия (внутриматочные). Разработано множество схем приема подобных лекарственных препаратов, и задача врача – выбрать оптимальный вариант.
- Хирургическое вмешательство кюретаж, или в просторечии – выскабливание. Сегодня считается устаревшим методом. Смысл процедуры понятен из названия. Такой операции присущи многочисленные недостатки: сильные болевые ощущения, необходимость большого расширения шейки матки. риск возникновения спаечного процесса в малом тазу. Проводится под общим наркозом. Необходимость в госпитализации зависит от физического состояния пациента и способности переносить наркоз. Возможен местный наркоз обезболивающими препаратами.
- Удаление матки или гистерэктомия — радикальный способ, который применяется исключительно при атипической гиперплазии. когда велик риск перерождения доброкачественных образований в злокачественные, или при рецидивирующей форме заболевания, не нуждающейся в терапии.

Помните, что лечение этой болезни носит индивидуальный характер. Нет единой панацеи, которая бы работала со стопроцентной гарантией во всех случаях без исключения. И только опытный гинеколог-эндокринолог определит ту схему, дозу и продолжительность лечения, которые «сработают» в каждом конкретном случае. Однако преимущественно назначается комбинированное лечение, которое подразумевает и хирургическое вмешательство, и гормональную терапию.
Вопрос — ответ
Работают ли народные средства лечения гиперплазии?
Сегодня на просторах интернета встречается масса рекомендаций, как вылечить гиперплазию пиявками, чистотелом, лопухом или крапивой. Однако эффективность этих способов в отношении этого заболевания в официальной медицине не подтверждена. Поэтому не стоит рисковать здоровьем из-за сомнительных рецептов.
Возможны ли рецидивы болезни?
Риск повторного возникновения этого заболевания велик и возникает в 30 % процентов случаев. При этом прогнозировать возникновения рецидива невозможно: он не зависит ни от течения заболевания, ни от выбранной схемы лечения. Поэтому проведение биопсии эндометрия спустя 3-6 месяцев после окончания лечения — обязательная процедура.
При этом прогнозировать возникновения рецидива невозможно: он не зависит ни от течения заболевания, ни от выбранной схемы лечения. Поэтому проведение биопсии эндометрия спустя 3-6 месяцев после окончания лечения — обязательная процедура.
Можно ли забеременеть при ГПЭ?
При болезни может отсутствовать овуляция, и сама слизистая оболочка иногда в не состоянии принять эмбрион. При этом после удачно проведенного лечения забеременеть естественным образом возможно. Детородная функция восстанавливается практически всегда. Поэтому если в планах женщины родить здорового и крепкого малыша, вылечить гиперплазию следует обязательно.
Как предупредить возникновение гиперплазии эндометрия?
Профилактические рекомендации в этом случае носят общий характер без специфических моментов. Это и регулярные визиты к гинекологу, и лечение воспалительных половых заболеваний, и занятия спортом.
Может ли гиперплазия «пройти сама»?
Помните, что гиперплазия эндометрия — потенциальный рак. Это доказано авторитетными зарубежными и отечественными исследователями. Не стоит надеяться, что разросшаяся слизистая «рассосется» сама собой. Без врачебной помощи это заболевание пройти не может.
ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ ЭНДОМЕТРИЯ. ДИАГНОСТИКА, КЛИНИКА, ЛЕЧЕНИЕ | Пушкарев
1. Ахундова С.С., Кирикова Ю.М., Миллер А.П., Караченцева И.В. Ближайшие и отдаленные результаты использования биполярной гистерорезекции для лечения различных видов внутриматочной патологии у пациенток различных возрастных групп // Вестник РГМУ. – 2008. №3(62). С. 9-11.
2. Бреусенко В., Голова Ю.А., Каппушева Л.М., Мишиева О.И., Кирикова Ю.М., Цечоева Т.С.. Современный подход в лечении пролиферативных процессов в постменопаузе // Избранные лекции. – М.: Из-во «МЕДпрессинформ», 2007. – С. 315-323.
– М.: Из-во «МЕДпрессинформ», 2007. – С. 315-323.
3. Берека Дж. Гинекология по Эмилю Новаку / Дж. Берека, И. Адаши, П. Хиллард. М.: Практика, 2002. 892 с.
4. Бохман Я.В. Руководство по онкогинекологии. СПб.: Фолиант, 2002. -540 с.
5. Бочкарева Н.В. Сочетание гиперплазии и рака эндометрия с миомой матки: роль половых гормонов, их рецепторов и ферментов метаболизма эстрогенов / Н.В. Бочкарева, Л.А. Коломиец, И.В. Кондакова // Вопр. Онкологии. 2005. Т. 51. №4. С. 427-433.
6. Кондрикова Н.И., Силакова А.В. Гиперпластические изменения и предраковые состояния эндометрия: вопросы терминологии и классификации // Архив патологии. – 2010. – Т. 72. №1. – С. 60-62.
7. Клинышкова Т.В. Клинико-морфологическое обоснование оптимизации лечения больных с гиперплазией эндометрия / Т.В. Клинышкова, Н.Б. Фролова, С.И. Мозговой // Российский вестник акушера-гинеколога. 2010. – №3. С. 16-20.
Клинышкова Т.В. Клинико-морфологическое обоснование оптимизации лечения больных с гиперплазией эндометрия / Т.В. Клинышкова, Н.Б. Фролова, С.И. Мозговой // Российский вестник акушера-гинеколога. 2010. – №3. С. 16-20.
8. Кузнецов Р.Э., Соколова Л.М. Применение амбулаторной гистерскопии у больных пожилого возраста // Военно-медицинский журнал. – 2009. -Т. СССХХХ. №7. С.69.
9. Мартиросян К.А. Современные методы лечения гиперпластических процессов эндометрия пациенток в постменопаузе / Соломатина А.А., Мишиева О.И., Мартиросян К.А. // Материалы Международной научно-практической конференции «Актуальные вопросы акушерства, гинекологии и перинатологии», Судак, 2012. С. 331-332.
10. Современные методы диагностики гиперпластических процессов эндометрия / О.С. Лобачевская, Л.С. Гуляева, О.В. Сасина [и др.] // Медицинская панорама. 2005. №8. С.24-25.
Лобачевская, Л.С. Гуляева, О.В. Сасина [и др.] // Медицинская панорама. 2005. №8. С.24-25.
11. Solomatina A., Martirosyan K., Tikhonov D. Influence of the receptor gene expression of the reproductive hormones at patients with endometrium pathology in postmenopause // XX FIGO World Congress of Gynecology and Obstetrics. Rome, 2012.
12. Simsek T. Impact of different hormone replacement therapy regimens on the size ofmyoma uteri in postmenopausal period: tibolone versus transdermal hormonal replacement system / T. Simsek, C. Karakus // Vaturitas. 2002. Vol. 42. P. 243-246.
Гиперплазия эндометрий лечение 🌟 Поликлиника №1 РАН
Содержание:
Риски
Гиперплазия эндометрия относится к доброкачественным процессам наряду с аденомиозом и миомой. Термин «гиперплазия» означает чрезмерное разрастание внутреннего функционального слоя матки, который преобразуется под влиянием гормонов, создавая благоприятные условия для наступления беременности. Если оплодотворения не происходит, слой отторгается и наступает менструация. Длительное поддержание одного уровня эстрогенов приводит к выраженной стимуляции эндометрия. Он состоит из железистой ткани (выполняющей специфическую функцию в каждом органе) и стромы (связывающего компонента из соединительной ткани). В результате железистая ткань сильно разрастается. При наступлении менструации ее отторжение сопровождается обильным кровотечением. В некоторых случаях длительно существующая гиперплазия может самостоятельно не разрешиться, а переродиться в злокачественный процесс. Гиперплазия в таком случае будет считаться предраковым заболеванием. Без должного контроля и лечения запущенные процессы грозят смертельными последствиями.
Термин «гиперплазия» означает чрезмерное разрастание внутреннего функционального слоя матки, который преобразуется под влиянием гормонов, создавая благоприятные условия для наступления беременности. Если оплодотворения не происходит, слой отторгается и наступает менструация. Длительное поддержание одного уровня эстрогенов приводит к выраженной стимуляции эндометрия. Он состоит из железистой ткани (выполняющей специфическую функцию в каждом органе) и стромы (связывающего компонента из соединительной ткани). В результате железистая ткань сильно разрастается. При наступлении менструации ее отторжение сопровождается обильным кровотечением. В некоторых случаях длительно существующая гиперплазия может самостоятельно не разрешиться, а переродиться в злокачественный процесс. Гиперплазия в таком случае будет считаться предраковым заболеванием. Без должного контроля и лечения запущенные процессы грозят смертельными последствиями.
Причины заболевания
Как уже было отмечено, основной причиной развития гиперпластических процессов в эндометрии служит стимуляция эпителия эстрогенами. Может отмечаться увеличение восприимчивости ткани к их действию, а также снижаться уровень прогестрерона. Источником эстрогенов для развития гиперплазии в старшем возрасте выступает жирования ткань при ожирении (как дополнительный орган, синтезирующий эстрон), высокий уровень фолликулостимулирующего гормона и гиперстимуляция яичников за счет угасающей с возрастом репродуктивной функции. У молодых девушек из-за незрелости регуляторных систем фолликулы (основные функционирующие единицы яичника), созревают и преобразуются в яйцеклетку иногда существенно дольше положенного и уровень гормонов падает не достаточно быстро. Кроме того, выделяют первичные заболевания, способные привести к патологическому уровню эстрогенов: гормонально активные опухоли любых органов, увеличение функциональной ткани яичников при медикаментозной стимуляции овуляции, перенесенное воспаление яичников.
Может отмечаться увеличение восприимчивости ткани к их действию, а также снижаться уровень прогестрерона. Источником эстрогенов для развития гиперплазии в старшем возрасте выступает жирования ткань при ожирении (как дополнительный орган, синтезирующий эстрон), высокий уровень фолликулостимулирующего гормона и гиперстимуляция яичников за счет угасающей с возрастом репродуктивной функции. У молодых девушек из-за незрелости регуляторных систем фолликулы (основные функционирующие единицы яичника), созревают и преобразуются в яйцеклетку иногда существенно дольше положенного и уровень гормонов падает не достаточно быстро. Кроме того, выделяют первичные заболевания, способные привести к патологическому уровню эстрогенов: гормонально активные опухоли любых органов, увеличение функциональной ткани яичников при медикаментозной стимуляции овуляции, перенесенное воспаление яичников.
Проявление болезни
Гиперпластические процессы разделяют на доброкачественные : полип и, собственно, гиперплазия и злокачественные (атипические) гиперплазии. Основным симптомом таких изменений будет маточное кровотечение (меноррагии или метроррагии), соответствующие менструальному циклу или не зависящие от него. Причиной таких кровотечений является отторжение гиперплазированных участков после их разрушения, тромбирования сосудов и других изменений.
Основным симптомом таких изменений будет маточное кровотечение (меноррагии или метроррагии), соответствующие менструальному циклу или не зависящие от него. Причиной таких кровотечений является отторжение гиперплазированных участков после их разрушения, тромбирования сосудов и других изменений.
Установлением и верификацией диагноза при обнаружении таких изменений занимается врач-гинеколог совместно с морфологом и онкологом, при отсутствии достоверного диагноза может потребоваться консультация терапевта и эндокринолога.
Диагностика
Первичные исследования обязательно включают комплексную оценку данных анамнеза, определение гормонального статуса, общий анализ крови, коагулограмма и другие исследования для проведения дифференциальной диагностики с заболеваниями крови. Золотым стандартом диагностики является получение материала измененной слизистой и изучение его под микроскопом. Чтобы получить материал, можно выполнить гистероскопию и раздельное диагностическое выскабливание полости матки на 5-7 день менструального цикла или аспирационную биопсию. УЗИ матки позволяет косвенно оценить размеры и структуру эндометрия. В нормальных условиях толщина эндометрия растет постепенно после менструации до 3-4 мм в первые 10 дней, и увеличивается до 12-15 мм накануне очередной менструации. Если эти размеры у девушки репродуктивного возраста больше перечисленных, то стоит продолжить обследование. У женщин в постменопаузе размер эндометрия составляет в норме не более 5 мм.
УЗИ матки позволяет косвенно оценить размеры и структуру эндометрия. В нормальных условиях толщина эндометрия растет постепенно после менструации до 3-4 мм в первые 10 дней, и увеличивается до 12-15 мм накануне очередной менструации. Если эти размеры у девушки репродуктивного возраста больше перечисленных, то стоит продолжить обследование. У женщин в постменопаузе размер эндометрия составляет в норме не более 5 мм.
Лечение заболевания
Лечение зависит от возраста пациентки и вида гиперпластического процесса. При поступлении девушки репродуктивного возраста с маточным кровотечением на фоне гиперплазии проводится гормональный гемостаз (используют способность сокращения кровоточащих сосудов и изменения слизистой под действием эстроген-гестагенных препаратов). Если женщина старшего возраста в состоянии менопаузы, то применяется диагностическое выскабливание полости матки как метод остановки кровотечения. Собственно для устранения и последующей профилактики гиперплазии широко используют лекарственные вещества, угнетающие функцию яичников и приводящие к атрофии эндометрия. Контроль лечения проводят через 4-6 месяцев с помощью повторного выскабливания полости матки и морфологического изучения полученного материала.
Контроль лечения проводят через 4-6 месяцев с помощью повторного выскабливания полости матки и морфологического изучения полученного материала.
Если заболевание сочетается с другой патологией матки, не поддается лечению и часто рецидивирует – нужно задуматься об оперативном лечении. Выполняют различные операции по удалению самого эндометрия или удалению матки с придатками. Способы будут зависеть от возраста, возможных предпочтений женщины и взглядов врача.
Гиперплазия эндометрия | Цены на операцию в клинике «Здоровая Женщина»
Операционное лечение гиперплазии эндометрия в Москве
При разрастании слизистой оболочки матки происходит нарушение работы всей репродуктивной системы. Такое заболевание может иметь различные причины, формы и требует срочного лечения. В клинике «Здоровая Женщина» вам проведут операцию при гиперплазии эндометрия по доступной цене с применением самых современных методик. Наш медицинский центр включает штат высококвалифицированных врачей, обладает современным диагностическим и операционным оборудованием, применяет лазерные технологии. Мы поможем вам справиться с любой проблемой и позаботиться о женском здоровье.
Мы поможем вам справиться с любой проблемой и позаботиться о женском здоровье.
Классификация
Сколько стоит операция при гиперплазии эндометрия, зависит от формы и степени заболевания. Выделяют два основных вида:
- Типичный (доброкачественный). В этом случае разрастание маточных желез происходит в результате гормонального дисбаланса.
- Атипичный. При этой форме происходит мутация клеток эпителия. Заболевание в такой форме не связано с гормональным фоном и нередко является предраковым состоянием, влекущим за собой образование злокачественной опухоли.
В любом случае заболевание требует срочного лечения. В нашей клинике вам проведут диагностику на высоком уровне и точно определят форму и степень заболевания.
Причины и симптомы
У возникновения гиперплазии эндометрия могут быть различные причины, чаще всего связанные с гормональными сбоями. Наиболее частыми факторами являются:
- хирургические аборты и выскабливание матки;
- бесконтрольный прием оральных контрацептивов;
- сбои в работе иммунной системы;
- длительная гормонотерапия;
- поликистоз, опухоли и другие заболевания яичников;
- хроническая артериальная гипертензия;
- ожирение и сбои в работе других систем организма.

Наиболее часто пациентки клиники при гиперплазии эндометрия жалуются на:
- маточное кровотечение;
- длительные задержки менструации;
- мажущие выделения из влагалища бурого цвета;
- повышение болезненности менструаций, увеличение объема кровянистых выделений.
Развитие гиперплазии эндометрия угрожает возникновению осложнений, имеющих серьезные последствия:
- бесплодие;
- невынашивание беременности;
- хронические воспалительные процессы;
- мастоплазия и миоматоз;
- рак эндометриоидной ткани.
Поэтому очень важно своевременно обратиться к врачу и пройти курс лечения. Наша клиника в Москве проводит операции при гиперплазии эндометрия по доступным ценам.
Способы лечения
В зависимости от формы и стадии болезни применяются различные виды операций. Наша клиника предлагает современные методики, позволяющие эффективно и минимально травматично решить проблемы с женским здоровьем.
- Выскабливание (кюретаж). С помощью специальных инструментов врач выскабливает верхний слой эпителия. Процедура проводится с применением гистероскопии, позволяющей контролировать процесс. Назначается при железисто-кистовой гиперплазии эндометрия, а также при его толщине не более 16 мм.
- Криодеструкция. Этот способ основан на воздействии жидким азотом на места развития патологии. Это одна из эффективных методик, позволяющая не травмировать здоровые ткани. Назначается при противопоказаниях к предыдущему методу, а также при атипичной форме заболевания.
- Лазерная абаляция. При регулярных рецидивах болезни назначается удаление патологически разрастающихся участков эпителия с помощью лазерного оборудования. Процедура практически не доставляет дискомфорта, не затрагивает здоровые ткани, позволяет снизить риск осложнений.
- Удаление матки. Когда гиперплазия эндометрия достигает значительных размеров и аденоматоз находится на последних стадия, щадящие методики могут оказаться неэффективными.
 В этом случае необходимо удаление матки. Это особенно важно при атипичной форме, поскольку такое заболевание может перерасти в онкологию.
В этом случае необходимо удаление матки. Это особенно важно при атипичной форме, поскольку такое заболевание может перерасти в онкологию.
Обращаясь к нам, вы можете рассчитывать на квалифицированный и внимательный персонал. Команда опытных врачей найдет оптимальный способ решения вашей проблемы, а современное оборудование, применяемое в нашей клинике, позволит сократить период реабилитации и сделать операцию безболезненной. Записаться на прием к специалисту в медицинский центр «Здоровая Женщина», чтобы проконсультироваться по вопросу гиперплазии эндометрия, вы можете по телефону, указанному на сайте.
Гиперплазия эндометрия ➡ лечение в Харькове
Гиперплазия эндометрия представляет собой гинекологический недуг, когда отмечается многослойное нарастание маточной слизистой оболочки. Согласно классификации гиперплазия матки может быть атипическая либо без атипии.
Гипоплазия эндометрия атипического характера выступает предраковым заболеванием, поэтому лечением такой формы недуга занимаются непосредственно онкологи.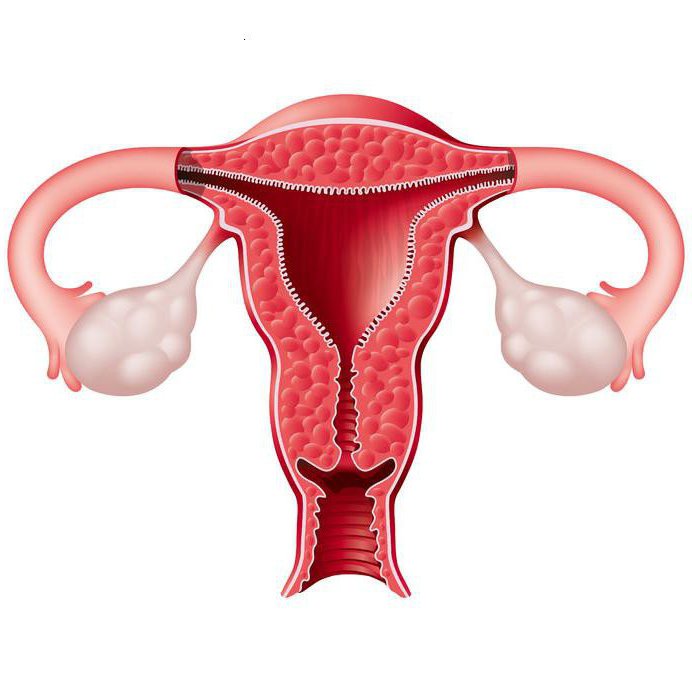
Обычная гипоплазия эндометрия носит доброкачественный характер, однако несвоевременное лечение данного недуга может стать причиной возникновения онкологии эндометрии, поэтому заболевание также нуждается в своевременном квалифицированном лечении
Симптоматика и причины возникновения
Основными симптомами гиперплазии являются:
- Менструации обильного характера.
- Дисбаланс менструального цикла: выделения до и после основных критических дней.
- Дисбаланс обычного режима менструального цикла.
- Дисбаланс периодичности менструального цикла: частые менструации либо задержки.
Причины возникновения:
- Возрастные изменения.
- Вредные привычки.
- Гормональные нарушения на фоне приема лекарственных средств.
- Гинекологическое оперативное вмешательство.
- Нарушение обмена веществ, сахарный диабет и др.
Все эти факторы, так или иначе, могут спровоцировать развитие гиперплазии эндометрии, которая подлежит диагностике и лечению.
Диагностика. Как лечить гиперплазию эндометрия в клинике Молекула
Квалифицированные специалисты предопухолевого центра «Молекула» (Харьков) диагностируют представленное заболевание, используя оборудование новейшего поколения, а также высокоточные методики, что сокращает срок установки точного диагноза до минимума.
Под обследованием можно понимать:
- Гинекологический осмотр и проведение трансвагинального УЗИ.
- Гистологическое исследование ткани эндометрии.
- Биопсия тканей матки.
Опираясь на результаты обследования и на индивидуальные особенности организма, врач назначает комплексное лечение гиперплазии эндометрия. Если гиперплазия носит обычный характер, зачастую назначается гормонотерапия, позволяющая устранить недуг и не допустить его появления в будущем. Если заболевание носит атипичный характер, то специалисты настоятельно рекомендуют проводить хирургическое вмешательство с сохранением органов половой системы или же без такового, в зависимости от стадии развития заболевания.
Выполнить запись на прием к врачам клиники Молекула возможно, как по телефону, так и с помощью кнопки «Запись на прием».
Гиперплазия эндометрия
Гиперплазия эндометрия – это заболевание, для которого характерно разрастание внутренней выстилки матки (эндометрия), в результате чего увеличивается его толщина и объем. Это заболевание диагностируется у женщин разного возраста, однако, чаще всего наблюдается у пациенток после 40 лет. С развитием менопаузы риск развития гиперплазии эндометрия увеличивается в несколько раз.Эндометрий состоит из двух слоев: функционального, который отторгается во время менструации и базального, за счет которого образуется вновь функциональный.
В норме – функциональный слой увеличивается в первой половине цикла – матка подготавливается к возможному оплодотворению. Если этого не произошло, то функциональный слой выводится во время менструации. Все эти циклические изменения регулируются правильным соотношением гормонов.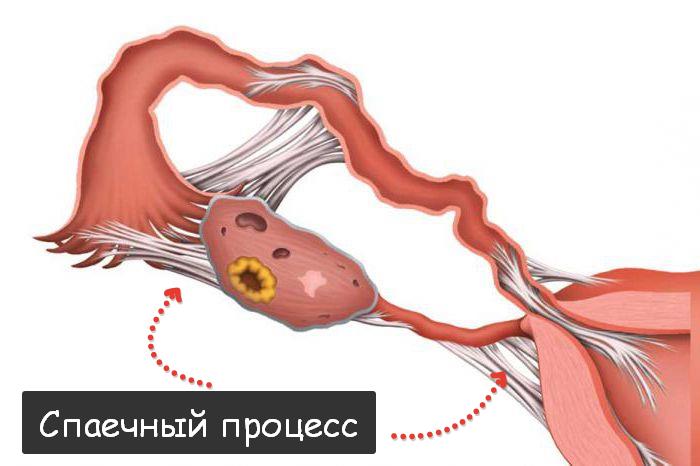
Причиной развития гиперплазии эндометрия являются дисгормональные процессы, при которых нарушается созревание и отторжение эндометрия и происходит его разрастание. Разрастание эндометрия может возникать равномерно в полости матки, так и на отдельных ее участках. Через определенное время эндометрий все же отторгается, но в большем количестве, что дает клинику обильных кровотечений. Кроме того, гиперплазия эндометрия может часто перерождаться в рак эндометрия.
ГРУППА РИСКА ДЛЯ ВОЗНИКНОВЕНИЯ ГИПЕРПЛАЗИИ ЭНДОМЕТРИЯ
- Ожирение.
- Сахарный диабет.
- Гипертоническая болезнь.
- Ановуляция.
- Синдром поликистозных яичников.
- Поздняя менопауза.
- Гранулематозная опухоль яичника.
- Использование экзогенных эстрогенов и тамоксифена.
ФОРМЫ ГИПЕРПЛАЗИИ ЭНДОМЕТРИЯ
- железистая форма – форма гиперплазии эндометрия с разрастанием преимущественно железистой ткани.
 Вероятность развития рака эндометрия составляет 2-7%.
Вероятность развития рака эндометрия составляет 2-7%. - железисто — кистозная гиперплазия эндометрия – форма гиперплазии, при которой железы кистозно изменены и гистологически выглядят как «швейцарский сыр». Риск ракового перерождения этой формы – незначительный.
- атипическая гиперплазия – это вид гиперплазии относят к предраковым формам. Переход такой гиперплазии в рак эндометрия наблюдается от 8 до 29 %.
- очаговая гиперплазия – вид гиперплазии при котором утолщение эндометрия происходит неравномерно. В отдельных локализациях эндометрий увеличен на несколько миллиметром, а в отдельных на несколько сантиметров, образуя полипы эндометрия.
КЛИНИЧЕСКАЯ КАРТИНА ГИПЕРПЛАЗИИ ЭНДОМЕТРИЯ
Основным клиническими проявлением гиперплазии эндометрия являются кровотечения:
- гиперменорея (обильные кровотечения во время менструации),
- межменструальные и постменопаузные кровотечения.

- Нередко болезнь проявляется бессимптомно и женщина обращается к гинекологу по поводу бесплодия.
ДИАГНОСТИКА ГИПЕРПЛАЗИИ ЭНДОМЕТРИЯ
- Трансвагинальное ультразвуковое исследование – позволяет выявить гиперплазию эндометрия, полипы эндометрия.
- Аспирационная биопсия эндометрия – позволяет исключить или подтвердить наличие злокачественного процесса.
- Гормональное исследование: уровень эстрогенов, прогестерона, гормоны щитовидной железы и надпочечников.
- Гистероскопия – специальный метод исследования с помощью оптического оборудования, который позволяет изучить эндометрий, обнаружить измененные участки, провести биопсию эндометрия и удалить полип эндометрия.
ЛЕЧЕНИЕ ГИПЕРПЛАЗИИ ЭНДОМЕТРИЯ
Лечение гиперплазии эндометрия зависит от ее формы, возраста пациентки и тяжести заболевания. При некоторых формах гиперплазии эндометрия, после получения гистологического заключения назначается консервативное медикаментозное лечение, которое направлено на нормализацию гормональных нарушений и подавление разрастания эндометрия.

При неэффективности консервативной терапии, в случае рецидива, при маточном кровотечении и наличии полипов показано оперативное лечение.
«Золотым стандартом» является – гистероскопия, которая особенно показана пациенткам репродуктивного и менопаузального возраста. Гистероскопия имеет ряд преимуществ, которыми являются: минимальная травматичность, прекрасная визуализация зоны операции, экономичность (уменьшение длительности операции,быстрое восстановление пациентки, минимизация пребывания в стационаре). Это позволяет сохранить матку как репродуктивный орган и избежать более травматичных операций.

Видео 1. Гистероскопия с абляцией эндометрия.
При наличии атипичной формы эндометрия – показано удаление матки, которое так же мы выполняем лапароскопически.
ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД
Сроки госпитализации в стационаре после выполнения гистероскопии – 5-8 часов после выполнения операции.
В послеоперационном периоде после гистерорезектоскопии назначается антибиотикотерпия и противовоспалительная терапия, которая продолжается амбулаторно.
В соблюдении какой либо диеты нет необходимости. На протяжении 14-24 дней могут быть кровянистые или сукровичные выделения из влагалища.
Через один менструальный цикл после операции я рекомендую пациентке пройти контрольный осмотр и контрольное вагинальное ультразвуковое исследование.
ПРОФИЛАКТИКА РЕЦИДИВА И ПОЯВЛЕНИЯ ГИПЕРПЛАЗИИ ЭНДОМЕТРИЯ
Чтобы свести к минимуму риск появления гиперплазии эндометрия или ее рецидива необходимо вовремя проводить коррекцию гормональных нарушений, инфекционных заболеваний гинекологической сферы.
 Так же, нужно отказаться от абортов и необоснованного приема оральных контрацептивов.
Так же, нужно отказаться от абортов и необоснованного приема оральных контрацептивов.При наличии заболеваний из факторов риска возникновения гиперплазии эндометрия необходимо постоянно и грамотное лечение этих заболеваний (при сахарном диабете – контроль гликемии, при ожирении – борьба с лишним весом, при гипертонической болезни – коррекция артериального давления и т.д.)
.
Учитывая то, что на ранних стадиях заболевание протекает практически бессимптомно – обязательным является регулярное посещение женщиной гинеколога.
Лечение и лечение гиперплазии эндометрия
Каковы осложнения гиперплазии эндометрия?
Все типы гиперплазии могут вызвать аномальное и сильное кровотечение, которое может вызвать анемию. Анемия развивается, когда в вашем организме не хватает эритроцитов, богатых железом.
При отсутствии лечения атипичная гиперплазия эндометрия может перейти в злокачественную опухоль. Рак эндометрия или матки развивается примерно у 8% женщин с нелеченой простой атипичной гиперплазией эндометрия. Около 30% женщин со сложной атипичной гиперплазией эндометрия, не получающих лечения, заболевают раком.
Около 30% женщин со сложной атипичной гиперплазией эндометрия, не получающих лечения, заболевают раком.
Как лечить и лечить гиперплазию эндометрия?
Если у вас повышенный риск рака из-за атипичной гиперплазии эндометрия, ваш врач может порекомендовать гистерэктомию для удаления матки. После гистерэктомии вы не сможете забеременеть. Многие люди видят улучшение симптомов при менее инвазивном лечении прогестином. Прогестин бывает разных форм:
Предыдущий: Диагностика и тесты Далее: ПрофилактикаПоследний раз проверял медицинский работник Cleveland Clinic 28.08.2020.
Список литературы
Получите полезную, полезную и актуальную информацию о здоровье и благополучии
е Новости Клиника Кливленда — некоммерческий академический медицинский центр. Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic.
Политика
Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic.
Политика
Лечение гиперплазии эндометрия — Мидвуд Бруклин, Нью-Йорк и Верхний Ист-Сайд Нью-Йорк, Нью-Йорк: д-р Грегори Шифрин, акушерство и гинекология PC
Гиперплазия эндометрия возникает, когда клетки эндометрия, которые обычно образуют внутреннюю оболочку матки, а затем ежемесячно выделяются с менструальным циклом, ненормально разрастаются и вызывают утолщение слизистой оболочки матки.Похожим и более широко известным заболеванием является эндометриоз, при котором клетки эндометрия покидают стенки матки и бесконтрольно растут за пределами матки. В обоих гинекологических состояниях рак эндометрия может развиваться или сосуществовать вместе с этими состояниями.
Гиперплазия эндометрия может проявляться в трех различных формах:
- Простая гиперплазия: незначительная скученность эндометриальных желез и низкий риск рака эндометрия
- Сложная гиперплазия: большая скученность желез и средний риск рака эндометрия
- Атипичная гиперплазия: сложная скученность желез и самый высокий риск рака эндометрия
Чтобы записаться на консультацию к врачу, специализирующемуся на лечении гиперплазии эндометрия, позвоните по телефону (718) 743-0505 или свяжитесь с нами через Интернет.
Причины и факторы риска гиперплазии эндометрия
Гиперплазия эндометрия чаще всего встречается у пожилых женщин, которые уже находятся в менопаузе или приближаются к менопаузе (перименопауза). Однако он также встречается у молодых женщин, только начинающих менструацию. Чаще всего это вызвано избыточной выработкой эстрогена — общей характеристикой женщин в перименопаузе — с недостаточной выработкой прогестерона. Эти ключевые женские гормоны также могут стать несбалансированными из-за приема лекарств, ожирения и гинекологических состояний, таких как синдром поликистозных яичников или бесплодие.
Гиперплазия эндометрия чаще всего возникает у женщин с одним или несколькими из следующих факторов риска:
- старше 35 лет
- европеоид
- семейный анамнез гинекологического рака (эндометрия, яичников, матки)
- курение
- ожирение
Симптомы гиперплазии эндометрия
Не совсем понятно, почему некоторые люди испытывают симптомы гиперплазии эндометрия, а другие нет. Когда возникают симптомы гиперплазии эндометрия, они обычно включают боль во время полового акта или различные нарушения менструального цикла, в том числе:
- Обильные менструации
- Кровотечение между менструациями или после менопаузы
- Аномально продолжительные периоды
- Отсутствие менструального кровотечения (аменорея)
- Менструальное кровотечение циклы без нормальной овуляции (ановуляторные периоды)
Гиперплазия эндометрия Диагностика
Если ее не диагностировать и не лечить, гиперплазия эндометрия обычно не проходит сама по себе. Гиперплазия эндометрия часто обнаруживается из-за аномального маточного кровотечения между менструациями или после менопаузы. Если вы испытываете нарушения менструального цикла, важно встретиться с вашим лечащим врачом, чтобы убедиться в вашем гинекологическом здоровье в целом и пройти обследование на гиперплазию эндометрия.
Гиперплазия эндометрия часто обнаруживается из-за аномального маточного кровотечения между менструациями или после менопаузы. Если вы испытываете нарушения менструального цикла, важно встретиться с вашим лечащим врачом, чтобы убедиться в вашем гинекологическом здоровье в целом и пройти обследование на гиперплазию эндометрия.
Биопсия эндометрия — один из безошибочных методов диагностики гиперплазии эндометрия, а также ее можно использовать для исключения рака эндометрия. Трансвагинальное ультразвуковое исследование (внутреннее ультразвуковое исследование, выполняемое с помощью палочки, введенной во влагалище) для оценки вашего эндометрия также используется для диагностики гиперплазии, а также с помощью гистероскопии, которая использует тонкий телескопический инструмент для обнаружения и лечения гиперплазии.
Варианты лечения гиперплазии эндометрия
Гиперплазию эндометрия можно лечить различными методами, включая гормональную терапию и небольшие операции. Прогестероновая терапия обычно является методом выбора, который помогает противодействовать избытку эстрогена в организме и истончать слизистую оболочку матки. Его вводят перорально, местно или с помощью инъекций, таблеток или внутриматочной спирали (ВМС).
Его вводят перорально, местно или с помощью инъекций, таблеток или внутриматочной спирали (ВМС).
В случаях сложной атипичной гиперплазии может потребоваться более агрессивное лечение для снижения риска развития рака.В этих случаях, если вы не планируете иметь больше детей, ваш лечащий врач может порекомендовать гистерэктомию.
Профилактика гиперплазии эндометрия
Планирование регулярных осмотров органов малого таза может помочь в раннем выявлении эндометрия или других гинекологических аномалий. Кроме того, гормоны играют ключевую роль в развитии гиперплазии эндометрия. Работа над поддержанием баланса гормонов, независимо от того, на каком этапе жизни вы находитесь, может помочь предотвратить развитие гиперплазии эндометрия.Ваш лечащий врач может предложить помощь в адаптации гормонального баланса к образу жизни, включая диету, физическую активность и рекомендации по добавкам.
Поскольку чрезмерный рост эндометрия обычно связан с ожирением, здоровое питание, отказ от жирной пищи, потеря веса и ежедневные упражнения могут снизить ваш риск.
Запросите дополнительную информацию о гиперплазии эндометрия, а также о вариантах тестирования и лечения сегодня. Звоните (718) 743-0505 или свяжитесь с нами через Интернет.
Вопросы женского здоровья — Профилактика
Хотя большинство случаев рака эндометрия невозможно предотвратить, есть определенные вещи, которые женщина может сделать, чтобы снизить риск развития этого заболевания:
Поддерживайте здоровую массу тела.
Рак эндометрия чаще встречается у женщин с избыточным весом и гораздо чаще встречается у женщин с ожирением, чем у женщин с нормальным весом. Избыток жира может увеличить уровень эстрогена в организме, что связано с повышенным риском.
Есть также некоторые свидетельства того, что женщины, страдающие диабетом, находятся в группе повышенного риска.
Борьба с ожирением и диабетом и сокращение количества потребляемых животных жиров и жирной пищи может помочь снизить риск рака эндометрия. Регулярные упражнения могут помочь вам поддерживать здоровую массу тела и вдвое снизить риск.
Регулярные упражнения могут помочь вам поддерживать здоровую массу тела и вдвое снизить риск.
Примите оральные контрацептивы.
Прием оральных контрацептивов (таблетки) может снизить риск развития рака эндометрия у женщины. Самый низкий риск у женщин, длительно принимающих оральные контрацептивы. Эта защита действует не менее 10 лет после того, как женщина перестает их принимать.
Знайте о рисках и преимуществах гормональной терапии.
Прием гормональной терапии (ЭТ) только эстрогенами увеличивает риск развития рака эндометрия у женщин.Этот повышенный риск сохраняется в течение как минимум пяти лет после того, как женщина прекратила прием ЭТ. Если вы планируете принимать гормональную терапию (ГТ) при симптомах менопаузы, принимайте вместе прогестин и эстроген. Хотя эстроген-прогестиновая терапия может снизить ваш риск, при длительном применении она может увеличить риск рака груди. Если вы планируете принимать ГТ, обсудите риски и преимущества со своим врачом.
Раннее обнаружение и лечение гиперплазии эндометрия.
Гиперплазия эндометрия — это увеличенный рост эндометрия.В отличие от рака легкая или простая гиперплазия может исчезнуть сама по себе или после гормонального лечения. Самый распространенный тип гиперплазии, простая гиперплазия, имеет очень небольшой риск стать злокачественным. Однако простая атипичная гиперплазия и сложная атипическая гиперплазия имеют риск стать злокачественным при отсутствии лечения примерно в 8% и до 29% случаев соответственно. Как можно раньше получить надлежащее лечение предраковых состояний эндометрия, таких как гиперплазия.
Если вы испытываете какие-либо симптомы рака эндометрия, обратитесь к врачу.
Выявление рака эндометрия на ранних стадиях может привести к успешному излечению. Самый ранний признак рака эндометрия — обычно необычное и нерегулярное кровотечение. Если у вас нерегулярное кровотечение, боль в области таза и / или необычные выделения из влагалища, скорее всего, в этом нет ничего серьезного, но вы должны немедленно сообщить об этих симптомах своему врачу. К счастью, большинство видов рака эндометрия обнаруживаются на ранней стадии, потому что симптомы обычно возникают на ранней стадии развития болезни. Однако некоторые виды рака эндометрия могут достигнуть поздней стадии до того, как признаки и симптомы станут заметны.
К счастью, большинство видов рака эндометрия обнаруживаются на ранней стадии, потому что симптомы обычно возникают на ранней стадии развития болезни. Однако некоторые виды рака эндометрия могут достигнуть поздней стадии до того, как признаки и симптомы станут заметны.
Не существует рекомендуемых скрининговых тестов или обследований, которые могли бы надежно обнаружить большинство видов рака эндометрия у женщин, у которых нет симптомов. Пап-тест может выявить некоторые ранние формы рака эндометрия, но в большинстве случаев не обнаруживается. Пап-тест обычно используется для выявления аномалий шейки матки.
Перейти на главную страницуПрогнозирование рецидива после отмены терапии у женщин с гиперплазией эндометрия: долгосрочное наблюдение наблюдаемый при первичном диагнозе может предсказывать рецидив.Материалы и методы: 57 женщин с гиперплазией эндометрия получали внутриматочную систему, пропитанную левоноргестрелом, или перорально прогестин в течение трех месяцев в течение 1998-2000 гг.
 Индексные биопсии были классифицированы в соответствии с ВОЗ1994 и системами D-score, а также иммуногистохимическим окрашиванием рецептора эстрогена α (ERα), рецептора эстрогена β (ERβ), рецептора прогестерона A (PRA), рецептора прогестерона B (PRB), B-клеточной лимфомы 2. / регулятор апоптоза (BCL2), BCL2-ассоциированный X-белок / регулятор апоптоза (BAX), парный бокс 2 (PAX2) и гомолог фосфатазы и тензина (PTEN), представленные как H-баллы.Результаты. За период наблюдения 157,8 месяцев у 23% (10/43) пациентов возник рецидив. Не было обнаружено корреляции с возрастом, индексом массы тела, паритетом, классификацией ВОЗ94 или D-оценкой. Только PRA (p = 0,004) и PRB (p = 0,038) показали определенную корреляцию с рецидивом. Заключение: гиперплазия эндометрия рецидивирует через много лет после успешной терапии прогестинами. Повышенная экспрессия PRB и сниженная экспрессия PRA достоверно коррелировали с рецидивом. Наши результаты подтверждают важность постоянной защиты эндометрия и потребность в новых клинических руководствах по эпиднадзору.
Индексные биопсии были классифицированы в соответствии с ВОЗ1994 и системами D-score, а также иммуногистохимическим окрашиванием рецептора эстрогена α (ERα), рецептора эстрогена β (ERβ), рецептора прогестерона A (PRA), рецептора прогестерона B (PRB), B-клеточной лимфомы 2. / регулятор апоптоза (BCL2), BCL2-ассоциированный X-белок / регулятор апоптоза (BAX), парный бокс 2 (PAX2) и гомолог фосфатазы и тензина (PTEN), представленные как H-баллы.Результаты. За период наблюдения 157,8 месяцев у 23% (10/43) пациентов возник рецидив. Не было обнаружено корреляции с возрастом, индексом массы тела, паритетом, классификацией ВОЗ94 или D-оценкой. Только PRA (p = 0,004) и PRB (p = 0,038) показали определенную корреляцию с рецидивом. Заключение: гиперплазия эндометрия рецидивирует через много лет после успешной терапии прогестинами. Повышенная экспрессия PRB и сниженная экспрессия PRA достоверно коррелировали с рецидивом. Наши результаты подтверждают важность постоянной защиты эндометрия и потребность в новых клинических руководствах по эпиднадзору.
Карцинома эндометрия — наиболее частое злокачественное новообразование женских половых путей, заболеваемость которым постоянно увеличивается (1, 2). Примерно 80% карциномы эндометрия (тип I) предшествуют предварительные стадии, известные как гиперплазия эндометрия, и каждый пятый случай гиперплазии прогрессирует до рака, если его не лечить (3). В течение последних нескольких десятилетий пероральная гормональная терапия прогестином иногда использовалась в качестве терапии гиперплазии эндометрия в качестве альтернативы хирургическому вмешательству (4-7).Последние данные свидетельствуют о том, что внутриматочная система, пропитанная левоноргестрелом (ЛНГ-ВМС), превосходит пероральную терапию и может успешно использоваться при гиперплазии эндометрия для предотвращения прогрессирования заболевания (7–12). Риск рецидива сохраняется даже после достижения регресса гиперплазии эндометрия, но нет международного консенсуса в отношении продолжительности наблюдения после успешного лечения или каких-либо рекомендаций относительно графика последующего наблюдения. Хотя некоторые исследования показали, что риск рецидива выше после пероральной терапии по сравнению с внутриматочной терапией, частота рецидивов после отмены лечения варьировала от 13.От 7% до 43% в различных группах пациентов (7, 13, 14).
Хотя некоторые исследования показали, что риск рецидива выше после пероральной терапии по сравнению с внутриматочной терапией, частота рецидивов после отмены лечения варьировала от 13.От 7% до 43% в различных группах пациентов (7, 13, 14).
Специфических и безопасных прогностических методов для выявления женщин с риском рецидива не существует, и до настоящего времени только одно долгосрочное исследование подтвердило клинические и биологические маркеры в качестве предикторов рецидива (7, 13, 14). Патогенез злокачественной трансформации эндометрия до конца не изучен, но общепринято считать, что такие злокачественные новообразования возникают в результате вызванных эстрогеном изменений, которым не препятствует прогестерон, в сочетании с лежащими в основе генетическими аберрациями (15-20).В-клеточная лимфома 2 (BCL2) и BCL2-ассоциированный X-белок (BAX) являются белками, участвующими в регуляции запрограммированной гибели клеток, и было показано, что оба они значительно подавляются в железах эндометрия, но активируются в строме в пациенты с полным регрессом гиперплазии после успешной терапии прогестинами (17, 18, 21-23). Было показано, что инактивация генов-супрессоров опухолей фосфатазы и гомолога тензина ( PTEN ) и парного бокс-гена 2 ( PAX2 ) мутацией, делецией или клональной потерей происходит на начальных стадиях рака эндометрия в 63% случаев. и 71% случаев соответственно (18, 24, 25).Для обоих генов клиренс мутировавших клонов был продемонстрирован после успешной терапии прогестином (25, 26). Однако корреляция между уровнями экспрессии рецепторов эстрогена (ERα, ERβ), рецепторов прогестерона (PRA, PRB), BCL2, BAX, PTEN и PAX и рецидивом после успешной терапии еще предстоит исследовать.
Было показано, что инактивация генов-супрессоров опухолей фосфатазы и гомолога тензина ( PTEN ) и парного бокс-гена 2 ( PAX2 ) мутацией, делецией или клональной потерей происходит на начальных стадиях рака эндометрия в 63% случаев. и 71% случаев соответственно (18, 24, 25).Для обоих генов клиренс мутировавших клонов был продемонстрирован после успешной терапии прогестином (25, 26). Однако корреляция между уровнями экспрессии рецепторов эстрогена (ERα, ERβ), рецепторов прогестерона (PRA, PRB), BCL2, BAX, PTEN и PAX и рецидивом после успешной терапии еще предстоит исследовать.
В настоящем обсервационном популяционном когортном исследовании женщины с гиперплазией эндометрия низкого и среднего риска наблюдались и обследовались на предмет рецидива в течение более 150 месяцев.Насколько нам известно, другой базы данных пациентов с сопоставимой продолжительностью наблюдения не существует. Наша цель состояла в том, чтобы определить, были ли какие-либо клинические или биологические маркеры, наблюдаемые и доступные на момент первичного диагноза, важны для прогнозирования индивидуального риска рецидива. Выявление таких маркеров может проложить путь к индивидуальной терапии и более тщательному наблюдению за пациентами из группы высокого риска, а также к разработке новых и более безопасных клинических руководств. Таким образом, клинические и демографические данные, а также профили иммуногистохимической экспрессии индексных биопсий были подтверждены как прогностические факторы рецидива.
Выявление таких маркеров может проложить путь к индивидуальной терапии и более тщательному наблюдению за пациентами из группы высокого риска, а также к разработке новых и более безопасных клинических руководств. Таким образом, клинические и демографические данные, а также профили иммуногистохимической экспрессии индексных биопсий были подтверждены как прогностические факторы рецидива.
Материалы и методы
Исследуемая популяция. В течение 1998–2000 гг. Были собраны две популяционные серии пациентов с гистологически подтвержденной гиперплазией эндометрия. Первая группа, в которую вошли 26 женщин в возрасте от 30 до 70 лет, получала лечение ЛНГ-ВМС (Мирена®, Bayer, высвобождающая 20 мкг левоноргестрела / день) в течение 3 месяцев. Другая группа, в которую вошли 31 последовательный пациент в возрасте от 30 до 70 лет, получала циклическую пероральную терапию прогестинами [медроксипрогестерон (МПА) 10 мг в день в течение 10 дней в месяц с повторением 3 цикла].Лекарство было выбрано и назначено местными гинекологами пациентов согласно терапевтическим рекомендациям на тот момент. Все женщины были включены в исследование после получения информированного согласия. Перед включением в исследование были получены индексные биопсии эндометрия с помощью аспирационной биопсии (N = 22) или дилатации и кюретажа (D&C) (N = 35). Наиболее частыми симптомами были менометроррагия и постменопаузальное кровотечение.
Все женщины были включены в исследование после получения информированного согласия. Перед включением в исследование были получены индексные биопсии эндометрия с помощью аспирационной биопсии (N = 22) или дилатации и кюретажа (D&C) (N = 35). Наиболее частыми симптомами были менометроррагия и постменопаузальное кровотечение.
Для оценки ответа на терапию через 3 месяца была проведена контрольная биопсия эндометрия.Независимо от ответа на терапию, все участники исследования получили долгосрочное наблюдение. Выбор дальнейшего лечения и наблюдения за женщинами, у которых возник рецидив после завершения исследования, оставался за их первичными гинекологами и основывался на индивидуальных потребностях пациентов и медицинских рекомендациях на тот момент. Время наблюдения для каждого пациента рассчитывалось с даты индексной биопсии до 1 января 2016 г. или до гистерэктомии или смерти. Рецидив рассматривался как исход только у женщин, ответивших на лечение после 3 месяцев первичной терапии. Все истории болезни систематически просматривались с помощью электронной системы записи, используемой в нашем регионе здравоохранения.
Все истории болезни систематически просматривались с помощью электронной системы записи, используемой в нашем регионе здравоохранения.
Биопсийные материалы. Гинекологи амбулаторных клиник в северной Норвегии отвечали за забор биопсий эндометрия. Все индексные биопсии, контрольные биопсии и дополнительные биопсии во время наблюдения были отправлены в отделение патологии Университетской больницы Северной Норвегии для рутинной оценки. Образцы фиксировали в забуференном формальдегиде, заливали парафином и обрабатывали в лаборатории перед тем, как сделать стандартные гистологические срезы.В соответствии с обычными диагностическими процедурами, обученный гинеколог-патолог (АО) и еще один общий патолог, которые не знали диагнозов друг друга, выполнили гистологические исследования в соответствии с классификацией ВОЗ94 (3) с использованием световой микроскопии. В случае противоречивых результатов консенсус всегда достигался после обсуждения на двуглавом микроскопе. Индексные биопсии были классифицированы в одну из трех групп в соответствии с классификацией ВОЗ94, которая считалась золотым стандартом для оценки гиперплазии эндометрия на момент проведения исследования: простая гиперплазия, сложная гиперплазия или атипичная гиперплазия (3).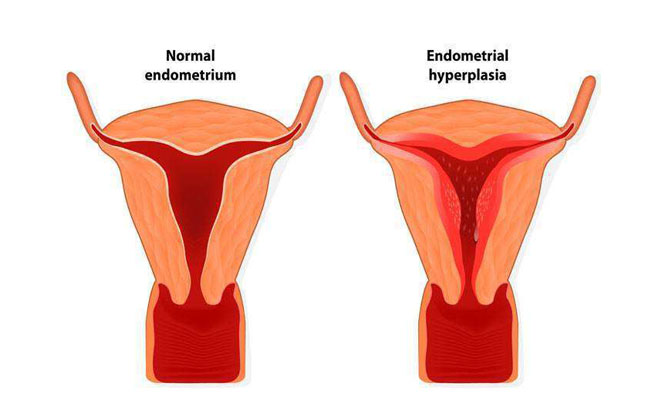 Ответ на первичную терапию определялся обнаружением обычного пролиферативного эндометрия или эндометрия с изменениями, вызванными прогестином, в контрольной биопсии. Стойкая гиперплазия в контрольной биопсии была классифицирована в соответствии с классификацией ВОЗ94 и определена как неэффективность первичной терапии. Дополнительные биопсии, полученные во время наблюдения, были оценены и классифицированы таким же образом. Вся информация из классификации ВОЗ94 по индексным, контрольным и дополнительным биопсиям эндометрия регистрировалась и сохранялась в отдельной базе данных, а затем дополнялась информацией из больничных записей.
Ответ на первичную терапию определялся обнаружением обычного пролиферативного эндометрия или эндометрия с изменениями, вызванными прогестином, в контрольной биопсии. Стойкая гиперплазия в контрольной биопсии была классифицирована в соответствии с классификацией ВОЗ94 и определена как неэффективность первичной терапии. Дополнительные биопсии, полученные во время наблюдения, были оценены и классифицированы таким же образом. Вся информация из классификации ВОЗ94 по индексным, контрольным и дополнительным биопсиям эндометрия регистрировалась и сохранялась в отдельной базе данных, а затем дополнялась информацией из больничных записей.
Морфометрический анализ D-оценка. После завершения диагностической микроскопии и достижения консенсуса по классификации ВОЗ94 были проведены морфометрия тканей и анализ D-баллов для улучшения стратификации риска. Было показано, что метод D-оценки превосходит классификацию ВОЗ94 в прогнозировании исходов рака (10, 17, 27-30). Считается, что пациенты с рейтингом D <0 имеют высокий риск сопутствующей или будущей карциномы, и в таких случаях рекомендуется гистерэктомия. Таким образом, только пациенты с D-оценкой 0 или выше имели право на участие в исследовании, и все они получали консервативные схемы и долгосрочное наблюдение. Анализ D-баллов проводился обученными специалистами. Первоначальное исследование компьютерного морфометрического анализа гиперплазии эндометрия включало в общей сложности 10 ядерных особенностей и 12 архитектурных особенностей. Используя пошаговую линейную регрессию и дискриминантный анализ, три из этих количественных характеристик были отобраны как имеющие значимое независимое прогностическое значение и были объединены в формулу, известную как D-оценка, как показано ниже: D-оценка = 0.6229 + 0,0439 × (объем стромы в процентах) — 3,9934 × Ln (стандартное отклонение кратчайшей ядерной оси) — 0,1592 × (внешняя поверхность желез плотности), где Ln — натуральный логарифм. Измерения проводились с использованием системы анализа изображений Q-PRODIT (версия 6.1, Leica, Кембридж, Великобритания). Метод D-score подробно описан в предыдущих исследованиях (10, 17, 27-30).
Таким образом, только пациенты с D-оценкой 0 или выше имели право на участие в исследовании, и все они получали консервативные схемы и долгосрочное наблюдение. Анализ D-баллов проводился обученными специалистами. Первоначальное исследование компьютерного морфометрического анализа гиперплазии эндометрия включало в общей сложности 10 ядерных особенностей и 12 архитектурных особенностей. Используя пошаговую линейную регрессию и дискриминантный анализ, три из этих количественных характеристик были отобраны как имеющие значимое независимое прогностическое значение и были объединены в формулу, известную как D-оценка, как показано ниже: D-оценка = 0.6229 + 0,0439 × (объем стромы в процентах) — 3,9934 × Ln (стандартное отклонение кратчайшей ядерной оси) — 0,1592 × (внешняя поверхность желез плотности), где Ln — натуральный логарифм. Измерения проводились с использованием системы анализа изображений Q-PRODIT (версия 6.1, Leica, Кембридж, Великобритания). Метод D-score подробно описан в предыдущих исследованиях (10, 17, 27-30).
Иммуногистохимия . Части индексной биопсии женщин, ответивших на первичную терапию, иммуноокрашивали на экспрессию ERa, ERβ, PRA, PRB, ERα, ERβ, BCL2, BAX, PTEN и PAX2.Однако из-за недостаточного количества материала в парафиновых блоках иммуноокрашивание проводилось не во всех случаях (для ERα и BCL2 материал был доступен для девяти случаев рецидива и 27 случаев устойчивого ответа; для ERβ, PRA, PRB и BAX, девять случаев рецидива и 28 случаев устойчивого ответа; а для PTEN и PAX2 — восемь случаев рецидива и 32 случая устойчивого ответа). Процедуры окрашивания выполняли, как указано в таблице I. Перед окрашиванием гистологические срезы (толщиной 5 мкм) вырезали из парафиновых блоков обычными методами, помещали на предметные стекла Superfrost + и инкубировали в течение ночи при 60 ° C.Контрастное окрашивание проводили вручную в три этапа: окрашивание гематоксилином, дегидратация и очистка ксилолом.
Таблица I. Методы иммуногистохимического окрашивания для каждого из маркеров, исследованных в настоящем исследовании.
Оценка экспрессии ERα, ERβ, PRA, PRB, BCL2 и BAX . Иммуноокрашивание на ERα, ERβ, PRA, PRB, BCL2 и BAX оценивали полуколичественно с использованием иммуногистохимической гистологической оценки (H-score), которая включает как интенсивность, так и распределение специфического окрашивания.H-оценка определяется как HS = ∑ (Pi x i) / 100. где Pi обозначает процент окрашенных клеток, а i обозначает интенсивность окрашивания от 1 до 3 (31). Экспрессию в железах и строме оценивали отдельно для каждого образца. Горячие точки (участки с наиболее сильным иммуноокрашиванием) диаметром 1 см исследовали при увеличении × 40. Подсчитывали как интенсивность окрашивания, так и количество окрашенных положительных клеток. Образцы с менее чем 10% положительных клеток считались рецепторно-отрицательными и получали нулевую оценку.Образцы с более чем 10% положительно окрашенных клеток считались рецептор-положительными, и процент положительно окрашенных клеток использовали для расчета H-балла. Шкала H-балла варьировалась от 0 до 3: 0 баллов указывал на отсутствие окрашивания, тогда как баллы 1, 2 и 3 указывали на слабую, умеренную и сильную иммунореактивность соответственно. H-балл оценивался обученным гинекологом-патологом (АО), который не знал первоначального диагноза, группы лечения и ответа на лечение.
Шкала H-балла варьировалась от 0 до 3: 0 баллов указывал на отсутствие окрашивания, тогда как баллы 1, 2 и 3 указывали на слабую, умеренную и сильную иммунореактивность соответственно. H-балл оценивался обученным гинекологом-патологом (АО), который не знал первоначального диагноза, группы лечения и ответа на лечение.
Оценка экспрессии PAX2 и PTEN . Гистологические образцы, окрашенные на PAX2 и PTEN, были исследованы под световым микроскопом обученным гинекологом-патологом (AO) и обученным техником (MA). Стекло оценивалось как отсутствие PTEN или отсутствие PAX2, если наблюдались одна или несколько желез эндометрия, лишенных окрашивания белка PAX2 или PTEN. Когда визуализировались все железы эндометрия, экспрессирующие PAX2 или PTEN, образец считался нормальным. Нулевые железы, как правило, были лишены белка PAX2 или PTEN во всех клетках.О наличии или отсутствии окрашивания всегда судили по консенсусу между двумя исследователями с использованием двуглавого микроскопа. Эта процедура всегда выполнялась дважды, и исследователи не знали о результатах лечения пациентов. Потеря иммуноокрашивания PAX2 и PTEN в основном характеризовалась перекрывающимся паттерном, происходящим в одних и тех же очагах.
Потеря иммуноокрашивания PAX2 и PTEN в основном характеризовалась перекрывающимся паттерном, происходящим в одних и тех же очагах.
Статистика. Статистический анализ был выполнен с использованием программного обеспечения STATA версии 14 (STATA Corp., College Station, TX, USA). Данные представлены с использованием стандартной описательной статистики хи-квадрат, и для сравнения категориальных и непрерывных переменных, в зависимости от ситуации, использовались двухвыборочные тесты t . p — Значения менее 0,05 считались значимыми.
Этическое одобрение. Исследование было одобрено Региональным комитетом по этике медицинских и медицинских исследований (номера одобрения PREKNORD17 / 2002 и 23/2004), Норвежским советом медицинских консультаций и Норвежским агентством по лекарственным средствам.
Результаты
Пациенты. Женщины в двух группах лечения демонстрировали сходные исходные характеристики в отношении возраста, индекса массы тела, паритета, гистологического диагноза ВОЗ94 и распределения D-баллов до лечения (32).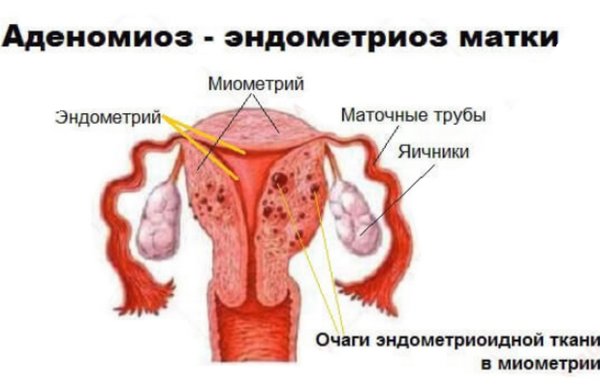 Все пациенты, получавшие ЛНГ-ВМС, показали отличный ответ с полным регрессом гиперпластического эндометрия через 3 месяца терапии. Напротив, только 55% (17/31) пациентов в группе перорального МПА достигли ответа на лечение (рис. 1). Независимо от первоначального ответа на терапию, все женщины в настоящем исследовании получили долгосрочное наблюдение со средним сроком наблюдения 155,4 месяца. Наблюдение за эндометрием проводилось с использованием вагинального УЗИ и биопсии эндометрия. Среднее число 5.У каждого пациента было получено 0 биопсий эндометрия (диапазон = 2-15). Один пациент умер от рака толстой кишки во время наблюдения. Все оставшиеся женщины были живы и все еще проживали на севере Норвегии в конце периода наблюдения. У четырех женщин был диагностирован инвазивный рак груди, у одной — карцинома груди in situ , у одной — рак яичников и у одной — злокачественная меланома.
Все пациенты, получавшие ЛНГ-ВМС, показали отличный ответ с полным регрессом гиперпластического эндометрия через 3 месяца терапии. Напротив, только 55% (17/31) пациентов в группе перорального МПА достигли ответа на лечение (рис. 1). Независимо от первоначального ответа на терапию, все женщины в настоящем исследовании получили долгосрочное наблюдение со средним сроком наблюдения 155,4 месяца. Наблюдение за эндометрием проводилось с использованием вагинального УЗИ и биопсии эндометрия. Среднее число 5.У каждого пациента было получено 0 биопсий эндометрия (диапазон = 2-15). Один пациент умер от рака толстой кишки во время наблюдения. Все оставшиеся женщины были живы и все еще проживали на севере Норвегии в конце периода наблюдения. У четырех женщин был диагностирован инвазивный рак груди, у одной — карцинома груди in situ , у одной — рак яичников и у одной — злокачественная меланома.
Долгосрочное наблюдение и рецидив после ответа на первичную терапию. В целом, 43 женщины достигли ответа на первичную терапию: 26 из 26 в группе ЛНГ-ВМС и 17 из 31 в группе перорального МПА. В течение среднего периода наблюдения 157,8 (диапазон = 5–212) месяцев у 10 (23%) из 43 женщин, которые первоначально ответили на терапию, произошел рецидив гиперплазии эндометрия. Пациенты, у которых был диагностирован рецидив, проходили режимы наблюдения, сравнимые с пациентами без рецидива, со средним значением пяти (диапазон = 3-10) биопсий эндометрия, полученных в группе рецидива, и четырьмя (диапазон = 2-9) в группе устойчивого ответа. Средняя продолжительность наблюдения среди пациентов с рецидивом составила 123,7 месяца по сравнению со 168 месяцами.1 месяц у пациентов, у которых не было рецидива. Частота рецидивов была одинаковой в двух группах лечения: 6/26 (23%) в группе ЛНГ-ВМС и 4/17 (23,5%) в группе перорального МПА (рис. 1). Хотя у большинства пациентов (7/10, 70%) рецидивы наблюдались в течение первых 2 лет после отмены терапии прогестинами, рецидивы наблюдались в течение 10 лет после первоначального лечения.
В течение среднего периода наблюдения 157,8 (диапазон = 5–212) месяцев у 10 (23%) из 43 женщин, которые первоначально ответили на терапию, произошел рецидив гиперплазии эндометрия. Пациенты, у которых был диагностирован рецидив, проходили режимы наблюдения, сравнимые с пациентами без рецидива, со средним значением пяти (диапазон = 3-10) биопсий эндометрия, полученных в группе рецидива, и четырьмя (диапазон = 2-9) в группе устойчивого ответа. Средняя продолжительность наблюдения среди пациентов с рецидивом составила 123,7 месяца по сравнению со 168 месяцами.1 месяц у пациентов, у которых не было рецидива. Частота рецидивов была одинаковой в двух группах лечения: 6/26 (23%) в группе ЛНГ-ВМС и 4/17 (23,5%) в группе перорального МПА (рис. 1). Хотя у большинства пациентов (7/10, 70%) рецидивы наблюдались в течение первых 2 лет после отмены терапии прогестинами, рецидивы наблюдались в течение 10 лет после первоначального лечения.
Долгосрочное наблюдение за женщинами с неэффективностью первичной терапии . Женщинам, у которых после трех месяцев пероральной терапии МПА (n = 14) были предложены различные терапевтические процедуры.Пяти женщинам была выполнена гистерэктомия, одной — трансцервикальная резекция эндометрия, четырем — дополнительная пероральная терапия МПА, а у четырех произошел спонтанный регресс. Ни у одной из этих женщин за период наблюдения не развился рак эндометрия. У этой группы пациентов средний период наблюдения составил 148,2 (диапазон = 20-212) месяцев, и в среднем у каждого пациента было собрано четыре (диапазон = 3-15) биопсий эндометрия.
Женщинам, у которых после трех месяцев пероральной терапии МПА (n = 14) были предложены различные терапевтические процедуры.Пяти женщинам была выполнена гистерэктомия, одной — трансцервикальная резекция эндометрия, четырем — дополнительная пероральная терапия МПА, а у четырех произошел спонтанный регресс. Ни у одной из этих женщин за период наблюдения не развился рак эндометрия. У этой группы пациентов средний период наблюдения составил 148,2 (диапазон = 20-212) месяцев, и в среднем у каждого пациента было собрано четыре (диапазон = 3-15) биопсий эндометрия.
Прогностические маркеры рецидива у женщин с ответом на первичную терапию .Только женщины, ответившие на первичную терапию (n = 43), оценивались на предмет рецидива гиперплазии эндометрия. Оценка прогностической значимости различных клинических характеристик не показала никакой связи с рецидивом (Таблица II). Клинические и гистологические характеристики женщин, переживших рецидив, представлены в таблице III. H-баллы для ERα, ERβ, PRA, PRB, BCL2 или BAX в железах и строме индексной биопсии не были связаны с рецидивом, за исключением H-баллов для PRA в строме и PRB в железах. .Между женщинами с рецидивом и без рецидива наблюдалась значительная разница в H-балле для PRA в строме и PRB в железах ( p = 0,0044 для PRA в строме и p = 0,0376 для PRB в железах) (Таблица IV) . Наличие или отсутствие мутаций PAX2 или PTEN в индексных биопсиях не показало какой-либо связи с рецидивом (Таблица V). Все контрольные биопсии, полученные после 3 месяцев терапии, также были исследованы иммуногистохимически и окрашены на ERα, ERβ, PRA, PRB, Bcl2, BAX, PTEN и PAX2.Однако статистической корреляции между рецидивом и каким-либо из исследованных маркеров не наблюдалось (данные не показаны).
.Между женщинами с рецидивом и без рецидива наблюдалась значительная разница в H-балле для PRA в строме и PRB в железах ( p = 0,0044 для PRA в строме и p = 0,0376 для PRB в железах) (Таблица IV) . Наличие или отсутствие мутаций PAX2 или PTEN в индексных биопсиях не показало какой-либо связи с рецидивом (Таблица V). Все контрольные биопсии, полученные после 3 месяцев терапии, также были исследованы иммуногистохимически и окрашены на ERα, ERβ, PRA, PRB, Bcl2, BAX, PTEN и PAX2.Однако статистической корреляции между рецидивом и каким-либо из исследованных маркеров не наблюдалось (данные не показаны).
Блок-схема, иллюстрирующая количество женщин, включенных в две группы лечения: Внутриматочная система, пропитанная левоноргестрелом (ЛНГ-ВМС) (Мирена®) в течение 3 месяцев (n = 26), сравнивалась с пероральной прогестиновой терапией медроксипрогестероном. (MPA) 10 мг в день в течение 10 дней в месяц, повторять три цикла (n = 31). Только женщины, ответившие на лечение после 3 месяцев терапии (43 из 57), наблюдались по поводу рецидива. У десяти из этих 43 женщин случился рецидив.
У десяти из этих 43 женщин случился рецидив.
Обсуждение
Насколько нам известно, это наблюдательное когортное исследование женщин с успешно вылеченной гиперплазией эндометрия низкого и среднего риска имеет самый длительный период наблюдения после прекращения терапии прогестинами. За период наблюдения, который длился до 212 месяцев, у 23% женщин случился рецидив. Однако частота рецидивов в этом исследовании значительно отличалась от результатов, представленных в нашем недавнем национальном рандомизированном контролируемом исследовании, в котором сравнивали 6 месяцев лечения внутриматочным и оральным прогестином.В этом исследовании 41% женщин испытали рецидив через 24 месяца наблюдения после отмены терапии (25). Для этой разницы нет очевидной причины, поскольку женщины в двух исследуемых группах получали одинаковую терапию и были сопоставимы по возрасту, ИМТ и половой принадлежности (33). В текущем исследовании большинство рецидивов (60%) наблюдались в течение первых 6 месяцев после прекращения терапии, но рецидив наблюдался в течение 10 лет после отмены. Это согласуется с результатами нашего рандомизированного контролируемого исследования, в котором 70% рецидивов произошли в течение первых 6 месяцев. хотя рецидивы были диагностированы в течение 24 месяцев наблюдения (25).Другое долгосрочное когортное исследование женщин с гиперплазией эндометрия, получавших терапию прогестинами, сообщило о рецидиве у пяти женщин через 60 месяцев после удаления ЛНГ-ВМС (34). Настоящее исследование показало аналогичную частоту рецидивов в двух группах лечения (LNG-IUS против перорального MPA). Другое популяционное обсервационное исследование 370 женщин с гиперплазией эндометрия низкого и среднего риска в северной Норвегии показало среднюю частоту рецидивов 37% после ЛНГ-ВМС и 40% после пероральной терапии прогестинами, но рецидивов не наблюдалось до тех пор, пока СПГ-ИУС остался на месте (7).В отличие от наших результатов, другое долгосрочное когортное исследование, проведенное Галлосом и его сотрудниками, сообщило о частоте рецидивов 13,7% после ЛНГ-ВМС, но 30,3% после пероральной терапии прогестинами (13,14).
Это согласуется с результатами нашего рандомизированного контролируемого исследования, в котором 70% рецидивов произошли в течение первых 6 месяцев. хотя рецидивы были диагностированы в течение 24 месяцев наблюдения (25).Другое долгосрочное когортное исследование женщин с гиперплазией эндометрия, получавших терапию прогестинами, сообщило о рецидиве у пяти женщин через 60 месяцев после удаления ЛНГ-ВМС (34). Настоящее исследование показало аналогичную частоту рецидивов в двух группах лечения (LNG-IUS против перорального MPA). Другое популяционное обсервационное исследование 370 женщин с гиперплазией эндометрия низкого и среднего риска в северной Норвегии показало среднюю частоту рецидивов 37% после ЛНГ-ВМС и 40% после пероральной терапии прогестинами, но рецидивов не наблюдалось до тех пор, пока СПГ-ИУС остался на месте (7).В отличие от наших результатов, другое долгосрочное когортное исследование, проведенное Галлосом и его сотрудниками, сообщило о частоте рецидивов 13,7% после ЛНГ-ВМС, но 30,3% после пероральной терапии прогестинами (13,14). Более высокая частота рецидивов в группе пероральной терапии в этом исследовании, вероятно, была связана с более короткой продолжительностью терапии в группе пероральной терапии (3-12 месяцев) по сравнению с группой ЛНГ-ВМС (5 лет). Таким образом, представленные результаты ясно показывают важность длительной терапии ЛНГ-ВМС для обеспечения постоянной защиты эндометрия и предотвращения рецидивов.
Более высокая частота рецидивов в группе пероральной терапии в этом исследовании, вероятно, была связана с более короткой продолжительностью терапии в группе пероральной терапии (3-12 месяцев) по сравнению с группой ЛНГ-ВМС (5 лет). Таким образом, представленные результаты ясно показывают важность длительной терапии ЛНГ-ВМС для обеспечения постоянной защиты эндометрия и предотвращения рецидивов.
Исходные характеристики участников, прошедших успешное лечение гиперплазии эндометрия внутриматочной системой, пропитанной левоноргестрелом (Мирена®) или пероральным прогестином, оцененные с точки зрения прогностической значимости. Уровни значимости отображаются в виде p-значений.
Таблица III.Клинические и гистологические характеристики 10 женщин, у которых возник рецидив гиперплазии эндометрия в течение периода наблюдения после ответа на первичное лечение.
Таблица IV. Уровни экспрессии биомаркера, оцененные по шкале H, в индексных биопсиях эндометрия у женщин, у которых случился рецидив, по сравнению с теми, у кого нет. Иммуногистохимическую экспрессию оценивали отдельно в железах и строме.
Иммуногистохимическую экспрессию оценивали отдельно в железах и строме.
В настоящее время ведется поиск клинических и биологических биомаркеров, которые могли бы предсказать высокий риск рецидива и помочь выбрать пациентов, которым будет полезна более длительная терапия и более тщательное наблюдение после ее завершения. Когортное исследование, проведенное Галлосом и соавторами, показало, что ИМТ> 35 кг / м 2 был сильным независимым предиктором рецидивирующей гиперплазии эндометрия, что в три раза повышало риск рецидива по сравнению с пациентами с ИМТ <35 кг / м 2 (13).В нашем текущем исследовании ИМТ, возраст и паритет до лечения не имели значения для прогнозирования рецидива. Интересно, что прогностическая ценность D-балла при индексной биопсии приблизилась к статистической значимости ( p = 0,08), тогда как классификация ВОЗ не показала связи с риском рецидива (3).
На сегодняшний день ни в одном исследовании не сообщалось об идеальном маркере рецидива на основе индексной биопсии (35). Об ограниченном количестве иммуногистохимических маркеров сообщалось в продольных исследованиях для выявления биомаркеров, связанных с резистентностью к прогестину или прогрессированием, но в большинстве этих исследований оценивались изменения до и сразу после терапии (23, 27, 30, 36, 37).Akesson и соавторы сообщили о значительно более высоких H-баллах для ER и PR в индексных биопсиях у пациентов, ответивших на терапию прогестином, по сравнению с пациентами, не ответившими на лечение. (36). Другое исследование, оценивающее прогностическую ценность PRA, PRB, BCL2, PTEN и PAX2 в индексной биопсии, показало, что высокая экспрессия PRB была связана с 90% снижением риска сохранения или прогрессирования атипичной гиперплазии, связанной с ЛНГ-ВМС (22). Наши результаты показали более высокий уровень железистого PRB и более низкий уровень PRA в строме в группе с рецидивом по сравнению с женщинами без рецидива.Недавнее исследование in vitro показало, что эпигенетическая дерепрессия стромального PR может быть потенциальной мишенью для сенсибилизации гормонорезистентных опухолей эндометрия к терапии прогестероном, и что стромальная экспрессия PR может представлять собой надежный биомаркер для прогнозирования ответа на гормональную терапию (38 ).
Об ограниченном количестве иммуногистохимических маркеров сообщалось в продольных исследованиях для выявления биомаркеров, связанных с резистентностью к прогестину или прогрессированием, но в большинстве этих исследований оценивались изменения до и сразу после терапии (23, 27, 30, 36, 37).Akesson и соавторы сообщили о значительно более высоких H-баллах для ER и PR в индексных биопсиях у пациентов, ответивших на терапию прогестином, по сравнению с пациентами, не ответившими на лечение. (36). Другое исследование, оценивающее прогностическую ценность PRA, PRB, BCL2, PTEN и PAX2 в индексной биопсии, показало, что высокая экспрессия PRB была связана с 90% снижением риска сохранения или прогрессирования атипичной гиперплазии, связанной с ЛНГ-ВМС (22). Наши результаты показали более высокий уровень железистого PRB и более низкий уровень PRA в строме в группе с рецидивом по сравнению с женщинами без рецидива.Недавнее исследование in vitro показало, что эпигенетическая дерепрессия стромального PR может быть потенциальной мишенью для сенсибилизации гормонорезистентных опухолей эндометрия к терапии прогестероном, и что стромальная экспрессия PR может представлять собой надежный биомаркер для прогнозирования ответа на гормональную терапию (38 ). Клиническое значение этих результатов неочевидно, но продолжение терапии прогестином с долгосрочным использованием ЛНГ-ВМС может иметь терапевтический эффект за счет постоянного подавления PRB.В другом долгосрочном последующем исследовании, посвященном оценке иммуногистохимической экспрессии ER, PR, циклооксигеназ (COX2), механизма репарации ошибочного спаривания ДНК (MLh2) и BCL2, ни один из исследованных биомаркеров не является предиктором рецидива. у женщин, лечившихся от атипичной и сложной гиперплазии (35). Значение различных уровней экспрессии PRA у женщин с рецидивом и без него еще предстоит объяснить, но изоформа PRA обычно доминирует в строме эндометрия (39). Уровни экспрессии железистых и стромальных PRA и PRB, сопоставимые с уровнями настоящего исследования, наблюдались в предыдущем исследовании, в котором сравнивали уровни экспрессии этих рецепторов до и после терапии (37).
Клиническое значение этих результатов неочевидно, но продолжение терапии прогестином с долгосрочным использованием ЛНГ-ВМС может иметь терапевтический эффект за счет постоянного подавления PRB.В другом долгосрочном последующем исследовании, посвященном оценке иммуногистохимической экспрессии ER, PR, циклооксигеназ (COX2), механизма репарации ошибочного спаривания ДНК (MLh2) и BCL2, ни один из исследованных биомаркеров не является предиктором рецидива. у женщин, лечившихся от атипичной и сложной гиперплазии (35). Значение различных уровней экспрессии PRA у женщин с рецидивом и без него еще предстоит объяснить, но изоформа PRA обычно доминирует в строме эндометрия (39). Уровни экспрессии железистых и стромальных PRA и PRB, сопоставимые с уровнями настоящего исследования, наблюдались в предыдущем исследовании, в котором сравнивали уровни экспрессии этих рецепторов до и после терапии (37).
Экспрессия гомолога фосфатазы и тензина (PTEN) и парный бокс 2 (PAX2) в индексных биоптатах эндометрия у женщин с рецидивом по сравнению с женщинами без него. Иммуногистохимическая экспрессия оценивалась только в железах.
Иммуногистохимическая экспрессия оценивалась только в железах.
В заключение, женщины с гиперплазией эндометрия могут испытать рецидив после успешной первичной терапии прогестинами. Последующее наблюдение после ответа на терапию по поводу гиперплазии эндометрия должно продолжаться в течение многих лет после отмены терапии. Было обнаружено, что повышенные уровни PRB в железах и низкие уровни PRA в стромальных клетках позволяют отличить людей с высоким риском от людей с постоянной ремиссией, но для подтверждения прогностической ценности этих маркеров потребуются рандомизированные исследования с более крупными выборками.Наши результаты подтверждают важность длительного использования ЛНГ-ВМС для обеспечения непрерывной защиты эндометрия и подчеркивают необходимость новых руководств по клиническому наблюдению.
Благодарности
Мы благодарим Региональный исследовательский совет Северной Норвегии (Helse Nord) за гранты. Мы также благодарим Роя А. Лайсаа, M.Sc., Ph.D. для изготовления художественных работ.
- Получено 13 марта 2017 г.
- Исправление получено 6 апреля 2017 г.
- Принято 11 апреля 2017 г.
- Copyright © 2017, Международный институт противораковых исследований (Dr.Джордж Дж. Делинасиос), Все права защищены
Гиперплазия эндометрия — Диагностика и лечение
Изображение: «Микрофотография сложной гиперплазии эндометрия. Биопсия эндометрия. Пятно H&E. » от Nephron — Собственная работа. Лицензия: CC BY-SA 3.0
.Определение и эпидемиология гиперплазии эндометрия
Эндометрий — это слизистая оболочка матки или самый внутренний слой матки; другие слои — миометрий и периметрий.Гиперплазия эндометрия — это аномальное утолщение эндометрия , которое подозревается, когда толщина эндометрия ≥ 5 мм у женщин в постменопаузе и> 1 см у женщин в пременопаузе. В некоторых случаях это связано со злокачественными новообразованиями.
В некоторых случаях это связано со злокачественными новообразованиями.
Заболеваемость гиперплазией эндометрия составляет 133 женщины на 100000 в год . Большинство случаев возникает после менопаузы у женщин от 50 до 90 285 лет. Атипичная гиперплазия чаще всего встречается у людей в возрасте от 60 до 64 лет.Оценки заболеваемости считаются низкими, поскольку многие женщины не сообщают о своих симптомах или сообщают о них только после их исчезновения.
Изображение: «Иллюстрация женской репродуктивной системы». Колледж OpenStax — анатомия и физиология, веб-сайт Connexions. http://cnx.org/contents/[email protected]:189, 19 июня 2013 г. Лицензия: CC BY 3.0
Хотя гиперплазия эндометрия чаще встречается у женщин в постменопаузе, она может возникать и в гораздо более молодом возрасте, когда эстроген не встречает сопротивления, как видно из синдрома поликистозных яичников и ожирения .
Некоторые случаи гиперплазии эндометрия, особенно атипичные, могут прогрессировать до рака эндометрия , поэтому важно изучить эти два случая вместе.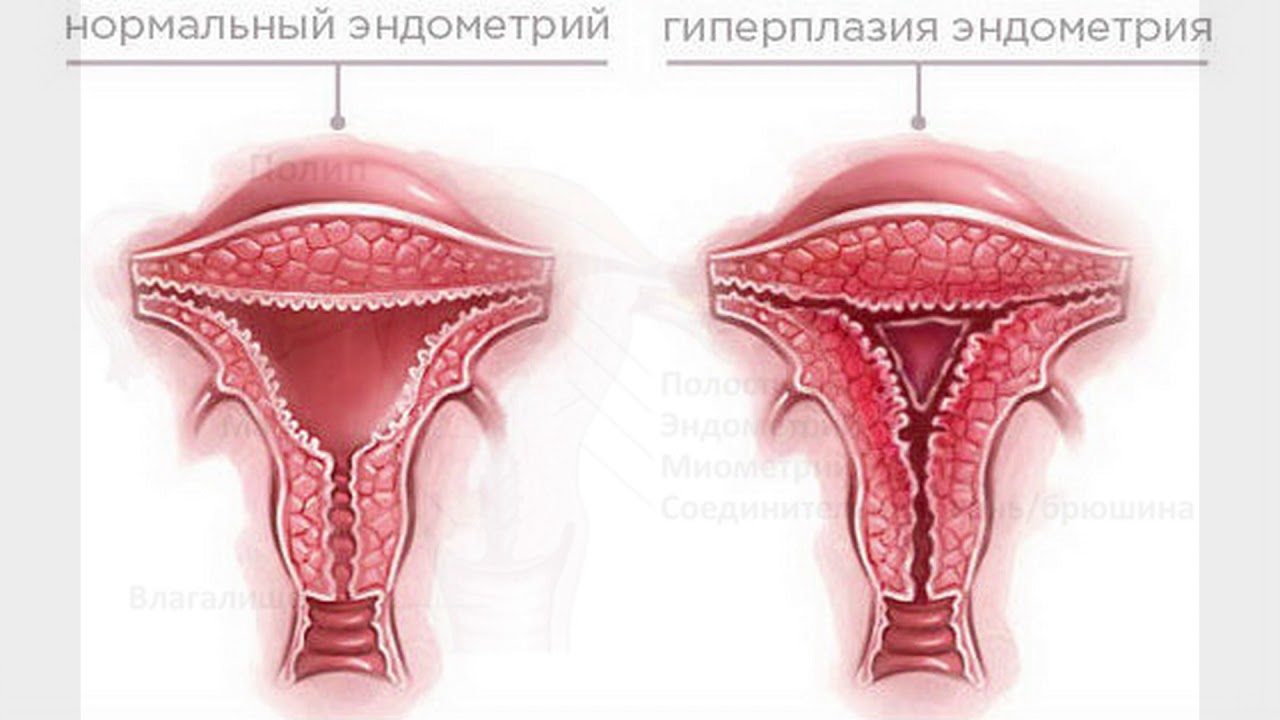 Рак эндометрия является наиболее распространенным гинекологическим раком в развитых странах и вторым по распространенности в развивающихся странах.
Рак эндометрия является наиболее распространенным гинекологическим раком в развитых странах и вторым по распространенности в развивающихся странах.
Примечание для экзамена на получение медицинской лицензии в США ( USMLE): Важно знать список наиболее распространенных видов рака у мужчин и женщин. Что касается гинекологического рака, рак шейки матки является наиболее распространенным в развивающихся странах из-за отсутствия скрининга и вакцинации против вируса папилломы человека (ВПЧ).На 100 000 женщин ежегодно регистрируется 25,4 новых случая заболевания, что приводит к смерти 4,5 на 100 000 женщин в год. У женщин пожизненный риск составляет 2,8%. Средний возраст постановки диагноза составляет от 55 до 67 лет. Только 5% случаев возникают у женщин моложе 40 лет.
Этиология гиперплазии эндометрия
Основной принцип состоит в том, что увеличение на эстрогена , что на не встречает сопротивления прогестерону , приводит к пролиферации ткани эндометрия .
Некоторыми важными факторами риска являются синдром поликистозных яичников , ожирение , недоношенность , ранняя менархе и поздняя менопауза .
Ожирение увеличивает риск из-за избытка эстрогена , производимого из увеличенного количества адипоцитов. Адипоциты содержат фермент под названием ароматаза , который имеет решающее значение для производства эстрогена.
Синдром Линча (наследственный неполипозный колоректальный рак) связан с пожизненным риском развития рака эндометрия в 22–50%.
Примечание для USMLE: Синдром Линча имеет аутосомно-доминантное наследование . Это вызвано мутациями в генах восстановления несоответствия ДНК, которые приводят к микросателлитной нестабильности (повторяющийся сегмент ДНК). У носителей почти определенный риск рака толстой кишки, а у женщин риск развития гинекологического рака составляет до 40%.
Некоторые исследования показали, что селективный модулятор рецептора эстрогена тамоксифен увеличивает риск из-за его частичного агонистического действия эстрогена на эндометрий. Однако недавнее исследование Программы надзора, эпидемиологии и конечных результатов показало, что это не увеличивает общий риск.
Однако недавнее исследование Программы надзора, эпидемиологии и конечных результатов показало, что это не увеличивает общий риск.
Хотя и редко, эстрадиол-секретирующая опухоль яичника s может вызывать гиперплазию эндометрия.
Классификация гиперплазии эндометрия
Всемирная организация здравоохранения (ВОЗ) имеет две классификации гиперплазии эндометрия:
- В зависимости от типа железистых стромальных изменений , которые описываются как простые или сложные
- На основании наличия или отсутствия атипии (структурно нерегулярных или аномальных клеток) в эндометрии
Это приводит к четырем категориям:
- Простой без атипии
- Комплекс без атипии
- Простой с атипией
- Комплекс с атипией
Простой описывается как небольшое увеличение числа желез, которые могут демонстрировать митоз.
Комплекс имеет увеличение отношения железы к строме более чем на 50% с клеточной дезорганизацией. Клетки обычно демонстрируют митоз.
Клетки обычно демонстрируют митоз.
Atypia представлена ядерным увеличением, аномальным хроматином и полиморфизмом.
Патофизиология гиперплазии эндометрия
Гиперплазия эндометрия вызвана повышенным уровнем эстрогена, которому не противодействует прогестерон.
В нормальном цикле эстроген высвобождается из яичников, что вызывает пролиферацию эндометрия при подготовке к имплантации. Овуляция вызывает повышение прогестерона, который стабилизирует и подготавливает эндометрий к возможной имплантации. Если имплантация не происходит, то уровень эстрогена и прогестерона снижается и наступает менструация .
Изображение: «Иллюстрация рака эндометрия». от Blausen Medical Communications, Inc. — Пожертвовано через OTRS, подробности см. в билете. Лицензия: CC BY 3.0
. По мере того, как женщина стареет и достигает перименопаузы и менопаузы , овуляция происходит реже или не происходит совсем.Из-за отсутствия овуляции происходит потеря прогестерона, чтобы противодействовать оставшемуся эстрогену. Затем эстроген способствует усиленному и беспрепятственному росту эндометрия.
Затем эстроген способствует усиленному и беспрепятственному росту эндометрия.
С увеличением пролиферации возникает риск аномальных изменений ядер — атипия. Атипия связана с 60% вероятностью наличия или развития рака эндометрия . Однако во многих случаях гиперплазия проходит сама по себе.
Если развивается злокачественных новообразований , большинство случаев составляют эндометриоидные аденокарциномы 1 типа, которых имеют более благоприятные исходы.
Признаки и симптомы гиперплазии эндометрия
Аномальное маточное кровотечение является наиболее частым признаком.
Дополнительные симптомы могут включать:
- Меноррагия: усиление кровопотери более 80 мл или кровотечение, продолжающееся более 8 дней.
- Менометроррагия: усиление нерегулярных кровотечений (считается смесью меноррагии и метроррагии)
- Кровотечение в постменопаузе: любое количество вагинальных кровотечений, включая кровянистые выделения или окрашивание после того, как женщина уже испытала прекращение менструации из-за менопаузы
Прогрессирование и особые формы гиперплазии эндометрия
Типы, которые представляют собой атипию , имеют самую сильную связь с прогрессированием до рака эндометрия .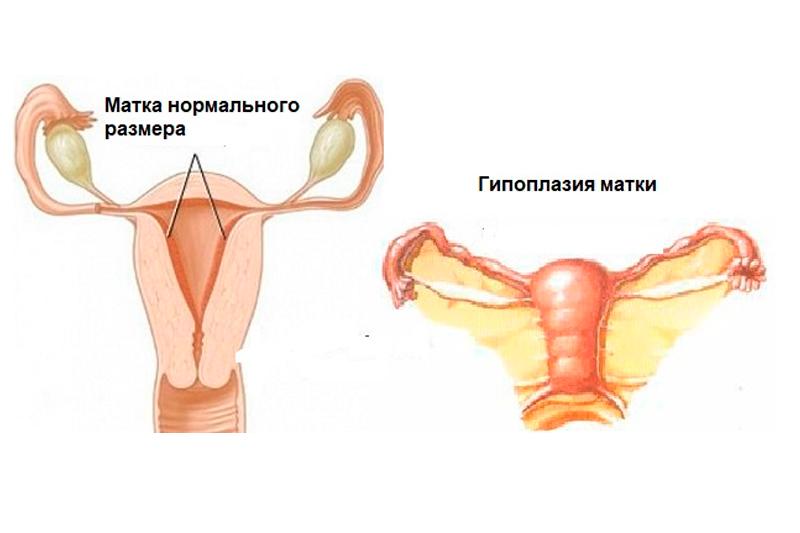
Женщины с синдромом Линча должны проходить скрининг на рак эндометрия начиная с 35 лет, поскольку у них высока вероятность развития этого заболевания (до 40%). Если женщина не планирует в дальнейшем иметь детей, рекомендуется гистерэктомия с двусторонней сальпингэктомией .
Диагностика и патология гиперплазии эндометрия
Не существует официального метода скрининга для населения в целом, поэтому скрининг обычно проводится при наличии признаков или симптомов.
Американский конгресс акушеров и гинекологов рекомендует, чтобы любая женщина старше 35 лет с аномальными маточными кровотечениями проходила скрининг на гиперплазию эндометрия. Также следует обследовать женщин моложе 35 лет, у которых наблюдается аномальное маточное кровотечение, которое не контролируется лекарствами.
Анамнез и физикальное обследование может помочь выяснить этиологию кровотечения. Медицинский осмотр может быть в целом нормальным и не выявить признаков злокачественности.
Изображение: «Процедура трансвагинального ультразвукового исследования». пользователя BruceBlaus. Лицензия: CC BY-SA 4.0
.Первоначальные тесты могут включать трансвагинальное УЗИ для измерения толщины эндометрия и выявления любых других потенциальных причин. Если предполагается, что эндометрий утолщен (> 5 мм), может быть выполнена биопсия эндометрия . Другие методы биопсии могут быть выполнены в операционной, включая дилатацию и выскабливание (обычно называемое «D и C») и гистероскопию .
Патология гиперплазии эндометрияПатология позволяет поставить окончательный диагноз и является наилучшим способом увидеть изменения эндометрия. В клинике для отбора проб ткани эндометрия используется трубка .
Эндометриоид типа 1 отвечает за 80% случаев рака эндометрия; к счастью, имеет благоприятный исход. Гистология показывает повышенное соотношение железы к строме и может быть обозначена как аденокарцинома из-за увеличенного количества и размера желез.
Серозные / светлые клетки 2 типа ответственны за 20% случаев рака эндометрия. В таких случаях исходы хуже из-за миометрия и внематочного вовлечения . Гистология больше зависит от типа видимых злокачественных клеток, но большинство из них имеют аденокарциному или смешанную основу.
Сообщалось о мутациях в p53, PTEN, PIK3CA, K-Ras и β-катенине.
Определение стадии карциномы осуществляется с помощью системы стадирования Международной федерации гинекологии и акушерства (также известной как FIGO) или по шкале TNM (опухоль [T], узлы [N] и метастазы [M]).
Дифференциальная диагностика гиперплазии эндометрия
Дифференциал включает любую причину аномального маточного кровотечения:
- Травмы живота или таза, особенно сексуального характера
- Гинекологический рак или другие злокачественные опухоли с метастазами в матку
- Атрофический вагинит
- Полипы или миомы эндометрия
- Эндометрит
- Сальпингит
- Цервицит
- Лейомиомы
- Менструация
- Вторичное кровотечение при заместительной гормональной терапии
- Беременность
Терапия и профилактика гиперплазии эндометрия
Терапия зависит от типа гиперплазии и стремления пациента к будущей фертильности .
Без атипии вероятность прогрессирования гиперплазии до рака эндометрия составляет 1–3%. Прогестинотерапия — наиболее распространенный метод лечения гиперплазии эндометрия без атипии.
Изображение: «Типы гистерэктомии». Автор: BruceBlaus — Собственная работа. Лицензия: CC BY-SA 4.0
.Прогестин можно вводить перорально или выделять при внутримышечной инъекции или внутриматочной спирали (ВМС). Терапия первой линии включает перорального медроксипрогестерона .Некоторым пациентам можно использовать смешанные эстроген-прогестиновые оральные контрацептивы. Левоноргестрел ВМС , такие как Мирена, оказались очень эффективными при лечении гиперплазии эндометрия и обеспечивают долговременную контрацепцию.
Гиперплазия эндометрия без атипии имеет очень хорошие показатели ответа, регресс наступает в течение трех-шести месяцев. Если по истечении этого времени регресса не произошло, следует увеличить дозу прогестина.
Гиперплазия эндометрия с атипией имеет более высокий риск развития рака. Если будущая беременность нежелательна, то гистерэктомия — лучшее и окончательное лечение. Женщинам в постменопаузе рекомендуется двусторонняя сальпингоофорэктомия .
Если будущая беременность нежелательна, то гистерэктомия — лучшее и окончательное лечение. Женщинам в постменопаузе рекомендуется двусторонняя сальпингоофорэктомия .
Если беременность желательна, то терапия прогестином используется, когда хирургическое вмешательство, даже консервативное, не позволяет забеременеть. Прогестин можно вводить перорально или высвобождать при внутримышечной инъекции или ВМС . Обычными пероральными прогестинами являются мегестрола ацетат и медроксипрогестерон .
Внутримышечная инъекция депо медроксипрогестерона (Депо-Провера) четыре раза в год показала свою эффективность. Опять же, можно использовать такие ВМС, как Мирена.
Если пациент продолжает терапию прогестином, биопсию следует повторять каждые 6–12 месяцев, чтобы отслеживать прогрессирование.
Результаты в целом хорошие, регресс в среднем составляет от шести до девяти месяцев. Текущие исследования показывают, что частота регресса составляет 86%, а частота рецидивов — 23–26%.
Когда возможно метастаза , химиотерапевтический препарат цисплатин оказался эффективным.
Метастазы в лимфатические узлы попадут в тазовые или парааортальные узлы. Если метастазы достигают этих узлов, их необходимо удалить.
В целом, после лечения, пациенты с раком эндометрия имеют 5-летнюю выживаемость 83%.
Осложнения гиперплазии эндометрияГистерэктомия с двусторонней сальпингоофорэктомией у женщин в пременопаузе приведет к хирургической менопаузе и приведет ко всем симптомам менопаузы, которые следует лечить соответствующим образом.
Профилактика гиперплазии эндометрияЖенщины могут принять следующие профилактические меры:
- Женщинам, принимающим эстроген, следует также принимать прогестерон , чтобы предотвратить беспрепятственный эффект эстрогена.
- Молодых женщин с нерегулярными менструациями следует лечить с помощью оральных контрацептивов , которые содержат как эстроген, так и прогестин, чтобы помочь регулировать их циклы.

- Женщины должны поддерживать здоровый индекс массы тела ; тем, кто страдает избыточным весом или ожирением, следует соответственно похудеть.
Курение сигарет было показано, что защищает от рака эндометрия. Однако из-за негативного воздействия курения на легкие и другие органы это не рекомендуется.
Метформин при гиперплазии эндометрия | Cochrane
Мы включили три РКИ, в которых приняли участие 77 женщин. Мы оценили качество доказательств как очень низкое для всех исходов из-за очень серьезного риска систематической ошибки (связанной с плохой отчетностью, выбыванием и ограничениями в дизайне исследования) и неточностью.
Мы провели метаанализ двух испытаний с 59 участниками. При сравнении метформина с мегестрола ацетатом у женщин с гиперплазией эндометрия мы обнаружили недостаточные доказательства, чтобы определить, были ли различия между группами по следующим исходам: регресс гистологии гиперплазии эндометрия в сторону нормальной гистологии (отношение шансов (OR) 3,34, 95% доверительный интервал (ДИ) от 0,97 до 11,57, два РКИ, n = 59, доказательства очень низкого качества), частота гистерэктомий (ОШ 0,91, 95% ДИ 0. 05–15.52, два РКИ, n = 59, доказательства очень низкого качества), и частота аномальных маточных кровотечений (OR 0,91, 95% ДИ 0,05–15,52, два РКИ, n = 44, доказательства очень низкого качества). Мы не нашли данных о рецидивах гиперплазии эндометрия или связанном со здоровьем качестве жизни. Оба исследования (n = 59) предоставили данные о прогрессировании гиперплазии эндометрия в рак эндометрия, а также одно (n = 16) сообщило о некоторых побочных эффектах в группе метформина, в частности о тошноте, тромбозе, лактоацидозе, нарушениях функции печени и почек. .
05–15.52, два РКИ, n = 59, доказательства очень низкого качества), и частота аномальных маточных кровотечений (OR 0,91, 95% ДИ 0,05–15,52, два РКИ, n = 44, доказательства очень низкого качества). Мы не нашли данных о рецидивах гиперплазии эндометрия или связанном со здоровьем качестве жизни. Оба исследования (n = 59) предоставили данные о прогрессировании гиперплазии эндометрия в рак эндометрия, а также одно (n = 16) сообщило о некоторых побочных эффектах в группе метформина, в частности о тошноте, тромбозе, лактоацидозе, нарушениях функции печени и почек. .
В другом испытании с участием 16 участников сравнивали метформин плюс мегестрола ацетат и только мегестрола ацетат у женщин с гиперплазией эндометрия. Мы обнаружили недостаточные доказательства, чтобы определить, были ли различия между группами по следующим исходам: регресс гистологии гиперплазии эндометрия к нормальной гистологии (OR 9,00, 95% ДИ от 0,94 до 86,52, одно РКИ, n = 16, доказательства очень низкого качества), рецидив гиперплазии эндометрия у женщин, достигших регресса (OR не поддается оценке, события не зарегистрированы, одно РКИ, n = 8, доказательства очень низкого качества), прогрессирование гиперплазии эндометрия до рака эндометрия (OR не поддается оценке, события не зарегистрированы, одно РКИ , n = 13, доказательства очень низкого качества) или частоту гистерэктомии (OR 0.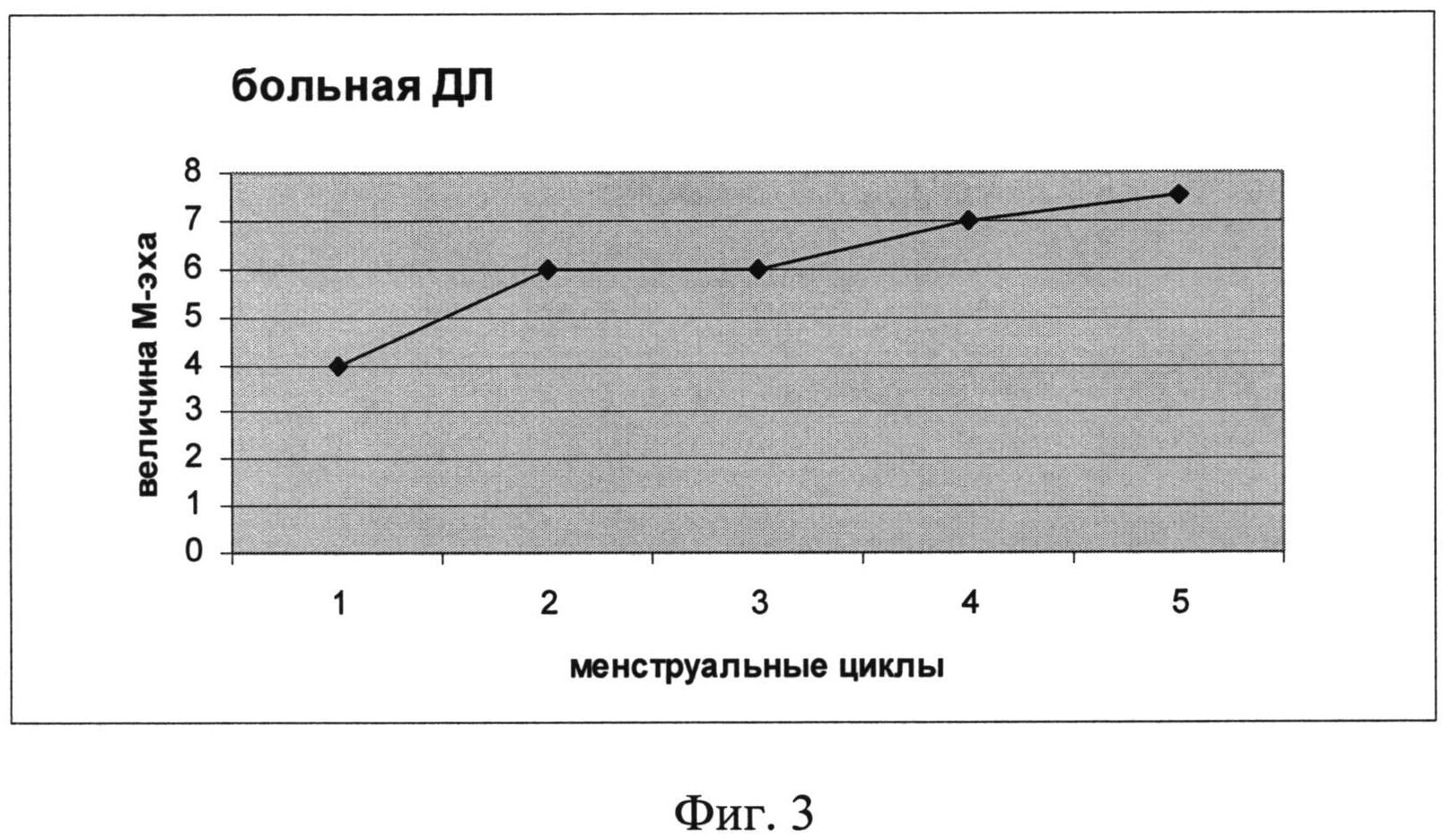 29, 95% ДИ 0,01–8,37, одно РКИ, n = 16, доказательства очень низкого качества). Исследователи не предоставили данных об аномальном маточном кровотечении или качестве жизни, связанном со здоровьем. Что касается побочных эффектов, трое из восьми участников (37,5%) в группе исследования метформин плюс мегестрола ацетат сообщили о тошноте.
29, 95% ДИ 0,01–8,37, одно РКИ, n = 16, доказательства очень низкого качества). Исследователи не предоставили данных об аномальном маточном кровотечении или качестве жизни, связанном со здоровьем. Что касается побочных эффектов, трое из восьми участников (37,5%) в группе исследования метформин плюс мегестрола ацетат сообщили о тошноте.
Гиперплазия эндометрия —
Что такое гиперплазия эндометрия?
Гиперплазия эндометрия возникает, когда эндометрий, слизистая оболочка матки, становится слишком толстым. Это не рак, но в некоторых случаях это может привести к раку матки.
Как эндометрий обычно изменяется на протяжении менструального цикла?
Эндометрий изменяется на протяжении менструального цикла в ответ на гормоны. Во время первой части цикла гормон эстроген вырабатывается яичниками. Эстроген заставляет слизистую оболочку расти и утолщаться, чтобы подготовить матку к беременности. В середине цикла яйцеклетка выходит из одного из яичников (овуляция). После овуляции уровень другого гормона, называемого прогестероном, начинает повышаться.Прогестерон подготавливает эндометрий для приема и питания оплодотворенной яйцеклетки. Если беременность не наступает, уровень эстрогена и прогестерона снижается. Снижение уровня прогестерона вызывает менструацию или отслаивание слизистой оболочки. Как только подкладка полностью сбрасывается, начинается новый менструальный цикл.
После овуляции уровень другого гормона, называемого прогестероном, начинает повышаться.Прогестерон подготавливает эндометрий для приема и питания оплодотворенной яйцеклетки. Если беременность не наступает, уровень эстрогена и прогестерона снижается. Снижение уровня прогестерона вызывает менструацию или отслаивание слизистой оболочки. Как только подкладка полностью сбрасывается, начинается новый менструальный цикл.
Что вызывает гиперплазию эндометрия?
Гиперплазия эндометрия чаще всего вызывается избытком эстрогена без прогестерона. Если овуляция не происходит, прогестерон не производится, и слизистая оболочка не теряется.Эндометрий может продолжать расти в ответ на эстроген. Клетки, составляющие подкладку, могут сбиваться вместе и стать ненормальными. Это состояние, называемое гиперплазией, у некоторых женщин может привести к раку.
Когда возникает гиперплазия эндометрия?
Гиперплазия эндометрия обычно возникает после менопаузы, когда прекращается овуляция и выработка прогестерона прекращается. Это также может произойти во время перименопаузы, когда овуляция может происходить нерегулярно. Ниже перечислены другие ситуации, в которых
Это также может произойти во время перименопаузы, когда овуляция может происходить нерегулярно. Ниже перечислены другие ситуации, в которых
женщин могут иметь высокий уровень эстрогена и недостаточное количество прогестерона:
- Использование лекарств, которые действуют как эстроген
- Долгосрочное использование высоких доз эстрогена после менопаузы (у женщин с не перенесли гистерэктомию)
- Нерегулярные менструации, особенно связанные с синдромом поликистозных яичников или бесплодием
- Ожирение
Какие факторы риска связаны с гиперплазией эндометрия?
Гиперплазия эндометрия чаще встречается у женщин со следующими факторами риска:
- Возраст старше 35 лет
- Белая раса
- Никогда не была беременна
- Пожилой возраст в период менопаузы
- Ранний возраст начала менструации
- В личном анамнезе были определенные состояния, такие как сахарный диабет, синдром поликистозных яичников, заболевание желчного пузыря или заболевание щитовидной железы
- Ожирение
- Курение сигарет
- Семейный анамнез рака яичников, толстой кишки или матки
Какие типы гиперплазии эндометрия ?
Гиперплазия эндометрия бывает простой и сложной. Он также классифицируется по тому, присутствуют или отсутствуют определенные клеточные изменения. Если присутствуют патологические изменения, это называется атипичным. Эти термины объединены для точного описания
Он также классифицируется по тому, присутствуют или отсутствуют определенные клеточные изменения. Если присутствуют патологические изменения, это называется атипичным. Эти термины объединены для точного описания
вида гиперплазии:
- Простая гиперплазия
- Сложная гиперплазия
- Простая атипичная гиперплазия
- Комплексная атипичная гиперплазия
Каковы признаки и симптомы гиперплазии эндометрия?
Наиболее частым признаком гиперплазии является аномальное маточное кровотечение.Если у вас есть что-либо из следующего, обратитесь к врачу:
- Обильное или продолжительное кровотечение во время менструального периода
- Менструальный цикл короче 21 дня (считая с первого дня менструального цикла). от менструального цикла до первого дня следующей менструации)
- Любое кровотечение после менопаузы
Как диагностируется гиперплазия эндометрия?
Есть много причин аномального маточного кровотечения. Если у вас аномальное кровотечение, и вам 35 лет или старше, или если вы моложе 35 лет и ваше аномальное кровотечение не купируется лекарствами, ваш врач может провести диагностические тесты на гиперплазию эндометрия и рак.
Если у вас аномальное кровотечение, и вам 35 лет или старше, или если вы моложе 35 лет и ваше аномальное кровотечение не купируется лекарствами, ваш врач может провести диагностические тесты на гиперплазию эндометрия и рак.
Трансвагинальное ультразвуковое исследование может быть выполнено для измерения толщины эндометрия. Для этого теста вам во влагалище вводится небольшое устройство. Звуковые волны от устройства преобразуются в изображения органов малого таза. Если эндометрий толстый, это может означать наличие гиперплазии эндометрия.
Единственный способ точно определить наличие рака — это взять небольшой образец ткани эндометрия и изучить его под микроскопом. Это можно сделать с помощью биопсии эндометрия, дилатации и выскабливания или гистероскопии.
Какие методы лечения доступны при гиперплазии эндометрия?
Во многих случаях гиперплазию эндометрия можно лечить прогестином. Прогестин вводится перорально, в виде инъекции, внутриматочной спирали или в виде вагинального крема. Сколько и сколько времени вы принимаете, зависит от вашего возраста и типа гиперплазии.Лечение прогестином может вызвать вагинальное кровотечение, подобное менструальному периоду.
Сколько и сколько времени вы принимаете, зависит от вашего возраста и типа гиперплазии.Лечение прогестином может вызвать вагинальное кровотечение, подобное менструальному периоду.
Если у вас атипичная гиперплазия, особенно сложная атипичная гиперплазия, риск рака увеличивается. Гистерэктомия обычно является лучшим вариантом лечения, если вы не хотите больше иметь детей.
Что я могу сделать, чтобы предотвратить гиперплазию эндометрия?
Чтобы снизить риск гиперплазии эндометрия, вы можете предпринять следующие шаги:
- Если вы принимаете эстроген после менопаузы, вам также необходимо принимать прогестин или прогестерон.
- Если у вас нерегулярные менструации, можно порекомендовать противозачаточные таблетки (оральные контрацептивы). Они содержат эстроген вместе с прогестином. Также можно принимать другие формы прогестина.
- Если у вас избыточный вес, может помочь похудание. Риск рака эндометрия увеличивается с увеличением степени ожирения.



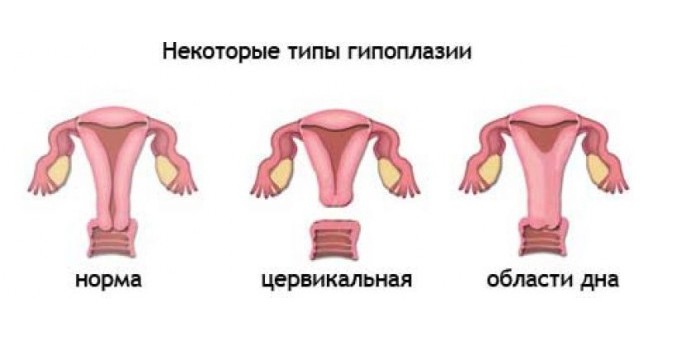 Незаменимый инструмент для выявления опухолевых заболеваний. Магнитный резонанс точно диагностирует спаечный процессв малом тазу, что невозможно сделать только с помощью ультразвукового исследования.
Незаменимый инструмент для выявления опухолевых заболеваний. Магнитный резонанс точно диагностирует спаечный процессв малом тазу, что невозможно сделать только с помощью ультразвукового исследования.



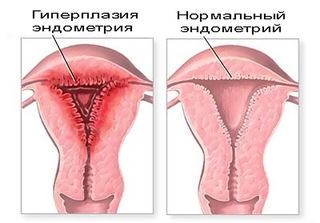 В этом случае необходимо удаление матки. Это особенно важно при атипичной форме, поскольку такое заболевание может перерасти в онкологию.
В этом случае необходимо удаление матки. Это особенно важно при атипичной форме, поскольку такое заболевание может перерасти в онкологию. Вероятность развития рака эндометрия составляет 2-7%.
Вероятность развития рака эндометрия составляет 2-7%.

