Дисбактериоз кишечника. Как лечить дисбактериоз
Организм человека – очень сложная и слаженная система, для нормальной работы которой важно поддержание внутреннего баланса. Но у организма есть и помощники – полезные бактерии, живущие в кишечнике. Они помогают переваривать пищу, получать питательные вещества, более того, они необходимы для работы иммунной системы и защищают организм от распространения вредных, патогенных бактерий. Однако иногда баланс микроорганизмов нарушается, что приводит к неприятным последствиям – развивается дисбактериоз.
Дисбактериоз кишечника – это нарушение состава нормальной микрофлоры кишечника. Количество полезных бактерий снижается, а патогенные микроорганизмы начинают усиленно размножаться. Это заболевание приводит к расстройству пищеварения, дефициту некоторых микроэлементов, снижению иммунитета и плохому самочувствию.
Дисбактериоз кишечника встречается очень часто: по некоторым данным ему подвержены до 90% всех взрослых людей.
Как лечить дисбактериоз?
Если по тем или иным причинам баланс нормальной кишечной микрофлоры был нарушен и развился дисбактериоз кишечника, лечение лучше начинать сразу, до перехода состояния в затяжную форму и развития более серьезных симптомов. Лечение дисбактериоза должно быть комплексным, поэтому как лечить дисбактериоз в каждом конкретном случае лучше всего расскажет лечащий врач. Дело в том, что дисбактериоз не является самостоятельным заболеванием и может быть симптомом различных болезней, чтобы избавиться от дисбактериоза, необходимо вылечить в первую очередь заболевание его вызвавшее.
Тем не менее, существуют общие рекомендации по лечению дисбактериоза кишечника. Для нормализации состава микрофлоры кишечника применяют, так называемые, бактериальные препараты, например, Линекс, Бификол, Энтерол и другие. Эти препараты содержат живые культуры, характерные для нормальной микрофлоры и помогут восстановить баланс. Кроме того, при дисбактериозе полезно употребление продуктов, содержащих лактобактерии и бифидобактерии. Для нормализации работы пищеварительной системы стоит исключить из рациона продукты, раздражающие слизистую кишечника, т.е. на время отказаться от острого, соленого и маринованного. Для того, чтобы предотвратить распространение патогенных микроорганизмов при дисбактериозе кишечника иногда применяют антибактериальные препараты. Однако выбор препарата и продолжительность курса должен оценивать врач. Применение антибиотиков без рекомендации врача может привести к усугублению дисбактериоза.
Ещё статьи:
Подходы к медикаментозному лечению дисбактериоза кишечника | Аджигайтканова С.
 К.
К.Под общим понятием «дисбактериоз» подразумевается клинико–лабораторный синдром, возникающий при ряде заболеваний и клинических ситуаций, характеризующийся изменением качественного и/или количественного состава нормальной микрофлоры, метаболическими и иммунными нарушениями, сопровождающимися у части больных клиническими проявлениями [1]. Таким образом, дисбактериоз – это не диагноз, а состояние.
При дисбактериозе кишечника появляется значительное количество микробов в тонкой кишке и изменение микробного состава толстой кишки. В толстой кишке меняется общее количество и свойства микроорганизмов, усиливается их инвазивность и агрессивность [11].
Дисбактериозами страдают пациенты практически всех стационаров и амбулаторных служб, жители экологически неблагоприятных регионов, нарушения нормальной микрофлоры которых формируются в результате воздействия на организм физических, химических, радиационных и других факторов [4,10].
 В состав флоры содержимого толстого кишечника входят анаэробные и аэробные бактерии. Нормальная микрофлора на 95% состоит из анаэробных видов бактерий, главными из которых являются бифидобактерии и лактобактерии. Функции полезной микрофлоры в организме человека неоценимы. Перечислим наиболее важные из них.
В состав флоры содержимого толстого кишечника входят анаэробные и аэробные бактерии. Нормальная микрофлора на 95% состоит из анаэробных видов бактерий, главными из которых являются бифидобактерии и лактобактерии. Функции полезной микрофлоры в организме человека неоценимы. Перечислим наиболее важные из них.
Защитная функция: нормальная микрофлора кишечника в процессе эволюции приобрела исключительно важную роль в формировании колонизационной резистентности организма. Одним из главных механизмов защиты от колонизации условно–патогенными и патогенными бактериями является присутствие в организме достаточного количества собственной полезной микрофлоры, к которой, в первую очередь, относятся лакто– и бифидобактерии. Очень важным фактором защиты является то, что представители нормофлоры продуцируют бактериоцины, лизоцим и другие антибиотикоподобные вещества, обуславливающие антагонистическую активность этих бактерий. Представители нормофлоры в кишечнике конкурируют с патогенной флорой за аргинин, треонин, аспарагиновую кислоту, серин, за область обитания – экологические ниши.

Синтетическая функция: бактерии кишечной флоры синтезируют витамины, необходимые для метаболических реакций. Бифидобактерии синтезируют витамины группы В, в частности, никотиновую, фолиевую кислоты, тиамин, биотин, цианокобаламин, а также аминокислоты и белки, обеспечивающие их всасывание. Лактобактерии образуют молочную кислоту, продуцируют лизоцим, леколин, низин, ацидофилин и др. Кишечная палочка способствует синтезу иммуноглобулинов, что препятствует развитию инфекции, вырабатывает канцеролитические вещества. Продуцируя молочную кислоту, бифидо– и лактобактерии создают в кишечнике кислую среду, подавляя гнилостную флору и способствуя всасыванию кальция, витамина Д и железа. Большое значение имеет продуцирование анаэробами биологически активных соединений – летучих жирных кислот, которые принимают участие в рециркуляции и абсорбции ионов натрия, калия, хлора, воды, а также кальция, магния и цинка. Кишечная нормофлора способна разлагать белки до конечных продуктов распада (индол, фенол, скатол), утилизировать непереваренные пищевые субстраты, образуя органические кислоты, аминокислоты и другие соединения, которые нормализуют обмен веществ в организме.
Иммунногенная функция: нормальная микрофлора способствует пролиферации плазматических клеток. Бифидобактерии стимулируют синтез антител к овальбумину, лактобактерии повышают активность фагоцитов и лимфоцитов. Повышение численности бифидо– и лактобактерий при их недостатке приводит к положительному эффекту в уменьшении воспалительных процессов слизистой кишечника и увеличении В–лимфоцитов в периферической крови. Иммуностимулирующий эффект под воздействием нормофлоры проявляется усилением фагоцитарной активности макрофагов, моноцитов, увеличением специфического А, синтезом цитокинов, стимуляцией клеточных иммунных механизмов защиты. К сожалению, не до конца оправдывают себя фагопрофилактика и фаготерапия дисбактериоза. Тому есть ряд причин: слишком узкая специфичность, быстрое появление фагорезистентных штаммов патогенных бактерий, а также возможность сенсибилизации организма этим видом чужеродного белка.

Симптомы дисбактериоза напрямую связаны с заболеванием или состоянием, которое вызвало дисбактериоз, и являются неспецифичными и разнообразными: снижение или отсутствие аппетита, тошнота, рвота, металлический привкус во рту, боли в животе (тупые или схваткообразные), возникающие спонтанно и при пальпации, отрыжка, метеоризм, чувство неполного опорожнения кишечника, императивные позывы на дефекацию, запоры, понос, заеды, зуд кожи и слизистых, высыпания на коже (при развитии аллергических реакций), утомляемость.

Необходимо помнить о том, что дисбактериоз всегда усугубляет течение хронических болезней пищеварительного тракта, а потому это состояние всегда требует своевременной диагностики и лечения. Лечение патологических состояний, связанных с дисбактериозом, должно быть комплексным и направленным на устранение избыточного бактериального обсеменения кишечника условно–патогенной микрофлорой, восстановление нормальной микрофлоры и нарушенной моторики толстого кишечника, улучшение кишечного пищеварения и всасывания, стимулирование реактивности организма.
В связи с этим в лечении дисбактериоза кишечника используются следующие группы препаратов: антибактериальные средства и антисептики, пробиотики, пребиотики, синбиотики, пищеварительные ферменты, регуляторы моторики кишечника, стимуляторы реактивности организма.
Применение антибиотиков должно быть оправданным, т.к. они сами могут оказывать губительное влияние на симбионтную микробную флору толстого кишечника. Антибактериальные средства желательно применять при наличии абсолютных показаний, таких как бактериемия и угроза энтерогенного сепсиса, причиной которых является дисбактериоз.
 Достаточно часто антибиотики применяют при избыточном обсеменении тонкой кишки условно–патогенной флорой, при заболеваниях, сопровождающихся нарушением всасывания и моторики кишечника [15]. Применяются препараты фторхинолоновой группы (офлоксацин или норфлоксацин по 400 мг 2 раза в сутки в течение 5–7 дней), пенициллины (амоксициллин по 500 мг 3 раза в сутки в течение 5–7 дней), тетрациклины (доксициклин по 100 мг 2 раза в сутки в течение 3–5 дней).
Достаточно часто антибиотики применяют при избыточном обсеменении тонкой кишки условно–патогенной флорой, при заболеваниях, сопровождающихся нарушением всасывания и моторики кишечника [15]. Применяются препараты фторхинолоновой группы (офлоксацин или норфлоксацин по 400 мг 2 раза в сутки в течение 5–7 дней), пенициллины (амоксициллин по 500 мг 3 раза в сутки в течение 5–7 дней), тетрациклины (доксициклин по 100 мг 2 раза в сутки в течение 3–5 дней).Наиболее предпочтительными препаратами при дисбактериозе кишечника являются антимикробные препараты, такие как ко–тримоксазол (по 480 мг 2 раза в сутки в течение 7 дней), налидиксовая кислота (по 1 г 4 раза в сутки в течение 7 дней), нифуроксазид (по 200 мг 4 раза в сутки в течение 5–7 дней), фуразолидон (по 100 мг 4 раза в сутки в течение 7 дней), антисептики – интетрикс (по 2 капс. 2 раза в сутки в течение 7 дней).
Препараты, применяемые для восстановления нормальной микрофлоры кишечника, принято подразделять на 3 группы: пробиотики, пребиотики и синбиотики [4,6,7,9,14,18].

Пробиотики – это живые микроорганизмы и вещества микробного происхождения, оказывающие при естественном способе введения позитивные эффекты на физиологические, биохимические и иммунные реакции организма хозяина через стабилизацию и оптимизацию функции его нормальной микрофлоры [2,3,14,16,17].
В России зарегистрировано несколько бифидосодержащих препаратов, которые применяются для лечения дисбактериоза в течение 2–3 недель.
Составляющим этих препаратов являются живые бифидобактерии, которые обладают антагонистической активностью против широкого спектра патогенных и условно–патогенных бактерий, основное назначение – обеспечение быстрой нормализации микрофлоры кишечного тракта. Быстрое заселение кишечника бифидобактериями способствует нормализации количественного и качественного состава микрофлоры и стимулирует репаративный процесс слизистой оболочки кишечника [1–6,9]. Ряд преимуществ имеет препарат бифиформ. Первое из них заключается в том, что капсула препарата кислотоустойчива, т.
 е. не растворяется соляной кислотой и пепсином. Это обеспечивает высвобождение в кишечнике высоких концентраций содержащихся в препарате бактерий практически без их инактивации на уровне желудка. Вторым важным преимуществом и особенностью бифиформа является наличие в его капсуле специфических факторов, которые, освобождаясь в кишечнике, ускоряют и усиливают его колонизацию бифидобактериями и энтерококками, причем бифидобактерии колонизируют толстую, а энтерококки – и толстую, и тонкую кишку.
е. не растворяется соляной кислотой и пепсином. Это обеспечивает высвобождение в кишечнике высоких концентраций содержащихся в препарате бактерий практически без их инактивации на уровне желудка. Вторым важным преимуществом и особенностью бифиформа является наличие в его капсуле специфических факторов, которые, освобождаясь в кишечнике, ускоряют и усиливают его колонизацию бифидобактериями и энтерококками, причем бифидобактерии колонизируют толстую, а энтерококки – и толстую, и тонкую кишку.Не менее важное место занимают лактосодержащие препараты. Длительность лечения зависит от причины развития дисбактериоза и индивидуальных особенностей (от 2 недель до 1,5 месяцев). Действующим началом этих препаратов являются живые лактобациллы, обладающие широким спектром антагонистической активности за счет продукции органических кислот, микробного лизоцима, перекиси водорода и различных антибиотических веществ. Лактобациллы синтезируют различные ферменты и витамины, принимающие участие в пищеварительной деятельности желудочно–кишечного тракта, обладают иммуномодулирующим действием, важным для восстановления естественных иммунных факторов защиты организма [2–6,9,17,18].

Коли–содержащие препараты применяются в течение 1–3 месяцев. Они обладают антагонистической активностью в отношении широкого спектра патогенных и условно–патогенных микроорганизмов, включая шигеллы, сальмонеллы, протей; оказывают корригирующее воздействие на нарушенный микробиоценоз; стимулируют местные репаративные процессы в кишечнике; способствуют улучшению пищеварения и обмена веществ; стимулируют естественные факторы защиты. Могут применяться для лечения больных хроническими колитами разной этиологии, реконвалесцентов острых кишечных инфекций при наличии дисфункций кишечника, протекающих на фоне дисбактериоза.
Сухие препараты достаточно долго хранятся при комнатной температуре. Но есть существенный недостаток – после процесса лиофилизации бактерии ослаблены и плохо приживаются в кишечнике, так как требуется 8–10 часов для их перехода от анабиоза к активному физиологическому состоянию, но к этому времени большая их часть уже элиминируется из кишечника.
Жидкие препараты представляют собой микробную массу бактерий в живой активной форме и имеют ряд преимуществ перед сухими: бактерии находятся в активном состоянии и способны к колонизации ЖКТ уже через 2 часа после попадания в организм; жидкие препараты кроме бактерий содержат продукты их жизнедеятельности – незаменимые аминокислоты, органические кислоты, интерферонстимулирующие вещества.

Пребиотики – это препараты немикробного происхождения, способные оказывать позитивный эффект на организм хозяина через селективную стимуляцию роста или усиления метаболической активности нормальной микрофлоры кишечника [1–4,8–9]. В эту группу входят препараты, относящиеся к различным фармакотерапевтическим группам, но обладающие общим свойством – стимулировать рост и развитие нормальной микрофлоры кишечника.
Из пребиотиков чаще всего используется Хилак форте. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочную кислоту, аминокислоты и жирные кислоты. Препарат способствует восстановлению нарушенной нормальной микрофлоры кишечника биологическим путем, вызывая сдвиг рН в ЖКТ в границах физиологической нормы, что создает неблагоприятные условия для развития патогенной и условно–патогенной микрофлоры, обеспечивает санацию кишечника. Продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. Хилак форте назначают по 40–60 капель 3 раза в сутки на срок до 4 нед.
 в сочетании с препаратами антимикробного действия или после их применения.
в сочетании с препаратами антимикробного действия или после их применения.По данным, приведенным в литературе, на сегодняшний день известно, что применение капель Хилак форте у больных хроническими заболеваниями органов пищеварения, осложненных дисбактериозом, способствовало уменьшению частоты дефекаций примерно вдвое уже через 3–5 суток после начала приема препарата. Больные отмечали также значительное уменьшение клинических проявлений. Использование препарата способствовало положительной динамике копрологических показателей: содержание перевариваемой клетчатки, внутриклеточного крахмала и йодофильной микрофлоры, определявшихся в значительном количестве у подавляющего числа больных до начала лечения Хилак форте, существенно уменьшалось в среднем через 2 недели от начала лечения, а к концу курса терапии в фекалиях практически не определялись крахмальные зерна и непереваренные мышечные волокна.
Использование Хилак форте улучшало микробное содержание толстой кишки. В процессе лечения у большинства больных 1 и 2 стадии дисбактериоза кишечника достигалась полная нормализация микробиоценоза.
 У больных с тяжелыми нарушениями кишечной микрофлоры (дисбактериоз 3 и 4 стадии), хотя и не был полностью достигнут эубиоз, наблюдалось уменьшение относительного количества эшерихий, стафилококков и бактерий рода клебсиелл и протея в фекалиях, что свидетельствовало о положительном влиянии препарата на состав кишечной микрофлоры. Кроме того, Хилак форте прекрасно переносился больными. Не было зарегистрировано побочных эффектов, которые бы потребовали его отмены.
У больных с тяжелыми нарушениями кишечной микрофлоры (дисбактериоз 3 и 4 стадии), хотя и не был полностью достигнут эубиоз, наблюдалось уменьшение относительного количества эшерихий, стафилококков и бактерий рода клебсиелл и протея в фекалиях, что свидетельствовало о положительном влиянии препарата на состав кишечной микрофлоры. Кроме того, Хилак форте прекрасно переносился больными. Не было зарегистрировано побочных эффектов, которые бы потребовали его отмены.Нами Хилак форте использовался у больных хронической алкогольной интоксикацией, у которых отмечались клинические проявления дисбактериоза. При длительном применении нормализовался стул, уменьшались диспесические явления.
В качестве пребиотиков также используют такие средства, как лактулоза, кальция пантотенат, лизоцим и др.
Синбиотики – это препараты, полученные в результате рациональной комбинации пробиотиков и пребиотиков. Часто это биологически активные добавки, входящие в состав функционального питания, обогащенные одним или несколькими штаммами представителей родов Lactobacillus и Bifidobacterium.
 В России известны несколько препаратов, содержащих бифидогенные факторы и биомассу B. bifidum, B. adolescentis, L. plantarum, мальтодекстрин, L. acidоphilus, L. bulgaricus, фруктоолигосахариды из топинамбура в комбинации и количестве, наиболее характерных для определенного возраста ребенка, подростка и взрослых лиц.
В России известны несколько препаратов, содержащих бифидогенные факторы и биомассу B. bifidum, B. adolescentis, L. plantarum, мальтодекстрин, L. acidоphilus, L. bulgaricus, фруктоолигосахариды из топинамбура в комбинации и количестве, наиболее характерных для определенного возраста ребенка, подростка и взрослых лиц. Регуляторы пищеварения и моторики кишечника назначаются в зависимости от наличия заболевания, явившегося причиной дисбактериоза.
Для повышения реактивности организма ослабленным больным также применяют иммуностимулирующие средства.
Таким образом, дисбактериоз является сложным симптомокомплексом, возникающим на фоне различных факторов и заболеваний. Лечение дисбактериоза достаточно сложное, требующее большого вклада сил и средств. В связи с этим необходимо проведение вторичной профилактики дисбактериоза: осторожно применять антибактериальные препараты, пытаться своевременно диагностировать и лечить хронические заболевания желудочно–кишечного тракта.
Литература
1. Отраслевой Стандарт «Протокол ведения больных. Дисбактериоз кишечника» (ОСТ 91500.11.0004–2003, Приказ Министерства здравоохранения РФ № 231 от 09.06.2003)
Отраслевой Стандарт «Протокол ведения больных. Дисбактериоз кишечника» (ОСТ 91500.11.0004–2003, Приказ Министерства здравоохранения РФ № 231 от 09.06.2003)
2. Бондаренко В.М., Воробьев А.А. Дисбиозы и препараты с пробиотической функцией. //Журн. микробиол. 2004. № 1.С. 84–92.
3. Бондаренко В.М., Грачева Н.М. Препараты пробиотики, пребиотики и синбиотики в терапии и профилактике кишечных дисбактериозов. // Фарматека. 2003.№ 7. С.56–63.
4. Бондаренко В.М., Грачева Н.М., Мацулевич Т.В. Дисбактериозы кишечника у взрослых. КМК Scientific Press. Москва, 2003. С.224.
5. Бондаренко В.М., Грачева Н.М., Мацулевич Т.В., Воробьев А.А.. Микроэкологические изменения кишечника и их коррекция с помощью лечебно–профилактических препаратов. Журн. гастроэнтерол. гепатол. колопроктол. 2003. № 4 (приложение № 20).С. 66–76.
6. Бондаренко В.М., Чупринина Р.П., Воробьева М.А. Механизм действия пробиотических препаратов. БиоПрепараты. 2003. № 3. С. 2–5.
7. Вахитов Т.Я., Момот Е.Н., Шалаева О.Н.и др. Состав и биологическая активность экзометаболитов Escherichia coli M–17. //Журн. микробиол. 2003; 6: 20–5.
Вахитов Т.Я., Момот Е.Н., Шалаева О.Н.и др. Состав и биологическая активность экзометаболитов Escherichia coli M–17. //Журн. микробиол. 2003; 6: 20–5.
8. Грачева Н.М., Бондаренко В.М. Пробиотические препараты в терапии и профилактике дисбактериоза кишечника. Инфекц. бол. 2004; 2: 53–8.
9. Звягинцева Т.Д., Сергиенко Е.И. Дисбактериоз кишечника: клиническое значение и перспективы лечения. //Эксперим. клин. гастроэнтерол. 2003. № 3. С.70–74.
10. Лобзин Ю.В., Макарова В.Г., Корвякова Е.Р., Захаренко С.М. Дисбактериоз кишечника (клиника, диагностика, лечение). СПб., 2003.
11. Парфенов А.И. Энтерология. Москва., 2002.
12. Парфенов А.И., Осипов Г.А., Ручкина И.Н., Справ.поликл.врача. 2003. №3, Т.3.
13. Чернин В.В., Червинец В.М., Бондаренко В.М., Базлов С.Н. Язвенная болезнь, хронический гастрит и эзофагит в аспекте дисбактериоза эзофагогастродуоденальной зоны. Тверь: Триада, 2004.
14. Collins M.D., Gibson G.R. Probiotics, prebiotics, and synbiotics: approaches for modulating the microbial ecology of the gut. Am.J.Clin.Nutr.1999. Vol.69. № 5. Р.1052–1057.
Am.J.Clin.Nutr.1999. Vol.69. № 5. Р.1052–1057.
15. Corazza GR, Sorge M., Strocchi A., et al . Non–absorbable antibiotics and small bowel bacterial overgrowth.// Ital. J. Gastroenterol. 1992;24:4–9.
16. Floch M.H., Hong–Curtiss J. Probiotics and functional foods in gastrointestinal disorders. Curr. Gastroenterol. Rep. 2001,3(4):343–350.
17. Fuller R. Probiotics: prospects of use in opportunistic infections. – N.Y., 1995.
18. Tannock G.W. Probiotics. A Critical Review. Horizon Sci.Press,Norfolk, England.1999.
.
ДИСБАКТЕРИОЗ КИШЕЧНИКА
ДИСБАКТЕРИОЗ КИШЕЧНИКА
СПИСОК ПРЕПАРАТОВ И ЛЕЧЕНИЕ НАРУШЕННОЙ МИКРОФЛОРЫ КИШЕЧНИКА
Состояние дисбактериоза в той или иной области организма знакомо практически каждому. Под этим понятием современная медицина чаще всего понимает не конкретное заболевание, а следствие какого-либо стороннего фактора, в том числе и болезни, в результате которого нарушается состав и свойства микрофлоры.
Определенный набор групп бактерий присутствует во всем человеческом организме. При этом для каждого конкретного места, будь то ротовая полость, кишечник, горло или влагалище, этот набор микроорганизмов свой. Более того, у каждого человека эти комбинации зачастую индивидуальны. Медики этот оптимальный набор бактерий называют эубиозом, реже биоценозом кишечника, а нарушение его состава, количества или свойств – дисбактериозом. Мы же разберемся в конкретной форме дисбактериоза – нарушении микрофлоры кишечника.
Это состояние или болезнь (дискуссионность последнего термина в отношении дисбактериоза не закрыта до сих пор) проявляется достаточно стандартным перечнем симптомов в зависимости от сложности протекания, но при этом причины возникновения дисбактериоза кишечника могут быть кардинально разные.
Банальные смена режима питания, переезд в другое место с изменением химического состава употребляемой воды, смена климата, стресс, диета могут привести к изменениям условно-патогенной микрофлоры кишечника и проявиться симптомами дисбактериоза. К этому же могут привести и более серьезные предпосылки: пищевое отравление, применение антибиотиков или болезни желудочно-кишечного тракта. И главное во всем этом то, что для избавления от симптомов нарушения микрофлоры кишечника, в первую очередь нужно избавиться от предпосылок возникновения такого состояния.
К этому же могут привести и более серьезные предпосылки: пищевое отравление, применение антибиотиков или болезни желудочно-кишечного тракта. И главное во всем этом то, что для избавления от симптомов нарушения микрофлоры кишечника, в первую очередь нужно избавиться от предпосылок возникновения такого состояния.
КЛАССИФИКАЦИЯ ДИСБАКТЕРИОЗА КИШЕЧНИКА ПО СИМПТОМАТИКЕ
Дисбактериоз по сложности изменений микрофлоры разделяют на четыре стадии, для каждой из которых характерны свои симптомы. Рассмотрим их для наглядности в форме таблицы:
| Стадия дисбактериоза | Симптомы | Способы устранения и возможные последствия |
| Первая стадия | Симптоматика практически не наблюдается. Возможно проявление несистемного урчания в животе. | Дисбактериоз первой стадии возникает сменой режима приема пищи или типа употребляемой воды.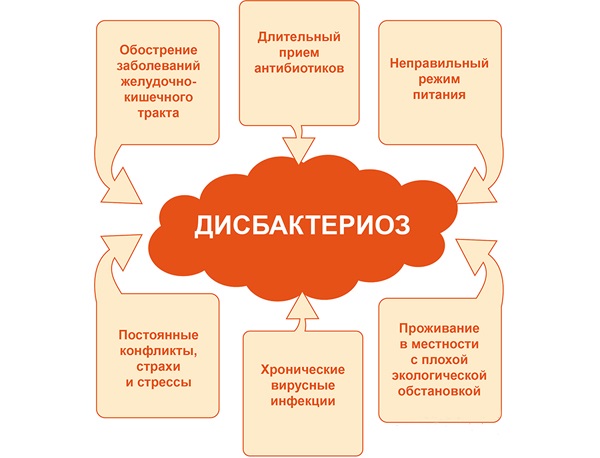 Устранение причины приводит к самостоятельной нормализации микрофлоры. Устранение причины приводит к самостоятельной нормализации микрофлоры. |
| Вторая стадия | Наблюдаются запоры или диарея, снижение аппетита, неприятный привкус во рту, вероятны тошнота и рвота. | Такие симптомы возникают при значительном изменении состава микрофлоры, которое провоцируется приемом антибиотиков или легким пищевым отравлением. |
| Третья стадия | Возникают боли в кишечнике, непереваренная пища выходит в кале, усиливаются симптомы второй стадии. | Дисбактериоз на этой стадии приводит к развитию воспаления стенок кишечника, нарушению процесса пищеварения. Требует медикаментозного вмешательства для избегания серьезных последствий. |
| Четвертая стадия | Симптоматика предыдущих стадий усиливается бессонницей, апатией, депрессией. | При практически полном изменении состава микрофлоры кишечника, развиваются анемия и авитаминоз. Без квалифицированного лечения дисбактериоз четвертой стадии может привести к серьезным инфекционным заболеваниям. |
КЛАССИФИКАЦИЯ ДИСБАКТЕРИОЗА ПО СОДЕРЖАНИЮ МИКРООРГАНИЗМОВ В КАЛЕ
Помимо этого, существует и ещё одна классификация сложности дисбактериоза кишечника, основанная на показаниях лабораторных исследований кала при нарушении микрофлоры. Для взрослых она разделена на две группы. Для наглядности приведем её также в виде таблицы:
| Возраст | Стадия дисбактериоза | Лабораторные показатели |
| До 50 лет | 1 стадия | Заниженный до 105-106 либо завышенный до 109-1010 показатель типичных эшерихий, заниженный до 105-106 показатель лактобактерий и заниженный до 106-107 показатель бифидобактерий. |
| 2 стадия | Завышенный до 105-107 показатель условно-патогенных микроорганизмов, заниженный до 107 показатель бифидобактерий и до 105 лактобактерий. |
|
| 3 стадия | Показатель условно-патогенных микроорганизмов превышает 107, показатель лактобактерий снижен до 105, бифидобактерий – до 107. | |
| После 50 лет | 1 стадия | Показатель типичных эшерихий вышел за пределы 105-1010, показатель лактобактерий снизился до 104 -105 , бифидобактерий – до 106-107 . |
| 2 стадия | Повышение показателя условно-патогенных микроорганизмов повышается до 105-107, показатель лактобактерий снижается до 104, бифидобактерий – до 106. | |
| 3 стадия | Показатель условно-патогенных микроорганизмов превышает 106-107, показатель лактобактерий снижен до 104, бифидобактерий – до 106. |
ВИЗУАЛЬНЫЙ АНАЛИЗ КАЛА ПРИ НАРУШЕНИИ МИКРОФЛОРЫ КИШЕЧНИКА
Также при дисбактериозе кишечника серьезное внимание обращается на характер кишечной патологии, которая достаточно просто определяется по типу и цвету кала, а также по состоянию стула.
Испражнения с желтоватым оттенком свидетельствуют о большом количестве непереваренной клетчатки в кале и об излишках крахмала. Для корректировки стула в таком случае рекомендуется белковая пища (отварное мясо, яйца, творог), которой нужно заместить сырые овощи, углеводы и молоко.
Очень темный кал с сильными зловониями демонстрирует наличие щелочной реакции в кишечнике, а также непереваренную волокнистую пищу. В этом случае из рациона нужно исключить мясо и жиры, возместив потребление калорий за счет отварных овощей и кисломолочных продуктов.
Дисбактериоз кишечника, который сопровождается поносом, устранять нужно диетой, основанной на «мягкой» пище. Блюда в рационе не должны быть ни горячими, ни холодными, пища по возможности должна быть отварная и протертая.
Если же нарушение микрофлоры кишечника проявляется запорами, то рацион нужно насытить продуктами с большим количеством клетчатки: яблоками, капустой, морковью, абрикосами.
ЛЕЧЕНИЕ ДИСБАКТЕРИОЗА У ВЗРОСЛЫХ
В начале мы уяснили, что, если обнаружен дисбактериоз кишечника лечение в первую очередь предполагает устранение причин его возникновения: лечение болезни, которая к нему привела, завершение курса приема антибиотиков или возвращение к исходному состоянию своего рациона. Но в большинстве случаев лечение требуется и для снятия симптомов нарушенной микрофлоры, и для ее восстановления. Для этих целей современная медицина рекомендует три типа терапии.
Но в большинстве случаев лечение требуется и для снятия симптомов нарушенной микрофлоры, и для ее восстановления. Для этих целей современная медицина рекомендует три типа терапии.
ДИЕТА ПРИ ДИСБАКТЕРИОЗЕ
Правильное питание при нарушении микрофлоры кишечника, особенно на начальных стадиях, способно полностью устранить проблему дисбактериоза. Выше мы уже рассмотрели варианты изменения рациона для нормализации стула, теперь же рассмотрим ряд других правил питания при этом состоянии.
Рацион человека при дисбактериозе должен быть максимально сбалансирован. В нем должны в достаточных количествах присутствовать белки, жиры и углеводы, а также жидкость. Врачи рекомендуют за полчаса до приема пищи выпивать стакан теплой воды.
Помимо этого, режим питания должен включать в себя пять приемов пищи, пусть и с меньшими порциями, а также с снижением нагрузок на кишечник перед сном.
Немаловажно, чтобы в употребляемых при дисбактериозе продуктах присутствовали следующие вещества:
- бифидо- и лактобактерии, которыми насыщены кисломолочные продукты и натуральное сливочное масло;
- пектины и пищевые волокна, содержащиеся в достаточных количествах в капусте, моркови, свекле и морских водорослях;
- аминокислоты глутамин и аргинин, источники которых – это курица, говядина, кисломолочные продукты, рыба, петрушка, шпинат, орехи, тыквенные семечки, пшеничная мука, горох.

Анализируя приведенный перечень продуктов можно прийти к выводу, что диета при дисбактериозе – это вовсе не перечень ограничений, а вкусное, полезное и сбалансированное питание. Главное, не переедать, не злоупотреблять «тяжелыми» продуктами, а также избегать в этот период употребления жаренного, острого и прочих, не самых полезных блюд.
ПРЕБИОТИКИ И ПРОБИОТИКИ ПРИ ДИСБАКТЕРИОЗЕ КИШЕЧНИКА
Для лечения дисбактериоза используются пребиотические и пробиотические препараты, которые, по заверениям, прекрасно справляются с нарушенной микрофлорой кишечника. Несмотря на схожесть названий, по своей сути пребиотики и пробиотики – кардинально разные препараты и стоит разобраться в их определении подробнее.
Пребиотики – это вещества, которые при попадании в кишечник оказывают положительное влияние на рост и активность имеющейся там полезной микрофлоры.
Пребиотики не всасываются органами желудочно-кишечного тракта и, если говорить совсем уж простым языком, являются кормом для нашей полезной микрофлоры. Среди фармацевтических форм пребиотиков чаще всего назначаются Лактулоза, Лактитол, Хилак Форте. Это лишь основные названия препаратов, так как их коммерческих наименований существуют десятки.
Среди фармацевтических форм пребиотиков чаще всего назначаются Лактулоза, Лактитол, Хилак Форте. Это лишь основные названия препаратов, так как их коммерческих наименований существуют десятки.
Помимо этого, есть и натуральные продукты, которые являются пребиотиками. Среди них молочные продукты, лук и чеснок, злаковые.
Теперь же о пробиотиках. Эти препараты являются набором необходимых организму человека микроорганизмов, которые при попадании в кишечник в достаточном количестве оказывают положительное влияние на состояние микрофлоры. При этом их применение является достаточно спорным вопросом.
Дело в том, что непосредственное введение микроорганизмов в виде пробиотиков имеет множество условностей. Одни микроорганизмы нужны в таких количествах, что получить их извне затруднительно, другие попросту ввести в живом виде нереально. Да и лабораторных доказательств реальной пользы от использования пробиотиков не так уж и много.
Из пробиотиков, положительное действие которых подтверждено исследованиями, в аптеках можно найти лактобактерии и бифидобактерии (Линекс, Бифиформ, Бифидумбактерин, Лактобактерин), сахаромицеты Буларди, энтерококки.
ЛЕЧЕНИЕ СЛОЖНЫХ ФОРМ ДИСБАКТЕРИОЗЕ
В тяжелых же формах дисбактериоз кишечника лечится более сложными фармацевтическими препаратами, которые делятся на три условных группы.
Первая из них – это антибактериальные средства. Они действуют на определенный тип условно-патогенной микрофлоры, останавливая ее рост и распространение. Назначаются антибактериальные препараты (кишечные антисептики) в зависимости от микроорганизма, который вызвал нарушение микрофлоры.
| Условно-патогенный микроорганизм | Применяемый антибактериальный препарат |
| Энтерококки | Эрсефурил, Фуразолидон, Энтерофурил, Левомицитин, макролиды. |
| Протеи | Невиграмон, Сульгин, Эрсефурил, Энтерофурил. |
| Стафилококки | Пиобактериофаг, Бактериофаг стафилококковый. |
| Кандиды и прочие грибковые агенты | Флуконазол, Микосист, Тербинафин, Амбизом. |
| Клостридии | Метронидазол, Ванкомицин. |
| Синегнойная палочка | Канамицин,Гентамицин. |
В том же направлении, что и антибактериальные средства, действуют и бактериофаги. В их составе содержатся специальные вирусы, которые подавляют определенный вид микроорганизмов. Как и антибактериальные препараты, бактериофаги делятся на группы по типу бактерий: синегнойные, стафилококковые и так далее.
Ну и напоследок нужно рассмотреть фармацевтические препараты, которые дополнительно назначают при дисбактериозе и которые устраняют его симптом и возможные последствия.
Иммуномодуляторы – средства для улучшения защитных свойств организма, прием которых при нарушении микрофлоры кишечник положительно влияет на процесс ее восстановления. Применение иммуномодуляторов должно проходить исключительно по назначению врача, а предпочтение стоит отдавать средствам на растительной основе: настойки эхинацеи и лимонника, Прополис, Дибазол.
Антигистаминные средства. Используются для избегания возникновения аллергических реакций, которые могут развиваться на фоне дисбактериоза кишечника. Самые простые из них – Цетрин, Зиртек и Кларитин, которые и назначаются в большинстве случаев.
Спазмолитики, применение которых зачастую необходимо при дисбактериозе, который сопровождается диареей. Самым популярным спазмолитическим средством является Но-Шпа, а конкретно от поноса рекомендуется Лоперамид. Если же нарушение микрофлоры кишечника сопровождается запорами, то для их устранения используются специальные свечи, вазелиновое масло, препарат Форлакс.
ДИСБАКТЕРИОЗ В СОВРЕМЕННОЙ МЕДИЦИНЕ
Мы уже отмечали вначале, что дисбактериоз отдельной болезнью классифицируется только на территории бывшего Советского Союза. Западная медицина обозначает его исключительно как состояние, спровоцированное определенными предпосылками. Дискуссии о правильности того или иного обозначения для простых людей вряд ли имеют смысл, но все же обозначим ряд интересных фактов, касающихся дисбактериоза:
- В Международной классификации болезней (официальном документе Всемирной организации охраны здоровья) диагноза «дисбактериоз» не существует.
 Максимально схожий с ним диагноз – СИБР (синдром избыточного бактериального роста). Ставится он при обнаружении более 105 микроорганизмов в миллилитре аспирата, взятого из тонкой кишки.
Максимально схожий с ним диагноз – СИБР (синдром избыточного бактериального роста). Ставится он при обнаружении более 105 микроорганизмов в миллилитре аспирата, взятого из тонкой кишки. - Западная медицина достаточно скептически относится к анализу кала для изучения микрофлоры кишечника. По мнению врачей, такое исследование не позволяет сделать какие-либо выводы, так как понятие «нормальной микрофлоры кишечника» очень размыто и сугубо индивидуально для каждого человека.
- На территории бывшего СССР понятие дисбактериоза очень активно распространяется производителями лекарственных препаратов. Оправдано ли это или же под этим продвижением скрыта лишь коммерческая выгода, судить сложно.
- Многие медики очень скептически относятся к использованию при нарушенной микрофлоре кишечника пробиотиков и бактериофагов. По их мнению, полученные извне микроорганизмы практически не имеют шансов прижиться в кишечнике, а бактериофаги перевариваются в желудке и никакой приписываемой им пользы не приносят.

Так что единственный верный вывод о дисбактериозе – это самое спорное заболевание в современной медицине. Но симптомы, как и причины возникновения у него вполне конкретные и устранять их можно абсолютно эффективно.
https://med.vesti.ru/articles/zabolevaniya/disbakterioz-kishechnika-spisok-preparatov-i-lechenie-narushennoj-mikroflory-kishechnika/
Записаться на консультацию к специалистам медицинского центра «ВИТА» вы можете по телефонам:
8-909-557-47-57
8 (815 36) 740-10
или отправить заявку, воспользовавшись услугой сайта ЗАПИСЬ НА ПРИЕМ.
КИШЕЧНЫЙ ДИСБАКТЕРИОЗ | #05-06/01 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи.
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 1014, что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 1011 бактерий, что составляет 30% сухого остатка кишечного содержимого.
Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 1011 бактерий, что составляет 30% сухого остатка кишечного содержимого.
Нормальная микробная флора кишечника
В тощей кишке здоровых людей находится до 105 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 107–108 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 1011 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м2. Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические особенности дисбактериоза
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В12-дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Основным симптомом псевдомембранозного колита является обильная водянистая диарея, началу которой предшествовало назначение антибиотиков. Затем появляются схваткообразные боли в животе, повышается температура тела, в крови нарастает лейкоцитоз. Эндоскопическая картина псевдомембранозного колита характеризуется наличием бляшковидных, лентовидных и сплошных «мембран», мягких, но плотно спаянных со слизистой оболочкой. Изменения наиболее выражены в дистальных отделах ободочной и прямой кишок. Слизистая оболочка отечная, но не изъязвлена. При гистологическом исследовании обнаруживают субэпителиальный отек с круглоклеточной инфильтрацией собственной пластинки, капиллярные стазы с выходом эритроцитов за пределы сосудов. На стадии образования псевдомембран под поверхностным эпителием слизистой оболочки возникают экссудативные инфильтраты. Эпителиальный слой приподнимается и местами отсутствует; оголенные места слизистой оболочки прикрыты лишь слущенным эпителием. На поздних стадиях болезни эти участки могут занимать большие сегменты кишки.
Затем появляются схваткообразные боли в животе, повышается температура тела, в крови нарастает лейкоцитоз. Эндоскопическая картина псевдомембранозного колита характеризуется наличием бляшковидных, лентовидных и сплошных «мембран», мягких, но плотно спаянных со слизистой оболочкой. Изменения наиболее выражены в дистальных отделах ободочной и прямой кишок. Слизистая оболочка отечная, но не изъязвлена. При гистологическом исследовании обнаруживают субэпителиальный отек с круглоклеточной инфильтрацией собственной пластинки, капиллярные стазы с выходом эритроцитов за пределы сосудов. На стадии образования псевдомембран под поверхностным эпителием слизистой оболочки возникают экссудативные инфильтраты. Эпителиальный слой приподнимается и местами отсутствует; оголенные места слизистой оболочки прикрыты лишь слущенным эпителием. На поздних стадиях болезни эти участки могут занимать большие сегменты кишки.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.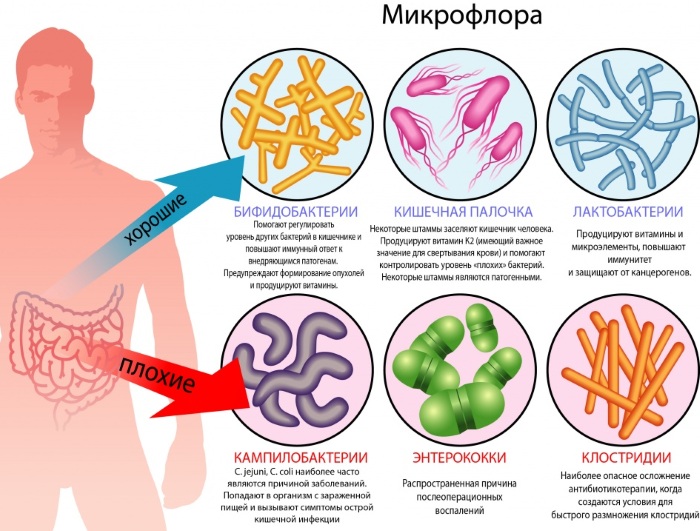
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма.
Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
Лечение
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.

Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия.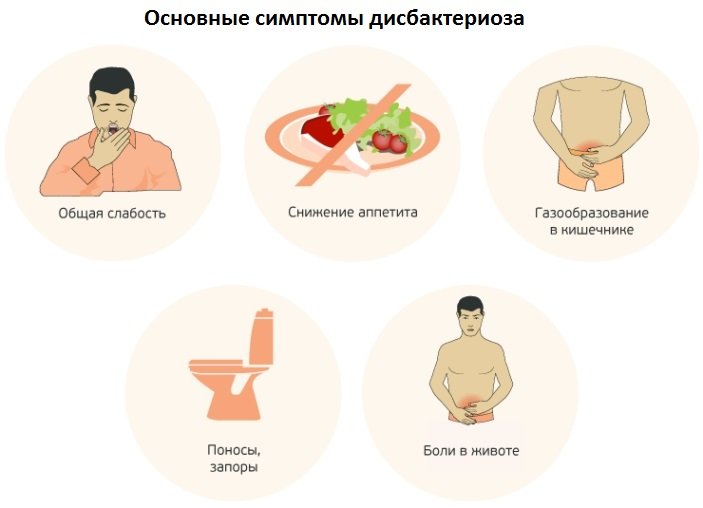 Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Дисбактериоз кишечника симптомы и лечение у взрослых
22. 11.2017Новости
партнеровПросмотров: 1828
11.2017Новости
партнеровПросмотров: 1828При диагнозе дисбактериоз кишечника симптомы и лечение у взрослых знать важно, так как это поможет вовремя заметить нарушения в работе организма и избежать осложнений. Для того чтобы организм нормально работал, в нем всегда должны находиться бактерии. Больше всего их в ЖКТ. Определенный баланс позволяет им контролировать работу кишечника и, как следствие, всех остальных органов и систем. Нарушение баланса называется дисбактериозом.
Симптоматика
Выделяют пять основных признаков развития дисбактериоза:
- Хронический запор, частые расстройства желудка или чередование этих неприятных явлений. Они не зависят от питания. Даже если в рационе присутствует достаточное количество питательных веществ и жидкости, стул не наладится. А все из-за того, что нарушен процесс поглощения жидкости стенками кишечника.
- Чрезмерное газообразование (метеоризм). Является следствием нарушения процесса переваривания пищи.
 Газы есть и в хорошо функционирующем организма. Но в нем налажен процесс их выведения. При дисбактериозе газы скапливаются, приводя к вздутию и болевым ощущениям.
Газы есть и в хорошо функционирующем организма. Но в нем налажен процесс их выведения. При дисбактериозе газы скапливаются, приводя к вздутию и болевым ощущениям. - Гниение и брожение в кишечнике. Проявляется вздутием, урчанием, тяжестью, коликами, тошнотой, изжогой и т.д.
- Неприятный запах изо рта, чрезмерное потоотделение, сильная слабость, аллергические реакции.
- Дефицит витаминов и других полезных веществ. Признаками гиповитаминоза являются утомляемость, нарушения сна (сонливость или бессонница), отсутствие работоспособности, проблемы с памятью, нестабильное эмоциональное состояние, раздражительность. Плюс ко всему ухудшается внешний вид человека. Волосы становятся тонкими и ломкими, ногти ломаются и расслаиваются, кожа становится проблемной. Может нарушиться и работа внутренних органов и систем.
Все эти симптомы требуют пристального внимания и немедленного обращения к врачу.
Медикаментозное лечение и правильное питание
Для лечения дисбактериоза кишечника используют несколько видов препаратов:
- Антибиотики и антигрибковые средства.
 Помогают очистить кишечник от болезнетворных микроорганизмов.
Помогают очистить кишечник от болезнетворных микроорганизмов. - Сорбенты. Собирают и выводят скопившиеся шлаки и остальные ненужные вещества.
- Пробиотики. Засеивают кишечник нужными бактериями.
- Пребиотики. Способствуют росту «правильной» микрофлоры.
Наряду с применение лекарственных средств необходимо пересмотреть свой рацион.
При лечении дисбактериоза питание должно подчиняться нескольким правилам:
- исключить из меню острые и жирные блюда;
- убрать те продукты, которые приводят к брожению. Это капуста, яблоки, хлеб, сдобная выпечка и т. д.;
- категорически запрещено употреблять спиртные напитки;
- чай и другие напитки можно пить только через 30 мин после приема пищи. Также нельзя запивать еду, поскольку это сильно затрудняет процесс ее переваривания;
- как можно чаще нужно употреблять кефир, йогурты и другие продукты, в составе которых есть живые бактерии;
- важно употреблять больше клетчатки.
 Она содержится в овощах, фруктах, злаках и хлебе из муки грубого помола;
Она содержится в овощах, фруктах, злаках и хлебе из муки грубого помола; - исключить сладости, мороженое и кофе;
- покупать свежие продукты, в которых содержится минимум консервантов, красителей и других вредных веществ.
Соблюдение этих простых рекомендаций и прием лекарственных средств помогут в короткие сроки восстановить микрофлору в кишечнике и наладить его работу.
Народные рецепты
Средства народной медицины, как и медикаменты, имеют показания и противопоказания. Поэтому их применение лучше обсудить с врачом.
Есть несколько природных лекарств, способствующих улучшению общего состояния организма и в частности кишечника:
- Чеснок. Необходимо съедать по 1 зубочку дважды в день. Первый раз утром натощак, а второй перед сном (через 22 часа после последнего приема пищи). Запивать можно водой, кефиром и другими напитками. Альтернативный вариант – чесночная настойка. Для ее приготовления нужен собственно чеснок и кислое молоко.
 Ингредиенты смешать и оставить на 2 часа для настаивания. Полученное средство поможет поддерживать баланс бактерий на должном уровне.
Ингредиенты смешать и оставить на 2 часа для настаивания. Полученное средство поможет поддерживать баланс бактерий на должном уровне. - Черемуха, кора дуба, кожура граната, корни кровохлебки. Эти растения оказывают на организм вяжущее действие. Благодаря этому, они эффективно борются с поносом.
- Если нужно справиться с запорами, на помощь придут природные слабительные – сена, корень крушины, сок алоэ. Не советуется применять тем, у кого есть геморрой и трещинки в области заднепроходного отверстия.
- Уничтожить микробов, вирусы и грибок помогут ягодные компоты и морсы (малина, черника, клюква, брусника и прочие).
Применение средств народной медицины должно быть частью комплексного лечения. Самостоятельно полностью справиться с дисбактериозом они не могут.
Что такое дисбактериоз? Это нарушение баланса бактерий, которые живут в кишечнике. Это состояние проявляется в неприятном запахе изо рта, частых поносах или запорах, гиповитаминозе и т.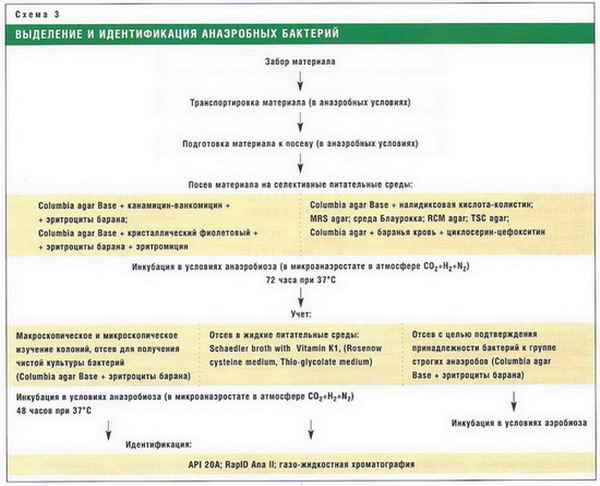 д. Избавиться от него можно с помощью грамотно подобранного лечения, которое подразумевает прием медикаментов, соблюдение диеты и использование средств народной медицины.
д. Избавиться от него можно с помощью грамотно подобранного лечения, которое подразумевает прием медикаментов, соблюдение диеты и использование средств народной медицины.
Источник: http://www.proctologi.com
🧬 Сумасшедший дисбактериоз
Слово «дисбактериоз» последнее время внушает практически мистический ужас — на него списывают все практически беды человечества. Болит живот? — Дисбактериоз! Прыщи? Расстройство желудка? Низкий жизненный тонус? — Дисбактериоз! Буркает, кастрюкает, да и вообще как-то не так? Вы еще сомневаетесь — это он, страшный и ужасный, Дис-бак-те-ри-оз…
Есть правда и обратная сторона — некоторые утверждают, что никакого дисбактериоза не существует. Нет на Западе такого понятия. И даже среди врачей эти мифы распространены: одни говорят «есть» и упорно его лечат, другие — «нет» и «не занимайтесь ерундой». Попробуем разобраться более детально с кандидатом медицинских наук, гастроэнтерологом и гепатологом GMS Clinic Сергеем Вяловым.
«А был ли мальчик?»
Для начала важно признать, что от микробов мы никуда не денемся. Они есть на коже, на еде, по разным оценкам, у нас в кишечнике их около 2-3 кг. Это много. У некоторых людей это почти 5 % веса. Поэтому неважно, как называется нарушение в кишечнике, но надо понимать, каково оно. В России, ещё во времена Мечникова, было открыто взаимодействие бактерий и фагоцитоза. Доказано, что это взаимодействие связано с работой иммунной системы. Но потом про это забыли. Позже западные коллеги вспомнили про это. Только назвали не «дисбактериозом», а «неправильной колонизацией кишечника» в немецком варианте, или, например, «синдромом избыточного бактериального роста» в английском. Суть одна, а названия — разные. Вот вам и смута в людских сердцах (и, как следствие, желудочно-кишечных трактах).
Дисбактериоз — есть! Он не может не есть…
В глобальном плане, нас не интересует количество нормальных бактерий. Они прекрасно живут и размножаются, если им комфортно. Но! Если мы включим в комнате температуру плюс 50 градусов, то дееспособные люди разбегутся из нее очень быстро. Тоже самое и с бактериями — они спешно покидают организм, если им некомфортно. Нарушения микрофлоры кишечника являются последствием какого-либо заболевания. Если нарушение есть по анализу или по метеоризму, боли в животе, и т. д. — надо понимать, отчего оно возникло. Либо это последствие приема антибиотиков, либо это наличие заболевания в кишечнике. Важно понимать: это временное нарушение после эпизода отравления или пищевой инфекции, или это воспалительный процесс, который надо лечить.
Они прекрасно живут и размножаются, если им комфортно. Но! Если мы включим в комнате температуру плюс 50 градусов, то дееспособные люди разбегутся из нее очень быстро. Тоже самое и с бактериями — они спешно покидают организм, если им некомфортно. Нарушения микрофлоры кишечника являются последствием какого-либо заболевания. Если нарушение есть по анализу или по метеоризму, боли в животе, и т. д. — надо понимать, отчего оно возникло. Либо это последствие приема антибиотиков, либо это наличие заболевания в кишечнике. Важно понимать: это временное нарушение после эпизода отравления или пищевой инфекции, или это воспалительный процесс, который надо лечить.
Не ждать милостей от природы, взять их у нее — наша задача!
Сегодня существует высокотехнологическое производство лактобактериальных препаратов, где выращивают микроорганизмы, прицельно действующие на какое-нибудь звено или процесс. Например, препараты, препятствующие побочному действию антибиотиков.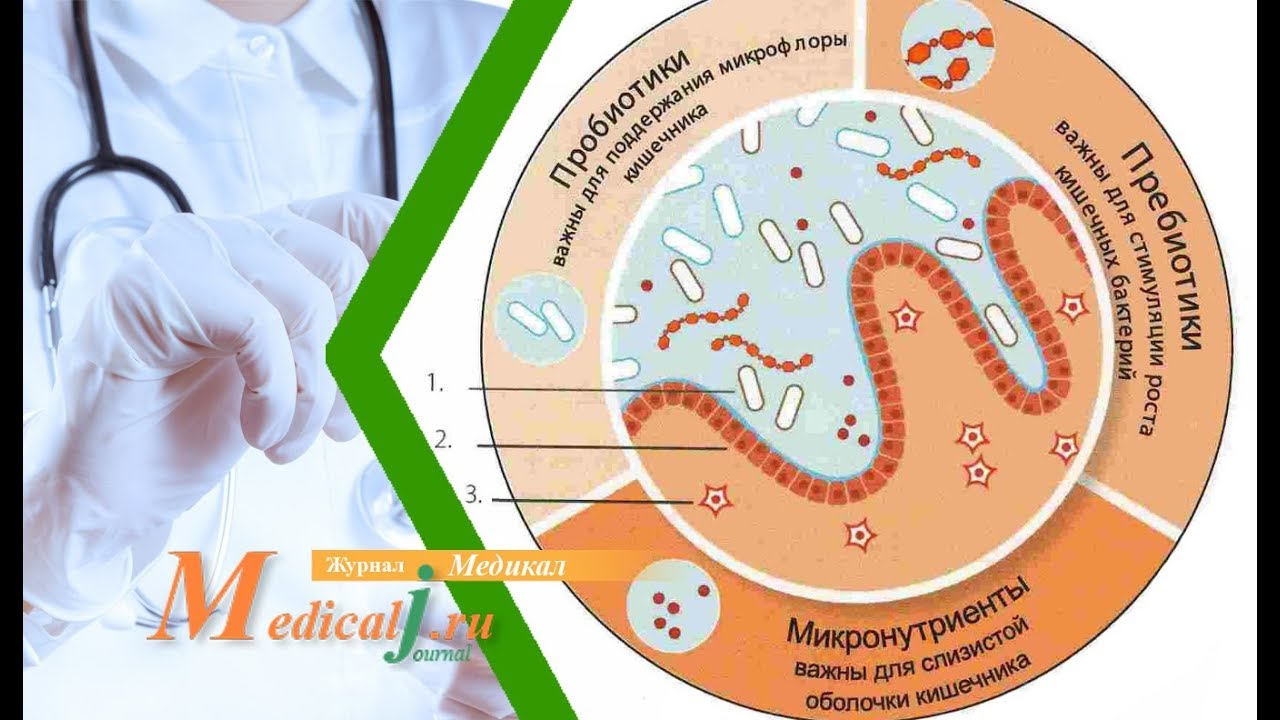 И они прекрасно с этим справляются. То есть не развиваются на фоне приема антибиотиков ни диарея, ни колиты.
И они прекрасно с этим справляются. То есть не развиваются на фоне приема антибиотиков ни диарея, ни колиты.
Есть препараты бактерий, выращенные, чтобы влиять на иммунную систему — и это не пробиотики, которые продаются в аптеках.
Есть препараты, недоступные в России, которые улучшают состояния у людей с энцефалопатией. Есть те, которые улучшают состояние у больных депрессией. И это доказанный эффект!
Напутственное слово
По большому счету, вреда от приема бактерий не будет. Пользы, правда, тоже может не быть.
Одно важно — в случае воспалительных процессов лечение только лишь бактериями может привести к серьезным осложнениям.
А еще с помощью грамотно подобранных бактерий можно добиться хороших результатов при различных, на вид не очень связанных с ЖКТ, заболеваний. Но тут, конечно, нужен грамотный специалист.
Лечение дисбактериоза у взрослых и детей
Микрофлора кишечника — это совокупность различных микроорганизмов, представляющих сбалансированную систему, в которой количественное и качественное изменение хотя бы одного компонента, влияет на всю систему в целом. В кишечнике здорового человека обитает более 500 видов микроорганизмов. Они участвуют в:
В кишечнике здорового человека обитает более 500 видов микроорганизмов. Они участвуют в:
- переваривании пищи,
- усвоении витаминов,
- отчасти стимулируют сокращение гладкомышечных волокон в стенке кишечника (улучшается перистальтика),
- нейтрализации токсических веществ,
- производят ряд веществ, играющих вспомогательную роль в работе многих систем организма.
Микрофлора кишечника индивидуальна у каждого человека и может иметь некоторые отклонения после перенесенных заболеваний или после воздействия некоторых агрессивных факторов.
Поэтому результаты анализов надо сравнивать с нормальными показателями и сопоставлять с клинической картиной. Т.е. решение о наличии у пациента дисбактериоза, является во многом субъективным. Это состояние требует тщательного исследования.
Почему возникает патология?
Причинами дисбактериоза могут быть:
- Прием лекарственных препаратов (антибиотики, химиотерапия, цитостатики, глюкокортикойды и т.
 д)
д) - Инфекционные заболевания ЖКТ.
- Ослабленный иммунитет
- Голодание, плохое питание.
- Стресс
- Смена географической зоны или страны проживания
- Ионизирующее излучение
Заболевание нередко встречается у беременных, что связано с гормональными изменениями в организме.
Дисбактериоз может способствовать снижению как местного, так и общего иммунитета. Это приводит к быстрой утомляемости, частым простудным заболеваниям, вялости. Могут возникнуть угревые высыпания в зрелом возрасте, аллергические реакции.
Прием у врача: диагностика
Помимо осмотра пациента и изучения жалоб, «золотым» стандартом на выявление дисбиоза являются:
- лабораторное исследование кала;
- ПЦР-диагностика – помогает определить возбудителя патологии;
- биохимический анализ микробных метаболитов (жирных кислот, которые вырабатываются бактериями).
- общий анализ крови.
 Иногда требуется консультация других узких специалистов.
Иногда требуется консультация других узких специалистов.Лечение дисбактериоза кишечника
Терапия направлена на уничтожение патогенных микроорганизмов и восстановление оптимального баланса кишечной микрофлоры. Для этого используются бактериофаги, пребиотики и пробиотики. Иногда целесообразно использование кишечных антисептиков (антибактериальные препараты).
Важной составляющей лечения является диета. Дисбактериоз — заболевание, которое нуждается в индивидуально подобранной схеме лечения. Врачи медицинского центра French Clinic используют передовые наработки в области диагностики и лечения дисбактериоза. Современная лаборатория позволит сдать все анализы в короткий срок и в одном месте. Запишитесь к нам на первичную консультацию.
ЗАПИШИТЕСЬ НА ПРИЕМ К ГАСТРОЭНТЕРОЛОГУ
Медицинский центр French Clinic оснащен передовым европейским диагностическим оборудованием. В нашем центре работают опытные врачи, которые постоянно повышают квалификацию не только в России, но и за рубежом. Мы поможем восстановить здоровье и хорошее самочувствие.
Мы поможем восстановить здоровье и хорошее самочувствие.
Оставьте свой номер телефона.
Вам перезвонит администратор клиники.
Популярные вопросы
1. Могут ли другие заболевания способствовать развитию дисбактериоза ?
Конечно. Привести к нарушению кишечной микрофлоры могут болезни ЖКТ. Например, язва, панкреатит, гастрит, патологии печени. Также влияют эндокринные заболевания.
2. Как избежать появления дисбиоза при приеме антибиотиков?
Принимать антибиотики необходимо только по предписанию врача в строго назначенной дозе. Для профилактики рекомендуется параллельный курс пробиотиков..
3. Могут ли появлению дисбактериоза способствовать гормональные препараты?
Да, неправильно подобранный курс гормональных препаратов может пагубно отразиться на состоянии микрофлоры кишечника.
IJMS | Бесплатный полнотекстовый | Желудочно-кишечные расстройства и метаболический синдром: дисбактериоз как ключевое звено и общие биологически активные компоненты питания, полезные для их лечения
1.
 Введение Желудочно-кишечные (ЖКТ) расстройства, распространенность которых увеличилась за последние несколько десятилетий, характеризуются физиологическими и морфологическими аномалиями: система желудочно-кишечного тракта, которые часто возникают в сочетании и включают нарушения моторики, висцеральную гиперчувствительность, изменение слизистой и иммунной функции, а также измененную микробиоту кишечника [1,2].Среди расстройств желудочно-кишечного тракта воспалительные заболевания кишечника (ВЗК), включая болезнь Крона (БК), хроническое заболевание кишечника, вызывающее очаги воспаления в желудочно-кишечном тракте [3], и язвенный колит (ЯК), который поражает только внутреннюю стенку кишечника. толстой кишки, являются наиболее серьезными заболеваниями [4]. Другие распространенные идиопатические и хронические воспалительные расстройства желудочно-кишечного тракта включают дивертикулярную болезнь, хроническое состояние небольших карманов кишечника и синдром раздраженного кишечника (СРК), определяемый как «дискомфорт в животе, связанный с измененными привычками кишечника» [5].
Введение Желудочно-кишечные (ЖКТ) расстройства, распространенность которых увеличилась за последние несколько десятилетий, характеризуются физиологическими и морфологическими аномалиями: система желудочно-кишечного тракта, которые часто возникают в сочетании и включают нарушения моторики, висцеральную гиперчувствительность, изменение слизистой и иммунной функции, а также измененную микробиоту кишечника [1,2].Среди расстройств желудочно-кишечного тракта воспалительные заболевания кишечника (ВЗК), включая болезнь Крона (БК), хроническое заболевание кишечника, вызывающее очаги воспаления в желудочно-кишечном тракте [3], и язвенный колит (ЯК), который поражает только внутреннюю стенку кишечника. толстой кишки, являются наиболее серьезными заболеваниями [4]. Другие распространенные идиопатические и хронические воспалительные расстройства желудочно-кишечного тракта включают дивертикулярную болезнь, хроническое состояние небольших карманов кишечника и синдром раздраженного кишечника (СРК), определяемый как «дискомфорт в животе, связанный с измененными привычками кишечника» [5]. Основными причинами желудочно-кишечных расстройств являются генетическая предрасположенность к заболеванию, фармакологические методы лечения (т. Е. Антибиотики, не ограничиваясь теми, которые вводятся для использования человеком, но также потенциально включают те, которые используются на сельскохозяйственных животных и сельскохозяйственных культурах и потребляются с полученными продуктами питания), нестероидные препараты. противовоспалительные препараты (НПВП) (например, аспирин, ибупрофен, диклофенак) и нездоровый образ жизни, включая нерегулярное питание, отсутствие физической активности, курение и диету с низким содержанием клетчатки [6,7,8,9]. Более того, около 50% мирового населения поражено Helicobacter pylori, грамотрицательным бактериальным патогеном, который может вызывать ВЗК и функциональные расстройства ЖКТ [10].Все расстройства желудочно-кишечного тракта обычно проявляются болью в животе, запором, диареей, вздутием живота, кислотностью желудочного сока, желудочно-кишечной рефлюксной болезнью (ГЭРБ), кровотечением из желудочно-кишечного тракта (ЖКТ), мальабсорбцией или недоеданием и кишечной непроходимостью [11,12].
Основными причинами желудочно-кишечных расстройств являются генетическая предрасположенность к заболеванию, фармакологические методы лечения (т. Е. Антибиотики, не ограничиваясь теми, которые вводятся для использования человеком, но также потенциально включают те, которые используются на сельскохозяйственных животных и сельскохозяйственных культурах и потребляются с полученными продуктами питания), нестероидные препараты. противовоспалительные препараты (НПВП) (например, аспирин, ибупрофен, диклофенак) и нездоровый образ жизни, включая нерегулярное питание, отсутствие физической активности, курение и диету с низким содержанием клетчатки [6,7,8,9]. Более того, около 50% мирового населения поражено Helicobacter pylori, грамотрицательным бактериальным патогеном, который может вызывать ВЗК и функциональные расстройства ЖКТ [10].Все расстройства желудочно-кишечного тракта обычно проявляются болью в животе, запором, диареей, вздутием живота, кислотностью желудочного сока, желудочно-кишечной рефлюксной болезнью (ГЭРБ), кровотечением из желудочно-кишечного тракта (ЖКТ), мальабсорбцией или недоеданием и кишечной непроходимостью [11,12]. Некоторые из лекарственных средств, применяемых в настоящее время для лечения желудочно-кишечных расстройств, включают слабительные, противодиарейные, опиоиды, противорвотные средства, усилители моторики, а также противокислотные, противоязвенные и противовоспалительные средства [13]. Обычные методы лечения ВЗК включают кортикостероиды, иммунодепрессанты и антитела против фактора некроза опухолей (TNF) -α, которые часто коррелируют с риском оппортунистических инфекций и дисплазий, что имеет дорогостоящие последствия для управления системой здравоохранения [14,15].Данные свидетельствуют о том, что диета по западному образцу (WPD) привела к широкому распространению ГЭРБ. Исследования показали, что распространенность ГЭРБ составляет 18,1–27,8% (североамериканцы), 8,8–25,9% (Европа), 11,6% (Австралия), 23% (Южная Америка), 2,5–7,8% (Восточная Азия) и 8,7%. –33,1% (Ближний Восток) [16]. Распространенность диспепсии может варьироваться от страны к стране, однако объединенная распространенность сообщается Ford et al.
Некоторые из лекарственных средств, применяемых в настоящее время для лечения желудочно-кишечных расстройств, включают слабительные, противодиарейные, опиоиды, противорвотные средства, усилители моторики, а также противокислотные, противоязвенные и противовоспалительные средства [13]. Обычные методы лечения ВЗК включают кортикостероиды, иммунодепрессанты и антитела против фактора некроза опухолей (TNF) -α, которые часто коррелируют с риском оппортунистических инфекций и дисплазий, что имеет дорогостоящие последствия для управления системой здравоохранения [14,15].Данные свидетельствуют о том, что диета по западному образцу (WPD) привела к широкому распространению ГЭРБ. Исследования показали, что распространенность ГЭРБ составляет 18,1–27,8% (североамериканцы), 8,8–25,9% (Европа), 11,6% (Австралия), 23% (Южная Америка), 2,5–7,8% (Восточная Азия) и 8,7%. –33,1% (Ближний Восток) [16]. Распространенность диспепсии может варьироваться от страны к стране, однако объединенная распространенность сообщается Ford et al. составлять 21% [17]. Среди взрослого населения США диарея является причиной более 128 000 госпитализаций и 3000 смертей [18,19].Точно так же доступная литература предполагает, что 12% населения мира страдали запорами [20]. Найроп и др. (2007) оценили среднегодовые прямые затраты на медицинское обслуживание некоторых расстройств желудочно-кишечного тракта в расчете на группу пациентов, посещающих клинику желудочно-кишечного тракта, в 5049 долларов (СРК), 6140 долларов (диарея), 7522 доллара (запор) и 7646 долларов (боль в животе) [21]. Несмотря на недавний прогресс в знаниях о патофизиологических механизмах, участвующих в расстройствах ЖКТ, их этиопатогенез еще не полностью выяснен, и нет маркера, который может привести к их окончательному диагнозу.Были идентифицированы некоторые этиологические факторы, такие как висцеральная гиперчувствительность, инфекции, генетические и эпигенетические факторы, стресс и изменения кишечной микробиоты, ведущие к дисбактериозу [22,23]. Метаболический синдром (РС) — это состояние хронического воспаления слабой степени, обусловленное как генетическими факторами, так и факторами окружающей среды, включая ряд факторов риска серьезных заболеваний, таких как гипергликемия, абдоминальное ожирение, гиперлипидемия и гипертензия [24,25].
составлять 21% [17]. Среди взрослого населения США диарея является причиной более 128 000 госпитализаций и 3000 смертей [18,19].Точно так же доступная литература предполагает, что 12% населения мира страдали запорами [20]. Найроп и др. (2007) оценили среднегодовые прямые затраты на медицинское обслуживание некоторых расстройств желудочно-кишечного тракта в расчете на группу пациентов, посещающих клинику желудочно-кишечного тракта, в 5049 долларов (СРК), 6140 долларов (диарея), 7522 доллара (запор) и 7646 долларов (боль в животе) [21]. Несмотря на недавний прогресс в знаниях о патофизиологических механизмах, участвующих в расстройствах ЖКТ, их этиопатогенез еще не полностью выяснен, и нет маркера, который может привести к их окончательному диагнозу.Были идентифицированы некоторые этиологические факторы, такие как висцеральная гиперчувствительность, инфекции, генетические и эпигенетические факторы, стресс и изменения кишечной микробиоты, ведущие к дисбактериозу [22,23]. Метаболический синдром (РС) — это состояние хронического воспаления слабой степени, обусловленное как генетическими факторами, так и факторами окружающей среды, включая ряд факторов риска серьезных заболеваний, таких как гипергликемия, абдоминальное ожирение, гиперлипидемия и гипертензия [24,25]. Клиническое значение рассеянного склероза было подчеркнуто Ривеном в 1988 г. при описании роли инсулинорезистентности в заболевании человека [26].Нелеченное и стойкое состояние рассеянного склероза может привести к ряду патологий, наиболее частыми из которых являются сердечно-сосудистые заболевания (ишемическая болезнь сердца, сердечная недостаточность и инсульт), сахарный диабет 2 типа и нарушения функции печени, такие как стеатоз печени [27, 28,29]. Как сообщил Садеги, различные метаболические нарушения, включая гипертензию, гипергликемию и подагру, были описаны еще в 1920-х годах [30]. Позже, в 1947 году, Ваг описал фенотип ожирения как связанный с метаболическими нарушениями, сахарным диабетом 2 типа (СД2) и сердечно-сосудистыми заболеваниями [31].Определение ВОЗ и Европейская группа по изучению инсулинорезистентности согласны с тем, что непереносимость глюкозы и инсулинорезистентность являются важными компонентами РС [32,33]. Используются несколько определений указанного синдрома, но с 2004 года Международная диабетическая федерация (IDF) установила единое определение рассеянного склероза, подчеркивая ключевую роль ожирения как фактора риска заболеваний, о которых сообщалось выше [34].
Клиническое значение рассеянного склероза было подчеркнуто Ривеном в 1988 г. при описании роли инсулинорезистентности в заболевании человека [26].Нелеченное и стойкое состояние рассеянного склероза может привести к ряду патологий, наиболее частыми из которых являются сердечно-сосудистые заболевания (ишемическая болезнь сердца, сердечная недостаточность и инсульт), сахарный диабет 2 типа и нарушения функции печени, такие как стеатоз печени [27, 28,29]. Как сообщил Садеги, различные метаболические нарушения, включая гипертензию, гипергликемию и подагру, были описаны еще в 1920-х годах [30]. Позже, в 1947 году, Ваг описал фенотип ожирения как связанный с метаболическими нарушениями, сахарным диабетом 2 типа (СД2) и сердечно-сосудистыми заболеваниями [31].Определение ВОЗ и Европейская группа по изучению инсулинорезистентности согласны с тем, что непереносимость глюкозы и инсулинорезистентность являются важными компонентами РС [32,33]. Используются несколько определений указанного синдрома, но с 2004 года Международная диабетическая федерация (IDF) установила единое определение рассеянного склероза, подчеркивая ключевую роль ожирения как фактора риска заболеваний, о которых сообщалось выше [34]. Основными факторами риска развития РС являются семейный анамнез [35], курение [36], чрезмерное употребление алкоголя [37], старение, низкий социально-экономический статус, постменопаузальный статус [38], малоподвижный образ жизни [39], нездоровый режим питания [40] и прием некоторых лекарств (атипичные нейролептики) [41].На рисунке 1 показано влияние нерегулируемого метаболизма на человеческий организм, иллюстрируя патогенный путь рассеянного склероза. Нарушения обмена веществ имеют общие патофизиологические механизмы, и поэтому различные фармакологические объекты используются в комбинации для терапевтических целей [42]. Эффективные вмешательства могут включать физические упражнения, модификации диеты и фармакологические агенты, такие как сенсибилизаторы инсулина, ингибиторы ренин-ангиотензин-альдостероновой системы (РААС), статины и фибраты [43,44]. За последние два десятилетия во всем мире произошло значительное увеличение числа людей с РС, связанное с глобальной эпидемией ожирения и СД2.
Основными факторами риска развития РС являются семейный анамнез [35], курение [36], чрезмерное употребление алкоголя [37], старение, низкий социально-экономический статус, постменопаузальный статус [38], малоподвижный образ жизни [39], нездоровый режим питания [40] и прием некоторых лекарств (атипичные нейролептики) [41].На рисунке 1 показано влияние нерегулируемого метаболизма на человеческий организм, иллюстрируя патогенный путь рассеянного склероза. Нарушения обмена веществ имеют общие патофизиологические механизмы, и поэтому различные фармакологические объекты используются в комбинации для терапевтических целей [42]. Эффективные вмешательства могут включать физические упражнения, модификации диеты и фармакологические агенты, такие как сенсибилизаторы инсулина, ингибиторы ренин-ангиотензин-альдостероновой системы (РААС), статины и фибраты [43,44]. За последние два десятилетия во всем мире произошло значительное увеличение числа людей с РС, связанное с глобальной эпидемией ожирения и СД2.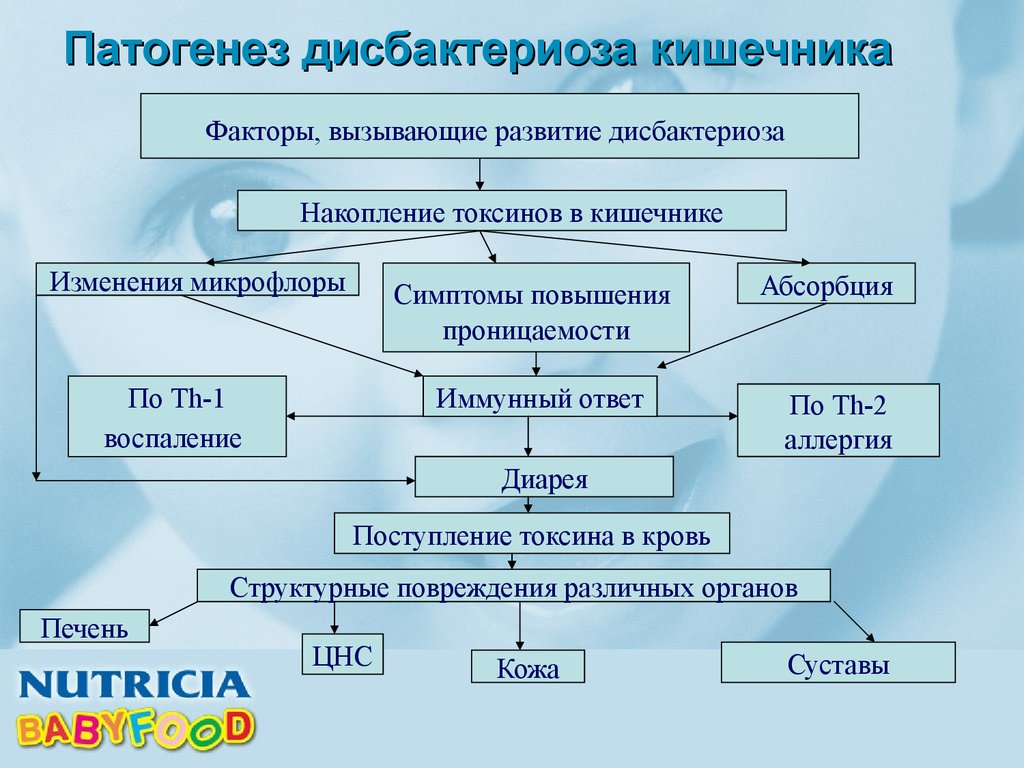 Около 20–25% взрослого населения мира живет с РС [45]. По оценкам ВОЗ, около 650 миллионов человек живут с ожирением, 422 миллиона — с диабетом и 1,13 миллиарда — с гипертонией [46, 47, 48]. Растущие данные свидетельствуют о том, что дисбактериоз микробиоты кишечника вызван множеством внутренних и внешних факторов, таких как генетические вариации, диета, стресс и фармакологическая терапия [49] связаны с патогенезом как кишечных, так и внекишечных заболеваний (рис. 2). Фактически, взаимодействие между микробиотой и иммунной системой хозяина считается ключевым элементом для нового понимания патогенеза большого спектра заболеваний, включая расстройства желудочно-кишечного тракта и рассеянный склероз [50].Текущие исследования подчеркивают роль здоровой микробиоты кишечника в модулировании возникновения различных заболеваний ЖКТ, таких как ВЗК, рак толстой кишки, целиакия и СРК. Кроме того, дисбактериоз — один из движущих факторов нарушения метаболизма. Hur et al. сообщают о важной роли кишечной микробиоты в патогенезе СД2, влияя на массу тела, провоспалительную активность и инсулинорезистентность [51].
Около 20–25% взрослого населения мира живет с РС [45]. По оценкам ВОЗ, около 650 миллионов человек живут с ожирением, 422 миллиона — с диабетом и 1,13 миллиарда — с гипертонией [46, 47, 48]. Растущие данные свидетельствуют о том, что дисбактериоз микробиоты кишечника вызван множеством внутренних и внешних факторов, таких как генетические вариации, диета, стресс и фармакологическая терапия [49] связаны с патогенезом как кишечных, так и внекишечных заболеваний (рис. 2). Фактически, взаимодействие между микробиотой и иммунной системой хозяина считается ключевым элементом для нового понимания патогенеза большого спектра заболеваний, включая расстройства желудочно-кишечного тракта и рассеянный склероз [50].Текущие исследования подчеркивают роль здоровой микробиоты кишечника в модулировании возникновения различных заболеваний ЖКТ, таких как ВЗК, рак толстой кишки, целиакия и СРК. Кроме того, дисбактериоз — один из движущих факторов нарушения метаболизма. Hur et al. сообщают о важной роли кишечной микробиоты в патогенезе СД2, влияя на массу тела, провоспалительную активность и инсулинорезистентность [51]. Ключевая роль микробиоты кишечника — это ферментация пищевых полисахаридов, которые человеческий организм не может переваривать иначе.Пищевые волокна состоят из неперевариваемой части растительных пищевых углеводов, содержащих нерастворимые и растворимые волокна. Растворимые волокна перевариваются ферментами, полученными из микробиоты кишечника, в короткоцепочечные жирные кислоты (SCFA). SCFAs (бутират, ацетат и пропионат) всасываются в кишечнике и используются хозяином в качестве энергии. Помимо своей роли в качестве энергетических субстратов, SCFA действуют как регуляторы потребления пищи или энергии и воспаления [52,53]. В частности, бутират способствует регенерации и защите кишечных клеток, выработке муцина, снижению уровней гиперхолестеринемии, а также высвобождению гормонов и / или нейромедиаторов, важных для регуляции перистальтики кишечника и резистентности к инсулину [54].У пациентов с СРК наблюдалось уменьшение боли в животе после приема бутирата из-за изменения высвобождения нейромедиаторов и снижения гиперчувствительности кишечных механорецепторов, что может привести к снижению давления в просвете и / или перистальтики [55,56].
Ключевая роль микробиоты кишечника — это ферментация пищевых полисахаридов, которые человеческий организм не может переваривать иначе.Пищевые волокна состоят из неперевариваемой части растительных пищевых углеводов, содержащих нерастворимые и растворимые волокна. Растворимые волокна перевариваются ферментами, полученными из микробиоты кишечника, в короткоцепочечные жирные кислоты (SCFA). SCFAs (бутират, ацетат и пропионат) всасываются в кишечнике и используются хозяином в качестве энергии. Помимо своей роли в качестве энергетических субстратов, SCFA действуют как регуляторы потребления пищи или энергии и воспаления [52,53]. В частности, бутират способствует регенерации и защите кишечных клеток, выработке муцина, снижению уровней гиперхолестеринемии, а также высвобождению гормонов и / или нейромедиаторов, важных для регуляции перистальтики кишечника и резистентности к инсулину [54].У пациентов с СРК наблюдалось уменьшение боли в животе после приема бутирата из-за изменения высвобождения нейромедиаторов и снижения гиперчувствительности кишечных механорецепторов, что может привести к снижению давления в просвете и / или перистальтики [55,56].
Сегодня образ жизни и диета признаны краеугольными камнями профилактики таких патологий, как сердечно-сосудистые заболевания, СД2, РС и расстройства желудочно-кишечного тракта. Более того, регулирование дисбактериоза кишечника с помощью пищевых добавок, согласно последним данным, используется для восстановления равновесия микробиоты кишечника.Учитывая, что дисбактериоз может быть общей связью между расстройствами желудочно-кишечного тракта и рассеянным склерозом, а правильная диета может использоваться для восстановления измененной микробиоты и считается первым подходом к лечению как расстройств желудочно-кишечного тракта, так и рассеянного склероза, цель этого обзора состоит в том, чтобы обобщить текущие знания о защитной роли функциональных диетических компонентов при желудочно-кишечном тракте и рассеянном склерозе, а также помочь в выработке общей точки зрения на эти обширные области.
Дисбиоз и микробиом
Дисбиоз — это состояние, вызванное дисбалансом бактериального сообщества (микробиома) кишечника человека. Дисбиоз нарушает экоустойчивость кишечника, что приводит к таким симптомам, как диарея, запор, вздутие живота и несварение желудка.
Дисбиоз нарушает экоустойчивость кишечника, что приводит к таким симптомам, как диарея, запор, вздутие живота и несварение желудка.
Что такое дисбактериоз?
Дисбактериоз, также называемый дисбактериозом, — это заболевание, поражающее желудочно-кишечный тракт. В организме есть колонии полезных бактерий, называемых микробиотой.
Эти организмы необходимы для здоровья и играют различные роли в пищеварительной системе. Но когда эти бактерии становятся несбалансированными, например, когда вредные бактерии превосходят или превосходят по численности хороших, это может привести к болезни.
Дисбиоз возникает, когда бактерии в кишечнике становятся несбалансированными, вызывая широкий спектр нарушений пищеварения.
Помимо симптомов, которые включают расстройство желудка, диарею, запор и вздутие живота, это может быть связано с другими состояниями, включая, помимо прочего, гастрит, язвенную болезнь, синдром раздраженного кишечника (СРК), воспалительное заболевание кишечника и рак толстой кишки.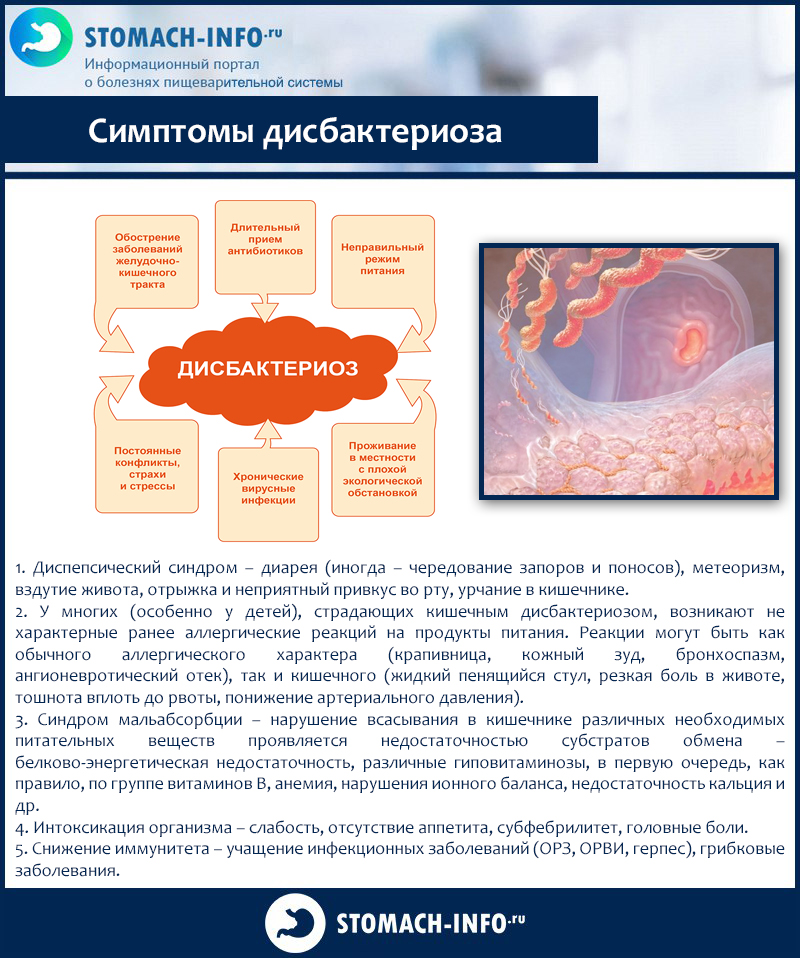
Микробиом кишечника
В желудочно-кишечном тракте живут триллионы микробов.В кишечнике более 400 видов бактерий, а это значит, что в пищеварительном тракте бактерий больше, чем клеток в организме.
Эти бактерии и микробы необходимы для переваривания пищи, борьбы с вредными патогенами и синтеза витаминов. Короче говоря, микробы жизненно важны для здоровья в целом, и без них вы не смогли бы выжить.
Также называемая микрофлорой, эта живая группа микробов всегда должна находиться в равновесии, при этом хорошие бактерии подавляют вредные бактерии.Когда определенные факторы влияют на баланс, это может привести к заболеванию, особенно к дисбактериозу.
В общем, плохие бактерии и дрожжи не представляют проблемы. Фактически, они работают рука об руку с остальными кишечными бактериями, если в организме имеется достаточное количество полезных бактерий.
Эти хорошие бактерии следят за тем, чтобы количество вредных бактерий находилось под контролем, и не подавляли их. Проблемы с пищеварением начинаются только тогда, когда количество вредных бактерий начинает превышать количество хороших.
Узнайте больше о микробиоме кишечника здесь.
Преимущества нормальной микрофлоры кишечника
Микробиом кишечника имеет множество преимуществ не только для пищеварительной системы, но и для здоровья в целом. Бактерии кишечника помогают вырабатывать гормоны, такие как серотонин, гормон хорошего самочувствия, связанный с контролем настроения.
Низкий уровень серотонина был связан с различными состояниями, такими как тревожность, депрессия, аутизм и синдром дефицита внимания с гиперактивностью (СДВГ).
Кроме того, кишечные бактерии помогают извлекать из пищи питательные вещества и калории. Эти питательные вещества включают витамины, аминокислоты, минералы, антиоксиданты и жирные кислоты.
Микробиом желудочно-кишечного тракта помогает контролировать аппетит и массу тела. Вот почему кишечные бактерии связаны с ожирением.
Вот почему кишечные бактерии связаны с ожирением.
Кишечные бактерии обладают множеством других преимуществ, включая переваривание клетчатки для образования стула, укрепление иммунной системы, контроль настроения и когнитивного здоровья, а также восстановление поврежденных тканей.
Они также полезны, потому что повышают уровень энергии, уменьшают количество случаев дрожжевой инфекции, улучшают уровень холестерина, улучшают здоровье полости рта и способствуют увеличению продолжительности жизни.
Что происходит при дисбактериозе?
При дисбактериозе кишечника происходят изменения в микробиоме кишечника. Эти изменения могут помешать человеку правильно переваривать пищу, что приводит к различным симптомам дисбактериоза.
Эти изменения могут быть связаны с чрезмерным употреблением антибиотиков, чрезмерным потреблением алкоголя, изменением диеты, которое увеличивает потребление сахара, белка или пищевых добавок, воздействием пестицидов, плохой гигиеной полости рта или стрессом.
Когда есть дисбаланс, плохие бактерии могут захватить хорошие бактерии, что приведет к воспалению кишечника, которое может повредить слизистую оболочку кишечника. В результате могут появиться симптомы нарушения пищеварения.
Кроме того, хроническое воспаление может привести к нарушениям пищеварения, таким как синдром повышенной проницаемости кишечника, кандидоз, синдром раздраженного кишечника (СРК) и избыточный бактериальный рост в тонком кишечнике (СИБР).
Поскольку около 80 процентов клеток иммунной системы находятся в кишечнике, дисбактериоз был связан с ослабленной иммунной защитой от болезней и болезней.
Это может привести к различным инфекциям, которые в дальнейшем могут сказаться на здоровье пациента.
Дисбиоз можно лечить пребиотиками и пробиотиками. Самое главное, изменение образа жизни и диетические изменения могут помочь вылечить кишечник и восстановить баланс нормальной флоры кишечника. Для предотвращения рецидивов и поддержания общего здоровья кишечника необходимо длительное лечение.
Диагностика дисбактериоза
Дисбактериоз — это состояние, при котором кишечные бактерии становятся несбалансированными, что приводит к широкому спектру нарушений пищеварения, включая вздутие живота, диарею, запоры и спазмы желудка, среди прочего.Это состояние было связано с различными заболеваниями, включая синдром раздраженного кишечника (СРК), воспалительное заболевание кишечника и гастрит, и это лишь некоторые из них.
Что такое дисбактериоз?
Дисбактериоз — это нарушение баланса кишечных бактерий. В результате возникает широкий спектр симптомов нарушения пищеварения, включая диарею, спазмы, запор, вздутие живота и несварение желудка. Когда наблюдается несоответствие нормальной микрофлоры кишечника из-за слишком малого количества полезных бактерий и чрезмерного роста вредных бактерий, это может вызвать дисбактериоз.
В микробиоме кишечника обнаружено не менее 400 видов бактерий. Они необходимы для здоровья в целом, поскольку помогают пищеварению, борются с патогенными микроорганизмами и синтезируют витамины. Нормальную флору тела можно найти в различных областях, и они необходимы для общего здоровья и хорошего самочувствия. Когда эти бактерии становятся несбалансированными, а вредные подавляют полезные бактерии или бесконтрольно разрастаются, это может вызвать болезнь.
Нормальную флору тела можно найти в различных областях, и они необходимы для общего здоровья и хорошего самочувствия. Когда эти бактерии становятся несбалансированными, а вредные подавляют полезные бактерии или бесконтрольно разрастаются, это может вызвать болезнь.
Что вызывает дисбактериоз?
Существует множество факторов, которые могут привести к заболеванию, включая чрезмерное или неправильное использование антибиотиков, чрезмерное употребление алкоголя, повышенное потребление сахара или белка, частое использование антацидов, воздействие пестицидов и хронический стресс, и это лишь некоторые из них.Также к дисбактериозу могут привести плохая гигиена полости рта и беспокойство.
В некоторых случаях исследования связывают дисбактериоз с рождением через кесарево сечение и вскармливанием смеси среди новорожденных.
Признаки и симптомы дисбактериоза
Основными признаками и симптомами дисбактериоза являются нарушения пищеварения. Люди с этим заболеванием могут испытывать частые газы или вздутие живота.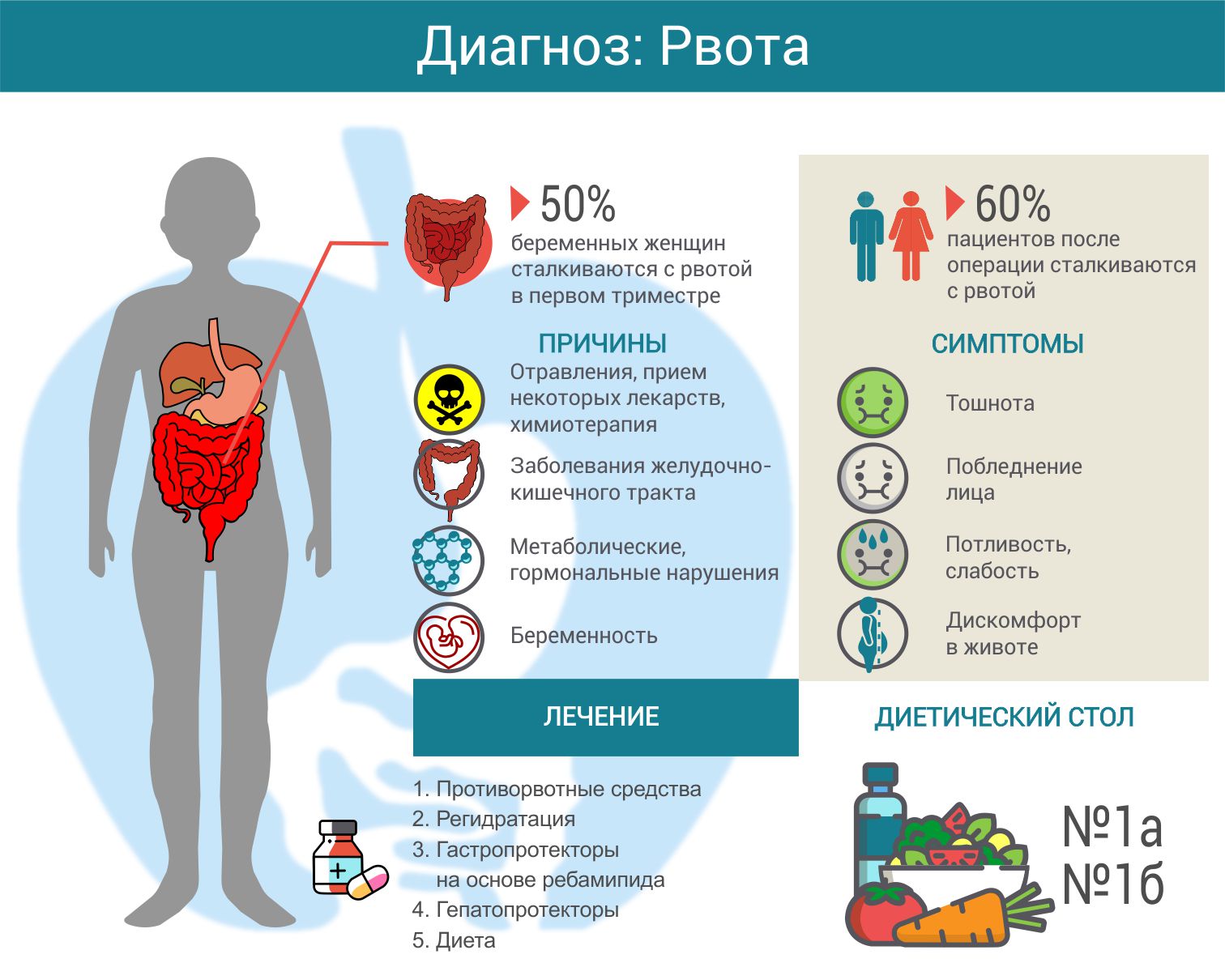 Это означает, что они ощущают вздутие живота почти все дни недели. Кроме того, они страдают от спазмов в животе, диареи и запоров со слизью в стуле.У них может быть сочетание диареи и запора, пищевой чувствительности, пищевой непереносимости и хронического неприятного запаха изо рта.
Это означает, что они ощущают вздутие живота почти все дни недели. Кроме того, они страдают от спазмов в животе, диареи и запоров со слизью в стуле.У них может быть сочетание диареи и запора, пищевой чувствительности, пищевой непереносимости и хронического неприятного запаха изо рта.
В некоторых случаях люди могут испытывать затруднения при мочеиспускании, вагинальный или ректальный зуд, боль в груди, сыпь, утомляемость, проблемы с концентрацией внимания, депрессию, беспокойство и туман в мозгу.
Диагностика дисбактериоза
Врач может диагностировать дисбактериоз на основании признаков и симптомов, истории болезни, физического осмотра и диагностических тестов. У человека может быть дисбактериоз, если у него или нее есть диагноз синдрома раздраженного кишечника (СРК), длительное употребление антибиотиков в анамнезе, аутоиммунное заболевание или гастроэнтерит в анамнезе.Однако для подтверждения диагноза врач может порекомендовать следующие диагностические тесты:
Тесты на органическую кислоту
Врач порекомендует тест на органическую кислоту. Это делается путем сбора пробы мочи и ее исследования в лаборатории. Они будут искать и проверять определенные кислоты, которые выделяют бактерии в кишечнике. Аномальные уровни означают, что некоторые бактерии выходят из-под контроля.
Это делается путем сбора пробы мочи и ее исследования в лаборатории. Они будут искать и проверять определенные кислоты, которые выделяют бактерии в кишечнике. Аномальные уровни означают, что некоторые бактерии выходят из-под контроля.
Комплексный анализ пищеварительного стула (CDSA)
Всесторонний анализ стула может дать наиболее глубокий анализ бактерий, как хороших, так и патогенных, которые обитают в кишечнике.Кроме того, исследование кала может определить наличие других оппортунистических инфекций, например, паразитарных организмов.
Врач разрешит пациенту взять домой специальное оборудование для взятия пробы стула. Затем образец будет отправлен в лабораторию. Стул будет исследован на наличие бактерий, дрожжей или грибков.
Водородный дыхательный тест
Водородный тест груди обнаруживает наличие газов, производимых бактериями в кишечнике. В водородном дыхательном тесте врач разрешает пациенту выпить раствор глюкозы или сахара. После этого пациент дышит в специальный баллон, где воздух исследуется на наличие газов, выделяемых бактериями. Когда газов слишком много или слишком много, это может указывать на дисбаланс кишечных бактерий.
После этого пациент дышит в специальный баллон, где воздух исследуется на наличие газов, выделяемых бактериями. Когда газов слишком много или слишком много, это может указывать на дисбаланс кишечных бактерий.
Биопсия
Врач может взять образец бактериальной ткани из кишечника, где есть активная инфекция, чтобы увидеть, какой тип бактерий присутствует.
Лечение дисбактериоза — это больше, чем просто прием пробиотиков для поддержания баланса в кишечнике.Это как-то связано с правильным выбором пищи, отказом от определенных продуктов и занятий, а также с ограничением потребления алкоголя или полным его искоренением. Здоровое питание и сокращение количества потребляемого сахара и пищевых добавок — многообещающий способ обуздать дисбактериоз и сохранить здоровье кишечника.
Дополнительная литература
Синдром избыточного бактериального роста: история вопроса, патофизиология, эпидемиология
Bures J, Cyrany J, Kohoutova D и др. Синдром избыточного бактериального роста в тонкой кишке. Мир J Гастроэнтерол . 2010, 28 июня, 16 (24): 2978-90. [Медлайн]. [Полный текст].
Виралли-Монод М, Тильманс Д., Кеворкян Дж. П. и др. Хроническая диарея и сахарный диабет: преобладание избыточного бактериального роста в тонкой кишке. Метаболизм диабета . 1998 24 декабря (6): 530-6. [Медлайн].
Куигли Е.М., Абу-Шанаб А.Избыточный бактериальный рост в тонком кишечнике. Инфекция Dis Clin North Am . 2010 декабря 24 (4): 943-59, viii-ix. [Медлайн].
Макэвой А., Даттон Дж., Джеймс О.Ф. Бактериальное заражение тонкого кишечника — важная причина скрытой мальабсорбции у пожилых людей. Br Med J (Clin Res Ed) . 1983, 17 сентября. 287 (6395): 789-93. [Медлайн].
Br Med J (Clin Res Ed) . 1983, 17 сентября. 287 (6395): 789-93. [Медлайн].
Parodi A, Paolino S, Greco A, Drago F, Mansi C, Rebora A. Избыточный бактериальный рост в тонком кишечнике при розацеа: клиническая эффективность его искоренения. Клин Гастроэнтерол Гепатол . 2008 июл.6 (7): 759-64. [Медлайн].
Rubio-Tapia A, Barton SH, Rosenblatt JE, Murray JA. Распространенность избыточного бактериального роста в тонкой кишке, диагностированная с помощью количественного посева кишечного аспирата при целиакии. Дж Клин Гастроэнтерол . 2009 Февраль 43 (2): 157-61. [Медлайн].
Ghoshal UC, Ghoshal U, Misra A, Choudhuri G. Частично поддающаяся лечению глютеновая болезнь, возникающая в результате избыточного бактериального роста в тонком кишечнике и непереносимости лактозы. БМК Гастроэнтерол . 2004 22 мая. 4:10. [Медлайн].
2004 22 мая. 4:10. [Медлайн].
Льюис С.Дж., Франко С., Янг Г., О’Киф С.Дж. Нарушение функции кишечника и избыточный бактериальный рост в двенадцатиперстной кишке у пациентов, получавших омепразол. Алимент Фармакол Тер . 1996 10 августа (4): 557-61. [Медлайн].
Элфик Д.А., Чу Т.С., Хайэм С.Е., Берд Н., Ахмад А., Сандерс Д.С. Избыточный бактериальный рост в тонкой кишке у пожилых людей с симптомами: можно ли диагностировать раньше? Геронтология .2005 ноябрь-декабрь. 51 (6): 396-401. [Медлайн].
Hoverstad T, Bjorneklett A, Fausa O, Midtvedt T. Короткоцепочечные жирные кислоты при синдроме избыточного бактериального роста в тонкой кишке. Сканд Дж Гастроэнтерол . 1985 Май. 20 (4): 492-9. [Медлайн].
Kocoshis SA, Schletewitz K, Lovelace G, Laine RA. Желчные кислоты двенадцатиперстной кишки у детей: кетопроизводные и избыточный рост аэробных бактерий в тонкой кишке [опубликованная ошибка опубликована в J Pediatr Gastroenterol Nutr 1988, январь-февраль; 7 (1): 155]. J Педиатр Гастроэнтерол Нутр . 1987 сентябрь-октябрь. 6 (5): 686-96. [Медлайн].
Желчные кислоты двенадцатиперстной кишки у детей: кетопроизводные и избыточный рост аэробных бактерий в тонкой кишке [опубликованная ошибка опубликована в J Pediatr Gastroenterol Nutr 1988, январь-февраль; 7 (1): 155]. J Педиатр Гастроэнтерол Нутр . 1987 сентябрь-октябрь. 6 (5): 686-96. [Медлайн].
Чалмерс Р.А., Вальман Х.Б., Либерман ММ. Измерение 4-гидроксифенилуксусной ацидурии в качестве скринингового теста на заболевание тонкой кишки. Clin Chem . 1979 25 октября (10): 1791-4. [Медлайн].
Sherr HP, Sasaki Y, Newman A, et al. Обнаружение бактериальной деконъюгации солей желчных кислот с помощью удобной техники анализа дыхания. N Engl J Med . 1971 16 сентября.285 (12): 656-61. [Медлайн].
Саад Р.Дж., Чей В.Д. Дыхательный тест на избыточный бактериальный рост в тонком кишечнике: максимальная точность теста. Клин Гастроэнтерол Гепатол . 2014 12 (12) декабря: 1964-72; викторина e119-20. [Медлайн].
Клин Гастроэнтерол Гепатол . 2014 12 (12) декабря: 1964-72; викторина e119-20. [Медлайн].
Гасбаррини А., Корацца Г.Р., Гасбаррини Г., Монтальто М., Ди Стефано М., Базилиско Г. Методология и показания тестирования h3-дыхания при желудочно-кишечных заболеваниях: Конференция Римского консенсуса. Алимент Фармакол Тер .2009 30 марта. 29 Дополнение 1: 1-49. [Медлайн].
Hofmann AF. оценка избыточного бактериального роста в тонком кишечнике: как, когда и почему. В: Перри Ф., Андриулли А., редакторы. Клиническое применение дыхательных тестов в гастроэнтерологии и гепатологии. 1998.
Stotzer PO, Kilander AF. Сравнение дыхательного теста на 1 грамм (14) C-D-ксилозы и дыхательного теста на 50 грамм водородной глюкозы для диагностики избыточного бактериального роста в тонком кишечнике. Пищеварение .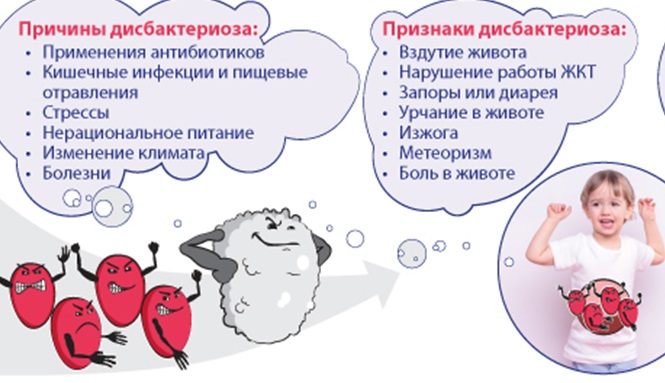 2000. 61 (3): 165-71. [Медлайн].
2000. 61 (3): 165-71. [Медлайн].
Peralta S, Cottone C, Doveri T, Almasio PL, Craxi A. Избыточный бактериальный рост в тонком кишечнике и симптомы, связанные с синдромом раздраженного кишечника: опыт применения рифаксимина. Мир J Гастроэнтерол . 2009, 7 июня. 15 (21): 2628-31. [Медлайн].
Пиментел М. Обзор рифаксимина для лечения СИБР и СРК. Заключение эксперта по исследованию наркотиков . 2009 марта 18 (3): 349-58. [Медлайн].
Scarpellini E, Gabrielli M, Lauritano CE, Lupascu A, Merra G, Cammarota G.Рифаксимин в высоких дозах для лечения избыточного бактериального роста в тонком кишечнике. Алимент Фармакол Тер . 2007 г., 1. 25 (7): 781-6. [Медлайн].
Frissora CL, Cash BD. Обзорная статья: роль антибиотиков по сравнению с традиционной фармакотерапией в лечении симптомов синдрома раздраженного кишечника.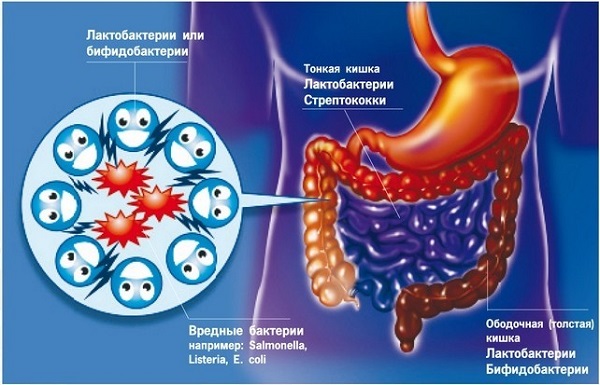 Алимент Фармакол Тер . 2007, 1. 25 (11): 1271-81. [Медлайн].
Алимент Фармакол Тер . 2007, 1. 25 (11): 1271-81. [Медлайн].
Тамер MA, Сантора TR, Сандберг DH. Терапия холестирамином при трудноизлечимой диарее. Педиатрия . 1974 Февраль 53 (2): 217-20. [Медлайн].
Castiglione F, Rispo A, Di Girolamo E, Cozzolino A, Manguso F, Grassia R, et al. Лечение антибиотиками избыточного бактериального роста в тонкой кишке у пациентов с болезнью Крона. Алимент Фармакол Тер . 2003 18 декабря (11-12): 1107-12. [Медлайн].
Vanderhoof JA, Young RJ. Этиология и патогенез избыточного бактериального роста. Клинические проявления и диагностика избыточного бактериального роста.Лечение избыточного бактериального роста UpToDate online, vol 18.1; Уэлсли, 2010. http://www.uptodate.com. Доступно на http://www.uptodate.com.
Quigley EM, Quera R. Избыточный бактериальный рост в тонком кишечнике: роль антибиотиков, пребиотиков и пробиотиков. Гастроэнтерология .2006, февраль 130 (2 приложение 1): S78-90. [Медлайн].
Онг Д.К., Митчелл С.Б., Барретт Дж.С., Шеперд С.Дж., Ирвинг П.М., Бьесекерски Дж. Р. и др. Манипулирование диетическими углеводами с короткой цепью изменяет характер газообразования и генезис симптомов синдрома раздраженного кишечника. Дж Гастроэнтерол Гепатол . 2010 25 августа (8): 1366-73. [Медлайн].
Макинтош К., Рид Д.Э., Шнайдер Т., Данг Ф., Кештели А.Х., Де Пальма Дж. И др. FODMAP изменяют симптомы и метаболизм пациентов с СРК: рандомизированное контролируемое исследование. Кишечник . 2017 июл.66 (7): 1241-1251. [Медлайн].
Кишечник . 2017 июл.66 (7): 1241-1251. [Медлайн].
Мари I, Дюкротте П., Дени П., Менар Дж. Ф., Левеск Х. Избыточный бактериальный рост тонкой кишки при системном склерозе. Ревматология (Оксфорд) . 2009 Октябрь 48 (10): 1314-9. [Медлайн].
Чжун Ц., Цюй Ц., Ван Б., Лян С., Цзэн Б. Пробиотики для профилактики и лечения избыточного бактериального роста в тонком кишечнике: метаанализ и систематический обзор имеющихся данных. Дж Клин Гастроэнтерол .2017 Апрель 51 (4): 300-311. [Медлайн].
[Рекомендации] Pimentel M, Saad RJ, Long MD, Rao SSC. Клинические рекомендации ACG: избыточный бактериальный рост в тонком кишечнике. Ам Дж. Гастроэнтерол . 2020 Февраль 115 (2): 165-178. [Медлайн].
[Руководство] Резайе А., Буреси М. , Лембо А., Лин Х., МакКаллум Р., Рао С. и др. Тестирование дыхания на основе водорода и метана при желудочно-кишечных расстройствах: Североамериканский консенсус. Ам Дж. Гастроэнтерол .2017 май. 112 (5): 775-784. [Медлайн].
, Лембо А., Лин Х., МакКаллум Р., Рао С. и др. Тестирование дыхания на основе водорода и метана при желудочно-кишечных расстройствах: Североамериканский консенсус. Ам Дж. Гастроэнтерол .2017 май. 112 (5): 775-784. [Медлайн].
Hill ID, Манн, Мэриленд, Хаусхэм, KC, Боуи, Мэриленд. Использование перорального гентамицина, метронидазола и холестирамина для лечения тяжелой стойкой диареи у младенцев. Педиатрия . 1986 Апрель, 77 (4): 477-81. [Медлайн].
Abraczinskas D, Goldfinger SE. Газы в кишечнике и вздутие живота. UpToDate в сети, 18.1. Уэлсли, 2010. http://www.uptodate.com. Доступно на http://www.uptodate.com.
Bouhnik Y, Alain S, Attar A, et al.Бактериальные популяции, загрязняющие верхний отдел кишечника у пациентов с синдромом избыточного бактериального роста в тонком кишечнике. Ам Дж. Гастроэнтерол . 1999 Май. 94 (5): 1327-31. [Медлайн].
Гастроэнтерол . 1999 Май. 94 (5): 1327-31. [Медлайн].
Дональд И.П., Китчингмам Дж., Дональд Ф., Купфер РМ. Диагноз избыточного бактериального роста в тонкой кишке у пожилых пациентов. J Am Geriatr Soc . 1992 июл. 40 (7): 692-6. [Медлайн].
Элфик Д.А., Чу Т.С., Хайэм С.Е., Берд Н., Ахмад А., Сандерс Д.С.Избыточный бактериальный рост в тонкой кишке у пожилых людей с симптомами: можно ли диагностировать раньше? Геронтология . 2005 ноябрь-декабрь. 51 (6): 396-401. [Медлайн].
Грейси М., Берк В., Ошин А. и др. Бактерии, соли желчных кислот и мальабсорбция кишечных моносахаридов. Кишечник . 1971 Сентябрь 12 (9): 683-92. [Медлайн].
Грегг CR. Кишечная бактериальная флора и синдром избыточного бактериального роста. Семин Гастроинтест Дис . 2002 окт.13 (4): 200-9. [Медлайн].
Семин Гастроинтест Дис . 2002 окт.13 (4): 200-9. [Медлайн].
Haboubi NY, Lee GS, Montgomery RD. Морфометрия слизистой оболочки двенадцатиперстной кишки у пожилых пациентов с избыточным бактериальным ростом в тонкой кишке: ответ на лечение антибиотиками. Возраст Старение . 1991, 20 января (1): 29-32. [Медлайн].
Килби AM, Dolby JM, Honor P, Walker-Smith JA. Бактериальная флора двенадцатиперстной кишки на ранних стадиях преходящей непереносимости моносахаридов у младенцев. Арка Дис Детский . 1977 г., 52 (3): 228-34.[Медлайн].
King CE, Toskes PP. Чрезмерный бактериальный рост в тонком кишечнике. Гастроэнтерология . 1979 Май. 76 (5, п.1): 1035-55. [Медлайн].
Klish WJ, Udall JN, Rodriguez JT, et al. Площадь поверхности кишечника у младенцев с приобретенной непереносимостью моносахаридов. Дж. Педиатр . 1978, апрель 92 (4): 566-71. [Медлайн].
Дж. Педиатр . 1978, апрель 92 (4): 566-71. [Медлайн].
Lin HC. Разрастание бактерий в тонком кишечнике: основа для понимания синдрома раздраженного кишечника. ЯМА . 2004 18 августа. 292 (7): 852-8. [Медлайн].
Матиас Дж. Р., Кленч М. Х. Обзор: патофизиология диареи, вызванной избыточным бактериальным ростом тонкой кишки. Am J Med Sci . 1985 июн. 289 (6): 243-8. [Медлайн].
Meyers JS, Ehrenpreis ED, Craig RM. Синдром избыточного бактериального роста в тонком кишечнике. Curr Treat Options Гастроэнтерол . 2001 Февраль 4 (1): 7-14. [Медлайн].
Николс В.Н., Фрейли Дж. К., Эванс К. Д., Николс Б. Л. мл.Приобретенная непереносимость моносахаридов у грудных детей. J Педиатр Гастроэнтерол Нутр . 1989, 8 (1): 51-7. [Медлайн].
[Медлайн].
Saltzman JR, Russell RM. Пищевые последствия чрезмерного бактериального роста в кишечнике. Компр Тер . 1994. 20 (9): 523-30. [Медлайн].
Tahan S, Melli LC, Mello CS, Rodrigues MS, Bezerra Filho H, de Morais MB. Эффективность триметоприм-сульфаметоксазола и метронидазола в лечении избыточного бактериального роста в тонком кишечнике у детей, живущих в трущобах. J Педиатр Гастроэнтерол Нутр . 2013 Сентябрь 57 (3): 316-8. [Медлайн].
Дисбактериоз и СРК — Канадский фонд здоровья пищеварительной системы
Дисбактериоз и СРК: небольшой урок истории
Вы знаете, что это просто еще один день в чудесном мире здоровья кишечника, когда мы бросаем вам еще одно сумасшедшее слово и соединяем его с аббревиатурой! Дисбактериоз и СРК? Что это такое и почему мы об этом говорим? Ну, это начинается с нашего микробиома, и ответы не черно-белые.
Доказательства микробиома человека были впервые обнаружены австрийским педиатром по имени Теодор Эшерих. Он фактически обнаружил тип бактерий (позже названный Escherichia coli ) в кишечнике как здоровых детей, так и детей, страдающих диарейными заболеваниями (возможно, СРК-Д?). После этого первоначального открытия того, что казалось безвредными бактериями, другие ученые начали описывать другие микроорганизмы, которые, казалось, существовали во многих других областях человеческого тела и на нем.Например; кожа, нос, рот, желудочно-кишечный тракт и т. д. Со временем в первом десятилетии двадцать первого века была разработана концепция того, что мы теперь знаем как «человеческий микробиом».
Благодаря этому раннему открытию мы узнали, что большая часть вашего микробиома располагается в вашем пищеварительном тракте, особенно в кишечнике. Мы называем это кишечной микробиотой, которая содержит десятки триллионов микроорганизмов. Хотя у каждого из нас есть уникальная микробиота кишечника, она всегда выполняет одни и те же физиологические функции, оказывая непосредственное влияние на наше здоровье. Вот некоторые из функций:
Вот некоторые из функций:
- Помогает организму переваривать определенные продукты, которые желудок и тонкий кишечник не могут переварить.
- Производство некоторых витаминов (B и K).
- Играет важную роль в иммунной системе, выполняя барьерный эффект.
Здоровая и сбалансированная микробиота кишечника — ключ к обеспечению правильного пищеварения.
Итак, что такое Дисбактериоз и какое отношение он имеет к СРК?
Итак, мы прошли долгий путь с тех пор, как Теодор Эшерих впервые открыл Escherichia coli, но мы все еще многого не знаем о микробиоте кишечника.Что мы действительно знаем, так это то, что люди со здоровой микробиотой кишечника, кажется, наполнены счастливыми сообществами микробов, которые работают вместе, чтобы поддерживать ваше здоровье, как физическое, так и психическое. Когда одна из этих счастливых маленьких колоний выходит из равновесия, это может привести к так называемому дисбактериозу . Это просто причудливый способ сказать, что все микробы, живущие в вашем кишечнике, не в порядке.
Так вот, в большинстве случаев, если произойдет небольшой дисбаланс, вы, возможно, будете страдать от чего-то столь же незначительного, как расстройство желудка.Однако, если беспокойство между вашими микробными сообществами перерастает из небольшого спора по соседству в полномасштабную войну в вашем кишечнике, будьте осторожны. Вы можете столкнуться с риском развития гораздо более серьезных осложнений со здоровьем. Недавние исследования связали дисбактериоз с расстройствами кишечника, такими как синдром раздраженного кишечника (СРК), и даже хроническими заболеваниями кишечника, такими как болезнь Крона и язвенный колит. Было также высказано предположение, что, хотя дисбактериоз может быть причиной этих расстройств, он также может ухудшить симптомы.В этой области предстоит еще много исследований.
Итак, что вызывает дисбактериоз?
Как всегда, когда дело касается кишечника, нет ничего универсального, поэтому ответ на этот вопрос сложен и у всех может сработать по-разному.
Например, многие эксперты предполагают, что диета с высоким содержанием пребиотиков может предотвратить дисбактериоз, однако это было бы сложным изменением образа жизни для многих людей с СРК, если бы они придерживались краткосрочной диеты с FODMAP. Причина этого в том, что многие продукты с высоким содержанием FODMAP являются диетическими пребиотиками.
Однако есть несколько типичных причин дисбактериоза, за которыми следует внимательно следить:
Антибиотики
Если вы регулярно принимаете обычные антибиотики или едите много мяса, выращенного с помощью антибиотиков, вы подвержены риску дисбактериоза. Некоторые антибиотики могут серьезно нарушить баланс вашего микробиома. Вот почему следует избегать злоупотребления антибиотиками.
Диета с высоким содержанием простых сахаров / углеводов
Мы пришли к выводу, что вы действительно то, что вы едите! Диета глубоко влияет на состав и функции кишечной микробиоты, потенциально способствуя развитию симптомов СРК. Например, потребление искусственных подсластителей может привести к нарушению регуляции кишечной микробиоты.
Например, потребление искусственных подсластителей может привести к нарушению регуляции кишечной микробиоты.
Высокобелковая диета
Хотя она может быть полезна для кратковременной потери веса и полезна для некоторых аспектов метаболического здоровья, диета с высоким содержанием белка может быть не идеальной в долгосрочной перспективе из-за своего воздействия на микробиоту кишечника . Исследователи обнаружили, что высокое потребление белка увеличивает ферментацию в толстой кишке, вызывая образование определенных токсичных бактериальных метаболитов, связанных с такими заболеваниями, как колоректальный рак.
Попробуйте поэкспериментировать с более сбалансированным питанием. Чтобы получить простое руководство о том, как составить более сбалансированное питание, обратитесь к Руководству по питанию Канады.
Стресс, как физический, так и психический
Было замечено, что длительный стресс у человека фактически подавляет его способность вырабатывать нечто, называемое иммуноглобулином A. Иммуноглобулин A на самом деле играет очень важную роль. Он помогает бороться (как вы уже догадались) с плохими микробами, также известными как патогены. Это означает, что пока вы находитесь в состоянии стресса, ваша естественная защита от кишечных плохих парней падает, и в вашем микробиоме прорывается ад.Эти патогены вытесняют хорошие микробы и начинают враждебный захват. Это одна из причин, почему стресс является огромным триггером для людей с СРК, о чем мы расскажем в этой статье.
Иммуноглобулин A на самом деле играет очень важную роль. Он помогает бороться (как вы уже догадались) с плохими микробами, также известными как патогены. Это означает, что пока вы находитесь в состоянии стресса, ваша естественная защита от кишечных плохих парней падает, и в вашем микробиоме прорывается ад.Эти патогены вытесняют хорошие микробы и начинают враждебный захват. Это одна из причин, почему стресс является огромным триггером для людей с СРК, о чем мы расскажем в этой статье.
Злоупотребление алкоголем
Злоупотребление алкоголем (употребление двух или более алкогольных напитков в день), как известно, является серьезным нарушителем микробного сообщества, живущего в нашем кишечнике. Может увеличить долю вредных бактерий, снизить уровень полезных бактерий; а также может спровоцировать чрезмерный рост микроорганизмов, что связано с заболеванием печени.Поскольку это может нарушить баланс бактерий в кишечнике, употребляйте меньше алкоголя или вообще избегайте его.
Желудочно-кишечные инфекции
Дисбактериоз также может вызывать так называемый постинфекционный СРК. Большинство людей, страдающих кишечными инфекциями (например, кишечной палочкой), быстро выздоравливают. Однако, к сожалению, некоторые этого не делают. Поскольку микробиота кишечника делает то, что делает лучше всего (защищает вас от вреда!), Она может проиграть битву с особенно серьезной инфекцией. Это может привести к дисбактериозу и впоследствии вызвать СРК у некоторых людей.
Большинство людей, страдающих кишечными инфекциями (например, кишечной палочкой), быстро выздоравливают. Однако, к сожалению, некоторые этого не делают. Поскольку микробиота кишечника делает то, что делает лучше всего (защищает вас от вреда!), Она может проиграть битву с особенно серьезной инфекцией. Это может привести к дисбактериозу и впоследствии вызвать СРК у некоторых людей.
Итак, дисбактериоз вызывает СРК?
Короткий ответ — наверное. Было показано, что дисбоз связан с несколькими заболеваниями и состояниями, одним из которых является СРК. В настоящее время ученые работают над тем, чтобы точно выяснить, КАК микробиота может влиять на симптомы СРК. Самое интересное во всем этом заключается в том, что недавно были получены очень многообещающие доказательства того, что да, и у мужчин, и у женщин с СРК есть микробиомы, которые существуют в состоянии дисбактериоза.Это захватывающе, потому что это действует как отправная точка. Способ начать углубляться в науку и найти причину, а однажды, возможно, даже найти лекарство.
Проблема в том, что ученым еще предстоит точно определить, где и как их микробиомы перешли от дисбактериоза к СРК. Какие штаммы микробов вымерли, вызывая СРК? Были ли введены новые штаммы патогенов? Если да, то сколько? А какой? Атакует ли вредоносный штамм и уничтожает другие штаммы? Или диета человека заставляла голодать колонии микробов? Это был стресс? Или это была комбинация всего этого?
Хотя детали все еще неясны, данные позволяют предположить, что у людей, живущих с СРК, в кишечнике действительно менее разнообразное и более нестабильное сообщество бактерий, чем у людей, которые не страдают этим заболеванием.
Однако будущее выглядит светлым. С каждым днем мы узнаем все больше и больше о микробиоме! А пока позаботьтесь о своем!
Ссылки
Хаврелак, Дж. А., и Майерс, С. П. (2004, июнь). Причины дисбактериоза кишечника: обзор. Получено с https://www.ncbi.nlm.nih.gov/pubmed/15253677/
Kennedy, P. J., Cryan, J. F., Dinan, T. G., & Clarke, G. (2014, 21 октября). Синдром раздраженного кишечника: расстройство оси микробиом-кишечник-мозг? Получено с https: // www.ncbi.nlm.nih.gov/pmc/articles/PMC4202342/
G., & Clarke, G. (2014, 21 октября). Синдром раздраженного кишечника: расстройство оси микробиом-кишечник-мозг? Получено с https: // www.ncbi.nlm.nih.gov/pmc/articles/PMC4202342/
Tamboli, C.P., Neut, C., Desreumaux, P., & Colombel, J. F. (2004, январь). Дисбактериоз при воспалительном заболевании кишечника. Получено с https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1773911/
Влияние микробиома кишечника на неинфекционные заболевания и поведение: основные результаты проекта Mynewgut Андреу Прадос-Хизер Галипо — https: / /www.gutmicrobiotaforhealth.com/en/the-gut-microbiomes-influence-on-non-communicable-diseases-and-behaviour-main-findings-of-mynewgut-project/
Интервью с Берндом Шнаблом: «хронический алкоголь. Изменяет кишечную микробиоту и может привести к избыточному бактериальному росту »Хизер Галипо — Редакционная группа GMFH — https: // www.gutmicrobiotaforhealth.com/en/interview-bernd-schnabl-chronical-alcohol-alters-gut-microbiota-can-lead-bacterial-overgrowth/
Кверцетин улучшает дисбактериоз кишечника у мышей, получавших антибиотики
rsc.org/schema/rscart38″> Разнообразие и активность микробиоты кишечника людей и животных в значительной степени зависят от диеты. Кверцетин, один из типичных полифенолов в рационе человека, обладает широким спектром биологических свойств. Целью этого исследования было изучить пребиотические эффекты кверцетина у мышей, получавших антибиотики.Дисбактериоз кишечника был успешно индуцирован у мышей обработкой коктейлем антибиотиков. Для исследования содержания короткоцепочечных жирных кислот, а также разнообразия и состава кишечных микробов использовались методы газовой хроматографии и высокопроизводительного секвенирования 16S рДНК. Результаты показали, что добавление кверцетина значительно улучшило разнообразие кишечного бактериального сообщества у мышей, получавших антибиотики ( P <0,05). Между тем, барьерная функция кишечника также заметно восстановилась, на что указывает снижение содержания сывороточной D -молочной кислоты и активности сывороточной диаминоксидазы ( P <0. 05). Длина ворсинок кишечника и толщина слизистой оболочки также значительно увеличились в ответ на лечение кверцетином ( P <0,05). Кроме того, продукция бутирата с фекалиями была значительно увеличена у мышей, получавших кверцетин ( P <0,05). В заключение, кверцетин эффективен для восстановления микробиоты кишечника у мышей после лечения антибиотиками и может действовать как пребиотик в борьбе с дисбактериозом кишечника.
05). Длина ворсинок кишечника и толщина слизистой оболочки также значительно увеличились в ответ на лечение кверцетином ( P <0,05). Кроме того, продукция бутирата с фекалиями была значительно увеличена у мышей, получавших кверцетин ( P <0,05). В заключение, кверцетин эффективен для восстановления микробиоты кишечника у мышей после лечения антибиотиками и может действовать как пребиотик в борьбе с дисбактериозом кишечника.У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент… Что-то пошло не так. Попробуйте еще раз?
Попробуйте еще раз?Дисбактериоз кишечника у детей с синдромом короткой кишки связан с нарушением исхода | Microbiome
Предпосылки
Детская кишечная недостаточность (IF) определяется как неспособность желудочно-кишечного тракта поддерживать адекватный рост, гидратацию и гомеостаз электролитов у детей без парентерального питания (PN).Синдром короткой кишки (SBS) — наиболее частая причина детской IF. Состояние вызвано массивной резекцией тонкой кишки из-за некротического энтероколита (НЭК) или заворота, а также врожденных пороков развития, таких как гастрошизис и атрезия тощей кишки. СБС новорожденных — заболевание с высокой заболеваемостью и смертностью [1]. Медицинское руководство SBS направлено на обеспечение полного энтерального / перорального кормления и прекращение приема PN.
Кишечная микробиота, по-видимому, является основным фактором в определении успешного клинического исхода при SBS, определяемом как независимость от лечения PN и адаптации кишечника.Изменения в микробиоте могут привести к серьезным осложнениям, таким как избыточный бактериальный рост в тонкой кишке (SBBO) и воспаление слизистой оболочки кишечника, что может предотвратить отлучение от ПП за счет нарушения абсорбционных функций кишечника [2,3]. При SBBO у детей рекомендовано длительное лечение люминальными / пероральными антибиотиками [4,5]. Большинство случаев SBS возникает у новорожденных в период, когда стерильный кишечник обычно заселяется бактериями, достигая микробного профиля, характерного для желудочно-кишечного тракта взрослых, примерно в возрасте от 2 до 4 лет [6].Нарушение сбалансированного микробного сообщества кишечника, то есть дисбактериоз, с повышенным относительным содержанием факультативных анаэробных Enterobacteriaceae в толстой кишке, наблюдается при воспалительном заболевании кишечника (ВЗК) на моделях мышей, у людей с болезнью Крона и НЭК у недоношенных детей [7,8].
На сегодняшний день нет сообщений о картировании кишечной микробиоты у детей с SBS. Здесь мы представляем первый отчет о микробном профиле у детей с SBS с использованием секвенирования гена 16S рРНК на платформе Illumina MiSeq.
Методы
Пациенты
Это исследование было одобрено региональным комитетом по этике медицинских исследований в Упсале (Dnr2012 / 002). Информированное письменное согласие на сбор образцов и последующие анализы было получено от родителей. Характеристики исследуемой группы и соответствующих здоровых братьев и сестер представлены в таблице 1. В исследование включены 11 детей в возрасте от 1,5 до 7 лет с диагнозом ИФ / СБС в неонатальном периоде, из которых двое относятся к группе тройняшек (2А и 3А) (таблица 1).Все дети, кроме одного, родились недоношенными. Ребенку 1А, 8А и 13А была проведена процедура удлинения кишечника с серийной поперечной энтеропластикой (STEP) [9]. Пятеро детей не были отлучены от ПП на момент исследования. Семь здоровых братьев и сестер служили контролем. Дети, получающие ПП, получали пероральный и / или энтеральный прием безлактозной гидролизованной белковой смеси и соответствующий возрасту потребление твердой пищи со снижением содержания дисахаридов в соответствии с таблицей 1.
Дети, получающие ПП, получали пероральный и / или энтеральный прием безлактозной гидролизованной белковой смеси и соответствующий возрасту потребление твердой пищи со снижением содержания дисахаридов в соответствии с таблицей 1.
Сбор данных и статистический анализ
Образцы фекалий собирали и хранили при -80 ° C до анализа.ДНК экстрагировали из каждого образца фекалий с помощью набора для выделения ультрачистой фекальной ДНК (MoBio, Naxo Ltd, Тарту, Эстония) в соответствии с инструкциями производителя.
Библиотеки секвенирования получали путем амплификации области V3-V4 гена 16S рРНК с использованием праймеров 341f-805r, описанных Hugerth et al. . [10]. После начальной амплификации была проведена вторая ПЦР для присоединения адаптеров Illumina, а также штрих-кодов, которые позволяют мультиплексировать. Образцы были секвенированы с использованием IlluminaMiSeq, что дало в общей сложности 10 136 440 считываний 2 × 300 пар оснований со средним значением 307 165 считываний на образец.Последовательности праймеров были обрезаны, а считывания парных концов, произведенные инструментом для секвенирования, были объединены с использованием SeqPrep версии 1.1 (https://github.com/jstjohn/SeqPrep) с параметрами по умолчанию и затем обработаны с помощью конвейера QIIME 1.8.0 ( Количественное понимание микробной экологии) [11]. Объединенные чтения были случайным образом разбиты на подвыборку до равной глубины 151 610 считываний на выборку, что было минимальным числом считываний среди выборок. Используя алгоритм UCLUST [12], встроенный в конвейер QIIME, последовательности были кластеризованы с 97% идентичностью по справочной базе данных Greengenes, что дало 4216 OTU (операционные таксономические единицы) [11].Для каждого образца; количество не-одноэлементных OTU, а также наиболее доминирующих OTU с соответствующим описанием представлено в дополнительных данных (Дополнительный файл 1).
Образцы были секвенированы с использованием IlluminaMiSeq, что дало в общей сложности 10 136 440 считываний 2 × 300 пар оснований со средним значением 307 165 считываний на образец.Последовательности праймеров были обрезаны, а считывания парных концов, произведенные инструментом для секвенирования, были объединены с использованием SeqPrep версии 1.1 (https://github.com/jstjohn/SeqPrep) с параметрами по умолчанию и затем обработаны с помощью конвейера QIIME 1.8.0 ( Количественное понимание микробной экологии) [11]. Объединенные чтения были случайным образом разбиты на подвыборку до равной глубины 151 610 считываний на выборку, что было минимальным числом считываний среди выборок. Используя алгоритм UCLUST [12], встроенный в конвейер QIIME, последовательности были кластеризованы с 97% идентичностью по справочной базе данных Greengenes, что дало 4216 OTU (операционные таксономические единицы) [11].Для каждого образца; количество не-одноэлементных OTU, а также наиболее доминирующих OTU с соответствующим описанием представлено в дополнительных данных (Дополнительный файл 1). Индексы Шеннона для разнообразия были рассчитаны для детей с SBS, получающих и не принимавших PN, и проверены на значимость с помощью критерия суммы рангов Вилкоксона. Используя конвейер QIIME, были получены невзвешенные расстояния UniFrac, которые использовались для исследования бета-разнообразия путем построения координат PCA. Подробные сведения о праймерах гена 16S рРНК, условиях амплификации и штрих-кодах образцов показаны в дополнительных данных (дополнительный файл 2).
Индексы Шеннона для разнообразия были рассчитаны для детей с SBS, получающих и не принимавших PN, и проверены на значимость с помощью критерия суммы рангов Вилкоксона. Используя конвейер QIIME, были получены невзвешенные расстояния UniFrac, которые использовались для исследования бета-разнообразия путем построения координат PCA. Подробные сведения о праймерах гена 16S рРНК, условиях амплификации и штрих-кодах образцов показаны в дополнительных данных (дополнительный файл 2).
Результаты
На рисунке 1 показано, что индекс разнообразия Шеннона значительно снижен у детей с SBS, все еще получающих PN, по сравнению с детьми, отлученными от PN. Ни у кого из детей, получавших ПП, не осталось ICV.
Рис. 1Индекс разнообразия Шеннона у детей с SBS, все еще получающих PN, по сравнению с детьми, отлученными от PN.
У детей, все еще получающих PN, четверо из пяти (1A, 3A, 8A и 9A) были обследованы на предмет нескольких эпизодов подозрения на SBBO, также во время взятия пробы кала (Таблица 1). Их лечили пероральным метронидазолом, триметоприм-сульфаметоксазолом, гентамицином или амоксициллин-клавулановой кислотой. У этих пациентов Enterobacteriacae были наиболее многочисленным таксономическим семейством и полностью доминировали в микробном сообществе этих детей (рис. 2). У оставшегося пациента в этой группе (12А), все еще принимающего ПП и с пониженным индексом разнообразия Шеннона, было обнаружено относительное преобладание Lactobacillaceae , за которым следовали Enterobacteriacae. В целом, высокая относительная численность Enterobacteriacae была связана с SBS у 6 из 11 пациентов (1А, 3А, 8А, 9А, 11А и 12А). У оставшихся пяти пациентов с SBS, все без PN (2A, 4A, 13A, 16A и 18A), был более разнообразный состав микробиоты и более равномерное распределение таксономических семейств. Однако ни один из детей SBS, кроме одного (2А), не достиг индексов разнообразия Шеннона на том же уровне, что и контрольная группа (таблица 1). У одного из детей, все еще получающих PN (1A), верхняя и нижняя эндоскопия с биопсией выявила макроскопическое и гистопатологическое острое воспаление в желудке, двенадцатиперстной кишке, тонкой кишке и проксимальном отделе толстой кишки.
Их лечили пероральным метронидазолом, триметоприм-сульфаметоксазолом, гентамицином или амоксициллин-клавулановой кислотой. У этих пациентов Enterobacteriacae были наиболее многочисленным таксономическим семейством и полностью доминировали в микробном сообществе этих детей (рис. 2). У оставшегося пациента в этой группе (12А), все еще принимающего ПП и с пониженным индексом разнообразия Шеннона, было обнаружено относительное преобладание Lactobacillaceae , за которым следовали Enterobacteriacae. В целом, высокая относительная численность Enterobacteriacae была связана с SBS у 6 из 11 пациентов (1А, 3А, 8А, 9А, 11А и 12А). У оставшихся пяти пациентов с SBS, все без PN (2A, 4A, 13A, 16A и 18A), был более разнообразный состав микробиоты и более равномерное распределение таксономических семейств. Однако ни один из детей SBS, кроме одного (2А), не достиг индексов разнообразия Шеннона на том же уровне, что и контрольная группа (таблица 1). У одного из детей, все еще получающих PN (1A), верхняя и нижняя эндоскопия с биопсией выявила макроскопическое и гистопатологическое острое воспаление в желудке, двенадцатиперстной кишке, тонкой кишке и проксимальном отделе толстой кишки. У ребенка 3А, также получавшего ПП, верхняя эндоскопия с биопсией показала атрофию ворсинок тонкой кишки.
У ребенка 3А, также получавшего ПП, верхняя эндоскопия с биопсией показала атрофию ворсинок тонкой кишки.
Микробные сообщества у детей с SBS, получавших PN (1A, 3A, 8A, 9A, 12A), детей с SBS, отлученных от PN (2A, 4A, 11A, 13A, 16A, 18A) и братьев и сестер (2C1, 2C2, 11C1, 11C2, 12C, 13C1, 13C2). На рисунке показана относительная численность 19 наиболее распространенных таксономических семейств, на которые приходится не менее 84% численности во всех выборках.
На рисунке 3 представлены индексы разнообразия Шеннона, а на рисунке 4 — невзвешенные расстояния UniFrac у детей с SBS на PN (1A, 3A, 8A, 9A, 12A), дети SBS, отлученные от PN (2A, 4A, 11A, 13A , 16A, 18A) и братьев и сестер (2C1, 2C2, 11C1, 11C2, 12C, 13C1, 13C2).
Рисунок 3 Индекс разнообразия Шеннона у детей с SBS, получавших PN (1A, 3A, 8A, 9A, 12A), детей с SBS, отлученных от PN (2A, 4A, 11A, 13A, 16A, 18A) и братьев и сестер (2C1 , 2C2, 11C1, 11C2, 12C, 13C1, 13C2).
График PCoA, описывающий невзвешенное расстояние UniFrac между образцами. Попарные расстояния между всеми образцами проецируются на двумерное пространство, где ось PC1 описывает наибольшую степень вариации. Таким образом, считается, что образцы, которые сгруппированы близко друг к другу, имеют большую долю филогенетического дерева по сравнению с образцами, которые более разделены.
У нас была уникальная возможность изучить тройню, представляющую все три группы. Ребенок 2А и ребенок 3А были тройняшками мужского пола, рожденными на 23 неделе беременности. Оба мальчика перенесли НЭК в неонатальном периоде, что привело к резекции тонкой кишки (таблица 1). Третий тройняшек (2С2) остался здоровым. У ребенка 2А было резецировано только 2 см тонкой кишки, однако у него развился ПФ после обширной НЭК и он стал зависимым от ПП. Во время лечения ПН у него не было признаков СБО. Его приучили к полноценному пероральному вскармливанию и без антибиотиков за 3 месяца до забора фекалий. Его кишечное бактериальное разнообразие было таким же, как у его здорового брата (SDI 4, 67 и 4, 97, соответственно).
Его кишечное бактериальное разнообразие было таким же, как у его здорового брата (SDI 4, 67 и 4, 97, соответственно).
Ребенок 12A лечился антибиотиками только в течение первых 2 недель постнатального периода, у него не было признаков SBBO, и отлучение от PN продвигалось, но медленно. Ее фекальное бактериальное разнообразие показало, что Lactobacillacae являются наиболее относительно многочисленным таксономическим семейством в соответствии с нашими предыдущими результатами (Рисунок 2) [13]. Мы смогли обнаружить Clostridium difficile у двух из десяти пациентов с SBS (пациенты 2A и 11A) и в очень низкой относительной численности (данные не показаны).
Выводы
Тенденция SBBO и воспаления кишечника к задержке или предотвращению отлучения от PN у этих детей с SBS, по-видимому, связана с микробным дисбиозом в кишечном тракте. Этот вывод согласуется с предыдущим исследованием, показывающим, что введение ПП было независимо связано с SBBO [14]. Влияние PN на изменение профиля из-за истощения микробиома маловероятно, так как нарушение всасывания при пероральном / энтеральном питании является основной проблемой при SBS. В целом, наблюдаемые изменения микробиоты у детей с SBS, скорее всего, являются как причиной, так и следствием болезненного статуса ребенка. Ограничением исследования является небольшая исследовательская группа, и смешанные факторы, которые могут повлиять на результаты, — это возраст, длина кишечника и лечение антибиотиками. Однако когорта в настоящем исследовании представляет детей с SBS в клинической практике.
В целом, наблюдаемые изменения микробиоты у детей с SBS, скорее всего, являются как причиной, так и следствием болезненного статуса ребенка. Ограничением исследования является небольшая исследовательская группа, и смешанные факторы, которые могут повлиять на результаты, — это возраст, длина кишечника и лечение антибиотиками. Однако когорта в настоящем исследовании представляет детей с SBS в клинической практике.
В нашем центре мы лечим SBBO пероральными антибиотиками в соответствии с рекомендациями других центров [4-6].Однако наиболее вероятно, что антибиотики еще больше будут способствовать развитию дисбактериоза у этих детей. У детей с SBS нормальная колонизация нарушается из-за раннего и частого использования антибиотиков, а уменьшение бактериального разнообразия позволяет потенциальным патогенным бактериям расширяться. Было высказано предположение, что антибиотики снижают устойчивость к колонизации против Enterobacteriacae , таких как Escherichia coli и Salmonella enterica , за счет повышения воспалительного тонуса слизистой оболочки кишечника [15]. Чаще всего пробиотики используются для изменения микробиоты кишечника при SBS; однако существуют противоречивые данные и сообщения о пробиотической септицемии [16].
Чаще всего пробиотики используются для изменения микробиоты кишечника при SBS; однако существуют противоречивые данные и сообщения о пробиотической септицемии [16].
Общее снижение бактериального разнообразия у наших детей с SBS согласуется с дисбактериозом кишечника у пациентов с IBD, младенцев с NEC, а также было описано в модели SBS у поросят [7,8,17,18]. Кроме того, у детей с рецидивирующей диареей, связанной с C. difficile- , наблюдается снижение фекального разнообразия с уменьшением на Bacteriodetes и Firmicutes [19].У таких детей успешность трансплантации фекальной микробиоты (FMT) превышает 90%. Такое лечение также успешно использовалось в качестве дополнения к лечению ВЗК [19,20]. Следовательно, FMT может оказаться альтернативой лечения в тщательно отобранных случаях SBS с дисбактериозом. Однако, поскольку дети с SBS часто уязвимы из-за своего исходного состояния здоровья, необходимо учитывать трудности и риски FMT. Хотя случаи серьезных побочных эффектов редки, одним из таких рисков является заражение донором, когда бессимптомные микроорганизмы, не вызывающие проблем у здорового донора, могут вызвать реакцию у реципиента.


 Максимально схожий с ним диагноз – СИБР (синдром избыточного бактериального роста). Ставится он при обнаружении более 105 микроорганизмов в миллилитре аспирата, взятого из тонкой кишки.
Максимально схожий с ним диагноз – СИБР (синдром избыточного бактериального роста). Ставится он при обнаружении более 105 микроорганизмов в миллилитре аспирата, взятого из тонкой кишки.

 Газы есть и в хорошо функционирующем организма. Но в нем налажен процесс их выведения. При дисбактериозе газы скапливаются, приводя к вздутию и болевым ощущениям.
Газы есть и в хорошо функционирующем организма. Но в нем налажен процесс их выведения. При дисбактериозе газы скапливаются, приводя к вздутию и болевым ощущениям. Помогают очистить кишечник от болезнетворных микроорганизмов.
Помогают очистить кишечник от болезнетворных микроорганизмов. Она содержится в овощах, фруктах, злаках и хлебе из муки грубого помола;
Она содержится в овощах, фруктах, злаках и хлебе из муки грубого помола; д)
д)