причины, симптомы, диагностика и методы лечения на сайте «Альфа-Центр Здоровья»
Воспалительное кожное заболевание, возникающее в результате воздействия физических, химических или биологических факторов, сопровождается покраснением кожи, зудом и жжением, образованием пузырьков и волдырей.Контактным называется любой дерматит, вызванный непосредственным взаимодействием каких-либо веществ с кожей. Контактный дерматит бывает простым и аллергическим. И тот, и другой может быть острым, подострым и хроническим.
Простой контактный дерматит
Простой контактный дерматит встречается чаще аллергического. Причиной его возникновения служит токсическое действие раздражающих веществ, ведущее к разрушению эпидермиса (внешнего слоя кожи) и воспалению кожи. С большинством раздражающих веществ человек сталкивается повседневно — в быту или на работе. Одни из них — слабые раздражители, вызывающие дерматит только при условии регулярных контактов с кожей (моющие средства, очистители, растворители). Другие — едкие вещества, способные вызвать дерматит после однократного контакта (хлорная известь, сильные кислоты, щелочи). От простого контактного дерматита не застрахован ни один человек.
Жалобы
Слабые раздражители вызывают эритему (покраснение кожи), образование трещин, сухость кожи. Зуд обычно слабый или умеренный. Чаще всего от простого контактного дерматита страдают кисти, а также лицо, особенно веки. В тяжелых случаях наблюдаются отек, мокнутие, боль. Едкие вещества через несколько часов после попадания на кожу вызывают болезненные пузыри.
Лечение
Задачи лечения врачом дерматовенерологом включают восстановление эпидермиса и его дальнейшую защиту от раздражающего вещества. При хроническом простом контактном дерматите нередко бывает достаточно свести к минимуму контакты с мылом и водой, применять смягчающие средства (кремы или мази) и при поражении кистей использовать перчатки. На острой стадии заболевания иногда приходится наносить мази глюкокортикоидов под повязки.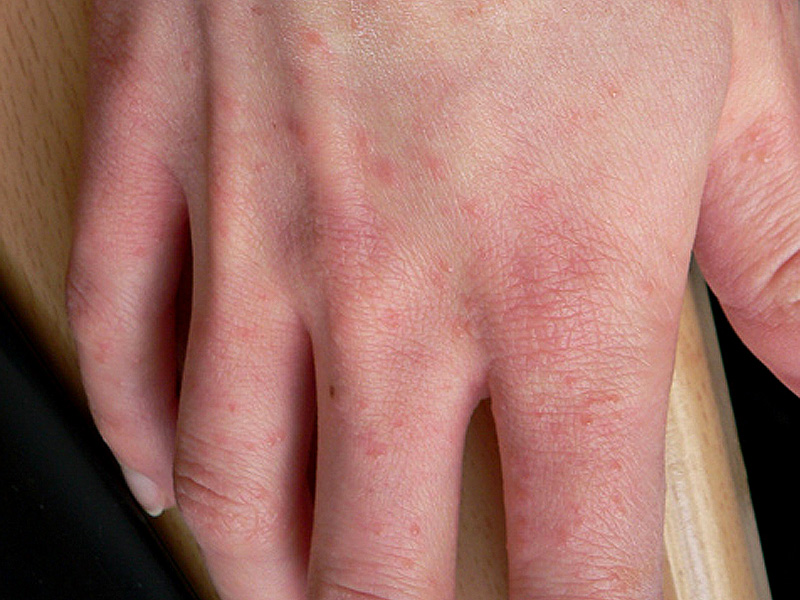
Аллергический контактный дерматит
Аллергический контактный дерматит представляет собой аллергическую реакцию на какое-либо вещество. Эта реакция может развиться как после однократного контакта с аллергеном (например, с некоторыми растениями), так и в результате его многолетнего регулярного воздействия (например, никеля или парфюмерных изделий).
Жалобы
В месте контакта сначала возникает сильный зуд, а затем — зудящая сыпь. Поскольку контакт с аллергеном и начало заболевания могут быть разнесены во времени на две недели, установить дату контакта часто не удается. Хронический аллергический контактный дерматит длится месяцами и годами.
На пораженных участках отмечаются покраснение, отек, сыпь и мокнутие. Локализация и расположение сыпи зависят от причины заболевания. Так, аллерген, содержащийся в декоративной косметике, приведет к поражению лица, никелевое кольцо — к поражению одного из пальцев, а резиновые шлепанцы — к поражению стоп.
Лечение
При сыпи и мокнутии помогают примочки с ацетатом алюминия (жидкость Бурова). После того как пораженные участки кожи подсохнут, назначают глюкокортикоиды для наружного применения. В тяжелых случаях требуются H1-блокаторы (антигистаминные препараты) и глюкокортикоиды внутрь. Для излечения важно выявить и устранить аллерген, но для этого зачастую нужны аппликационные пробы. Проведение аппликационных проб особенно полезно для тех пациентов, которые на работе контактируют со множеством химических веществ.
Распространенные кожные заболевания у собак: симптомы и лечение
К сожалению, кожные заболевания у собак весьма распространены. Некоторые аллергические реакции становятся причиной беспрестанного расчесывания, вылизывания, покусывания и ерзанья, доставляя питомцам сильный дискомфорт.
Внешние факторы
Иногда у собак наблюдается чувствительность к газонной траве — она вызывает раздражение. Скопление влаги на коже тоже может привести к повреждениям кожи — образованию так называемых «горячих точек», от которых больше всего страдают собаки с густой или длинной, склонной к скатыванию шерстью.
Другие факторы окружающей среды, например пыль, плесень, цветочная пыльца, мучнистая роса и прочие ингаляционные аллергены, также могут вызвать зуд и доставить дискомфорт вашему питомцу. В итоге это приведет к образованию болезненных поражений кожи и выпадению шерсти. Не забывайте, что парфюмерия и табачный дым тоже могут вызвать у собаки повышенную чувствительность.
Пищевая аллергия
Пищевая аллергия у собак — явление крайне редкое, вызываемое, как правило, белками, содержащимися в говядине, свинине, баранине, курице, яйцах и рыбе, а также белками растительного происхождения, получаемыми из пшеницы. Больше всего проблем со здоровьем у животных вызывают говядина, молочные продукты и пшеница.
К основным симптомам пищевой аллергии относятся раздражение кожи и чрезмерное расчесывание, но могут появиться и проблемы с пищеварением, такие как рвота и диарея. Неважно, какие признаки аллергии вы заметили, — лучше всего сразу обратиться к ветеринарному врачу.
Паразитарная аллергия
У собак может наблюдаться аллергическая реакция на укусы блох (по сути — иммунный ответ на слюну блохи), называемая паразитарным дерматитом. Проявляется в форме повышенного зуда, воспаления и выпадения шерсти.
Несмотря на то что наиболее распространенной причиной паразитарного дерматита у собаки являются блохи, укусы клещей тоже могут вызвать у животного аллергическую реакцию.
Инфекционный дерматит
У собак может развиваться такая болезнь, как инфекционный дерматит, вызываемый бактериями, грибами и вирусами. Одной из весьма распространенных причин инфекционного дерматита являются грибы дерматофиты, более известные как стригущий лишай. Еще одним возбудителем инфекционного дерматита является дрожжевой грибок малассезия (Malassezia pachydermatis), активизирующийся на фоне других заболеваний. Для лечения грибковой формы дерматита в дополнение к препаратам, применяемым для лечения основного заболевания, назначаются антибиотики или противогрибковые средства.
Как помочь животному
Проще всего вылечить паразитарный дерматит. Если вы заметили, что причиной зуда у щенка стали именно паразиты, обработайте дом и остальных животных средством от эктопаразитов и в дальнейшем используйте профилактические препараты. Прочие виды аллергии и возбудителей самостоятельно выявить нелегко. Поэтому если от блох вы избавились, а животное по-прежнему страдает от непрекращающегося зуда, кожного раздражения и выпадения шерсти, необходимо обратиться к ветеринарному врачу. При обращении в клинику вашей собаке наверняка сделают ряд анализов крови, возьмут образцы кожи и назначат другие лабораторные исследования, чтобы выявить истинную причину заболевания.
Не исключено, что сужение круга возможных причин кожного зуда у собаки будет проходить путем проб и ошибок, но вам необходимо набраться терпения. Ветеринарный специалист посоветует вам перейти на диетический корм, чтобы уменьшить зуд у вашего питомца. После выявления раздражителя или аллергена необходимо удалить его из окружающей обстановки или пищи вашего любимца.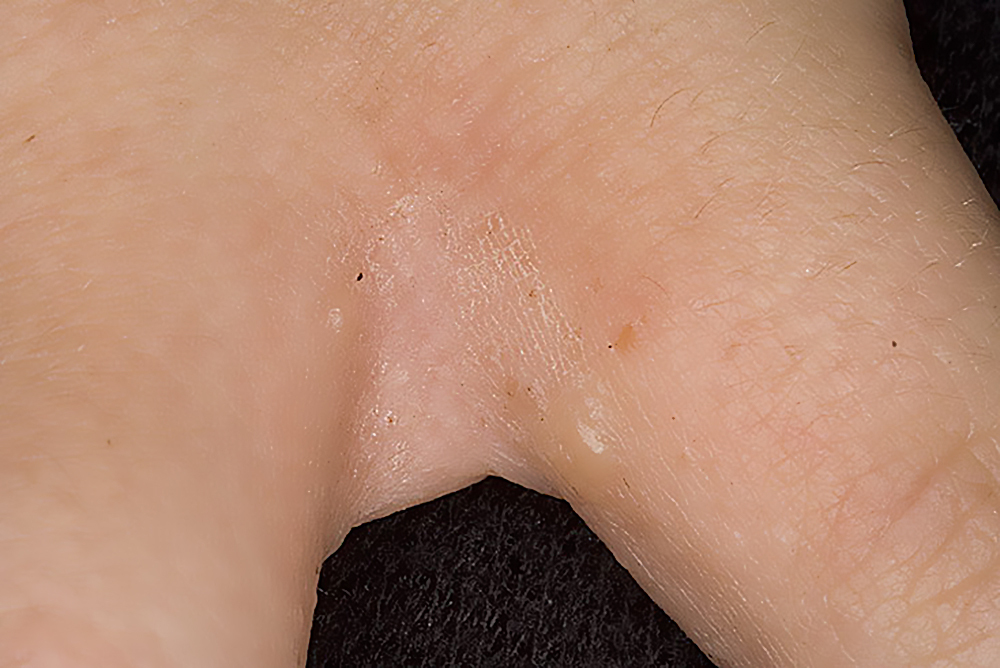
При тяжелых поражениях кожи и признаках инфекции необходимо использовать антибиотики. Еще ветеринарный специалист наверняка посоветует вам пользоваться специальными шампунями и ополаскивателями, помогающими немного облегчить состояние питомца.
Невозможно спокойно наблюдать за страданиями вашего любимца. Первое, что вы можете сделать, чтобы помочь четвероногому другу, — это выявить причины заболевания и обратиться к ветеринарному специалисту.
Contributor Bio
Жан-Мари Баухаус
Жан-Мари Баухаус — автор художественных произведений, писатель и редактор-фрилансер. Она часто пишет о домашних животных и уходе за ними, работая в домашнем офисе в городе Талса, штат Оклахома. Коты Жан-Мари обычно сидят у нее на коленях и помогают в написании статей.
Первые признаки аллергии: симптомы, диагностика, лечение первых признаков аллергии
Чихание
Чихание — естественный для организма способ избавления от раздражающих субстанций (пыль, песок и т.д.), которые удаляются вместе с небольшим количеством секреторной жидкости. При аллергии эта реакция становится преувеличенной. Приступы чихания длятся изо дня в день без очевидной причины, при отсутствии признаков простуды.
Заложенность носа, насморк
При аллергии слизистая оболочка носа воспаляется и утолщается. Это приводит к нарушению нормального оттока слизи из носовых ходов или даже полностью его блокирует. Попытки высморкаться ни к чему не приводят и только усиливают заложенность носа. Часто аллергия проявляется непрерывным или эпизодическим выделением из носа большого количества прозрачной водянистой слизи («вода из носа»), тогда как при простуде выделения обычно желтоватые и более густые.
Покраснение и зуд глаз, слезотечение
Покраснение глаза, слезы, зуд и жжение могут возникать при попадании в глаз инородного предмета (соринка, песчинка, ресница), но как только причина раздражения устранена, дискомфорт проходит. Однако если у Вас аллергия, ситуация резко меняется: зуд в глазах возникает без внешней причины, и ничто не может его уменьшить. Этот зуд может продолжаться неделями. Веки обычно бывают покрасневшими и опухшими. Характерным является одновременное и одинаковое поражение обоих глаз.
Кашель
Кашель «придуман» организмом для удаления микроорганизмов, пылевых и других инородных частиц, попавших в бронхи. Он является нормальной защитной реакцией при простудном заболевании. Однако, при бронхиальной астме кашель не несет защитную функцию, а является следствием сужения просвета дыхательных путей из-за аллергического воспаления в бронхах. Для такого кашля характерным является приступообразность, «сухость» (т.е. отсутствие мокроты), кашель может быть изнуряющий, «до рвоты». Часто при бронхиальной астме приступ сухого кашля заканчивается обильным отхождением светлой немного пенистой мокроты, после чего наступает облегчение.
Одышка, свисты при дыхании
Одышка – всем хорошо знакомое ощущение нехватки воздуха после пробежки, при занятиях в спортзале, т.е. при интенсивной физической нагрузке. Патологическая одышка при аллергическом воспалении в бронхах возникает в покое или при незначительной физической нагрузке, часто сопровождается ощущением затрудненного выдоха. Нередко такая одышка сопровождается свистами и хрипами при дыхании, которые слышны окружающим.
Приступы удушья
Приступ удушья – это мучительное, вызывающее страх состояние, при котором невозможность дышать проявляется в большей степени затруднением выдоха. Часто такой приступ удушья разрешается кашлем с отхождением белой пенистой мокроты. При приступе возникает желание принять сидячее положение с небольшим наклоном вперед, выпить горячей воды, что в ряде случаев приносит облегчение.
Кожный зуд, покраснения и высыпания на коже
Аллергия – частая, но не единственная причина зуда и кожных высыпаний. В то же время аллергические заболевания кожи всегда сопровождаются зудом. Кожные проявления аллергии могут выглядеть как ожог крапивой или расчесанные укусы насекомых (крапивница), отеки лица и других частей тела отеки (отеки Квинке), а также как красные шелушащиеся пятна различного размера (дерматит).
Высыпания при крапивнице обычно не располагаются на теле симметрично, каждый волдырь держится на коже не более суток, новые волдыри образуются в новых местах.
Излюбленное расположение очагов воспаления при аллергическом дерматите – локтевые и коленные сгибы, внутренняя поверхность рук от локтя до кистей. Такие очаги могут сохраняться годами, изменяя структуру кожи.
Ветряная оспа (ветрянка)
Ветрянка (ветряная оспа) — высокозаразное острое инфекционное заболевание, протекающее с характерной пузырьковой сыпью.
Чаще болеют дети, посещающие детский сад или школу — места с большим скоплением людей.
Заболевание вызывается одним из вирусов герпеса (герпесвирус 3-го типа). Ветряная оспа — очень заразное заболевание. Вирус передается от больного человека к здоровому воздушно-капельным путем (при разговоре, пребывании в одном небольшом помещении). С током воздуха ветрянка может распространяться на большие расстояния (до 20 м). Заражение также может произойти от больного опоясывающим лишаем (вызывается той же разновидностью вируса герпеса). Вирус малоустойчив во внешней среде, поэтому заключительную дезинфекцию после больного не проводят.
Больной ветрянкой становится заразным за два дня до появления высыпаний, и остается заразным в течение первых 5-7 дней после появления сыпи.
Инкубационный период ветрянки 7-21 день. В организм человека вирус попадает через слизистые оболочки носа, рта и глотки. Затем вирус разносится по организму лимфой и кровью, проникает в кожу и слизистые оболочки, где происходит его размножение. Мишенями для вируса являются клетки шиповидного слоя кожи и эпителий слизистых оболочек. После первичной инфекции вирус пожизненно пребывает в нейронах спинальных ганглиев, ганглиев лицевого и тройничного нервов. Как и все герпесвирусы, вирус ветряной оспы обладает способностью подавлять иммунную систему — что приводит к нарушению со стороны иммунного ответа по гуморальному и клеточному типам и нарушению факторов врожденной устойчивости к инфекциям.
Мишенями для вируса являются клетки шиповидного слоя кожи и эпителий слизистых оболочек. После первичной инфекции вирус пожизненно пребывает в нейронах спинальных ганглиев, ганглиев лицевого и тройничного нервов. Как и все герпесвирусы, вирус ветряной оспы обладает способностью подавлять иммунную систему — что приводит к нарушению со стороны иммунного ответа по гуморальному и клеточному типам и нарушению факторов врожденной устойчивости к инфекциям.
Иммунитет при ветряной оспе является нестерильным т.е. обусловливает невосприимчивость к новому заражению и не обеспечивает удаление вируса из организма. Вирус пожизненно пребывает в спинальных ганглиях, ядрах черепно-мозговых нервов, которые связаны с зонами кожи, наиболее пораженных при первичной инфекции. Повторная активация вируса происходит в условиях ослабленного иммунитета в виде опоясывающего герпеса.
Симптомы ветрянки у детей
Заболевание проявляет себя в первую очередь лихорадочным состоянием, резким повышением температуры тела до 39-40 градусов, головной болью. Самый яркий признак ветряной оспы – сыпь и зуд.
Сыпь в виде мелких, заполненных жидкостью пузырьков, может покрывать значительную часть тела и слизистых оболочек. Пузырьки довольно быстро лопаются и превращаются в маленькие язвочки, которые необходимо обрабатывать водным раствором зеленки или марганцовки, ацикловиром и другими мазями по назначению врача. Заживая, сыпь покрывается корочкой, которая постепенно отпадает, демонстрируя тем самым выздоровление. Обычно сыпь заживает бесследно, однако если ее расчесать – на коже после заживления могут остаться рубцы и шрамы.
У детей ветрянка протекает в более простой форме, нежели у взрослых, которые могут страдать в дальнейшем от осложнений.
Крайне редко ветряная оспа может протекать без высыпаний и пузырьков – в таком случае для уточнения диагноза необходима дополнительная консультация специалиста.
Лечение ветрянки
Обычно ветрянка проходит сама собой в течение недели или 10 дней.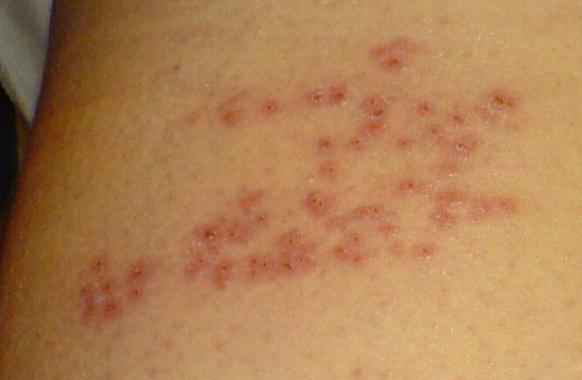 При этом температура может нормализоваться уже через два-три дня, хотя, в некоторых случаях, она сохраняется на протяжении всего периода болезни.
При этом температура может нормализоваться уже через два-три дня, хотя, в некоторых случаях, она сохраняется на протяжении всего периода болезни.
Лечение ветрянки носит симптоматический характер (т.е. лечатся проявления заболевания: высокая температура, сыпь на коже), поскольку медицина на данном этапе не знает ни способов предотвращения, ни средств лечения этого заболевания. Цель лечения — не допустить нагноения пузырьков. Для этого отлично подойдет зелёнка, можно использовать жидкость Кастеллани, водный раствор фукорцина или марганцовки и т.д. Спиртовые растворы дети переносят очень болезненно.
Купать ребенка при ветрянке нужно, чтобы предотвратить появление вторичной инфекции кожи. При этом нельзя пользоваться мочалкой и лучше не использовать мыло, добавляя в ванночку слабый раствор марганцовки. Создайте коже малыша максимально комфортные условия: не одевайте плотную и тесную одежду, используйте только хлопчатобумажное белье.
Если вашего ребенка беспокоит сильный зуд, скажите об этом врачу: он назначит противоаллергические средства.
При повышении температуры выше 38оС, ознобе, ребенку необходимо дать жаропонижающие средства (парацетомол, ибупрофен).
Заболевшего ветрянкой изолируют дома в течение девяти дней с начала болезни. В детских дошкольных учреждениях устанавливается карантин продолжительностью 21 день.
Осложнения ветрянки
Осложнения ветрянки встречаются редко и чаще всего связаны с неаккуратной обработкой высыпаний и их нагноением, что впоследствии приводит к образованию рубцов.
Крайне редко у ослабленных детей встречаются тяжелые формы ветрянки с поражением головного мозга, внутренних органов. Подобные формы болезни лечат в больницах, применяя специальные терапевтические методы.
Вакцина и прививка от ветрянки
Вакцина в достаточной степени предохраняет от ветрянки и ее осложнений. Ее рекомендуют проводить детям в возрасте 12 месяцев и старше, а также подросткам и взрослым, ранее не болевшим ветрянкой и не получивших вакцинацию.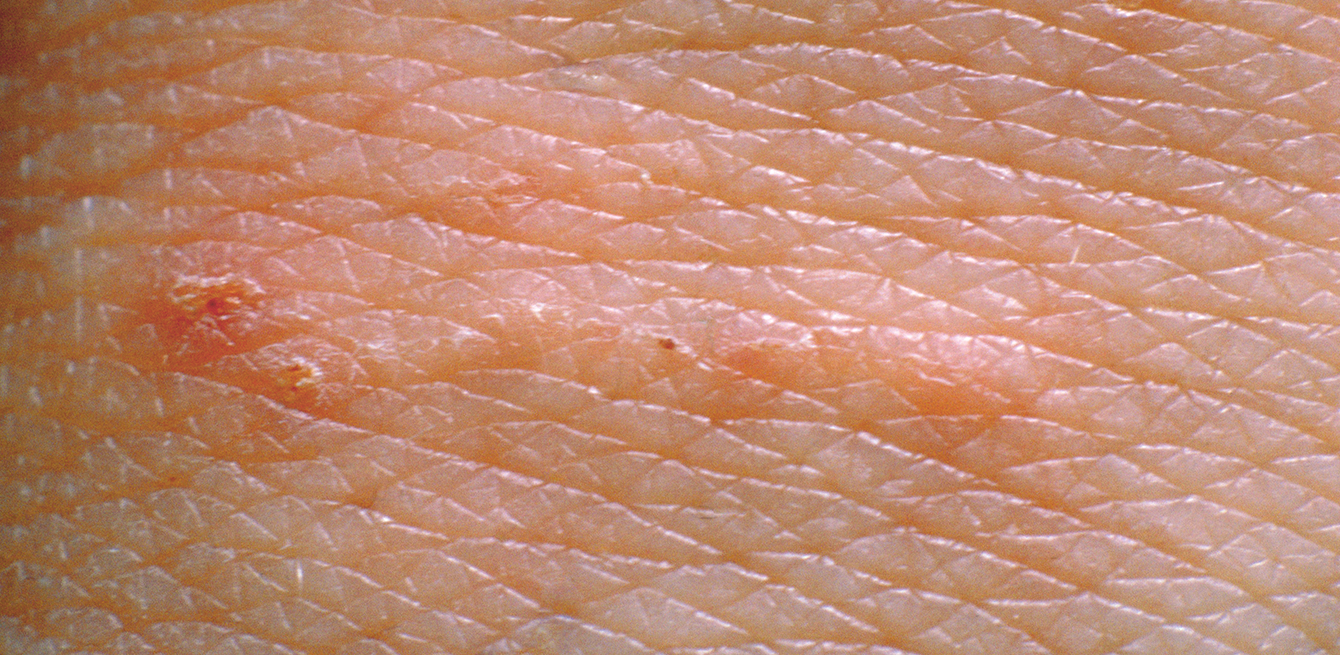 Вакцина защищает от заболевания на 10 и более лет. В редких случаях люди, получившие вакцинацию против ветрянки, могут заболеть ветрянкой, но заболевание будет протекать в легкой форме.
Вакцина защищает от заболевания на 10 и более лет. В редких случаях люди, получившие вакцинацию против ветрянки, могут заболеть ветрянкой, но заболевание будет протекать в легкой форме.
В настоящее время в США, Японии и некоторых других странах прививка от ветрянки является обязательной для приема ребенка в детское дошкольное учреждение. Но в России вакцинация детей от ветрянки еще не получила широкого распространения, и это остается выбором родителей.
Стоит отметить, что некоторым люди с ослабленной иммунной системой (в результате болезни или приема лекарств, влияющих на иммунитет) не стоит вакцинироваться, поскольку у них возможно развитие осложнений. Поэтому прежде чем получать вакцину против ветрянки пациенту с ослабленной иммунной системой, следует проконсультироваться с врачом.
Ветрянка у детей
Ветрянка или ветряная оспа на сегодняшний день остается одним из самых распространённых инфекционных заболеваний, поражающих детей в возрасте от шести месяцев до десяти лет.
Ветрянка или ветряная оспа на сегодняшний день остается одним из самых распространённых инфекционных заболеваний, поражающих детей в возрасте от шести месяцев до десяти лет. Ветрянкой болеют и взрослые, однако реже и тяжелее.
Как передается ветрянка?
В большом детском коллективе ветрянка может носить эпидемиологический характер и поочередно затрагивать каждого члена группы.
Известно, что заболевание провоцируется одним из вирусов герпеса и является крайне заразным, хотя в большинстве случаев и неопасным. Вирус достаточно быстро переходит воздушно-капельным путем от больного человека к здоровому. При этом человек, передающий заболевание, в этот момент может не испытывать симптомов болезни. Он может заражать окружающих за несколько дней до появления сыпи и повышения температуры. Так что иногда бывает очень сложно отследить заранее источник болезни и предотвратить ее передачу.
Ветрянка находится в инкубационном периоде от одной до трех недель, при этом симптомы могут появиться не ранее семи дней с момента заражения, но не позже 21 дня.
Человек перестает быть заразным спустя неделю или десять дней после первого проявления признаков ветрянки.
Симптомы ветрянки у детей
Симптомы ветрянки у всех детей и взрослых похожи. Заболевание начинается довольно резко с повышения температуры в основном до 38 градусов, но бывает и до 40 градусов, отмечается слабость, головная боли. Но главный симптом ветрянки – обильная сыпь, распространяющаяся на всей поверхности кожи и даже слизистых оболочках. Сыпь в виде маленьких пузырьков с жидкостью сопровождается сильным зудом, который дети очень плохо переносят.
Основная локализация сыпи – туловище, голова (лицо и волосистая часть), половые органы, рот.
Первые признаки ветряной оспы – покраснение кожи диаметром до одного сантиметра. На их месте спустя довольно короткое время появляются волдыри с прозрачной жидкостью, которые впоследствии трансформируются и приобретают вид подсохших корочек.
Течение болезни обычно волнообразно, поэтому высыпания могут появляться несколько раз.
Лечение ветрянки у детей
Лечение ветрянки у детей и взрослых направлено на преодоление неприятных симптомов. Само заболевание не лечится, а проходит постепенно и, как правило, бесследно. Осложнения у детей встречаются редко, куда более подвержены им взрослые люди.
Так как дети склонны к расчесыванию сыпи, основное лечение должно быть направлено на снятие зуда и недопущения нагноения язвочек и пузырьков. Для этого кожу обрабатывают слабым водным раствором зеленки или марганцовки, фукроцина или жидкостью Кастеллани.
Как лечить ветрянку у детей и что использовать для достижения оптимального результата – вопрос сугубо индивидуальный, который должен решаться родителями совместно с лечащим врачом.
Ветрянка у грудничков
Заболеть ветрянкой может любой ребенок в возрасте от шести месяцев. Как правило, течение болезни у грудного ребенка довольно сложное – младенцы плохо переносят симптомы ветрянки и нуждаются в тщательном уходе и постоянном внимании со стороны матери.
Ветрянка у новорожденных проявляется теми же симптомами, что и у детей более старшего возраста. Однако, в особо сложной форме ветрянка может нанести серьезный вред организму, повлияв на развитие внутренних органов. Лечение ветрянки у грудничков должно происходить под контролем специалиста.
Вакцина против ветрянки
Врачи рекомендуют делать детям в возрасте старше 12 месяцев прививку от ветряной оспы. Она эффективно защищает организм от этого заболевания на протяжении нескольких лет.
Стоит, однако, сказать, что ряд специалистов придерживается мнения о том, что ветрянкой стоит переболеть в детстве и получить иммунитет на всю жизнь, чем столкнуться с этим заболеванием в зрелом возрасте и пострадать от опасных
Ветрянка у взрослых
Ветрянка у взрослых развивается и протекает так же стремительно, как и у детей, но более тяжело и чаще дает осложнения.
Взрослые люди, не переболевшие в свое время ветрянкой в детстве, подвержены риску заболеть в возрасте, когда течение этой болезни и ее последствия могут быть очень серьезными.
Как передается ветрянка у взрослых?
Ветрянка, или ветряная оспа — заболевание, которое активно передается от больного человека здоровому воздушно-капельным путем. Защитить себя и свою семью от него довольно сложно, поскольку не всегда можно что называется «поймать» момент и понять, что общение с тем или иным человеком приведет к болезни.
Ветрянка у взрослых развивается и протекает так же стремительно, как и у детей, спустя 7-21 день инкубационного периода.
Человек остается заразным на протяжении примерно недели после первого проявления симптомов.
Симптомы ветрянки у взрослых
Симптомы ветрянки у взрослых идентичны симптомам этого заболевания у детей. Резко повышается температура, развивается лихорадочное состояние – слабость, головная боль, нарушение аппетита и сна. По всему телу появляется сначала интенсивное покраснение кожи, а потом сыпь, которая сопровождается сильным зудом. Сыпь может покрывать торс и спину, лицо и волосистую часть головы, слизистые оболочки полости рта и половых органов. Крайне редко ветрянка может протекать без обильной сыпи, однако процент таких случаев ничтожно мал.
Сыпь может покрывать торс и спину, лицо и волосистую часть головы, слизистые оболочки полости рта и половых органов. Крайне редко ветрянка может протекать без обильной сыпи, однако процент таких случаев ничтожно мал.
Проявление симптомов ветрянки у взрослых происходит волнообразно – сыпь и высокая температура появляются несколько раз в течение недели.
Сыпь обычно проходит бесследно – если ее не трогать и не расчесывать. В противном случае могут возникать очаги нагноения, а после их заживления – оставаться шрамы и рубцы.
Лечение ветрянки у взрослых
Ветрянка – болезнь, которая проходит обычно сама собой без специфического лечения. Однако симптомы этого заболевания требуют внимания. В основном, это касается зуда и сыпи, которую необходимо периодически обрабатывать слабым водным раствором марганцовки или зеленки, смазывать ацикловиром или другой мазью, назначенной лечащим врачом.
Осложнения при ветрянке у взрослых
Ветрянка опасна для взрослых, прежде всего, осложнениями – поражением внутренних органов, пневмонией. Опасна ветрянка и для беременных женщин – болезнь может поразить ребенка и привести к серьезным дородовым патологиям. Поэтому во взрослом возрасте лечение ветрянки должно производиться под контролем специалиста и только теми препаратами, которые он назначает.
Острицы
Острицы — один из наиболее распространенных кишечных гельминтов.
Острицы — это крошечные паразитические нематоды (2-14 мм), которые живут в кишечнике и откладывают яйца на коже вокруг заднего прохода.
Инфицирование острицами также известно как «энтеробиоз».
Заболевание чаще всего встречается у детей в возрасте от 5 до 10 лет.
Человек заражается при заглатывании яиц гельминта.
В кишечнике из яиц выходят личинки, которые паразитируют в нижних отделах тонкого, а в толстом кишечнике превращаются во взрослую особь.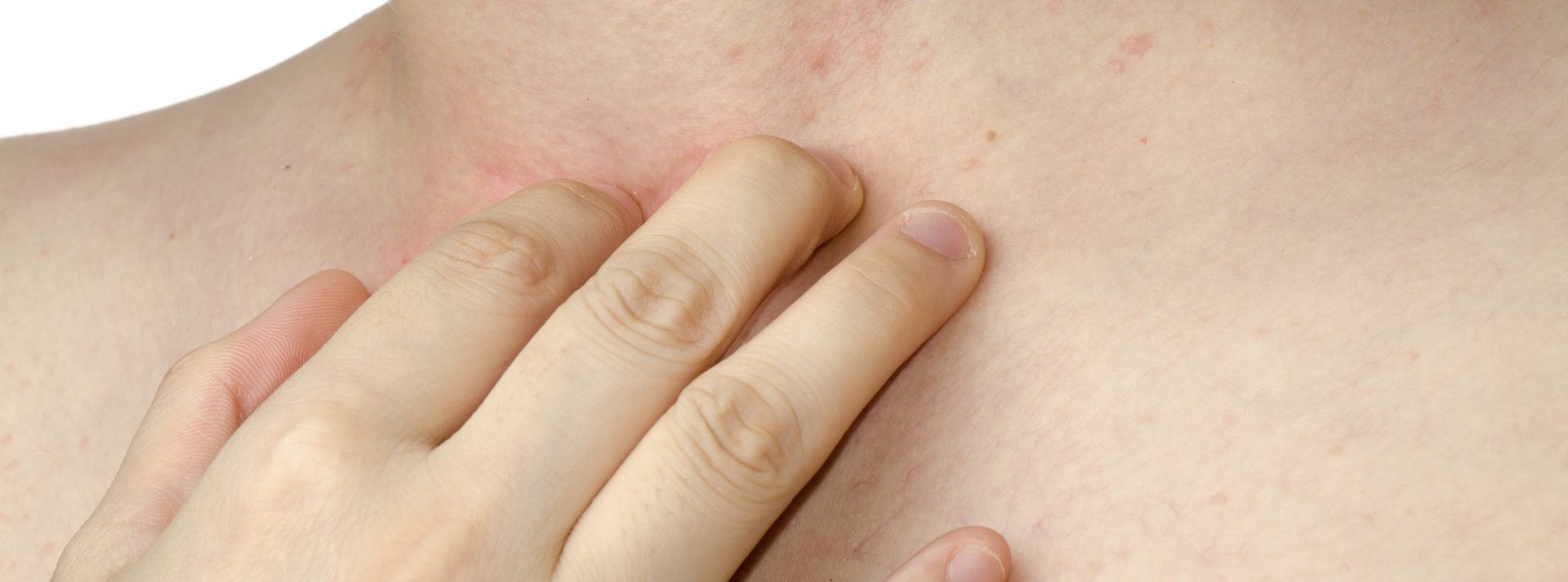
В ночное время зрелая самка выходит из заднего прохода и откладывает яйца на коже в складки кожи вокруг заднего прохода, промежности, ягодицах откладывает яйца (от 2 до 15 тыс.).
Через 4-5 часов яйца становятся «инвазионными» (заразными) для человека, т.к. за это время в яйцах созревают личинки.
Если зараженный человек касается предметов домашнего обихода, таких как постельное белье, одежда, сиденье унитаза или игрушки, яйца переносятся на эти предметы.
Яйца также могут переноситься с загрязненных пальцев непосредственно на продукты питания.
Хотя это и редкость, взрослые также могут вдыхать находящиеся в воздухе яйца при встряхивании загрязненного постельного белья, полотенец или одежды.
Возбудитель энтеробиоза устойчив к различным дезинфицирующим средствам. На игрушках, постельных принадлежностях, ковровых покрытиях и других предметах обихода возбудитель энтеробиоза сохраняет жизнеспособность до 21 дня, на объектах окружающей среды — в верхних слоях почвы игровых площадок, песка из песочниц — до 14 дней, в водопроводной и сточной водах — до 7 дней. Устойчивость яиц остриц во внешней среде увеличивается по мере их созревания. При температуре плюс 22-28°С и снижении влажности до 60% яйца остриц сохраняют жизнеспособность до 8 дней.
Кто подвержен риску заражения энтеробиозом?
Острицы поражают людей всех возрастов, энтеробиоз распространен повсеместно.
Наиболее восприимчивы к заражению:
- дети, посещающие организованные учреждения (особенно детские сады, лагеря)
- члены семьи или лица, ухаживающие за инфицированными
- люди, проживающие в общественных учреждениях, таких как общежития
- люди, не соблюдающие правила личной гигиены, а именно регулярное и тщательное мытье рук перед едой
- дети, которые имеют привычку сосать пальцы, грызть ногти
Можно ли заразиться острицами от домашних питомцев?
Нет, единственный источник инфекции – человек.
Симптомы энтеробиоза:
- Зуд, расчесы, сопровождающие выползание остриц на кожу
- Расчесывание кожных покровов провоцирует распространение яиц остриц и повторное самозаражение, вследствие которого заболевание может продолжаться длительное время. Яйца могут выжить в течение нескольких часов на руках, под ногтями.
- Аллергическая реакция, сыпь
- Раздражение, плаксивость, беспокойный сон
- Наличие остриц в кале
Некоторые люди с энтеробиозом могут не испытывать никаких симптомов.
Опасность энтеробиоза заключается в том, что острицы, паразитирующие в кишечнике человека, вырабатывают токсины – продукты жизнедеятельности, вызывающие интоксикацию организма. Острицы, паразитируя на слизистой, травмируют ее, что может привести к присоединению вторичной грибковой или бактериальной инфекции
Диагноз ставится на основании лабораторного исследования.
Лечение назначает врач.
Детей, инвазированных острицами, являющихся источниками распространения энтеробиоза, не допускают в дошкольные образовательные учреждения на период лечения и проведения контрольного лабораторного обследования.
Помимо выполнения рекомендаций врача необходимо провести профилактику распространения инфекции и риска повторного самозаражения.
Мытье рук с мылом и теплой водой после посещения туалета, смены подгузников и перед едой — самый эффективный способ предотвращения заражения острицами.
Родителям рекомендовано следить за тем, чтобы дети не грызли ногти.
Соблюдайте правила личной гигиены и меняйте ежедневно нательное белье.
Зараженные люди не должны совместно купаться с другими людьми.
Инфицированные должны избегать принятие ванн. Душ принимать необходимо каждое утро.
Профилактика энтеробиоза включает комплекс мероприятий:
- выявление больных (паразитоносителей) энтеробиозом
- лечение выявленных инвазированных лиц и профилактика лиц, находившихся в контакте с инвазированными
- мониторинг циркуляции возбудителя энтеробиоза в группах повышенного риска заражения
В очаге инфекции проводится дезинвазия:
- мебель и другие поверхности протирают специальными дезинфекционными-дезинвазионными средствами
- мягкие игрушки, мягкую мебель и ковры обрабатывают с помощью пылесоса с последующим обеззараживанием пыли. В процессе обработки рекомендовано убрать ковры и игрушки на 3 дня.
- Белье, постельное белье – подвергают кипячению
- Твердые игрушки – моют с моющими средствами.
14.01.2019
Симптомы рака кожи и методы его диагностики
Страшное слово «рак» знакомо даже людям, далеким от медицины. Принято считать, что этот термин — синоним скорой неотвратимой смерти, ведь на слуху у всех трагические истории из жизни знаменитостей или знакомых, которым был поставлен такой диагноз.Различные злокачественные новообразования кожи были диагностированы у Хью Джекмана (Люди Икс, Росомаха), Хлои Кардашьян (американская телевизионная персона, участница реалити-шоу «Семейство Кардашян), всем известный отец «Ералаша» продолжает борьбу за жизнь с метастазами меланомы – «Получилось, что из маленькой родинки выросла большая болезнь» – вздыхает Грачевский. От последствий развития опухоли кожи погибли: Боб Марли (ямайский музыкант, гитарист), победительница конкурса «Мисс Вселенная 2006» –российская модель Анна Литвинова. В 2012 году у Анны была диагностирована меланома, она уехала на лечениев Германию где умерла около года спустя, 22 января 2013 года, в 31-летнем возрасте.
Однако, рак можно победить, если выявить его на ранней стадии и обратиться за квалифицированной медицинской помощью. Потому поговорим об одном из самых распространенных онкологических заболеваний в России — злокачественных новообразованиях кожи, которыезанимают второе место по распространенности среди всех злокачественных новообразований у женщин (после рака молочной железы) и третье – у мужчин (после рака легких и рака предстательной железы).
Потому поговорим об одном из самых распространенных онкологических заболеваний в России — злокачественных новообразованиях кожи, которыезанимают второе место по распространенности среди всех злокачественных новообразований у женщин (после рака молочной железы) и третье – у мужчин (после рака легких и рака предстательной железы).
Ситуация в России остается тревожной: зачастую пациенты попросту игнорируют первые симптомы рака кожи и обращаются в больницу с запущенной стадией опухоли, когда гарантии выздоровления быть не может. Так при 4-ой стадии меланомы – наиболее злокачественного новообразования кожи, даже при условии правильного лечения, лишь половина из 10-ти пациентов живет дольше 5-ти лет. А ведь в отличие от рака внутренних органов, злокачественные опухоли кожи всегда на виду.
Причины рака кожи
Появление любого злокачественного новообразования — следствие сбоя в работе организма: в норме иммунная система уничтожает дефектные клетки до того, как они приступают к бесконтрольному делению. Если же по каким-то причинам защитные механизмы не срабатывают, опухоль увеличивается в размерах и становится неуязвимой для собственной защитной системы. В случае с раком кожи наиболее опасными факторами внешней среды, повышающим вероятность развития опухоли, являются ультрафиолетовое и ионизирующее облучение, а также воздействие агрессивных химических веществ.
Эксперты отмечают, что злокачественные новообразованиякожи, в частности меланома нередко провоцируются посещением солярия: мода на бронзовый загар привела к значительному увеличению частоты появления злокачественных новообразований (в США именно по этой причине ежегодно выявляется более 170 тысяч заболевших). «…Белокожая Аня всегда старалась следовать моде, она, как и многие сейчас, посещала солярии, любила ездить в экзотические страны, где много солнца» — вспоминает подруга Анны Литвиновой, Ксения Волкова.
Симптомы и признаки рака кожи
Любая разновидность злокачественных опухолей вначале проявляется локально — в месте поражения, а затем, при отсутствии лечения, сказывается на самочувствии больного в целом. В случае с раком кожи соотношение между местными и общими симптомами — в пользу местных: до поздних стадий заболевания окружающие могут не подозревать, что человек болен. Местные симптомы рака кожи заметны невооруженным глазом: это может быть ранка, которая не заживает на протяжении нескольких недель или месяцев, пятно, постепенно увеличивающееся в размерах, или родинка, которая изменила форму или цвет. В зависимости от вида опухоли рост новообразования бывает медленным или быстрым, но в любом случае изменение кожных покровов прогрессирует. В пораженной области часто наблюдается зуд, боль, кровотечение или шелушение, подобные жалобы должны насторожить не только больного, но и его родных — откладывать визит к врачу в таких случаях категорически не рекомендуется.
В случае с раком кожи соотношение между местными и общими симптомами — в пользу местных: до поздних стадий заболевания окружающие могут не подозревать, что человек болен. Местные симптомы рака кожи заметны невооруженным глазом: это может быть ранка, которая не заживает на протяжении нескольких недель или месяцев, пятно, постепенно увеличивающееся в размерах, или родинка, которая изменила форму или цвет. В зависимости от вида опухоли рост новообразования бывает медленным или быстрым, но в любом случае изменение кожных покровов прогрессирует. В пораженной области часто наблюдается зуд, боль, кровотечение или шелушение, подобные жалобы должны насторожить не только больного, но и его родных — откладывать визит к врачу в таких случаях категорически не рекомендуется.
Виды, стадии и прогноз
Злокачественные новообразования кожи включают сразу несколько онкологических заболеваний, имеющих разное происхождение, специфичные симптомы и прогноз. Такие опухоли, как базалиома, плоскоклеточный рак кожи и меланома диагностируются статистически чаще прочих, но встречаются и более редкие варианты. Достоверно установить диагноз способен только онколог-дерматолог.
Базалиома (базальноклеточный рак кожи) — самый распространенный вид рака кожи, который развивается из клеток эпидермиса. Вначале, опухоль выглядит как небольшой розовый узелок, под поверхностью которого видна сеть кровеносных сосудов. По мере роста,новообразование может изъязвляться и кровоточить, на поверхности появляется без видимых причин корка, которая может проходить, но затем появляется вновь. Чаще базалиома возникает на коже лица, реже — на других участках кожи. Обычно болезнь развивается медленно и не дает метастазов, поэтому прогноз для больных — благоприятный, а лечение включает только удаление опухоли.
Плоскоклеточный рак кожи может иметь несколько клинических вариантов, в одном случае он может быть представлен, также, как и базалиома – одиночным узлом с кровоточащей язвочкой или коркой на поверхности, длительно-незаживающей язвой или локальным кератозом, напоминающий «кожный рог». Плоскоклеточный рак нередко располагается на красной кайме губ, открытых участках кожи, подверженных воздействию ультрафиолета. Этот рак способен к инвазивному росту и метастазированию – т.е. проникает в глубокие слои кожи и с током крови переноситься по телу к другим органам и тканям.
Плоскоклеточный рак нередко располагается на красной кайме губ, открытых участках кожи, подверженных воздействию ультрафиолета. Этот рак способен к инвазивному росту и метастазированию – т.е. проникает в глубокие слои кожи и с током крови переноситься по телу к другим органам и тканям.
Меланома — опухоль, которая развивается из пигментированных клеток кожи – меланоцитов. Как правило, развивается на месте родинок, представляющих собой скопление пигмента или, появляется самостоятельно.
При прогрессировании меланома склонна к быстрому агрессивному росту и способна образовывать метастазы (отдаленные опухоли). Однако, до начала инвазивного роста обычно проходит несколько лет, пока меланома растет в пределах эпидермиса (самого верхнего слоя кожи) – «стадия горизонтального роста» и лечение, которое заключается в удалении опухоли, в этот момент практически полностью исключает риск формирования отдаленных метастазов и развитие грозных осложнений для жизни. Именно поэтому так важно следить за внешним видом родинок: если одна из них изменила форму, цвет или выглядит припухшей, стала чесаться или кровоточить, необходимо срочно обратиться к врачу.
Напротив, в старшей возрастной группе чаще формируется нодулярная или узловая меланома, которая практически не имеет стадии внутриэпидермального роста и быстро становиться инвазивной, поэтому очень важно также следить за появлением новых темных узловых новообразований на коже наших пожилых близких и родственников.
Людей, у которых диагностирован рак, всегда интересует прогноз течения заболевания. «Доктор, сколько я проживу?» — популярный вопрос в практике онкологов. Если речь идет о раке кожи, то перспективы выздоровления в большинстве случаев хорошие, потому как самая распространенная опухоль — базалиома —не дает метастазов, и для ее устранения достаточно небольшого хирургического вмешательства. Ключевым параметром в онкологии является показатель выживаемости. Он говорит о том, например, какое число больных с данной стадией рака смогло прожить более 5-ти лет после выявления опухоли. Так, при базалиоме показатель выживаемости приближается к 100% вне зависимости от размеров новообразования. А при меланоме 2 стадии через 5-летний рубеж даже при условии грамотного лечения перешагивает только 50% пациентов.
Так, при базалиоме показатель выживаемости приближается к 100% вне зависимости от размеров новообразования. А при меланоме 2 стадии через 5-летний рубеж даже при условии грамотного лечения перешагивает только 50% пациентов.
Методы диагностики
Врачи, специализирующиеся на диагностике рака кожи, имеют впечатляющий арсенал диагностических методик, позволяющих подтвердить или опровергнуть диагноз, а также классифицировать опухоль. Осмотр — самый очевидный и простой способ заподозрить наличие новообразования. Если вы волнуетесь, что у вас развивается рак кожи, — покажите необычный участок тела доктору. Он сравнит подозрительную родинку или язвочку с другими скоплениями пигментных клеток. Если будут основания для беспокойства, врач назначит дополнительные методы диагностики. Для более точной диагностики онкологи-дерматологи используют дерматоскоп — прибор, позволяющий разглядеть структуру новообразования детально, в поляризованном свете. Для окончательного подтверждения природы опухоли используется биопсия, при которой врач забирает небольшой участок ткани пациента из пораженной области, чтобы в условиях лаборатории изучить его под микроскопом. Ультразвук и томография необходимы, чтобы выявить возможные метастазы
Врачи иногда говорят, что при выявлении рака важно не дать диагнозу «парализовать сознание». Информированность о современных диагностических и лечебных возможностях и сотрудничество с врачами помогут победить коварную болезнь!
Как часто нужно показываться врачу, чтобы своевременно выявить заболевание?
Периодичность осмотров составляет 6-12 месяцев.
Как пройти осмотр в Центре им. В.П. Аваева?
В нашем Центре приём пациентов ведёт онколог-дерматолог, кандидат медицинских наук Дубенский Владислав Валерьевич
Запись по телефону: (4822) 633-123.
записаться на прием к онкологу-дерматологу
покрытых коркой чесотки на коже головы, имитирующей себорейный дерматит | Клинические инфекционные болезни
(См.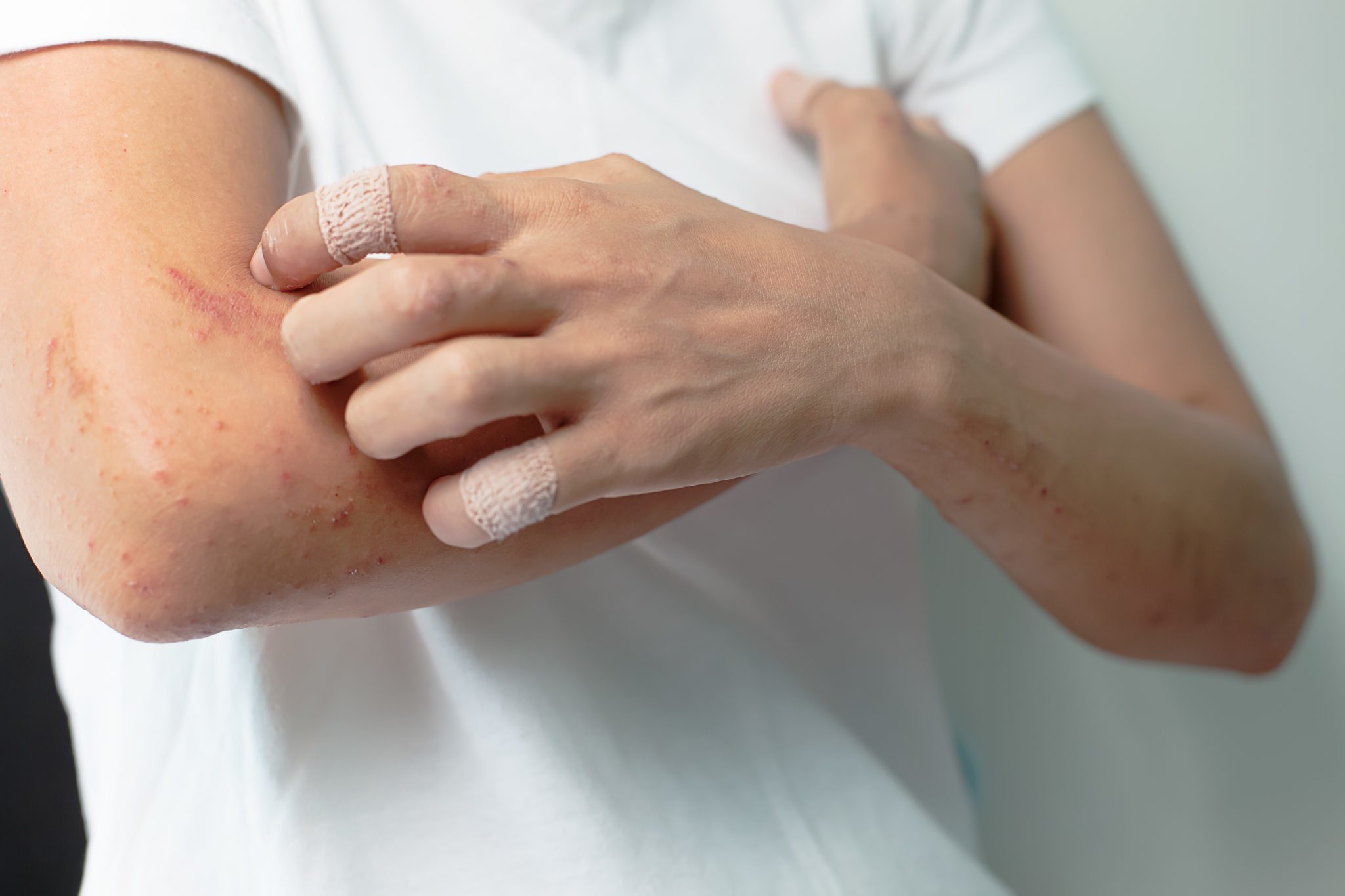 Страницу 844 для фото-викторины.)
Страницу 844 для фото-викторины.)
Диагноз: покрытая коркой чесотка
85-летняя женщина обратилась в дерматологическую клинику для удаления чешуек на коже черепа в течение нескольких недель. Клиническая картина представлена на рис. 1. Соскоб с кожи показал наличие нескольких чесоточных клещей при микроскопическом исследовании (рис. 2). Диагностирована корковая чесотка. Прописали крем кротамитион и 1% гексахорид γ-бензола.Через 2 недели гиперкератотические бляшки рассосались.
Рис. 1.
Эритема с гиперкератотическими чешуйками над левой височной областью и ухом.
Рисунок 1.
Эритема с гиперкератотическими чешуйками над левой височной областью и ухом.
Рисунок 2.
Соскоб кожи показал 3 чесоточных клеща (стрелки) под микроскопом (× 100).
Рис. 2.
Соскоб кожи показал 3 чесоточных клеща (стрелки) под микроскопом (× 100).
Корковая чесотка, впервые описанная Дэниелсоном и Боком в 1848 году [1], считается неадекватной реакцией хозяина на клеща Sarcoptes scabei , что приводит к гиперинфестации тысяч клещей. Это состояние обычно возникает у людей с основными иммунодепрессивными заболеваниями, включая инфекцию вируса иммунодефицита человека, инфекцию лимфотропного вируса 1 человеческих Т-клеток и лейкоз, но также наблюдалось у здоровых пациентов [2]. Клинически корковая чесотка представляет собой псориазиформный дерматит с акральным распространением и эритематозными чешуйчатыми высыпаниями на лице, шее, волосистой части головы и туловище.Покрытая коркой чесотка очень заразна и вызывает вспышки среди членов семьи инфицированного пациента и среди пациентов в больничных палатах, когда принимаются неадекватные профилактические меры. Однако бляшки при чесотке с коркой иногда могут быть ошибочно диагностированы как псориаз, экзема, болезнь Дарье, контактный дерматит, ихтиоз или побочная реакция на лекарственные препараты. Когда поражение проявляется на коже черепа, это может имитировать себорейный дерматит [3]. Из-за большого количества чесоточных клещей, присутствующих в покрытой коркой чесотке, провести диагностику соскабливанием кожи проще, чем при классической чесотке.Практикующие должны помнить об этом диагнозе, особенно в случае пациентов из группы высокого риска. Лечение было похоже на лечение классической чесотки, но удаление корки и чешуек необходимо для адекватного проникновения чесотки.
Из-за большого количества чесоточных клещей, присутствующих в покрытой коркой чесотке, провести диагностику соскабливанием кожи проще, чем при классической чесотке.Практикующие должны помнить об этом диагнозе, особенно в случае пациентов из группы высокого риска. Лечение было похоже на лечение классической чесотки, но удаление корки и чешуек необходимо для адекватного проникновения чесотки.
Банкноты
Подтверждение.
Мы хотели бы поблагодарить доктора Meng-Yun Hsieh из больницы Национального Тайваньского университета за ее предложения.
Возможный конфликт интересов.
Все авторы: о конфликтах не сообщалось.
Все авторы заполнили форму ICMJE для раскрытия информации о потенциальных конфликтах интересов. Выявлены конфликты, которые редакция считает относящимися к содержанию рукописи.
Список литературы
1.,.Норвежская чесотка
,Arch Derm Syphilol
,1941
, vol.43
(стр.678
—81
) 2.,.Чесотка
,Ланцет
,2006
, т.367
(стр.1767
—74
) 3 ..Чесотка
,N Engl J Med
,2006
, vol.354
(стр.1718
—27
)© Автор, 2012 г. Опубликовано издательством Oxford University Press от имени Общества инфекционистов Америки. Все права защищены. Для получения разрешений обращайтесь по электронной почте: [email protected].
Чесотка — обзор | Темы ScienceDirect
Обсуждение
Чесотку следует подозревать у любого пациента с зудом.
Чесотка была бичом людей на протяжении тысячелетий. Заболевание вызвано клещом Sarcoptes scabiei , var. человек . Взрослый особь практически не виден невооруженным глазом. Организм — облигатный паразит, которому для выживания требуется соответствующий хозяин. Клещи питаются растворенными человеческими тканями, но не кровью. Взрослая самка клеща имеет форму черепахи и имеет размер от 0,3 до 0,4 мм. Мужской клещ примерно в два раза меньше женского.Хотя клещи не умеют летать и прыгать, они могут ползать по теплой коже со скоростью 2,5 см / мин. После спаривания на поверхности кожи беременная самка клеща растворяет роговой слой с протеолитическими выделениями, а затем зарывается в кожу головой вперед. Яйца откладывают от 2 до 3 в день. И мужские, и женские клещи живут около 1 месяца. Молодые клещи развиваются быстро, покидая норы, попадая в волосяные фолликулы и кожные складки, в которых можно спрятаться и кормиться. Созревают в течение 10-14 дней, после чего происходит спаривание, начиная новый цикл.Клещи могут жить только до 3 дней вне среды тела хозяина.
Клещи питаются растворенными человеческими тканями, но не кровью. Взрослая самка клеща имеет форму черепахи и имеет размер от 0,3 до 0,4 мм. Мужской клещ примерно в два раза меньше женского.Хотя клещи не умеют летать и прыгать, они могут ползать по теплой коже со скоростью 2,5 см / мин. После спаривания на поверхности кожи беременная самка клеща растворяет роговой слой с протеолитическими выделениями, а затем зарывается в кожу головой вперед. Яйца откладывают от 2 до 3 в день. И мужские, и женские клещи живут около 1 месяца. Молодые клещи развиваются быстро, покидая норы, попадая в волосяные фолликулы и кожные складки, в которых можно спрятаться и кормиться. Созревают в течение 10-14 дней, после чего происходит спаривание, начиная новый цикл.Клещи могут жить только до 3 дней вне среды тела хозяина.
Реакция гиперчувствительности замедленного типа на клещей, их яйца, слюну и сцибалу (пакеты с фекалиями) происходит примерно в течение 2–6 недель после заражения. Эта воспалительная реакция является причиной сильного зуда (отличительного признака этого заболевания). Хотя чесоточные поражения выше шеи у детей и взрослых встречаются редко, у младенцев может поражаться лицо (рис. 177-7). Чесотка у младенца обычно означает, что источником инфекции является тесный контакт со взрослым.
Отличительная высококонтагиозная форма чесотки, известная как «Норвежская чесотка», или «покрытая коркой или кератотическая чесотка», имеет склонность к людям с ослабленным иммунитетом, пожилым людям, ослабленным или умственно отсталым. Пациент заражается тысячами или миллионами клещей, в отличие от обычного случая чесотки, когда в среднем инфицированный взрослый человек имеет от 10 до 15 живых взрослых клещей женского пола на его или ее теле в любой момент времени. Кожные проявления кератотической чесотки намного тяжелее, но последняя обычно не вызывает сильного зуда.
Чесотка передается в основном при тесном личном контакте, но может передаваться через одежду, белье или полотенца.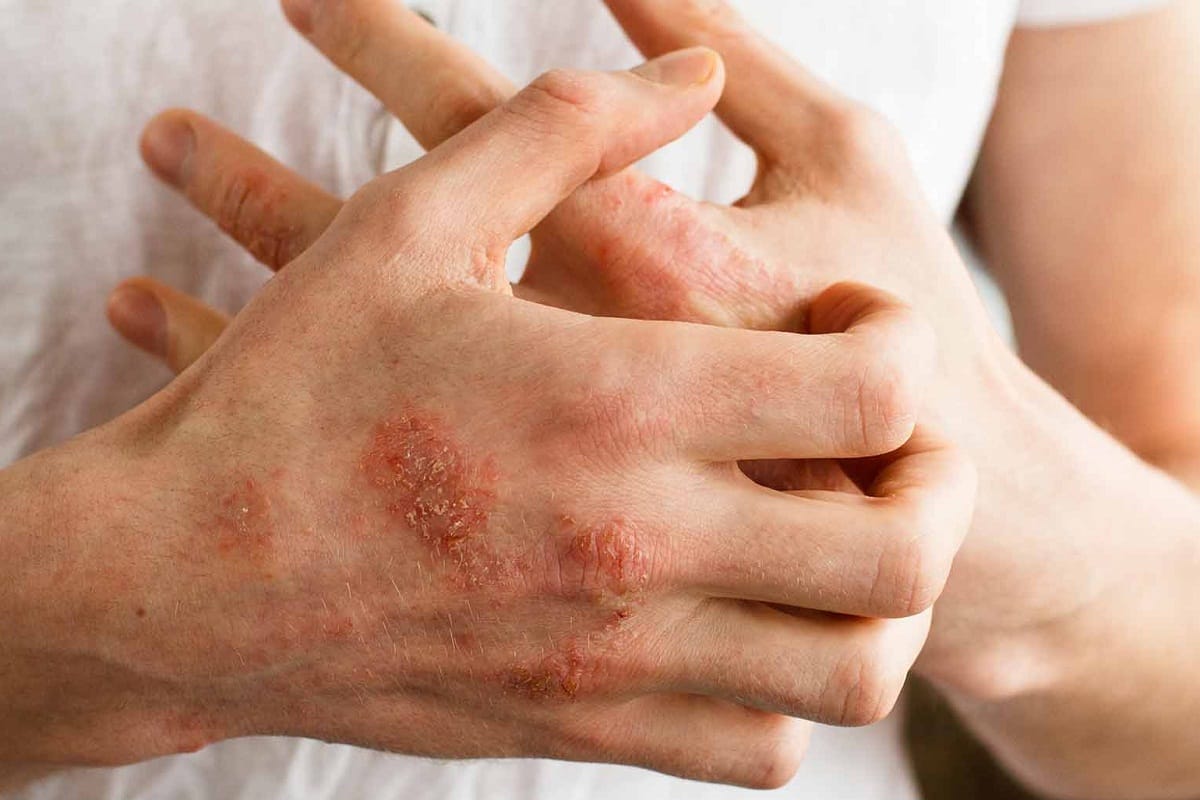
Менее чем в 25% случаев наблюдаются характерные серпигинозные следы от 2 до 3 мм. Другой метод выявления чесотки, кроме соскобов кожи, — это видеодерматоскопия. Это неинвазивная визуализация кожи in vivo при увеличении до 600 × для обнаружения признаков заражения (клещей, яиц и фекалий).
Семьи могут заразиться чесоткой собак, когда в дом приносят щенка.Распространение поражений у людей, инфицированных собачьей чесоткой, заметно отличается от такового у людей. Ребенок, который обнимает зараженного домашнего питомца, будет сильнее всего соприкасаться с его хоботом и руками, и поэтому при таком распределении наблюдается большинство высыпаний. Чесотка у собак проявляется в течение 24–96 часов. Обычно это самоограничение у людей, потому что клещи не могут завершить свой жизненный цикл и, следовательно, не выживают более нескольких дней на чужом хозяине. Для тех пациентов, которые не хотят ждать, пока эта форма чесотки исчезнет сама по себе, предпочтительным методом лечения является 5% перметрин, применяемый местно.Для лечения питомца рекомендуется помощь ветеринара.
Чесотка: применение нового инструмента «Идентифицировать-изолировать-информировать» для обнаружения и лечения
| Автор | Принадлежность |
|---|---|
| Табита А. Ченг, Мэриленд | Калифорнийский университет, Сан-Диего, Отделение неотложной медицины, Ла-Хойя, Калифорния |
| Bandr Mzahim, MD | Медицинский городок короля Фахда, Саудовская Аравия |
| Кристи Л.Кениг, Мэриленд | Калифорнийский университет, Ирвин, отделение неотложной медицины, Оранж, Калифорния; Округ Сан-Диего, Агентство здравоохранения и социальных служб, Скорая медицинская помощь, Сан-Диего, Калифорния |
| Abdulrahman Alsugair, MD | Медицинский городок короля Фахда, Саудовская Аравия |
| Abdussalam Al-Wabel, MD | Медицинский городок короля Фахда, Саудовская Аравия |
| Bandar Saad Almutairi, MD | Управление государственной безопасности, консультант по чрезвычайным ситуациям, Саудовская Аравия |
| Эшмави Майса, Мэриленд | Медицинский городок короля Фахда, Саудовская Аравия |
Кристофер А.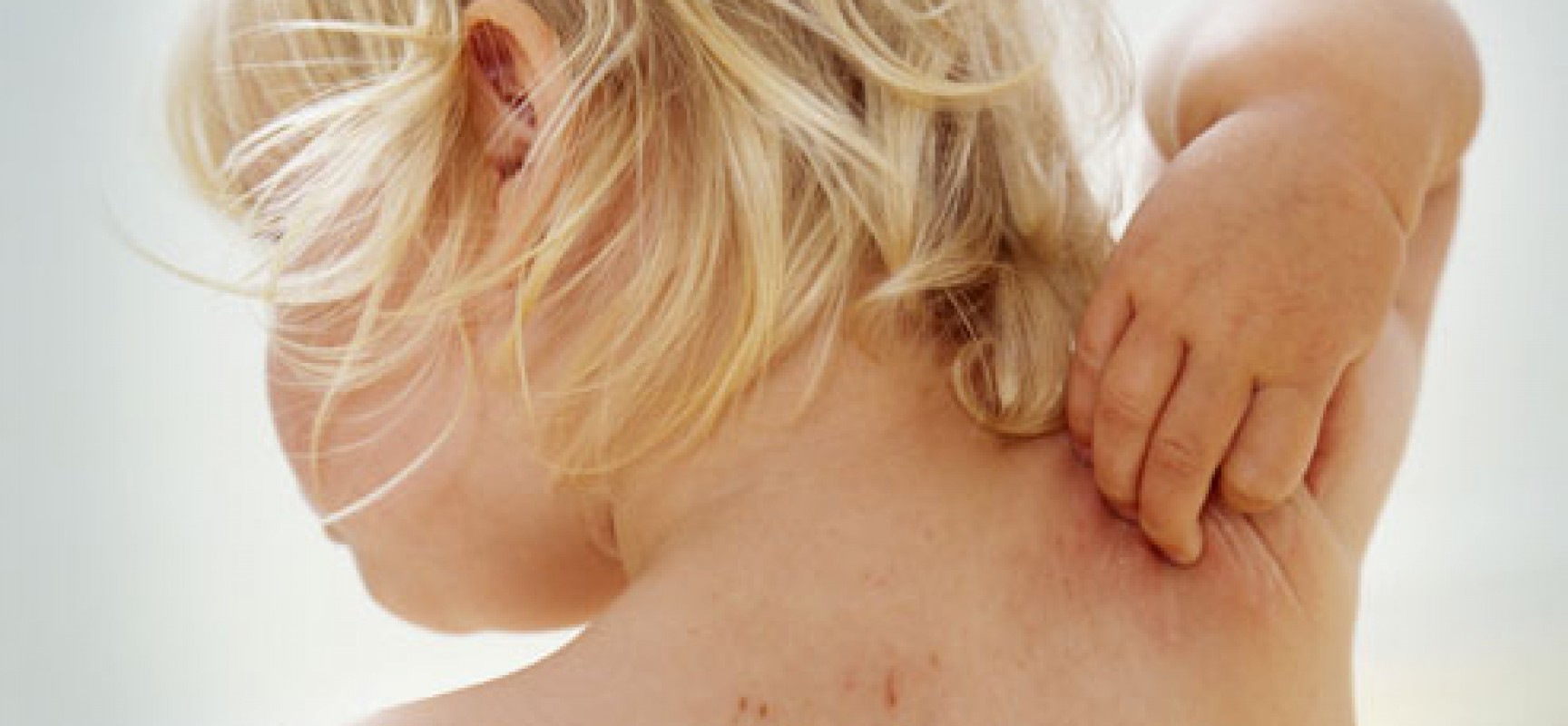 Кан, Мэриленд, MPH Кан, Мэриленд, MPH | Калифорнийский университет, Сан-Диего, Отделение неотложной медицины, Ла-Хойя, Калифорния |
Введение
Клиническая картина
Факторы риска
Диагностика
Осложнения и особые группы населения
Передача и средства индивидуальной защиты
Дифференциальный диагноз
Лечение
Профилактика
Расположение
Идентифицировать-изолировать-проинформировать (3i)
Заключение
РЕФЕРАТ
Чесотка — очень заразное, глобально распространенное паразитарное поражение кожи, вызываемое Sarcoptes scabiei var.hominis, также известный как чесоточный клещ. Вспышки были не только в развивающихся, но и в развитых странах среди беженцев и лиц, ищущих убежища. Зараженные чесоточным клещом пациенты с симптомами, а также бессимптомные носители быстро распространяют болезнь через прямой контакт кожи с кожей. Обычно симптомы чесотки характеризуются эритематозной папулезной зудящей сыпью, связанной с норками. Лечение чесотки включает использование местных или системных чесоточных средств и лечение вторичных бактериальных инфекций, если таковые имеются.Принимая во внимание распространенность и заразность чесотки, необходимы меры по предотвращению ее распространения. Благодаря применению нового инструмента «Идентифицировать-изолировать-информировать» (3I) поставщики неотложной медицинской помощи могут легко идентифицировать факторы риска заражения и важные симптомы заболевания, тем самым ограничивая его распространение с помощью своевременной терапии чесотками; изолировать пациента до окончания лечения; и, при необходимости, проинформировать местные органы здравоохранения и больничные службы профилактики инфекций. В конечном счете, эти три действия могут помочь общественному здравоохранению в борьбе с распространением чесотки, обеспечивая тем самым защиту населения от этого очень заразного заражения кожи.
ВВЕДЕНИЕ
Человеческая чесотка — очень заразное, глобально распространенное паразитарное поражение кожи, вызываемое Sarcoptes scabiei var . hominis , также известный как чесоточный клещ. Этот паразит был идентифицирован в 1687 году Бономо и Честони с помощью светового микроскопа; тем не менее, есть доказательства чесотки еще в 1200 году до нашей эры. 1 Наиболее частые симптомы чесотки, зуда и кожной сыпи вызываются реакцией гиперчувствительности к белкам и фекалиям паразита примерно через четыре-шесть недель после заражения.Сильный зуд, особенно в ночное время, — самый ранний и наиболее частый симптом чесотки. Также часто встречается эритематозная папулезная зудящая сыпь с углублениями на руках, запястьях, туловище и ступнях. 1
hominis , также известный как чесоточный клещ. Этот паразит был идентифицирован в 1687 году Бономо и Честони с помощью светового микроскопа; тем не менее, есть доказательства чесотки еще в 1200 году до нашей эры. 1 Наиболее частые симптомы чесотки, зуда и кожной сыпи вызываются реакцией гиперчувствительности к белкам и фекалиям паразита примерно через четыре-шесть недель после заражения.Сильный зуд, особенно в ночное время, — самый ранний и наиболее частый симптом чесотки. Также часто встречается эритематозная папулезная зудящая сыпь с углублениями на руках, запястьях, туловище и ступнях. 1
Чесотка продолжает оставаться распространенным дерматологическим заболеванием во всем мире. Систематический обзор оценил распространенность чесотки в различных странах от 0,2% до 71%. 2 В Великобритании оценка распространенности чесотки в базе данных общей практики составила 2.2 и 2,8 на 1000 у мужчин и женщин соответственно. 3 Исследования из Греции и Испании, проведенные в дерматологических клиниках, показали, что чесотка встречается примерно в 4% посещений, особенно среди иммигрантов и пациентов с низким социально-экономическим статусом. 4, 5 В развивающихся странах распространенность может быть намного выше, 6- 9 и достигая 87% в одном исследовании в тайских детских домах. 10 Хотя распространенность чесотки в развитых странах низкая, перед органами здравоохранения стоит задача выявлять и лечить людей с чесоткой в кратчайшие сроки, чтобы избежать передачи инфекции среди ближайших групп населения, например среди растущего числа просителей убежища и беженцев. 11, 12
Чесотка остается риском для здоровья населения, и очень важно, чтобы поставщики медицинских услуг выявляли потенциальные случаи заболевания. Возможны как недостаточный, так и избыточный диагноз, и каждый из них проблематичен. В то время как отсутствие диагноза может привести как к постоянному дискомфорту отдельного пациента, так и к быстрому распространению среди населения, чрезмерный диагноз может привести к неадекватному индивидуальному лечению пациента и может создать нагрузку на системы здравоохранения с ограниченными ресурсами.
Отделения неотложной помощи (ED) могут встретиться с этими пациентами и лечить их в качестве первого контактного лица.После обзора болезни и важной информации, относящейся к передаче и лечению, эта статья адаптирует инструмент 3I (Identify-Isolate-Inform) для помощи поставщикам медицинских услуг в выявлении и лечении потенциальных случаев чесотки, поступающих в ED (Рисунок 1). . Инструмент 3I изначально был разработан для лечения болезни, вызванной вирусом Эбола, а затем модифицирован для использования при кори, ближневосточном респираторном синдроме (MERS), паротите, вирусе Зика, гепатите A, коклюше и нКоВ 2019 (COVID-19). 13- 20
Рисунок 1
Инструмент «Определить, изолировать, проинформировать» (3I) для лечения чесотки.
КЛИНИЧЕСКАЯ ПРЕЗЕНТАЦИЯ
Признаки и симптомы чесотки различаются в зависимости от времени, прошедшего с момента заражения, степени заражения, иммунной компетентности хозяина и сосуществования других кожных патологий. Когда люди впервые заражаются чесоткой, они обычно не проявляют никаких симптомов в течение 4–6 недель. Обычно первым симптомом является сильная ночная зудящая сыпь. Сыпь обычно характеризуется как эритематозная с папулами и связанными с ними норками. Норы описываются как тонкие серые или коричневые линии длиной примерно 5 мм.Наличие нор — это классический признак чесотки, но редко визуализируется из-за раздражения кожи или наличия вторичных инфекций. У взрослых и детей старшего возраста сыпь чаще всего встречается в ладонной части запястий, межпальцевых перепонках, околопупочной области, передних подмышечных складках, ягодицах и гениталиях. 21 У младенцев и тех, кто живет в тропических регионах, сыпь может быть генерализованной, а также затрагивать кожу головы, шею, лицо, ладони и подошвы. 22
ФАКТОРЫ РИСКА
К группам повышенного риска чесотки относятся дети, пожилые люди, люди с ослабленным иммунитетом и люди, живущие в условиях массового скопления людей, включая лагеря беженцев.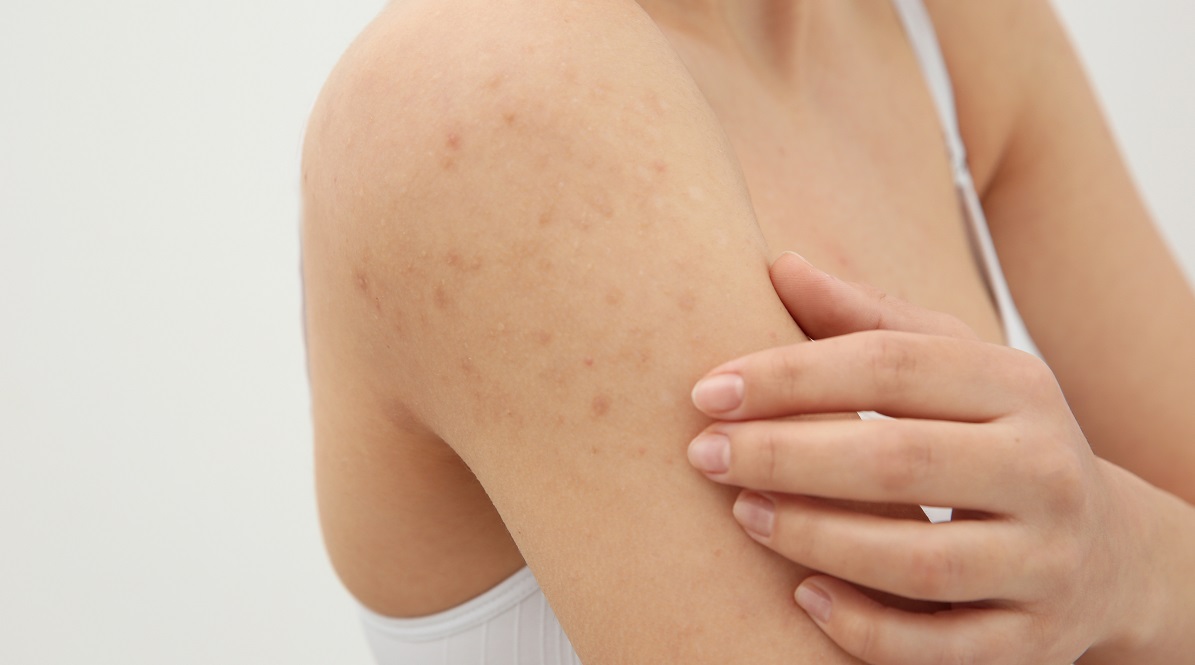 Чесотка встречается во всем мире, и риск заражения присутствует независимо от пола, расы или социально-экономического статуса; однако более высокая распространенность чесотки связана с тропическим и субтропическим климатом, странами с ограниченными ресурсами и районами с вооруженными конфликтами, бездомностью, скоплением людей и совместным использованием одежды, кроватей, одеял или подушек. 2, 23- 25
Чесотка встречается во всем мире, и риск заражения присутствует независимо от пола, расы или социально-экономического статуса; однако более высокая распространенность чесотки связана с тропическим и субтропическим климатом, странами с ограниченными ресурсами и районами с вооруженными конфликтами, бездомностью, скоплением людей и совместным использованием одежды, кроватей, одеял или подушек. 2, 23- 25
ДИАГНОСТИКА
Предположительный диагноз чесотки может быть поставлен на основании предполагаемых клинических признаков, таких как ночной зуд, контакты с чесоткой в анамнезе и / или типичный внешний вид и распространение кожных поражений с наличием нор.Однако постановка окончательного диагноза зависит от идентификации клещей, яиц или фекалий с помощью световой микроскопии. Поражения следует соскрести скальпелем. С помощью скальпеля папулу нужно соскоблить несколько раз, чтобы удалить верхнюю часть (видео-пример: техника соскабливания кожи при чесотке). Добавление нескольких капель минерального масла на кожу перед соскабливанием может помочь соскабливанию материала прилипнуть к лезвию. Большинство больничных патологоанатомических лабораторий принимают соскоб для микроскопического исследования.Здесь для справки представлены протоколы патологии для методов соскоба кожи при чесотке в двух университетских больницах: Университете Айовы и Университете Мичигана. Здесь показан характерный микроскопический вид. Однако даже при идеальной технике неспособность найти клещей, яйца или фекалии является обычным явлением и не исключает болезнь. 26, 27 Чувствительность этого подхода составляет от 40% до 90%, а специфичность достигает 100%. 26
Капсула для исследования здоровья населения
Что мы уже знаем об этой проблеме?
Чесотка — это очень заразное паразитарное поражение кожи, вспышки которого наблюдаются в развитых странах, а также среди групп риска в развивающихся странах.
Какой был вопрос исследования?
Исследователи модифицировали инструмент «Определить, изолировать, проинформировать» (3I) для использования при выявлении и лечении чесотки.
Каков был главный вывод исследования?
Новый инструмент Scabies 3I Tool создан для применения в режиме реального времени у пациентов отделения неотложной помощи (ED).
Как это улучшает здоровье населения?
Инструмент Scabies 3I Tool помогает поставщикам неотложной помощи, которые играют важную роль в выявлении и эффективном лечении чесотки, чтобы избежать распространения заражения.
В качестве альтернативы можно использовать тест чернил норы. В этом методе чернила впитываются норками и будут видны в виде волнистых линий (рис. 2). 24, 25 Для этого метода требуется моющийся маркер с темным фломастером или перьевая ручка поверх пораженного участка и тампон со спиртом для очистки поверхности от чернил. Любые оставшиеся темные чернила под кожей указывают на наличие нор чесотки (рис. 2). Чувствительность и специфичность теста с чернилами в норе невозможно рассчитать на основе французского дерматологического исследования. 26 Тем не менее, для любого случая, связанного с чесоткой в отделении неотложной помощи, это простой тест, который может помочь диагностировать чесотку.
Рисунок 2
Тест чернил при чесотке 50
Заменой теста чернил норы является тест флуоресценции тетрациклина, в котором тетрациклин используется вместо чернил. 28, 29 Этот метод позволяет бесцветную идентификацию нор. Как и чернила, раствор тетрациклина для местного применения наносится на пораженный участок и протирается спиртом, чтобы удалить излишки раствора с поверхности.Затем лампа Вуда используется для визуализации тетрациклина, просочившегося в норы. 28
Другие методы диагностики чесотки, которые вряд ли будут использоваться в отделении неотложной помощи, включают видеодерматоскопию, полимеразную цепную реакцию (ПЦР) и иммуноферментный анализ (ИФА) и тестирование на антитела IgE.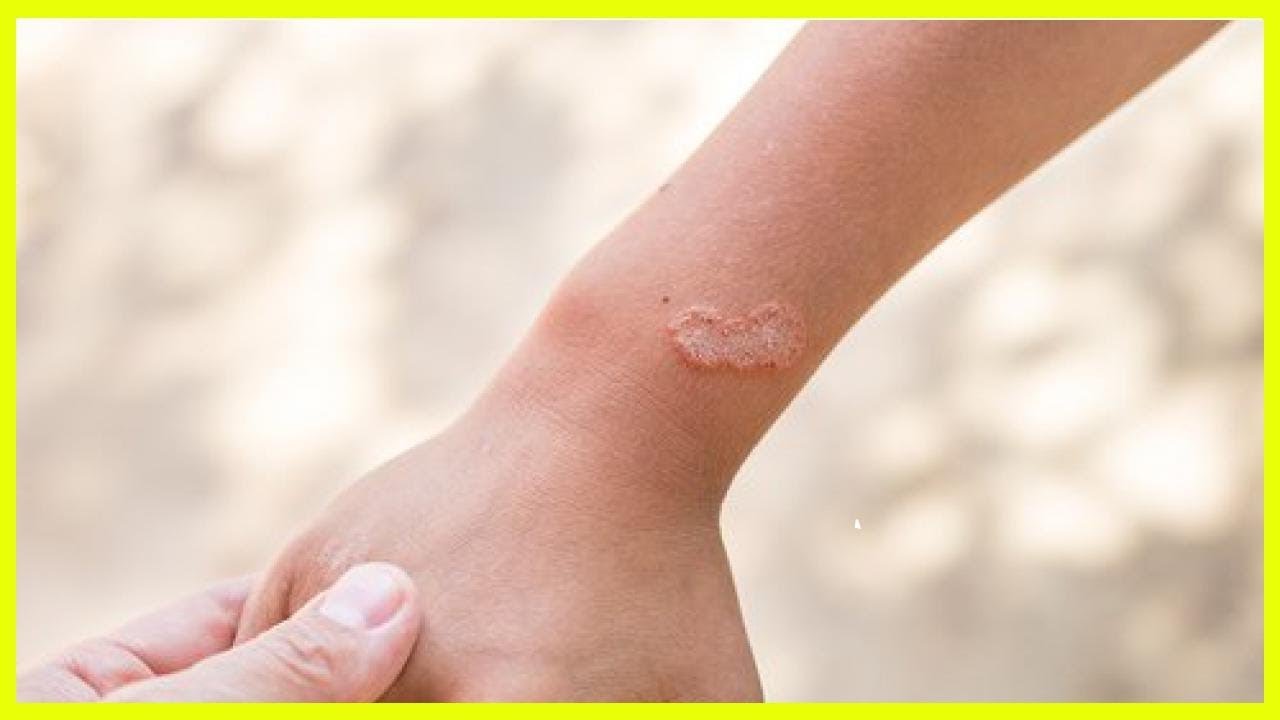 Видеодерматоскопия особенно полезна в случаях атипичного распространения или появления высыпаний. 30 Серологические тесты появляются как для диагностики, так и для мониторинга эффективности лечения.Одно исследование показало, что тесты ПЦР и ИФА в реальном времени полезны для мониторинга эффективности лечения. 31 В другом исследовании сообщалось о 100% чувствительности и 93% специфичности с использованием антител IgE против Sarcoptes scabiei . 32
Видеодерматоскопия особенно полезна в случаях атипичного распространения или появления высыпаний. 30 Серологические тесты появляются как для диагностики, так и для мониторинга эффективности лечения.Одно исследование показало, что тесты ПЦР и ИФА в реальном времени полезны для мониторинга эффективности лечения. 31 В другом исследовании сообщалось о 100% чувствительности и 93% специфичности с использованием антител IgE против Sarcoptes scabiei . 32
ОСЛОЖНЕНИЯ И ОСОБЫЕ НАСЕЛЕНИЯ
Вторичные бактериальные инфекции могут развиваться у людей, инфицированных чесоткой, особенно потому, что сыпь, как правило, вызывает сильный зуд, а расчесывание нарушает кожный барьер и может привести к проникновению бактерий, особенно у пациентов с плохой гигиеной ногтей.Стрептококковые или стафилококковые инфекции могут вызывать импетиго, паронихию, целлюлит или абсцессы. 33 Последствия этих бактериальных инфекций включают бактериемию, приводящую к сепсису, острому постстрептококковому гломерулонефриту и ревматической болезни сердца. 22, 33
Наиболее уязвимыми к заражению чесоткой группами населения являются дети младшего возраста, пожилые люди и люди с ослабленным иммунитетом. Эти популяции особенно подвержены вторичным осложнениям заражения.Учитывая, что передача инфекции является предпочтительной в условиях скученности и плохой санитарии, вспышки заболевания наблюдались в лагерях беженцев и приютах для лиц, ищущих убежища. 12
Покрытая коркой чесотка, также известная как норвежская чесотка, особенно опасна из-за высокого уровня смертности от бактериального сепсиса. 34 Вызванная гиперинвазией чесоточных клещей, покрытая корками чесотка характеризуется развитием тяжелой воспалительной реакции и гиперкератоза (утолщение кожных корок). 35 Может быть поражен любой участок кожи, но обычно поражаются участки кожи головы, рук и ног.Корки имеют неприятный запах, ногти утолщаются и обесцвечиваются. Большинство случаев покрытого коркой варианта связаны с хозяевами с ослабленным иммунитетом; однако случаи корковой чесотки имели место без выявленных факторов риска. 35 С точки зрения общественного здравоохранения пациенты с покрытой коркой чесоткой очень заразны и, поскольку они переносят значительное количество клещей, они могут быть основным источником вспышки чесотки в сообществе. Кроме того, чесотку с коркой трудно лечить, часто требуя нескольких процедур. 35
Большинство случаев покрытого коркой варианта связаны с хозяевами с ослабленным иммунитетом; однако случаи корковой чесотки имели место без выявленных факторов риска. 35 С точки зрения общественного здравоохранения пациенты с покрытой коркой чесоткой очень заразны и, поскольку они переносят значительное количество клещей, они могут быть основным источником вспышки чесотки в сообществе. Кроме того, чесотку с коркой трудно лечить, часто требуя нескольких процедур. 35
ПЕРЕДАЧИ И СРЕДСТВА ИНДИВИДУАЛЬНОЙ ЗАЩИТЫ
Чесотка человека — паразитарная кожная инфекция, вызываемая проникновением эктопаразитарного клеща. Sarcoptes scabiei var. hominis в эпидермис. Жизненный цикл самки клеща начинается с откладывания яиц в норах кожи. Эти личинки вылупляются, создают новые норы, а затем созревают, спариваются и повторяют этот цикл. 1 Зараженные чесоточным клещом пациенты с симптомами, а также бессимптомные носители могут легко распространять болезнь. 1, 36
Обычно передача происходит от человека к человеку при прямом контакте с кожей, в том числе половым путем. Из-за бессимптомного периода после заражения передача может произойти до появления симптомов. 1 Кроме того, возможна передача фомита через зараженные предметы, такие как мебель и одежда, особенно при варианте чесотки с коркой. 1, 36 Вне человеческого тела и при комнатной температуре и нормальной влажности клещи могут жить не более 3 дней, тогда как внутри кожи человека они могут жить до 60 дней. 1, 36 Более низкая температура и более высокая влажность продлевают выживаемость клеща вне хозяина. 23
Для предотвращения передачи в медицинских учреждениях пациенты должны находиться в контактной изоляции в течение 8 часов после лечения. 36 Средства индивидуальной защиты для медицинских работников, лечащих больных чесоткой, включают следующее: халаты, перчатки и бахилы. 36 Правильное использование мер инфекционного контроля, включая мытье рук и недопущение контакта кожи с кожей, также следует использовать при работе с пациентами с потенциальным заражением чесоткой.
36 Правильное использование мер инфекционного контроля, включая мытье рук и недопущение контакта кожи с кожей, также следует использовать при работе с пациентами с потенциальным заражением чесоткой.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Общие проявления шелушения и экскориации могут ухудшить визуализацию кожи, что делает дифференциальный диагноз очень широким. Клиницисты должны рассматривать папулезную крапивницу, вторичный сифилис, фолликулит, контактный дерматит, атопический дерматит, псориаз, себорею, розовый лишай, красный плоский лишай и герпетиформный дерматит.
ЛЕЧЕНИЕ
Варианты лечения зависят от клинических проявлений чесотки: классические или покрытые коркой (таблица).Как правило, лекарства состоят из чесотки, которую можно применять местно или принимать внутрь. При классической чесотке перметрин или ивермектин для перорального применения считаются препаратами первой линии. 23 Режимы дозирования включены в таблицу. Хотя качественные исследования, сравнивающие препараты для лечения чесотки, отсутствуют, систематический Кокрановский обзор пришел к выводу, что перметрин более эффективен, чем ивермектин. 37 Однако более поздний систематический обзор 2018 г. пришел к выводу, что ивермектин, и перметрин обладают одинаковой эффективностью. 38
Таблица дозирования и сроков лечения чесотки с вариациями для норвежской (покрытой коркой) чесотки.| Лекарство | Дозирование | Сроки | Вариант норвежской чесотки |
|---|---|---|---|
| Крем перметрин 5% | Наносить местно на все тело | Смыть через 8–14 часов | Повторять ежедневно в течение 7 дней, затем дважды в неделю до выписки или излечения ** Рекомендуемая комбинированная терапия с ивермектином |
| Ивермектин | 200 мкг / кг / доза перорально | 2 дозы с интервалом в 1 неделю | 3, 5 или 7 доз в зависимости от степени тяжести 3 Режим дозирования: дни 1, 2, 85 Режим доз: дни 1, 2, 8, 9, 15 # Режим дозирования 7: дни 1, 2, 8, 9, 15, 22, 29 # Рекомендуемая комбинированная терапия с перметрином |
| Серная мазь (5% –10%) | Наносить местно на все тело | Смыть через 24 часа Повторить 3 приема | Не рекомендуется |
мкг / кг / доза, микрограммы на килограмм на дозу.
При использовании по назначению 5% перметрин для местного применения имеет высокие показатели излечения, приближаясь к 90% в рандомизированных исследованиях. 39 Перметрин применяется местно у пациентов старше 2 месяцев от шеи до подошв ног и смывается через 8–14 часов. Учитывая, что чесотка также может поражать лицо, кожу головы и шею у младенцев и детей младшего возраста, местное применение следует распространить на эти области. 36, 40 В тяжелых случаях необходимо повторение местного лечения перметрином через одну или две недели после первого лечения. 36 Устные ивермектин является альтернативной терапией, которая может использоваться, если местное лечение не помогает; Однако его безопасность для беременных и детей с массой тела менее 15 кг не установлена. 34, 46, 37, 41- 43
При чесотке с коркой следует одновременно назначать пероральный и местный скабицид (таблица). 15, 19, 37 Использование ивермектина также описано для борьбы с чесоткой в эндемичных районах или при вспышках, где местное применение скабицида может быть затруднено. 12 Рандомизированное контролируемое исследование массового применения ивермектина для лечения чесотки показало снижение распространенности с 32,1% до 1,9% в группе ивермектина по сравнению с уменьшением с 41,7% до 15,8% в контрольной группе, получавшей перметрин. 44
Другие местные агенты, такие как сера, бензилбензоат, кротамитон и линдан, также являются вариантами, если лечение первой линии не дает результата. Местная сера считается безопасной при использовании для лечения младенцев в возрасте до 2 месяцев и беременных женщин. 36, 40, 41 В дополнение к скабицидам, лечение вторичных бактериальных инфекций, таких как пиодермия или импетиго, при их наличии, показано путем введения соответствующих системных антибиотиков.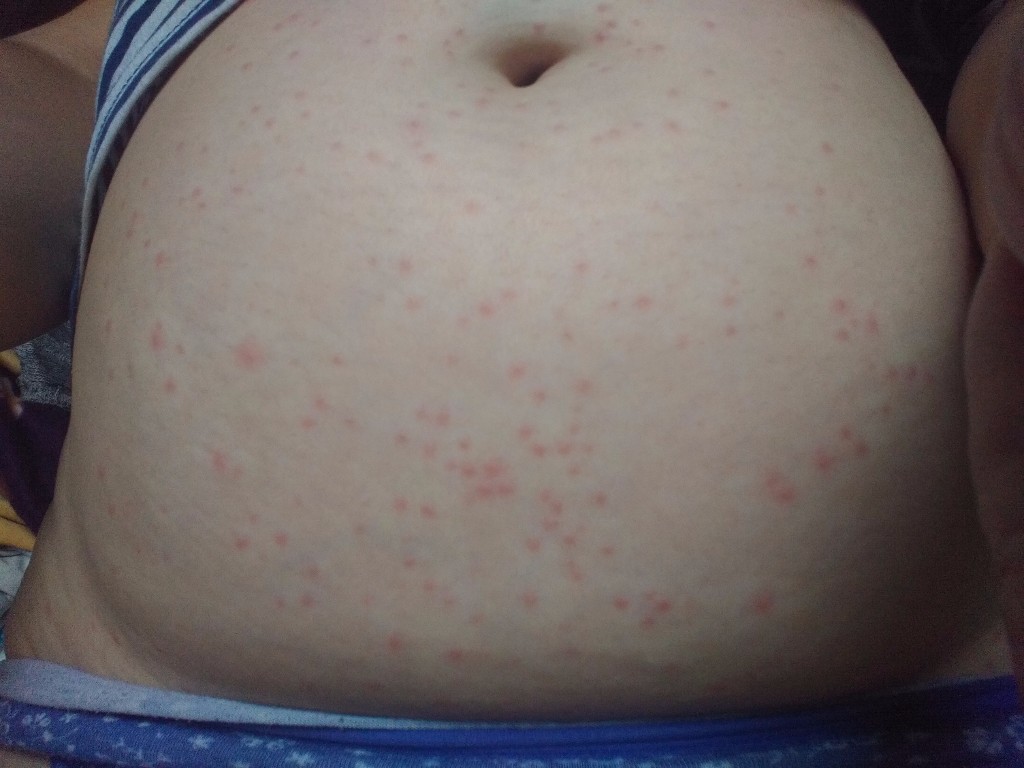 36 Совет пациентам и родителям маленьких пациентов держать ногти короткими и чистыми может помочь предотвратить вторичные инфекции.
36 Совет пациентам и родителям маленьких пациентов держать ногти короткими и чистыми может помочь предотвратить вторичные инфекции.
Пациенты, получающие лечение от чесотки, могут иметь стойкий зуд до 4 недель. Многие пациенты возвращаются в отделение неотложной помощи с опасениями по поводу неэффективности лечения или повторного заражения.Эти стойкие симптомы не обязательно указывают на неэффективность лечения. Симптоматическое лечение и успокоение часто являются единственными необходимыми методами лечения. Симптомы, которые сохраняются или ухудшаются по прошествии 2–4 недель, особенно если сыпь усиливается или появляются новые норы, должны побудить врача рассмотреть другие причины, такие как неправильный диагноз, неэффективность лечения из-за сопротивления или неправильного применения, вторичные инфекции и / или повторное заражение. . 45
ПРОФИЛАКТИКА
Чтобы искоренить и предотвратить повторное заражение чесоточного клеща, необходимо одновременно лечить тесные контакты (в течение предыдущих 30 дней).Кроме того, предметы, которыми пользовались пациенты и их близкие в предшествующие несколько дней, такие как одежда и постельное белье, следует стирать и сушить при высоких температурах (≥60 ° C), подвергать химчистке или помещать в пластиковый пакет не менее чем на 72 часа, если невозможно отмыть. 36, 46 Другим аспектом борьбы с этим заболеванием является предотвращение прямого контакта кожи с кожей с подозреваемыми или подтвержденными случаями чесотки в течение 8 часов после лечения. 36 В некоторых случаях неудачи в лечении возникают из-за неправильного или неадекватного применения лекарств, повторного заражения вследствие неправильного обращения с одеждой и постельным бельем, недостаточного лечения близких контактов и устойчивости к некоторым лекарствам, таким как линдан. 34, 35, 37, 41- 43, 47 Профилактика корковой (норвежской) чесотки и борьба с ней сложнее, поскольку кратковременный контакт кожи с кожей может распространить инфекцию. В этих случаях многочисленным контактам может потребоваться лечение, чтобы предотвратить крупномасштабную вспышку. 35, 41 В общинах с высокой распространенностью чесотки массовое введение чесотки использовалось для эффективной борьбы. Это может быть стратегия при крупных вспышках; однако перед применением этого подхода следует проконсультироваться с местными органами здравоохранения. 48
В этих случаях многочисленным контактам может потребоваться лечение, чтобы предотвратить крупномасштабную вспышку. 35, 41 В общинах с высокой распространенностью чесотки массовое введение чесотки использовалось для эффективной борьбы. Это может быть стратегия при крупных вспышках; однако перед применением этого подхода следует проконсультироваться с местными органами здравоохранения. 48
УТИЛИЗАЦИЯ
Госпитализация не рекомендуется пациентам с чесоткой, если у них нет других показаний, таких как покрытая коркой (норвежская) чесотка или тяжелые вторичные инфекции. Необходимо организовать последующее наблюдение через 2–4 недели после лечения для оценки неэффективности приема лекарств, а также повторного заражения. 38 На основании общих рекомендаций Центров по контролю и профилактике заболеваний пациенты с чесоткой могут вернуться на работу или в школу через 1 день после начала лечения и до последующего наблюдения. 36 Медицинские работники с чесоткой, которые оказывают непосредственную помощь пациентам и сохраняют симптомы после начала лечения, могут вернуться к работе, если они соблюдают стандартные меры предосторожности, включая использование одноразовых перчаток, до тех пор, пока не будут уверены, что они больше не заражены. 36
ИДЕНТИФИКАЦИЯ-ИЗОЛЯЦИЯ-ИНФОРМАЦИЯ (3I)
Инструмент «Идентифицировать-изолировать-информировать» (3I) был разработан во время вспышки болезни, вызванной вирусом Эбола, в 2014 году и позже модифицирован для применения в оценке ED и ведении пациентов с другими инфекционными заболеваниями. 14- 20 Представленная здесь новая модификация этого инструмента может быть применена для оценки ЭД и ведения пациента, обследуемого на чесотку. Инструмент Scabies 3I Tool — это алгоритм, который начинается с , выявляя подозреваемых случаев на основе симптомов, истории заражения и тестирования по мере необходимости.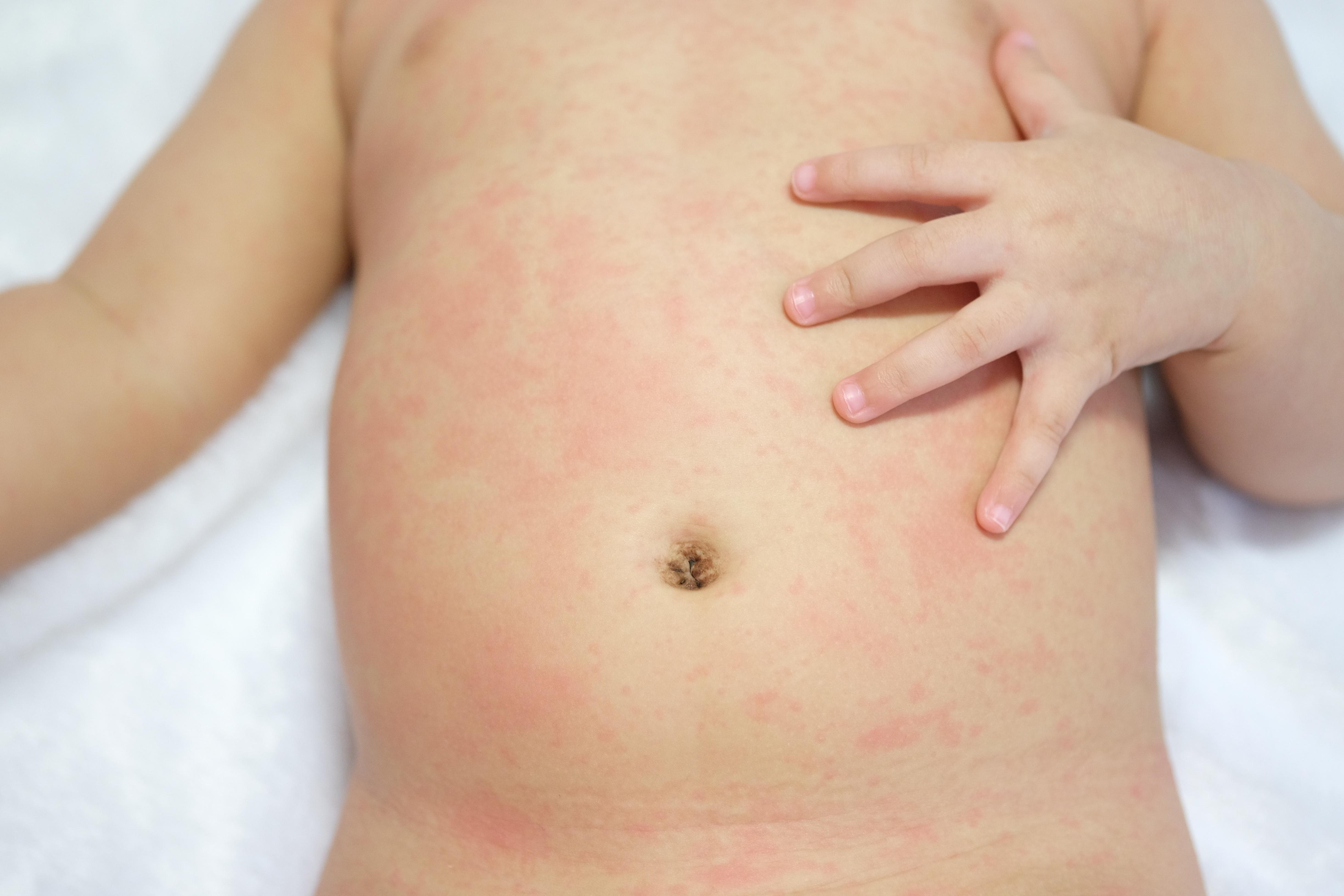 История воздействия важна, поскольку пациенты могут передавать чесотку до появления симптомов. Выявление близких контактов также является важным шагом в борьбе с распространением заражения.
История воздействия важна, поскольку пациенты могут передавать чесотку до появления симптомов. Выявление близких контактов также является важным шагом в борьбе с распространением заражения.
Чтобы предотвратить передачу в медицинских учреждениях, пациенты должны быть изолированы контактной изоляцией в течение 8 часов после лечения. 36 Средства индивидуальной защиты для медицинских работников, лечащих больных чесоткой, включают в себя следующие защитные предметы одежды: халаты, перчатки и бахилы. 36 Правильное использование мер инфекционного контроля, включая предотвращение контакта кожи с кожей и мытье рук, следует соблюдать при обращении с пациентами с потенциальным заражением чесоткой. 36
Учитывая передаваемость этого заболевания и потенциальные вспышки, которые могут угрожать общественному здоровью, персонал ED должен немедленно информировать местный орган здравоохранения о случаях вспышки, определяемой как два или более последовательных случая чесотки среди жителей / персонала в течение 4–6 недель. . 49 Своевременное уведомление о вспышке особенно важно в случаях чесотки, выявленных в медицинских учреждениях, приютах или других общинах, где болезнь может быстро распространяться, включая приюты для беженцев и мигрантов.Согласно онлайн-обзору политики 20 больниц в Соединенных Штатах, ни одна больница не требовала информирования больничного инфекционного контроля о случаях чесотки; однако политика отдельных больниц может отличаться как в США, так и за рубежом. Поэтому важно знать правила местных больниц в отношении сообщений о чесотке и соблюдать их. Кроме того, следует незамедлительно изолировать случаи покрытой коркой (норвежской) чесотки, а также проинформировать всех близких людей и лечить их, учитывая высокую скорость передачи. 35, 41 Используя этот инструмент 3I Identify-Isolate-Inform, медицинские работники могут быть более подготовлены к выявлению потенциальных случаев чесотки и ведению их.
ЗАКЛЮЧЕНИЕ
Оперативное распознавание передаваемых заболеваний, таких как чесотка, работниками скорой медицинской помощи необходимо для предотвращения распространения. Чесотку бывает сложно диагностировать, и как недостаточная, так и чрезмерная диагностика чесотки имеют негативные последствия для здоровья и ресурсов. Новый инструмент выявления чесотки-изолировать-информировать (3I) может помочь персоналу отделения неотложной помощи быстро распознать ключевые факторы риска заражения и характерные симптомы болезни, тем самым инициируя внедрение соответствующих протоколов изоляции и уведомление больниц и органов общественного здравоохранения, в зависимости от обстоятельств. .
Сноски
Редактор раздела: Марк И. Лангдорф, MD, MHPE
Полный текст доступен в открытом доступе по адресу http://escholarship.org/uc/uciem_westjem
Адрес для переписки: Табита А. Ченг, доктор медицины, Калифорнийский университет, Сан-Диего, отделение неотложной медицины, 200 W. Arbor Dr. # 8676, Сан-Диего, Калифорния 92103. Электронная почта: [email protected]. 3/2020; 21: 191 — 198
История поступления: доработка получена 9 декабря 2019 г .; Поступила 1 января 2020 г. Принят в печать 22 января 2020 г.
Конфликты интересов : Согласно соглашению о представлении статей West JEM, все авторы обязаны раскрывать всю аффилированность, источники финансирования и финансовые или управленческие отношения, которые могут быть восприняты как потенциальные источники предвзятости.Автор не имеет профессиональных или финансовых отношений с компаниями, имеющими отношение к данному исследованию. Нет никаких конфликтов интересов или источников финансирования, о которых следует заявлять.
ССЫЛКИ
1. Арлиан Л.Г., Морган М.С. Обзор Sarcoptes scabiei: прошлое, настоящее и будущее. Векторы паразитов . 2017; 10 (1): 297.
2. Романи Л., Стир А.С., Уитфельд М.Дж., Калдор Дж.М. Распространенность чесотки и импетиго во всем мире: систематический обзор. Lancet Infect Dis .2015; 15 (8): 960-967.
Lancet Infect Dis .2015; 15 (8): 960-967.
3. Ласса С., Кэмпбелл М.Дж., Беннет С.Е. Эпидемиология распространенности чесотки в Великобритании по данным общей практики. Br J Дерматол . 2011; 164 (6): 1329-1334.
4. Вакирлис Э., Теодосиоу Г., Апалла З. и др. Ретроспективное эпидемиологическое исследование кожных заболеваний среди педиатров, посещающих специализированный дерматологический центр в Северной Греции. Clin Cosmet Investig Dermatol . 2017; 10: 99-104.
5. Альбарес М.П., Белинчон И., Рамос Дж. М., Санчес-Пая Дж., Бетлох И. Actas Dermosifiliogr . 2012; 103 (3): 214-222.
6. Терри BC, Kanjah F, Sahr F, Kortequee S, Dukulay I, Gbakima AA. Заражение Sarcoptes scabiei среди детей в лагере для перемещенных лиц в Сьерра-Леоне. Общественное здравоохранение . 2001; 115 (3): 208-211.
7. Озтюрккан С., Озчелик С., Сайги Г. Распространение чесотки и pediculus humanus среди детей в приюте Сивас. Индийский педиатр . 1994; 31 (2): 210-213.
8. Бокари MJ, Александр Н.Д., Казура JW, Бокари Ф., Гриффин Л., Альперс М.П.Лечение ивермектином снижает высокую распространенность чесотки в деревне в Папуа-Новой Гвинее. Acta Trop . 2000; 75 (1): 127-130.
9. Мухаммад Зайид М., Саидатул Саада Р., Адил А. Р., Рохела М., Джамайя I. Распространенность чесотки и вшей среди детей в доме престарелых в Пулау-Пинанге, Малайзия. Троп Биомед . 2010; 27 (3): 442-446.
10. Пруксачаткунакорн С., Вонгтхани А., Касиват В. Чесотка в тайских детских домах. Педиатр Инт . 2003; 45 (6): 724-727.
11. Кортас А.З., Поленц Дж., Фон Хайек Дж. И др. Скрининг на инфекционные заболевания среди лиц, ищущих убежища, вновь прибывших в Германию в 2015 году: систематический одноцентровый анализ. Общественное здравоохранение . 2017; 153: 1-8.
12. Beeres DT, Ravensbergen SJ, Heidema A, et al. Эффективность массового применения ивермектина для борьбы с чесоткой у лиц, ищущих убежища, в Нидерландах: ретроспективное когортное исследование с января 2014 г.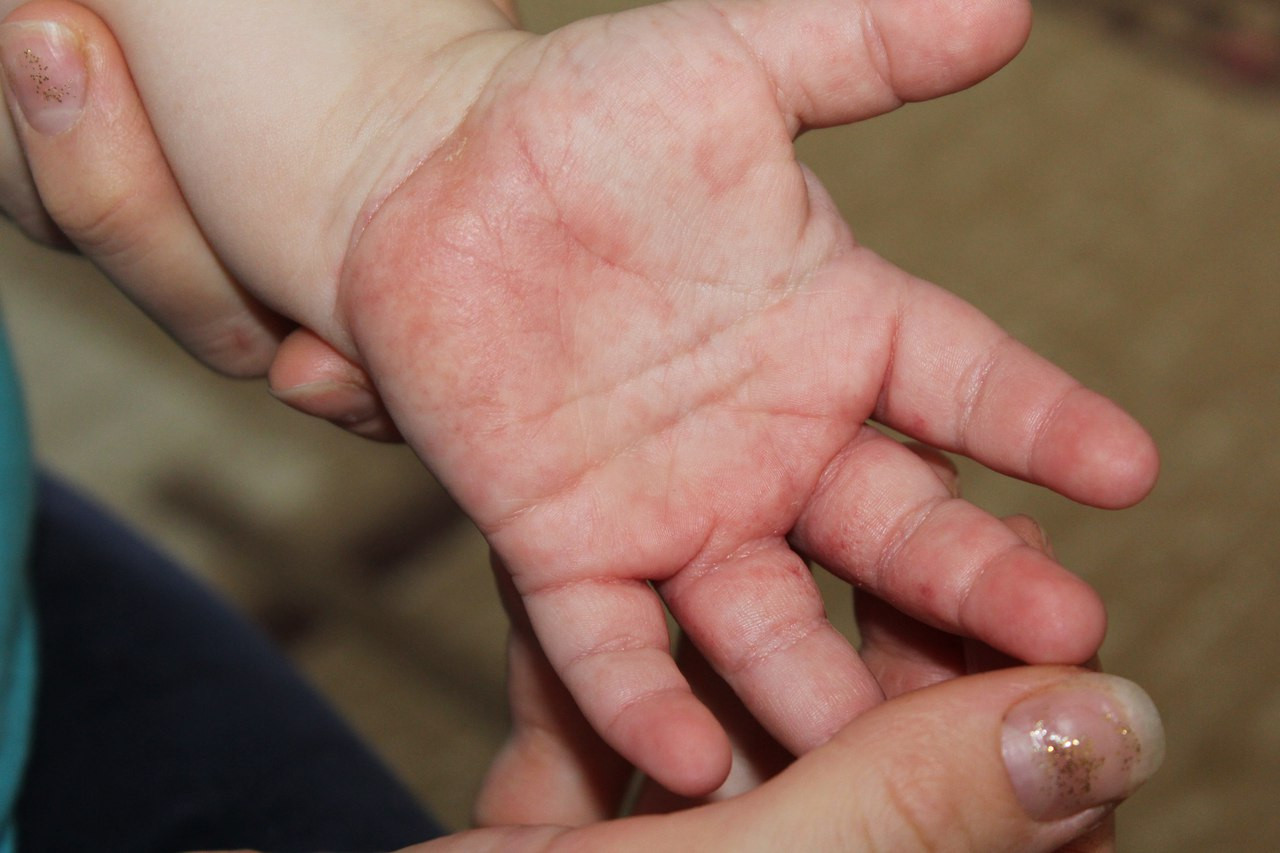 по март 2016 г. PLoS Negl Trop Dis . 2018; 12 (5): e0006401.
по март 2016 г. PLoS Negl Trop Dis . 2018; 12 (5): e0006401.
13. Koenig KL. Выявить, изолировать, проинформировать: трехкомпонентный подход к управлению чрезвычайными ситуациями в области общественного здравоохранения. Disaster Med Public Health Prep . 2015; 9 (1): 86-87.
14. Koenig KL. Identify-Isolate-Inform: модифицированный инструмент для первоначального выявления и лечения пациентов с респираторным синдромом на Ближнем Востоке в отделении неотложной помощи. West J Emerg Med . 2015; 16 (5): 619-624.
15. Кениг К.Л., Алассаф В., Бернс М.Дж. Идентифицировать-изолировать-информировать: инструмент для первичного выявления и ведения больных корью в отделении неотложной помощи. West J Emerg Med . 2015; 16 (2): 212-219.
16. Кениг К.Л., Альмадхян А., Бернс М.Дж. Идентифицировать-изолировать-информ: инструмент для первичного выявления и лечения пациентов с вирусом Зика в отделении неотложной помощи. West J Emerg Med . 2016; 17 (3): 238-244.
17. Кениг К.Л., Шастри С., Мзахим Б., Альмадхян А., Бернс М.Дж. Вирус паротита: модификация инструмента «Идентифицировать-изолировать-информировать» для передовых медицинских учреждений. West J Emerg Med . 2016; 17 (5): 490-496.
18.Кениг К.Л., Шастри С., Бернс М.Дж. Вирус гепатита А: необходимые знания и новый инструмент идентификации-изолирования-информирования для передовых медицинских учреждений. West J Emerg Med . 2017; 18 (6): 1000-1007.
19. Кениг К.Л., Фарах Дж., Макдональд Э.С., Тихалолипаван С., Бернс М.Дж. Коклюш: средство выявления, изоляции, информирования, применяемое при рецидивирующем респираторном заболевании. West J Emerg Med . 2019; 20 (2): 191-197.
20. Koenig KL, Beÿ CK, McDonald EC. 2019-nCoV: инструмент «Идентифицировать-изолировать-информировать» (3I), применяемый к новому появляющемуся коронавирусу. West J Emerg Med . 2020; 21 (2): 184-90.
21. Маккарти Дж. С. , Кемп Д. Д., Уолтон С. Ф., Карри Б. Дж.. Чесотка: больше, чем просто раздражение. Postgrad Med J . 2004; 80 (945): 382-387.
, Кемп Д. Д., Уолтон С. Ф., Карри Б. Дж.. Чесотка: больше, чем просто раздражение. Postgrad Med J . 2004; 80 (945): 382-387.
22. Эндрюс Р. М., Маккарти Дж., Карапетис Дж. Р., Карри Б. Дж.. Кожные заболевания, в том числе пиодермия, чесотка и инфекции опоясывающего лишая. Педиатрическая клиника North Am . 2009; 56 (6): 1421-1440.
23. Heukelbach J, Feldmeier H. Scabies. Ланцет . 2006; 367 (9524): 1767-1774.
24.Фельдмайер Х., Джексон А., Ариза Л. и др. Эпидемиология чесотки в бедном сообществе в сельских районах Бразилии: наличие и тяжесть заболевания связаны с плохими условиями жизни и неграмотностью. J Am Acad Dermatol . 2009; 60 (3): 436-443.
25. Ван С.Х., Ли С.К., Хуанг С.С., Као Ю.К., см. LC, Ян Ш. Факторы риска чесотки на Тайване. J Microbiol Immunol Infect . 2012; 45 (4): 276-280.
26. Вудли Д., Сорат Дж. Х. Тест Burrow Ink и чесоточный клещ. J Am Acad Dermatol . 1981; 4 (6): 715-722.
27. Шимосе Л., Муньос-Прайс Л.С. Диагностика, профилактика и лечение чесотки. Curr Infect Dis Rep . 2013; 15 (5): 426-431.
28. Барри М., Кауфман К.Л., Уилсон Б.Б., Розен Э., Рош А.Дж. Обследование чесотки: поиск нор клещей . Доступно по адресу: https://emedicine.medscape.com/article/1109204-workup#c7. Доступ 21 декабря 2019 г.
29. Burkhart CG, Burkhart CN, Burkhart KM. Эпидемиологическая и терапевтическая переоценка чесотки. Cutis . 2000; 65 (4): 233-240.
30. Lacarrubba F, Musumeci ML, Caltabiano R, Impallomeni R, West DP, Micali G. Видеодерматоскопия с большим увеличением: новый неинвазивный диагностический инструмент для лечения чесотки у детей. Педиатр дерматол . 2001; 18 (5): 439-441.
31. Bezold G, Lange M, Schiener R, et al. Скрытая чесотка: диагностика методом полимеразной цепной реакции. Br J Дерматол . 2001; 144 (3): 614-618.
32. Джаярадж Р., Хейлз Б., Виберг Л. и др. Диагностический тест на чесотку: специфичность IgE к рекомбинантному аллергену Sarcoptes scabiei. Диагностика Microbiol Infect Dis . 2011; 71 (4): 403-407.
Диагностика Microbiol Infect Dis . 2011; 71 (4): 403-407.
33. Карапетис Дж. Р., Стир А. К., Малхолланд Е. К., Вебер М. Глобальное бремя стрептококковых заболеваний группы А. Lancet Infect Dis . 2005; 5 (11): 685-694.
34. Currie BJ, McCarthy JS. Перметрин и ивермектин от чесотки. N Engl J Med . 2010; 362 (8): 717-725.
35. Робертс Л.Дж., Хаффам С.Е., Уолтон С.Ф., Карри Б.Дж.. Корковая чесотка: клинические и иммунологические данные у семидесяти восьми пациентов и обзор литературы. J Заразить . 2005; 50 (5): 375-381.
36. Ресурсы CDC-Scabies для медицинских работников . Доступно по адресу: https://www.cdc.gov/parasites/scabies/health_professionals/. По состоянию на 14 августа 2019 г.
37. Уокер Г.Дж., Джонстон П.В. Вмешательства для лечения чесотки. Кокрановская база данных Syst Rev . 2000 (3): CD000320.
38. Розумек С., Наст А., Дресслер С. Ивермектин и перметрин для лечения чесотки. Кокрановская база данных Syst Rev .2018 (4): CD012994.
39. Джонстон П., Стронг М. Чесотка. BMJ Clin Evid . 2014: 2014.
40. Картикеян К. Чесотка у детей. Arch Dis. Детское обучение, изд. . 2007; 92 (3): ep65-69.
41. Дэвис Дж. С., МакГлафлин С., Тонг С. Ю., Уолтон С. Ф., Карри Б. Дж.. Новая клиническая шкала для оценки лечения чесотки с коркой. PLoS Negl Trop Dis . 2013; 7 (9): e2387.
42. Пасай К., Маунси К., Стивенсон Г. и др. Акарицидная активность соединений на основе эвгенола против чесоточных клещей. PLoS One . 2010; 5 (8): e12079.
43. Шарма Р., Сингал А. Актуальный перметрин и пероральный ивермектин в лечении чесотки: проспективное, рандомизированное, двойное слепое, контролируемое исследование. Indian J Dermatol Venereol Leprol . 2011; 77 (5): 581-586.
44. Romani L, Whitfeld MJ, Koroivueta J, et al. Массовое управление лекарствами для борьбы с чесоткой среди населения с эндемическими заболеваниями.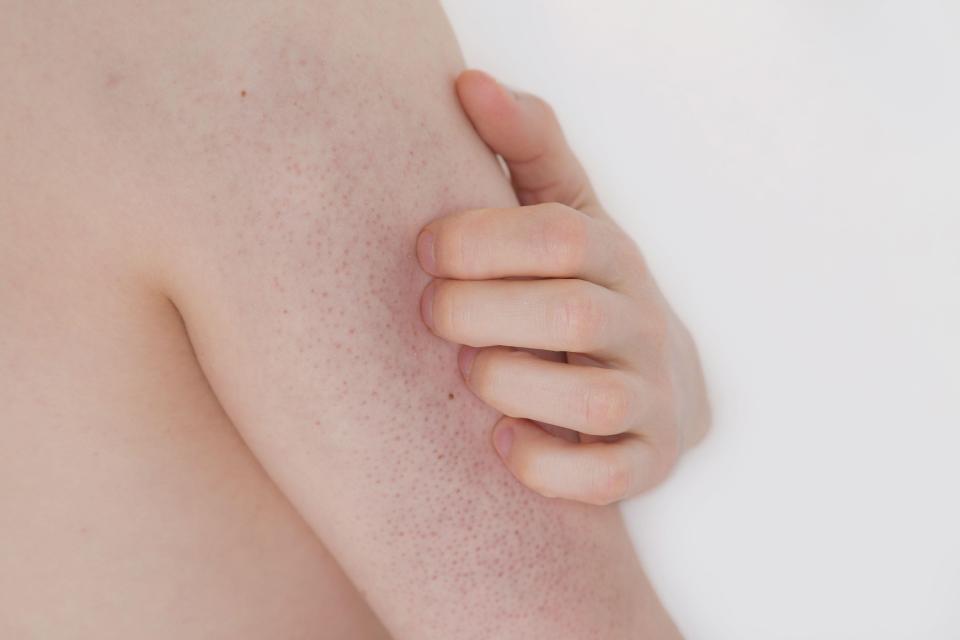 N Engl J Med . 2015; 373 (24): 2305-2313.
N Engl J Med . 2015; 373 (24): 2305-2313.
45. Global Health, Отдел паразитарных болезней Паразиты: чесотка — лечение .Доступно по адресу: htts: //www.cdc.gov/parasites/scabies/treatment.html. Доступ 30 июля 2019 г.
46. Бурштейн Г.Р., Ворковский К.А. Рекомендации по лечению заболеваний, передающихся половым путем. Curr Opin Pediatr . 2003; 15 (4): 391-397.
47. Картикеян К. Лечение чесотки: новые перспективы. Postgrad Med J . 2005; 81 (951): 7-11.
48. Романи Л., Маркс М., Сокана О. и др. Эффективность массового введения лекарств с ивермектином для борьбы с чесоткой и импетиго с одновременным введением азитромицина: исследование вмешательства на уровне сообщества с участием одного человека. Lancet Infect Dis . 2019; 19 (5): 510-518.
49. Ведение вспышек чесотки в медицинских учреждениях Калифорнии . Доступно по адресу: https://www.cdph.ca.gov/Programs/CID/DCDC/CDPH%20Document%20Library/MgmntofScabiesOutbreaksinHCFacilities.pdf. По состоянию на 19 сентября 2019 г.
50. Гомес ФК. Тест чернил на чесотку . 2019.
% PDF-1.3 % 2 0 obj > эндобдж 8 0 объект [ 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0500500 434 238 438 843 693 820 654 434 366 366 530 610 434 610 434 512 610 610 610 610 610 610 610 610 610 610 434 434 610 610 610 566 931 731 630 619 722 625 607 680 768 546 665 611 551 883 813 798 533 876 640 693 696 737 675 1040 724 635 693 376 550 376 610 627 556 556 593 514 587 559 508 531 578 280 403 540 274 777 523 526 535 520 480 487 471 520 486 684 590 553 538 366 421 366 610 500 619 500 434 589 430 675 610 597 556 1241 693 610 1194 500 693 500 500 226 226 434 434 610 441 883 556 883 507 610 897 500 538 635 476 238 610 793 610 610 421 635 556 795 610 639 610 610 795 627 610 610 610 610 556 610 761 610 556 610 610 639 610 610 610 566 731 731 731 731 731 731 1087 619 625 625 625 625 546 546 546 546 722 813 798 798 798 798 798 610 798 737 737 737 737 635 521 534 556 556 556 556 556 556 912 514 559 559 559 559 280 280 280 280 280 509 523 526 526 526 526 526 610 533 520 520 520 520 553 535 553 ] эндобдж 11 0 объект [ 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0500500 299 238 424 843 693 820 654 388 366 366 530 480 277 417 249 512 610450610610610610610610610610299299381 510381 524 931 731 630 603 722 625 607 680 768 546 665 611 551 883 797 798 521 876 628 693 680 737 650 1040 724 635 693 376 550 376 581 627 556 512 593 514 587 548 508 531 578 280 403 540 274 777 523 526 535 520 480 487 471 520 486 684 590 521 538 366 421 366 598 500 610 500 299 427 412 675 597 597 556 1241 693 381 1194 500 693 500 500 180 180 394 394 387 441 883 556 883 403 381 897 500 538 635 299 238 623 793 612 636 404 635 556 795 527 578 480 417 795 627 409 480 651 651 556 520 694 249 556 651 449 578 651 651 651 524 731 731 731 731 731 731 1087 603 625 625 625 625 546 546 546 546 722 797 798 798 798 798 798 480 798 737 737 737 737 635 52 1443 512 512 512 512 512 512 912 514 548 548 548 548 280 280 280 280 280 509 523 526 526 526 526 526 480 526 520 520 520 520 521 535 431 ] эндобдж 14 0 объект > поток x ڕ Xn6 + xTD + ɲlEmauQND [l $ Qu} 3, Md0 «ZCμy367> K & Nh» D4Rinυieo_2ͼiYoga: poT ي $ TIJ, — ^ «? b3 @, ewNh +, @ ϻd 풮 c + tWI v
Q ؝ md] ~ AVΊ + Jhl8 / 8BqhL} h0ѩizmhyh ᭄6 CNXE # = | = gQIpv {2u] lp $ z: iWk 砷 boE
i / Ŧ ޙ #} i (aRV`SƁ Q-LxYs} HZ? D & | N1ȄcxY މ VZ ּ L | 5hM, ^) 42 и 8 @ HQ ~ SƒE {
| Определение (CHV) | Инфекционное воспаление кожи, вызванное укусом клеща. |
| Определение (MEDLINEPLUS) | Чесотка — это кожный зуд, вызываемый микроскопическим клещом Sarcoptes scabei.Это распространено во всем мире и может повлиять на кого угодно. Чесотка быстро распространяется в условиях скопления людей, при частом контакте кожи с кожей между людьми. Больницы, детские центры и дома престарелых являются примерами. Чесотка легко может заразить половых партнеров и других членов семьи. Совместное использование одежды, полотенец и постельного белья также может распространить чесотку. Нельзя заразиться чесоткой от домашнего животного. Домашние животные заражаются другим клещом — чесоткой. Симптомы
Ваш лечащий врач диагностирует чесотку, глядя на кожную сыпь и находя на коже борозды. Для лечения чесотки существует несколько лосьонов. Одежду, постельное белье и полотенца инфицированного человека следует выстирать в горячей воде и высушить в горячей сушилке. Лечение также рекомендуется для членов семьи и сексуальных партнеров. Центры по контролю и профилактике заболеваний |
| Определение (MSHCZE) | Parazitární kožní onemocnění vyvolané roztočem zákožkou svrabovou (Sarcoptes scabiei).Samička vrtá v kži až několik milimetrů dlouhé chodbičky, v nichž klade vajíčka. Člověk se nakazí obv. непржимо (např. ložním prádlem). По инкубации, 2–6, ты сидишь на объекте, силне, свидени, ктере зесили по улехнута (в тепле). На kži se objevují červené pupínky (často dvojice — začátek a konec chodbičky), které se mohou druhotně infikovat. Časté je postižení meziprstních prostor, okolí pohlavních orgánů, kolen, podpaží aj. Nález u osob s dobrou hygienou však nemusí být takto typický. K léčbě se používají skabicidní přípravky (např.линдан), эв. magistraliter přípravky obsahující mj. síru. (Cit. Velký lékařský slovník online, 2013 http://lekarske.slovniky.cz/) |
| Определение (NCI) | Заразная кожная инфекция, которая вызывается роющим паразитическим клещом sarcoptes scabiei и характеризуется сильным зудом и небольшими выступающими красными пятнами в области норок клеща. |
| Определение (MSH) | Инфекционное кожное воспаление, вызванное укусом клеща SARCOPTES SCABIEI. Он характеризуется зудящими папулезными высыпаниями и зародышами и поражает в первую очередь подмышечные впадины, локти, запястья и гениталии, хотя может распространяться на все тело. |
| Концепции | Заболевание или синдром ( T047 ) |
| MSH | D012532 |
| ICD9 | 133.0 |
| ICD10 | B86 |
| SnomedCT | 266224002, 154422001, 187215008, 67172004, 128869009 |
| Английский | Чесотка, чесотка, чесотка (диагностика), чесотка [заболевание / обнаружение], заражение Sarcoptes scabiei (заболевание), саркоптозный зуд, заражение Sarcoptes scabiei var hominis (заболевание), заражение Sarcoptes scabiei var hominis, Sarcoptes scabiei var hominis; акариоз, Sarcoptes scabiei; инвазия, инвазия; Sarcoptes scabiei, заражение; клещи, чесотка, инвазия; чесотка, акариаз; Sarcoptes scabiei, клещи; инвазия, чесотка, чесотка; заражение, заражение Sarcoptes scabeii, заражение чесоткой, заражение Sarcoptes scabiei |
| Голландский | Sarcoptes scabeii-infestatie, чесотка, чесотка, инфекция, Sarcoptes scabiei; акариоз, Sarcoptes scabiei; инвазии, акариаз; Sarcoptes scabiei, infestatie; Sarcoptes scabiei, infestatie; mijten, schurft, infestatie; чесотка, миджтен; инвазии, шурфт, чесотка; infestatie, чесотка, скабиретинопатия bijes |
| французский | Заражение по Sarcoptes scabeii, Gale, Psore, Scabiose |
| Немецкий | Befall durch Sarcoptes scabeii, Skabies, Krätze |
| Итальянский | Infestazione da Sarcoptes scabeii, Infestazione da scabbia, Scabbia |
| Португальский | Sarna, Infestão por Sarcoptes scabeii, Infestação por Sarcoptes scabiei, Escabiose |
| Испанский | Sarna, Infestación por Sarcoptes scabeii, infestación por Sarcoptes scabiei (trastorno), infestación por Sarcoptes scabiei, Infección por Sarcoptes scabiei, sarna, sarna (trastornotes scabiei), sarna, sarna (trastorno, scabiei) поросячий, разновидность, infestaciós , prurito sarcóptico, prurito, Escabiosis |
| Японский | 疥 癬 寄生, 疥 癬, ヒ ト 疥 癬 感染, カ イ セ ン, ヒ ト カ イ ン カ ン セ ン, カ イ セ ン キ セ イ |
| шведский | Скабб |
| Чешский | svrab, Infestace parazitem Sarcoptes scabiei, Svrab, Infestace svrabem, чесотка, скабиес |
| финский | Сыйхы |
| Русский | ЧЕСОТКА ЗУДНЕВАЯ, ЧЕСОТКА, ЧЕСОТКА, ЧЕСОТКА ЗУДНЕВАЯ |
| Корейский | 옴 |
| Польский | Ierwierzb |
| Венгерский | чесотка infestatio, Sarcoptes scabeii infestatio, чесотка |
| Норвежский | Скабб |
Чесотка — Советник по дерматологии
Передача чесотки от человека к другим видам (саркоптоз собак, например, с S scabiei var canis) может происходить, но заражение носит краткосрочный характер и самоограничивается, поскольку клещи являются не могут воспроизводиться на хозяине другого вида.Распространение поражений также не является характерным для чесотки человека.
Передача чесотки у человека чаще всего происходит при прямом кожном контакте; следовательно, в определенных возрастных группах это может считаться заболеванием, передающимся половым путем. Клещ может оставаться жизнеспособным в течение 2 или 3 дней вдали от своего хозяина, но при правильных условиях (высокая влажность, умеренная температура) клещ может выжить — и, следовательно, инфицировать хозяина — до 5 дней.
Поскольку жизненный цикл полностью протекает на коже хозяина и внутри нее, заражение от фомитов является необычным (заразиться должна беременная самка или спаривающаяся пара).В случае обширного заражения (например, покрытой коркой чесотки) большое количество проливных клещей может позволить заразиться от фомитов.
После заражения может пройти от нескольких недель до месяцев, прежде чем появится реакция гиперчувствительности замедленного типа и, следовательно, появится симптом зуда с сопутствующим зудом и экскориациями. В этот период состояние заразно, но не диагностируется. При повторном заражении зуд начинает наступать быстрее, так как пациент уже сенсибилизирован к клещу.
Хотя зуд обычно считается доброкачественным (хотя и крайне неприятным) состоянием, наблюдается ряд серьезных осложнений. Недавно сообщалось о некротической инфекции мягких тканей, вторичной по отношению к инфекции Staphylococcus aureus, вызванной экскориациями вульвы. Сообщалось также, что постстрептококковый гломерулонефрит возникает после вторичного инфицирования экскориаций Streptococcus pyogenes.
Однако более распространенной является простая импетигенизация раздраженных участков.В частности, в странах третьего мира кожная бактериальная инфекция была серьезным осложнением заражения чесоткой. Согласно недавнему отчету из Австралии, например, чесотка, которая является эндемической среди многих аборигенов, является причиной от 50% до 70% стрептококковой пиодермии.
Местные методы лечения чесотки перечислены в таблице II.
Таблица II.
| Перметрин 5% крем |
| 5% раствор малатиона |
| От 2% до 10% серы в петролатуме |
| 10% бензилбензоат |
| 5% гексахлорид гамма-бензола (линдан) |
| Кротамитон 10% крем |
| Масло австралийского чайного дерева |
| Ивермектин для местного применения |
СИСТЕМНАЯ ТЕРАПИЯ
-Ивермектин 200 мкг / кг (и 250 мкг / кг)
Средство выбора при чесотке — крем с перметрином 5%, применяемый местно.Хотя одноразовое лечение считается излечивающим, рекомендуется повторить его через неделю — возможно, для захвата недавно вылупившихся организмов или, возможно, для достижения участков кожи, которые могли быть пропущены при первом применении. Это лечение выбора при беременности, разрешенное до 2-месячного возраста.
К сожалению, устранение возбудителя чесотки с помощью однократного применения 5% крема с перметрином не устраняет ни зуда, ни экзематозной сыпи, которые, вероятно, связаны с иммунологической реакцией на присутствие микроорганизма (и его детрита) в организме. stratum corneum норы.
Применение местных или системных стероидов может обеспечить временное облегчение зуда после того, как окончательная терапия прекратила заражение. Пероральные антигистаминные или другие противозудные средства в таких случаях не особенно полезны. Поэтому я обычно делаю инъекцию приблизительно 1 мг / кг триамцинолона ацетонида пациентам, страдающим сильным зудом после лечения заражения.
В случае пациента, который не принимает инъекции (или врача, который не хочет вводить парентеральные стероиды), я бы рекомендовал пероральный преднизон или его эквивалент в дозе от 1 мг / кг до 60 мг в день в Курс от 10 до 14 дней с возможностью снижения дозы на 50% на 7 день.Можно использовать любой местный стероид средней силы, хотя мой любимый рецепт — это раствор клобетазола 0,05% 50 мл, добавляемый во флакон 220 мл лосьона Sarna и применяемый два раза в день до три раза в день.
Линдан (также GBHC или гексахлорид гамма-бензола) используется в течение многих лет для успешного лечения чесотки. Из-за токсичности для окружающей среды и нейротоксичности он был запрещен в Калифорнии и ряде стран. Он эффективен и по-прежнему доступен во многих странах. Прямых исследований GBHC и перметрина не проводилось.Он помечен как препарат второго ряда и должен использоваться только в случае неэффективности лечения одним или несколькими препаратами первого ряда. Я не использовал его в течение многих лет, но предпочитаю немедленно перейти на пероральный прием ивермектина, если кажется, что лечение перметрином неэффективно.
Сера, 10% в петролатуме, оказалась столь же эффективной, как линдан, и кажется безопасной. Обычно его назначают младенцам в возрасте до 2 лет. До принятия отчета о безопасности перметрина при беременности в этой ситуации использовалась сера в петролатуме; сегодня мы используем перметрин.Водный малатион 0,5% также эффективен; Примечание: доступная в США форма малатиона не одобрена для лечения чесотки: в основе лежит изопропиловый спирт, который раздражает генитальные и другие воспаленные участки кожи.
Крем Кротамитон доступен в Соединенных Штатах, но при прямом сравнении с перметрином кротамитон был значительно хуже. Единственное его преимущество в том, что он обладает легким противозудным действием.
Бензилбензоат от 10% до 25% недоступен в США.Недавний Кокрановский обзор показал, что данных для сравнения относительной эффективности перметрина и бензилбензоата не существует. Однако он оказался чрезвычайно эффективным.
Ивермектин входит в группу препаратов авермектина, препарат выбора для лечения онхоцеркоза и одобрен FDA для этого состояния, а также стронгилоидоза; он использовался не по назначению для лечения чесотки без каких-либо сообщений о значительных побочных эффектах. Рекомендуемая доза составляет от 200 до 250 мкг / кг, повторять через 1 неделю.Он не одобрен для использования у детей младше 5 лет или с массой тела менее 15 кг.
Составной ивермектин для местного применения, приготовленный в виде 1% раствора в пропиленгликоле, был признан эффективным в нескольких отдельных отчетах. Группа из Колумбии сообщила об использовании местного 1% ивермектина в пропиленгликоле, 400 мкг / кг у 12 взрослых и 20 детей в возрастной группе от 1 до 10 лет со 100% излечением и отсутствием побочных эффектов после двух курсов лечения. с разницей в неделю. Общая применяемая доза составляет 400 мкг / кг 1% раствора, пациент весом 50 кг получит 400 мкг X50 — или 20 мг местно, или 2 мл.К этому добавляли еще 10 мл пропиленгликоля, чтобы получить объем, достаточный для покрытия всего тела. Опять же, это использование не по назначению.
Оптимальный подход к лечению этого заболевания
Лечением выбора при чесотке остается крем с 5% перметрином, применяемый местно, хотя были разрозненные сообщения о резистентности. Хотя одноразовое лечение считается излечивающим, рекомендуется повторить его через 1 неделю — возможно, для захвата недавно вылупившихся организмов или, возможно, для достижения участков кожи, которые могли быть пропущены при первом применении.Это лечение выбора при беременности, разрешенное до 2-месячного возраста.
Ведение пациентов
При местном лечении взрослых и детей старше 5 лет препарат следует наносить от шеи до подошв ног, уделяя особое внимание кожным складкам (шея, подмышечные впадины, паховые области, межъягодичные и межпальцевые области). В детской возрастной группе также лечат лицо и кожу головы.
В идеале, лечить следует всех членов семьи, независимо от того, зуд они или нет.Утром (после обработки) постельное белье и всю одежду, которую носили накануне, следует постирать в стиральной машине и сушилке. Вещи, которые нельзя стирать, можно гладить, стирать в химчистке или сушить в сушилке для одежды.
Такие предметы, как чучела животных, кожа или другие термочувствительные материалы, могут быть запечатаны в пластиковые пакеты на срок до двух недель. В летние месяцы я рекомендую сушить такие вещи на воздухе на солнце в течение нескольких дней. Чесоточный клещ выживает только 72 часа или около того вдали от хозяина в лучших условиях (высокая влажность, низкая температура), и эта сушка на воздухе может быть всем, что необходимо.Не рекомендуется проводить более тщательную уборку.
Необычные клинические сценарии, которые следует учитывать при ведении пациентов
У пациентов с ослабленным иммунитетом и чрезмерно выраженной чесоткой или чесоткой с коркой зуд может быть минимальным (или отсутствовать). Необходимо учитывать диагноз любой стойкой псориазоподобной или хронической экзематозной сыпи у этих пациентов, которые не ответили на стандартную терапию этих расстройств.
Какие есть доказательства?
Рамос-э-Силва, М. «Джован Козимо Бономо (1663–1696): первооткрыватель этиологии чесотки». Int J Dermatol. об. 37. 1998. pp. 8 625-30. (Доктор Рамос-э-Силва написал восхитительное историческое повествование об этой болезни и ее признании.)
Хенгге, У.Р., Карри, Б.Дж., Джагер, Г., Лупи, О., Шварц, РА. «Чесотка: широко распространенное запущенное кожное заболевание». Lancet Infect Dis. об. 6. 2006. С. 769–79. (Отличный обзор чесотки на сегодняшний день.)
Уолтон, Сан-Франциско. «Иммунология восприимчивости и устойчивости к чесотке». Parasite Immunol. об.32. 2010. С. 532-40. (Подробный обзор иммунологии чесотки и анализ факторов, приводящих к покрытой коркой чесотке.)
Вольф, Р., Давидовичи, Б. «Лечение чесотки и педикулеза: факты и противоречия». Clin Dermatol. об. 28. 2010. С. 511-8. (Превосходный обзор лечения линданом и перметрином, а также проблема, которую долгое время часто называли в среднем 12 клещей на инфицированного пациента.)
Micali, G, Lacarrubba, F, Verzì, AE, Chosidow, O, Schwartz, RA.«Чесотка: достижения в неинвазивной диагностике». PLoS Negl Trop Dis. об. 10. 2016, 16 июня. (Обновленный обзор новых средств диагностики, включая недорогую видеодерматоскопию, и ряд интересных фотографий, которые можно загрузить.)
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
Обзор Sarcoptes scabiei: прошлое, настоящее и будущее | Паразиты и переносчики
Происхождение чесоточного клеща Sarcoptes scabiei , паразитирующего на людях и многих семьях млекопитающих, неизвестно. Точно так же неизвестно, как давно началась совместная эволюция S. scabiei с конкретными млекопитающими-хозяевами и как она развивалась с течением времени. Однако акарологи и маммологи, использующие молекулярные инструменты и геномную информацию, могут со временем прояснить эти вопросы.
Ронкалли [1] и Фридман [2] рассказывают историю чесотки у людей и в ветеринарии с библейских времен до начала 1900-х годов. Самое раннее письменное упоминание о кожном заболевании людей и других млекопитающих, которое могло быть чесоткой, встречается в книге Левит в Библии (1200 г. до н.э.) [1]. Согласно Фридману [2], причинно-следственная связь между чесоточным клещом Acarus scabiei (ныне Sarcoptes scabiei ) и заболеванием людей была обнаружена Бономо и Честони в 1687 году, и «это впервые ознаменовало создание история медицины однозначно известной причины любого заболевания человека ».Сегодня чесотка — это забытое, широко распространенное во всем мире заразное кожное заболевание человека и многих домашних и диких млекопитающих, вызывающее значительную заболеваемость и смертность.
Классификация чесоточных клещей
Sarcoptes scabiei первоначально был отнесен к роду Acarus и назван Acarus scabiei DeGeer, 1778. По мере развития номенклатуры клещей изменилась и классификация S. scabiei . Sarcoptes scabiei теперь помещен в надсемейство Sarcoptoidea и семейство Sarcoptidae вместе со многими другими эктопаразитарными клещами млекопитающих.Среди акари S. scabiei принадлежат к надотряду Acariformes, отряду Sarcoptiformes, подотряду Oribatida, Infraorder Desmonomata и группе (гипоотряд) Astigmata (вместе с клещами домашней пыли Dermatophagoides farinae , Dermatophagoides farinae , Dermatophagoides farinae , D. maynei ) [3].
Семейство Sarcoptidae включает три подсемейства (Sarcoptinae, Teinocoptinae и Diabolicoptinae), включая 16 родов и 118 видов, которые все являются обитателями кожи млекопитающих [4, 5].Подсемейство Sarcoptinae включает четыре рода Sarcoptes (1 вид), Prosarcoptes (3 вида), Trixacarus (3 вида) и Kutzerocoptes (1 вид). И Sarcoptes , и Trixacarus caviae выглядят очень похоже, и их можно спутать. Trixacarus caviae является паразитом морских свинок и намного меньше, чем Sarcoptes [6]. Trixacarus caviae может вызывать зудящий дерматит у людей, которые держат зараженных морских свинок или имеют дело с ними [7].Помимо различий в размерах, есть несколько других особенностей, которые легко отличают Sarcoptes от T. caviae . Спинные щетинки у самок T. caviae простые, у S. scabiei конусообразные и шиповидные, а спинные чешуйки у T. caviae более обширны, чем у S. scabiei , и простираются до задняя часть идиосомы [7]. Спинные щетинки sci, l1 и d1 у T. caviae не пластинчатые, как у S.scabiei (рис.1).
Рис. 1Сканирующие электронные микрофотографии самки Sarcoptes scabiei var. hominis ( a ), S. scabiei var. suis ( b ) и S. scabiei var. canis ( c , d ) с дорсальными шипами, грубыми кутикулярными бороздками и внутренними пластинчатыми щетинками лопатки ( sci ), дорсальными щетинками ( d1 ) и спинным щитком (DS). Масштабные линейки : и , 100 мкм; b , 10 мкм; c , 100 мкм; d , 10 мкм
Морфология
Подробные описания S. scabiei со схемами были опубликованы ранее [2, 4,5,6]. Вкратце, S. scabiei имеет овальное черепахоподобное тело (идиосома), которое вентрально плоское и дорсально выпуклое (Рис. 1). Дорсальная идиосома несет толстые боковые ( l ) и дорсальные ( d ) щетинки, кутикулярные шипы и грубые, поперечно ребристые кутикулярные бороздки.Дорсальные щетинки sci, l1 и d1 пластинчатые (рис. 1г).
Все ноги у самок и самцов короткие и короткие (рис. 1, 2). Ноги III и IV у обоих полов не выходят за латерально-задний край идиосомы, в то время как ноги I и II выходят за передний край идиосомы с лапкой, на которой находится стебельчатый эмподиум, который заканчивается подушечкой (рис. 2а). . Ноги IV самцов также несут эмподиум на стебле, который заканчивается подушечкой. Все остальные ноги самцов и самок (III и IV ноги самок и III ноги самцов) оканчиваются длинными щетинками.На всех конечных сегментах ног как самцов, так и самок коготки (рис. 2). На концевых сегментах I, II, III и IV ног самок имеются два шпорцевидных когтя. У самцов два шпорцевидных когтя на ногах I, II и III и по одному на ноге IV.
Рис. 2Электронные микрофотографии самки Sarcoptes scabiei var. канис . a Ноги I и II, показывающие лапку с когтями ( c ) и стебельком эмподиума ( e ), который заканчивается подушечкой. b Ноги III и IV с двумя когтями ( c ) и длинной щетинкой ( s ) на предплюсне. c Гнатазома (педипальпы и хелицеры) и нога I. Масштабные линейки : a , 10 мкм; b , 10 мкм; c , 10 мкм
Гнатосома (capitalum) состоит из коротких толстых хелицер и педипальп (рис. 2c). Анальное отверстие у самок находится сзади / дорсально с сосочком копулятрисы сумки, расположенным кпереди от анального отверстия (рис.3). Средняя сырая и сухая масса самок составляет 5,62 ± 1,25 мкг и 2,8 ± 0,86 мкг соответственно [8]. Самцы намного мельче: влажный вес 1,49 ± 0,59 мкг и сухой вес 0,39 ± 0,16 мкг [8].
Рис. 3Сканирующая электронная микрофотография (вид сзади) самки Sarcoptes scabiei var. canis в норе в роговом слое, показывая дорсальное терминальное анальное отверстие ( a ) и копулятивный сосочек ( cp ) копулятивной сумки. Шкала : 10 мкм
Животные модели для изучения биологии чесоточного клеща
Отсутствие большого количества S.scabiei var. человекоподобных клещей человеческих клещей ограничены обширными исследованиями биологии человеческих клещей чесотки. Иногда для этой цели от пациента с покрытой коркой чесоткой (норвежская чесотка) можно получить большое количество клещей. Таким образом, многие биологические исследования, исследования взаимодействия с хозяином, иммунологические, протеомные и геномные исследования должны опираться на штаммы чесоточных клещей на животных и модели животных-хозяев, таких как кролики или свиньи. Если возможно прямое сравнение, var. canis и var. человекоподобных клещей клещей имеют сходную биологию.
В настоящее время доступны две модели на животных для распространения чесоточного клеща для изучения как клеща, его иммуномодулирующей способности, так и взаимодействия паразит-хозяин, и на них лежит большая часть знаний о чесоточных клещах, полученных за последние 30 лет. Модель чесотки кроликов и собак была разработана много лет назад [9]. Однако неясно, является ли это межвидовой моделью. Вполне может быть модель кролик / кролик. Первоначальным источником чесоточного клеща, использованного для экспериментального заражения кроликов, были бродячие собаки.Но эти собаки могли быть инфицированы от кроликов, на которых собаки охотились в пищу (переход от добычи к хищнику обсуждается в разделе «Переход от одного вида к другому»). Легкость, с которой кролики были заражены клещами, собранными у бродячих собак, предполагает эту возможность, но нет никакого способа узнать происхождение клещей. Другая модель, использованная в более поздних исследованиях, использует клещей свиней (var. suis ) и свиней-хозяев [10].
Жизненный цикл
Стадии развития S.scabiei состоит из яйца, личинки, протонимфы, тритонимфы и взрослой особи. Этот жизненный цикл типичен для других астигматидных клещей. Существует значительная разница в продолжительности жизненного цикла S. scabiei var. человек . Сообщенная продолжительность жизненного цикла чесоточного клеща от человека составляет от 12 до 17 дней [11], от 17 до 21 дня [12], от 7 до 10 дней [13], от 9 до 15 дней [14] и около 15 дней [2]. ]. В исторической опубликованной литературе предполагается, что самки откладывают 40–50 или более яиц в течение 26–40 дней [2].
Систематическое исследование жизненного цикла S. scabiei var. In vivo. canis с использованием модели кролика сообщил, что продолжительность от яйца до взрослой особи составляет от 10 до 13 дней [15]. Личинки выходили из яиц через 50–53 ч инкубации. Продолжительность личиночной стадии составляла около 3-4 дней, тогда как для протонимфальной и тритонимфальной стадий она составляла около 2-3 дней для каждой стадии жизни. Для var. suis свиней [16].
Причины различий в заявленной продолжительности жизненного цикла S. scabiei неизвестны. Вариации, вероятно, связаны с трудностью наблюдения за их развитием в коже in vivo. Различные методы наблюдения, используемые для получения этой информации, различные условия температуры и относительной влажности во время периодов наблюдения, а также наблюдение за чесоточными клещами от разных хозяев могут быть способствующими факторами.
Поиск хоста
Sarcoptes scabiei Клещи ищут источник стимулов, исходящих от хозяина, когда они находятся вне хозяина, но в непосредственной близости от него.Такое поведение может облегчить им поиск хозяина, если они вытеснены из него и загрязняют среду хозяина. Таким образом, прямой контакт с зараженным хозяином может не потребоваться для людей и других млекопитающих, чтобы заразиться S. scabiei . В случае чесотки у человека источником инфекции могут быть живые клещи в постельных принадлежностях, мебели, игрушках и одежде. Sarcoptes scabiei var. человекообразных животных были извлечены из белья для стирки в доме престарелых [17]. Для диких и домашних млекопитающих источником заражения чесоточными клещами могут служить общие или общие места для ночлега, стойла в сараях и загонах.
Эксперименты с вар. canis показали, что самки клещей, размещенные на металлической проволоке (диаметром 1 мм, расположенной перпендикулярно хозяину и касающейся хозяина) на разном расстоянии от хозяина, шли по проволоке к хозяину [18]. Более 68% протестированных самок клещей двигались к хозяину при размещении на расстоянии 4,9 см (1,93 дюйма) от него, в то время как 100% перемещались в этом направлении при размещении на расстоянии 4,2 см (1,65 дюйма). Около 20% тестовых клещей мигрировали к хозяину при размещении 11.На расстоянии 2 см (4,41 дюйма). Таким образом, способность воспринимать и реагировать на хозяина уменьшается с увеличением расстояния от источника. В этих экспериментах стимулом хозяина, который вызывал реакцию, мог быть запах тела и тепло, исходящие от хозяина, и / или CO 2 на выдохе.
Дополнительные эксперименты показали, что клещи будут искать источник теплового стимула без присутствия хозяина [18]. Более 83% самок клещей искали источник тепла на расстоянии 5,6 см (2,2 дюйма).Однако самки одинаково (по 50% на каждый) реагировали как на искусственный тепловой стимул, так и на запах от кожи хозяина, когда им давали возможность выбора из двух одновременно и в непосредственной близости (2,5 см = 1 дюйм) к стимулам. На расстоянии 6,5 см (4,41 дюйма) от обоих стимулов 38% клещей выбрали стимулы от живого хозяина, 5% выбрали искусственный тепловой стимул при 32 ° C и 57% не выбрали ни одного, что предполагает, что запах хозяина был сильнее. аттрактант, чем тепло, когда два стимула предлагались вместе. 57%, которые не ответили ни на один из них, возможно, были сбиты с толку двумя стимулами, на которые они ответили, когда каждый из них предлагался отдельно, а теперь предлагался вместе, но с противоположных сторон.В других экспериментах с двумя вариантами выбора чесоточные клещи выбрали воздух, содержащий запах хозяина, в отсутствие CO 2 , поэтому CO 2 не требуется для индукции ответа.
Mellanby et al. [19] отметили, что S. scabiei var. hominis , помещенный в температурный градиент от 20 ° C до 30 ° C, показал аналогичную термотаксическую реакцию. Sarcoptes scabiei var. hominis , помещенный ниже 24 ° C, переместился в более горячую часть градиента. Клещи не перемещались в районы с температурой ниже 24 ° C.
Эти эксперименты ясно показывают, что чесоточные клещи в окружающей среде рядом с хозяином воспринимают стимулы (запах, температуру тела) от хозяина и будут искать источник.
Фотоответ
Способность обнаруживать свет и его интенсивность могут быть важными факторами наряду с запахом хозяина и теплой температурой тела при обнаружении хозяина клещами Sarcoptes . Фотоответ чесоточных клещей широко не изучался. Sarcoptes scabiei var. hominis Ранее сообщалось, что не реагирует (положительно или отрицательно) на световой раздражитель, хотя никаких данных представлено не было [19].Напротив, S. scabiei var. canis притягивается к люминесцентному потолочному свету в помещении при 63 fc (678 лм / м 2 ) и 100 fc (1076 лм / м 2 ) (Таблица 1). Большинство клещей, появившихся из чешуйчатой корки кожи, мигрировали на свет, а не оставались в темноте на арене наблюдения.
Таблица 1 Распространение Sarcoptes scabiei var. canis на арене выбора света / темноты после выпуска в темнотеВыживание вне хозяина
Контакт с инфицированным хозяином обычно считается основным способом заражения человека чесоткой.Эта идея во многом основана на исследованиях Мелланби [11], который обнаружил, что только 4 человека из 272 протестированных заразились чесоткой после сна в кроватях, используемых сильно инфицированными пациентами. Однако роль фомитов, выживаемость клещей вне хозяина и их инфекционная способность в передаче чесотки никогда широко не исследовались. Способность чесоточных клещей выживать и оставаться заразными вдали от хозяина является ключевым фактором заражения хозяев клещами в окружающей среде.
Штаммы животных S. scabiei являются подходящими моделями для определения выживаемости и сохранения инфекционности клещей в среде хозяина. Исследование Arlian et al. [20] обнаружили, что S. scabiei var. canis самок выживали в течение недели или более при температуре 15 ° C (59 ° F) и относительной влажности (RH) выше 75% (рис. 4). При более высокой температуре 25 ° C (77 ° F) самки выживали 1-2 дня при всех тестируемых RH (рис. 4). Время выживания самцов вне хозяина было намного короче, чем у самок.Эти исследования показали, что обычно более высокие температуры резко сокращают время выживания при каждой влажности. В этом исследовании клещи явно умерли от обезвоживания из-за своей неспособности поддерживать водный баланс (вопрос будет рассмотрен позже). Более высокая относительная влажность и температура ниже 20 ° C позволили увеличить время выживания.
Рис. 4Наблюдаемое время для достижения 100% смертности в тестовых популяциях самок S. scabiei var. canis клещей подвергаются воздействию определенных комбинаций температуры и относительной влажности (RH).Количество клещей в каждой тестовой группе колебалось от 8 до 26. Данные из [20]
С другой стороны, S. scabiei var. hominis голодные самки клещей могут выжить 19 дней при 10 ° C и относительной влажности 97% и 8 дней при 10 ° C и 25% относительной влажности [20]. Sarcoptes scabiei var. hominis , которых держали вдали от хозяина с чередующимися 12-часовыми периодами 4 ° C или 10 ° C и 95% относительной влажности и комнатных условиях (21 ° C и 45% RH) в течение 4 дней, оставались заразными и все еще могли проникать через кожу кролика [20].
Замораживание может помочь убить чесоточного клеща в таких предметах, как мягкие и твердые игрушки, маленькие подушки и постельные принадлежности. Замораживание женское вар. canis клещей при -25 ° C и относительной влажности 50% в течение 1,5 ч привели к 100% гибели. После 1 часа замораживания 23% тестовых клещей выжили, но они не начали проникать, когда их поместили обратно на кожу хозяина [20]. Неизвестно, как долго эти клещи могут выжить при температуре от -15 ° C до -17 ° C, температуре обычной домашней морозильной камеры.
Mellanby et al.[19] определили точку термической смерти S. scabiei var. hominis самок, подвергшихся воздействию различных температур в течение 10 и 30 минут при относительной влажности 0–90%. Летальные температуры составляли 49 ° C (120 ° F) за 10 минут и 47,5 ° C (117,5 ° F) за 30 минут. После извлечения из организма-хозяина они обнаружили, что выживаемость составила 84,7, 30,5, 6,8, 1,7 и 0% в течение 1, 2, 3, 4 и 5 дней воздействия соответственно при 21,0–25,5 ° C и относительной влажности 90%. Выживаемость при 24–25 ° C и относительной влажности 30% составила 63,5, 6,8 и 0% через 1, 2 и 3 дня воздействия соответственно.Однако 61, 52, 35, 30 и 26% клещей выжили 5, 6, 7, 9 и 11 дней, соответственно, при относительной влажности 90%, но немногие клещи выжили 14 дней. Напротив, только 4 и 2% клещей выжили 2 и 4 дня соответственно при 30% относительной влажности. Таким образом, высокая относительная влажность и низкая температура также продлевают вар. hominis выживаемость клещей вне хозяина. Клещи действительно проявляли некоторую способность выдерживать отрицательные температуры. Все тестовые клещи выжили 2 дня при 0 ° C, а 28,6% выжили 8 дней.
Инфекционность
Важным аспектом передачи через окружающую среду (фомита) является то, как долго клещи остаются заразными, когда они находятся вне хозяина.Как упоминалось ранее, время выживания вне организма-хозяина напрямую связано с относительной влажностью и температурой окружающей среды. Исследования с использованием кролика-хозяина и S. scabiei var. Штамм canis обнаружил, что большинство клещей, удерживаемых от хозяина в течение 24 часов, инициируют проникновение через кожу очень скоро после того, как их снова поместят на кожу хозяина [20]. Они стали наполовину или полностью погружены во вновь образовавшуюся нору в течение часа. Женский var. Клещи canis начинают проникать примерно через 20 минут, в то время как самцы, нимфы и личинки зарываются менее чем через 5 минут после того, как их помещают на кожу.Восемьдесят процентов самок, которых держали вдали от хозяина в течение 36 часов при 75% относительной влажности и 22 ° C, могли полностью проникнуть через кожу хозяина в среднем за 97 минут. Как отмечалось ранее, самки, которых держали вдали от хозяина в течение 24 часов, проникли через кожу за гораздо меньшее время, в то время как ни один клещ не выжил через 48 часов при 75% относительной влажности и 22 ° C. Для сравнения: живые чесоточные клещи человека (разновидность hominis ), полученные из постельного белья, в котором спали пациенты, сильно инфицированные чесоткой, могли инициировать проникновение через кожу в течение 10 минут после помещения на кролика и полностью проникнуть в течение 31 минуты [20]. .
Таким образом, в домах, школах и домах престарелых не следует требовать тщательной очистки, дезинфекции и стирки для уничтожения клещей чесотки в сухом климате. Если оставить кровать, спальню, постельное белье и одежду изолированными на 48 часов при комнатной температуре, чесоточные клещи погибнут. В сухом климате (<50% относительной влажности) клещи, вероятно, выживают и остаются заразными менее 36 часов.
Проникновение через кожу хозяина
Когда чесоточные клещи заражают хозяина, они сначала должны проникнуть через роговой слой эпидермиса кожи.Наблюдать за этим процессом под микроскопом — утомительная задача. Однако на всех стадиях жизни как S. scabiei, var. canis и S. scabiei var. hominis экспериментально наблюдались под микроскопом, когда они проникали через кожу хозяина [20]. Клещи, помещенные на кожу, выделяют прозрачную жидкость (предположительно слюну), которая образует лужу вокруг их тела. Похоже, что роговой слой растворяется (лизируется), и клещ погружается в углубление на коже.Когда он тонет, ноги I и II, кажется, двигаются как черепаха (рытье, ползать / плыть). Действие ног продвигает клеща вперед, так как образуется туннель-нора в роговом слое. Время, чтобы полностью погрузиться в роговой слой, удивительно мало, как описано выше.
Водный баланс
Свежие тела самок и самцов S. scabiei var. canis содержат 57 ± 12% и 69 ± 18% воды по массе соответственно [8]. Получение межклеточной жидкости хозяина, по-видимому, необходимо клещам для получения достаточного количества воды для поддержания своего водного баланса [8].Некоторые виды клещей и клещей обладают способностью поддерживать водный баланс без попадания внутрь воды за счет поглощения воды из ненасыщенного окружающего воздуха, когда относительная влажность превышает критический уровень [21]. Например, родственные клещи домашней пыли, D. farinae и D. pteronyssinus , обладают активным механизмом извлечения воды из ненасыщенного воздуха с относительной влажностью выше примерно 70% для восполнения всей воды, которая теряется при испарении, секреции и другие процессы в организме (выделение и дефекация) [22, 23].Обезвоженные клещи домашней пыли и клещи набирают воду и, следовательно, массу тела при помещении во влажный воздух с влажностью выше критического уровня. Чесоточные клещи, по-видимому, неспособны активно поглощать достаточное количество воды из ненасыщенного воздуха на поверхности кожи или в норе, чтобы поддерживать водный баланс, и при обезвоживании не могут восстановить потерянную воду из почти насыщенного воздуха (Таблица 2). Чесоточные клещи теряют воду в организме и обезвоживаются, когда их держат вдали от хозяина при относительной влажности 97,5% [8]. Таким образом, в отличие от клещей домашней пыли, чесоточные клещи не могут поглощать водяной пар из ненасыщенного окружающего воздуха, чтобы удовлетворить свои потребности в воде.Самки теряют 30–34% массы воды своего тела при выдерживании в течение 16 часов при 97,5% относительной влажности. Таким образом, они должны глотать / впитывать от хозяина воду, необходимую для поддержания водного баланса.
Таблица 2 Вес самок Sarcoptes scabiei var. canis сразу после извлечения из хозяина (в сыром виде) и их вес после удерживания вне хозяина при 97,5% относительной влажности в течение 16 часов для трех групп клещейСкорость метаболизма (потребность в кислороде) чесоточных клещей была определена с использованием декартовой дайверской техники и недостаточна для обеспечения чесоточного клеща значительным количеством метаболической воды [8].
Обеспечение питанием
Чесотные клещи обитают в норах, которые они делают в неживом роговом слое эпидермиса кожи млекопитающих. Когда-то считалось, что эти клещи питаются лизированным роговым слоем. Однако последующие исследования показали, что клещи поглощают межклеточную жидкость (лимфу), которая просачивается в норку вокруг ротового аппарата клеща, когда они зарываются глубоко в роговой слой рядом с живой тканью (клетками) нижнего эпидермиса. Это подтверждают несколько линий доказательств.Как сканирующая электронная микроскопия, так и световая микроскопия показывают, что клещи в роговом слое кожи обитают на границе между прозрачным слоем и зернистым слоем [24,25,26], где межклеточная жидкость находится близко к месту расположения клеща и может проникать в нору. Клещи, по-видимому, зарываются вниз по направлению к дерме, чтобы сохранить это место, поскольку базальный слой клеток разрастается, а верхний слой сухого рогового слоя подталкивается к поверхности кожи. Демонстрация присутствия антител IgG хозяина в пищеводе и средней кишке свежих чесоточных клещей, удаленных от хозяина, является доказательством того, что эти клещи глотают сыворотку хозяина [27].Они, по-видимому, неспособны переваривать IgG и обладают относительно ограниченным набором ферментативной активности, что соответствует сывороточной диете [28].
Чесоточные клещи являются аэробными. Самки и самцы используют 0,00206 мкл O 2 / ч / клеща и 0,00076 мкл O 2 / ч / клеща, соответственно [8]. Экстраполируя это и используя кроличьего модельного хозяина, у которого инфицировано 30% площади поверхности тела, было установлено, что энергетические потребности клещей у хозяина незначительны, даже несмотря на то, что эти клещи получают все свое питание от хозяина.
Расположение чесоточных клещей на теле хозяина
Инфекции чесоточного клеща человека обычно локализуются в определенных частях тела. Руки, запястья и локти являются наиболее часто инфицированными участками у взрослых пациентов [11]. Однако гениталии, ступни, ягодицы, подмышечные впадины, грудь и талия также являются предпочтительными местами инфицирования [11].
Неизвестно, почему одни участки тела заражаются чаще, чем другие. Инфекции рук и запястий могут быть просто результатом прикосновения к инфицированным людям и работы с материалами, зараженными клещами.Однако характер распределения позволяет предположить, что клещи выбирают предпочтительные участки, и эти участки могут быть предпочтительны отчасти из-за липидного состава и других специфичных для участка факторов кожи на этих участках.
Arlian & Vyszenski-Moher [29] оценили реакцию на всех стадиях жизни S. scabiei var. canis до нескольких концентраций 21 липидного соединения, которые обычно обнаруживаются в эпидермисе кожи человека или на нем. Они обнаружили, что ряд этих липидов привлекает чесоточных клещей, включая 13 жирных кислот, 5 метиловых эфиров жирных кислот, холестерин, сквален и трипальмитин.Молярная концентрация, вызывающая наибольший отклик, варьировалась в зависимости от соединения. Сравнение различных стадий жизни показало, что реакция на стадиях жизни зависит от соединения и молярной концентрации этого конкретного соединения. В некоторых случаях одна стадия жизни реагировала на концентрацию соединения, а другая — нет. В целом, женщины были наиболее отзывчивыми.
Липидное содержание и липидные смеси кожи различаются в разных анатомических областях тела. Следовательно, трудно понять значение реакции чесоточного клеща на различные молярные концентрации этих изолированных липидных соединений.Пристрастие клещей к определенным участкам тела не изучено, но, вероятно, связано с взаимодействием множества факторов на коже и на коже. Исследование ясно продемонстрировало, что чесоточных клещей привлекали многие из липидов кожи, которые были протестированы, и поэтому липиды могут участвовать в привлечении клещей к предпочтительным участкам тела.
Агрегация, пол и феромоны сборки
Было замечено, что чесоточные клещи на всех стадиях жизни покидают свои норы и блуждают по коже.Даже при небольшом количестве клещей на хозяине самцы и самки находят друг друга и спариваются. Вероятно, в этих процессах участвуют феромоны, выделяемые клещами. Было показано, что гуанин, другие пуриновые соединения и другие азотистые отходы паукообразных и фенольные соединения являются феромонами сборки-притяжения-прикрепления или половыми феромонами у клещей и клещей [30,31,32,33,34]. Другие акари, такие как S. scabiei , вероятно, продуцируют аналогичные соединения и реагируют на них. В исследовании Arlian & Vyszenski-Moher [35] 10 азотистых метаболитов и 3 фенольных соединения были предложены отдельно для всех стадий жизни S.scabiei var. канис. Гуанин, пурин, аденин, аллантоин, гипоксантин, ксантин, мочевая кислота, хлорид аммония, нитрат аммония и сульфат аммония привлекли значительное количество клещей чесотки. Все этапы жизни также были значительно привлечены тремя тестируемыми фенольными соединениями. К ним относятся 2,6-дихлорфенол, метилсалицилат и 2-нитрофенол. Самки ответили на большинство концентраций различных соединений, а мужчины — на наименьшее.Похоже, что азотистые и фенольные соединения могут действовать как феромоны для чесоточных клещей, как и для других акари.
Взаимодействие между хозяином и паразитом (иммунная модуляция)
По мере того, как чесоточные клещи проникают в кожу, они выделяют вещества, которые вызывают воспалительные и иммунные реакции хозяина, а также вещества, которые могут подавлять определенные аспекты этих реакций, позволяя клещам обходить защитные механизмы хозяина. Последний помогает клещам изначально выжить в коже хозяина и создать популяцию.На границе раздела клещ-кожа происходит сложное взаимодействие, которое определяет баланс между двумя конкурирующими процессами с течением времени и, следовательно, течение инфекции и возможное проявление клинических симптомов. Поскольку кожные симптомы не проявляются в течение четырех или более недель при первичной инфекции, похоже, что на ранней стадии первичной инфекции врожденные / иммунные события подавляются, но со временем, по мере размножения клещей и создания популяции, происходит переход к проявляются более доминирующие воспалительные и иммунные реакции и симптомы заболевания.Что является причиной сдвига, неизвестно, но неоспоримые доказательства того, что чесоточные клещи, как и многие другие паразиты, могут модулировать различные аспекты врожденных и адаптивных иммунных ответов млекопитающих. Выявленные иммуномодулирующие способности клещей включают противовоспалительную, противоиммунную активность и активность против комплемента.
Из-за того, что клещ находится на границе раздела межклеточной жидкости в эпидермисе, растворимые вещества (включая слюну, ферменты и гормоны линьки, фекалии и азотистые выделения) от клещей, обладающие антигенной и фармакологической активностью, диффундируют в жидкость, омывающую клетки эпидермис и дерма.Эти вещества вызывают ответы клеток в этих тканях, включая кератиноциты, фибробласты, макрофаги, тучные клетки, лимфоциты, клетки Лангерганса и другие дендритные клетки, а также эндотелиальные клетки микрососудов.
Исследования in vitro показывают, что молекулы S. scabiei var. canis стимулировал культивированные нормальные эпидермальные кератиноциты человека для значительного увеличения секреции интерлейкина-6 (IL-6) и фактора роста эндотелия сосудов (VEGF), а также для незначительного увеличения секреции фактора стимуляции колоний гранулоцитов (G-CSF) [36].Никакого влияния на секрецию IL-1α и IL-1β не наблюдалось. Кроме того, экстракт чесоточного клеща вызывал снижение секреции агониста рецептора IL-1 (IL-1ra) и IL-8 этими клетками после того, как они были стимулированы липополисахаридом (LPS). Аналогичным образом, вещества в этом экстракте стимулировали культивированные нормальные дермальные фибробласты человека для увеличения секреции IL-6, IL-8, G-CSF и VEGF. В коже коллективная повышающая регуляция IL-6 и VEGF, сопровождаемая понижающей регуляцией IL-1ra, будет способствовать воспалению (хотя IL-6 может иметь как провоспалительную, так и противовоспалительную функции).VEGF способствует увеличению проницаемости сосудов, что принесет пользу клещу, предоставив ему больше питательной сыворотки, которую он может проглотить.
Последующее исследование показало, что S. scabiei var. canis экстракт в присутствии провоспалительных цитокинов (IL-1α, IL-1β и фактор некроза опухоли α [TNFα]) вместе с IL-17, которые, вероятно, присутствуют в скабиетических поражениях in vivo , все еще подавлены Уровни ИЛ-8 в супернатантах как эпидермальных кератиноцитов человека, так и дермальных фибробластов через 8 ч, но этот эффект со временем исчез [37].Секреция гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) фибробластами также уменьшалась. Это исследование также показало, что молекулы экстракта чесоточного клеща индуцируют секрецию связанного с ростом онкогена-α (GROα), трансформирующего фактора роста-α (TGFα) и кожного хемокина, привлекающего Т-клетки (CTACK) из кератиноцитов, и подтвердили усиленную секрецию ИЛ-6 и Г-КСФ из фибробластов. Сдвиг уровней IL-8 в супернатантах, вероятно, связан с присутствием в экстракте клещей двух разных молекул: одной, которая стимулирует выработку IL-8, а другой связывается с IL-8 по мере его производства [37].Известно, что клещи продуцируют белок, связывающий IL-8 (Evasin-3), который избирательно связывает и нейтрализует IL-8, подавляя рекрутирование нейтрофилов в место инвазии паразитов [38,39,40].
В живой коже кератиноциты, фибробласты и эндотелиальные клетки микрососудов взаимодействуют друг с другом в коллагеновой матрице и взаимодействуют с помощью цитокинов, хемокинов и контакта. Эти взаимодействия могут влиять на реакцию отдельных типов клеток на экстракт чесоточного клеща. Кроме того, живые клещи могут выделять вещества, которые количественно и качественно отличаются от компонентов экстракта всего тела.Таким образом, для моделирования реальной кожи эквиваленты кожи человека (HSE) были заражены S. scabiei var. canis и живыми клещами [41]. Модель HSE состоит из дермы фибробластов в коллагеновой матрице, расположенной ниже эпидермиса, состоящей из слоя многослойных кератиноцитов. Модель HSE допускает взаимодействие фибробластов и кератиноцитов, которое происходит in vivo при стимуляции чесоточными клещами и их продуктами, что невозможно наблюдать в экспериментах по монокультуре клеток.Живые клещи проникают в роговой слой этих эквивалентов кожи точно так же, как они делают это в неповрежденной коже хозяина [41]. Роющие клещи индуцировали секрецию CTACK, стромального лимфопоэтина тимуса (TSLP), IL-1α, IL-1β, IL-1ra, IL-6, IL-8, моноцитарного хемоаттрактантного белка-1 (MCP-1), GM-CSF, и фактор, стимулирующий колонии макрофагов (M-CSF), на поверхность HSE. Основное различие между ответом на экстракт клещей монокультурных кератиноцитов и фибробластов заключалось в том, что HSE продуцировал значительные количества провоспалительных цитокинов IL-1α и IL-1β и их ингибитора IL-1ra в ответ на роющих клещей.Повышенная регуляция IL-1ra может быть важной частью механизма, используемого этими клещами для подавления воспалительной реакции хозяина, позволяя создать популяцию клещей.
Исследования экспрессии генов в HSE также подтвердили и расширили результаты экспериментов по монокультуре in vitro. Чесоточные клещи, зарывающиеся в HSE, индуцировали повышенную экспрессию 189 генов и подавляли экспрессию 152 генов в кератиноцитах и фибробластах в этих HSE [42].Гены ряда цитокинов были активированы, что соответствовало профилям секреции цитокинов, описанным выше [41]. Особо следует отметить повышенную активность IL-20. Этот цитокин способствует пролиферации кератиноцитов, и его повышенная регуляция может способствовать развитию чешуйчатой и покрытой коркой кожи, что характерно для хронической чесотки. Кроме того, наиболее активным был ген кератина 1 типа, преобладающего структурного белка в кератиноцитах. Многие другие гены подавлялись, когда клещи зарывались в HSE, включая несколько членов семейства цитохрома p450.Отсылаем читателя к [42], чтобы ознакомиться с полным списком генов, которые дифференциально экспрессировались в ответ на закапывание в норы клещей S. scabiei в модели HSE.
Культивированные эндотелиальные клетки кожных микрососудов человека кожи, стимулированные S. scabiei var. canis Экстракт снижает индуцированную TNFα экспрессию молекул клеточной адгезии E-селектина и молекулы адгезии сосудистых клеток-1 (VCAM-1), а также уровни IL-8, в то же время повышая экспрессию цитокинового рецептора CXCR-1 [ 43].Последующее исследование подтвердило, что экстракт чесоточного клеща все еще способен снижать TNFα-индуцированную экспрессию VCAM-1 в присутствии некоторых провоспалительных медиаторов (например, гистамина, лейкотриена B4 и цитокинов IL-1), которые могут возникать при чесоточных поражениях in vivo [44]. . Вызванная IL-1α и IL-1β секреция IL-6 также снижалась в присутствии экстракта чесоточного клеща.
Исследования in vitro показывают, что мононуклеарные клетки периферической крови (PBMC, в основном моноциты) от здоровых доноров-людей, стимулированные S.scabiei var. Экстракт canis активирует секрецию IL-1β, IL-6, IL-8 и TNFα [45]. Дендритные клетки, полученные из этих моноцитов, подавляли секрецию IL-6 и IL-8 после того, как они были стимулированы LPS для индукции секреции этих цитокинов [45]. Аналогичным образом Walton et al. [46] обнаружили, что PBMC от пациентов с обычной чесоткой продуцируют более высокие уровни IL-5 и IL-13 и более низкие уровни гамма-интерферона (IFNγ) при стимуляции рекомбинантной цистеиновой протеазой человека Yv5032C08.PBMC от пациентов с обычной чесоткой или чесоткой с коркой также показали сильный пролиферативный ответ при стимуляции этой молекулой.
В другом исследовании смешанные популяции лимфоцитов и моноцитов от здоровых доноров (с предшествующей сенсибилизацией к чесотке и без нее) стимулировали S. scabiei var. canis экстракт [47]. У всех доноров наблюдалась повышенная секреция IL-10 и IFNγ в ответ на стимуляцию экстрактом чесотки. Отсутствие продукции IL-2 или IL-4 предполагает, что регуляторные Т-клетки (Treg) ответственны за создание этого цитокинового профиля.Аналогичным образом, PBMC от людей, не подвергавшихся воздействию чесотки, вырабатывали повышенный уровень IL-10 при стимуляции цистеиновой протеазой Yv5032C08 [46]. Повышенная регуляция продукции IL-10 является значительной, поскольку этот цитокин подавляет воспалительные и иммунные реакции у людей и, таким образом, может способствовать отсроченному проявлению клинических симптомов, характерных для ранних инфекций чесотки.
Проникая в нижний эпидермис кожи, чесоточные клещи поглощают плазму хозяина, которая содержит антитела хозяина [27] и другие компоненты плазмы, включая сериновые протеазы, комплемент и другие ферменты, которые могут повредить слизистую оболочку кишечника клеща, которая имеет решающее значение для переваривание и усвоение питательных веществ.Кишечник клещей секретирует, помимо прочего, каталитически неактивные паралоги сериновых протеаз (SMIPP) [48, 49]. SMIPPs могут ингибировать активность комплемента, связывая C1q, маннозу-связывающий лектин и пропердин в трех путях комплемента, и, таким образом, они защищают слизистую оболочку кишечника клеща от атаки комплемента и повреждения [48,49,50]. Кроме того, ингибиторы сериновых протеаз (серпины), также называемые SMS (от чесоточных серпинов клещей), локализуются в кишечнике и кале клеща [51]. Два рекомбинантных серпина, SMS B3 и SMS B4, могут неэффективно ингибировать сериновые протеазы млекопитающих, но не сериновые или цистеиновые протеазы клещей.Mika et al. [51] показали, что эти серпины клещей могут связываться с несколькими белками плазмы в классической, альтернативной и лектиновой системах комплемента человека, а также, возможно, блокировать или снижать эффективность всех трех систем комплемента. Следовательно, эти клещи развили множество молекул, позволяющих им защищаться от защитных механизмов комплемента хозяина.
Вторичные бактериальные инфекции часто развиваются при чесоточных поражениях и сопровождают чесоточную инфекцию [52,53,54].Ингибиторы комплемента SMIPP и SMS в кале клещей могут способствовать выживанию и росту бактерий на коже хозяина [52, 53]. Клещи откладывают фекальные шарики в норе позади себя, когда кормятся, и удлиняют нору. Таким образом, выделенные фекальные гранулы, содержащие SMIPP и SMS, которые откладываются на коже, могут ингибировать активность комплемента хозяина в коже / плазме, окружающей клещей, а также ингибировать атаку комплемента на бактерии в поражении и, таким образом, способствовать колонизации бактерий, которые часто сопровождает хроническую чесотку.
В совокупности все эти сложные взаимодействия, вероятно, задерживают иммунный и воспалительный ответ на ранней стадии инфекции, пока создается популяция клещей. Эта задержка в конечном итоге отменяется, когда популяция клещей достигает порогового значения и возникает воспалительная реакция.
Ответ клеток первичной лимфоидной ткани хозяина на молекулы чесотки
Исследования на мышах показывают, что экспрессия мРНК молекулы межклеточной адгезии-1 (ICAM-1), ICAM-2, VCAM-1 и L-селектина и Рецепторы TNF I и II (TNF RI и TNF RII) в ткани селезенки были снижены у мышей, подвергшихся воздействию живых S.scabiei var. canis (первичный ответ) [55]. Напротив, мышей, сначала иммунизированных S. scabiei var. canis , а затем воздействие живых чесоточных клещей (вторичный ответ) действительно увеличивало экспрессию генов для ICAM-1, ICAM-2, TNF RI и RII. Это говорит о том, что иммунизация соответствующими антигенами чесоточного клеща будет полезна для снижения способности клещей подавлять иммунный ответ и, таким образом, может помочь защитить от чесотки.
Кроме того, экспрессия мРНК B- и T-клетками селезенки мышей, подвергшихся воздействию живых чесоточных клещей, демонстрировала пониженную экспрессию B7–2 / CD86, CD4, CD8 и CD45 [55].Эти мембранные молекулы играют ключевую роль во взаимодействии В-клеток и клеток-помощников Th3, а также между клетками-помощниками Th2 и цитотоксическими Т-клетками в иммунной реакции, и предполагает, что чесоточные клещи производят что-то, что может подавлять иммунную реакцию в лимфоидной ткани.
Профиль Т-хелперов спленоцитов и лимфатических узлов также определялся у мышей [56]. У мышей, подвергшихся воздействию живых чесоточных клещей, увеличивалась продукция IL-4 клетками лимфатических узлов и IFNγ спленоцитами. Напротив, мыши, иммунизированные экстрактом клещей до заражения, изменяли ответ клеток лимфатических узлов с ответа Th3 (IL-4) на ответ Th2 (INFγ).
Геномика чесоточного клеща
Развитие молекулярных методов открыло новые возможности для исследований, позволяющих понять биологию чесоточных клещей и взаимодействия между клещами и их хозяевами. Геномы S. scabiei var. canis [57], var. hominis [58, 59] и var. suis [58, 59] в настоящее время секвенированы, и эти данные доступны для использования в качестве инструментов для выяснения филогенетических отношений и предпочтения хозяев чесоточных клещей, паразитирующих на различных млекопитающих, идентификации белков, участвующих в модуляции защитных реакций хозяина, и идентификации генов, кодирующих для белков, которые являются антигенными и могут быть кандидатами для включения в вакцину или диагностический анализ крови.
Аннотированный S. scabiei var. canis. Проект генома был получен и доступен в базах данных NCBI и VectorBase [57], в то время как var. hominis и var. suis геномные данные доступны в репозиториях NCBI и GigaScience [58, 59]. В целом геномы трех штаммов очень похожи. Вариант var. canis Геном содержал гены для 10 644 предсказанных белков [57], в то время как var. Геном hominis содержал 13 226 предполагаемых кодирующих последовательностей [58].Для сравнения: оба генома чесоточного клеща имеют меньше генов, чем прогнозировалось для четырех других акари с аннотированными геномами на сегодняшний день. Пылевой клещ Dermatophagoides farinae содержит 16 376 предсказанных белков, в то время как паутинный клещ Tetranychus urticae — 18 423, оленный клещ Ixodes scapularis — 20 474, а мезостигматидный клещ Metasei,63,61,61 Occidentalis. ]. S. scabiei var. canis Геном содержит 3351 предсказанный белок, которые не являются ортологами белков, присутствующих в других клещах [57].Это важно, потому что смешивающим фактором при идентификации белков, которые необходимо включить в вакцину или использовать в анализе крови для точного выявления инфекции чесотки, является перекрестная реактивность между многими белками чесоточного клеща и повсеместно распространенными антигенами пылевого клеща.
Используя предсказанный протеом, можно было окончательно идентифицировать> 150 белков, присутствующих в водорастворимых и нерастворимых экстрактах целых тел клещей, с помощью масс-спектрометрии MALDI-TOF / TOF [64]. Многие из этих белков распознаются IgM и / или IgG в сыворотке крови пациентов с обычной чесоткой и могут быть кандидатами для включения в диагностический тест для этого заболевания.Другие не связывают циркулирующие антитела и могут участвовать в модуляции иммунной защиты хозяина для защиты клеща.
Геном также был исследован для идентификации предсказанных белков, которые могут быть связаны с взаимодействиями чесоточного клеща и хозяина и с выбранными важными биологическими процессами [65].
Генетическое разнообразие чесоточных клещей
Одно из первых молекулярно-биологических исследований S. scabiei выявило микросателлиты множественных нуклеотидных последовательностей в частичной геномной библиотеке S.scabiei var . hominis [66]. Среди них повторы динуклеотидного GA (гуанин-аденин) были относительно многочисленными с длиной повтора до 20. Было высказано предположение, что выбранные микросателлитные паттерны могут быть использованы для дифференциации между различными популяциями клещей.
Использование описанного выше метода ДНК-фингерпринта на чесоточных клещах от людей и собак дало некоторые интересные выводы о генетической изменчивости S. scabiei как внутри, так и между видами хозяев [67].Было обнаружено, что паттерны микросателлитных нуклеотидных повторов у клещей, собранных у людей в северной Австралии и в Панаме, значительно отличаются от ДНК, выделенной из клещей, собранных у собак (некоторые из тех же мест), что позволяет предположить, что два штамма клещей имеют разные циклы передачи, даже для инфицированные люди и собаки, живущие в одном доме. Таким образом, чесоточные клещи от собак вряд ли являются источником стойких инфекций чесотки у людей, по крайней мере, в северо-западной Австралии.Сравнивая чесоточных клещей от собак в сообществе, они обнаружили, что могут быть значительные генотипические различия, а могут и не быть. Последние данные свидетельствуют о наличии значительных субпопуляций S. scabiei у собак. Когда они сравнили различные человеческие изоляты, обнаружилась также значительная генетическая изменчивость между чесоточными клещами из разных домохозяйств в пределах сообществ в Австралии, но небольшая генетическая дифференциация между чесоточными клещами от людей в одном доме. Последнее открытие указывает на общий источник чесоточного клеща для инфицированных людей, живущих в одном доме.Аналогичным образом, генетические различия существовали между чесоточными клещами от людей в сообществах в Австралии и чесоточными клещами от людей в Панаме. Взятые вместе, эти данные свидетельствуют о наличии субпопуляций чесоточных клещей в пределах одного вида-хозяина, и это повышает вероятность появления нескольких видов чесоточных клещей у людей и других популяций хозяев. Эта концепция была недавно подтверждена исследованиями в Китае, предполагающими, что существует множество различных штаммов (видов) чесоточных клещей, паразитирующих на людях [68].На основании гена субъединицы 1 митохондриальной цитохрома c оксидазы (мтДНК cox 1), Sarcoptes от людей в Австралии, Панаме и двух популяциях в Китае, как сообщается, представляют 4 различных вида из Sarcoptes [68] .
Исследования по анализу второй внутренней транскрибированной спейсерной ДНК рибосом (рДНК ITS2) и митрохрондриальной 16S ДНК (мтДНК 16S) не обнаружили межвидовых различий между клещами Sarcoptes , собранными от разных видов хозяев [69,70,71,72].Однако другие исследования, в которых анализировались мтДНК 16S и мтДНК cox 1 и рДНК ITS2 чесоточных клещей от разных животных-хозяев, обнаружили, что они обнаруживают различия [73, 74]. Аналогичный анализ Zhao et al. [68] идентифицировали чесоточных клещей от людей и чесоточных клещей от собак в Китае как отдельные популяции Sarcoptes , но люди могли быть инфицированы Sarcoptes от собак [68]. Однако они также пришли к выводу, что на основе гена мтДНК cox 1 длиной 317 п.о. чесоточные клещи буйволов, кроликов, овец, вомбатов, валлаби, свиней, шимпанзе и собак принадлежат к одному и тому же виду и что чесоточные клещи от людей являются отдельный вид от вида животных [68].
Аналогично, Andriantsoanirina et al. [75] путем анализа митрохондриального гена, кодирующего 12S-рРНК клещей от разных хозяев, пришел к выводу, что клещи от вомбатов, собак и людей не отличаются филогенетически и что чесотка у вомбатов в Австралии, вероятно, произошла от людей и / или их животных. Это контрастирует с более ранним исследованием, которое показало, что клещи, собранные у вомбатов, не группируются с клещами, полученными у людей или собак [67].
Другое исследование с использованием cox 1 этой же группы [76] также показало, что чесоточные клещи человека не составляют единую гомогенную популяцию.Кроме того, используя полиморфизмы гена cox 1 клещей от людей во Франции, собак и данные из GenBank, они пришли к выводу, что чесоточные клещи от людей были распределены по трем генетически различным и изолированным кладам (A, B и C) и что собака и человек клещи генетически не отличались. Кроме того, Clade C содержал клещей чесотки от людей и 12 других видов хозяев (собаки, кролики, шимпанзе, свиньи, овцы, водяные буйволы, крупный рогатый скот, вомбат, валлаби, енотовидные собаки, серы и куницы), и этот поток генов происходит между клещами из разных видов. хосты.
Исследование Mofiz et al. [59] сообщили, что последовательности митохондриального генома клещей, собранные у людей, свиней и собак, очень похожи. Затем они идентифицировали однонуклеотидные полиморфизмы (SNP), которые были использованы для обнаружения шести гаплотипов среди var. hominis и var. suis образцов. Данные показали, что клещи от одного пациента-человека выглядели по существу клональными, в то время как клещи, собранные от другого пациента, демонстрировали сильно расходящиеся гаплотипы, в том числе те, которые сгруппировались с гаплотипами, присутствующими у клещей от свиней.
Исследования с использованием микросателлитной ДНК для изучения генетического разнообразия между симпатрическими и несимпатрическими хозяевами и их паразитами чесоточного клеща предоставили некоторую дополнительную интересную косвенную информацию о специфичности хозяина и генетическом разнообразии [74, 77,78,79]. Как правило, микросателлитный анализ предполагает, что существует только один сильно изменчивый вид S. scabiei [74, 77,78,79]. Тем не менее, микросателлитное генотипирование отдельных клещей S. scabiei , собранных в трех европейских странах из 15 популяций диких млекопитающих, принадлежащих к 10 видам хозяев, сгруппированных в 3 группы (производные от таксона-хозяина): полученные от травоядных, полученные от плотоядных и всеядные. [80].Как правило, результаты микросателлитного анализа показывают отсутствие потока генов между этими группами, но поток генов может происходить внутри группы. Однако виды млекопитающих, не страдающие чесоткой, могут жить в той же географической области, что и паршивые животные, поэтому физиологические, иммунные защиты и другие свойства хозяина предотвращают передачу и колонизацию между различными симпатрическими потенциальными видами хозяев.
Возможно, что генетический состав (наличие и частота аллелей) штамма чесотки может изменяться (дрейфовать) с течением времени.Alasaad et al. [78] с использованием одного мультиплекса из 9 микросателлитных локусов дополнительно исследовали временное генетическое разнообразие в популяциях клещей за 11 лет и обнаружили незначительные изменения в генетическом разнообразии S. scabiei среди симпатрических популяций диких млекопитающих с S. scabiei в популяциях. из пиренейской серны в Астурии (Испания) благородный олень, косуля и рыжая лисица.
Неясно, насколько специфичен для хозяина S. scabiei , собранный от разных млекопитающих-хозяев, и существует ли несколько видов Sarcoptes как внутри, так и между видами хозяев.Исследования кроссбридинга невозможны, а исследования перекрестной инфекционности очень ограничены. Результаты молекулярных исследований дают некоторое интересное понимание этого вопроса, но также не дают однозначных ответов, поскольку в этих исследованиях использовались различные ядерные, рибосомные и митохондриальные гены.
Межвидовые передачи между хозяевами
Клещи от собак, инфицированных чесоткой, могут вызывать постоянные инфекции у домашних кроликов, и эти клещи могут повторно заражать собак [9]. Это говорит о том, что бродячие / выездные домашние собаки и дикие собаки, которые охотятся на диких кроликов с чесоткой, могут заразиться чесоткой от этих хозяев, и, таким образом, чесотка является перекрестной инфекцией между некоторыми видами собак и кроликами-хозяевами.Точно так же было показано, что дикая серна с чесоткой заражает домашних коз, и наоборот, а красные лисицы чесоткой могут заражать домашних собак [81]. Анализ девяти микросателлитных маркеров позволяет предположить, что еноты в Германии могут заразиться чесоткой от зараженных чесоткой красных лисиц [82].
В другом анализе с использованием мультиплекса из 9 микросателлитных маркеров Oleaga et al. [83] сравнили генетическое разнообразие чесоточных клещей, собранных у симпатрических иберийских волков, серны, благородного оленя, косули и лисицы.Клещи иберийского волка обладали наибольшим генетическим разнообразием. Это говорит о том, что переход от добычи к хищнику может изменить взаимоотношения таксонов хозяина. Казалось бы логичным, что передача паразита от жертвы к хищнику и коэволюция паразита в этих ассоциациях хищник-жертва важны для передачи S. scabiei между хозяевами и, таким образом, совместного использования общего штамма S. scabiei между хозяевами. жертва и хищник весьма вероятны. Gakuya et al. [84, 85] предложили переход от добычи к хищнику между дикими кошачьими и копытными в Африке.
Диагностика и анализ крови на чесотку
Диагностировать чесотку у людей с корковой чесоткой, а также у домашних и диких животных с запущенной чесоткой (включая собак, лис, койотов, оленей, коз, серну, кроликов и др.) Несложно, потому что на них обитают тысячи клещей, которых легко удалить, соскоблив кожу. Однако ранняя диагностика заражения обычным чесоточным клещом у людей и других млекопитающих очень трудна, потому что на ранней стадии заражение поражает очень мало клещей, и в течение многих недель симптомы отсутствуют или проявляются минимально.Сообщается, что количество взрослых клещей, обнаруживаемых у человека с обыкновенной чесоткой, невелико и составляет менее 15 (в среднем 11,2) [86]. Это количество основано на обследовании около 900 взрослых пациентов. Ранние инфекции чесотки у собак и других животных также вызывают мало клещей. Это очень затрудняет постановку диагноза чесотки по ссадине кожи. Кроме того, диагностика чесотки осложняется еще и тем, что клинические проявления чесоточной инфекции сходны с клиническими проявлениями других кожных заболеваний (атопический дерматит, экзема, псориаз, опрелости, укусы насекомых, ядовитый плющ и т. Д.).) и кожные заболевания, вызванные раздражающими веществами (мыло / моющие средства, лосьоны, ароматизаторы, металлы, латекс, резина и другие химические вещества). Предположительный диагноз может быть поставлен на основании клинических симптомов, таких как сильный зуд, сыпь и эритематозные пятна, но окончательный диагноз ставится на основании микроскопического исследования клещей, их яиц и / или фекальных гранул, а также бороздок в эпидермисе, которые удаляются из эпидермиса. кожу соскребом скальпелем. Однако найти и соскоблить чесоточные поражения может быть сложно.Таким образом, существует большой интерес к разработке диагностического анализа крови на чесотку как у людей, так и у животных. Ясно, что инфекции чесоточного клеща вызывают гуморальный ответ хозяина, который приводит к циркуляции антител (которые могут быть, а могут и не быть защитными). Таким образом, анализ крови возможен, но все же требует значительных исследований для достижения почти 100% специфичности и чувствительности. Анализ крови, основанный на обнаружении сывороточных антител к антигенам чесоточного клеща, будет большим преимуществом для ранней диагностики чесотки, когда выявление клещевого материала в соскобе кожи затруднено.
Анализ крови для диагностики инфекции чесотки требует идентификации и продуцирования соответствующих антигенов чесоточного клеща, а также определения соответствующего изотипа и специфичности антител хозяина. Адекватные количества чесоточных клещей нельзя массово культивировать in vivo или in vitro для получения больших количеств антигена для использования в диагностическом тесте или для разработки вакцины для защиты от инфекции. Из-за нехватки клещевого материала молекулы антигена, необходимые как для диагностического теста, так и для разработки вакцины, вероятно, будут зависеть от идентификации и производства рекомбинантных молекул, которые распознаются циркулирующими антителами, которые хозяин вырабатывает в ответ на активное заражение чесоткой.Некоторые рекомбинантные молекулы были получены и исследованы с этой целью на собаках, свиньях и кроликах. Прогресс наблюдается, но ключевые рекомбинанты еще предстоит идентифицировать. Одной из проблем, которые необходимо преодолеть при разработке этого теста, является высокий уровень перекрестной реактивности между антигенами чесоточных клещей и антигенами родственных повсеместно распространенных клещей домашней пыли. Во всем мире высокий процент людей страдает аллергией на клещей домашней пыли и вырабатывает антитела IgE и IgG к своим аллергенам и антигенам соответственно.Серологический тест, основанный на обнаружении специфических IgE к чесоточным клещам, не годится для выявления инфекций чесоточного клеща, потому что, как и в случае аллергии на клещей домашней пыли, не все пациенты предрасположены к выработке IgE к ним, и, следовательно, у них нет аллергии на их антигены. Пациент с чесоткой может иметь или не иметь аллергию на клещей домашней пыли, но большинство пациентов с чесоткой, по-видимому, чувствительны к клещам домашней пыли [87].
Как упоминалось ранее, важен изотип антитела, используемый для обнаружения антигена чесоточного клеща.Хозяева, вероятно, продуцируют антитела IgM к антигену клещей перед переключением на IgG. Таким образом, ранняя диагностика, вероятно, должна основываться на обнаружении IgM или обоих IgM и IgG в крови больных чесоткой. Предварительное исследование поддерживает эту концепцию. Исследование Arlian et al. [87] обнаружили, что 45,1%, 27,5% и 73,6% из 91 пациента с обычной чесоткой имели сывороточные антитела Ig, IgG и IgM к антигенам чесоточного клеща соответственно. Только 2,2% имели IgE, направленный на антигены чесоточного клеща. Однако, как отмечалось ранее, перекрестная реактивность и сенсибилизация к клещам домашней пыли усложняют картину.Из 91 пациента с чесоткой 84,6%, 91,2% и 86,8% имели IgG к D. farinae , D. pteronyssinus и E. maynei соответственно. Аналогичным образом, 75,8%, 83,5% и 84,6% имели IgM, направленный против этих трех видов клещей, соответственно. Но только 2–3% имели IgE, направленный к любому из четырех протестированных видов клещей ( S. scabiei , D. farinae , D. pteronyssinus и E. maynei ). Многие антигены клещей домашней пыли имеют перекрестно-реактивные эпитопы с антигенами клещей чесотки [88,89,90,91,92].Таким образом, белковые молекулы, используемые для обнаружения антител к чесотке, не должны иметь перекрестной реакции с какими-либо антигенными белками или пептидами клещей домашней пыли. Вполне вероятно, что диагностический анализ крови должен будет содержать смесь белков / пептидов чесоточного клеща [87]. Если действительно существует несколько штаммов S. scabiei , которые инфицируют людей в разных географических регионах мира, как было предложено [68], эта комбинация антигенов и профиль антител в крови, возможно, потребуется разработать и адаптировать к конкретным районам / регионы мира.
В отличие от пациентов с обычной чесоткой, похоже, что большинство пациентов с корковой чесоткой имеют IgE, направленный на антигены чесоточного клеща. Исследование Arlian et al. [93] исследовали профили IgE и IgG у пациентов с обычной и покрытой корками чесоткой. Иммуноблоттинг показал, что 6 из 6 пациентов с корковой чесоткой имели сывороточный IgE, который распознавал от 11 до 21 белка / пептида во всем теле S. scabiei var. Экстракт canis , разделенный с помощью SDS-PAGE [93]. Напротив, только 3 из 7 пациентов с обычной чесоткой имели IgE и только 2 из 7 имели IgG, который распознавал белковые полосы, и их связывание было слабее, что указывает на гораздо более низкие титры.Walton et al. [46] также продемонстрировали, что пациенты с корковой чесоткой имели значительно более высокие уровни сывороточного IgE, который распознал 4 рекомбинантных S. scabiei var. hominis белков гомологичны аллергенам пылевых клещей, чем пациенты с обычной формой заболевания.
Серологический иммуноферментный анализ (ELISA) для диагностики чесотки был разработан и оценен для использования в нескольких различных видах хозяев. Эти тесты показали различный успех, и результаты зависели от степени и продолжительности заражения и используемого антигена-мишени.
В первых исследованиях использовались водные антигенные экстракты, полученные из целых тел клещей S. scabiei (таблица 3). Производство этих экстрактов требовало утомительной работы по сбору клещей от различных хозяев. Лунки в планшетах для ELISA были покрыты антигеном в этих экстрактах. В некоторых случаях антиген клеща был сопоставлен со штаммом клеща, ответственным за инфекцию (например, антиген лисьего клеща и инфицированные лисы, антиген свиного клеща и инфицированные свиньи). В других случаях антиген клеща от одного вида хозяев использовали для обнаружения антител в сыворотке от другого вида хозяев, инфицированных чесоткой.Например, антиген лисьего клеща использовали для обнаружения антител в сыворотке инфицированных свиней, а антиген клеща собачьей чесотки использовали для обнаружения антител в сыворотке людей, инфицированных чесоткой. Таким образом, результаты основывались на перекрестной реакции или общих антигенах между чесоточными клещами от разных видов хозяев. Лабораторные исследования с использованием перекрестного иммуноэлектрофореза и иммуноблоттинга прямо продемонстрировали перекрестную реактивность между антигенами чесоточных клещей свиней (var. suis ), собак (var. canis ) и людей (вар. hominis ) и что эти клещи являются источниками перекрестно реагирующих антигенов или эпитопов, что поддерживает подход к использованию антигена, полученного из одного штамма клещей, для обнаружения антител в сыворотке инфицированного хозяина. с другим штаммом [94].
Таблица 3 Характеристики опубликованных ELISA с использованием сырого экстракта клещей в качестве антигена-мишени для обнаружения антител, циркулирующих в сыворотке скабиетических хозяевHollanders et al.[95] использовали антигены S. scabiei var. Экстракт vulpes (гомогенат целого тела клеща из лисьих клещей) в ELISA для обнаружения антител в сыворотке документированных зараженных чесоткой свиней-отъемышей, свиней на откорме и свиноматок. Анализ обнаружил антитела у 80%, 77,8% и 50% отъемышей, откормочных свиней и свиноматок, соответственно, в то время как более 98% контрольных свиней без чесотки не имели обнаруживаемых сывороточных антител к антигенам клещей.
Три коммерческих ELISA (Checkit® Sarcoptest, Sarcoptes-ELISA 2001 PIG и Acar-Test P * ELISA) были использованы для обнаружения антител IgG у свиней, экспериментально зараженных S.scabiei var. suis в разное время по мере прогрессирования инфекции [96]. Это контролируемое исследование показало, что эти системы ELISA могут обнаруживать антитела у большинства инфицированных свиней через 5-6 недель заражения чесоточными клещами. В аналогичном исследовании использовались четыре различных набора ELISA для определения IgG для определения сывороточного IgG к антигену чесоточного клеща у естественно инфицированных свиноматок и свиней, виновных в этом заболевании [97]. В одном тестовом наборе использовался антиген из S. scabiei var. suis (свиньи клещи), в то время как три других набора содержали антиген из S.scabiei var. vulpes (лисий клещ). Серологические положительные результаты варьировались от 30% до 88,6% в зависимости от используемого теста. Однако соскобы кожи были положительными только у 48,6% этих свиней. Таким образом, некоторые диагностические серологические тесты могут значительно улучшить диагностику.
Van der Heijden et al. [98] также разработали ELISA службы здоровья животных (AHS-ELISA) для выявления чесотки у свиней. Детектирующий антигенный материал получали из S. scabiei var. suis клещей собрано от свиноматок с коркой чесотки.AHS-ELISA обнаружил сывороточные антитела через 6 недель у 5% свиней и у 74,2% свиней после 16 недель заражения. Это показывает, что ответы антител развиваются медленно или что титр низкий и ниже предела обнаружения метода во время ранних инфекций чесотки.
Чесотка может быть серьезной угрозой для дикой серны и козерога в южной Европе [99,100,101]. Разработка серологического теста поможет менеджерам по ресурсам отслеживать инфекции у этих животных. Rambozzi et al.[99] разработали ELISA, амплифицированный биотин-авидином (LAB-ELISA), с использованием антигена из S. scabiei var. vulpes от красных лисиц ( Vulpes vulpes ) для выявления антител в сыворотках серны, инфицированной чесоткой, и отличия их от здоровой серны. Используя этот тест, 37 из 40 сывороток с чесоткой были положительными по ИФА, а 101 из 104 сывороток, собранных с неинфицированной серны, были отрицательными.
ELISA также использовался для диагностики чесотки у собак. Lower et al. [99] оценили непрямой ИФА (Imovet sarcoptes) у 19 собак с подтвержденными инфекциями чесотки.Захватывающим антигеном в этом тесте был S. scabiei var. vulpes от лисиц и 84,2% собак имели определяемые уровни IgG к антигену лисьего клеща, в то время как 89,2% контрольных собак без чесотки в анамнезе не имели.
ELISA с использованием антигена из S. scabiei var. ovis был использован для обнаружения сывороточных антител у овец, инфицированных var. ovis [102]. Этот ELISA диагностировал 87,6% овец с чесоткой, в то время как только 62,8% были положительными при соскобе кожи.
Bornstein et al. [103] использовали планшеты для ELISA, покрытые водным экстрактом антигенов, полученных из S. scabiei var. vulpes и вторичные антитела против IgG собаки для обнаружения антител в окрашенных кровью жидкостях полостей тела рыжих лисиц. Наличие антител к антигену чесоточного клеща было обнаружено у 62 из 65 (95%) рыжих лисиц, имевших клинические признаки саркоптоза.
ELISA с использованием моноклональных антител к собаке IgG был использован для обнаружения сывороточного IgG, направленного на антиген из S.scabiei var. vulpes для диагностики у собак, инфицированных S. scabies var. canis клещей [104]. У 10 из 12 (83%) собак подтверждено наличие S. scabiei var. Инфекция canis дала положительный результат ELISA для S. scabiei var. vulpes антигенов.
Haas et al. [105] оценили возможность использования S. scabiei var. vulpes антиген от клещей лисицы в формате ELISA для диагностики чесотки человека.Планшеты для ELISA покрывали антигеном лисьего клеща, а затем реагировали с сывороткой больных чесоткой. Сыворотки 41 человека с подтвержденным диагнозом S. scabiei var. человекообразных животных подвергали скринингу с помощью ELISA для выявления антител IgG. Сорок восемь процентов больных чесоткой имели сывороточный IgG, который четко распознавал var. vulpes антиген и 17% были погранично положительными. Однако большинство пациентов, у которых не было IgG, распознавшего S. scabiei var. vulpes имел симптомы в течение менее 4 недель, и анализ не тестировал связывание антител IgM.Таким образом, изотип антител IgM, который продуцируется до переключения на продукцию IgG, мог быть лучше для выявления инфекции чесотки, как было предложено Arlian et al. [87].
Более поздние исследования были сосредоточены на использовании рекомбинантных молекул для разработки ELISA для диагностики чесоточного клеща (таблица 4). Иберийский благородный олень ( Cervus elaphus hispanicus ) в европейских странах может быть заражен саркоптозом [106]. Oleaga et al. [106] использовали ELISA для оценки наличия специфических антител против чесоточного клеща в образцах сыворотки, собранных у 327 благородных оленей без явных саркоптозных поражений.В этом ELISA использовали рекомбинантный антиген чесоточного клеща Ssλ20ΔB3, выделенный из S. scabiei var. Библиотека экспрессии hominis [107]. Он был распознан антителами в сыворотке 6 из 8 щитовидных благородных оленей.
Таблица 4 Характеристики опубликованных ELISA с использованием рекомбинантных белков в качестве антигена-мишени для обнаружения антител, циркулирующих в сыворотке скабиетических хозяевВ другом исследовании рекомбинантный Ssλ20ΔB3, полученный из S. scabiei var. hominis показал с помощью ELISA для обнаружения антител у 7 серн ( Rupicapra rupicapra ) и 3 оленей с подтвержденной инфекцией чесотки [107]. Из здоровых животных, не подвергавшихся воздействию чесотки, только 1 из 33 серн и 1 из 33 оленей были иммунопозитивными. Хотя размер выборки инфицированных животных был небольшим, исследование показало, что белок чесоточного клеща человека действительно идентифицирует антитела к антигенам чесоточного клеща в крови двух разных видов животных-хозяев.
Дикий европейский кролик ( Oryctolagus cuniculus ) встречается на северо-востоке Средиземноморья в Испании и служит добычей для многих хищников, а также в качестве дичи для охотников [108]. Sarcoptes scabiei паразитирует в некоторых популяциях этих кроликов, и есть опасения, что болезнь может значительно повлиять на популяцию кроликов и что она может передаваться другим диким животным. Таким образом, Millan et al. [108] использовали ELISA на основе рекомбинантного человеческого антигена чесоточного клеща Ssλ20ΔB3 для исследования серологической распространенности антител против чесотки у кроликов в отдельных провинциях или на островах Испании. Большинство проанализированных сывороток было получено от кроликов, отстреленных охотниками. Результаты показали, что человеческий антиген клеща можно использовать для выявления чесотки у диких кроликов и что воздействие S.scabiei был широко распространен среди диких кроликов по всей Испании.
He et al. [109] использовали рекомбинантный кальмодулин, клонированный из РНК, экстрагированной из S. scabiei , собранных у кроликов, для разработки ELISA для определения наличия S. scabiei- специфических антител в сыворотке кроликов, инфицированных S. scabiei или с Psoroptes cunniculi, другим эктопаразитом кроликов. Хотя этот анализ имел чувствительность 88%, его специфичность составила всего 23% из-за перекрестной реактивности высококонсервативного кальмодулина от чесоточных клещей с этим белком из P.Кузнецова .
Mattsson et al. [110] использовали рекомбинантный фрагмент размером 17,5 кДа var. vulpes парамиозин (миниатюрный парамиозин) для обнаружения антител в сыворотках собак и свиней, инфицированных чесоткой, с помощью иммуноблоттинга. Эта молекула распознается антителами иммунизированных кроликов, но не может быть легко обнаружена антителами в сыворотке инфицированных чесоткой собак и свиней.
В совокупности эти исследования демонстрируют достаточную перекрестную реактивность между антигенами чесоточного клеща от разных хозяев, которые являются естественными или рекомбинантными S.scabiei от одного вида хозяев можно использовать для обнаружения сывороточных антител у хозяина, инфицированного другим штаммом чесоточных клещей. Кроме того, эти исследования показывают вариабельность и сложность обнаружения сывороточных антител у естественно инфицированных животных, когда история инфекции неизвестна. Ключевые вопросы, которые влияют на полезность анализа крови на чесотку: (i) сколько времени проходит после начала инфекции, прежде чем антитела могут быть обнаружены в сыворотке, и (ii) какой изотип антител должен обнаруживать этот тест (e.грамм. IgM, IgG, IgE и т. Д.)? Это факторы, которые еще предстоит определить, но при раннем обнаружении, вероятно, следует искать IgM, поскольку этот изотип вырабатывается на ранней стадии гуморального ответа. Кроме того, должен ли анализ крови быть разработан для обнаружения сывороточных антител, направленных против одного антигена, или он должен будет содержать смесь антигенов для обнаружения сывороточных антител, созданных против нескольких антигенов или определенного профиля антигенов? Например, в исследовании Kuhn [111], может ли смешивание целевых антигенов SsE3 и SsE5 повысить чувствительность до 100% (Таблица 4)? Это важные факторы, которые следует учитывать при разработке анализа крови на чесотку.
Появление молекулярных методов в сочетании с доступностью геномных последовательностей клещей дает возможность для разработки альтернативных методов диагностики. Angelone-Alasaad et al. [112] разработали два основанных на ПЦР метода диагностики чесотки, основанных на амплификации 135 п.н. митохондриальной 16S рДНК. Оба метода были успешно протестированы на чесоточных клещах, собранных у 23 видов хозяев. Использование технологии на основе ПЦР является многообещающим, но по-прежнему требует извлечения клещевого материала в кожном соскобе, что остается сложной задачей.
Вакцинация против заражения чесоточным клещом
Акарициды доступны для лечения чесотки, но развилась значительная резистентность к этим акарицидам, что приводит к неэффективности лечения [113,114,115]. Кроме того, эти химические вещества обладают известным и неизвестным токсическим воздействием на людей и животных. Таким образом, вакцинация для защиты от заражения чесоточными клещами является привлекательной альтернативой доступным в настоящее время химиотерапевтическим средствам.
Вакцинация против S.scabiei — реальная цель по нескольким причинам. Чесотные клещи вызывают как врожденный, так и адаптивный иммунный ответ у паразитированного хозяина. Адаптивный ответ включает выработку IgM, IgG и изотипов антител IgE и IgA в некоторых человеческих хозяевах к антигенам, которые клещи выделяют в эпидермисе, когда они зарываются. Клещи поглощают сывороточные антитела, когда зарываются в нижний эпидермис и питаются им. Некоторые данные свидетельствуют о том, что сыворотка является составной частью их рациона. Системные акарициды, такие как ивермектин, убивают клещей на коже, предположительно потому, что клещи их проглатывают.Исследование с использованием флуоресцентно меченых антител показало, что антитела хозяина связываются со слизистой оболочкой кишечника живых клещей, удаленных от хозяина [27]. Антитела-хозяева, которые связываются с молекулами клеток кишечника и пищеварительными ферментами, вырабатываемыми этими клетками, которые имеют решающее значение для пищеварения и поглощения питательных веществ, могут блокировать эти процессы и, таким образом, препятствовать выживанию клеща. Точно так же антитело хозяина, направленное на молекулы клеща, которые имеют решающее значение для подавления защитных реакций хозяина, будет препятствовать способности клеща выживать и создавать популяцию в коже хозяина, потому что хозяин теперь может обеспечить успешный защитный ответ.
Другие данные свидетельствуют о том, что вакцинация может вызывать защиту от чесоточных клещей. Было обнаружено, что титры антител хозяина развиваются быстрее и с большей интенсивностью во время второй инфекции по сравнению с начальной (первичной) инфекцией чесоточными клещами [116]. Животные, выздоровевшие от заражения чесоточным клещом, демонстрируют снижение уровня клещей при последующем повторном заражении [11, 116, 117, 118, 119]. Arlian et al. [117] обнаружили, что 8 собак, излеченных от S. scabiei и затем повторно инфицированных, проявили защитный иммунитет.У семи из 8 собак развились кратковременные инфекции, которые полностью исчезли со временем без какого-либо лечения. Наконец, кроликов иммунизировали экстрактом всего тела S. scabiei var. canis продуцировал антител к большему количеству антигенов, чем кролики, инфицированные этим клещом [120].
Опубликованы результаты нескольких испытаний вакцинации. Исследование Tarigan et al. [118] оценили защитный эффект вакцинации коз экстрактом, полученным из целых тел чесоточных клещей, собранных от инфицированных коз, и несколькими фракциями этого экстракта, полученными с помощью анионообменной хроматографии.Они не обнаружили различий в степени тяжести кожных повреждений между иммунизированными и неиммунизированными козами в течение нескольких раз после экспериментального заражения, хотя ранее инфицированные животные действительно проявляли защитный иммунитет.
Harumal et al. [121] исследовали защитный эффект иммунизации кроликов рекомбинантными антигенами Ssag1 и Ssag2 (от клещей разновидности hominis ). Иммунизированные кролики продуцировали антитела к обоим антигенам, однако кролики не проявляли защитного иммунитета или снижения численности клещей.Молекулы Ssag 1 и Ssag 2 располагались вокруг внутренних органов и кутикулы чесоточного клеща и в яйцах. По-видимому, эти белковые фрагменты недоступны для антител, или связывание антител с ними не ингибирует жизненно важные функции, необходимые для выживания клещей.
Casias et al. [122] вакцинировали кроликов смесью рекомбинантных антигенов Ssλ20ΔB3 и GST-Ssλ15, полученных из S. scabiei var. человекообразных животных клещей. Затем этим кроликам вводили S.scabiei var. cuniculi (чесоточные клещи от кроликов) и проявляли высокие уровни специфического IgG и повышенные уровни общего IgE, но не были защищены от заражения этими клещами.
Исследования показали, что клещи домашней пыли D. farinae и D. pteronyssinus перекрестно реагируют с антигенами в экстрактах S. scabiei [88, 89]. Это свидетельствует о том, что вакцинация экстрактами клещей домашней пыли может индуцировать защиту от S. scabiei .Большое количество чесоточных клещей недоступно для изготовления вакцины для целей иммунизации, но клещей домашней пыли можно культивировать в количествах, равных килограммам. Иммунизация смесью 50/50 экстрактов D. farinae и D. pteronyssinus индуцировала защитный иммунитет к S. scabies var. canis у кроликов, о чем свидетельствует заметное снижение паразитарной нагрузки по сравнению с неиммунизированным контролем [90].
Другие исследования подтверждают принцип защиты от эктопаразитарного клеща.Овец и кроликов вакцинировали родственным клещом парши Psoroptes sp. Частичный иммунитет к инфекции P. cuniculi (клещ из парши кролика) развился после четырех иммунизаций экстрактом всего тела [123]. Вакцинированные кролики обеспечивали сопоставимую защиту по сравнению с естественно инфицированными кроликами. Аналогичным образом, вакцинация овец экстрактами всего тела P. ovis (клеща из струпа овцы), приготовленными в физиологическом растворе или 1% твине, привела к значительной защите от заражения [124].Последующее исследование показало, что определенная фракция, полученная с помощью анионообменной хроматографии исходного экстракта, дает большую защиту, чем другие фракции, и чем сам исходный экстракт [125]. Однако профиль фракции в SDS-PAGE показал, что она содержит много белков, поэтому молекулы, ответственные за повышенную защиту, не могут быть идентифицированы.
Gu et al. [126] исследовали иммунный ответ, индуцированный у мышей с помощью S. scabiei var. cuniculi ДНК-вакцина, кодирующая парамиозин.ДНК-вакцина вызвала гуморальный и клеточный иммунный ответ, характеризующийся более высокими уровнями IgG, IgG1, IgG2a, IgE и IgM, повышенной секрецией IL-2, IL-4, IL-5 и IFNγ спленоцитами и пролиферацией лимфоцитов в селезенка. Парамиозин является обычным белком у многих беспозвоночных и имеет высокую гомологию между видами. Эти эксперименты создают основу для дальнейшего изучения возможной ДНК-вакцины для защиты от чесотки. Не было определено, вызывает ли это какой-либо защитный иммунитет.
В совокупности все эти данные ясно показывают, что вакцинация представляет собой реальную возможность защитить популяции людей и животных от чесоточных клещей. При рассмотрении испытаний вакцины от чесотки в игру вступают многие факторы, помимо антигена или смеси антигенов. Многие из сообщенных неудачных попыток иммунизации могут быть связаны с адъювантами, графиком иммунизации, дозой антигена и способом доставки. Ключевой антиген или смесь антигенов еще предстоит идентифицировать и получить с помощью рекомбинантной технологии.Кроме того, необходимо будет определить все компоненты протокола иммунизации.
Выводы
Заболевание чесоткой известно тысячелетия. Однако отсутствие большого количества чесоточных клещей от гипер-инфицированных хозяев, методов культивирования in vitro или животных моделей in vivo ограничивает типы возможных исследований. Знания о биологии чесоточных клещей, взаимодействиях хозяина и паразита, молекулах, которые производят клещи (антигены, неантигены и иммуномодулирующие), способности модуляции хозяина, врожденных и адаптивных иммунных ответах хозяина, а также протеомике и геномике клещей значительно расширились в течение последние 30 лет.
