Стеноз гортани у ребенка — ПроМедицина Уфа
Стеноз гортани у детей – заболевание, характеризующееся сужением просвета, вследствие чего качественно затрудняется дыхание на некоторый временной промежуток.
Смертность среди маленьких детей с развитым стенозом слишком высока и при первых же симптомах отсчет уже идет на часы и минуты жизни ребенка.
Стеноз гортани у детей начинается всегда одинаково: с признаков банальной простуды. Поначалу ребенок становится очень тревожным и беспокойным, появляется первое покашливание, поднимается температура. Несколько дней может сохраняться полная видимость вирусной инфекции и не более того. Но довольно быстро клиническая картина меняется, иногда хватает нескольких часов, чтобы у малыша начало развиваться удушье.
Причины
Причиной стеноза могут быть не только вирусы или бактерии, но и аллергические реакции на домашнее лечение: мед, малину, ингаляции с травами, сосновыми почками, пихтовым маслом. Очень часто дети выдают удушье на запах вьетнамского бальзама «Звездочка», цветущих растений, косметики, духов, бензина и других химических веществ.
Симптомы
Первые признаки недуга у крохи могут быть не замечены даже самыми внимательными родителями. Объясняется это тем, что симптоматика стеноза очень схожа с клиническими проявлениями обычного ОРЗ. У крохи может незначительно повыситься температура тела, а также появиться насморк.
Следующая стадия развития стеноза характеризуется сильным приступообразным кашлем, осипшим голосом и учащенным шумным дыханием. Опасение у родителей должно вызвать и то, что состояние ребенка стремительно ухудшается, он становится вялым и раздражительным, что свидетельствует о начале гипоксии.
Диагностика
Стеноз гортани у детей диагностируется дифференциальным методом, вследствие чего можно выявить причины и различить гортанный стеноз от ларингоспазма, стеноза трахеи, приступа бронхиальной астмы. Стеноз выявляется путем проведения осмотра и пальпации на фоне выраженной симптоматики.
Для качественного выявления причины стеноза проводят следующие обследования: томография, ларингоскопия, рентгенография гортани и полностью пищевода, ультразвуковое исследование щитовидной железы, бактериологические исследования из зева, трахеобронхоскопия.
Лечение
Стеноз гортани у детей развивается слишком быстро и тут не стоит терять время. При очевидном удушье можно сделать укол преднизалона, чтобы облегчить ребенку процесс дыхания. Только нужно точно знать, что иного выбора нет и судить, по возможности, здраво: если врачи уже на подходе, а горячий пар и растирание ножек помогают, ребенок дышит, то колоть препарат не стоит.
Вызвать «скорую» с последующим посещением участкового педиатра жизненно необходимо для выздоровления. Во-первых, приступ может повториться, а колоть всякий раз препарат нельзя. Ребенок остро нуждается в хорошем и комплексном лечении, прохождении курса физиотерапии, лечении антибиотиками и ликвидации отечности гортани.
В момент приступа часто бывает критическая ситуация, тогда специалистам приходится на месте проводить операцию. Делается сечение в области трахеи с целью поступления воздуха, вставляется специальная трубка.
Делается сечение в области трахеи с целью поступления воздуха, вставляется специальная трубка.
Во время кризиса необходимо постоянное наблюдение и обеспечить его возможно только в стационарных условиях.
» Стеноз гортани у детей
Стеноз гортани у детей — это заболевание, которое характеризуется сужением просвета гортани. В итоге происходит затруднение поступления воздуха в легкие, что учащает дыхание ребенка. Стеноз приводит к нарушению защитной, дыхательной и голосовой функции. Сегодня данное заболевание отмечается достаточно часто и требует соответствующего лечения.
Разновидности стеноза
В зависимости от симптоматики и длительности заболевания принято различать несколько форм стеноза:
Острая форма получила наибольшее распространение. Продолжительность такого заболевания может составлять как несколько минут, так и один месяц. Следует сказать, что молниеносный стеноз, продолжительность которого может достигать нескольких минут, крайне опасен для жизни ребенка.
Подострый стеноз имеет время развития от 1 до 3 месяцев.
Хроническая форма заболевания имеет длительность более трех месяцев. Такое сужение гортани может быть приобретенным или врожденным. Достаточно часто хронический стеноз отмечается на фоне образования рубцовой ткани в гортани и доброкачественных новообразований.
Факторы, вызывающие появление стеноза у детей
Следует сказать, что вызывать данное заболевание могут различные причины. Можем сказать, что достаточно часто стеноз появляется на фоне:
- Различных воспалительных заболеваний. Так, например такое сужение трахеи может отмечаться на фоне гортанной ангины, подкладочного фарингита и ларингита.
- Различных инфекционных заболеваний.
- Заболеваний пищевода, гортани и трахеи.
- При механических травмах гортани, что может возникать при медицинском вмешательстве или же бытовым способом.
- Наличие различных врождённых аномалий гортани.
- Появление острой аллергической реакции.

- Острого отравления организма.
Симптоматика стеноза у детей
Следует сказать, что симптоматика данного заболевания напрямую зависит от его стадии. Так, например, на стадии компенсации отмечается легкое состояние у ребенка, при котором лишь отмечается учащенное дыхание. При повышенной физической нагрузке у ребенка может отмечаться одышка.
При стадии неполной компенсации отмечается средняя тяжесть состояния ребенка. На коже и слизистых появляются бледные цвета, дыхание нарушенное и имеет выраженный шум. Также у ребенка могут отмечаться признаки гипоксемии.
Стадия декомпенсации оценивается как тяжелое состояние ребенка. Внешнее дыхание нарушено, ребенок может закрывать глаза, цвет кожи существенно изменен. На слизистых оболочках отмечается цианоз. Дети быстро устают, при этом отмечается выраженное нарушение дыхания. Глубокая гипоксия тканей способствует тахикардии, аритмии и замедлению пульса.
Лечение детского стеноза
Следует сказать, что успешность проводимого лечения данного заболевания напрямую зависит от стадии, на которой выявлен стеноз у ребенка. Необходимо ликвидировать дыхательную недостаточность и приступы удушья. Лечение данного заболевания может проводиться как разнообразными физиотерапевтическими процедурами, так и приемом соответствующих лекарственных средств. В редких случаях требуется хирургическое вмешательство, что позволяет полностью устранить проблемы с дыханием у ребенка. Необходимо соблюдение всех предписаний врача, а само лечение выполняется исключительно под присмотром специалиста.
Необходимо ликвидировать дыхательную недостаточность и приступы удушья. Лечение данного заболевания может проводиться как разнообразными физиотерапевтическими процедурами, так и приемом соответствующих лекарственных средств. В редких случаях требуется хирургическое вмешательство, что позволяет полностью устранить проблемы с дыханием у ребенка. Необходимо соблюдение всех предписаний врача, а само лечение выполняется исключительно под присмотром специалиста.
Стеноз гортани | Медицинский центр «Президент-Мед»
Недомогание, при котором происходит сужение просвета гортани называется стенозом. Развитие патологии затрудняет процесс дыхания и глотания пищи. В группе риска прогрессирования недуга дети (особенно недоношенные), хотя часто наблюдается болезнь и у взрослых пациентов.
Стеноз гортани довольно тяжелое заболевание, оно без корректного лечения может привести к летальному исходу. В младенческом возрасте проявляется патология, если ребенок после рождения не мог самостоятельно дышать и долго находился на искусственном дыхании. У взрослых больных и детей постарше спровоцировать сужение просвета гортани могут многие факторы.
У взрослых больных и детей постарше спровоцировать сужение просвета гортани могут многие факторы.
Первопричины развития стеноза гортани:
- Инфекционные болезни: сыпной и брюшной тиф, скарлатина, туберкулез, малярия, корь и другие.
- Механические травмы горла.
- Аллергическая реакция.
- Ожог гортани химическими веществами или пламенем.
- Интубация трахеи, гастроскопия и бронхоскопия.
- Опухоли гортани различного характера.
- Патологии щитовидной железы.
Перед подбором лечения важно определить причину и форму течения болезни. Стеноз гортани может быть острым (развивается быстро) или же хроническим.
Симптомы стеноза гортани
Проявление симптоматики стеноза гортани зависит от состояния иммунной системы человека и стадии развития заболевания.
Степени и признаки стеноза:
I стадия (компенсированный стеноз) – диагностируется сужение гортани до 50%, при этом у пациента диагностируется наличие затрудненного дыхания, одышки при физических нагрузках и симптомов брадикардии.
II стадия (субкомпенсированная вариация) – сужение просвета до 70%. Больному тяжело выдыхать воздух, беспричинно появляется одышка, дыхание становиться шумным.
III стадия (декомпенсированный вариант) – просвета в гортани остается очень мало, до 1% (сужение 99%). Развивается гипоксия, в результате чего появляется синюшность кожных покровов. Кроме того, пациент вынужден только сидеть, поскольку в другой позе дышать он не может, дыхание при этом очень громкое и присоединяется тахикардия.
IV стадия (асфиксия) – 100% сужение просвета. Это самая страшная степень стеноза гортани, поскольку происходит остановка дыхания, появляются судороги, больной теряет сознание и пульс не прощупывается. Без мгновенной реанимации пациент умирает.
Быстрому лечению поддаются только начальные степени стеноза гортани, поэтому при проявлении симптомов следует обратиться к отоларингологу.
Диагностика и лечение стеноза гортани
При подозрении на стеноз гортани врач назначит ларингоскопию. Такое инструментальное обследование позволит увидеть состояние трахеи, а также уточнить ширину оставшегося просвета гортани. Доктор может направить пациента на УЗИ щитовидной железы, компьютерную томографию или рентгенологическую диагностику пищевода. Обязательно проводиться бактериологический анализ мазка из зева. Все эти диагностические мероприятия помогают не только уточнить диагноз, но и выявить первопричину развития патологии, а значит, подобрать эффективную терапию.
Такое инструментальное обследование позволит увидеть состояние трахеи, а также уточнить ширину оставшегося просвета гортани. Доктор может направить пациента на УЗИ щитовидной железы, компьютерную томографию или рентгенологическую диагностику пищевода. Обязательно проводиться бактериологический анализ мазка из зева. Все эти диагностические мероприятия помогают не только уточнить диагноз, но и выявить первопричину развития патологии, а значит, подобрать эффективную терапию.
Больных стенозом лечат в стационаре реанимационного отделения. Медикаментозная терапия может включать в себя антибиотики, глюкокортикостероиды, противоотечные и противоаллергические средства. Кроме того, внутривенно вводят препараты, сужающие сосуды, а также кальций. В процессе борьбы со стенозом гортани могут применяться и специальные теплые компрессы на горло или грудь со щелочными минеральными водами, а также согревающие ножные ванны.
Если наступает удушье, проводят срочную трахеотомию (вскрытие просвета трахеи). В случае, когда диагностируется асфиксия, показана коникотомия – в определенной области шеи делают разрез и вводят в образовавшийся просвет трубку, через нее воздух поступает в дыхательные пути больного.
В случае, когда диагностируется асфиксия, показана коникотомия – в определенной области шеи делают разрез и вводят в образовавшийся просвет трубку, через нее воздух поступает в дыхательные пути больного.
Лечение стеноза сложное, оно должно производиться только под четким контролем докторов. Самолечение сужения просвета гортани может привести к усугублению процесса и необратимым последствиям.
Для диагностики и лечения стеноза гортани обращайтесь в медицинские клиники «Президент-Мед» в Москве (на Коломенской и ВДНХ) и в Видном
Автор: Мамунц Цовинар Алексеевна
Главный врач Президент-Мед г. Видное
Высшее медицинское, Пермский государственный медицинский институт, лечебный факультет, специальность-лечебное дело
Записаться к врачу
ОТЗЫВЫ КЛИЕНТОВ
Ольга
Спасибо Юлие Владимировне! Врач очень опытная, внимательная, а самое главное ее очень любят дети! Приходилось уже несколько раз с ребёнком обращаться и всегда каждый приём на высоте. Как хорошо, когда есть такие хорошие врачи[…]
Как хорошо, когда есть такие хорошие врачи[…]Щетининой О.Н.
Большое спасибо всем работникам клиники за слаженную работу и хорошее настроение. Отдельное спасибо Ивановой Ю.А. за профессионализм, отзывчивость, индивидуальный подход.[…]Острый стеноз гортани (=круп). Что делать?
Он же острый ларинготрахеит.
Он же ложный круп.
Состояние, при котором на фоне ОРВИ развивается:
🔹 Лающий кашель;
🔹 Осиплость голоса;
🔹 Шумный ВДОХ с затрудненным дыханием.
Причина — воспаление слизистой в области голосовых складок гортани.
Чаще всего встречается у детей до 3 лет.
Основная причина Такой реакции на ОРВИ — наследственность. У родителей, страдавших в детстве от ложного крупа, и дети, скорее всего, будут этим страдать.
Важно знать:
🔹 Эти эпизоды пройдут с возрастом.
🔹 НЕ связаны с аллергией.
Типичная картина: у ребенка признаки ОРВИ (насморк, температура).
Ночью ребенок просыпается от дающего кашля и затрудненного дыхания.
Он испуган, плачет, может быть возбужден.
Что делать?
1️⃣ Успокоиться самим и успокоить ребенка. Ларинготрахеит в большинстве случаев не угрожает жизни и проходит самостоятельно (хотя выглядит это страшно, особенно в первый раз). Лечить можно дома. К тому же чем выраженнее беспокойство у ребенка, тем тяжелее ему дышать.
Возьмите на руки, утешьте, включите мультик.
2️⃣ Откройте окно, чтобы в комнате стало прохладно. Подойдите с ребенком к окну и вместе посмотрите, что там (отвлечение). Включите увлажнитель. Если его нет — идите с ребенком в ванну и включите воду.
3️⃣ Используйте глюкокортикостероиды (ГКС).
Гормоны могут быть в виде таблеток, уколов или ингаляции через небулайзер.
Нет никаких преимуществ у уколов в сравнении с таблетками, так как препарат не мгновенного действия, а эффект наступает в течение 2 часов (да, это не препарат скорой помощи, об этом написано в инструкции)
4️⃣ Доза Пульмикорта выше, чем при обструктивном бронхите — 2 мг за раз.
5️⃣ Если отвлечение, успокоение и гормоны без эффекта — ребенку все ещё тяжело дышать — вызывайте скорую.
Новости Педиатрического университета
С каждым годом все больше детей рождаются преждевременно и выхаживаются с применением искусственной вентиляции легких. Многие из них впоследствии имеют трудности с дыханием из-за заращения гортани (говоря медицинским языком, рубцового стеноза). Чтобы дать возможность таким детям самостоятельно дышать и жить полноценной жизнью, оториноларингологи Педиатрического университета разработали и успешно применяют уникальную реконструкцию гортани и трахеи трансплантатом реберного хряща. О возможностях лечения пациентов со стенозом гортани мы побеседовали с заведующим кафедрой оториноларингологии, доктором медицинских наук Павловым Павлом Владимировичем.
О возможностях лечения пациентов со стенозом гортани мы побеседовали с заведующим кафедрой оториноларингологии, доктором медицинских наук Павловым Павлом Владимировичем.
Павел Владимирович, из-за чего возникает рубцовый стеноз гортани?
Рубцовый стеноз гортани — это тяжелая жизнеугрожающая патология, которая, как правило, является последствием длительной интубации. Эндотрахеальная интубация подразумевает введение специальной трубки в трахею с целью обеспечения проходимости дыхательных путей и вентиляции легких. Эта процедура проводится при остром стенозе гортани, длительной искусственной вентиляции легких у новорожденных с перинатальной патологией, а также у пациентов с черепно-мозговыми травмами, комами, при операциях на сердце. Все перечисленные патологии наиболее часто влекут за собой возникновение рубцового стеноза гортани.
При рубцовом стенозе гортани дети не могут дышать через естественные пути, в подавляющем большинстве случаев дыхание осуществляется через трахеостому. И чтобы их излечить, нужны действительно серьезные реконструктивные вмешательства на гортани и трахее, которые считаются высшим пилотажем в оториноларингологии. Наша кафедра и клиника давно специализируется в этом, непрерывно развивая методики, и сейчас уровень проведения таких манипуляций нашими специалистами не уступает лучшим мировым клиникам. Пациенты едут к нам как со всей России, так из других стран.
И чтобы их излечить, нужны действительно серьезные реконструктивные вмешательства на гортани и трахее, которые считаются высшим пилотажем в оториноларингологии. Наша кафедра и клиника давно специализируется в этом, непрерывно развивая методики, и сейчас уровень проведения таких манипуляций нашими специалистами не уступает лучшим мировым клиникам. Пациенты едут к нам как со всей России, так из других стран.
Сколько раз в год проводятся подобные операции?
Мы выполняем около 80 ларинготрахеопластик в год, примерно половина из них именно при рубцовых стенозах.
Всем ли можно восстановить гортань при стенозе?
Стеноз гортани часто сопровождается тяжелой соматической и неврологической патологией, поэтому операцию иногда нужно откладывать. Когда ребенок подрастает и его состояние улучшается, операция по восстановлению гортани становится возможной.
В чем суть вмешательства?
Выполняется наружный доступ (рассекается гортань), вырезается небольшой фрагмент ребра пациента, из него формируются передние и задние трансплантаты, которые, соответственно, помещаются в переднюю и заднюю стенку гортани, после чего в просвет устанавливается силиконовый стент и рана ушивается. Через месяц производят удаление стента и деканюляцию, т.е. избавление пациента от трахеостомы.
В чем особенность случая с Эдемом?
Каждый двадцатый пациент со стенозом гортани имеет полное ее рубцовое заращение, т.е. просвета в гортани нет вообще. Это действительно большая проблема. Часто рутинные операции по восстановлению дыхательных путей не приносят должного эффекта, возникает повторное сужение гортани, и снова приходится дышать через трахеостому.
В Клинике Педиатрического университета накоплен большой опыт ларинготрахеопластик, поэтому наши уникальные методики позволяют добиться выздоровления даже при полном заращении гортани. Пятилетний Эдем как раз один из таких пациентов. Подробнее о нем расскажет лечащий врач к.м.н. Захарова Мария Леонидовна:
Пятилетний Эдем как раз один из таких пациентов. Подробнее о нем расскажет лечащий врач к.м.н. Захарова Мария Леонидовна:
«Трахеостома была наложена Эдему в месячном возрасте из-за стеноза гортани, после продленной интубации. Неоднократные попытки лечения по месту жительства привели только к ухудшению состояния ребенка, у него сформировался полный рубцовый стеноз. В оториноларингологическом отделении Клиники Педиатрического университета ему сделали ларинготрахеальную реконструкцию с постановкой фрагментов собственных ребер, в переднюю и заднюю стенку гортани и месячным стентированием. После удаления стента у него сформировался правильный просвет гортани, трахеостома зажила, восстановлено дыхание через естественные пути. Поскольку у Эдема не было подачи воздуха на голосовые связки, то пока он не может разговаривать. Но теперь, после восстановления полноценного дыхания, говорить он обязательно научится».
Павел Владимирович, у Эдема хороший прогноз?
Да.
То есть в результате проведенной операции он выздоровеет?
Да, он уже дышит через естественные пути, отверстие от трахеостомы закрылось и зажило, теперь нужна реабилитация, чтобы восстановился голос, и это уже задача педагогов.
Успешное устранение стеноза гортани у 2-х летнего ребенка — НАУЧНО-ПРАКТИЧЕСКИЙ ЦЕНТР СПЕЦИАЛИЗИРОВАННОЙ МЕДИЦИНСКОЙ ПОМОЩИ ДЕТЯМ имени В.Ф.Войно-Ясенецкого
В ЛОР отделение нашего Центра поступил ребенок в возрасте двух лет и пяти месяцев для проведения хирургического вмешательства на гортани.
Предыстория этого случая такова. Девочка родилась недоношенной на 27 неделе беременности с патологией бронхо-лёгочной системы и врождённой патологией зрения. Она не могла дышать самостоятельно и с самого рождения находилась на ИВЛ. На седьмой день жизни пациентку перевели на самостоятельное дыхание, а позднее выписали домой под наблюдение педиатра, но проблемы с нормальным дыхание всё же остались. Они проявилось в 2018 году, когда ей была проведена плановая операция по коррекции зрения под эндотрахеальным наркозом. Сразу после оперативного вмешательства у девочки начались выраженные проблемы с дыханием, и в экстренном порядке ребенку была установлена трахеостома. При обследованиях на компьютерной томографии органов шеи и грудной клетки врачи обнаружили интенсивное сужение гортани в подскладочном пространстве и трахеи на протяжении 1 см. Был поставлен диагноз: рубцовый стеноз гортани.
Они проявилось в 2018 году, когда ей была проведена плановая операция по коррекции зрения под эндотрахеальным наркозом. Сразу после оперативного вмешательства у девочки начались выраженные проблемы с дыханием, и в экстренном порядке ребенку была установлена трахеостома. При обследованиях на компьютерной томографии органов шеи и грудной клетки врачи обнаружили интенсивное сужение гортани в подскладочном пространстве и трахеи на протяжении 1 см. Был поставлен диагноз: рубцовый стеноз гортани.
В 2019 году родители девочки обратились к зарубежным специалистам, которые предприняли попытку восстановления просвета гортани путем баллонной дилатации, но она не привела к положительному эффекту.
В ЛОР отделение НПЦ ребенок поступил в состоянии средней тяжести на самостоятельном адекватном дыхании через трахеостомическую трубку, без признаков воспаления. При выполнении фиброларингоскопии врачи отметили рубцовое сужение гортани, перекрывающее на 2/3 просвет подскладочного пространства.
На консилиуме было принято решение о проведении операции – клиновидной ларингопластики под эндоскопическим контролем. Специалистами ЛОР-отделения рубцовая ткань была полностью удалена, просвет гортани и трахеи восстановлен на всем их протяжении.
Осложнений во время операции не было, и девочку выписали из ЛОР отделения в удовлетворительном состоянии. Первым этапом успешного хирургического лечения родители остались довольны.
Через 6 месяцев после окончательного заживления послеоперационной раны с формированием достаточного просвета подскладочного пространства ребенку будет удалена трахеостомическая трубка и девочку переведут на самостоятельное дыхание.
Приобретенные гортаннотрахеальные стенозы у детей | #10/01
Обзор литературы
Приобретенные гортаннотрахеальные стенозы остаются одной из сложнейших проблем детской оториноларингологии. Это связано не только с трудностью и многоэтапностью восстановления просвета дыхательных путей, но и с сочетанным с дыхательным стенозом и длительным трахеальным канюленосительством развитием патологических изменений в других органах и системах организма. Такие изменения приводят к инвалидности и социальной неполноценности, что требует тесного взаимодействия специалистов нескольких педиатрических дисциплин, таких, как оториноларингология, анестезиология, реаниматология, хирургия, пульмонология, гастроэнтерология, генетика [5, 10, 13, 18].
Это связано не только с трудностью и многоэтапностью восстановления просвета дыхательных путей, но и с сочетанным с дыхательным стенозом и длительным трахеальным канюленосительством развитием патологических изменений в других органах и системах организма. Такие изменения приводят к инвалидности и социальной неполноценности, что требует тесного взаимодействия специалистов нескольких педиатрических дисциплин, таких, как оториноларингология, анестезиология, реаниматология, хирургия, пульмонология, гастроэнтерология, генетика [5, 10, 13, 18].
Ведущей причиной формирования рубцовых стенозов гортани является продленная чрезгортанная назотрахеальная интубация, проводимая по поводу острого стенозирующего ларинготрахеобронхита, операций и иных экстремальных ситуаций, требующих реанимационных мероприятий и искусственной вентиляции легких [5, 7, 11, 13, 33]. Повреждение тканей гортани при проведении интубации возникает в случае превышения капиллярного давления. Это вызывает ишемию тканей с последующим развитием воспаления, отека, изъязвления слизистой оболочки и дальнейшим возникновением хондроперихондрита и некроза, что можно сравнить с развитием «гортанного пролежня» [14]. Кроме того, стенозы могут быть связаны со спортивной, бытовой, транспортной и медицинской травмами [2, 14, 34, 35].
Кроме того, стенозы могут быть связаны со спортивной, бытовой, транспортной и медицинской травмами [2, 14, 34, 35].
При бактериологическом исследовании отделяемого из трахеи у детей, нуждающихся в восстановительном лечении по поводу рубцового стеноза гортани, отмечается полимикробная флора (до восьми типов микроорганизмов одновременно), в том числе сочетание как аэробной, так и анаэробной флоры [15]; при этом, характер микробной флоры у детей и взрослых различается. Чаще всего у детей инфицирование происходит Pseudomonas aeruginosa, Staphylococcus aureus, Acinetobacter и Haemophilus influenzae [31].
Рентгенографическое исследование, являющееся наиболее распространенным дополнительным методом диагностики [2, 44], в связи с малой контрастностью тканевых структур гортани не всегда дает объективную картину [42], а ультразвуковое исследование гортани к настоящему времени еще не получило широкого распространения [4]. «Золотым стандартом» диагностики рубцового стеноза гортани и трахеи являются прямая микроларингоскопия и трахеобронхоскопия с использованием операционного микроскопа и оптических трубок [13, 18, 23, 36]. Эти методы позволяют точно оценить протяженность и степень стеноза, его характер и локализацию; следует также иметь в виду, что у 1/5–1/2 пациентов возможны комбинированные поражения на различных уровнях дыхательных путей [18, 23].
Эти методы позволяют точно оценить протяженность и степень стеноза, его характер и локализацию; следует также иметь в виду, что у 1/5–1/2 пациентов возможны комбинированные поражения на различных уровнях дыхательных путей [18, 23].
В результате повреждения дыхательных путей могут формироваться различные виды обструкции. Повреждения гортани у новорожденных и детей младшего возраста часто (до 22% случаев) протекают с явлениями хондроперихондрита, лечение которого включает в себя противовоспалительную и гормональную терапию [9]. У детей младшего возраста эндоскопическое бужирование гортани в сочетании с противовоспалительным лечением в процессе формирования рубцовой ткани при ее незрелости и остаточных воспалительных процессах на ограниченном участке может оказаться эффективным. В то же время диффузный перихондрит хрящевого каркаса гортани и сформировавшийся рубец являются противопоказаниями к проведению бужирования [11].
Наиболее тяжелое осложнение чрезгортанной интубации трахеи и трахеостомии — это развитие рубцового стеноза. Рубцы могут локализоваться в различных отделах дыхательных путей — между черпаловидными хрящами, на уровне голосовых складок, в подскладковом отделе, в шейном и грудном отделах трахеи [14, 32]. По данным Э. А. Цветкова (1996), более чем у 70% больных детей рубцовый процесс занимает подголосовой отдел гортани и гортаннотрахеальное сочленение. Согласно исследованиям А. Д. Понкратенко, Е. К. Онуфриевой (1997), среди 183 детей с рубцовым стенозом гортани рубцы локализовались в голосовом отделе у 36 больных, в подскладковом — у 118, сочетанное поражение разных отделов гортани отмечено у 29 пациентов.
Рубцы могут локализоваться в различных отделах дыхательных путей — между черпаловидными хрящами, на уровне голосовых складок, в подскладковом отделе, в шейном и грудном отделах трахеи [14, 32]. По данным Э. А. Цветкова (1996), более чем у 70% больных детей рубцовый процесс занимает подголосовой отдел гортани и гортаннотрахеальное сочленение. Согласно исследованиям А. Д. Понкратенко, Е. К. Онуфриевой (1997), среди 183 детей с рубцовым стенозом гортани рубцы локализовались в голосовом отделе у 36 больных, в подскладковом — у 118, сочетанное поражение разных отделов гортани отмечено у 29 пациентов.
Хирургическое устранение рубцового стеноза возможно двумя принципиально разными доступами — через естественные пути или с рассечением гортани и трахеи. Эндоскопические хирургические вмешательства при рубцовых стенозах всегда предпочтительнее эндоларингеальных с наружным доступом [11, 29]. Прямая микроларингоскопия и эндоларингеальная микрохирургия, особенно с использованием лазерной техники, позволяет у значительной части больных устранить рубцовый стеноз гортани и гортаннотрахеального отдела с достаточно хорошим функциональным эффектом. Лазерные операции практически бескровны, отличаются малой травматичностью и вследствие этого не сопровождаются выраженными реактивными явлениями. Другим преимуществом лазерных операций по сравнению с операцией наружным доступом является интактность хрящевого остова, что способствует более быстрому заживлению и восстановлению просвета гортани, позволяя максимально сохранить голосовую функцию [13]. Особенности процессов репарации после лазерных операций дают возможность у большинства больных, в том числе у детей младшего (до трех лет) возраста, восстанавливать просвет дыхательных путей без дополнительного применения стентов [1, 9, 13], хотя в ряде случаев их приходится использовать для поддержания воссозданного просвета [6, 48]. Лазерная хирургия рубцовых стенозов эффективна также в случаях, когда предыдущие операции с применением других методик не дали хорошего результата [37]. Катамнестические наблюдения свидетельствуют о том, что воссозданный с помощью лазерной операции просвет дыхательных путей сохраняется с ростом гортани и обеспечивает нормальную дыхательную функцию [5].
Лазерные операции практически бескровны, отличаются малой травматичностью и вследствие этого не сопровождаются выраженными реактивными явлениями. Другим преимуществом лазерных операций по сравнению с операцией наружным доступом является интактность хрящевого остова, что способствует более быстрому заживлению и восстановлению просвета гортани, позволяя максимально сохранить голосовую функцию [13]. Особенности процессов репарации после лазерных операций дают возможность у большинства больных, в том числе у детей младшего (до трех лет) возраста, восстанавливать просвет дыхательных путей без дополнительного применения стентов [1, 9, 13], хотя в ряде случаев их приходится использовать для поддержания воссозданного просвета [6, 48]. Лазерная хирургия рубцовых стенозов эффективна также в случаях, когда предыдущие операции с применением других методик не дали хорошего результата [37]. Катамнестические наблюдения свидетельствуют о том, что воссозданный с помощью лазерной операции просвет дыхательных путей сохраняется с ростом гортани и обеспечивает нормальную дыхательную функцию [5].
Одним из главных критериев отбора больных для эндоскопической лазерной хирургии является протяженность рубца, которая не должна превышать 1,5-2 см [1, 7, 13, 25]. Лечение оказывается малоэффективным при вовлечении в рубцовый процесс хрящевого скелета [7]. Кроме того, необходимо учитывать фазу формирования стеноза. В тех случаях, когда имеются явления хондроперихондрита, вопрос о необходимости лазерной операции целесообразно отложить до ликвидации воспалительных явлений [9]. Предпочтительнее всего проводить операцию через год и более после травматического повреждения гортани и формирования стеноза, однако положительного результата удается достичь и при лечении детей в ближайшие сроки (до двух месяцев) после травмы дыхательных путей [12]. При анализе результатов повторных операций по поводу рубцового стеноза гортани отмечается определенная связь: при неэффективном первичном хирургическом вмешательстве в 50% наблюдений результат повторной операции оказывается аналогичным. Показанием к повторной операции является хотя бы минимальный эффект от предыдущей — небольшое увеличение просвета дыхательной трубки [13, 29]. При удовлетворительном результате первичной операции повторная в 80-90% наблюдений приводит к дальнейшему улучшению [12].
Показанием к повторной операции является хотя бы минимальный эффект от предыдущей — небольшое увеличение просвета дыхательной трубки [13, 29]. При удовлетворительном результате первичной операции повторная в 80-90% наблюдений приводит к дальнейшему улучшению [12].
Показаниями к операции по устранению рубцового стеноза гортани наружным доступом служат протяженный (более 1-3 см) рубец, потеря хрящевой опоры выше или в области трахеостомы, отсутствие эффекта от эндоскопических операций, в том числе проводимых с помощью лазера [13, 26]. В литературе имеется скудная информация об оптимальных сроках подобных операций у детей. В то же время случаи возникновения различного рода осложнений и гибели детей при случайной деканюляции или закупорке трахеотомической трубки коркой наблюдаются достаточно часто и составляют до 4,6% [49]. Ларингостомия и длительное формирование просвета гортани с применением Т-образной трубки у детей затруднены, так как относительно толстые стенки трубки суживают и без того неширокий просвет дыхательных путей, вызывая развитие дисфагических явлений, бронхитов, аспирационных пневмоний, асфиксии [41]; применение Т-образных трубок эффективно только у 50% пациентов в возрасте до 10 лет по сравнению с 80% больных старше 10 лет [20]. Реконструктивные операции у детей младшего возраста имеют высокий статистически значимый риск неудачи, несмотря даже на меньшую тяжесть повреждения дыхательных путей, по сравнению со старшими детьми [50]. В то же время некоторые авторы рекомендуют оперировать детей раннего возраста как можно раньше в целях восстановления нормального речевого общения; при этом хронические трахеоканюляры, по сравнению с ранее не трахеотомированными больными, требуют более агрессивной тактики лечения; они имеют меньше шансов на успех операции, у таких больных чаще развиваются осложнения в послеоперационном периоде [25]. Среди новорожденных и детей младшего возраста предрасполагающими факторами к развитию осложнений являются вес меньше 4 кг и гестационный срок меньше 30 недель [28].
Реконструктивные операции у детей младшего возраста имеют высокий статистически значимый риск неудачи, несмотря даже на меньшую тяжесть повреждения дыхательных путей, по сравнению со старшими детьми [50]. В то же время некоторые авторы рекомендуют оперировать детей раннего возраста как можно раньше в целях восстановления нормального речевого общения; при этом хронические трахеоканюляры, по сравнению с ранее не трахеотомированными больными, требуют более агрессивной тактики лечения; они имеют меньше шансов на успех операции, у таких больных чаще развиваются осложнения в послеоперационном периоде [25]. Среди новорожденных и детей младшего возраста предрасполагающими факторами к развитию осложнений являются вес меньше 4 кг и гестационный срок меньше 30 недель [28].
Для формирования стойкого просвета гортани осуществляются различные варианты редрессации печатки перстневидного хряща [8, 11, 46], ларинготрахеальной декомпрессии с расширением просвета дыхательных путей (в области как передней, так и задней стенки), в том числе путем пересадки аутохряща (реберного, ушной раковины, перегородки носа) [17, 19, 40], васкуляризированного трансплантата из тела подъязычной кости с грудинно-подъязычной мышцей [11, 24, 27] и других тканей. Наиболее частыми причинами неудач операций, проведенных наружным доступом, являются недостаточная предоперационная диагностика гортаннотрахеального стеноза, интраоперационные дефекты, ошибки, связанные с выбором типа и длины стента и длительностью его использования, склонность к развитию келлоидных рубцов, недостаточное послеоперационное наблюдение [16], а также такая сопутствующая патология, как ларингомаляция, трахеомаляция и пролапс черпаловидных хрящей [38]. В ряде случаев для успешной деканюляции требуется несколько повторных операций наружным доступом; лечение может затягиваться на десятки лет [22]. Противопоказаниями к операции наружным доступом являются незаконченный процесс рубцевания, тяжелые поражения ЦНС, заболевания легких, неизлеченное первичное заболевание, невозможность послеоперационного наблюдения и лечения [11, 25].
Наиболее частыми причинами неудач операций, проведенных наружным доступом, являются недостаточная предоперационная диагностика гортаннотрахеального стеноза, интраоперационные дефекты, ошибки, связанные с выбором типа и длины стента и длительностью его использования, склонность к развитию келлоидных рубцов, недостаточное послеоперационное наблюдение [16], а также такая сопутствующая патология, как ларингомаляция, трахеомаляция и пролапс черпаловидных хрящей [38]. В ряде случаев для успешной деканюляции требуется несколько повторных операций наружным доступом; лечение может затягиваться на десятки лет [22]. Противопоказаниями к операции наружным доступом являются незаконченный процесс рубцевания, тяжелые поражения ЦНС, заболевания легких, неизлеченное первичное заболевание, невозможность послеоперационного наблюдения и лечения [11, 25].
В последние годы появились сообщения об устранении обширных стенозов гортани и трахеи у детей путем резекции стенозированного участка с последующим наложением межтрахеального и гортаннотрахеального анастомозов [30, 39]. Показанием к операции является изолированный подскладковый или трахеальный стеноз, расположенный как минимум на 10 мм ниже голосовых складок; протяженность стеноза должна быть от 1 до 6 см [45]. При формировании анастомоза между гортанью и трахеей возникают значительные трудности из-за несоответствия размеров сшиваемых концов. Эти операции в основном используются при лечении взрослых больных; к настоящему времени отдаленные результаты такого лечения у детей еще не изучены (хотя эксперимент на кроликах показал адекватный рост дыхательных путей после резекции перстневидного хряща и первого кольца трахеи [47]), у них высок риск развития дигисценций в области анастомоза, повреждения возвратных нервов; кроме того, в случае неудачи операции дальнейшее лечение крайне затруднительно [18]. Даже незначительный отек тканей в месте анастомоза может вызывать у ребенка выраженный дыхательный стеноз, связанный с малым диаметром трахеи; при этом трахея ребенка менее толерантна к растяжению, чем у взрослого, в связи с чем резекция у ребенка возможна лишь на относительно меньшей, по сравнению со взрослым, части трахеи [21].
Показанием к операции является изолированный подскладковый или трахеальный стеноз, расположенный как минимум на 10 мм ниже голосовых складок; протяженность стеноза должна быть от 1 до 6 см [45]. При формировании анастомоза между гортанью и трахеей возникают значительные трудности из-за несоответствия размеров сшиваемых концов. Эти операции в основном используются при лечении взрослых больных; к настоящему времени отдаленные результаты такого лечения у детей еще не изучены (хотя эксперимент на кроликах показал адекватный рост дыхательных путей после резекции перстневидного хряща и первого кольца трахеи [47]), у них высок риск развития дигисценций в области анастомоза, повреждения возвратных нервов; кроме того, в случае неудачи операции дальнейшее лечение крайне затруднительно [18]. Даже незначительный отек тканей в месте анастомоза может вызывать у ребенка выраженный дыхательный стеноз, связанный с малым диаметром трахеи; при этом трахея ребенка менее толерантна к растяжению, чем у взрослого, в связи с чем резекция у ребенка возможна лишь на относительно меньшей, по сравнению со взрослым, части трахеи [21]. По мнению В. Г. Зенгера (2001), при циркулярной резекции трахеи и дополнительной мобилизации подъязычной кости происходит вмешательство в очень сложный механизм, обеспечивающий одну из важнейших функций гортани — защитную, так как возникает опасность проявления аспирационных осложнений. В случае возникновения осложнений необходимо дополнительное разобщение отрезков воздухопроводящих путей, т. е. выполнение трахеостомии и введение трахеальной канюли с раздувной манжеткой, что сводит на нет все преимущества столь сложной и небезопасной для больного операции. Поэтому возможность частичной резекции дыхательных путей с наложением анастомоза должна рассматриваться лишь в качестве крайнего варианта [3].
По мнению В. Г. Зенгера (2001), при циркулярной резекции трахеи и дополнительной мобилизации подъязычной кости происходит вмешательство в очень сложный механизм, обеспечивающий одну из важнейших функций гортани — защитную, так как возникает опасность проявления аспирационных осложнений. В случае возникновения осложнений необходимо дополнительное разобщение отрезков воздухопроводящих путей, т. е. выполнение трахеостомии и введение трахеальной канюли с раздувной манжеткой, что сводит на нет все преимущества столь сложной и небезопасной для больного операции. Поэтому возможность частичной резекции дыхательных путей с наложением анастомоза должна рассматриваться лишь в качестве крайнего варианта [3].
Несмотря на использование различных по технике операций, эффективность устранения рубцового стеноза гортани и деканюляции достигает, согласно наблюдениям различных авторов, 63–64 % [5, 11, 18, 43]. На эффективность лечения влияют степень сужения дыхательных путей и протяженность стеноза: если при стенозе гортани до 70% просвета удается деканюлировать до 100% детей, то при полной атрезии органа эффективность оперативного вмешательства снижается до 67% деканюлированных больных (в том числе и после повторных операций) [46]; кроме того, чем короче стенозированный участок, тем результативнее лечение [12]. По мнению B. Benjamin (1993), при сочетанном поражении складкового и подскладкового отделов гортани, особенно при их тотальной облитерации рубцовой тканью, реконструктивные операции достигают успеха приблизительно в 50% случаев.
По мнению B. Benjamin (1993), при сочетанном поражении складкового и подскладкового отделов гортани, особенно при их тотальной облитерации рубцовой тканью, реконструктивные операции достигают успеха приблизительно в 50% случаев.
Литература
- Богомильский М. Р., Гаращенко Т. И., Онуфриева Е. К. и др. Эндоскопическое применение хирургических лазеров при стойких обструктивных процессах в гортанной части глотки, гортани и трахее у детей // Вестник оторинолар. 1999. № 1. С. 39-41.
- Зенгер В. Г., Наседкин А. Н. Повреждения гортани и трахеи. М.: Медицина, 1991. 221 с.
- Зенгер В. Г. К вопросу о восстановлении просвета гортани после ее циркулярной резекции с последующей окклюзией и хроническим канюленосительством / Заболевания голосового аппарата и верхних дыхательных путей / Юбилейный сб. науч. трудов симпозиума, посвященного 10-летию Ассоциации фониатров и фонопедов, 24-27 мая 2001 г. (г. Владимир). Москва — Владимир, 2001. С. 193-196.

- Петухова Л. И., Солдатский Ю. Л., Быковский В. А., Романов Д. В. Ультразвуковые аспекты диагностики заболеваний гортани у детей младшего возраста // Эхография. 2000. Т. 1. № 3. С. 330-334.
- Понкратенко А. Д., Онуфриева Е. К. Отдаленные результаты эндоскопической СО2 -лазерной хирургии рубцовых стенозов гортани у детей // Вестник оторинолар. 1997. № 4. С. 16-19.
- Понкратенко А. Д., Солдатский Ю. Л., Нурмухаметов Р. Х. Применение стентов в СО2-лазерной эндоскопической хирургии рубцовых стенозов гортани у детей // Новости оториноларингологии и логопатологии. 1998. № 1. С. 80-83.
- Руин А. Г. Проблемы деканюляции у детей с хроническим трахеальным канюленосительством при рубцовых стенозах гортани и шейного отдела трахеи: Автореф. дис. … канд. мед. наук. М., 2000. 20 с.
- Савин А. Н. Ларингопластика с редрессацией задней стенки гортани при рубцовых и паралитических стенозах. Автореф. дис. … канд. мед. наук. СПб., 1997.
 22 с.
22 с. - Солдатский Ю. Л., Понкратенко А. Д., Онуфриева Е. К. Лазерная хирургия постинтубационных стенозов гортани у детей младшего возраста // Лазерная медицина. 1999. Т. 3. № 2. C. 18-21.
- Фадеева И. А. Гортанно-кардиальные взаимодействия у детей // Новости оториноларингологии и логопатологии. 1998. № 1. С. 84-89.
- Цветков Э. А. Современные проблемы этиологии и лечения рубцовых стенозов гортани у детей // Новости оториноларингологии и логопатологии. 1996. № 3-4. С. 76-78.
- Чирешкин Д. Г., Зенгер В. Г., Онуфриева Е. К., Шустер А. М. Об оптимизации хирургического лечения детей с приобретенным рубцовым стенозом гортани и шейного отдела трахеи // Вестник оторинолар. 1991. № 6. С. 47-51.
- Чирешкин Д. Г. Хроническая обструкция гортанной части глотки, гортани и трахеи у детей. Этиология, клиника и методы устранения. М.: Рапид-Принт. 1994. 144 с.
- Benjamin B. Prolonged intubation injuries of the larynx: endoscopic diagnosis, classification, and management //Ann Otol Rhinol Laryngol.
 1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p.
1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p. - Brown O. E., Manning S. C. Microbial flora of the subglottis in intubated pediatric patients // Int. J. Pediatr Otorhinolaryngol. 1996. Vol. 35. № 2. P. 97-105.
- Choi S. S., Zalzal G. H. Pitfalls in laryngotracheal reconstruction // Arch. Otolaryngol. Head Neck. Surg. 1999. Vol. 125. № 6. P. 650-653.
- Cotton R. T., Myer C. M. 3d, O’Connor D. M., Smith M. E. Pediatric laryngotracheal reconstruction with cartilage grafts and endotracheal tube stenting: The single-stage approach // Laryngoscope. 1995. Vol. 105. № 8. Pt. 1. P. 818-821.
- Cotton R. T. Management of subglottic stenosis // Otolaryngol. Clin. Norht. Am. 2000. Vol. 33, № 1. P. 111-130.
- De Jong A. L., Park A. H., Raveh E., Schwartz M. R., Forte V. Comparsion of thyroid, auricular, and costal cartilage donor sites for laryngotracheal reconstruction in an animal model // Arch. Otolaryngol. Head. Neck. Surg. 2000.
 Vol. 126. № 1. P. 49-53.
Vol. 126. № 1. P. 49-53. - Gaissert H. A., Grillo H. C., Mathisen D. J., Wain J. C. Temporary and permanent restoration of airway continuity with the tracheal T tube // J. Thorac. Cardiovasc. Surg. 1994. Vol. 107. № 2. P. 600-606.
- Grillo H. C. Pediatric tracheal problems // Chest Surg Clin North Am. 1996. Vol. 6. № 4. P. 693-700.
- Gustafson L. M., Hartley B. E. J., Cotton R. T. Acquired total (grade 4) subglottic stenosis in children //Ann. Otol. Rhinol. Laryngol. 2001. Vol. 110. № 1. P. 16-19.
- Holinger L. D., Lusk R. P., Green C. G. Pediatric laryngology and bronchoesophagology. Philadelphia-New York: Lippincott-Raven, 1997. 402 p.
- Keghian J., Lawson G., Orban D., Remacle M. Composite hyoid-sternohyoid interposition graft in the surgical treatment of laryngotracheal stenosis // Eur. Arch. Oto-Rhino-Lar. 2000. Vol. 257. № 10. P. 542-547.
- Lesperance M. M., Zalzal G. H. Laryngotracheal stenosis in children // Eur Arch Otorhinolaryngol.
 1998. Vol. 255. № 1. P. 12-17.
1998. Vol. 255. № 1. P. 12-17. - McCaffrey T. V. Management of laryngotracheal stenosis on the basis of site and severity // Otolaryngol. Head. Neck. Surg. 1993. Vol. 109. № 3. Pt 1. P. 468-473.
- McGuirt W. F. Jr., Little J. P., Healy G. B. Anterior cricoid split. Use of hyoid as autologous grafting material // Arch. Otolaryngol. Head. Neck. Surg. 1997. Vol. 123. № 12. P. 1277-1280.
- McQueen C. T., Shapiro N. L., Leighton S., Guo X. G., Albert D. M. Single-stage laryngotracheal reconstruction. The Great Ormond experience and guidelines for patient selection // Arch. Otolaryngol. Head. Neck. Surg. 1999. Vol. 125. № 3. P. 320-322.
- Mehta A. C., Harris R. J., De Boer G. E. Endoscopic management of binign airway stenosis // Clin. Chest. Med. 1995. Vol. 16. № 3. P. 401-413.
- Monnier P., Lang F., Savary M. Partial cricotracheal resection for severe pediatric subglottic stenosis: update of the Lausanne experience // Ann Otol.
 Rhinol. Laryngol. 1998. Vol. 107. № 11, Pt. 1. P. 961-968.
Rhinol. Laryngol. 1998. Vol. 107. № 11, Pt. 1. P. 961-968. - Morar P., Singh V., Jones A. S., Hughes J., van Saene R. Impact of tracheotomy on colonization and infection of lower airways in children requiring long-term ventilation: a prospective observational cohort study // Chest. 1998. Vol. 113. № 1. P. 77-85.
- Myer C. M.3d, Hartley B. E .J. Pediatric laryngotracheal surgery // Laryngoscope. 2000. Vol. 110. № 11. P. 1875-1883.
- Pereira K. D., Mitchell R. B., Younis R. T., Lazar R. H. Subglottic stenosis complicating cardiac surgery in children // Chest. 1997. Vol. 111. № 6. P. 1769-1772.
- Perkins J. A., Inglis A. F. Jr., Richardson M. A. Iatrogenic airway stenosis with reccurrent respiratory papillomatosis // Arch. Otolaryngol. Head. Neck. Surg. 1998. Vol. 124. № 3. P. 281-287.
- Randestad A., Lindholm C. E., Fabian P. Dimensions of the cricoid cartilage and the trachea // Laryngoscope. 2000. Vol. 110. № 11. P. 1957-1961.

- Richtsmeier W. J., Scher R. L. Telescopic laryngeal and pharyngeal surgery // Ann. Otol. Rhinol. Laryngol. 1997. Vol. 106. № 12. P. 995-1001.
- Rimell F. L., Dohar J. E. Endoscopic management of pediatric posterior glottic stenosis // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 4. P. 285-290.
- Rutter M. J., Link D. T., Liu J. H., Cotton R. T. Laryngotracheal reconstruction and the hidden airway lesion // Laryngoscope. 2000. Vol. 110. № 11. P. 1871-1874.
- Rutter M. J., Hartley B. E. J., Cotton R. T. Cricotracheal resection in children // Arch. Otolaryngol. Head. Neck. Surg. 2001. Vol. 127. № 3. P. 289-292.
- Silva A. B., Lusk R. P., Muntz H. R. Update on the of auricular cartilage in laryngotracheal reconstruction // Ann. Otol. Rhinol. Laryngol. 2000. Vol. 109. № 4. P. 343-347.
- Stern Y., Willging P. J., Cotton R. T. Use of Montgomery T-tube in laryngotracheal reconstruction in children: is it safe? // Ann.
 Otol. Rhinol. Laryngol. 1998. Vol. 107. № 12. P. 1006-1009.
Otol. Rhinol. Laryngol. 1998. Vol. 107. № 12. P. 1006-1009. - Tostevin P. M., de Bruyn R., Hosni A., Evans J. N. The value of radiological investigations in pre-endoscopic assessment of children with stridor // J. Laryngol. Otol. 1995. Vol. 109. № 9. P. 844-848.
- Triglia J. M., Nicollas R., Roman S. Management of subglottic stenosis in infancy and childhood // Eur. Arch. Oto-Rhino-Lar. 2000. Vol. 257. № 7. P. 382-385.
- Walner D. L., Ouanounou S., Donnelly L. F., Cotton R. T. Utility of radiographs in the pediatric airway obstruction // Ann. Otol. Rhinol .Laryngol. 1999. Vol. 108. № 4. P. 378-383.
- Walner D. L., Stern Y., Cotton R.T. Margins of partial cricotracheal resection in children // Laryngoscope. 1999. Vol. 109. № 10. P. 1607-1610.
- Ward R. F., Gordon M., Rabkin D., April M. M. Modifications of airway reconstruction in children // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 5. Pt 1. P. 365-369.
- Ward R. F., Triglia J. M. Airway growth after cricotracheal resection in a rabbit model and clinical application to the treatment of subglottic stenosis in children // Laryngoscope. 2000. Vol. 110. № 5. P. 835-844.
- Werkhaven J. A., Beste D. Diagnosis and management of pediatric laryngeal stenosis // Otolaryngol. Clin. North Am. 1995. Vol. 28. № 4. P. 797-808.
- Wetmore R. F., Marsh R. R., Thompson M. E., Tom L. W. C. Pediatric tracheotomy: a changing procedure? // Ann. Otol. Rhinol. Laryngol. 1999. Vol. 108. № 7. Pt 1. P. 695-699.
- Zalzal G. H., Choi S. S., Patel K. M. Ideal timing of pediatric laryngotracheal reconstruction // Arch. Otolaryngol. Head. Neck. Surg. 1997. Vol. 123. № 2. P. 206-208.
Стеноз гортани у детей: виды, степени и стратегии лечения
Вступление: Стеноз гортани у детей встречается нечасто и обычно является вторичным после интубации трахеи. Цели этого исследования состояли в том, чтобы рассмотреть результаты отдельных эндоскопических и хирургических процедур и предложить техническую модификацию для одного из них.
Методы: Ретроспективный обзор пациентов с диагнозом стеноза гортани, пролеченных в академическом учреждении третичной медицинской помощи в период с 2000 по 2017 год.Были проанализированы следующие переменные: демографические данные, эндоскопические данные, включая анатомический тип и тяжесть поражения, связанные аномалии, тип лечения, исходы и время последующего наблюдения.
Полученные результаты: В исследование были включены 78 детей (39 мальчиков) со средним возрастом на момент постановки диагноза 9 месяцев, и у 33 (42,3%) была выявлена сопутствующая аномалия. Поражения были приобретены у 84 человек.В 6% случаев наиболее часто поражалась подсвязочная область (77%). Тридцать пациентов (38,4%) имели стеноз тяжелой степени (III и IV степени по Майер-Коттону), а 38 пациентам (48,7%) в качестве начального лечения была выполнена трахеотомия. В целом, 91% пациентов, подвергшихся эндоскопическому или хирургическому лечению, показали хороший результат, а частота деканюляции в серии составила 79,4%. Четырнадцати пациентам велось консервативное лечение. Медиана наблюдения составила 29 месяцев (внутренний диаметр 10–60 мес.). ВЫВОДЫ: Стеноз гортани у детей обычно приобретенный и имеет широкий спектр анатомических проявлений.Эндоскопические терапевтические процедуры могут быть полезны при лечении незрелого стеноза низкой степени. Реконструктивные хирургические методы могут обеспечить высокий уровень успеха при соответствующем отборе кандидатов.
Ключевые слова: Дети; Стеноз гортани; Реконструкция гортани и трахеи; Частичная резекция крикотрахеального отдела; Трахеотомия.
Подсвязочный стеноз | Детская больница Филадельфии
Подсвязочный стеноз (SGS) — это сужение дыхательных путей ниже голосовых связок (над голосовыми связками) и над трахеей.Подсвязочный стеноз будет включать сужение перстневидного хряща, единственного полного хрящевого кольца в дыхательных путях. Это сужение часто вызывается рубцами в гортани чуть ниже голосовых связок, но также может затрагивать голосовые связки и влиять на голос.
Подсвязочный стеноз бывает двух форм: приобретенный и врожденный.
Эндоскопический вид врожденного стеноза подсвязочного канала.
- Приобретенный стеноз подсвязочного канала часто возникает после длительных периодов интубации и вентиляции при респираторных заболеваниях.
- Врожденный стеноз подсвязочного канала возникает как редкий врожденный дефект и может быть связан с другими генетическими синдромами и состояниями. Дыхательные пути остаются узкими, потому что хрящ дыхательных путей не сформировался должным образом до рождения.
Точная причина рубцевания в настоящее время неизвестна. В отдельных отделениях интенсивной терапии новорожденных есть только небольшое количество младенцев, у которых развивается это состояние, и недостаточно пациентов в каждом отдельном отделении, чтобы иметь статистически значимые данные.Чтобы лучше понять причину стеноза подсвязочного канала, необходимы многоцентровые исследования.
Однако текущие данные свидетельствуют о том, что к ряду важных факторов риска относятся длительная интубация, низкий вес при рождении, рефлюкс, сепсис и другие. Кроме того, трахеостомия может вызвать стеноз или малацию (размягчение) в месте трахеостомии, особенно если она расположена высоко в трахее.
Признаки подсвязочного стеноза включают:
- Шумное дыхание (стридор)
- Респираторный дистресс
- Повторяющийся круп
- Неспособность дышать без трахеостомической трубки
Рентгенограмма шеи показывает подсвязочное сужение (стрелки).Для постановки диагноза важна история конкретных факторов риска. Ваш врач будет искать причины респираторного дистресс-синдрома в отношении длительной интубации и вентиляции, крайних случаев недоношенности, низкой массы тела при рождении, хронической бронхолегочной дисплазии (заболевания легких) и гастроэзофагеального рефлюкса.
Дальнейшее обследование проводится с помощью рентгеновских лучей. Рентген шеи может выявить подсвязочные сужения или подсвязочные образования. На этих снимках трахею оценивают на предмет сужения или стеноза трахеи или полных колец.Окончательный диагноз ставится при эндоскопии с микроларингоскопией и бронхоскопией.
Хирург может определить размер дыхательных путей с помощью пластиковой эндотрахеальной трубки. Степень тяжести стеноза подсвязочного канала классифицируется, как показано на рисунке выше.
Оценка аэродинамического пищеварения
Во время посещения центра дыхательных путей ваш ребенок пройдет обследование у детского гастроэнтеролога, а также оценку питания. Детский пульмонолог также может оценить состояние легких вашего ребенка, а терапевт по речи и глотанию может оценить глотание и голос.Эти специалисты оценят вашего ребенка и определят необходимость дальнейших обследований. Наша группа по планированию хирургического вмешательства организует полное эндоскопическое обследование и обследование желудочно-кишечного тракта в операционной. Это будет включать микроларингоскопию, бронхоскопию (MLB) и эндоскопию верхних отделов желудочно-кишечного тракта (EGD), зондирование импеданса и легочные осциллографы.
Во время EGD биопсии будут взяты с нескольких уровней вверх и вниз по пищеварительному тракту, и они будут проверены на наличие признаков воспаления, указывающих на рефлюкс (ГЭРБ) или воспаление пищевой аллергии (эозинофильный эзофагит).Пациента считают подходящим для операции на дыхательных путях, когда стеноз созрел, ГЭРБ находится под контролем и состояние легких стабильно. Если ГЭРБ не находится под контролем, тогда лечение пациента может быть скорректировано или изменено, и потребуется повторное тестирование. В редких случаях может потребоваться антирефлюксная операция.
Кроме того, перед реконструктивной операцией на дыхательных путях ребенок будет проходить официальную оценку кормления, которая включает эндоскопическую оценку глотания (FEES), проводимую в офисе, или модифицированную глотку с барием.Если ваш ребенок не принимает пищу и полагается исключительно на зонд для кормления, то для обнаружения скопления и аспирации будет использоваться гибкий зонд с несколькими каплями зеленого красителя. Это необходимо для того, чтобы ваш ребенок мог хорошо глотать и защитить свои новые расширенные дыхательные пути после реконструкции. Если эти исследования выглядят достаточно нормально, тогда ребенку может быть проведено хирургическое лечение стеноза подсвязочного канала.
Лечение стеноза подсвязочного канала зависит от того, насколько серьезно он влияет на дыхание ребенка.Кроме того, другие заболевания пациента могут повлиять на решение о том, как лечить стеноз хирургическим путем. Существует множество вариантов лечения, которые зависят от этих и других факторов.
Лечение легких случаев
Система оценок стеноза подсвязочного канала. Легкий стеноз подсвязочного канала: стеноз 1 и 2 степени, а также тонкие перепонки и полосы.
- Наблюдение. В самых легких случаях, когда пациенты могут оставаться бессимптомными, может просто потребоваться тщательное наблюдение.Чаще всего условия улучшаются со временем по мере роста дыхательных путей. Врожденный стеноз 1 степени часто проходит сам по себе и не требует вмешательства. Наблюдение имеет решающее значение для детей с легким стенозом подсвязочного канала, потому что у них чаще возникают проблемы с дыханием при распространенных заболеваниях верхних дыхательных путей (простуда, бронхит).
- Эндоскопическая хирургия. В некоторых случаях стеноза легкой степени может потребоваться эндоскопическое лечение. Тонкие перепонки можно разделить серповидным ножом и расширить с помощью баллона для ангиопластики.Более толстый стеноз также может быть расширен баллоном. Мягкий стеноз и стеноз подсвязочного канала, связанные с системными заболеваниями, такими как ГЭРБ и гранулематоз Вегенера, лучше всего лечить с помощью баллонной дилатации дыхательных путей. Лазеры и микродебридеры (вращающиеся лезвия с приводом, которые сбривают мягкие ткани) также используются для удаления сегментарных участков рубцовой ткани.
Лечение тяжелых случаев
Тяжелый стеноз подсвязочного канала: стеноз 3 и 4 степени.
Почти всем пациентам с тяжелым стенозом подсвязочного аппарата требуется трахеостомическая трубка для дыхания.Часто для коррекции стеноза и достижения деканюляции (удаления трахеостомической трубки) требуется открытая операция по реконструкции ларинготрахеальной хирургии (LTR) или частичная резекция крикотрахеальной артерии (CTR).
Устранение подсвязочного стеноза
Обсуждение подсвязочного стеноза и его лечения — реконструкция гортани и трахеи
LTR. При операции по реконструкции гортани и трахеи хирург использует кусочки реберного хряща для расширения дыхательных путей. Хирург делает вертикальный разрез суженного дыхательного пути снаружи, чтобы восстановить поврежденный участок внутри.Хрящевым трансплантатам с помощью скальпеля придают эллиптическую форму. Задний (задний) трансплантат также имеет эллиптическую форму с выступом, чтобы зафиксировать его в положении за срезанными краями перстневидного хряща (хряща). Трансплантаты могут быть размещены в переднем или заднем положении или в обоих одновременно. LTR может выполняться в один этап, когда трахеотомическая трубка удаляется во время операции, или в два этапа, когда операция выполняется с установленной трахеотомической трубкой. Когда дыхательные пути заживают, трахеотомическую трубку удаляют позже.Существуют определенные показания для одноэтапной или поэтапной операции LTR, и решение принимается индивидуально с учетом особенностей ребенка.
CTR. В наиболее тяжелых случаях может быть выполнена частичная резекция крикотрахеального отдела, когда рубцевание ограничивается подсвязкой и не затрагивает голосовые связки. В ходе этой процедуры рубцовая ткань и большая часть переднего перстневидного хряща вырезаются, и вместо нее восстанавливается нормальная трахея. CTR также может выполняться одноэтапно в более простых ситуациях и поэтапно в более сложных случаях, таких как ревизионная операция.
Показатели долгосрочного успеха как LTR, так и CTR выдаются.
CHOP сообщил, что общий уровень деканюляции у детей, перенесших LTR заднего трансплантата, составил 96 процентов. Это означает, что окончательная скорость деканюляции составляет 96 процентов, но некоторым детям может потребоваться более одной процедуры.
Мы обнаружили 70-процентную частоту деканюляции в зависимости от операции для пациентов, перенесших двухэтапный LTR. В конечном итоге 95 процентов этих пациентов деканюлированы. Скорость деканюляции для конкретной операции — это скорость успешной деканюляции после одной основной операции.
Мы обнаружили, что удельная скорость деканюляции составляет 92 процента для одноступенчатого LTR, а максимальная скорость деканюляции составляет 100 процентов. Эти результаты выгодно отличаются от других сообщений в литературе. Более того, общий уровень успеха зависит от многих факторов, включая патологию, состояние здоровья пациента и предыдущую неудачную операцию, а также другие неизвестные внутренние факторы.
Cheng J, Jacobs I. Ларинготрахеопластика с использованием трансплантата щитовидной железы и хряща для закрытия большого педиатрического кожно-трахеологического свища.International J Ped Otolaryngology. 2012 (в печати).
Дурден Ф., Соболь С. Баллонная ларингопластика как основное лечение стеноза подсвязочного канала. Arch Otolaryngol Head Neck Surg. 2007 август; 133 (8): 772-5.
Майер К., О’Коннор Д., Коттон Р. Предлагаемая система классификации стеноза подсвязочного канала на основе размеров эндотрахеальной трубки. Анн Отол Ринол Ларингол. 1994 апр; 103 (4, п.1): 319-23.
Rizzi MD, Thorne MC, Zur KB, Jacobs IN. Реконструкция гортани с использованием трансплантатов заднего реберного хряща: результаты в одном учреждении.Otolaryngol Head Neck Surg. 2009 Март; 140 (3): 348-53. Цитируется в PubMed; PMID 19248941.
Smith LP, Jur KB, Jacobs IN. Одноэтапная или двухэтапная реконструкция гортани и трахеи. Arch Otolaryngol Head Neck Surg. 2010 Янв; 136 (1): 60-5. Цитируется в PubMed; PMID 20083780.
Подсвязочный стеноз
Симптомы
Симптомы подсвязочного стеноза включают:
- Одышка при физической нагрузке и иногда в покое
- Шумное дыхание (стридор)
- Кашель
- Рецидивный круп
- Изменения голоса, например, охриплость
- Ощущение слизи в дыхательных путях
Причины стеноза подсвязочного канала
Стеноз подсвязочного канала может быть вызван травмой или инфекцией (приобретенной) или возникать при рождении (врожденный).
Врожденный стеноз подсвязочного канала возникает, когда хрящ дыхательных путей не развивается должным образом до рождения и приводит к сужению дыхательных путей.
Приобретенный стеноз подсвязочного канала часто связан с длительным пребыванием в дыхательной трубке. Рубцы от давления трубки на дыхательные пути могут вызвать стеноз. Другие причины могут включать:
- Редкие заболевания, вызывающие воспаление дыхательных путей
- Травма, например, травма от вдыхания химического вещества или вещества, вызывающего ожоги
- Идиопатический (неизвестно)
Диагностика стеноза подсвязочного канала
Подсвязочный канал трудно увидеть и проверить в клинике.Детей часто безуспешно лечат от более распространенных заболеваний, таких как астма, до того, как будет поставлен диагноз подсвязочного стеноза.
Мы используем микроларингоскопию и бронхоскопию для диагностики стеноза подсвязочного канала у детей. Для этих тестов ваш ребенок ложится спать в операционной, и в его дыхательные пути вводят специальный телескоп. Это используется для поиска сужения.
Мы также можем использовать рентген или компьютерную томографию по телефону:
- Проверьте размер дыхательных путей вашего ребенка
- Проверить степень сужения
- Поищите другие образования, которые могут давить на дыхательные пути
Лечение подсвязочного стеноза
Лечение подсвязочного стеноза зависит от тяжести симптомов у ребенка.
- Легкий стеноз подсвязочного канала — ребенку может не потребоваться вмешательство. Однако им нужно будет регулярно посещать врача.
- Умеренный или тяжелый стеноз подсвязочного канала. Ребенку может потребоваться операция, чтобы увеличить размер дыхательных путей. Это поможет им дышать легче. В некоторых случаях ваш врач может захотеть провести трахеотомию ниже уровня сужения дыхательных путей. Это обеспечит вашему ребенку безопасные дыхательные пути и облегчит дыхание.
Когда ваш ребенок будет готов, ваш врач может начать процедуры реконструктивной хирургии дыхательных путей.Это может включать:
Эндоскопическая хирургия
Этот тип хирургии используется у детей со стенозом подсвязочного канала легкой и средней степени тяжести. С помощью камеры узкие части разделяются и / или расширяются с помощью специальных воздушных шаров.
Открытая хирургия
Если у вашего ребенка сужение от умеренного до сильного, может потребоваться более сложное лечение. Эта операция проводится для увеличения участка с сужением или стенозом. Есть два основных способа проведения открытой операции.
Реконструкция гортани (LTR) или ларинготрахеопластика (LTP)
В LTR расширена суженная часть дыхательного горла, прямо под голосовым ящиком.Для этого в дыхательные пути вводят трансплантат или кусок хряща. Большинство трансплантатов состоят из хряща ребра, но также используются хрящи уха или щитовидной железы. Операция проводится в один этап или поэтапно, в зависимости от состояния вашего ребенка.
Одноэтапный (SSLTR): если у вашего ребенка установлена трахеостомическая трубка, она будет удалена во время операции. После операции вашему ребенку через нос вставят дыхательную трубку. Дыхательная трубка поддерживает дыхательные пути и поддерживает место восстановления, пока трансплантат заживает и укрепляется.Пока дыхательная трубка находится внутри, вашему ребенку может потребоваться успокоительное и искусственное дыхание с помощью респиратора. Во многих случаях место ремонта проверяется в операционной перед тем, как вынуть дыхательную трубку.
Двойной этап (DSLTR): есть два варианта этой операции. Вашему ребенку может быть вставлен стент (устройство, похожее на полую трубку) в дыхательные пути над трахеотомической трубкой (трахеотомией). ЛОР-врач может решить использовать Т-образную трубку вместо трахеи и стента. Тройник похож на трахею и стент, но все в одном.Стент или Т-образная трубка удерживают дыхательные пути ребенка открытыми, пока трансплантат заживает. Ваш врач решит, как долго Т-образная трубка или стент остается на месте.
Крикотрахеальная резекция (CTR) или трахеопластика шейным сдвигом
При CTR и шейной трахеопластике удаляется узкая часть трахеи. Затем снова прикрепляют здоровые концы трахеи. Эта операция может быть одноэтапной или поэтапной.
Позвоните врачу вашего ребенка, если:
Ваш ребенок:
- Имеет проблемы с удерживанием пищи и все время ее срыгивает
- Худеет или не набирает вес
- Начинает меньше кормить и быстро утомляется во время кормления
- Борьба между едой и дыханием
Отведите ребенка в больницу, если ваш ребенок:
- Прекращает дыхание более чем на 10 секунд
- Губы темно-синего цвета, дыхание шумное
- Имеет втягивание груди или шеи, которое не прекращается при изменении положения или пробуждении ребенка
Профилактика и лечение стеноза гортани у младенцев и детей
Приобретенный стеноз гортани является хорошо задокументированным осложнением эндотрахеальной интубации.Недоношенные дети, которым требуется искусственная вентиляция легких для лечения респираторного дистресс-синдрома, подвержены повышенному риску развития стеноза гортани. До недавнего времени методы лечения стеноза гортани требовали временной трахеотомии, что усложняло лечение и приводило к летальному исходу. В 1980 году было описано использование переднего перстневидного хряща для лечения стеноза гортани у младенцев. Методика была изменена: процедура переднего разделения перстневидного хряща, как первоначально описывалась, требовала одного вертикального разреза по средней линии через переднее хрящевое кольцо перстневидного хряща и верхние 2 кольца трахеи; модификация представляет собой расширение верхнего предела разреза щитовидного хряща в пределах 2 мм от надреза щитовидной железы.Методика использовалась у 45 детей в возрасте от 4 дней до 28 месяцев. Помимо того, что они представляют ценность для лечения стеноза гортани у недоношенных детей (29 пациентов), были выявлены 2 другие клинические группы детей, которым полезен продукт; 11 младенцев, у которых в первые 2 года жизни развился стеноз гортани вследствие интубации, и у которых передний перстневидный разрез использовался в качестве альтернативы трахеотомии; 5 младенцев в возрасте до 2 лет, каждому из которых была выполнена трахеотомия по поводу стеноза гортани, у которых передний перстневидный разрез использовался в качестве альтернативы более обширным методам реконструкции гортани и трахеи.Из недоношенных детей (29) 18 были успешно экстубированы, 5 все еще нуждались в трахеотомии и 6 умерли до завершения экстубации; Преобладающей причиной смерти была дыхательная недостаточность, вторичная по отношению к основной бронхолегочной дисплазии. Из 11 детей с обструкцией верхних дыхательных путей, вызванной постепенным развитием стеноза гортани, 9 были успешно вылечены без трахеотомии, а двоим потребовалась трахеотомия с последующей реконструкцией гортани и трахеи. Все 5 пациентов со стенозом гортани и трахеотомией были экстубированы.Интраоперационной летальности и серьезных осложнений не было. Результаты исследования подтверждают следующие выводы: передний перстневидный разрез является полезным методом лечения стеноза гортани у детей в возрасте до 2 лет без использования трахеотомии. У ребенка должен быть достаточный легочный резерв для проведения процедуры и последующей экстубации. Процедура требует высокого уровня медицинских, хирургических и медсестринских навыков и должна выполняться только в центрах третичной медицинской помощи.
Индексные слова
Подсвязочный стеноз
Стеноз гортани
трахеотомия
Рекомендуемые статьи Цитирующие статьи (0)
Полный текстАвторские права © 1985 Опубликовано Elsevier Inc.
Рекомендуемые статьи
stenosis Отделение оторино-ларингологической службы
Стеноз гортани означает сужение дыхательных путей на любом уровне, от надгортанника до трахеи.Сужение голосовых связок называется стенозом голосовых связок , а стеноз чуть ниже голосовых связок . Сужение может затрагивать один или несколько уровней гортани.
Голосовая перепонка представляет собой мембрану разной толщины и может включать голосовые связки разной длины. Стеноз задней (задней) части голосовой щели с фиксацией или без фиксации суставов голосовых связок называется стенозом задней голосовой щели . Сужение гортани на всех уровнях называется трансглоточным стенозом.
Ребенок может родиться с врожденной аномалией перстневидного хряща (врожденный стеноз подсвязочного канала). Очень недоношенный ребенок может иметь предрасположенность к такой патологии. Часто такого младенца интубируют в течение нескольких недель, что приводит к приобретенной форме стеноза (в данном случае смешанной форме: приобретенному по врожденной причине). Врожденный стеноз подсвязочного канала будет иметь диаметр менее 4,0 мм у доношенного новорожденного и 3,0 мм у недоношенного ребенка.
Случайное удушение, травмы шеи, проглатывание едких продуктов — некоторые другие причины стеноза дыхательных путей.Может быть ассоциированный стеноз глотки и пищевода (пищевода).
Симптомы
Стеноз гортани с респираторными и голосовыми жалобами. Проблемы с задней голосовой щелью влияют на дыхание. Голосовые жалобы связаны с передней голосовой щелью. Легкий стеноз подсвязочного канала может иметь незначительные симптомы. Умеренное сужение может вызвать шумное дыхание (стридор) и ограничить активность, поскольку у ребенка возникает одышка. У малышей могут быть проблемы с кормлением.При тяжелом стенозе подсвязочного канала и сращении голосовых связок требуется введение трахеотомической трубки, чтобы ребенок мог дышать. Голос обычно нормальный, если стеноз не очень серьезный или полный.
Дети и младенцы со стенозом подсвязочного канала могут иметь другие сопутствующие проблемы и сопутствующие заболевания, такие как сложные заболевания легких (бронхолегочная дисплазия), сердечные и неврологические состояния, гастроэзофагеальный рефлюкс, проблемы с глотанием и кормлением. Чтобы получить наилучшие результаты при лечении стеноза дыхательных путей, важно, чтобы все связанные с этим проблемы и сопутствующие заболевания лечила многопрофильная бригада.Это позволит создать наилучшие условия до того, как мы исправим стеноз дыхательных путей. Также может быть несколько синдромов (например, трисомия 21 или синдром Дауна), которые требуют комплексного подхода и особого ухода для достижения оптимальных результатов.
Уход
Существует лечение всех видов стеноза гортани. В общих чертах, лечение может быть эндоскопическим или внешним хирургическим вмешательством. Это решение принимается во время эндоскопического обследования. Иногда может быть несколько уровней стеноза.В таком случае мы никогда не сможем думать о деканюляции (удалении трахеостомической канюли), если все уровни не были обработаны оптимальным образом.
Для коррекции стеноза подсвязочного канала используются две основные операции: реконструкция гортани и трахеи (LTR) и резекция крикотрахеального канала (CTR). Обе эти операции могут проводиться в один или два этапа, и это решение зависит от каждого конкретного случая.
- Реконструкция гортани и трахеи (LTR) — это процедура расширения дыхательных путей, выполняемая путем введения хрящевых трансплантатов (взятых из ребра, уха или гортани).Со временем расширительный хрящ интегрируется в стенки трахеи и подсвязочного пространства и становится частью дыхательных путей.
Одноэтапный LTR в ближайшем послеоперационном периоде потребует, чтобы ребенку установили назальную эндотрахеальную трубку и поместили в реанимацию на 5-7 дней. Операции, выполняемые в 2 этапа, будут иметь стент (Laryngotracheal LT Mold Монье) и трахеостомию. Форма LT используется для калибровки расширенных дыхательных путей и стабилизации реконструкции хряща. Форма LT хранится от нескольких недель до месяцев в зависимости от каждого конкретного случая.Для удаления стента требуется отдельная эндоскопическая процедура. Трахеостому удаляют после успешных испытаний деканюляции ( читать ниже ).
Третья разновидность хирургии — это расширенная операция CTR , которая сочетает в себе принципы расширения дыхательных путей с трансплантатом хряща и резекцией крикотрахеального отдела.
Следует помнить, что при проведении хирургических вмешательств на дыхательных путях это всегда компромисс между ВОЗДУШНЫМ ПУТИ и ГОЛОСОМ.Приоритет отдается деканюляции (удалению канюли трахеостомы), которая меняет качество жизни пациента и позволяет избежать множества проблем, связанных с трахеостомией.
Выбор типа операции зависит от точного места стеноза, длины стеноза, поражения голосовых связок в стенозирующем сегменте и сопутствующих сопутствующих заболеваний.
Комбинированный аэро-пищеварительный стеноз требует поэтапного лечения и включает ЛОР плюс педиатрических или пищеварительных хирургов.
Важно отметить, что наилучшие результаты реконструкции дыхательных путей и последующей деканюляции (удаления трахеостомы) достигаются при первой операции.
Рост трахеи нормальный и остается неизменным после этих вмешательств. У ребенка нормальное развитие, и качество его жизни значительно улучшилось.
Баллонная дилатационная ларингопластика при подсвязочном стенозе у детей: восьмилетний опыт | Ларингология | JAMA Отоларингология — хирургия головы и шеи
Цель Оценить результаты баллонной ларингопластики при стенозе гортани у детей.
Дизайн Ретроспективное исследование.
Учреждение Академическое отделение педиатрической отоларингологии.
Пациенты Все дети, получавшие лечение баллонной дилатацией гортани (первично или вторично после операции на гортани) с 2002 по 2010 гг.
Результаты Всего 44 ребенка в возрасте от 1 месяца до 10 лет (14 [32%] со стенозом II степени, 25 [59%] со стенозом III степени и 4 [9%] со стенозом IV степени. ) были включены.Двенадцать детей [27%] имели врожденный стеноз гортани, а у остальных 32 [ 7 3%] стеноз был приобретен. Всего было выполнено 52 ларингопластики с баллонной дилатацией, из которых 37 (71%) были признаны успешными. Двадцать из 31 пациента, перенесшего первичную дилатацию (65%), имели успешные результаты, а у остальных 11 [35%] результаты были неудачными (у 4 был стеноз II степени и у 7 стеноз III степени), и потребовалось либо ларинготрахеальная реконструкция, либо трахеотомия. Двадцать одно баллонное расширение было выполнено в качестве вторичной процедуры после недавней открытой операции; 17 процедур (81%) были успешными, поэтому хирургического вмешательства удалось избежать.
Заключение Ларингопластика с баллонной дилатацией — эффективный и безопасный метод лечения как первичного, так и вторичного стеноза гортани у детей.
Несмотря на то, что за последнее десятилетие многие достижения позволили улучшить лечение врожденного и приобретенного стеноза гортани и трахеи у детей, принятие терапевтических решений остается сложной задачей для отоларингологов. Различные варианты лечения включают трахеотомию, открытые хирургические процедуры и миниинвазивные операции.Первоначально о баллонной дилатации сообщалось Hebra et al. -1 для лечения стеноза гортани или трахеи у детей с использованием классических сферических баллонов для ангиопластики. Durden and Sobol 2 недавно пересмотрели методы баллонной дилатации для приобретенного педиатрического стеноза подсвязочного канала с использованием новых типов баллонов. Этот минимально инвазивный подход кажется привлекательным как в качестве первичного лечения, так и в качестве вторичного лечения после открытых хирургических вмешательств. Вторичная послеоперационная дилатация после ларинготрахеальных реконструкций (LTR) направлена на уменьшение количества рецидивов и открытых хирургических вмешательств.С тех пор несколько авторов 3 , 4 сообщили о различных результатах и связанных с ними эндоскопических методах, включая использование лазерной диссекции, микроинструментов, баллонного расширения, стентирования и инъекций стероидов и / или применения митомицина.
Нашей основной целью было исследовать некоторые противоречия относительно этой новой техники, чтобы определить лучшие показания и ограничения: (1) соответствующий отбор пациентов для лечения первичной баллонной дилатации; (2) идентификация прогностических факторов успеха или неудачи первичной баллонной дилатации; (3) определение предлагаемой стандартной программы для последовательностей расширения: количество сеансов, периодичность и задержка; и (4) оценка эффективности и показаний к лечению вторичной дилатации после открытой операции на гортани.
Мы провели ретроспективный анализ досье пациентов, включая всех пациентов, которым была выполнена баллонная дилатация по поводу подвязочного стеноза с января 2002 г. по сентябрь 2010 г. Демографические и клинические данные, включая возраст, пол, сопутствующие заболевания и этиологию стеноза, были собраны для всех детей. Стенозы оценивали эндоскопически до всех дилатаций с использованием классификации Myer et al. 5 (далее по классификации Myer-Cotton).Были выделены два типа клинических ситуаций: группа первичного лечения, включающая всех детей, лечившихся в первую очередь с помощью баллонной дилатации или с историей открытых операций на гортани более 1 года назад, и группа вторичного лечения, включающая всех детей, перенесших дилатацию менее года. после LTR. Минимальная задержка между открытыми процедурами и баллонным расширением составляла 10 дней для LTR и 3 недели для анастомоза трахеи, чтобы избежать разрывов дыхательных путей или утечки. Успешная программа дилатации определялась отсутствием значительного рецидивирующего стеноза (эндоскопическая степень 0 или I) по крайней мере через 1 год.
Программа баллонной дилатации была определена как серия от 1 до 4 последовательных процедур дилатации в течение максимального периода в 6 месяцев. Техника дилатации включала эндоскопический баллонный катетер высокого давления под общей анестезией со спонтанной вентиляцией по стандартному протоколу. Прямая ларингоскопия выполнялась с использованием телескопа 2,7 или 4 мм 0 ° (модель 10324 AA; Karl Storz) и баллонного катетера (пищеводный баллон MaxForce; Boston Scientific), введенного в просвет гортани через стеноз.Затем его надували с помощью ручки для надувания / спуска, установленной с узлом шприца и манометра (Boston Scientific), предназначенного для контроля и поддержания давления в баллоне в течение 30 секунд или до тех пор, пока уровень насыщения кислородом пациента не упадет ниже 92%. Размер и диаметр баллона были выбраны в соответствии с теоретическим идеальным диаметром перстневидного кольца (таблица 1). Минимальный диаметр баллона 6 мм. Эту процедуру выполняли 2 или 3 раза в течение каждого сеанса под общей анестезией, после чего следовали 1-2 минуты местного нанесения наложений котоноидов, пропитанных митомицином, 1 мг / мл, если таковые имеются.В большинстве случаев дети не были интубированы после дилатации, находились под наблюдением в педиатрическом отделении интенсивной терапии в течение 24–48 часов и подвергались контрольной эндоскопии через 5–7 дней в зависимости от клинического прогресса. При контрольной эндоскопии при необходимости выполнялась вторая баллонная дилатация. Все пациенты получали от 3 до 10 дней системные стероиды (преднизолон, 1-2 мг / кг / день), ингибиторы протонной помпы (эзомепразол, 2 мг / кг / день) и небулайзеры адреналина. Контрольная эндоскопия проводилась еженедельно в течение 3 недель, каждые 3 недели до полного заживления, а затем каждые 6 месяцев.Последующая эндоскопия выполнялась с использованием назофиброскопа (FNL 10 RP3; Pentax), подключенного к камере (Karl Storz), под местной анестезией с кислородом и закисью азота, доставляемыми с помощью вентиляции с помощью маски. Общая анестезия требовалась при небольшом количестве последующих эндоскопий.
Была получена описательная статистика, и 2 группы детей были сравнены (первичная и вторичная дилатация, а также успешные и неудачные случаи) с использованием χ 2 или критериев суммы рангов Манна-Уитни, где это было необходимо.Многофакторный анализ логистической регрессии был проведен для оценки потенциальных предикторов отказа. Все статистические анализы были выполнены с использованием программного обеспечения Sigmastat 3.0 (Systat Software). P <0,05 считалось статистически значимым.
В исследование были включены 44 пациента: 15 девочек и 29 мальчиков со средним (SD) начальным возрастом 26 (34) месяцев (диапазон от 1 дня до 140 месяцев) и средним исходным весом 11,0 (7.0) кг (диапазон 2,0-35,0 кг). Все пациенты были госпитализированы по поводу стеноза подсвязочного канала, который был подтвержден эндоскопически и классифицирован в соответствии с классификацией Myer-Cotton под общей анестезией. 5 Стенозы были распределены следующим образом: 14 (32%) имели стеноз II степени, 26 (59%) имели стеноз III степени и 4 (9%) имели стеноз IV степени. У 32 детей (72%) были приобретенные стенозы. Они были связаны с интубацией трахеи в 24 случаях, 18 из которых были недоношенными, или вторичными по отношению к другим заболеваниям в 8 случаях (например, папилломатоз гортани, ветряная оспа, подсвязочная гемангиома, псевдовоспалительная опухоль).Двенадцать детей (27%) имели врожденные стенозы, из которых 5 (42%) имели ассоциированные микроделеции 22q11 (синдром ДиДжорджи). Пятерым детям (42%) перед оценкой стеноза гортани была сделана трахеотомия. В таблице 2 показаны демографические данные пациентов и результаты, а также показано, является ли лечение первичным или вторичным.
Сорок четыре пациента были включены в 52 программы баллонного лечения и прошли в общей сложности 98 процедур баллонной дилатации. Тридцать семь программ дилатации были признаны успешными в соответствии с описанными здесь критериями, что дает общий показатель успеха 71%.Для обеспечения стабильной проходимости дыхательных путей потребовалось шестьдесят шесть эндоскопических процедур (т.е. 1,8 ± 1 процедура на успешный случай). Одной процедуры дилатации хватило в 19 из 37 случаев (51%). На рисунке 1 показано распределение этих эндоскопических процедур. Не наблюдалось клинически значимых осложнений при баллонной дилатации (в частности, кровотечения, эмфиземы шейки матки или пневмоторакса). Узкий диаметр спущенных баллонов делал эндоскопическую дилатацию возможной во всех случаях, даже при точечном стенозе, без дополнительных маневров.Распределение степеней стеноза не отличалось в успешных случаях (13 случаев стеноза II степени, 21 степень III и 3 степени IV) по сравнению с неудачными случаями (3 случая II степени, 11 случаев III степени и 1 случай стеноза III степени). IV класс) (тест по сумме баллов P = 0,48). Митомицин использовался в 40 из 52 программ баллонного лечения без существенной разницы в частоте успеха (28 из 40 [70%] против 9 из 12 [75%]). Пятеро детей умерли во время наблюдения: все смерти были связаны с тяжелыми сопутствующими заболеваниями, и ни один из них не был напрямую вызван стенозом дыхательных путей.
Вторичная дилатация против первичной
Тридцать один пациент получил эндоскопическую баллонную дилатацию в качестве основного лечения (9 девочек и 22 мальчика). Их средний возраст (SD) составлял 26 (31) месяцев (диапазон от 2 недель до 118 месяцев), а их средний вес в начале лечения составлял 11,5 (8,0) кг (диапазон 3,3-35,0 кг).Двадцать три ребенка (74%) имели приобретенные стенозы гортани, 8 из которых (35%) имели врожденные стенозы гортани, в том числе 2 ребенка с микроделецией 22q11. Пятеро из этих детей (22%) имели в анамнезе LTR более 1 года назад. Двадцать детей (65%) успешно прошли курс лечения с помощью баллонной дилатации. Не было статистической разницы между успешными и неудачными случаями с точки зрения веса (11,9 [7,0] кг против 10,9 [10,0] кг), возраста (28 [21] месяцев против 22 [35] месяцев) и степени (степень II по сравнению со степенью). III: 8 из 12 случаев против 3 из 8 случаев).В успешных случаях участвовали 3 ребенка с массой тела менее 3,0 кг. Частота успеха была выше при приобретенных стенозах, чем при врожденных стенозах (16 из 23 [т.е. 70%] против 4 из 8 [50%]), но эта разница не была значимой ( P = 0,41).
Двадцать один ребенок (9 девочек и 12 мальчиков) получил баллонную дилатацию в качестве вторичного лечения в течение года после LTR (диапазон от 5 дней до 11 месяцев). Их средний возраст (SD) составлял 27,0 (35,0) месяцев (диапазон от 1 до 145 месяцев), а их средний вес составлял 11.3 (9,0) кг (диапазон 1,7-35,0 кг). У восьми из этих детей, которым требовалось лечение вторичной баллонной дилатации, не удалось провести первичное лечение дилатации до операции. Семнадцать детей (81%) были успешно вылечены. Разницы между приобретенным и врожденным стенозом не было (10 из 12 [83%] против 7 из 9 [78%]). Только 4 ребенка не ответили на вторичную эндоскопическую дилатацию. Двое из них были недоношенными младенцами младше 1 месяца, которые не могли быть экстубированы после дилатации из-за тяжелого легочного заболевания и сопутствующих заболеваний, и в конце концов умерли.
Хотя вторичная дилатация кажется более успешной, чем первичная, не было обнаружено значительных различий между обеими группами ( P = 0,15 и P = 0,23, соответственно) (χ 2 с поправкой Йетса и точным критерием Фишера). Рисунок 2 иллюстрирует эволюцию нашей практики, показывая преобладание первичных дилатаций во втором периоде исследования. На рисунках 3 и 4 показаны эндоскопические изображения до и после лечения дилатации в выборках успешных и неудачных случаев.
Роль потенциальных факторов прогнозирования
Многофакторный анализ предикторов неэффективности дилатации (таблица 3) не показал значимой связи с полом, недоношенностью, этиологией стеноза, степенью Myer-Cotton или применением митомицина. Однако была значительная связь с гастроэзофагеальным рефлюксом (ГЭР) ( P <.02) и незначительная связь со вторичной дилатацией по сравнению с первичной ( P = 0,07), когда требовалось 3 или более дилатации ( P <.10) и в меньшей степени, когда вес был ниже 5 кг ( P <0,15). 5 детей, которые умерли во время наблюдения, умерли в результате тяжелых сердечных и / или легочных сопутствующих заболеваний.
Предложено несколько хирургических подходов к лечению стеноза подсвязочного канала у детей.С начала 1980-х годов золотым стандартом была открытая хирургия гортани, сочетающая расширение гортани с разрезом перстневидного хряща и / или хрящевыми трансплантатами и различными типами стентирования. 9 -11 Одномоментная ларинготрахеопластика была внедрена в 1990-х годах и заменила трахеостомию эндотрахеальной интубацией в первые дни послеоперационного заживления. Общий успех этих процедур составляет около 80% и зависит от нескольких факторов, таких как степень стеноза, возраст и вес пациента, а также связь ГЭР и других сопутствующих заболеваний. 12 -14 Monnier et al. 15 впервые представили концепцию полной резекции стеноза и сообщили об отличном исходе около 90% при частичной резекции крикотрахеального отдела.
До этих достижений терапевтические возможности включали длительную трахеостомию и / или «бужирование», часто неэффективную, а иногда и опасную технику расширения, от которой впоследствии отказались. Несмотря на хорошо продемонстрированную эффективность баллонного расширения при сосудистых заболеваниях и стенозе пищевода, многие отоларингологи все еще неохотно используют эти новые методы в дыхательных путях. 4 Тем не менее, есть несколько теоретических преимуществ баллонной дилатации по сравнению с жесткими методами: меньшие силы сдвига, радиальное надувание баллона, ограниченная травма, вызванная расширением даже при точечных стенозах, и более низкая частота осложнений. 1
Несмотря на продолжающееся совершенствование открытых хирургических методов, методов лечения коморбидных заболеваний (GER) и достижения в педиатрической интенсивной терапии, некоторым пациентам по-прежнему требуется несколько открытых процедур для получения патента и стабильных дыхательных путей. 9 Баллонные дилатации начали постепенно внедряться в нашу практику, начиная с 1990 года, и оказались очень полезными при лечении стенозов анастомоза после восстановления атрезии пищевода и в некоторых случаях стеноза трахеи или бронхов. 1 , 15 , 16 В последнее время были введены новые типы воздушных шаров, которые характеризуются более высокой прочностью и стабильностью благодаря своей продолговатой форме. Эти воздушные шары кажутся особенно хорошо подходящими для использования в просвете гортани и трахеи.С 2002 года мы постепенно расширяем использование баллонной дилатации для включения стенозов гортани, и она стала важным дополнением в послеоперационном уходе при открытой хирургии гортани. Обоснованием было то, что, хотя нормальный перстневидный рубец представляет собой нерасширяемую хрящевую структуру и, следовательно, не подходит для расширения, передние и / или задние отделы, а иногда и боковые участки перстневидного рубца, выполняемые во время процедур LTR, восстанавливают некоторую способность к расширению. 11 , 17 В нашей серии вторичная дилатация была успешной примерно в 80% случаев, при среднем количестве двух сеансов дилатации и избежания повторной хирургической операции.Подобные результаты были недавно получены у 10 детей Bent et al, 4 , тогда как Quesnel et al 3 получили только 60% успеха у 20 детей после вторичного баллонного расширения. С 2005 года мы используем баллонную дилатацию в качестве основного метода у детей со стенозом гортани и трахеи. У большинства детей был приобретенный стеноз, и полученные результаты были сопоставимы с таковыми у детей со вторичными стенозами. Хотя количество пациентов ограничено, мы наблюдаем, что врожденный стеноз хорошо поддается вторичной дилатации.Первичные дилатации при врожденном заболевании кажутся менее эффективными, вероятно, из-за аномальной толщины перстневидного хряща и значительных сил, необходимых для разрушения хрящевого кольца в этих случаях.
Недавно Mirabile et al. 18 сообщили об успешности лечения в 83% случаев в группе из 18 детей, перенесших эндоскопическое расслоение перстневидного хряща в сочетании с баллонной дилатацией. Этот показатель успешности сопоставим с таковым у пациентов из нашей серии, которым выполнялась первичная дилатация по поводу приобретенных стенозов.В их исследование было включено 8 детей с врожденным стенозом с вероятностью успеха 75%, хотя пациенты получили до 7 послеоперационных дилатаций. Эти результаты предполагают, что эндоскопическое разделение перстневидного хряща может не быть необходимым при приобретенном стенозе, но может повысить вероятность успеха при врожденном заболевании. Недавние экспериментальные данные на кроликах показали, что баллонные расширения нормальной гортани вызывают переломы перстневидного хряща на более тонкой части перстневидного кольца, имитирующие перстневидный перелом. 19 Эти данные согласуются с нашими результатами и могут объяснить хорошие результаты, полученные при приобретенных стенозах, и неудачи при врожденных случаях, связанных с утолщением перстневидного хряща.
Как подчеркивается в самых последних отчетах, 3 не существует единого мнения относительно конкретных показаний к расширению гортани и открытой операции по поводу стеноза подсвязочного канала у детей. Тем не менее, наш опыт баллонной дилатации за последние 10 лет привел к тому, что эта техника стала нашим первым выбором при приобретенном или врожденном субгортальном стенозе малой степени. Открытая операция предлагается в случаях, когда дилатация не удается, или в контексте двусторонней неподвижности голосовых складок или тяжелого точечного врожденного стеноза.В нашей серии исследований этиология стеноза (приобретенный или врожденный) не была значимым фактором неудачи, но пациенты с очень тяжелым врожденным стенозом были исключены. В нашей серии интервал между двумя дилатациями составил около 7 дней. Этот интервал зависел от воспалительных процессов и процессов заживления, а также от регулярных эндоскопических обследований. Неудача дилатации может ожидаться в тех случаях, когда очевидного улучшения диаметра подсвязочного канала не достигается после 2 или 3 процедур. Некоторые авторы сообщают о детях, которым было выполнено более 7 процедур дилатации до успешного исхода. 1 , 3 , 18 Мы считаем, что в этих конкретных случаях требуется пересадка или резекция хряща и что более раннее решение о проведении открытой процедуры предпочтительнее, чтобы избежать длительной госпитализации и частого проведения общей анестезии. В нашей серии исследований ГЭР и первичная дилатация в сравнении с вторичной являются двумя наиболее значимыми прогностическими факторами неудачи.
В заключение, наше исследование иллюстрирует растущее количество доказательств того, что баллонная дилатация безопасна и эффективна при лечении стеноза подсвязочного канала у детей и снижает потребность в открытой операции на гортани на 70–80%.Хорошие показания включают первичное или вторичное лечение приобретенного стеноза всех степеней, вторичное лечение врожденного стеноза и первичное лечение некоторых отдельных врожденных случаев. Открытая операция остается лучшим выбором в случае тяжелого врожденного стеноза, неподвижности голосовой щели или после 2-3 процедур расширения без значительного улучшения.
Для корреспонденции: Тьерри Ван ден Аббеле, доктор медицинских наук, отоларингологическая служба, больница Роберта Дебре, 48 Boulevard Serurier, 75019 Paris, France ([email protected]).
Представлено для публикации: 22 августа 2011 г .; окончательная доработка получена 26 октября 2011 г .; принята 6 декабря 2011 г.
Опубликовано онлайн: 20 февраля 2012 г. doi: 10.1001 / archoto.2011.1439
Вклад авторов: Все авторы имели полный доступ ко всем данным в исследовании и несут ответственность за целостность данных и точность анализа данных.
Концепция и дизайн исследования : Ван Ден Аббеле. Сбор данных : Отфор, Тейсье и Виала. Анализ и интерпретация данных : Отфор, Тейсье и Ван ден Аббеле. Составление рукописи : Отфор, Виала и Ван ден Аббеле. Критический пересмотр рукописи для важного интеллектуального содержания : Teissier. Наблюдение за исследованием : Ван Ден Аббеле.
Раскрытие финансовой информации: Не сообщалось.
Предыдущая презентация: Часть этого исследования была принята для подиума и была представлена на 24-м ежегодном собрании Американского общества детской отоларингологии; 23 мая 2009 г .; Сиэтл, Вашингтон.
Дополнительные материалы: Кристофер Брашер, доктор медицины, предоставил полезные критические замечания и исправления к рукописи.
1.Hebra A, Powell DD, Smith CD, Othersen HB Jr. Баллонная трахеопластика у детей: результаты 15-летнего опыта. J Педиатр Хирургия . 1991; 26 (8): 957-9611919989PubMedGoogle ScholarCrossref 2. Дурден Ф., Соболь С.Е. Баллонная ларингопластика как основное лечение стеноза подсвязочного канала. Хирургическая хирургия головы и шеи Arch Otolaryngol .2007; 133 (8): 772-77517709614PubMedGoogle ScholarCrossref 3.Quesnel AM, Lee GS, Nuss RC, Volk MS, Jones DT, Rahbar R. Минимально инвазивное эндоскопическое лечение подсвязочного стеноза у детей: успехи и неудачи. Int J Педиатр Оториноларингол . 2011; 75: 652-65621377219PubMedGoogle ScholarCrossref 4.Bent JP, Shah MB, Nord R, Parikh SR. Баллонная дилатация при рецидивирующем стенозе после детской ларинготрахеопластики. Анн Отол Ринол Ларингол . 2010; 119 (9): 619-62721033030PubMedGoogle Scholar5.Майер CM III, О’Коннор DM, Коттон RT. Предлагаемая система оценки стеноза подсвязочного канала на основе размеров эндотрахеальной трубки. Анн Отол Ринол Ларингол . 1994; 103 (4, pt 1): 319-3238154776PubMedGoogle Scholar6.Fayoux P, Devisme L, Merrot O, Marciniak B. Определение размера эндотрахеальной трубки в перинатальной популяции: анатомическое и экспериментальное исследование. Анестезиология . 2006; 104 (5): 954-96016645447PubMedGoogle ScholarCrossref 7.Eckel HE, Koebke J, Sittel C, Sprinzl GM, Pototschnig C, Stennert E.Изучена морфология гортани человека первых пяти лет жизни на серийных срезах целых органов. Анн Отол Ринол Ларингол . 1999; 108 (3): 232-23810086614PubMedGoogle Scholar8. Аль-Мазроу К.А., Абдулла К.М., Ансари Р.А., Абдельмегид М.Э., Туркестани А. Сравнение внешнего диаметра наиболее подходящей эндотрахеальной трубки с диаметром дыхательных путей, измеренным с помощью МРТ. уровень перстневидного хряща. Eur J Анестезиол . 2009; 26 (9): 736-73919461523PubMedGoogle ScholarCrossref 9. Koempel JA, Cotton RT.История детской ларинготрахеальной реконструкции. Otolaryngol Clin North Am . 2008; 41 (5): 825-835, vii18775336PubMedGoogle ScholarCrossref 10. Нарси П., Контенсин П., Флиньи И., Франсуа М. Хирургическое лечение стеноза гортани и трахеи у педиатрических пациентов. Хирургическая хирургия головы и шеи Arch Otolaryngol . 1990; 116 (9): 1047-10502383390 PubMedGoogle ScholarCrossref 11. Дрейк А.Ф., Контенсин П., Нарси Ф., Коттон RT. Боковые перстневидные надрезы в качестве дополнительной меры для увеличения стенозированных подсвязочных дыхательных путей: анатомическое исследование. Int J Педиатр Оториноларингол . 1989; 18 (2): 129-1372625389PubMedGoogle ScholarCrossref 12. Сейд А.Б., Пранский С.М., Кирнс ДБ. Одноэтапная ларинготрахеопластика. Хирургическая хирургия головы и шеи Arch Otolaryngol . 1991; 117 (4): 408-4102007011PubMedGoogle ScholarCrossref 13.Cotton RT, Myer CM III, O’Connor DM, Smith ME. Реконструкция гортани у детей с хрящевыми трансплантатами и стентированием эндотрахеальной трубки: одноэтапный подход. Ларингоскоп . 1995; 105 (8, pt 1): 818-8217630293PubMedGoogle ScholarCrossref 14.Ndiaye I, van den Abbeele T., François M, Viala P, Tanon-Anoh MJ, Narcy P. Хирургическое лечение стеноза гортани у детей. Анн Отоларингол Чир Цервикофак . 1999; 116 (3): 143-14810399529PubMedGoogle Scholar 15. Монье П., Ланг Ф., Савари М. Частичная резекция крикотрахеальной артерии по поводу тяжелого стеноза подсвязочного канала у детей: обновление опыта Лозанны. Анн Отол Ринол Ларингол . 1998; 107 (11, pt 1): 961-9689823847 PubMedGoogle Scholar 16. Полоновски Дж. М., Герц Панье Л., Франсуа М., Гарель С., Хассан М., Нарси П.Баллонная дилатация трахеобронхиальных стенозов у детей: около 4 случаев. Анн Отоларингол Чир Цервикофак . 1991; 108 (7): 411-4161789614PubMedGoogle Scholar 17.Baculard F, Couloigner V, François M, Narcy P, Van den Abbeele T. Реконструкция ларинготрахеопластики с четырехквадрантным разделением перстневидного хряща у детей. Анн Отоларингол Чир Цервикофак . 2004; 121 (2): 104-10915107736PubMedGoogle ScholarCrossref 18. Мирабайл Л., Серио П.П., Багги Р.Р., Кулуаньер В.В. Эндоскопическое расщепление переднего перстневидного хряща и баллонная дилатация при стенозе подсвязочного канала у детей. Int J Педиатр Оториноларингол . 2010; 74 (12): 1409-141420980061PubMedGoogle ScholarCrossref 19. Анг А.Х., Моди В.К., Райтата Р., Эйприл М.М., Уорд РФ. Пилотное исследование баллонной дилатации на модели животных, приводящей к перелому перстневидного хряща: последствия для стеноза дыхательных путей у детей. Ларингоскоп . 2010; 120 (10): 2094-209720740502PubMedGoogle ScholarCrossrefПодсвязочный стеноз | Rush System
Подсвязочный стеноз — это сужение дыхательных путей чуть ниже голосовых связок.Это сужение может вызвать серьезные затруднения дыхания.
Подсвязочный стеноз может возникать у детей и взрослых. Это часто обнаруживается после того, как затрудненное дыхание не поддается лечению от других состояний, таких как астма или бронхит.
Если вам или вашему ребенку поставили диагноз «стеноз подсвязочного канала» или у вас проблемы с дыханием, и вы не знаете, почему, то вам могут помочь педиатрические ЛОР-специалисты и наши эксперты по голосу, дыхательным путям и глотанию в Rush.
Причины стеноза подсвязочного канала
- Подсвязочный стеноз может быть врожденным (с чем вы родились) или приобретенным (обычно из-за рубцовой ткани).
- Часто бывает менее тяжелым, если врожденный, улучшается по мере роста гортани.
- Частая или длительная интубация (наличие дыхательной трубки) является наиболее частой причиной приобретенного стеноза подсвязочного канала у детей и взрослых.
- Другие причины включают травмы и раздражение этой области дыхательных путей.
- Подсвязочный стеноз также может наблюдаться при редких воспалительных состояниях, таких как гранулематоз с полиангититом (редкая форма васкулита, ограничивающая кровоток), саркоидоз и рецидивирующий полихондрит.
Симптомы стеноза подсвязочного канала
У большинства людей с легким стенозом подсвязочного канала нет никаких симптомов. Другие пациенты с более серьезным стенозом подсвязочного канала могут иметь один или несколько из следующих симптомов:
- Охриплость
- Затрудненное дыхание (одышка), особенно после нагрузки
- Рецидивный круп
- Высокий шум (называемый стридором) при вдохе и / или выдохе является основным признаком стеноза подсвязочного канала. Его часто принимают за свистящее дыхание, симптом астмы.
Как мне получить помощь при стенозе подсвязочного канала?
Позвоните своему лечащему врачу или педиатру вашего ребенка, если вы или ваш ребенок испытываете проблемы с дыханием или симптомы подсвязочного стеноза.
Ваш врач может направить вас к специалисту по уху, носу и горлу (ЛОР) для диагностики и лечения.
- Детям может потребоваться посещение детского ЛОР, у которого есть опыт и специальные знания для лечения этого состояния у более молодых пациентов.
- Взрослых можно направить к специалисту по голосу, айвари и глотанию в Rush.
Лечение стеноза подсвязочного канала при спешке
Существуют различные варианты лечения в зависимости от возраста пациента, локализации и размера подсвязочного стеноза, а также от общего состояния здоровья пациента. Ваш врач обсудит с вами возможные варианты.
Для взрослых:
- Противорефлюксные препараты могут помочь уменьшить раздражение пораженного участка.
- Серийные инъекции стероидов в подсвязочный канал могут быть вариантом для некоторых пациентов с легкими случаями стеноза подсвязочного канала.
- Эндоскопическая дилатация — это минимально инвазивная процедура, выполняемая через рот для расширения дыхательных путей.
- Во время процедуры врачи используют баллон и / или лазер, чтобы сделать отверстие большего размера.
- Поскольку стеноз чаще всего возникает из рубцовой ткани, могут потребоваться повторные процедуры по мере роста рубцовой ткани.
- В зависимости от тяжести стеноза врач может установить стент в дыхательные пути, чтобы дыхательные пути оставались открытыми.
- Открытая операция через шею иногда необходима, когда подсвязочный стеноз более серьезен, чтобы удалить узкий сегмент и расширить дыхательные пути.
- Трахеостомия (трубка, вставляемая в шею для облегчения дыхания) может потребоваться в некоторых случаях для открытия дыхательных путей ниже сужения.



 22 с.
22 с. 1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p.
1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p. Vol. 126. № 1. P. 49-53.
Vol. 126. № 1. P. 49-53. 1998. Vol. 255. № 1. P. 12-17.
1998. Vol. 255. № 1. P. 12-17. Rhinol. Laryngol. 1998. Vol. 107. № 11, Pt. 1. P. 961-968.
Rhinol. Laryngol. 1998. Vol. 107. № 11, Pt. 1. P. 961-968.
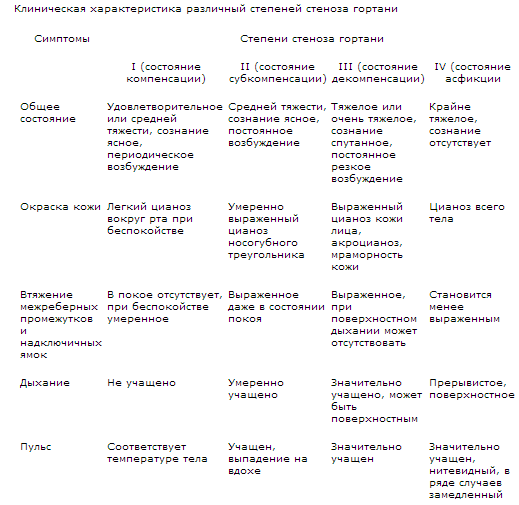 Otol. Rhinol. Laryngol. 1998. Vol. 107. № 12. P. 1006-1009.
Otol. Rhinol. Laryngol. 1998. Vol. 107. № 12. P. 1006-1009.