современные возможности лечения и профилактики переломов uMEDp
В статье обсуждаются вопросы патогенеза и диагностики постменопаузального остеопороза. Дается обзор бисфосфонатов как наиболее изученной и широко применяемой при патогенетической терапии остеопороза группы препаратов. Разбираются механизмы действия и терапевтическая эффективность бисфосфонатов. На основании данных международных исследований показано, что применение ризедроната соответствует решению основной цели лечения остеопороза – снижению риска остеопоротических переломов различных локализаций.Таблица. Сравнительная активность бисфосфонатов
Рис. 1. Химическая структура бисфосфонатов
Рис. 2. Сравнительная активность различных бисфосфонатов*
Во всем мире остеопороз все сильнее привлекает внимание врачей.
Большую часть людей, подверженных остеопорозу, составляют женщины. Известно, что в первые пять лет после наступления менопаузы потеря костной массы может составить до трети от общей массы кости, утраченной за всю жизнь [4, 5]. В постменопаузе почти у трети женщин отмечается остеопороз, а у около 54% – остеопения, что предопределяет их уязвимость в плане развития остеопороза и остеопоротических переломов [6, 7]. Постменопаузальный остеопороз представляет собой наиболее распространенную форму заболевания – его доля в структуре первичного остеопороза равняется 85%. После менопаузы усиливаются процессы резорбции кости. Необходимо отметить, что в развитии постменопаузального остеопороза наиболее важную роль играют следующие факторы: костная масса ко времени начала менопаузы и последующая скорость потери костного вещества.
В основе функционирования костной системы лежат два тесно взаимосвязанных процесса: образование новой и разрушение старой кости – костное ремоделирование. На протяжении всей жизни этот процесс осуществляется с различной скоростью, меняется и направленность ремоделирования кости. Ежегодно перестраивается от 2–4 до 10% костной массы, иными словами, за 10–20 лет обновляется примерно половина скелета. Примерно до 35–40 лет поддерживается нулевой баланс. Возраст, в котором начинается потеря костной массы, точно не определен. Принято считать, что потери костной массы начинаются с конца третьего десятилетия жизни, их скорость зависит от пола и возраста. У мужчин они составляют 0,3–0,5% в год. У женщин процесс снижения плотности костной массы более сложен: до начала периода климактерия костная масса ежегодно снижается на 0,7–1,3%, а после наступления менопаузы ее потери достигают 2–3% в год.
У женщин в период менопаузы активируется полный цикл ремоделирования кости, при этом процессы резорбции преобладают над процессами костеобразования. Хотя возрастная потеря костной массы, составляющая в среднем 1% от уровня пика костной ткани, начинается уже в репродуктивном периоде, наибольшей выраженности процесс достигает, как правило, спустя 5–10 лет после наступления менопаузы. При этом костные потери могут достигать до 5% ежегодно [8]. В итоге масса кости снижается примерно на 25–30% и резко повышается риск атравматических переломов под влиянием минимальных нагрузок.
Хотя возрастная потеря костной массы, составляющая в среднем 1% от уровня пика костной ткани, начинается уже в репродуктивном периоде, наибольшей выраженности процесс достигает, как правило, спустя 5–10 лет после наступления менопаузы. При этом костные потери могут достигать до 5% ежегодно [8]. В итоге масса кости снижается примерно на 25–30% и резко повышается риск атравматических переломов под влиянием минимальных нагрузок.
В патогенезе постменопаузального остеопороза пусковым фактором является дефицит эстрогенов, вызывающий ускорение потери костной массы. Однако, несмотря на то что все женщины в менопаузе имеют эстрогеновую недостаточность, недуг развивается только у каждой третьей из них. Это свидетельствует о влиянии различных факторов, включая генетические, на возникновение и развитие остеопороза. Кроме прочего, при остеопорозе нет характерных, в том числе ранних, клинических проявлений. В этой связи своевременный учет факторов риска в диагностике заболевания имеет особое значение.
В любом возрасте, включая период постменопаузы, на фоне возрастного дефицита эстрогенов наиболее выраженные изменения происходят в трабекулярной (губчатой) кости, в основном представленной в телах позвонков, плоских костях, в костях предплечья и в пяточных костях. Так, например, масса трабекулярной кости позвонков снижается в год на 5%, а кортикального слоя – на 1,5%. Переломы тел позвонков, возникающие, как правило, раньше остеопоротических переломов любой другой локализации, являются наиболее частым осложнением заболевания, составляя около половины всех переломов [9]. Клинические проявления позвоночных переломов, включающие синдром острой или хронической боли в спине, нарушения осанки и снижение роста, ведут к депрессии, ухудшению качества жизни и инвалидности [2, 10].
Так, например, масса трабекулярной кости позвонков снижается в год на 5%, а кортикального слоя – на 1,5%. Переломы тел позвонков, возникающие, как правило, раньше остеопоротических переломов любой другой локализации, являются наиболее частым осложнением заболевания, составляя около половины всех переломов [9]. Клинические проявления позвоночных переломов, включающие синдром острой или хронической боли в спине, нарушения осанки и снижение роста, ведут к депрессии, ухудшению качества жизни и инвалидности [2, 10].
Остеопороз – это основная причина переломов шейки бедра, часто встречающихся у женщин старше 65 лет. Печально, что в наши дни наметилась четкая тенденция к увеличению частоты переломов шейки бедра и в возрастной группе 50–60 лет. Риск переломов данной локализации у женщин достигает 15%, что приближается к уровню заболеваемости раком молочной железы, яичников и эндометрия, вместе взятых [3, 5, 7]. Лечение переломов проксимального отдела бедра считается экономически наиболее затратным, так как, среди прочего, требуется госпитализация.
К сожалению, поздняя диагностика и несвоевременное начало фармакотерапии остеопороза характерны для 75% женщин и 90% мужчин [5]. Согласно данным Национального комитета качества здравоохранения США, в стране более 90% взрослых с сердечно-сосудистыми заболеваниями получают β-блокаторы и только 19% взрослых с частыми переломами лечатся от остеопороза [11]. Приоритетной задачей практической медицины является не только своевременная диагностика, но и адекватное лечение остеопороза и его осложнений, имеющих порой фатальный характер, – остеопоротических переломов [1, 3, 6, 7]. Бесспорно, что рано начатое лечение может существенно повлиять на прогрессирование и исходы заболевания. Разрешению этой задачи, несомненно, способствует более широкое информирование о проблеме остеопороза как врачей различных специальностей, так и населения в целом.
В настоящее время существуют эффективные программы лечения заболевания, включающие сочетание нефармакологических методов с современными противоостеопоротическими препаратами. Бисфосфонаты (БФ), представляя собой стабильные аналоги природных неорганических фосфатов, широко применяются в терапии постменопаузального остеопороза как препараты первой линии и позволяют проводить патогенетическую терапию заболевания, поскольку они наиболее выраженно ингибируют костную резорбцию [4, 6, 12]. История применения БФ насчитывает не один десяток лет. Этот класс лекарственных препаратов характеризуется следующей химической структурой: заменой атома кислорода в молекуле пирофосфата на атом углерода (Р-С-Р), в боковых цепях присутствуют два радикала: R БФ сохраняются в местах нового костеобразования до тех пор, пока не произойдет замена старой кости на новую [13, 14, 15].
БФ сохраняются в местах нового костеобразования до тех пор, пока не произойдет замена старой кости на новую [13, 14, 15].
Основным фармакологическим эффектом БФ является снижение костного ремоделирования с более выраженным угнетением костной резорбции, нежели чем костеобразования, а также снижение частоты активации новых очагов ремоделирования [13, 16]. Вместе с тем БФ уменьшают или предупреждают отрицательное влияние на кость практически всех известных стимуляторов резорбции [13, 14]. Проникая в костную ткань и создавая высокую концентрацию в лакунах резорбции, БФ концентрируются вокруг остеокластов. В пределах этих клеток БФ вызывают много изменений, которые в итоге снижают способность остеокластов к резорбции костной ткани (например, потеря щеточной каймы, разрушение цитоскелета, неспособность остеокластов к передвижению или связыванию с костной тканью) [13, 15, 17]. Однако, несмотря на то что используемые в настоящее время препараты данной группы являются химически сходными, их механизмы действия различны. Антирезорбтивная активность отдельных БФ существенно варьирует, что связано с особенностями химической структуры препарата (табл.).
Антирезорбтивная активность отдельных БФ существенно варьирует, что связано с особенностями химической структуры препарата (табл.).
Первое поколение БФ – этидронат, клодронат и тилудронат, не содержащие в своей структуре атомов азота, метаболизируются остеокластами внутриклеточно до цитотоксичных аналогов аденозин трифосфата. В свою очередь, азотсодержащие БФ блокируют синтез фарнезилдифосфата синтазы. Тем самым снижается образование мевалоната – вещества, необходимого для поддержания нормальной цитоархитектоники и жизнедеятельности остеокластов [14, 15]. Азотсодержащие БФ являются более сильными ингибиторами остеокластической активности и остеолизиса по сравнению с препаратами, не содержащими в своей структуре азота [16, 17]. Структурные отличия в азотсодержащей цепочке БФ также влияют на их эффективность в отношении ингибирования костной резорбции (рис. 2). Присутствие атома азота в боковой цепи объясняет особый механизм действия азотсодержащих БФ, связанный со способностью ингибировать процесс модификации белков в остеокластах, что ведет к апоптозу зрелых клеток и подтверждается появлением специфических изменений в клетке и структуре ядра [17, 18]. Одновременно отмечается потеря клетками-предшественниками остеокластов способности дифференцировки и созревания, что приводит к уменьшению числа остеокластов. Тем не менее некоторые детали механизма их действия остаются не до конца изученными.
Одновременно отмечается потеря клетками-предшественниками остеокластов способности дифференцировки и созревания, что приводит к уменьшению числа остеокластов. Тем не менее некоторые детали механизма их действия остаются не до конца изученными.
Остеобласты также являются потенциальными мишенями для БФ [18]. Данные in vitro свидетельствуют, что под воздействием БФ остеобласты снижают секрецию остеокласт-стимулирующего фактора [13, 15]. Препараты обладают и рядом анаболических эффектов, поскольку блокируют апоптоз остеобластов и остеоцитов, даже индуцированных глюкокортикоидами, а также стимулируют образование новой кости [13, 17].
До настоящего времени при остеопорозе на практике в основном использовались этидронат и алендронат, как наиболее изученные препараты. В 2010 г. в России появился пока единственный препарат ризедроновой кислоты – Ризендрос®. Ризендрос® относится к азотсодержащим БФ и используется в терапии постменопаузального остеопороза перорально по 35 мг 1 раз в неделю [19, 20].
Клиническая эффективность ризедроната (Ризендрос®) была подтверждена данными ряда многоцентровых исследований по изучению влияния препарата на минеральную плотность костной ткани (МПК) и качество кости, на риск развития новых переломов и переносимость препарата [8, 19, 20, 21, 22, 23].
Одним из важных результатов исследований эффективности ризедроната [9, 10] с практических позиций явилось доказательство того, что препарат способен снижать риск переломов в течение первого года терапии. Так, применение ризедроната позволило уменьшить риск перелома позвонков на 66% уже через 6 месяцев терапии по сравнению с контрольной группой [9].
Важно отметить положительное влияние ризедроната на механическую прочность кости. Длительное применение препарата, как и других БФ, сопровождается положительными изменениями костной микроархитектоники и увеличением толщины трабекул [4]. Так, исследование B. Borah и соавт. (2005) с использованием трехмерной микрокомпьютерной томографии в течение года костных биоптатов показало, что ризедронат сохраняет трабекулярную архитектонику кости у женщин в ранней постменопаузе [19]. Интересные результаты получены и в исследовании D. Mellstrom и соавт., которое продемонстрировало, что через 6–7 лет лечения ризедронатом МПК поясничных позвонков продолжала увеличиваться и частота остеопоротических переломов оставалась стабильной [24]. В метаанализе G. Wells и соавт., который включал 14 049 пациенток с постменопаузальным остеопорозом, было продемонстрировано, что ризедронат эффективен при вторичной профилактике переломов позвонков, периферических переломов, включая переломы бедра [25].
Интересные результаты получены и в исследовании D. Mellstrom и соавт., которое продемонстрировало, что через 6–7 лет лечения ризедронатом МПК поясничных позвонков продолжала увеличиваться и частота остеопоротических переломов оставалась стабильной [24]. В метаанализе G. Wells и соавт., который включал 14 049 пациенток с постменопаузальным остеопорозом, было продемонстрировано, что ризедронат эффективен при вторичной профилактике переломов позвонков, периферических переломов, включая переломы бедра [25].
Терапия остеопороза, являющегося тяжелым хроническим заболеванием, должна проводиться в течение длительного времени (около 3–5 лет), а в случае тяжелого остеопороза у пациентов с переломами – не менее 5 лет [12, 26]. Согласно результатам исследования D. Mellstrom и соавт., долгосрочное лечение ризедронатом у женщин с постменопаузальным остеопорозом является безопасным и не сопровождается повышенным риском побочных явлений при приеме препарата в дозировках, принятых для лечения заболевания [24]. Еженедельный прием 35 мг ризедроната хорошо переносится и сейчас является стандартом схемы применения. К числу побочных эффектов, прежде всего, относятся нарушения со стороны желудочно-кишечного тракта (6–30% случаев): тошнота, рвота, диспепсические явления, абдоминальные боли, изъязвления слизистой оболочки пищевода и желудка [6, 7]. В этом плане интересно, что в сравнительном исследовании, касающемся безопасности различных БФ (ризедронат и алендронат), показано снижение случаев язвы желудка на 69% при использовании ризедроната [17]. Для уменьшения риска раздражающего действия на слизистую оболочку пищевода не следует разжевывать или рассасывать таблетку; также не следует принимать лежачее положение, по крайней мере, на протяжении получаса после приема препарата. Риск побочных явлений со стороны ЖКТ повышается при одновременном назначении ризедроната с нестероидными противовоспалительными препаратами. Поскольку препараты этой группы проникают через плаценту и могут отрицательно влиять на плод, их не следует применять во время беременности.
Еженедельный прием 35 мг ризедроната хорошо переносится и сейчас является стандартом схемы применения. К числу побочных эффектов, прежде всего, относятся нарушения со стороны желудочно-кишечного тракта (6–30% случаев): тошнота, рвота, диспепсические явления, абдоминальные боли, изъязвления слизистой оболочки пищевода и желудка [6, 7]. В этом плане интересно, что в сравнительном исследовании, касающемся безопасности различных БФ (ризедронат и алендронат), показано снижение случаев язвы желудка на 69% при использовании ризедроната [17]. Для уменьшения риска раздражающего действия на слизистую оболочку пищевода не следует разжевывать или рассасывать таблетку; также не следует принимать лежачее положение, по крайней мере, на протяжении получаса после приема препарата. Риск побочных явлений со стороны ЖКТ повышается при одновременном назначении ризедроната с нестероидными противовоспалительными препаратами. Поскольку препараты этой группы проникают через плаценту и могут отрицательно влиять на плод, их не следует применять во время беременности.
В практическом плане важно, что по результатам клинических исследований не выявлено каких-либо различий в эффективности или безопасности ризедроната в зависимости от возраста пациента [4, 19, 20, 21]. Иначе говоря, корректировать дозу препарата у пациентов пожилого возраста не требуется. Кроме того, коррекцию дозы не нужно проводить у пациентов с почечной недостаточностью легкой или средней степени тяжести. Следует иметь в виду, что при одновременном приеме пищи и напитков (включая минеральную воду), препаратов кальция, антацидов и некоторых других препаратов для перорального приема может снижаться всасывание ризедроновой кислоты. Именно поэтому между приемом препарата Ризендрос® и любых других пероральных препаратов или пищи пациенты должны соблюдать, по крайней мере, получасовой интервал. Ризедроновая кислота не влияет на активность ферментов цитохрома Р450 и слабо связывается с белками крови. Следует учитывать, что длительная терапия БФ эффективна при дополнительном приеме солей кальция (1–1,5 г в сутки) и 500 МЕ витамина D [6, 12].
В заключение следует отметить, что в настоящее время признана главенствующая роль бисфосфонатов в практике лечения постменопаузального остеопороза и профилактики его осложнений. Применение ризедроната (Ризендрос®) соответствует решению основной цели лечения остеопороза – снижению риска остеопоротических переломов различных локализаций.
Postmenopauzal’nyy osteoporoz: patofiziologiya, klinicheskie proyavleniya, podkhody k lecheniyu | Kuznetsova
Остеопороз – системное заболевание скелета, характеризующееся уменьшением костной массы и нарушением микроархитектоники костной ткани, что приводит к повышению ломкости костей и увеличению риска переломов (определение ВОЗ). Постменопаузальный остеопороз – заболевание, в основе которого лежит прогрессирующая потеря костной ткани после естественной или индуцированной менопаузы, – наиболее распространенная форма остеопороза. Данное патологическое состояние является первичным (инволюционным) процессом, так же как и старческий остеопороз, который встречается у обоих полов после 70 лет, однако, в отличие от постменопаузального остеопороза, характеризуется поражением трубчатых костей. Постменопаузальный остеопороз поражает в первую очередь губчатые кости, поэтому его результатом через 10–15 лет после прекращения менструаций является повышение частоты переломов позвонков и шейки бедра до 35% по сравнению с репродуктивным периодом.Потеря костной ткани может быть замедлена и даже остановлена при устранении таких предотвратимых факторов риска, как отсутствие физической активности, низкое потребление кальция, первичный гиперпаратиреоз, курение и др.Антирезорбтивная терапия существует в четырех вариантах: женские половые гормоны, препараты кальцитонина (миакальцик), бисфосфонаты, антиэстрогены (селективные модуляторы эстрогенных рецепторов – тамоксифен, ралоксифен). Эффективность методов терапии зависит прежде всего от возраста, который и определяет выбор при прочих равных условиях.
Данное патологическое состояние является первичным (инволюционным) процессом, так же как и старческий остеопороз, который встречается у обоих полов после 70 лет, однако, в отличие от постменопаузального остеопороза, характеризуется поражением трубчатых костей. Постменопаузальный остеопороз поражает в первую очередь губчатые кости, поэтому его результатом через 10–15 лет после прекращения менструаций является повышение частоты переломов позвонков и шейки бедра до 35% по сравнению с репродуктивным периодом.Потеря костной ткани может быть замедлена и даже остановлена при устранении таких предотвратимых факторов риска, как отсутствие физической активности, низкое потребление кальция, первичный гиперпаратиреоз, курение и др.Антирезорбтивная терапия существует в четырех вариантах: женские половые гормоны, препараты кальцитонина (миакальцик), бисфосфонаты, антиэстрогены (селективные модуляторы эстрогенных рецепторов – тамоксифен, ралоксифен). Эффективность методов терапии зависит прежде всего от возраста, который и определяет выбор при прочих равных условиях. У женщин с менопаузальным (климактерическим) синдромом средством первого выбора профилактики и лечения постменопаузального остеопороза является гормональная терапия.Препаратом выбора является алендронат в сочетании с приемом витамина D и кальция. Нет никаких сомнений в том, что время начала и длительность терапии определяют ее протективный эффект, но даже непродолжительные циклы приема бисфосфонатов оказывают положительное воздействие на процессы ремоделирования кости. Лечение остеопороза представляет собой в настоящее время многоэтапный процесс, но на одном из этих этапов в комплекс терапии должны включаться бисфосфонаты.
У женщин с менопаузальным (климактерическим) синдромом средством первого выбора профилактики и лечения постменопаузального остеопороза является гормональная терапия.Препаратом выбора является алендронат в сочетании с приемом витамина D и кальция. Нет никаких сомнений в том, что время начала и длительность терапии определяют ее протективный эффект, но даже непродолжительные циклы приема бисфосфонатов оказывают положительное воздействие на процессы ремоделирования кости. Лечение остеопороза представляет собой в настоящее время многоэтапный процесс, но на одном из этих этапов в комплекс терапии должны включаться бисфосфонаты.
Остеопороз – системное заболевание скелета, характеризующееся уменьшением костной массы и нарушением микроархитектоники костной ткани, что приводит к повышению ломкости костей и увеличению риска переломов (определение ВОЗ). Постменопаузальный остеопороз – заболевание, в основе которого лежит прогрессирующая потеря костной ткани после естественной или индуцированной менопаузы, – наиболее распространенная форма остеопороза [41]. Данное патологическое состояние является первичным (инволюционным) процессом, так же как и старческий остеопороз, который встречается у обоих полов после 70 лет, однако, в отличие от постменопаузального остеопороза, характеризуется поражением трубчатых костей. Постменопаузальный остеопороз поражает в первую очередь губчатые кости, поэтому его результатом через 10–15 лет после прекращения менструаций является повышение частоты переломов позвонков и шейки бедра до 35% по сравнению с репродуктивным периодом. В патогенезе заболевания лежит дефицит половых гормонов, приводящий к ускорению процессов костного метаболизма с нарушением равновесия в сторону костной резорбции [1]. Уменьшение костной массы происходит особенно быстро в течение 3–4 лет постменопаузы и приводит к потере трабекулярных пластин и возрастанию риска переломов.
Постменопаузальный остеопороз – заболевание, в основе которого лежит прогрессирующая потеря костной ткани после естественной или индуцированной менопаузы, – наиболее распространенная форма остеопороза [41]. Данное патологическое состояние является первичным (инволюционным) процессом, так же как и старческий остеопороз, который встречается у обоих полов после 70 лет, однако, в отличие от постменопаузального остеопороза, характеризуется поражением трубчатых костей. Постменопаузальный остеопороз поражает в первую очередь губчатые кости, поэтому его результатом через 10–15 лет после прекращения менструаций является повышение частоты переломов позвонков и шейки бедра до 35% по сравнению с репродуктивным периодом. В патогенезе заболевания лежит дефицит половых гормонов, приводящий к ускорению процессов костного метаболизма с нарушением равновесия в сторону костной резорбции [1]. Уменьшение костной массы происходит особенно быстро в течение 3–4 лет постменопаузы и приводит к потере трабекулярных пластин и возрастанию риска переломов. Роль эстрогенного дефицита в патогенезе остеопороза подтверждают эпидемиологические данные. Остеопороз выявляется у каждой третьей женщины в возрасте старше 50 лет. В Европе, США и Японии им страдают около 75 млн человек [29], и 80% из них составляют женщины [33]. По мере старения населения повышается не только частота остеопороза, но и риск остеопоретических переломов [10, 36, 47]. Распространенность остеопоретических переломов увеличивается с возрастом, приводя к повышению риска смертности [9, 20, 35], болей [10, 16], инвалидизации [29] и других переломов всех типов, включая переломы бедренных костей [21]. Среди женщин с одним переломом в анамнезе уровень смертности с учетом возраста увеличивается на 23% по сравнению с популяционными показателями [23]. Наличие в анамнезе пациенток с постменопаузальным остеопорозом перелома позвоночника повышает относительный риск смерти на 60% [19]. Объясняет повышенный риск смертельного исхода при остеопорозе высокая распространенность фатальных сердечно-сосудистых и легочных заболеваний после перелома [22, 24, 32].
Роль эстрогенного дефицита в патогенезе остеопороза подтверждают эпидемиологические данные. Остеопороз выявляется у каждой третьей женщины в возрасте старше 50 лет. В Европе, США и Японии им страдают около 75 млн человек [29], и 80% из них составляют женщины [33]. По мере старения населения повышается не только частота остеопороза, но и риск остеопоретических переломов [10, 36, 47]. Распространенность остеопоретических переломов увеличивается с возрастом, приводя к повышению риска смертности [9, 20, 35], болей [10, 16], инвалидизации [29] и других переломов всех типов, включая переломы бедренных костей [21]. Среди женщин с одним переломом в анамнезе уровень смертности с учетом возраста увеличивается на 23% по сравнению с популяционными показателями [23]. Наличие в анамнезе пациенток с постменопаузальным остеопорозом перелома позвоночника повышает относительный риск смерти на 60% [19]. Объясняет повышенный риск смертельного исхода при остеопорозе высокая распространенность фатальных сердечно-сосудистых и легочных заболеваний после перелома [22, 24, 32]. Выделяют непредотвратимые и предотвратимые факторы риска остеопороза [1]. Потеря костной ткани может быть замедлена и даже остановлена при устранении таких предотвратимых факторов риска, как отсутствие физической активности, низкое потребление кальция, первичный гиперпаратиреоз, курение и др. В целом рассматриваются и рекомендуются к выявлению следующие факторы риска. Генетический фактор, который устанавливается по наличию у родственников первой линии низкотравматичных переломов. Факторы окружающей среды, к которым относятся курение, злоупотребление алкоголем, отсутствие физической активности, астеническое телосложение, диета с низким содержанием кальция, недостаточное количество солнечного света. Особенности менструальной функции, среди которых имеют значение ранняя менопауза (до 45 лет) и эпизоды аменореи в репродуктивном возрасте. К потере костной ткани приводят некоторые медикаменты: глюкокортикоиды (от 7,5 мг/сут преднизона более 3 мес), противоэпилептические препараты (фенитоин), передозированная заместительная терапия (тироксин, гидрокортизон), антикоагулянты (гепарин, варфарин).
Выделяют непредотвратимые и предотвратимые факторы риска остеопороза [1]. Потеря костной ткани может быть замедлена и даже остановлена при устранении таких предотвратимых факторов риска, как отсутствие физической активности, низкое потребление кальция, первичный гиперпаратиреоз, курение и др. В целом рассматриваются и рекомендуются к выявлению следующие факторы риска. Генетический фактор, который устанавливается по наличию у родственников первой линии низкотравматичных переломов. Факторы окружающей среды, к которым относятся курение, злоупотребление алкоголем, отсутствие физической активности, астеническое телосложение, диета с низким содержанием кальция, недостаточное количество солнечного света. Особенности менструальной функции, среди которых имеют значение ранняя менопауза (до 45 лет) и эпизоды аменореи в репродуктивном возрасте. К потере костной ткани приводят некоторые медикаменты: глюкокортикоиды (от 7,5 мг/сут преднизона более 3 мес), противоэпилептические препараты (фенитоин), передозированная заместительная терапия (тироксин, гидрокортизон), антикоагулянты (гепарин, варфарин). Риск остеопороза повышается при ряде заболеваний, в частности, эндокринопатиях (первичный гиперпаратиреоз, тиреотоксикоз, синдром Кушинга, болезнь Аддисона), болезнях крови (миелома, системный мастоцитоз, лимфома, лейкемия, пернициозная анемия), ревматических заболеваниях (ревматоидный артрит, анкилозирующий спондилит), желудочно-кишечной патологии (синдромы мальабсорбции, хронические заболевания печени). Клиническая диагностика остеопороза затруднена и не имеет патогномоничных симптомов. Клинические проявления весьма вариабельны: от полного отсутствия субъективных ощущений и жалоб до жалоб на боли в спине, «во всех костях». Выраженные боли в позвоночнике могут свидетельствовать о возникновении одного из основных осложнений остеопороза – перелома позвонков. Непереносимая, изнуряющая боль порою мучает пациентов неделями и месяцами, иногда хроническая боль сохраняется годами. Следствием переломов позвонков становится кифоз – искривление позвоночника, приводящее к уменьшению роста (иногда на 10–15 см), абдоминальная протрузия и горб в верхней части позвоночника.
Риск остеопороза повышается при ряде заболеваний, в частности, эндокринопатиях (первичный гиперпаратиреоз, тиреотоксикоз, синдром Кушинга, болезнь Аддисона), болезнях крови (миелома, системный мастоцитоз, лимфома, лейкемия, пернициозная анемия), ревматических заболеваниях (ревматоидный артрит, анкилозирующий спондилит), желудочно-кишечной патологии (синдромы мальабсорбции, хронические заболевания печени). Клиническая диагностика остеопороза затруднена и не имеет патогномоничных симптомов. Клинические проявления весьма вариабельны: от полного отсутствия субъективных ощущений и жалоб до жалоб на боли в спине, «во всех костях». Выраженные боли в позвоночнике могут свидетельствовать о возникновении одного из основных осложнений остеопороза – перелома позвонков. Непереносимая, изнуряющая боль порою мучает пациентов неделями и месяцами, иногда хроническая боль сохраняется годами. Следствием переломов позвонков становится кифоз – искривление позвоночника, приводящее к уменьшению роста (иногда на 10–15 см), абдоминальная протрузия и горб в верхней части позвоночника.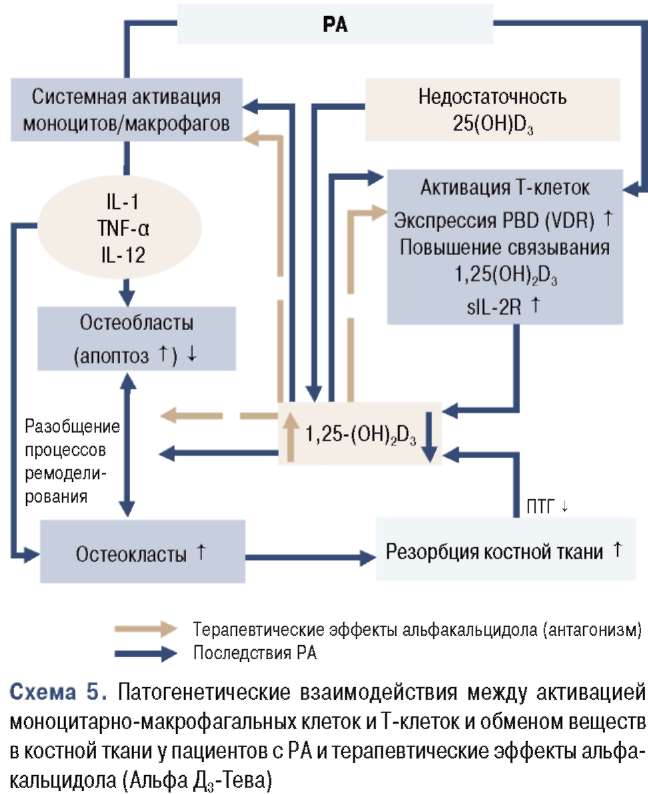 Кифоз в сочетании с болью ограничивает способность больных к повседневной деятельности: у пациентов появляется постоянное чувство страха падения. По мере усиления кифоза теряется ортостатическая стабильность, и в итоге пациент не может передвигаться без посторонней помощи [29]. Наличие переломов позвонков в анамнезе предрасполагает к последующим переломам всех видов. Перелом позвоночника в 2–4 раза увеличивает риск повторного перелома этой же локализации и переломов всех типов, в том числе бедренных костей [22, 28]. С позиций прогноза именно переломы бедренных костей являются наиболее тяжелыми. Относительный риск смерти после переломов бедренных костей в 6 раз выше, чем в популяции того же возраста [7]. Медицинская и социальная значимость переломов и их последствий в совокупности с поздней и не имеющей характерных признаков симптоматикой остеопороза обусловливает необходимость ранней диагностики этого заболевания. В процессе диагностики оцениваются степень тяжести остеопороза (инструментальные методы) и степень активности процесса (биохимические методы).
Кифоз в сочетании с болью ограничивает способность больных к повседневной деятельности: у пациентов появляется постоянное чувство страха падения. По мере усиления кифоза теряется ортостатическая стабильность, и в итоге пациент не может передвигаться без посторонней помощи [29]. Наличие переломов позвонков в анамнезе предрасполагает к последующим переломам всех видов. Перелом позвоночника в 2–4 раза увеличивает риск повторного перелома этой же локализации и переломов всех типов, в том числе бедренных костей [22, 28]. С позиций прогноза именно переломы бедренных костей являются наиболее тяжелыми. Относительный риск смерти после переломов бедренных костей в 6 раз выше, чем в популяции того же возраста [7]. Медицинская и социальная значимость переломов и их последствий в совокупности с поздней и не имеющей характерных признаков симптоматикой остеопороза обусловливает необходимость ранней диагностики этого заболевания. В процессе диагностики оцениваются степень тяжести остеопороза (инструментальные методы) и степень активности процесса (биохимические методы). Степень тяжести оценивается по двум параметрам: потере минеральной плотности кости (МПК) и наличию переломов. Для оценки МПК используют инструментальные методы: рентгенографию, одно- и двухфотонную денситометрию (абсорбциометрию), одно- и двухэнергетическую рентгеновскую абсорбциометрию, количественную компьютерную томографию, ультразвуковое исследование пяточной кости. Рентгенография для диагностики остеопении и начальных форм остеопороза неинформативна. Для выявления групп риска развившегося остеопороза и оценки ответа на терапию проводят денситометрию. «Золотым стандартом» среди методов костной денситометрии считается двухэнергетическая рентгеновская денситометрия (абсорбциометрия) позвоночника и проксимального отдела бедра. Проведение денситометрии в постменопаузе показано всем женщинам старше 65 лет и женщинам более молодого возраста, имеющим один и более факторов риска [34]. Остеопороз характеризуется снижением МПК более чем на 2,5 стандартного отклонения, при остеопении МПК находится в пределах 1–2,5 стандартного отклонения от среднего значения пиковой костной массы молодых здоровых женщин [38].
Степень тяжести оценивается по двум параметрам: потере минеральной плотности кости (МПК) и наличию переломов. Для оценки МПК используют инструментальные методы: рентгенографию, одно- и двухфотонную денситометрию (абсорбциометрию), одно- и двухэнергетическую рентгеновскую абсорбциометрию, количественную компьютерную томографию, ультразвуковое исследование пяточной кости. Рентгенография для диагностики остеопении и начальных форм остеопороза неинформативна. Для выявления групп риска развившегося остеопороза и оценки ответа на терапию проводят денситометрию. «Золотым стандартом» среди методов костной денситометрии считается двухэнергетическая рентгеновская денситометрия (абсорбциометрия) позвоночника и проксимального отдела бедра. Проведение денситометрии в постменопаузе показано всем женщинам старше 65 лет и женщинам более молодого возраста, имеющим один и более факторов риска [34]. Остеопороз характеризуется снижением МПК более чем на 2,5 стандартного отклонения, при остеопении МПК находится в пределах 1–2,5 стандартного отклонения от среднего значения пиковой костной массы молодых здоровых женщин [38]. Оценка степени активности остеопороза проводится по биохимическим маркерам костной резорбции и ремоделирования в крови и моче (щелочная фосфатаза, пиридинолин и др.). Целью терапии постменопаузального остеопороза является снижение частоты переломов. Сохранение костной массы и предотвращение первого перелома позвоночника – жизненно важная задача, определяющая необходимость раннего начала терапии [21]. При наличии двух и более факторов риска и/или снижения МПК необходимо решить вопрос о тактике предотвращения потери костной ткани. В комплексе профилактических мероприятий важное место занимают рекомендации немедикаментозного характера, такие как сбалансированная диета, прием адекватного количества кальция и витамина D, физические упражнения, отказ от курения и избыточного приема алкоголя, предотвращение падений. Естественно, эти рекомендации должны быть максимально индивидуализированы. Для получения хорошего результата по изменению образа жизни необходимо периодически проводить оценку образа жизни конкретной пациентки, модифицируя советы по питанию, физической активности, приему витаминов и минералов и т.
Оценка степени активности остеопороза проводится по биохимическим маркерам костной резорбции и ремоделирования в крови и моче (щелочная фосфатаза, пиридинолин и др.). Целью терапии постменопаузального остеопороза является снижение частоты переломов. Сохранение костной массы и предотвращение первого перелома позвоночника – жизненно важная задача, определяющая необходимость раннего начала терапии [21]. При наличии двух и более факторов риска и/или снижения МПК необходимо решить вопрос о тактике предотвращения потери костной ткани. В комплексе профилактических мероприятий важное место занимают рекомендации немедикаментозного характера, такие как сбалансированная диета, прием адекватного количества кальция и витамина D, физические упражнения, отказ от курения и избыточного приема алкоголя, предотвращение падений. Естественно, эти рекомендации должны быть максимально индивидуализированы. Для получения хорошего результата по изменению образа жизни необходимо периодически проводить оценку образа жизни конкретной пациентки, модифицируя советы по питанию, физической активности, приему витаминов и минералов и т. д. Риск падения должен быть оценен особо, желательно непосредственно после наступления менопаузы. Начинать лечение постменопаузального остеопороза с целью профилактики переломов следует при снижении МПК (T-критерий) ниже 2,5 вне зависимости от факторов риска и ниже 1,1 при наличии факторов риска (семейный анамнез остеопороза и/или переломов при низком уровне травмы у родственников в возрасте 50 лет и старше, предшествующие переломы, ранняя или преждевременная менопауза, овариэктомия в молодом возрасте, низкая масса тела) [28]. Антирезорбтивная терапия существует в четырех вариантах: женские половые гормоны, препараты кальцитонина (миакальцик), бисфосфонаты, антиэстрогены (селективные модуляторы эстрогенных рецепторов – тамоксифен, ралоксифен). Эффективность методов терапии зависит прежде всего от возраста, который и определяет выбор при прочих равных условиях. У женщин с менопаузальным (климактерическим) синдромом средством первого выбора профилактики и лечения постменопаузального остеопороза является гормональная терапия.
д. Риск падения должен быть оценен особо, желательно непосредственно после наступления менопаузы. Начинать лечение постменопаузального остеопороза с целью профилактики переломов следует при снижении МПК (T-критерий) ниже 2,5 вне зависимости от факторов риска и ниже 1,1 при наличии факторов риска (семейный анамнез остеопороза и/или переломов при низком уровне травмы у родственников в возрасте 50 лет и старше, предшествующие переломы, ранняя или преждевременная менопауза, овариэктомия в молодом возрасте, низкая масса тела) [28]. Антирезорбтивная терапия существует в четырех вариантах: женские половые гормоны, препараты кальцитонина (миакальцик), бисфосфонаты, антиэстрогены (селективные модуляторы эстрогенных рецепторов – тамоксифен, ралоксифен). Эффективность методов терапии зависит прежде всего от возраста, который и определяет выбор при прочих равных условиях. У женщин с менопаузальным (климактерическим) синдромом средством первого выбора профилактики и лечения постменопаузального остеопороза является гормональная терапия. Гормональная терапия может быть первой фазой длительной программы профилактики/лечения остеопороза и при отсутствии климактерического синдрома с последующим использованием селективных модуляторов рецепторов эстрогенов и/или бисфосфонатов и терипаратида по показаниям. При нежелании женщины принимать гормоны или при наличии противопоказаний к их назначению, а также при первичном обращении в возрасте старше 60 лет методом первого выбора профилактики и лечения остеопороза становятся бисфосфонаты. Следует отметить, что прием гормонов не исключает возможность использования бисфосфонатов, более того, комбинация гормонотерапии и бисфосфонатов оказывает синергичное действие на МПК. По химической структуре бисфосфонаты являются стабильными синтетическими аналогами пирофосфата, имеющими высокое сродство к гидроксиапатиту, который составляет минеральную основу костной ткани. Антирезорбтивное действие бисфосфонатов на костный метаболизм многопланово. Оно осуществляется благодаря влиянию на обмен кальция: снижению его резорбции из костей и снижению экскреции почками, а также образованию физико-химических связей с гидроксиапатитом в участках резорбции костной ткани [3].
Гормональная терапия может быть первой фазой длительной программы профилактики/лечения остеопороза и при отсутствии климактерического синдрома с последующим использованием селективных модуляторов рецепторов эстрогенов и/или бисфосфонатов и терипаратида по показаниям. При нежелании женщины принимать гормоны или при наличии противопоказаний к их назначению, а также при первичном обращении в возрасте старше 60 лет методом первого выбора профилактики и лечения остеопороза становятся бисфосфонаты. Следует отметить, что прием гормонов не исключает возможность использования бисфосфонатов, более того, комбинация гормонотерапии и бисфосфонатов оказывает синергичное действие на МПК. По химической структуре бисфосфонаты являются стабильными синтетическими аналогами пирофосфата, имеющими высокое сродство к гидроксиапатиту, который составляет минеральную основу костной ткани. Антирезорбтивное действие бисфосфонатов на костный метаболизм многопланово. Оно осуществляется благодаря влиянию на обмен кальция: снижению его резорбции из костей и снижению экскреции почками, а также образованию физико-химических связей с гидроксиапатитом в участках резорбции костной ткани [3]. Кроме того, бисфосфонаты воздействуют на процессы резорбции и ремоделирования кости [18]. Костная резорбция зависит от функции остеокластов, которая оценивается по активности протеин-тирозинкиназы (ПТК) и протеин-тирозинфосфатазы (ПТФ), в то время как ингибитор ПТК гербимицин А и ингибитор ПТФ ортованадат демонстрируют антирезорбтивную активность. Бисфосфонаты могут оказывать влияние на фундаментальные фосфатзависимые биохимические процессы. Так, алендронат ингибирует активность как ПТК, так и нескольких представителей семейства ПТФ, в частности ПТФd и ПТФmeg1, т.е. антирезорбтивная активность бисфосфонатов, в частности наиболее изученного алендроната, реализуется и посредством вмешательства в процессы внутриклеточного взаимодействия [37]. Бисфосфонаты уменьшают пул остеокластов за счет подавления их дифференцировки из клеток-предшественников и усиления апоптоза. Также бисфосфонаты положительно влияют на среднюю продолжительность жизни остеоцитов. В итоге эффект бисфосфонатов реализуется в сдвиге баланса костного метаболизма в сторону костеобразования [44].
Кроме того, бисфосфонаты воздействуют на процессы резорбции и ремоделирования кости [18]. Костная резорбция зависит от функции остеокластов, которая оценивается по активности протеин-тирозинкиназы (ПТК) и протеин-тирозинфосфатазы (ПТФ), в то время как ингибитор ПТК гербимицин А и ингибитор ПТФ ортованадат демонстрируют антирезорбтивную активность. Бисфосфонаты могут оказывать влияние на фундаментальные фосфатзависимые биохимические процессы. Так, алендронат ингибирует активность как ПТК, так и нескольких представителей семейства ПТФ, в частности ПТФd и ПТФmeg1, т.е. антирезорбтивная активность бисфосфонатов, в частности наиболее изученного алендроната, реализуется и посредством вмешательства в процессы внутриклеточного взаимодействия [37]. Бисфосфонаты уменьшают пул остеокластов за счет подавления их дифференцировки из клеток-предшественников и усиления апоптоза. Также бисфосфонаты положительно влияют на среднюю продолжительность жизни остеоцитов. В итоге эффект бисфосфонатов реализуется в сдвиге баланса костного метаболизма в сторону костеобразования [44]. Наконец, в эксперименте и в нескольких контролируемых исследованиях были выявлены хондропротективные свойства бисфосфонатов, препятствующие деструкции хрящевой ткани [5]. Дополнительное, не вполне изученное свойство бисфосфонатов, это их анальгетический эффект. Согласно наиболее распространенной точке зрения, бисфосфонаты, ингибируя остеокласты, снижают выраженность воспалительной реакции, сопровождающей остеолизис. Однако результаты экспериментальных исследований позволяют предположить, что в анальгетическом эффекте данной группы лекарственных средств реализуются и другие механизмы, например, центральное антиноцицептивное действие, опосредованное через изменение метаболизма кальция [4]. Ионы кальция играют важную роль в эндогенной регуляции болевой чувствительности [6]. В острых ситуациях блокаторы кальциевых каналов проявляют свойства антиноцицептиков, в клинических исследованиях болеутоляющий эффект морфина потенцируется блокаторами кальциевых каналов [45]. В клинических исследованиях установлено, что терапия бисфосфонатами увеличивает МПК в позвоночнике и бедренных костях, способствует сохранению высоты тел позвонков и препятствует снижению роста тела.
Наконец, в эксперименте и в нескольких контролируемых исследованиях были выявлены хондропротективные свойства бисфосфонатов, препятствующие деструкции хрящевой ткани [5]. Дополнительное, не вполне изученное свойство бисфосфонатов, это их анальгетический эффект. Согласно наиболее распространенной точке зрения, бисфосфонаты, ингибируя остеокласты, снижают выраженность воспалительной реакции, сопровождающей остеолизис. Однако результаты экспериментальных исследований позволяют предположить, что в анальгетическом эффекте данной группы лекарственных средств реализуются и другие механизмы, например, центральное антиноцицептивное действие, опосредованное через изменение метаболизма кальция [4]. Ионы кальция играют важную роль в эндогенной регуляции болевой чувствительности [6]. В острых ситуациях блокаторы кальциевых каналов проявляют свойства антиноцицептиков, в клинических исследованиях болеутоляющий эффект морфина потенцируется блокаторами кальциевых каналов [45]. В клинических исследованиях установлено, что терапия бисфосфонатами увеличивает МПК в позвоночнике и бедренных костях, способствует сохранению высоты тел позвонков и препятствует снижению роста тела. Бисфосфонаты облегчают боль, связанную с остеопорозом, и этот эффект крайне важен с позиций улучшения качества жизни пациентов. Очень важно и то обстоятельство, что бисфосфонаты значительно снижают риск внепозвонковых переломов [8]. В настоящее время выделяют три поколения бисфосфонатов. • I поколение: этидронат, клодронат; • II поколение: алендронат, памидронат, тилудронат; • III поколение: ризедронат, ибандронат. Одним из наиболее изученных и широко применяемых бисфосфонатов является алендронат. Международные рекомендации по лечению остеопороза и профилактике переломов позвонков предлагают для предотвращения риска повторных переломов у женщин с множественными переломами позвонков назначение ризедроната в сочетании с приемом кальция и витамина D. При наличии остеопороза у женщин, имеющих и не имеющих переломы позвонков в анамнезе, предотвращение риска переломов всех локализаций рекомендуется проводить с помощью алендроната 10 мг/сут или 70 мг один раз в неделю, также с кальцием и витамином D.
Бисфосфонаты облегчают боль, связанную с остеопорозом, и этот эффект крайне важен с позиций улучшения качества жизни пациентов. Очень важно и то обстоятельство, что бисфосфонаты значительно снижают риск внепозвонковых переломов [8]. В настоящее время выделяют три поколения бисфосфонатов. • I поколение: этидронат, клодронат; • II поколение: алендронат, памидронат, тилудронат; • III поколение: ризедронат, ибандронат. Одним из наиболее изученных и широко применяемых бисфосфонатов является алендронат. Международные рекомендации по лечению остеопороза и профилактике переломов позвонков предлагают для предотвращения риска повторных переломов у женщин с множественными переломами позвонков назначение ризедроната в сочетании с приемом кальция и витамина D. При наличии остеопороза у женщин, имеющих и не имеющих переломы позвонков в анамнезе, предотвращение риска переломов всех локализаций рекомендуется проводить с помощью алендроната 10 мг/сут или 70 мг один раз в неделю, также с кальцием и витамином D.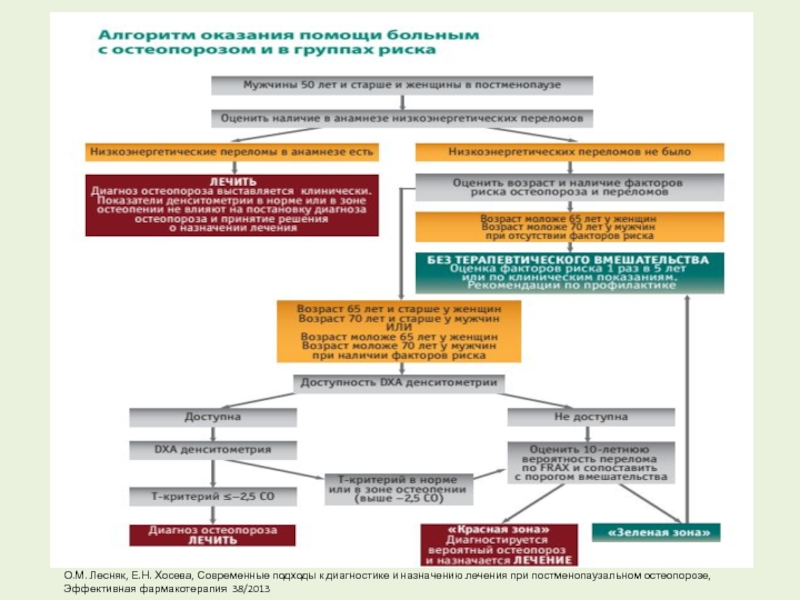 С позиций предотвращения остеопороза у женщин, имеющих остеопению и факторы риска остеопороза, важно не столько вернуть, сколько стабилизировать показатели МПК. Для достижения этого эффекта доза 5 мг/сут алендроната признается более предпочтительной и рекомендуется к использованию с целью профилактики остеопороза [17, 31, 40]. На фоне приема алендроната уже через 1 мес терапии отмечается снижение маркеров костной резорбции до уровня пременопаузы, в то время как уровни маркеров костеобразования снижаются через 3 мес терапии [5]. Алендронат быстро повышает плотность кости в поясничном отделе позвоночника, показатели которой становятся достоверно выше уже через 6 мес лечения. После 24 мес максимальное повышение МПК позвоночника на фоне еженедельного приема алендроната составляет 6,8%, а ежедневного приема – 7,4% [41]. Через 3 года терапии алендронат, накапливаясь в костной ткани, увеличивает МПК в поясничном отделе позвоночника на 8,8% и шейке бедренной кости на 5,9%, а по окончании 7 лет терапии – на 11,2%.
С позиций предотвращения остеопороза у женщин, имеющих остеопению и факторы риска остеопороза, важно не столько вернуть, сколько стабилизировать показатели МПК. Для достижения этого эффекта доза 5 мг/сут алендроната признается более предпочтительной и рекомендуется к использованию с целью профилактики остеопороза [17, 31, 40]. На фоне приема алендроната уже через 1 мес терапии отмечается снижение маркеров костной резорбции до уровня пременопаузы, в то время как уровни маркеров костеобразования снижаются через 3 мес терапии [5]. Алендронат быстро повышает плотность кости в поясничном отделе позвоночника, показатели которой становятся достоверно выше уже через 6 мес лечения. После 24 мес максимальное повышение МПК позвоночника на фоне еженедельного приема алендроната составляет 6,8%, а ежедневного приема – 7,4% [41]. Через 3 года терапии алендронат, накапливаясь в костной ткани, увеличивает МПК в поясничном отделе позвоночника на 8,8% и шейке бедренной кости на 5,9%, а по окончании 7 лет терапии – на 11,2%. Прием 10 мг/сут алендроната в течение 10 лет приводит к кумулятивному увеличению МПК поясничного отдела позвоночника на 13,7% от исходного показателя, т.е. при продолжении лечения уровень МПК не достигает плато, а продолжает повышаться в прямой зависимости от дозы и срока терапии. Это увеличение МПК в проведенных исследованиях коррелировало с динамикой биохимических маркеров костной резорбции на 2-м месяце лечения, маркеров остеогенеза – на 6-м месяце терапии. Биохимическое мониторирование лечения важно с прогностической точки зрения, так как изменение показателей маркеров костного метаболизма позволяет прогнозировать минеральную плотность кости на 2-м году терапии [13]. Целью лечебных мероприятий при остеопорозе является профилактика переломов. В результате применения алендроната риск переломов позвоночника, бедра и кисти снижается на 40–50% и предотвращается потеря высоты тела [17, 27]. В исследовании FIT (Fracture Intervention Trial), включавшем 2027 женщин с переломами позвонков в анамнезе, результаты приема 5 мг алендроната ежедневно в течение 2 лет с последующим увеличением дозы до 10 мг/сут в течение заключительных 9 мес исследования сравнивали с плацебо.
Прием 10 мг/сут алендроната в течение 10 лет приводит к кумулятивному увеличению МПК поясничного отдела позвоночника на 13,7% от исходного показателя, т.е. при продолжении лечения уровень МПК не достигает плато, а продолжает повышаться в прямой зависимости от дозы и срока терапии. Это увеличение МПК в проведенных исследованиях коррелировало с динамикой биохимических маркеров костной резорбции на 2-м месяце лечения, маркеров остеогенеза – на 6-м месяце терапии. Биохимическое мониторирование лечения важно с прогностической точки зрения, так как изменение показателей маркеров костного метаболизма позволяет прогнозировать минеральную плотность кости на 2-м году терапии [13]. Целью лечебных мероприятий при остеопорозе является профилактика переломов. В результате применения алендроната риск переломов позвоночника, бедра и кисти снижается на 40–50% и предотвращается потеря высоты тела [17, 27]. В исследовании FIT (Fracture Intervention Trial), включавшем 2027 женщин с переломами позвонков в анамнезе, результаты приема 5 мг алендроната ежедневно в течение 2 лет с последующим увеличением дозы до 10 мг/сут в течение заключительных 9 мес исследования сравнивали с плацебо. Частота новых переломов позвонков (включая клинически манифестированные) оказалась на 47% ниже частоты аналогичных переломов в группе плацебо. Сходные результаты были получены по частоте переломов бедра и запястья [2]. Риск переломов бедра снижался на 63% после 18 мес приема алендроната [10], причем снижение риска переломов значительно опережало повышение МПК именно на фоне приема алендроната, что отличает его от других видов антирезорбтивной терапии. Сходный эффект демонстрируют ралоксифен и некоторые представители бисфосфонатов, но суть этого дополнительного протективного влияния в отношении бедренной кости не ясна [39]. В рекомендуемых дозах и при соблюдении режима приема (вертикальное положение тела в течение 30 мин после приема, запивание таблетки стаканом воды) бисфосфонаты обычно хорошо переносятся и характеризуются высокой степенью безопасности для пациентов. К побочным эффектам бисфосфонатов относятся нарушения со стороны верхних отделов желудочно-кишечного тракта (ЖКТ). При использовании алендроната описаны случаи эзофагита, симптомы которого появляются в пределах 1 мес от начала терапии [17].
Частота новых переломов позвонков (включая клинически манифестированные) оказалась на 47% ниже частоты аналогичных переломов в группе плацебо. Сходные результаты были получены по частоте переломов бедра и запястья [2]. Риск переломов бедра снижался на 63% после 18 мес приема алендроната [10], причем снижение риска переломов значительно опережало повышение МПК именно на фоне приема алендроната, что отличает его от других видов антирезорбтивной терапии. Сходный эффект демонстрируют ралоксифен и некоторые представители бисфосфонатов, но суть этого дополнительного протективного влияния в отношении бедренной кости не ясна [39]. В рекомендуемых дозах и при соблюдении режима приема (вертикальное положение тела в течение 30 мин после приема, запивание таблетки стаканом воды) бисфосфонаты обычно хорошо переносятся и характеризуются высокой степенью безопасности для пациентов. К побочным эффектам бисфосфонатов относятся нарушения со стороны верхних отделов желудочно-кишечного тракта (ЖКТ). При использовании алендроната описаны случаи эзофагита, симптомы которого появляются в пределах 1 мес от начала терапии [17]. Заболевания верхних отделов ЖКТ, затрудняющие эвакуацию пищи из пищевода, такие как ахалазия и пищеводные стриктуры, являются абсолютными противопоказаниями для терапии алендронатом, а гастро-эзофагеальная рефлюксная болезнь рассматривается как относительное противопоказание. Такие заболевания, как гастрит, язвенная болезнь двенадцатиперстной кишки вне обострения, не являются противопоказанием к назначению бисфосфонатов. Алендронату, как и всем препаратам этой фармакологической группы, свойственна низкая абсорбция из кишечника, особенно в присутствии продуктов и лекарственных средств с высоким содержанием кальция и поливалентных катионов. Поэтому с целью минимизации побочных эффектов и увеличения абсорбции лекарственного средства рекомендуется принимать алендронат, запивая таблетку стаканом воды, находясь в вертикальном положении, по крайней мере за 30 мин до завтрака. Побочные эффекты и особенности приема бисфосфонатов могут снижать приверженность пациентов терапии. Но надо критично относиться к негативным реакциям, сопутствующим приему этой группы препаратов.
Заболевания верхних отделов ЖКТ, затрудняющие эвакуацию пищи из пищевода, такие как ахалазия и пищеводные стриктуры, являются абсолютными противопоказаниями для терапии алендронатом, а гастро-эзофагеальная рефлюксная болезнь рассматривается как относительное противопоказание. Такие заболевания, как гастрит, язвенная болезнь двенадцатиперстной кишки вне обострения, не являются противопоказанием к назначению бисфосфонатов. Алендронату, как и всем препаратам этой фармакологической группы, свойственна низкая абсорбция из кишечника, особенно в присутствии продуктов и лекарственных средств с высоким содержанием кальция и поливалентных катионов. Поэтому с целью минимизации побочных эффектов и увеличения абсорбции лекарственного средства рекомендуется принимать алендронат, запивая таблетку стаканом воды, находясь в вертикальном положении, по крайней мере за 30 мин до завтрака. Побочные эффекты и особенности приема бисфосфонатов могут снижать приверженность пациентов терапии. Но надо критично относиться к негативным реакциям, сопутствующим приему этой группы препаратов. Плацебо-контролируемые исследования выявили частоту жалоб со стороны ЖКТ, составляющую 11% при приеме бисфосфонатов и 13% при приеме плацебо [15]. Побочные реакции реже возникали у пациентов (8%), ранее принимавших бисфосфонаты по сравнению с больными (16%), впервые начавшими использовать этот метод терапии. В целом даже столь длительное лечение, как 10-летнее использование бисфосфонатов, хорошо переносилось мотивированными пациентами, практически не отмечавшими побочных эффектов [46]. Оптимальная продолжительность терапии бисфосфонатами не установлена. Очевидно, 6-месячный курс приема бисфосфонатов недостаточен для длительной программы предотвращения остеопороза и переломов, так как за 6–9 мес после отмены лечения биохимические маркеры костного метаболизма возвращаются к исходному уровню [43]. С другой стороны, у женщин, принимавших бисфосфонаты в течение 6–7 лет, минеральная плотность кости сохраняется на достигнутом уровне в течение первых двух лет после прекращения терапии [26], хотя биохимические маркеры реагируют на отмену лечения непосредственно после его окончания.
Плацебо-контролируемые исследования выявили частоту жалоб со стороны ЖКТ, составляющую 11% при приеме бисфосфонатов и 13% при приеме плацебо [15]. Побочные реакции реже возникали у пациентов (8%), ранее принимавших бисфосфонаты по сравнению с больными (16%), впервые начавшими использовать этот метод терапии. В целом даже столь длительное лечение, как 10-летнее использование бисфосфонатов, хорошо переносилось мотивированными пациентами, практически не отмечавшими побочных эффектов [46]. Оптимальная продолжительность терапии бисфосфонатами не установлена. Очевидно, 6-месячный курс приема бисфосфонатов недостаточен для длительной программы предотвращения остеопороза и переломов, так как за 6–9 мес после отмены лечения биохимические маркеры костного метаболизма возвращаются к исходному уровню [43]. С другой стороны, у женщин, принимавших бисфосфонаты в течение 6–7 лет, минеральная плотность кости сохраняется на достигнутом уровне в течение первых двух лет после прекращения терапии [26], хотя биохимические маркеры реагируют на отмену лечения непосредственно после его окончания. Прием алендроната в дозе 5 мг в течение 5 лет у женщин с остеопенией стабилизировал костную массу позвоночника, бедра и организма в целом и имел сходные итоговые показатели по МПК в сравнении с режимом приема алендроната в дозе 20 мг в течение 3 лет. Потеря костной массы, закономерно возобновляющаяся после отмены лечения, происходит со скоростью, характерной для ранней постменопаузы, следовательно, протективный эффект бисфосфонатов в отношении остеопороза и переломов сохраняется в течение нескольких лет [40]. В настоящее время в России зарегистрировано несколько препаратов, содержащих алендронат, к ним относятся Фосамакс® оригинальный алендроната натрия тригидрат 70 мг 1 раз/нед и 10 мг/сут и Осталон® производства ОАО «Гедеон Рихтер». Проведенные исследования по сопоставимости действия этих двух препаратов in vitro и in vivo показали полную их биоэквивалентность. В Венгрии проведено постмаркетинговое исследование IV фазы по изучению эффективности и переносимости Осталона® в течение 12 мес терапии пациентов с остеопорозом.
Прием алендроната в дозе 5 мг в течение 5 лет у женщин с остеопенией стабилизировал костную массу позвоночника, бедра и организма в целом и имел сходные итоговые показатели по МПК в сравнении с режимом приема алендроната в дозе 20 мг в течение 3 лет. Потеря костной массы, закономерно возобновляющаяся после отмены лечения, происходит со скоростью, характерной для ранней постменопаузы, следовательно, протективный эффект бисфосфонатов в отношении остеопороза и переломов сохраняется в течение нескольких лет [40]. В настоящее время в России зарегистрировано несколько препаратов, содержащих алендронат, к ним относятся Фосамакс® оригинальный алендроната натрия тригидрат 70 мг 1 раз/нед и 10 мг/сут и Осталон® производства ОАО «Гедеон Рихтер». Проведенные исследования по сопоставимости действия этих двух препаратов in vitro и in vivo показали полную их биоэквивалентность. В Венгрии проведено постмаркетинговое исследование IV фазы по изучению эффективности и переносимости Осталона® в течение 12 мес терапии пациентов с остеопорозом. В исследование были включены 4360 пациентов с остеопорозом из 294 центров, большинство (73,4%) из которых были женщины с постменопаузальным остеопорозом. Исследование продемонстрировало положительный эффект Осталона® на МПК позвоночника и проксимального отдела бедра: у 72,5% пациентов прирост составил более 5%, и только у 2,83% было снижение МПК более 5%. На фоне лечения отмечалось достоверное снижение маркеров костеобразования: щелочной фосфатазы и остеокальцина и более значимое снижение маркера костной резорбции – С-телопептида коллагена I типа. Переносимость препарата была хорошей. Были зарегистрированы нежелательные явления, связанные с поражением ЖКТ, однако они встречались достаточно редко. При этом отличную переносимость отметили 88,3% пациентов через 6 мес и 77,1% через 12 мес лечения, а плохую – лишь 0,7 и 0,2% соответственно. Таким образом, проведенное исследование показало, что препарат Осталон® эффективен, безопасен у пациентов с остеопорозом и может использоваться в ежедневной клинической практике [14].
В исследование были включены 4360 пациентов с остеопорозом из 294 центров, большинство (73,4%) из которых были женщины с постменопаузальным остеопорозом. Исследование продемонстрировало положительный эффект Осталона® на МПК позвоночника и проксимального отдела бедра: у 72,5% пациентов прирост составил более 5%, и только у 2,83% было снижение МПК более 5%. На фоне лечения отмечалось достоверное снижение маркеров костеобразования: щелочной фосфатазы и остеокальцина и более значимое снижение маркера костной резорбции – С-телопептида коллагена I типа. Переносимость препарата была хорошей. Были зарегистрированы нежелательные явления, связанные с поражением ЖКТ, однако они встречались достаточно редко. При этом отличную переносимость отметили 88,3% пациентов через 6 мес и 77,1% через 12 мес лечения, а плохую – лишь 0,7 и 0,2% соответственно. Таким образом, проведенное исследование показало, что препарат Осталон® эффективен, безопасен у пациентов с остеопорозом и может использоваться в ежедневной клинической практике [14]. Сравнительные исследования эффективности разных методов антирезорбтивной терапии позволяют сделать вывод о сопоставимом влиянии всех видов лечения на минеральную плотность кости. Исключение составляет кальцитонин, терапия которым приводит к меньшему повышению МПК по сравнению с алендронатом, назначаемым в дозе 10 мг. Так, прирост МПК после 1 года терапии алендронатом составил 5,16% в поясничном отделе позвоночника, кальцитонином – 1,18%, в шейке бедра – 2,78 и 0,58% соответственно [11]. В отношении риска переломов было выявлено, что гормональная терапия эстрогенами и прогестинами повышает МПК и уменьшает риск переломов как позвонков, так и других локализаций [48]. Бисфосфонаты и гормоны обладают сравнимым влиянием на МПК. Совместное назначение этих лекарственных средств увеличивает их лечебный и профилактический потенциал [5]. Однако заместительная гормональная терапия имеет ряд ограничений по состоянию общего здоровья пациенток и возрасту. При наличии противопоказаний к проведению гормональной терапии либо при обращении пациенток в возрасте старше 60 лет бисфосфонаты становятся первой линией терапии постменопаузального остеопороза.
Сравнительные исследования эффективности разных методов антирезорбтивной терапии позволяют сделать вывод о сопоставимом влиянии всех видов лечения на минеральную плотность кости. Исключение составляет кальцитонин, терапия которым приводит к меньшему повышению МПК по сравнению с алендронатом, назначаемым в дозе 10 мг. Так, прирост МПК после 1 года терапии алендронатом составил 5,16% в поясничном отделе позвоночника, кальцитонином – 1,18%, в шейке бедра – 2,78 и 0,58% соответственно [11]. В отношении риска переломов было выявлено, что гормональная терапия эстрогенами и прогестинами повышает МПК и уменьшает риск переломов как позвонков, так и других локализаций [48]. Бисфосфонаты и гормоны обладают сравнимым влиянием на МПК. Совместное назначение этих лекарственных средств увеличивает их лечебный и профилактический потенциал [5]. Однако заместительная гормональная терапия имеет ряд ограничений по состоянию общего здоровья пациенток и возрасту. При наличии противопоказаний к проведению гормональной терапии либо при обращении пациенток в возрасте старше 60 лет бисфосфонаты становятся первой линией терапии постменопаузального остеопороза. Частота переломов уменьшается и на фоне применения других антирезорбтивных препаратов (кальцитонина, ралоксифена), но установлено, что при одинаковом увеличении МПК наибольшим позитивным потенциалом в отношении риска переломов всех локализаций обладают бисфосфонаты, а в группе бисфосфонатов – алендронат, редуцирующий относительный риск внепозвонковых переломов в среднем на 50%, по сравнению с 25% при применении ризендроната [39]. Наконец, важным преимуществом бисфосфонатов перед другими видами антирезорбтивной терапии является персистенция лечебного эффекта после окончания терапии. В то время как прекращение терапии другими антирезорбтивными препаратами немедленно знаменуется возобновлением потери костной массы, после отмены алендроната МПК сохраняет достигнутые значения в пределах 2 лет при условии достаточно длительного предшествующего приема несмотря на быстрое изменение маркеров костной резорбции. Фармакотерапия бисфосфонатами позволяет добиться существенного сокращения потерь костной массы и достигнуть нормализации и стабилизации показателей костного обмена, снижения риска возникновения переломов и улучшения качества жизни больных.
Частота переломов уменьшается и на фоне применения других антирезорбтивных препаратов (кальцитонина, ралоксифена), но установлено, что при одинаковом увеличении МПК наибольшим позитивным потенциалом в отношении риска переломов всех локализаций обладают бисфосфонаты, а в группе бисфосфонатов – алендронат, редуцирующий относительный риск внепозвонковых переломов в среднем на 50%, по сравнению с 25% при применении ризендроната [39]. Наконец, важным преимуществом бисфосфонатов перед другими видами антирезорбтивной терапии является персистенция лечебного эффекта после окончания терапии. В то время как прекращение терапии другими антирезорбтивными препаратами немедленно знаменуется возобновлением потери костной массы, после отмены алендроната МПК сохраняет достигнутые значения в пределах 2 лет при условии достаточно длительного предшествующего приема несмотря на быстрое изменение маркеров костной резорбции. Фармакотерапия бисфосфонатами позволяет добиться существенного сокращения потерь костной массы и достигнуть нормализации и стабилизации показателей костного обмена, снижения риска возникновения переломов и улучшения качества жизни больных.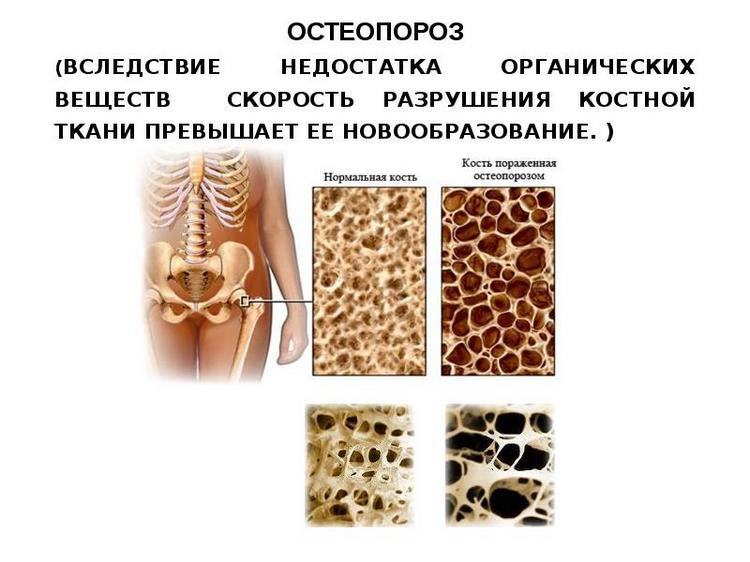 Будучи одной из составляющих общей программы по увеличению продолжительности и качества жизни женщин в постменопаузе терапия бисфосфонатами должна шире назначаться с целью профилактики остеопоретических переломов. Выбор дозы и режима назначения может варьировать в зависимости от конкретных целей, состояния скелета пациентки, ее возраста, переносимости терапии. Антирезорбтивную терапию постменопаузального остеопороза следует назначать при показателях МПК менее 2,5 SD вне зависимости от факторов риска остеопороза и 1,1–2,5 SD – при наличии факторов риска. Препаратом выбора является алендронат в сочетании с приемом витамина D и кальция. Нет никаких сомнений в том, что время начала и длительность терапии определяют ее протективный эффект, но даже непродолжительные циклы приема бисфосфонатов оказывают положительное воздействие на процессы ремоделирования кости. Лечение остеопороза представляет собой в настоящее время многоэтапный процесс, но на одном из этих этапов в комплекс терапии должны включаться бисфосфонаты.
Будучи одной из составляющих общей программы по увеличению продолжительности и качества жизни женщин в постменопаузе терапия бисфосфонатами должна шире назначаться с целью профилактики остеопоретических переломов. Выбор дозы и режима назначения может варьировать в зависимости от конкретных целей, состояния скелета пациентки, ее возраста, переносимости терапии. Антирезорбтивную терапию постменопаузального остеопороза следует назначать при показателях МПК менее 2,5 SD вне зависимости от факторов риска остеопороза и 1,1–2,5 SD – при наличии факторов риска. Препаратом выбора является алендронат в сочетании с приемом витамина D и кальция. Нет никаких сомнений в том, что время начала и длительность терапии определяют ее протективный эффект, но даже непродолжительные циклы приема бисфосфонатов оказывают положительное воздействие на процессы ремоделирования кости. Лечение остеопороза представляет собой в настоящее время многоэтапный процесс, но на одном из этих этапов в комплекс терапии должны включаться бисфосфонаты.
- Сметник В.П. Постменопаузальный остеопороз. Медицина климактерия. Ярославль: ООО «Изд — во Литтерра», 2006; 656–86.
- Black D.M, Cummings S.R, Karpf D.B et al. Randomised trial of effect of alendronate on risk of fracture in women with existing vertebral fractures. Lancet 1996; 348: 1535–41.
- Bishop N.J, Nincovic M, Alexander G.J et al. Changes in calcium homeostasis in patients undergoing liver transplantation: effects of a single infusion of pamidronate administered pre — operatively. Clin Sci 1999; 97: 157–163.
- Bonabello A, Galmozzi M.R, Bruzzese T, Zara G.P. Analgetic effect of biphosphonates in mice. Pain 2001; 91: 269–75.
- Bone H.G, Greenspan S.L, Mc Keever C, Bell N et al. Alendronate and estrogen effects in postmenopausal women with low dose bone mineral density. J Clin Endocrinol Metab 2000; 85: 720–6.

- Carr D.B, Goudas L.C. Acute pain. Lancet 1999; 353: 2051–8.
- Cauley J.A, Thompson D.E, Ensrud K.S et al. Risk of mortality following clinical fractures. Osteoporos Int 2000; 11: 556–61.
- Cranney A, Wells G, Willan A et al. IX: Summary of meta — analyses of therapies for postmenopausal osteoporosis. Endocr Rev 2002; 23: 570–8.
- Center J.R, Nguen T.V, Schneider D et al. Mortality after all mayor types of osteoporetic fracture in men and women: an observational study. Lancet 1999; 353: 878–92.
- Cummings S.R, Melton L.I. Epidemiology and outcomes of osteoporotic fractures. Lancet 2002; 359: 1761–7.
- Downs Jr.R.W, Bell N.H, Ettinger M.P et al. Comparison of alendronate and intranasal calcitonin for treatment of osteoporosis in postmenopausal women. J Clin Endocrinol Metab 2000; 85: 1783–8.
- Fulfaro F, Casuccio A, Ticozzi C, Ripamonti C.
 The role of biphosphonates in the treatment of painful metastatic bone disease: a review of phase III trials. Pain 1998; 78: 157–69.
The role of biphosphonates in the treatment of painful metastatic bone disease: a review of phase III trials. Pain 1998; 78: 157–69. - Garnero P, Shih W.J, Gineyts E et al. Comparison of new biochemical markers of bone turnover in late postmenopausal osteoporotic women in response to alendronate treatment. J Clin Endocrinol Metab 1994; 79: 1693–700.
- Geza B. Vizsgalatok a genericus alendronat natriummal, a Sedronnal. Praxis 2008; 17: 731–41.
- Greenspan S, Field-Munves E, Tonino R et al. Tolerability of once — weekly alendronate in patients with osteoporosis: a randomized, double — blind, placebo — controlled study. Mayo Clin Proc 2002; 77: 1044–52.
- Hodgson S.F, Watts N.B, Belezikian J.P et al. American Assotiation of Clinical Endocrinologist medical guidelines for clinical practice for the prevention and treatment of postmenopausal osteoporosis: 2001 edition, with selected updates for 2003.
 Endocr Pract 2003; 9: 544–64.
Endocr Pract 2003; 9: 544–64. - Hosking D, Chilvers C.E.D, Christiansen C et al. Prevention of bone loss with alendronate in postmenopaus
Cited-By
Article Metrics
Refbacks
- There are currently no refbacks.
Остеопороз: стандарты диагностики и лечения | Сыч Сергей ЕвгеньевичСыч Сергей Евгеньевич Остеопороз: стандарты диагностики и лечения
Е. Л. Насонов Институт ревматологии РАМН, Москва
Определение, классификация и клиническое значение.
Хорошо известно определение остеопороза как «прогрессирующего системного заболевания скелета, характеризующегося снижением массы кости и нарушением структуры (микроархитектоники) костной ткани, приводящего к увеличению хрупкости кости и риска переломов».
Выделяют две основные формы остеопороза: первичный и вторичный. В свою очередь первичный остеопороз условно подразделяется на постменопаузальный и сенильный.
Первичный остеопороз может развиваться у мужчин и женщин в любом возрасте, но чаще у женщин в период менопаузы и у мужчин в пожилом возрасте.
Вторичный остеопороз обычно является осложнением различных заболеваний (эндокринных, воспалительных, гематологических, гастроэнтерологических и др.) или лекарственной терапии (например, глюкокортикоидный остеопороз). По некоторым оценкам, вторичный остеопороз составляет 60% от всех случаев остеопороза у мужчин (наиболее часто связан с гипогонадизмом, приемом глюкокортикоидов и алкоголизмом), и примерно половину от всех случаев остеопороза у женщин в перименопаузе (гипоэстрогенемия, применение глюкокортикоидов, тиреоидных гормонов и противосудорожных препаратов).
Клиническое значение остеопороза определяется в первую очередь риском переломов костей скелета. Наиболее частыми и характерными являются возникающие после минимальной травмы (нетравматические) переломы позвоночника, дистального отдела лучевой кости и проксимального отдела бедренной кости (перелом шейки бедра).
Рис. 1.
А. Тело неизмененного позвонка (приводим в качестве сравнения).
Б. Компрессионный перелом позвонка при остеопорозе.
Обращает на себя внимание характерная структура остеопорозно измененного тела позвонка: значительное уменьшение количества горизонтальных трабекул и истончение вертикальных.
Рис. 2.
Рентгенограмма позвоночника при компрессионном переломе нижнегрудного позвонка (указан стрелкой).
У пациентки с постменопаузальным остеопорозом перелом произошел на фоне минимальной бытовой травмы.
Таблица 1. Диагностические категории, основанные на определении МПКТ и рекомендации по каждой категории.
| Т-индекс | Диагноз | Риск переломов | Рекомендации (см. табл. 4) |
|---|---|---|---|
| +2,0 до –1 | Нормальная МПКТ | Уровень 1: низкий | Только диетические рекомендации или добавки кальция и витамина D, физические упражнения |
| –1,0 до –2,5 | Остеопения | Уровень 2: умеренный риск | Добавки кальция и витамина D, возможно других препаратов |
| –2,5 или меньше без предшествующих переломов | Остеопороз | Уровень 3: высокий | Обязательно лечение антиостеопоретическими препаратами, предотвращение потерь равновесия |
| –2,5 или меньше с предшествующими переломами | Тяжелый остеопороз | Уровень 4: очень высокий | То же, что и уровень 2, но более интенсивно |
Таблица 2.
 Факторы, предрасполагающие к развитию остеопороза
Факторы, предрасполагающие к развитию остеопорозаГенетические или конституциональные
- Принадлежность к европеоидной или монголоидной расам
- Семейная предрасположенность (нетравматические переломы у родственников первой степени родства)
- Хрупкое телосложение
- Большая осевая длина шейки бедра
Образ жизни и питания
- Низкое потребление кальция и витамина D
- Курение
- Алкоголизм
- Низкая физическая активность
- Длительная иммобилизация
- Длительное парентеральное питание
- Низкая масса тела
- Отсутствие беременности
Заболевания
- Нарушение менструального статуса (длительная вторичная аменорея, преждевременная менопауза – до 45 лет, позднее начало менструаций)
- Эндокринные болезни (первичный гиперпаратиреоз, тиреотоксикоз, сахарный диабет, синдром Кушинга, болезнь Аддисона, первичный гипогонадизм, гиперпролактинемия)
- Болезни крови (множественная миелома, системный масцотоз, лимфома, лейкоз, пернициозная анемия)
- Воспалительные ревматические заболевания (ревматоидный артрит, анкилозирующий спондилоартрит, полимиозит/дерматомиозит, системная красная волчанка)
- Заболевания ЖКТ (нарушение всасывания, вызванное желудочно-кишечными заболеваниями), болезнь Крона, хронические заболевания печени)
- Хронические обструктивные заболевания легких
- Хронические неврологические заболевания
- Застойная сердечная недостаточность
- Хроническая почечная недостаточность
- Состояние после пересадки органов
Лекарственные препараты
- Глюкокортикоиды (>7,5 мг преднизолона более 6 мес)
- Тиреотропные препараты (тироксин)
- Антикоагулянты (непрямые, прямые)
- Агонисты и антагонисты гонадотропина
- Противосудорожные препараты (фенитоин)
- Фосфат–связывающие антациды
Таблица 3.
 Диагностические процедуры при остеопорозе
Диагностические процедуры при остеопорозеОбязательные
- Анамнез и физический осмотр
- Анализ крови (лейкоциты, СОЭ, уровень кальция, альбумина)
- Анализы фосфатов, щелочной фосфатазы в сыворотке, печеночных трансаминаз, белка сыворотки, электрофорез, анализ мочи
- Рентгенография поясничного и грудного отдела позвоночника
- Определение МПКТ (любым стандартизованным методом, предпочтительней DXA)
- Тестостерон и гонадотропин (у мужчин)
Дополнительные
- Маркеры метаболизма костной ткани в сыворотке и моче
- ПТГ, 25-OHD, тиреотропный гормон в сыворотке, маркеры злокачественных новообразований
- Гонадотропины и свободный кортизол в моче
- Стернальная пункция
- Биопсия крестцово-подвздошной кости после двойной маркировки тетрациклином для гистоморфометрии и анализа костного мозга
Таблица 4. Рекомендации по профилактике и лечению остеопороза и остеопоретических переломов
| Основные направления | Рекомендации |
|---|---|
I. Профилактика Профилактика | |
| – Физическая активность | Гимнастика, изометрические упражнения, плавание |
| – Питание | Пища с высоким содержанием кальция и витамина D (молочные продукты) и относительно низким содержанием фосфатов, поваренной соли и клетчатки |
| – Устранение факторов риска остеопороза | Курение, избыточный прием алкоголя, кофеина, тяжелые физические нагрузки |
| – Устранение факторов риска случайных потерь равновесия | Избегать приема снотворных, седативных препаратов и т.п. |
| – Снижение риска переломов при потере равновесия | Защита тазобедренного сустава |
| – Лекарственные препараты | Препараты кальция и витамин Di (особенно в зимнее время года и у пожилых больных) |
| II. Лечение | |
| – Подавление костной резорбции | См. табл. 5 |
| – Подавление болей, связанных с остеопоретическими переломами | Физиотерапия, «простые» анальгетики (парацетамол), нестероидные противовоспали-тельные препараты, центральные анальгетики (трамадол), опиоидные анальгетики |
| – Лечение остеопоретических переломов | Хирургические операции |
Таблица 5.
 Эффективность антиостеопоретических препаратов в отношении уменьшения риска переломов, по данным рандомизированных контролируемых исследований
Эффективность антиостеопоретических препаратов в отношении уменьшения риска переломов, по данным рандомизированных контролируемых исследований| Препарат | Снижение риска переломов | |||
|---|---|---|---|---|
| позв. и непозв. | только позв. | только непозв. | только переломы бедра | |
| Алендронат | + | + | ||
| ГЗТ | +/- | |||
| Ризедронат | + | + | ||
| Кальцитонин МИАКАЛЬЦИК | + | + | ||
| Этидронат | + | |||
| Ралоксифен | + | |||
| Кальцитриол | +/- | |||
| Кальций + витамин Di | + | + | ||
Примечание. Позв. – позвоночные, непозв. – непозвоночные. Позв. – позвоночные, непозв. – непозвоночные. | ||||
Определение минеральной плотности костной ткани
В настоящее время принято оценивать степень тяжести остеопороза на определении минеральной плотности костной ткани (МПКТ).
Однако, поскольку вклад МПКТ в суммарную прочность кости не превышает 70%, немаловажное значение в развитии остеопоретических переломов играют другие факторы. К ним относят нарушение качества (микроархитектоника, микротравмы, дефекты минерализации) костной ткани, а также «не скелетные» факторы, например случайные потери равновесия.
В будущем, по-видимому, большое значение будет придаваться биохимическим маркерам резорбции (дезоксипиридинол, C- и N-телопептиды проколлагена типа I и др.), которые, как полагают, позволяют дать характеристику нарушения «качества» кости требует дальнейшего уточнения и изучения.
Хотя скрининговые исследования для выявления остеопороза в принципе могут проводится с помощью любых стандартизованных методов, «золотым стандартом» в настоящее время является биэнергетическая рентгеновская абсорбциометрия (DXA), которая позволяет с высокой чувствительностью и воспроизводимостью определять МПКТ в наиболее важных, с точки зрения риска, остеопоретических переломов участках скелета – позвоночнике и бедренной кости.
Для диагностических целей при исследовании женщин были предложены два пороговых значения МПКТ (табл. 1). Значение МПКТ (Т-индекс) на 2,5 стандартных отклонения ниже усредненной МПКТ у взрослых женщин (пиковая костная масса) свидетельствует об остеопорозе (высокий риск остеопоретических переломов), а на 1 стандартное отклонение – об остеопении. Полагают, что именно у больных с остеопенией профилактика потери костной массы может быть наиболее эффективной. Определение «тяжелый» остеопороз используется в тех случаях, когда у пациента в прошлом уже имел место один остеопоретический перелом или более.
Риск переломов примерно удваивается при уменьшении МПКТ на одно стандартное отклонение от пиковой костной массы, а также если пациент уже перенес остеопоретический перелом.
Факторы риска, диагноз и дифференциальный диагноз остеопороза
Клинические факторы риска, которые могут быть успешно применены для активного выявления больных с остеопорозом представлены в табл. 2.
К наиболее существенным, частично не зависимым от МПКТ, относятся преждевременная менопауза, длительное лечение глюкокортикоидами (ГК), наличие некоторых заболеваний и переломов до 45 лет, низкий индекс массы тела (Обследование больных с остеопорозом включает стандартный набор диагностических тестов, их диапазон зависит от тяжести заболевания, возраста пациента и наличия переломов позвоночника (табл. 3).
Данные анамнеза, осмотра пациентов и лабораторных исследований позволяют решить следующие задачи:
- Исключить заболевания, которые могут быть приняты за остеопороз.
- Выявить причины остеопороза и предрасполагающие факторы.
- Оценить тяжесть остеопороза для определения прогноза болезни, т.е. вероятности последующих переломов.
- Выбрать наиболее адекватный метод лечения.
- Провести базовое обследование для последующего наблюдения за развитием болезни.
Высокий риск остеопороза характерен для широкого круга заболеваний (см. табл. 2). Многие из них легко диагностируются в процессе сбора анамнеза или при осмотре пациентов. На поиск этих заболеваний врача должны настроить необычные проявления остеопороза (например, развитие остеопороза в возрасте до 50 лет и остеопороза у мужчин).
2). Многие из них легко диагностируются в процессе сбора анамнеза или при осмотре пациентов. На поиск этих заболеваний врача должны настроить необычные проявления остеопороза (например, развитие остеопороза в возрасте до 50 лет и остеопороза у мужчин).
Потеря костной массы и переломы часто связаны с развитием остеомаляции и злокачественных новообразований.
Остеомаляция характеризуется дефектами минерализации костного матрикса, чаще всего вызванными нарушением потребления, выработки или обмена витамина D. К другим причинам относятся нарушение транспорта фосфатов или длительный прием некоторых препаратов, таких как соли алюминия (и других фосфатсвязывающих антацидов), больших доз препаратов фтора, биофосфонатов первого поколения (этидронат) и противосудорожных препаратов. Остеомаляция может быть заподозрена на основании анамнеза и изменения биохимических показателей, а именно снижение уровня кальция в сыворотке и моче, фосфатов и 25-гидроксивитамина D в сыворотке, а также увеличение концентрации щелочной фосфатазы и ПТГ. Для подтверждения дефекта минерализации иногда необходимо проведение биопсии подвздошной кости после проведения метки тетрациклином.
Для подтверждения дефекта минерализации иногда необходимо проведение биопсии подвздошной кости после проведения метки тетрациклином.
Диффузный остеопороз (с или без патологических переломов) часто встречается у пациентов с множественной миеломой. О развитии этой патологии могут свидетельствовать сильные боли в костях, увеличение СОЭ, протеинурия Бенс-Джонса, а для подтверждения диагноза используют стернальную пункцию и электроиммунофорез сыворотки и мочи.
Патологические переломы, вызванные костными метастазами, могут напоминать остеопоретические переломы.
Переломы позвоночника при остеопорозе следует дифференцировать от деформации позвоночника, вызванной другими заболеваниями, такими как сколиоз, остеоартроз и болезнь Шейермана–Мау.
Лечение и профилактика остеопороза
В течение последних 30 лет было проведено очень большое число разнообразных исследований, посвященных лечению остеопороза. Полученные данные позволили провести детальный анализ сравнительной эффективности антиостеопоретических препаратов с позиций «медицины доказательств» (табл. 4).
4).
Установлено, что лечение подавляющим большинством антиостеопоретических препаратов приводит к увеличению МПКТ различных участков скелета. Однако, поскольку основная цель лечения остеопороза – снижение частоты остеопоретических переломов, то адекватными являются результаты только таких исследований, в которых в качестве конечного результата оценивалась эффективность антиостеопоретических препаратов в отношении снижения частоты переломов костей скелета (табл. 5).
Требует специального обсуждения целесообразность разделения (хотя и условного) тактики ведения пациентов на два направления: профилактика остеопороза и его лечение. Под профилактикой остеопороза подразумевают предотвращение потери костной массы у пациентов с остеопенией или даже нормальной МПКТ, а под лечением – снижение риска остеопоретических переломов. Однако это разделение не имеет существенного значения для клинической практики и теоретически не обосновано. Под профилактическими мероприятиями следует подразумевать рекомендации для лиц молодого возраста в отношении увеличения пиковой костной массы, а для лиц пожилого возраста с остеопорозом – в отношении профилактики случайных потерь равновесия.
Необходимо иметь в виду, что хотя на фоне приема некоторых антиостеопоретических препаратов снижение риска переломов развивается довольно быстро (алендронат, кальций + витамин D), все же для существенного снижения частоты переломов необходима длительная (вероятно пожизненная) терапия, поскольку ее эффект быстро проходит после прерывания лечения.
Препараты кальция и витамина D
Особое внимание в последнее время уделяется оценке эффективности препаратов кальция и витамина D, как наиболее доступного и теоретически хорошо обоснованного подхода к снижению риска остеопоретических переломов. Имеются данные о том, что субклинический дефицит кальция и витамина D, приводя к увеличению уровня паратиреоидного гормона (ПТГ), играет важную роль в патогенезе остеопороза.
У пациентов с остеопорозом не зависимо от возраста наблюдается снижение кишечной абсорбции кальция, что приводит к отрицательному кальциевому балансу. Поскольку в норме абсорбция кальция регулируется витамином D, развитие остеопороза и увеличение риска переломов отражают дефицит витамина D или резистентность к витамину D.
В постменопаузе у женщин с низкой концентрацией витамина D МПКТ ниже, чем у женщин с нормальной концентрацией витамина D. Кроме того, у этих женщин отмечается снижение сывороточного уровня кальция и повышение уровня ПТГ.
Более чем у трети пациентов с переломами бедра выявляются признаки такого классического проявления дефицита витамина D, как остеомаляция.
Следует подчеркнуть, что субклинический дефицит витамина D широко распространен не только у пожилых пациентов, но имеет место примерно у половины пациентов более молодого (около 60 лет) возраста и особенно выражен в зимнее время года. По некоторым данным, у половины пациентов пожилого возраста наблюдается снижение образования эндогенного витамина D в коже и потребление витамина D с пищей.
Адекватное потребление кальция и витамина D не только приводит к быстрому увеличению МПКТ, но и к снижению частоты позвоночных и непозвоночных переломов, включая переломы бедра.
Примечательно, что прием только витамина D, без кальция, как и кальция без витамина D не оказывает столь положительного влияния на МПКТ и риск переломов костей скелета, как их сочетанный прием. Потребление 800 МЕ витамина D и 1200 мг элементарного кальция в сутки рекомендуется всем лицам в возрасте старше 60 лет. К сожалению, в молоке (основной источник витамина D в пище) содержится недостаточное количество витамина D (только 100 МЕ витамина D на 250 мл). Поэтому следует настоятельно рекомендовать всем лицам этой возрастной группы дополнительный прием препаратов кальция и витамина Di в дозе не менее 400–800 МЕ витамина D и 1000–1200 мг элементарного кальция в зависимости от особенностей питания. Необходимо также иметь в виду, что для оптимального лечения всех форм остеопороза с использованием других антиостеопоретических препаратов требуется назначение оптимальных доз кальция и витамина D в качестве базовой терапии.
Потребление 800 МЕ витамина D и 1200 мг элементарного кальция в сутки рекомендуется всем лицам в возрасте старше 60 лет. К сожалению, в молоке (основной источник витамина D в пище) содержится недостаточное количество витамина D (только 100 МЕ витамина D на 250 мл). Поэтому следует настоятельно рекомендовать всем лицам этой возрастной группы дополнительный прием препаратов кальция и витамина Di в дозе не менее 400–800 МЕ витамина D и 1000–1200 мг элементарного кальция в зависимости от особенностей питания. Необходимо также иметь в виду, что для оптимального лечения всех форм остеопороза с использованием других антиостеопоретических препаратов требуется назначение оптимальных доз кальция и витамина D в качестве базовой терапии.
Прием кальция и витамина D рассматривается как минимально необходимая терапия у всех пациентов, которым показана длительная глюкокортикоидная терапия.
Оссеин-гидроксиаппатитный комплекс
Определенное вспомогательное значение для нормализации кальциевого гомеостаза и улучшения костного обмена может иметь оссеин-гидроксиаппатитный комплекс (остеогенон).
Важно, что этот препарат практически не имеет противопоказаний и может использоваться для коррекции дефицита кальция у беременных и кормящих женщин.
Бисфосфонаты
Результаты крупных клинических исследований свидетельствуют о том, что лечение бисфосфонатами (алендронат и ризедронат) приводит к дозозависимому увеличению МПКТ и снижению риска позвоночных и непозвоночных переломов на 30–50% у больных с первичным и глюкокортикоидным остеопорозом.
Гормональная заместительная терапия (ГЗТ)
ГЗТ является общепринятым подходом к профилактике и лечению постменопаузального остеопороза. Снижение риска переломов достигается только после 6–7 лет постоянного приема препаратов и быстро исчезает после их отмены. Не исключается, что снижение частоты переломов в большей степени связано с общим улучшением состояния здоровья женщин, а не со специфическим антиостеопорозным эффектом ГЗТ.
Эффективность селективных модуляторов эстрогеновых рецепторов (ралоксифен) в отношении снижения риска переломов позвоночника (но не переломов других локализаций) была доказана в крупном контролируемом исследовании. Достоинством модуляторов эстрогеновых рецепторов по сравнению со стандартной ГЗТ является преимущественное влияние на костную ткань и отсутствие нежелательного действия на молочные железы и эндометрий.
Достоинством модуляторов эстрогеновых рецепторов по сравнению со стандартной ГЗТ является преимущественное влияние на костную ткань и отсутствие нежелательного действия на молочные железы и эндометрий.
Кальцитонин лосося — МИАКАЛЬЦИК
Эффективность кальцитонина, который применяется для лечения остеопороза в течение более 30 лет, в отношении снижения риска позвоночных переломов была подтверждена в ходе крупных клинических исследований. Предполагается также эффективность кальцитонина лосося в отношении снижения риска непозвоночных переломов.
Кальцитонин лосося обладает анальгетической и, вероятно, антиартрозной активностью, это делает его применение особенно предпочтительным у пациентов с остеопоретическими переломами позвоночника и болями в спине, связанными с дегенеративным поражением позвоночника.
Активные метаболиты витамина D (кальцитриол и альфа-кальцидол)
Хотя предварительные результаты свидетельствуют об эффективности активных метаболитов витамина D в отношении снижения риска переломов костей скелета, эти результаты получены на относительно небольших группах больных и требуют дальнейшего подтверждения.
Современные принципы профилактики и лечения постменопаузального остеопороза
В.В. Поворознюк, д.м.н., профессор, руководитель отдела клинической физиологии и патологии опорно-двигательного аппарата, Н.В. Григорьева, д.м.н., Институт геронтологии АМН Украины, Украинский научно-медицинский центр проблем остеопороза, г. Киев
Остеопороз – наиболее распространенное системное заболевание скелета, характеризующееся снижением костной массы и структурными изменениями костной ткани, которые выражены настолько, что даже при незначительной травме возможно возникновение переломов. В последние десятилетия эта проблема приобрела особое значение вследствие тесно связанных демографических процессов: резкого увеличения в популяции доли людей пожилого и старческого возраста, и в частности в значительной мере – женщин в постменопаузе. Приблизительно у каждой третьей женщины после 65 лет случается как минимум один перелом костей (J.A. Kanis, 1993). Остеопоротические переломы существенно влияют на уровень общей заболеваемости и смертность. Переломы бедра приводят к снижению ожидаемой средней продолжительности жизни на 12-15% (В. Lees et al., 1993). После перенесенного перелома бедра до 20% больных умирают в течение первых 6 мес, около 50% – не могут передвигаться без посторонней помощи, а треть теряют способность к самообслуживанию. Суммарный риск остеопоротических переломов в возрасте 50 лет составляет 39,7% для женщин и 13,1% для мужчин (J.A. Kanis, F.A. Pitf, 1992).
Переломы бедра приводят к снижению ожидаемой средней продолжительности жизни на 12-15% (В. Lees et al., 1993). После перенесенного перелома бедра до 20% больных умирают в течение первых 6 мес, около 50% – не могут передвигаться без посторонней помощи, а треть теряют способность к самообслуживанию. Суммарный риск остеопоротических переломов в возрасте 50 лет составляет 39,7% для женщин и 13,1% для мужчин (J.A. Kanis, F.A. Pitf, 1992).
Несомненно, что с позиции медицины, а также с учетом социально-экономической стороны проблемы, предотвратить потерю костной массы и грозные осложнения остеопороза (переломы) легче и дешевле, поэтому особое внимание необходимо уделять его профилактике.
Основными задачами профилактики системного остеопороза являются:
• достижение как можно большего пика костной массы в период созревания, фоpмиpования скелета с максимальными пpочностными хаpактеpистиками;
• снижение и предотвращение отрицательного влияния экзогенных и эндогенных факторов на костную ткань;
• предотвращение потери костной массы и (по возможности) повышение плотности костной ткани.
Основными принципами профилактики постменопаузального остеопороза являются:
• соблюдение сбалансированной диеты с адекватным содержанием кальция (особенно в пре- и пубертатном периодах) и витамина D, что чрезвычайно важно в старческом возрасте;
• использование физических упражнений с весовой нагрузкой на скелет (в пре- и постпубертатном периодах – для накопления костной массы; в пожилом и старческом возрасте – для профилактики ее потери). Занятия физическими упражнениями за счет укрепления мышечной системы и улучшения координации движений снижают также вероятность падений;
• прекращение курения. По сравнению с некурящими у курящих женщин раньше наступает менопауза, быстрее катаболизируются экзогенные эстрогены, чаще встречаются остеопоротические переломы;
• применение заместительной гормональной терапии (ЗГТ) (эстрогены или комбинация эстрогенов с прогестагенами) в сочетании с кальцием и витамином D у пациенток с высоким риском развития остеопороза и его осложнений.
Профилактика системного остеопороза, в частности его постменопаузальной формы, предусматривает продолжительное использование препаратов кальция и витамина D.
Кальций и витамин D. Кальций и его соединения играют ключевую роль в процессах минерализации и формирования скелета. В зависимости от возраста относительное содержание кальция в организме колеблется в пределах от 0,8 до 1,7%. В абсолютных цифрах это составляет около 25-30 г у новорожденных и 850-1400 г у взрослых. Приблизительно 98-99% кальция находится в костной ткани в виде кристаллов гидроксилапатита, остальная часть – в мягких тканях и внеклеточной жидкости. Поскольку кальций в основном концентрируется в костях, изменение его баланса непосредственно связано с усилением роста или резорбцией скелета. По мнению многих исследователей (R.R. Recker, 1993; J.A. Kanis, 1994; T.M. Murray, 1996; J.J. Anderson et al., 1996), именно кальцию принадлежит определяющая роль в формировании пика костной массы и в метаболизме костной ткани.
Количество кальция, всасываемое в кишечнике, зависит от уровня его потребления. При недостаточном поступлении его с пищей преобладает активный трансцеллюлярный транспорт в двенадцатиперстной кишке над пассивным парацеллюлярным транспортом, характерным для тонкой и тощей кишок при нормальном или избыточном потреблении кальция. Биологическая способность кальция к всасыванию при высоком уровне его потребления (более 800 мг/сут) не слишком важна. Достаточное потребление витамина D является еще одним важным моментом, поскольку активный транспорт кальция является прямо пропорциональным наличию в клетках кишечника калбиндина, биосинтез которого полностью зависит от присутствия витамина D.
Выведение кальция из организма обусловлено характером питания. Преобладание в рационе питания продуктов с кислой реакцией среды (мясо, крупа, хлеб) приводит к его выделению с мочой, продуктов с основным рН – к выделению кальция с калом.
Норма потребления кальция для взрослых и связь между его потреблением и возникновением остеопороза в настоящее время являются предметом многочисленных дискуссий. Разные исследователи предлагают как норму потребления кальция значения от 300 мг/сут до величин, в четыре раза и более превышающих этот показатель. Разногласие в этом вопросе можно объяснить существенными различиями в питании и культурных традициях этнических групп, значительными индивидуальными колебаниями потребности в кальции и уровнями физической активности. Большинство ученых придерживаются точки зрения, что для предупреждения отрицательного кальциевого баланса в пожилом и старческом возрасте необходимо потребление кальция в количестве не менее 1000-1500 мг/сут. Доказано, что ранее принятая в ряде стран норма (800 мг/сут) недостаточна; выявлено наличие отрицательного баланса кальция у 34% обследуемых при таком потреблении, что способствует развитию остеопороза и его осложнений. При увеличении поступления кальция до 1200 мг/сут баланс становится положительным, а при дальнейшем увеличении (до 2300 мг) улучшение в балансе не происходит (R.P. Heaney, 1991).
Разные исследователи предлагают как норму потребления кальция значения от 300 мг/сут до величин, в четыре раза и более превышающих этот показатель. Разногласие в этом вопросе можно объяснить существенными различиями в питании и культурных традициях этнических групп, значительными индивидуальными колебаниями потребности в кальции и уровнями физической активности. Большинство ученых придерживаются точки зрения, что для предупреждения отрицательного кальциевого баланса в пожилом и старческом возрасте необходимо потребление кальция в количестве не менее 1000-1500 мг/сут. Доказано, что ранее принятая в ряде стран норма (800 мг/сут) недостаточна; выявлено наличие отрицательного баланса кальция у 34% обследуемых при таком потреблении, что способствует развитию остеопороза и его осложнений. При увеличении поступления кальция до 1200 мг/сут баланс становится положительным, а при дальнейшем увеличении (до 2300 мг) улучшение в балансе не происходит (R.P. Heaney, 1991).
Нами изучен уровень потребления кальция женщинами Украины в постменопаузальном периоде (В. В. Поворознюк, Н.В. Григорьева, 2001). Исследования, проведенные совместно с сотрудниками лаборатории гигиены питания Института геронтологии АМН Украины, показали, что фактический рацион питания женщин украинской популяции в постменопаузальном периоде характеризуется значительным дефицитом основных макро- и микронутриентов, в том числе и кальция. Только у 3,2% лиц содержание кальция в пищевом рационе превышает 1000 мг/сут, у половины пациенток данный показатель составляет менее 200 мг/сут (рис. 1) при норме потребления кальция для женщин в постменопазульном периоде 1500 мг/сут.
В. Поворознюк, Н.В. Григорьева, 2001). Исследования, проведенные совместно с сотрудниками лаборатории гигиены питания Института геронтологии АМН Украины, показали, что фактический рацион питания женщин украинской популяции в постменопаузальном периоде характеризуется значительным дефицитом основных макро- и микронутриентов, в том числе и кальция. Только у 3,2% лиц содержание кальция в пищевом рационе превышает 1000 мг/сут, у половины пациенток данный показатель составляет менее 200 мг/сут (рис. 1) при норме потребления кальция для женщин в постменопазульном периоде 1500 мг/сут.
Основными источниками кальция являются молочные (молоко, творог, твердые сыры и т.д.), рыбные продукты, лесной орех, цветная и морская капуста (табл. 1). Усвоению кальция препятствуют продукты с высоким содержанием щавелевой кислоты (шпинат, крыжовник, смородина, ревень), а также заболевания желудочно-кишечного тракта (ЖКТ) (язвенная болезнь, желчнокаменная болезнь, хронические гепатиты и дp.) (В.В. Поворознюк и др. , 1995).
, 1995).
Продукты питания также должны включать достаточное количество белков (мясо, бобовые) и, что особенно важно, витамин D, высокое содержание которого отмечено в морской рыбе, яйцах, какао, сливках.
Соответствующее поступление кальция и витамина D в организм рассматривается как один из наиболее рациональных подходов к профилактике остеопороза. У взрослых адекватное потребление кальция достоверно коррелирует со снижением скорости потери костной массы и риска возникновения переломов костей скелета. Важно то, что другие компоненты диеты не влияют так существенно на частоту переломов шейки бедренной кости, а тенденция к увеличению риска переломов сохраняется даже после исключения потенциального влияния других факторов, способствующих развитию остеопороза (курение, прием алкоголя, уровень физической активности и масса тела). Прием кальция в адекватном количестве приводит к стабилизации минеральной плотности костной ткани (КТ) у лиц пожилого и старческого возраста, в частности у женщин в постменопаузе, снижению уровня биохимических маркеров, которые характеризуют резорбцию КТ, в том числе и у лиц в раннем постменопаузальном периоде, коррекции индуцируемого паратиреоидным гормоном (ПТГ) увеличения костного обмена.
Прием 1 г кальция в вечерние часы в раннем постменопаузальном периоде приводит к снижению резорбции костной ткани. Известно, что у женщин в пре- и в постменопаузальном периодах наблюдаются циркадные изменения резорбции с максимальной ее выраженностью в утренние часы, которые отображают суточные колебания синтеза ПТГ. Именно поэтому препараты кальция наиболее эффективны при приеме в вечерние часы.
Анализ литературных данных свидетельствует, что на фоне приема кальция в рекомендованных дозах побочные эффекты развиваются чрезвычайно редко (приблизительно с такой же частотой, как и в группе больных, которые принимали плацебо).
Экспертами Американского национального фонда по изучению остеопороза разработаны рекомендации по применению кальция и витамина D, среди которых имеются следующие:
1. Лечение препаратами кальция экономически эффективно даже у женщин с нормальными показателями минеральной плотности КТ.
2. На фоне лечения препаратами кальция риск возникновения переломов снижается не менее чем на 10%.
3. У больных с дефицитом витамина D лечение препаратами кальция и витамином D снижает риск развития переломов костей скелета на 30%.
4. Адекватное потребление кальция (с пищей и/или добавление препаратов кальция) следует рекомендовать всем женщинам, независимо от приема других антиостеопоротических препаратов.
Таким образом, дефицит кальция и витамина D следует рассматривать как распространенное патологическое состояние, которое создает предпосылки для развития наиболее частых болезней у лиц пожилого и старческого возраста. В связи с этим соблюдение диетических рекомендаций и прием препаратов кальция и витамина D имеют стратегически большое значение для профилактики остеопороза и его осложнений, увеличения продолжительности и качества жизни населения.
К первому поколению препаратов кальция относятся его простые соли: карбонат, хлорид, моно-, ди-, три- и глицерофосфат, цитрат, глюконат, лактат. Содержание элементарного кальция в различных солях варьирует. Наибольшее относительное содержание кальция имеется в карбонате и трифосфате кальция. Из других простых солей кальция особого внимания заслуживает цитрат, который усваивается независимо от времени приема пищи и состояния ЖКТ. Простые соли кальция стоят недорого и общедоступны. Вместе с тем для полноценного усвоения их необходимо комбинировать с витамином D (из расчета не менее 400 МЕ в сутки) или с его активными метаболитами.
Из других простых солей кальция особого внимания заслуживает цитрат, который усваивается независимо от времени приема пищи и состояния ЖКТ. Простые соли кальция стоят недорого и общедоступны. Вместе с тем для полноценного усвоения их необходимо комбинировать с витамином D (из расчета не менее 400 МЕ в сутки) или с его активными метаболитами.
Вышеуказанное обстоятельство послужило стимулом к разработке препаратов второго поколения – комплексов солей кальция (чаще всего карбоната) с витамином D. Результатом этого стало увеличение биодоступности кальция и повышение эффективности лечения. Однако использование этих лекарственных средств требует взвешенного подхода в отношении длительности приема. Общеизвестно, что жирорастворимые витамины, в том числе и витамин D, при длительном приеме склонны накапливаться в организме. Чем больше содержание витамина D в препарате, тем выше риск кумуляции и развития гипервитаминоза. Последствиями гипервитаминоза D могут быть нарушения сократительной способности миокарда, расстройства функций печени, почек, других органов и систем. При длительном приеме таких лекарств обязательным является регулярный контроль уровня кальция в крови и в моче. В связи с этим фармакологи и клиницисты настойчиво искали способ снизить содержание витамина D в препаратах кальция не в ущерб их эффекту.
При длительном приеме таких лекарств обязательным является регулярный контроль уровня кальция в крови и в моче. В связи с этим фармакологи и клиницисты настойчиво искали способ снизить содержание витамина D в препаратах кальция не в ущерб их эффекту.
Результатом этих поисков стало появление препаратов третьего поколения, в которых на помощь витамину D приходят микроэлементы, дублирующие его кальцийсберегающие функции и положительно влияющие на метаболизм костной и хрящевой тканей, – прежде всего бор, цинк, медь и марганец. Например, цинк обеспечивает активность более 200 ферментов, в том числе и щелочной фосфатазы. Медь участвует в синтезе коллагена и эластина, препятствуя деминерализации костей. Марганец нормализует синтез гликозоаминогликанов, необходимых для формирования костной и хрящевой ткани. Бор регулирует активность ПТГ, ответственного за обмен кальция, магния, фосфора. Включение перечисленных микроэлементов в состав препарата позволяет снизить содержание данного витамина, увеличить его безопасность при длительном приеме и расширить сферу применения.
В последнее десятилетие медицина обогатилась значительным арсеналом лечебных антиостеопоротических средств (табл. 2). В настоящее время в Украине дополнительно к препаратам кальция и витамина D для лечения системного остеопороза используют четыре основные фармакологические стратегии: ЗГТ, селективные регуляторы эстрогенной активности – тиболон, бисфосфонаты (алендронат) и кальцитонин лосося.
Вышеуказанные группы препаратов увеличивают показатели минеральной плотности костной ткани (МПКТ) и снижают риск возникновения перелома. Однако каждая из них имеет свои преимущества и риск побочных осложнений, в связи с чем для практического врача одно лекарственное средство может быть эффективнее по сравнению с другими, в зависимости от клинического состояния больной. Обязательным при их назначении является адекватное ежедневное применение витамина D (400-800 МЕ) и элементарного кальция (1000-1500 мг) (B.L. Riggs, L.J. Melton, 1992; D.W. Isenbarger, B.L. Chapin, 1997). В связи с тем, что более высокие дозы кальция ведут к снижению его эффективной абсорбции, относительно безопасным является добавление его к диете с достижением общей дозы 1500 мг/сут. Очень высокие дозы кальция могут быть причиной заболеваний почек, молочно-щелочного синдрома, гиперкальциемии, гиперкальциурии и побочных эффектов со стороны ЖКТ.
Очень высокие дозы кальция могут быть причиной заболеваний почек, молочно-щелочного синдрома, гиперкальциемии, гиперкальциурии и побочных эффектов со стороны ЖКТ.
Одним из важных и патогенетически обоснованных методов лечения постменопаузального остеопороза является ЗГТ половыми стероидами. Основная цель ЗГТ – обеспечение организма женщины минимальными физиологическими концентрациями гормонов, необходимыми для поддержания гомеостаза и профилактики развития менопаузальных нарушений в климактерическом периоде жизни.
Для ЗГТ в постменопаузе могут использоваться препараты, содержащие один гормон или комбинацию половых стероидов яичника – эстрогенов, прогестерона и андрогенов. Наиболее распространенным и оправданным является применение препаратов, содержащих эстрогены, с возможной комбинацией их с прогестагенами.
Показания к назначению ЗГТ и принципы ее проведения существенно изменились после 2002 г., когда были оглашены результаты исследования Women Health Initiative (WHI). Согласно рекомендациям International Menopause Society, ЗГТ в настоящее время показана для лечения вегетососудистых и психоэмоциональных проявлений менопаузы, а также для профилактики остеопороза; однако не должна использоваться для первичной и вторичной профилактики сердечно-сосудистых заболеваний. Длительность ее использования в большинстве случаев должна быть не более 5 лет (Position Statement on Practice of Climacteric, 2003).
Длительность ее использования в большинстве случаев должна быть не более 5 лет (Position Statement on Practice of Climacteric, 2003).
Применяют различные режимы ЗГТ (монотерапию эстрогенами, прогестинами, андрогенами, комбинированную терапию эстрогенами и гестагенами и/или андрогенами в постоянном или циклическом режиме), которые выбирают в зависимости от стадии климактерия, перенесенных оперативных вмешательств на органах репродуктивной системы и т.д. При выборе наиболее подходящей формы введения эстрогена важное значение имеет индивидуальная чувствительность к эстрогенам, сопутствующая патология, желание пациентки и т.д.
Первый опыт применения заместительной терапии эстрогенами для коррекции структурно-функциональных нарушений КТ был получен у женщин после двусторонней овариоэктомии. На сегодняшний день в экспериментальных исследованиях in vivo и в культуре костных клеток человека in vitro подтверждена гипотеза о том, что эстрогены действуют на клетки КТ как непосредственно, так и опосредованно.
В многочисленных рандомизированных плацебо-контролируемых исследованиях доказана защитная роль эстрогенов в первичной и вторичной профилактике остеопоротических переломов (как вертебральных, так и невертебральных) (Lufkin et al., 1992; Hulley et al., 1998; Komulainen et al., 1998). При изучении частоты переломов в когортных исследованиях установлено, что ЗГТ уменьшает риск возникновения переломов лучевой, бедренной кости и тел позвонков на 50-90% по сравнению с контрольной группой (B. Dawson-Hughes et al., 1990). В другом исследовании отмечено снижение частоты остеопоротических переломов на 50-60% (N.S. Weіss et al., 1988).
В рамках проведения рандомизированного плацебо-контролируемого исследования WHI риск развития переломов бедренной кости у женщин, принимавших ЗГТ, составил 0,66 (95% доверительный интервал [ДИ]: 0,45-0,98) – 106 случаев, а оцениваемый уровень риска составил 0,76 (95% ДИ: 0,69-0,85) для переломов разных локализаций (WHI, 2002).
Минимальная длительность терапии, необходимой для профилактики переломов бедра, остается спорной. Так, показана эффективность ЗГТ в течение 5-10 лет, хотя дискуссионным остается вопрос относительно наличия положительного влияния данного вида лечения в возрасте после 75 лет. Это особенно важно в связи с тем, что частота возникновения переломов бедра высокая у женщин именно этого возраста, и пролонгированная терапия необходима, чтобы защитить их от переломов в старости, во время наибольшего риска.
Так, показана эффективность ЗГТ в течение 5-10 лет, хотя дискуссионным остается вопрос относительно наличия положительного влияния данного вида лечения в возрасте после 75 лет. Это особенно важно в связи с тем, что частота возникновения переломов бедра высокая у женщин именно этого возраста, и пролонгированная терапия необходима, чтобы защитить их от переломов в старости, во время наибольшего риска.
Остеопротекторный эффект эстрогенов тем выше, чем раньше после менопаузы начато их применение. Сложнее увеличивать костную массу при остеопорозе, который уже развился, поэтому ЗГТ следует проводить как можно раньше. Кроме того, важно помнить, что при уже существующем остеопорозе гормонотерапия только блокирует процессы резорбции кости, но не восстанавливает ее архитектонику. Таким образом, половые гормоны следует назначать параллельно с препаратами, стимулирующими формирование КТ (В.В. Поворознюк, Н.В.Григорьева, 2004).
По данным многих авторов (В.П. Сметник, 1995; Г. Чижова, Т.Ф. Татарчук, В. В. Поворознюк, 2000; Т. Алтухова, 2002), длительность проведения ЗГТ для коррекции менопаузальных нарушений должна составлять от нескольких месяцев до полутора-двух лет. Гормонопрофилактика поздних обменно-эндокринных нарушений постменопаузы, а именно остеопороза и остеоартроза, целесообразна при ее длительности не менее 5-7 лет, однако применение ее ограничено в связи с повышенным риском возникновения рака молочной железы (МЖ). После отмены эстрогенов, по одним данным, минеральная плотность КТ быстро возвращается к изначально низкому уровню, по другим – поддерживается на достигнутом уровне.
В. Поворознюк, 2000; Т. Алтухова, 2002), длительность проведения ЗГТ для коррекции менопаузальных нарушений должна составлять от нескольких месяцев до полутора-двух лет. Гормонопрофилактика поздних обменно-эндокринных нарушений постменопаузы, а именно остеопороза и остеоартроза, целесообразна при ее длительности не менее 5-7 лет, однако применение ее ограничено в связи с повышенным риском возникновения рака молочной железы (МЖ). После отмены эстрогенов, по одним данным, минеральная плотность КТ быстро возвращается к изначально низкому уровню, по другим – поддерживается на достигнутом уровне.
В случае использования ЗГТ с целью профилактики остеопороза в постменопаузе следует помнить и о возможной сопутствующей патологии со стороны сердечно-сосудистой, репродуктивной систем и желчного пузыря.
Важным принципом профилактики и лечения постменопаузального остеопороза является назначение ЗГТ на фоне приема препаратов кальция и активных метаболитов витамина D, особенно в условиях выраженного кальциевого дефицита, характерного для женщин в постменопаузальном периоде в Украине.
Широкое применение ЗГТ у пациенток в постменопаузе ограничивается рядом противопоказаний (злокачественные новообразования МЖ, яичников и т.д.) и побочных эффектов (менструальноподобные реакции и кровомазания, мастодиния, тромбоэмболические осложнения и др.) В связи с этим в последние годы все большее внимание уделяется поиску эффективных и безопасных препаратов, которые бы уменьшали нейровегетативные проявления постменопаузы, предупреждали потерю костной ткани, положительно влияли на липидный спектр крови. Среди них особое внимание уделяется как препаратам растительного происхождения – фитоэстрогенам (ФЭ), так и искусственно синтезированным лекарственным веществам (препаратам группы селективных модуляторов эстрогенной активности [СТЭАР] и селективных модуляторов эстрогенных рецепторов [СЭРМ]).
Фитоэстрогены являются растительными веществами, обладающими эстрогенной активностью благодаря способности связываться с эстрогенными рецепторами (ЭР). Свидетельства эстрогеноподобного влияния ФЭ в профилактике потери КТ доказаны в нескольких исследованиях. Так, подтвержден положительный эффект двух разных доз соевых изофлавоноидов на минеральную плотность КТ у женщин в постменопаузальном периоде уже через 6 мес от начала лечения (S.M. Potter et al., 1998). Достоверное увеличение минеральной плотности КТ по сравнению с контрольной группой наблюдалось при назначении сои в суточной дозе 90 мг. Однако результаты других наблюдений не подтверждают эти данные (T.M. Knudson Schult, K.E. Ensrud, T. Blackwell et al., 2004), хотя и доказывают положительное влияние сои на метаболизм липидов.
Так, подтвержден положительный эффект двух разных доз соевых изофлавоноидов на минеральную плотность КТ у женщин в постменопаузальном периоде уже через 6 мес от начала лечения (S.M. Potter et al., 1998). Достоверное увеличение минеральной плотности КТ по сравнению с контрольной группой наблюдалось при назначении сои в суточной дозе 90 мг. Однако результаты других наблюдений не подтверждают эти данные (T.M. Knudson Schult, K.E. Ensrud, T. Blackwell et al., 2004), хотя и доказывают положительное влияние сои на метаболизм липидов.
Полезным источником ФЭ считают соевые бобы, поскольку они содержат большое количество изофлавоноидов, использующихся в очищенном виде в качестве лекарственных препаратов и пищевых добавок (C. Gennari et al., 1997).
В 2004 г. проведен анализ 13 рандомизированных клинических исследований по изучению эффективности сои в коррекции менопаузальных нарушений (A. Huntley, E. Ernst, 2004). В 5 испытаниях подтверждено положительное влияние сои на динамику вегетативно-вазомоторных проявлений климактерического синдрома, в 6 – не обнаружено данной закономерности, а в 2 исследованиях положительная динамика была выявлена как в группе пациенток, получавших сою, так и в группе плацебо.
В последнее время в Украине широко используют препарат из сухого экстракта корневищ Cimicifuga racemosa. Как подтверждают результаты многочисленных исследований, субстанции в экстракте C. racemosa обладают органоселективным действием вследствие связывания с ЭР. Препарат эффективно устраняет климактерические расстройства, воздействуя на центральную нервную систему и гипофиз. Кроме того, в отличие от конъюгированных эстрогенов, он не оказывает отрицательного влияния на состояние эндометрия.
В метаанализе, проведенном F. Borrelli и соавт., представлены результаты 15 испытаний на лабораторных животных, а также 15 исследований in vitro, в которых изучена эффективность C. racemosa. Результаты этих наблюдений подтверждают факт влияния C. racemosa на ЦНС, однако механизмы ее действия на сегодняшний день до конца не изучены (F. Borrelli, A.A. Izzo, E. Ernst, 2003).
По данным двойного слепого рандомизированного контролируемого мультицентрового 12-недельного пилотного исследования, проведенного D. Wuttke и соавт. (2002), целью которого было сравнение эффективности, безопасности и переносимости C. racemosa с конъюгированными эстрогенами и плацебо, было показано, что C. racemosa эффективно устраняет климактерические расстройства, воздействуя на ЦНС и гипофиз, вероятно, сочетая в себе эстрогенподобное и допаминэргическое действия. Кроме того, выявлено положительное влияние C. racemosa на динамику биохимических маркеров ремоделирования КТ.
Wuttke и соавт. (2002), целью которого было сравнение эффективности, безопасности и переносимости C. racemosa с конъюгированными эстрогенами и плацебо, было показано, что C. racemosa эффективно устраняет климактерические расстройства, воздействуя на ЦНС и гипофиз, вероятно, сочетая в себе эстрогенподобное и допаминэргическое действия. Кроме того, выявлено положительное влияние C. racemosa на динамику биохимических маркеров ремоделирования КТ.
Проведенное нами в клинике исследование эффективности экстракта C. racemosa у женщин в постменопаузальном периоде с выраженными климактерическими нарушениями доказало его эффективность в уменьшении вегетососудистых и психоневротических проявлений постменопаузы, снижении выраженности вертебрального болевого синдрома, профилактике потери КТ (В.В. Поворознюк, Н.В. Григорьева, 2004).
Представителем другого класса препаратов, активно предупреждающим потерю КТ в постменопаузе, является тиболон. Последний принадлежит к группе СТЭАР, является синтетическим стероидом, обладающим слабым эстрогенным, прогестагенным и андрогенным действиями, и больше двадцати лет используется в Европе с целью профилактики и лечения симптомов, связанных с менопаузой (H. J. Kloosterboer, 2002). Тиболон, подобно эстрогенам, уменьшает интенсивность резорбции костной ткани, выраженность климактерических симптомов, не стимулируя клетки эндометрия и МЖ (J.M. Rymer, 1998; S. Palacios, 2001). Эффект тиболона объясняется не тотальным замещением эстрогенодефицита, а его тканеспецифическим действием, которое заключается в превращении тиболона в метаболиты, обладающие различной биологической активностью; в связывании со стероидными рецепторами и в локальном специфическом метаболизме в тканях (S. Palacios, 2001).
J. Kloosterboer, 2002). Тиболон, подобно эстрогенам, уменьшает интенсивность резорбции костной ткани, выраженность климактерических симптомов, не стимулируя клетки эндометрия и МЖ (J.M. Rymer, 1998; S. Palacios, 2001). Эффект тиболона объясняется не тотальным замещением эстрогенодефицита, а его тканеспецифическим действием, которое заключается в превращении тиболона в метаболиты, обладающие различной биологической активностью; в связывании со стероидными рецепторами и в локальном специфическом метаболизме в тканях (S. Palacios, 2001).
Во многочисленных исследованиях изучена эффективность тиболона в предупреждении потери КТ, особенно у женщин в раннем и позднем постменопаузальных периодах (Rymer J. et al., 1994; Berning В. et al., 1996). Двухлетнее исследование МПКТ у пациенток в ранней постменопаузе показало, что за период лечения показатели МПКТ увеличились на 4-5% в группе, принимавшей тиболон, и снизились приблизительно на 3% в группе плацебо (Berning В. et al., 1996).
Тиболон положительно влияет на костную массу у женщин с установленным остеопорозом. В двухлетнем плацебо-контролируемом исследовании лечение тиболоном приводило к увеличению костной массы на 8%, в то время как у женщин группы плацебо наблюдалась 4% потеря КТ (P. Geusens et al., 1991). В другом двухлетнем плацебо-контролируемом исследовании применение тиболона привело к увеличению МПКТ в поясничном отделе позвоночника на 6,9% и в области шейки бедра на 4,5% (P.W. Pavlov et al., 1999).
В двухлетнем плацебо-контролируемом исследовании лечение тиболоном приводило к увеличению костной массы на 8%, в то время как у женщин группы плацебо наблюдалась 4% потеря КТ (P. Geusens et al., 1991). В другом двухлетнем плацебо-контролируемом исследовании применение тиболона привело к увеличению МПКТ в поясничном отделе позвоночника на 6,9% и в области шейки бедра на 4,5% (P.W. Pavlov et al., 1999).
Проведенное нами экспериментальное исследование доказало, что тиболон на фоне адекватного потребления кальция у овариоэктомированных самок крыс зрелого возраста достоверно улучшает структурно-функциональное состояние КТ за счет увеличения ее прочностных характеристик, положительных изменений в химическом составе костей ( В.В. Поворознюк, В.И. Лузин, Н.В. Григорьева, 2002). Применение тиболона в клинике у женщин в постменопаузальном периоде с нарушениями структурно-функционального состояния КТ доказало его эффективность в снижении выраженности вертебрального болевого синдрома, увеличении индекса прочности КТ через 6 и 12 мес после лечения (В. В. Поворознюк, Н.В. Григорьева, 2002).
В. Поворознюк, Н.В. Григорьева, 2002).
Селективные эстроген-рецепторные модуляторы являются агонистами эстрогенных рецепторов в отношении КТ, липидного спектра крови и их антагонистами в отношении МЖ и матки. СЭРМ взаимодействуют с ЭР, однако оказывают различное влияние в зависимости от типа ткани, системы органов и физиологического состояния пациентки.
Одним из первых нестероидных антиэстрогенов был тамоксифен, который является антагонистом эстрогенов в МЖ и широко используется у больных раком МЖ. При этом он оказывает положительное влияние на состояние КТ и на уровень липидов в сыворотке крови. Однако, несмотря на противоопухолевое действие тамоксифена при раке МЖ, препарат может оказывать пролиферативный эффект на эндометрий и привести к развитию рака (В.M. Fischer, J.P. Constantino, C.R. Redmond et al. 1994; B.H. Mitlak, F.J. Cohen, 1997; F Cosman., R. Lindsay, 1999), что предполагает необходимость назначения на фоне терапии тамоксифеном прогестагенов в течение 10-12 сут курса лечения с целью снижения уровня гиперпластических процессов в эндометрии.
Эффект тамоксифена в профилактике потери КТ доказан как у здоровых пациенток, так и у лиц с перенесенным раком МЖ. В трехлетнем исследовании (T.J. Powles, T. Hickish., J.A. Kanis et al., 1996) у 54 женщин в постменопаузе, получавших химиотерапию по поводу перенесенного рака МЖ, показано, что терапия тамоксифеном приводит к достоверному (по сравнению с плацебо) увеличению МПКТ в поясничном отделе позвоночника (на 4,7%, р<0,05) и в шейке бедренной кости (на 3,6%, p<0,005).
Препараты СЭРМ второго поколения являются более селективными по сравнению с тамоксифеном. Так, ралоксифен, связываясь с ЭР, положительно влияет на состояние КТ (F. Cosman, R. Lindsay, 1999), выражает антиэстрогенное действие на клетки МЖ, однако не оказывает эстрогенподобного влияния на эндометрий (B.H. Mitlak, F.J. Cohen, 1997; F. Cosman, R. Lindsay, 1999). Так, по данным Cohen и соавт. (2000), ралоксифен не вызывает пролиферирующего влияния на эндометрий и не повышает риск развития рака эндометрия после 40 мес лечения у женщин в постменопаузе.
В настоящее время, несмотря на то что количество веществ, относящихся к группе СЭРМ, достаточно большое, только ралоксифен одобрен для лечения и профилактики остеопороза. Следует отметить, что как тамоксифен, так и ралоксифен обладает рядом побочных эффектов, среди которых наиболее важными являются вазомоторные симптомы (приливы и ночная потливость), связанные с дефицитом эстрогенов (F. Cosman, R. Lindsay, 1999).
Многочисленные клинические исследования по применению ралоксифена у женщин в постменопаузе доказали его эффективность в профилактике и лечении постменопаузального остеопороза. Так, ралоксифен достоверно повышает МПКТ и предотвращает дальнейшую потерю костной массы, улучшая биохимические показатели костного обмена, а также снижает риск возникновения вертебральных и невертебральных переломов.
В трехлетнем рандомизированном двойном плацебо-контролируемом исследовании (C.C.J. Johnston, N.H. Bjarnason, F.J. Cohen et al., 2000) с участием 576 здоровых лиц, находящихся в раннем постменопаузальном периоде, установлено достоверную разницу показателей МПКТ у женщин, принимавших ралоксифен по схеме 60 мг/сут, по сравнению с пациентками группы плацебо (1,7% для всего скелета, 2,6% – для поясничного отдела позвоночника и 2,5% – для шейки бедренной кости; р<0,05 для всех показателей).
Эффективность ралоксифена в предупреждении новых вертебральных переломов костей была доказана в результате проведения рандомизированного двойного слепого плацебо-контролируемого исследования MORE (Multiple Outcomes of Raloxifene Evalution) (B. Ettinger, D.M. Black, B.H. Mitlak, 1999). После двухлетнего лечения ралоксифеном относительный риск развития вертебральных переломов у пациенток составил 0,56 от соответствующего показателя в группе плацебо, то есть уменьшился на 44%. Различий между группами в отношении возникновения новых непозвоночных переломов не было. Трехлетнее продолжение лечения ралоксифеном привело к снижению риска вертебральных переломов на 30-50%. Относительный риск возникновения новых переломов позвонков у женщин с остеопорозом и предшествующими переломами составлял 0,5 (95% ДИ: 0,3-0,7), а для пациенток без вертебральных переломов в анамнезе – 0,7 (95% ДИ: 0,6-0,9). Кроме того, отмечено достоверное увеличение МПКТ на 2-3% (2,6% в поясничном отделе позвоночника и 2,1% в шейке бедренной кости) в группе пациенток, принимавших ралоксифен, по сравнению с показателями в группе плацебо (B.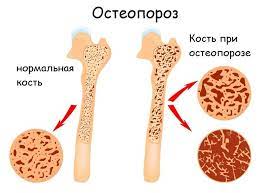 Ettinger, D.M. Black, B.H. Mitlak, 1999).
Ettinger, D.M. Black, B.H. Mitlak, 1999).
Таким образом, в настоящее время установлено, что СЭРМ являются эффективными препаратами для профилактики и лечения остеопороза, рака МЖ и, возможно, сердечно-сосудистых заболеваний у женщин в постменопаузе.
Кальцитонин (синоним тиреокальцитонин) – пептидный гормон, физиологическая функция которого состоит в регуляции обмена кальция и фосфорa. Кальцитонин экскретируется преимущественно парафолликулярными клетками (С-клетками) щитовидной железы (Р.А. Красноперов и соавт., 1996; D.H. Copp, 1994). Последнее десятилетие изучения природы кальцитонина дало возможность получить этот гормон синтетическим путем и использовать его в качестве лекарственного средства. Он замедляет снижение МПКТ в скелете, в первую очередь в поясничном отделе позвоночника при остеопорозе, воздействует не только как лечебное, но и профилактическое средство (P.N. Sambrook, J. Jones, 1995; I. Arnala, J. Saastamoinen, E.M. Alhava, 1996; PROOF Study Group, C.H. Chesnut, S. Silverman et al., 2000).
Chesnut, S. Silverman et al., 2000).
Первичным местом влияния кальцитонина (его органом-мишенью) является КТ. Основной эффект кальцитонина проявляется гипокальциемией и гипофосфатемией, а его продукцию стимулирует гиперкальциемия. Биологическое действие гормона состоит в торможении резорбтивных процессов в КТ. Гипокальциемический эффект, обусловленный способностью подавлять резорбцию КТ, проявляется лишь тогда, когда костная резорбция замедлена до уровня снижения выделения кальция из кости в кровь. Кальцитонин способствует репаративному формированию костей при переломах и ингибирует не только спонтанную костную резорбцию, но и остеолиз, который может стимулироваться ПТГ, витамином D и другими факторами (Н.Т. Старкова, 1996).
Антикатаболический эффект кальцитонина используется для лечения системных заболеваний скелета с активными процессами остеолиза (болезни Педжета, гиперпаратиреоза, метастаз злокачественных опухолей в кости). Кальцитонин также обладает выраженным анальгетическим эффектом, который напоминает действие опиоидных анальгетиков. Комбинированный анальгетический и антирезорбционный эффект кальцитонина чрезвычайно ценен при лечении клинически активной фазы остеопороза.
Комбинированный анальгетический и антирезорбционный эффект кальцитонина чрезвычайно ценен при лечении клинически активной фазы остеопороза.
В клинической практике используют четыре препарата кальцитонина: лосося, угря, свиньи и человека. Гипокальциемический эффект кальцитонина лосося и угря в десятки раз превышает эффективность такового у человека или свиньи. Это объясняется неодинаковой чувствительностью кальцитониновых рецепторов (М. Azria et al., 1995). В настоящее время наиболее эффективным и популярным в мировой клинической практике является синтетический кальцитонин лосося, поступающий в аптечную сеть Украины в виде двух лекарственных форм: ампул для парентерального введения и аэрозоля для интраназального применения. Интерес к кальцитонину в профилактике и в лечении остеопороза существенно возрос после появления новой клинической формы для интраназального введения, биодоступность которой на 10-25%, а фармакологическая биоэквивалентность на 40% выше по сравнению с парентеральными формами (K. Overgaard et al., 1991).
Overgaard et al., 1991).
Ряд авторов считают кальцитонин вторым по эффективности средством профилактики и лечения постменопаузального остеопороза при помощи проведения ЗГТ (B.C. Лукьянчиков, А.П. Калинин, 1997). Многочисленные исследования подтвердили его эффективность как в профилактике, так и в лечении установленного остеопороза. Препарат назначают ежедневно или через день парентерально по 50-100 МЕ, интраназально по 100-200 МЕ непрерывными или прерывистыми курсами (по 3-4 мес с такими же перерывами).
Проведен метаанализ рандомизированных клинических исследований, изучавших частоту возникновения вертебральных и других остеопоротических переломов (шейки бедра, предплечья) при лечении кальцитонином (J.A. Kanis, E.V. McCloskey, 1999). Относительный риск возникновения любого перелома для пациентов, получавших кальцитонин, по сравнению с пациентами, не принимавшими препарат, составил 0,43. Эффект был очевидным как для вертебральных (0,45), так и невертебральных (0,34) переломов. Таким образом, лечение кальцитонином приводит к значительному уменьшению количества вертебральных и невертебральных переломов.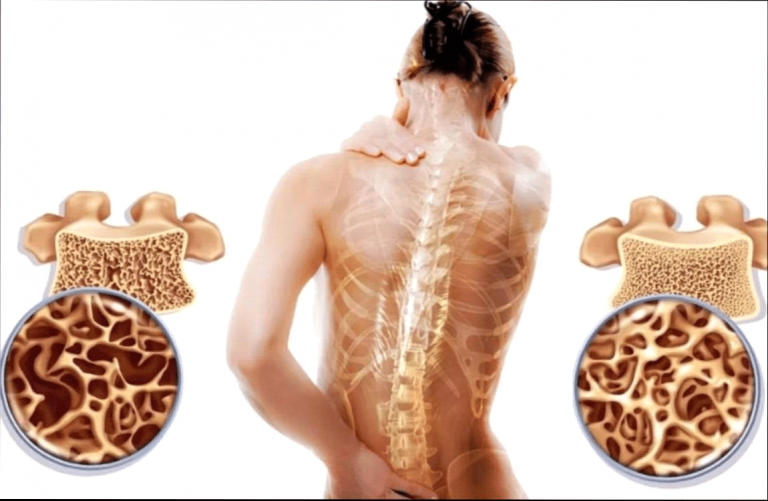
Подкожные или внутримышечные инъекции кальцитонина часто (25-50%) сопровождаются побочными эффектами: гиперемией, тошнотой, рвотой, головной болью, повышением артериального давления и эпигастральными спазмами (W. Horst-Sikorska et al., 1996). Частота побочных эффектов снижается при дальнейшем приеме препарата, достигая 10% (S.J. Wimalawansa, 1992). Различные исследования показали, что кальцитонин в аэрозольной форме для интраназального введения не только более удобен по сравнению с инъекционными формами, но и значительно лучше переносится больными – побочные эффекты встречаются достаточно редко и носят невыраженный характер.
Бисфосфонаты. Главное действие бисфосфонатов на скелет – замедление минерализации кости и хряща, а также ингибирование вызываемой остеокластами резорбции КТ. В случае этидроната ингибирование минерализации происходит в дозах, почти эквивалентных дозам, тормозящим резорбцию КТ (N.B. Watts et al., 1990; C. Vitte et al., 1990; S.T. Harris et al., 1994). Благодаря этой особенности, этидронат используется при гетеротопной кальцификации после хирургических вмешательств на бедре при параплегии. Замедление минерализации связывают с ингибированием роста кристаллов. Для алендроната доза, нарушающая минерализацию КТ, в 6000 раз выше эффективной антирезорбтивной дозы.
Благодаря этой особенности, этидронат используется при гетеротопной кальцификации после хирургических вмешательств на бедре при параплегии. Замедление минерализации связывают с ингибированием роста кристаллов. Для алендроната доза, нарушающая минерализацию КТ, в 6000 раз выше эффективной антирезорбтивной дозы.
Действия различных бисфосфонатов на резорбцию кости существенно отличаются. Существуют также различия в их сравнительной активности с разными системами тестов. В перспективе клинического использования вызывают интерес новые бисфосфонаты с минимальным нежелательным эффектом на минерализацию и выраженным антирезорбтивным действием. В этом аспекте аминопроизводные проявляют значительную активность без увеличения влияния на минерализацию кости или изменения их сродства к гидроксиапатиту. Памидронат приблизительно в 100 раз мощнее этидроната в отношении предотвращения резорбции метафиза у крыс. Алендронат в 10 раз более мощный, чем памидронат. Имеется некоторая корреляция между активностью бисфосфонатов и длиной боковой цепочки. Однако удлинение боковой цепочки за счет более 4 атомов углерода приводит к уменьшению активности (например неридронат). Расширение антирезорбтивного действия может быть достигнуто добавлением боковых цепочек к аминогруппе (ибандронат) или циклической заменой, особенно содержащей азот (ризедронат).
Однако удлинение боковой цепочки за счет более 4 атомов углерода приводит к уменьшению активности (например неридронат). Расширение антирезорбтивного действия может быть достигнуто добавлением боковых цепочек к аминогруппе (ибандронат) или циклической заменой, особенно содержащей азот (ризедронат).
В последние годы увеличился интерес к возможности использования бисфосфонатов в лечении остеопороза (J.E. Compston, 1994; G.A. Rodan, H. Fleisch, 1996; H. Fleisch, 1997). Все представители данной группы лекарственных препаратов способны существенно замедлять перестройку КТ. При этом препараты последних генераций оказывают существенное влияние на резорбцию КТ. Этидронат – наиболее изученный бисфосфонат. Непрерывная терапия постменопаузального остеопороза этидронатом впервые была применена 20 лет назад с результатом, который вызвал определенное недоумение: у больных развивалась остеомаляция и гиперфосфатемия (A. Heaney et al., 1997). Через десятилетия исследователи остановились на циклических режимах применения бисфосфонатов.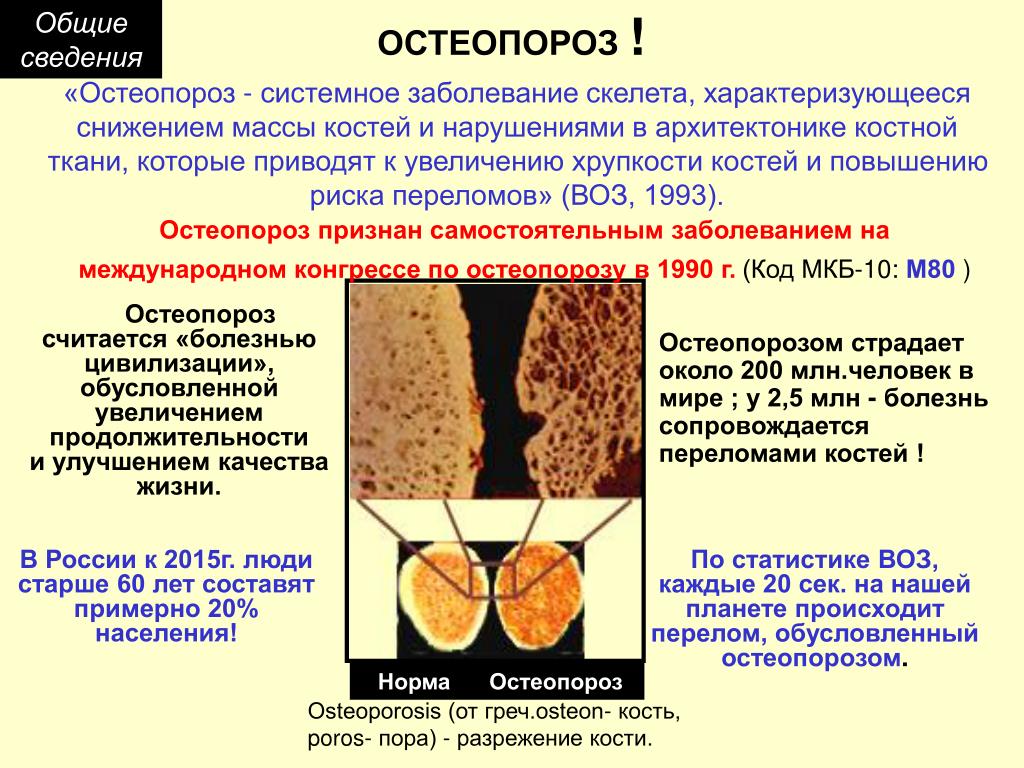 Этидронат в таком режиме приема был одобрен для лечения остеопороза в нескольких странах, но не в США. Недавно проведенное многоцентровое исследование показало, что прерывистая циклическая терапия этидронатом (400 мг/сут в течение 2 нед, каждые 13 нед в сочетании с кальцием и витамином D) в течение четырех лет приводит к увеличению минеральной плотности КТ позвоночника и бедра (соответственно на 4 и 2% выше показателей в контрольной группе), но частота переломов увеличилась на протяжении третьего года исследования (D.W. Axelrod, S.L. Teitelbaum, 1994). Таким образом, вопрос о том, снижает ли этидронат риск возникновения вертебральных переломов при прерывистом циклическом режиме приема, все еще остается открытым (H. Fleish, 1999). В настоящее время исследователи сосредоточили свое внимание на новых бисфосфонатах, таких как алендронат, тилудронат, памидронат и ризедронат.
Этидронат в таком режиме приема был одобрен для лечения остеопороза в нескольких странах, но не в США. Недавно проведенное многоцентровое исследование показало, что прерывистая циклическая терапия этидронатом (400 мг/сут в течение 2 нед, каждые 13 нед в сочетании с кальцием и витамином D) в течение четырех лет приводит к увеличению минеральной плотности КТ позвоночника и бедра (соответственно на 4 и 2% выше показателей в контрольной группе), но частота переломов увеличилась на протяжении третьего года исследования (D.W. Axelrod, S.L. Teitelbaum, 1994). Таким образом, вопрос о том, снижает ли этидронат риск возникновения вертебральных переломов при прерывистом циклическом режиме приема, все еще остается открытым (H. Fleish, 1999). В настоящее время исследователи сосредоточили свое внимание на новых бисфосфонатах, таких как алендронат, тилудронат, памидронат и ризедронат.
Ризедронат (3-пиридинил-2-гидрооксиэтилидин бисфосфонат) оказывает более быстрое и существенное влияние на КТ осевого скелета по сравнению с этидронатом (S. A. Khan et al., 1994; В.В. Поворознюк, 1999). Существенное влияние бисфосфонатов на скелет в первую очередь объясняется снижением скорости ремоделирования в трабекулярной кости осевого скелета. При этом влияние на компактную кость незначительно, что обусловлено более низким метаболизмом компактной КТ по сравнению с губчатой. Бисфосфонаты второго и третьего поколений не вызывают нарушений минерализации КТ или избыточного угнетения процессов костного ремоделирования. Они представляют собой высокоэффективные средства для лечения остеопороза, однако их способность предотвращать новые переломы до конца не изучена.
A. Khan et al., 1994; В.В. Поворознюк, 1999). Существенное влияние бисфосфонатов на скелет в первую очередь объясняется снижением скорости ремоделирования в трабекулярной кости осевого скелета. При этом влияние на компактную кость незначительно, что обусловлено более низким метаболизмом компактной КТ по сравнению с губчатой. Бисфосфонаты второго и третьего поколений не вызывают нарушений минерализации КТ или избыточного угнетения процессов костного ремоделирования. Они представляют собой высокоэффективные средства для лечения остеопороза, однако их способность предотвращать новые переломы до конца не изучена.
Алендронат натрия – аминобисфосфонат – действует как мощный специфический ингибитор остеокластиндуцированной резорбции кости и таким образом нормализует скорость перестройки кости, что позволяет относить его к патогенетическим антирезорбтивным средствам. В результате лечения алендронатом натрия формируется кость нормальной структуры, без нарушения минерализации. Присутствие P-C-P структуры определяет резистентность алендроната натрия к гидролизу и ограничивает его возможность проникать через клеточные мембраны, что объясняет низкую токсичность данного препарата. В экспериментальных исследованиях было показано, что это лекарственное средство избирательно концентрируется на поверхностях резорбции кости под присоединившимся остеокластом. В процессе резорбции, остеокласты могут потерять активность, что определяется отсутствием щеточной каймы (плазмолеммной оборки), характеризующей активную резорбцию кости, так как в этой области происходит выделение остеокластами лизосомальных ферментов (в том числе кислой фосфатазы и проколлагеназ) и кислоты. Следовательно, формирующиеся в процессе резорбции лакуны будут мелкими и менее определяемыми, что в дальнейшем приведет к установлению положительного баланса между формированием и резорбцией кости. Уменьшение количества резорбированной кости менее выражено, чем связанное с ним увеличение вновь сформированной нормальной кости, что приводит к приросту костной массы, повышению ее минеральной плотности при лечении алендронатом. Исследования последних лет показали, что длительное использование бисфосфонатов приводит к уменьшению частоты переломов у пациентов с остеопорозом.
В экспериментальных исследованиях было показано, что это лекарственное средство избирательно концентрируется на поверхностях резорбции кости под присоединившимся остеокластом. В процессе резорбции, остеокласты могут потерять активность, что определяется отсутствием щеточной каймы (плазмолеммной оборки), характеризующей активную резорбцию кости, так как в этой области происходит выделение остеокластами лизосомальных ферментов (в том числе кислой фосфатазы и проколлагеназ) и кислоты. Следовательно, формирующиеся в процессе резорбции лакуны будут мелкими и менее определяемыми, что в дальнейшем приведет к установлению положительного баланса между формированием и резорбцией кости. Уменьшение количества резорбированной кости менее выражено, чем связанное с ним увеличение вновь сформированной нормальной кости, что приводит к приросту костной массы, повышению ее минеральной плотности при лечении алендронатом. Исследования последних лет показали, что длительное использование бисфосфонатов приводит к уменьшению частоты переломов у пациентов с остеопорозом.
Алендронат имеет достаточно широкое терапевтическое окно; он относительно безопасен и достаточно эффективен в предотвращении потери КТ у лиц с установленным остеопорозом. Алендронат обычно назначают в дозе 10 мг ежедневно, однако в связи с частыми побочными эффектами со стороны ЖКТ была предложена доза 70 мг один раз в неделю. Она оказалась такой же эффективной, как и доза в 10 мг в лечении постменопаузального остеопороза, а частота осложнений была значительно ниже (T. Schnitzer et al., 2000; N. Watts , 2001).
В проведенном недавно метаанализе (A. Cranney, G.Wells, A. Willan et al., 2002) сравнивали эффективность различных бисфосфонатов в снижении риска остеопоротических переломов (табл. 3).
Интересными представляются исследования, изучающие аддитивный эффект бисфосфонатов и ЗГТ (S.J. Wimalawansa, 1998; R. Lindsay, F. Cosman, R.A. Lobo, 1999; H.G. Bone, S.L. Greenspan, C. McKeever et al., 2000; S. Palomba, Jr.F. Orio, A. Colao et al., 2002). Доказано, что комбинированное назначение препаратов ЗГТ и этидроната у женщин в постменопаузе в течение четырех лет приводит к более выраженному увеличению МПКТ в поясничном отделе позвоночника и бедре по сравнению с монотерапией каким-либо одним препаратом.
Препараты стронция. На сегодняшний день установлено, что некоторые элементы, в том числе и стронций (Sr) имеют химическое сродство к кальцию. Однако в предыдущие годы использование стронция в медицине не нашло широкого применения в связи с непониманием разницы между эффектами природного стабильного стронция и радиоактивного изотопа Sr 90, который образуется при ядерной реакции.
Стронций и кальций имеют одни и те же механизмы всасывания в стенки ЖКТ, хотя аффинитет выше для кальция, чем для стронция (P.J. Marie, P Ammann., G. Boivin, C. Rey, 2001). Активная кишечная абсорбция стронция опосредована действием витамина D и снижается при старении, применении хелатов, потреблении пищи, высоком содержании кальция и/или фосфатов в рационе питания. Поскольку стронций является элементом, химически и физически сродным с кальцием, он обладает способностью накапливаться в скелете в той же степени, что и кальций. Распределение стронция в скелете пропорционально его уровню в плазме, при этом его эффект является дозозависимым (G. Boivin, P. Deloffre, B. Penrat et al., 1996). Содержание стронция в кости зависит от длительности экспозиции, пола и локализации в скелете. Преимущественно стронций инкорпорируется в трабекулярную кость (S.G. Dahl, P. Allain, P.J. Marie et al., 2001) в основном в виде кристаллов апатита (R.Z. LeGeros, 1990). Кристаллы, содержащие стронций, являются более стабильными и имеют более правильные формы. (P. J. Marie, P. Ammann, G. Boivin, C. Rey, 2001).
Boivin, P. Deloffre, B. Penrat et al., 1996). Содержание стронция в кости зависит от длительности экспозиции, пола и локализации в скелете. Преимущественно стронций инкорпорируется в трабекулярную кость (S.G. Dahl, P. Allain, P.J. Marie et al., 2001) в основном в виде кристаллов апатита (R.Z. LeGeros, 1990). Кристаллы, содержащие стронций, являются более стабильными и имеют более правильные формы. (P. J. Marie, P. Ammann, G. Boivin, C. Rey, 2001).
В настоящее время установлена антирезорбтивная активность препаратов стронция и его анаболический эффект на кость, в связи с чем в последние годы все больше внимания уделяется применению данных препаратов для профилактики и лечения остеопороза.
Высокие дозы стронция могут вызывать скелетные аномалии, в том числе индуцировать развитие рахита, дефектов минерализации и нарушений минерального состава кости, особенно у животных с низким уровнем кальция в рационе питания (T. Morohashi, T. Sano, S. Yamada, 1994; P.J. Marie, P. Ammann, G. Boivin, C. Rey, 2001).
Rey, 2001).
Во многочисленных экспериментальных исследованиях на здоровых животных показано, что стронций в низких дозах снижает интенсивность костной резорбции (J. Buehler, P. Chappuis, J.L. Saffar et al., 2001) и способствует формированию КТ, в результате чего увеличивается костная масса. Доказано, что введение солей стронция в низких дозах здоровым животным стимулирует увеличение объема трабекулярной кости (без изменения минерального состава КТ) эндостальное (M.D. Grynpas, E. Hamilton, R. Cheung et al., 1996) и периостальное костеобразование (P. Ammann, R. Rizzoli, P. Deloffre et al., 1995), при этом полученные данные свидетельствовали о прямом эффекте стронция на формирование КТ.
При изучении влияния различных солей стронция у лиц с остеопорозом было установлено, что стронция лактат усиливает у них задержку кальция в скелете, улучшает процессы минерализации в позвонках большинства женщин в постменопаузе, а введение стронция в виде карбоната в дозах 6,8-8,0 ммоль/сут в течение 6 мес у пациентов с остеопорозом стимулирует эндостальное костное формирование, увеличивает поверхность активных остеобластов и соответственно формирование костного матрикса при отсутствии влияния на минерализацию. Многочисленные обзорные и рандомизированные исследования доказали эффективность стронция ранелата в дозе 5,9 ммоль/сут (0,1 мг/кг/сут для пациента весом 60 кг) в лечении постменопаузального остеопороза (P.J. Meunier, D.O. Slosman, P.D. Delmas et al., 1996; P.J. Meunier, D.O. Slosman, P.D. Delmas et al., 1997; J.Y. Reginster, C. Roux, I. Juspin et al., 1998; J.Y. Reginster, C. Roux, Y. Tsouderos, I. Juspin 1998).
Многочисленные обзорные и рандомизированные исследования доказали эффективность стронция ранелата в дозе 5,9 ммоль/сут (0,1 мг/кг/сут для пациента весом 60 кг) в лечении постменопаузального остеопороза (P.J. Meunier, D.O. Slosman, P.D. Delmas et al., 1996; P.J. Meunier, D.O. Slosman, P.D. Delmas et al., 1997; J.Y. Reginster, C. Roux, I. Juspin et al., 1998; J.Y. Reginster, C. Roux, Y. Tsouderos, I. Juspin 1998).
Установлено дозозависимое повышение МПКТ у женщин, получавших стронция ранелат, с 1,4% в группе принимавших 0,5 г/сут препарата до 3,0% в группе пациенток, получавших 2 г/сут стронция, что было достоверно выше по сравнению с группой плацебо (р<0,01). Повышение МПКТ сопровождалось достоверными изменениями маркеров костного ремоделирования (повышение активности костной фракции щелочной фосфатазы и снижение экскреции N-телопептида). Кроме того, отмечено достоверное уменьшение количества пациенток с новыми вертебральными переломами через 2 года терапии стронцием в дозе 2 г/сут (относительный риск = 0,56 (0,35-0,89) 95% ДИ). В проведенных исследованиях отмечается хорошая переносимость препарата (P.J. Meunier, D.O. Slosman, P.D. Delmas, 2002; J.Y. Reginster, P.J. Meunier, 2003).
В проведенных исследованиях отмечается хорошая переносимость препарата (P.J. Meunier, D.O. Slosman, P.D. Delmas, 2002; J.Y. Reginster, P.J. Meunier, 2003).
У больных, получавших стронция ранелат в течение трех лет, выявлено повышение МПКТ в поясничном отделе позвоночника на 12,7%, в шейке бедренной кости на 7,2% и на всем бедре на 8,6% (р<0,001) по сравнению с исходными показателями, соответственно разница с группой плацебо и леченной группой за три года составила: для поясничного отдела позвоночника 14,4% (р<0.001), шейки бедренной кости 8,3% (р<0,001), всей бедренной кости (total hip) – 9,8%. Прочность кости увеличивалась прямо пропорционально МПКТ (P.J. Meunier, C. Roux, E. Seeman et. at., 2004).
За время трехлетнего наблюдения комплайентность терапии составила 83% в группе женщин, получавших стронция ранелат, и 85% в группе плацебо, а уровень побочных эффектов был соизмерим в обеих группах. Наиболее частым из них была диарея, однако этот побочный эффект исчезал после первых 3 мес лечения. Несколько ниже был уровень выявления гастритов в группе лиц, получавших стронция ранелат 3,6 и 5,5% (р=0,07) (Meunier P.J., Roux C., Seeman E. et. at., 2004).
Несколько ниже был уровень выявления гастритов в группе лиц, получавших стронция ранелат 3,6 и 5,5% (р=0,07) (Meunier P.J., Roux C., Seeman E. et. at., 2004).
Выявленное снижение возникновения относительного риска новых вертебральных переломов, полученное в исследовании SOTI (The Spinal Osteoporosis Therapeutic Intervention), соизмеримо с подобным риском при лечении другими антиостеопоротическими средствами (табл. 4), а методы оценки, используемые в этих исследованиях, – подобны, что позволяет их сравнивать. Кроме того, важно отметить, что стронция ранелат снижает не только риск новых вертебральных деформаций, но и риск множественных вертебральных и симптоматических переломов.
Таким образом, в настоящее время установлено, что стронция ранелат является эффективным антиостеопоротическим средством, которое повышает минеральную плотность КТ у здоровых женщин и пациенток с остеопорозом, улучшая уровень маркеров костного ремоделирования и снижая риск как вертебральных, так и невертебральных переломов.
На основании данных литературы и собственных исследований, с учетом демографических тенденций, можно предположить, что остеопороз с его дорогостоящими технологиями лечения и реабилитации переломов будет занимать по финансовым затратам одно из ведущих мест в бюджете здравоохранения. Своевременная профилактика и лечение этого заболевания являются необходимыми и позволят снизить показатели смертности, а также улучшить качество жизни пациентов старших возрастных групп.
Остеопороз (потеря костной массы) является широко распространенным заболеванием.
Что такое остеопороз
Остеопороз, также известный как потеря костной массы, является метаболическим заболеванием скелета, при котором кости теряют свою прочность. Они становятся пористыми и хрупкими. Заболевание протекает бессимптомно. Первым симптомом может стать перелом позвоночника или шейки бедра.
По данным Всемирной организации здравоохранения (ВОЗ), остеопороз является одним из самых распространенных заболеваний нашего времени. Остеопорозом страдает приблизительно каждая четвертая женщина старше 50 лет. Частота остеопороза превышает частоту рака молочной железы, инсульта и инфаркта.1
Остеопорозом страдает приблизительно каждая четвертая женщина старше 50 лет. Частота остеопороза превышает частоту рака молочной железы, инсульта и инфаркта.1
Основная задача для врачей и пациентов — как можно быстрее выявить заболевание. Если остеопороз диагностируется на ранней стадии, его проявления можно эффективно устранить, хотя излечение пока что невозможно.
Физические упражнения и здоровое питание (витамин D и кальций) являются эффективными мерами Предшественником остеопороза является остеопения (уменьшение плотности кости). При регулярном наблюдении и выполнении рекомендаций врача остеопения может никогда не перейти в остеопороз. В случае прогрессирования возникает остеопороз и необходимость снова посетить врача, чтобы он назначил соответствующую терапию.
Как развивается остеопороз?
Некоторые считают, что кости — это прочные структуры, не подверженные изменениям. На самом деле, это не так. Кость постоянно обновляется путем посредством одновременного разрушения костного вещества и образования нового. Гормоны, витамины и другие активные вещества контролируют этот процесс (ремоделирование кости). В юности и молодости процесс костеообразование преобладает над разрушением. С возрастом образование кости замедляется. После смещения равновесия в сторону разрушения костной ткани кость постепенно утрачивает свою прочность.
Оценить плотность костей можно с помощью специального исследования — денситометрии.
Остеопороз разделяют на две формы: первичный и вторичный.
Первичный остеопороз
Первичный остеопороз
Приблизительно 95 % случаев потери костной массы обусловлено первичным остеопорозом.
Остеопороз I типа:
Первый тип остеопороза развивается у женщин в постменопаузе (постменопаузальный остеопороз). При данном типе остеопороза переломам наиболее подвержены позвонки.
Остеопороз II типа:
Остеопороз II типа обычно возникает после 70 лет (сенильный остеопороз). При данном типе остеопороза чаще всего ломаются позвонки, бедренные кости и кости предплечья.
Факторы риска первичного остеопороза:
- Старение
- Изменение гормонального фона (позднее менархе, ранняя менопауза)
- Гиподинамия
- Длительный период иммобилизации
- Дефицит массы тела
- Диета с недостаточным поступлением кальция или диета с высоким потреблением фосфатов (еда в сетях быстрого питания, сладкие газированные напитки)
- Злоупотребление алкоголем, кофе
- Курение
Вторичный остеопороз
Вторичный остеопороз
Вторичный остеопороз возникает в результате других заболеваний или является побочным действием определенных медикаментозных препаратов:
- Противовоспалительные гормональные препараты для лечения астмы или ревматизма (кортизон)
- Нарушения гормональной регуляции, например гипертиреоз
- Опухолевые заболевания
Факторы риска вторичного остеопороза:
- Длительный прием гормональных препаратов (астма, ревматизм)
- Длительный прием производных кумарина (маркумар)
- Систематическое нарушение работы желудочно-кишечного тракта, в том числе при заболеваниях поджелудочной железы, кишечника, печени
- Хронические заболевания почек
- Нарушение обмена гормонов щитовидной железы (гипотиреоз) и поджелудочной железы (диабет)
- Онкологические заболевания
Диагностика остеопороза
Правильно и быстро поставленный диагноз имеет решающее значение для немедленного начала лечения. Поэтому рекомендуется регулярно посещать врача и проводить скрининговые исследования (денситометрия) при наличии факторов риска. Это касается женщин в постменопаузе, а также мужчин пожилого и старческого возраста. Всякий раз при наличии подозрений на снижение костной массы эти подозрения должны быть подтверждены или опровергнуты инструментальными методами диагностики. Симптомами, позволяющими заподозрить остеопороз, являются:
- снижение роста и формирование гиперкифоза грудного отдела позвоночника (горб)
- выраженные хронические боли в спине или грудине
- Переломы костей без видимых причин, особенно переломы позвоночника под тяжестью собственного веса
Профилактика остеопороза
Существуют различные способы замедлить процесс разрушения костной ткани. Профилактику остеопороза нужно начинать уже в юности, когда есть возможность сформировать более массивные кости, на ослабление которых спустя десятилетия потребуется дополнительное время. К профилактическим мерам относятся:
- регулярная гимнастика и умеренные мышечные тренировки (специальные упражнения для тренировки разных групп мышц замедляют потерю костной массы),
- здоровое и сбалансированное питание с достаточным потреблением витаминов, белков и кальция.
Комбинация физической активности и правильного питания позволяет на долгие годы сохранить кости и мышцы здоровыми.
Лечение остеопороза
Лечение остеопороза направлено на улучшение качества жизни пациентов. Терапия заключается в комбинировании нескольких подходов, которые профильными специалистами объединены в клинические рекомендации по остеопорозу. Эффективная терапия остеопороза должна быть многокомпонентной:
Медикаментозная терапия
Для лечения остеопороза используются следующие группы препаратов:
СМРЭ
СМРЭ (селективные модуляторы рецепторов эстрогена) по своей химической структуре похожи на гормон эстроген, выработка которого понижается после наступления менопаузы. СМРЭ активизируют рецепторы эстрогена и увеличивают образование костной ткани. При этом данная группа препаратов в отличие от эстрогена не повышает риск рака молочной железы и сердечно-сосудистых заболеваний.
Бифосфонаты
Бисфосфонаты замедляют деградацию костной ткани и таким образом замедляют процесс потери костной массы.
Кальций и витамин D
Кальция и витамин D. Кальций является основным элементом минерального компонента костной ткани. Он должен поступать в организм в достаточном количестве с питанием. При недостаточном потреблении кальция рекомендуется прием препаратов кальция. Витамин D облегчает всасывание кальция из желудочно-кишечного тракта и встраивание элемента в структуру кости.
Паратиреоидный гормон / терипаратид
Паратиреоидный гормон / терипаратид стимулирует образование остеобластов и повышает их активность. Остеобласты — это специальные клетки, ответственные за образование костной и ремоделирование костной ткани.
Анальгетики
Обезболивающие препараты уменьшают боль непосредственно после переломов (в остром периоде) и облегчают хроническую боль, возникающую в результате переломов позвонков. Как известно, боль ограничивает активность, поэтому пациенты с остеопорозом должны получать адекватную обезболивающую терапию.
Двигательный режим
Физические упражнения являются методом лечения остеопороза. Специальные физические упражнения, разработанные специалистами по лечебной физкультуре и врачами, повышают двигательную активность, улучшают функциональное состояние мышц и координацию, положительно влияют на общее эмоциональное состояние.
Лечебная гимнастика, особенно упражнения на тренировку силы мышц туловища, должны выполняться постоянно.
Специальный тренажер-корректор, работающий по принципу биологической обратной связи, поддерживает позвоночник в физиологическом положении и тренирует мышцы брюшного пресса и спины. В дополнение к лечебной физкультуре пациентам с остеопорозом рекомендуются следующие виды физической активности:
Идеальным сочетанием является сочетание тренировок силы и выносливости. Чем больше мышечная масса, тем лучше прогноз относительно качества костной ткани.
Упражнения на свежем воздухе особенно эффективны, так как солнечный свет стимулирует естественное образование в коже витамина D.
Важная информация: Пациенты с остеопорозом всегда должны согласовывать с врачом уровень своей физической активности и упражнения лечебной физкультуры.
Силовые тренировки способствует формированию костной ткани
Силовые тренировки создают биомеханические и биохимические стимулы для образования костной ткани. Одновременно, эти упражнения способствуют формированию хорошей осанки. Сильные мышцы работают гармонично и скоординировано.
Тренажер-корректор Spinomed при правильном использовании также тренирует мышцы. Система ремней и алюминиевая шина создают усилие, которое стимулирует собственную мускулатуру. Таким образом, изделие работает практически на подсознательном уровне. Использование Spinomed согласовывается с клиническими рекомендациями по лечению остеопороза.3
Планирование тренировокИдеальным является сочетание разных видов спортивной активности. В результате повышается мышечная масса, улучшается качество кости, общее состояние и чувство равновесия. Подобрать подходящие Вам виды спорта и физические упражнения поможет лечащий врач или врач лечебной физкультуры.
Функциональное ортезирование
Работа костной и мышечной систем тесно связана, поэтому обычно происходит одновременная потеря костной и мышечной массы.
По это причине лечение переломов позвоночника должно быть функциональным, а не только медикаментозным. Перелом позвонка резко увеличивает вероятность последующего перелома и является причиной хронической боли, низкой физической активности и связанной с этим потерей мышечной массы. Современные средства реабилитации при переломе позвоночника одновременно тренируют мышцы и исправляют осанку одновременно.
В прошлом практиковалась иммобилизация после переломов позвоночника в жестких корсетах, но это приводило лишь к прогрессированию остеопороза. В настоящее время от использования жестких корсетов при переломах позвоночника на фоне остеопороза отказывается все большее число врачей, ведь есть современные средства, например тренажер-корректор Spinomed.
Продукция medi: ортезирование при остеопорозе
Переломы позвонков при остеопорозе сопровождаются хроническими болями в спине, что сильно ограничивает двигательную активность пациентов и ведет к еще большему прогрессированию заболевания. Тренажер-корректор Spinomed тренирует мышцы и уменьшает болевые ощущения, что было подтверждено в проведенных клинических исследованиях.4,5
Эффективность Spinomed и Spinomed active подтверждена в нескольких клинических исследованиях 5,6:
- сила мышц живота и туловища увеличивается на 73 и 56 %, соответственно,
- уменьшается отклонение тела от вертикальной оси на 25 %,
- происходит уменьшение угла грудного гиперкифоза на 11 %,
- происходит уменьшение интенсивности боли на 47 %,
- физическая активность становится более комфортной — на 18 %,
- дыхательная функция легких улучшается на 19 %.
Тренажер-корректоры Spinomed и Spinomed active разработаны профессором Гельмутом Ф. Минне (Helmut W. Minne) в сотрудничестве с компанией medi. Spinomed по дизайну схож с рюкзаком. Spinomed active выполнен в виде боди и может использоваться под верхней одеждой. Все модели Spinomed оказывают свое действие по принципу обратной биологической связи.
Источники
1 Epidemiologie der Osteoporose: Bone Evaluation Study, Deutsches Ärzteblatt 2013,4, 52 ff.
2 Hadji P et al. Dtsch Arztebl Int 2013;110(4):52–57.
3 Лесняк О.М., Беневоленская Л.И. Остеопороз. Диагностика, профилактика и лечение. Клинические рекомендации. Изд. 2-е. — М.: «ГЕОТАР-МЕД», 2010.
4 Pfeifer M et al. Die Wirkungen einer neu entwickelten Rückenorthese auf Körperhaltung, Rumpfmuskelkraft und Lebensqualität bei Frauen mit postmenopausaler Osteoporose. Eine randomisierte Studie. Am J Phys Med Rehabil 2004;83(3):177-186.
5 Pfeifer M et al. Die Wirkungen von zwei neu entwickelten Rückenorthesen auf Rumpfmuskelkraft, Körperhaltung und Lebensqualität bei Frauen mit postmenopausaler Osteoporose. Eine randomisierte Studie. Am J Phys Med Rehabil 2011;90(5):805-815.
Советы по продукции
Тренажер-корректор для лечения остеопороза
medi Spinomed
Диагностика и лечение
Типы, причины и лечение болей в спине
Боль в спине
Остеопороз / Заболевания / Клиника ЭКСПЕРТ
Остеопороз — это системное заболевание скелета, основными проявлениями которого является снижение костной массы и нарушение микроархитектоники костной ткани, ведущее к увеличению риска переломов. Заболевание связано со снижением прочности кости и проявляющееся переломами костей при неадекватно малой травме.
Мы относимся к своему скелету, как к некоему крепкому каркасу, который по завершении роста остается неизменным до конца жизни. Это вовсе не так: костная ткань является живой, постоянно меняющейся структурой, где непрерывно происходят два противоположных процесса – разрушение «старой» кости и образование «новой». Кость также является хранилищем микроэлементов (кальция, фосфора, магния). Любое патологическое изменение количества этих элементов в крови, незамедлительно скажется на кости – она начнет продуцировать в кровь недостающие минеральные вещества, поддерживая метаболизм. Естественно, подобное «донорство», особенно, если оно становится частым, не может не сказаться на качестве кости. Заболеваний костной системы великое множество, остеопороз – лишь одно из них.
Классификация
Первичный остеопороз
Это наиболее частая форма заболевания. К ней относятся:
- постменопаузальный остеопороз
- сенильный (т.е. старческий) остеопороз
- ювенильный (т.е. остеопороз в юношеском возрасте)
- идиопатический остеопороз (когда явной причины страдания кости не найдено).
Вторичный остеопороз
Он имеет множество причин, когда возникает не первичное поражение костной ткани, а совсем другие заболевания организма, одним из проявлений которых является остеопороз.
В эту группу относят остеопороз при эндокринных заболеваниях, при заболеваниях желудочно-кишечного тракта, заболеваниях почек, системных заболеваниях, заболеваниях крови и даже приеме многих медикаментов.
Симптомы
По сути, остеопороз — бессимптомное, до поры до времени «молчаливое» заболевание. Его можно распознать по следующим проявлениям:
- иногда пациенты могут пожаловаться на хронические боли в спине или в костях конечностей, в ребрах. Боли способны присутствовать как в покое, так и усиливаться при длительном статическом положении (стоя, сидя), при небольшой физической нагрузке
- больные могут самостоятельно отметить изменение осанки — спина стала «круглой», уменьшилось расстояние между ребрами и костями таза, увеличился живот (стал «выпирающим вперед» и не убирающимся при втягивании)
- может стать заметным снижение в росте, как правило, на этот симптом обращают внимание родственники или сам пациент может заметить, что «раньше дотягивался до мебельных полок, а теперь не могу достать», «не могу развесить белье, т.к. не дотягиваюсь до повешенной несколько лет назад бельевой веревки».
- переломы костей, которые не могут остаться незамеченными (это в основном переломы костей конечностей, а переломы и деформации позвонков могут клинически себя не проявить – и пациент не будет о них знать до рентгенологического обследования). Особенно должны насторожить переломы от минимальной травмы, неадекватной силе травмирующего агента. Это так называемые низкоэнергетичные переломы (падение с высоты собственно роста, резкие повороты туловища, поднятие тяжестей, интенсивный массаж и т.д.).
Длительное время считалось, что болеют только женщины пожилого и старческого возраста (это было заболевание пожилых женщин). Конечно, чаще так и бывает – заболевание поражает женщин старшей возрастной группы, находящихся в менопаузе. Но остеопороз может поражать и мужчин, и женщин молодого возраста, а иногда даже детей.
Диагностика
«Золотым стандартом» диагностики является рентгеновская денситометрия поясничного отдела позвоночника и бедра. Этот метод позволяет оценить минеральную массу кости, что будет информативно при установлении диагноза, и что немаловажно, при наблюдении за состоянием кости в ходе лечения. Определяемая по денситометрии костная масса способна сориентировать, насколько пациент рискует получить остеопоротический перелом.
Может потребоваться традиционное рентгенологическое исследование (рентген костей различных отделов скелета). Этот давно известный метод не ушел в прошлое, он позволяет определить деформации костей, переломы, наличие зон перестройки костной ткани.
Уточнение состояния фосфорно-кальциевого обмена — лабораторное исследование крови и мочи, по результатам которого будет определяться необходимое индивидуальное лечение.
Необходимо оценить лабораторно также функцию почек и печени. Иногда может потребоваться эндоскопическое исследование ЖКТ с малоинвазиной и безболезненной для пациента биопсией слизистой оболочки желудка и двенадцатиперстной кишки для уточнения изменений в этих отделах.
Зачастую, приходится уточнять лабораторные показатели, отражающие функцию эндокринных желез. Функциональное состояние этих органов способно существенно повлиять на костную ткань.
Назначать необходимое обследование должен только компетентный врач эндокринолог после очного осмотра пациента. В силах врача обеспечить пациента информацией по заболеванию именно у него, обсудить дальнейшее лечение, и почему именно это лечение является выбором для пациента; как наблюдать, обследовать и на что обращать внимание в ходе терапии.
Лечение
Поскольку в основе развития остеопороза лежит преобладание разрушения кости над образованием костной ткани, то общим принципом лечения остеопороза является назначение препаратов, угнетающих резорбцию кости (т.е. дальнейшую потерю костной минеральной массы). Иногда требуется назначение препаратов, стимулирующих образование костной ткани. Это патогенетическая терапия (направленная на сам патологический механизм страдания кости). Препарат для лечения «не один», поэтому сориентироваться в правильном лечении может только специалист, имеющий опыт в лечении остеопороза.
Лечение остеопороза также не обходится без дополнительного назначения препаратов кальция и витамина D.Терапия препаратами кальция и витамина D не является самостоятельным лечение остеопороза, это как бы фон лечения, призванный обеспечить строительный материал для кости. Т.е. кальций — это «камень» в «постройке кости», а витамин D — «рабочий», помогающий строить.
В нашей клинике мы имеем опыт применения всего арсенала медикаментозных препаратов для лечения остеопороза, опыт контроля в ходе лечения заболевания, что обеспечивает наилучший эффект от терапии.
Прогноз
При грамотном лечении и наблюдении за больным, прогрессирование потери костной массы и риск переломов можно притормозить. Уже возникшие переломы позвонков и периферических костей, конечно, не исправить. Но даже остановка прогрессирования болезни на фоне остеотропной терапии считается успехом в лечении. Если же удается добиться прироста массы кости, то это еще более позитивно сказывается на течении заболевания.
Поскольку в лечении такого серьезного заболевания, как остеопороз мы работаем больше «на перспективу», стараясь остановить прогрессирование заболевания, то эффект от лечения заметен не быстро.
Для пациента важно не бросить лечение на полпути, а постоянно быть в контакте с лечащим врачом для обсуждения деталей лечения.
Это возможно только при грамотном кураторстве (так называемом «ведении» больного основным лечащим врачом с привлечением консультативной помощи врачей других специальностей, если того требует конкретная клиническая ситуация). Прогноз при таком подходе к терапии наиболее благоприятен в отношении качества жизни больного и лечения заболевания.
Рекомендации и профилактика
Генетическую предрасположенность к остеопорозу мы изменить не в силах, но зато можем повлиять на другие факторы, способствующие болезни. Коррекция образа жизни: активный образ жизни, занятие физкультурой, отказ от курения и умеренное потребление алкоголя, поддержание нормальной массы тела (без фанатичного достижения низкого веса, граничащего с истощением, но и без ожирения), активное потребление продуктов, обеспечивающих положительный кальциевый баланс, позволят предотвратить потерю костной массы. Обсуждение с лечащим врачомпринимаемых препаратов для лечения других заболеваний и влияния их на костную ткань, обсуждение мер защиты костей от побочного влияния препаратов тоже способно уберечь кости от остеопороза.
Как известно, лучшее лечение — это профилактика болезни. Поскольку заболевание может иметь множество причин, то и профилактика тоже должна быть многоплановой.
Часто задаваемые вопросы
Как заподозрить остеопороз?
Из самых простых и доступных средств необходимо просто измерить рост и обратить внимание на осанку. В обычной взрослой жизни мы не измеряем свой рост и при обращении врача к нам с данным вопросом просто указываем на свой «рост в молодости» или ориентируемся на рост, указанный на ярлычке нашей одежды. Тем не менее, полезно уточнять свой рост ежегодно. Снижение в росте более 5 см в сравнении с ростом в молодости или снижение в росте более 2,5 см за год говорит о высокой вероятности остеопороза. Дело в том, что изменение осанки, округление спины, согбенность являются внешними признаками остеопороза, когда снижается высота позвонков (возникают патологические компрессионные переломы тел позвонков). Иногда пациенты обращают внимание на «никак не убирающийся живот» при отсутствии общего избытка веса. Это тоже может свидетельствовать об остеопорозе, когда в результате бессимптомных переломов и деформаций позвонков уменьшается высота позвоночника, следовательно, уменьшается объем брюшной полости. Внутренним органам нужен для своего комфортного размещения прежний объем, вот и происходит выступание живота вперед.
Перелом костей скелета при неадекватно малой травме – основной признак остеопороза. Правда, случившийся перелом свидетельствует о далеко зашедшем процессе страдания кости, когда потеря костной массы уже велика и возврат ее к норме просто невозможен. Пациенты справедливо спрашивают: «Неужели нужно просто сидеть и ждать перелома, чтобы удостовериться в болезни?!». Считается, что поголовное обследование всех пациентов на предмет выявления остеопороза нецелесообразно, но оно точно потребуется людям, которые больше других рискуют заболеть остеопорозом.
Переломы каких костей скелета являются типичными при остеопорозе?
Поскольку остеопороз – процесс, затрагивающий весь скелет, то остеопоротический перелом может случиться в любом отделе скелета. Наиболее частыми, «излюбленными местами» являются кости предплечья («перелом запястья», как называют его пациенты), шейка бедра (очень тяжелый перелом, после которого пациент нередко погибает или становится инвалидом), позвонки.
Стоит ли идти на прием к врачу и затевать обследование? Кто точно нуждается в обследовании и наблюдении за состоянием костной ткани?
Вы в группе риска по развитию остеопороза и переломов костей скелета, а возможно, уже болеете, если:
- У Вас были переломы костей от минимальной травмы: спонтанные или при падении с высоты собственного роста, случайно обнаруженные при рентгенографии компрессионные переломы позвоночника
- Ваш возраст старше 65 лет
- В Вашей семье есть больные остеопорозом (этот диагноз не обязательно должен стоять в амбулаторной карте), т. е. если в семье есть близкие родственники: мать, отец, родные сестры и братья, перенесшие переломы костей от минимальной травмы в возрасте после 45-50 лет
- Вы имеете низкую массу тела, Ваш индекс массы тела (ИМТ) менее 20 кг/м2 или вес ниже 57 кг
- У Вас выявлен дефицит половых гормонов. Ранняя менопауза у женщин (40-45 лет), хирургическая менопауза (удаление матки и/или придатков), длительная аменорея (более года) у молодых пациенток; недостаток тестостерона у мужчин – признаки, указывающие на возможность появления остеопороза.
- Злоупотребление алкоголем, курение — значимые факторы в развитии остеопороза
- Вы не любите молочные продукты (основной источник кальция). Низкое потребление кальция с пищей способствует развитию остеопороза. Организм человека не синтезирует кальций самостоятельно. Мы всецело зависим от поступления этого минерала извне. И если этого элемента (крайне важного, участвующего во всех процессах жизнедеятельности – от свертывания крови до передачи нервного импульса) поступает недостаточно, он вымывается из костной ткани.
- У Вас есть хотя бы одно их хронических заболеваний, таких как сахарный диабет, ревматические заболевания, воспалительные заболевания желудочно-кишечного тракта, целиакия, хронические заболевания печени, состояния после резекции желудка, кишечника, заболевания эндокринной системы, заболевания почек, заболевания крови.
- Вы принимаете преднизолон или его аналоги (по любому заболеванию), или вынуждены принимать противосудорожные препараты, или принимаете психотропные лекарственные средства.
(По материалам «Клинических рекомендаций по остеопорозу» под ред. проф. Лесняк, проф. Беневоленской, 2010г).
Вы обнаружили у себя факторы риска развития остеопороза, что необходимо сделать дальше?
Естественно, необходимо внимательно отнестись к оценке состояния костной ткани, возможному сбережению имеющейся костной массы, дабы избежать переломов костей. Для этого нужно обратиться к врачу и обсудить план дальнейшего обследования. Именно очная беседа с врачом позволит не упустить важные обследования и избежать «лишних» анализов.
В результате обследования был выявлен остеопороз. Еще ничего не беспокоит, переломов костей не было, а нужно ли лечиться?
При установленном остеопорозе необходимо и лечиться, и наблюдать за состоянием костной ткани. Здесь мы работаем «на перспективу», дабы приостановить или свести к минимуму потерю костной массы.
Если болезнь появилась и все равно ее не удастся «полностью вылечить», а только притормозить, существуют ли лекарственные средства против этого заболевания?
Лекарственные препараты для профилактики и лечения остеопороза существуют. Базовой терапией необходимо назначить препараты кальция, так чтобы поступление кальция в организм с лекарствами и пищей соответствовало нормальному (1000-1500 мг в сутки). Но только назначением препаратов кальция ограничиться нельзя – это не основное лечение заболевания, кальций является лишь одним из «строительных блоков в реставрации кости». Далее обязательно подключаются специальные препараты, тормозящие разрушение кости или стимулирующие костеобразование.
Назначить лечение, определиться с выбором препарата, отследить переносимость и эффективность лечения может только врач эндокринолог.
Я получаю лечение по остеопорозу и «ничего не чувствую», как узнать действует ли лекарство и помогает ли оно?
Отследить эффективность лечения можно не сразу, кость достаточно медленно набирает массу, поэтому только спустя 1-2 года лечения мы можем сделать специальное рентгенологическое обследование и уточнить прирост кости. Лабораторные показатели кальциевого обмена можно и нужно неоднократно на фоне лечения, они тоже позволят сориентироваться в правильности выбора терапии.
Тот факт, что я получаю лечение от остеопороза, является 100% гарантией, что переломов костей не будет?
К сожалению, такой 100% гарантии даже при условии правильного лечения, врачи дать не в состоянии. Перелом костей возможен и на фоне лечения, и после окончания лечения. Тем не менее, если в один ряд поставить пациентов с остеопорозом, которые лечились и тех, кто лечения не получал, то в первой группе (леченных) частота переломов будет значительно ниже.
Истории лечения
Случай №1
Пациентка С., 58 лет. Жалуется на боли в спине, возникающие при ходьбе и при длительном вертикальном положении. После отдыха в положении лежа боли уменьшаются, но спина «постоянно устает». Родственники больной заметили, что пациентка стала меньше ростом, сгорбилась. Сама пациентка отметила, что перестала доставать до навесных полок в кухне, связала это 2с возрастом». Самостоятельно от болей в спине использовала различные гели, мази, которые производили временный эффект. Пациентка частным порядком обратилась за помощью к массажисту. Рентгенологического обследования до проведения процедур не проводилось. На фоне третьего сеанса интенсивного массажа спины возникла резкая боль в области позвоночника. Боли в спине не утихали, пациента не могла встать с кровати из-за болей. Была госпитализирована в отделение травматологии, где был выявлен «свежий перелом» одного из позвонков в грудном отделе позвоночника и множественные «старые» переломы и деформации позвонков в грудном и поясничном отделах позвоночника, о которых ранее пациентка не знала.
Установлен диагноз остеопороза. В беседе с пациенткой установлено, что рано прекратились менструации (с 41 года), и гормональной заместительной терапии половыми гормонами не проводилось. Имеется сопутствующая патология желудочно-кишечного тракта – хронический атрофический гастрит, дуоденит. Пациентка практически не употребляет молочных продуктов (не любит, прием молока часто дает вздутие живота, послабление стула). При уточнении наследственности стало известно, что мать пациентки умерла в возрасте 74 лет после перелома шейки бедра.
Пациентке было проведено лабораторное обследование для уточнения состояния кальциевого обмена. Назначена терапия для лечения остеопороза. После улучшения самочувствия пациентка проходила реабилитационное лечение в специализированном отделении. Эффект от лечения отмечает, но жалеет, что не знала о таком заболевании, как «остеопороз» и не обратилась за помощью раньше.
Случай №2
Пациентка К., 52 года. В течение 4-х лет стала отмечать боли в спине, в костях таза, в ногах. Судороги в мышцах рук и ног. Присутствовала общая слабость, самопроизвольно стал снижаться вес (за 4 года похудела на 18 кг).
В связи с болями в спине, ограничивающими передвижение, неоднократно выполнялось обследование: МРТ, рентгенография различных отделов позвоночника. Описывались признаки распространенного остеохондроза с грыжеобразованием в поясничном и крестцовом отделах позвоночника. Получала терапию противовоспалительными, обезболивающими, противосудорожными препаратами, но ощутимого эффекта от терапии не было. В связи с продолжающимся снижением веса, нарастающими жалобами на общую слабость, пациентка была обследована для исключения онкологической патологии, в ходе обследования данное предположение не подтвердилось. Постепенно самочувствие еще более ухудшилось, появились переломы костей (ребра, ключица, кости голени) при небольшой травме (упала дома), перестала сама передвигаться даже в условиях квартиры. При лабораторном обследовании было выявлено значительное снижение гемоглобина, низкий уровень кальция крови и очень высокий уровень паратиреоидного гормона. Был выявлен тяжелый остеопороз.
В связи с полученными данными, в ходе уточняющего обследования у пациентки была выявлена целиакия. Этот диагноз у данной пациентки был впервые установлен уже в зрелом возрасте. Раньше пациентка о данной болезни не знала.
При ретроспективном расспросе, больная указывала, что «всегда трудно было набрать вес, была всю жизнь худенькой», стул был частым (3-5 раз в сутки), при приеме некоторых продуктов (хлеб, овсяная каша) возникали поносы. С детства часто болел живот. Должного внимания на данные расстройства тогда не уделялось. Сама пациентка давно привыкла к особенностям функции своего желудочно-кишечного тракта, считая это своей индивидуальной нормой, старалась «подстроиться» под ситуацию. Прогрессирующая клиника (боли, переломы, изменения в лабораторных показателях) возникла только в возрасте более 50 лет, после наступления менопаузы.
Правильно установленный диагноз и лечение в виде постоянной специализированной диеты, при минимальном медикаментозном лечении, позволили остановить прогрессирование болезни. Пациентка чувствует себя хорошо, переломов не было, боли в костях не беспокоят. При динамическом обследовании выявлено улучшение состояния костной плотности.
Эти примеры демонстрируют необходимость всестороннего обследования пациентов для выявления причины остеопороза, не списывая все проявления патологии костной ткани только на «возраст». Патология желудочно-кишечного тракта может значительно изменять метаболизм костной ткани, приводя к развитию тяжелого остеопороза.
Медикаментозное лечение остеопороза | РевмаКлиник
Главная цель лечения остеопороза — снизить риск переломов, поэтому в терапии остеопороза могут использоваться только препараты, клиническая эффективность которых в отношении снижения риска переломов доказана в длительных многоцентровых клинических испытаниях.
Курс лечения остеопороза продолжается 3 года (при отсутствии переломов в постменопаузальный период в анамнезе), 5 лет при наличии переломов в постмено-паузальном периоде в анамнезе. Если пациент принимает глюкокортикоидные гормоны для лечения какого-то сопутствующего заболевания, то лечение остеопороза продолжается весь период приема гормонов.
Для лечения остеопороза рекомендован постоянный прием препаратов кальция и витамина «D» без перерывов на весь курс лечения, так как это является строительным материалом для костной ткани. Препараты кальция выпускаются в виде нескольких кальциевых солей и различных форм.
Выбор препарата кальция и витамина «D» зависит от возраста, сопутствующих заболеваний пациентов.
АЛЬФАДОЛ-Са
Препарат, содержащий кальция карбонат и активный метаболит витамина «D» (альфакальцидол), то есть витамин «D» в этом препарате находится в легко усваиваемой форме. Этот препарат назначается пожилым пациентам с остеопорозом и пациентам с заболеваниями почек. Является препаратом выбора при тяжелом остеопорозе. Схема приема: по 1 капсуле 2 раза в день.
ОСТЕОГЕНОН
Оссеин-гидроксиапатитный комплекс, назначается по 2 таб 2 раза в день, обладает смешанным механизмом действия. Назначается совместно с раствором витамина «D3» в каплях (12-14 капель 1 раз в неделю). Значительно ускоряет сроки консолидации переломов.
Кроме постоянного приема препарата Са и витамина «D», врач должен назначить препараты, нормализующие костный обмен. Они действуют непосредственно на клетки костной ткани. При их приеме образование костной ткани начинает преобладать над ее рассасыванием, и кость становится более плотной и прочной. Выбор препарата зависит от конкретной клинической ситуации (тяжесть остеопороза, наличие противопоказаний к конкретному препарату), а при назначении бисфосфонатов — также и от предпочтите-льного пути введения (перорально или внутривенно). Чаще всего назначаются бисфосфанаты. Эти препараты действуют на клетки, разрушающие костную ткань (действуют на костную резорбцию), при этом синтез костной ткани начинает преобладать над разрушением. К этим препаратам относятся алендронат (БИНОСТО), ризедронат, ибандронат (ВИВАНАТ), золедроновая кислота.
НАТЕКАЛЬ1000
Препарат, регулирующий Витамин — кальциево-фосфорный обмен. Страна производитель препарата — Италия. Препарат появился на российском рынке недавно, поэтому еще нет страха за наличие копий и подделок в аптечной сети.
Одна таблетка НАТЕКАЛЬ1000 состоит из 1500 мг кальция карбоната (600 мг алиментарного кальция) и 1000 МЕ (0,025) колекальциферола ( нативного витамина D3), то есть полностью покрывает суточную потребность в препарате кальция и витамине «D» у больного с остеопорозом, остеопенией. Впервые можно восполнить суточную потребность в кальции и витамине «D», при помощи всего лишь одной таблетки в сутки, без дополнительного приема вимамина «D» в каплях и капсулах.
У бисфосфанатов доказанная эффективность:
- У женщин в постменопаузе бисфосфонаты повышают костную плотность в поясничном отделе позвоночника и в бедре, а также снижают риск переломов позвонков.
- У женщин в постменопаузе алендронат (БИНОСТО), Золедроновая кислота и ризедронат снижают риск переломов бедра, а алендронат — и переломов предплечья.
- Золедроновая кислота, назначенная после перелома проксимального отдела бедра, снижает частоту всех новых клинических переломов и риск летальных исходов независимо от их причины.
Золедроновая кислота
Зарекомендовала себя как высокоэффективный бисфосфонат. Избирательно действует на клетки костной ткани, которые отвечают за ее разрушение, не оказывая нежелательного воздействия на формирование, минерализацию и механические свойства костной ткани.
БИНОСТО (алендроновая кислота)
Золотой стандарт в лечении остеопороза (для приема внутрь). Один из самых изученных препаратов для лечения остеопороза.
ВИВАНАТ (ибандроновая кислота)
Ингибитор костной резорбции. Отличается удобством в применении, хорошей переносимостью.
ФОРСТЕО (терипаратид) 20 мкг
Наиболее эффективный препарат для лечения остеопороза на сегодняшний день. Для начала лечения препаратом форстео необходимо провести ряд исследований крови: общий кальций, паратиреоидный гормон, щелочная фосфотаза, креатин, общий анализ крови (ИНВИТРО). Также следует исключить наличие метастазов в кости при подозрении на онкологические заболевания.
ДЕНОСУМАБ 60 мг
Деносумаб увеличивает костную плотность позвонков, проксимальных отделов бедренной кости и дистального отдела предплечья, уменьшает риск переломов тел позвонков, бедра и других периферических переломов у женщин с постменопаузальным остеопорозом. Продолжительность лечения до 6 лет.
СТРОНЦИЯ РАНЕЛАТ 2г.
Вторая линия лечения остеопороза. Применение стронция ранелата в рамках зарегистрированных показаний рекомендован для лечения тяжелых форм остеопороза для тех пациентов, у которых имеются противопоказания или непереносимость других препаратов, зарегистрированных для лечения остеопороза при отсутствии ишемической болезни сердца, неконтролируемой артериальной гипертензии, заболеваний периферических артерий и цереброваскулярных заболеваний.
Как судить об эффективности медикаментозного лечения?
- Оценка эффективности лечения остеопороза проводится с помощью рентгеновской денситометрии через 1-3 года от начала терапии, но не чаще чем 1 раз в год.
- Для динамической оценки рекомендуется использовать рентгеновский денситометр одного и того же производителя.
- Лечение считается эффективным, если минеральная плотность костной ткани увеличилась или осталась на прежнем уровне.
- Продолжающаяся потеря костной массы по денситометрии или новый перелом кости могут свидетельствовать о плохой приверженности пациента рекомендованному лечению или неэффективности проводимого лечения.
- Измерение уровней маркёров формирования костного матрикса возможно уже через 3 месяца лечения с целью прогноза эффективности лечения. Изменение уровня маркеров на 30% и больше (снижение при антирезорбтивной терапии и увеличение при лечении терипаратидом) прогнозирует хорошую эффективность лечения.
Скачать
Диагностика и лечение остеопороза
1. Национальный фонд остеопороза. Руководство клинициста по профилактике и лечению остеопороза. Вашингтон, округ Колумбия: Национальный фонд остеопороза; 2014 ….
2. Министерство здравоохранения и социальных служб США. Здоровье костей и остеопороз: отчет главного хирурга. Роквилл, штат Мэриленд: Министерство здравоохранения и социальных служб США, Управление главного хирурга; 2004.
3. Национальный фонд остеопороза. Здоровье костей Америки: состояние остеопороза и низкой костной массы в нашей стране.Вашингтон, округ Колумбия: Национальный фонд остеопороза; 2002.
4. Всемирная организация здравоохранения. Научная группа ВОЗ по оценке остеопороза на уровне первичной медико-санитарной помощи: итоговый отчет о заседании. Брюссель, Бельгия; 5–7 мая 2004 г. Женева, Швейцария: Всемирная организация здравоохранения; 2007.
5. Целевая группа по профилактическим услугам США. Скрининг на остеопороз: рекомендации Рабочей группы США по профилактическим услугам. Энн Интерн Мед. . 2011. 154 (5): 356–364.
6. Наяк С., Олькин I, Лю Х, и другие. Мета-анализ: точность количественного ультразвукового исследования для выявления пациентов с остеопорозом. Энн Интерн Мед. . 2006. 144 (11): 832–841.
7. Schousboe JT, Пастух Ж.А., Билезикян Ю.П., Баим С. Краткое содержание конференции Международного общества клинической денситометрии 2013 года по разработке позиции по денситометрии костей. Дж Клин Денситом .2013. 16 (4): 455–466.
8. Гурлей М.Л., Хорошо JP, Preisser JS, и другие.; Изучение группы исследования остеопоротических переломов. Интервал измерения плотности костной ткани и переход к остеопорозу у пожилых женщин. N Engl J Med . 2012. 366 (3): 225–233.
9. Ягодный СД, Самельсон Э.Дж., Pencina MJ, и другие. Повторите скрининг минеральной плотности костной ткани и прогнозируйте перелом бедра и большой остеопоротический перелом. ЯМА . 2013. 310 (12): 1256–1262.
10. Фитцпатрик Л.А. Вторичные причины остеопороза. Mayo Clin Proc . 2002. 77 (5): 453–468.
11. Коэн А, Флейшер Дж., Freeby MJ, МакМахон DJ, Ирани Д, Шейн Э. Клинические характеристики и использование лекарств у женщин в пременопаузе с остеопорозом и низкой МПК: опыт справочного центра по остеопорозу. J Womens Health (Larchmt) .2009. 18 (1): 79–84.
12. Эбелинг ПР. Клиническая практика. Остеопороз у мужчин. N Engl J Med . 2008; 358 (14): 1474–1482.
13. Cerdá Gabaroi D, Перис П, Monegal A, и другие. Поиск скрытых вторичных причин у женщин в постменопаузе с остеопорозом. Менопауза . 2010. 17 (1): 135–139.
14. Ведение остеопороза у женщин в постменопаузе: Заявление о позиции Североамериканского общества менопаузы в 2010 году. Менопауза . 2010. 17 (1): 25–54.
15. Всемирная организация здравоохранения. Профилактика и лечение остеопороза: отчет научной группы ВОЗ. Женева, Швейцария; 2003. http://whqlibdoc.who.int/trs/WHO_TRS_921.pdf. По состоянию на 6 сентября 2014 г.
16. Crandall CJ, Ньюберри SJ, Диамант А, и другие. Сравнительная эффективность фармакологических методов лечения для предотвращения переломов: обновленный систематический обзор. Энн Интерн Мед. .2014. 161 (10): 711–723.
17. Каринканта S, Пииртола М, Sievänen H, Ууси-Раси К, Каннус П. Подходы физиотерапии для снижения риска падений и переломов у пожилых людей. Нат Рев Эндокринол . 2010. 6 (7): 396–407.
18. Мойер В.А.; Целевая группа по профилактическим услугам США. Профилактика падений среди пожилых людей, проживающих в сообществах: рекомендация Целевой группы США по профилактическим услугам. Энн Интерн Мед. .2012. 157 (3): 197–204.
19. Джангрегорио Л.М., Папайоанну А, Макинтайр, штат Нью-Джерси, и другие. Слишком подходит для перелома: рекомендации по упражнениям для людей с остеопорозом или остеопоротическим переломом позвонков. Остеопорос Инт . 2014. 25 (3): 821–835.
20. Американское гериатрическое общество. Руководство AGS / BGS по клинической практике по предотвращению падений у пожилых людей. Нью-Йорк, штат Нью-Йорк: Американское гериатрическое общество; 2010.
21.Сантессо Н, Карраско-Лабра А, Бриньярделло-Петерсон Р. Протекторы бедра для предотвращения переломов бедра у пожилых людей. Кокрановская база данных Syst Rev . 2014; (3): CD001255.
22. Юн В., Маалуф Н.М., Сахаи К. Влияние курения на метаболизм костей. Остеопорос Инт . 2012. 23 (8): 2081–2092.
23. Maurel DB, Буассо Н, Бенхаму CL, Яффр К. Алкоголь и кости: обзор эффектов доз и механизмов. Остеопорос Инт . 2012; 23 (1): 1–16.
24. Кузов JJ, Бергманн П., Боонен С, и другие. Немедикаментозное лечение остеопороза: консенсус Бельгийского костного клуба. Остеопорос Инт . 2011. 22 (11): 2769–2788.
25. Самбрук П.Н., Кэмерон ID, Чен Дж.С., и другие. Работает ли повышенное воздействие солнечного света как стратегия улучшения статуса витамина D у пожилых людей: кластерное рандомизированное контролируемое исследование. Остеопорос Инт . 2012. 23 (2): 615–624.
26. MacLean C, Ньюберри S, Maglione M, и другие. Систематический обзор: сравнительная эффективность методов лечения для предотвращения переломов у мужчин и женщин с низкой плотностью костей или остеопорозом. Энн Интерн Мед. . 2008. 148 (3): 197–213.
27. Лекарства от постменопаузального остеопороза. Мед Летт Лекарства Ther . 2014; 56 (1452): 91–96.
28. First Databank, Inc.AnalySource Ежемесячно. http://www.fdbhealth.com/policies/drug-pricing-policy. Доступ 5 сентября 2014 г.
29. Sweet MG, Сладкий JM, Иеремия МП, Галазка СС. Диагностика и лечение остеопороза. Ам Фам Врач . 2009. 79 (3): 193–200.
30. Ringe JD, Фабер Х, Фараманд П., Дорст А. Эффективность ризедроната у мужчин с первичным и вторичным остеопорозом: результаты 1-летнего исследования. Ревматол Инт .2006. 26 (5): 427–431.
31. Orwoll E, Эттингер М, Вайс С, и другие. Алендронат для лечения остеопороза у мужчин. N Engl J Med . 2000. 343 (9): 604–610.
32. Adachi JD, Сааг КГ, Дельмас П.Д., и другие. Двухлетний эффект алендроната на минеральную плотность костей и переломы позвонков у пациентов, получающих глюкокортикоиды: рандомизированное двойное слепое плацебо-контролируемое расширенное исследование. Революционный артрит . 2001. 44 (1): 202–211.
33. Wallach S, Коэн С, Рид Д.М., и другие. Влияние лечения ризедронатом на плотность костей и переломы позвонков у пациентов, получающих кортикостероидную терапию. Кальциф Ткань Инт . 2000. 67 (4): 277–285.
34. Чеснут СН III, Скаг А, Кристиансен C, и другие. Пероральное исследование перелома позвонков при остеопорозе ибандроната в Северной Америке и Европе (BONE).Влияние ежедневного или периодического перорального приема ибандроната на риск переломов при постменопаузальном остеопорозе. Дж Боун Минер Рес . 2004. 19 (8): 1241–1249.
35. Siris ES, Харрис ST, Розен CJ, и другие. Приверженность к терапии бисфосфонатами и частота переломов у женщин с остеопорозом: связь с переломами позвонков и непозвонков из 2 баз данных заявлений США. Mayo Clin Proc . 2006. 81 (8): 1013–1022.
36.Боонен С, Регинстер JY, Кауфман Дж. М., и другие. Риск переломов и терапия золедроновой кислотой у мужчин с остеопорозом. N Engl J Med . 2012. 367 (18): 1714–1723.
37. Delmas PD, Адами С, Стругала С, и другие. Внутривенные инъекции ибандроната у женщин в постменопаузе с остеопорозом: результаты исследования дозирования внутривенного введения через год. Революционный артрит . 2006. 54 (6): 1838–1846.
38. Черный ДМ, Шварц А.В., Энсруд К.Е., и другие.; FLEX Research Group. Эффекты от продолжения или прекращения приема алендроната после 5 лет лечения: Долгосрочное продление лечения переломов (FLEX): рандомизированное исследование. ЯМА . 2006. 296 (24): 2927–2938.
39. Woo SB, Хельштейн JW, Kalmar JR. Описательный [исправленный] обзор: бисфосфонаты и остеонекроз челюстей [опубликованное исправление опубликовано в Ann Intern Med.2006; 145 (3): 235]. Энн Интерн Мед. . 2006. 144 (10): 753–761.
40. Мейер Р.П., Perneger TV, Штерн R, Риццоли Р, Питер RE. Увеличение частоты атипичных переломов бедренной кости, связанных с применением бисфосфонатов. Арк Интерн Мед. . 2012. 172 (12): 930–936.
41. Сильверман С.Л., Азрия М. Обезболивающая роль кальцитонина после остеопоротического перелома. Остеопорос Инт . 2002. 13 (11): 858–867.
42. Оверман РА, Borse M, Gourlay ML. Использование кальцитонина лосося и связанный с этим риск рака. Энн Фармакотер . 2013. 47 (12): 1675–1684.
43. Черный ДМ, Билезикян Ю.П., Энсруд К.Е., и другие.; Исследователи исследования PaTH. Один год приема алендроната после одного года приема паратироидного гормона (1–84) при остеопорозе. N Engl J Med . 2005. 353 (6): 555–565.
44. Каммингс С.Р., Сан-Мартин Дж., Макклунг MR, и другие.; СВОБОДА Испытание. Деносумаб для профилактики переломов у женщин в постменопаузе с остеопорозом [опубликованная поправка опубликована в N Engl J Med. 2009; 361 (19): 1914]. N Engl J Med . 2009. 361 (8): 756–765.
45. Джамал С.А., Юнггрен О, Stehman-Breen C, и другие. Влияние деносумаба на переломы и минеральную плотность костей на уровне функции почек. Дж Боун Минер Рес . 2011; 26 (8): 1829–1835.
46.Коли Дж. А., Роббинс Дж, Чен З, и другие.; Исследователи Инициативы по охране здоровья женщин. Влияние эстрогена и прогестина на риск переломов и минеральную плотность костей: рандомизированное исследование «Инициатива женского здоровья». ЯМА . 2003. 290 (13): 1729–1738.
47. Линдси Р., Галлахер Дж. К., Клеерекопер М, Pickar JH. Влияние более низких доз конъюгированных конских эстрогенов с медроксипрогестерона ацетатом и без него на кости у женщин в раннем постменопаузе. ЯМА . 2002. 287 (20): 2668–2676.
48. Левецки Э.М. Мониторинг плотности костной ткани для мониторинга терапии остеопороза в клинической практике. Ам Фам Врач . 2010. 82 (7): 749–754.
49. Расчески БП, Раппапорт М, Каверли ТиДжей, Мэтлок ДД. «Срок» для сканирования: изучение возможности мониторинга денситометрии. JAMA Intern Med . 2013; 173 (21): 2007–2009.
Рассмотрение подхода, фармакологическая терапия, диетические меры
Porter JL, Varacallo M.Остеопороз. 2020 Январь [Medline]. [Полный текст].
Джонстон CB, Дагар М. Остеопороз у пожилых людей. Мед Клин Норт Ам . 2020 Сентябрь 104 (5): 873-884. [Медлайн].
Lynn SG, Sinaki M, Westerlind KC. Характеристики баланса лиц с остеопорозом. Arch Phys Med Rehabil . 1997 г., 78 (3): 273-7. [Медлайн].
[Рекомендации] Cosman F, de Beur SJ, LeBoff MS, Lewiecki EM, Tanner B, Randall S, et al.Руководство клинициста по профилактике и лечению остеопороза. Остеопорос Инт . 2014 25 октября (10): 2359-81. [Медлайн]. [Полный текст].
[Рекомендации] Schousboe JT, Shepherd JA, Bilezikian JP, Baim S. Краткое изложение конференции Международного общества клинической денситометрии 2013 года по разработке позиции по денситометрии костей. Дж Клин Денситом . 2013 окт-дек. 16 (4): 455-66. [Медлайн].
Gosfield E 3rd, Bonner FJ Jr.Оценка минеральной плотности костной ткани при остеопорозе. Am J Phys Med Rehabil . 2000 май-июнь. 79 (3): 283-91. [Медлайн].
Kanis JA, McCloskey EV, Johansson H, Oden A, Melton LJ 3rd, Khaltaev N. Справочный стандарт для описания остеопороза. Кость . 2008 г., 42 (3): 467-75. [Медлайн].
Сильверман SL. Отбор пациентов для лечения остеопороза. Энн Н. И Акад. Наук . 2007 ноябрь 1117: 264-72. [Медлайн].
Czerwinski E, Badurski JE, Marcinowska-Suchowierska E, Osieleniec J. Текущее понимание остеопороза в соответствии с позицией Всемирной организации здравоохранения (ВОЗ) и Международного фонда остеопороза. Ortop Traumatol Rehabil . 2007 июль-август. 9 (4): 337-56. [Медлайн].
Канис Я. Оценка риска переломов и ее применение к скринингу на постменопаузальный остеопороз: синопсис отчета ВОЗ. Исследовательская группа ВОЗ. Остеопорос Инт . 1994 4 ноября (6): 368-81. [Медлайн].
[Руководство] Камачо П.М., Петак С.М., Бинкли Н., Диаб Д.Л., Элдейри Л.С., Фаруки А. и др. АМЕРИКАНСКАЯ АССОЦИАЦИЯ КЛИНИЧЕСКИХ ЭНДОКРИНОЛОГОВ / АМЕРИКАНСКИЙ КОЛЛЕДЖ ЭНДОКРИНОЛОГИИ ОБНОВЛЕНИЕ КЛИНИЧЕСКОЙ ПРАКТИКИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ПОСТМЕНОПАУЗНОГО ОСТЕОПОРОЗА-2020. Эндокр Практик . 2020 май. 26 (Дополнение 1): 1-46. [Медлайн]. [Полный текст].
[Рекомендации] Бакли Л., Гайатт Г., Финк Х.А., Кэннон М., Гроссман Дж., Хансен К.Э. и др.Руководство Американского колледжа ревматологии по профилактике и лечению остеопороза, вызванного глюкокортикоидами, 2017 г. Центр лечения артрита (Хобокен) . 2017 Август 69 (8): 1095-1110. [Медлайн]. [Полный текст].
Аль Саеди А., Ступка Н., Дуке Г. Патогенез остеопороза. Handb Exp Pharmacol . 2020 16 апреля. 115 (12): 3318-25. [Медлайн].
Majumdar SR, Lier DA, Beaupre LA, Hanley DA, Maksymowych WP, Juby AG и др.Специалист по лечению остеопороза у пациентов с переломом шейки бедра: результаты анализа экономической эффективности, проведенного в рамках рандомизированного исследования. Arch Intern Med . 2009 12 января. 169 (1): 25-31. [Медлайн].
Cosman F, de Beur SJ, LeBoff MS, Lewiecki EM, Tanner B, Randall S, et al. Руководство клинициста по профилактике и лечению остеопороза. Остеопорос Инт . 2014 25 октября (10): 2359-81. [Медлайн].
Мэйбери К. Укрепление коммуникации о здоровье костей.Гэллап. Доступно по адресу http://www.gallup.com/poll/5851/Strengtning-Communication-Bone-Health.aspx?g_source=osteoporosis&g_medium=search&g_campaign=tiles. 23 апреля 2002 г .; Дата обращения: 21 января 2021 г.
Хаас А.В., ЛеБофф М.С. Остеоанаболические агенты при остеопорозе. J Endocr Soc . 1 августа 2018 г. 2 (8): 922-932. [Медлайн].
Всемирная организация здравоохранения. Научная группа ВОЗ по оценке остеопороза на уровне первичной медико-санитарной помощи: итоговый отчет совещания.Доступно на http://www.who.int/chp/topics/Osteoporosis.pdf. 2007; Дата обращения: 21 января 2021 г.
Кларк Б. Анатомия и физиология нормальной кости. Clin J Am Soc Nephrol . 2008 г., 3 ноября, приложение 3: S131-9. [Медлайн].
Bono CM, Einhorn TA. Обзор остеопороза: патофизиология и факторы, определяющие прочность костей. Eur Spine J . 12 октября 2003 г., приложение 2: S90-6. [Медлайн].
Seeman E, Delmas PD.Качество костей — материальная и структурная основа прочности и хрупкости костей. N Engl J Med . 2006 25 мая. 354 (21): 2250-61. [Медлайн].
С. Танака, К. Накамура, Н. Такахас. Роль RANKL в физиологической и патологической резорбции кости и терапевтических средствах, направленных на сигнальную систему RANKL-RANK. Иммунол Ред. . 2005. 208: 30-49. [Полный текст].
Mora S, Gilsanz V. Определение максимальной костной массы. Endocrinol Metab Clin North Am .2003 марта 32 (1): 39-63. [Медлайн].
Föger-Samwald U, Dovjak P, Azizi-Semrad U, Kerschan-Schindl K, Pietschmann P. Остеопороз: патофизиология и варианты лечения. ИСКЛЮЧИТЕЛЬНО J . 2020.19: 1017-1037. [Медлайн].
Raisz LG. Патогенез остеопороза: концепции, конфликты, перспективы. Дж. Клин Инвест . 2005 декабрь 115 (12): 3318-25. [Медлайн].
Jilka RL, Hangoc G, Girasole G, Passeri G, Williams DC, Abrams JS и др.Повышенное развитие остеокластов после потери эстрогена: посредничество интерлейкина-6. Наука . 1992 г. 3 июля. 257 (5066): 88-91. [Медлайн].
Föger-Samwald U, Dovjak P, Azizi-Semrad U, Kerschan-Schindl K, Pietschmann P. Остеопороз: патофизиология и варианты лечения. ИСКЛЮЧИТЕЛЬНО J . 2020.19: 1017-1037. [Медлайн].
Клайн-Смит А., Аксельбаум А., Шашкова Е., Чакраборти М., Сэнфорд Дж., Панесар П. и др. Овариэктомия активирует хроническое воспаление низкой степени, опосредованное Т-клетками памяти, которое способствует остеопорозу у мышей. J Bone Miner Res . 2020 июн. 35 (6): 1174-1187. [Медлайн].
Demontiero O, Vidal C, Duque G. Старение и потеря костной массы: новые идеи для клинициста. Ther Adv Musculoskelet Dis . 2012 Апрель 4 (2): 61-76. [Медлайн].
Варринер А.Х., Паткар Н.М., Кертис Дж. Р., Делзелл Э., Гэри Л., Килгор М. и др. Какие переломы чаще всего связаны с остеопорозом ?. J Clin Epidemiol . 2011 Январь 64 (1): 46-53. [Медлайн].
Каммингс С.Р., Мелтон Л.Дж.Эпидемиология и исходы остеопоротических переломов. Ланцет . 2002 18 мая. 359 (9319): 1761-7. [Медлайн].
Розен CJ, Тененхаус А. Биохимические маркеры обновления костной ткани. Ознакомьтесь с лабораторными исследованиями, отражающими состояние костей. Постградская медицина . Октябрь 1998. 104 (4): 101-2, 107-10.
Nusse R. Передача сигналов Wnt при заболевании и развитии. Ячейка Res . 2005 15 января (1): 28-32. [Медлайн].
Ling L, Nurcombe V, Cool SM.Передача сигналов Wnt контролирует судьбу мезенхимальных стволовых клеток. Ген . 2009 15 марта. 433 (1-2): 1-7. [Медлайн].
Питтенгер М.Ф., Маккей А.М., Бек С.К., Джайсвал Р.К., Дуглас Р., Моска Д.Д. и др. Многолинейный потенциал мезенхимальных стволовых клеток взрослого человека. Наука . 1999, 2 апреля. 284 (5411): 143-7. [Медлайн].
Рао Т.П., Кюль М. Обновленный обзор сигнальных путей Wnt: прелюдия к большему. Circ Res . 25 июня 2010 г.106 (12): 1798-806. [Медлайн].
Clevers H, Nusse R. Передача сигналов Wnt / ß-катенина и заболевание. Ячейка . 2012 июн 8. 149 (6): 1192-205. [Медлайн].
Кришнан В., Брайант Х.Ю., Макдугалд О.А. Регулирование костной массы с помощью передачи сигналов Wnt. Дж. Клин Инвест . 2006 май. 116 (5): 1202-9. [Медлайн]. [Полный текст].
Бойден Л.М., Мао Дж., Бельски Дж., Мицнер Л., Фархи А., Митник М.А. и др. Высокая плотность костей из-за мутации белка, связанного с рецепторами ЛПНП 5. N Engl J Med . 2002 16 мая. 346 (20): 1513-21. [Медлайн].
Van Wesenbeeck L, Cleiren E, Gram J, Beals RK, Bénichou O, Scopelliti D, et al. Шесть новых миссенс-мутаций в гене белка 5, связанного с рецептором ЛПНП (LRP5), в различных условиях с повышенной плотностью костей. Ам Дж. Хам Генет . 2003 Mar.72 (3): 763-71. [Медлайн]. [Полный текст].
Levasseur R, Lacombe D, de Vernejoul MC. Мутации LRP5 при синдроме остеопороза-псевдоглиомы и нарушениях с высокой костной массой. Костный сустав позвоночника . 2005 Май. 72 (3): 207-14. [Медлайн].
Zhu Y, Sun Z, Han Q, Liao L, Wang J, Bian C и др. Мезенхимальные стволовые клетки человека подавляют пролиферацию раковых клеток, секретируя DKK-1. Лейкемия . 2009 Май. 23 (5): 925-33. [Медлайн].
Kawano Y, Kypta R. Секретные антагонисты пути передачи сигнала Wnt. J Cell Sci . 1 июля 2003 г., 116: 2627-34. [Медлайн].
Кайзер М., Мит М., Либиш П., Оберлендер Р., Радемахер Дж., Якоб С. и др.Концентрация DKK-1 в сыворотке крови коррелирует со степенью заболевания костей у пациентов с множественной миеломой. Eur J Haematol . 2008 июн. 80 (6): 490-4. [Медлайн].
Tai N, Inoue D. [Антитело против Dickkopf1 (Dkk1) как костный анаболический агент для лечения остеопороза]. Клин Кальций . 2014 24 января (1): 75-83. [Медлайн].
Bonewald LF. Удивительный остеоцит. J Bone Miner Res . 2011 26 февраля (2): 229-38.[Медлайн]. [Полный текст].
Li X, Zhang Y, Kang H, Liu W, Liu P, Zhang J и др. Склеростин связывается с LRP5 / 6 и противодействует канонической передаче сигналов Wnt. Дж. Биол. Хим. . 2005 г. 20 мая. 280 (20): 19883-7. [Медлайн].
FDA одобрило новое лечение остеопороза у женщин в постменопаузе с высоким риском переломов. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Доступно по адресу https://www.fda.gov/news-events/press-announcements/fda-approves-new-treatment-osteoporosis-postmenopausal-women-high-risk-fracture.09 апреля 2019 г .; Дата обращения: 21 января 2021 г.
Ringe JD, Farahmand P. Достижения в лечении кортикостероидного остеопороза с помощью бисфосфонатов. Clin Rheumatol . 2007 26 апреля (4): 474-84. [Медлайн].
Dennison EM, Syddall HE, Sayer AA, Gilbody HJ, Cooper C. Вес при рождении и вес в 1 год являются независимыми детерминантами костной массы в седьмом десятилетии: когортное исследование Хартфордшира. Педиатр Рес .2005 апр. 57 (4): 582-6. [Медлайн].
Фолл С., Хиндмарш П., Деннисон Э, Келлингрей С., Баркер Д., Купер С. Программирование секреции гормона роста и минеральной плотности костей у пожилых мужчин: гипотеза. Дж. Клин Эндокринол Метаб . 1998, январь, 83 (1): 135-9. [Медлайн].
Марини Ф, Чианферотти Л, Брэнди МЛ. Эпигенетические механизмы в биологии костей и остеопорозе: могут ли они определять терапевтический выбор ?. Int J Mol Sci . 2016 12 августа.17 (8): [Medline].
Коланджело Л., Биамонте Ф, Пепе Дж., Чиприани С., Минисола С. Понимание и лечение вторичного остеопороза. Эксперт Рев Эндокринол Метаб . 2019 14 марта (2): 111-122. [Медлайн].
Кельман А, переулок NE. Ведение вторичного остеопороза. Лучший Практик Res Clin Rheumatol . 2005 декабря 19 (6): 1021-37. [Медлайн].
Адамс Дж. С., Сонг К. Ф., Канторович В. Быстрое восстановление костной массы у мужчин с гиперкальциурией и остеопорозом, получавших гидрохлоротиазид. Энн Интерн Мед. . 1999 г. 20 апреля. 130 (8): 658-60. [Медлайн].
Манн ГБ, Канг Ю.К., Бренд C, Эбелинг ПР, Миллер Дж. Вторичные причины низкой костной массы у пациентов с раком груди: необходимость большей бдительности. Дж Клин Онкол . 2009, 1. 27 (22): 3605-10. [Медлайн].
Холик MF. Дефицит витамина D. N Engl J Med . 2007 июля 19, 357 (3): 266-81. [Медлайн].
di Munno O, Mazzantini M, Sinigaglia L, Bianchi G, Minisola G, Muratore M и др.Влияние низких доз метотрексата на плотность костей у женщин с ревматоидным артритом: результаты многоцентрового поперечного исследования. Дж. Ревматол . 2004 июля 31 (7): 1305-9. [Медлайн].
Migliaccio S, Brama M, Malavolta N. Управление остеопорозом, вызванным глюкокортикоидами: роль терипаратида. Ther Clin Risk Manag . 2009 5 (2): 305-10. [Медлайн]. [Полный текст].
van Staa TP, Leufkens HG, Cooper C. Эпидемиология остеопороза, вызванного кортикостероидами: метаанализ. Остеопорос Инт . 2002 13 октября (10): 777-87. [Медлайн].
Licata AA. Проблемы оценки риска переломов с помощью DXA: изменение представлений о прочности и плотности костей. Aerosp Med Hum Perform . 2015 Июль 86 (7): 628-32. [Медлайн].
Оценка риска переломов и ее применение для скрининга постменопаузального остеопороза. Отчет исследовательской группы ВОЗ. Представитель World Health Organ Tech Rep Ser . 1994 г.843: 1-129. [Медлайн].
Lyles KW, Schenck AP, Colón-Emeric CS. Переломы бедра и другие остеопоротические переломы увеличивают риск последующих переломов у обитателей домов престарелых. Остеопорос Инт . 2008 19 августа (8): 1225-33. [Медлайн]. [Полный текст].
Финк Х.А., Кусковски М.А., Тейлор Б.К., Шоусбой Д.Т., Орволл Э.С., Энсруд К.Э. Связь болезни Паркинсона с ускоренной потерей костной массы, переломами и смертностью у пожилых мужчин: исследование остеопоротических переломов у мужчин (MrOS). Остеопорос Инт . 2008 сентября 19 (9): 1277-82. [Медлайн].
Синаки М. Физические упражнения и остеопороз. Arch Phys Med Rehabil . 1989 марта 70 (3): 220-9. [Медлайн].
Yaturu S, DjeDjos S, Alferos G, Deprisco C. Изменения минеральной плотности костной ткани при андрогенной депривационной терапии рака простаты и ответ на антирезорбтивную терапию. Рак предстательной железы Простатический Dis . 2006. 9 (1): 35-8. [Медлайн].
Буско М.Химическое вещество в зубной пасте связано с остеопорозом у женщин. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/8. 26 июня 2019 г .; Дата обращения: 27 июня 2019 г.
Hansen D, Bazell C, Pelizzari P, Pyenson B. Стоимость программы Medicare при остеопоротических переломах: клиническое и финансовое бремя важного последствия остеопороза. Доступно по адресу https://static1.squarespace.com/static/5c0860aff793924efe2230f3/t/5d76b949deb7e9086ee3d7dd/1568061771769/Medicare+Cost+of+Osteoporotic+Fractures+201
.pdf. Август 2019; Дата обращения: 21 января 2021 г.
Купер С., Кэмпион Дж., Мелтон Л.Дж. 3-й. Переломы бедра у пожилых людей: мировая проекция. Остеопорос Инт . 1992, 2 (6): 285-9. [Медлайн].
Кто кандидаты для профилактики и лечения остеопороза ?. Остеопорос Инт . 1997. 7 (1): 1-6. [Медлайн].
Jensen GF, Christiansen C, Boesen J, Hegedüs V, Transbøl I. Эпидемиология переломов позвоночника и длинных костей в постменопаузе.Единый подход к постменопаузальному остеопорозу. Clin Orthop Relat Res . 1982 июн. 75–81. [Медлайн].
Мелтон Л.Дж., 3-й, Кан Ш., Фрай М.А., Ванер Х.В., О’Фаллон В.М., Риггс Б.Л. Эпидемиология переломов позвонков у женщин. Am J Epidemiol . 1989 Май. 129 (5): 1000-11. [Медлайн].
Смит Р., Вордсворт П. Остеопороз. Клинические и биохимические заболевания скелета . 2005. 123.
Chon KS, Sartoris DJ, Brown SA, Clopton P.Связанная с алкоголизмом потеря костной массы позвоночника и бедра у воздерживающихся мужчин-алкоголиков, измеренная с помощью двойной рентгеновской абсорбциометрии. Скелетная радиология . 1992. 21 (7): 431-6. [Медлайн].
Роббинс Дж., Арагаки А.К., Куперберг С., Уоттс Н., Вактавски-Венде Дж., Джексон Р.Д. и др. Факторы, связанные с 5-летним риском перелома шейки бедра у женщин в постменопаузе. JAMA . 2007 28 ноября. 298 (20): 2389-98. [Медлайн].
Басс М.А., Шарма А., Нахар В.К., Челф С., Зеллер Б., Фам Л. и др.Минеральная плотность костной ткани у мужчин и женщин в возрасте от 35 до 50 лет. Дж. Ам Остеопат Асс . 1 июня 2019 г. 119 (6): 357-363. [Медлайн]. [Полный текст].
Вулф Д., Pfleger B. Бремя основных условий опорно-двигательного аппарата. Орган здоровья Bull World . 2003. 81 (9): 646-56. [Медлайн]. [Полный текст].
Бальфур Ф. Китайское «Демографическое цунами». Bloomberg Businessweek. 5 января 2012 г. Доступно по адресу http://www.businessweek.com/magazine/chinas-demographic-tsunami-01052012.html. Доступ: 16 февраля 2012 г.
Морин С.Н., Ликс Л.М., Маджумдар С.Р., Лесли В.Д. Временные тенденции в частоте остеопоротических переломов. Curr Osteoporos Rep . 2013 декабрь 11 (4): 263-9. [Медлайн].
Melton LJ 3rd, Sampson JM, Morrey BF, Ilstrup DM. Эпидемиологические особенности переломов костей таза. Clin Orthop Relat Res . 1981 март-апрель. 43-7. [Медлайн].
Cauley JA, Lui LY, Ensrud KE, Zmuda JM, Stone KL, Hochberg MC и др.Минеральная плотность костей и риск случайных переломов позвоночника у черных и белых женщин. JAMA . 2005 4 мая. 293 (17): 2102-8. [Медлайн].
Здоровье костей и остеопороз: отчет главного хирурга. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб; 2004. [Полный текст].
Бердж Р., Доусон-Хьюз Б., Соломон Д.Х. и др. Заболеваемость и экономическое бремя переломов, связанных с остеопорозом, в США, 2005-2025 гг. J Bone Miner Res . 2007 марта 22 (3): 465-75. [Медлайн].
Hackethal V. Лекарства от остеопороза могут больше всего помочь самым пожилым и больным женщинам. Medscape Medical News . 18 июня 2019 г. Доступно по адресу https://www.medscape.com/viewarticle/
3#vp_2.
Ensrud KE, Kats AM, Boyd CM, Diem SJ, Schousboe JT, Taylor BC, et al. Связь определения заболевания, бремени коморбидности и прогноза с вероятностью перелома бедра среди женщин позднего возраста. JAMA Intern Med . 17 июня 2019 г. [Medline].
Шарон Чоу, доктор медицины, Анджали Гровер, доктор медицины, и Мерил С. ЛеБофф, доктор медицины. Новые остеопоротические / компрессионные переломы позвонков. Доступно на https://www.ncbi.nlm.nih.gov/books/NBK279035/. 19.09.18; Дата обращения: 27.12.20.
Cooper C, Atkinson EJ, Jacobsen SJ и др. Популяционное исследование выживаемости после остеопоротических переломов. Am J Epidemiol . 1 мая 1993 г., 137 (9): 1001-5. [Медлайн].
Кадо Д.М., Браунер В.С., Палермо Л., Невитт М.С., Генант Г.К., Каммингс С.Р. Переломы позвонков и смертность у пожилых женщин: проспективное исследование. Изучение группы исследования остеопоротических переломов. Arch Intern Med . 1999, 14 июня. 159 (11): 1215-20. [Медлайн].
Вестергаард П., Рейнмарк Л., Мосекилде Л. Повышенная смертность пациентов с переломом бедра — эффект преморбидных состояний и осложнений после перелома. Остеопорос Инт .2007 декабря 18 (12): 1583-93. [Медлайн].
Trombetti A, Herrmann F, Hoffmeyer P, Schurch MA, Bonjour JP, Rizzoli R. Выживаемость и потенциальные годы жизни, потерянные после перелома бедра у мужчин и женщин того же возраста. Остеопорос Инт . 2002 Сентябрь 13 (9): 731-7. [Медлайн].
Michel JP, Hoffmeyer P, Klopfenstein C, et al. Прогноз функционального восстановления через 1 год после перелома бедра: типичные профили пациентов с помощью кластерного анализа. Дж. Геронтол А Биол Науки и Медицины .2000 Сентябрь 55 (9): M508-15. [Медлайн].
Линдси Р., Сильверман С.Л., Купер С. и др. Риск нового перелома позвонка через год после перелома. JAMA . 2001 17 января. 285 (3): 320-3. [Медлайн].
Klotzbuecher CM, Ross PD, Landsman PB, et al. Пациенты с предыдущими переломами имеют повышенный риск будущих переломов: краткое изложение литературы и статистический анализ. J Bone Miner Res . 2000 Апрель, 15 (4): 721-39.[Медлайн].
Морин С.Н., Ликс Л.М., Лесли В.Д. Важность предыдущего места перелома для диагностики остеопороза и случайных переломов у женщин. J Bone Miner Res . 2014 июл.29 (7): 1675-80. [Медлайн].
Инструмент Всемирной организации здравоохранения по оценке риска переломов. Доступно на http://www.shef.ac.uk/FRAX/. Доступ: 5 мая 2008 г.
Лесли В.Д., Морин С, Ликс Л.М. Изучение отчетов о рисках переломов и начала лечения остеопороза до и после. Энн Интерн Мед. . 2 ноября 2010 г. 153 (9): 580-6.
Шварц А.В., Виттингхофф Э., Бауэр Д.К. и др. Связь показателей МПК и FRAX с риском перелома у пожилых людей с диабетом 2 типа. JAMA . 1 июня 2011 г. 305 (21): 2184-92. [Медлайн].
Tremollieres FA, Pouilles JM, Drewniak N, Laparra J, Ribot CA, Dargent-Molina P. Прогнозирование риска перелома с использованием МПК и клинических факторов риска у женщин в раннем постменопаузе: чувствительность инструмента FRAX ВОЗ. J Bone Miner Res . 2010 май. 25 (5): 1002-9. [Медлайн]. [Полный текст].
Grisso JA, Kelsey JL, Strom BL, Chiu GY, Maislin G, O’Brien LA, et al. Факторы риска падений как причины перелома бедра у женщин. Группа по изучению перелома северо-восточного бедра. N Engl J Med . 1991, 9 мая. 324 (19): 1326-31. [Медлайн].
Nellans KW, Kowalski E, Chung KC. Эпидемиология переломов дистального отдела лучевой кости. Ручная клиника . 2012 май.28 (2): 113-25. [Медлайн]. [Полный текст].
Sandhu SK, Nguyen ND, Center JR, Pocock NA, Eisman JA, Nguyen TV. Прогноз перелома: оценка точности прогноза алгоритма FRAX и номограммы Гарвана. Остеопорос Инт . 2010 май. 21 (5): 863-71. [Медлайн].
Канис JA, Харви NC, Йоханссон H, Odén A, McCloskey EV, Leslie WD. Обзор инструментов прогнозирования разрушения. Дж Клин Денситом . 2017 июль — 20 сентября (3): 444-450.[Медлайн].
Cooper C, Atkinson EJ, O’Fallon WM, et al. Частота клинически диагностированных переломов позвонков: популяционное исследование, Рочестер, Миннесота, 1985–1989 годы. J Bone Miner Res . 1992 7 февраля (2): 221-7. [Медлайн].
Cook DJ, Guyatt GH, Adachi JD, Clifton J, Griffith LE, Epstein RS и др. Проблемы качества жизни у женщин с переломами позвонков из-за остеопороза. Rheum артрита . 1993 июн. 36 (6): 750-6.[Медлайн].
Schnatz PF, Marakovits KA, Dubois M, O’Sullivan DM. Рекомендации по скринингу и лечению остеопороза: соблюдаются ли они? Менопауза . 2011 18 октября (10): 1072-8. [Медлайн].
Geusens P, Dumitrescu B, van Geel T, van Helden S, Vanhoof J, Dinant GJ. Влияние систематической реализации стратегии выявления клинических случаев на диагностику и терапию постменопаузального остеопороза. J Bone Miner Res .23 июня 2008 г. (6): 812-8. [Медлайн].
[Рекомендации] Скрининг на остеопороз: рекомендация рабочей группы США по профилактическим услугам. Энн Интерн Мед. . 2011 г. 1. 154 (5): 356-64. [Медлайн].
Здоровье костей и остеопороз: отчет главного хирурга . [Полный текст].
Чжу К., Дивайн А., Льюис-младший, Дхаливал СС, Принц Р.Л. Тестирование по времени и измерение минеральной плотности костной ткани для прогнозирования переломов. Arch Intern Med . 2011 Октябрь 10, 171 (18): 1655-61. [Медлайн].
Наяк С., Робертс М.С., Гринспен С.Л. Экономическая эффективность различных стратегий скрининга остеопороза у женщин в постменопаузе. Энн Интерн Мед. . 2011, 6 декабря. 155 (11): 751-61. [Медлайн].
[Рекомендации] Лю Х., Пейдж Н.М., Голдцвейг К.Л., Вонг Э., Чжоу А., Сутторп М.Дж. и др. Скрининг на остеопороз у мужчин: систематический обзор рекомендаций Американского колледжа врачей. Энн Интерн Мед. . 2008 6 мая. 148 (9): 685-701. [Медлайн]. [Полный текст].
Spiegel R, Nawroth PP, Kasperk C. Влияние золедроновой кислоты на риск переломов у мужчин с остеопорозом. Дж Эндокринол Инвест . 2014 марта 37 (3): 229-32. [Медлайн].
Диттмер Д.К., Тизелл Р. Осложнения иммобилизации и постельного режима. Часть 1: Скелетно-мышечные и сердечно-сосудистые осложнения. Врач Джан Фам . 1993 июн.39: 1428-32, 1435-7. [Медлайн].
Guglielmi G, Muscarella S, Bazzocchi A. Комплексный подход к визуализации при остеопорозе: современный обзор и обновление. Рентгенография . 2011 сентябрь-октябрь. 31 (5): 1343-64. [Медлайн].
Khoo BC, Brown K, Cann C и др. Сравнение поверхностной минеральной плотности костной ткани, полученной с помощью QCT и DXA, и показателей T. Остеопорос Инт . 2009 Сентябрь 20 (9): 1539-45. [Медлайн].
Ссылка TM.Осевая и периферическая ККТ. Гульельми Г, изд. Измерения остеопороза и костной денситометрии . Нью-Йорк, штат Нью-Йорк: Springer Heidelberg; 2013. 123-32.
Beaudoin C, Moore L, Gagné M, Bessette L, Ste-Marie LG, Brown JP, et al. Использование инструментов прогнозирования для выявления лиц с риском нетравматических переломов: систематический обзор, метаанализ и мета-регрессия. Остеопорос Инт . 2019 30 апреля (4): 721-740. [Медлайн].
Paunier L.Влияние магния на обмен фосфора и кальция. Monatsschr Kinderheilkd . 1992 сентябрь 140 (9 приложение 1): S17-20. [Медлайн].
Ли В.Й., О, К.В., Ри Э.Дж., Юнг Ч., Ким С.В., Юн Э.Дж. и др. Связь между субклинической дисфункцией щитовидной железы и минеральной плотностью кости шейки бедра у женщин. Arch Med Res . 2006 май. 37 (4): 511-6. [Медлайн].
Танненбаум К., Кларк Дж., Шварцман К., Валленштейн С., Лапински Р., Мейер Д.Результаты лабораторных исследований для выявления вторичных факторов остеопороза у здоровых женщин. Дж. Клин Эндокринол Метаб . 2002 Октябрь 87 (10): 4431-7. [Медлайн].
Лю JM, Zhao HY, Ning G, Chen Y, Zhang LZ, Sun LH и др. IGF-1 как ранний маркер низкой костной массы или остеопороза у женщин в пременопаузе и постменопаузе. Дж. Костяной Шахтер Метаб . 2008. 26 (2): 159-64. [Медлайн].
Васикаран С., Купер С., Истелл Р., Грисмахер А., Моррис Н.А., Тренти Т. и др.Позиция Международного фонда остеопороза и Международной федерации клинической химии и лабораторной медицины в отношении стандартов костных маркеров при остеопорозе. Clin Chem Lab Med . 2011 августа 49 (8): 1271-4. [Медлайн].
Резник Д., Крансдорф М. Остеопороз. Визуализация костей и суставов . Третье издание. 2005. 551.
Hillier TA, Stone KL, Bauer DC, Rizzo JH, Pedula KL, Cauley JA и др. Оценка ценности повторных измерений минеральной плотности костной ткани и прогнозирование переломов у пожилых женщин: исследование остеопоротических переломов. Arch Intern Med . 2007 22 января. 167 (2): 155-60. [Медлайн].
Наяк С., Робертс М.С., Гринспен С.Л. Экономическая эффективность различных стратегий скрининга остеопороза у женщин в постменопаузе. Энн Интерн Мед. . 2011, 6 декабря. 155 (11): 751-61. [Медлайн]. [Полный текст].
Lin JT, Lane JM. Бисфосфонаты. J Am Acad Orthop Surg . 2003 январь-февраль. 11 (1): 1-4. [Медлайн].
Faulkner KG, Wacker WK, Barden HS, Simonelli C, Burke PK, Ragi S, et al.Индекс силы бедра позволяет прогнозировать перелом бедра независимо от плотности кости и длины оси бедра. Остеопорос Инт . 2006. 17 (4): 593-9. [Медлайн].
Prevrhal S, Shepherd JA, Faulkner KG, Gaither KW, Black DM, Lang TF. Сравнение структурного анализа тазобедренного сустава методом ДРА с объемной ККТ. Дж Клин Денситом . 2008 апр-июн. 11 (2): 232-6. [Медлайн].
Kaptoge S, Beck TJ, Reeve J, Stone KL, Hillier TA, Cauley JA и др. Прогнозирование риска перелома бедра с помощью переменных геометрии бедра, измеренных с помощью структурного анализа бедра при исследовании остеопоротических переломов. J Bone Miner Res . 2008 г., 23 (12): 1892-904. [Медлайн]. [Полный текст].
Бек Т.Дж. Распространение DXA за пределы минеральной плотности кости: понимание анализа структуры бедра. Curr Osteoporos Rep . 2007 июн. 5 (2): 49-55. [Медлайн].
Hans D, Barthe N, Boutroy S, Pothuaud L, Winzenrieth R, Krieg MA. Корреляция между оценкой трабекулярной кости, измеренной с использованием переднезадней двухэнергетической рентгеновской абсорбциометрии, и трехмерными параметрами костной микроархитектуры: экспериментальное исследование трупных позвонков человека. Дж Клин Денситом . 2011 июль-сен. 14 (3): 302-12. [Медлайн].
Pothuaud L, Barthe N, Krieg MA, Mehsen N, Carceller P, Hans D. Оценка потенциального использования шкалы губчатой кости для дополнения минеральной плотности кости при диагностике остеопороза: предварительное сопоставление МПК позвоночника, случай-контроль изучать. Дж Клин Денситом . 2009 Апрель-июнь. 12 (2): 170-6. [Медлайн].
Силва BC, Лесли В.Д., Реш Х., Лами О., Лесняк О., Бинкли Н. и др.Оценка трабекулярной кости: неинвазивный аналитический метод, основанный на DXA-изображении. J Bone Miner Res . 2014 29 марта (3): 518-30. [Медлайн].
Schuit SC, van der Klift M, Weel AE, de Laet CE, Burger H, Seeman E, et al. Частота переломов и связь с минеральной плотностью костей у пожилых мужчин и женщин: Роттердамское исследование. Кость . 2004 г., 34 (1): 195-202. [Медлайн].
Имаи К. Современные методы оценки остеопороза и риска переломов. Последние исследования Pat Endocr Metab Immune Drug Discov . 2014 8 (1): 48-59. [Медлайн].
Ян Л., Палермо Л., Блэк Д.М., Истелл Р. Прогнозирование перелома бедра с расчетной силой бедренной кости с помощью анализа методом конечных элементов DXA-сканирований при изучении остеопоротических переломов. J Bone Miner Res . 2014 29 декабря (12): 2594-600. [Медлайн].
Torres-del-Pliego E, Vilaplana L, Güerri-Fernández R, Diez-Pérez A. Измерение качества кости. Curr Rheumatol Rep . 2013 15 ноября (11): 373. [Медлайн].
Prior JC, Vigna YM, Wark JD и др. Потеря костной массы, связанная с пременопаузальной овариэктомией: рандомизированное двойное слепое однолетнее исследование конъюгированного эстрогена или медроксипрогестерона ацетата. J Bone Miner Res . 1997 12 ноября (11): 1851-63. [Медлайн].
Henzell S, Dhaliwal S, Pontifex R и др. Погрешность точности двух веерных рентгеновских абсорбциометрий позвоночника, бедра и предплечья. Дж Клин Денситом . 2000 Зима. 3 (4): 359-64. [Медлайн].
White J, Harris SS, Dallal GE, Dawson-Hughes B. Прецизионное сканирование минеральной плотности бедренной кости при одном сканировании по сравнению с двусторонним. Дж Клин Денситом . 2003 Лето. 6 (2): 159-62. [Медлайн].
Bauer JS, Henning TD, Müeller D, Lu Y, Majumdar S, Link TM. Объемная количественная КТ позвоночника и бедра, полученная с помощью МДКТ с контрастным усилением: коэффициенты пересчета. AJR Am J Roentgenol .2007 май. 188 (5): 1294-301. [Медлайн].
Engelke K, Adams JE, Armbrecht G, et al. Клиническое использование количественной компьютерной томографии и периферической количественной компьютерной томографии в лечении остеопороза у взрослых: официальные положения ISCD 2007 г. Дж Клин Денситом . 2008 Янв-март. 11 (1): 123-62. [Медлайн].
Лю Г., Павлин М., Эйлам О., Дорулла Г., Браунштейн Е., Джонстон С.С. Влияние остеоартроза поясничного отдела позвоночника и бедра на минеральную плотность костей и диагностика остеопороза у пожилых мужчин и женщин. Остеопорос Инт . 1997. 7 (6): 564-9. [Медлайн].
[Рекомендации] Касим А., Форсиа М.А., Маклин Р.М., Денберг Т.Д., для Комитета по клиническим руководствам Американского колледжа врачей. Лечение низкой плотности костей или остеопороза для предотвращения переломов у мужчин и женщин: обновленное руководство по клинической практике Американского колледжа врачей. Энн Интерн Мед. . 9 мая 2017 г. [Полный текст].
Фрибург Д., Тан С, Сра П, Деламартер Р., Бэ Х.Частота последующих переломов позвонков после кифопластики. Позвоночник (Phila Pa 1976) . 2004 15 октября. 29 (20): 2270-6; обсуждение 2277. [Medline].
Моврин И., Венгуст Р., Комадина Р. Переломы смежных позвонков после чрескожной аугментации позвонков при остеопоротическом компрессионном переломе позвоночника: сравнение баллонной кифопластики и вертебропластики. Хирургическая хирургия для лечения травм ортопедической дуги . 2010 сентябрь 130 (9): 1157-66. [Медлайн].
Кастнер М, Straus SE.Инструменты поддержки клинических решений для лечения остеопороза: систематический обзор рандомизированных контролируемых исследований. J Gen Intern Med . 2008 г., 23 (12): 2095-105. [Медлайн]. [Полный текст].
Кнопп Дж. А., Diner BM, Blitz M, Lyritis GP, Rowe BH. Кальцитонин для лечения острой боли при остеопоротических компрессионных переломах позвонков: систематический обзор рандомизированных контролируемых исследований. Остеопорос Инт . 2005 16 октября (10): 1281-90. [Медлайн].
Киршблюм SC.Реабилитационная медицина: принципы и практика. DeLisa JA, Gans BM. Ортезы для позвоночника и верхних конечностей . 3-й. Филадельфия, Пенсильвания: Липпинкотт-Рэйвен; 1998. 635-50.
Stillo СП. Ортезы поясницы. Phys Med Rehab Clin North Am . 1992. 3: 57-94.
[Рекомендации] Eastell R, Rosen CJ, Black DM, Cheung AM, Murad MH, Shoback D. Фармакологическое лечение остеопороза у женщин в постменопаузе: Руководство по клинической практике эндокринного общества *. Дж. Клин Эндокринол Метаб . 2019 1 мая. 104 (5): 1595-1622. [Медлайн].
Герц Б.Дж., Голландия С.Д., Клайн В.Ф., Матушевский Б.К., Фриман А., Куан Х. и др. Исследования пероральной биодоступности алендроната. Clin Pharmacol Ther . 1995 Сентябрь 58 (3): 288-98. [Медлайн].
Абрахамсен Б., Эйкен П., Истелл Р. Использование ингибиторов протонной помпы и эффективность алендроната против переломов. Arch Intern Med . 2011, 13 июня. 171 (11): 998-1004.[Медлайн].
Harris ST, Watts NB, Genant HK, McKeever CD, Hangartner T, Keller M и др. Влияние лечения ризедронатом на переломы позвонков и позвоночника у женщин с постменопаузальным остеопорозом: рандомизированное контролируемое исследование. Группа исследования эффективности вертебральной терапии ризедронатом (VERT). JAMA . 1999, 13 октября. 282 (14): 1344-52. [Медлайн]. [Полный текст].
Black DM, Delmas PD, Eastell R, et al. Золедроновая кислота для лечения постменопаузального остеопороза один раз в год. N Engl J Med . 2007 3 мая. 356 (18): 1809-22. [Медлайн].
Boonen S, Reginster JY, Kaufman JM, Lippuner K, Zanchetta J, Langdahl B, et al. Риск переломов и терапия золедроновой кислотой у мужчин с остеопорозом. N Engl J Med . 2012 ноябрь 367 (18): 1714-23. [Медлайн].
Boonen S, Orwoll E, Magaziner J, Colón-Emeric CS, Adachi JD, Bucci-Rechtweg C, et al. Золедроновая кислота один раз в год у пожилых мужчин по сравнению с женщинами с недавним переломом шейки бедра. J Am Geriatr Soc . 2011 ноябрь 59 (11): 2084-90. [Медлайн].
Odvina CV, Zerwekh JE, Rao DS, Maalouf N, Gottschalk FA, Pak CY. Сильное подавление метаболизма костной ткани: возможное осложнение терапии алендронатом. Дж. Клин Эндокринол Метаб . 2005 Март 90 (3): 1294-301. [Медлайн].
Halasy-Nagy JM, Rodan GA, Reszka AA. Подавление резорбции костей алендронатом и ризедронатом не требует апоптоза остеокластов. Кость . 2001 29 декабря (6): 553-9. [Медлайн].
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Сообщение FDA по безопасности лекарств: новое противопоказание и обновленное предупреждение о почечной недостаточности для Рекласта (золедроновой кислоты). Доступно на http://www.fda.gov/Drugs/DrugSafety/ucm270199.htm. 1 сентября 2011 г .; Дата обращения: 19 июня 2019 г.
Информация о безопасности: Зомета (золедроновая кислота) для инъекций. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Доступно на https: // www.accessdata.fda.gov/drugsatfda_docs/label/2016/021817s022lbl.pdf. Апрель 2016 г .; Дата обращения: 15 июня 2019 г.
Хан А.А., Моррисон А., Хэнли Д.А., Фельзенберг Д., МакКоули Л.К. и др. И др. Диагностика и лечение остеонекроза челюсти: систематический обзор и международный консенсус. J Bone Miner Res . 2015 30 января (1): 3-23. [Медлайн].
Стрампель В., Эмки Р., Чивителли Р. Меры безопасности с бисфосфонатами для лечения остеопороза. Сейф с наркотиками . 2007. 30 (9): 755-63. [Медлайн].
Зебич Л., Патель В. Профилактика медикаментозного остеонекроза челюсти. BMJ . 2019 8 мая. 365: l1733. [Медлайн].
Park-Wyllie LY, Mamdani MM, Juurlink DN, Hawker GA, Gunraj N, Austin PC, et al. Использование бисфосфонатов и риск переломов челюстно-лицевой области или диафиза бедренной кости у пожилых женщин. JAMA . 2011 г. 23 февраля. 305 (8): 783-9. [Медлайн].
Lo JC, Neugebauer RS, Ettinger B, Chandra M, Hui RL, Ott SM, et al.Риск полного атипичного перелома бедренной кости при пероральном приеме бисфосфонатов более трех лет. BMC Musculoskelet Disord . 2020 3 декабря. 21 (1): 801. [Медлайн].
Geusens P. Бисфосфонаты для лечения постменопаузального остеопороза: определение продолжительности лечения. Curr Osteoporos Rep . 2009 Март 7 (1): 12-7. [Медлайн].
[Рекомендации] Адлер Р.А., Эль-Хадж Фулейхан Г., Бауэр округ Колумбия, Камачо П.М., Кларк Б.Л., Клинес Г.А. и др. Управление остеопорозом у пациентов, получающих длительное лечение бисфосфонатами: отчет рабочей группы Американского общества исследований костей и минералов. J Bone Miner Res . 2016 31 января (1): 16-35. [Медлайн]. [Полный текст].
Grady D, Cauley JA, Stock JL, Cox DA, Mitlak BH, Song J и др. Влияние ралоксифена на общую смертность. Am J Med . 2010 май. 123 (5): 469.e1-7. [Медлайн].
Линдси Р., Галлахер Дж. К., Каган Р., Пикар Дж. Х., Константин Г. Эффективность тканеселективного комплекса эстрогенов базедоксифена / конъюгированных эстрогенов для профилактики остеопороза у женщин в постменопаузе из группы риска. Fertil Steril . 2009 Сентябрь 92 (3): 1045-52. [Медлайн].
Гилсенан А., Харрис Д., Рейнольдс М., МакСорли Д., Мидкифф К., Джексон Л. и др. Долгосрочное наблюдение за раком: результаты исследования по надзору в реестре пациентов Forteo. Остеопорос Инт . 2020 5 ноября. [Medline].
Quattrocchi E, Kourlas H. Teriparatide: обзор. Клин Тер . 2004 Июнь 26 (6): 841-54. [Медлайн].
Koski AM, Sikiö A, Forslund T.Лечение терипаратидом, осложненное злокачественной миеломой. BMJ Case Rep . 2010 13 августа 2010: [Medline]. [Полный текст].
Body JJ, Gaich GA, Scheele WH, Kulkarni PM, Miller PD, Peretz A. Рандомизированное двойное слепое испытание для сравнения эффективности терипаратида [рекомбинантного паратиреоидного гормона человека (1-34)] с алендронатом у женщин в постменопаузе с остеопорозом . Дж. Клин Эндокринол Метаб . 2002 Октябрь 87 (10): 4528-35. [Медлайн].
Dempster DW, Cosman F, Kurland ES, Zhou H, Nieves J, Woelfert L, et al.Влияние ежедневного лечения паратироидным гормоном на микроархитектуру и метаболизм костей у пациентов с остеопорозом: исследование парной биопсии. J Bone Miner Res . 2001 16 октября (10): 1846-53. [Медлайн].
Neer RM, Arnaud CD, Zanchetta JR, Prince R, Gaich GA, Reginster JY, et al. Влияние паратироидного гормона (1-34) на переломы и минеральную плотность костей у женщин в постменопаузе с остеопорозом. N Engl J Med . 2001 May 10. 344 (19): 1434-41.[Медлайн].
Kurland ES, Heller SL, Diamond B, McMahon DJ, Cosman F, Bilezikian JP. Важность терапии бисфосфонатами для поддержания костной массы у мужчин после терапии терипаратидом [человеческий паратиреоидный гормон (1-34)]. Остеопорос Инт . 2004 15 декабря (12): 992-7. [Медлайн].
Финкельштейн JS, Hayes A, Hunzelman JL, Wyland JJ, Lee H, Neer RM. Эффекты паратиреоидного гормона, алендроната или того и другого у мужчин с остеопорозом. N Engl J Med . 2003 25 сентября. 349 (13): 1216-26. [Медлайн].
Cosman F, Nieves J, Zion M, Woelfert L, Luckey M, Lindsay R. Daily и циклический паратиреоидный гормон у женщин, получающих алендронат. N Engl J Med . 2005 11 августа. 353 (6): 566-75. [Медлайн].
Deal C, Omizo M, Schwartz EN, Eriksen EF, Cantor P, Wang J и др. Комбинированная терапия терипаратидом и ралоксифеном при постменопаузальном остеопорозе: результаты 6-месячного двойного слепого плацебо-контролируемого исследования. J Bone Miner Res . 2005 20 ноября (11): 1905-11. [Медлайн].
Ste-Marie LG, Schwartz SL, Hossain A, Desaiah D, Gaich GA. Влияние терипаратида [rhPTH (1-34)] на МПК при назначении женщинам в постменопаузе, получающим заместительную гормональную терапию. J Bone Miner Res . 2006 21 февраля (2): 283-91. [Медлайн].
Tsai JN, Uihlein AV, Lee H, Kumbhani R, Siwila-Sackman E, McKay EA, et al. Терипаратид и деносумаб, по отдельности или в комбинации, у женщин с постменопаузальным остеопорозом: рандомизированное исследование DATA. Ланцет . 2013 июл 6. 382 (9886): 50-6. [Медлайн].
Leder BZ, Tsai JN, Uihlein AV, Wallace PM, Lee H, Neer RM и др. Переходы деносумаба и терипаратида при постменопаузальном остеопорозе (исследование DATA-Switch): продолжение рандомизированного контролируемого исследования. Ланцет . 2015 19 сентября. 386 (9999): 1147-55. [Медлайн].
Bouxsein ML, Chen P, Glass EV, Kallmes DF, Delmas PD, Mitlak BH. Терипаратид и ралоксифен снижают риск новых переломов соседних позвонков у женщин в постменопаузе с остеопорозом.Результаты двух рандомизированных контролируемых исследований. J Bone Joint Surg Am . 2009 июнь 91 (6): 1329-38. [Медлайн].
Кендлер Д.Л., Марин Ф., Цербини КАФ, Руссо Л.А., Гринспен С.Л., Зикан В. и др. Влияние терипаратида и ризедроната на новые переломы у женщин в постменопаузе с тяжелым остеопорозом (VERO): многоцентровое двойное слепое рандомизированное контролируемое исследование с двойной фиксацией. Ланцет . 2017 9 ноября. [Medline].
Gomberg SJ, Wustrack RL, Napoli N, Arnaud CD, Black DM.Терипаратид, витамин D и кальций излечили двусторонние подвертельные стрессовые переломы у женщины в постменопаузе с 13-летней историей непрерывной терапии алендронатом. Дж. Клин Эндокринол Метаб . 2011 Июнь 96 (6): 1627-32. [Медлайн].
Салех А., Хегде В.В., Потти АГ, Шнайдер Р., Корнелл С.Н., Лейн Дж. М.. Стратегия ведения симптоматических неполных атипичных переломов бедренной кости, связанных с бисфосфонатами. HSS J . 2012 июл.8 (2): 103-10. [Медлайн].[Полный текст].
Лау А.Н., Адачи Д.Д. Разрешение остеонекроза челюсти после терапии терипаратидом [рекомбинантный человеческий ПТГ- (1-34)]. Дж. Ревматол . 2009 августа, 36 (8): 1835-7. [Медлайн].
Cheung A, Seeman E. Терипаратидная терапия алендронат-ассоциированного остеонекроза челюсти. N Engl J Med . 2010 16 декабря. 363 (25): 2473-4. [Медлайн].
Наронгроекнавин П., Данила М.И., Хамфрис Л.Г. мл., Бараш А., Кертис-мл.Бисфосфонат-ассоциированный остеонекроз челюсти с заживлением после терипаратида: обзор литературы и описание случая. Специалист по уходу за стоматологом . 2010 март-апрель. 30 (2): 77-82. [Медлайн]. [Полный текст].
Миллер П.Д., Хаттерсли Г., Риис Б.Дж., Уильямс Г.К., Лау Э., Руссо Л.А. и др. Эффект абалопаратида по сравнению с плацебо на новые переломы позвонков у женщин в постменопаузе с остеопорозом: рандомизированное клиническое испытание. JAMA . 2016 16 августа. 316 (7): 722-33.[Медлайн]. [Полный текст].
Cosman F, Miller PD, Williams GC, Hattersley G, Hu MY, Valter I, et al. Восемнадцать месяцев лечения подкожным абалопаратидом с последующими 6 месяцами лечения алендронатом у женщин в постменопаузе с остеопорозом: результаты исследования ACTIVExtend. Mayo Clin Proc . 2017 Февраль 92 (2): 200-210. [Медлайн]. [Полный текст].
Peichl P, Holzer LA, Maier R, Holzer G. Паратироидный гормон 1-84 ускоряет заживление переломов лонных костей у пожилых женщин с остеопорозом. J Bone Joint Surg Am . 2011 7 сентября. 93 (17): 1583-7. [Медлайн].
Cosman F, Crittenden DB, Adachi JD, Binkley N, Czerwinski E, Ferrari S и др. Лечение ромосозумабом у женщин в постменопаузе с остеопорозом. N Engl J Med . 2016 18 сентября [Medline]. [Полный текст].
Saag KG, Petersen J, Brandi ML, Karaplis AC, Lorentzon M, Thomas T. и др. Ромосозумаб или алендронат для профилактики переломов у женщин с остеопорозом. N Engl J Med . 2017 Октябрь 12, 377 (15): 1417-1427. [Медлайн]. [Полный текст].
Lewiecki EM, Dinavahi RV, Lazaretti-Castro M, Ebeling PR, Adachi JD, Miyauchi A, et al. Один год приема ромосозумаба, а затем два года приема деносумаба способствует снижению риска переломов: результаты расширенного исследования FRAME. J Bone Miner Res . 2019 марта 34 (3): 419-428. [Медлайн].
Lewiecki EM, Blicharski T, Goemaere S, Lippuner K, Meisner PD, Miller PD, et al.Рандомизированное плацебо-контролируемое испытание фазы III для оценки эффективности и безопасности ромосозумаба у мужчин с остеопорозом. Дж. Клин Эндокринол Метаб . 2018 сен 1. 103 (9): 3183-3193. [Медлайн].
Saag KG, Petersen J, Brandi ML, Karaplis AC, Lorentzon M, Thomas T. и др. Ромосозумаб или алендронат для профилактики переломов у женщин с остеопорозом. N Engl J Med . 2017 Октябрь 12, 377 (15): 1417-1427. [Медлайн].
Body JJ, Facon T, Coleman RE, Lipton A, Geurs F, Fan M и др.Исследование биологического активатора рецептора ядерного фактора — ингибитора лиганда каппаВ, деносумаба, у пациентов с множественной миеломой или метастазами в кости от рака груди. Clin Cancer Res . 2006 15 февраля. 12 (4): 1221-8. [Медлайн].
McClung MR, Lewiecki EM, Cohen SB, Bolognese MA, Woodson GC, Moffett AH, et al. Деносумаб у женщин в постменопаузе с низкой минеральной плотностью костей. N Engl J Med . 2006 23 февраля. 354 (8): 821-31. [Медлайн].
Orwoll E, Teglbjærg CS, Langdahl BL, Chapurlat R, Czerwinski E, Kendler DL, et al.Рандомизированное плацебо-контролируемое исследование эффектов деносумаба при лечении мужчин с низкой минеральной плотностью костей. Дж. Клин Эндокринол Метаб . 2012 сентябрь 97 (9): 3161-9. [Медлайн].
Block GA, Bone HG, Fang L, Lee E, Padhi D. Исследование однократной дозы деносумаба у пациентов с различной степенью почечной недостаточности. J Bone Miner Res . 2012 июля. 27 (7): 1471-9. [Медлайн]. [Полный текст].
Saag KG, Wagman RB, Geusens P, Adachi JD, Messina OD, Emkey R, et al.Сравнение деносумаба и ризедроната при остеопорозе, индуцированном глюкокортикоидами: многоцентровое рандомизированное двойное слепое активно-контролируемое двойное манекен-исследование не меньшей эффективности. Ланцет Диабет Эндокринол . 6 апреля 2018 г. [Medline].
Каммингс С.Р., Сан-Мартин Дж., Макклунг М.Р., Сирис Е.С., Истелл Р., Рейд И.Р. и др. Деносумаб для профилактики переломов у женщин в постменопаузе с остеопорозом. N Engl J Med . 2009 20 августа. 361 (8): 756-65. [Медлайн].
Смит М.Р., Эгерди Б., Эрнандес Торис Н., Фельдман Р., Таммела Т.Л., Саад Ф. и др.Деносумаб у мужчин, получающих андроген-депривационную терапию рака простаты. N Engl J Med . 2009 20 августа. 361 (8): 745-55. [Медлайн].
Лю Х., Джунди Б., Сюй С., Тедески С.К., Йошида К., Чжао С. и др. Сравнение деносумаба и бисфосфонатов у пациентов с остеопорозом: метаанализ рандомизированных контролируемых исследований. Дж. Клин Эндокринол Метаб . 2019 1 мая. 104 (5): 1753-1765. [Медлайн].
Шварц EM, Ритчлин Коннектикут.Клиническая разработка анти-RANKL терапии. Arthritis Res Ther . 2007. 9 Приложение 1: S7. [Медлайн]. [Полный текст].
Tsai JN, Uihlein AV, Lee H, Kumbhani R, Siwila-Sackman E, McKay EA, et al. Терипаратид и деносумаб, по отдельности или в комбинации, у женщин с постменопаузальным остеопорозом: рандомизированное исследование DATA. Ланцет . 2013 14 мая. [Medline].
Анастасилакис А.Д., Полизос С.А., Макрас П., Обри-Розье Б., Каури С., Лами О.Клинические особенности 24 пациентов с переломами позвонков, связанными с рикошетом, после отмены деносумаба: систематический обзор и дополнительные случаи. J Bone Miner Res . 2017 июн.32 (6): 1291-1296. [Медлайн].
Постмаркетинговая информация о безопасности лекарств для пациентов и поставщиков медицинских услуг — Вопросы и ответы: изменения в группе пациентов, принимающих миакальцин (кальцитонин-лосось). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Доступно на сайте http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm388641.htm. 1 сентября 2015 г .; Дата обращения: 21 января 2021 г.
Россоу Дж. Э., Андерсон Г. Л., Прентис Р. Л. и др. Риски и преимущества применения эстрогена и прогестина у здоровых женщин в постменопаузе: основные результаты Рандомизированного контролируемого исследования инициативы «Здоровье женщин». JAMA . 2002, 17 июля. 288 (3): 321-33. [Медлайн].
Блейк Г.М., Фогельман И. Долгосрочный эффект лечения ранелатом стронция на МПК. J Bone Miner Res . 2005 ноя.20 (11): 1901-4. [Медлайн].
Burlet N, Reginster JY. Стронция ранелат: первое средство двойного действия для лечения постменопаузального остеопороза. Clin Orthop Relat Res . 2006 февраль 443: 55-60. [Медлайн].
Bischoff-Ferrari HA, Dawson-Hughes B, Willett WC, Staehelin HB, Bazemore MG, Zee RY и др. Влияние витамина D на падения: метаанализ. JAMA . 2004, 28 апреля. 291 (16): 1999-2006. [Медлайн].
Росс А.С., Мэнсон Дж. Э., Абрамс С. А., Алоя Дж. Ф., Браннон П. М., Клинтон С. К. и др.Отчет Института медицины о рекомендуемом потреблении кальция и витамина D с пищей за 2011 год: что необходимо знать врачам. Дж. Клин Эндокринол Метаб . 2011 Январь 96 (1): 53-8. [Медлайн]. [Полный текст].
Bruni V, Dei M, Filicetti MF, Balzi D, Pasqua A. Предикторы потери костной массы у молодых женщин с ограничительными расстройствами пищевого поведения. Педиатр эндокринол Ред. . 2006, 3 января, Дополнение 1: 219-21. [Медлайн].
Тан Б.М., Эслик Г.Д., Ноусон С., Смит К., Бенсуссан А.Использование кальция или кальция в сочетании с добавкой витамина D для предотвращения переломов и потери костной массы у людей в возрасте 50 лет и старше: метаанализ. Ланцет . 2007 25 августа. 370 (9588): 657-66. [Медлайн].
Bischoff-Ferrari HA, Willett WC, Wong JB, Stuck AE, Staehelin HB, Orav EJ, et al. Профилактика непозвоночных переломов пероральным приемом витамина D и дозозависимость: метаанализ рандомизированных контролируемых исследований. Arch Intern Med . 2009 23 марта.169 (6): 551-61. [Медлайн].
Warensjö E, Byberg L, Melhus H, et al. Потребление кальция с пищей и риск переломов и остеопороза: проспективное продольное когортное исследование. BMJ . 2011 24 мая. 342: d1473. [Медлайн]. [Полный текст].
Группа DIPART (индивидуальный анализ пациентов с витамином D в рандомизированных исследованиях). Объединенный анализ на уровне пациентов 68 500 пациентов из семи крупных исследований переломов витамина D в США и Европе. BMJ .12 января 2010 г. 340: b5463. [Медлайн]. [Полный текст].
Li K, Kaaks R, Linseisen J, Rohrmann S. Связи потребления кальция с пищей и добавок кальция с инфарктом миокарда и риском инсульта и общей смертностью от сердечно-сосудистых заболеваний в Гейдельбергской когорте исследования Европейского проспективного исследования рака и питания (EPIC-Heidelberg ). Сердце . 2012 июн. 98 (12): 920-5. [Медлайн].
Curhan GC, Willett WC, Speizer FE, Spiegelman D, Stampfer MJ.Сравнение диетического кальция с дополнительным кальцием и другими питательными веществами как факторов, влияющих на риск образования камней в почках у женщин. Энн Интерн Мед. . 1997 г., 1. 126 (7): 497-504. [Медлайн].
Candelas G, Martinez-Lopez JA, Rosario MP, Carmona L., Loza E. Добавки кальция и риск образования камней в почках при остеопорозе: систематический обзор литературы. Clin Exp Rheumatol . 2012 ноябрь-декабрь. 30 (6): 954-61. [Медлайн].
Favus MJ.Риск образования камней в почках: имеет значение форма кальция. Ам Дж. Клин Нутр . 2011 Июль 94 (1): 5-6. [Медлайн].
Синаки М. Постменопаузальный остеопороз позвоночника: физиотерапия и принципы реабилитации. Mayo Clin Proc . 1982, ноябрь 57 (11): 699-703. [Медлайн].
Тинетти М.Э., Спичли М. Профилактика падений среди пожилых людей. N Engl J Med . 1989, 20 апреля. 320 (16): 1055-9. [Медлайн].
Sinaki M, Mikkelsen BA.Постменопаузальный остеопороз позвоночника: упражнения на сгибание и разгибание. Arch Phys Med Rehabil . 1984 Октябрь 65 (10): 593-6. [Медлайн].
Sinaki M, Itoi E, Wahner HW, Wollan P, Gelzcer R, Mullan BP и др. Более сильные мышцы спины снижают частоту переломов позвонков: проспективное 10-летнее наблюдение за женщинами в постменопаузе. Кость . 2002 июн.30 (6): 836-41. [Медлайн].
Sinaki M, Itoi E, Rogers JW, Bergstralh EJ, Wahner HW.Корреляция силы разгибателей спины с грудным кифозом и поясничным лордозом у женщин с дефицитом эстрогена. Am J Phys Med Rehabil . 1996 сентябрь-октябрь. 75 (5): 370-4. [Медлайн].
Chien MY, Wu YT, Hsu AT, Yang RS, Lai JS. Эффективность 24-недельной программы аэробных упражнений для женщин в постменопаузе с остеопенией. Calcif Tissue Int . 2000 Декабрь 67 (6): 443-8. [Медлайн].
Snow CM, Shaw JM, Winters KM, Witzke KA. Длительные упражнения с использованием утяжеленных жилетов предотвращают потерю кости бедра у женщин в постменопаузе. Дж. Геронтол А Биол Науки и Медицины . 2000 Сентябрь 55 (9): M489-91. [Медлайн].
Howe TE, Shea B., Dawson LJ, et al. Упражнения для профилактики и лечения остеопороза у женщин в постменопаузе. Кокрановская база данных Syst Rev . 2011 6 июля. CD000333. [Медлайн].
Iwamoto J, Takeda T, Ichimura S. Влияние физических упражнений и детренированности на минеральную плотность костей у женщин в постменопаузе с остеопорозом. Дж. Ортоп Ски .2001. 6 (2): 128-32. [Медлайн].
Kerschan-Shindl K, Uher E, Kainberger F, Kaider A, Ghanem AH, Preisinger E. Долгосрочная программа домашних упражнений: эффект у женщин с высоким риском переломов. Arch Phys Med Rehabil . 2000 Мар. 81 (3): 319-23. [Медлайн].
Робертсон М.С., Девлин Н., Гарднер М.М., Кэмпбелл А.Дж. Эффективность и экономическая оценка программы домашних упражнений, проводимых медсестрой для предотвращения падений. 1: Рандомизированное контролируемое исследование. BMJ . 2001 24 марта. 322 (7288): 697-701. [Медлайн]. [Полный текст].
Уокер М., Клентроу П., Чоу Р., Плили М. Продольная оценка контролируемых и неконтролируемых программ упражнений для лечения остеопороза. Eur J Appl Physiol . 2000 ноябрь 83 (4-5): 349-55. [Медлайн].
Wolf SL, Barnhart HX, Kutner NG, McNeely E, Coogler C., Xu T. Снижение слабости и падений у пожилых людей: исследование тайцзи и компьютеризированной тренировки равновесия.Атланта Группа ФИКСИТ. Хрупкость и травмы: совместные исследования методов вмешательства. J Am Geriatr Soc . 1996 май. 44 (5): 489-97. [Медлайн].
Картер Н.Д., Хан К.М., Пети М.А., Хейнонен А., Уотерман С., Дональдсон М.Г. и др. Результаты 10-недельной программы тренировки силы и равновесия для снижения факторов риска падений: рандомизированное контролируемое исследование с участием женщин 65-75 лет с остеопорозом. Br J Sports Med . 2001 окт. 35 (5): 348-51.[Медлайн]. [Полный текст].
Риггс Б.Л., Мелтон Л.Дж. 3-й. Профилактика и лечение остеопороза. N Engl J Med . 1992 27 августа. 327 (9): 620-7. [Медлайн].
Ивамото Дж., Сато И., Удзава М., Такеда Т., Мацумото Х. Сравнение эффектов алендроната и ралоксифена на минеральную плотность поясничной кости, метаболизм костной ткани и липидный обмен у пожилых женщин с остеопорозом. Йонсей Мед Дж. . 2008 29 февраля, 49 (1): 119-28. [Медлайн].[Полный текст].
Gourlay ML, Fine JP, Preisser JS, May RC, Li C, Lui LY, et al. Интервал измерения плотности костной ткани и переход к остеопорозу у пожилых женщин. N Engl J Med . 2012 19 января. 366 (3): 225-33. [Медлайн]. [Полный текст].
Schwab P, Кляйн РФ. Нефармакологические подходы для улучшения здоровья костей и уменьшения остеопороза. Curr Opin Rheumatol . 2008 20 марта (2): 213-7. [Медлайн].
Lin JT, Lane JM.Немедицинское лечение остеопороза. Curr Opin Rheumatol . 14 июля 2002 г. (4): 441-6. [Медлайн].
Gourlay ML, Fine JP, Preisser JS, May RC, Li C, Lui LY, et al. Интервал измерения плотности костной ткани и переход к остеопорозу у пожилых женщин. N Engl J Med . 2012 19 января. 366 (3): 225-33. [Медлайн]. [Полный текст].
[Рекомендации] Вишванатан М., Редди С., Беркман Н., Каллен К., Миддлтон Дж. К., Николсон В. К. и др. Скрининг для предотвращения остеопоротических переломов: обновленный отчет о доказательствах и систематический обзор для Целевой группы профилактических служб США. JAMA . 26 июня 2018 г. 319 (24): 2532-2551. [Медлайн]. [Полный текст].
[Руководство] Обновления к Руководству для врачей по профилактике и лечению остеопороза. Национальный фонд остеопороза. Доступно по адресу https://my.nof.org/bone-source/Incorporation-of-diagnostic-criteria-to-be-used-to-establish-a-clinical-diagnosis-of-osteoporosis. 11 ноября 2015 г .; Дата обращения: 21 января 2021 г.
[Рекомендации] Eastell R, Rosen CJ, Black DM, Cheung AM, Murad MH, Shoback D.Фармакологическое лечение остеопороза у женщин в постменопаузе: эндокринное общество * Руководство по клинической практике. Дж. Клин Эндокринол Метаб . 2019 25 марта. [Medline]. [Полный текст].
Конференция NIH Consensus. Оптимальное потребление кальция. Группа разработки консенсуса NIH по оптимальному потреблению кальция. JAMA . 1994 28 декабря. 272 (24): 1942-8. [Медлайн].
Bauer DC. Увеличение позвонков по сравнению с нехирургической терапией: улучшение симптомов, улучшение выживаемости или ни то, ни другое? JAMA Intern Med . 2013 9 сентября. 173 (16): 1522-3. [Медлайн].
Bolland MJ, Gray A, Avenell A, Gamble GD, Reid IR. Добавки кальция с витамином D или без него и риск сердечно-сосудистых событий: повторный анализ набора данных с ограниченным доступом Инициативы по охране здоровья женщин и метаанализ. BMJ . 2011, 19 апреля. 342: d2040. [Медлайн]. [Полный текст].
Hsia J, Heiss G, Ren H, Allison M, Dolan NC, Greenland P, et al. Добавки кальция / витамина D и сердечно-сосудистые заболевания. Тираж . 2007 20 февраля. 115 (7): 846-54. [Медлайн].
Ван Л., Мэнсон Дж. Э., Сонг Y, Sesso HD. Систематический обзор: добавление витамина D и кальция в профилактике сердечно-сосудистых событий. Энн Интерн Мед. . 2 марта 2010 г. 152 (5): 315-23. [Медлайн].
Компстон Дж., Боуринг С., Купер А., Купер С., Дэвис С., Фрэнсис Р. и др. Диагностика и лечение остеопороза у женщин в постменопаузе и пожилых мужчин в Великобритании: обновление Национальной группы рекомендаций по остеопорозу (NOGG) 2013. Maturitas . 2013 Август 75 (4): 392-6. [Медлайн].
Лю Дж., Кертис Э.М., Купер С., Харви, Северная Каролина. Современное состояние в оценке риска и лечении остеопороза. Дж Эндокринол Инвест . 2019 Октябрь 42 (10): 1149-1164. [Медлайн].
Постменопаузальный остеопороз — Консультант по эндокринологии
Вы уверены, что у пациента остеопороз?
Остеопороз — это заболевание скелета, характеризующееся снижением прочности костей, что предрасполагает к повышенному риску переломов.
Прочность кости — это сочетание плотности кости и качества кости и включает такие факторы, как степень минерализации, микроповреждения, структура коллагена, трабекулярное соединение, усталостное повреждение и макроархитектурные изменения, например. увеличение длины шейки бедра ослабляет кость.
В 1994 году Всемирная организация здравоохранения (ВОЗ) установила рабочее определение остеопороза, основанное на минеральной плотности костей (МПК), и со временем это определение стало стандартным.T-балл сравнивает индивидуальную МПК со средним значением для молодых нормальных людей, выраженным в стандартных отклонениях (SD), а Z-балл сравнивает значения, соответствующие возрасту, полу и полу.
Нормальный: Т-балл -1,0 или выше
Низкая костная масса (остеопения): Т-балл от -1,0 до -2,5
Остеопороз: Т-балл -2,5 или ниже
Остеопороз также можно диагностировать клинически при возникновении хрупкого перелома.
Клинические результаты
Симптомы, связанные с остеопорозом, не проявляются, если нет переломов. Значительная потеря роста должна предупреждать о возможности перелома позвонков, даже если он протекает бессимптомно. Однако некоторая потеря высоты может быть вторичной по отношению к сужению межпозвонкового пространства. Переломы позвонков могут возникнуть спонтанно или после незначительной травмы. Клиническое течение у человека непредсказуемо. Они обычно связаны с болью в спине, острой или хронической, локализованной или корешковой, и могут мешать повседневной деятельности.Возможны деформация, длительная инвалидность и изменение самооценки.
При осмотре может присутствовать локальная болезненность, связанная либо с переломом, спазмом паравертебральных мышц, либо с развитием усиленного грудного кифоза с последующим изменением положения спины.
При множественных компрессионных переломах и деформации позвонков может наблюдаться сужение движений грудной клетки с одышкой и вздутие живота с ранним насыщением.
Большинство непозвоночных переломов возникает в результате падения.Переломы бедра являются наиболее серьезным осложнением остеопороза со смертностью до 20-25% в течение года после перелома. Восстановление после перелома бедра может быть продлено, если 50% пациентов с переломом бедра, которые были независимыми до перелома, не восстановили независимость или не нуждались в вспомогательных приспособлениях для передвижения через год.
Перелом одного позвонка увеличивает риск другого в 5 раз, а у тех, кто перенес 2 или более переломов позвонков, риск увеличивается в 12 раз.
Многие пациенты после перелома запястья страдают от боли, деформации, артрита и ограничения функций.
Факторы риска потери костной массы и переломов
Факторы риска низкой МПК у женщин в постменопаузе:
пожилой возраст
генетика (70-80% костной структуры определяется генетически)
низкая масса тела (низкий индекс массы тела)
Низкое потребление кальция и витамина D
курение
климактерический статус
Факторы риска переломов, связанных с остеопорозом:
Факторы, повышающие риск падения и получения перелома:
неврологические расстройства
нарушение зрения
нарушение слуха
хрупкость
саркопения
лекарственные средства: седативные, снотворные, гипотензивные, наркотические анальгетики
факторов окружающей среды: плохое освещение, лестницы, скользкие полы, неровные поверхности, препятствия на полу
На каждое уменьшение стандартного отклонения МПК с поправкой на возраст риск переломов увеличивается примерно в 2 раза.Измерения МПК на конкретном участке лучше всего предсказывают переломы на этом участке. Например, МПК бедра предсказывает переломы бедра лучше, чем МПК на других участках.
Что еще может быть у пациента?
Остеомаляция
Остеомаляция (нарушение минерализации костей) с сопутствующим остеопорозом или без него может вызвать снижение костной массы. Его всегда следует рассматривать как сопутствующий фактор у пациентов с остеопорозом. Остеомаляция у людей в постменопаузе чаще всего возникает из-за дефицита витамина D из-за небольшого воздействия солнечного света, снижения потребления или мальабсорбции.
Клинические проявления остеомаляции включают боли в мышцах и суставах, мышечную слабость и нарушение равновесия.
Низкий уровень 25 OH витамина D может быть связан со вторичным гиперпаратиреозом с низким содержанием кальция и фосфата в сыворотке крови и повышенным уровнем паратиреоидного гормона (ПТГ).
Рентгенограммы длинных костей с тяжелой нагрузкой могут указывать на псевдопереломы, патогномоничные для остеомаляции.
Вторичные причины остеопороза
Эндокринные / метаболические
Пищевые
Алкоголизм
Нервная анорексия
Дефицит кальция
Дефицит витамина D
Желудочно-кишечный
Лекарства
Ингибиторы ароматазы
Андрогенная депривационная терапия
Химиотерапия / иммунодепрессанты
Depo Provera
Противосудорожные средства: фенобарбитал, фенитоин, вальпроат, карбамазепин, примидон
Глюкокортикоиды
Агонисты гонадотропин-рилизинг-гормона
Гепарин
Литий
Дозы супрафизиологических гормонов щитовидной железы
Ингибиторы протонной помпы
Селективные ингибиторы обратного захвата серотонина
Тиазолидиндионы
Коллагеновые нарушения
Синдром Элерса-Данлоса
Гомоцистинурия
Синдром Марфана
Несовершенный остеогенез
Другое
Анкилозирующий спондилит
Иммобилизация
Хроническая болезнь почек
Ревматоидный артрит
Системный мастоцитоз
Множественная миелома
Лимфома, лейкемия
Трансплантация органов
Почечный канальцевый ацидоз
Талассемия
Ключевые лабораторные и визуализирующие исследования
Измерение плотности костной ткани
МПКявляется основным фактором, определяющим риск перелома, и его измерение часто важно для принятия управленческих решений.Однако его следует заказывать только в том случае, если результаты повлияют на принятие клинического решения.
BMD следует рассматривать у женщин в постменопаузе следующим образом:
Все женщины в возрасте 65 лет и старше
Более молодые женщины в постменопаузе с хрупкими переломами в анамнезе (перелом или падение с высоты стоя)
Начало или продолжение длительной терапии глюкокортикоидами
Рентгенологическая остеопения
Клинические факторы риска остеопороза: худоба (масса тела <127 фунтов или ИМТ <21 кг / м2), перелом позвоночника или бедра у родителей, курение сигарет, употребление алкоголя более 3 единиц в день (одна единица составляет 8 унций пива, 4 унции вина, 1 унция ликера
Двухэнергетическая рентгеновская абсорбциометрия (DXA) позвоночника, бедра и предплечья точна и воспроизводима.Бедро (бедро в целом и шейка бедра) и позвоночник обычно измеряются, и диагностические критерии и терапевтические результаты проверяются для этих участков, а не для периферических участков. Периферийные измерения могут идентифицировать пациентов с повышенным риском переломов. Предплечье, в первую очередь 1/3 дистального отдела лучевой кости, полезно, когда позвоночник ненадежен или имеется или подозревается первичный гиперпаратиреоз.
У некоторых людей, особенно в пожилом возрасте, измерения позвоночника могут стать неточными из-за дегенеративных изменений, склероза, сколиоза или перелома.Тогда значения искусственно завышены и могут дать ложное представление о том, что потеря костной массы менее значительна или терапевтическое вмешательство работает. Наиболее надежные результаты получаются при использовании одного и того же инструмента в одном центре плотности кости.
Плотность костной ткани выражается либо как поверхностная плотность (DXA) в граммах минерала на квадратный сантиметр, либо как объемная плотность (количественная CT) в миллиграммах на кубический сантиметр. Затем эти значения сообщаются как T- или Z-баллы. T-оценка представляет собой количество отклонений от нормальных средних значений для молодых взрослых.Z-оценка представляет собой количество SD от нормального среднего значения для сопоставимых по возрасту, полу и полу контрольных субъектов. T-показатель используется для диагностики остеопороза, а низкий Z-показатель может указывать на вторичную причину остеопороза.
У пациентов без перелома в прошлом МПК является единственным лучшим показателем будущих переломов. На каждое уменьшение стандартного отклонения риск перелома увеличивается примерно вдвое (в 1,6–2,6 раза). Хотя вероятность возникновения переломов выше, чем ниже плотность кости, более 50% хрупких переломов происходит у пациентов с МПК в категории с низкой массой кости.
Когда повторять определение плотности костной ткани
Потеря костной массы может начаться до наступления менопаузы. В течение пяти лет до и после прекращения менструации потеря костной массы может составлять в среднем 1% в год. В некоторых ставка выше. После этого скорость потери костной массы замедляется.
У нелеченных женщин в постменопаузе исследование плотности костной ткани следует повторить через 2-5 лет.
У пациентов, получающих лечение от остеопороза, исследование плотности костной ткани следует повторить через 1-2 года.Многие сторонние страховщики платят за проверку плотности костной ткани ежегодно, но Medicare обычно платит каждые два года.
У пациентов, находящихся в отпуске с наркотиками, целесообразно и полезно повторное обследование плотности костной ткани через 1-2 года.
Что указывает на значительное изменение в тестировании МПК?
Значение, равное или превышающее наименьшее значимое изменение (LSC), считается значимым. LSC следует устанавливать в каждом центре плотности кости.Несмотря на то, что значения BMD, которые могут выглядеть изменяющимися, если они попадают в пределы LSC, их следует считать стабильными и находящимися в пределах точности прибора. Для оценки изменений следует использовать значения МПК, а не Т-балл.
Рентгенограммы позвоночника
Рентгенограммы позвоночника, либо стандартная оценка латерального грудного и поясничного отделов позвоночника, либо оценка перелома позвоночника (VFA) на основе измерений DXA, могут помочь идентифицировать переломы или деформации позвонков. Это знание может изменить терапевтические решения. Пациентам с необъяснимой потерей роста, кифозом или острой болью в спине следует рассмотреть возможность визуализации позвоночника.
Лабораторные исследования для выявления вторичных причин остеопороза
Общий анализ крови: анемия. множественная миелома, хроническое заболевание
Кальций в сыворотке:
высокий — первичный гиперпаратиреоз
низкий — дефицит витамина D, остеомаляция
Фосфор сыворотки:
высокий — почечная недостаточность
низкий — первичный гиперпаратиреоз, остеомаляция
Сывороточный альбумин: низкий.используется для коррекции сывороточного кальция, дефицита питательных веществ
Ферменты печени сыворотки: высокий. болезнь печени
Щелочная фосфатаза сыворотки: высокая. Болезнь Педжета, остеомаляция, дефицит витамина D, заживление перелома, заболевание печени,
Креатинин сыворотки: высокий. почечная недостаточность
Электролиты сыворотки: высокий уровень CO2. ацидоз
Сыворотка 25 ОН витамин D: низкий. дефицит витамина D, мальабсорбция
Кальций и креатинин в суточной моче: высокое содержание кальция в моче.гиперпаратиреоз, почечная утечка кальция, высокое потребление кальция, множественная миелома, метастатический рак, гипертиреоз
Тиротропин сыворотки: низкий. гипертиреоз
ПТГ в сыворотке: высокий. первичный или вторичный гиперпаратиреоз
Электрофорез белков сыворотки: M spike. множественная миелома, моноклональная гаммопатия неопределенной значимости
Другие тесты, которые могут оказаться полезными с диагностической точки зрения
Тканевая трансглутаминаза: высокая — целиакия
Кислотно-основные исследования: отклонения от нормы — ацидоз, почечный канальцевый ацидоз
Свободный кортизол в моче, кортизол слюны: высокий — гиперкортизолизм
Триптаза сыворотки: высокий — мастоцитоз
N-телопептид в моче, повышенный уровень C-телопептида в сыворотке — повышенный риск перелома
Маркеры метаболизма кости
Маркеры обновления костной ткани полезны для оценки функции скелета.Маркеры остеокластической резорбции кости включают N-телопептид мочи (NTx), C-телопептид сыворотки (CTx) и дезоксипиридинолин. Маркеры образования остеобластической кости включают костно-специфическую щелочную фосфатазу, N-концевой пропептид проколлагена 1 типа и остеокальцин. Эти маркеры нельзя использовать для диагностики остеопороза, но повышенные маркеры обновления костной ткани связаны с повышенным риском переломов. Они имеют разную степень предсказания индивидуального ответа на терапию, хотя быстрое снижение может наблюдаться в течение 2-3 месяцев после начала терапии.Их полезность ограничена, потому что они меняются изо дня в день, зависят от приема пищи и времени суток и демонстрируют изменчивость анализа.
NTx мочи должен быть получен на втором утреннем образце без мочеиспускания перед едой и CTx сыворотки перед едой. Однако они могут быть ранним признаком ответа на терапию. Повышенные маркеры резорбции костного обмена, несмотря на антирезорбтивную терапию, могут указывать на отсутствие ответа на терапию или несоблюдение режима приема лекарств.
Ведение и лечение болезни
Менеджмент и лечение
Терапевтический подход к лечению остеопороза и предотвращению дальнейшей потери костной массы включает два подхода:
1.Немедикаментозные: кальций, витамин D, питание, упражнения, профилактика падений
2. Фармакологические: эстроген, ралоксифен, кальцитонин, бисфосфонаты, терипаратид, деносумаб
Немедикаментозная терапия
1. Кальций
Достаточное количество кальция важно для любого возраста. Для женщин старше 50 лет рекомендуемая суточная норма кальция составляет 1200 мг (диета с добавками). Суточное потребление кальция снижается с возрастом. Среднее потребление кальция для женщин в постменопаузе составляет около 600 мг.С возрастом потребление кальция уменьшается, всасывание кальция в кишечнике уменьшается, часто наблюдается дефицит витамина D и 1,25 (OH) 2 витамина D, активной формы витамина D.
Желательно получать необходимое количество кальция из пищевых источников, в первую очередь из молочных продуктов и продуктов, обогащенных кальцием. Однако это часто бывает сложно. Пищевой кальций легко доступен, питателен и лучше усваивается, чем таблетки кальция.
Существует множество кальциевых добавок в виде различных солей кальция.Двумя наиболее распространенными являются препараты карбоната кальция и цитрата кальция. Количество элементарного кальция в карбонате кальция составляет 40%, а в цитрате кальция — 21%. Таким образом, таблетка карбоната кальция на 1250 мг содержит 500 мг элементарного кальция, а таблетка на 750 мг содержит 300 мг элементарного кальция. Важно знать, что представляет собой препарат кальция и сколько таблеток, каплетов или пакетов составляют размер порции. Это может сбивать с толку пациентов. Попросите их принести на рассмотрение свои препараты кальция, витамина D и поливитамины.
Карбонат кальция содержит больше всего кальция, поэтому требует меньшего количества таблеток и, как правило, является наименее дорогим. Однако это может вызвать дискомфорт в животе с вздутием живота и запором. Для абсорбции ему также требуется желудочная кислота, и он плохо всасывается, если проводится терапия ингибиторами протонной помпы. Лучше всасывается при приеме с пищей.
Цитрат кальция содержит меньше кальция на таблетку, поэтому требуется больше таблеток и часто он дороже. Однако, как правило, он лучше всасывается, не зависит от желудочного сока и вызывает меньше жалоб со стороны желудочно-кишечного тракта (ЖКТ).
Не более 500-600 мг кальция за один раз. Если требуются более высокие дозы, их следует разделить. Для тех, кто не может глотать таблетки, доступны жевательные таблетки и жидкие препараты кальция.
Кальций можно считать слабым антирезорбтивным средством. Исследования показали небольшое увеличение МПК, но не снижение числа переломов без витамина D. Небольшое увеличение экскреции кальция с мочой может наблюдаться при приеме добавок кальция, но не обязательно значительное увеличение камней в почках.Пациенты с известной историей нефролитиаза должны быть обследованы на предмет причины, прежде чем назначать кальциевые добавки.
2. Витамин D
Недостаточность и дефицит витамина D могут быть обычным явлением у женщин в постменопаузе, особенно у тех, кто живет в северных широтах. Это также распространено среди лиц, находящихся в специализированных учреждениях, и лиц, прикованных к дому.
Витамин D не широко доступен в пищевых продуктах, за исключением жирной рыбы и продуктов, обогащенных витамином D, таких как молоко, хлопья и хлеб.Витамин D может вырабатываться естественным путем из предшественников в коже, но преобразование блокируется солнцезащитным кремом, имеющим коэффициент защиты от солнца 8 или выше.
Национальный фонд остеопороза рекомендует употреблять 800–1000 МЕ витамина D в день. Недавние рекомендации Института медицины рекомендуют потребление витамина D в размере 600 МЕ для женщин в возрасте 51-70 лет и 800 МЕ для лиц старше 70 лет. Многие эксперты рекомендуют уровни в диапазоне 1000-2000 МЕ, а иногда и выше, чтобы поддерживать адекватный уровень сыворотки крови 25 ОН уровень витамина D.Институт медицины считает безопасным верхний предел в 4000 МЕ.
Достаточность витамина D оценивается путем измерения уровня 25-ОН витамина D в сыворотке, а не 1,25 (ОН) 2 витамина D. Отчет Института медицины предполагает, что уровень в сыворотке 20 нг / мл защитит 97,5% населения от неблагоприятных рисков для скелета, таких как переломы. Многие считают, что это слишком мало, а минимально допустимый уровень находится в диапазоне 30 нг / мл. Ниже этого уровня повышается уровень паратироидного гормона и снижается фракционное всасывание кальция.Они считают, что лучший диапазон для 25 OH витамина D составляет 30-60 нг / мл, хотя уровни до 100 нг / мл вряд ли вызовут проблемы.
Уровень витамина D в сыворотке 25 OH повышается примерно на 1 нг / мл на каждые 100 МЕ в день дополнительного холекальциферола (витамина D3). После изменения дозы витамина D для достижения нового устойчивого состояния требуется 3 месяца. В большинство препаратов кальция и витаминов добавляется витамин D. В высоких дозах витамин D3 (холекальциферол) примерно на 30% эффективнее витамина D2 (эргокальциферол).
Иногда при дефиците витамина D назначают высокие дозы витамина D2 по 50 000 МЕ еженедельно в течение 8–12 недель. Другие схемы предлагают ежедневно в течение 5-7 дней или 2-3 раза в неделю в течение нескольких недель. Затем эти схемы сопровождаются витамином D3 1000–2000 МЕ ежедневно.
Один только витамин D (700-800 МЕ) или с добавками кальция (1000 мг кальция), как сообщалось, уменьшает вероятность переломов бедра и непозвоночных переломов.
Витамин D улучшает мышечную силу и равновесие, а также снижает риск падения.Все другие положительные эффекты витамина D не для скелета не доказаны.
3. Другие питательные вещества и витамины
Не было доказано, что добавки магния увеличивают МПК, снижают риск переломов или увеличивают абсорбцию кальция. Добавки магния подходят людям с чрезмерными потерями, например. Заболевания желудочно-кишечного тракта с нарушением всасывания и петлевыми диуретиками.
Низкие дозы витамина К (1 мг / день) могут снизить потерю костной массы, но это необходимо подтвердить. Витамин К противопоказан лицам, принимающим варфарин.
Необходимо обеспечить адекватное потребление белка с пищей. Изофлавоны сои (естественные эстрогены) не доказали однозначно, что они увеличивают МПК или снижают риск переломов.
Следует избегать чрезмерного употребления алкоголя из-за его пагубного воздействия на риск переломов из-за повышенной склонности к падению, дефицита кальция и витамина D и заболеваний печени. Женщины в постменопаузе не должны употреблять более 7 единиц алкоголя в неделю. (1 единица соответствует 8 унциям пива, 4 унциям вина, 1 унции ликера).
Ограничьте потребление кофеина 8-12 унциями один или два раза в день.Сюда входят напитки с кофеином.
Курение сигарет — фактор риска потери костной массы, возможно, из-за увеличения метаболизма эндогенного эстрогена.
4. Упражнение
Упражнения с весовой нагрузкой и силовые тренировки могут привести к небольшому, но значительному увеличению МПК, улучшить баланс и мышечную силу и снизить риск падений. Нет необходимости в интенсивных упражнениях, полезны даже такие легкие, как 30-60-минутная ходьба. Бег трусцой обеспечивает дополнительную ударную нагрузку на скелет.В программах силовых тренировок используются прогрессивные отягощения с тренажерами, но можно использовать и свободные веса, или отягощения. Упражнения должны быть нацелены на определенные группы мышц спины, бедер и рук. Пациентам с тяжелым остеопорозом следует избегать упражнений с высокой ударной нагрузкой, упражнений на сгибание туловища или боковых сгибаний, а также использования тяжелых весов. Упражнения по водной аэробике могут помочь, а легкие упражнения на разгибание позвоночника, выполняемые в кресле, укрепляют мышцы-разгибатели спины.
Консультации по физиотерапии могут быть полезны, особенно при тяжелом остеопорозе и переломах.
5. Защита от падений
Большинство остеопоротических переломов, особенно невертебральных, связаны с падением. Профилактика падений должна быть частью всех программ лечения остеопороза. Программа упражнений для улучшения баланса и мышечной силы снижает вероятность падений. Корректировка или прекращение приема лекарств, таких как психотропные препараты, наркотики, бензодиазепины, нейролептики и антидепрессанты. Повысьте безопасность в доме, улучшив освещение, убрав беспорядок и препятствия, избегая скользких полов, используйте нескользящие коврики, установите поручни в ванной и поручни на лестницах.Протекторы для бедер могут помочь тем, кто склонен к падению, но они плохо соблюдают правила.
Фармакологическая терапия
Фармакологическое вмешательство следует рассматривать у всех пациентов с остеопорозом, с остеопоротическими переломами или с высоким риском переломов.
Риск перелома:
Риск перелома может быть определен путем сочетания МПК с клиническими факторами риска. В 2008 году Всемирная организация здравоохранения выпустила инструмент оценки риска переломов (FRAX). Это доступно на www.shef.ac.uk/FRAX и учитывает клинические факторы риска и МПК шейки бедренной кости при определении риска переломов. Он оценивает 10-летнюю вероятность переломов шейки бедра и серьезных остеопоротических переломов у нелеченного человека. Клинические факторы риска включают возраст, индекс массы тела, предыдущие переломы в анамнезе, переломы шейки бедра у родителей, терапию глюкокортикоидами, текущее курение сигарет, употребление алкоголя, ревматоидный артрит и вторичный остеопороз. В расчетах используется плотность кости шейки бедра.
Рекомендации по лечению женщин в постменопаузе (Национальный фонд остеопороза)
Перелом бедра или позвоночника.
T-оценка -2,5 или ниже по позвоночнику, шейке бедра или общее количество hp
Т-балл от -1,0 до -2,5 и высокий 10-летний риск перелома с использованием адаптированного для США инструмента FRAX. Лечите, если 10-летний риск составляет 3% или более для переломов бедра или 20% и более для серьезных переломов, связанных с остеопорозом
Бисфосфонаты
Для лечения постменопаузального остеопороза бисфосфонаты являются терапией первой линии. Они увеличивают плотность костей и снижают риск переломов позвоночника, бедра и невертебральных переломов.Бисфосфонаты обычно безопасны и хорошо переносятся. Их клинически применяли для лечения остеопороза с тех пор, как алендронат был впервые одобрен в 1995 году.
Бисфосфонаты представляют собой синтетические аналоги пирофосфата, которые связываются с гидроксиапатитом в кости и ингибируют резорбцию костной ткани остеокластами.
Бисфосфонаты для приема внутрь плохо всасываются, обычно менее 1%. Их следует принимать натощак, запивая 8 унциями простой воды. Пациенты должны оставаться в вертикальном положении в течение 30 минут (60 минут для ибандроната) и избегать еды, питья (кроме простой воды) и приема других лекарств в течение этого времени.
Пациенты не должны получать бисфосфонаты, если они проявляют к ним гиперчувствительность или гипокальциемию, пока это не будет исправлено. Он также не рекомендуется пациентам с клиренсом креатинина <35 мл / мин.
Пероральные бисфосфонаты следует применять с осторожностью пациентам с проблемами верхних отделов ЖКТ (например, рефлюксом). Их не следует назначать пациентам с пищеводом Барретта, варикозным расширением вен пищевода или тем, у кого есть аномалии, задерживающие транзит таблетки (например, ахалазия или стриктуры).
Внутривенные бисфосфонаты (ибандронат и золедроновая кислота) могут вызывать симптомы острой фазы у 30–35% пациентов, получивших первую дозу. Эти реакции включают жар, боли в мышцах и суставах, симптомы гриппа и головную боль. Они временные, обычно возникают в течение первых 24 часов и длятся 24-72 часа (иногда дольше). Эти симптомы менее вероятны, если ранее был назначен пероральный бисфосфонат, а частота этих симптомов острой фазы заметно снижается при последующих инфузиях.
У некоторых пациентов, получающих бисфосфонаты, на любом этапе лечения могут развиться боли в мышцах, суставах и костях.
Остеонекроз челюсти (ONJ) редко возникает при лечении остеопороза бисфосфонатами. ONJ — это наличие обнаженной кости в челюстно-лицевой области, которая не заживает в течение 8 недель после идентификации врачом. Это наблюдается в первую очередь у онкологических больных, получающих бисфосфонаты внутривенно в дозах, гораздо более высоких (в 10-12 раз), чем при лечении остеопороза.Факторы риска включают инвазивные стоматологические процедуры, плохую гигиену полости рта и другие стоматологические проблемы. Пациенты должны позаботиться о серьезных стоматологических проблемах до начала терапии бисфосфонатами и соблюдать надлежащую гигиену зубов с регулярным наблюдением.
Сообщалось об атипичных переломах бедренной кости подвертельной области и диафиза бедренной кости при применении бисфосфонатов. Хотя они встречаются редко, они более вероятны при более длительной терапии. Они могут быть двусторонними. Механизм не ясен, но может быть связан с чрезмерным подавлением метаболизма кости, что не позволяет восстановить микротрещины.Иногда пациенты жалуются на боль в ноге или ноющее ощущение перед переломом, и это может быть связано с нераспознанным стрессовым переломом.
Алендронат
Алендронат (Fosamax), теперь также в форме дженерика, одобрен Управлением по контролю за продуктами и лекарствами (FDA) для следующих веществ:
Профилактика постменопаузального остеопороза: 5 мг перорально ежедневно, 35 мг перорально еженедельно
Лечение постменопаузального остеопороза: 10 мг перорально ежедневно, 70 мг перорально еженедельно
Лечение остеопороза, вызванного глюкокортикоидами, у мужчин и женщин с повышенным уровнем эстрогена: 5 мг внутрь ежедневно
Лечение остеопороза, вызванного глюкокортикоидами, у женщин с дефицитом эстрогена: 10 мг перорально ежедневно
Лечение остеопороза у мужчин: 10 мг перорально ежедневно, 70 мг перорально еженедельно
Алендронат увеличивает МПК в позвоночнике и бедре и предотвращает потерю костной массы в предплечье.Снижает риск перелома позвоночника, бедра и непозвоночных участков.
Наиболее частыми побочными эффектами являются верхние отделы желудочно-кишечного тракта с изжогой, несварением желудка и затрудненным глотанием. В одном отчете после прекращения приема алендроната через 5 лет наблюдается медленное снижение плотности костей, но через 10 лет МПК все еще выше исходного уровня, а частота переломов аналогична 10-летнему лечению, за исключением более высокой частоты клинических переломов позвонков. . Однако женщины с тяжелым остеопорозом были исключены из исследования.
Ризедронат
Ризедронат (Актонел) одобрен FDA для следующих целей:
Профилактика постменопаузального остеопороза: 5 мг перорально ежедневно, 35 мг перорально еженедельно, 150 мг перорально ежемесячно
Лечение постменопаузального остеопороза: 5 мг перорально ежедневно, 35 мг перорально еженедельно, 150 мг перорально ежемесячно
Профилактика остеопороза, вызванного глюкокортикоидами: 5 мг внутрь ежедневно
Лечение остеопороза, вызванного глюкокортикоидами: 5 мг перорально ежедневно
Лечение остеопороза у мужчин: 35 мг перорально еженедельно, 150 мг перорально ежемесячно
Ризедронат увеличивает МПК в позвоночнике и бедре и предотвращает потерю костной массы в предплечье.Снижает риск переломов позвоночника, бедра и непозвоночных участков.
После прекращения приема ризедроната может произойти медленная потеря костной массы, и через 1 год показатели метаболизма костной ткани вернутся к исходному уровню.
Наиболее частые побочные эффекты связаны с системой верхних отделов ЖКТ.
Ибандронат
Ибандронат (Boniva) одобрен FDA для следующих целей:
Профилактика постменопаузального остеопороза: 2,5 мг перорально ежедневно, 150 мг перорально ежемесячно
Лечение постменопаузального остеопороза: 2.5 мг перорально ежедневно, 150 мг перорально ежемесячно, 3 мг внутривенно каждые 3 месяца
Ибандронат снижает риск переломов позвоночника у женщин с постменопаузальным остеопорозом, но в проспективных исследованиях не показал снижения непозвоночных переломов или переломов бедра. В ретроспективном анализе пациентов с Т-оценкой шейки бедренной кости ниже -3,0 было отмечено снижение риска переломов, не связанных с позвонками.
Ибандронат увеличивает МПК в позвоночнике и бедре и предотвращает потерю костной массы в предплечье.
Побочные эффекты обычно затрагивают верхние отделы желудочно-кишечного тракта.
Золедроновая кислота
Золедроновая кислота (Рекласт) одобрена FDA для следующих веществ:
Профилактика постменопаузального остеопороза: 5 мг внутривенно каждые два года
Лечение постменопаузального остеопороза: 5 мг внутривенно один раз в год
Профилактика остеопороза, вызванного глюкокортикоидами: 5 мг внутривенно один раз в год
Лечение остеопороза, вызванного глюкокортикоидами: 5 мг внутривенно один раз в год
Лечение остеопороза у мужчин: 5 мг внутривенно один раз в год
После хирургического лечения перелома шейки бедра: 5 мг внутривенно 1 раз в год
Золедроновая кислота снижает риск переломов позвоночника, бедра и невертебральных переломов.Это также снижает частоту новых клинических переломов у пациентов, получавших хирургическое лечение перелома бедра, и снижает смертность у этих пациентов с переломом бедра. Золедроновая кислота увеличивает МПК в позвоночнике и бедре.
Симптомы острой фазы (лихорадка, боли в мышцах и суставах, симптомы гриппа) были зарегистрированы у 32% субъектов после первой инфузии; 7% после второго и 3% после третьего. Пациенты должны получать достаточное количество жидкости, могут принимать парацетамол или нестероидные противовоспалительные средства и должны продолжать прием кальция и витамина D.Перед инфузией следует проверить сывороточный кальций и креатинин.
Потенциальная проблема остеохондроза нижней челюсти описывалась в основном у пациентов, которые получали бисфосфонаты внутривенно при метастазах в скелет у онкологических больных в дозе, намного превышающей дозу, назначаемую при остеопорозе.
Ралоксифен
Ралоксифен (Evista) — это селективный модулятор рецепторов эстрогена (SERM), который действует на различные ткани как агонист или антагонист эстрогена. Ралоксифен одобрен FDA для профилактики и лечения постменопаузального остеопороза, а также для снижения риска инвазивного рака груди у женщин с постменопаузальным остеопорозом или с высоким риском рака груди.Доза составляет 60 мг внутрь ежедневно, и ее можно принимать в любое время дня, независимо от приема пищи.
Ралоксифен снижает риск переломов позвоночника у женщин с постменопаузальным остеопорозом, но не переломов бедра или непозвонков. Увеличивает МПК в позвоночнике и бедре. Побочные эффекты включают приливы, ночную потливость, мышечные и суставные боли и судороги ног. Заболеваемость венозной тромбоэмболией увеличивается в 3 раза, как и при приеме эстрогена.
Нет положительных или отрицательных эффектов на сердечно-сосудистую систему.Также не наблюдается увеличения цереброваскулярных событий, хотя в большом исследовании было отмечено общее увеличение числа смертельных инсультов.
Безопасность определена на срок до 8 лет. После прекращения приема ралоксифена положительный эффект теряется через 1-2 года.
Терипаратид
Терипаратид (Фортео) представляет собой фрагмент рекомбинантного человеческого ПТГ (1-34) и является единственным анаболическим средством, доступным для лечения постменопаузального остеопороза. Он одобрен FDA для следующего:
Лечение постменопаузального остеопороза: 20 микрограмм SQ в день
Лечение остеопороза, вызванного глюкокортикоидами: 20 мкг SQ в день
Лечение остеопороза у мужчин: 20 мкг SQ в день
Терипаратид уменьшает количество переломов позвонков и непозвонков у женщин с постменопаузальным остеопорозом.Он увеличивает МПК позвоночника, но мало влияет на плотность бедер или предплечий.
Побочные эффекты легкие и преходящие, включая тошноту, ортостатическую гипотензию, судороги ног и небольшое повышение уровня кальция в сыворотке крови в течение нескольких часов после инъекции.
Это предупреждение в виде черного ящика, потому что у крыс, которым вводили дозы терипаратида, в 60 раз превышающие дозу, назначаемую при остеопорозе у людей, наблюдалось увеличение остеосаркомы. Этого не наблюдалось у людей, получавших терипаратид. Скелет крысы отличается от человеческого.Он растет на протяжении всей своей жизни (а не переделывается у людей), и если терипаратид вводится в возрасте от 2 недель до 6 месяцев, то в конечном итоге его назначают более чем на 75% от 2-летней продолжительности жизни крыс по сравнению с 2- 3% для человека. По этой причине терипаратид противопоказан пациентам с повышенным исходным риском остеосаркомы; Костная болезнь Педжета, открытый эпифиз, облучение скелета в анамнезе или необъяснимое повышение уровня щелочной фосфатазы.
По данным крыс, терипаратид не рекомендуется применять более 2 лет.Он доступен для лечения более 10 лет.
После прекращения приема терипаратида МПК снижается в следующем году, но снижение риска переломов может продолжаться. После лечения терипаратидом введение антирезорбтивного агента, такого как бисфосфонаты, может помочь предотвратить потерю костной массы и сохранить прирост.
Кальцитонин
Кальцитонин для инъекций и назальный спрей одобрен FDA для лечения постменопаузального остеопороза. Кальцитонин для инъекций вводится в виде 100 МЕ в сутки SQ или IM.Назальный спрей (Миакальцин, Фортикал) по 200 МЕ в день.
Назальный спрей кальцитонин лосося снижает риск переломов позвонков, но не переломов бедра или непозвоночных переломов. При введении кальцитонина для инъекций не наблюдалось уменьшения переломов.
Кальцитонин вызывает небольшое увеличение МПК позвоночника, но не других участков.
Потеря костной массы происходит быстро после прекращения приема.
деносумаб
Деносумаб (Prolia) — человеческое моноклональное антитело против RANKL (лиганд RANK).Это снижает дифференцировку клеток-предшественников в зрелые остеокласты и снижает функцию и выживаемость активированных остеокластов.
Деносумаб одобрен FDA для следующего:
Деносумаб уменьшает переломы позвоночника, бедра и непозвоночные переломы. Он увеличивает МПК в позвоночнике, бедре и предплечье.
Побочные эффекты включают небольшое увеличение числа серьезных инфекций, таких как кожные инфекции, которые не увеличиваются при продолжении использования. О ONJ сообщалось в основном, когда деносумаб давали пациентам с раком в более высоких дозах, чем при остеопорозе.
После прекращения приема МПК снизилась до исходного уровня, а маркеры метаболизма костной ткани увеличились на 12 месяцев.
Он не влияет на функцию почек и может назначаться пациентам с нарушением функции почек.
Заместительная терапия эстрогенами / гормонами
Эстроген одобрен для профилактики остеопороза. Не одобрен для лечения. Основная причина назначения эстрогена — лечение симптомов менопаузы.
Доступно множество различных составов эстрогенов.Если матка не повреждена, то следует назначить прогестин, в противном случае эстроген без сопротивления связан с повышенным риском гиперплазии эндометрия и рака.
Было показано, что конъюгированный конский эстроген снижает риск переломов позвоночника, непозвоночных переломов и переломов бедра. Эстроген также увеличивает МПК в позвоночнике, бедре и предплечье.
Существуют серьезные разногласия относительно побочных эффектов заместительной гормональной терапии. В Инициативе по охране здоровья женщин (WHI) комбинация эстрогена и прогестина вызвала повышенный риск рака груди, сердечно-сосудистых событий, тромбоэмболических и цереброваскулярных событий.В исследовании WHI только с эстрогенами не было отмечено увеличения риска сердечно-сосудистых событий или рака груди.
Терапия эстрогенами увеличивает риск холелитиаза, задержки жидкости, головных болей и в 3 раза увеличивает количество тромбоэмболических событий.
Эффект сохраняется только до тех пор, пока продолжается лечение, и ускоренная потеря костной массы происходит, как только лечение прекращается.
Что такое неответчик?
Значительное снижение МПК (большее, чем наименее значимое изменение) или новый перелом можно считать неответчиком.Однако у этих пациентов могла быть большая потеря костной массы или больше переломов, если бы они не получали лечения, и, следовательно, могли показать некоторую пользу от лечения. В этих двух условиях должна быть проведена оценка соответствия лечению, оценка вторичных причин потери костной массы и пересмотр изменения режима лечения.
Если при пероральном приеме препарата возникают проблемы с абсорбцией, и кто-то хочет продолжить прием бисфосфоната, перейдите на внутривенное введение бисфосфоната.Также можно использовать парентеральный деносумаб. Если вы принимаете ралоксифен, подумайте о переходе на бисфосфонат. Деносумаб или терипаратид также можно использовать при очень низкой МПК. Если вы принимаете бисфосфонат, подумайте о переходе на анаболический агент, терипаратид.
Как долго лечить?
Нет ни единого мнения, ни каких-либо последовательных данных о продолжительности лечения или о том, когда возобновить терапию после наркологического отпуска. Идея отпуска от лекарств заключается в том, что лекарства, такие как бисфосфонаты, сохраняются в скелете от месяцев до лет, и, дав отпуск, вы все равно увидите положительный эффект, но уменьшите вероятность некоторых побочных эффектов, наблюдаемых при длительном лечении. терапия.
Разумно рассмотреть вопрос о том, чтобы пациенты с остеопорозом от легкой до умеренной степени без перелома взяли перерыв в лечении после 5 лет лечения и пересмотрели возможность возобновления лечения через несколько лет, когда есть доказательства снижения МПК или нового перелома.
У пациентов с тяжелым остеопорозом и переломами можно рассмотреть возможность отпуска после 10 лет лечения и возобновления терапии через 1-2 года или при наличии свидетельств снижения МПК или нового перелома.
Во время отпуска по наркотикам следует рассмотреть возможность использования агента из другого класса.
Какие доказательства? / Ссылки
Вт, NB, Билезикян, JP, Камачо, PM, Гринспен, SL, Харрис, ST. «Медицинские рекомендации Американской ассоциации клинических эндокринологов для клинической практики по диагностике и лечению постменопаузального остеопороза». Эндокринная практика. об. 16. 2010. С. 1-37. (Подробный и обширный обзор с большим списком ссылок.)
«Ведение остеопороза у женщин в постменопаузе: Заявление о позиции 2010 г. Североамериканского общества менопаузы». Менопауза. об. 17. 2010. С. 25-54. (Обновление предыдущего заявления о позиции NAMS от 2006 г. Подробный и обширный обзор с большим списком ссылок.)
«Заявление о позиции Североамериканского общества по менопаузе в 2012 году в отношении гормональной терапии». Менопауза. об. 19. 2012. С. 257–271. (Обсуждается влияние гормональной терапии на многие аспекты здоровья женщины).
Брауэр, Калифорния, Кока-Перрайон, М., Катлер, DM, Розен, AB. «Заболеваемость и смертность от переломов шейки бедра в США». JAMA. об. 302. 2009. С. 1573-9. (В США частота переломов шейки бедра и последующая смертность среди людей 65 лет и старше снижается.)
Tang, BMP, Eslick, GD, Nowson, C, Smith, C, Bensoussan, A. «Использование кальция или кальция в сочетании с добавками витамина D для предотвращения переломов и потери костной массы у людей в возрасте 50 лет и старше: мета анализ». Ланцет. об. 370. 2007. С. 657-66. (Мета-анализ 17 исследований показал, что при дозах кальция 1200 мг и витамина D не менее 800 МЕ наблюдается снижение частоты переломов и увеличение минеральной плотности костей.)
Росс, А.С., Мэнсон, Дж. Э., Абрамс, С. А., Алоя, Дж. Ф., Браннон, П. М.. «Отчет Института медицины о рекомендуемом потреблении кальция и витамина D с пищей за 2011 год: что необходимо знать врачам». J Clin Endocrinol Metab. об. 96. 2011. С. 53-8. (Резюме с обоснованием недавнего отчета МОМ.)
Rosen, CJ. «Недостаточность витамина D». N Engl J Med. об. 364. 2011. С. 248-54. (Хорошее обсуждение нашего понимания и неуверенности в отношении уровней витамина D и добавок.)
Khosla, S, Burr, D, Cauley, J. «Бисфосфонат-ассоциированный остеонекроз челюсти: отчет рабочей группы Американского общества исследований костей и минералов». J Bone Miner Res. об. 22. 2007. С. 1479–91. (Обсуждение с определением, факторами риска и клиническими последствиями.)
Шейн, Э, Берр, Д., Эберлинг, ПР, Абрахамсен, Б., Адлет, РА. «Атипичные подквертельные и диафизарные переломы бедренной кости: отчет рабочей группы Американского общества исследований костей и минералов». J Bone Miner Res. об. 25. 2010. С. 2267–94. (Подробное обсуждение атипичных переломов бедренной кости, включая возможную связь с длительным приемом бисфосфонатов, механизмы, клинические проявления и необходимость в дополнительной информации.)
Black, DM, Schwartz, AV, Ensrud, KE, Cauley, JA, Levis, S. «Эффекты продолжения или прекращения приема алендроната после 5 лет лечения. Долгосрочное продление исследования по лечению переломов (FLEX): рандомизированное исследование ». JAMA. об. 296.2006. С. 2927-38. (Прекращение приема алендроната через 5 лет показало умеренное снижение МПК и постепенное повышение маркеров метаболизма костной ткани, но не более высокий риск переломов, кроме клинических переломов позвонков, по сравнению с теми, кто продолжал прием алендроната в течение 10 лет.)
Вт, NB, Diab, DL. «Длительное применение бисфосфонатов при остеопорозе». J Clin Endocrinol Metab. об. 95. 2010. С. 1555–65. (Они рекомендуют лекарственный отпуск после 5-10 лет лечения в зависимости от риска перелома.Пациенты с низким риском могут оставаться на лечении до тех пор, пока МПК стабильна и не возникают переломы. Пациенты с более высоким риском снова начинают лечение после 1-2-летнего перерыва.)
Уитакер, М., Го, Дж., Кехоу, Т., Бенсон, Г. «Бисфосфонаты при остеопорозе. Куда мы будем двигаться дальше?». N Engl J Med. об. 366. 2012. С. 2048-2051. (FDA рассмотрело долгосрочную эффективность и безопасность бисфосфонатов. Они предложили обновить маркировку, но не ограничили продолжительность использования нормативными требованиями.)
Блэк, Д.М., Бауэр, округ Колумбия, Шварц, А.В., Каммингс, С.Р., Розен, С.Дж.«Продолжение лечения остеопороза бисфосфонатами — для кого и как долго». N Engl J Med. об. 366. 2012. С. 2051-2053. (Предложите рекомендации по прекращению или продолжению приема бисфосфонатов через 3-5 лет лечения.)
Weinstein, RS. «Заболевание костей, вызванное глюкокортикоидами». N Engl J Med. об. 365. 2011. С. 62–70. (Обзор подхода и лечения этой общей клинической проблемы.)
Лобо, РА. «Где мы находимся через 10 лет после Инициативы по охране здоровья женщин». J Clin Endocrinol Metab. об. 98. С. 1771-1780.
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
Лечение остеопороза: лекарства могут помочь
Лечение остеопороза: лекарства могут помочь
Лечение остеопороза может включать прием лекарств наряду с изменением образа жизни.Получите ответы на некоторые из самых распространенных вопросов о лечении остеопороза.
Персонал клиники МэйоЕсли вы проходите курс лечения остеопороза, вы делаете шаг в правильном направлении для здоровья своих костей. Но, возможно, у вас есть вопросы по поводу вашей терапии. Подходит ли вам лекарство, которое вы принимаете? Как долго тебе придется это принимать? Почему ваш врач рекомендует еженедельно принимать таблетки, если ваш друг принимает таблетку только раз в месяц?
Какие лекарства от остеопороза обычно пробуют в первую очередь?
Бисфосфонаты обычно являются препаратами первого выбора для лечения остеопороза.К ним относятся:
- Алендронат (Фосамакс), еженедельная таблетка
- Ризедронат (Актонел), еженедельно или ежемесячно
- Ибандронат (Бонива), ежемесячная таблетка или ежеквартальная внутривенная (IV) инфузия
- Золедроновая кислота (Рекласт), годовая инфузия IV
Другой распространенный препарат от остеопороза — деносумаб (Prolia, Xgeva). Не связанный с бисфосфонатами, деносумаб может применяться у людей, которые не могут принимать бисфосфонаты, например у некоторых людей с пониженной функцией почек.
Деносумаб вводится мелкими инъекциями, прямо под кожу, каждые шесть месяцев. Если вы принимаете деносумаб, вам, возможно, придется делать это на неопределенный срок, если ваш врач не переведет вас на другой препарат. Недавние исследования показывают, что после прекращения приема препарата может возникнуть высокий риск переломов позвоночника, поэтому важно, чтобы вы принимали его постоянно.
Каковы общие побочные эффекты таблеток бисфосфоната?
Основными побочными эффектами таблеток бисфосфонатов являются расстройство желудка и изжога.Не ложитесь и не наклоняйтесь в течение 30-60 минут, чтобы лекарство не попало обратно в пищевод. Большинство людей, которые следуют этим советам, не имеют этих побочных эффектов.
Таблетки бисфосфоната плохо всасываются желудком. Может помочь прием лекарства натощак, запивая стаканом воды. Не кладите больше ничего в желудок в течение 30-60 минут, после чего вы можете есть, пить другие жидкости и принимать другие лекарства.
Есть ли преимущества у бисфосфонатов для внутривенного введения по сравнению с таблетками?
Внутривенные формы бисфосфонатов, такие как ибандронат и золедроновая кислота, не вызывают расстройства желудка.Некоторым людям может быть проще запланировать ежеквартальную или ежегодную инфузию, чем не забывать принимать еженедельные или ежемесячные таблетки.
Внутривенные бисфосфонаты вызывают у некоторых людей легкие симптомы гриппа, но обычно только после первой инфузии. Вы можете уменьшить эффект, приняв ацетаминофен (тайленол и другие) до и после инфузии.
Могут ли лекарства от остеопороза повредить кости?
Очень редкое осложнение приема бисфосфонатов и деносумаба — перелом или трещина в середине бедренной кости.Эта травма, известная как атипичный перелом бедренной кости, может вызвать легкую боль в бедре или паху, которая может постепенно усиливаться.
Бисфосфонаты и деносумаб также могут вызывать остеонекроз челюсти — редкое состояние, при котором часть челюстной кости заживает медленно или не заживает, обычно после удаления зуба или другой инвазивной стоматологической операции. Это чаще встречается у людей с раком, поражающим кость, которые принимают гораздо большие дозы бисфосфонатов, чем те, которые обычно используются при остеопорозе.
Следует ли мне взять отпуск от приема бисфосфонатов?
Риск развития атипичного перелома бедренной кости или остеонекроза челюсти, как правило, увеличивается с увеличением продолжительности приема бисфосфонатов. Поэтому ваш врач может предложить вам временно прекратить прием этого типа лекарств. Эта практика известна как наркологический отпуск.
Однако, даже если вы прекратите прием лекарства, его положительные эффекты могут сохраниться. Это потому, что после нескольких лет приема бисфосфонатов лекарство остается в вашей кости.
Из-за этого продолжающегося эффекта большинство экспертов считают, что для людей, которые хорошо себя чувствуют во время лечения — тех, у кого нет переломов костей и которые сохраняют плотность костей — разумно отказаться от приема бисфосфоната после его приема в течение пяти лет.
Используются ли гормоны для лечения остеопороза?
Эстроген, иногда в сочетании с прогестином, когда-то широко использовался для лечения остеопороза. Это лечение может увеличить риск образования тромбов, рака эндометрия, рака груди и, возможно, сердечных заболеваний.Сейчас он обычно предназначен для женщин с высоким риском переломов, которые не могут принимать другие препараты от остеопороза.
Женщины, которые рассматривают заместительную гормональную терапию для уменьшения симптомов менопаузы, таких как приливы, могут учитывать улучшение здоровья костей при оценке преимуществ и рисков лечения эстрогенами. Текущие рекомендации говорят, что нужно использовать минимальную дозу гормонов в течение самого короткого периода времени.
Ралоксифен (Эвиста) имитирует благотворное влияние эстрогена на плотность костей у женщин в постменопаузе, без некоторых рисков, связанных с эстрогеном.Прием этого препарата может снизить риск некоторых видов рака груди. Приливы — частый побочный эффект. Ралоксифен также может увеличить риск образования тромбов.
Как действуют лекарства от остеопороза?
На протяжении всей жизни здоровые кости постоянно ломаются и восстанавливаются. С возрастом — особенно после менопаузы — кости разрушаются быстрее. Поскольку восстановление костей не успевает за темпами, кости разрушаются и становятся слабее.
Большинство лекарств от остеопороза снижают скорость разрушения костей.Некоторые работают, ускоряя процесс наращивания костей. Любой из этих механизмов укрепляет кость и снижает риск переломов.
Какие лекарства помогают ускорить процесс наращивания костей?
К препаратам, строящим кости, относятся:
- Терипаратид (Фортео)
- Абалопаратид (Тимлос)
- Ромосозумаб (четность)
Эти типы лекарств обычно предназначены для людей с очень низкой плотностью костей, у которых были переломы или у которых остеопороз вызван стероидными препаратами.
Терипаратид и абалопаратид требуют ежедневных инъекций. Исследования на лабораторных крысах показали увеличение риска рака костей, поэтому эти лекарства не используются у людей с высоким риском рака костей. До сих пор не было обнаружено увеличения заболеваемости раком костей у людей, принимавших эти лекарства.
Ромосозумаб вводится в виде ежемесячной инъекции в офисе вашего врача. Это новый препарат, и о долгосрочных побочных эффектах известно меньше, но его не назначают людям, недавно перенесшим инсульт или сердечный приступ.Лечение прекращается после 12 месячных доз.
Эти препараты для наращивания костей можно принимать только один или два года, и после прекращения приема их польза начинает быстро исчезать. Чтобы защитить образовавшуюся кость, вам нужно начать принимать стабилизирующие кости лекарства, такие как бисфосфонат.
Может ли остеопороз лечить только лекарство?
Не полагайтесь исключительно на лекарства как на единственное средство от остеопороза. Эти методы также важны:
- Упражнение. Физические нагрузки с отягощениями и упражнения, улучшающие равновесие и осанку, могут укрепить кости и снизить вероятность перелома. Чем больше вы активны и в хорошей форме с возрастом, тем меньше вероятность того, что вы упадете и сломаете кость.
- Полноценное питание. Соблюдайте здоровую диету и убедитесь, что вы получаете достаточно кальция и витамина D.
- Бросить курить. Курение сигарет ускоряет потерю костной массы.
- Ограничьте употребление алкоголя. Если вы решите употреблять алкоголь, делайте это умеренно.Для здоровых женщин это означает до одного напитка в день. Для здоровых мужчин это будет до двух порций в день.
- Остеопороз: углубленный. Национальный институт артрита, скелетно-мышечных и кожных заболеваний. https://www.niams.nih.gov/health-topics/osteoporosis/advanced. Проверено 9 июня 2020 г.
- Goldman L, et al., Eds. Остеопороз. В: Медицина Гольдмана-Сесила. 26-е изд. Эльзевир; 2020. https://www.clinicalkey.com.Проверено 9 июня 2020 г.
- Eastell R, et al. Фармакологическое лечение остеопороза у женщин в постменопаузе: Руководство по клинической практике эндокринного общества. Журнал эндокринологии и метаболизма. 2019; DOI: 10.1210 / jc2009-00221.
- Ferri FF. Остеопороз. В: Клинический советник Ферри 2020. Elsevier; 2020. https://www.clinicalkey.com. Проверено 9 июня 2020 г.
- Rosen HN, et al. Обзор лечения остеопороза у женщин в постменопаузе. https: // www.uptodate.com/contents/search. Проверено 9 июня 2020 г.
- Rosen HN. Риски терапии бисфосфонатами у пациентов с остеопорозом. https://www.uptodate.com/contents/search. Проверено 9 июня 2020 г.
- Bone HG, et al. 10 лет лечения деносумабом у женщин в постменопаузе с остеопорозом: результаты рандомизированного исследования FREEDOM фазы 3 и открытого расширения. Ланцетный диабет и эндокринология. 2017; DOI: 10.1016 / S2213-8587 (17) 30138-9.
- Кернс А.Е. (заключение эксперта).Клиника Майо. 15 июня 2020 г.
Продукция и услуги
- Книга: Руководство Mayo Clinic по профилактике и лечению остеопороза
- Книга: Mayo Clinic The Menopause Solution
.
Остеопороз — Диагностика и лечение
Диагноз
Плотность вашей кости можно измерить с помощью аппарата, который использует низкие уровни рентгеновского излучения для определения доли минералов в ваших костях.Во время этого безболезненного теста вы лежите на мягком столе, пока сканер проходит по вашему телу. В большинстве случаев проверяется только несколько костей — обычно в области бедра и позвоночника.
Дополнительная информация
Показать дополнительную информациюЛечение
Рекомендации по лечению часто основываются на оценке вашего риска перелома кости в следующие 10 лет с использованием такой информации, как тест на плотность кости. Если ваш риск невысок, лечение может не включать лекарство, а вместо этого может быть сосредоточено на изменении факторов риска потери костной массы и падений.
Биофосфонаты
Как для мужчин, так и для женщин с повышенным риском переломов наиболее широко назначаемыми лекарствами от остеопороза являются бисфосфонаты. Примеры включают:
- Алендронат (Биносто, Фосамакс)
- ризедронат (Actonel, Atelvia)
- Ибандронат (Бонива)
- Золедроновая кислота (Рекласт, Зомета)
Побочные эффекты включают тошноту, боль в животе и симптомы, похожие на изжогу. Это менее вероятно, если лекарство будет принято правильно.
Внутривенные формы бисфосфонатов не вызывают расстройства желудка, но могут вызывать жар, головную боль и боли в мышцах на срок до трех дней. Может быть проще запланировать ежеквартальную или ежегодную инъекцию, чем не забывать принимать еженедельные или ежемесячные таблетки, но это может быть дороже.
Лекарства с моноклональными антителами
По сравнению с бисфосфонатами деносумаб (Prolia, Xgeva) дает аналогичные или лучшие результаты по плотности костей и снижает вероятность всех типов переломов.Деносумаб вводится каждые шесть месяцев в виде инъекции под кожу.
Если вы принимаете деносумаб, возможно, вам придется продолжать принимать это бесконечно. Недавние исследования показывают, что после прекращения приема препарата может возникнуть высокий риск переломов позвоночника.
Очень редкое осложнение приема бисфосфонатов и деносумаба — перелом или трещина в середине бедренной кости.
Второе редкое осложнение — задержка заживления челюстной кости (остеонекроз челюсти). Это может произойти после инвазивной стоматологической процедуры, такой как удаление зуба.
Перед началом приема этих лекарств вам следует пройти стоматологическое обследование, и вы должны продолжать хорошо заботиться о своих зубах и регулярно посещать стоматолога, пока они принимают их. Убедитесь, что стоматолог знает, что вы принимаете эти лекарства.
Гормональная терапия
Эстроген, особенно если его начать вскоре после менопаузы, может помочь сохранить плотность костей. Однако терапия эстрогенами может увеличить риск образования тромбов, рака эндометрия, рака груди и, возможно, сердечных заболеваний.Следовательно, эстроген обычно используется для здоровья костей у молодых женщин или у женщин, симптомы менопаузы которых также требуют лечения.
Ралоксифен (Эвиста) имитирует благотворное влияние эстрогена на плотность костей у женщин в постменопаузе, без некоторых рисков, связанных с эстрогеном. Прием этого препарата может снизить риск некоторых видов рака груди. Приливы — частый побочный эффект. Ралоксифен также может увеличить риск образования тромбов.
У мужчин остеопороз может быть связан с постепенным возрастным снижением уровня тестостерона.Заместительная терапия тестостероном может помочь улучшить симптомы низкого уровня тестостерона, но лекарства от остеопороза лучше изучены для лечения остеопороза у мужчин, поэтому их рекомендуют отдельно или в дополнение к тестостерону.
Лекарства, укрепляющие кости
Если вы не переносите более распространенные методы лечения остеопороза или если они недостаточно эффективны, ваш врач может предложить попробовать:
- Терипаратид (Фортео). Этот мощный препарат похож на гормон паращитовидной железы и стимулирует рост новых костей.Его вводят ежедневно под кожу. После двух лет лечения терипаратидом принимается еще один препарат от остеопороза для поддержания роста новой кости.
- Абалопаратид (Тимлос) — еще один препарат, похожий на гормон паращитовидной железы. Вы можете принимать его только два года, после чего последуют еще одно лекарство от остеопороза.
- Ромосозумаб (Четность). Это новейший костный препарат для лечения остеопороза. Его делают ежемесячно в кабинете врача в виде инъекции.Он ограничен одним годом лечения, за которым следует прием других лекарств от остеопороза.
Дополнительная информация
Показать дополнительную информациюКлинические испытания
Изучите исследования клиники Мэйо, в которых тестируются новые методы лечения, вмешательства и тесты как средства предотвращения, обнаружения, лечения или контроля этого состояния.
Образ жизни и домашние средства
Эти рекомендации могут помочь снизить риск развития остеопороза или перелома костей:
- Не курите. Курение увеличивает скорость потери костной массы и вероятность переломов.
- Избегайте чрезмерного употребления алкоголя. Употребление более двух алкогольных напитков в день может уменьшить образование костей. Пребывание в состоянии алкогольного опьянения также может увеличить риск падения.
- Предотвращение падений. Носите обувь на низком каблуке с нескользящей подошвой и проверяйте свой дом на наличие электрических шнуров, ковриков и скользких поверхностей, которые могут стать причиной падения. Держите комнаты ярко освещенными, установите поручни внутри и снаружи двери душа и убедитесь, что вы легко можете залезть в кровать и выйти из нее.
Альтернативная медицина
Имеются ограниченные доказательства того, что определенные добавки, такие как витамин K-2 и соя, могут помочь снизить риск переломов при остеопорозе, но необходимы дополнительные исследования, чтобы доказать преимущества и определить риски.
Подготовка к приему
Ваш семейный врач может посоветовать проверить плотность костной ткани. Скрининг на остеопороз рекомендуется всем женщинам к 65 годам. Некоторые руководящие принципы также рекомендуют обследовать мужчин к 70 годам, особенно если у них есть проблемы со здоровьем, которые могут вызвать остеопороз.Если у вас сломана кость после незначительной силовой травмы, такой как простое падение, плотность кости может быть важна для оценки риска повторных переломов.
Если результаты теста на плотность костной ткани сильно отклоняются от нормы или у вас есть другие сложные проблемы со здоровьем, вас могут направить к врачу, специализирующемуся на нарушениях обмена веществ (эндокринолог), или к врачу, специализирующемуся на заболеваниях суставов, мышц или костей (ревматолог).
Вот некоторая информация, которая поможет вам подготовиться к встрече.
Что вы можете сделать
- Запишите симптомы, которые вы заметили, , хотя, возможно, у вас их может и не быть.
- Запишите ключевую личную информацию, , включая серьезные стрессы или недавние изменения в жизни.
- Составьте список всех лекарств, витаминов и добавок, которые вы принимаете или принимали, включая дозы. Это особенно полезно, если вы записываете тип и дозу добавок кальция и витамина D, потому что доступно множество различных препаратов.Если вы не знаете, какая информация может понадобиться вашему врачу, возьмите флаконы с собой или сфотографируйте этикетку смартфоном и поделитесь ею с врачом.
- Запишите вопросы, которые вы можете задать своему врачу.
Основные вопросы, которые следует задать врачу при остеопорозе:
- Нужно ли мне проходить обследование на остеопороз?
- Какие методы лечения доступны и какие вы рекомендуете?
- Какие побочные эффекты можно ожидать от лечения?
- Есть ли альтернативы лечению, которое вы предлагаете?
- У меня другое состояние здоровья.Как мне лучше всего управлять ими вместе?
- Нужно ли мне ограничивать свои действия?
- Нужно ли мне менять диету?
- Нужно ли мне принимать добавки?
- Есть ли программа физиотерапии, которая принесет мне пользу?
- Что я могу сделать, чтобы не упасть?
Не стесняйтесь задавать другие вопросы.
Чего ожидать от врача
Ваш врач, скорее всего, задаст вам вопросы, например:
- Были сломаны кости?
- Вы стали короче?
- Как ваша диета, особенно потребление молочных продуктов? Как вы думаете, вы получаете достаточно кальция? Витамин Д?
- Как часто вы занимаетесь спортом? Какие упражнения ты делаешь?
- Как ваш баланс? Ты упал?
- Были ли у вас в семье случаи остеопороза?
- Родитель сломал бедро?
- Были ли у вас операции на желудке или кишечнике?
- Принимали ли вы кортикостероидные препараты (преднизон, кортизон) в виде таблеток, инъекций или кремов?
Постменопаузальный остеопороз: мини-обзор
ЭПИДЕМИОЛОГИЯ
Остеопороз — системное заболевание скелета, характеризующееся ухудшением микроархитектуры и высокой хрупкостью костной ткани, что приводит к низкой минеральной плотности костной ткани (МПК) и низкому качеству костей, что обычно связано с дефицитом эстрогена или старением. 1 Остеопороз обычно считается тихим заболеванием, пока он не осложняется системной болью, деформацией позвоночника, уменьшением роста и переломом из-за хрупкости. Хрупкость, или остеопороз, перелом — самое опасное осложнение остеопороза. Эти переломы могут возникнуть в результате незначительной травмы, но могут возникнуть и спонтанно. 1 В скелетной системе позвоночник, бедро и дистальный отдел предплечья являются областями, наиболее подверженными остеопоротическим переломам. В США> 9.У 9 миллионов человек диагностирован остеопороз и 43,1 миллиона человек находятся в состоянии остеопении. 2,3 Из них около 1,5 миллиона пациентов ежегодно получают переломы из-за хрупкости. 2,3 В Европе у 27,6 миллиона человек ежегодно диагностируется остеопороз, при этом> 3,5 миллиона из них ежегодно получают остеопоротические переломы. 3,4 По оценкам, до 2006 года примерно 69,4 миллиона человек в возрасте старше 50 лет страдали остеопорозом, а 2,1 миллиона человек в Китае страдали остеопенией. 5 Согласно эпидемиологическому исследованию населения Пекина, частота переломов позвоночника составляла около 15% у женщин старше 50 лет. 5 Кроме того, частота переломов шейки бедра резко увеличилась на 42% у мужчин и 110% у женщин в период 1990–1992 годов по сравнению с 2002–2006 годами. 5 Хрупкий перелом увеличивает инвалидность и смертность пациентов с остеопорозом; например, около 20% пациентов с хрупкими переломами умерли от различных осложнений в течение 1 года после перелома бедра, в то время как около половины выживших, перенесших перелом бедра, остались инвалидами. 5 Все вышеупомянутые факторы ложатся тяжелым социально-экономическим бременем во всем мире. Поскольку дефицит эстрогена представляет собой наиболее частую причину остеопороза, эта статья будет сосредоточена на теме постменопаузального остеопороза.
ПАТОФИЗИОЛОГИЯ ПОСТМЕНОПАУЗНОГО ОСТЕОПОРОЗА
Критическая роль дефицита эстрогенов в патогенезе остеопороза основана на том факте, что женщины в постменопаузе подвергаются наибольшему риску развития этого заболевания (рис. 1).Костный метаболизм у женщин в постменопаузе характеризуется высоким метаболизмом костной ткани, который определяется как одновременное увеличение резорбции костной ткани и образования костной ткани. 6 Однако резорбция кости превышает образование кости после менопаузы, что приводит к дисбалансу ремоделирования кости и быстрой чистой потере костной массы. 6 В первые 5 лет после менопаузы потеря костной массы происходит резко и в первую очередь в губчатой кости, в то время как в более поздние годы костная масса уменьшается медленнее и в основном затрагивает кортикальное и губчатое костное пространство, процесс, который может длиться> 10 лет . 7
В физиологических условиях непрерывное и гармоничное ремоделирование кости поддерживается за счет организованной последовательности резорбции кости с последующим образованием кости, что называется сцеплением остеокластов и остеобластов. Это партнерство развивается в ответ на двойное регулирование механической силы и эндокринных факторов. 8 Корпорация костного матрикса на основе кальция и коллагена I типа имеет решающее значение для опосредованного остеобластами образования кости, которое находится под контролем эндокринных факторов, особенно эстрогена. 8 Эстроген играет центральную роль в нормальном физиологическом ремоделировании; Дефицит эстрогена нарушает баланс остеокластогенеза и остеобластогенеза, что приводит к прогрессирующей потере костной массы (рис. 1).
Рецепторы эстрогена (OR) ORα и ORβ были обнаружены в остеобластах, остеокластах и остеоцитах. Ядерный рецептор ORα в первую очередь регулирует метаболизм костей. 7 После связывания со своим лигандом ORα рекрутирует коактиваторы или корепрессоры и соответственно модулирует транскрипцию эстроген-чувствительных генов-мишеней.Кроме того, ORα может взаимодействовать с факторами транскрипции, включая NFκB, и, как результат, подавлять свои собственные нижестоящие сигналы. 9 Остеобласты и остеокласты участвуют в изменениях судьбы клеток в ответ на дефицит эстрогена, таких как пролиферация, дифференцировка, запрограммированная гибель клеток и измененная экспрессия генов-мишеней.
Хорошо известно, что предшественники остеокластов экспрессируют активатор рецептора NF κB (RANK), тогда как остеобласты экспрессируют лиганд RANK (RANKL) и антагонист RANK остеопротегерин (OPG).С физиологической точки зрения эстроген регулирует остеокластогенез через основной путь передачи сигналов RANK / RANKL / OPG как in vitro , так и in vivo . 10,11 В отсутствие эстрогена усиленная перекрестная помеха между RANKL и RANK обеспечивает ключевой сигнал для ускорения созревания остеокластов и активации функции остеокластов. 12 Кроме того, сниженный антагонизм OPG к RANKL также способствует образованию и активации остеокластов. Кроме того, сообщалось, что воспалительная микросреда является решающим фактором для эстроген-опосредованной регуляции остеокластогенеза, например, эстроген поддерживает баланс ремоделирования костей за счет усиления апоптоза остеокластов, опосредованного повышенной продукцией TGF-β. 13 Однако в среде с дефицитом эстрогена образование остеокластов ускоряется повышением остеокластогенных провоспалительных цитокинов, включая IL-1, IL-6, IL-17 и TNF-α, которые негативно регулируются эстрогеном. 14
Костные морфогенетические белки (BMP), TGF-β, рецептор инсулиноподобного фактора роста 1 и путь WNT являются общепризнанными ключевыми сигналами, участвующими в регуляции остеобластогенеза и формировании костей, которые прямо или косвенно регулируются эстрогеном. 15 Эстроген положительно регулирует остеобластогенез, стимулируя выработку про-остеобластогенных факторов, таких как BMP, TGF-β, факторы роста фибробластов, инсулиноподобный фактор роста 1, паратироидный гормон и проколлаген, что способствует образованию остеобластов, активность и продолжительность жизни. 16
Недавно сообщалось, что плюрипотентные стволовые клетки играют решающую роль в регуляции функции и регенерации местных тканей. Мезенхимальные стволовые клетки (МСК) обычно рассматриваются как предшественники остеобластов, которые имеют решающее значение для поддержания баланса образования и резорбции кости или баланса образования кости и образования жира. 17 Остеогенная дифференцировка МСК регулируется сложной передачей сигналов. Например, функциональные дефекты путей ALP, ERK и FAS; 18 эпигенетический регуляторный фермент ЭЖ3; 19 и GCN5 20 вызывают дисфункцию МСК, последовательный дисбаланс костного метаболизма и окончательный остеопороз. Заболевания МСК в основном считаются ключевым патологическим фактором в развитии потери костной массы, вызванной дефицитом эстрогена. 21 Дефицит эстрогена вызывает хроническое воспаление (за счет стимуляции активности TNFα, IFN-γ, IL-1 и IL-6), которое блокирует функцию MSC и дополнительно инициирует остеопороз. 14 Более того, во время остеопоротического процесса микроРНК (миРНК) играют важную роль в регуляции функции МСК на посттранскрипционном уровне. Дефицит эстрогена изменяет профиль микроРНК МСК. микроРНК, такие как let-7, miR-17, 22 miR-26a, 23,24 miR-181a, 25 miR-705 и miR-3077, 26,27 могут положительно или отрицательно регулировать остеогенная дифференцировка развития МСК и остеопороза.
Кроме того, оксидативный стресс предлагался в качестве альтернативной этиологии остеопороза в течение примерно двух десятилетий. 28 Повышение уровня активных форм кислорода после дефицита эстрогена усиливает апоптоз остеобластов и блокирует выживание МСК и их функции. 29 Избыточное количество активных форм кислорода при постменопаузальном остеопорозе может быть в значительной степени приписано активации прооксидантной ферментной системы и ухудшению ферментативной антиоксидантной системы. Наблюдалось, что НАДФН-оксидаза 4 провоцируется, в то время как супероксиддисмутаза марганца и каталаза снижались во время постменопаузального остеопороза. 28,30,31 Восстановление баланса прооксидантной и антиоксидантной систем эффективно предотвращает потерю костной массы, вызванную дефицитом эстрогена.
Недавно микробиота кишечника была исследована как важный регулятор метаболических нарушений костей при остеопоротических заболеваниях. Модель мыши без микробов, помещенная в стерильную среду, использовалась для понимания взаимосвязи между микробиотой, здоровьем костей и системной асептикой. 32 Беспроблемные мыши показали более высокую плотность костей по сравнению с мышами, выращенными в обычных условиях, что позволяет предположить, что микробиом был тесно связан со здоровьем костей. 32 Аберрантная микробиота кишечника привела к потере костной массы, тогда как было продемонстрировано, что введение пробиотиков или антибиотиков спасает дегенерацию костей за счет модуляции иммунной системы, абсорбции кишечного кальция при остеопорозе, вызванном дефицитом эстрогена. 32 CD4 + Т-клетки и воспалительные факторы обычно рассматриваются как промоторы остеокластогенеза при дефиците эстрогена. 33 После лечения пробиотиками в костном мозге наблюдалось сильное снижение популяции CD4 + Т-клеток и воспалительных факторов. 32 Однако влияние микробиоты кишечника на здоровье костей сложное, и точные механизмы остаются неуловимыми.
ДИАГНОСТИКАПоказания для диагностики остеопороза
Остеопороз — болезнь тихая. Большинство пациентов с остеопорозом не осознают, что у них есть заболевание, пока не возникнут серьезные осложнения. Гинекологи или врачи семейной медицины обычно первыми сталкиваются с проблемой; Таким образом, им необходимы показания для подозрения на остеопороз, чтобы решить, следует ли направлять пациенток на тестирование МПК.Национальный фонд остеопороза США (NOF) сделал следующие рекомендации, выделяя наиболее подверженные риску: 1) женщин старше 65 лет, независимо от клинических факторов риска; 2) более молодые женщины в постменопаузе и женщины в менопаузальном переходе; 3) взрослые, перенесшие перелом после 50 лет; и 4) взрослые с заболеванием скелета или принимающие лекарства, связанные с низкой костной массой.
Традиционный диагностический режим
Нормированный показатель Т-шкалы 1–4 поясничных позвонков, бедра или шейки бедренной кости на основе МПКявляется международным золотым стандартом диагностики остеопороза на основе двухэнергетической рентгеновской абсорбциометрии (DXA).Т-балл рассчитывается по формуле: (МПК кандидата — пиковая МПК для населения того же пола) / стандартное отклонение максимальной МПК для населения того же пола. Кандидаты с T-баллом ≥-1,0 считаются здоровыми; Т-баллы от -2,5 до -1,0 диагностируются как остеопения; и показатель Т ≤-2,5 диагностирован как остеопоротический. 1
BMD является основой оценки риска будущих переломов, и с начала 1990-х годов сообщалось, что она отрицательно связана с риском возникновения переломов в будущем. 34 Однако неточно оценивать риск перелома, используя только МПК, из-за того, что пациенты с остеопорозом с аналогичной МПК иногда демонстрируют разные риски переломов. Поэтому Алгоритм риска переломов Всемирной организации здравоохранения (ВОЗ) (FRAX ® ) 35 был разработан на основе МПК шейки бедренной кости и клинических факторов риска (текущий возраст, пол, перенесенный остеопоротический перелом, низкий ИМТ, ревматоидный артрит, вторичные причины остеопороза, наличие у родителей перелома шейки бедра, статус курильщика, употребление алкоголя и пероральные глюкокортикоиды) для оценки 10-летней вероятности серьезного остеопоротического перелома. 35 Однако это не правило, а скорее клиническое руководство; все управленческие решения должны приниматься с учетом клинической оценки в каждом конкретном случае. Таким образом, рассмотрение внутренних и внешних факторов риска, независимых от МПК, было предложено ВОЗ для улучшения стратегии оценки риска остеопоротических переломов. Несколько факторы риска были идентифицировали, включая факторы образа жизни (низкую добавку кальция, чрезмерную худобу, иммобилизацию и падение), генетические заболевания, эндокринные расстройствами, гипогонадизм состояния, ревматологические и аутоиммунные заболевания, желудочно-кишечные расстройства, гематологические заболевания, неврологические и скелетно-мышечные расстройства, разное болезни и фармацевтическое вмешательство. 1
Биомаркеры метаболизма костной ткани в сыворотке и моче были разработаны для оценки состояния костеобразования и резорбции кости, которые, как правило, неинвазивны и очень рентабельны. Наиболее широко доступные маркеры включают сывороточный остеокальцин; специфическая для костей щелочная фосфатаза; и общие N-концевые пропептиды проколлагена I типа (tPINP), которые являются маркерами образования кости; и С-концевые перекрестно-связывающие телопептиды в моче или сыворотке с коллагеном типа I (CTX-1) и кислой фосфатазой, устойчивой к тартрату, которые являются маркерами резорбции кости. 1,36 Сыворотки tPINP и CTX-1 рекомендованы для вспомогательной диагностики остеопороза Международным фондом остеопороза (IOF). 6 Корреляция между остеопоротическим статусом / переломами и биомаркерами костного обмена, не зависящая от МПК, была обнаружена в популяции остеопорозов, включая женщин в постменопаузе. 6 Хотя маркеры метаболизма кости разрабатывались десятилетиями, их точность, специфичность, чувствительность и стабильность все еще не определены в клиническом подходе к лечению остеопороза.
Новый диагностический режим
Недавно циркулирующие микроРНК стали новыми биомаркерами для диагностики остеопороза и прогнозирования переломов. Циркулирующие микроРНК представляют собой тип малых РНК, которые существуют в жидкости организма, которые всегда специфически экспрессируются in vivo и сохраняют стабильность в течение длительного времени in vitro . 37 По сравнению с традиционными маркерами метаболизма костной ткани в сыворотке крови, циркулирующие микроРНК обладают преимуществами более высокой чувствительности, большей специфичности и лучшей стабильности.Сообщалось, что нарушение регуляции экспрессии циркулирующей микроРНК всегда тесно связано с патологической физиологией заболеваний. 38-40 Таким образом, циркулирующая микроРНК имеет потенциал в качестве молекулярного диагностического биомаркера в клинике. 41 Согласно исследованию с размером выборки 120, сывороточные miR-21 и miR-133a продемонстрировали высокий потенциал в качестве диагностических маркеров остеопороза. 42 Исследователи наблюдали, что уровень miR-21 в сыворотке подавлялся среди здоровых участников, пациентов с остеопенией и пациентов с остеопорозом; обратное верно для miR-133a.Кроме того, miR-21, miR-23a, miR-24, miR-25, miR-100, miR-125b, miR-382-3p, miR-550a-5p, miR-122-5p и miR-125- Сообщалось также, что 5р являются потенциальными предикторами остеопоротического перелома. 38,43,44 Более того, комбинационная панель из девяти циркулирующих микроРНК (включая miR-942-5p, miR-155-5p, miR-330-3p, miR-203a и miR-181c-5p) показала удовлетворительную прогностическая эффективность с площадью под кривой 0,97 для оценки остеопоротического перелома. 45
Однако нельзя игнорировать ограничения этих биомаркеров.Биомаркеры ограничены рядом факторов, таких как легкая деградация, временная изменчивость, влияние приема пищи. 36 Несмотря на эти недостатки, еще три дополнительных момента могут повлиять на перспективу применения биомаркеров для остеопороза: 1) уточнить происхождение биомаркеров и то, действуют ли биомаркеры во время развития остеопороза; 2) отслеживать динамические изменения биомаркеров для оценки эффектов антиостеопоротической терапии; и 3) разработать более эффективную диагностическую стратегию в сочетании с традиционными мерами.Персонализированная диагностика и лечение могут стать возможными в будущем для лечения остеопороза за счет комбинированного применения МПК, клинических факторов риска и биомаркеров конкретных заболеваний.
ТЕРАПЕВТИКА
Традиционные процедуры
В настоящее время наиболее распространенным подходом к профилактике и лечению остеопороза является ингибирование остеокластов. Некоторые антирезорбтивные фармацевтические препараты, одобренные Управлением по контролю за продуктами и лекарствами США (FDA), применялись для лечения остеопороза.Бисфосфонаты, включая алендронат, ибандронат, ризедронат и золедроновую кислоту, являются антирезорбтивными препаратами, которые специфически связываются с гидроксиапатитом в костных тканях и последовательно ингибируют прикрепление остеокластов к поверхности кости, а также посредством подавления лизосомального фермента, пирофосфатазы и простагландина. предотвратить резорбцию костей. 46 Бисфосфонаты получили широкое распространение; группа препаратов представляет собой большой прогресс в лечении остеопороза и профилактике переломов, со снижением примерно на 50% риска переломов позвонков, в то время как уменьшение непозвоночных переломов имеет очень изменчивый диапазон. 47,48 Однако сообщалось о нескольких побочных эффектах, связанных с использованием бисфосфонатов, таких как желудочно-кишечные расстройства, остеонекроз челюсти, воспаление глаз, атипичные переломы бедренной кости и нарушение функции почек. 1 Следовательно, растет консенсус в отношении рекомендации введения бисфосфонатов в низких дозах в еженедельных составах, и реакции BMD и маркеров метаболизма костной ткани не отличаются от ответов для ежедневных составов. 49,50
Деносумаб представляет собой моноклональное антитело с высокой специфичностью и сродством к активатору рецептора RANKL. 51 Он показал заметную эффективность при постменопаузальном остеопорозе со снижением частоты переломов примерно на 70%, 40% и 20% при переломах позвонков, бедра и не позвонков, соответственно, в течение 3 лет. 51 Кроме того, сообщалось, что деносумаб улучшает МПК у мужчин с высоким риском переломов. Однако при прекращении приема деносумаба наблюдалась реакция абстиненции с быстрым увеличением маркеров метаболизма костной ткани. 52,53 Кроме того, частота хрупких переломов вернулась к исходному уровню во время стадии вне лечения. 52,53 Таким образом, при систематическом лечении пациентов с остеопорозом следует применять альтернативные препараты для предотвращения потери костной массы, связанной с депривацией деносумаба.
Заместительная терапия эстрогенами — это предпочтительное симптоматическое лечение для восстановления потери костной массы в постменопаузе и снижения риска остеопоротических переломов. Инициатива по здоровью женщин (WHI) показала, что риск переломов центрального скелета был снижен примерно на 30%, а остеопоротических переломов периферического скелета — примерно на 20% при 5-летнем режиме заместительной терапии эстрогенами. 1 Тем не менее, WHI также сообщил о повышенных рисках сердечно-сосудистых заболеваний, инвазивного рака груди, тромбоза глубоких вен и легочной эмболии после длительного использования заместительной терапии эстрогенами. Кроме того, за лишением эстрогена следует реакция воздержания с резкой потерей костной массы. Эти серьезные побочные эффекты приводят к низкому энтузиазму по поводу применения заместительной эстрогена в терапии остеопороза. Тем не менее, заместительная терапия эстрогенами все еще остается вариантом для женщин в постменопаузе с высоким риском переломов. 54 Кроме того, селективный модулятор рецепторов эстрогена, особенно ралоксифен, снижает риск предшествующих переломов позвонков примерно на 55% и рефракций позвонков примерно на 30% за 3 года, в то время как он не влияет на переломы непозвонков. 1 Однако безопасность ралоксифена также вызывает беспокойство, поскольку он повышает риск тромбоэмболии, инсульта, приливов и судорог ног. 1
Терипаратид, также известный как N-концевая 34 аминокислота паратироидного гормона, активирует резорбцию кости и образование кости одновременно. 55 Он снижает риск переломов позвонков и переломов, не связанных с хрупкостью позвонков, примерно на 65% и 50% у пациентов с остеопорозом, соответственно. 1 Однако, как сообщалось, он вызывает побочные эффекты, такие как гиперкальциемия, тошнота и головокружение в исследованиях на людях, и даже остеосаркома в исследованиях на животных. 1
Следовательно, необходимо срочно разработать более безопасную, более эффективную альтернативу с повышенной рентабельностью для лечения остеопороза с учетом побочных эффектов и долгосрочных проблем безопасности при клиническом использовании текущих терапевтических стратегий.
НОВЫЕ ПРОЦЕДУРЫ
Поскольку функциональные дефекты МСК являются решающей этиологией развития остеопороза, исследователи пытались лечить остеопороз с помощью местной или целевой трансплантации нормальных МСК. Исследование показало, что инъекция в костный мозг смеси мезенхимальных стволовых клеток костного мозга (BMMSC) и альгината гидрогеля значительно улучшила отложение костной ткани, твердость и объем губчатой кости у кроликов с дефицитом эстрогена. 56 Кроме того, после инфузии BMMSC в костный мозг увеличивалась масса губчатой кости у овариэктомированных крыс. 57 BMMSC связывание LLP2A, как сообщается, усиливает формирование костной ткани и, наконец, увеличивает минеральную плотность костной ткани как при остеопорозе, вызванном дефицитом эстрогена, так и при возрастном остеопорозе. 17 Кроме того, трансплантация BMMSC также применялась для облегчения остеодиспластических заболеваний, связанных с дисфункцией МСК. Многочисленные клинические испытания показали, что трансплантация BMMSC увеличивала рост и качество кости, а также снижала частоту переломов у пациентов с несовершенным остеогенезом. 58 Трансплантация МСК улучшает остеопороз не только за счет получения нормальных стволовых клеток, но также за счет модуляции микроокружения хозяина и улучшения остеогенной функции МСК хозяина. Системное введение MSC способствует остеогенезу BMMSC и, наконец, восстанавливает остеопоротическую потерю костной ткани при дефиците эстрогена, 59 глюкокортикоидов, 60 диабете, 61 и моделях системной красной волчанки. 62 Кроме того, местное применение клеточных агрегатов МСК резко снизило частоту остеопоротических переломов бедренной кости с 93.От 75% до 37,50% в моделях крыс с удаленными яичниками. 63 Кроме того, экзосомы, полученные из нормальных МСК, также демонстрируют удовлетворительную эффективность при лечении остеопороза, что приписывается сигнальным веществам, содержащимся в экзосомах, таким как функциональные белки, малая РНК и так далее. 18 Таким образом, терапия на основе МСК является многообещающим кандидатом на лечение остеопороза.
В последние годы все больший энтузиазм вызывает лечение остеопоротических заболеваний с использованием традиционной китайской медицины в качестве новой альтернативы из-за меньшего количества побочных эффектов и накопленного за тысячи лет опыта использования в медицине (Таблица 1).
Китайские лекарственные травы, содержащие несколько компонентов, обычно оказывают терапевтическое действие на постменопаузальный остеопороз посредством сложных механизмов. Было обнаружено множество путей для восстановления баланса остеобластогенеза и остеокластогенеза, включая рецепторно-зависимые пути эстрогена, RANK / RANKL / OPG, BMP, Wnt / β-катенин, ERK, TGF-β и сигнальные пути Notch. 74,75 Помимо восстановления баланса между остеобластогенезом и остеокластогенезом, китайские лекарственные травы также были созданы для модуляции баланса адипоцитов и остеобластов, что также имеет решающее значение для метаболизма костей. 75 Более того, многие китайские лекарственные травы имеют химическую структуру или химические группы, похожие на эстроген. Они обладают эстрогеноподобными функциями, а также иммунорегулирующими и антиоксидантными функциями, которые, как было показано, облегчают остеопороз. 75 Кроме того, китайские лекарственные травы и другие природные небольшие молекулы, такие как мелатонин, 59 рапамицин, 76 и ликохалкон А, 63 , также использовались в предварительной обработке МСК для улучшения терапии на основе МСК при остеопоротических заболеваниях.Представляется целесообразным и ценным разработка новых терапевтических средств для лечения остеопороза, основанных на комбинированном применении МСК и китайских лекарственных трав.
AACE выпускает Руководство по клинической практике лечения постменопаузального остеопороза 2020 г.
Американская ассоциация клинических эндокринологов (AACE) и Американская коллегия эндокринологов (ACE) Клинические практические рекомендации по диагностике и лечению постменопаузального остеопороза — обновление 2016 г. и алгоритм были опубликованы в сентябре 2016 г.
Совсем недавно Американский колледж врачей (ACP) опубликовал новые рекомендации по остеопорозу (просмотреть или загрузить PDF-файл, и хотя AACE / ACE одобряет усилия ACP по решению важности выявления и контроля остеопороза и риска переломов у женщин в постменопаузе и пожилых мужчин, необходимо прояснить важные отличия от руководящих принципов AACE / ACE.
Посмотреть или скачать алгоритм 2020 (PDF)
Рекомендации во всех руководствах AACE / ACE отражают не только последние научно-обоснованные научные данные, но также клинический опыт и мнения экспертов, основанные на протоколах AACE 2010 и 2014 гг. выпуск руководств по клинической практике.
Антирезорбтивная фармакотерапия продемонстрировала эффективность для снижения риска переломов, но анаболическая терапия также играет важную роль в лечении остеопороза, особенно у пациентов с тяжелым остеопорозом и тех, у кого есть клинические переломы во время антирезорбтивного применения.
Продолжительность терапии необходимо подбирать индивидуально. Рекомендация 5 лет терапии может быть подходящей для некоторых, но не для других пациентов. Также важно отметить, что периоды приема лекарств не рекомендуются тем, кто принимает деносумаб, поскольку защита от перелома позвонков может быть потеряна в течение 3-18 месяцев после прекращения приема.
В рекомендацияхAACE / ACE рекомендуется после начала терапии повторно оценивать пациентов с помощью двойной абсорбциометрии (DXA) минеральной плотности кости (BMD) каждые 1-2 года до тех пор, пока результаты не станут стабильными, с продолжением интервального мониторинга в зависимости от клинических обстоятельств. Таким образом, частота повторной оценки МПК должна быть индивидуальной. Получение последующего сканирования DXA для выявления людей, которые не реагируют на терапию, имеет решающее значение для возможности изменить терапию до возникновения клинического перелома, который может изменить жизнь.
Эти люди часто страдают недиагностированными заболеваниями, способствующими потере костной массы, или могут иметь проблемы с абсорбцией или приверженностью. На данный момент Рекомендация 4 ACP «ACP не рекомендует проводить мониторинг плотности костной ткани в течение 5-летнего периода фармакологического лечения остеопороза у женщин», отмечена как не имеющая сильной доказательной базы («Степень: слабая рекомендация; доказательства низкого качества. »).
Ралоксифен не рекомендуется для использования в рекомендациях ACP. Хотя ралоксифен не эффективен в снижении риска перелома шейки бедра, рекомендации AACE / ACE указывают, что он может быть подходящей начальной терапией у некоторых женщин, которым требуется только терапия, специфичная для позвоночника.Для женщин с высоким риском перелома позвоночника, но не подверженных риску перелома бедра или невертебральных переломов, ралоксифен может быть подходящим, особенно когда другие антирезорбтивные препараты не переносятся или противопоказаны, а также для пациентов, ищущих потенциальную дополнительную «пользу» в виде снижения риска рака груди.
AACE / ACE соглашается с заявлением Американского общества исследований костей и минералов (ASBMR) о том, что рекомендации ACP по остеопорозу «не соответствуют» ключевым принципам лечения и лечения остеопороза, особенно в области частоты мониторинга минеральной плотности костей, лечения анаболические агенты и продолжительность терапии антирезорбтивными агентами.
РекомендацииAACE / ACE предоставляют врачам и передовым медицинским работникам клинически значимые знания, которые помогут предотвратить переломы у женщин в постменопаузе с повышенным риском переломов.
Источник: AACE
Камачо П.М., Петак С.М., Бинкли Н. и др. Американская ассоциация клинических эндокринологов / Американская коллегия эндокринологов руководящие принципы клинической практики по диагностике и лечению постменопаузального остеопороза — обновление 2020 г. Эндокр Практик .2020; 26 (1): 1-46.
.

 The role of biphosphonates in the treatment of painful metastatic bone disease: a review of phase III trials. Pain 1998; 78: 157–69.
The role of biphosphonates in the treatment of painful metastatic bone disease: a review of phase III trials. Pain 1998; 78: 157–69. Endocr Pract 2003; 9: 544–64.
Endocr Pract 2003; 9: 544–64.