Диффузный токсический зоб | Городская клиническая больница им. Ф.И. Иноземцева
Диффузный токсический зоб (ДТЗ, гипертиреоз, болезнь Грейвса-Базедова) – аутоиммунное заболевание, развивающееся вследствие выработки антител к репепторам ТТГ (рТТГ), клинически проявляющееся поражением щитовидной железы (ЩЖ) с развитием синдрома тиреотоксикоза. Стоит отметить, что вырабатывающиеся при ДТЗ антитела оказывают на орган-мишень не разрушающее, как при других аутоиммунных заболеваниях, а стимулирующее действие.
Впервые это заболевание было описано в 1835 году ирландцем Робертом Джеймсом Грейвсом (1797–1853). Почти одновременно с ним, в 1840 году, немецкий врач Карл Адольф фон Базедов (1799–1854) описал наблюдаемую им у четырех пациентов так называемую мерзебургскую триаду (по названию города Мерзебурга, где он работал) — тахикардию, экзофтальм и зоб, которые являются характерными симптомами ДТЗ. Сам Базедов назвал описанное им заболевание экзофтальмической кахексией.
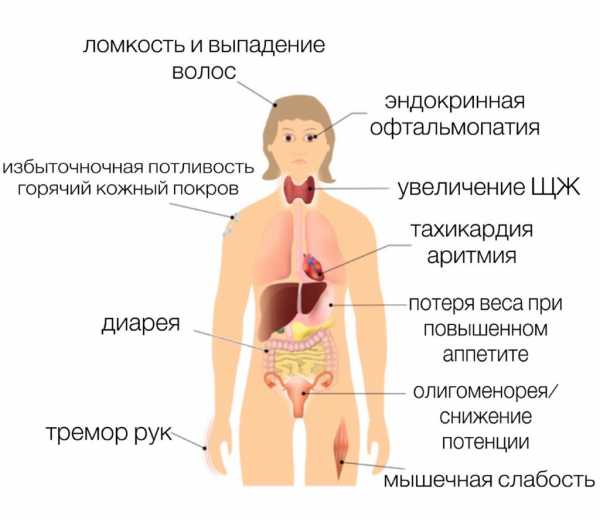
КЛИНИЧЕСКАЯ КАРТИНА:
Жалобы: на увеличение ЩЖ, повышенную возбудимость, эмоциональную лабильность, плаксивость, беспокойство, нарушение сна, суетливость, нарушение концентрации внимания, слабость, частый стул, нарушение менструального цикла, снижение потенции
Сердечно-сосудистая система: экстрасистолия, постоянная или реже пароксизмальная синусовая тахикардия, фибрилляция предсердий (мерцательная аритмия) с повышенным риском тромбоэмболических осложнений, артериальная гипертензия => миокардиодистрофия и сердечная недостаточность.
Катаболический синдром: похудание при повышенном аппетите, горячие кожные покровы, субфебрилитет, избыточная потливость, мышечная слабость
Синдром эктодермальных нарушений: ломкость ногтей, ломкость и выпадение волос
Нервная система: тремор рук (симптом Мари) и/или всего тела (симптом телеграфного столба), повышение сухожильных рефлексов
Глаза: у части пациентов развивается эндокринная офтальмопатия; характеризующаяся поражением мягких тканей орбиты, зрительного нерва и вспомогательного аппарата глаз (слезной железы, роговицы, конъюнктивы и век)
ДИАГНОСТИКА:
ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ (высокий уровень свободного Т4 и свободного Т3 и низкое содержание ТТГ в крови). Специфическим маркером ДТЗ являются антитела к рТТГ.
ДТЗ = ↓ТТГ + ↑ Т4 свободный + ↑Т3 свободный + ↑антитела к рецепторам ТТГ

СЦИНТИГРАФИЯ используется для определения функциональной активности ЩЖ и дифференциальной
диагностики диффузного и узлового токсического зобов. Наиболее часто для
сканирования ЩЖ используется изотоп технеция – 99mTc (имеет короткий период
полураспада – 6 часов, что значительно уменьшает дозу облучения), I
МСКТ и МРТ помогают определить размеры и расположение ЩЖ, расположение по отношению к окружающим структурам, выявить смещение или сдавление трахеи и пищевода.
ЛЕЧЕНИЕ:
Консервативное (прием антитиреоидных препаратов)
Консервативное лечение назначается для достижения эутиреоза перед оперативным лечением или радиойоДтерапией, а также, в отдельных группах пациентов, в качестве базового длительного курса лечения, который, в некоторых случаях, приводит к стойкой ремиссии. В первую очередь, речь идет о пациентах с умеренным увеличением объема ЩЖ (до 40 мл). Тиамазол (тирозол, мерказолил) является препаратом выбора для всех пациентов, которым планируется проведение консервативного лечения ДТЗ, за исключением лечения ДТЗ в первом триместре беременности, тиреотоксического криза и развития побочных эффектов на тиамазол, когда предпочтение следует отдать пропилтиоурацилу (ПТУ, пропицилу). При наличии стойких умеренных и легких побочных эффектов антитиреоидной терапии необходимо отменить тиреостатик и направить пациента на терапию радиоактивным йодом или хирургическое вмешательство, или перевести его на другое антитиреоидное средство, если терапия радиоактивным йодом или операция пока не показаны.
Если тиамазол выбран в качестве начальной терапии ДТЗ, то лекарственная терапия должна продолжаться около 12-18 месяцев, после чего она постепенно отменяется, если у пациента нормальный уровень ТТГ. Перед отменой тиреостатической терапии желательно определить уровень антител к рТТГ, так как это помогает в прогнозировании исхода лечения: больше шансов на стойкую ремиссию имеют пациенты с низким уровнем антител к рТТГ. При правильно проведенном лечении частота рецидивов после отмены тиреостатических препаратов составляет 70% и более. Если у пациента с ДТЗ после отмены тиамазола вновь развивается тиреотоксикоз, необходимо рассмотреть вопрос о проведении радиойодтерапии или тиреоидэктомии.
Длительную консервативную терапию нецелесообразно планировать у пациентов с выраженными осложнениями тиреотоксикоза (фибрилляция предсердий, остеопороз и др.)
Оперативное
При ДТЗ объем оперативного лечения один – тотальная тиреоидэктомия.
Перед проведением тиреоидэктомии необходимо достижение эутиреоидного состояния (нормальный уровень свободного Т3, свободного Т4) на фоне терапии тиреостатиками.
В послеоперационном периоде в обязательном порядке производится определение уровня кальция, осмотр ЛОР врачом (на предмет подвижности голосовых складок). Препараты левотироксина (эутирокс, L-тироксин) назначаются из расчета 1.7 мкг/кг веса пациента. Определить уровень ТТГ следует через 6-8 недель после операции.
Лечение радиоактивным йодом (РЙТ)
РЙТ при ДТЗ проводится в случае рецидива тиреотоксикоза после правильно проведенного консервативного лечения (непрерывная терапия тиреостатическими препаратами с подтвержденным эутиреозом в течение 12-18 месяцев), невозможности приема тиреостатических препаратов (лейкопения, аллергические реакции), отсутствия условий для консервативного лечения и наблюдения за больным.
Целью радиойодтерапии является ликвидация тиреотоксикоза путем разрушения гиперфункционирующей ткани ЩЖ и достижение стойкого гипотиреоидного состояния.
Минусы:
- Дороговизна метода и длительность ожидания очереди;
- Объем ЩЖ не должен превышать 40 см3;
- Противопоказана при беременности, лактации и эндокринной офтальмопатии;
- Лучевую нагрузку получают все ткани и органы;
Рецидив тиреотоксикоза.
inozemtcev.ru
Три эффективных метода борьбы с ДТЗ
Доброго времени суток всем, кто заглянул на огонек! Я не буду лить много воды, понимаю, что вы здесь исключительно только ради информации. А потому…
- Какие методы используют сейчас в медицине при лечении ДТЗ.
- Какие препараты принимаются при этом заболевании и как.
- Какие побочные эффекты ждать от препаратов.
- Кому нужна операция при ДТЗ.
- О возможных осложнениях во время и после операции.
- Кому поможет радиойодтерапия и что от нее ждать.
- Можно ли вылечиться от ДТЗ и какой прогноз для жизни?
Диффузный токсический зоб без лечения вызывает очень грозные осложнения, в основном на сердце и кости. О признаках этого заболевания я написала очень подробно в статье «Внимание! Диффузный токсический зоб — сердечный убийца», поэтому рекомендую вам прочитать сначала эту статью.
Если вы уже и так все знаете о своей болезни и у вас этот диагноз стоит в личной карточке, то данная статья поможет понять, какой метод подходит именно вам.
Лечение диффузного токсического зоба требует особой ответственности, ибо во время лечения используются довольно токсичные препараты, которые при неграмотном применении могут принести еще больший вред здоровью.
Методы лечения ДТЗ
Для лечения диффузного токсического зоба в России применяют 3 способа:
- Медикаментозный.
- Хирургический.
- Лучевой.
Все методы приводят к снижению тиреоидных гормонов. Каждый метод имеет свои показания и противопоказания. В каком случае используется тот или иной метод, я буду говорить по ходу статьи.
В России и западной Европе основным методом является медикаментозный. В США чаще используется лечение радиоактивным йодом.
Лечение диффузного токсического зоба таблетками
Это, возможно, самый длительный метод лечения и, как оказалось после последних исследований, самый неэффективный. Сейчас я объясню, почему.
Препараты, которые применяют для лечения этого заболевания, можно разделить на 2 большие группы:
- тиреостатики (препараты, которые непосредственно блокируют работу щитовидной железы)
- вспомогательные (препараты, которые устраняют какие-либо симптомы заболевания)
Тиреостатики
Для лечения диффузного токсического зоба используют препараты тиомочевины. В России это мерказолил (Россия) или тирозол (Германский аналог мерказолила), карбимазол и пропилурацил (пропицил).
Дозы мерказолила назначаются в зависимости от тяжести заболевания и колеблются от 20 до 40 мг/сут. После исчезновения симптоматики, а это в среднем происходит через 1 месяц, дозу снижают до поддерживающей. В такой дозировке нужно принимать препарат в течение двух лет (вот почему самый длительный). Поддерживающая доза, которую нужно принимать каждый день, в среднем составляет 5-7,5 мг/сут.
Если после отмены препарата происходит рецидив заболевания, то лечение начинается сначала по прежней схеме. Если после второго курса лечения происходит рецидив, то имеет место решение вопроса об оперативном лечении или лечении радиоактивным йодом, т. к. успеха в повторном лечении тиреостатиками ждать не приходится.
Так было до недавнего времени. Сейчас эндокринологи пришли к выводу, что не стоит назначать повторного курса тиреостатиков, поскольку даже после первого курса рецидив развивается в 70 % случаев (вот почему неэффективный). Поэтому в некоторых случаях пациенту сразу предлагают более радикальные методы лечения, о которых я буду говорить дальше.
Еще один довод в пользу отказа от повторных курсов: пациентам склонным к рецидивам, не рекомендуется продолжать лечиться мерказолилом долгие годы, т. к., по мнению ряда авторов, повышается вероятность возникновения рака щитовидной железы.
Для прогноза ремиссии используют определение антител к рецепторам ТТГ (а/т к рецепторам ТТГ). В том случае, когда достигается ремиссия, а а/т к рецепторам ТТГ не снижаются, высокая вероятность возникновения рецидива заболевания. Более подробно вы можете прочитать об этих антителах в статье «Какие нужны анализы на гормоны щитовидки», очень рекомендую.
Пропицил выпускается в таб. по 50 мг. Он отличается от мерказолила следующим:
- меньшей активностью
- коротким сроком действия
- меньше проникает через плаценту и в грудное молоко, поэтому широко используется при лечении беременных и кормящих женщин
НО… он достаточно токсичен для печени и может вызывать даже некроз печени, поэтому пациентам с заболеваниями печени он не назначается. Да и в последнее время прошел слух, что его также не рекомендуют беременным и кормящим женщинам.
Осложнения вследствие приема тиреостатиков
- Агранулоцитоз (снижение лейкоцитов крови) наблюдается у 0,4-0,7 % больных. Один из первых признаков — фарингит. Поэтому производится ежемесячное определение лейкоцитов крови, проще говоря, общий анализ крови (ОАК).
- Токсический гепатит.
- Острый некроз печени.
- Кожные проявления.
- Лихорадка.
- Боли в суставах и мышцах.
- Желудочно-кишечные расстройства.
В случае непереносимости этих препаратов обязательна их отмена и выбор другого метода лечения.
Вспомогательные средства
Возникают случаи, при которых происходит чрезмерная блокада синтеза тиреоидных гормонов и быстрое их снижение в крови. В ответ на это начинает вырабатываться ТТГ, а он вызывает увеличение щитовидной железы в объеме. Таким образом, получается, что пациенту становится лучше, т. к. симптомы тиреотоксикоза проходят, но при этом увеличивается щитовидная железа.
Чтобы этого избежать, необходимо порой назначать на фоне приема мерказолила или пропицила прием L-тироксина в дозе 25-50 мкг/сут. Эта схема лечения называется «блокируй и замещай». Но во время беременности она противопоказана.
Для снижения пульса применяют бета-блокаторы (атенолол, метопролол, анаприлин и пр.). Наряду со способностью урезать пульс они могут превращать активную форму Т3 в неактивную (реверсивный Т3), тем самым также снимая симптоматику тиреотоксикоза.
Глюкокортикоиды применяют для лечения аутоиммунной офтальмопатии, которая является очень частой спутницей этого заболевания.
Также не стоит забывать о лечении остеопороза, если таковой имеется, для предотвращения развития переломов. Как лечить остеопороз при ДТЗ, написано в статье «Лечение остеопороза».
Также для уменьшения психических симптомов возможно применение успокоительных сборов трав.
Хирургический метод лечения ДТЗ
Для лечения диффузного токсического зоба этим методом сначала определяют показания, поскольку не каждого возьмут на операцию.
Вот они:
- Большие размеры зоба (объем 35-40 мл)
- Сдавливание или смещение трахеи, пищевода, крупных сосудов.
- Загрудинный зоб.
- Непереносимость препаратов.
- Сочетание с другими заболеваниями (например, с сахарным диабетом).
- Беременность.
- Тяжелый тиреотоксикоз с осложнениями
- Склонность к рецидивам.
Перед операцией проводится подготовка. Она заключается в:
- Достижении эутиреоза (нормализация гормонов Т4 и Т3).
- Назначении больших доз бетта-блокаторов и глюкокортикоидов при непереносимости тиреостатиков.
В результате операции производится почти полное удаление ткани щитовидной железы. Оставляют те участки ткани, где находятся паращитовидные железы.
Как и при любой другой операции, могут возникнуть осложнения.
Послеоперационные осложнения:
- Рецидив (при недостаточном удалении ткани железы).
- Парез возвратного нерва (осиплость или потеря голоса).
- Гипопаратиреоз (при ошибочном удалении паращитовидных желез).
- Нагноение послеоперационной раны.
ГИПОТИРЕОЗ вследствие операции не считается осложнением, это является ее целью. Он хорошо компенсируется приемом L-тироксина, после чего человек может жить без ограничений, в том числе планировать беременность.
Лучевой метод лечения диффузного токсического зоба
В России производится в единственном месте — в г. Обнинске Калужской области. Этот метод очень популярен в США. Но из-за дорогостоимости этого метода его редко кому проводят бесплатно (выделяется квота), в основном это платные пациенты.
Для этого метода лечения также имеются свои показания:
- Возраст должен быть больше 40 лет (хотя сейчас обсуждается проведение у более молодых)
- Рецидив после операции
- Отказ от операции
- Наличие противопоказаний к операции
Перед проведением лечения требуется такая же подготовка, как и при операции, т. е.
Противопоказания следующие:
- Не проводится лицам моложе 40 лет и детям (обсуждается).
- Беременность и лактация.
- Большой зоб.
- Загрудинный зоб.
- Заболевания крови, почек, язвенная болезнь.
Лечение тиреотоксического криза
Тиреотоксический криз — это жизнеугрожающее состояние, которое лечится только в условиях реанимационного отделения стационара.
Все мероприятия направлены на снижение уровня тиреоидных гормонов, лечение надпочечниковой недостаточности, устранение сердечно-сосудистых нарушений.
Увеличивают дозы тиреостатиков. Внутривенно вводят 1 % раствор Люголя, тем самым заменяя калия йодит йодидом натрия — он проникает в щитовидную железу и блокирует ее работу. Для уменьшения надпочечниковой недостаточности внутривенно вводят глюкокортикоиды (преднизолон, гидрокортизон), препараты ДОКСА. При лечении сердечно-сосудистых расстройств применяются бета-блокаторы также внутривенно.
Некоторые авторы предлагают применение плазмафереза для более быстрого вывода избыточных тиреоидных гормонов.
Прогноз и трудоспособность
При ранней диагностике и начале лечения диффузного токсического зоба возможно практическое выздоровление. Поздняя диагностика и неадекватная терапия способствуют к потере трудоспособности.
При появлении симптомов недостаточности надпочечников, поражении печени, сердечной недостаточности прогноз в отношении трудоспособности и жизни пациента неблагоприятен.
Прогноз офтальмопатии сложен и не всегда параллелен прогнозу тиреотоксикоза. Даже при нормализации Т3 и Т4 офтальмопатия может прогрессировать, поскольку это самостоятельное заболевание. Почитайте отдельную статью на эту тему «Эндокринная офтальмопатия».
По решению КЭК (клинико-экспертная комиссия) больной должен быть освобожден от тяжелого физического труда, ночных смен и сверхурочных работ, переведен на легкий физический или умственный труд. В тяжелых случаях пациент оформляется на инвалидность.
gormonivnorme.ru
Осложнения дтз
Тиреотоксический криз
Подострая дистрофия печени
Тиреотоксическое сердце
Лечение дтз
Цель лечения – нормализация повышенного выделения тиреоидных гормонов и вызванных ими нарушений функций. В терапевтической деятельности выделяют два периода:
Начальный период — в течение этого периода стремятся к быстрой ликвидации болезненных симптомов со стороны сердечно-сосудистой и нервной систем, достижению эутиреоза.
Продолжительный период — в течение этого периода стремятся к удержанию состояния эутиреоза.
Методы лечение ДТЗ:
Применение тиреостатических препаратов.
Хирургическое лечение, чаще всего при помощи субтотальной струмэктомии.
Применение радиоактивного изотопа йода.
Выбор метода лечения зависит от тяжести болезни, размеров щитовидной железы, возраста больного, сопутствующих заболеваний.
Терапия тиреостатическими препаратами
Тиреостатические препараты тормозят различные этапы синтеза гормонов щитовидной железы. В последние годы появились данные об иммунодепрессивном действии мерказолила.
Показания: диффузно-токсический зоб легкой и средней степени тяжести; ДТЗ с увеличением щитовидной железы не более III степени; в качестве предоперационной подготовки к хирургическому лечению ДТЗ; тиреотоксический криз; ДТЗ у беременных; токсическая аденома; неоперабельные случаи ДТЗ и отсутствие возможности проведения радиойодтерапии; до и после введения лечебной дозы J131.
Тиреостатические препараты:
Таблица 9
Мерказолил (метотирин)
(Mercazolil, metothyrin)
Таблетки по 0,005 (5мг)
Тиамазол (метизол)
(Thyamazol)
Таблетки по 0,005 (5мг)
Тирозол
(Thyrazol)
Таблетки по 0,005 (5мг)
Метилтиоурацил
(Methylthiouracilum)
Таблетки по 0,1 (100 мг)
Пропилтиоурацил (пропицил) (Propylthiouraculum)
Таблетки по 0,1 (100 мг)
Начинают лечение тиреостатиками с высоких доз:
мерказолил (тиамазол, метилмазол): при легкой степени – 30 мг/сут; при средней тяжести и тяжелом тиреотоксикозе – 40-60 мг/сут в 4 приема;
Лечение проводят под контролем частоты пульса, клинического исследования крови. Эффект начинает проявляться через 1-2 недели. В момент достижения клинического эутиреоза, выражающегося замедлением деятельности сердца, повышением веса, исчезновением симптомов чрезмерной возбудимости, нормализацией концентрации в крови тиреоидных гормонов Т4 и Т3 начинают снижение дозы до 1/3 исходной величины. Эту дозу удерживают несколько дней, затем переходят ко 2-му этапу лечения – поддерживающему, длительному.
Поддерживающая доза для мерказолила составляет 2,5-10 мг, для метилтиоурацила 12,5-50 мг, для пропилтиоурацила 12,5-50 мг. Если состояние ремиссии стойко сохраняется в течение 4-6 месяцев, прием препарата прекращают, но наблюдение продолжают. При повторном появлении симптомов тиреотоксикоза снова назначают адекватные дозы препаратов.
Отдельные авторы рекомендуют поддерживающее лечение проводить в течение 1-2 лет. Однако нужно помнить, что даже длительное и систематическое лечение тиреостатиками дает стойкую ремиссию лишь у 50 % пациентов!
Побочные действия тиреостатиков: лейкопения, агранулоцитоз, токсико-аллергические реакции (зуд, крапивница), зобогенный эффект, медикаментозный гипотиреоз, катаральные явления со стороны ЖКТ, нарушения функций печени.
Наличие ДТЗ у беременных является показанием к прерыванию беременности в сроки до 12 недель. В большем сроке беременности предпочтительна терапия тиреостатиками при легкой и средней степени тяжести тиреотоксикоза и небольшом увеличении щитовидной железы. При более тяжелом течении тиреотоксикоза женщин направляют на оперативное лечение.
Карбонат лития (Lithii carbonas) — таблетки по 0.3, покрытые оболочкой.
Препарат используется в качестве самостоятельной терапии при легкой и средней степени тяжести тиреотоксикоза.
Механизм действия: непосредственное ингибирование синтеза гормонов в щитовидной железе и снижение обмена их на периферии.
Назначают в начальной дозе 900-1500 мг/сут (3-5 таблеток).
Препараты йода (р-р Люголя, дийодтирозин) в настоящее время для лечения ДТЗ применяются редко.
В комплексное лечение с тиреостатическими препаратами для лечения ДТЗ включают β-адреноблокаторы (обзидан=индерал=анаприлин, атенолол).
Показания для β-адреноблокаторов: стойкая, не уступающая терапии тиреостатиками, тахикардия, нарушение сердечного ритма (экстрасистолия, мерцательная аритмия). Дозы: от 40 мг до 160-200 мг/сут. Признаки адекватности дозы: уменьшение частоты сердечных сокращений, болевых ощущений в сердце. Эффект наступает обычно в течение 5-7 дней, затем дозу можно постепенно уменьшить до 10-20 мг/сут.
Кортикостероиды используют при ДТЗ с целью компенсации относительной надпочечниковой недостаточности, иммуносупрессии процесса в щитовидной железе, при тяжелом течении заболевании. Дозы: преднизолон 10-15 мг/сут. 2/3 дозы назначается утром в 7-8 ч, 1/3 дозы – в 11 ч.
Анаболические стероиды (метандростенолон, ретаболил и др.) – повышают массу тела.
Антигистаминные препараты — перитол (в таблетках по 0,004) — предупреждает и облегчает течение аллергических реакций, оказывает седативный эффект.
Лечение эндокринной офтальмопатии проводится эндокринологом и офтальмологом.
Необходимо добиться эутиреоидного состояния.
Назначается преднизолон в суточной дозе 40-80 мг с постепенным снижением через 2-3 недели и полной отменой через 3-4 месяца.
Плазмаферез – при стероидорезистентной офтальмопатии
Гемосорбция в сочетании со стероидной терапией. Курс лечения – 2-3 сеанса с интервалом в 1 неделю.
Дистанционная рентгенотерапия на область орбит. Используются малые дозы лучевой терапии (16-20 Гр на курс, ежедневно или через день, в разовой дозе 75-200 Р). Применяется при тяжелых формах офтальмопатии: резко выраженный экзофтальм, отек и гиперемия конъюктивы, ограничение взора, ослабление конвергенции, появление диплопии, выраженные боли в глазных яблоках. Сочетается с лечением глюкокортикоидами.
Хирургическое лечение (в стадии фиброза).
Хирургическое лечение ДТЗ
Показания: тиреотоксикоз тяжелой степени, большое увеличение щитовидной железы, отсутствие эффекта от консервативной терапии, загрудинный зоб, непереносимость тиреостатических препаратов.
Противопоказания: легкая форма ДТЗ, малые размеры щитовидной железы, тяжелые декомпенсированные соматические заболевания. Лиц старше 65 лет и с наличием ИБС желательно не направлять на хирургическое лечение (опасность тромбоэмболических осложнений!). При инфекционно-воспалительных заболеваниях оперировать больного разрешается лишь через 1-1.5 месяца после их ликвидации.
Больные направляются на хирургическое лечение после предварительной подготовки тиреостатическими препаратами в комбинации с β-адреноблокаторами и кортикостероидами (преднизолон назначается в дозе 15-20 мг/сут за 2-3 дня до операции; в день операции в/в вводится 50-100 мг гидрокортизона).
Послеоперационные осложнения: парез возвратного нерва и афония, гипопаратиреоз в результате удаления или травмы паращитовидных желез, гипотиреоз, тиреотоксический криз.
Лечение радиоактивным йодом 131J
Радиоактивный изотоп 131Jнакапливается в щитовидной железе и излучает β-лучи, оказывающие преимущественно местное действие, нарушает клетки щитовидной железы, вызывает их уменьшение, снижает тем самым выработку тиреоидных гормонов.
Показания: возраст не моложе 40 лет, тяжелая сердечная недостаточность и токсический гепатит, сочетание ДТЗ с туберкулезом, тяжелой артериальной гипертонией, перенесенным инфарктом миокарда, нейропсихическими расстройствами, геморрагическим синдромом. Отсутствие эффекта от консервативной терапии, проводимой в течение нескольких лет. Рецидив ДТЗ после хирургического лечения.
Противопоказания: беременность и лактация, стойкая лейкопения. Молодой возраст теперь не является безусловным противопоказанием к лечению радиоактивным йодом, и такое лечение в обоснованных случаях применяется у лиц моложе 35 лет. Лечение проводится в специализированных стационарах. За рубежом этот метод наиболее широко используется, в том числе и у детей, и в амбулаторных условиях.
Методика: обычно применяют дробный метод лечения – вначале больному дают 3-4 мКи внутрь, а через 3-4 месяца при необходимости назначают такую же дозу или меньшую.
Осложнения: гипотиреоз, тиреотоксический криз.
Прогноз. Трудоспособность
Зависит от своевременной диагностики и адекватности лечения.
Поздняя диагностика, как и неадекватное лечение, приводит к развитию осложнений: тиреотоксическому сердцу, недостаточности надпочечников, поражению печени, что ведет к потере трудоспособности и неблагоприятному прогнозу жизни.
Больные ДТЗ подлежат диспансерному наблюдению. Эндокринологом осматриваются 6 раз в год, офтальмологом и невропатологом 1-2 раза в год. 2 раза в год выполняется УЗИ щитовидной железы и исследуется кровь на содержание тиреоидных гормонов.
Больным показано освобождение от тяжелого физического труда, ночных смен, сверхурочных работ.
При стойкой утрате трудоспособности – по решению МСЭК устанавливаются III или II группы инвалидности.
Тиреотоксический криз
Является наиболее тяжелым, угрожающим жизни больного, осложнением ДТЗ.
studfile.net
Диффузный токсический зоб (гипертиреоз, тиреотоксикоз) – причины, патогенез, симптомы, диагностика, лечение
Диффузный токсический зоб (синонимы: гипертиреоз, тиреотоксикоз, болезнь Грейвса, базедова болезнь, болезнь Грейвса-Базедова, токсический узловой зоб) – заболевание, обусловленное поступлением в организм большого количества гормонов щитовидной железы. Избыток гормонов щитовидной железы оказывает негативное воздействие на организм человека – возникает тиреотоксикоз, который проявляется нарушением обмена веществ, изменениями со стороны сердечно-сосудистой, пищеварительной, нервной и других систем организма.
Диффузный токсический зоб является распространенным заболеванием, встречается повсеместно, возникает в любом возрасте, преимущественно между 20 и 50 годами и чаще у женщин. Соотношение числа больных женщин и мужчин в неэндемических по зобу районах 7:1. Важную роль в развитии заболевания играют генетические факторы.
Этиология и патогенез
Этиология окончательно не установлена. В сыворотке крови больных обнаруживают тиреостимулирующие иммуноглобулины (ТСИ) или тиреостимулирующие антитела (ТСАТ), представляющие собой 7S-IgG. Антитела образуются в результате дефекта или дефицита Т-супрессоров, что приводит к взаимодействию одного из «запрещенных» клонов Т-лимфоцитов с органоспецифическими антигенами щитовидной железы. В иммунологический процесс вовлекаются В-лимфоциты, стимулирующие образование ТСИ.
В настоящее время диффузный токсический зоб рассматривается как наследственное аутоиммунное заболевание, которое передаётся многофакторным (полигенным) путём. Факторы провоцирующие развитие заболевания: психические травмы, острые и хронические инфекции (грипп, ангина, ревматизм), черепно-мозговые травмы, избыточная инсоляция, беременность, прием больших доз йода («йод-базедов»), заболевания носоглотки.
Развитие клинической картины заболевания связано с увеличением чувствительности адренорецепторов к катехоламинам, активацией катаболизма белков, сопровождающейся уменьшением экскреции с мочой азота, фосфора, калия и мочевой кислоты. Тиреоидные гормоны влияют на углеводный обмен, их избыток тормозит переход углеводов в жиры, понижает содержание гликогена в печени, усиливает мобилизацию жира из депо и вызывает похудание больных. Избыток тиреоидных гормонов нарушает окислительное фосфорилирование, что является причиной нарушения образования АТФ, мышечной слабости и субфебрилитета.
Симптомы
Заболевание характеризуется многочисленными и разнообразными симптомами. Общими являются жалобы на раздражительность, плаксивость, повышенную возбудимость, нарушения сна, тремор, мышечную слабость, потливость, непереносимость жары, потерю массы тела, несмотря на нормальный или повышенный аппетит, половые расстройства. У женщин в пременопаузе бывает олигоменорея или аменорея. Характерны жалобы на сердцебиения, одышку, а у пожилых – на приступы стенокардии.
Больные выглядят моложавыми, беспокойными, суетливыми. Кожа тонкая, бледная, теплая, влажная, имеет сниженную эластичность. Часто наблюдается ломкость ногтей, выпадение волос, стойкий дермографизм. Характерен тремор пальцев и кончика языка.
Ведущими в клинике тиреотоксикоза являются изменения сердечно-сосудистой системы: тахикардия, достигающая 100 ударов в минуту в покое и 200 ударов при физической нагрузке; экстрасистолия и пароксизмальная мерцательная аритмия; усиление первого тона и систолический шум над всеми точками; кардиомегалия; увеличение пульсового давления. При прогрессировании заболевания развиваются признаки хронической сердечной недостаточности.
Желудочно-кишечный тракт поражается у половины больных. Нарушения иногда могут быть выраженными и занимать центральное место в клинической картине заболевания. У больных развиваются боли в животе, появляется учащенный кашицеобразный стул, тошнота, рвота. Эти симптомы могут возникнуть остро, напоминая почечную или печеночную колики и обострение язвенной болезни желудка.
Специфические проявления диффузного токсического зоба — диффузный зоб, поражения глаз и кожи.
Зоб может иметь дольчатое строение и быть асимметричным. В соответствии с классификацией О.В. Николаева выделяют 5 степеней увеличения щитовидной железы:
- I – железа не видна, но прощупывается перешеек;
- II – железа видна при глотании, пальпируются перешеек и увеличенные доли;
- III – симптом «толстой шеи»;
- IV – выраженный зоб, изменение конфигурации шеи;
- V – зоб очень больших размеров.
Над железой выслушивается сосудистый шум, что свидетельствует о тиреотоксикозе. При других формах зоба этот шум отсутствует.
Cимптомы поражения глаз подразделяются на спастические и механические. Спастические симптомы обусловлены повышением симпатического тонуса и проявляются блеском глаз, расширением глазных щелей, редким миганием. Характерны пристальный или испуганный взгляд, отставание века при взгляде вниз, при взгляде вверх больной не может прищурить глаз, при взгляде прямо видна полоска склеры над радужкой. Эти симптомы могут быть без экзофтальма, уменьшаются или исчезают полностью при излечении тиреотоксикоза.
Механические симптомы составляют офтальмопатию Грейвса, включающую экзофтальм, офтальмоплегию и сдавление структур глазницы. Экзофтальм развивается в результате воспалительной инфильтрации наружных мышц глаза и ретробульбарной клетчатки, сопровождающейся увеличением их объема. Офтальмоплегия – слабость наружных мышц глаза, приводящая к парезу взора вверх и конвергенции, косоглазию и диплопии различной степени выраженности. Сдавление структур глазницы проявляется хемозом, конъюнктивитом и отеком век.
Специфическое поражение кожи называется претибиальной микседемой, располагается на передней поверхности голени. Пораженная кожа утолщена, отграничена от здоровой, напоминает апельсиновую кожуру. На ее поверхности могут появиться бляшки, папулы или узелки.
У пожилых больных метаболические проявления тиреотоксикоза могут быть стертыми, а в клинической картине преобладают вялость, адинамия, слабость. У таких больных до развития тиреотоксикоза появляются симптомы патологии сердечно-сосудистой системы. Присоединение тиреотоксикоза, даже легкой формы, вызывает прогрессирование ХСН, развитие нарушений ритма (экстрасистолии и пароксизмальной мерцательной аритмии), появление застойных явлений в большом и малом кругах кровообращения.
Осложнения тиреотоксикоза
Сердечная недостаточность развивается в результате как прямого действия Т4 и Т3 на миокард, так и их периферических эффектов. Прямое действие проявляется увеличением работы сердца и ЧСС. Повышение возбудимости предсердий является причиной экстрасистолии и мерцательной аритмии. Периферические эффекты обусловлены повышением обмена веществ в периферических тканях, сопровождающимся увеличением кровотока. Длительное сочетание центрального и периферического действия Т4 и Т3 приводит к развитию декомпенсации сердечно-сосудистой системы и ХСН.
Тиреотоксический криз – это быстрое нарастание проявлений тиреотоксикоза. Тиреотоксические кризы развиваются обычно у нелеченных или неправильно леченных больных после травм, неотложных операций, шока и тиреоидэктомии. Предполагают, что пусковым фактором криза является быстрое повышение уровней свободных радикалов Т4 и Т3. Проявляется криз выраженным беспокойством, чрезвычайной раздражительностью, делирием, высокой (до 40 °С) температурой, артериальной гипотонией, тахикардией, рвотой и поносом.
Диагностика
Наличие характерной клинической картины заболевания, жалоб больного и данных о семейном анамнезе аутоиммунных заболеваний, особенно щитовидной железы, позволяют практически сразу же предположить диагноз гипертиреоз.
Определение в крови гормонов щитовидной железы и ТТГ. Общий T4 и свободный T4 повышены почти у всех больных с тиреотоксикозом. Общий T3 и свободный T3 также повышены (менее чем у 5% больных повышен только общий T3, тогда как общий T4 остается нормальным — такие состояния называют T3-тиреотоксикозом). Базальный уровень ТТГ сильно снижен, либо ТТГ не определяется.
Поглощение радиоактивного йода (123I или 131I) щитовидной железой. Для оценки функции щитовидной железы важен тест на поглощение небольшой дозы радиоактивного йода в течение 24 ч. Спустя 24 часа после приема внутрь дозы 123I или 131I измеряется захват изотопа щитовидной железой и затем выражается в процентном соотношении. Необходимо учитывать, что поглощение радиоактивного йода существенно зависит от содержания йода в пище и в окружающей среде. Высокое поглощение радиоактивного йода характерно для токсического зоба.
Радионуклидное сканирование. Функциональное состояние щитовидной железы можно определить в тесте с захватом радиофармпрепарата (радиоактивного йода или технеция пертехнетата). При использовании изотопа йода области железы, которые захватывают йод, видны на сцинтиграмме. Нефункционирующие области не визуализируются и называются «холодными».
Супрессивные пробы с T3 или T4. При тиреотоксикозе поглощение радиоактивного йода щитовидной железой под влиянием экзогенных тиреоидных гормонов (3 мг левотироксина однократно внутрь либо по 75 мкг/сут лиотиронина внутрь в течение 8 сут) не уменьшается. В последнее время эту пробу используют редко, поскольку разработаны высокочувствительные методы определения ТТГ и методы сцинтиграфии щитовидной железы. Проба противопоказана при заболеваниях сердца и пожилым больным.
Ультразвуковое исследование (УЗИ), или эхография, или ультрасонография. Для диффузного токсического зоба характерно увеличение объема щитовидной железы (увеличение объема более 18 см3 у женщин и более 25 см3 у мужчин), усиление кровотока в щитовидной железе.
ЭКГ фиксирует наличие отклонений в работе сердечно-сосудистой системы.
Установление причины тиреотоксикоза:
- Тиреостимулирующие аутоантитела — маркеры диффузного токсического зоба. Выпускаются наборы для определения этих аутоантител методом иммуноферментного анализа (ИФА).
- Все аутоантитела к рецепторам ТТГ (включая тиреостимулирующие и тиреоблокирующие аутоантитела) определяют, измеряя связывание IgG из сыворотки больных с рецепторами ТТГ. Эти аутоантитела выявляются примерно у 75% больных с диффузным токсическим зобом. Проба на все аутоантитела к рецепторам ТТГ проще и дешевле, чем проба на тиреостимулирующие аутоантитела.
- Антитела к миелопероксидазе специфичны для диффузного токсического зоба (а также для хронического лимфоцитарного тиреоидита), поэтому их определение помогает отличить диффузный токсический зоб от других причин тиреотоксикоза.
- Сцинтиграфию щитовидной железы проводят у больных с тиреотоксикозом и узловым зобом, чтобы выяснить:
- Имеется ли автономный гиперфункционирующий узел, который накапливает весь радиоактивный йод и подавляет функцию нормальной тиреоидной ткани.
- Имеются ли множественные узлы, накапливающие йод.
- Являются ли пальпируемые узлы холодными (гиперфункционирующая ткань располагается между узлами).
Дифференциальный диагноз проводят с тревожными состояниями, при которых, как и при тиреотоксикозе, выявляют тахикардию, тремор, раздражительность, слабость, потерю массы тела. Но при тревожных состояниях обычно отсутствуют метаболические нарушения, характерные для тиреотоксикоза.
Феохромоцитома имеет одинаковые клинические проявления с тиреотоксикозом: приступы сердцебиений, потливость, непереносимость жары. Но при феохромоцитоме лабораторные данные (концентрация Т3 и Т4, поглощение Т3) нормальные.
Двусторонний экзофтальм может развиваться при злокачественной гипертонии, ХОЗЛ, синдроме Кушинга, уремии, алкоголизме, имеющих отличные от тиреотоксикоза клинические проявления. В отличие от тиреотоксикоза при этих заболеваниях выявляют низкие титры тиреостимулирующих или тиреоблокирующих антител. Супрессорная проба с Т3 нормальная.
Лечение
Лечение направлено на ограничение выработки тиреоидных гормонов. Существуют три подхода: применение антитиреоидных средств, удаление ткани железы хирургическим путем и ее разрушение с помощью 131I.
Антитиреоидные препараты (тиамазол, пропилтиоурацил, йодиды и др.) уменьшают йодирование тироксина в щитовидной железе путем блокады включения атома йода в молекулу тироксина, ускоряют выведение из щитовидной железы йодидов и угнетают активность ферментных систем, участвующих в окислении йодидов в йод.
Тиамазол (мерказолил) – синтетическое антитиреоидное вещество – назначают внутрь после еды (при легких и средних формах тиреотоксикоза – по 0,005 г 3–4 раза в день, при тяжелой форме – по 0,01 г 3–4 раза в день). После наступления ремиссии (через 5–6 недель) суточную дозу уменьшают каждые 5–10 дней по 0,005–0,01 г и подбирают минимальную поддерживающую дозу (0,005 г 1 раз в день или через день).
Пропилтиоурацил назначают по 75–100 мг/сут, в тяжелых случаях – до 300–600 мг/сут в несколько приемов, поддерживающая доза 25–150 мг/сут. У пропилтиоурацила есть важное преимущество перед тиамазолом: он подавляет периферическое превращение Т4 в Т3 и быстрее уменьшает симптоматику тиреотоксикоза.
Антитиреоидную поддерживающую терапию продолжают 1–2 года, после чего у 40–65% больных наступает устойчивая ремиссия или полное излечение, признаками которых являются уменьшение зоба, нормализация супрессивной пробы с Т3, исчезновение антител к рецептору ТТГ.
Антитиреоидные средства имеют различные побочные эффекты: тошноту, рвоту, нарушение функции печени, боль в суставах и мышцах. Главный побочный эффект – лейкопения. Легкая лейкопения развивается примерно у 10% больных и не является противопоказанием для продолжения лечения. Антитиреоидные препараты отменяют при уменьшении гранулоцитов до 1500 мкл-1. У 0,2% больных возможно острое развитие агранулоцитоза. У некоторых больных развиваются аллергические реакции, которые устраняются Н1-блокаторами. Целесообразен переход на другой препарат. При агранулоцитозе и тяжелых аллергических реакциях следует отменить любые антитиреоидные препараты.
Йодиды (калия йодид и перхлорит, натрия йодид, трийодтиронин и др.) быстрее блокируют высвобождение Т4 и Т3 из щитовидной железы, чем антитиреоидные препараты, но их эффект преходящий. Йодиды применяют главным образом при тиреотоксическом кризе, в комплексной терапии с антитиреоидными средствами и для поддержания эутиреоза в начале лечения 131I.
При тяжелом тиреотоксикозе показаны глюкокортикоиды, снижающие уровень Т4. Назначают дексаметазон 2 мг через 6 ч. Для уменьшения адренергических проявлений тиреотоксикоза (тахикардии, тремора, потливости) применяют в-адреноблокаторы. Чаще всего используют пропранолол по 40–120 мг/сут.
При антитиреоидной терапии длительная ремиссия наступает менее чем у 50% больных. Рецидивы возникают обычно в течение 4–6 мес после отмены препаратов. Поэтому каждые 4–6 недель необходимо проводить клиническое исследование больных и определять уровень Т4 и ТТГ в сыворотке. Вероятность развития гипотиреоза по сравнению с получавшими радиоактивный йод больными значительно меньше.
Хирургическое лечение. Субтотальная резекция щитовидной железы приводит к быстрому эффекту. Большинство больных излечиваются полностью. Рецидивы развиваются в отдаленный период только у 10% больных. Хирургическое лечение показано молодым больным при неэффективности антитиреоидной терапии; больным, отказывающимся от 131I, и беременным с тяжелым тиреотоксикозом или его рецидивом.
Всем больным необходима предоперационная подготовка, в течение которой необходимо добиться эутиреоза с помощью антитиреоидных препаратов. После этого назначают йодиды (например, йодид калия по 1–2 капли внутрь 3 раза в сутки), одновременно продолжается прием антитиреоидных препаратов. Йодиды усиливают кровоток в щитовидной железе и ускоряют инволюцию ее ткани.
Субтотальную резекцию должен проводить опытный хирург, в руках которого операция бывает эффективной и безопасной. Во время операции возможны кровотечения и повреждения возвратного нерва, приводящего к парезу голосовых связок. Послеоперационный период иногда осложняется инфекциями, гипотиреозом и гипопаратиреозом, редко выявляется преходящая, не требующая лечения гипокальциемия.
Лечение радиоактивным йодом. Радиоактивный йод считается средством выбора, он так же эффективен, как и хирургический метод. Лечение радиоактивным йодом показано пожилым, так как операция у них сопряжена с высоким риском; молодым, у которых тиреотоксикоз рецидивировал после хирургического лечения, и тем больным, у которых есть тяжелая сопутствующая болезнь, являющаяся противопоказанием к операции.
Применяют обычно дозу 131I 5,9 МБк на 1 г расчетной массы щитовидной железы, вызывающую гипотиреоз. Его профилактику проводят замещающими дозами левотироксина. Возможно применение меньшей дозы – 3 МБк на 1 г массы железы, но гипотиреоз наступает значительно позже. Поэтому одновременно назначают антитиреоидные препараты и пропранолол. Эффект терапии выявляется в течение 2–3 мес. Больного необходимо обследовать ежемесячно и измерять уровень Т4 в сыворотке. Если эффект не проявляется в течение месяца, лечение следует повторить.
Лечение радиоактивным йодом обычными дозами имеет кумулятивный риск гипотиреоза: в течение 10 лет он возникает у 50–70% больных. Гипотиреоз развивается медленно и скрыто, может проявиться тяжелыми осложнениями. Поэтому рекомендуется раннее назначение левотироксина в замещающих дозах.
Редким осложнением является лучевой тиреоидит, развивающийся через 7–10 суток после приема 131I и обусловленный вымыванием гормонов из ткани железы. Проявляется тиреоидит тиреотоксическим кризом или декомпенсацией сердечной недостаточности, которые развиваются у больных с тяжелым тиреотоксикозом и сопутствующей ХСН II А-Б ст. Поэтому таким больным назначают антитиреоидные средства. За 3 сут до приема 131I их отменяют и вновь назначают через 3–4 дня после него.
Установлено, что лечение радиоактивным йодом не увеличивает риск рака щитовидной железы, лейкоза и развития генетических нарушений. Риск радиоактивного йода сравним с риском бариевой клизмы или внутривенной урографии.
Лечение тиреотоксического криза направлено на максимально быстрое уменьшение проявлений тиреотоксикоза. Больного необходимо поместить в прохладную палату, в которой возможна подача увлажненного кислорода. Проводят регидратацию с внутривенным введением солевого раствора и глюкозы с комплексом витаминов В. Показано введение глюкокортикоидов, восстанавливающих резерв коры надпочечников, снижающийся при кризе.
При шоке необходимо внутривенное ведение вазопрессоров (норадреналина, дофамина, изопротеренола, добутамина или амринона). Развившийся пароксизм мерцательной аритмии купируют внутривенным введением новокаинамида или дизопирамида, аймолина или кордарона.
Гипертиреоз уменьшается быстрым и длительным приемом внутрь антитиреоидных препаратов (например, 100 мг пропилтиоурацила каждые 2 ч). Одновременно внутривенно или перорально водят большие дозы йода – до 1 г/сут с целью торможения секреции гормонов. В комплекс лечения криза должны быть включены β-адреноблокаторы. Назначают пропранолол внутрь по 40–80 мг каждые 6 ч или внутривенно по 2 мг при тщательном электрокардиологическом контроле.
Целесообразно продолжение внутривенного введения дексаметазона по 2 мг или преднизолона по 30 мг каждые 6 ч. Глюкокортикоиды тормозят секрецию тиреоидных гормонов, нарушают образование в тканях Т3 из Т4 и нормализуют активность коры надпочечников. Терапию криза продолжают до нормализации общего состояния больных. После этого разрабатывают систему планового лечения тиреотоксикоза.
medicoterapia.ru
Диффузный токсический зоб. Лечение диффузно токсического зоба ― Клиника Щитовидной Железы доктора А. В. Ушакова
Диффузно токсический зоб (ДТЗ)
Гиперкомпенсаторное (усиленное) напряжение щитовидной железы с распространённым увеличением её объёма и избыточным насыщением организма щитовидными гормонами (Т3 и Т4), оказывающими специфическое влияние.К синонимам этого состояния относятся понятия:
1) гипертиреоз, как увеличение в крови щитовидных гормонов,
2) тиреотоксикоз, как влияние избытка тиреоидных гормонов на организм,
3) струма (увеличение щитовидной железы).
Диффузный токсический зоб в популяции занимает от 0,47% до 1,53%, преобладая в области гипертиреоидного синдрома (до 70-80%), к которому относятся гипертиреоидный процесс и узловой гипертиреоз.
Традиционные обозначения ДТЗ связаны с именами Базедова (Германия) и Грейвса (Великобритания), описавшими в 19 веке этот синдром: увеличение щитовидной железы, сердцебиение и экзофтальм. Сочетание трёх признаков болезни непостоянно и зависит от индивидуальных компенсаторных особенностей. На это обстоятельство обращал внимание С.П. Боткин, призывая коллег лишь ориентироваться на этот синдром (т.е. на необязательность сочетания признаков болезни), нацеливая основное внимание на сущность болезни.
Классификация ДТЗ
Вариации диффузного зоба различают на следующих уровнях:1. структуры (по величине зоба),
2. избытка тиреоидных гормонов,
3. активизации иммунной системы,
4. присутствия осложнений,
5. источника гипертиреоза,
6. величины внещитовидной компенсации (тяжести течения).
Первые классификации зоба основывались на критериях пальпаторной и зрительной заметности зоба ― от его отсутствия до очень большой величины. Это было связано с невозможностью точного измерения объёма железы. С введением в клиническую практику ультразвуковой диагностики специалисты получили возможность сравнительно точно вычислять объём железы.
В отличие от русской классификации О.Н. Николаева (1949, 1955) и ВОЗ (1994, 2001), нацеленных лишь на физикальную оценку увеличения щитовидной железы (т. е. зоба) путём пальпации и внешнего осмотра, в Клинике А.В. Ушакова создана и успешно применяется классификация зоба, позволяющая точно оценивать зоб по объёму железы (в мл), с учётом компенсаторного процесса.
Внешняя оценка зоба служит предварительной диагностической ориентацией. Поэтому определять степень зоба по классификации ВОЗ (1994, 2001) или по О.В. Николаеву (1949, 1955) неверно при ультразвуковом исследовании, относящемуся к аппаратной диагностике. Это способы диагностики разного уровня. Поэтому они должны иметь разный классификационный оценочный инструмент. Вместо приблизительного определения зоба по принципу «нет ― вероятно ― есть» требуется чёткое и точное ориентирование в известных единицах измерения (мл). Наша Клиника использует и предлагает коллегам к применению следующую классификацию степеней зоба (см. таблицу).
| Степень | Состояние | Признак |
| 1 | Малой компенсации | Объём щитовидной железы больше среднего конституционального (по полу, возрасту, массе тела и росту), но не превышает двойной объём. Обычно, для взрослых более 12-14 мл, но менее 20-23 мл. |
| 2 | Значительной компенсации | Объём щитовидной железы увеличен от 2 до 4 раз от среднего конституционального (по полу, возрасту, массе тела и росту). Обычно, для взрослых более 23-24 мл, но менее 40 мл. |
| 3 | Субкомпенсации | Объём щитовидной железы увеличен от 4 до 6 раз от среднего конституционального (по полу, возрасту, массе тела и росту). Обычно, для взрослых более 40 мл, но менее 60 мл. |
| 4 | Малой декомпенсации | Объём щитовидной железы увеличен от 6 до 10 раз от среднего конституционального (по полу, возрасту, массе тела и росту). Обычно, для взрослых более 60 мл, но менее 100-110 мл. |
| 5 | Значительной декомпенсации | Объём щитовидной железы увеличен более чем в 10 раз от среднего конституционального (по полу, возрасту, массе тела и росту). Обычно, для взрослых более 110-120 мл. |
В основе этой классификации находятся три критерия:
1. компенсаторный
2. измерительный (в мл)
3. кратный
Это делает классификацию сущностной, точной и при этом простой (удобной для запоминания и применения).
Избыток тиреоидных гормонов в крови определяет тактику лечения, включая дозировку тиреостатических средств, и прогноз болезни. В связи с изменчивой динамикой гипертиреоза, чётких критериев разграничения ДТЗ не создано. Тем не менее, в научной литературе встречаются указания на разную степень избытка щитовидных гормонов в крови, обозначаемые обычно: малый, средний, большой избыток гормонов.
Активность иммунной системы проявляется титром антител к элементам щитовидной железы. Количество антител АТ-ТПО и АТ-ТГ указывает на величину функционального напряжения и истощение ткани железы. Изменение титра антител к рецепторам ТТГ (АТ-рТТГ) ориентирует на интенсивность регуляции гормонообразования, что тоже соответствует функциональной напряжённости железы.
Среди осложнений при диффузном тиреотоксикозе могут встречаться тиреотоксический криз, офтальмопатия, сердечная недостаточность, гипертонический криз.
Среди источников гипертиреоза при ДТЗ выделяют три патогенетических варианта: первичный (щитовидной железы), вторичный (гипофизарный) и третичный (гипоталамический).
При диффузном токсическом зобе различают несколько степеней тяжести течения гипертиреоза. Разные исследователи выделяют от двух до пяти степеней. Некоторые ошибочно называют их стадиями. Эти изменения провоцируются избытком тиреоидных гормонов, но не относятся к самой щитовидной железе, являясь менее и более выраженными признаками истощения компенсации внещитовидных структур.
Причины возникновения диффузного токсического зоба
Основной и более распространённой причиной диффузного токсического зоба щитовидной железы является значимое психическое перенапряжение. Любого рода психический стресс может оказать провоцирующее болезнь влияние.Исследователи описывают разные жизненные обстоятельства, ведущие к активной реакции щитовидной железы с гиперпродукцией гормонов. Среди них: сильный страх и связанный с ним испуг, психические потрясения, вызванные судебным процессом, межличностным общением (измена, развод, уход из жизни или болезнь близкого человеком…), опасностью (жизни своей или другого, экономической…). Все эти и подобные причины могут оказать провокационное влияние в развитии токсического зоба.
Стрессовое перенапряжение, ведущее к гипертиреозу с образованием зоба, может быть вызвано течением беременности, общим болезненным состоянием и, особенно, заболеваниями органов головы и шеи. Интенсивно текущие тонзилярная ангина, ларингит, фронтит, гайморит, отит способны стать источником активизации щитовидной железы (через сегментарную нервную систему). Кроме того, значительные стоматологические заболевания, лечебные мероприятия (например, имплантация) и агрессивные косметические процедуры могут оказать стимулирующее действие.
К причинам токсического зоба относятся стрессовые адаптационные и переадаптационные нагрузки. Кратковременная (1-2 недели) поездка из холодного климата в тёплый, резкое смещение сна-бодрствования из-за перелёта в другой часовой пояс, поход в горы без постепенной тренировочной подготовки, интеллектуальный штурм в трудовой и личной жизнедеятельности ― все эти и подобные обстоятельства могут спровоцировать диффузные процессы в щитовидной железе с развитием гипертиреоза и зоба.
Симптомы диффузно токсического зоба
Синдрому «диффузный токсический зоб» соответствует три основных симптома ― увеличение объёма щитовидной железы (зоб), усиление сердечных сокращений, воспринимаемых пациентом как сердцебиение, и выпячивание глазных яблок из орбит (экзофтальм). Такое сочетание встречается не всегда. Оно не обязательно, поскольку зависит от индивидуальных компенсаторных резервов со стороны сердечно-сосудистой системы, самой щитовидной железы и глазного аппарата.Вместе с тем, понятие «диффузный токсический зоб» некоторыми специалистами характеризуется как болезнь, и потому обладающее соответствующими нозологическими категориями ― этиологией, патогенезом, клиническим проявлением, прогнозом и лечебной тактикой. В связи с этим, к ДТЗ относят определённые симптомы, которые, впрочем, наблюдаются при гипертиреозе без зоба и даже при гипотиреозе.
Многие пациенты и нередко врачи ориентируются на симптомы, как на чёткие ориентиры в распознавании болезни. Это неверно. Например, якобы характерные для гипертиреоза явления исхудания, слабости мышц, сердцебиение могут наблюдаться при гипотиреозе. С другой стороны, при гипертиреозе пациент может иметь обычное умеренное и даже «более плотное» телосложение, общую зябкость или ощущение холода в ступнях ног, т.е. всё то, что свойственно гипотиреозу.
Диффузный зоб может протекать с ощущениями дискомфорта в шее или без них. Пациенты испытывают разные ощущения. Это могут быть чувство давления в шее, доходящее до удушения, некоторая неопределенность восприятия, называемая «дискомфорт» или «неудобство», ощущение чего-то лишнего или избытка слизи в горле, также нередко встречается ощущение «кома в горле». Все эти чувства обычно временны. Появляются периодически. Если же они присутствуют ежедневно, то обязательно имеют периоды усиления и уменьшения.
Дискомфорт и ком в горле при токсическом зобе не зависит от объёма щитовидной железы, а связан с величиной перенапряжения сегментарной вегетативной нервной системы шеи. Этот симптом встречается, по данным нашей Клиники, почти в 25-30% случаев всех заболеваний щитовидной железы. Описание его в научной литературе встречается редко. Впервые пояснение источника этого симптома разъяснено в монографии А.В. Ушакова «Доброкачественные заболевания щитовидной железы Клиническая классификация».
Осложнения диффузно токсического зоба
К осложнениям при диффузном тиреотоксикозе относят: 1) изменения со стороны зрительного аппарата, 2) истощение компенсации сердечно-сосудистой системы и 3) тиреотоксический криз.У некоторых пациентов при тиреотоксикозе (независимо от присутствия диффузного зоба) наблюдаются так называемые «глазные» симптомы. Чаще это встречается при значительном гипертиреозе с очень большим увеличением гормонов Т3св. и Т4св. в крови. Эти явления могут быть односторонними и двусторонними. В последнем случае также может быть заметно преобладание признаков болезни с одной из сторон. Такое одностороннее течение связано с преобладанием активности в правой или левой сегментарной нервной системе.
Среди глазных признаков может быть заметно выпячивание глазных яблок из орбит ― экзофтальм («пучеглазие»). Кроме того, это явление может сопровождаться признаками отставания век, ухудшением ирригации слёз, нарушением остроты зрения. Встречаются симптомы Мебеуса (нарушение конвергенции глаз), Кохера (при взгляде вверх сохранение полоски склеры вверху), Дельримпля (значительное раскрытие глазной щели), Штельвага (редкое мигание). Все симптомы закономерны, зависимы от величины выпячивания глазных яблок и увеличения объёма и пареза глазных мышц.
При длительно текущем тиреотоксикозе возможно истощение компенсаторных резервов сердечно-сосудистой системы. Могут наблюдаться явления сердечной недостаточности.
В результате стрессовых обстоятельств (физической перегрузке, операции на щитовидной железе, в период беременности, остром заболевании или обострения течения хронического процесса) у пациентов с диффузным токсическим зобом возможно развитие тиреотоксического криза, ведущего в том числе к коматозному состоянию. Это происходит в результате активизации проводниковой симпатической и метаболической (адреналовой) систем из-за избыточного поступления в кровь щитовидных гормонов (Т3св. и Т4св.). Криз проявляется тахикардией, сердечной аритмией (в т.ч. мерцательной), гипертензией (умеренной или значительной), увеличением температуры тела, крупным тремором на периферии. Также могут наблюдаться психическое возбуждение, психоз, желудочная и кишечная диспепсия (тошнота, рвота, диарея). Пиком такого состояния становится кома с апатией и торможением жизненно важных функций. Обязательно применение неотложных лечебных мер.
Диагностика ДТЗ
Диагностические мероприятия при диффузном токсическом зобе сводятся к анализу гормонального обмена в крови и ультразвуковому исследованию (УЗИ). Остальные диагностические мероприятия относятся к вспомогательным.Важен анализ крови. Признаками тиреотоксического процесса служат значительное уменьшение ТТГ (обычно менее 0,01 мкЕд/л) в сочетании с увеличением Т3св. (свободного трийодтиронина) и Т4св. (свободного тироксина) выше референсных значений лаборатории. Обязательно при любом анализе крови (начальном или контрольном) оценивать эти три показателя вместе.
Среди всех этих показателей более важным следует считать Т3св.! Ошибочно оценивать только ТТГ. Даже при «нулевом» ТТГ (гормон гипофиза, заставляющий щитовидную железу производить гормоны Т4св. и Т3св.) показатель Т3св. может находиться у верхнего края референтного предела, что безусловно, укажет на улучшение.
Показатель активности иммунной системы АТ-рТТГ (антитела к рецепторам ТТГ) указывает на увеличение или уменьшение возбуждения нервной системы, активизирующей щитовидную железу. Антитела к рТТГ являются регуляторными ― блокирующими (а при необходимости ― стимулирующими) производство железой Т3св. и Т4св. По уменьшению АТ-рТТГ можно судить о восстановительной динамике, а по увеличению ― об обострении болезни. Ошибочно характеризовать увеличение АТ-рТТГ при тиреотоксическом зобе как признак агрессии иммунной системы и отсутствие излечения. Антитела к ТГ и ТПО указывают на величину перенапряжения и истощения щитовидной железы при диффузном токсическом зобе.
УЗИ щитовидной железы позволяет оценить степень зоба, что, в свою очередь, указывает на величину компенсаторного перенапряжения. В Клинике доктора А.В. Ушакова применяют классификацию зоба, позволяющую оценивать степень компенсации по 5 степеням. Первые две степени отражают начальные изменения в ткани железы, связанные преимущественно с гипертрофией. Механизм этих изменений внутриклеточный и внутрифолликулярный. Третья степень вместе с 4-й и 5-й степенями указывают на истощение этих вспомогательных (гиперпластических) резервов компенсации и присоединение тканевых изменений ― формирование новых клеток, фолликулов и долек.
Если первые две степени хорошо обратимы при правильном лечении, третья степень ― частично обратима, то четвёртая и пятая степени зоба мало и почти не обратимы. Впрочем, такая условная «необратимость», тем не менее, позволяет улучшать компенсаторный резерв и восстанавливать гормональный обмен до эутиреоза даже при 5-й степени зоба.
Вспомогательные диагностические способы позволяют уточнять особенности болезни. К ним относится сцинтиграфия щитовидной железы и томография (а также МРТ). Первая поможет уточнить топографические функциональные особенности ткани правой и левой долей, а вторая ― смещение органов шеи, размеры железы и величину смещения железы за ключицу в грудную клетку.
Лечение
Во всём мире распространена подавляюще-разрушающая тактика в отношении щитовидной железы при диффузном токсическом зобе. Поскольку развитие ДТЗ связывается с агрессивной стимуляцией иммунной системой ткани щитовидной железы, то предлагаемая тактика сводится к начальной блокировке щитовидной железы тиреостатическими препаратами, и при отсутствии улучшения в течение 1,5-2 лет ― к операционному удалению или радиоактивному повреждению большей части железы. Это ведёт к гипотиреозу. В дальнейшем применяют заместительную лекарственную помощь, введением искусственных гормонов. По мнению нашей Клиники, этот путь вспоможения и повреждения не рационален.В КЛИНИКЕ ЩИТОВИДНОЙ ЖЕЛЕЗЫ доктора А.В. Ушакова применяется противоположная тактика. Лечебными мероприятиями осуществляется уменьшение стимуляции со стороны вегетативной нервной системы на щитовидную железу, что ведёт к уменьшению производства ею гормонов и формированию эутиреоза. У пациентов, по данным анализа крови, нормализуются ТТГ, Т3св и Т4св. а также восстанавливается уровень антител ― АТ-рТТГ, АТ-ТПО, АТ-ТГ. Примеры такого восстановления представлены на нашем сайте.
Достигается устойчивый в годах результат. С лечебной целью применяются физиотерапевтические методики Клиники, в частности, лазеротерапия и фототерапия. О лечебных возможностях фототерапии и противопоказаниях сможете прочесть на сайте в соответствующих разделах.
www.dr-md.ru
Диффузно-токсический зоб. Важно знать.
Диффузно-токсический зоб (ДТЗ) -это воспалительное (аутоиммунного характера) заболевание щитовидной железы, проявляющееся синдромом тиреотоксикоза=гипертиреоза (см. статью «Тесты самодиагностики дисфункции щитовидной железы») — то есть действием на организм избыточного количества гормонов щитовидной железы — Т3 и Т4.ДТЗ достаточно распространён в северо-западном регионе России и заслуживает пристального внимания к себе. А почему, вы поймёте прочитав следующие краткие тезисы.
Итак, если вам выставлен диагноз «Диффузно-токсический зоб».
1. ДТЗ — состояние жизнеугрожающее! Есть такое осложнение ДТЗ — тиретоксический криз (по аналогии с гипертоническим кризом), в своём исходе это состояние имеет острую сердечную недостаточность! И разовьётся тиреотоксический криз в том случае, если не лечить ДТЗ совсем (в течение более 2-4 лет от начала заболевания).
2. ДТЗ «склонен» к рецидивам (то есть возврату болезни повторно). Особенно, при неправильном лечении, раннем прерывании лечения (чем «грешат пациенты», так как лечение достаточно длительное 1-2 года). Но и самостоятельно, при соблюдении всех условий лечения, рецидив ДТЗ, к сожалению, может быть.
3. Более 2-х рецидивов ДТЗ — является показанием к удалению щитовидной железы оперативно или с помощью радиойодтерапии (о ней будет отдельная статья).
4. При лечении ДТЗ надо регулярно сдавать для контроля гормонального фона следующие анализы: ТТГ, Т4 свободный, Т3 свободный, и ходить с результатами анализов к врачу не реже 1 раза в 2 месяца Самостоятельно изменять дозу вы не можете!
По опыту знаю: лечить ДТЗ — это целое искусство, так как, зачастую, заболевание сочетается с другой патологией щитовидной железы, например АИТ (аутоиммунный тиреоидит), что усложняет терапию и т.д.).
5. ДТЗ не противопоказание к беременности и кормлению грудью. При беременности течение ДТЗ всегда стабилизируется!
6.Тиреостатики (препараты для лечения ДТЗ)не противопоказаны при беременности и кормлении, только надо правильно подобрать дозу с лечащим врачом.
7. ДТЗ при беременности встречается реже, чем гипотиреоз (и ДТЗ менее опасен для плода, чем Гипотиреоз).
8. Препараты йода при ДТЗ не принимают! А вот Л-тироксин — принимают. Есть такая схема лечения ДТЗ, называется «блокируй-замещай», куда входят как тиреостатики, так и Л-тироксин, его так же используют при сочетании ДТЗ с АИТ.
9. ДТЗ не исключает одновременного развития других заболеваний щитовидной железы — узлового зоба, АИТ, рака щитовидной железы.
10. При течении ДТЗ надо избегать любого перегрева: пребывания в бане, сауне, на солнце, в солярии. Это может спровоцировать рецидив!
11. ДТЗ — острое состояние, а не хроническое.
12. Склонность к ДТЗ наследуется.
13. Не удивляйтесь: ДТЗ провоцируется стрессом!
14. Самое неприятное эстетическое осложнение ДТЗ (радует то, что бывает не у всех пациентов) — тиреотоксическая офтальмопатия! (по-народному «пучеглазие»). Это отёк век, клетчатки за глазами, что создаёт впечатление «вышедших из орбит» глаз. Чтобы избежать этого состояния, прежде всего, надо — бросить курить, регулярно ходить к врачу и корректировать дозы препарата, показаться окулисту — эндокринологу (он проведет осмотр, назначит лечение и отправит на УЗИ орбит для уточнения дальнейшего прогноза).
15. При тяжёлом течении ДТЗ показана госпитализация.
16. У 50% пациентов с ДТЗ наступает полное излечение!
www.mc21.ru
Лечение диффузного токсического зоба | Компетентно о здоровье на iLive
Лекарственное лечение диффузного токсического зоба
Для медикаментозного лечения диффузного токсического зоба используются препараты тиомочевины — мерказолил (зарубежные аналоги methimazole и thiamazole), карбимазол и пропилтиоурацил, блокирующие синтез тиреоидных гормонов на уровне перехода монойодтирозина в дийодтирозин. В последнее время появились данные о воздействии тиреостатических препаратов на иммунную систему организма. Иммунодепрессивное действие мерказолила наряду с непосредственным действием на синтез тиреоидных гормонов, по-видимому, обусловливает преимущество мерказолила для лечения диффузного токсического зоба перед другими иммунодепрессантами, так как ни один из них не обладает способностью нарушать синтез тиреоидных гормонов и избирательно накапливаться в щитовидной железе. Лечение мерказолилом может проводиться при любой тяжести заболевания. Однако условием для успешного медикаментозного лечения является увеличение железы до III степени. В более тяжелых случаях больные после предварительной подготовки тиреостатическими препаратами направляются на хирургическое лечение или радиоиодтерапию. Дозы мерказолила колеблются от 20 до 40 мг/сут в зависимости от тяжести заболевания. Лечение проводят под контролем частоты пульса, массы тела, клинического исследования крови. После уменьшения симптомов тиреотоксикоза назначают поддерживающие дозы мерка-золила (2,5-10 мг/сут). Общая продолжительность медикаментозной терапии при диффузном токсическом зобе составляет 12-18 мес. При невозможности снять мерказолил в связи с ухудшением состояния на поддерживающих дозах и возникновением рецидивов заболевания больных следует направлять на хирургическое лечение либо радиойодтерапию. Больных со склонностью к рецидивам лечить мерказолилом в течение многих лет не рекомендуется, так как существует возможность на фоне усиления продукции тиреотропного гормона морфологических изменений в щитовидной железе. На вероятность возникновения рака щитовидной железы в результате длительной, в течение ряда лет проводимой тиреостатической терапии указывают многие авторы. До сих пор отсутствуют надежные методы определения активности иммунных изменений в течение тиреостатического лечения. Целесообразным для прогноза ремиссии или ее отсутствия является определение тиреостимулирующих антител. В тех случаях, когда достигается эутиреоидное состояние, а содержание тиреостимулирующих антител не снижается, как правило, возникают рецидивы. По последним данным, может быть полезно определение гистосовместимости по системе HLA. У носителей определенных антигенов (В8, DR3) после медикаментозной терапии наблюдалось значительно более частое рецидивирующее течение. При терапии тиреостатическими препаратами могут наблюдаться осложнения в виде токсико-аллергических реакций (зуд, крапивница, агранулоцитоз и т. д.), зобогенного эффекта, медикаментозного гипотиреоза. Наиболее серьезным осложнением является агранулоцитоз, который возникает у 0,4-0,7 % больных. Одним из первых признаков этого состояния является фарингит, поэтому жалобы больного на появление болей или неприятных ощущений в горле не должны оставаться без внимания. Необходим тщательный контроль за количеством лейкоцитов в периферической крови. К другим побочным действиям мерказолила относятся дерматиты, артралгии, миалгии, лихорадка. При появлении симптомов непереносимости тиреостатических препаратов лечение мерказолилом должно быть прекращено. Зобогенный эффект является следствием чрезмерной блокады синтеза тиреоидных гормонов с последующим выбросом ТТГ, что в свою очередь обусловливает гипертрофию и гиперплазию щитовидной железы. Для предотвращения зобогенного эффекта при достижении эутиреоза к лечению мерказолилом добавляют тироксин 25-50 мкг.
Лечебное применение препаратов йода в настоящее время строго ограничено. У больных диффузным токсическим зобом (базедовой болезнью) в результате длительной терапии этими лекарственными веществами увеличивается и уплотняется щитовидная железа при отсутствии достаточной компенсации тиреотоксикоза. Эффект препарата носит преходящий характер, нередко наблюдается постепенный возврат симптомов тиреотоксикоза с развитием рефрактерности к йоду и антитиреоидным препаратам. Применение первого не влияет на уровень тиреостимулирующей активности крови больных с диффузным токсическим зобом. Препараты йода лишь в редких случаях могут быть использованы как самостоятельный метод лечения.
Диффузный токсический зоб является медицинским показанием для искусственного прерывания беременности в сроки до 12 нед. В настоящее время при сочетании беременности и диффузного токсического зоба легкой и средней степени тяжести и небольшого увеличения щитовидной железы назначают антитиреоидные препараты. При более тяжелом тиреотоксикозе больных направляют на оперативное лечение. В период беременности доза тиреостатических препаратов должна быть снижена до минимальной (не более 20 мг/сут). Тиреостатики (за исключением пропицила) противопоказаны при кормлении ребенка грудью. Добавление тиреоидных препаратов к тиреостатическим средствам во время беременности противопоказано, так как антитиреоидные вещества в противоположность тироксину проходят через плаценту. Поэтому для достижения эутиреоидного состояния у матери необходимо увеличение дозировки мерказолила, что является нежелательным для плода.
К антитиреоидньм препаратам, применяемым для лечения диффузного токсического зоба, относится перхлорат калия, блокирующий проникновение йода в щитовидную железу. Дозы перхлората калия подбирают в зависимости от захвата 131I щитовидной железой. При легких формах назначают 0,5-0,75 г/сут, при формах средней тяжести — 1-1,5 г/сут. Применение перхлората калия иногда вызывает диспепсические явления и кожные аллергические реакции. К редким осложнениям при приеме этого лекарственного вещества относятся апластическая анемия и агранулоцитоз. Поэтому обязательным условием его применения является систематический контроль за картиной периферической крови.
В качестве самостоятельной терапии при легкой и средней тяжести тиреотоксикоза в отдельных случаях используется карбонат лития. Существуют два возможных пути воздействия лития на функцию щитовидной железы: непосредственное ингибирование синтеза гормонов в железе и влияние на периферический обмен тиронинов. Карбонат лития в таблетках по 300 мг назначают из расчета 900-1500 мг/сут в зависимости от выраженности симптомов. При этом эффективная терапевтическая концентрация иона лития в крови составляет 0,4-0,8 мэкв/л, что редко приводит к нежелательным побочным реакциям.
Учитывая патогенетические механизмы формирования кардиоваскулярных нарушений при диффузном токсическом зобе, наряду с тиреотоксическими препаратами применяются бета-адреноблокаторы (индерал, обзидан, анаприлин). По нашим данным, бета-блокаторы существенно расширяют возможности терапевтических мероприятий при диффузном токсическом зобе (базедовой болезни), а рациональное их применение способствует повышению эффективности проводимой терапии. Показаниями для назначения этих препаратов являются стойкая, не уступающая терапии тиреостатиками, тахикардия, нарушение сердечного ритма в виде экстрасистолии, мерцательной аритмии. Назначение лекарств проводится с учетом индивидуальной чувствительности и с предварительным проведением больным функциональных проб под контролем ЭКГ. Дозы препаратов варьируют от 40 мг до 100-120 мг/сут. Признаками адекватности дозы является уменьшение частоты сердечных сокращений, болевых ощущений в области сердца, отсутствие побочных проявлений. На фоне комплексной терапии бета-адреноблокаторами в течение 5-7 дней наступает отчетливый положительный эффект, улучшается общее состояние больных, урежается частота сердечных сокращений, уменьшаются или исчезают экстрасистолы, тахисистолическая форма мерцательной аритмии переходит в нормо- или брадисистолическую форму, а в отдельных случаях восстанавливается сердечный ритм; уменьшаются или исчезают боли в области сердца. Назначение бета-блокаторов оказывает положительное действие на больных, которые ранее лечились тиреостатическими препаратами без особого эффекта, и, кроме того, позволяет в ряде случаев значительно уменьшить дозу мерказолила. Бета-блокаторы успешно применяются в предоперационной подготовке больных с непереносимостью даже малых доз тиреостатических препаратов. Назначение в таких случаях обзидана или атенолола в сочетании с преднизолоном (10-15 мг) или гидрокортизоном (50-75 мг) позволяет добиться клинической компенсации тиреотоксикоза. Бета-блокаторы воздействуют на симпатическую нервную систему (симпатолическое действие) и непосредственно на сердечную мышцу, снижая ее потребность в кислороде. Кроме того, эти препараты влияют на метаболизм тиреоидных гормонов, способствуя превращению тироксина в неактивную форму трийодтиронина — реверсивный (RT3) Т3. Уменьшение уровня Т3, увеличение RT3 считается специфическим действием пропранолола на обмен тиреоидных гормонов на периферии.
В лечении диффузного токсического зоба широко используются кортикостероиды. Положительный эффект применения кортикостероидов обусловлен компенсацией относительной надпочечниковой недостаточности при диффузном токсическом зобе, влиянием на метаболизм тиреоидных гормонов (под действием глюкокортикоидов тироксин превращается в RT3), а также иммунодепрессивным действием. Для компенсации надпочечниковой недостаточности в зависимости от степени тяжести ее используют преднизолон в физиологичных дозировках — 10-15 мг/сут. В более тяжелых случаях рекомендовано парентеральное введение глюкокортикоидов: гидрокортизона 50-75 мг, внутримышечно или внутривенно.
Лечение эндокринной офтальмопатии проводится совместно эндокринологом и офтальмологом с учетом степени тяжести заболевания, активности иммуновоспалительного процесса и наличия клинических признаков нарушения функции щитовидной железы. Непременным условием успешного лечения офтальмопатии при диффузном токсическом зобе (базедовой болезни) является достижение эутиреоидного состояния. Патогенетическим методом лечения ЭОП является терапия глюкокортикоидами, которые оказывают иммуносупрессивное, противовоспалительное, противоотечное действие. Суточная доза 40-80 мг преднизолона с постепенным снижением через 2-3 нед и полной отменой через 3-4 мес. Ретробульбарное введение преднизолона нецелесообразно в связи с образованием рубцовой ткани в ретробульбарной области, затрудняющей отток крови и лимфы. Кроме того, эффект ГК при ЭОП связан с их системным, а не местным действием.
В литературе существуют противоречивые сведения об эффективности лечения экзофтальма и миопатии иммунодепрессантами (циклофосфаном, циклоспорином, азатиаприном). Однако эти препараты имеют большое число побочных эффектов, убедительных доказательств же в их эффективности до настоящего времени не получено. В связи с чем рекомендовать их к широкому применению не следует.
Одним из возможных медиаторов патологического процесса в орбитах является инсулиноподобный фактор роста I, поэтому в качестве лечения офтальмопатии предложен длительно действующий аналог соматостатина октреотид. Октреотид, подавляя секрецию гормона роста, снижает активность инсулиноподобного фактора роста I и тормозит его действие на периферии.
При стероидорезистентных формах офтальмопатии проводится плазмаферез или гемосорбция. Плазмаферез — избирательное удаление плазмы из организма с последующим замещением ее свежезамороженной донорской плазмой. Гемосорбция обладает широким спектром действия: иммунорегулирующим, детоксикационным, повышающим чувствительность клеток к глюкокортикоидам. Как правило, гемосорбцию сочетают со стероидной терапией. Курс лечения состоит из 2-3 сеансов с интервалом 1 нед.
При тяжелых формах офтальмопатии, проявляющихся резко выраженным экзофтальмом, отеком и гиперемией конъюнктивы, ограничением взора, ослаблением конвергенции, появлением диплопии, выраженных болей в глазных яблоках, проводится дистанционная рентгенотерапия на область орбит с прямых и боковых полей с защитой переднего отрезка глаза. Рентгенотерапия оказывает антипролиферативное, противовоспалительное влияние, приводя к снижению выработки цитокинов и секреторной активности фибробластов. Отмечена эффективность и безопасность малых доз лучевой терапии (16-20 Гр на курс, ежедневно или через день в разовой дозе 75-200 Р). Наилучший терапевтический эффект отмечается при сочетании лучевой терапии с глюкокортикоидами. Эффективность рентгенотерапии необходимо оценивать в течение 2 мес после окончания лечения.
Хирургическое лечение офтальмопатии проводят на стадии фиброза. Существуют 3 категории хирургических вмешательств:
- Операции на веках в связи с поражением роговицы;
- Корригирующие операции на глазодвигательных мышцах при наличии диплопии;
- Декомпрессия орбит.
Лечение тиреотоксического криза направлено в первую очередь на снижение в крови уровня тиреоидных гормонов, купирование надпочечниковой недостаточности, профилактику обезвоживания и борьбу с ним, устранение сердечно-сосудистых и нервно-вегетативных нарушений. При развитии тиреотоксических реакций в виде повышения температуры, возбуждения, тахикардии необходимо начинать мероприятия по ликвидации угрожающих симптомов.
Больным увеличивают дозы тиреостатических препаратов, назначают кортикостероиды. При развитии криза внутривенно вводят 1 % раствор «Люголя (заменяя йодид калия йодидом натрия).
Для купирования симптомов гипокортицизма используют большие дозы кортикостероидов (гидрокортизон 400-600 мг/сут, преднизолон 200-300 мг), препараты ДОКСА. Суточная доза гидрокортизона определяется тяжестью состояния больного и в случае необходимости может быть увеличена.
Для уменьшения гемодинамических нарушений и проявлений симпатико-адреналовой гиперреактивности используют бета-адреноблокаторы. Пропранолол или индерал вводится внутривенно — 1-5 мг 0,1 % раствора, но не более 10 мг в течение 1-х суток. Затем переходят на пероральные препараты (обзидан, анаприлин). Применять бета-блокаторы следует с осторожностью, под контролем пульса и артериального давления, отменять их надо постепенно.
Для уменьшения симптомов нервного возбуждения показаны барбитураты, седативные препараты. Необходимо принимать меры против возникновения сердечной недостаточности. Показано введение увлажненного кислорода. Проводится борьба с обезвоживанием и гипертермией. При присоединении инфекции назначают антибиотики широкого спектра действия.
Появились сообщения, что для лечения больных с тиреотоксическим кризом стали прибегать к плазмаферезу как методу, позволяющему быстрее выводить большие количества тиреоидных гормонов и иммуноглобулинов, циркулирующих в крови.
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Хирургическое лечение диффузного токсического зоба
Показаниями к хирургическому лечению ДТЗ являются большие размеры зоба, сдавление или смещение трахеи, пищевода и крупных сосудов, загрудинный зоб, тяжелые формы тиреотоксикоза, осложнившегося мерцательной аритмией, отсутствием стойкой компенсации на фоне проводимой медикаментозной терапии и наклонность к рецидивам, непереносимость тиреотоксических препаратов.
Больные направляются на хирургическое лечение после предварительной подготовки тиреотоксическими препаратами в комбинации с кортикостероидами и бета-блокаторами. При появлении аллергических реакций и непереносимости мерказолила необходимая предоперационная подготовка проводится большими дозами кортикостероидов и бета-блокаторов. Основными клиническими показателями готовности больного к операции являются состояние, близкое к эутиреоидному, уменьшение тахикардии, нормализация артериального давления, увеличение массы тела, нормализация психоэмоционального состояния.
При диффузном токсическом зобе проводится субтотальная субфасциальная резекция щитовидной железы по методике О. В. Николаева. Комплексная патогенетически обоснованная предоперационная подготовка, соблюдение всех деталей оперативного вмешательства гарантируют благоприятное течение послеоперационного периода и хороший результат операции.
Лечебное применение 131I
Применение радиоактивного 131I с лечебной целью получило широкое признание как в отечественной, так и в зарубежной медицинской практике.
Использованию 131I с лечебной целью предшествовало большое число экспериментальных работ. Было установлено, что введение предельно широких доз 131I животным вызывает полное разрушение щитовидной железы, но не повреждает другие органы и ткани. Радиоактивный йод, поступая в щитовидную железу, распределяется в ней неравномерно, и лечебное действие в первую очередь сказывается на центральных участках, а периферические зоны эпителия сохраняют способность продуцировать гормоны. Такая избирательная концентрация и отсутствие выраженного побочного влияния его на окружающие ткани зависят от физических свойств изотопа, образующегося при распаде бета- и гамма-частиц, ведущих себя в тканях по-разному. Основную часть 131I составляют бета-частицы с максимальной энергией в 0,612 МэВ и длиной пробега не более 2,2 мм. Они полностью поглощаются центральными участками ткани щитовидной железы и разрушают их, тогда как окружающие паращитовидные железы, трахея, гортань, возвратный нерв почти не подвергаются действию лучей. В противоположность бета-лучам гамма-лучи с энергией от 0,089 до 0,367 МэВ обладают выраженной проникающей способностью. При этом отрицательное влияние радиоизотопа на окружающие ткани возрастает пропорционально увеличению зоба. Установлено, что начальный период лечения характеризуется более активной концентрацией радиоизотопа в диффузной части железы в участках выраженной гиперплазии, затем он накапливается в оставшемся узле. Поэтому эффект лечения при смешанных зобах значительно ниже и, по нашим данным, не превышает 71 %.
Показания к терапии 131I: лечение должно проводиться в возрасте не моложе 40 лет; тяжелая сердечная недостаточность у больных, при которой хирургическое лечение рискованно; сочетание диффузного токсического зоба (базедовой болезни) с туберкулезом, тяжелой гипертонической болезнью, перенесенным инфарктом миокарда, нейропсихическими расстройствами, геморрагическим синдромом; рецидив тиреотоксикоза после субтотальной тиреоидэктомии, категорический отказ больного от оперативного вмешательства на железе.
Противопоказания к лечению 131I: беременность, период лактации, детский, юношеский и молодой возраст; большая степень увеличения щитовидной железы или загрудинное расположение зоба; заболевания крови, почек и язвенная болезнь.
Предварительная подготовка в стационаре включает проведение мер против сердечно-сосудистой недостаточности, лейкопении, нервной перевозбудимости. В период лечения, связанного с повышенным поступлением гормонов в кровяное русло, необходимо за несколько дней до и в течение 2-4 нед после введения I назначать тиреостатические препараты. Однако данная комбинация естественно в некоторой степени снижает лечебный эффект 131I, но не оказывает его выраженных побочных действий. Так, Л. Г. Алексеев и соавт., применив комбинированное лечение, отметили гипотиреоз всего лишь у 0,5-2,1 % больных, тогда как при введении только одного 131I процент гипотиреоза возрастает до 7,4 %.
Помимо такой комбинации, можно сочетать 131I с бета-блокаторами, которые, как известно, ослабляют многие симптомы тиреотоксикоза. В рациональной подготовке больных к лечению 131I немалое значение придается витаминотерапии, особенно применению комплекса витаминов группы В и аскорбиновой кислоты.
При выборе терапевтической дозы имеет значение тяжесть заболевания. Так, по нашим данным, у бальных среднетяжелым тиреотоксикозом средняя доза составила от 4 до 7,33 мКи, а у тяжелых больных — 11,38 мКи. Не менее важным является и масса железы, для определения которой используют метод сканирования. Определенную роль в подборе дозы играют диагностические показатели содержания 131I в железе. Замечено, что чем они выше, тем большие дозы приходится применять. При их расчете учитывается и эффективный период полураспада. Он значительно убыстряется у тяжелых больных с тиреотоксикозом. Для правильного подбора дозы следует принимать во внимание и возраст больных. Известно, что чувствительность железы к радиации у пожилых возрастает. В связи с многообразием причин, оказывающих влияние на выбор терапевтической дозы, предлагается ряд формул, облегчающих эту задачу.
Не менее важное значение имеет и метод применения. Одни считают, что можно вводить однократно всю дозу, другие — дробно — через 5-6 дней и, наконец, дробно-протяженно. Сторонники первого метода полагают, что применение таким образом 131I позволяет быстро ликвидировать тиреотоксикоз и исключить возможность развития резистентности щитовидной железы к 131I. Защитники дробного и дробно-протяженного методов утверждают, что такое введение позволяет учитывать индивидуальные особенности организма и тем самым можно предупредить развитие гипотиреоза. Интервал между первым и вторым курсами — 2-3 мес — позволяет восстановить функцию костного мозга и других органов после лучевого воздействия первоначальной дозы йода, а также предупредить быстрое разрушение щитовидной железы и максимальное наводнение организма тиреоидными гормонами. Для предупреждения гипотиреоза лучше вводить препарат дробно. Помимо того, больным тяжелым тиреотоксикозом рекомендуется также вводить препарат курсами для предупреждения и других осложнений (тиреотоксический криз, токсический гепатит и т. п.).
У больных со среднетяжелым течением заболевания можно ограничиться и разовым введением 131I. Повторный прием лучше проводить через 2-3 мес. Практическое значение имеет и величина повторной дозы. Она должна увеличиваться на 25-50 % в сравнении с первоначальной при дробном введении и уменьшаться вдвое при разовом.
При расчете терапевтической дозы, по нашим данным, на 1 г массы щитовидной железы у больных со среднетяжелым течением тиреотоксикоза необходимо вводить его от 60-70 мкКи, а при тяжелом течении и лицам более молодого возраста до 100 мкКи, причем расчет первоначальной дозы при всех формах заболевания не должен превышать 4-8 мкКи. Результаты лечения сказываются через 2-3 нед: уменьшаются потливость, тахикардия, падает температура, прекращается снижение массы тела. Через 2-3 мес полностью исчезают сердцебиение и слабость, восстанавливается трудоспособность. Полная ремиссия после лечения наступает в 90-95 % случаев. Рецидив тиреотоксикоза возможен не более чем в 2-5 % случаев. Чаще он бывает у больных со смешанным зобом, а при ДТЗ не более чем у 1 % больных.
Критерием оценки лечебного эффекта I является функциональное состояние щитовидной железы, определяемое по содержанию тироксина, трийодтиронина, тиреотропного гормона, тесту с тиреолиберином или включению в щитовидную железу 99mТс.
Ближайшие осложнения после лечения могут наступить уже в первые часы после введения 131I (головные боли, сердцебиение, чувство жара во всем теле, головокружения, диарея и боли во всем теле). Они длятся недолго и не оставляют последствий. Поздние осложнения наступают на 5-6-е сутки и характеризуются более выраженными симптомами: появлением или усилением сердечно-сосудистой недостаточности, болями в суставах и их припухлостью. Может несколько увеличиться объем шеи, возникнуть покраснение в области щитовидной железы и болезненность — начинается так называемый асептический тиреоидит, который отмечается в 2-6 % случаев. Может развиться и желтуха, указывающая на токсический гепатит. Наиболее серьезным осложнением является тиреотоксический криз, но он отмечается не более чем в 0,88 %/ Одно из частых осложнений — гипотиреоз, который наблюдается в 1-10 % случаев.
Е. Eriksson и соавт. считают, что лечение этого осложнения заместительной терапией — тироксином — необходимо начать, если уровень ТТГ в крови увеличивается вдвое вне зависимости от клинических проявлений. Стойкий гипотиреоз может развиться как при применении больших, так и небольших доз I.
ilive.com.ua
