что это такое, причины, лечение
Среди заболеваний простаты ДГПЖ занимает далеко не последнее место, и после 40 лет риск развития данной патологии только увеличивается. Что же представляет собой ДГПЖ предстательной железы и почему она возникает? Об этом, а также о методах лечения болезни и мерах ее профилактики и пойдет речь в статье.
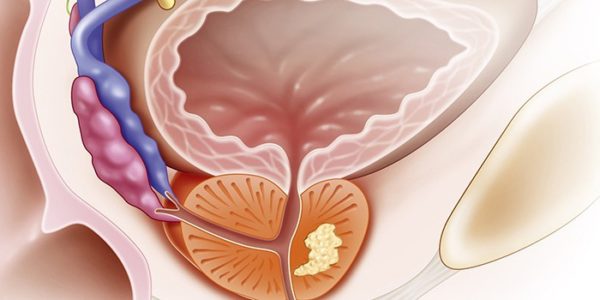
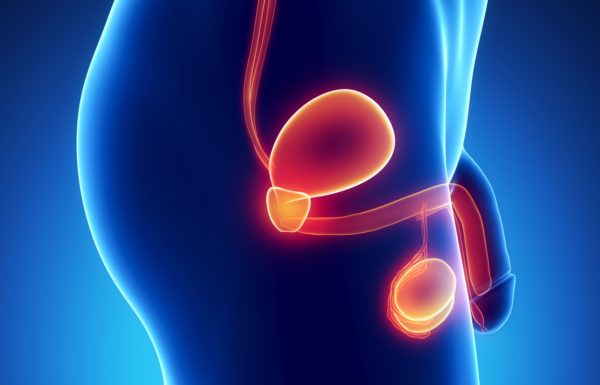
ДГПЖ предстательной железы: что это такое, причины, лечение и профилактика
Характеристика заболевания
ДГПЖ – сокращенное название доброкачественной гиперплазии простаты, больше известной, как аденома простаты. Так обозначается состояние, при котором в простате формируются мелкие образования (узелки), постепенно увеличивающиеся в размерах. Их патологическое разрастание приводит к сдавливанию мочевыводящего канала, что проявляется серьезными нарушениями в работе мочевыводящей системы.
Заболевание относится к доброкачественным, то есть, не дает метастазов, хотя под воздействием ряда факторов может перейти в рак простаты. Но даже если этого не случится, наличие опухоли в железе негативно влияет на мужское здоровье и на весь организм в целом, существенно снижая качество жизни. У молодых мужчин ДГПЖ встречается редко, а вот после 50-60 лет ее диагностируют в каждом третьем случае. К восьмидесяти годам риск развития заболевания увеличивается до 70%.
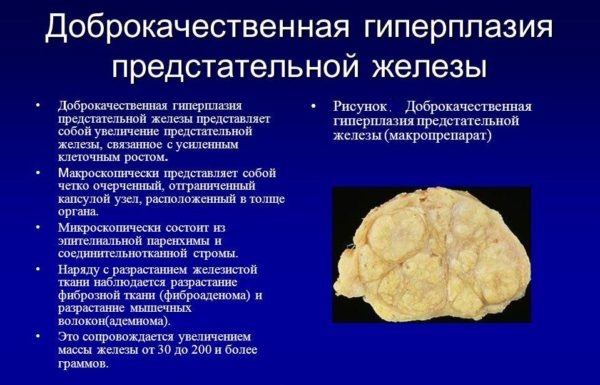
Характеристики ДГПЖ
Предстательная железа состоит из трех типов тканей – мышечной, железистой и соединительной, и любая из них может вовлекаться в патологический процесс. Обычно очаг поражения располагается в центральной части органа и затрагивает боковые доли, в некоторых случаях он может смещаться в одну или другую сторону. Разрастание тканей чаще всего происходит в одном направлении, вследствие чего выделяют три формы патологии.
Таблица. Формы ДГПЖ по типу роста
| Форма патологии | Основные характеристики |
|---|---|
| Подпузырная | Считается наиболее распространенной. Ткани разрастаются в сторону прямой кишки, в результате чего ухудшается моторика простатической части уретры, и моча выходит не полностью. На сам процесс мочеиспускания данная форма влияет не сильно. |
| Внутрипузырная | Ткани разрастаются по направлению к мочевому пузырю. Опухоль через мочеиспускательный канал перекрывает просвет мочевого пузыря, сдавливает внутренний сфинктер и частично либо полностью нарушает его работу. |
| Ретротригональная | Наблюдается редко. Опухоль формируется между внутренним выходом уретры и устьями мочеточников. Самая тяжелая форма, характеризующаяся одновременным ухудшением оттока мочи и затруднением ее прохождения устьями. |
Очаг заболевания чаще бывает единичным, хотя и множественные встречаются не так уж и редко. В зависимости от этого меняются и проявления патологии. Размер опухоли в самых запущенных случаях может превышать 80 мм в диаметре, но обычно варьируется в пределах 10-40 мм.
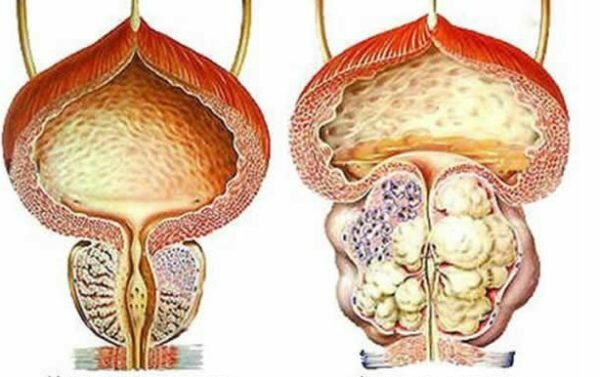
Размеры опухоли варьируются в зависимости от стадии и формы ДГПЖ
Развитие ДГПЖ происходит поэтапно, и специалисты выделяют три стадии патологии:
- компенсированная – ранняя стадия, развивающаяся на протяжении 1-3 лет. Характеризуется легкими нарушениями мочеиспускания, небольшим увеличением железы, изменением ее плотности;
- субкомпенсированная
- декомпенсированная – наиболее тяжелая стадия с ярко выраженными нарушениями в работе мочевого пузыря. У многих мужчин сопровождается почечной недостаточностью с типичными проявлениями.
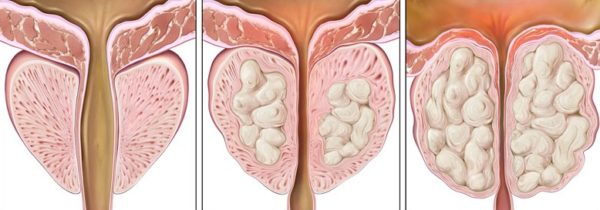
Стадии развития ДГПЖ
Каждая стадия имеет свои характерные проявления и, соответственно, требует различных методик лечения.
Причины и симптомы ДГПЖ
Основной причиной патологии принято считать гормональные изменения в мужском организме, при которых нарушается баланс тестостерона и эстрогена. Это приводит к неконтролируемому росту клеток простаты, вследствие чего и развивается аденома. Среди факторов риска главным является естественное угасание половых функций, которое начинается примерно с 50 лет.

Основной причиной развития ДГПЖ считаются возрастные изменения гормонального фона мужчины
Реже развитие ДПГЖ возникает по другим причинам:
- наличие хронических заболеваний мочеполовой сферы;
- инфекционные поражения мочевыводящих путей;
- травмы;
- наличие онкологических опухолей и метастаз.
Хронические заболевания и воспалительные процессы в мочеполовой системе тоже могут провоцировать развитие аденомы простаты
На раннем этапе определить развитие аденомы может только специалист, ведь первые симптомы выражены слабо и схожи с проявлениями других заболеваний простаты. Позже, когда в тканях железы начинают формироваться узелки, появляются общие признаки, которые уже являются поводом обратиться к врачу:
- позывы к мочеиспусканию возникают чаще, особенно в ночное время, при этом струя мочи заметно слабее, чем раньше;
- ухудшается контроль над мочеиспусканием, может возникать недержание;
- периодически возникает общая слабость и апатия, снижается масса тела;
- чаще беспокоят запоры;
- снижается эрекция.

Симптомы ДГПЖ
С развитием ДГПЖ симптоматика обостряется, возникает болевой синдром, характер и выраженность которого зависит от формы опухоли, стадии болезни и наличия сопутствующих патологий в организме. Нередко заболевание сопровождается формированием в простате конкрементов, что значительно осложняет процесс лечения. У больных с запущенной формой ДГПЖ моча мутная, часто с примесью крови, выделяется малыми порциями.
Методы диагностики
На основании указанных симптомов самостоятельно ставить себе диагноз и подбирать лечение нельзя, ведь это может привести к самым тяжелым последствиям. На лечении ДГПЖ специализируется врач-уролог, он же назначает и все необходимые для постановки диагноза исследования. Чтобы точно определить наличие опухоли, ее локализацию, размеры, возможные осложнения, применяется сразу несколько методик комплексной диагностики.
Таблица. Методы диагностики ДГПЖ
| Метод исследования | Характеристики |
|---|---|
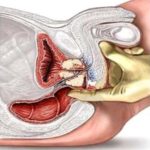 Ректальная диагностика | С помощью пальцевого исследования специалист определяет наличие уплотнений в простате, ее размер, болезненность. Дополнительно это позволяет взять на анализ секрет железы, который выделяется при массировании долек. |
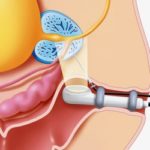 Трансректальное УЗИ | Применение ультразвукового датчика позволяет получить точное изображение больного органа и определить размеры узелков, локализацию очага опухоли, наличие конкрементов в железе. |
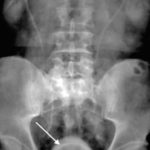 Рентгенография | Данный метод помогает точно оценить состояние мочеполовой системы, выявить возможные осложнения в виде камней в мочевом пузыре и почках, образования дивертикулов и так далее. Исследование может проводиться как с применением контраста, так и без него. |
 Лабораторная диагностика | Обязательно включает биохимический и общий анализ крови, анализ мочи, при необходимости исследуется секрет простаты или мазок (при подозрении на наличие инфекции). |
 Урофлоуметрия | Неинвазивный метод для оценки состояния мочеиспускательного канала. Выполняется во время мочеиспускания и заключается в измерении скорости потока и некоторых других параметров. |
При подозрении на злокачественный характер заболевания, врач назначает биопсию. В отдельных случаях может дополнительно назначаться МРТ органов таза, особенно, если заболевание запущено и сопровождается тяжелыми нарушениями в работе почек.
При подозрении на злокачественную форму опухоли назначается биопсия простаты
Лечение ДГПЖ
В современной медицине для лечения ДГПЖ применяется несколько методик с высокой эффективностью. Выбор оптимального способа лечения зависит, прежде всего, от стадии и формы заболевания, а также от наличия осложнений и общего состояния организма.
Медикаментозная терапия
При первой стадии ДГПЖ лекарственные препараты назначаются не всегда, поскольку для нормализации работы мочеполовой системы обычно хватает лечебных упражнений и диеты. При необходимости врач может назначить прием ингибиторов 5 альфа-редуктазы, подавляющих рост опухоли в простате. К наиболее действенным препаратам данной группы относятся: «Аводарт», «Пенестер», «Урофин».

Инструкция по применению аводарта
Для второй стадии прием медикаментов является основным видом терапии, так как позволяет устранить болевые проявления, нормализовать отток мочи, замедлить разрастание узелков. Помимо ингибиторов альфа-редуктазы, больному показаны адреноблокаторы и препараты на растительной основе, оказывающие спазмолитическое действие. Самые известные из них – «Омник», «Корнам», «Кардура», экстракты тыквы и ромашки.

«Омник»: инструкция по применению
На третьей стадии медикаменты назначаются в качестве вспомогательной терапии до проведения операции и после нее. Вид препаратов подбирается исключительно специалистом, в зависимости о состояния самой простаты и мочевыводящей системы.
Таблетки «Кардура»
Неоперативные методы
В перечень консервативных методик лечения входят:
- ультразвуковая терапия;
- вживление специальных расширяющих стентов в уретру;
- криотерапия;
- радиочастотное лечение с введением особых игл через уретру.
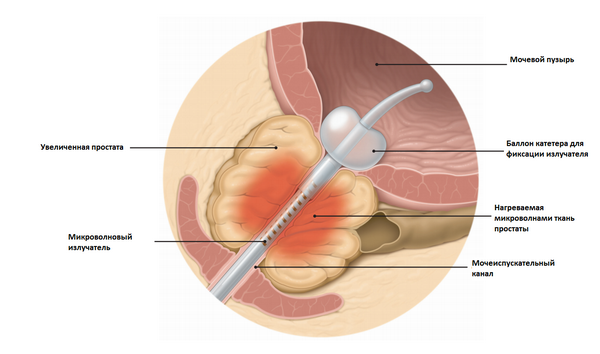
Микроволновая коагуляция простаты
Помимо указанных процедур большое значение имеет лечебная физкультура (особенно на раннем этапе болезни), что способствует улучшению кровообращения в пораженных тканях, оттоку жидкости, устранению застойных явлений в железе. Комплекс упражнений тоже подбирает врач, а выполнять их нужно регулярно на протяжении длительного времени.
Комплекс упражнений при ДГПЖ
Оперативное лечение
Хирургическое вмешательство тоже осуществляется по-разному. В тяжелых запущенных случаях проводят открытую операцию по удалению опухоли. Если образования не слишком крупные и отсутствуют осложнения, применяют малоинвазивные способы, например, лазерная вапоризация. После хирургического лечения больному устанавливают катетер для отведения мочи, назначают медикаментозную терапию и диету.
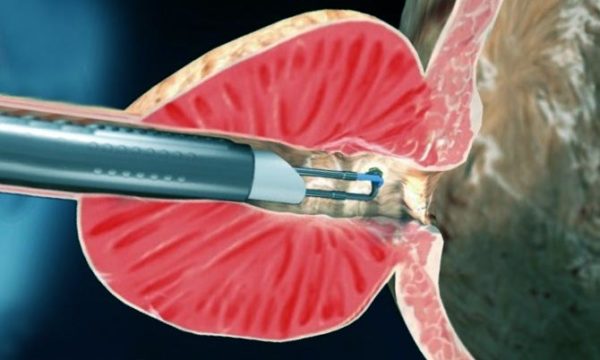
Лазерная вапоризация при ДГПЖ
Профилактика ДГПЖ
Профилактика заболевания играет далеко не последнюю роль, что уже доказано многолетними исследованиями в урологии. Предупредить развитие ДГПЖ не так уж и сложно, если придерживаться следующих правил:
- придерживаться здорового образа жизни;
- по возможности отказаться от злоупотребления спиртным и курения;
- больше внимания уделять физической активности;
- своевременно обращаться с проблемами в мочеполовой сфере к врачу, не запускать болезни;
- регулярно проходить обследования в уролога после 40 лет.

Для здоровья простаты следует ограничить употребление алкоголя, вредной пищи и меньше времени проводить на диване
Но самое главное — не заниматься самодиагностикой и самолечением, ведь в большинстве случаев это приводит к ухудшению самочувствия, развитию побочных осложнений и снижению шансов на полноценное восстановление мужского здоровья.
Видео — ДГПЖ предстательной железы: что это такое, причины, лечение и профилактика
При условии своевременного выявления ДГПЖ и грамотного подхода в лечении, прогнозы данного заболевания обычно благоприятные. Но затягивание с визитом к врачу может привести к развитию злокачественной формы опухоли, вылечить которую гораздо сложнее. Как проявляется рак простаты и насколько эффективным является его лечение, можно прочитать на нашем сайте.
prostatit-doc.ru
Рекомендации по диагностике и лечению доброкачественной гиперплазии простаты
Доброкачественная гиперплазия простаты (ДГП) — наиболее частая доброкачественная опухольу мужчин.ДГП является медицинской проблемой, четко связанной с возрастом.
Она не представляет угрозы для жизни но характерные для нее симптомы нижних мочевых путей (СНМП) снижают качество жизни пациентов.
Доставляющие беспокойство СНМП наблюдаются у 30% мужчин в возрасте старше 65 лет.
Эпидемиологическая распространенность клинически значимой доброкачественной гиперплазии простаты является сложной задачей для изучения и остается неизвестной.
Вместе с тем, известно, что первые симптомы ДГП в виде ноктурии отмечаются примерно у 10% мужчин уже после 40 лет. С возрастом частота гистологической и клинически значимой доброкачественной гиперплазии простаты увеличивается.
По данным статистики, средняя частота обращаемости мужчин к урологу по поводу ДГП составляет 137 человек на 100 000 мужского населения. Таким образом, доброкачественная гиперплазия простаты представляет собой наиболее часто встречающуюся возрастную патологию мочеполовой системы которая существенно влияет на качество жизни мужчины.
Этиология ДГП мультифакториальная. Важными факторами в оценке развития заболевания являются возраст, уровень простатспецифического антигена (ПСА) и объем простаты. На основании многочисленных данных эпидемиологических и долгосрочных клинических рандомизированных исследований доброкачественной гиперплазии простаты рассматривается как хроническое прогрессирующее заболевание.
Доказанными факторами риска прогрессирования доброкачественной гиперплазии простаты являются возраст, уровень ПСА > 1,5 нг/мл, объем простаты г 30 см3 и симптомы со стороны нижних мочевыводящих путей средней и тяжелой степени. Вместе с тем, на основе этих факторов может быть определена группа пациентов с повышенным риском прогрессирования заболевания, которым можно рекомендовать раннее профилактическое лечение.
В настоящее время активно дискутируется вопрос о целесообразности профилактической терапии доброкачественной гиперплазии простаты. Есть работы, показывающие эффективность такого подхода.
Тем не менее, необходимость хирургического лечения доброкачественной гиперплазии простаты увеличивается с возрастом и с увеличением степени выраженности симптомов. Прогностическими факторами, вероятно, являются ноктурия и изменения потока струи мочи (урофлоуметрия).
Диагностика доброкачественной гиперплазии простаты
Точная и ранняя диагностика ДГП позволяет получить лучшие результаты лечения и предопределяет выбор метода лечения.В рекомендациях по диагностике доброкачественной гиперплазии простаты (Европейская ассоциация урологов, 2007) все методы принято делить на рекомендуемые, факультативные и нерекомендуемые.
Рекомендуемые методы исследования доброкачественной гиперплазии простаты (проводятся во всех случаях диагностики ДГП):
1. Сбор анамнеза. При сборе анамнеза следует уточнить длительность имеющихся СНМП, их эволюцию, проводилось или проводится ли в настоящее время какое-либо лечение, оценивается ли его переносимость, комплаентность. эффективность. Необходимо выяснить другие возможные причины СНМП (патология позвоночника, головного и спинного мозга, сахарный диабет, несахарный диабет, почечная недостаточность, сердечно-сосудистая недостаточность и т.д.). Оценивается также общесоматический статус пациента.
2. Сбор жалоб и оценка симптоматики проводится с использованием специальных анкет-опросников, позволяющих систематизировать имеющиеся СНМП. Среди всех различных систем оценки выраженности симптомов рекомендуется применение опросника IPSS-QOL как наиболее широко применяемого метода оценки симптомов при заболеваниях простаты. На основании суммарного балла симптомов пациент может быть отнесен к одной из трех групп: с мягкой симптоматикой (0-7 баллов, чаще всего требуется динамическое наблюдение), с умеренной симптоматикой (8-19 баллов, чаще всего требуется консервативное лечение) и с выраженной симптоматикой (20-35 баллов, как правило, это кандидаты на оперативное лечение при неэффективности медикаментозного).
3. Пальцевое ректальное исследование простаты и семенных пузырьков остается, несмотря на современные методы визуализации простаты. важным элементом обязательного обследования больного с СНМП на фоне ДГП. Он прост, доступен и позволяет опытному клиницисту провести первичную дифференциальную диагностику между ДГП, раком простаты и простатитом, что предопределяет дальнейшую схему обследования.
4. Общий анализ мочи выполняется всем пациентам для выявления признаков мочевой инфекции.
5. При обследовании пациентов с СНМП минимальным и обязательным требованием является также изучение функции верхних мочевых путей путем определения уровня креатинина крови.
6. Анализ крови на ПСА позволяет проводить дифференциальную диагностику между ДГП и раком простаты.
7. Урофлоуметрия — неинвазивный скрининг-метод оценки суммарной функции опорожнения мочевого пузыря. Метод прост, физиологичен, выполняется в условиях естественного наполнения мочевого пузыря. Для повышения достоверности результатов урофлоуметрии рекомендуется выполнение ее не менее 2 раз при эффективном объеме мочеиспускания на менее 150-200 мл, что не всегда возможно, например, при наличии у пациента выраженных императивных симптомов.
Наиболее информативным является показатель максимальной объемной скорости мочеиспускания (МОСМ), в норме составляющий у мужчин более 15 мл/с При явлениях инфравезикальной обструкции этот показатель закономерно снижается. Умеренным снижением МОСМ считается показатель 10-15 мл/с, а при МОСМ менее 10 мл/с диагностируются значительные нарушения опорожнения, В норме урофлоуметрограмма имеет вид перевернутого колокола, причем фаза подъема МОСМ составляет не более 1/3 от всего времени мочеиспускания.
При инфравезикальной обструкции на фоне ДГП на г рафиках удлиняется фаза достижения МОСМ, удлиняется время мочеиспускания, кривая потока мочи становится пологой. При стриктуре мочеиспускательного канала МОСМ не достигает своего нормального значения, а кривая потока струи мочи имеет вид линии, почти параллельной оси времени мочеиспускания, «плато» (рис 21.2).

Рис. 21.2. Кривые потока мочи в норме и при инфравезикальной обструкции различного генеза: 1 — нормальный вид кривой потока мочи; 2 — кривая потока мочи при ДГП; 3 — кривая потока мочи при стриктуре мочеиспускательного канала
В то же время по урофлоуметрии невозможно раздельно оценить функцию детрузора и степень внутриуретрального сопротивления, иными словами, при снижении МОСМ только по результатам урофлоуметрии нельзя определить за счет каких механизмов развивается это снижение: уменьшения силы сокращения детрузора (гипотония, атония) или большого внутриуретрального сопротивления на выходе за счет инфравезикальной обструкции.
Факультативные методы исследования (не требуются на начальном этапе обследования, но могут оказаться полезными при планировании тактики ведения больного):
1. Исследование «давление-поток» имеет особое значение при наличии СНМП у больных с патологией нервной системы и увеличенной простатой. Оно позволяет определить вклад имеющихся нейрогенных расстройств в симптоматику ДГП. Это исследование — единственный способ отделить мужчин с низкой МОСМ вследствие нарушения функции детрузора от пациентов с истинной инфравезикальной обструкцией на фоне ДГП.
Исследование «давление-поток» должно проводиться у пациентов, которым впервые предложено хирургическое лечение, в следующих подгруппах:
a. Молодые пациенты (младше 50 лет).
b. Пожилые пациенты (старше 80 лет).
c. Объем остаточной мочи более 300 мл.
d. Максимальная скорость потока мочи более 15 мл/с.
e. Подозрение на нейрогенную дисфункцию мочевого пузыря.
f. После радикальной тазовой хирургии.
g. После неуспешного инвазивного лечения ДГП
2. Эндоскопия. Рекомендуется проводить у ретро цистоскопию для оценки размеров и формы простаты. Уретроцистоскопия показана пациентам с гематурией или подозрением на сопутствующие опухоли мочевого пузыря (по данным ультразвукового исследования (УЗИ) или экскреторной урографии). Эндоскопические исследования рекомендованы во время проведения хирургического вмешательства для выявления другой патологии и оценки формы и размеров простаты, которые могут иметь влияние на выбор модальности лечения.
3. Ультразвуковое определение остаточной мочи является простым и надежным способом, дающим возможность выявить признаки нарушения функции детрузора. Наличие остаточной мочи является важным прогностическим фактором стратегии и тактики ведения больного с ДГП.
Увеличение объема остаточной мочи на фоне специфического лечения указывает на его неэффективность, а при объеме остаточной мочи более 100 мл обсуждаются вопросы оперативной коррекции СНМП. Б норме после мочеиспускания остается не более 10 мл мочи. Наличие остаточной мочи отражается значком R (мл) в формулировке диагноза ДГП по системе SLVR, где S — суммарный балл по шкале IPSS-QOL (0-35), L — индекс качества жизни по этой же шкале (0-6), V — объем простаты по УЗИ (см3), R — объем остаточной мочи (мл).
4. Диагностическая визуализация мочевых путей. Визуализация простаты путем трансабдоминального УЗИ позволяет уточнить ее размеры, особенности роста ДГП, структуру простаты, выявить подозрительные очаги. Четкой зависимости между размером аденомы и характером и частотой дизурических явлений нет. однако размер железы имеет важное значение при выборе метода оперативного лечения.
Визуализация простаты посредством трансректального ультразвукового исследования (ТРУЗИ) позволяет проводить дифференциальную диагностику с раком простаты, склерозом простаты, выявлять среднюю долю, резистентную к медикаментозной терапии. Размер простаты необходимо оценивать при планировании открытой простатэктомии или трансуретральной резекции простаты (ТУРП), а также при лечении финастеридом, что определяет тактику дальнейшего ведения больного.
5. Заполнение дневника мочеиспусканий в течение не менее 3 дней является полезной методикой общей оценки ритма суточных спонтанных мочеиспусканий и эпизодов императивного недержания мочи, равно как.
Нерекомендуемые методы исследования (нет данных, подкрепляющих необходимость проведения следующих процедур):
1. Визуализация верхних мочевых путей посредством экскреторной урографии. Достигнут консенсус, что для визуализации почек и верхних мочевых путей достаточную информацию дает УЗИ.
Экскреторная урография раньше широко применялась в диагностике ДГП для уточнения анатомо-функциональных изменений верхних мочевых путей. Но в настоящее время она не является рутинным методом исследования при ДГП и проводится лишь у отдельных категорий больных:
• инфекции мочевыводящих путей (ИМП) в анамнезе или наличие в настоящее время;
• макро-и микрогематурия;
• мочекаменная болезнь в анамнезе или наличие в настоящее время;
• в анамнезе хирургические вмешательства на мочевых путях;
• в анамнезе уротелиальные опухоли;
• задержка мочи;
• ретенционные изменения верхних мочевых путей на фоне ДГП (по результатам УЗИ).
2. Цистометрия наполнения.
3. Ретроградная уретрография.
4. Компьютерная томография (КТ) или магнитно-резонансная томография (МРТ) не являются методами выбора при рутинном обследовании верхних мочевых путей у пожилых пациентов с СНМП.
Лечение ДГП
Цель лечения — облегчение СНМП, улучшение качества жизни пациентов, а также предотвращение осложнений, связанных с ДГП.Основные методы лечения:
1. Выжидательная тактика, или динамическое наблюдение.
2. Медикаментозная терапия.
3. Хирургическое лечение.
Динамическое наблюдение
Динамическое наблюдение может быть рекомендовано пациентам с мягкими или умеренно-тяжелым и симптомами, которые не влияют или минимально влияют на качество жизни (0-7 баллов по шкале IP55-QOL).Динамическое наблюдение подразумевает разъяснение пациенту сущности имеющихся у него симптомов, предупреждение его о необходимости внесения некоторых изменений в свою жизнь, обучение режиму мочеиспускания. Кроме того, проводится периодический мониторинг простаты с целью своевременного выявления необходимости начала специфической терапии.
Медикаментозная терапия
Этот метод лечения в связи с революционным прорывом в области фармакологии является сегодня наиболее популярным (до 70% пациентов с СНМП на фоне ДГП сегодня лечатся консервативно). Консервативная терапия ДГП прошла большую эволюцию, многие препараты (в частности, эстрогены) в настоящее время исключены из реестра терапии ДГП как устаревшие.Консервативная терапия назначается пациентам, не имеющим показаний к оперативному лечению, а также пациентам с противопоказаниями к оперативному лечению или нежеланием оперироваться. Она позволяет поддерживать достаточный уровень качества жизни, а также может уменьшить риск развития осложнений ДГП острой задержки мочи и оперативного вмешательства.
Основными группами препаратов для лечения ДГП являются:
• а1-адреноблокаторы,
• ингибиторы 5а-редуктазы,
• препараты растительного происхождения.
Прочие группы препаратов, ранее применявшихся для консервативной терапии ДГП, представленные леворином и мепартрицином, а также женскими половыми гормонами, в настоящее время представляют лишь исторический интерес. Комбинация препаратов из перечисленных выше основных трех групп повышает эффективность терапии ДГП.
Терапия а1-адреноблокдторами является методом выбора для пациентов с умеренными и тяжелыми СНМП. Все а1-адреноблокаторы (альфузозин, доксасозин, тамсулозик, теразозин) обладают схожей клинической эффективностью только при использовании в адекватных дозировках, при этом они несопоставимы в плане развития нежелательных реакций.
По механизму действия все а1-адреноблокаторы обеспечивают снижение внутриуретрального сопротивления за счет блокады а1-а и a1-d-адренорецепторов шейки мочевого пузыря и проксимальной части мочеиспускательного канала. Кроме того, доказано прямое влияние этих препаратов (в частности, для доксазозина) на мочепузырное кровообращение. Таким образом, эти препараты улучшают мочеиспускание не только за счет снижения статического компонента инфравезикальной обструкции, но и за счет улучшения кровоснабжения и биоэнергетики детрузора (Лоран О. Б. и соавт., 1998).
Следует отметить, что по воздействию на рецепторы мочеполового тракта все а1-адреноблокаторы практически идентичны. Принимают эти препараты один раз в сутки. Отличия заключаются в воздействии на рецепторы сосудистой стенки, в результате чего при приеме так называемых «вазоактивных» препаратов чаще отмечается некоторое снижение уровня артериального давления (АД), которое может привести к ортостатическим реакциям гипотонического типа.
Поэтому такие препараты (доксазозин, теразозин) требуют постепенной титрации дозы и принимаются на ночь. «Вазонеактивные» а1-адреноблокаторы (тамсулозин альфузозин) оказывают менее выраженное воздействие на сосудистый тонус, поэтому применяются утром и не требуют титрации дозы. Очень удобны в применении препараты последних поколений с медленным высвобождением действующего вещества. Например, такие лекарственные формы разработаны для тамсулозина, Окас (компания «Астеллас Фарма») является наиболее назначаемым а1-адреноблокатором в мире.
Данная группа препаратов является сегодня «золотым стандартом» консервативной терапии ДГП и рекомендована к широкому применению. Эффективность терапии а1-адреноблокаторами может быть оценена не ранее, чем через 2-4 недели с момента начала лечения,
В настоящее время эти препараты широко применяются как при плановой терапии ДГП, так и при острой задержке мочи на фоне кратковременной (3 суток) катетеризации мочевого пузыря. По имеющимся многочисленным данным последних лет, эффективность а1-адреноблокаторов в лечении острой задержки мочи на фоне ДГП достигает 45-50% (Перепанова Т.С., Камалов А.А., 2003).
Основные противопоказания к назначению а1-адреноблокаторов: тенденция к гипотонии, тяжелые нарушения функции печени, почек, сердечно-сосудистой системы, нарушения ритма сердца.
Ингибиторы 5а-редуктазы (финастерид (Проскар), назначаемый по 5 мг в сутки перорально, и дутастерид (Аводарт), назначаемый в дозе 0,5 мг в сутки перорально) применяются у пациентов, имеющих факторы риска прогрессирования заболевания: уровень ПСА > 1,5 нг/мл, объем простаты > 30 см3, СНМП средней и тяжелой степени.
Оба препарата уменьшают объем простаты и способны уменьшать риск прогрессирования ДГП. Двойной ингибитор 5а-редуктазы дутастерид. в отличие от финастерида, селективного ингибитора 5а-редуктазы типа II, обладает более мощным супрессивным и продолжительным воздействием на синтез дигидротестостерона. При назначении подобной терапии с пациентом следует обсудить ее длительность (не менее одного года), побочные эффекты, стоимость, особенности, связанные с диагностикой рака простаты.
Характерной особенностью терапии данными препаратами является ее достаточная длительность и систематичность, поэтому первые результаты лечения этими препаратами следует оценивать не ранее, чем через 4-6 месяцев с момента начала терапии.
Из числа обычно применяемых препаратов для консервативного лечения мужчин, страдающих ДГП, лишь 5а-редуктаза способна влиять на патологию, лежащую в основе заболевания.
Важным условием при использовании ингибиторов 5а-редуктазы является безопасность простаты с точки зрения онкологии, так как эти препараты снижают уровень сывороточного ПСА (в течение 6 мес, лечения уровень ПСА снижается на 50%). Поэтому при интерпретации результатов исследования сывороточного ПСА у мужчин, получающих терапию ингибиторами 5а-редуктазы уровень ПСА следует умножать на два и только затем сравнивать его с нормативами мужчин, не получающих подобную терапии.
Учитывая данные последних исследований можно говорить о том. что прием ингибиторов 5а-редуктазы не затрудняет своевременную диагностику рака простаты. Более того, в этой ситуации повышается эффективность теста ПСА для диагностики рака простаты, в том числе, высокой градации.
Очень перспективен сегодня двойной ингибитор 5а-редуктазы и типов I и II дутастерид (Аводарт), который назначается однократно в дозе 0,5 мг/сут перорально. Данный препарат приводит к уменьшению объема простаты уже после первого месяца лечения, а при длительном приеме этот показатель понижается на 27% и более по сравнению с исходным.
При этом снижается риск развития острой задержки мочи на 57% и необходимость в оперативном лечении на 48% по сравнению с плацебо через 2 года лечения (Лопаткин Н.А. и соавт., 2007). Сегодня Аводарт является ведущим препаратом из группы ингибиторов 5а-редуктазы, который при соблюдении показаний к назначению демонстрирует высокую эффективность и превосходный комплаенс терапии у большинства пациентов.
Результаты недавно завершившегося исследования REDUCE продемонстрировали способность Аводарта снижать на 23% риск развития подтвержденного биопсией рака простаты у мужчин с повышенным риском развития заболевания без увеличения количества опухолей высокой градации.
Комбинированное лечение а1-адреноблокаторами и ингибиторами 5а-редуктазы представляется более эффективным и дающим более стойкие результаты, чем монотерапия. Эти выводы следуют из результатов исследований МТОР5, в ходе которого финастерид назначался в комбинации с доксазозином. а также COMBAT, где исследовалась комбинация дугастерида и тамсулозина.
Международное мультицентровое исследование COMBAT, исследующее долгосрочную эффективность комбинированной терапии цутастеридом (Аводартом) и тамсулозином у пациентов, имеющих риск прогрессирования заболевания, со среднетяжелыми и тяжелыми симптомами и увеличенной простатой, впервые продемонстрировало значительное преимущество в улучшении симптомов при использовании комбинированной терапии по сравнению с монотерапией каждым препаратом в течение первых 12 месяцев лечения.
Через 4 года применения комбинированной терапии дутастеридом и тамсулозином отмечено снижение риска развития острых задержек мочи или оперативного лечения на 65.8% по сравнению с монотерапией тамсулозином. Преимущество данной комбинации в отношении симптомов и скорости потока мочи также сохраняется на протяжении 4 лет лечения.
Различные и комплементарные механизмы действия ингибиторов 5а-редуктазы и а-адреноблокаторов — мощное, рациональное обоснование для комбинированной терапии. Вместе с тем, собственная клиническая практика показывает более высокую эффективность комбинированной терапии при лечении ДГП. По нашему мнению, она должна быть достаточно продолжительной, а с учетом длительности развития эффекта ингибиторов 5а-редуктазы ее следует проводить по крайней мере не менее 6-12 месяцев.
Растительные препараты не могут быть пока рекомендованы для лечения пациентов с СНМП на фоне ДГП, поскольку механизмы их действия остаются малоизученными. Тем не менее, для ряда растительных экстрактов, применяемых сегодня, декларируется угнетение пролиферации фибробластов. стимулированной фактором в-FGF, а также противовоспалительное и противоотечное действие.
Пока что только для Таденана проведены рандомизированные исследования эффективности, показавшие возможность его назначения пациентам с мягкой симптоматикой ДГП, а также есть работы по возможности его длительного применения в качестве профилактического средства» тормозящего развитие ДГП. Назначается он по 50 мг 2 раза в день или по 100 мг однократно в сутки курсами не менее 3-4 месяцев, желательно непрерывно или с перерывами между курсами не более 1 месяца (иначе теряется клинический эффект).
Хирургическое лечение
Хирургическое лечение является радикальным методом лечения ДГП. Методиками первой линии («золотым стандартом») хирургического лечения ДГП являются трансуретральная инцизия простаты (ТУИП) при объеме простаты менее 30 мл и без удаления средней доли, трансуретральная резекция простаты при объеме железы 30-80 мл и открытая простатэктомия при объеме железы более 80 мл.Хирургическое лечение показано пациентам:
• при неэффективности консервативной терапии;
• отказывающимся от консервативной терапии и требующим активной тактики:
• с абсолютными показаниями к оперативному лечению (острая задержка мочи; ИМП обусловленная ДГП; гематурия обусловленная ДГП; почечная недостаточность обусловленная ДГП; камни мочевого пузыря; большой дивертикул мочевого пузыря).
Таким образом. хирургическое лечение (ТУРП, ТУИП, открытая простатэктомия) рекомендовано как лечение первой линии пациентам с осложненной ДГП (абсолютные показания к лечению) на фоне СНМП.
Трансуретральная электровапоризация простаты (ТУВП) — альтернатива ТУРП, особенно у пациентов большого риска с малой аденомой.
Различные виды лазерной хирургии обычно назначают пациентам высокого риска. Существенная послеоперационная смертность, неутешительные результаты и высокая стоимость в своей совокупности являются причиной недостаточно широкого применения в клинике лазеров. Они не рекомендуются как лечение первой линии пациентам с СНМП, но могут применяться в лечении пациентов в подгруппах высокого риска.
Гольмий-лазерная резекция простаты является обещающей новой технологией с результатами, сопоставимыми с таковыми при ТУРП и открытой простатэктомией.
Трансуретральная микроволновая термотерапия (ТУМТ) является приемлемой альтернативой ТУРП, особенно для желающих избежать хирургического лечения или тех, кто больше не отвечает на медикаментозное лечение. ТУМТ также подходит для пациентов группы высокого риска, имеющих рецидивирующие задержки мочи.
При ТУМТ часто наблюдаются осложнения в виде солевой инкрустации, инфекции мочевой системы и болевого синдрома.
Новые методы (используются пока только в клинических испытаниях):
• Трансректальная HIFU-терапия (высокоинтенсивный фокусированный ультразвук).
• Химиоабляция простаты.
• Водоиндуцированная термотерапия (WIT, wafer-Induced thermotherapy).
• Плазменная энергия в солевом растворе (Плазмакинетик).
Устаревшие методы:
• Баллонная дилатация мочеиспускательного канала.
• Трансректальная/трансуретральная гипертермия.
Наблюдение
Все пациенты получающие лечение по поводу ДГП, нуждаются в наблюдении. Мероприятия по наблюдению зависят от назначенного и проводимого вида лечения (табл. 21.2).Таблица 21.2. Рекомендованное наблюдение после лечения ДГП

Чрезвычайно важны повторные посещения пациента для оценки эффекта лечения и побочных эффектов терапии. Для выбора времени наблюдения можно использовать следующую схему (табл. 21.3).
Таблица 21.3. Рекомендованные временные интервалы для наблюдения после лечения ДГП

С.Ю. Калинченко, И.А. Тюзиков
Опубликовал Константин Моканов
medbe.ru
Лечение доброкачественной гиперплазии предстательной железы
Причины возникновения доброкачественной гиперплазии предстательной железы
Доброкачественная гиперплазия предстательной железы (ДГПЖ) — новообразование доброкачественного характера, разрастающееся в структуре простаты (в железистом его эпителии или стромальном компоненте). Заболевание относится к обусловленным возрастным фактором. Так, в возрасте до 40 лет оно диагностируется у 10-15% мужчин, в то время как в возрасте 75-80 лет — у 80%. При этом симптомы гиперплазии наблюдаются уже у большинства мужчин 50 лет и старше, причиной чего совсем не обязательно является именно данная патология. Расстройства мочеиспускания, кроме ДГПЖ, могут быть обусловлены раком предстательной железы, нарушениями сократительной активности детрузора, нестабильностью детрузора и прочими дисфункциями мочевого пузыря.
Доброкачественная гиперплазия предстательной железы в своей основе содержит комплекс факторов. Причины возникновения ДГПЖ по степени значимости можно изложить следующим образом:
- особенности гормонального статуса, в частности выработки тестостерона — изменения в метаболизме, при которых тестостерон в клетках предстательной железы превращается в дигидротестостерон; превращение свободного тестостерона в дигидротестостерон регулируется воздействием фермента 5а-редуктазы; в цитоплазме клетки дигидротестостерон связывается с андрогенным белковым рецептором, формируется андроген-рецепторный комплекс, проникающий в клеточное ядро и активирующий ДНК, что приводит к росту и дифференциации клеток предстательной железы, то есть к возникновению ДГПЖ;
- роль 5а-андростендиолов — они совместно с эстрогенами ощутимым образом увеличивают концентрацию андрогенных рецепторов в предстательной железе; уменьшение числа 5а-андростендиола приводит к увеличению функциональной активности и количества а1-адренорецепторов предстательной железы, шейки мочевого пузыря и простатического отдела уретры, к сокращению гладкой мускулатуры этих органов, и именно это может создавать основу возникновения ирритативных симптомов заболевания;
- относительное повышение уровня эстрогенов — приводит к пролиферации клеток стромы, а значит, к стромальной гиперплазии и ДГПЖ в частности;
- нарушения кровообращения в предстательной железе — что происходит отчасти и на фоне нарушенных метаболических процессов в тканях предстательной железы; нарушенное кровообращение может быть основополагающим для развития асептического воспаления в результате.
По своей сути доброкачественная гиперплазия представляет собой пролиферацию железистой и/или стромальной ткани предстательной железы. Зависимо от локализации изменений различают железистую, стромальную и смешанную формы заболевания. Развитие процесса гиперплазии обычно начинается из переходной (транзиторной) зоны предстательной железы. В дальнейшем развивается полицентрический рост узлов в ее ткани, при этом происходит увеличение массы и объема предстательной железы.
При нормальном течении физиологических процессов предстательная железа расположена вокруг заднего отдела мочеиспускательного канала таким образом, что не препятствует нормальному мочеиспусканию и в целом функционированию канала. Когда же ткани разрастаются, происходит сдавливание простатического отдела уретры, сужение просвета уретры, нормальный отток мочи становится невозможным. Вследствие больной не испытывает ощущения опорожнения мочевого пузыря, сам акт мочеиспускания существенным образом осложняется. Одновременно появляются и другие симптомы болезни, обусловленные изменениями мышц мочевого пузыря и усилением раздражения а-рецепторов простатического отдела уретры, шейки мочевого пузыря и самой предстательной железы.
Сами по себе клинические проявления ДГПЖ не зависят от объема этого органа напрямую, решающее значение в данном случае имеет направление роста узлов. При интравезикальном их росте (т. н. росте средней доли) железа характеризуется небольшими размерами, она нависает над внутренним отверстием уретры, будто клапан, и тем самым вызывает значительные затруднения мочеиспускания. Примечательно, что железа больших размеров нередко разрастается по направлению прямой кишки, а потому выраженными клиническими проявлениями не знаменуется.
Доброкачественная гиперплазия предстательной железы имеет три стадии развития:
- стадия компенсации — наблюдаются расстройства акта мочеиспускания даже при полном опорожнении мочевого пузыря; струя мочи отличается вялостью, развиваются императивные позывы, в частности по ночам; хоть мочеиспускание и затруднено, но патологических изменений со стороны почек и верхних мочевых путей не наблюдается;
- стадия субкомпенсации — нарушения функции мочевого пузыря характеризуются как значительные, появляется остаточная моча; струя мочи обычно истончена, а после мочеиспускания возникает чувство неполного опорожнения, ведь часть мочи все же остается в пузыре; может наблюдаться острая задержка мочеиспускания, нарушается функция почек;
- стадия декомпенсации — характеризуется полной атонией мочевого пузыря, парадоксальной ишурией, выраженным расширением верхних мочевыводящих путей и прогрессивным нарушением функций почек.
Симптомы ДГПЖ возникают вокруг основного ее проявления — нарушения мочеиспускательного акта. К нему присоединяются симптомы заболеваний, которыми может осложняться гиперплазия — это острая задержка мочеиспускания, гематурия, камни мочевого пузыря, пиелонефрит, цистит, уретрит, простатит, орхиэпидидимит, хроническая почечная недостаточность.
Симптомы ДГПЖ разделяют на
- обструктивные — связанные с механическим сдавливанием шейки мочевого пузыря и уретры увеличенной предстательной железой и затруднением оттока мочи из мочевого пузыря; проявляются в момент мочеиспускания и указывают на наличие инфравезикальной обструкции и снижение сократительной способности детрузора:
- затрудненное мочеиспускание,
- вялая струя мочи,
- увеличение времени мочеиспускания,
- необходимость напрягать брюшную стенку при мочеиспускании,
- подтекание мочи по каплям после акта мочеиспускания,
- ощущение неполного опорожнения мочевого пузыря,
- парадоксальная ишурия.
- ирритативные — обусловленные изменениями функции детрузора, сфинктера мочевого пузыря и гиперактивностью α1-адренорецепторов шейки мочевого пузыря, простатического отдела уретры и шейки мочевого пузыря; проявляются вне мочеиспускательного акта, еще на этапе накопления мочи в мочевом пузыре:
- ночная поллакиурия,
- учащенное мочеиспускание малыми порциями,
- болезненное мочеиспускание,
- императивные позывы к мочеиспусканию,
- недержание мочи при позывах.
Симптоматика отличается волнообразным течением, прогрессирует нестремительно, но сопровождается выраженными изменениями во всех органах мочевой системы — от канала до почек.
Как лечить доброкачественная гиперплазия предстательной железы?
Лечение доброкачественной гиперплазии предстательной железы представлено несколькими стратегиями, которые определяются степенью нарушения оттока мочи из мочевого пузыря, размерами предстательной железы, выраженностью ирриативных и обструктивных симптомов.
Если качество жизни больного не страдает вследствие заболевания, ему будет предложено выжидательное наблюдение. Такие пациенты остаются под наблюдением уролога и подвергаются периодическим обследованиям. Активное лечение назначается лишь при ухудшении оттока мочи или усиливающейся симптоматике заболевания.
Применимы две традиционные стратегии — консервативное лечение и хирургическое вмешательство.
Медикаментозная терапия предполагает использование ингибиторов 5α-редуктазы и α-адреноблокаторов либо по отдельности, либо комплексно:
- ингибиторы 5α-редуктазы используются с целью уменьшения активности фермента 5α-редуктазы, что воспрепятствует образованию дигидротестостерона из тестостерона; действие медикамента обуславливает сокращение объема предстательной железы, уменьшение механического компонента инфравезикальной обструкции;
- α-адреноблокаторы используются с целью снижения тонуса гладкой мускулатуры шейки мочевого пузыря, заднего отдела мочеиспускательного канала и предстательной железы и, соответственно, к уменьшению динамического компонента обструкции; уменьшаются как обструктивные, так и ирриативные симптомы, увеличивается скорость потока мочи.
В преобладающем числе случаев целесообразна комбинированная терапия ингибиторами 5а-редуктазы и а1-адреноблокаторами.
Когда медикаментозное лечение не приносит ощутимых результатов, а качество жизни больного непреклонно снижается, может быть назначена операция. Наиболее популярными ее воплощениями сегодня являются аденомэктомия открытого типа и трансуретральная резекция простаты (ТУР), однако применяются и прочие методики:
- открытая аденомэктомия — крайне радикальный способ устранения ДГПЖ, считающееся решением при наличии осложнений или при результатах диагностики, демонстрирующих отсутствие результата от ранее предпринятой медикаментозной терапии;
- ТУР предстательной железы — «золотой стандарт» лечения ДГПЖ, отличающийся высокой эффективностью и низкой травматичностью, по сравнению с аденомэктомией отличается следующими плюсами:
- отсутствие рассечения здоровых тканей при подходе к патологическому очагу;
- достижение надежного контроля гемостаза
- сравнительно легкое течение послеоперационного периода;
- возможность выполнения вмешательства у пациентов пожилого и старческого возраста с выраженной сопутствующей патологией.
- трансуретральная электровапоризация предстательной железы — проводится с использованием роликового электрода под названием вапотрод или посредством лазера; заключается в выпаривании патологически разросшейся ткани предстательной железы с одновременным ее подсушиванием и коагуляцией;
- трансуретральная игольчатая абляция предстательной железы — введение в гиперплазированную ткань простаты двух игольчатых электродов, соединенных с радиочастотным генератором;
- трансуретральная электроинцизия предстательной железы — эффективна в лечении ДГПЖ небольших размеров, а также у пожилых пациентов с таким сопутствующими заболеваниями, которые влекут высокий риск при более основательных оперативных вмешательствах.
С какими заболеваниями может быть связано
Доброкачественная гиперплазия предстательной железы сопровождается весьма неприятными, характерными для нее синдромами, часто осложняется прочими заболеваниями мочеполовой системы.
Гипертрофия детрузора развивается при вынужденном сокращении мышц пузыря с большой силой, что осуществляется с целью преодоления сопротивления в зоне инфравезикальной обструкции. Прогрессируя, переходит в частичное замещение мышц мочевого пузыря соединительной тканью, что приводит к атонии мочевого пузыря.
Двусторонний уретерогидронефроз — нарушение функции почек вследствие застоя мочи в чашечно-лоханочной системе почек при выраженном растяжении мочевого пузыря и нарушенном транспорте мочи по мочеточникам.
К осложнениям ДГПЖ относятся:
- острая задержка мочеиспускания — обычно на фоне приема алкоголя или пряной пищи, неудовлетворенного полового возбуждения, переохлаждения, стресса, несвоевременного опорожнения мочевого пузыря; проявляется в невозможности самостоятельно произвести акт мочеиспускания;
- мочекаменная болезнь — по причине застоя мочи в мочевом пузыре и изменениях ее реакции; характеризуется учащенным мочеиспусканием, болевым синдромом;
- гематурия — микро- или макро-, источником крови становится расширение варикозных вен в шейке мочевого пузыря;
- гидроуретер — скопление мочи в одном из мочеточников в связи с нарушением оттока мочи из почечной лоханки по причине выраженной обструкции простатического отдела мочеиспускательного канала и шейки мочевого пузыря за счет гиперплазии; сопровождается повышением давления в мочевом пузыре, зиянием устьев мочеточников, нарушением оттока мочи из мочеточников и почек;
- гидронефроз — расширение почечной лоханки и чашки, что происходит вследствие прогрессирующего расширения мочеточников; благодатные обстоятельства для присоединения инфекции и развития пиелонефрита.
Лечение доброкачественной гиперплазии предстательной железы в домашних условиях
Лечение доброкачественной гиперплазии предстательной железы может проводиться в домашних условиях, однако после предварительной консультации профильного специалиста. Если доктор в качестве стратегии определяет выжидательное наблюдение или медикаментозную терапию, то больной может вести привычный образ жизни с некоторыми изменениями, представляющими лечение простаты. Важно соблюдать режим дня, диетическое питание, умеренные физические нагрузки и активный образ жизни.
Если же состояние больного ДГПЖ осложнено сопутствующими заболеваниями или осложнениями, допускающими проведение оперативного вмешательства, то целесообразна госпитализация. Особенности послеоперационного периода определяются выбранной техникой, однако на завершающем своем этапе также могут проводиться в домашних условиях.
Какими препаратами лечить доброкачественная гиперплазия предстательной железы?
На сегодняшний день медикаментозное лечение доброкачественной гиперплазии предстательной железы пользуется популярностью, отличается эффективностью. При этом используются две категории препаратов либо в сочетании, либо по отдельности:
- ингибиторы 5α-редуктазы:
- Аводарт — в дозе 0,5 мг однократно в сутки; курс лечения не менее 6 месяцев;
- Финастерид — в дозе 0,5 мг однократно в сутки; курс лечения не менее 6 месяцев;
- α-адреноблокаторы:
- Альфузозин — внутрь по 2.5 мг 3 раза/сутки;
- Доксазозин — средняя суточная доза может составлять 2-4 мг, более подробно определяет лечащий врач;
- Тамсулозин — внутрь (запивая достаточным количеством воды), по 0,4 мг/сутки;
- Теразозин — в суточной дозе 1-5 мг в 1-2 приема.
Лечение доброкачественной гиперплазии предстательной железы народными методами
Лечение доброкачественной гиперплазии предстательной железы не должно проводиться в рамках самолечения, а потому любое лечебное мероприятие, в том числе и применение народных средств, должно быть предметом для консультации с медицинским специалистом. Врач может порекомендовать сочетание традиционных и народных методик, а также использование препаратов растительного происхождения. Последние не могут быть рекомендованы для широкого использования, однако клинические исследования показывают их эффективность и безопасность, а потому они могут быть рекомендованы в частных случаях.
Что же касается народных рецептов для домашнего приготовления, то популярностью пользуются следующие:
- чистотел — 1 ст.л. сухой травы заварить стаканом кипятка, спустя два часа процедить; принимать по 1 ст.л. трижды в день за полчаса до еды;
- травяной сбор — соединить 8 грамм травы золотой розги, 10 грамм листа лещины, 10 грамм цветов боярышника, 10 грамм травы шандры, 10 грамм травы цепкого помаренника 15 грамм травы воробейника лекарственного, 20 грамм корневищ стальника; 1 ст.л. смеси заварить ½ литра кипятка, проварить на медленном огне до 10 минут, настаивать 30 минут, процедить; принимать 4 раза в течение дня между приемами пищи;
- пчелиный подмор — 2 ст.л. пчел залить ½ литра горячей воды, довести до кипения и проварить на медленном огне в течение 2 часов; охладить до комнатной температуры, процедить и держать в холодильнике; принимать перед едой по 1-2 ложки в течение месяца;
- шелуха лука — 1 ст. шелухи тщательно промыть, залить ½ литра кипятка и проварить на медленном огне 5-7 минут, настоять 40 минут, процедить; добавить 3 ст.л. меда; принимать по ½ стакана перед едой.
Также отличается целебными действиями свежий лук, петрушка, морковь, грецкие орехи, которые рекомендуется регулярно потреблять в пищу.
К каким докторам обращаться, если у Вас доброкачественная гиперплазия предстательной железы
ДГПЖ на ранней стадии может быть выявлена в ходе профилактических осмотров, которые рекомендованы мужчинам в зрелом возрасте. Даже если это не входит в планы среднестатистического мужчины, то обратиться к урологу целесообразно уже при первых расстройствах мочеиспускания, примечательно, что даже такого рода нарушения не всегда стимулируют мужчину к посещению специалиста.
Обязательные методы исследования для первоначальной оценки состояния больного представлены:
- сбором подробного анамнеза заболевания и выяснением симптомов болезни на момент обращения пациента к врачу, оценкой качества жизни;
- заполнением дневника мочеиспускания;
- общим физикальным обследованием;
- пальпацией предстательной железы и семенных пузырьков через ампулу прямой кишки;
- общим анализом мочи;
- оценкой функционального состояния почек путем определения уровня креатинина в сыворотке крови.
Целесообразно при подозрениях на ДГПЖ провести дифференциальную диагностику со схожими заболеваниями, поскольку симптоматика ДГПЖ не является специфической, а схожие ей патологии могут быть значительно опаснее — это стриктуры уретры, склероз и рак предстательной железы, цистит, рак и камни мочевого пузыря, нестабильность детрузора, простатит, камни нижней трети мочеточника.
Лечение других заболеваний на букву — д
Информация предназначена исключительно для образовательных целей. Не занимайтесь самолечением; по всем вопросам, касающимся определения заболевания и способов его лечения, обращайтесь к врачу. EUROLAB не несет ответственности за последствия, вызванные использованием размещенной на портале информации.
www.eurolab.ua
Оперативное лечение доброкачественной гиперплазии (аденомы) предстательной железы
В зависимости от доступа к предстательной железе различают чреспузырную, позадилонную, промежностную, чрезбрюшинную, ишиоректальную, трансректальную и трансуретральную аденомэктомии. Наибольшее распространение получили операции чреспузырным, внепузырным позадилонным и трансуретральным доступами. Остальные методы в настоящее гремя практически не применяются и имеют лишь историческое значение.
Оперативное лечение может быть неотложным или плановым.
Неотложная аденомэктомия выполняется по ургентным показаниям. В свою очередь она может быть экстренной, если произведена в пределах 24 ч с момента заболевания, и срочной, если осуществляется в любой срок с момента острого заболевания (осложнения), но не позднее 72 ч с момента поступления больного в урологическое отделение. Экстренная аденомэктомия показана в случае угрожающего жизни кровотечения или острой задержкой мочеиспускания при общем удовлетворительном состоянии больного.
Острая задержка мочеиспускания является одной из наиболее частых причин неотложных операций. Это осложнение редко разрешается самостоятельно. В большинстве случаев катетеризация мочевого пузыря является вынужденной мерой оказания помощи больному. После катетеризации мочевого пузыря и применения α1-адреноблокаторов самостоятельное мочеиспускание может восстановиться.
Если консервативное лечение не имеет успеха, такие больные нуждаются в неотложной операции. В неосложненных случаях методом выбора является открытая или трансуретральная аденомэктомия. При невозможности аденомэктомии показано надлобковое дренирование мочевого пузыря путем троакарной цистостомии (рис. 1).
Рис. 1. Троакарная цистостомия
Неотложная аденомэктомия противопоказана в случае острого воспалительного процесса в мочевой системе, сопутствующих заболеваний в стадии декомпенсации (гипертоническая болезнь III стадии, сахарный диабет и др.), терминальной стадии хронической почечной недостаточности.
Трансуретральная резекция простаты сегодня является основным методом оперативного лечения больных доброкачественной гиперплазией предстательной железы, что связано с ее малой травматичностью и высокой эффективностью. Данный метод обладает рядом преимуществ по сравнению с открытой операцией: отсутствием травмы мягких тканей при доступе к предстательной железе, четко контролируемым гемостазом, коротким периодом послеоперационной реабилитации больных. Применение трансуретральной хирургии значительно расширяет показания к оперативному лечению с выраженными сопутствующими интеркуррентными заболеваниями, которые до недавнего времени были обречены на пожизненное отведение мочи путем цистостомии.
Рекомендуется следующая последовательность выполнения трансуретральной резекции: уретроцистоскопия с определением эндоскопических ориентиров и объема оперативного вмешательства, собственно резекция аденомы простаты, гемостаз, эвакуация фрагментов резецированной ткани из мочевого пузыря, эндоскопическая ревизия операционного поля, адекватное дренирование мочевого пузыря.
Осложнения трансуретральной резекции
Несоблюдение методики эндоскопического вмешательства влечет за собой возникновение осложнений. Одним из наиболее часто встречающихся осложнений является кровотечение, которое может возникать как в ходе операции, так и в послеоперационном периоде. Основной причиной интраоперационных кровотечений следует считать повреждение в ходе резекции крупных артериальных или венозных сосудов, кровоснабжающих предстательную железу.
Поздние кровотечения (на 7—8, 13—14, 21 сутки) чаще всего связаны с отхождением послеоперационного струпа, носят интермиттирующий характер и в большинстве случаев купируются консервативно (гемостатическая терапия, установление уретрального катетера с натяжением). При непрекращающемся в течение суток кровотечении показаны повторное эндоскопическое вмешательство и коагуляция кровоточащих сосудов. В патогенезе поздних кровотечений немаловажную роль играют хроническая инфекция в предстательной железе и гнойно-воспалительные осложнения в ближайшем послеоперационном периоде, способствующие торможению заживления раневой поверхности и раннего отхождения струпа.
Одним из самых грозных послеоперационных осложнений трансуретральной резекции является водная интоксикация организма (ТУР-синдром) (0,5—2%), которая развивается из-за поступления в кровоток большого количества гипоосмолярной ирригационной жидкости через вскрытые во время oпe рации венозные синусы. Клинически этот синдром проявляется уже в раннем послеоперационном периоде и включает брадикардию, снижение артериального давления, изменения биохимических показателей электролитного состава крови (гипонатриемия, гипокалиемия) на фоне гиперволемии.
В дальнейшем наблюдается резкое ухудшение состояния пациента на фоне падения артериального давления, массированного гемолиза эритроцитов и олигоанурии на фоне общего беспокойства, цианоза, одышки, болей в груди и судорог. Смерть больного наступает от острой почечно-печеночной недостаточности и грубых электролитных нарушений. При возникновении водной интоксикации организма необходимо проведение экстренных консервативных мероприятий, направленных на нормализацию водно-электролитного баланса и стабилизацию гемодинамики.
Инфекционно-воспалительные осложнения после трансуретральной резекции наиболее часто встречаются в виде уретрита, фуникулита, эпизидимоорхита, простатита, цистита и связаны с активизацией госпитальной флоры на фоне уретрального катетера. Нередко они сопровождаются развитием гнойно-деструктивных изменений органов мошонки, что вынуждает к проведению экстренных оперативных вмешательств, вплоть до органоуносящих.
К другим осложнениям относят ятрогенные повреждения мочевых путей. Среди них травмы мочевого пузыря и устьев мочеточников, чаще всего наблюдаемые при резекции больших внутрипузырных долей доброкачественной гиперплазии предстательной железы, повреждения уретры и предстательной железы, являющиеся причиной возникновения стриктур мочеиспускательного канала, нарушение целости наружного сфинктера уретры, приводящее к недержанию мочи, повреждение семенного бугорка.
Из поздних осложнений трансуретральной резекции предстательной железы необходимо отметить стриктуру уретры и склероз шейки мочевого пузыря. Несмотря на то что после эндоскопической операции они встречается реже, чем после открытой аденомэктомии, частота подобных осложнений остается достаточно высокой (8—15%).
Ретроградная эякуляция после трансуретральной резекции наблюдается в 75—93% случаев. Это необходимо учитывать при определении оперативной тактики у больных молодого возраста с сохранной половой функцией.
С целью уменьшения травматичности лечения, риска кровотечения, снижения уровня осложнений и улучшения результатов все шире при аденоме предстательной железы применяются малоинвазивные эндоскопические методы: электровапоризация (электровыпаривание) и электроинцизия (рассечение) простаты. Электровапоризация осуществляется с помощью стандартного эндоскопического оборудования и электродов специальной конструкции с повышенными выпаривающими и коагулирующими свойствами. Предложено несколько модификаций таких электродов (вапортродов), отличающихся конфигурацией и различным направлением распространения энергии: роликовых, петлевых, клиновидных (рис. 2).
Рис. 2. Различия применения обычной резекционной петли (а) и петли с клиновидным сечением (б)
В отличие от трансуретральной резекции при электровапоризации в зоне контакта вапортрода с тканью простаты возникает сразу несколько физических явлений: выпаривание ткани с одновременным подсушиванием и коагуляцией. Сила электрического тока, используемого при электровапоризации на 25—50% выше, чем при стандартной ТУР, а глубина коагуляции — примерно в 10 раз больше, что значительно снижает кровоточивость ткани во время операции.
В настоящее время вапоризация все шире используется как этап трансуретральной резекции простаты. После завершения такой операции уретральный катетер устанавливается на 1—2 дня.
В отличие от трансуретральной резекции, при которой осуществляется электрохирургическое удаление тканей с помощью режущей петли, при электроинцизии проводится лишь ее продольное рассечение по естественным междолевым границам предстательной железы на 5, 7 и 12 ч условного циферблата копьевидным электродом через всю толщину гиперплазированной ткани до хирургической капсулы. В конце операции коагулируются кровоточащие сосуды, а мочевой пузырь дренируется уретральным катетером на 1 сут.
Метод показан пациентам относительно молодого возраста с сохранной половой функцией и пациентам высокого риска с небольшой предстательной железой и расстоянием от семенного бугорка до шейки мочевого пузыря не более 4 см. Окончательно сделать выбор между рассечением и резекцией можно лишь при уретероцистоскопии, которая позволяет четко определить размеры предстательной железы и форму ее роста.
Среди многообразия методов, предлагаемых в настоящее время для лечения аденомы простаты, открытая аденомэктомия остается наиболее радикальным способом. К преимуществам чреспузырной аденомэктомии относят возможность ее выполнения при любом типе роста и размерах аденомы.
Показаниями к данной операции являются также большие или множественные камни мочевого пузыря, уретероцеле, дивертикулы, опухоль мочевого пузыря, изменение лобковых костей, препятствующее позадилонной аденомэктомии, или невозможность помещения больного в урологическое кресло из-за анкилоза тазобедренных суставов, что делает проблематичным выполнение трансуретральной резекции простаты. Операция проводится под общей или перидуральной анестезией в положении больного на спине с приподнятым тазом.
К недостаткам операции относят невозможность полного визуального контроля за остановкой кровотечения из ложа и технические трудности при удалении аденомы простаты малого объема.
У больных с тяжелым интеркуррентным фоном, ослабленных пациентов пожилого возраста или в случае возникновения осложнений при операции по поводу сопутствующего аденоме простаты другого урологического заболевания лечение может быть проведено в два этапа. Сначала выполняют операцию на мочевом пузыре и дренируют его через надлобковый свищ, а затем, после соответствующей подготовки, через 1,5—3 мес производят аденомэктомию.
Цистостомию можно выполнять методом чрескожной пункции с последующим установлением дренажной трубки (троакарная цистостомия) или оперативно (эпицистостомия). Дренирование мочевого пузыря позволяет подготовить больного к аденомэктомии в более благоприятных условиях. Для некоторых больных цистостомия может стать пожизненной мерой паллиативного лечения.
Внепузырная позадилонная аденомэктомия показана при неосложненных формах аденомы простаты и рекомендуется при большем объеме гаперплазированной ткани с преимущественным внепузырным ростом. Вместе с тем этим способом трудно удалить узлы гиперплазии, растущие внутрипузырно.
К достоинствам позадилонной аденомэктомии можно отнести отсутствие необходимости вскрытия мочевого пузыря и сокращение срока послеоперационного периода. Она противопоказана при камнях, опухоли и дивертикулах мочевого пузыря, уретероцеле и камнях интрамурального отдела мочеточника. Недостатками операции являются большая глубина операционного поля, возможность образования гнойных процессов в малом тазу и стриктуры мочеиспускательного канала. К специфическим осложнениям относят просачивание мочи в позадилонное пространство, нагноение раны с образованием флегмоны тазовой клетчатки, остеита и остеомиелита лобковых костей, тазового тромбофлебита.
Лопаткин Н.А., Пугачев А.Г., Аполихин О.И. и др.
Урология
Опубликовал Константин Моканов
medbe.ru
симптомы, лечение, последствия операции по удалению предстательной железы

Аденома предстательной железы — это доброкачественная опухоль, которая развивается из стромы или железистого эпителия простаты. Сама по себе аденома не дает метастазов, однако может с течением времени переродиться в аденокарциному (простатический рак).
Многие специалисты, говоря об аденоме простаты, предпочитают пользоваться термином «доброкачественная гиперплазия предстательной железы» (ДГБЖ), подчеркивая таком образом ее полицентрический рост на фоне выраженного дисгормонального характера происходящих в предстательной железе изменений.
Распространенность заболевания
Аденома простаты является одним из самых распространенных урологических заболеваний у мужчин. Раньше она редко обнаруживалась до 54-летнего возраста и обычно возникала у 57–60-летних мужчин.
В настоящее время заболевание значительно «помолодело». Например, начальные признаки гиперплазии простаты все чаще появляются в возрасте 25 лет. Согласно данным, полученным при вскрытии умерших от различных заболеваний, в настоящее время аденома простаты встречается до 30 лет у 8%, до 50 лет — у 50%, а после 80 лет аденомой страдают более 80% мужчин.
Считается, что в Китае, Японии аденома простаты встречается очень редко, а наиболее часто — в Северной Америке, Европе, Египте и Индии.
К сожалению, сегодня продолжает сохраняться тенденция к появлению аденомы у молодых, а также рост числа случаев данного заболевания в целом.
Экскурс в анатомию и особенности функционирования простаты
Анатомия
В обычных условиях форма предстательной железы напоминает каштан, размеры которого немного изменяются с возрастом. В 30 лет она 3х4 см и весит около 16 грамм. Расположена простата таким образом, что ее ткани со всех сторон окружают мочеиспускательный канал (именно по этой причине при аденоме в первую очередь начинает страдать нормальное мочеиспускание). Ее ближайшие «соседи» в малом тазу — прямая кишка и мочевой пузырь, поэтому заболевания предстательной железы могут отражаться на общем состоянии и функционировании данных органов.
У новорожденного мальчика простата весит менее 1 грамма, а к 30 годам увеличивается почти в 20 раз. После 45–50 лет простатические железки постепенно атрофируются и замещаются соединительной тканью, из которой практически полностью состоит данная железа, начиная с 65-летнего возраста.
Особенности функционирования
Простата относится к гормонозависимым органам. Ее деятельность контролирует так называемая гипоталамо-гипофизарно-гонадная система, а за ее нормальный рост и функционирование преимущественно «отвечает» мужской гормон тестостерон.
Наиболее интенсивная гормональная перестройка мужского организма начинается после 40–45 лет, когда в плазме происходит снижение тестостерона и увеличение эстрадиола. Эти изменения все более прогрессируют к старости. Во время этой перестройки возможны периоды дестабилизации уровня гормонов, что может послужить толчком к развитию аденомы.
Причины развития аденомы простаты
Точный ответ на вопрос, почему же развивается аденома простаты, на сегодняшний день не даст ни один из специалистов, занимающихся изучением этого заболевания. Дело в том, что гиперплазия железы встречается у мужчин, как с бурной, так и низкой сексуальной активностью, у курящих и некурящих, злоупотребляющих алкоголем и непьющих.

Тем не менее, замечено, что возраст и уровень мужских гормонов очень сильно влияют на частоту возникновения аденомы. Также развитию гиперплазии способствуют наследственный фактор и сидячий образ жизни (отмечается в 60% случаев аденомы). Выявлено также, что аденома не развивается у кастрированных мужчин, поэтому кастрация одно время предлагалась как один из способов лечения ДГПЖ.
Многие специалисты считают, что непосредственную причину развития аденомы простаты следует искать в сложном взаимодействии клеток простаты между собой, изменении их чувствительности к воздействию гормонов и т. п.
Стадии заболевания в зависимости от симптомов
Современная медицина выделяет 4 стадии развития аденомы предстательной железы.
Первая стадия: компенсированная форма
Постепенно увеличиваясь, предстательная железа начинает все более сжимать мочеиспускательный канал, что сразу сказывается на характере мочеиспускания: моча начинает выделяться с затруднением и вялой струей.
Испытывая постоянное сопротивление для обычного оттока мочи, мышцы мочевого пузыря постепенно гипертрофируются, увеличиваются в объеме для того, чтобы буквально «выдавить» мочу наружу.
Наиболее характерные изменения мочеиспускания этой стадии:
- более частое,
- менее свободное,
- не такой интенсивности, как прежде (струя мочи уже не имеет вид характерной параболы, а падает почти вертикально).
Постепенно нарушается ночной сон, так как пациенты вынуждены вставать помочиться 2–3 раза за ночь. Однако этот факт обычно не настораживает, и легко объясняется другими причинами, например, бессонницей, приемом жидкости и т. п.
В дневное время частота мочеиспусканий может остаться прежней, однако в большинстве случаев моча начинает выделяться лишь через некоторое время ожидания (особенно утром после пробуждения).
По мере дальнейшего роста простаты и усиления сдавления мочеиспускательного канала появляются следующие симптомы:
- учащение позывов к мочеиспусканию днем,
- уменьшение выделяемого объема мочи,
- учащение случаев неудержимого желания помочиться (так называемых императивных позывов),
- участие вспомогательных мышц: пациент для лучшего опорожнения время от времени натуживает живот в начале или в конце мочеиспускания.
Не смотря на наличие этих симптомов, почки и мочеточники не изменяются, и общее состояние страдающего аденомой может еще долгие годы оставаться стабильным без каких-либо существенных признаков прогрессирования заболевания.
Однако уже даже на этой стадии периодически может возникать острая задержка мочи.
Вторая стадия: субкомпенсация или периодические нарушения
На этой стадии мочевой пузырь уже опорожняется не полностью, а количество мочи, остающееся в нем после мочеиспускания, достигает 1–2 стаканов.
Характерные симптомы этой стадии:
- увеличение объема мочевого пузыря,
- необходимость натуживаться во время всего мочеиспускания,
- струя мочи выделяется прерывисто, волнообразно,
- из-за наличия периодов отдыха, когда моча не выделяется, весь акт мочеиспускания растягивается на несколько минут.
Из-за постоянного роста объема оставшейся в мочевом пузыре мочи, постепенно начинают происходить изменения и верхних отделов мочевыделительной системы:
- расширяются мочеточники,
- появляются признаки почечной недостаточности.
Прочие возможные симптомы на данной стадии:
- сухость кожных покровов,
- жажда,
- почки — нарушение азотовыделительной функции и развитие начальной стадии почечной недостаточности.
Третья стадия: декомпенсация
Постепенно организм утрачивает способность сопротивляться тому огромному количеству мочи, которое постоянно остается из-за увеличившейся аденомы простаты. Мочевой пузырь перерастянут, поэтому практически не сокращается и не помогает изгнать мочу наружу, даже натуживание во время акта мочеиспускания практически не помогает.
На этой стадии мочевой пузырь похож на переполненный жидкостью шар, достигающий уровня пупка или даже выше.
Симптомы, характерные для этой стадии:
- ощущение постоянного желания опорожнить мочевой пузырь,
- появление сильной боли в нижней части живота,
- частое выделение мочи по каплям или очень малыми порциями.
Постепенно организм адаптируется к данному состоянию, и боли проходят. Моча постоянно «капает», что создает впечатление недержания. Однако данная ситуация связана не с тем, что мочевой пузырь не удерживает мочу, а с тем, что из-за большой аденомы она просто не может выйти в большем количестве. Это явление известно, как «парадоксальная задержка мочи».
В верхних отделах мочеиспускательной системы также происходят изменения:
- значительно нарушаются функции почек, что приводит к развитию декомпенсированной почечной недостаточности,
- максимально расширяются мочеточники.
Из-за утраты почками очистительной функции в организме постепенно начинают скапливаться шлаки, что сопровождается:
- потерей аппетита,
- рвотой, тошнотой,
- общей слабостью,
- характерным запахом тела.
Из-за ограничения принимаемой жидкости в этом периоде пациенты постоянно испытывают жажду, у нах наблюдается сухость во рту, осиплость голоса. Со стороны психики отмечается апатия, подавленность, тревожность.
Четвертая стадия: терминальная
По мере прогрессирования паталогического процесса возникают не совместимые с жизнью явления почечной недостаточности: происходит резкое нарушение водно-электролитного баланса, нарастание содержания азота в крови, и человек умирает от уремии.
Осложнения аденомы предстательной железы
Даже на начальных стадиях, когда гиперплазия предстательной железы еще относительно невелика и нарушение мочеиспускания незначительное, периодически может возникать острая задержка мочеиспускания или обнаруживаться кровь в моче (гематурия). В дальнейшем аденома простаты может осложниться образованием камней или присоединением инфекции мочеполовых органов. Рассмотрим некоторые виды осложнений более подробно.
Острая задержка мочи
Острая задержка мочи — это состояние, когда совершенно невозможно помочиться при переполненном мочевом пузыре. Наиболее часто встречается на второй и третьей стадиях заболевания.

Причины развития острой задержки при аденоме простаты:
- переохлаждение,
- злоупотребление пищей, содержащей пряности,
- прием мочегонных средств,
- длительная задержка мочеиспускания,
- запоры,
- переутомление,
- длительное пребывание в лежачем или сидячем положении,
- прием алкоголя.
Все эти состояния способствуют возникновению отечности тканей и без того увеличенной простаты и т. п.
Как проявляется:
- отсутствие мочи во время акта мочеиспускания,
- боли внизу живота (над лобком),
- в надлобковой области появление «пузырного шара» — выбухание переполненного мочевого пузыря,
- беспокойство, тревожность со стороны больного.
Очень редко острая задержка мочи при аденоме проходит самостоятельно, поэтому мочевой пузырь опорожняют с помощью катетеризации или оперативного вмешательства.
Гематурия
Появление крови в моче при аденоме простаты возникает спонтанно, если произошло кровотечение из расширенных вен в области шейки мочевого пузыря или уретру повредили во время какой-либо манипуляции (например, катетеризации).
Гематурия может быть небольшой, выявляющейся только под микроскопом, или очень значительной, с образованием множества сгустков крови и последующей тампонадой ими мочевого пузыря. В этом случае страдающего аденомой необходимо срочно прооперировать.
Камни мочевого пузыря
Формируются на тех стадиях развития аденомы, когда в мочевом пузыре начитает оставаться достаточно большой объем мочи. Другой путь — миграция камня из почки по мочеточникам и невозможность его выхода через суженный просвет уретры.
Симптомы наличия камня в мочевом пузыре:
- учащенное мочеиспускание,
- боли в области головки пениса, усиливающиеся при движении, ходьбе и исчезающие в горизонтальном положении,
- периодическое появление симптома «закладывания струи мочи».
Инфекционные осложнения
К ним относятся:
Зачастую развитию инфекции способствуют застойные явления в мочевом пузыре, а также катетеризация.
Развитие почечной недостаточности
Характерно для третьей и терминальной стадии развития аденомы и связано с уменьшением выработки мочи почками.
Симптомы:
1. Стадия скрытых проявлений: периодическая сухость во рту, слабость, при сдаче анализов — временами небольшое нарушение электролитов крови.
2. Стадия компенсации: учащение мочеиспускания, изменения в анализах крови (рост уровня мочевины, креатинина).
3. Стадия декомпенсации:
- сухость во рту,
- снижение аппетита,
- тошнота,
- рвота,
- быстрая утомляемость,
- общая слабость,
- снижение иммунитета, проявляющееся в более тяжелом течении обычных простудных заболеваний,
- тремор пальцев,
- подергивания мышц,
- боли в костях и суставах,
- сухость кожи,
- неприятный запах изо рта,
- в крови — повышение мочевины, креатинина.
Стресс, нарушения диеты, чрезмерная физическая нагрузка обостряют проявления почечной недостаточности.
4. Терминальная стадия:
- нарушение ночного сна,
- неадекватность поведения,
- заторможенность,
- эмоциональная лабильность,
- запах мочи от больного,
- живот вздут,
- снижение температуры (гипотермия),
- кожный зуд,
- серо-желтый цвет кожи и лица,
- зловонный стул,
- стоматит,
- изменения практически во всех внутренних органах и нервной системы из-за явлений уремической интоксикации.
В конечном итоге почечная недостаточность приводит к смерти. Единственный возможный способ продления жизни больного — почечно-заместительная терапия (гемодиализ, перитонеальный диализ).
Диагностика аденомы простаты
Комплексная диагностика аденомы проводится на основании данных опроса пациента, урологического осмотра и ряда дополнительных лабораторно-инструментальных методов обследования.
Опрос
Во время беседы врач осведомляется о жалобах, а также проводит опрос согласно разработанному ВОЗ стандартизированному международному опроснику IPSS и его приложению QOL, оценивающего общее качество жизни. В нем содержатся вопросы относительно частоты и характера мочеиспускания, приходилось ли натуживаться во время попытки помочиться и т. п.
Урологический осмотр
Помимо внешнего осмотра половых органов включает обязательное исследование простаты через прямую кишку. Проводится оно следующим образом:
- Перед тем, как прийти на прием к урологу, пациент должен предварительно опорожнить прямую кишку.
- На приеме врач наденет стерильную медицинскую перчатку, смажет палец вазелином и аккуратно введет его в прямую кишку.
- Далее мягкими движениями он осуществит пальпацию (ощупывание) задней стенки простаты.
При аденоме предстательная железа увеличенная, эластичная, безболезненная.
Лабораторные методы
Как правило, назначаются: общий анализ мочи, почечные пробы, анализ крови на определение простатоспецифического антигена, а также гистологическое исследование тканей аденомы (в случае необходимости).
По общему анализу мочи судят о возможном кровотечении, присоединении инфекции мочеполовых органов, признаках почечной недостаточности.
Почечные пробы также важны для выявления недостаточного функционирования почек. Особое внимание обращают на уровень креатинина и остаточного азота, которые по мере прогрессирования почечной недостаточности повышаются.
Уровень простатспецифического антигена определяют для того, чтобы исключить рак предстательной железы, который может наблюдаться вместе с аденомой. При раке уровень данного антигена повышается.
Гистологическое исследование проводится путем биопсии простаты для исключения вероятности рака.
Инструментальные методы
Наиболее часто для диагностики аденомы простаты используются следующие методы:
 1. УЗИ. Дает представление о степени увеличения простаты, ее структуре, выявить узловые образования в железе, а также получить представление о наличии камней в мочевом пузыре и объеме остаточной мочи. Выполняется обычным способом, при котором датчик размещается на передней поверхности живота или помещается в прямую кишку (так называемое трансректальное исследование — ТрУЗИ).
1. УЗИ. Дает представление о степени увеличения простаты, ее структуре, выявить узловые образования в железе, а также получить представление о наличии камней в мочевом пузыре и объеме остаточной мочи. Выполняется обычным способом, при котором датчик размещается на передней поверхности живота или помещается в прямую кишку (так называемое трансректальное исследование — ТрУЗИ).
2. Рентгенологические методы. К ним относятся обзорная рентгенограмма и экскреторная урография. Последняя делается с использованием контраста и позволяет определить расширение мочеточников, лоханок почек, изменение их формы, наличие выпячиваний (дивертикулов) в стенке мочевого пузыря.
3. Урофлоуметрия. Данное исследование проводится с помощью специального аппарата, представляющего собой воронку, которая соединяется с компьютером или самописцем. За час до процедуры необходимо выпить 1 литр чистой негазированной воды, а затем помочиться в воронку аппарата. На бумаге или экране монитора изобразится кривая, по характеру которой врач получит представление о функционировании мочеиспускательного канала и сфинктера мочевого пузыря.
По показаниям проводятся также другие исследования уродинамики, например:
- многоканальная уродинамика,
- профилометрия уретры,
- видеоуродинамика,
- «давление-поток».
4. Уретроцистоскопия. Позволяет визуально оценить характер сужения уретры и выявить возможные изменения в мочевом пузыре.
Полученные результаты помогают определиться с тактикой лечения, выбрав наиболее эффективную для каждого конкретного случая методику. Считается, что в случае аденомы простаты должны настораживать следующие результаты лабораторно-инструментального исследования:
- простатспецифический антиген выше 1,4 нг/мл,
- объем простаты свыше 40 см3,
- по опроснику IPSS более 7,
- максимальная скорость потока мочи меньше 10 мл/с.
Лечение аденомы предстательной железы
В настоящее время не существует единого метода лечения гиперплазии простаты, потому что в каждом случае приходится учитывать многие факторы, например:
- общее состояние и возраст пациента,
- его согласие на операцию,
- стадию аденомы,
- сопутствующие заболевания,
- степень нарушения уродинамики,
- имеются ли признаки рака простаты,
- возможности того или иного лечебного учреждения.
В целом, аденома простаты может лечиться как консервативно, так и оперативно. Использование того или иного метода лечения зависит от стадии развития аденомы:
- Первая стадия. Обычно на этом этапе гиперплазия предстательной железы лечится консервативным путем: назначаются медикаментозные средства, даются рекомендации по режиму и образу жизни — вести физически активный образ жизни, избегать употребления специй и прочих раздражающих продуктов, копченостей, исключить алкоголь, кофе. При возникновении затруднений мочеиспускания может быть рекомендована трансуретральная электрорезекция.
- Вторая стадия. Золотой стандарт оказания помощи на этой стадии — удаление аденомы с помощью операции, используя различные малоинвазивные и классические методики.
- Третья стадия. Здесь основные задачи — это обеспечение хорошего оттока мочи, чтобы снять азотемическую интоксикацию. В этом случае используют чрезкожную пункционную нефростомию, цистостомию и т. п. Далее нормализуют состояние печени, почек, сердечно-сосудистой системы, а потом решают вопрос о возможном дальнейшем оперативном лечении.
Медикаментозное лечение
Препараты, использующиеся для лечения аденомы, не приводят к ее полному исчезновению. Их необходимо применять длительно, регулярно, иначе аденома начнет прогрессировать. Обычно назначаются препараты следующих групп:
 1. Лекарственные средства, расслабляющие тонус гладкой мускулатуры в области шейки мочевого пузыря и простаты, что приводит к ослаблению давления на уретру и облегчению оттока мочи наружу. Это α-адреноблокаторы длительного (пролонгированного) и короткого действия:
1. Лекарственные средства, расслабляющие тонус гладкой мускулатуры в области шейки мочевого пузыря и простаты, что приводит к ослаблению давления на уретру и облегчению оттока мочи наружу. Это α-адреноблокаторы длительного (пролонгированного) и короткого действия:
- доксазозин,
- празозин,
- теразозин,
- альфузозин,
- тамсулозин и прочие.
2. Препараты, блокирующие превращение тестостерона в активную форму и тем самым уменьшающие объем простаты (блокаторы 5-α-редуктазы):
- дутастерид,
- финастерид.
3. Фитопрепараты. В настоящее время растительные препараты в виду низкой эффективности и отсутствия доказанного клинического эффекта во многих развитых европейских странах и США для лечения аденомы не используются. Тем не менее, в ряде стран назначаются растительные средства, в состав которых входят липидостероловые экстракты, например, Serenoa repens, Pygeum africanum и др. Считается, что они обладают противовоспалительным действием, уменьшают отечность, блокируют превращение тестостерона в активную форму и останавливают рост аденомы.
4. Комбинированные средства. В настоящее время «золотым стандартом» является совместный прием препаратов первых двух групп в течение 3–4 лет. Это позволяет практически сразу улучшить мочеиспускание и по прошествии нескольких лет на четверть снизить объем предстательной железы.
Параллельно производится лечение сопутствующих заболеваний — цистита, простатита, пиелонефрита, уретрита.
Оперативные методы лечения
Являются радикальными методами лечения аденомы простаты и широко используются в урологии. К ним относятся:
1. Открытая аденомэктомия. Она может выполняться различными способами, наиболее известным из которых является трансвезикуряная аденомэктомия. Через обычный хирургический разрез обеспечивается доступ к предстательной железе и производится ее удаление. Как правило, используется в случае невозможности использования менее травматичных методик.
 2. Эндоскопические операции. Все они выполняются с помощью специальных хирургических инструментов, вводимых непосредственно в мочеиспускательный канал под контролем видеоаппаратуры. К ним относятся:
2. Эндоскопические операции. Все они выполняются с помощью специальных хирургических инструментов, вводимых непосредственно в мочеиспускательный канал под контролем видеоаппаратуры. К ним относятся:
- трансуретральная резекция простаты (ТУР), являющаяся «золотым стандартом» хирургического лечения аденомы — во время ее проведения через уретру специальным инструментом делается разрез и иссекается ткань простаты;
- трансуретральная электровапоризация — все также доступ к простате обеспечивается через уретру, а затем с помощью тока ткани нагреваются до высокой температуры и испаряются, а мелкие кровеносные сосуды коагулируются;
- трансуретральная инцизия — в области простатического отдела уретры делают разрез, благодаря чему просвет мочеиспускательного канала расширяется, данная операция эффективна в случае аденомы небольшого размера.
3. Эмболизация артерий предстательной железы. Эта операция выполняется сосудистыми хирургами и сводится к тому, что артерии простаты закупоривают специальным полимером, обеспечивая к ним доступ через бедренную артерию.
4. Цистотомия. Используется в качестве промежуточного этапа лечения для того, чтобы разгрузить органы мочеиспускательной системы от избыточного количества скопившейся мочи в экстренном порядке и снять интоксикацию.
Хотя хирургическое лечение является лучшим и зачастую единственным методом успешного лечения, существует целый ряд осложнений, включающих:
- недержание мочи,
- образование спаек в мочеточнике или его сращение,
- учащенное мочеиспускание,
- сохранение значительного количества остаточного объема мочи,
- заброс спермы в мочевой пузырь,
- импотенцию и т. п.
Неоперативные методы
Наиболее известные среди них:
- Баллонная дилатация простаты (суженный участок расширяется с помощью баллона).
- Стентирование уретры (в область сужения вставляется достаточно упругий элемент, который препятствует сужению просвета уретры).
- Испарение тканей простаты микроволнами — микроволновая коагуляция.
- Криодеструкция (замораживание тканей простаты и их последующий некроз).
- Испарение тканей гиперплазированной железы ультразвуком высокой частоты.
- Трансуретральная игольчатая абляция — в простату устанавливаются маленькие иглы, а далее, воздействуя радиоволнами, нагревают и разрушают ткани предстательной железы.
- Удаление тканей простаты с помощью лазера.
Все эти методы занимают промежуточное положение между медикаментозным и хирургическим лечением и используются для сравнительно быстрого восстановления мочеиспускания с меньшим количеством побочных эффектов и лучшей переносимости.
Образ жизни
Всем, страдающим аденомой простаты, рекомендуется регулярно выполнять специальные упражнения, улучшающие кровообращение органов малого таза и препятствующие застою крови, например, «ходить на ягодицах» в течение нескольких минут.
Также необходимо нормализовать свой вес, а в ежедневный рацион питания ввести продукты, богатые цинком и селеном — сардины, лосось, сельдь, тыквенные семена, гречку и овсянку, оливковое масло, сельдерей и пастернак.
bezboleznej.ru

 При условии своевременного выявления ДГПЖ и грамотного подхода в лечении, прогнозы данного заболевания обычно благоприятные. Но затягивание с визитом к врачу может привести к развитию злокачественной формы опухоли, вылечить которую гораздо сложнее. Как проявляется рак простаты и насколько эффективным является его лечение, можно прочитать на нашем сайте.
При условии своевременного выявления ДГПЖ и грамотного подхода в лечении, прогнозы данного заболевания обычно благоприятные. Но затягивание с визитом к врачу может привести к развитию злокачественной формы опухоли, вылечить которую гораздо сложнее. Как проявляется рак простаты и насколько эффективным является его лечение, можно прочитать на нашем сайте.