Заболевания щитовидной железы и беременность | Бурумкулова
В своей практике как эндокринологи, так и акушеры-гинекологи часто встречаются с различными заболеваниями щитовидной железы (ЩЖ) у беременных, что представляет собой значительный клинический и научный интерес как для изучения патологии этих нарушений, так и в плане их лечения.
Как известно, беременность часто ведет к возникновению зоба. Увеличение размеров и объема ЩЖ во время беременности наблюдается вследствие как более интенсивного кровоснабжения ткани ЩЖ, так и увеличения массы ткани ЩЖ. Стимулировать функцию ЩЖ во время беременности могут 3 фактора: возрастание степени связывания тиреоидных гормонов (ТГ) с белками крови, повышение уровня хорионического гонадотропина (ХГ) в крови беременных и недостаточное снабжение ЩЖ йодом в связи с повышенной экскрецией йода с мочой во время беременности (см. рисунок).
Возрастание связывания ТГ с белками крови. Более 99% циркулирующих в крови ТГ связано с белками плазмы: тироксинсвязывающим глобулином (ТСГ), тироксинсвязывающим преальбуми- ном и альбумином. Относительное распределение величины связывания ТГ с различными связывающими белками напрямую зависит от степени их сродства и концентрации. 80% ТГ связано с ТСГ. Связанная и неактивная фракции ТГ находятся в равновесии со «свободной» несвязанной фракцией, которая представляет собой лишь небольшую долю всех циркулирующих ТГ: 0,03—0,04% для свободного тироксина (свТ
При беременности, уже через несколько недель после зачатия сывороточный уровень ТСГ прогрессивно повышается в результате стимуляции значительным количеством эстрогенов, вырабатываемых плацентой. Затем уровень ТСГ достигает плато, которое поддерживается до момента родов. И, напротив, уровень 2 других циркулирующих связывающих белков имеет тенденцию к снижению, главным образом в результате пассивного
Схема стимуляции ЩЖ при беременности
разведения вследствие увеличенного сосудистого пула (кровяного депо).
Результатом повышения при беременности продукции ТСГ является повышение общего уровня ТГ. Уровни общих Т4 (обТ4) и Т3 (обТ3) -значительно повышаются в течение первой половины беременности и достигают плато к 20-й неделе, оставаясь в дальнейшем на том же уровне. Транзи- торное снижение количества свТ
Адекватное поддержание тиреоидного гомеостаза нарушено примерно у 1/3 беременных женщин, что приводит к развитию состояния относительной гипотироксинемии.
Стимуляция функции ЩЖ во время беременности ХГ. ХГ секретируется плацентой только у приматов. Он вырабатывается в больших количествах синцитиотрофобластом плаценты, особенно в первой четверти беременности. Важнейшая функция ХГ — стимуляция стероидогенеза сначала в желтом теле, затем в плаценте.
Значение ХГ для стимуляции ЩЖ женщин во время беременности не до конца изучено. Известно, что существует корреляция между подавлением секреции ТТГ и повышением концентрации ХГ, а также между уровнем ХГ и уровнем свТ4. ХГ способен оказывать прямое стимулирующее действие на ЩЖ матери (причем это влияние наиболее выражено в конце I триместра беременности) благодаря молекулярному сходству ХГ с ТТГ. Действуя на ранних сроках беременности как слабый ’’аналог” ТТГ, ХГ ответствен за небольшое повышение сывороточных уровней свТ4 и свТ3 и как следствие за снижение сывороточного уровня ТТГ. У подавляющего большинства здоровых беременных сти- муляторный эффект ХГ на ЩЖ является коротким и незначительным. Однако у 1—2% всех беременных во время I триместра беременности отмечается снижение концентрации ТТГ и повышение уровня свТ
Возможными причинами повышения уровня ХГ и развития ГТТ могут быть следующие: 1) несбалансированная продукция ХГ вследствие тран- зиторной суперэкспрессии гена, кодирующего Р-субъединицу ХГ; 2) изменения в степени гликозилирования молекулы ХГ, что в свою очередь приводит к удлинению периода его полувыведения; 3) увеличение массы синцитиальных клеток трофобласта плаценты у некоторых женщин (например, при многоплодной беременности).
ГТТ нередко сопровождается неукротимой рвотой беременных (hyperemesis gravidatum), что затрудняет его диагностику из-за того, что на ранних сроках беременности в принципе характерны тошнота и рвота. Это состояние обычно носит транзиторный характер и разрешается ко II триместру беременности. Диагноз ГТТ ставят на основании повышенного уровня ХГ, незначительно подавленной концентрации ТТГ, увеличения сывороточных уровней свТ4 и свТ3 до показателей, характерных для гипертиреоза. Лечение тиреостатиками ГТТ не показано; при выраженных клинических симптомах достаточно только короткого курса р-адреноб- локаторов.
Таким образом, клиницистам важно знать, что симптоматика тиреотоксикоза при беременности имеет специфические отличия и может являться следствием не только аутоиммунного процесса в ЩЖ, но и гормональных изменений, присущих собственно беременности.
Понижение доступности йода при одновременном повышении потребности в нем при беременности. Повышение потребности в йоде во время беременности связано с двумя факторами. С одной стороны, при беременности наблюдается дополнительная потеря йода из организма матери за счет усиленного почечного клиренса йодида, с другой — потеря йодида во второй половине беременности усиливается из-за того, что часть материнского пула неорганического йодида потребляется фето- плацентарным комплексом и идет на синтез ТГ ЩЖ плода.
Для женщин, проживающих в странах с достаточным уровнем потребления йода (таких, как Япония, США или Скандинавия), потеря йода во время беременности не имеет существенного значения, поскольку суточное потребление йода составляет больше 150—200 мкг/сут и остается удовлетворительном в течение всей беременности.
В то же время в регионах с умеренной и тяжелой степенью йодного дефицита в биосфере, к которым относится подавляющая часть территории России, пониженное потребление йода (менее 100 мкг/сут) является довольно жестким фактором стимуляции ЩЖ во время беременности.
Риск развития заболевания ЩЖ во время беременности выше у женщин с наличием в анамнезе зоба (диффузного или узлового), причем количество и размер узлов могут увеличиваться во время беременности. Повторная беременность приводит к дальнейшему увеличению размеров ЩЖ и усилению узлообразования.
В 1989 г. D. Glinoer и соавт. предложили гипотезу, согласно которой усиленная тиреоидная стимуляция во время беременности может вести к образованию диффузного нетоксического зоба (ДНЗ), а беременность представляет собой один из факторов, вызывающих патологические изменения в ЩЖ.
В клинической практике для выявления повышенной тиреоидной стимуляции во время беременности было предложено использовать следующие биохимические показатели.
— Наличие относительной гипотироксинемии, наблюдаемой примерно у 1/3 всех беременных. Для ее диагностики рекомендуются определенные отношения Т4/ТСГ.
— Увеличение секреции Т3, проявляющееся в повышении отношения Т3/Т4 более 0,025 и отражающее стимуляцию ЩЖ в условиях йодного дефицита.
— Изменение концентрации ТТГ в крови. После начальной фазы подавления уровня ТТГ вследствие высокой секреции ХГ в конце I триместра беременности уровень ТТГ прогрессивно повышается и его концентрация к моменту родов удваивается по отношению к исходной. Повышение уровня ТТГ обычно остается в пределах нормы (<4 мЕД/л).
— Изменение концентрации тиреоглобулина (Тг) в сыворотке крови. Сывороточный уровень Тг представляет собой чувствительный индикатор стимуляции ЩЖ, который часто повышается во время беременности : его увеличение наблюдается уже в I триместре, однако наиболее явно выражено в III триместре и к моменту родов. К моменту родов 60% беременных имеют повышенный уровень Тг в крови.
Увеличение концентрации Тг коррелирует с другими показателями тиреоидной стимуляции, такими как небольшое повышение уровня ТТГ и увеличение отношения Т3/Т Наличие кореляции между уровнем Тг и объемом ЩЖ (по данным ультразвукового исследования — УЗИ подтверждает, что уровень Тг в крови представляет собой достаточно надежный биохимический маркер зобогенного действия беременности.
Наличие кореляции между уровнем Тг и объемом ЩЖ (по данным ультразвукового исследования — УЗИ подтверждает, что уровень Тг в крови представляет собой достаточно надежный биохимический маркер зобогенного действия беременности.
Недостаточное потребление йода во время беременности оказывает отрицательное влияние на ЩЖ плода и в дальнейшем на интеллектуальное и физическое развитие ребенка. Как известно, ЩЖ плода приобретает способность концентрировать йод и синтезировать йодтиронины на 10—12-й неделе внутриутробного развития. Средние показатели концентрации свТ4, обТ
Вопрос о проницаемости плаценты для ТГ длительное время остается дискуссионным. В настоящее время предполагается, что ЩЖ матери и плода регулируются автономно, однако не независимо друг от друга. По-видимому, трансплацентарный переход ТГ из организма матери к плоду наблюдается только на ранней стадии внутриутробного развития.
Кроме того, активность ЩЖ плода полностью зависит от поступления йода из материнского организма. В результате как недостаточного поступления йода в организм матери, так и низкого собственного интратиреоидного запаса йода происходит стимуляция ЩЖ плода, что находит отражение в значительном повышении (по сравнению с аналогичными показателями матери) уровней неонатального ТТГ и Тг, а также развитии зоба у плода. Развитие гипотиреоза во внутриутробном и неонатальном периодах может привести к необратимому снижению умственного развития ребенка вплоть до эндемического кретинизма.
Для лечения ДНЗ при беременности в регионах с недостаточным потреблением йода целесообразно рекомендовать прием йода из расчета 150—250 мкг/сут. Для этого можно использовать имеющийся в аптечной сети препарат «Антиструмин» (1000 мкг калия йодида в 1 таблетке) по 1 таблетке 1—2 раза в неделю.
Другим препаратом йода являются таблетки ’’Калия йодид-200″, выпускаемые фирмой «Бер- лин-Хеми». обТ4 и обТ3, что не отражает истинного функционального состояния ЩЖ.
обТ4 и обТ3, что не отражает истинного функционального состояния ЩЖ.
Для лечения ДТЗ у беременных во всех странах предпочтение отдается тиреостатическим препаратам (мерказолил, метимазол, пропилтиоурацил). Хирургическое лечение рекомендуется только в исключительных случаях, таких как выраженные побочные эффекты, зоб очень большого размера, подозрение на малигнизацию или необходимость использовать высокие дозы тиреостатиков для поддержания эутиреоза у матери. Оптимальным сроком для проведения субтотальной резекции ЩЖ считается II триместр беременности. Назна-‘ чение йодидов во время беременности противопоказано из-за риска развития гипотиреоза у плода и — зоба вследствие эффекта Вольфа—Чайкова.
Каких же принципов следует придерживаться при лечении беременной с ДТЗ?
- Выбор конкретного тиреостатика определяется как личным опытом врача, так и доступностью того или иного препарата. В нашей стране для лечения ДТЗ на фоне беременности чаще применяют мерказолил (1 -метил-2-меркаптоимидазол) или его аналоги (метимазол, тиамазол). За рубежом в аналогичной ситуации предпочтение отдается пропилтиоурацилу (6-пропил-2-тиоурацил). В настоящее время в России зарегистрирован и стал доступен препарат этой группы под названием «Пропи- цил» (фирма «Кали-Хеми).
Частота побочных эффектов терапии одинакова для пропилтиоурацила и мерказолила. Оба препарата проникают через плаценту, и чрезмерные их дозы могут вызвать развитие гипотиреоза и зоба во внутриутробном и неонатальном периодах.
Назначение пропилтиоурацила при беременности тем не менее имеет ряд преимуществ. Во-первых, кинетика пропилтиоурацила не меняется при беременности, во-вторых, период полувыведения пропилтиоурацила из крови не зависит от наличия печеночной или почечной недостаточности, в- третьих, пропилтиоурацил в большей степени по сравнению с мерказолилом связывается с белками и обладает ограниченной липофильностью, что затрудняет его проникновение через биологические мембраны, такие как плацента и эпителий молочной железы.
- Клиническое улучшение при лечении тиона- мидами проявляется уже к концу 1-й недели терапии, а эутиреоз достигается через 4—6 нед. В результате хорошо известного иммуносупрессивного действия беременности, проявляющегося повышением числа Т-супрессоров и снижением количества Т-хелперов, ДТЗ при беременности имеет тенденцию к спонтанной ремиссии. Знание этой особенности течения тиреотоксикоза при беременности позволяет контролировать функцию ЩЖ матери с помощью относительно низких начальных, так и поддерживающих доз тиреостатиков. Препараты необходимо назначать в минимальной возможной начальной дозировке (не выше, чем 10— 15 мг мерказолила или 100 мг пропилтиоурацила в сутки) с переходом на поддерживающую дозу (2,5 мг/сут для мерказолила и 50 мг/сут для пропилтиоурацила) .
- Лечение по методу ’’блокируй и замещай» высокими дозами тионамидов в сочетании с заместительной терапией Т4 при беременности противопоказано. При данном режиме терапии Т4 обеспечивает сохранение эутиреоза только у матери, в то же время это может вызвать гипотиреоз у плода, так как высокие дозы тиреостатиков в противоположность Т4 легко проходят через плаценту.
- Использование p-адренергических антагонистов при беременности, осложнившейся развитием тиреотоксикоза, нежелательно, так как они могут вызвать уменьшение массы плаценты, задержку внутриутробного развития плода, постнатальную брадикардию и гипогликемию, а также ослабить реакцию на гипоксию, р—блокаторы могут быть использованы только на короткий период для подготовки к оперативному лечению или при развитии тиреотоксического криза.
- Оптимальным методом контроля эффективности лечения тиреотоксикоза при беременности является определение концентрации свТз и свТ4 в крови. Уровни свТ4 и свТ3 в сыворотке крови матери при лечении тиреостатиками следует поддерживать на верхней границе нормы во избежание гипотиреоза у плода.
Вследствие физиологических изменений секреции ТТГ во время различных фаз беременности уровень ТТГ в крови не является надежным критерием для суждения об адекватности лечения.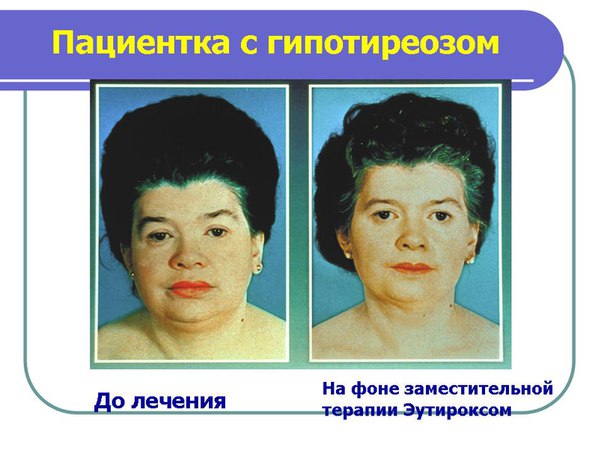 Вместе с тем очень высокий уровень ТТГ указывает на развитие медикаментозного гипотиреоза и требует немедленной отмены или снижения дозы тионамидов. Рекомендуемые рядом авторов ультразвуковое определение размеров ЩЖ плода и исследование уровня ТТГ, Т3 Т4 в крови плода, к сожалению, доступны только небольшому кругу высокоспециализированных медицинских учреждений и пока не могут широко применяться.
Вместе с тем очень высокий уровень ТТГ указывает на развитие медикаментозного гипотиреоза и требует немедленной отмены или снижения дозы тионамидов. Рекомендуемые рядом авторов ультразвуковое определение размеров ЩЖ плода и исследование уровня ТТГ, Т3 Т4 в крови плода, к сожалению, доступны только небольшому кругу высокоспециализированных медицинских учреждений и пока не могут широко применяться.
- При наличии стойкой компенсации в последние месяцы беременности тиреостатические препараты могут быть отменены. В то же время следует помнить о частом рецидиве тиреотоксикоза в послеродовом периоде.
- При лактации тионамиды могут проникать в грудное молоко, причем мерказолил в большей степени, чем пропилтиоурацил. Однако, по существующим данным, низкие дозы тионамидов (до 15 мг мерказолила и 150 мг пропилтиоурацила), принимаемые женщиной во время кормления груч дью, по-видимому, не влияют на функцию ЩЖ ребенка.
Почему так важно лечить тиреотоксикоз на фоне беременности?
Заболевание беременных тиреотоксикозом повышает риск рождения мертвого ребенка, наступления преждевременных родов или развития преэклампсии. Также отмечается повышение частоты неонатальной смертности и вероятности рождения ребенка с дефицитом массы тела. Декомпенсированный тиреотоксикоз может вызвать и усугубить сердечно-сосудистую недостаточность у матери, а также способствовать развитию тиреотоксического криза во время родовых схваток и потуг.
Следует отметить, что вышеперечисленные осложнения чаще наблюдаются при развитии тиреотоксикоза во время беременности, чем в случае наступления беременности у женщин с ранее леченным ДТЗ. Несомненно, что адекватный контроль р лечение тиреотоксикоза у матери являются главным фактором улучшения прогноза беременное™ и родов.
У детей, рожденных от матерей с декомпенсированным ДТЗ, отмечено повышение риска врожденных пороков развития и других фетальных нарушений (6%). В то же время у детей, чьи матер] во время беременности находились в состояни] медикаментозного эутиреоза на фоне лечения ме тимазолом, частота фетальных нарушений анало гична таковой среди детей здоровых эутиреоидны матерей (< 1%). длится 2—3 мес, может являться трансплацента! ный пассаж стимулирующих ЩЖ иммуноглобулинов. Клиническими симптомами неонатального тиреотоксикоза являются тахикардия, гиперчувствительность, задержка роста, увеличение костного возраста, зоб (не всегда), преждевременный, краниостеноз, повышенная смертность и заболеваемость.
длится 2—3 мес, может являться трансплацента! ный пассаж стимулирующих ЩЖ иммуноглобулинов. Клиническими симптомами неонатального тиреотоксикоза являются тахикардия, гиперчувствительность, задержка роста, увеличение костного возраста, зоб (не всегда), преждевременный, краниостеноз, повышенная смертность и заболеваемость.
Неонатальный гипертиреоз требует как можно более раннего и активного лечения тионамидами. Новорожденным назначают метимазол (0,5—1 мг/кг массы тела в день) или пропилтиоурацил (5— 10 мг/кг массы тела в день) в 3 приема. Возможно назначение пропранолола для урежения частоты сердечных сокращений и снижения катехоламиновой активности. При тяжелом заболевании можно давать насыщенный раствор йодида (1 капля раствора в день на протяжении не более 3 нед) для ингибирования высвобождения ранее синтезированных ТГ.
В тяжелых случаях необходимо добавление глюкокортикоидов, которые, помимо общего воздействия, также обладают способностью блокировать конверсию Т4вТ3.
Причинами первичного гипотиреоза у беременных женщин наиболее часто являются хронический аутоиммунный тиреоидит (АИТ) и состояние после резекции ЩЖ по поводу ДТЗ и разных форм зоба. Гипотиреоз вследствие АИТ в большинстве случаев выявляется и компенсируется до наступления беременности, однако иногда его дебют совпадает с беременностью.
С целью выявления АИТ во время беременности необходимо в ранние сроки обследовать беременных с подозрением на дисфункцию ЩЖ на наличие в сыворотке крови антител к тиреоглобулину и тиреоидной пероксидазе.
Как уже описывалось ранее, вследствие иммуносупрессивного действия беременности ранее диагностированный АИТ может иметь тенденцию к ремиссии во время беременности с рецидивом в послеродовом периоде.
Наиболее типичными симптомами гипотиреоза при беременности являются слабость, повышенная сухость кожи, быстрая утомляемость и запоры, однако следует помнить, что эти симптомы могут быть также проявлениями самой беременности в отсутствие понижения функции ЩЖ. Диагноз гипотиреоза при беременности ставят на основании снижения уровня свТ4 и повышения концентрации ТТГ в сыворотке крови.
Диагноз гипотиреоза при беременности ставят на основании снижения уровня свТ4 и повышения концентрации ТТГ в сыворотке крови.
Подбор адекватной дозы Т4 проводят под контролем уровня ТТГ и свТ4 в сыворотке крови (100—150 мкг Т4 в сутки). До недавнего времени считалось, что беременные женщины с ранее леченным гипотиреозом не нуждаются в повышении дозы Т4 на основании того, что повышенная потребность в гормонах ЩЖ компенсируется увеличением их концентрации в сыворотке крови и уменьшением метаболической конверсии Т4. Однако в настоящее время стало ясно, что женщинам, болеющим гипотиреозом и получающим заместительную терапию Т4, нередко во время беременности необходимо увеличивать дозу Т4.
Вероятными причинами повышения потребности в тг во время беременности могут быть как повышение массы тела с увеличением срока беременности, так и адаптационная регуляция оси гипоталамус—гипофиз—ЩЖ, а также возможные изменения периферического метаболизма Т4 из-за наличия фето-плацентарного комплекса.
Неадекватное лечение материнского гипотиреоза может привести к таким осложенениям беременности, как анемия, преэклампсия, отслойка плаценты, послеродовые кровотечения и нарушения функции сердечно-сосудистой системы. Кроме того, у плода и новорожденного с врожденным гипотиреозом трансплацентарный пассаж материнского Т4 на ранних стадиях беременности может играть критическую роль в нормальном развитии мозга.
Блокирующие антитела к рецепторам ТТГ, переходящие через плаценту к плоду, могут вызывать фетальный и неонатальный гипотиреоз (по аналогии с фетальным и неонатальным гипертиреозом). Важно отметить, что у детей матерей, болеющих гипотиреозом с присутствием антител, блокирующих рецептор ТТГ, имеется повышенный риск заболеть внутриутробным или послеродовым гипотиреозом даже при достижении эутиреоидного состояния матери после проведения заместительной терапии Т4.
Фетальный гипотиреоз сопровождается внутриутробным замедлением роста, брадикардией, запоздалым развитием ядер окостенения, а также нарушением процессов развития центральной нервной системы плода.
Неонатальный гипотиреоз обычно длится в течение 1—4 мес (период полувыведения материнских антител из крови ребенка в среднем составляет 3 нед). Наиболее типичными признаками гипотиреоза в ранний постнатальный период являются переношенная беременность (гестационный возраст > 42 нед), большая масса тела при рождении (> 4 кг), макроглоссия, периферический цианоз и отеки, затруднение дыхания, низкий грубый голос при плаче и крике. Диаметр затылочного родничка превышает 5 мм, период желтухи удлиняется (> 3 дней). В дальнейшем могут отмечаться сонливость, снижение аппетита, пониженная активность, гипотермия, сухость и бледность кожных покровов.
Другими причинами транзиторного гипотиреоза могут быть функциональная незрелость гипота- ламо-гипофизарной системы у недоношенных детей, а также тяжелый йодный дефицит у матери во время беременности и назначение высоких доз тиреостатиков по поводу ДТЗ. Доказанная роль ТТГ в развитии плода, а также влияние ТГ на рост и развитие в неонатальном периоде (особенно в течение 1-го года жизни) обусловливают необходимость проведения скрининга на врожденный (в том числе и транзиторный) гипотиреоз.
Транзиторная гипотироксинемия в большинстве случаев проходит самостоятельно при исчезновении причины, ее вызвавшей. В ряде случаев показано назначение новорожденному Т4 в дозе 10—15 мкг/кг массы тела в день коротким курсом (3—4 нед).
В послеродовом периоде у 4—16,7% женщин с отсутствием в анамнезе заболеваний ЩЖ может развиться послеродовой тиреоидит (ПТ). Этиология этого заболевания до сих пор до конца неясна. Выявленная взаимосвязь между ПТ и выявлением аутоантител к ткани ЩЖ (к тиреоидной пероксидазе и микросомальным антигенам), наличием определенных HLA-маркеров и лимфоцитарной инфильтрации ткани ЩЖ позволяет рассматривать ПТ как разновидность АИТ.
В течение ПТ отмечается определенная фазо- вость. После необязательной фазы деструктивного гипертиреоза, протекающей в виде безболевого асимптомного тиреоидита (1—4-й месяц послеродового периода), примерно в 23% случаев наступает фаза стойкого гипотиреоза (5—7-й месяц послеродового периода).
Клинические проявления гипотиреоза при ПТ обычно типичны (слабость, сухость кожи, склонность к запорам и т. д.). При сканировании ЩЖ отмечается пониженное поглощение радиоактивного изотопа йода. Для ультразвуковой картины ПТ характерны диффузное или мультифокальное снижение эхогенности ЩЖ и структурные изменения, характерные для лимфоцитарной инфильтрации ЩЖ и нарушения тиреоидной морфологии.
При развитии стойкого гипотиреоза назначается заместительная терапия Т4 по обычной схеме.
В настоящее время исследуется взаимосвязь между наличием в послеродовом периоде повышенного титра антител к ткани ЩЖ и послеродовой депрессией. Предполагается, что эти антитела могут модулировать функцию нейротрансмиттеров, а также воздействовать на цитокиновые рецепторы мозга.
В заключение хотелось бы отметить, что своевременное и адекватное лечение заболеваний ЩЖ у беременных женщин способствует как нормальному течению беременности, так и правильному физическому и интеллектуальному развитию ребенка.
Диффузный эутиреоидный зоб: диагностика и лечение | #02/07
Термином «диффузный эутиреоидный зоб» (ДЭЗ) обозначается видимое и/или пальпируемое увеличение щитовидной железы.
ДЭЗ — общее диффузное увеличение щитовидной железы без нарушения ее функции. Основной причиной ДЭЗ является недостаточное содержание йода в окружающей среде и, как следствие, сниженное его потребление населением с привычными продуктами питания. В зависимости от распространенности ДЭЗ, в популяции различают спорадический и эндемический зоб.
Зоб считается эндемическим, если в обследуемом регионе частота встречаемости зоба у детей младшего и среднего школьного возраста составляет более 5%. ДЭЗ — патология молодых людей. Более чем в 50% случаев он развивается до 20-летнего возраста, причем у женщин зоб развивается в 2–3 раза чаще, чем у мужчин, при этом, как правило, в те периоды, когда повышена потребность в йоде (половое созревание, беременность, кормление грудью).
ДЭЗ — патология молодых людей. Более чем в 50% случаев он развивается до 20-летнего возраста, причем у женщин зоб развивается в 2–3 раза чаще, чем у мужчин, при этом, как правило, в те периоды, когда повышена потребность в йоде (половое созревание, беременность, кормление грудью).
В соответствии с критериями, принятыми ВОЗ, ЮНИСЕФ (Фонд ООН помощи детям) и ICCIDD (Международный Совет по контролю за йоддефицитными состояниями), регион может считаться свободным от йодного дефицита, если медиана йодурии находится в пределах 100–300 мкг/л, а распространенность зоба не превышает 5%. В России практически не существует территории, благополучной в плане риска развития йоддефицитного зоба. По данным эпидемиологических обследований 1991–2006 гг., частота различных форм зоба в РФ составляет от 10 до 40%.
Наиболее распространенной причиной развития ДЭЗ является дефицит йода. При этом гипертрофия и гиперплазия щитовидной железы носят компенсаторный характер и направлены на обеспечение организма тиреоидными гормонами. Каковы же механизмы такой адаптации к недостаточному поступлению йода?
Во-первых, увеличивается поглощение йода щитовидной железой за счет усиления его активного захвата.
Во-вторых, происходит преимущественный синтез трийодтиронина (Т3), который является наиболее активным тиреоидным гормоном, при этом на его синтез требуется не 4, а всего 3 атома йода.
В-третьих, уменьшается секреция йода почками, увеличивается реутилизация эндогенного йода, что повышает эффективность биосинтеза тиреоидных гормонов.
В-четвертых, снижается содержание йода в коллоиде (за счет преимущественного синтеза монойодтирозина, а не дийодтирозина) и тиреоглобулина в коллоиде (за счет усиления протеолиза).
На ранних стадиях развития зоба (т. е. у детей, подростков и молодых людей) происходит компенсаторная гипертрофия тиреоцитов. Щитовидная железа представлена массой мелких фолликулов, практически не содержащих коллоида. Такой зоб называют паренхиматозным, он представляет собой результат успешной адаптации.
Такой зоб называют паренхиматозным, он представляет собой результат успешной адаптации.
Другой морфологический вариант ДЭЗ — коллоидный зоб. Он состоит из крупных фолликулов, содержащих огромное количество коллоида. При формировании такого типа зоба целый ряд механизмов препятствует оптимальной работе щитовидной железы. Возникает дисбаланс между синтезом и гидролизом тиреоглобулина, снижается степень йодирования тиреоглобулина. Происходит утечка йода из щитовидной железы и снижение синтеза йодтиронинов. Изменения подобного типа преобладают в ткани щитовидной железы прооперированных пациентов.
Несомненно, что все реакции адаптации стимулируются и контролируются тиреотропным гормоном (ТТГ). Однако, как было показано во многих работах, уровень ТТГ при ДЭЗ не повышается. В ходе ряда исследований in vivo и in vitro были получены новые данные об ауторегуляции щитовидной железы йодом и аутокринными ростовыми факторами (АРФ). По современным представлениям, повышение продукции ТТГ или повышение к нему чувствительности тиреоцитов имеет лишь второстепенное значение в патогенезе йоддефицитного зоба. Основная роль при этом отводится АРФ, таким как инсулиноподобный ростовой фактор 1-го типа (ИРФ-1), эпидермальный ростовой фактор (ЭРФ) и фактор роста фибробластов (ФРФ), которые в условиях снижения содержания йода в щитовидной железе оказывают мощное стимулирующее воздействие на тиреоциты. Экспериментально было показано, что при добавлении в культуру тиреоцитов КI наблюдалось снижение ТТГ-индуцируемой, цАМФ(циклический аденозинмонофосфат)-опосредованной экспрессии М-РНК ИРФ-1, с полным ее прекращением при значительном увеличении дозы йодида.
Хорошо известно, что йод сам по себе не только является субстратом для синтеза тиреоидных гормонов, но и регулирует рост и функцию щитовидной железы. Пролиферация тиреоцитов находится в обратной зависимости от интратиреоидного содержания йода. Высокие дозы йода ингибируют поглощение йода, его органификацию, синтез и секрецию тиреоидных гормонов, поглощение глюкозы и аминокислот. Йод, поступая в тиреоцит, вступает во взаимодействие не только с тирозильными остатками в тиреоглобулине, но и с липидами. Образованные в результате этого соединения (йодолактоны и йодальдегиды) являются основными физиологическими блокаторами продукции АРФ. В щитовидной железе человека идентифицировано много различных йодолактонов, которые образуются за счет взаимодействия мембранных полиненасыщенных жирных кислот (арахидоновой, доксагексеновой и др.) с йодом в присутствии лактопероксидазы и перекиси водорода.
Йод, поступая в тиреоцит, вступает во взаимодействие не только с тирозильными остатками в тиреоглобулине, но и с липидами. Образованные в результате этого соединения (йодолактоны и йодальдегиды) являются основными физиологическими блокаторами продукции АРФ. В щитовидной железе человека идентифицировано много различных йодолактонов, которые образуются за счет взаимодействия мембранных полиненасыщенных жирных кислот (арахидоновой, доксагексеновой и др.) с йодом в присутствии лактопероксидазы и перекиси водорода.
В условиях хронической йодной недостаточности возникает снижение образования йодлипидов — веществ, сдерживающих пролиферативные эффекты АРФ (ИРФ-1, ФРФ, ЭРФ). Кроме того, при недостаточном содержании йода происходит повышение чувствительности этих АРФ к ростовым эффектам ТТГ, снижается продукция трансформирующего фактора роста-b (ТФР-b), который в норме является ингибитором пролиферации, активируется ангиогенез.
Все это приводит к увеличению щитовидной железы, образованию йоддефицитного зоба.
В целом развитие ДЭЗ зависит от многих факторов, которые до конца не изучены. Помимо йодного дефицита, к другим факторам, имеющим отношение к развитию зоба, относятся курение, прием некоторых лекарственных средств, эмоциональный стресс, очаги хронической инфекции. Имеют значение также пол, возраст, наследственная предрасположенность.
При эндемическом зобе генетическая предрасположенность может реализоваться только при наличии соответствующего внешнего фактора — дефицита йода в окружающей среде. При отсутствии генетической предрасположенности легкий или даже умеренный йодный дефицит может и не привести к формированию зоба, поскольку этот дефицит будет компенсирован более эффективной работой систем, обеспечивающих синтез тиреоидных гормонов. При тяжелом йодном дефиците даже максимальная активизация компенсаторных процессов не всегда может предотвратить образование зоба у лиц, не имеющих генетической предрасположенности.
Для оценки степени увеличения щитовидной железы методом пальпации ВОЗ (2001) рекомендована следующая классификация.
Нулевая степень — зоба нет (объем каждой доли не превышает объем дистальной фаланги большого пальца руки обследуемого).
1-я степень — зоб пальпируется, но не виден при нормальном положении шеи. Сюда же относятся узловые образования, не приводящие к увеличению самой железы.
2-я степень — зоб четко виден при нормальном положении шеи.
Чувствительность и специфичность метода пальпации для оценки степени зоба довольно низкие. Поэтому для точного определения размеров и объема щитовидной железы в рамках эпидемиологического исследования рекомендуется проведение ультразвукового исследования (УЗИ).
Объем щитовидной железы подсчитывается с учетом ширины (Ш), длины (Д) и толщины (Т) каждой доли и коэффициента поправки на эллипсоидность по следующей формуле
V щж = [(Шпр х Дпр х Тпр) + (Шл х Дл х Тл)] х 0,479.
У взрослых зоб диагностируется, если объем железы, по данным УЗИ, превышает 18 мл у женщин и 25 мл у мужчин. У ребенка объем щитовидной железы зависит от степени физического развития, поэтому перед исследованием измеряются рост и вес ребенка и по специальной шкале или по формуле вычисляется площадь поверхности тела. У детей объем щитовидной железы сопоставляется с нормативными показателями (в зависимости от площади поверхности тела).
Клиническая картина ДЭЗ зависит от степени увеличения щитовидной железы, поскольку функция ее остается нормальной. Сам по себе факт небольшого увеличения щитовидной железы при ее нормальной функции практически не отражается на работе других органов и систем. В подавляющем большинстве случаев в условиях легкого и умеренного йодного дефицита небольшое увеличение щитовидной железы обнаруживается лишь при целенаправленном обследовании.
В условиях тяжелого йодного дефицита зоб может достигать гигантских размеров. Также на фоне ДЭЗ в дальнейшем может развиться узловой зоб, в том числе и с автономно функционирующими узлами.
Лечение ДЭЗ
Мероприятия по ликвидации йодного дефицита в СССР были приняты благодаря эпидемиологическим исследованиям, начатым еще до Второй мировой войны выдающимся хирургом-эндокринологом и специалистом по профилактике О. В. Николаевым. Они включали в себя массовое производство йодированной пищевой поваренной соли, использование таблетированных препаратов йода среди групп риска, создание противозобных диспансеров. На фоне проведения этой программы йодный дефицит в России был в значительной мере преодолен в период с 1955 по 1970 г. После того как это свершилось, в знак «победы над ДЭЗ» было решено постепенно сворачивать мероприятия по его ликвидации, а диагноз «эндемический зоб» заменить на «гиперплазию щитовидной железы».
В Западной Европе вплоть до 60-х годов прошлого века использовались препараты экстрактов щитовидной железы, эффективность которых определялась не только содержанием тиреоидных гормонов, но и большим количеством йода.
На сегодняшний день существует три варианта консервативной терапии ДЭЗ:
- монотерапия левотироксином,
- монотерапия препаратами йода,
- комбинированная терапия препаратами йода и левотироксина.
Монотерапия левотироксином была научно обоснована в лечении ДЭЗ при описании регуляции щитовидной железы гипоталамо-гипофизарной системой. В эксперименте на крысах было показано, что искусственно смоделированный тяжелый йодный дефицит приводит к повышению уровня ТТГ, который, в свою очередь (равно как и экзогенно вводимый ТТГ), может приводить к образованию зоба. Предполагалось, что в условиях дефицита йода снижаются синтез и секреция тироксина Т4 и Т3, для которых йод является основным структурным компонентом, что по принципу отрицательной обратной связи ведет к усилению секреции ТТГ. Поэтому основной целью терапии левотироксином было подавление ТТГ, способствующего увеличению объема щитовидной железы (супрессивная терапия). Однако неоднократно было показано, что уменьшение объема железы не зависит от степени супрессии ТТГ. Также существуют исследования, доказывающие, что средний уровень ТТГ в йоддефицитных районах достоверно ниже, чем в тех районах, где потребление йода нормальное. Более того, есть данные экспериментальных работ, демонстрирующих, что простимулировать рост фолликулов, содержащих достаточное количество йода, не удается введением ТТГ.
Поэтому основной целью терапии левотироксином было подавление ТТГ, способствующего увеличению объема щитовидной железы (супрессивная терапия). Однако неоднократно было показано, что уменьшение объема железы не зависит от степени супрессии ТТГ. Также существуют исследования, доказывающие, что средний уровень ТТГ в йоддефицитных районах достоверно ниже, чем в тех районах, где потребление йода нормальное. Более того, есть данные экспериментальных работ, демонстрирующих, что простимулировать рост фолликулов, содержащих достаточное количество йода, не удается введением ТТГ.
Как было сказано выше, назначение левотироксина широко применялось для лечения ДЭЗ в прошлом. При этом на начальном этапе достигались отличные результаты. Многие клинические исследования показали, что спустя уже 3–4 мес от начала терапии, происходило значительное (не менее 20%) уменьшение объема железы. В литературе приводятся данные об эффективности использования различных доз и комбинаций тиреоидных гормонов. Так T3 в дозе 50 мкг в день является наиболее эффективным для уменьшения объема щитовидной железы. Далее по мере снижения эффективности следуют варианты:
- (T4 50 мкг + T3 12,5 мкг) дважды в день;
- T4 150 мкг в день + йод 150 мкг в день;
- T4 75 мкг в день + T3 18,75 мкг в день;
- T4 200 мкг в день;
- T3 37,5 мкг в день.
Чаще всего в клинической практике использовались дозы — 150 мкг у взрослых и 100 мкг у подростков. Однако многочисленные работы однозначно продемонстрировали «феномен отмены» — увеличение размеров щитовидной железы почти до исходного уровня через короткое время после прекращения лечения. Данный феномен объясняется прежде всего тем, что при подавлении ТТГ снижается активность Na+/I–симпортера, а следовательно, уменьшается активный захват йода щитовидной железой. На фоне резкого падения интратиреоидного содержания йода при отмене лекарственного препарата происходит новый рост железы. Также к побочным эффектам терапии гормонами щитовидной железы относят возможное возникновение лекарственного тиреотоксикоза, тахиаритмии, остеопороза, что ограничивает использование этой группы препаратов при длительном лечении ДЭЗ. Однако иногда с целью быстрого достижения терапевтического эффекта прибегают к назначению кратковременного курса лечения левотироксином с дальнейшим переходом на поддерживающую терапию препаратами йода.
Также к побочным эффектам терапии гормонами щитовидной железы относят возможное возникновение лекарственного тиреотоксикоза, тахиаритмии, остеопороза, что ограничивает использование этой группы препаратов при длительном лечении ДЭЗ. Однако иногда с целью быстрого достижения терапевтического эффекта прибегают к назначению кратковременного курса лечения левотироксином с дальнейшим переходом на поддерживающую терапию препаратами йода.
Монотерапия препаратами йода является этиотропной терапией. Работы последних 10–15 лет показали, что повышение продукции ТТГ или повышение к нему чувствительности тиреоцитов имеет лишь второстепенное значение в патогенезе йоддефицитного зоба. При недостаточном поступлении йода в железу снижается количество йодированных липидов (основных ингибиторов факторов роста), что оказывает мощное стимулирующее воздействие на рост тиреоцитов.
Основная роль при этом отводится местным АРФ, таким как ИРФ-1, ЭРФ и ФРФ.
Этап «возрождения» терапии ДЭЗ йодом наступил в 80-х годах прошлого столетия. Многие исследования были ограничены тем, что в то время не могло быть выполнено ультразвуковое измерение размеров щитовидной железы. Так, G. Hintze и D. Emrich в 1983 г. в своей работе, посвященной лечению йоддефицитного зоба, в качестве основного маркера изменения объема щитовидной железы использовали величину окружности шеи. Авторами было показано, что назначение 400 мкг йода также эффективно снижает объем щитовидной железы, как и 150 мкг левотироксина (оценка через 12 мес от начала лечения), и при этом, в отличие от левотироксина, результат терапии йодом сохраняется еще длительное время после его отмены.
По мере все более широкого внедрения в практическую медицину УЗИ, начинают проводиться рандомизированные контролируемые исследования по влиянию на течение йоддефицитного зоба различных режимов терапии. При этом дозы йода колебались от 100 мкг и выше, включая фармакологические, в случае использования йодированного масла. Назначение 100–150 мкг йода хорошо зарекомендовало себя при лечении зоба у детей.
Назначение 100–150 мкг йода хорошо зарекомендовало себя при лечении зоба у детей.
У взрослых йод в дозе 100–150 мкг в сутки оказался не столь эффективен, как у детей, но тенденция к уменьшению объема щитовидной железы также прослеживается. В научной литературе 80-х годов XX в. можно найти работы, где для лечения зоба использовался йод в дозах и 500 мкг, и 400 мкг, и 300 мкг в сутки. И все они демонстрируют сравнимую эффективность монотерапии йодом с монотерапией левотироксином и комбинированной терапией препаратами йода и левотироксина, а также самый стойкий эффект после отмены препаратов. Однако есть данные, согласно которым использование высоких доз йода иногда вызывает дисфункцию щитовидной железы (гипо- или гипертиреоз). И хотя для признания этого факта нужны более весомые доказательства, в настоящее время общепринятым является следующее положение: лечебные дозы йода при ДЭЗ почти не отличаются от профилактических и составляют 150–200 мкг в сутки. Так, при проведении двойного слепого плацебо контролируемого исследования в Германии была подтверждена эффективность 200 мкг йода для лечения йоддефицитного зоба. Объем щитовидной железы уменьшился на 38% за 6 мес и сохранялся таким еще как минимум такое же время. В другом исследовании оценивалось влияние на размеры железы 200 мкг йода и 100 мкг левотироксина. Была показана сравнимая эффективность этих двух дозировок, причем еще раз акцентировалось внимание на том, что степень уменьшения объема щитовидной железы не зависит от уровня ТТГ.
В многочисленных современных работах продемонстрирован успех в снижении распространенности зоба благодаря внедрению программ всеобщего йодирования соли. Что касается проведения групповой профилактики, теперь вполне достаточно 150 мкг йода в сутки для подростков, 200 мкг — для беременных и кормящих женщин.
В научной литературе последних лет широко обсуждается вопрос развития аутоиммунных процессов в щитовидной железе на фоне приема йодсодержащих препаратов. При этом имеются работы как подтверждающие это влияние, так и отрицающие. G. Kahaly в своих работах изучал эффективность и безопасность низких доз йода при ДЭЗ. Он отметил, что при использовании 200 мкг йода в сутки повышение уровня антител к тиреоидной пероксидазе, антител к тиреоглобулину, значительное возрастание лимфоцитарной инфильтрации в ткани железы происходят только в 97% случаев. В противоположность этим фактам группа исследователей из Австрии вообще не обнаружила вышеописанных изменений при назначении 200 мг йода пациентам с йоддефицитным зобом. В целом развитие аутоиммунных процессов в щитовидной железе, скорее всего, зависит от популяционных особенностей региона, что требует проведения более детальных, тщательно спланированных исследований.
При этом имеются работы как подтверждающие это влияние, так и отрицающие. G. Kahaly в своих работах изучал эффективность и безопасность низких доз йода при ДЭЗ. Он отметил, что при использовании 200 мкг йода в сутки повышение уровня антител к тиреоидной пероксидазе, антител к тиреоглобулину, значительное возрастание лимфоцитарной инфильтрации в ткани железы происходят только в 97% случаев. В противоположность этим фактам группа исследователей из Австрии вообще не обнаружила вышеописанных изменений при назначении 200 мг йода пациентам с йоддефицитным зобом. В целом развитие аутоиммунных процессов в щитовидной железе, скорее всего, зависит от популяционных особенностей региона, что требует проведения более детальных, тщательно спланированных исследований.
Комбинированная терапия препаратами йода и левотироксина может осуществляться как одновременным приемом препаратов левотироксина и калия йодида, так и применением их фиксированных комбинаций. Среди них наиболее часто используются препараты, содержащие 100 мкг левотироксина и 100 мкг йодида (йодтирокс). Терапия йодтироксом, как было неоднократно показано, имеет ряд преимуществ.
Во-первых, воздействуя на несколько патогенетических механизмов образования зоба, подавляется и гипертрофия, и гиперплазия тиреоцитов. Это позволяет добиться результатов, по эффективности сопоставимых с монотерапией левотироксином (при гораздо меньшем его содержании), что, в свою очередь, уменьшает количество побочных эффектов, связанных с приемом тиреоидных препаратов.
Во-вторых, снижается также склонность к развитию «феномена отмены» при кратковременном перерыве в лечении.
В-третьих, менее выражено подавление уровня ТТГ, например, по сравнению с эффектом левотироксина в дозе 150 мкг.
- Уменьшение объема зоба более выражено в случае комбинированной терапии (40%), чем при монотерапии левотироксином (24%) (Schumm и соавт.).
- Меньше частота побочных эффектов левотироксина и калия йодида (так как используются меньшие дозировки, чем при монотерапии).

- Эффект (уменьшение зоба) развивается быстрее, чем при монотерапии калия йодида.
- Не требуется титрование дозы левотироксина, так как соотношение действующих веществ подобрано оптимально.
Существует много работ, подтверждающих эти преимущества. В одной из них сравнивалось лечение ДЭЗ у 74 случайно отобранных больных. Пациенты получали либо 150 мкг левотироксина, либо 100 мкг левотироксина + 100 мкг йода в течение 6 мес. На фоне комбинированной терапии уменьшение объема железы было несколько более выраженным (на 30% по сравнению с 25%, различие недостоверно). Уменьшение размеров железы не зависело от степени супрессии ТТГ. Кроме того, в группе пациентов, получавших комбинированное лечение, в дальнейшем было возможным поддерживать редуцированный объем железы при заместительной терапии 100 мкг йода ежедневно. В группе больных, лечившихся только левотироксином, подобное профилактическое лечение было менее эффективным. Во второе исследование были включены 82 пациента, которым в случайном порядке с лечебной целью назначались либо 100 мкг левотироксина, либо 100 мкг левотироксина + 100 мкг йода так же на протяжении 6 мес. Уменьшение объема железы на фоне левотироксина составило 24% по сравнению с 40% на фоне комбинации препаратов, различия имели статистическую значимость. Таким образом, у взрослых пациентов комбинация «левотироксин плюс йод» является более предпочтительным лечением по сравнению с монотерапией йодом (по крайней мере, в тех же дозах) и сопоставимо с аналогичной дозой левотироксина. Многие исследователи отмечают, что 150 мкг йода в сочетании с индивидуально подобранной дозой левотироксина из расчета 1 мкг/кг веса более предпочтительно для лечения эндемического зоба у взрослых.
Подводя итог вышесказанного, можно сделать вывод, что основной целью в лечении йоддефицитного зоба является не только снижение объема щитовидной железы, но и поддержание достигнутого результата. Для этого подойдут препараты йода как в виде монотерапии, так и в составе комбинированной терапии с левотироксином.
Остается вопрос, что же назначать в первую очередь. Очевидно, что интратиреоидная концентрация йода достоверно сильнее повышается при первоначальном приеме препаратов йода, чем комбинированных с левотироксином препаратов. Этот факт еще раз подтверждает этиотропный характер терапии йодом, а также целесообразность начала лечения именно с назначения препаратов йода.
На наш взгляд, алгоритм терапии ДЭЗ может быть представлен следующим образом.
- Для лечения детей с ДЭЗ рекомендован калия йодид в дозе 100–150 мкг в сутки, подростков — в дозе 150–200 мкг в сутки.
- Лечение взрослых должно проводиться в молодом возрасте (до 45–50 лет), так как при этом чаще удается добиться желаемого результата, а также существует малый риск наличия функциональной автономии щитовидной железы, при которой прием йода может спровоцировать тиреотоксикоз. В первые 6 мес оправдан прием 200 мкг калия иодида в сутки.
Лицам с ДЭЗ старше 45–50 лет показано активное динамическое наблюдение с ежегодным определением уровня ТТГ и проведением УЗИ щитовидной железы.
- При отсутствии выраженного эффекта от приема препаратов йода через 6 мес может быть рекомендован переход на комбинированную терапию. При этом предпочтение должно отдаваться либо фиксированной комбинации 100 мкг йода и 100 мкг левотироксина (йодтирокс), либо индивидуально подобранной дозе левотироксина из расчета 1 мкг/кг веса в сочетании с 150 мкг йода в сутки.
Но, исходя из современных представлений, какое бы первоначальное лечение зоба не проводилось, резкое его прекращение не может быть рекомендовано без дальнейшего проведения профилактических мероприятий — использования йодированной соли.
Литература
- Герасимов Г. А., Фадеев В. В., Свириденко Н. Ю., Мельниченко Г. А., Дедов И. И. Йоддефицитные заболевания в России. М., 2002.
- Gartner R., Dugrillon A., Bechtner G. Evidence that iodolactones are the mediators of growth inhibition by iodine on the thyroid// Acta Med Austriaca.
 1996; 23(1–2): 47–51.
1996; 23(1–2): 47–51. - Knudsen N., Bulow I., Laurberg P., Ovesen L., Perrild H. Low socio-economic status and familial occurrence of goitre are associated with a high prevalence of goitre// Eur J Epidemiol. 2003; 18(2): 175–81.
- Kohn L. D., Shimura H., Shimura Y., Hidaka A., Giuliani C., Napolitano G., Ohmori M., Laglia G., Saji M. The thyrotropin receptor// Vitam Horm. 1995; 50: 287–384.
- Edmonds C. Treatment of sporadic goitre with thyroxine// Clin. Endocrinol. 1992; 36(1): 21–23.
- Einenkel D., Bauch K. H., Benker G. Treatment of juvenile goitre with levothyroxine, iodide or a combination of both: the value of ultrasound grey-scale analysis// Acta Endocrinol. 1992; 127(4): 301–306.
- Hintze G., Emrich D., Koebberling J. Treatment of endemic goitre due to iodine deficiency with iodine, levothyroxine or both: results of a multicentre trial. // Eur. J. Clin. Invest. 1989; 19(6): 527 — 534.
- Leisner B., Henrich B., Knorr D., Kantlehner R. Effect of iodide treatment on iodine concentration and volume of endemic non-toxic goitre in childhood// Acta Endocrinol. 1985; 108(1): 44–50.
- Feldkamp J., Seppel T., Becker A., Klisch A., Schlaghecke R., Goretzki P. E., Roher H. D. Iodide or L-thyroxine to prevent recurrent goiter in an iodine-deficient area: prospective sonographic study// World J Surg. 1997; 21(1): 10–14.
- Wilders-Truschnig M. M., Warnkross H., Leb G. The effect of treatment with levothyroxine or iodine on thyroid size and thyroid growth stimulating immunoglobulins in endemic goiter patients// Clin Endocrinol (Oxf). 1993; 39 (3): 281–286.
- Papanastasiou L., Alevizaki M., Piperingos G., Mantzos E., Tseleni-Balafouta S., Koutras D. A. The effect of iodine administration on the development of thyroid autoimmunity in patients with nontoxic goiter// Thyroid. 2000; 10(6): 493–7.
- Kahaly G. J., Dienes H. P., Beyer J., Hommel G.
 Iodide induces thyroid autoimmunity in patients with endemic goitre: a randomized, double-blind, placebo-controlled trial// Eur J Endocrinol. 1998; 139(3): 290–297.
Iodide induces thyroid autoimmunity in patients with endemic goitre: a randomized, double-blind, placebo-controlled trial// Eur J Endocrinol. 1998; 139(3): 290–297. - Pfannenstiel P. Therapie der endemischen Struma mit Levothyroxin und Jodid. Ergebnisse einer multizentrischen Studie// Deutsche Med. Wochenschr. 1988; 113(9): 326–331.
- Saller B., Hoermann R., Ritter M., Morell R., Kreisig T., Mann K. Course of thryroid iodine concentration during treatment of endemic goiter with iodine or combination of iodine or levothyroxine// Acta endocrinologica. 1991; 125: 662–667.
Е. А. Трошина, доктор медицинских наук
Н. В. Галкина
ЭНЦ РАМН, Москва
Радиойодтерапия тиротоксикоза у детей. Показания, эффективность и безопасность. Обзор литературы. | Румянцев
1. Rivkees SA. Controversies in the management of Graves' disease in children. J Endocrinol Invest. 2016;39(11): 1247-1257. doi: 10.1007/s40618-016-0477-x.
2. Kraiem Z, Newfield RS. Graves' disease in childhood. J Pediatr Endocrinol Metab. 2001;14(3):229-243. doi: 10.1515/JPEM.2001.14.3.229.
3. Croom RD, 3rd, Thomas CG, Jr., Reddick RL, Tawil MT. Autonomously functioning thyroid nodules in childhood and adolescence. Surgery. 1987;102(6):1101-1108.
4. Niedziela M, Breborowicz D, Trejster E, Korman E. Hot nodules in children and adolescents in western Poland from 1996 to 2000: clinical analysis of 31 patients. J Pediatr Endocrinol Metab. 2002;15(6):823-830. doi: 10.1515/JPEM.2002.15.6.823.
5. Cooper DS. Antithyroid drugs for the treatment of hyperthyroidism caused by Graves' disease. Endocrinol Metab Clin North Am. 1998;27(1):225-247. doi: 10.1016/S0889-8529(05)70308-X.
Cooper DS. Antithyroid drugs for the treatment of hyperthyroidism caused by Graves' disease. Endocrinol Metab Clin North Am. 1998;27(1):225-247. doi: 10.1016/S0889-8529(05)70308-X.
6. Glaser NS, Styne DM, Organization of Pediatric Endocrinologists of Northern California Collaborative Graves' Disease Study G. Predicting the likelihood of remission in children with Graves' disease: a prospective, multicenter study. Pediatrics. 2008;121(3):e481-488. doi: 10.1542/peds.2007-1535.
7. Hamburger JI. Management of hyperthyroidism in children and adolescents. J Clin Endocrinol Metab. 1985;60(5): 1019-1024. doi: 10.1210/jcem-60-5-1019.
8. Gruneiro-Papendieck L, Chiesa A, Finkielstain G, Heinrich JJ. Pediatric Graves' disease: outcome and treatment. J Pediatr Endocrinol Metab. 2003;16(9):1249-1255. doi: 10.1515/JPEM.2003.16.9.1249.
9. Lazar L, Kalter-Leibovici O, Pertzelan A, et al. Thyrotoxicosis in prepubertal children compared with pubertal and postpubertal patients. J Clin Endocrinol Metab. 2000;85(10): 3678-3682. doi: 10.1210/jcem.85.10.6922.
10. Leger J, Gelwane G, Kaguelidou F, et al. Positive impact of long-term antithyroid drug treatment on the outcome of children with Graves' disease: national long-term cohort study. J Clin Endocrinol Metab. 2012;97(1):110-119. doi: 10.1210/jc.2011-1944.
11. Jevalikar G, Solis J, Zacharin M. Long-term outcomes of pediatric Graves' disease. J Pediatr Endocrinol Metab. 2014;27(11-12):1131-1136. doi: 10.1515/jpem-2013-0342.
2014;27(11-12):1131-1136. doi: 10.1515/jpem-2013-0342.
12. Cooper DS. Antithyroid drugs. N Engl J Med. 2005;352(9): 905-917. doi: 10.1056/NEJMra042972.
13. Rivkees SA, Stephenson K, Dinauer C. Adverse events associated with methimazole therapy of Graves' disease in children. Int J Pediatr Endocrinol. 2010;2010:176970. doi: 10.1155/2010/176970.
14. Tajiri J, Noguchi S. Antithyroid drug-induced agranulocytosis: how has granulocyte colony-stimulating factor changed therapy? Thyroid. 2005;15(3):292-297. doi: 10.1089/thy.2005.15.292.
15. Razvi S, Vaidya B, Perros P, Pearce SH. What is the evidence behind the evidence-base? The premature death of block-replace antithyroid drug regimens for Graves' disease. Eur J Endocrinol. 2006;154(6):783-786. doi: 10.1530/eje.1.02169.
16. Ron E, Doody MM, Becker DV, et al. Cancer mortality following treatment for adult hyperthyroidism. Cooperative Thyrotoxicosis Therapy Follow-up Study Group. JAMA. 1998;280(4):347-355. doi: 10.1001/jama.280.4.347.
17. Harper L, Chin L, Daykin J, et al. Propylthiouracil and carbimazole associated-antineutrophil cytoplasmic antibodies (ANCA) in patients with Graves' disease. Clin Endocrinol (Oxf). 2004;60(6):671-675. doi: 10.1111/j.1365-2265.2004.02029.x.
18. Румянцев П.О., Коренев С.В. История появления терапии радиоактивным йодом. // Клиническая и экспериментальная тиреоидология. – 2015 – Т. 11. – № 4. – С. 51–55. [Rumiantsev PO, Korenev SV. The history of radioiodine therapy beginnings. Clinical and Experimental Thyroidology. 2015;11(4):51-55. (in Russ.)]. doi: 10.14341/ket2015451-55.
– 2015 – Т. 11. – № 4. – С. 51–55. [Rumiantsev PO, Korenev SV. The history of radioiodine therapy beginnings. Clinical and Experimental Thyroidology. 2015;11(4):51-55. (in Russ.)]. doi: 10.14341/ket2015451-55.
19. Dobyns BM, Sheline GE, Workman JB, et al. Malignant and benign neoplasms of the thyroid in patients treated for hyperthyroidism: a report of the cooperative thyrotoxicosis therapy follow-up study. J Clin Endocrinol Metab. 1974;38(6):976-998. doi: 10.1210/jcem-38-6-976.
20. Safa AM, Schumacher OP, Rodriguez-Antunez A. Long-term follow-up results in children and adolescents treated with radioactive iodine (131I) for hyperthyroidism. N Engl J Med. 1975;292(4):167-171. doi: 10.1056/NEJM197501232920401.
21. Brandao CD, Miranda AE, Correa ND, et al. Radioiodine therapy and subsequent pregnancy. Arq Bras Endocrinol Metabol. 2007;51(4):534-540. doi: 10.1590/S0004-27302007000400006.
22. Sandeep TC, Strachan MW, Reynolds RM, et al. Second primary cancers in thyroid cancer patients: a multinational record linkage study. J Clin Endocrinol Metab. 2006;91(5): 1819-1825. doi: 10.1210/jc.2005-2009.
23. Румянцев П.О., Ильин А.А., Румянцева У.В., Саенко В.А. Рак щитовидной железы. Современные подходы к диагностике и лечению. М.: ГЭОТАР-Медиа; 2009. 448 p. [Rumyantsev PO, Ilyin AA, Rumyantseva UV, Saenko VA. Rak shchitovidnoy zhelezy. Sovremennye podkhody k diagnostike i lecheniyu. Moscow: GEOTAR-Media; 2009. 448 p. (in Russ.)]
24. Boice JD, Jr. Thyroid disease 60 years after Hiroshima and 20 years after Chernobyl. JAMA. 2006;295(9):1060-1062. doi: 10.1001/jama.295.9.1060.
Thyroid disease 60 years after Hiroshima and 20 years after Chernobyl. JAMA. 2006;295(9):1060-1062. doi: 10.1001/jama.295.9.1060.
25. Sheline GE, Lindsay S, Bell HG. Occurrence of thyroid nodules in children following therapy with radioiodine for hyperthyroidism. J Clin Endocrinol Metab. 1959;19(1):127-137. doi: 10.1210/jcem-19-1-127.
26. Read CH, Jr., Tansey MJ, Menda Y. A 36-year retrospective analysis of the efficacy and safety of radioactive iodine in treating young Graves' patients. J Clin Endocrinol Metab. 2004;89(9):4229-4233. doi: 10.1210/jc.2003-031223.
27. Rivkees SA, Dinauer C. An optimal treatment for pediatric Graves' disease is radioiodine. J Clin Endocrinol Metab. 2007;92(3):797-800. doi: 10.1210/jc.2006-1239.
28. Maxon HR, Thomas SR, Hertzberg VS, et al. Relation between effective radiation dose and outcome of radioiodine therapy for thyroid cancer. N Engl J Med. 1983;309(16):937-941. doi: 10.1056/NEJM198310203091601.
29. Graham GD, Burman KD. Radioiodine treatment of Graves' disease. An assessment of its potential risks. Ann Intern Med. 1986;105(6):900-905. doi: 10.7326/0003-4819-105-6-900.
30. Rivkees SA, Cornelius EA. Influence of iodine-131 dose on the outcome of hyperthyroidism in children. Pediatrics. 2003;111(4 Pt 1):745-749. doi: 10.1515/JPEM.2002.15.6.823.
31. Kadmon PM, Noto RB, Boney CM, et al. Thyroid storm in a child following radioactive iodine (RAI) therapy: a consequence of RAI versus withdrawal of antithyroid medication. J Clin Endocrinol Metab. 2001;86(5):1865-1867. doi: 10.1210/jcem.86.5.7473.
J Clin Endocrinol Metab. 2001;86(5):1865-1867. doi: 10.1210/jcem.86.5.7473.
32. Ross DS, Daniels GH, De Stefano P, et al. Use of adjunctive potassium iodide after radioactive iodine (131I) treatment of Graves' hyperthyroidism. J Clin Endocrinol Metab. 1983;57(2):250-253. doi: 10.1210/jcem-57-2-250.
33. Bahn RS, Burch HB, Cooper DS, et al. Hyperthyroidism and other causes of thyrotoxicosis: management guidelines of the American Thyroid Association and American Association of Clinical Endocrinologists. Endocr Pract. 2011;17(3): 456-520. doi: 10.1089/thy.2010.0417.
34. Barnes HV, Blizzard RM. Antithyroid drug therapy for toxic diffuse goiter (Graves disease): thirty years experience in children and adolescents. J Pediatr. 1977;91(2):313-320. doi: 10.1016/S0022-3476(77)80843-3.
35. Miccoli P, Vitti P, Rago T, et al. Surgical treatment of Graves' disease: subtotal or total thyroidectomy? Surgery. 1996;120(6):1020-1024; discussion 1024-1025. doi: 10.1016/S0039-6060(96)80049-3.
36. Bartalena L, Fatourechi V. Extrathyroidal manifestations of Graves' disease: a 2014 update. J Endocrinol Invest. 2014;37(8):691-700. doi: 10.1007/s40618-014-0097-2.
Узловой зоб. Диагностика. Основные принципы лечения
Узловой эутиреоидный зоб
Зобом называют любое увеличение щитовидной железы. Существуют клиническое и морфологическое определения понятия «зоб». С позиции морфолога зоб это любое диффузное или узловое увеличение щитовидной железы, обусловленное избыточным накоплением коллоида в фолликулах (коллоидный зоб), или гиперплазией (увеличением количества клеток) фолликулярного эпителия. С точки зрения клинициста зоб это собирательное понятие, так как этим термином называют различные по происхождению заболевания щитовидной железы гиперпластического, неопластического и воспалительного характера, сопровождающиеся увеличением этого органа. Одной из основных причин увеличения щитовидной железы является дефицит йода в воде и продуктах питания. Клиническое и социальное значений йододефицитных состояний заключается не только в увеличении щитовидной железы и формировании зоба, но и нарушением ее функциональной активности, оказывающем негативное влияние на физическое и умственное развитие людей.
С точки зрения клинициста зоб это собирательное понятие, так как этим термином называют различные по происхождению заболевания щитовидной железы гиперпластического, неопластического и воспалительного характера, сопровождающиеся увеличением этого органа. Одной из основных причин увеличения щитовидной железы является дефицит йода в воде и продуктах питания. Клиническое и социальное значений йододефицитных состояний заключается не только в увеличении щитовидной железы и формировании зоба, но и нарушением ее функциональной активности, оказывающем негативное влияние на физическое и умственное развитие людей.
Узловой эутиреоидный зоб – клиническое понятие, объединяющее все очаговые образования в щитовидной железе, имеющие различную морфологическую картину. Узлом щитовидной железы обычно называют образование, выявленное в ней при осмотре и/или пальпации. Подавляющее большинство узловых образований щитовидной железы доброкачественные. Злокачественные образования щитовидной железы составляют 5-8%.
Этиология и патогенезОбщепринята теория, согласно которой дефицит йода или изменения его метаболизма (нарушение всасывания в ЖКТ, либо окисления при генетических дефектах в энзимной системе и др. ) приводят к снижению концентрации тиреоидных гормонов в крови, что по механизму обратной связи приводит к увеличению образования тиреотропного гормона гипофиза, и щитовидная железа подвергается мощной стимуляции. В результате развивается компенсаторная гипертрофия щитовидной железы, способствующая восполнению недостатка тиреоидных гормонов, и в гипоталамо-гипофизарно-тиреоидной системе наступает временное равновесие. При продолжающем воздействии первичных этиологических факторов такое равновесие быстро нарушается, наступает новая волна тиреотропной стимуляции. В итоге компенсаторный процесс переходит в патологический, и образуется зоб.
Большую роль в патологии щитовидной железы играют и аутоиммунные процессы. Развитие зоба связывают с влиянием ТТГ-подобных факторов, иммуноглобулинов, стимулирующих рост железы, но не влияющих на ее функциональное состояние, а также с образованием тиреоидстимулирующих и тиреоидингибирующих антител.
Узловой эутиреоидный зоб включает в себя следующие морфологические формы:
- узловой коллоидный, в разной степени пролиферирующий зоб;
- фолликулярная аденома;
- гипертрофическая форма аутоиммунного тиреоидита;
- солитарная киста;
- рак щитовидной железы.
Узловой коллоидный зоб.
Наиболее частый вариант узлового зоба патогенетически обусловлен дефицитом йода в организме. Коллоидный зоб формируется за счет избыточного накопления коллоида в полости фолликулов и бывает диффузным, а чаще узловым.
Фолликулярная аденома.
В отличие от коллоидного зоба фолликулярная аденома (до 25% случаев узлового зоба) является доброкачественной опухолью из фолликулярного эпителия (А-клеток). Среди фолликулярных аденом выделяют несколько мофологических вариантов: трабекулярная, микрофолликулярная и макрофолликулярная. Аденома развивающаяся приемущественно из В-клеток щитовидной железы, называется В-клеточной аденомой или опухоль из клеток Гюртле-Ашкенази.
Киста щитовидной железы.
Киста представляет собой полостное, заполненное жидкостью образование в ткани щитовидной железы. На долю кист приходится около 5% всех узловых образований щитовидной железы. Истинную кисту от ложной отличает наличие клеток фолликулярного эпителия, выстилающих полость кисты. Выявление кисты при УЗИ не представляет трудностей, тем не менее не позволяет дифференцировать от цистаденомы или цистаденокардиномы.
Гипертрофическая форма аутоиммунного тиреоидита (АИТ).
Аутоиммунный тиреоидит с узлообразованием может протекать как самостоятельно, так и сочетаться с фолликулярной аденомой или раком.
Рак щитовидной железы.
Раки щитовидной железы по морфологическим признакам принято делить на две группы. Это дифференцированный и недифференцированный рак. Они резко отличаются как по своей структуре, так и по клиническому течению. Дифференцированный рак (фолликулярный и папиллярный) встречаются значительно чаще, характеризуются сохранением гистотипических свойств тиреоидной ткани и отличается сравнительно длительным развитием и относительно благоприятным течением. Недифференцированный рак (анапластический) характеризуется выраженными морфологическими признаками тиреоидной атипии и быстропрогрессирующим течением. Промежуточное положение между дифференцированными и недифференцированными раками щитовидной железы по клиническому течению занимает медуллярный рак, происходящий из С-клеток. Все карциномы щитовидной железы идентифицируют согласно классификации TNM Международного противоракового союза (UICC). Т1- размер опухоли не более 1 см; Т2- размер карциномы 1-4 см; Т3- опухоль более 4 см; Т4- каринома с инвазией капсулы железы независимо от размеров. Для дифференцированных форм рака щитовидной железы введен возрастной критерий. При этом, у больных моложе 45 лет независимо от размера опухоли и поражения регионарных лимфоузлов, при отсутствии отдаленных метастазов устанавливают I стадию. При наличии у данной категории больных отдаленных метастазов – относят ко II стадии.
Они резко отличаются как по своей структуре, так и по клиническому течению. Дифференцированный рак (фолликулярный и папиллярный) встречаются значительно чаще, характеризуются сохранением гистотипических свойств тиреоидной ткани и отличается сравнительно длительным развитием и относительно благоприятным течением. Недифференцированный рак (анапластический) характеризуется выраженными морфологическими признаками тиреоидной атипии и быстропрогрессирующим течением. Промежуточное положение между дифференцированными и недифференцированными раками щитовидной железы по клиническому течению занимает медуллярный рак, происходящий из С-клеток. Все карциномы щитовидной железы идентифицируют согласно классификации TNM Международного противоракового союза (UICC). Т1- размер опухоли не более 1 см; Т2- размер карциномы 1-4 см; Т3- опухоль более 4 см; Т4- каринома с инвазией капсулы железы независимо от размеров. Для дифференцированных форм рака щитовидной железы введен возрастной критерий. При этом, у больных моложе 45 лет независимо от размера опухоли и поражения регионарных лимфоузлов, при отсутствии отдаленных метастазов устанавливают I стадию. При наличии у данной категории больных отдаленных метастазов – относят ко II стадии.
Диагностика узлового зоба
Разделение узловых образований на доброкачественные и злокачественные является кардинальным вопросом диагностики. При сборе анамнеза и осмотре необходимо выявить факторы высокого онкологического риска. К числу неблагоприятных факторов, увеличивающих вероятность наличия карциномы, относятся:
- быстрый рост узла;
- очень плотная консистенция, неровность и несмещаемость узла;
- парез голосовой связки на стороне узла;
- шейная лимфоаденопатия;
- пациенты моложе 20 лет;
- облучение головы или шеи в прошлом;
- рак щитовидной железы у родственников.
- сдавление окружающих органов;
- загрудинный зоб.

При наличии двух или более факторов риска показано оперативное лечение независимо от результатов дополнительных лабораторных и инструментальных обследований.
Выявить рак щитовидной железы на основании только данных анамнеза и осмотра довольно сложно. Это связано с тем, что большинство злокачественных опухолей щитовидной железы относятся к высокодифференцируемым и ничем не отличаются от доброкачественных узлов щитовидной железы. Такие общепрнятые критерии злокачественности, как быстрый рост узла и плотная консистенция, мало помогают в дифференциальной диагностике доброкачественных заболеваний и рака щитовидной железы. Так, с одной стороны, быстрый рост узла наблюдают при кровоизлиянии в аденому, а у лиц с тиреоидитом Хашимото в щитовидной железе обнаруживают плотные узлы, с другой — злокачественный узел может быть мягким при пальпации и длительно существовать в щитовидной железе без признаков роста. Такие критерии злокачественности узла, как отсутствие смещаемости при глотании, осиплость голоса, увеличение регионарных лимфоузлов, являются более специфическими, однако встречаются крайне редко и обычно наблюдаются при далеко зашедшем онкологическом процессе.
УЗИ щитовидной железы
Коллоидные узлы в большинстве случаев определяются как изо- или гипоэхогенные образования обычно овальной формы или реже округлой формы, имеющие четкие, ровные контуры и окруженные гипоэхогенным ободком. При этом в них часто определяются дегенеративные изменения в виде участков сниженной, повышенной эхогенности и кист. В режиме цветного допплеровского картирования (ЦДК) коллоидные узлы, как правило, аваскулярны. На основании нескольких ультразвуковых признаков можно сделать лишь предположение о характере узлового образования.
Аденома в большинстве случаев имеет вид четко очерченного гиперэхогенного образования с гомогенной структурой, окруженной ободком с резко повышенной интенсивностью отраженных эхосигналов. Возможно наличие микрокальцинатов по периферии узла. При ЦДК определяется периферический, перинодулярный кровоток.
При ЦДК определяется периферический, перинодулярный кровоток.
Рак щитовидной железы выявляется в виде гипоэхогенного образования, с нечеткими и неровными контурами, с наличием гиперэхогенных включений и микрокальцинатов внутри узла. В ЦДК режиме картируется интранодулярный кровоток.
Радиоизотопное сканирование
Возможности сцинтиграфии в плане дифференциальной диагностики узлового зоба ограничены. Тем не менее, следует отметить, что: до 10% автономно функционирующих («горячих») узлов являются злокачественными. Для «холодных» узлов этот показатель гораздо выше. Поэтому выявление «холодных узлов» при сцинтиграфии определяет лишь «мишень» для последующего ТАБ под контролем УЗИ.
ТАБ под контролем УЗИ
На сегодняшний день имеет решающее значение в плане морфологической верификации любых узловых тиреоидных образований и является обязательным компонентом в протоколе обследования больных с узловым зобом. ТАБ определяет дальнейшую программу ведения пациента и показания для оперативного лечения. Основные ограничения метода связаны с тем, что с его помощью идентифицируются морфологические изменения, происходящие только на уровне клетки. В связи с этим нет возможности оценить наличие инвазии опухолевых клеток в капсулу узла или в сосуды. В таком случае больные направляются на оперативное лечение. Тактика ведения больных с узловыми образованиями щитовидной железы представлена на рис. 18. 1.
Функциональная автономия щитовидной железы (ФА)
Автономия определяется как функционирование фолликулярных клеток щитовидной железы независимое от влияния ТТГ гипофиза. Самым частым клиническим вариантом функциональной автономии щитовидной железы является многоузловой токсический зоб. Для функциональной автономии щитовидной железы характерны два основных критерия:
- локальные изменения, проявляющиеся наличием высокоактивных очагов, определяемых при сканировании щитовидной железы;
- «молчание» неавтономной ткани железы, связанное с ослаблением тиреоидной стимуляции.

В условиях йодного дефицита щитовидная железа подвержена воздействию комплекса стимулирующих факторов. В результате, у наиболее предрасположенных лиц происходит увеличение щитовидной железы, формируется диффузный эутиреоидный зоб. Отдельные клетки щитовидной железы оказываются более чувствительными к указанным стимулирующим влияниям, благодаря чему получают преимущественный рост. Так формируется узловой и многоузловой эутиреоидный зоб. Отдельные активно делящиеся тиреоциты приобретают способность автономно, то есть вне регулирующих эффектов тиреотропного гормона (ТТГ), продуцировать тиреоидные гормоны. Конечным этапом является развитие узлового и/или многоузлового токсического зоба.
Основным следствием автономии является неконтролируемая секреция тиреоидных гормонов. Уровень этой секреции определяется количеством автономных тиреоидных клеток, их активностью и обеспеченностью йодидом. При достаточно крупных узлах повышенное поступление йодида приводит к увеличению секреции и в конце концов к тиреотоксикозу. Это свидетельствует об отсутствии эффективного ауторегуляторного механизма в таких клетках и объясняет возникновение случаев тиреотоксикоза после увеличения содержания йода в диете.
Узловой токсический зоб является йододефицитным заболеванием, при котором стойкая патологическая гиперпродукция тиреоидных гормонов обусловлена формированием в щитовидной железе автономно функционирующих тиреоцитов. Клиническая картина такого зоба в первую очередь определяется проявлениями тиреотоксикоза со стороны отдельных органов и систем.
Клинические проявления
Синдром поражения сердечно-сосудистой системы
Тахикардия, мерцательная аритмия, развитие дисгормональной миокардиодистрофии («тиреотоксическое сердце»), высокое пульсовое давление. Кардиальные нарушения связаны как с токсическим действием переизбытка гормонов на миокард, так и усиленной работой сердца в связи с возросшими потребностями периферических тканей в кислороде в условиях интенсивного обмена. В результате увеличения УО, МОС и ускорения кровотока повышается систолическое АД, на верхушке сердца и над сонными артериями выслушивается систолический шум. Механизм снижения диастолического АД связан с развитием недостаточности коры надпочечников и недостаточного синтеза глюкокортикоидов – основных регуляторов тонуса сосудистой стенки.
В результате увеличения УО, МОС и ускорения кровотока повышается систолическое АД, на верхушке сердца и над сонными артериями выслушивается систолический шум. Механизм снижения диастолического АД связан с развитием недостаточности коры надпочечников и недостаточного синтеза глюкокортикоидов – основных регуляторов тонуса сосудистой стенки.
Синдром поражения желез внутренней секреции
Кроме надпочечников часто поражается поджелудочная железа с развитием тиреогенного сахарного диабета. Усиленный распад гликогена с поступлением большого количества глюкозы в кровь заставляет работать железу в напряжении, что в итоге приводит к истощению компенсаторных механизмов и развитию инсулиновой недостаточности. У женщин отмечается дисфункция яичников с нарушением менструального цикла, фиброзно-кистозная мастопатия (тиреотоксическая мастопатия, болезнь Вельяминова). У мужчин может развиться гинекомастия.
Синдром поражения центральной и
периферической нервной системы
Проявления поражения центральной и периферической нервной системы — повышенная возбудимость, психоэмоциональная лабильность, снижение концентрации внимания, плаксивость, быстрая утомляемость, нарушение сна, тремор пальцев (симптом Мари) и всего тела (симптом «телеграфного столба»), повышенная потливость, стойкий красный дермографизм, повышение сухожильных рефлексов.
Синдром метаболических нарушений
Повышение основного обмена приводит к похуданию при повышенном аппетите, сопровождается субфебрильной температурой тела и мышечной слабостью.
Синдром поражения органов пищеварительной системы
Проявляется неустойчивым стулом со склонностью к диарее, приступами болей в животе, иногда желтухой, связанной с дисфункцией печени.
Глазные симптомы
Симптом Дальримпля – расширение глазной щели с появлением белой полоски склеры между радужкой и верхним веком.
Симптом Греффе – отставние верхнего века от радужки при фиксации взгляда на медленно перемещающемся вниз предмете, при этом между верхним веком и радужкой остается белая полоска склеры. Симптом Кохера – при фиксации взгляда на медленно перемещающемся вверх предмете, между нижним веком и радужкой остается белая полоска склеры. Симптом Штельвага – редкое мигание век. Симптом Мебиуса – потеря способности фиксировать взгляд на близком расстоянии, вследствие слабости приводящих мышц. Фиксированные на предмете глазные яблоки расходятся и занимают исходное положение. Симптом Репнева-Мелехова – «гневный взгляд».
В основе их развития лежит гипертонус мышц глазного яблока и верхнего века вследствие нарушения вегетативной иннервации под влиянием избытка тиреоидных гормонов в крови.
Тиреогенный экзофтальм следует отличать от эндокринной офтальмопатии – аутоиммунного заболевания. При этом поражаются периорбитальные ткани: инфильтрация лимфоцитами, отложение кислых гликозаминов, выделяемых фибробластами, развивается отек и увеличение ретробульбарной клетчатки, миозит и разрастание соединительной ткани в периокулярных мышцах. При этом больные жалуются на боли, двоение, ощущение «песка» в глазах, слезотечение. Различают три стадии эндокринной офтальмопатии:
- припухлость век, слезотечение, «песок» в глазах;
- диплопия, ограничение отведения глаз, парез взора кверху;
- неполное закрытие глазной щели, изьязвление роговицы, стойкая диплопия, атрофия зрительного нерва.
При тиреотоксикозе также развивается и претибиальная микседема, которая проявляется поражением кожи передней поверхности голени, ее отеком и утолщением, что сопровождается зудом и эритемой.
Отметим, что клиническая картина тиреотоксикоза имеет закономерную возрастную особенность: у молодых людей, у которых, как правило, речь идет о болезни Грейвса, в большинстве случаев имеет место развернутая классическая клиническая картина тиреотоксикоза, тогда как у пожилых пациентов, единственным его проявлением может служить необъяснимый субфебрилитет или суправентрикулярная аритмия, которую обычно связывают с ИБС.
На следующем этапе диагностического поиска у пациентов с клиническими симптомами тиреотоксикоза должен быть подтвержден или отвергнут при гормональном исследовании. Функциональная автономия примерно в 20% случаев развивается при отсутствии отчетливых узловых образований в щитовидной железе (диссеминированная автономия). В то же время болезнь Грейвса может развиваться на фоне предшествующего ей банального эутиреоидного коллоидного зоба. Более специфичным диагностическим методом является сцинтиграфия щитовидной железы: для болезни Грейвса характерно диффузное повышение захвата радиофармпрепарата, при функциональной автономии выявляются «горячие» узлы, либо чередование зон повышенного и пониженного накопления. Нередко оказывается, что в многоузловом зобе наиболее крупные узлы, выявленные при УЗИ, по данным сцинтиграфии оказываются «холодными» или «теплыми», а тиреотоксикоз развивается в результате гиперфункционирования ткани, окружающей узлы.
Ценным исследованием, которое позволяет дифференцировать болезнь Грейвса и функциональную автономию, является определение уровня антител к щитовидной железе. Высокие титры антител к тиреоидной пероксидазе (ТПО) и тиреоглобулину (ТГ) встречаются примерно в 80% случаев болезни Грейвса. При функциональной автономии щитовидной железы они в большинстве случаев отсутствуют.
Консервативное лечение
При лечении эутиреоидного узлового зоба обычно назначают препараты йода и L-тироксин. Однако эффективность подобной терапии низка — лишь у 15% пациентов удается достигнуть уменьшения размеров узлов. Подобное лечение можно рассматривать лишь как профилактическое, направленное на стабилизацию состояния.
Лечение токсического зоба является весьма трудоемкой и кропотливой задачей для врача. Как уже указывалось, методы лечения болезни Грейвса и различных клинических вариантов функциональной автономии щитовидной железы отличаются. Главное отличие заключается в том, что в случае функциональной автономии щитовидной железы на фоне тиреостатической терапии невозможно достижение стойкой ремиссии тиреотоксикоза; после отмены тиреостатиков он закономерно развивается вновь. Таким образом, лечение функциональной автономии подразумевает хирургическое удаление щитовидной железы или ее деструкцию при помощи радиоактивного йода131. В случае болезни Грейвса у отдельных групп пациентов возможно проведение длительной консервативной терапии, которая при правильном отборе больных в 30-40% случаев приведет к стойкой ремиссии заболевания. Для тиреостатической терапии могут использоваться различные препараты. В нашей стране и в странах Европы наиболее популярны препараты тиамазола (Метизол). Кроме того, могут использоваться препараты пропилтиоурацила, которые наиболее популярны в США. Пропилтиоурацил назначают внутрь по 100-150 мг каждые 6 часов, или тиамазол, по 10-30 мг каждые 8 часов. Через 12 месяцев примерно у 30% больных функция щитовидной железы нормализуется и после отмены препарата сохраняется эутиреоз. По мере восстановления функции щитовидной железы, дозы антитиреоидных средств постепенно уменьшают. Антитиреоидные препараты могут вызывать агранулоцитоз. При уменьшении числа лейкоцитов ниже 4500, а гранулоцитов ниже 45%, следует отменить данные препараты.
Таким образом, лечение функциональной автономии подразумевает хирургическое удаление щитовидной железы или ее деструкцию при помощи радиоактивного йода131. В случае болезни Грейвса у отдельных групп пациентов возможно проведение длительной консервативной терапии, которая при правильном отборе больных в 30-40% случаев приведет к стойкой ремиссии заболевания. Для тиреостатической терапии могут использоваться различные препараты. В нашей стране и в странах Европы наиболее популярны препараты тиамазола (Метизол). Кроме того, могут использоваться препараты пропилтиоурацила, которые наиболее популярны в США. Пропилтиоурацил назначают внутрь по 100-150 мг каждые 6 часов, или тиамазол, по 10-30 мг каждые 8 часов. Через 12 месяцев примерно у 30% больных функция щитовидной железы нормализуется и после отмены препарата сохраняется эутиреоз. По мере восстановления функции щитовидной железы, дозы антитиреоидных средств постепенно уменьшают. Антитиреоидные препараты могут вызывать агранулоцитоз. При уменьшении числа лейкоцитов ниже 4500, а гранулоцитов ниже 45%, следует отменить данные препараты.
При неэффективности тиреостатической терапии в течение года, а так же в случае декомпенсации тиреотоксикоза показано оперативное лечение, после предоперационной подготовки в условиях стационара. Субтотальная резекция щитовидной железы считается операцией выбора более 50 лет и является эффективным способом лечения тиреотоксикоза. Операцию проводят только на фоне удовлетворительного самочувствия пациента. Поэтому в предоперационном периоде необходимо нормализовать уровень тиреоидных гормонов с помощью антитиреоидных препаратов. За 7-10 дней до операции назначают йодиды, чтобы уменьшить кровоснабжение щитовидной железы и увеличить ее плотность. При подготовке больных с тяжелым тиреотоксикозом применяют Бета-адреноблокаторы, механизм действия которых связан не только с уменьшением потребностей миокарда в кислороде, но и с замедлением периферической конверсии Т4 в активный Т3. Назначают пропранолол по 5-40 мг в сутки. Прием препарата продолжают и в течение нескольких суток после операции, так как время полужизни Т4 составляет 7 дней. Применение Бета-адреноблокаторов особенно оправдано в тех случаях, когда больные не переносят антитиреоидные средства.
Прием препарата продолжают и в течение нескольких суток после операции, так как время полужизни Т4 составляет 7 дней. Применение Бета-адреноблокаторов особенно оправдано в тех случаях, когда больные не переносят антитиреоидные средства.
Источник: Основы клинической хирурги. Практическое руководство, Издание 2-е, переработанное и дополненное Под редакцией профессора Н.А.Кузнецова, Москва, Издательская группа «ГЭОТАР-Медиа»,2009
Статья добавлена 24 мая 2016 г.
Дифференциальная диагностика гипотиреоза и синдрома эутиреоидной слабости у собак
Автор: Гусева В. А., кандидат ветеринарных наук, главный ветеринарный врач клиники «Велес», г. Санкт-Петербург.Гипотиреоз у собак – это заболевание, сопровождающееся длительным, стойким недостатком гормонов щитовидной железы, которое провоцируется деструкцией паренхимы щитовидной железы либо нарушением работы гипоталамо-гипофизарной системы, вследствие чего происходит недостаточная выработка гормонов щитовидной железой.
Синдром эутиреоидной слабости – состояние, сопровождающееся снижением концентрации гормонов щитовидной железы в крови, вызванное первичной патологией, не связанной с функцией самой щитовидной железы.
Эутиреоз – состояние щитовидной железы, при котором орган выделяет нормальное количество тиреоидных гормонов.
Введение
При гипотиреозе у собак происходит сниженная выработка тироксина щитовидной железой (первичный гипотиреоз), а иногда и недостаточная секреция тиреотропного гормона (ТТГ) гипофизом (вторичный гипотиреоз)6. Недостаточная секреция тиреолиберина гипоталамусом (третичный гипотиреоз) у собак встречается крайне редко: описан всего один клинический случай, который был связан с поражением гипоталамуса опухолью1.Синдром эутиреоидной слабости сопровождается снижением уровня тироксина в крови, что способствует замедлению обмена веществ в период какой-либо первичной болезни и является приспособительным механизмом.
 Также при синдроме эутиреоидной слабости может происходить угнетение выработки ТТГ из-за подавления гипоталамо-гипофизарной системы первичным заболеванием, снижение способности плазмы связывать белки, а также угнетение дейодирования тетрайодтиронина (Т4) в трийодтиронин в периферических тканях (Т3). Как известно, именно за счет функционирования Т3 в периферических тканях щитовидная железа реализует свои основные функции.
Также при синдроме эутиреоидной слабости может происходить угнетение выработки ТТГ из-за подавления гипоталамо-гипофизарной системы первичным заболеванием, снижение способности плазмы связывать белки, а также угнетение дейодирования тетрайодтиронина (Т4) в трийодтиронин в периферических тканях (Т3). Как известно, именно за счет функционирования Т3 в периферических тканях щитовидная железа реализует свои основные функции. При системных заболеваниях, не связанных с щитовидной железой, уровень тироксина часто находится ниже референтных интервалов, а при довольно тяжелых состояниях, таких как анемия и кардиомиопатия, уровень тироксина может быть значительно снижен. При этом истинный гипотиреоз может приводить как к анемии, так и к кардиомиопатии, соответственно, в связи с этим перед клиницистом нередко стоит непростая задача по проведению дифференциальной диагностики.
Грамотно дифференцировать гипотиреоз и синдром эутиреоидной слабости у собак достаточно проблематично, особенно при отсутствии возможности определения свободного тироксина. Свободный тироксин, в отличие от общего тироксина, не связан с белками плазмы крови и, следовательно, менее подвержен колебаниям, вызванным наличием первичных патологий или приемом препаратов, чем общий тироксин. Определение концентрации свободного тироксина допустимо только методом равновесного диализа, который недоступен в России. Исходя из этого, для лабораторной диагностики гипотиреоза и синдрома эутиреоидной слабости у собак мы используем определение концентрации в крови общего тироксина и тиреотропного гормона соответственно6.
Важно понимать, что нормальные уровни тиреоидных гормонов свидетельствуют об эутиреозе, в то время как снижение тироксина не всегда говорит о наличии гипотиреоза.
При первичном гипотиреозе уровень общего тироксина находится ниже референтного интервала либо на нижней границе нормы при повышенном ТТГ (первичный гипотиреоз составляет 95 % всех случаев гипотиреоза у собак), в то время как при вторичном гипотиреозе уровень общего тироксина будет находиться ниже референтного интервала, а ТТГ – в референтном интервале (на вторичный гипотиреоз у собак приходятся оставшиеся 5% случаев). При первичном нетиреоидном заболевании и развитии синдрома эутиреоидной слабости общий тироксин вторично снижается, а уровень ТТГ остается нормальным либо возрастает. Однако, согласно одному из исследований4, при синдроме эутиреоидной слабости повышение ТТГ отмечается довольно редко, всего в 8% случаев. Таким образом, из приведенной статистики (рис. 1, 2) ясно, что если мы имеем дело с гипотиреозом, то, вероятнее всего, общий тироксин будет снижен/ на нижней границе нормы, а ТТГ – повышен. В случае сниженного общего тироксина при нормальном ТТГ, скорее всего, у животного присутствует синдром эутиреоидной слабости, развивающийся вследствие сопутствующей патологии.
Естественно, недопустимо проведение дифференциальной диагностики только лишь на основании лабораторных данных, для дальнейшей работы необходимо провести тщательный сбор анамнеза и оценить наличие или отсутствие характерных для гипотиреоза клинических признаков4.
Этиология
Считается, что причиной первичного гипотиреоза у собак является аутоиммунное разрушение ткани щитовидной железы, в частности лимфоцитарный тиреоидит либо идиопатическая атрофия, в то время как причиной вторичного гипотиреоза у собак является наличие новообразований, кист передней доли гипофиза3.Этиология синдрома эутиреоидной слабости более разнообразна, поскольку многие системные заболевания могут приводить к его возникновению, а именно: почечная, печеночная, сердечная недостаточность, инфекционные заболевания, сахарный диабет и синдром Кушинга. Этот список болезней можно было бы продолжить, однако перечисленные заболевания являются самыми распространенными причинами появления синдрома эутиреоидной слабости.
Способствовать развитию синдрома эутиреоидной слабости могут также голодание, кахексия, содержание животных в холодных условиях, прием некоторых лекарственных препаратов (глюкокортикостероиды, антиконвульсанты, фуросемид, препараты для общей анестезии в течение 36 часов после применения, сульфаниламиды). Причем такие препараты, как сульфаниламиды, снижают не только Т4 общий, но и ТТГ.
У некоторых пород собак, таких как салюки и борзые, часто встречается снижение общего тироксина в крови (в норме) без наличия гипотиреоза или синдрома эутиреоидной слабости.
Патогенез
Если в случае с гипотиреозом понятно, что аутоиммунная/идиопатическая атрофия щитовидной железы либо повреждение передней доли гипофиза приводит к сниженной выработке/стимуляции выработки общего тироксина щитовидной железой, то в случае с синдромом эутиреоидной слабости все не так очевидно.Почему же сопутствующие системные болезни могут приводить к снижению уровня гормонов щитовидной железы? Ответ кроется непосредственно в самих функциях гормонов щитовидной железы и хорошо описан в медицинских источниках на примере больных гипотиреозом людей, где объясняется, что снижение уровней гормонов щитовидной железы при тяжелых системных заболеваниях происходит с целью приспособления к измененному гомеостазу и, как следствие, к уменьшению расходуемой энергии, предотвращению катаболизма белка в организме2, 5. Исходя из этого можно предположить, что у собак развитие синдрома эутиреоидной слабости происходит по той же причине. Согласно некоторым данным, прослеживается даже зависимость уровня тироксина от тяжести системного заболевания у собак: чем тяжелее протекает системное заболевание, тем больше выражено снижение тироксина в крови и, соответственно, тем хуже прогноз4. В частности, подробно описан патофизиологический механизм развития синдрома эутиреоидной слабости у собак, больных бабезиозом. При бабезиозе у собак происходит повышенная выработка фактора некроза опухолей-α (ФНО-α) и интерлейкина-6, что приводит к угнетению гипоталамо-гипофизарно-тиреоидной связи и, как следствие, к снижению секреции гормонов щитовидной железы. Также повышается активность фермента дейодиназы, который способствует переходу тироксина в трийодтиронин и угнетает выработку ТТГ в гипоталамусе. По данным исследований, степень снижения уровня тироксина в сыворотке у больных бабезиозом собак была связана с тяжестью проявления клинических признаков бабезиоза и смертностью животных8.
Диагностика
Грамотное проведение дифференциальной диагностики гипотиреоза и синдрома эутиреоидной слабости будет зависеть от тщательности собранного анамнеза, правильной интерпретации данных клинического осмотра и лабораторных исследований.Для гипотиреоза у собак наиболее характерными являются следующие клинические признаки: летаргия, билатеральная симметричная невоспалительная алопеция, алопеция в местах трения, гиперпигментация кожи, увеличение массы тела, гипотрофия мышечной массы, микседема, анестрия, снижение либидо и т. д. Важно учитывать, что гипотиреоз более характерен для собак среднего и старшего возраста.
При синдроме эутиреоидной слабости ведущие клинические признаки будут зависеть от основного заболевания. Ввиду того что синдром эутиреоидной слабости является следствием другого системного заболевания, симптом выраженной слабости, вероятно, будет встречаться довольно часто. Синдром эутиреоидной слабости может проявиться в любом возрасте.
Что же касается лабораторных исследований, то исходя из статистических данных по колебанию общего тироксина и ТТГ при гипотиреозе и синдроме эутиреоидной слабости можно сделать следующие выводы:
- Т4 общий ниже нормы, ТТГ повышен: высока вероятность гипотиреоза при наличии характерных клинических признаков. Синдром эутиреоидной слабости встречается в 8% случаев при таком уровне гормонов щитовидной железы. Целесообразно начинать лечение левотироксином при соответствующих клинических признаках.
- Т4 общий ниже нормы, ТТГ в норме: высока вероятность синдрома эутиреоидной слабости. Гипотиреоз возможен в 5% случаев при условии наличия характерных клинических признаков. Целесообразно провести пробную терапию левотироксином. При надлежащем ответе на терапию (купирование клинических признаков через 1 мес., а дерматологических – через 3 мес.) диагноз «гипотиреоз» будет считаться подтвержденным. Наиболее наглядной будет проба с отменой левотироксина: при возвращении симптомов заболевания, которые будут купированы в процессе возобновленного лечения, диагноз «гипотиреоз» будет считаться подтвержденным. Либо нужно будет провести повторное исследование гормонов через 3 мес.
- Т4 на нижней границе нормы, ТТГ повышен: сомнительный результат. Эндокринную болезнь можно подозревать при характерных клинических признаках гипотиреоза. Возможен гипотиреоз в начале заболевания. Необходимо проанализировать условия содержания животного, фазу полового цикла, прием препаратов, сопутствующие патологии. При отсутствии характерных симптомов гипотиреоза необходимо иметь в виду синдром эутиреоидной слабости.
- Т4 на нижней границе нормы, ТТГ в норме: вероятнее всего, имеет место суточное колебание тироксина, синдром эутиреоидной слабости. Необходимо проанализировать условия содержания, породную предрасположенность (салюки, борзые), фазу полового цикла, прием препаратов, сопутствующие патологии. При подозрении на гипотиреоз следует повторно исследовать гормоны щитовидной железы через 3 мес.
Также есть данные о том, что тиреоидный статус, вероятно, связан с таким заболеванием, как дилатационная кардиомиопатия (ДКМП). Хроническая сердечная недостаточность, являющаяся следствием ДКМП, может приводить к синдрому эутиреоидной слабости. Возможна и обратная ситуация, когда гипотиреоз приводит к эхокардиографическим изменениям, схожим с ДКМП, в частности к снижению фракции сократимости, увеличению полости левого желудочка в систолу и диастолу, уменьшению свободной стенки левого желудочка и межжелудочковой перегородки, что обусловлено инфильтрацией миокарда мукополисахаридами. При этом однозначная связь между гипотиреозом у собак и ДКМП не установлена9.
В заключение необходимо отметить, что для проведения грамотной дифференциальной диагностики гипотиреоза и синдрома эутиреоидной слабости необходимо учитывать клинические признаки, лабораторные данные и сопутствующие факторы, такие как прием некоторых препаратов, условия содержания животного, породную предрасположенность, фазу полового цикла, и придерживаться рекомендованного алгоритма действия.
Литература:
- Игнатенко Н. А. Нарушения функции щитовидной железы у собак. – Vet Pharma № 5. – 2015, стр. 40–47.
- Иноземзева М. П., Иноземцев П. В., Панова Т. Н. Оценка тиреоидного статуса у больных с хронической почечной недостаточностью. ссылка.
- Смирнова О. О. Эндокринная патология – гипотиреоз собак. ссылка.
- Нельсон Р., Фельдман Э. Эндокринология и репродукция собак и кошек. – «Софион», 2008. – 1256.
- Трошина Е. А., Юкина М. Ю. Синдром гипотиреоза. – Клиницист № 1. – 2008, стр. 45–50.
- Торранс Э. Д. и Муни К. Т. Эндокринология мелких домашних животных. – «Аквариум». – 2006, 311с.
- Moony C. Canine hypothyroidism: A review of aetiology and diagnosis. New Zealand Veterinary Journal. – 2011, pp. 105–111.
- Zygner V., Zygner O., Euthyroid sick syndromу in Canine babesiosis caused by babesia canis. – Bulletin of the Veterinary Institute in Pulawy. – № 1. – 2013, p. 525–527.
- Satish Karlapudi, Devarakonda Srikala. Hypothyroidism – A cause for dilated cardiomyopathy in dogs; four year study (2008–2011). Vet World. – 2012, Vol. 5(12): 742–747.
Эутиреоз
Пользователи также искали:
аит эутиреоз, чем опасен эутиреоз, эутиреоз клинические рекомендации, эутиреоз лечение, эутиреоз отзывы форум, эутиреоз питание, эутиреоз таблетки, эутиреоз у подростка, Эутиреоз, эутиреоз, рекомендации, эутиреоз питание, эутиреоз лечение, эутиреоз у подростка, эутиреоз отзывы форум, эутиреоз клинические рекомендации, аит эутиреоз, эутиреоз таблетки, опасен, питание, лечение, подростка, отзывы, форум, клинические, таблетки, чем опасен эутиреоз, cтатьи по эндокринологии. эутиреоз,
…
Лабораторная диагностика заболеваний щитовидной железы
РЕФЕРЕНТНЫЕ ПРЕДЕЛЫ ТТГ И ТИРЕОИДНЫХ
ГОРМОНОВ В ЗАВИСИМОСТИ ОТ ВОЗРАСТА И СРОКА
БЕРЕМЕННОСТИ (95% ДОВЕРИТЕЛЬНЫЙ ИНТЕРВАЛ)
|
Возраст |
ТТГ (мкМЕ/мл) |
Т4 общий (нмоль/л) |
Т4 свободн. (пмоль/л) |
Т3 общий (нмоль/л) |
Т3 свободн. (пмоль/л) |
|
Новорожденные |
11,6 – 35,9 |
105 — 290 |
21 — 49 |
0,84 – 3,63 |
|
|
Дети в возрасте: 2 суток 3 суток 1 неделя 2 недели 3 недели 1 месяц 6 месяцев 1 год 5 лет 10 лет 15 лет |
8,3 – 19,8 1,0 – 10,9 1,2 – 5,8
0,7 – 6,4 0,7 – 6,4 0,7 – 6,4 0,7 – 6,4 0,7 – 6,4 |
83 – 303 110 – 285 93 – 247 88 – 225 94 – 259 112 – 243 103 – 210 92 – 189 89 – 173 71 – 145 64 — 149 |
21 – 38 19 – 37 18 – 35 18 – 35 17 – 33 16 – 33 15 – 29 14 – 23 13 – 23 12 – 22 12 — 23 |
1,95 – 3,63 0,81 – 3,39 0,65 – 1,90 0,59 – 1,84 0,77 – 2,15 1,10 – 3,10 1,43 – 3,17 1,75 – 3,50 1,80 – 3,10 1,70 – 3,10 1,50 – 2,80 |
|
|
Взрослые: до 60 лет старше 60 лет |
0,3 – 4,0 0,5 – 7,8 |
50 – 150 65 — 135 |
10 – 25 10 — 18 |
1,0 — 3,0 0,62 – 2,79 |
3,0 – 7,0 |
|
Беременные: 1 триместр 2 триместр 3 триместр |
0,3 – 4,5 0,5 – 4,6 0,8 – 5,2 |
79 — 227 |
9 – 26 6 – 21 6 — 21 |
1,79 – 3,80 |
3,2 – 5,9 3,0 — 5,2 3,0 – 5,2 |
ПРИМЕЧАНИЕ: Коэффициент пересчета ТТГ: 1 мкМЕ/мл = 1 мЕ/л.
Нормы могут изменяться при использовании различных стандартных коммерческих наборов.
КАК ПРАВИЛЬНО ПОДГОТОВИТЬСЯ К ИССЛЕДОВАНИЮ ФУНКИОНАЛЬНОЙ АКТИВНОСТИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ В КЛИНИКО – ДИАГНОСТИЧЕСКОЙ ЛАБОРАТОРИИ
1) Исследование производится утром натощак – между последним приемом пищи и взятием крови должно пройти не менее 8 – 12 часов. Вечером предшествующего дня рекомендуется необильный ужин. Желательно за 1 – 2 дня до обследования исключить из рациона жирное, жареное и алкоголь. Если накануне состоялось застолье или было посещение бани или сауны – необходимо перенести лабораторное исследование на 1-2 дня. За 1 час до взятия крови необходимо воздержаться от курения.
2) Не следует сдавать кровь после рентгенологических исследований, физиотерапевтических процедур.
3) Необходимо исключить факторы, влияющие на результаты исследований: физическое напряжение (бег, подъем по лестнице), эмоциональное возбуждение. Перед процедурой следует отдохнуть 10 – 15 минут и успокоиться.
4) Необходимо помнить, что результат исследования может быть искажен действием принимаемых лекарственных препаратов или продуктами их метаболизма. Назначение и отмена любого лекарственного препарата сопровождается изменением лабораторных показателей. Поэтому перед сдачей анализа следует проконсультироваться у врача о возможности ограничения приема лекарственных препаратов для подготовки к исследованию. Рекомендуется отказаться от приема лекарственных препаратов перед сдачей крови на исследование, то есть забор крови производится до приема лекарственных препаратов.
5) Учитывая суточные ритмы изменения показателей крови повторные исследования целесообразно проводить в одно и то же время.
6) В разных лабораториях могут применяться разные методы исследования и единицы измерения. Чтобы оценка результатов обследования была корректной и была приемлемость результатов, желательно проводить исследования в одной и той же лаборатории, в одно и то же время.
Исследование на тиреоидные гормоны. За 2 – 3 дня до проведения исследования исключается прием йодсодержащих препаратов, за 1 месяц – тиреоидных гормонов (чтобы получить истинные базальные уровни), если нет специальных указаний врача- эндокринолога. Однако, если целью исследования является контроль за дозой препаратов тиреоидных гормонов, забор крови производится на фоне приема обычной дозы. Следует иметь ввиду, что прием левотироксина вызывает транзиторное значимо повышенное содержание общего и свободного тироксина в крови примерно в течение 9 часов (на 15 – 20 %).
Исследование на тиреоглобулин целесообразно проводить спустя как минимум 6 недель после тиреоэктомии, либо проведенного лечения. Если назначены такие диагностические процедуры, как биопсия или сканирование ЩЖ, то исследование уровня ТГ в крови нужно строго проводить до процедур. Поскольку больные после радикального лечения дифференцированного рака ЩЖ получают высокие дозы тиреоидных гормонов (для подавления секреции ТТГ), на фоне которого также снижается уровень ТГ, его концентрацию следует определять через 2 – 3 недели после отмены супрессивной терапии тиреоидными гормонами.
ТИРЕОТРОПНЫЙ ГОРМОН (ТТГ, ТИРЕОТРОПИН)
ТТГ – опорный критерий лабораторной оценки функции ЩЖ. Именно с него следует начинать диагностику при подозрении на отклонения в гормональной активности ЩЖ. ТТГ – гликопротеидный гормон, который вырабатывается в передней доле гипофиза и стимулирующий синтез и йодирование тиреоглобулина, образование и секрецию тиреоидных гормонов. Гипофизарная секреция ТТГ очень чувствительна к изменениям концентрации Т3 и Т4 в сыворотке крови. Снижение или повышение этой концентрации на 15-20 % приводит к реципроктным сдвигам в секреции ТТГ (принцип обратной связи).
Существование зависимости образования и секреции ТТГ от действия лекарственных препаратов, суточного ритма изменения уровня ТТГ, состояния стресса и наличия у пациента соматических заболеваний должно учитываться при интерпретации результатов исследования.
Период биологической полужизни ТТГ – 15 — 20 минут.
ПОКАЗАНИЯ К ОПРЕДЕЛЕНИЮ ТТГ: диагностика нарушений функции ЩЖ, различные виды гипотиреоза, гипертиреоз, задержка умственного и полового развития у детей, сердечные аритмии, миопатия, депрессия, алопеция, бесплодие, аменорея, гиперпролактинемия, импотенция и снижение либидо.
-наблюдение за состоянием пациентов на фоне заместительной гормональной терапии: секреция ТТГ подавляется во время стандартной терапии или в течение послеоперационной заместительной терапии.
Нормальные или повышенные уровни ТТГ свидетельствуют о неадекватной дозе препарата, неверно проводимой гормональной терапии или наличии антител к антигенам ЩЖ. В ходе заместительной терапии при гипотиреозе оптимальный уровень ТТГ находиться в пределах нижних значений референтных величин. В ходе заместительной терапии кровь на исследование ТТГ необходимо забирать через 24 часа после последнего приема лекарственного препарата.
·скрининг врожденного гипотиреоза: На 5-е сутки жизни ребенка проводят определение уровня ТТГ в сыворотке крови или пятне крови на фильтровальной бумаге. Если уровень ТТГ превышает 20 мМЕ/л, необходимо провести повторный анализ нового образца крови. При концентрации ТТГ в диапазоне от 50 до 100 мМЕ/л существует высокая вероятность наличия заболевания. Концентрации выше 100 мМЕ/л являются типичным для врожденного гипотиреоза.
ФИЗИОЛОГИЧЕСКИЕ СОСТОЯНИЯ, ПРИВОДЯЩИЕ К ИЗМЕНЕНИЮ УРОВНЯ ТТГ В КРОВИ
У здоровых новорожденных при рождении отмечается резкий подъем уровня ТТГ в крови, снижающийся до базального уровня к концу первой недели жизни.
У женщин концентрация ТТГ в крови выше, чем у мужчин примерно на 20 %. С возрастом концентрация ТТГ незначительно повышается, уменьшается количество выбросов гормона в ночное время. У пожилых людей часто наблюдаются пониженные уровни ТТГ и в этих случаях необходимо принимать во внимание низкую чувствительность к стимуляции.
Концентрация ТТГ увеличивается во время беременности (оральные контрацептивы и менструальный цикл не влияют на динамику гормона)
Для ТТГ характерны суточные колебания секреции: наивысших величин ТТГ в крови достигает к 24 – 4 часам ночи, в утренние часы наибольший уровень в крови определяется в 6 – 8 часов. Минимальные значения ТТГ определяются в 15 – 18 часов вечера. Нормальный ритм секреции ТТГ секреции нарушается при бодрствовании ночью. На уровне ТТГ не сказывается интервал после приема левотироксина. Рекомендуется повторное проведение анализа, если полученные результаты не соответствуют клинической картине и параметрам других исследований.
У женщин среднего возраста и старых мужчин максимальный пик ТТГ в сыворотке крови приходиться на декабрь.
При климаксе может наблюдаться повышение содержания ТТГ при интактной ЩЖ.
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ ТТГ В КРОВИ
|
ПОВЫШЕНИЕ УРОВНЯ ТТГ |
СНИЖЕНИЕ УРОВНЯ ТТГ |
|
Гемодиализ. Гестоз (преэклампсия). Контакт со свинцом. Некомпенсированная первичная надпочечниковая недостаточность. Подострый тиреоидит (фаза выздоровления). После тяжелых физических нагрузок. Избыточная секреция ТТГ при аденомах гипофиза (тиротропинома): тиреотоксикоз центрального генеза. Прекращение курения. Секреция ТТГ аденомами гипофиза не всегда является автономной, а подвержена частичной регуляции по типу обратной связи. При назначении таким больным тиреостатических препаратов (метилтиоурацил, мерказолил и другие) и снижения у них под влиянием лечения уровня тиреоидных гормонов в крови наблюдается дальнейшее повышение содержания ТТГ в сыворотке крови. Первичный гипотиреоз. Синдром нерегулируемой секреции ТТГ. Синдром резистентности к тиреоидным гормонам. Тиреоидит Хашимото с клиническим и субклиническим гипотиреозом. Тяжелые соматические и психические заболевания. Упражнения на велоэргометре. Холецистэктомия. Эктопическая секреция ТТГ (опухоли легкого, молочной железы). Секрецию ТТГ стимулируют низкая температура и пониженное АД. |
Акромегалия. Вторичная аменорея. Гипертиреоз беременных и послеродовой некроз гипофиза. Гипофизарным нанизмом. Голодание. Диффузный и узловой токсический зоб. Замедленное половое развитие. Курение. Неврогенная анорексия. Общие заболевания в пожилом возрасте. Психологический стресс. Синдром Клайнфельтера. Синдром Кушинга. Субклинический тиротоксикоз. Т3-токсикоз. Тепловой стресс. Травма гипофиза. Транзиторный тиротоксикоз при аутоиммунном тиреоидите. ТТГ-независимый тиротоксикоз. Угнетающее действие СТГ на синтез и высвобождение ТТГ. Хроническая почечная недостаточность. Цирроз печени. Экзогенная терапия гормонами ЩЖ. Эндогенные депрессии. Эндокринная офтальмопатия.
|
КЛИНИКО-ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ ТТГ
· У пролеченных гипертиреоидных больных ТТГ может оставаться низким в течение 4-6 недель после достижения эутиреоидного состояния.
· У беременных и женщин, принимающих контрацептивы, нормальный уровень ТТТ и повышенные уровни Т3 и Т4 имеют место при эутиреозе.
· Отсутствие первичного заболевания ЩЖ можно констатировать у любого пациента, имеющего нормальный ТТГ и Т4 в сочетании с изолированным отклонением (в любую сторону) Т3.
· У тяжелых больных при нормальной концентрации Т4 и Т3 продукция ТТГ может нарушаться.
· Секреция ТТГ подавляется при лечении с применением тироксина и в постоперационной заместительной терапии. Нормальные или повышенные уровни ТТГ в этих случаях свидетельствуют о малой дозе препарата, периферической резистентности к тиреоидным гормонам или наличии антител к гормонам ЩЖ.
· В ходе заместительной терапии при гипотиреозе оптимальный уровень ТТГ должен находиться ниже значений референтных величин.
ОСНОВНЫЕ КРИТЕРИИ ДИФФЕРЕНЦИАЛЬНОГО ДИАГНОЗА СУБКЛИНИЧЕСКОГО ГИПОТИРЕОЗА
|
Основные состояния, сопровождающиеся подъемом уровня ТТГ |
|
* Вторичный и третичный гипотиреоз сопровождается в 25% случаев небольшим повышением уровня ТТГ со сниженной биологической активностью при значительном снижении Т4 . |
|
* При синдроме резистентности к тиреоидным гормонам выявляется незначительное увеличение уровня ТТГ при повышенном содержании тиреоидных гормонов в крови. |
|
* Некомпенсированная первичная надпочечниковая недостаточность иногда сопровождается повышением уровня ТТГ, который нормализуется при назначении глюкокортикостероидов. |
|
* При ТТГ- продуцирующей аденоме гипофиза определяется повышенный уровень ТТГ и тиреоидных гормонов. |
|
* Хроническая почечная недостаточность может сопровождаться повышением ТТГ как из-за задержки выведения йода (истинный гипотиреоз), так из-за применения препаратов, повышающих уровень ТТГ в крови и накопления метаболитов. |
|
* При обострении психических заболеваний у каждого четвертого пациента может быть транзиторное повышение уровня ТТГ, связанное с активацией гипоталамо-гипофизарно-тиреоидной системы. |
|
* Влияние антидофаминовых препаратов (метоклопрамида и сульпирида), амиодарона. |
|
* Синдром нетиреоидных заболеваний. |
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ОКАЗЫВАЮЩИЕ ВЛИЯНИЕ НА УРОВЕНЬ ТТГ В КРОВИ
|
ЗАВЫШЕНИЕ РЕЗУЛЬТАТА |
ЗАНИЖЕНИЕ РЕЗУЛЬТАТА |
|
АМИОДАРОН (ЭУТИРЕОИДНЫЕ И ГИПОТИРЕОИДНЫЕ БОЛЬНЫЕ) БЕТА-АДРЕНОБЛОКАТОРЫ (АТЕНОЛОЛ, МЕТОПРОЛОЛ, ПРОПРАНОЛОЛ) ГАЛОПЕРИДОЛ ЙОДИДЫ КАЛЬЦИТОНИН (МИАКАЛЬЦИК) КЛОМИФЕН ЛИТИЙ ЛОВАСТАТИН (МЕВАКОР) МЕТИМИЗОЛ (МЕРКАЗОЛИЛ) МОРФИЙ НЕЙРОЛЕПТИКИ (ФЕНОТИАЗИНЫ, АМИНОГЛЮТЕТИМИД) ПАРЛОДЕЛ (БРОМКРИПТИН) ПРЕДНИЗОН ПРОТИВОРВОТНЫЕ СРЕДСТВА (МОТИЛИУМ, МЕТОКЛОПРАМИД, ДОМПЕРИДОН) ПРОТИВОСУДОРОЖНЫЕ ПРЕПАРАТЫ (БЕНЗЕРАЗИД, ФЕНИТОИН, ВАЛЬПРОЕВАЯ КИСЛОТА) РЕНТГЕНОКОНТРАСТНЫЕ СРЕДСТВА РИФАМПИЦИН СУЛЬФАТ ЖЕЛЕЗА (ГЕМОФЕР, ФЕРРОГРАДУМЕНТ) СУЛЬПИРИД (ЭГЛОНИЛ) ФЛУНАРИЗИН ХЛОРПРОМАЗИН (АМИНАЗИН) ЭРИТРОЗИН
|
АМИОДАРОН (ГИПЕРТИРЕОИДНЫЕ БОЛЬНЫЕ) АНАБОЛИЧЕСКИЕ СТЕРОИДЫ АНТАГОНИСТЫ ДОФАМИНОВЫХ РЕЦЕПТОРОВ АСПИРИН БЕТА-АДРЕНОМИМЕТИКИ (ДОБУТАМИН, ДОПЕКСАМИН) ВЕРАПАМИЛ (ИЗОПТИН, ФИНОПТИН) ГЕПАРИН ДИНАЗОЛ ДОПАМИН ИНТЕРФЕРОН-2 КАРБАМАЗЕПИН (ФИНЛЕПСИН, ТЕГРЕТОЛ) КАРБОНАТ ЛИТИЯ (СЕДАЛИТ) КЛОФИБРАТ (МИСКЛЕРОН) КОРТИЗОЛ (УГНЕТАЕТ СЕКРЕЦИЮ ТТГ) КОРТИКОСТЕРОИДЫ ЛЕВОДОПА (ДОПАКИН, НАКОМ, МАДОПАР) ЛЕВОТИРОКСИН (ЭУТИРОКС) МЕТЭРГОЛИН НИФЕДИПИН (АДАЛАТ, КОРДИПИН, КОРИНФАР) ОКТРЕОТИД (САНДОСТАТИН) ПИРИДОКСИН (ВИТАМИН В6) СОМАТОСТАТИН СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ГИПЕРПРОЛАКТИНЕМИИ (ПЕРИБЕДИЛ, ТРИЙОДТИРОНИН ФЕНТОЛАМИН ЦИМЕТИДИН (ГИСТОДИЛ) ЦИПРОГЕПТАДИН (ПЕРИТОЛ) ЦИТОСТАТИК |
ТИРОКСИН ( Т4 )
Тироксин – тиреоидный гормон, биосинтез которого происходит в фолликулярных клетках ЩЖ под контролем ТТГ. Основная фракция органического йода в крови находится в форме Т4. Около 70 % Т4 связано с тироксинсвязывающим глобулином (ТС), 20 % — с тироксинсвязывающим преальбумином (ТСПА) и 10 % — с альбумином. Только 0,02 – 0,05 % Т4 циркулирует в крови в несвязанном с белками состоянии — свободная фракция Т4. Концентрация Т4 в сыворотке зависит не только от скорости секреции, но и от изменения связывающей способности белков. Свободный Т4 составляет 0,02 – 0,04 % общего тироксина.
Период биологической полужизни Т4 – 6 суток.
ФИЗИОЛОГИЧЕСКИЕ СОСТОЯНИЯ, ПРИВОДЯЩИЕ К ИЗМЕНЕНИЮ УРОВНЯ Т4 В КРОВИ
У здоровых новорожденных концентрация свободного и общего Т4 выше, чем у взрослых.
Уровень гормона у мужчин и женщин остается относительно постоянным в течение всей жизни, снижаясь только после 40 лет.
Во время беременности концентрация тироксина нарастает, достигая максимальных величин в 3 триместре.
В течение дня максимальная концентрация тироксина определяется с 8 до 12 часов, минимальная – с 23 до 3 часов. В течение года максимальные величины Т4 наблюдаются в период между сентябрем и февралем, минимальные в летнее время.
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ Т4 В КРОВИ
Гемолиз, многократное оттаивание и замораживание сыворотки могут привести к снижению результатов Т4. Высокие концентрации билирубина в сыворотке способствуют завышению результатов. Наличие консерванта ЭДТА дает ложнозавышенные результаты для свободного Т4. Голодание, плохое питание с низким содержанием белка, контакт со свинцом, тяжелые мышечные упражнения и тренировки, чрезмерное физическое усилие, различные виды стрессов, потери веса у женщин при ожирении, хирургические операции, гемодиализ могут способствовать снижению показателей общего и свободного Т4. Гиперемия, ожирение, прерывание приема героина (вследствие увеличения транспортных белков) вызывают увеличение Т4, героин снижает свободный Т4 в сыворотке крови. Курение вызывает как снижение, так и завышение результатов исследования на тироксин. Наложение жгута при взятии крови с работой и без «работы рукой» вызывает увеличение общего и свободного Т4.
Уровни Т4 в крови из пупочной вены ниже у недоношенных младенцев по сравнению с доношенными и положительно коррелируют с весом при рождении доношенных детей. Высокие величины Т4 у новорожденных вызваны повышенным ТСГ, свободный Т4 близок к уровню у взрослых. Величины резко повышаются в первые часы после рождения и постепенно снижаются к 5 годам. У мужчин происходит снижение в период полового созревания, у женщин этого не наблюдается.
Концентрация свободного Т4, как правило, остается в пределах нормы при тяжелых заболеваниях, не связанных со ЩЖ (концентрация общего Т4 может быть пониженной).
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ ОБЩЕГО Т4
|
ПОВЫШЕНИЕ УРОВНЯ ОБЩЕГО Т4 |
СНИЖЕНИЕ УРОВНЯ ОБЩЕГО Т4 |
|
ВИЧ – инфекция. Острый гепатит (4 недели) и подострый гепатит. Гипертиреоидизм, состояния с повышением ТСГ (беременность, генетическое повышение, острая перемежающая порфирия, первичный билиарный цирроз). Гиперэстрогения (повышение содержания общего Т4 за счет увеличения ТСГ, при этом уровень свободного Т4 остается нормальным). Диффузный токсический зоб. Ожирение. Острые психические расстройства. Острый тиреоидит (отдельные случаи). Послеродовая дисфункция ЩЖ. Синдром резистентности к тиреоидным гормонам. Тиреотропинома. Токсическая аденома. Тиреоидиты. ТТГ – независимый тиреотоксикоз. Хориокарцинома |
Вторичный гипотиреоз (синдром Шихана, воспалительные процессы в области гипофиза). Гипотиреоидизм, состояния со снижением ТСГ (нефротический синдром, хронические заболевания печени, потеря белка через ЖКТ, нарушения питания, генетическое снижение ТСГ). Пангипопитуитаризм. Первичный гипотиреоз (врожденный и приобретенный: эндемический зоб, АИТ, неопластические процессы в ЩЖ). Третичный гипотиреоз (черепно-мозговые травмы, воспалительные процессы в области гипоталамуса).
|
КЛИНИКО-ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ Т4
· изолированное повышение общего Т4 на фоне нормальных значений ТТГ и Т3 может быть редкой находкой. Это, по-видимому, пациент с нормальной тиреоидной функцией, но врожденной избыточной печеночной продукцией белков-переносчиков тиреоидных гормонов.
· при «изолированном» Т3-гипертиреозе уровень свободного и общего Т4 – в пределах нормы.
· на начальной стадии гипотиреоза уровень свободного Т3 понижается раньше, чем общий Т4. Диагноз подтверждается в случае повышения ТТГ или чрезмерного ответа на ТРГ-стимуляцию.
· нормальный уровень Т4 не является гарантией нормальной тиреоидной функции. Т4 в пределах нормы может быть при эндемическом зобе, супрессивной или заместительной терапии, при скрытой форме гипертиреоза или скрытой форме гипотиреоза.
· при гипотиреозе тироксин способствует нормализации ТТГ и Т4.Повышенные концентрации общего и свободного Т4 и концентрация ТТГ в районе нижнего предела нормы наблюдается при подборе адекватной заместительной терапии.
· во время тиреостатической терапии уровень Т4 в районе верхнего предела нормы свидетельствует об адекватном выборе поддерживающей дозы.
· повышенный уровень свободного Т4 не всегда свидетельствует о нарушении функции ЩЖ. Это может быть следствием приема некоторых лекарственных препаратов или тяжелых общих заболеваний.
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ОКАЗЫВАЮЩИЕ ВЛИЯНИЕ НА УРОВЕНЬ ОБЩЕГО Т4 В КРОВИ
|
ЗАВЫШЕНИЕ РЕЗУЛЬТАТА |
ЗАНИЖЕНИЕ РЕЗУЛЬТАТА |
|
АМИОДАРОН (В НАЧАЛЕ ЛЕЧЕНИЯ И ПРИ ДЛИТЕЛЬНОМ ЛЕЧЕНИИ) АМФЕТАМИНЫ ГЕРОИН ДЕКСТРО-ТИРОКСИН ДИНОПРОСТ ТРОМЕТАИН ИНСУЛИН ЛЕВАТЕРЕНОЛ ЛЕВОДОПА (ДОПАКИН, НАКОМ, МАДОПАР, СИНЕМЕТ) ОПИАТЫ (МЕТАДОН) ПЕРОРАЛЬНЫЕ КОНТРАЦЕПТИВЫ ПРЕПАРАТЫ ГОРМОНОВ ЩЖ ПРОПИЛТИОУРАЦИЛ ПРОПРАНОЛОЛ (АНАПРИЛИН) ПРОСТАГЛАНДИН РЕНГЕНОКОНТРАСТНЫЕ ЙОДСОДЕРЖАЩИЕ ПРЕПАРАТЫ (ИОПАНОЕВАЯ КИСЛОТА, ИПОДАТ, ТИРОПАНОЕВАЯ КИСЛОТА) ТАМОКСИФЕН ТИРЕОЛИБЕРИН ТИРЕОТРОПИН ФЕНОТИАЗИН ФЛУОРОУРАЦИЛ (ФТОРФЕНАЗИН) ХОЛЕЦИСТОГРАФИЧЕСКИЕ В-ВА ЭСТРОГЕНЫ СИНТЕТИЧЕСКИЕ (МЕСТРАНОЛ, СТИЛЬБЕСТРОЛ) ЭФИР (ПРИ ГЛУБОКОМ НАРКОЗЕ) |
АМИНОГЛЮТЕМИД (СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ) АМИОДАРОН (КОРДАРОН) АНДРОГЕНЫ (СТАНОЗОЛОЛ, НАНДРОНОЛОЛ), ТЕСТОСТЕРОНОН АНТИКОНВУЛЬСАНТЫ (ВАЛЬПРОЕВАЯ КИСЛОТА, ФЕНИТОИН, ФЕНОБАРБИТАЛ, КАРБАМАЗЕПИН) АСПАРАГИНАЗА АСПИРИН АТЕНОЛОЛ БАРБИТУРАТЫ ГИПОЛИПИДЕМИЧЕСКИЕ СРЕДСТВА (ЛОВАСТАТИН, КЛОФИБРАТ, ХОЛЕСТИРАМИН) ДАНАЗОЛ ДИАЗЕПАМ (ВАЛИУМ, РЕЛАНИУМ, СИБАЗОН) ИЗОТРЕТИОНИН (РОАККУТАН) КОРТИЗОЛ КОРТИКОСТЕРОИДЫ (КОРТИЗОН, ДЕКСАМЕТАЗОН) КОРТИКОТРОПИН ЛИТИЙ МЕТАМИЗОЛ (АНАЛЬГИН) НПВС (ДИКЛОФЕНАК, ФЕНИЛБУТАЗОН) ОКСИФЕНБУТАЗОН (ТАНДЕРИЛ) ПЕНИЦИЛЛИН ПРЕПАРАТЫ СУЛЬФОНИЛМОЧЕВИНЫ (ГЛИБЕНКЛАМИД, ДИАБЕТОН, ТОЛБУТАМИД, ХЛОРПРОПАМИД) ПРОТИВОГРИБКОВЫЕ ПРЕПАРАТЫ (ИНТРАКОНАЗОЛ, КЕТОКОНАЗОЛ) ПРОТИВОТУБЕРКУЛЕЗНЫЕ СРЕДСТВА (АМИНОСАЛИЦИЛОВАЯ КИСЛОТА, ЭТИОНАМИД) РЕЗЕРПИН РИФАМПИН СОМАТОТРОПИН СУЛЬФАНИЛАМИДЫ (КО-ТРИМОКСАЗОЛ) ТРИЙОДТИРОНИН ФУРОСЕМИД (ПРИЕМ В БОЛЬШИХ ДОЗАХ) ЦИТОСТАТИКИ |
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ОКАЗЫВАЮЩИЕ ВЛИЯНИЕ НА УРОВЕНЬ СВОБОДНОГО Т4
|
ЗАВЫШЕНИЕ РЕЗУЛЬТАТА |
ЗАНИЖЕНИЕ РЕЗУЛЬТАТА |
|
АМИОДАРОН АСПИРИН ВАЛЬПРОЕВАЯ КИСЛОТА ГЕПАРИН ДАНАЗОЛ ДИФЛЮНИСАЛ ИОПАНОЕВАЯ КИСЛОТА ЛЕВОТИРОКСИН МЕКЛОФЕНАМИНОВАЯ КИСЛОТА ПРОПИЛТИОУРАЦИЛ ПРОПРАНОЛОЛ РАДИОГРАФИЧЕСКИЕ ПРЕПАРАТЫ |
АНТИКОНВУЛЬСАНТЫ (ФЕНИТОИН, КАРБАМАЗЕПИН) – ПРИ ДЛИТЕЛЬНОМ ЛЕЧЕНИИ И БЕРЕМЕННЫХ ЖЕНЩИН С ЭПИЛЕПСИЕЙ МЕТАДОН |
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ СВОБОДНОГО Т4
|
ПОВЫШЕНИЕ УРОВНЯ СВОБОДНОГО Т4 |
СНИЖЕНИЕ УРОВНЯ СВОБОДНОГО Т4 |
|
Гипертиреоидизм. Гипотиреодизм, леченный тироксином. Заболевания, связанные с повышением свободных жирных кислот. Послеродовая дисфункция ЩЖ. Синдром резистентности к тиреоидным гормонам. Состояния, при которых снижается уровень или связывающая способность ТСГ. Тиреоидиты. Тиреотоксическая аденома. Токсический зоб. ТТГ-независимый тиреотоксикоз. Хронические заболевания печени.
|
Вторичный гипотиреоз (синдром Шихана, воспалительные заболевания в области гипофиза, тиреотропинома). Диета с низким содержанием белка и значительная недостача йода. Колебания уровней свободного Т4 могут наблюдаться у эутиреоидных пациентов при острых или хронических нетиреоидных болезнях Контакт со свинцом. Первичный гипотиреоз, не леченный тироксином (врожденный и приобретенный: эндемический зоб, АИТ, новообразования в ЩЖ, обширная резекция ЩЖ). Поздняя беременность. Резкое снижение массы тела у женщин с ожирением. Третичный гипотиреоз (ЧМТ, воспалительные процессы в области гипоталамуса). Хирургические вмешательства. |
ТРИЙОДТИРОНИН ( Т3 )
Трийодтиронин – тиреоидный гормон, на 58% состоящий из йода. Часть сывороточного Т3 образуется путем ферментативного дейодирования Т4 в периферических тканях, и только небольшое количество образуется прямым синтезом в ЩЖ.. Менее, чем 0,5 % Т3, циркулирующего в сыворотке, находится в свободной форме и биологически активна. Оставшийся Т3 находится в обратимой связи с сывороточными белками: ТСГ, ТСПА и альбумином. Афинность Т3 к сывороточным белкам в 10 раз ниже, чем Т4. В связи с этим уровень свободного Т3 не имеет такого большого диагностического значения, как уровень свободного Т4. По меньшей мере 80 % циркулирующего Т3 получено в результате монодейодизации Т4в периферических тканях. Т3 в 4 – 5 раз более активен в биологических системах, чем Т4. Хотя минимальные сывороточные концентрации Т3 в 100 раз ниже, чем концентрация Т4, большинство иммуноанализов имеют незначительную перекрестную реактивность с Т4. Так как уровни Т3 быстро меняются под влиянием стресса или других нетиреоидных факторов, измерение Т3 не является лучшим общим тестом определения тиреоидного статуса. Свободный Т3 составляет около 0,2 – 0,5 % общего Т3.
Период биологической полужизни Т3 составляет — 24 часа.
ПОКАЗАНИЯ К ОПРЕДЕЛЕНИЮ Т3
· дифференциальная диагностика заболеваний ЩЖ,
· контрольное исследование при изолированном Т3-токсикозе,
· начальная стадия гиперфункции ЩЖ, в частности автономных клеток,
· острый гипертиреоз после подавляющей терапии тироксином,
· рецидив гипертиреоза.
· для исключения передозировки лекарственных препаратов необходимо проводить контроль уровня Т3, который должен находиться в пределах нормы.
ФИЗИОЛОГИЧЕСКИЕ СОСТОЯНИЯ, ПРИВОДЯЩИЕ К ИЗМЕНЕНИЮ УРОВНЯ Т3 В КРОВИ
Концентрация Т3 в сыворотке крови новорожденных составляет 1/3 от его уровня, наблюдаемого у взрослых, но уже в течение 1 – 2 суток увеличивается до концентрации, выявляемой у взрослых. В раннем детском возрасте концентрация Т3 несколько уменьшается, а в подростковом возрасте (к 11 – 15 годам) вновь достигает уровня взрослого человека. После 65 лет наблюдается более значительное снижение уровня Т3 по сравнению с Т4. У женщин отмечаются более низкие концентрации Т3 , чем у мужчин, в среднем на 5 – 10 %.
Во время беременности (особенно в 3 триместре) концентрация Т3 в крови возрастает в 1,5 раза. После родов уровень гормона нормализуется в течение 1 недели.
Для показателей Т3 характерны сезонные колебания: максимальный уровень приходится на период с сентября по февраль, минимальный – на летний период.
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ Т3 В КРОВИ
|
ПОВЫШЕНИЕ РЕЗУЛЬТАТА |
СНИЖЕНИЕ РЕЗУЛЬТАТА |
|
Большая высота над уровнем моря. Героинмания. Нарастание веса тела. Прерывание приема героина. При дефиците йода происходит компенсаторное повышение уровней общего и свободного Т3. При наложении жгута с целью взятия крови на 3 мин. без «работы рукой» возможно увеличение Т3 примерно на 10 %. Физические упражнения. |
Гемодиализ. Гипертермия. Голодание. Недоношенные новорожденные. Низкокалорийная диета. Острые заболевания. Плазмоферез. Плохое питание с низким содержанием белков. После абортов. Потеря веса. Тяжелые соматические заболевания. Тяжелые физические нагрузки у женщин. Электроконвульсивная терапия. |
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ ОБЩЕГО Т3
|
ПОВЫШЕНИЕ РЕЗУЛЬТАТА |
СНИЖЕНИЕ РЕЗУЛЬТАТА |
|
Гипертиреоз. Йоддефицитный зоб. Леченный гипертиреоидизм. Начальная нетиреоидная недостаточность. Состояния с повышенным ТСГ. Т3-тиреотоксикоз.
|
Гипотиреоз (при раннем или легком первичном гипотиреоидизме Т4 снижается больше, чем Т3 – высокое соотношение Т3/Т4). Некомпенсированная первичная надпочечниковая недостаточность. Острые и подострые нетиреоидные заболевания. Первичный, вторичный и третичный гипотиреоз. Период выздоровления после тяжелых заболеваний. Синдром эутиреоидного больного. Состояния с пониженным ТСГ. Тяжелая нетиреоидная патология, включая соматические и психические заболевания. Хронические заболевания печени. |
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ОКАЗЫВАЮЩИЕ ВЛИЯНИЕ НА УРОВЕНЬ ОБЩЕГО Т3
|
ЗАВЫШЕНИЕ РЕЗУЛЬТАТА |
ЗАНИЖЕНИЕ РЕЗУЛЬТАТА |
|
АМИОДАРОН (КОРДАРОН) АНДРОГЕНЫ АСПАРАГИНАЗА ГЕРОИН ДЕКСТРОТИРОКСИН ДИНОПРОСТ ТРОМЕТАИН (ЭНЗАПРОСТ) ИЗОТРЕТИОНИН (РОАККУТАН) ЙОДИДЫ ЛИТИЙ МЕТАДОН (ДОЛОФИН, ФИСЕПТОН) ПЕРОРАЛЬНЫЕ КОНТРАЦЕПТИВЫ ПРОПИЛТИОУРАЦИЛ ПРОПРАНОЛОЛ (АНАПРИЛИН) ПРОТИВОСУДОРОЖНЫЕ СРЕДСТВА САЛИЦИЛАТЫ ТЕРБУТАЛИН ХОЛЕЦИСТОГРАФИЧЕСКИЕ В – ВА ЦИМЕТИДИН (ГИСТОДИЛ) ЭСТРОГЕНЫ |
ДЕКСАМЕТАЗОН (СЫВОРОТОЧНАЯ КОНЦЕНТРАЦИЯ МОЖЕТ УМЕНЬШАТЬСЯ НА 20 – 40 %) |
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ СВОБОДНОГО Т3
|
ПОВЫШЕНИЕ УРОВНЯ СВОБОДНОГО Т3 |
СНИЖЕНИЕ УРОВНЯ СВОБОДНОГО Т3 |
|
Гипертиреоидизм. Т3-токсикоз. Синдром периферического сопротивления сосудов. |
Гипотиреоидизм. Третий триместр беременности. При нетиреоидных заболеваниях низкий уровень свободного Т3 является неспецифической находкой. |
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ОКАЗЫВАЮЩИЕ ВЛИЯНИЕ НА УРОВЕНЬ СВОБОДНОГО Т3
|
ЗАВЫШЕНИЕ РЕЗУЛЬТАТА |
ЗАНИЖЕНИЕ РЕЗУЛЬТАТА |
|
ДЕКСТРОТИРОКСИН ФЕНОПРОФЕН (НАЛФОН) |
АМИОДАРОН (КОРДАРОН) ВАЛЬПРОЕВАЯ КИСЛОТА (КОНВУЛЕКС, ЭНКОРАТ, ДЕПАКИН) НЕОМИЦИН (КОЛИМИЦИН) НИАЦИН ПРАЗОЗИН ПРОБУКОЛ ПРОПРАНОЛОЛ (АНАПРИЛИН, ОБЗИДАН) ТИРОКСИН ФЕНИТОИН (ДИФЕНИН) ХОЛЕЦИСТОГРАФИЧЕСКИЕ ПРЕПАРАТЫ (ИОПАНОЕВАЯ КИСЛОТА, ИПОДАТ) |
КЛИНИКО-ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ Т3
· при дефиците йода наблюдается компенсаторное повышение общего и свободного Т3. Таким образом, организм приспосабливается к недостатку «сырья». Обеспечение достаточным количеством йода влечет за собой нормализацию Т3. Никакого лечения эти лица не требуют. Неверная трактовка повышенного уровня Т3 как Т3-токсикоза, невзирая на нормальный ТТГ и иногда даже сниженный Т4, может привести к необоснованному назначения тиреостатиков, что является грубой ошибкой.
· при гипотиреозе уровни общего и свободного Т3 могут длительное время находиться в районе нижнего предела нормы, так как повышенное периферическое превращение Т4 в Т3 компенсирует снижение Т3 .
· нормальный уровень Т3 может быть при скрытых функциональных дефектах тиреоидной функции, при гипотиреозе, компенсированном превращении Т4 в Т3.
· во время лечения зоба или послеоперационной заместительной терапии тироксином уровни ТТГ и Т3 измеряют для предупреждения дозировки.
· при лечении гипотиреоза тироксином повышение Т3 значительно меньше по сравнению с Т4. При введении больших доз тироксина ТТГ подавляется до нерегистрируемых значений. Для исключения передозировки лекарственных препаратов проводят анализ уровня Т3, который должен находиться в пределах нормы.
· в начале курса тиреостатической терапии уровень Т3 может возрастать в результате процессов компенсации.
· определение уровня Т3 в сыворотке имеет низкую чувствительность и специфичность при гипотиреозе, так как активизация конверсии Т4 в Т3 поддерживает уровень Т3 в пределах нормы до развития тяжелого гипотиреоза. Пациенты с НТЗ или в состоянии энергетического голода имеют низкие показатели с Т3 и о Т3. Уровень Т3 следует определять в сочетании с свободным Т4 при диагностике сложных и необычных проявлений гипертиреоза или некоторых редких состояний. Высокий уровень Т3 является частым и ранним признаком рецидива болезни Грейвса. Высокий или нормальный уровень Т3 встречается при гипертиреозе у пациентов с НТЗ на фоне снижения содержания ТТГ (менее 0,01 мМЕ/л). Высокий или нормальный уровень Т3 встречается при кордарониндуцированном гипертиреозе.
АЛГОРИТМ ЛАБОРАТОРНОЙ ОЦЕНКИ ФУНКЦИИ
ЩИТОВИДНОЙ ЖЕЛЕЗЫ
|
ТТГ повышен, свободный Т4 повышен или в норме, свободный Т3 понижен или в норме.
|
* Прием амиодарона, йодсодержащих рентгеноконтрастных средств, больших доз пропранолола. * Тяжелая нетиреоидная патология, включая соматические и психические заболевания. * Некомпенсированная первичная надпочечниковая недостаточность. * Период выздоровления. |
|
ТТГ повышен, свободный Т4 повышен или в норме, клинический эутиреоз. |
* Тотальная резистентность к тиреоидным гормонам.
|
|
ТТГ повышен, свободный Т4 в норме
|
* Недавно проведенная коррекция гормонами ЩЖ. * Недостаточная терапия гормонами ЩЖ., пациенты не предъявляют жалоб. |
|
ТТГ понижен, свободный Т4 повышен, свободный Т3 понижен. |
* Артифициальный тиреотоксикоз вследствие самоназначения Т4. |
|
ТТГ понижен, свободный Т4 в норме. |
* Избыточная терапия гормонами ЩЖ. * Прием препаратов, содержащих Т3. |
|
ТТГ в норме, свободный Т4 и Т3 понижены. |
* Прием больших доз салицилатов.
|
|
ТТГ повышен, свободный Т4 повышен, клинический тиреотоксикоз. |
* ТТГ – секретирующие опухоли. |
|
ТТГ в норме, повышение уровня общего Т4 при нормальном уровне св. Т4. |
* Семейная дисальбуминемическая гипертироксинемия.
|
|
ТТГ повышен, свободный и общий Т4 снижены, общий и свободный Т3 снижены. |
* Хронические заболевания печени: хронический гепатит, цирроз печени. |
|
Аномальные концентрации общегоТ4 и общегоТ3 |
* Чаще всего являются результатом нарушений со стороны связывающего белка, а не результатом тиреоидной дисфункции. При изменении уровня ТСГ расчетные показатели свободногоТ4 более надежны, чем содержание общегоТ4. При расхождении показателей свободных гормонов следует определить общийТ4 и общийТ3. |
ИСТОЧНИКИ И МЕХАНИЗМЫ ДЕЙСТВИЯ ОРГАНИЧЕСКИХ
КОНТРТИРЕОИДНЫХ СРЕДСТВ
|
Химическое название |
Источники |
Механизм действия |
|
Тиоцианаты и изотиоцианаты |
Растения семейства крестоцветных, курение |
Ингибирование йодконцентрирующих механизмов |
|
Гойтрин |
Желтая репа |
Препятствие органификации йодида и образованию активных тиреоидных гормонов в ЩЖ (активность гойтрина составляет 133% активности пропилтиоурацила). |
|
Цианогенные гликозиды |
Маниок, маис, сладкий картофель, побеги бамбука |
Превращаются в организме в изотиоцианаты |
|
Дисульфиды |
Лук, чеснок |
Тиомочевиноподобное антитиреоидное действие |
|
Флавоноиды |
Просо, сорго, бобы, земляные орехи |
Ингибирование ТПО и дейодиназ йодтиронинов – торможение периферического метаболизма тиреоидных гормонов. |
|
Фенолы (резорцин) |
Питьевая вода, угольная пыль, сигаретный дым |
Торможение органификации йода в ЩЖ и ингибирование ТПО |
|
Полициклические ароматические углеводороды |
Пищевые продукты, питьевая вода, грунтовые воды |
Ускорение метаболизма Т4 за счет активации печеночной УДФ-глюкуронилтрансферазы и образования глюкуронида Т4 |
|
Эфиры фталевой кислоты |
Изделия из пластмассы, некоторые виды рыб |
Ингибирование ТПО и включения йода в тиреоидные гормоны |
|
Полихлорированные и полибромированные бифенилы |
Пресноводная рыба |
Развитие АИТ |
|
ДДТ |
Питьевая вода, продукты питания |
Гиперплазия фолликулярного эпителия, ускорение метаболизма тиреоидных гормонов, повышение активности микросомальных ферментов |
|
Высокий уровень или дефицит лития, селена |
|
Могут блокировать протеолиз коллоида и выход ТГ из фолликулов, поступление йода в ЩЖ, связь тиреоидных гормонов с белками сыворотки, ускорять процесс их дейодирования. |
ВИДЫ СИНДРОМА НЕТИРЕОИДНЫХ ЗАБОЛЕВАНИЙ,
ИХ ЗНАЧЕНИЕ И МЕХАНИЗМЫ РАЗВИТИЯ
|
Варианты синдрома нетиреоидных заболеваний (СНТЗ) |
|
Низкий уровень Т3 |
|
Снижение уровня Т3 наблюдается у 70% пациентов стационаров при системных заболеваниях при нормальной функции ЩЖ. Общий Т3 ниже нормы на 60%, свободный Т3 – на 40%.Уровень Т4 – нормальный. Вариант СНТЗ связан с нарушением превращения Т4 в Т3вследствие снижения активности 5-монодейодиназы. Данное состояние также характерно для голодания и представляет собой адаптивную реакцию организма, связанную со снижением основного обмена. |
|
Низкий уровень Т3 и Т4 |
|
Одновременное снижение уровня Т3 и Т4 часто встречается у пациентов палат интенсивной терапии. При этом низкий уровень общего Т4 – неблагоприятный прогностический признак. Данный вариант СНТЗ связан с присутствием в крови ингибитора связывания тиреоидных гормонов и увеличением метаболического клиренса Т4. |
|
Высокий уровень Т4 |
|
Повышение уровня сывороточного Т4 и реверсивного Т3 наблюдается при острой порфирии, хроническом гепатите, первичном билиарном циррозе. При этом уровень общего Т3 и свободного Т4 – в пределах нормы, уровень свободного Т3 – на нижней границе нормы или снижен. |
ЛЕКАРСТВЕННЫЕ ВЗАИМОДЕЙСТВИЯ, ВЛИЯЮЩИЕ
НА ЭФФЕКТИВНОСТЬ ТЕРАПИИ ТИРОКСИНОМ
|
МЕХАНИЗМ ВЗАИМОДЕЙСТВИЯ |
ЛЕКАРСТВЕННОЕ ВЕЩЕСТВО |
|
|
Одновременное использование может потребовать увеличение дозы L-тироксина |
||
|
Лекарственные средства, блокирующие рецепторы, как истинных катехоламинов, так и образующихся из тироксина псевдомедиаторов. |
Пропранолол (анаприлин, обзидан) |
|
|
Лекарственные средства, снижающие абсорбцию L-тироксина. |
Холестирамин (квестран) Гидроокись алюминия Сульфат железа (гемофер) Сукральфат (вентер) Колестипол Карбонат кальция |
|
|
Лекарственные средства, ускоряющие метаболизм Л-тироксина в печени |
Фенобарбитал Фенитоин (дифенин) Карбамазепин (финлепсин) Рифампицин |
|
|
Одновременное использование может потребовать уменьшение дозы L-тироксина |
||
|
Лекарственные средства, уменьшающие уровень тироксинсвязывающего глобулина в сыворотке крови |
Андрогены Анаболические стероиды Глюкокортикостероиды |
|
КЛИНИЧЕСКИЕ СИТУАЦИИ, ИЗМЕНЯЮЩИЕ
ПОТРЕБНОСТЬ В ТИРОКСИНЕ
|
ПОВЫШЕНИЕ ПОТРЕБНОСТИ В ТИРОКСИНЕ |
|
* Снижение абсорбции Т4 в кишечнике: заболевания слизистой тонкого кишечника (спру и т.п.), поносы при диабете, цирроз печени, после операции еюно-еюнального шунтирования или резекции тонкой кишки, беременность. * Препараты, увеличивающие выведение неметаболизированного Т4: рифампицин, карбамазепин, фенитоин. * Прием препаратов, снижающих абсорбцию тироксина: холестирамин, гидроокись алюминия, сульфат железа, карбонат кальция, сукральфат, колестипол. * Препараты, блокирующие конверсию Т4 в Т3: амиодарон (кордарон), дефицит селена. |
|
СНИЖЕНИЕ ПОТРЕБНОСТИ В ТИРОКСИНЕ |
|
* Старение (возраст более 65 лет). * Ожирение. |
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ВЛИЯЮЩИЕ НА
ФУНКЦИЮ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
|
ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ |
ВЛИЯНИЕ НА ЩИТОВИДНУЮ ЖЕЛЕЗУ |
|
Йодсодержащие препараты и рентгеноконтрастные вещества |
Индуцирование гипотиреоза за счет ингибирования синтеза и секреции гормонов ЩЖ – снижение уровня Т4 и повышение содержания ТТГ. Снижение скорости образования Т3 из Т4. (Иногда препараты, содержащие йод, могут вызывать феномен «йод-Базедов») |
|
Препараты лития |
Подавляют секрецию Т4 и Т3 и снижают превращение Т4 в Т3, подавляют протеолиз тиреоглобулина. |
|
Сульфаниламиды (в том числе препараты, используемые для лечения СД) |
Оказывают слабое супрессивное влияние на ЩЖ, тормозят синтез и секрецию тиреоидных гормонов (оказывают структурные и функциональные нарушения ЩЖ). |
|
Дофамин |
Подавляет секрецию ТТГ. |
|
Тестостерон, метилтестостерон, нандролон |
Уменьшение содержания в сыворотке ТСГ и концентрации общего Т4 и стимулирование синтеза ТТГ. |
|
Фенитоин, Фенобарбитал, Карбамазепин
|
Усиливают катаболизм Т4 ферментными системами печени (при длительном применении требуется контроль функции щитовидной железы). При длительном лечении фенитоином уровень свободного Т4 и ТТГ могут оказаться аналогичными таковым при вторичном гипотиреозе. |
|
Оральные контрацептивы |
Могут вызвать значительное повышение общего Т4, но не свободного Т4. |
|
Салицилаты |
Блокируют захват йода ЩЖ, повышают свободный Т4 за счет снижения связывания Т4 с ТСГ. |
|
Бутадион |
Влияет на синтез гормонов ЩЖ, снижая уровень общего и свободного Т4. |
|
Глюкокортикоиды (при кратковременном приеме в больших дозах и при длительной терапии в средних дозах) |
Снижают превращение Т4 в Т3 за счет увеличения конценрации неактивного реверсивного Т3, ингибируют секрецию тиреоидных гормонов и ТТГ и уменьшают его выделение на ТРГ. |
|
Бета-блокаторы |
Замедляют конверсию Т4 в Т3 и понижают уровень Т3. |
|
Фуросемид (в больших дозах) |
Вызывает падение общего и свободного Т4 с последующим повышением ТТГ. |
|
Гепарин |
Подавляет поглощение Т4 клетками. При проведении гепаринотерапии может быть выявлен неадекватно высокий уровень свободного Т4. |
|
Амиодарон |
Эффекты разнонаправленные, в зависимости от исходного обеспечения йодом и состояния ЩЖ. * Амиодарониндуцированный гипотиреоз наиболее часто наблюдается в йоддостаточных регионах. Патогенез: Амиодарон ингибируя ТТГ-зависимую продукцию цАМФ, снижает синтез тиреоидных гормонов и йодный метаболизм; ингибирует 5-дейодиназу – селенопротеина, обеспечивающего превращение Т4 в Т3 и реверсионный Т3, что приводит к снижению экстра- и интратиреоидного содержания Т3. * Амиодарониндуцированный тиреотоксикоз наиболее часто встречается в йоддефицитных или районах умеренного йодного дефицита. Патогенез: йод, высвобождаемый из амиодарона, приводит к повышению синтеза тиреоидных гормонов в существующих зонах автономии в ЩЖ. Также возможно развитие деструктивных процессов в ЩЖ, причиной которых стало действие самого амиодарона.
|
ПАЦИЕНТЫ, ПРИНИМАЮЩИЕ АМИОДАРОН (КОРДАРОН)
До лечения необходимо исследование базального уровня ТТГ и анти-ТПО. Содержание свободногоТ4 и свободногоТ3 проверяют, если изменен уровень ТТГ. Повышение уровня анти-ТПО является фактором риска тиреоидной дисфункции на фоне терапии кордароном.
В течение первых 6 месяцев после начала терапии уровень ТТГ может не соответствовать уровню периферических тиреоидных гормонов (высокий уровень ТТГ / высокий уровень свободногоТ4 / низкий уровень свободногоТ3). При сохранении эутиреоза показатель ТТГ со временем обычно нормализуется.
Длительное наблюдение. Уровень ТТГ в ходе терапии кордароном следует определять каждые 6 месяцев. Именно уровень ТТГ в таких условиях является надежным показателем тиреоидного статуса.
Прием амиодарона вначале вызывает изменения уровня ТТГ в сторону повышения. За этим следует динамика уровней реверсивного Т3, Т4 и Т3.Прогрессивное снижение уровня Т3 отражает нарушение периферического превращения Т4 в Т3.Увеличение содержания общего и свободного Т4 может быть связано со стимулирующим эффектом ТТГ и/или со снижением клиренса Т4.
ПАЦИЕНТЫ С НЕТИРЕОИДНЫМИ
ЗАБОЛЕВАНИЯМИ (НТЗ)
Острые и хронические НТЗ оказывают сложное влияние на результаты тиреоидных тестов. Тестирование по возможности следует отложить до выздоровления, за исключением случаев отягощенного анамнеза или появления симптомов дисфункции ЩЖ. У тяжелобольных, а также при интенсивном медикаментозном лечении результаты некоторых тиреоидных тестов не поддаются интерпретации.
Сочетанное определение уровня ТТГ и Т4 позволяет наиболее надежно дифференцировать истинную первичную тиреоидную патологию (совпадение изменений уровня Т4 и ТТГ) и транзиторные сдвиги, вызванные самими НТЗ (расхождение изменений уровня Т4 и ТТГ).
Патологический уровень свободного Т4 у пациентов с тяжелыми соматическими болезнями не доказывает наличия тиреоидной патологии. В случае патологического уровня свободного Т4 необходимо исследовать содержание общего Т4.Если оба показателя (свободный Т4 и общий Т4) однонаправлено выходят за пределы нормы, тиреоидная патология возможна. Если же показатели свободного Т4 и общего Т4 расходятся, то это, скорее всего, обусловлено не тиреоидной дисфункцией, а соматическим заболеванием, приемом медикаментов. При выявлении патологического уровня общего Т4 необходимо соотнести данный результат с тяжестью соматического заболевания. Низкий уровень общего Т4 типичен лишь для тяжело- и агонирующих больных. Низкий уровень общего Т4 у пациентов вне реанимационного отделения позволяет предполагать гипотиреоз. Повышенный уровень общего Т3 и свободного Т3 является надежным показателем гипертиреоза при соматических заболеваниях, но нормальный или низкий уровень Т3 не исключает гипертиреоз.
Определение уровня ТТГ у больных с НТЗ. Определение уровня ТТГ и Т4 (свободного Т4 и общего Т4) – наиболее эффективная комбинация для выявления тиреоидной дисфункции больных с соматической патологией. В таких случаях следует расширить референтные интервалы ТТГ до 0,05-10,0 мМЕ/л. Уровень ТТГ может транзиторно снижаться до субнормальных величин в острой фазе болезни и повышаться в фазе выздоровления.
ДИАГНОСТИКА ЗАБОЛЕВАНИЙ ЩИТОВИДНОЙ
ЖЕЛЕЗЫ ВО ВРЕМЯ БЕРЕМЕННОСТИ
Изменение функционирования ЩЖ у женщин происходит уже с первых недель беременности. На нее воздействует множество факторов, большая часть которых прямо или косвенно стимулирует ЩЖ женщины. Преимущественно это происходит в первой половине беременности.
Тиреотропный гормон. Буквально с первых недель беременности под влиянием хорионического гонадотропина (ХГ), обладающего структурной гомологией с ТТГ, стимулируется продукция тиреоидных гормонов ЩЖ. В связи с этим по механизму обратной связи подавляется продукция ТТГ, уровень которого на протяжении первой половины беременности оказывается сниженным примерно у 20% беременных. При многоплодной беременности, когда уровень ХГ достигает очень высоких значений, уровень ТТГ в первой половине беременности оказывается значительно снижен, а порой подавлен, практически у всех женщин. Наиболее низкие показатели уровня ТТГ в среднем приходятся на 10 – 12 неделю беременности. Тем не менее, в отдельных случаях он может оставаться нескольким сниженным вплоть до поздних сроков беременности.
Тиреоидные гормоны. Определение уровня общих тиреоидных гормонов во время беременности не информативно, поскольку он всегда будет повышен (в целом продукция тиреоидных гормонов во время беременности в норме увеличивается на 30 – 50%). Уровень свободного Т4 в первом триместре беременности, как правило, высоконормален, но примерно у 10% с подавленным уровнем ТТГ превышает верхнюю границу нормы. По мере увеличения сроков беременности уровень свободного Т4 будет постепенно снижаться и к концу беременности очень часто оказывается низконормальным. У части пациенток, даже не имеющих патологии ЩЖ и получающих индивидуальную йодную профилактику, на поздних сроках беременности может обнаруживаться пограничное снижение уровня свободного Т4 в сочетании с нормальным уровнем ТТГ. Уровень свободного Т3, как правило, меняется однонаправлено с уровнем свободного Т4, но повышенным оказывается реже.
Общие принципы диагностики заболеваний ЩЖ во время беременности.
* Необходимо сочетанное определение ТТГ и свободного Т4.
* Определение уровня общего Т4 и Т3 во время беременности малоинформативно.
* Уровень ТТГ в первой половине беременности в норме понижен у 20-30% женщин.
* Уровни общих Т4 и Т3 в норме всегда повышены (примерно в 1,5 раза).
* Уровень свободного Т4 в первом триместре несколько повышен примерно у 2% беременных и у 10% женщин с подавленным ТТГ.
* На поздних сроках беременности в норме часто определяется низконормальный или даже погранично сниженный уровень свободного Т4 при нормальном уровне ТТГ.
ТИРЕОГЛОБУЛИН (ТГ)
Тиреоглобулин – гликопротеин, содержащий йод. ТГ является основным компонентом коллоида фолликулов щитовидной железы и выполняет функцию накопления тиреоидных гормонов. На поверхности ТГ происходит синтез тиреоидных гормонов. Секреция ТГ контролируется ТТГ.
Период биологической полужизни ТГ в плазме крови — 4 суток.
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ ТГ В КРОВИ
Повышение содержания в крови ТГ отражает нарушение целостности гематофолликулярного барьера и наблюдается при заболеваниях, протекающих с нарушением структуры железы либо сопровождающихся дефицитом йода. Выход ТГ в кровоток увеличивается при стимуляции и структурных поражениях ЩЖ. Определение ТГ не имеет смысла в ближайшие 2 – 3 недели после пункционной биопсии, так как уровень ТГ может быть повышен из-за пассивного выхода коллоида в кровь при травматизации железы. Уровень ТГ повышается в ближайшие сроки после операций на ЩЖ. Потребление большого количества йода с пищей подавляет выход тиреоидных гормонов из ЩЖ, сдвигая равновесие между образованием и распадом ТГ в сторону его образования и накопления в коллоиде. Уровень ТГ может быть повышен при ДТЗ, подостром тиреоидите, увеличении ЩЖ под действием ТТГ, в некоторых случаях доброкачественной аденомы ЩЖ.
Присутствие антител к ТГ может быть причиной ложноотрицательных результатов, поэтому параллельно с ТГ желательно определять антитела к ТГ.
У больных недифференцированным раком ЩЖ концентрация ТГ в крови увеличивается редко. При дифференцированных опухолях с низкой функциональной активностью уровень ТГ повышается в меньшей степени, чем в опухолях с высокой функциональной активностью. Повышение уровня ТГ установлено при высокодифференцированном раке ЩЖ. Большое диагностическое значение имеет определение уровня ТГ для выявления метастазов карциномы ЩЖ и динамического контроля за состоянием больных на фоне лечения фолликулярной карциномы. Также установлено, что метастазы рака ЩЖ имеют способность синтезировать ТГ.
Снижение после перенесенной хирургической операции или лучевой терапии уровня ТГ в крови исключает наличие метастазов. Напротив, нарастание уровня ТГ может служить признаком генерализованного процесса.
Поскольку больные после радикального лечения дифференцированного рака ЩЖ получают высокие дозы тиреоидных гормонов ( для подавления секреции ТТГ ), на фоне которого также снижается уровень ТГ, его концентрацию следует определять через 2 – 3 недели после отмены супрессивной терапии тиреоидными гормонами.
В педиатрической эндокринологии определение ТГ имеет большое значение при ведении детей с врожденным гипотиреозом для подбора дозы заместительной гормональной терапии. При аплазии ЩЖ, когда ТГ в крови не определяется, показана максимальная дозировка, тогда как при других вариантах обнаружение и увеличение концентрации ТГ позволяет предполагать обратимое течение болезни, в связи с чем дозировка гормона может быть уменьшена.
ФИЗИОЛОГИЧЕСКИЕ СОСТОЯНИЯ, ПРИВОДЯЩИЕ К ИЗМЕНЕНИЮ УРОВНЯ ТГ В КРОВИ
Значения ТГ у новорожденных повышены и значительно снижаются в течение первых 2 лет жизни.
ПОКАЗАНИЯ К ОПРЕДЕЛЕНИЮ ТГ
— карцинома ЩЖ (за исключением медуллярного рака),
— раннее выявление рецидивов и метастазов высокодифференцированного рака ЩЖ у оперированных больных,
— оценка эффективности радийодтерапии метастазов рака ЩЖ (по убыли его содержания в крови до нормальных значений),
— метастазы в легких неясного происхождения,
— метастазы в костях неясного происхождения, патологическая ломкость костей,
— определение ТГ нельзя проводить с целью дифференциальной диагностики доброкачественных и злокачественных опухолей ЩЖ.
КОНЦЕНТРАЦИЯ ТГ У ЗДОРОВЫХ ЛИЦ И ПРИ РАЗЛИЧНЫХ ЗАБОЛЕВАНИЯХ ЩЖ
Здоровые лица 1,5 – 50нг/мл
Рак щитовидной железы:
До операции 125,9 +8,5 нг/мл
После операции без метастазов и рецидивов 6,9+1,8 нг/мл
Метастазы и рецидивы высокодифференцированного 609,3 + 46,7 нг/мл
рака ЩЖ у оперированных больных
Доброкачественные опухоли (до операции) 35,2 + 16,9 нг/мл
Тиреотоксикоз (тяжелая форма) 329,2 + 72,5 нг/мл
АНТИТЕЛА К ТИРЕОГЛОБУЛИНУ ( АНТИ – ТГ )
Щитовидная железа, содержащая специфические антигены, может приводить иммунную систему организма в состояние аутоагрессии. Одним из таких антигенов является тиреоглобулин. Повреждение ЩЖ при аутоиммунных или неопластических заболеваниях может вызвать попадание ТГ в кровеносное русло, что, в свою очередь, ведет к активации иммунного ответа и синтезу специфических антител. Концентрация анти-ТГ изменяется в широком диапазоне и зависит от заболевания. Поэтому определение концентрации анти-ТГ может быть использовано для диагностики и мониторинга лечения заболеваний ЩЖ.
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ АНТИ-ТГ В КРОВИ
Анти-ТГ являются важным параметром для выявления аутоиммунных заболеваний ЩЖ и их тщательно измеряют во время наблюдения за ходом болезни. Повышение уровня анти-ТГ определяется при тиреоидите Хашимото (больше 85 % случаев), болезни Грейвса (больше 30 % случаев), рака ЩЖ(45 %случаев), идиопатической микседеме (больше 95 % случаев), пернициозной анемии (50 % случаев, низкие титры), СКВ (около 20 % случаев), подостром тиреоидите де Кервена( низкие титры), гипотиреозе (около 40 % случаев), ДТЗ (около 25 % случаев), слабоположительный результат может быть получен при нетоксическом зобе.
Эстроген-прогестероновая терапия с целью контрацепции увеличивает титр антител к тиреоглобулину и пероксидазе. У женщин с АИТ при приеме данных препаратов титр антител значительно выше, чем у лиц с АИТ, не принимающих эти лекарственные препараты.
Повышенный титр анти-ТГ может быть получен у больных с неэндокринными заболеваниями при приеме препаратов, влияющих на характер иммунного ответа.
У больных тиреоидитом Хашимото титр анти-ТГ в процессе лечения, как правило, снижается, но могут встречаться больные, у которых анти-ТГ могут персистировать или обнаруживаться волнообразно с периодом около 2 – 3 лет. Титр анти-ТГ у беременных женщин с болезнью Грейвса или Хашимото снижается прогрессивно в течение беременности и кратковременно возрастает после родов, достигая пика через 3 – 4 месяца. Нормальный титр анти-ТГ не исключает тиреоидита Хашимото. Тест определения микросомальных антител более чувствителен по отношению к тиреоидиту Хашимото, чем тест анти-ТГ, особенно у пациентов моложе 20 лет.
Определение анти-ТГ дает возможность прогнозировать нарушение функции ЩЖ у больных с другими аутоиммунными эндокринными заболеваниями и у членов семей с наследственными органоспецифическими аутоиммунными заболеваниями. Слабо положительные результаты обычно обнаруживаются при других аутоиммунных расстройствах и хромосомных нарушениях таких, как синдром Турнера и синдром Дауна.
Положительные результаты у некоторых больных гипертиреоидизмом позволяют думать о сочетании с тиреоидитом. Использование анти-ТГ для выявления аутоиммунных заболеваний ЩЖ особенно оправдано в йоддефицитных районах.
У детей, рожденных от матерей с высокими титрами анти-ТГ, в течение жизни могут развиваться аутоиммунные тиреоидные заболевания, что требует отнести таких детей к группе риска.
Около 5 — 10 % практически здоровых людей могут иметь низкий титр анти-ТГ без симптомов болезни, чаще у женщин и пожилых людей, что связано, вероятно, с выявлением лиц, имеющих субклинические формы аутоиммунного тиреоидита.
ПОКАЗАНИЯ К ОПРЕДЕЛЕНИЮ АНТИ-ТГ: — новорожденные: высокий титр анти-ТГ у матерей, — хронический тиреоидит Хашимото, — дифференциальная диагностика гипотиреоза, — диффузный токсический зоб (болезнь Грейвса), — послеоперационное ведение больных высокодифференцированным раком ЩЖ в комплексе с ТГ, — в йоддефицитных районах оценка уровня анти-ТГ в сыворотке способствует диагностике аутоиммунной тиреоидной патологии у пациентов с узловым зобом.
РЕФЕРЕНТНЫЕ ПРЕДЕЛЫ – 0 – 100 мЕ/мл
АНТИТЕЛА К ТИРЕОИДНОЙ ПЕРОКСИДАЗЕ
(АНТИ – ТПО)
Тест анти-ТПО используется для верификации аутоиммунных тиреопатий. Обладая способностью связываться с комплементом, анти-ТПО принимают прямое участие в аутоагрессии, то есть являются показателем агрессии иммунной системы по отношению к собственному организму. Тиреоидная пероксидаза обеспечивает образование активной формы йода, который способен включаться в процесс йодификации тиреоглобулина, то есть играет ключевую роль в процессе синтеза тиреоидных гормонов. Антитела к ферменту блокируют его активность, вследствие чего снижается секреция тиреоидных гормонов, в основном тироксина. Анти-ТПО – наиболее чувствительный тест для обнаружения аутоиммунных заболеваний ЩЖ. Обычно их появление является первым сдвигом, который наблюдается в ходе развития гипотиреоза вследствие тиреоидита Хашимото.
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ АНТИ-ТПО
Аутоиммунные заболевания ЩЖ являются основным фактором, лежащим в основе гипотиреоза и гипертиреоза, и развиваются у генетически предрасположенных лиц. Таким образом, измерение циркулирующих анти-ТПО является маркером генетической предрасположенности. Наличие анти-ТПО и повышенный уровень ТТГ позволяет прогнозировать развитие гипотиреоза в будущем.
Высокая концентрация анти-ТПО наблюдается при тиреоидите Хашимото (чувствительность 90–100 %)и болезни Грейвса (чувствительность 85 %). Уровень анти-ТПО повышается в 40 – 60 % при ДТЗ, но в меньшем титре, чем при активной стадии тиреоидита Хашимото.
Обнаружение анти-ТПО во время беременности говорит о риске развития у матери послеродового тиреоидита и возможном влиянии на развитие ребенка.
В низких концентрациях анти-ТПО могут встречаться у 5 – 10 % здорового населения и у пациентов с заболеваниями, не связанными со ЩЖ, например, при воспалительных ревматических заболеваниях.
Титр анти-ТПО увеличивается при лечении эстроген-прогестероновыми препаратами и приеме препаратов, влияющих на характер иммунного ответа.
ПОКАЗАНИЯ К ОПРЕДЕЛЕНИЮ АНТИ-ТПО
— аутоиммунный тиреоидит,
— прогноз риска гипотиреоза при изолированном повышении уровня ТТГ,
— прогноз послеродового тиреоидита у женщин из групп высокого риска,
— офтальмопатия: увеличение окологлазных тканей (подозрение на «эутиреоидную болезнь Грейвса»).
— новорожденные: гипертиреоз и высокий уровень анти-ТПО или болезнь Грейвса у матери,
— фактор риска тиреоидной дисфункции при терапии интерфероном, интерлейкином-2, препаратами лития, кордароном,
— фактор риска невынашивания беременности и неудачи при оплодотворении.
РЕФЕРЕНСНЫЕ ПРЕДЕЛЫ – 0 – 30 мЕ/мл.
АНТИТЕЛА К МИКРОСОМАЛЬНОЙ ФРАКЦИИ
(АНТИ-МФ)
Аутоантитела к микросомальной фракции выявляются при всех видах аутоиммунных заболеваний ЩЖ, однако, могут обнаруживаться и у здоровых людей. Анти-МФ являются цитотоксичным фактором, непосредственно вызывающим повреждение тиреоидных клеток. Микросомальный антиген является липопротеидом, из которого состоят мембраны пузырьков, содержащие тиреоглобулин. Аутоиммунный тиреоидит – заболевание, которое характеризуется образованием антител к различным компонентам ЩЖ с развитием ее лимфоидной инфильтрации и разрастанием фиброзной ткани. Анти-МФ способны разрушать ЩЖ и снижать ее функциональную активность.
ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ, ПРИ КОТОРЫХ ВОЗМОЖНЫ ИЗМЕНЕНИЯ УРОВНЯ АНТИ-МФ
Наиболее высокие уровни анти-МФ обнаруживаются у пациентов с АИТ Хашимото( у 95 % больных), идиопатической мексидемой, на последней стадии хронического атрофического тиреоидита, особенно у пожилых женщин, довольно часто встречаются у пациентов с выявленной нелеченной формой болезни Грейвса. Анти-МФ определяются у 85 % больных ДТЗ, что указывает на его аутоиммунный генез. Анти-МФ иногда выявляются при раке ЩЖ. Повышенные уровни анти-МФ в ходе 1 триместра беременности указывают на определенную степень риска послеродового тиреоидита.
ПОКАЗАНИЯ К ОПРЕДЕЛЕНИЮ АНТИ-МФ
— тиреоидит Хашимото,
— аутоиммунный характер заболеваний ЩЖ,
— прогноз послеродового тиреоидита у женщин из групп высокого риска,
— высокая степень риска возникновения тиреоидита при наследственной предрасположенности к данному заболеванию, при других формах аутоиммунных процессов (сахарный диабет 1 типа, болезнь Аддисона, пернициозная анемия).
АНТИТЕЛА КРЕЦЕПТОРАМ ТТГ (TTT—RP)
Рецепторы тиреотропного гормона — мембранные структуры тиреоцитов (и, возможно, клеток других органов и тканей). ТТГ-RP являются регуляторными белками, интегрированными в мембране тиреоидной клетки и влияющими как на синтез и секрецию ТГ, так и на клеточный рост. Они специфически связывают ТТГ гипофиза и обеспечивают реализацию его биологического действия. Причиной развития диффузного токсического зоба (болезнь Грейвса) считается появление в крови больных особых иммуноглобулинов — аутоантител, специфически конкурирующих с ТТГ за связывание с рецепторами тиреоцитов и способных оказывать на щитовидную железу стимулирующее влияние, аналогичное ТТГ. Выявление высокого уровня аутоантител к ТТГ-рецепторам в крови больных с болезнью Грейвса является прогностическим предвестником рецидива заболевания (чувствительность 85 % и специфичность 80 %). Фетоплацентарный перенос этих антител является одной из причин врожденного гипертиреоза у новорожденных, если мать страдает болезнью Грейвса. Для получения доказательства об обратимом характере заболевания необходим лабораторный мониторинг, направленный на установление элиминации антител к ТТГ-RP из организма ребенка. Исчезновение антител у ребенка после медикаментозного достижения эутиреоза и устранения зоба служит основанием для решения вопроса о прекращении лекарственной терапии.
Аутоантитела к ТТГ-рецепторам в повышенных количествах могут быть обнаружены у больных с зобом Хашимото, при подостром АИТ. Уровень аутоантител прогрессивно снижается при медикаментозном лечении этих заболеваний или после тиреоидэктомии, что может быть использовано для контроля за эффективностью проводимого лечения.
ПОКАЗАНИЯ К НАЗНАЧЕНИЮ:
|
АБСОЛЮТНЫЕ |
ОТНОСИТЕЛЬНЫЕ |
|
· Дифференциальный диагноз послеродового тиреоидита и БГ при послеродовом тиреотоксикозе. · Прогноз риска фетального/неонатального тиреотоксикоза у женщин с предшествовавшей радиоаблацией ЩЖ по поводу БГ или на фоне текущей терапии тионамидами. |
· Диагностика эутиреоидной офтальмопатии Грейвса. · Расчёт длительности терапии и риска рецидива у пациентов, получающих терапию по поводу БГ (особенно у детей).
|
РЕФЕРЕНСНЫЕ ПРЕДЕЛЫ: Уровень аутоантител к ТТГ-рецепторам в сыворотке в норме составляет до 11 ЕД/л.
Сдавайте анализы постоянно в одной и той же лаборатории – и вашему врачу будут примерно известны Ваши личные показатели нормы и любое отклонение от нормы будет сразу им замечено.
Заболевания, не связанные с щитовидной железой — Консультант по эндокринологии
Вы уверены, что у пациента не щитовидная железа?
Критическое заболевание вызывает множественные неспецифические изменения концентраций гормонов щитовидной железы, которые связаны с тяжестью заболевания у пациентов, у которых нет врожденного заболевания щитовидной железы. Продолжаются дискуссии о том, являются ли такие изменения физиологической адаптацией или патологическим нарушением. Из-за сложности эутиреоидного синдрома вполне вероятно, что роль играют как физиологические, так и патологические эффекты.
Несмотря на отклонения в параметрах сывороточных гормонов щитовидной железы, мало доказательств того, что у тяжелобольных пациентов имеется клинически значимая дисфункция щитовидной железы. Таким образом, в настоящее время нет данных в пользу терапии гормонами щитовидной железы при ведении больного эутиреоидным пациентом. Синдром слабого эутиреоида следует рассматривать не как изолированное патологическое событие, а как часть скоординированной системной реакции на заболевание, которая затрагивает как иммунную, так и эндокринную системы.
Концепция свободных гормонов
Важное значение для понимания регуляции функции щитовидной железы и изменений циркулирующих гормонов щитовидной железы, наблюдаемых при критических состояниях, является концепция «свободного гормона», согласно которой только несвязанный гормон обладает метаболической активностью.Общая функция щитовидной железы регулируется секрецией тиреотропного гормона (ТТГ) гипофизом при любых изменениях концентрации свободных гормонов щитовидной железы. Изменения либо концентраций связывающих белков, либо сродства связывания гормона щитовидной железы со связывающими белками сыворотки оказывают значительное влияние на общие уровни гормонов в сыворотке из-за высокой степени связывания Т4 и Т3 с этими белками. Однако эти изменения не обязательно могут быть связаны с дисфункцией щитовидной железы.
Этиология
В то время как причина изменений в экономии гормонов щитовидной железы при критическом заболевании в значительной степени неизвестна, было показано, что цитокины, такие как фактор некроза опухоли альфа, интерлейкин 1 и интерлейкин 6, воспроизводят многие черты эутиреоидного синдрома у обоих животных. и исследования на людях. Остается определить, является ли синдром слабого эутиреоида результатом активации сети цитокинов или просто представляет собой эндокринный ответ на системное заболевание, вызванное теми же медиаторами, которые запускают каскад цитокинов.
Патогенез можно разделить на три раздела:
Нарушения периферических путей метаболизма гормона щитовидной железы
Изменения оси гипофиз — щитовидная железа
Изменения в сывороточных связывающих белках
Нарушения периферических путей метаболизма гормона щитовидной железы
Основным путем метаболизма Т4 является последовательное монодейодирование типами 1 (D1) и 2 (D2) для образования Т3 (активирующий путь) или дейодиназы 3 типа (D3) для образования rT3 (инактивирующий путь).Одним из первых изменений при остром заболевании является ингибирование D1 и D2 в периферических тканях и последующее нарушение преобразования T4 в T3, в результате чего уровни T3 в сыворотке и тканях падают вскоре после начала острого заболевания. D1 также деиодирует rT3, поэтому деградация нарушается, и уровни этого неактивного гормона повышаются пропорционально падению уровня T3. Недавние исследования показали, что D3 может увеличиваться в определенных тканях, что приводит к увеличению удаления T3 в этих тканях. Недейодирующие пути метаболизма, такие как сульфоконъюгация, также увеличиваются при критических состояниях (см. Таблицу 1).
Таблица 1.nИнгибиторы активности 5’дейодиназы I типа
Изменения оси гипофиз-щитовидная железа
В то время как уровни ТТГ в сыворотке обычно нормальны на ранних этапах острого заболевания, уровни часто падают по мере прогрессирования болезни из-за воздействия различных тормозящих факторов, которые являются обычными при лечении тяжелобольного пациента. Использование дофамина, повышенный уровень глюкокортикоидов, эндогенных или экзогенных, и тормозящие сигналы от высших корковых центров также могут играть роль в снижении секреции ТТГ.Определенные метаболиты тиреоидных гормонов, количество которых увеличивается при других заболеваниях, также могут иметь значение (см. Таблицу 2).
Таблица 2.nФакторы, снижающие секрецию ТТГ
Изменения сывороточных связывающих белков
И Т4 (связывание 99,97%), и Т3 (связывание 99,7%) циркулируют в сыворотке крови в основном связанными с тиронин-связывающим белком (ТБГ), а связывание гормонов щитовидной железы с ТБГ зависит от множества факторов при остром заболевании. Поскольку метаболической активностью обладает только несвязанный гормон, изменения либо концентраций, либо связывания с ТБГ будут иметь серьезные последствия для общих уровней гормонов в сыворотке, но минимальные изменения в концентрациях свободных гормонов, и, таким образом, общая функция щитовидной железы сохраняется ( См. Таблицу 3).
Таблица 3.nФакторы, которые изменяют привязку T4 к TBG
Каковы стадии эутиреоидного синдрома?
Синдром больного эутиреоидом можно разделить на четыре стадии:
Низкий T3
Высокий T4
Низкий T4
Восстановление
Хотя это помогает понять прогрессирование аномалий, приводящих к эутиреоидному синдрому, важно понимать, что не все пациенты проходят все стадии.Тем не менее, это помогает отличить синдром слабого эутиреоида от внутренней дисфункции щитовидной железы. Например, у пациента с повышенным уровнем ТТГ в начале курса интенсивной терапии (ОИТ) более вероятно наличие выраженного гипотиреоза, в то время как такое же повышение ТТГ в конце курса ОИТ с большей вероятностью связано с выздоровлением от основного заболевания.
Низкое состояние T3
Общим для всех аномалий концентрации гормонов щитовидной железы, наблюдаемых у тяжелобольных пациентов, является существенное снижение уровня Т3 в сыворотке, которое может произойти уже через 24 часа после начала заболевания и затрагивает большинство пациентов, поступающих в медицинское учреждение. .Это можно объяснить исключительно ингибированием периферической конверсии Т4 в Т3. Эта стадия часто встречается у пациентов с застойной сердечной недостаточностью и острым сердечным повреждением. У пациентов с сердечными заболеваниями концентрации Т3 в сыворотке крови являются отрицательным прогностическим фактором и обратно пропорциональны смертности.
Высокое состояние T3
Уровни Т4 в сыворотке могут быть повышены на ранних стадиях острого заболевания, в основном из-за острого ингибирования превращения Т4 в Т3. По мере увеличения продолжительности болезни недейодирующие пути деградации Т4 увеличиваются и возвращают уровни Т4 в сыворотке к нормальному диапазону.
Низкое состояние T4
По мере увеличения тяжести и продолжительности заболевания общий уровень Т4 в сыворотке может снижаться до субнормального диапазона в результате уменьшения связывания Т4 с ТБГ, снижения уровня ТТГ в сыворотке, приводящего к снижению выработки Т4 и увеличение недейодинативных путей метаболизма Т4. Снижение уровня Т4 в сыворотке коррелирует с прогнозом у пациентов без кардиологического отделения интенсивной терапии, с увеличением смертности, когда уровень Т4 в сыворотке падает ниже 4 мкг / дл и приближается к 80% у пациентов с уровнями Т4 в сыворотке <2 мкг / дл.Несмотря на заметное снижение общих уровней Т4 и Т3 в сыворотке до гипотиреоидного диапазона, уровни свободных гормонов часто в норме; таким образом, состояние низкого уровня Т4 является более вероятным маркером мультисистемной недостаточности у этих критически больных пациентов, чем состояние истинного гормонального дефицита.
Состояние восстановления
Изменения концентрации гормонов щитовидной железы исчезают по мере исчезновения болезни. Эта стадия может быть продолжительной и характеризуется умеренным повышением уровня ТТГ в сыворотке. Полное выздоровление с восстановлением нормального уровня гормонов щитовидной железы может занять до нескольких месяцев после выписки пациента из больницы.
Что еще могло быть у пациента?
Дифференциальный диагноз — это просто наличие или отсутствие дисфункции щитовидной железы (например, гипотиреоз или гипертиреоз).
Ключевые лабораторные и визуализирующие исследования
Обычный скрининг популяции ОИТ на предмет дисфункции щитовидной железы не рекомендуется из-за высокой распространенности аномальных тестов функции щитовидной железы и низкой распространенности истинной дисфункции щитовидной железы. По возможности лучше отложить оценку щитовидно-гипофизарной оси до тех пор, пока пациент не выздоровеет от острого заболевания.Ни один тест не может дать однозначного решения при наличии внутренней дисфункции щитовидной железы.
По определению, синдром больного эутиреоидом — это наличие аномальных функциональных тестов щитовидной железы в условиях других заболеваний и при отсутствии внутренней дисфункции щитовидной железы. Наиболее частым отклонением от нормы является низкий уровень Т3, хотя обычно это не первый проводимый тест. Аномальные уровни ТТГ обычно приводят к измерениям индекса свободного Т4 (FT4) или индекса свободного Т4 (FTI), которые часто являются отклонениями.
Разумным начальным подходом является получение как индекса свободного Т4 (FTI) (или, в меньшей степени, FT4), так и измерения ТТГ у пациентов с высоким клиническим подозрением на внутреннюю дисфункцию щитовидной железы. Оценка этих значений в контексте продолжительности, тяжести и стадии болезни пациента позволит поставить правильный диагноз большинству пациентов. Если диагноз все еще неясен, измерение антител к щитовидной железе может быть полезным в качестве маркера внутреннего заболевания щитовидной железы. Измерение уровня Т3 в сыворотке показано только в случае подавленного ТТГ и FTI от среднего до высокого.
Анализы ТТГ
Аномальные значения ТТГ были зарегистрированы почти у 20% госпитализированных пациентов, более 80% из которых не имели внутренней дисфункции щитовидной железы при контрольном обследовании, когда они были здоровы. Аномальные значения ТТГ требуют дополнительной биохимической и клинической оценки, прежде чем можно будет поставить диагноз дисфункции щитовидной железы.
Концентрации T4
Измерения только общего Т4 мало пригодны для остро больных пациентов, поскольку нарушения связывания с белками сыворотки являются обычным явлением.Измерение истинных концентраций свободного Т4 в сыворотке с помощью равновесного диализа или ультрафильтрации занимает много времени и дорого; таким образом, оценки концентраций свободного Т4 получают либо с помощью FTI, либо с помощью FT4 с помощью аналогового измерения.
Итого T3
Нет показаний для рутинного измерения уровней Т3 в сыворотке при первоначальной оценке функции щитовидной железы у тяжелобольного пациента, так как на концентрации Т3 в сыворотке в наибольшей степени влияют изменения в экономии гормонов щитовидной железы в результате острого заболевания.Единственная ситуация, при которой уровни Т3 в сыворотке могут быть полезны, — это присутствие подавленного значения чувствительного ТТГ, когда повышенная или высокая нормальная концентрация Т3 в сыворотке часто помогает дифференцировать тиреотоксикоз и синдром больного эутиреоида.
Другие тесты, которые могут оказаться полезными с диагностической точки зрения
Аутоантитела щитовидной железы
Аутоантитела к щитовидной железе — это вторичные тесты, которые повышают специфичность аномальных значений ТТГ и FTI при диагностике внутреннего заболевания щитовидной железы.
Предикторы смертности
При наиболее серьезных медицинских и хирургических заболеваниях, которые приводят к эутиреоидному синдрому, уровни Т4 в сыворотке служат предикторами смертности, причем смертность возрастает с уменьшением уровней Т4 в сыворотке. Однако у пациентов, госпитализированных с осложнениями СПИДа, уровни Т3 в сыворотке являются лучшими предикторами смертности, поскольку уровни Т3 в сыворотке выше у этих пациентов, чем у пациентов, не страдающих СПИДом, с аналогичной степенью заболевания. Уровни Т3 в сыворотке обратно пропорциональны прогнозу у пациентов с застойной сердечной недостаточностью.
Ведение и лечение болезни
Неотложная терапия направлена только на основное заболевание, не связанное с щитовидной железой. Эффективность лечения гормоном щитовидной железы не доказана, и оно не показано пациентам с эутиреоидным синдромом.
Вопрос о том, представляет ли эутиреоидный синдром у тяжелобольных пациентов патологические изменения функции щитовидной железы, которые негативно влияют на этих пациентов, или просто отражает мультисистемную недостаточность (т. Е.дыхательная, сердечная, почечная, печеночная недостаточность), возникающая у пациентов в критическом состоянии, до сих пор остается дискуссионной. Что не является спорным, так это то, что заместительная гормональная терапия щитовидной железы не показала положительного эффекта у подавляющего большинства этих пациентов в опубликованных на сегодняшний день исследованиях. Фактические данные свидетельствуют о положительном влиянии L-T3 на увеличение выживаемости органов, полученных от доноров органов с мертвым мозгом.
Хотя L-T3, по-видимому, немного улучшает гемодинамические и нейрогуморальные параметры у пациентов с застойной сердечной недостаточностью, эти преимущества могут представлять фармакологический эффект T3, а не физиологический замещающий гормональный эффект.Кроме того, исследования с участием пациентов с застойной сердечной недостаточностью, получавших Т3, не имели пагубного эффекта от лечения L-T3, но, по-видимому, не имели какого-либо устойчивого клинического преимущества. Однако, похоже, что будущие исследования у этой популяции пациентов оправданы. В настоящее время, в отсутствие каких-либо клинических доказательств гипотиреоза, не существует убедительных доказательств использования терапии гормонами щитовидной железы у любого пациента со сниженными параметрами гормонов щитовидной железы из-за синдрома больного эутиреоидом.
Голод / недоедание
Пациенты общего отделения интенсивной терапии
Нет пользы от L-T4 для пациентов общего профиля, ожоговых пациентов, пациентов с острой почечной недостаточностью или трансплантатом почек.
Недоношенные
Отсутствие влияния L-T4 на показатели развития недоношенных детей на сроке беременности 26–28 недель.
Возможный положительный эффект L-T4 на младенцев на сроке гестации 25-26 недель, но возможный вредный эффект на младенцев на сроке беременности 27-30 недель.
Нет преимуществ L-T3
Мета-анализ не показывает значительных эффектов лечения недоношенных детей гормонами щитовидной железы.
Кардиохирургические пациенты
Небольшие исследования показывают улучшение гемодинамических параметров с L-T3
Крупные исследования не показали положительного эффекта L-T3 у пациентов, перенесших сердечное шунтирование.
Возможное улучшение гемодинамических параметров и пребывания в стационаре с L-T3 у детей, перенесших кардиохирургические операции.
Сердечные доноры
Различные результаты (полезные, без пользы) о влиянии L-T3 на сохранение функции нормального сердца у сердечных доноров с мертвым мозгом до трансплантации.
Возможные преимущества L-T3 в улучшении функции пораженного сердца до трансплантации, потенциально увеличивая пул органов, доступных для трансплантации.
Консенсусные конференции рекомендуют использовать L-T3 как часть гормональной реанимации у доноров, фракция выброса сердца которых составляет <45%.
Застойная сердечная недостаточность
Небольшое неконтролируемое исследование показало, что краткосрочная терапия L-T4 увеличивает сердечный выброс и функциональную способность, а также снижает системное сосудистое сопротивление.
Улучшение гемодинамических параметров и нейрогуморальных профилей при кратковременной внутривенной инфузии L-T3, возможно, требующей супрафизиологических концентраций.
Концентрация гормона щитовидной железы должна вернуться к нормальному диапазону, как только пациент полностью выздоровеет от своего основного заболевания.Целесообразно повторение FT4 / FTI и TSH через 2-3 месяца после окончания острой госпитализации.
Какие доказательства? / Ссылки
Адлер С.М., Вартофски Л. «Синдром не щитовидной железы». Endocrinol Metab Clin North Am. т. 36. 2007. С. 657–72. (Недавний обзор с подробностями по вопросам, обсуждаемым в этой главе, с обширными ссылками.)
Петерс, Р.П., Воутерс, П.Дж., Каптейн, Э., ван Тоор, Х., Виссер, Т.Дж., Ван ден Берг, Г. «Сниженная активация и повышенная инактивация гормона щитовидной железы в тканях тяжелобольных пациентов». J Clin Endocrinol Metab. т. 88. 2003. С. 3202-11. (Основная статья об измерении изменений тканевого метаболизма гормонов щитовидной железы у тяжелобольных людей.)
Спенсер, К., Элген, А., Шен, Д., Дуда, М., Куоллс, С., Вайс, С., Николофф, Дж. «Специфичность чувствительных анализов тиреотропина (ТТГ), используемых для скрининга заболеваний щитовидной железы у госпитализированных пациентов». Clin Chem. т. 33. 1987. pp. 1391-6. (Классическая статья, в которой описана разработка и использование чувствительных анализов ТТГ исследователями, которые разработали эти анализы.)
Ван ден Берге, Г., де Зегер, Ф., Лауэрс, П. «Дофамин и синдром больного эутиреоидом при критическом заболевании». Clin Endocrinol (Oxf). т. 41. 1994. С. 731-7. (Документирует влияние дофамина на секрецию ТТГ, основного медиатора аномальных тестов функции щитовидной железы в отделении интенсивной терапии.)
Каптейн, Э.М., Вайнер, Дж. М., Робинсон, У. Дж., Уиллер, В. С., Николофф, Дж. Т.. «Связь измененных показателей гормонов щитовидной железы с выживаемостью при других заболеваниях щитовидной железы». Clin Endocrinol (Oxf). т. 16. 1982. С. 565-574. (Описывает различные показатели гормонов щитовидной железы при заболеваниях, не связанных с щитовидной железой.)
Pingitore, A, Landi, P, Taddei, MC, Ripoli, A, L’Abbate, A, Iervasi, G. «Уровни трийодтиронина для стратификации риска пациентов с хронической сердечной недостаточностью». Am J Med. т. 118. 2005. С. 132-6. (Классические статьи об использовании показателей гормонов щитовидной железы в качестве предикторов смертности у тяжелобольных.)
DeGroot, LJ. «Синдром не тиреоидного заболевания» — это функциональный центральный гипотиреоз, и в тяжелом случае уместна заместительная гормональная терапия в свете имеющихся знаний ». J Endocrinol Invest. т. 26. 2003. С. 1163-70. (Ведущий исследователь предлагает пересмотреть использование гормональной терапии щитовидной железы при эутиреоидном синдроме.)
Фарвелл, AP. «Лечение эутиреоидного синдрома гормоном щитовидной железы не показано». Endocr Practice. т. 14. 2008. С. 1180-7. (Недавний обзор исследований гормональной терапии щитовидной железы при эутиреоидном синдроме.)
Клемперер, Д. Д., Кляйн, И., Гомес, М., Хельм, Р. Э., Охамаа, К., Томас, С. Дж., Исом, О. В., Крейгер, К.«Лечение гормонами щитовидной железы после аортокоронарного шунтирования». N Engl J Med. т. 333. 1995. С. 1522-7. (Изучает роль заместительной терапии гормонами щитовидной железы при синдроме слабого эутиреоидного синдрома, вызванном операцией аортокоронарного шунтирования.)
Новицки, Д., Купер, Д. К., Розендейл, Д. Д., Кауфман, Н. М.. «Гормональная терапия донора органов с мертвым мозгом: экспериментальные и клинические исследования». Трансплантация. т. 82. 2006. pp. 1396-401. (Рассматривается роль терапии Т3 в «реанимации» пораженного сердца.)
Осборн, Д.А. «Гормоны щитовидной железы для предотвращения нарушений развития нервной системы у недоношенных детей». Cochrane Database Syst Rev. 2001. pp. CD001070 (Мета-анализ эффектов лечения гормонами щитовидной железы у недоношенных детей.)
Pingitore, A, Galli, E, Barison, A, Iervasi, A, Scarlattini, M, Nucci, D, L’Abbate, A, Mariotti, R, Iervasi, G. «Острые эффекты заместительной терапии трийодтиронином (T3) при пациенты с хронической сердечной недостаточностью и синдромом низкого уровня Т3: рандомизированное плацебо-контролируемое исследование ». J Clin Endocrinol Metab. т. 93. 2008. pp. 1351-8. (Недавнее исследование, предполагающее возможную роль L-T3 у пациентов с ХСН.)
Boelen, A, Kwakkel, J, Fliers, E. «За пределами низкого T3 в плазме: местный метаболизм гормонов щитовидной железы во время воспаления и инфекции». Эндокринные обзоры. т. 32. 2011. С. 670-93. (Всесторонний обзор эффектов клеточных и иммунологических состояний острого заболевания в различных органах.)
Гурин, К.Г., Джонсон, Дж. Т., Рэндольф, Г.«Послеоперационные осложнения». Хирургия щитовидной и паращитовидной железы. 2003. С. 433-43.
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
Достижение эутиреоида возможно при приеме L-тироксина 1 раз в неделю
AUSTIN. Среди пациентов с гипотиреозом прием L-тироксина один раз в неделю был приемлемой альтернативой ежедневного приема, как сообщили здесь исследователи.
Под руководством Сатиша Васури, доктора медицины из больницы Парк в Индии, и его коллег, проспективное обсервационное исследование показало, что эутиреоз достижим при приеме L-тироксина один раз в неделю среди взрослых молодого и среднего возраста, ранее не соблюдающих правила.
Представленное на ежегодном собрании Американской ассоциации клинических эндокринологов исследование показало аналогичные результаты даже среди пациентов, у которых недавно был диагностирован гипотиреоз.
- Обратите внимание, что это исследование было опубликовано в виде аннотации и представлено на конференции.Эти данные и выводы следует рассматривать как предварительные, пока они не будут опубликованы в рецензируемом журнале.
Авторы выделили текущие рекомендации по лечению взрослых с гипотиреозом, в которых говорится, что ежедневный прием L-тироксина является «подходящей терапией золотого стандарта». Типичная суточная доза составляет от 1,6 до 1,8 мкг / кг / день.
ГруппаВасури рандомизировала 180 пациентов в возрасте от 18 до 55 лет на три исследовательские группы, все с установленным диагнозом гипотиреоз.Все участники были проверены на мальабсорбцию до начала исследования, и, как сообщается, ни один из них не получал каких-либо препаратов, которые ингибировали бы абсорбцию L-тироксина.
Первая исследовательская группа, в которую вошли 60 человек, получала еженедельную дозу L-тироксина, в семь раз превышающую обычную суточную дозу. Эти люди, которые до вмешательства ежедневно принимали L-тироксин, также имели исходные значения ТТГ 4,2 или меньше.
Шестьдесят участников были включены во вторую исследовательскую группу, которым еженедельно вводили дозу, в семь раз превышающую обычную дневную дозу, но доза была более индивидуальной, особенно для дозирования с точки зрения массы тела и значения ТТГ.Все участники этой группы имели значения ТТГ более 4,2 и ранее также принимали ежедневные дозы.
Третья группа, в которую вошли 60 пациентов с впервые установленным диагнозом, которые еще не получали лечения, получала еженедельную дозу L-тироксина, специально измеренную для индивидуальной массы тела и уровней ТТГ, все из которых были выше 4,2.
Самая низкая недельная доза L-тироксина, о которой сообщалось во время исследования, составляла 175 мкг, а максимальная — 1050 мкг.
Во всех исследовательских группах большинство участников смогли добиться полного восстановления эутиреоза с помощью L-тироксина один раз в неделю.Все, кроме одного пациента (n = 59) в первой группе исследования, смогли достичь эутиреоза к 12 неделям, продолжая лечение в течение 24 недель. Только один участник был исключен из этой группы из-за симптомов гипертиреоза.
Всего 52 участника второй исследовательской группы достигли эутиреоза к 12 неделям. К 24 неделям пять оставшихся участников все еще не достигли нормальной функции щитовидной железы. Группа Васури отметила, что это может быть связано с внешними нарушениями обмена веществ, такими как ожирение или диабет.
К 12 неделям в третьей группе 54 участника имели нормальную функцию щитовидной железы, а 59 из них достигли эутиреоза к 24 неделям. Исследователи отметили, что последний пациент в этой группе переехал и не завершил исследование.
ГруппаВасури заявила, что эти данные свидетельствуют о том, что более высокая еженедельная лечебная доза может быть «действенным терапевтическим вариантом, а также может рассматриваться как терапия первой линии», особенно среди тех, кто не придерживается ежедневного приема. Они добавили, что это может быть особенно подходящим для взрослых трудоспособного возраста, которые могут испытывать нарушение абсорбции из-за времени приема пищи.
Также сообщалось о значительных различиях в уровнях ЛПНП и триглицеридов между группами 2 и 3. Однако авторы добавили, что в некоторой литературе более высокие уровни FT4 связаны с повышенным риском внезапной сердечной смерти, и рекомендуют будущие исследования по оценке сердечной безопасности при дозировке раз в неделю. .
«Если бы мы провели такой же эксперимент с цитомелем [лиотиронин натрия] или Т3, это было бы очень опасно», — добавил С. Сету Редди, доктор медицины, председатель комитета годовой программы AACE и модератор устной сессии, подчеркнув, что метод абсорбции этого лечения был жизненно важен.
Щелкните здесь, чтобы ознакомиться с клиническими рекомендациями AACE по лечению гипотиреоза у взрослых.
Последнее обновление 5 мая 2017 г.
Редкое проявление острой иммунной тромбоцитопении, резистентной к терапии первой линии, несмотря на эутиреоидный статус | Кровь
ИТП — это аутоиммунное гематологическое заболевание, характеризующееся иммуноопосредованным разрушением тромбоцитов. У до 90% пациентов болезнь проходит самостоятельно до 6 месяцев (2, 3).У большинства пациентов количество тромбоцитов увеличивается при лечении стероидами и / или внутривенным иммуноглобулином (ВВИГ) для предотвращения осложнений в течение 24-72 часов. (2, 3). ИТП может возникать у здоровых детей или совпадать с другими аутоиммунными заболеваниями, такими как тиреоидит Хашимото. Предыдущие сообщения о случаях предполагают, что индукция эутиреоидного состояния левотироксином улучшала реакцию тромбоцитов на ВВИГ и стероиды (1). Мы сообщаем о случае 15-летней женщины с диагнозом острой ИТП, у которой также обнаружен тиреоидит Хашимото, у которой ИТП оказалась невосприимчивой к терапии первой линии, несмотря на достижение эутиреоидного состояния при лечении левотироксином.
Женщина 15 лет обратилась с жалобами на продолжительное менструальное кровотечение и легкие синяки, связанные с утомляемостью, в течение 3 недель. У пациента постепенно увеличивалась щитовидная железа. В остальном обзор систем был отрицательным, а семейный анамнез не имел значения. При физикальном обследовании показатели жизненно важных функций показали вес на 97-м процентиле и тахикардию. Бледность ладоней и конъюнктивы. Тиромегалия плотная, без болезненных ощущений, без пальпируемых узелков. У нее были желто-пурпурные круглые экхимозы размером 3 см на правой передней внутренней стороне бедра и левом верхнем квадранте живота.Неврологические, сердечно-сосудистые, легочные и желудочно-кишечные обследования в остальном были нормальными.
Первоначальная лабораторная оценка показала микроцитарную анемию с гемоглобином 5,3 г / дл, средним корпускулярным объемом 76,3 мкл, числом ретикулоцитов 3,2% и числом тромбоцитов 5 x 10 3 / мкл, с небольшим количеством крупных тромбоцитов на периферии. мазок. Цитометрия периферического кровотока оказалась отрицательной на лейкоз и лимфому. Оценка других причин тромбоцитопении, включая инфекцию и семейную тромбоцитопению, была отрицательной.У нее было нормальное абсолютное количество нейтрофилов и отрицательный прямой тест Кумба, исключающий синдром Эвана. Ее исследования щитовидной железы предполагали гипотиреоз с уровнем тиреотропного гормона (ТТГ) 233,40 мк [МЕ] / мл, свободного Т4 0,3 нг / дл, антител к тиреоглобулину> 1000 [МЕ] / мл и антител к тироидной пероксидазе> 900 [МЕ] / мл. Ультразвук шеи выявил увеличенную неоднородную щитовидную железу с множественными небольшими эхогенными узелками без тени, что соответствует тиреоидиту Хашимото.
Во время госпитализации пациенту была оказана поддерживающая терапия в виде 2 курсов ВВИГ и эритроцитов (эритроцитов).Перед выпиской уровень гемоглобина повысился до 8,7 г / дл, а уровень тромбоцитов — 34 x 10 3 / мкл. Первоначально ее ТТГ составлял 233 мкг [МЕ] / мл, который снизился до 87 мк [МЕ] / мл после стационарного лечения 88 мкг левотироксина в день. Она продолжала снижать дозу стероидов в течение 21 дня.
У нее продолжались стойкие симптомы тромбоцитопении и микроцитарной анемии. Ей потребовалась повторная госпитализация из-за продолжительного носового кровотечения и меноррагии из-за тромбоцитопении с количеством тромбоцитов 2 x 10 3 / мкл во время стероидной терапии.Из-за рефрактерной реакции на стероиды и ВВИГ, несмотря на лечение гипотиреоза, гематологи начали лечение второй линии пероральным элтромбопагом. Зоб не уменьшился в размере, но ТТГ пациентки стабилизировался на уровне 4,51 мк [МЕ] / мл, а свободный Т4 — на уровне 0,9 нг / дл. Она улучшила количество тромбоцитов до 209 x 10 3 / мкл в течение 2 недель терапии элтромбопагом, и у нее не было симптомов. Врач-подросток также начал принимать оральные противозачаточные таблетки для регулирования менструального цикла. Поскольку количество тромбоцитов у пациентки значительно улучшилось, гематология снизила дозу элтромбопага, и пациентка сохранила количество тромбоцитов в пределах 200-400 x 10 3 / мкл.
Это редкий педиатрический случай сосуществования ИТП и тиреоидита Хашимото, при котором тромбоцитопения не улучшилась при терапии первой линии ИТП, несмотря на достижение эутиреоидного состояния с помощью левотироксина. Первоначально она отреагировала кратковременным, минимальным улучшением количества тромбоцитов, что потребовало скорейшего решения о назначении терапии второй линии. Терапия второй линии обычно назначается пациентам с хронической ИТП (тромбоцитопения более 6 месяцев). Основываясь на ответе нашего пациента, мы могли бы предложить использование элтромбопага у пациентов с острой ИТП, которые не поддаются терапии первой линии.
Раскрытие информации
Нет значимого конфликта интересов, о котором следует заявлять.
Лечение гипотиреоза
Аутоиммунная болезнь Хашимото — наиболее частая причина недостаточной активности щитовидной железы, и этому есть несколько причин. В любом случае, лечение недостаточной активности щитовидной железы, хирургически удаленной железы или врожденно поврежденной или отсутствующей железы представляет собой замену гормонов щитовидной железы отпускаемым по рецепту препаратом для щитовидной железы.
Как работает щитовидная железа
Как только человек начинает прием препаратов, замещающих гормоны щитовидной железы, цели лечения становятся довольно простыми.К ним относятся:
- Нормализация уровня гормонов щитовидной железы, в частности тироксина (Т4) и тиреотропного гормона (ТТГ)
- Устранение симптомов гипотиреоза, таких как запор, утомляемость и непереносимость холода
- Прекращение и устранение любых эффектов, которые гипотиреоз может оказывать на различные системы органов (например, повышение уровня холестерина)
- Уменьшение размера зоба, если таковой имеется, как иногда бывает при болезни Хашимото
Левотироксин (T4)
Гипотиреоз лечится назначением пероральных препаратов гормона щитовидной железы (обычно левотироксина, препарата Т4).Дозировка должна быть достаточной, чтобы восстановить нормальный уровень гормона щитовидной железы, не вызывая токсичности из-за слишком большого количества гормона щитовидной железы.
Составы
Существуют разные составы Т4, производимые разными производителями.Хотя все одобренные FDA составы считаются подходящими, большинство экспертов рекомендуют придерживаться той же рецептуры, которую вы начинаете, поскольку эквиваленты доз могут несколько различаться для разных препаратов.
В США левотироксин доступен в виде дженерика левотироксина, а также в виде фирменных таблеток Synthroid, Levothroid и Levoxyl.Тирозинт — это жидкая форма левотироксина в форме гелевых капсул, которая присутствует на рынке с 2011 года.
Дозирование
У молодых, здоровых людей врачи обычно начинают с того, что оценивается как «полная заместительная доза» Т4 (то есть доза, которая должна полностью восстановить нормальную функцию щитовидной железы). Полная заместительная доза оценивается в зависимости от массы тела и для большинства людей составляет от 50 до 200 мкг (мкг) в день.
У пожилых людей или людей с ишемической болезнью сердца начало заместительной терапии щитовидной железы обычно проводится более постепенно, начиная с 25-50 мкг в день и постепенно увеличиваясь.Взаимодействие с другими людьми
Администрация
Людям следует принимать Т4 натощак, чтобы предотвратить беспорядочное всасывание лекарства. Кроме того, врачи обычно рекомендуют принимать лекарство в первую очередь утром, а затем подождать не менее часа, чтобы позавтракать или выпить кофе. Прием лекарства перед сном, через несколько часов после последнего приема пищи, также работает и может быть более удобным подходом для некоторых людей.
Мониторинг
Уровни ТТГ контролируются, чтобы помочь оптимизировать дозу Т4.ТТГ вырабатывается гипофизом в ответ на уровни гормонов щитовидной железы. Поэтому, когда уровни гормонов щитовидной железы низкие (например, при гипотиреозе), уровни ТТГ реагируют повышением, пытаясь «вытолкнуть» больше гормонов щитовидной железы из щитовидной железы. .
При адекватном лечении гипотиреоза уровень ТТГ обычно падает до нормального диапазона. Итак, опорой при определении лучшей дозы Т4 является измерение уровня ТТГ.
Хотя симптомы гипотиреоза обычно начинают исчезать в течение двух недель после начала лечения, для стабилизации уровня ТТГ требуется около шести недель.Вот почему уровень ТТГ обычно измеряется через шесть недель после начала лечения.
Если уровни ТТГ остаются выше целевого диапазона, доза Т4 увеличивается примерно на 12-25 мкг в день, и уровни ТТГ повторяются еще через шесть недель. Этот процесс продолжается до тех пор, пока уровень ТТГ не достигнет желаемого диапазона и симптомы не исчезнут.
Как только оптимальная доза Т4 определена, уровни ТТГ измеряются каждый год или около того, чтобы убедиться, что лечение остается оптимальным.
Лиотиронин (T3)
Хотя стандартный подход к лечению гипотиреоза (заместительная терапия Т4) работает для большинства людей, некоторые люди продолжают испытывать симптомы.
Согласно исследованию 2016 года, опубликованному в журнале Journal of Clinical Endocrinology and Metabolism , около 15% людей с гипотиреозом в Соединенных Штатах продолжают чувствовать себя плохо, несмотря на лечение от этого заболевания.
Некоторые врачи могут рассматривать лиотиронин (Т3) в качестве дополнительного лечения для отдельных лиц, хотя это является предметом споров.Взаимодействие с другими людьми
Противоречие
Т4 — основной циркулирующий гормон щитовидной железы, но не активный гормон. Т4 превращается в Т3 в тканях по мере необходимости. А Т3 — это гормон щитовидной железы, который выполняет всю работу. Т4 — это просто прогормон — хранилище потенциальных Т3 и способ убедиться, что достаточно Т3 может быть создано ежеминутно по мере необходимости.
Когда врачи назначают Т4, а не Т3, они «доверяют» тканям человека с гипотиреозом преобразовать нужное количество Т4 в Т3 в нужном месте и в нужное время.
Однако появляются новые данные, свидетельствующие о том, что, по крайней мере, у некоторых людей с гипотиреозом отсутствует эффективное преобразование Т4 в Т3. Другими словами, несмотря на то, что их уровни Т4 могут быть нормальными, их уровни Т3 могут быть низкими. , особенно в тканях, где Т3 действительно выполняет свою работу.
Почему преобразование Т4 в Т3 может быть ненормальным у некоторых людей, на данный момент в значительной степени является предположением, хотя по крайней мере одна группа пациентов была идентифицирована с генетическим вариантом (в гене диодиназы 2), который снижает преобразование Т4 в Т3.
В любом случае, похоже, что врачи должны лечить по крайней мере некоторых людей (хотя, скорее всего, небольшую группу), у которых есть гипотиреоз как с T4, так и с T3.
Составы
Лиотиронин представляет собой синтетическую форму Т3, и он доступен в производственной форме под торговой маркой Cytomel, а также как общий лиотиронин. Т3 также может быть смешан.
Дозирование
Дать соответствующие дозы Т3 сложнее, чем правильно дозировать Т4.Т4 неактивен, поэтому, если вы дадите слишком много, немедленного прямого воздействия на ткани не будет. Другое дело, что Т3 — это активный гормон щитовидной железы. Таким образом, если вы дадите слишком много Т3, вы можете напрямую вызвать гипертиреоидный эффект — например, риск для людей с сердечными заболеваниями.
При добавлении Т3 к Т4 во время заместительной терапии щитовидной железы большинство экспертов рекомендуют назначать соотношение Т4: Т3 от 13: 1 до 16: 1, что является соотношением, которое существует у людей без заболеваний щитовидной железы.
Мониторинг
У людей, принимающих комбинированную терапию Т4 / Т3, врачи обычно проверяют уровень ТТГ через шесть недель после начала лечения. Уровни Т3 обычно не проверяются, поскольку доступные в настоящее время составы Т3 приводят к широким колебаниям уровня Т3 в крови в течение дня.
Экстракт сушеной щитовидной железы
Высушенный экстракт щитовидной железы содержит как тироксин (Т4), так и трийододтиронин (Т3), и его получают из щитовидной железы свиней.Взаимодействие с другими людьми
Составы
Несколько марок сушеной щитовидной железы доступны по рецепту в Соединенных Штатах и в некоторых других странах, включая Nature thyroid, WP Thyroid, Armor Thyroid, общий NP Thyroid (производства Acella) и канадский природный тироид от производителя Erfa.
Важное примечание
Хотя высушенный экстракт щитовидной железы доступен по рецепту, врачи его редко рекомендуют, так как нет научных доказательств, что он имеет какие-либо преимущества перед синтетическим Т4.
Более того, соотношение Т4 и Т3 в обезвоженном экстракте щитовидной железы (примерно 4: 1) не такое же, как у человека (примерно четырнадцать: 1). Другими словами, хотя высушенный экстракт щитовидной железы часто называют «естественным», его соотношение гормона Т4 к Т3 не соответствует физиологии человека.
Для младенцев
У младенца с диагнозом врожденный гипотиреоз цель состоит в том, чтобы восстановить уровни щитовидной железы до нормальных значений как можно быстрее и безопаснее. Чем быстрее нормализуется уровень щитовидной железы, тем нормальнее развиваются когнитивные и двигательные навыки ребенка.
Левотироксин — препарат выбора при врожденном гипотиреозе.
Администрация
Часто младенцам назначают жидкую форму левотироксина. Важно не смешивать левотироксин с соевой детской смесью или какими-либо препаратами, обогащенными кальцием или железом. Соя, кальций и железо могут снизить способность ребенка правильно усваивать лекарство.
Если таблетки левотироксина даются младенцу, родители должны измельчить таблетку левотироксина и смешать ее с грудным молоком, смесью или водой, которую скармливают ребенку.
Мониторинг
Дети, получающие лечение от врожденного гипотиреоза, проходят регулярное обследование, часто каждые несколько месяцев, по крайней мере, в течение первых трех лет жизни.
Согласно Европейскому обществу детской эндокринологии, при врожденном гипотиреозе анализы крови на Т4 или свободный Т4 и ТТГ должны выполняться в следующие сроки:
- Каждые 1-3 месяца в течение первых 12 месяцев жизни
- Каждые 1–4 месяца в возрасте от 1 до 3 лет
- Каждые шесть-12 месяцев после этого до завершения роста
- Каждые две недели после начала лечения Т4 и каждые две недели до нормализации уровня ТТГ
- Через четыре-шесть недель после любого изменения дозы
- С более частыми интервалами, когда соответствие ставится под сомнение или получаются ненормальные результаты
Постоянный или пожизненный врожденный гипотиреоз может быть установлен путем визуализации и ультразвуковых исследований, показывающих, что щитовидная железа отсутствует или является эктопической, либо подтвержден дефект способности синтезировать и / или секретировать гормон щитовидной железы.
Если стойкий гипотиреоз не установлен, лечение левотироксином может быть прекращено на месяц в возрасте 3 лет и ребенок сдан повторно. Если уровень остается нормальным, предполагается преходящий гипотиреоз. Если уровни становятся ненормальными, предполагается постоянный гипотиреоз.
Тем не менее, дети с преходящим врожденным гипотиреозом, которые прекращают прием лекарств, должны проходить периодическое обследование и повторное обследование щитовидной железы, поскольку эти дети сталкиваются с повышенным риском развития проблем с щитовидной железой на протяжении всей своей жизни.Взаимодействие с другими людьми
Беременность
Чтобы защитить вашу беременность и здоровье вашего ребенка, очень важно, чтобы у женщины было достаточно гормона щитовидной железы на протяжении всей беременности.
До беременности
Согласно рекомендациям Американской тироидной ассоциации, доза заместительного препарата гормона щитовидной железы (левотироксина) для женщины с уже существующим гипотиреозом должна быть скорректирована так, чтобы ее уровень ТТГ был ниже 2,5 мМЕ / л до зачатия.Взаимодействие с другими людьми
Во время беременности
Традиционный референсный диапазон, используемый врачом для диагностики и лечения гипотиреоза, значительно уже во время беременности. Взаимодействие с другими людьми
Уровень ТТГ должен поддерживаться на следующих уровнях для каждого триместра:
- Первый триместр: от 0,1 до 2,5 мМЕ / л
- Второй триместр: от 0,2 до 3,0 мМЕ / л
- Третий триместр: от 0,3 до 3,0 мМЕ / л
Дополнительная альтернативная медицина (CAM)
В дополнение к традиционному лечению гипотиреоза с помощью замены гормонов щитовидной железы, внедрение привычек образа жизни, психофизических практик и диетические изменения в вашем медицинском обслуживании могут принести много пользы.Взаимодействие с другими людьми
Например, некоторые эксперты предполагают, что определенные позы йоги (в частности, стойки на плечах и перевернутые позы, когда ступни приподняты) могут быть полезны для притока крови к щитовидной железе или для снижения общего стресса, который способствует ухудшению симптомов гипотиреоза.
Более того, некоторые люди считают, что управляемая медитация полезна для щитовидной железы, как и другие стратегии снижения стресса, такие как молитва, нежная йога, тай-чи и рукоделие.
Самолечение
Важно отметить, что самолечение проблемы с щитовидной железой с помощью добавок и / или внесение некоторых изменений в рацион — не лучшая идея.Лечение недостаточной активности щитовидной железы — сложный процесс, требующий тщательного контроля симптомов и дозирования со стороны врача.
Также имейте в виду, что добавки не регулируются государством, а это означает, что нет научного консенсуса относительно их безопасности и эффективности. Другими словами, то, что добавка «натуральная» или доступна без рецепта, не обязательно означает, что она на самом деле безвредна.
Важно с самого начала открыто и честно рассказать своему врачу об использовании дополнительных методов лечения, чтобы вы могли убедиться, что ничто из того, что вы делаете (или не хотите попробовать), не помешает вашему уходу за щитовидной железой.
Наконец, хотя некоторые практикующие холистики или CAM могут порекомендовать подходы для поддержки вашей щитовидной железы, иммунной и гормональной систем, важно с осторожностью относиться к любому продукту, который продается как «лекарство» от вашей болезни, или к продукту, который, как говорят, не имеет побочные эффекты.
Диагностика и лечение гипотиреоза и тиреоидита у собак (Материалы)
Причины гипотиреозаГипотиреоз приводит к снижению выработки тироидных гормонов тироксина (Т4) и трийодтиронина (Т3) щитовидной железой.Считается, что не менее 95% случаев гипотиреоза у собак вызваны приобретенным первичным гипотиреозом. Разрушение щитовидной железы может быть результатом лимфоцитарного тиреоидита, идиопатической атрофии щитовидной железы или, в редких случаях, опухолевой инвазии. Вторичный гипотиреоз (дефицит ТТГ) хорошо описан у людей, но редко распознается у собак. Причины приобретенного вторичного гипотиреоза у собак включают неоплазию гипофиза и пороки развития гипофиза, такие как кистозный мешочек Ратке. Третичный гипотиреоз (дефицит TRH) у собак не зарегистрирован.
SignalmentУ любой породы может развиться гипотиреоз, однако некоторые породы, такие как золотистый ретривер и доберман, были подвержены более высокому риску в нескольких исследованиях. Предполагается, что у многих других пород есть предрасположенность к гипотиреозу. Собаки среднего возраста подвержены повышенному риску гипотиреоза. В одном исследовании средний возраст постановки диагноза составлял 7,2 года с диапазоном от 0,5 до 15 лет. Стерилизованные самки и кастрированные кобели имеют повышенный риск развития гипотиреоза по сравнению с неповрежденными половым путем животными.
Клинические признакиПоскольку гормоны щитовидной железы влияют на функции многих органов, гипотиреоз учитывается при дифференциальной диагностике широкого круга проблем. Клинические признаки гипотиреоза могут быть неспецифическими и незаметными в начале, и гипотиреоз обычно диагностируется неправильно. Общие клинические признаки, относящиеся к гипотиреозу, включают свидетельства снижения скорости метаболизма, такие как летаргия, умственная тупость, увеличение веса, нежелание выполнять упражнения и непереносимость холода.Дерматологические изменения также распространены. Проявления включают сухую чешуйчатую кожу, изменение качества или цвета волосяного покрова, алопецию, себорею (сухую или олеозную) и поверхностную пиодермию. Также могут возникать гиперкератоз, гиперпигментация, образование комедонов, гипертрихоз, церуминозный отит, плохое заживление ран, усиление синяков и микседема. Репродуктивная недостаточность и неврологическая дисфункция — менее частые проявления гипотиреоза.
Диагностика гипотиреозаКлиническое подозрение на гипотиреоз должно быть получено путем оценки сигналов, истории болезни и физического обследования, результатов гемограммы, биохимической панели и анализа мочи, а также измерения общей концентрации Т4.Тесты, которые могут использоваться для подтверждения диагноза, включают измерение концентрации свободного Т4 и ТТГ, провокационные тесты функции щитовидной железы и реакцию на добавление гормонов щитовидной железы. Выбор и интерпретация диагностических тестов во многом основаны на индексе подозрения на гипотиреоз.
Клиническая патология
Клинико-патологические изменения, которые обычно наблюдаются у собак с гипотиреозом, представляют собой нормоцитарную нормохромную нерегенеративную анемию, гипертриглицеридемию натощак и гиперхолестеринемию.
Базальные концентрации гормонов щитовидной железы
Двумя наиболее важными гормонами щитовидной железы, секретируемыми щитовидной железой, являются тироксин (Т4) и 3,5,3’трийодтиронин (Т3). Тироксин является основным секреторным продуктом щитовидной железы, тогда как большая часть сывороточного Т3 образуется в результате экстратироидного деиодирования Т4. И Т3, и Т4 являются белками, в высокой степени связывающимися с белками-носителями сыворотки, такими как тироид-связывающий глобулин, транстиретин и альбумин. Только несвязанный (свободный) гормон проникает через клеточные мембраны, связывается с рецепторами и обладает биологической активностью.Гормон, связанный с белком, действует как резервуар и буфер для поддержания постоянной концентрации свободного гормона в плазме, несмотря на быстрые изменения высвобождения и метаболизма Т3 и Т4, а также изменения концентрации белков в плазме. Свободный Т4 внутри клеток монодейодируется до Т3, который связывается с рецепторами и индуцирует клеточные эффекты гормона щитовидной железы.
Общая концентрация Т4
Общая концентрация Т4 — это наиболее часто выполняемое статическое измерение тироидных гормонов и хороший начальный скрининговый тест на гипотиреоз собак.В целом можно предположить, что у собаки с концентрацией Т4, находящейся в пределах нормы, функция щитовидной железы нормальная, однако базальная концентрация Т4 ниже нормы не является диагностическим признаком гипотиреоза. В этом случае животное может быть нормальным, иметь гипотиреоз или страдать не тироидным заболеванием с вторичным снижением базальной концентрации Т4 (синдром слабого эутиреоида). Такие факторы, как время суток, возраст, порода и температура окружающей среды, могут влиять на общую концентрацию Т4 без изменения метаболически активных концентраций свободных гормонов щитовидной железы.В одном исследовании 50-60% нормальных собак имели низкий общий уровень Т4 в сыворотке в какое-то время в течение дня. Эструс, беременность, ожирение, недоедание, экзогенные глюкокортикоиды и лекарства, такие как триметоприм / сульфаметоксазол, противосудорожные препараты, салицилаты и фенилбутазон, также могут изменять базальную концентрацию Т4. Системные заболевания, которые с большой вероятностью снижают базальную концентрацию Т4, включают гиперадренокортицизм, сахарный диабет, гипоадренокортицизм, почечную недостаточность, печеночную недостаточность и инфекции.Изменения в связывании с белками, снижение превращения Т4 в Т3, ингибирование секреции ТТГ и ингибирование синтеза тироидных гормонов щитовидной железой являются потенциальными механизмами снижения общей концентрации Т4 у больных эутиреоидных собак.
Концентрация свободного Т4
Поскольку биологически активна только несвязанная фракция сывороточного Т4, было выдвинуто предположение, что измерение свободного Т4 полезно для дифференциации эутиреоидных собак от гипотиреозных собак. Несмотря на полезность анализов свободного Т4 у людей, большинство одноэтапных твердофазных (аналоговых) коммерческих анализов свободного Т4, по-видимому, не превосходит измерение общего Т4 у собак, вероятно, из-за различий в сывороточных связывающих белках.Анализ свободного Т4, который использует стадию равновесного диализа (прямой диализ), имеет лучшую точность, чем аналоговые методы, а также более чувствителен и специфичен для диагностики гипотиреоза, чем общий Т4.
Общая концентрация Т3
Концентрация Т3 менее точна для отличия эутиреоидных собак от гипотиреоидных, поскольку концентрации Т3 колеблются в пределах и за пределы нормального диапазона даже больше, чем концентрации Т4 у эутиреоидных собак. Ложные измерения Т3 также могут происходить из-за присутствия антител против Т3, которые могут мешать коммерческим тестам на Т3.Антитела против Т3 в большинстве анализов приводят к ложно завышенным значениям Т3.
Концентрация ТТГ
Измерение концентрации ТТГ у собак полезно у собак с низкой общей концентрацией Т4, потому что низкий Т4 в сочетании с высоким ТТГ очень специфичен для диагностики гипотиреоза. Основным недостатком измерения ТТГ является отсутствие чувствительности для диагностики гипотиреоза у собак. Примерно у тридцати процентов собак с гипотиреозом концентрация ТТГ находится в пределах нормы.Причины отсутствия чувствительности неясны. Было высказано предположение, что текущий анализ ТТГ может измерять только определенные изоформы ТТГ. Другие возможности включают суточные колебания ТТГ, влияние сопутствующего заболевания или лекарств и истощение гипофиза.
Тест стимуляции ТТГ
Тест стимуляции ТТГ оценивает реакцию щитовидной железы на экзогенно вводимый ТТГ и является тестом на резерв щитовидной железы. Это точный тест функции щитовидной железы у собак, но его использование ограничено дороговизной и ограниченной доступностью ТТГ.Протокол требует сбора образца сыворотки для измерения базального Т4 с последующим внутривенным введением бычьего ТТГ в дозе 0,1 единиц / кг (максимальная доза 5 единиц). Второй образец для измерения Т4 собирают через 6 часов. Рекомбинантный ТТГ человека теперь также доступен, хотя и довольно дорог. Рекомендуемая доза составляет 75 мкг внутривенно при взятии проб через 0 и 4 часа. Результаты аналогичны результатам, полученным при использовании коровьего продукта, и этот продукт можно замораживать не менее 8 недель без потери активности.Результаты могут выявить нормальный ответ, притупленный ответ (синдром слабого эутиреоида) или отсутствие ответа (гипотиреоз).
Тест стимуляции ТРГ
У людей этот тест используется для оценки функции гипофиза (изменение ТТГ после введения ТРГ), однако у собак тест использовался для оценки функции щитовидной железы путем измерения изменения концентрации Т4 после Администрация TRH. К сожалению, изменение не такое большое, как после введения ТТГ, и у некоторых собак с нормальной функцией щитовидной железы реакция на ТТГ снижена.По этой причине клиническое применение этого теста ограничено. Сообщалось о различных протоколах с наиболее часто используемой дозой 0,1 мг / кг TRH, вводимой внутривенно, с образцами для измерения T4, собранными до и через 4-6 часов после введения TRH. Могут наблюдаться такие побочные эффекты, как слюноотделение, рвота, мочеиспускание, дефекация, миоз, тахикардия и тахипноэ. Недавние исследования показали, что более низкая фиксированная доза 100-600 мкг TRH внутривенно с образцами, собранными через 0 и 4 часа, так же надежна, как и более высокая доза, и с меньшей вероятностью приведет к побочным эффектам.
УЗИ щитовидной железы
Определение размера и объема щитовидной железы с помощью ультразвука также может быть полезным дополнительным тестом для дифференциации гипотиреоидных и эутиреоидных собак. Важно, чтобы исследование проводил опытный оператор.
Терапевтическое испытание
В некоторых случаях наиболее практичным подходом к подтверждению диагноза гипотиреоза является терапевтическое испытание. Это приемлемая практика, при условии, что соблюдаются следующие рекомендации: Перед началом терапевтического испытания необходимо предпринять все усилия, чтобы исключить не тироидное заболевание.Нет никаких доказательств того, что добавление гормонов щитовидной железы полезно для собак с эутиреоидным синдромом и может быть вредным. Добавку тироксина следует начинать с дозы 20 мкг / кг (0,1 мг / 10 фунтов) каждые 12 часов. Есть очень ограниченные исследования, подтверждающие сравнительную эффективность доступных препаратов тироксина у собак. Однако важно использовать продукт, с которым клиницист знаком и который дает последовательный ответ на его опыте. Небольшие различия между биодоступностью продукта не важны, если терапевтический мониторинг используется для определения окончательной дозы, однако рекомендуется использовать один и тот же продукт постоянно, а не часто менять торговую марку.Для оценки ответа на лечение следует использовать объективные критерии. В случае положительного ответа на лечение врач должен быть готов отменить терапию, чтобы подтвердить возвращение клинических признаков. Это гарантирует, что собаки с заболеваниями, связанными с заболеваниями щитовидной железы, не будут продолжать получать добавки для щитовидной железы на всю жизнь. Собаки с заболеваниями щитовидной железы — это те собаки, у которых клинические признаки улучшаются из-за неспецифических эффектов гормона щитовидной железы или не связанных с терапией. Если терапия безуспешна, следует проводить терапевтический мониторинг для выявления причины неудачи лечения.Поскольку неправильный диагноз является наиболее частой причиной неудач лечения, врач должен быть готов отказаться от лечения и поставить другие диагнозы.
Диагностика тиреоидитаАнтитела к тиреоглобулину
Антитела против тиреоглобулина (АТА) обнаруживаются у 42-59% собак с гипотиреозом и считаются результатом утечки тиреоглобулина в кровоток из-за лимфоцитов. тиреоидит. Коммерчески доступный анализ ELISA для ATA является чувствительным и специфическим индикатором тиреоидита, с ложноположительными результатами, полученными менее чем у 5% собак с другими эндокринными заболеваниями.Поскольку антитела к тиреоглобулину чаще встречаются у собак с гипотиреозом, чем у собак с эутиреоидом, их присутствие может быть полезно для интерпретации других тестов функции щитовидной железы. Однако важно понимать, что у эутиреоидных собак может наблюдаться положительный титр АТА. Доля эутиреоидных собак с АТА, у которых в конечном итоге разовьется гипотиреоз, неизвестна. В одном исследовании примерно у 20% эутиреоидных собак с тиреоидитом появились признаки дисфункции щитовидной железы в течение одного года. Небольшой процент собак (15%) стал отрицательным по АТА через 12 месяцев.Исследования в нашей лаборатории показывают, что вакцинация также может вызвать краткосрочный положительный результат на АТА. Неизвестно, могут ли другие переменные, такие как вирусные инфекции, также вызывать преходящий тиреоидит. Измерение АТА рекомендуется для скрининга племенного поголовья с целью окончательного исключения наследственных форм тиреоидита. Еще предстоит доказать, что это эффективный подход.
Антитела к Т3 и Т4
Антитела, направленные против Т3 и Т4, также встречаются при тиреоидите собак, хотя они менее распространены, чем АТА.Антитела против Т3 могут быть идентифицированы примерно у 30% собак с гипотиреозом. Также встречаются антитела против Т4, хотя они встречаются реже (15% собак с гипотиреозом). Однако, поскольку у некоторых эутиреоидных собак также могут быть антитела к Т3 или Т4, их наличие не является диагностическим признаком гипотиреоза. Однако при наличии других сомнительных результатов наличие антител к щитовидной железе увеличивает вероятность гипотиреоза. Поскольку сами по себе Т3 и Т4 являются небольшими молекулами, эти антитела к тиреоидным гормонам, вероятно, развиваются против Т3 и Т4, содержащих эпитопы тиреоглобулина.Антитироидные антитела чаще встречаются у гипотиреоза по сравнению с эутиреоидными собаками, а антитела наиболее распространены у молодых собак и у пород с высокой распространенностью гипотиреоза. Антитела, направленные против Т3 и Т4, могут мешать тестам на гормоны, приводя к ложному увеличению (наиболее часто) или снижению измеренной концентрации гормона. Теоретически эти антитела могут также повышать низкую концентрацию Т4 до нормального или высокого диапазона и приводить к ложному диагнозу эутиреоза или гипертиреоза.Антитела к щитовидной железе не влияют на реакцию на добавку щитовидной железы у собак с гипотиреозом.
Лечение гипотиреозаСинтетические гормоны щитовидной железы предпочтительнее продуктов животного происхождения, поскольку синтетические продукты (соли Т3 или Т4) более стабильны и лучше стандартизированы по активности. Левотироксин натрия (синтетический Т4) — первая добавка выбора для щитовидной железы. Левотироксин имеет период полувыведения из сыворотки крови 12-16 часов, а пиковые концентрации достигаются через 4-12 часов после приема.Рекомендации для начала терапии — введение левотироксина в дозе 20 мкг / кг два раза в день. Некоторым собакам в конечном итоге потребуется принимать добавки только один раз в день. Как только будет достигнут клинический ответ, можно будет начать испытание с терапией один раз в день. Некоторые авторы рекомендуют дозировку, исходя из площади поверхности тела (0,5 мг / м2). У животных с сопутствующим заболеванием сердца внезапное увеличение скорости основного обмена в связи с началом терапии может привести к дестабилизации сердца. Этим животным следует начать с 50% рекомендованной начальной дозы тироксина, а затем дозу скорректировать с помощью терапевтического мониторинга.
Введение синтетического триодтиронина показано только в тех немногих ситуациях, когда добавление Т4 не дало эффекта у собаки с подтвержденным гипотиреозом. Это может произойти из-за нарушения всасывания Т4 из желудочно-кишечного тракта. Добавки Т3 не рекомендуются для начальной терапии, потому что нормализуются только концентрации Т3 в сыворотке, в то время как уровни Т4 остаются низкими. Собаки, получающие добавку Т3, могут быть более восприимчивы к ятрогенному тиреотоксикозу, поскольку сывороточные концентрации Т4 важны для регуляции обратной связи гипоталамо-гипофизарно-тироидной оси.По схожим причинам следует избегать комбинированных продуктов, содержащих как Т3, так и Т4. Период полувыведения синтетического Т3 из плазмы составляет 5-6 часов, поэтому его нужно вводить три раза в день. Начальная доза составляет 4-6 мкг / кг каждые 8 часов.
Ответ на терапию
Клиническое улучшение должно наблюдаться через 4-6 недель после начала терапии, хотя улучшение уровня активности пациента может произойти в течение 1 недели. Для полного устранения дерматологических аномалий может потребоваться несколько месяцев, и первоначально внешний вид шерсти может ухудшиться по мере выпадения старых волос.Репродуктивные и клинико-патологические нарушения обычно разрешаются в последнюю очередь.
Плохой ответ на терапию
Отсутствующий или неадекватный ответ на терапию может быть вызван неправильным диагнозом, плохой комплаентностью владельца, неадекватной дозой добавок для щитовидной железы, плохой пероральной абсорбцией добавок для щитовидной железы или использованием добавок для щитовидной железы животного происхождения. Дефектное превращение Т4 в Т3 и устойчивость периферических тканей к действию гормона щитовидной железы являются теоретическими причинами неэффективности лечения, которые не были хорошо документированы у собак.
Терапевтический мониторинг
Мониторинг сывороточной концентрации Т4 и / или ТТГ позволит клиницисту определить причину отсутствия реакции на добавку щитовидной железы и позволит индивидуализировать дозу и частоту дозирования. Измерение концентрации Т4 в сыворотке крови следует проводить по крайней мере после одного месяца терапии. Образец сыворотки берут до и через 4-6 часов после лечения и отправляют для измерения концентрации Т4. Затем можно соответствующим образом скорректировать дозировку и частоту приема добавок для щитовидной железы.Измерение Т4 перед приемом таблетки должно быть в нормальном контрольном диапазоне, и обычно концентрация Т4 после приема таблетки немного выше контрольного диапазона (до 6 мкг / дл считается приемлемым). Если можно собрать только один образец, следует взять образец после приема таблетки. Полезность измерения концентрации ТТГ во время терапевтического мониторинга неясна, поскольку чувствительность анализа не позволяет выявить легкий гипертиреоз. Однако документальное подтверждение нормального уровня ТТГ будет дополнительным доказательством адекватного приема добавок.
Список литературыPanciera DL: Гипотиреоз у собак: 66 случаев (1987–1992). JAVMA 204: 761, 1994.
Dixon RM et al: Эпидемиологические, клинические, гематологические и биохимические характеристики гипотиреоза собак. Vet Rec 145: 481, 1999.
Jaggy A, et al: Неврологические проявления гипотиреоза: ретроспективное исследование 29 собак. J Vet Intern Med 8: 328, 1994.
Nachreiner RF и др.: Распространенность аутоантител к тиреоглобулину у собак с другими заболеваниями, не связанными с щитовидной железой.Am J Vet Res 59: 951, 1998.
Грэм П.А. и др.: Лимфоцитарный тиреоидит. Vet Clinics NA 31: 915, 2001.
Dixon RM et al: Эпидемиологические, клинические, гематологические и биохимические характеристики гипотиреоза собак. Vet Rec 145: 481, 1999.
Nachreiner RF, et al: Распространенность аутоантител к гормонам щитовидной железы в сыворотке крови у собак с клиническими признаками гипотиреоза. JAVMA 220: 466, 2002.
Peterson ME и др.: Измерение общего тироксина, трийодтиронина, свободного тироксина и тиреотропина в сыворотке для диагностики гипотиреоза у собак.JAVMA 211: 1396, 1997.
Scott-Moncrieff JC, et al: Концентрации тиреотропина в сыворотке у здоровых собак с гипотиреозом и эутиреоидных собак с сопутствующим заболеванием. JAVMA 212; 387, 1998.
Reese S, Breyer U, et al. Сонография щитовидной железы как эффективный инструмент для различения эутиреоидных собак и собак с гипотиреозом. JVIM 2005; 19: 491-498.
Bromel C, Pollard RE, et al. Ультрасонографическая оценка щитовидной железы у здоровых, гипотиреозных и эутиреоидных золотистых ретриверов с другими заболеваниями.JVIM 2005; 19: 499-506.
Diaz Espineira MM, Mol JA, Peeters ME, et al. Оценка функции щитовидной железы у собак с низкой концентрацией тироксина в плазме. J Vet Int Med 2007; 21: 25-32.
Отделение хирургии — Узлы щитовидной железы
Увеличение щитовидной железы (зоб) и образования внутри нее (узелки) встречаются относительно часто. Они могут быть очевидны невооруженным глазом или могут быть обнаружены случайно при визуализации шеи, такой как сонограмма сонных артерий или КТ или МРТ позвоночника.Большинство зобов и узлов щитовидной железы не влияют на здоровье человека.
Интервью Медицинского центра UCSF с доктором Инсу Су: Лечение узлов и рака щитовидной железы
Обзор
Зоб и узелки щитовидной железы, вызывающие нежелательные симптомы или отрицательно влияющие на здоровье человека, требуют лечения, часто хирургического вмешательства на щитовидной железе. Эти ситуации включают:
- Большой зоб, вызывающий дискомфорт или затрудняющий дыхание или глотание.
- Многоузловой зоб, особенно зоб, сужающий дыхательные пути, пищевод или кровеносные сосуды.
- Узлы щитовидной железы, диагноз которых не установлен или которые считаются подозрительными на рак после биопсии.
- Узловой зоб, вызывающий гипертиреоз (гиперактивность щитовидной железы), при котором лечение радиоактивным йодом или антитероидными препаратами невозможно.
- Зоб или узелки злокачественные (рак щитовидной железы)
Тироидэктомия — это хирургическая процедура по удалению всей (полная тиреоидэктомия) или части щитовидной железы (частичная тиреоидэктомия).Пациентам может также потребоваться прием препарата левотироксин, перорального синтетического гормона щитовидной железы, после операции в зависимости от того, какая часть железы удалена.
Что такое зоб?
Зоб относится к увеличению щитовидной железы, органа в форме бабочки, обернутого вокруг передней и боковых сторон дыхательного горла (или трахеи) в нижней части шеи.
Щитовидная железа обычно размером с два больших пальца, соединенных вместе в форме буквы V.Он может увеличиваться, когда он неэффективен в производстве гормонов щитовидной железы, воспален или занят опухолями.
Увеличение щитовидной железы может быть генерализованным и гладким, так называемый диффузный зоб ; или он может стать больше из-за роста одной или нескольких отдельных шишек (узелков) внутри железы, узловой зоб .
Зоб может продолжать вырабатывать необходимое количество гормонов щитовидной железы, и в этом случае он называется эутиреоидным или нетоксичным зобом ; или зоб может развиться в условиях либо гиперпродукции гормона щитовидной железы, называемого токсическим зобом , либо неспособности производить достаточное количество гормонов щитовидной железы, называемого зобным гипотиреозом .
Что такое узелок щитовидной железы?
Узел щитовидной железы — это просто уплотнение или образование в щитовидной железе. Узлы щитовидной железы встречаются относительно часто; 6% взрослых женщин и 2% взрослых мужчин в США имеют узелки щитовидной железы, которые можно прощупать при осмотре. Более того, тщательный осмотр щитовидной железы с помощью сонографического изображения показывает, что у одной трети женщин и одной пятой мужчин в железах есть небольшие узелки.
Щитовидная железа может содержать только один узел ( одиночный узелок щитовидной железы или одноузловой зоб ) или несколько из них ( многоузловой зоб ).Узлы щитовидной железы могут быть твердыми, если они состоят из клеток щитовидной железы или других клеток или скопления накопленного гормона щитовидной железы, называемого коллоидом. Когда узелки содержат жидкость, они называются кистозными узелками. Они могут быть полностью заполнены жидкостью ( простых кист) или частично твердыми и частично жидкими ( сложных кист) .
Узлы щитовидной железы сильно различаются по размеру. Многие из них достаточно большие, чтобы их можно было увидеть и почувствовать ( пальпируемых узелков, ). Некоторые многоузловые зоб могут стать огромными, выпирая из шеи и над ключицами или распространяясь вниз в грудную клетку за грудиной, состояние, называемое субтернальным зобом .С другой стороны, большинство узлов щитовидной железы слишком малы, чтобы их можно было вообще увидеть или почувствовать, и их называют непальпируемыми узлами .
Такие маленькие узелки обнаруживаются, когда человеку проводят медицинскую визуализацию по какой-либо другой причине, например, сонограмму сонных артерий; компьютерная томография или МРТ шеи, головы или груди; или сканирование ПЭТ. Эти очень маленькие, случайно обнаруженные узелки щитовидной железы называются инциденталомами щитовидной железы.
Наконец, конечно, узелки щитовидной железы также можно классифицировать как доброкачественные или злокачественные в зависимости от того, имеют ли клетки, из которых они состоят, возможность распространяться за пределы щитовидной железы в соседние ткани или отдаленные части тела.Конкретные причины узелков щитовидной железы и способы их различения обсуждаются ниже.
Зоб многоузловой
Многоузловой зоб — это увеличенная щитовидная железа с зобом, состоящим из множественных узлов щитовидной железы. Узелки могут быть очень маленькими (часто всего несколько миллиметров) или большего размера (несколько сантиметров), и часто бывает доминирующий узелок. Ключевой вопрос заключается в том, являются ли узелки доброкачественными или злокачественными (злокачественными). Более подробно это обсуждается ниже.
Что делает щитовидная железа
Чтобы понять, почему развиваются некоторые типы зоба, сначала важно знать, какова нормальная функция щитовидной железы и как она регулируется. Щитовидная железа вырабатывает и выделяет в кровь два небольших химических вещества, называемых гормонами щитовидной железы: тироксин (T4) и трийодтиронин (T3) . Каждая из них состоит из пары связанных аминокислот тирозина, к которым присоединены четыре или три молекулы йода соответственно.
Йод, необходимый для выработки гормонов щитовидной железы, поступает из нашего рациона: морепродукты, молочные продукты, покупной хлеб и йодированная соль. После абсорбции йод в крови улавливается специальным насосом в клетках щитовидной железы, который называется симпортером йодида натрия. В щитовидной железе также есть несколько специализированных биохимических «связывающих машин», называемых ферментами, которые затем выполняют шаги, необходимые для присоединения йода к определенным частям очень большого белка, называемого тиреоглобулином, который производится только клетками щитовидной железы.
Некоторая часть этого тиреоглобулина с присоединенными молекулами йода хранится в железе в виде липкой пасты, называемой коллоидом , которая обычно располагается в центре фолликулов, которые представляют собой шары щитовидной железы с полым центром.
Регулируемое количество гормонов щитовидной железы постоянно отделяется от тиреоглобулина и выделяется в кровь для доставки в ткани по всему телу. В ядре почти каждой клетки гормоны щитовидной железы связываются с молекулами, называемыми рецепторами Т3, которые прикреплены к сегментам ДНК, которые регулируют определенные гены.Точный контроль того, сколько белков произведено из этих генетических схем, поддерживает нормальное или эутиреоидное состояние щитовидной железы. Чрезмерная активация этих генов аномально высокими уровнями гормонов щитовидной железы вызывает гипертиреоз; неадекватная активация генов из-за недостаточного производства гормонов щитовидной железы вызывает гипотиреоз.
Обычно щитовидная железа вырабатывает нужное количество гормонов под строгим контролем гипофиза, который является продолжением мозга. Специализированные клетки гипофиза вырабатывают тиреотропный гормон (ТТГ), который перемещается с кровью в щитовидную железу, где ТТГ связывается со своими собственными рецепторами на клетках щитовидной железы, побуждая их расти и производить больше гормонов щитовидной железы.Обычно эта система поддерживается в равновесии за счет отрицательной обратной связи гормонов щитовидной железы с секретирующими ТТГ клетками гипофиза (а также с той частью мозга, которая их контролирует).
Причины зоба
Три категории проблем являются причиной почти всех случаев увеличения щитовидной железы: неэффективное производство гормонов щитовидной железы, воспаление железы и опухоли щитовидной железы:
- Когда железа неэффективна в производстве достаточного количества гормона щитовидной железы, она компенсирует это за счет увеличения.Во всем мире наиболее распространенной причиной является дефицит йода в рационе , состояние, которое, по оценкам, все еще поражает 100 миллионов человек, живущих в бедных обществах. Йод является важным строительным материалом для гормонов щитовидной железы; при отсутствии адекватного питания железа становится больше.
Когда более 10% населения страдает зобом из-за йодной недостаточности, это называется эндемическим зобом . Другие последствия тяжелого дефицита йода включают гипотиреоз и кретинизм, синдром умственной отсталости, низкий рост, глухоту и характерные лицевые деформации, которые поражают детей, рожденных от гипотиреозных матерей в регионах с дефицитом йода.(Для получения дополнительной информации см. Веб-сайт Международного совета по проблемам йододефицитной недостаточности: www.iccidd.org.)
Люди с дефектами в их генетических схемах белков, которые позволяют щитовидной железе производить гормон щитовидной железы (например, мутации в молекулярной насос, который позволяет щитовидной железе концентрировать йод внутри себя), как правило, приводит к развитию зоба. Некоторые лекарства также могут нарушать нормальную функцию щитовидной железы и приводить к компенсаторному увеличению железы, например карбонат лития, который вызывает зоб у 10% людей, принимающих это лекарство.
- Воспаление щитовидной железы ( тиреоидит ) может вызвать отек железы. Некоторые формы воспаления щитовидной железы довольно распространены, например, аутоиммунный тиреоидит и безболезненный (послеродовой) тиреоидит. Аутоиммунный тиреоидит (также называемый тиреоидитом Хашимото) возникает, когда иммунная система человека обращается против его собственной щитовидной железы, вызывая ее воспаление, обычно вызывая набухание железы и часто делая ее неактивной.
Аутоиммунный тиреоидит может впервые появиться у детей и молодых людей, но его заболеваемость резко возрастает у людей среднего и пожилого возраста.К другим типам тиреоидита, вызывающего зоб, относятся: 1. безболезненный (послеродовой) тиреоидит, самоограничивающееся воспаление щитовидной железы, которое может исчезнуть без лечения и затрагивает не менее пяти процентов женщин в течение года после беременности; 2. подострый тиреоидит, вызывающий болезненное увеличение щитовидной железы в результате вирусной инфекции; и 3. другие более редкие формы инфекционного тиреоидита; и 4. лекарственный тиреоидит, например, вызванный амиодароном и интерфероном альфа; и 5. редкое фиброзное заболевание, называемое тиреоидитом Рейдела.(Для получения дополнительной информации см. Knol по тиреоидиту.)
- Зоб может быть результатом опухолей щитовидной железы, которые обычно доброкачественные, но иногда и злокачественные. Большинство опухолей щитовидной железы представляют собой отдельные узелки, но есть несколько видов рака щитовидной железы, которые могут вызывать общий отек железы. К ним относятся инфильтрирующий папиллярный рак щитовидной железы, лимфома и анапластический рак щитовидной железы. Некоторые факты заставляют задуматься о том, что зоб может быть злокачественным.
К ним относятся один или несколько из следующих симптомов: быстрое увеличение зоба в течение нескольких недель, появление новой боли, связанной с щитовидной железой, затрудненное глотание, одышка или кашель с кровью; или зоб у кого-то с факторами риска рака щитовидной железы, например, у человека, у которого в детстве было облучение шеи или у кого-то есть близкий родственник с раком щитовидной железы. (См. Ниже и кнол по раку щитовидной железы.)
Таблица 1. Причины, особенности и методы лечения некоторых распространенных причин зоба
| Тип зоба | Причина | Типичные симптомы и признаки |
|---|---|---|
| Дефицит йода (эндемический зоб) | Недостаточное потребление йода с пищей | Увеличение щитовидной железы (зоб) |
| Болезнь Грейвса (диффузный токсический зоб) | Аутоиммунная стимуляция щитовидной железы | Зоб |
| Аутоиммунный тиреоидит (Хашимото, хронический лимфоцитарный) | Стойкое воспаление иммунной системы собственной щитовидной железы человека | Зоб |
| Подострый тиреоидит (болезненный, по де Кервену) | Вирусная инфекция | Болезненная, болезненная и опухшая железа |
| Токсическая аденома и токсический многоузловой зоб | Доброкачественная опухоль (опухоли) щитовидной железы | Узловой зоб |
| Зоб и узлы щитовидной железы с подозрением на злокачественное новообразование | Злокачественные опухоли щитовидной железы | Нет симптомов |
Причины узелков щитовидной железы
Узлы щитовидной железы, образования в щитовидной железе, могут быть результатом чрезмерного роста доброкачественных клеток (аденоматозная гиперплазия) или фактических дискретных опухолей, состоящих из клеток щитовидной железы, которые могут быть доброкачественными или злокачественными.Узлы щитовидной железы иногда могут содержать жидкость, которая обычно собирается из-за кровотечения из хрупких кровеносных сосудов при опухолях щитовидной железы, так называемая кистозная дегенерация. Это событие иногда вызывает внезапное появление боли и отека в передней части шеи, который обычно проходит в течение нескольких дней.
К счастью, более 90% узлов щитовидной железы не являются раком, но злокачественность следует учитывать у каждого пораженного человека. Часто пациентов с небольшими узелками щитовидной железы, менее 1 см в диаметре и отсутствием факторов риска рака щитовидной железы, можно просто повторно обследовать или визуализировать с помощью сонографии, чтобы убедиться, что узелок не увеличивается.Для более крупных узелков обычно указываются дополнительные исследования, как описано ниже.
Ключевые проблемы при зобе и узлах щитовидной железы
Каждый раз, когда у человека появляется зоб или узелок щитовидной железы, необходимо ответить на три вопроса.
- Железа или ее часть настолько велики, что растягивают, сжимают или вторгаются в близлежащие структуры?
Набухание щитовидной железы может вызывать ощущение стянутости или, что реже, боли в передней части шеи.Зоб или узелок могут сдавливать дыхательное горло (трахею), вызывая кашель или одышку, в то время как давление на глотательную трубку (пищевод) может вызвать дискомфорт при глотании или даже невозможность опустить что-либо. Когда зоб распространяется вниз в грудную клетку, кровь, возвращающаяся из шеи и головы, может быть частично заблокирована, что приводит к вздутию шейных вен. Когда зоб или узелок вызваны раком, опухоль может фактически прорасти в близлежащие структуры, вызывая боль, охриплость при поражении нервов голосового аппарата или кашель с кровью при проникновении в трахею.
- Железа функционирует нормально, гиперактивна или понижена?
Зоб — характерный признак всех распространенных форм гипертиреоза. Например, при гипертироидной болезни Грейвса обычно бывает диффузный или генерализованный зоб; а при токсических аденомах и токсическом многоузловом зобе в железе встречаются одиночные и множественные узелки соответственно. Люди с гипертиреозом, вызванным безболезненным тиреоидитом или подострым тиреоидитом, также обычно имеют умеренный диффузный зоб.И наоборот, люди с гипотиреозом часто болеют зобом. Например, наиболее частая причина гипотиреоза, аутоиммунный тиреоидит, обычно вызывает диффузное увеличение железы, которое в 1,5–3 раза превышает нормальный размер. Следовательно, функция щитовидной железы должна быть оценена у всех пациентов с зобом или узлом щитовидной железы. Лучшим тестом для скрининга обоих состояний является концентрация тиреотропного гормона (ТТГ) в сыворотке крови, которая снижена до низкого уровня у людей с гипертиреозом и повышена у людей с гипотиреозом.
- В-третьих, причиной зоба или узла щитовидной железы является злокачественная опухоль? К счастью, у большинства пациентов с зобом или узлом щитовидной железы нет рака щитовидной железы. Часто другие признаки у пациента с зобом, такие как признаки гипертиреоидной болезни Грейвса, делают ненужным проведение дополнительных тестов для исключения рака. С другой стороны, почти каждый человек с узлом щитовидной железы более 1,0–1,5 см в диаметре должен быть обследован на предмет наличия рака щитовидной железы.Подход к этим диагностическим оценкам обсуждается ниже.
Ответ на эти три важных вопроса начинается со сбора определенных фактов об истории болезни человека и любых недавних симптомах. (Таблица 2)
Таблица 2. Ключевые проблемы, которые необходимо оценить у человека с зобом или узлом щитовидной железы
Пол и возраст | Зоб и узелки чаще встречаются у женщин и пожилых людей, но узелки у мужчин и моложе более склонны к раку |
Местные симптомы шеи | Отек или боль в передней части шеи |
Симптомы возможного распространения рака | Боль в костях в одной точке без облегчения |
Симптомы гипертиреоза | Похудание, непереносимость тепла, дрожащие руки, учащенное сердцебиение, бессонница, беспокойство, учащенное опорожнение кишечника — особенно если симптомы новые или постоянные |
Симптомы гипотиреоза | Увеличение веса, непереносимость холода, запор, очень сухая кожа, замедленное мышление, подавленное настроение, мышечные судороги — особенно если симптомы новые или постоянные |
Факторы риска рака щитовидной железы | Облучение шеи в детстве |
Диагноз
Врач при физикальном осмотре осмотрит признаки увеличения щитовидной железы: вся железа или узелок; его твердость, подвижность и нежность; и есть ли увеличение близлежащих лимфатических узлов.Врач также будет искать признаки избытка или недостатка гормонов щитовидной железы. Хотя анамнез и физикальное обследование иногда дают важные подсказки, почти всегда необходимо проводить дополнительные диагностические тесты, чтобы с уверенностью ответить на ключевые клинические вопросы.
Сонограмма щитовидной железы передает неслышимые звуковые волны в шею, а отраженные эхо-сигналы отражают щитовидную железу и окружающие ткани; это может подтвердить, что шишка на шее находится в щитовидной железе, показать, кистозная она или твердая, и точно измерить ее размер.Анализ крови на ТТГ может исключить все распространенные причины гипертиреоза и гипотиреоза.
Если ТТГ низкий, то есть вероятность, что у человека доброкачественная, но гиперфункционирующая аденома щитовидной железы; поэтому следующим шагом для этих людей часто является радионуклидное сканирование щитовидной железы, чтобы увидеть, действительно ли увеличение железы является «горячим» узлом. Это важно, потому что почти все раковые узлы щитовидной железы «холодные» при радионуклидном сканировании; К сожалению, так много доброкачественных узлов щитовидной железы, поэтому этот тест не очень полезен для людей, у которых еще нет низкого уровня ТТГ, предполагающего гипертиреоз.
Если ТТГ повышен, у человека, вероятно, недостаточно активна щитовидная железа, и ее увеличение может быть признаком аутоиммунного тиреоидита. Если ТТГ в норме или высокий, то большинству людей с узлом щитовидной железы более 1,0-1,5 см (1/2 дюйма) в диаметре, а также лицам с подозрительным зобом необходимо пройти тонкоигольную аспирационную биопсию для получения клеток щитовидной железы. цитологическая оценка экспертом-патологом.
Результаты биопсии щитовидной железы делятся на четыре категории.) Во-первых, это неадекватный образец, в котором просто недостаточно ткани щитовидной железы для постановки диагноза. Людям с этой находкой требуется повторная биопсия.
Во-вторых, и, к счастью, чаще всего отчет о биопсии доброкачественный. Люди с этой категорией узелков обычно не нуждаются в хирургическом вмешательстве и могут периодически осматриваться врачом, чтобы убедиться, что их зоб или узелок не увеличивается постепенно.
В-третьих, биопсия может убедительно предположить наличие рака щитовидной железы. Когда результаты биопсии являются злокачественными, в 95% случаев у человека действительно обнаруживается рак щитовидной железы при последующей операции, поэтому операция показана, если у человека нет других серьезных проблем со здоровьем.
Четвертая категория результатов биопсии щитовидной железы является неопределенной или неопределенной. Каждая пятая биопсия попадает в эту группу, в которой была получена адекватная ткань, но особенности наблюдаемых клеток просто недостаточно характерны для доброкачественного или злокачественного узелка, чтобы быть уверенным. Этой последней группе обычно также показано хирургическое вмешательство (см. Ниже), потому что среди людей с таким исходом биопсии у 15% окажется рак щитовидной железы после того, как узелок будет удален хирургическим путем и полностью обследован.
Лечение
Необходимость лечения зоба зависит от ответов на три ключевых клинических вопроса. Если щитовидная железа настолько велика, что вызывает симптомы из-за растяжения или сжатия соседних структур, или если она настолько велика, что выглядит некрасиво, может потребоваться хирургическое удаление щитовидной железы (тиреоидэктомия). Если зоб связан с состоянием, вызывающим гипертиреоз, как, например, болезнь Грейвса или токсический узловой зоб, лечение радиоактивным йодом может быть эффективным как для контроля гиперактивности железы, так и для уменьшения ее размера.
Некоторые нормально функционирующие (нетоксичные) узловой зоб можно уменьшить с помощью терапии радиоактивным йодом. Если щитовидная железа увеличена в результате аутоиммунного (Хашимото) тиреоидита и железа также недостаточно активна из-за высокого уровня ТТГ в крови, то начало приема гормонов щитовидной железы (L-тироксин) может одновременно лечить гипотиреоз и частично уменьшить железу.
Хирургический
Точно так же узелки щитовидной железы могут потребовать хирургического удаления или радиоактивного йода в зависимости от их размера и того, вызывают ли они гипертиреоз.Кроме того, узелки щитовидной железы, подозрительные на злокачественные новообразования, должны быть удалены вместе с остальной частью щитовидной железы, чтобы предотвратить распространение рака щитовидной железы.
Большинству людей с цитологически неопределенным результатом также рекомендуется удалить как минимум половину щитовидной железы с удаленным узлом, потому что у каждого седьмого из этих людей будет обнаружен рак щитовидной железы. Использование гормона щитовидной железы для восстановления работы щитовидной железы и уменьшения узлов щитовидной железы — часто предписываемое в прошлом — в настоящее время оказалось относительно неэффективным.
Преимущества и риски хирургии
Операция на щитовидной железе позволяет удалить половину (лобэктомия щитовидной железы или гемитиреоидэктомия) или всю щитовидную железу (полная тиреоидэктомия), чтобы с уверенностью установить, является ли зоб или узелок раком. Операция по удалению увеличенной щитовидной железы может уменьшить сдавление близлежащих структур и улучшить симптомы у пациентов с затрудненным глотанием, кашлем или одышкой. Хирургия щитовидной железы также может вылечить некоторые формы повышенной активности щитовидной железы, связанные с зобом или узелками.
Операция на щитовидной железе почти всегда требует госпитализации и анестезии. Разрез вызывает боль в течение одного или двух дней после операции и оставляет шрам, который обычно не виден через год. Как и при любой операции, кровотечение и инфекция могут осложнить операцию на щитовидной железе.
За щитовидной железой находятся два набора важных структур, которые могут быть случайно повреждены во время операции на щитовидной железе.Возвратные гортанные нервы проходят вдоль дыхательного горла на пути к голосовой коробке (гортани), где они контролируют мышцы, которые двигают голосовые связки. Если один из этих нервов перерезан, раздроблен или прекращено кровоснабжение, человек в определенной степени потеряет голос.
Этот паралич голосовых связок может привести к разнообразным изменениям голоса, от потери одной или двух октав во время пения до неспособности кричать и до сильно вырубающего шепота голоса. Если повреждены оба возвратных гортанных нерва, у человека может возникнуть затрудненное дыхание, и ему потребуется создать отверстие, соединяющее дыхательное горло с передней частью шеи (трахеостомия).
Четыре паращитовидные железы также расположены позади щитовидной железы: по две с каждой стороны. Если паращитовидные железы случайно удалены или повреждены, уровень кальция в крови пациента упадет, что приведет к покалыванию, онемению и мышечным спазмам. В редких случаях очень низкий уровень кальция может привести к спазму горла или судорогам. К счастью, эти осложнения необычны для опытного хирурга, специализирующегося на щитовидной железе; легкие травмы часто проходят спонтанно в течение нескольких дней или недель после операции; и есть методы лечения, которые могут улучшить положение.
Радиоактивный йод
Радиоактивный йод в основном используется для лечения зоба или узелка, когда он является причиной сверхактивной щитовидной железы. Радиоактивный йод также иногда используется для уменьшения гиперактивного зоба.
UCSF — крупный специализированный центр эндокринной хирургии. Эндокринные хирурги в UCSF выполняют большое количество операций на щитовидной железе с отличными результатами.
Для получения дополнительной информации о хирургии щитовидной железы
Посетите сайт обучения пациентов AAES
KoreaMed Synapse
Гипотиреоз — распространенное эндокринное заболевание, которое встречается у 2–3% населения в целом.1, 2) Терапевтическая цель гипотиреоза — восстановить клинический и биохимический эутиреоз путем адекватной замены гормонов щитовидной железы. Стандартным лечением гипотиреоза является введение левотироксина (L-T4) для нормализации уровня ТТГ в сыворотке крови. Этот подход был подтвержден гипотезой о том, что дейодиназа в периферических тканях может продуцировать адекватное количество активного трийодтиронина (Т3) из тироксина (Т4). Физиологически только 20% Т3 секретируется щитовидной железой, а 80% вырабатывается дейодиназой из Т4 в периферических тканях.Кроме того, L-T4 имеет длительный период полувыведения, что позволяет принимать его один раз в день и обеспечивать стабильные уровни T3. 3, 4)
Однако недавние исследования показали, что значительная часть пациентов, получавших монотерапию L-T4, имеет стойкие симптомы и жалобы, несмотря на нормализованные уровни ТТГ в сыворотке.1, 5, 6, 7) Это может быть связано с тем, что уровни Т3 в сыворотке могут быть недостаточными. нормализуется только при периферийном преобразовании T4-T3 8, 9)
Уровень Т3 в сыворотке может быть важным показателем для лечения гипотиреоза; однако в руководстве не рекомендуется измерять общий уровень Т3 в сыворотке или уровень свободного Т3 (fT3).3, 4) Уровни Т3 варьируются в зависимости от циркадных изменений или других заболеваний, и известно, что эффективность анализов, используемых для измерения уровня Т3 в сыворотке, неадекватна. .
В этом исследовании мы стремились оценить различия в параметрах гормонов щитовидной железы и взаимосвязь этих гормонов после лечения L-T4. Мы сравниваем уровни гормонов щитовидной железы у пациентов, получавших эутиреоидный L-T4 после тотальной тиреоидэктомии и терапии радиоактивным йодом (RAI), и у здоровых эутиреоидных контрольных субъектов.Гормоны щитовидной железы от пациентов, перенесших тотальную тиреоидэктомию и абляцию радиоактивным йодом, были получены исключительно из L-T4, и эти пациенты могли быть хорошими объектами для анализа изменений гормонов щитовидной железы при лечении L-T4. Уровни свободного Т4 (fT4) и fT3 в сыворотке измеряли с использованием двух наборов для анализа от двух разных компаний для проверки.
Объекты исследования
Мы ретроспективно проанализировали медицинские карты пациентов, перенесших тотальную тиреоидэктомию и абляционную терапию RAI и находившихся под наблюдением в Медицинском центре Асан в период с августа 2017 г. по сентябрь 2017 г.Мы нашли 70 пациенток с атиреозом, получавших эутиреоидный L-T4, с образцами остаточной крови в клинической лаборатории после измерения запрошенных анализов крови в амбулаторной клинике. После исключения 1 пациента, получавшего комбинированную терапию лиотиронином и L-T4, в это исследование были включены 69 пациентов, получавших монотерапию L-T4. Мы также ретроспективно нашли 90 здоровых женщин с образцами остаточной крови в качестве контроля. Все эти субъекты прошли плановое медицинское обследование в нашей больнице, и в течение того же периода у них был выявлен эутиреоз.Мы отбирали только субъектов в возрасте 20–80 лет без каких-либо заболеваний щитовидной железы, принимающих какие-либо лекарства, влияющие на функцию щитовидной железы, другие виды рака или какие-либо признаки хронического / острого заболевания. Уровни fT3 и fT4 в сыворотке ретроспективно анализировали у этих субъектов с использованием образцов остаточной крови с использованием двух наборов для анализа. Эутиреоз определялся как уровень ТТГ в сыворотке в нормальном диапазоне (0,4–5,0 мМЕ / л). Исследование было одобрено институциональным наблюдательным советом нашего учреждения. Информированное согласие было отклонено из-за ретроспективного характера этого исследования.
Лабораторные методы
Уровни ТТГ в сыворотке измеряли с помощью иммунорадиометрического анализа (B · R · A · H · M · S TSH 1 RIA kit; B · R · A · H · M · SGmbH, Henningsdorf) с функциональной чувствительностью 0,07 мЕд / л. . Уровни fT3 и fT4 в сыворотке измеряли с использованием двух разных наборов от двух разных компаний, соответственно. Функциональная чувствительность анализа наборов от компании A (Kit As) составляла 1,0 пмоль / л для fT3 и 2,34 пмоль / л для fT4. Функциональная чувствительность анализа наборов от компании B (Kit Bs) составляла 1.2 пмоль / л для fT3 и 5 пмоль / л для fT4.
Статистика
Для анализа данных использовались R studio (версия 3.1.2) и библиотеки R xlsx, lubridate, Survival, Car, Psy и gdata (R Foundation for Statistical Computing, http://www.R-
Характеристики субъектов
Характеристики для контроля (n = 90) и пациента (n = 69) показаны в таблице 1. Все испытуемые были женщинами, средний возраст пациентов составлял 55 лет. У всех участников был эутиреоз, а средний уровень ТТГ составил 2,50 мМЕ / л (IQR 1,60–3,45). Возраст и уровень ТТГ не различались между контрольной группой и пациентами (p = 0,139 и p = 0,739). Всем 69 пациентам была выполнена полная тиреоидэктомия с терапией аблацией RAI из-за папиллярного рака щитовидной железы, и у них не было доказательств статуса заболевания в течение медианы 9.3 года наблюдения.
Согласно набору As, медиана уровня fT4, fT3 и соотношения fT3 / fT4 у всех испытуемых составляла 1,5 нг / дл, 2,8 пг / мл и 0,19 соответственно. Уровень fT4 в сыворотке был достоверно выше у пациентов (p <0,001). Уровень fT3 в сыворотке и соотношение fT3 / fT4 были значительно выше в контроле (p = 0,047 и p <0,001). Согласно набору Bs, медиана уровня fT4, fT3 и соотношения fT3 / fT4 у всех испытуемых составляла 1,2 нг / дл, 3,6 пг / мл и 0,29 соответственно. Уровень fT4 в сыворотке крови был значительно выше у пациентов (p = 0.046) и соотношение fT3 / fT4 было значительно выше в контроле (p = 0,009), но уровень fT3 в сыворотке не отличался между группами. Несмотря на то, что уровень fT3 был ниже у пациентов, все уровни fT3 у пациентов находились в рекомендованном производителем референсном диапазоне.
Когда мы оценивали значения ICC гормонов щитовидной железы в соответствии с наборами, уровни fT4 в сыворотке показали умеренную надежность, а уровни fT3 в сыворотке показали хорошую надежность между различными наборами (таблица 2).
Взаимосвязь между ТТГ и свободным Т3, свободным Т4, соотношением свободного Т3 / свободного Т4
Мы оценили взаимосвязь между fT3, fT4, соотношением fT3 / fT4 и ТТГ в контрольной группе и группе пациентов.Как показано на рисунке 1, уровни fT3, измеренные обоими наборами As и Bs, представляют обратную корреляцию с уровнем TSH (tau = -0,16, p = 0,005 в наборе A и tau = -0,18, p = 0,001 в наборе B. ). Уровни fT4 также обратно коррелировали с уровнем ТТГ (tau = -0,11, p = 0,046 в наборе A и tau = -0,13, p = 0,026 в наборе B). Однако соотношение fT3 / fT4 не коррелировало с уровнем ТТГ (tau = -0,03, p = 0,584 в наборе As и tau = -0,03, p = 0,598 в наборе Bs) (Таблица 3).
|
Эти отношения отличались в группе пациентов от контрольной группы.В контрольной группе уровни fT3 в сыворотке были стабильными и не коррелировали с уровнем TSH (тау = -0,10, p = 0,18 в наборе A и тау = -0,06, p = 0,40). Уровни fT4 в сыворотке достоверно коррелировали с уровнем ТТГ (тау = -0,16, p = 0,049 в наборе A и тау = -0,16, p = 0,034). Однако в группе пациентов только уровни fT3 значимо коррелировали с уровнем ТТГ (тау = -0,22, p = 0,012 в наборе A и tau = -0,31, p <0,001 в наборе B) (таблица 3).
Когда мы оценивали значения AUC для соотношения fT3, fT4 и fT3 / fT4 для отделения группы пациентов от контрольной в обоих наборах, набор As показал более высокие значения, чем набор Bs, по всем параметрам гормонов щитовидной железы (таблица 4).
В этом углубленном анализе гормонов щитовидной железы мы обнаружили существенные различия в параметрах гормонов щитовидной железы и взаимосвязи этих гормонов между эутиреоидными пациентами с атиреозом и эутиреоидными здоровыми людьми. Уровни fT4 в сыворотке крови у пациентов с атиретозом были значительно выше, чем в контрольной группе. Напротив, сывороточные уровни fT3 были значительно ниже у пациентов с атиреозом, чем в контрольной группе, что привело к значительно более низкому соотношению fT3 / fT4 у пациентов с атиреозом. Этот феномен не отличался между двумя разными наборами.Наши результаты согласуются с предыдущими исследованиями7, 8, 11), а также предполагают, что конверсия периферического T3 из T4 может быть недостаточной для пациентов с атиреозом, леченных L-T4, для поддержания нормального уровня T3.5, 8, 12)
Взаимосвязь между уровнем ТТГ в сыворотке и уровнями fT4 или fT3 также различалась между группой пациентов и контрольной группой. У здоровых людей с эутиреоидом уровни fT3 в сыворотке были стабильными, и только уровни fT4 в сыворотке были обратно коррелированы с уровнем TSH в сыворотке. Однако уровни fT3 в сыворотке варьировали и обратно коррелировали с уровнем TSH в сыворотке у эутиреоидных пациентов с атиреозом, получавших L-T4.Эти отношения также не различались между двумя разными наборами. Эти результаты означают, что поддержание стабильных уровней Т3 важно для здоровых людей, а активность дейодиназы может положительно коррелировать с уровнями ТТГ в сыворотке для поддержания уровней Т3 у эутиреоидных здоровых субъектов, как сообщалось ранее.5, 9, 13) Однако у пациентов с атиреозом, эутиреоидом, отношения не восстанавливались даже при нормальном уровне ТТГ в сыворотке после достаточного лечения L-T4. Наши результаты показывают, что монотерапия L-T4 может не быть оптимальным методом замещения для некоторых пациентов с гипотиреозом, и предполагают возможные преимущества комбинации низких доз лиотиронина с L-T4.5, 6, 13, 14, 15). Необходимы дальнейшие хорошо спланированные проспективные исследования, чтобы прояснить наилучшее лечение послеоперационного гипотиреоза.
У эутиреоидных здоровых субъектов не только уровни fT3, но также отношения fT3 / fT4 были стабильными независимо от уровня TSH. Это открытие предполагает, что уровень fT3 или соотношение fT3 / fT4 может быть надежным индикатором индивидуального функционального статуса щитовидной железы у субъектов с функциональной щитовидной железой, и предполагают, что послеоперационный уровень fT3 в сыворотке или соотношение fT3 / fT4 может быть полезным биомаркером для выявления пациентов, у которых есть проблемы с преобразованием T4-T3.Предыдущее исследование показало, что уровни fT3 в сыворотке после тиреоидэктомии у пациентов с умеренно сниженным уровнем ТТГ были эквивалентны дооперационным уровням, а у пациентов с нормальным уровнем ТТГ были ниже, чем дооперационные уровни16)
Значения fT4 и fT3 в сыворотке, измеренные двумя разными наборами, соответствовали от умеренного до хорошего, но медианные уровни fT4 были выше с набором A, а средние уровни fT3 были выше с набором B (p <0,001 и p <0,001, данные не показаны) . Когда мы сравниваем гормоны щитовидной железы между пациентами и контрольной группой, гормоны щитовидной железы, измеренные с помощью набора As, показали более значительные различия с более высокими значениями AUC для отличия пациентов от контроля, чем те, которые измерялись с помощью набора B.Эти данные свидетельствуют о том, что уровни свободных гормонов щитовидной железы и их соотношение могут варьироваться в зависимости от методов анализа, и этот способ сравнения может быть полезен при выборе подходящих наборов для анализа.
В этом исследовании есть некоторые ограничения. Во-первых, количество субъектов в этом исследовании было небольшим, и в него были включены только женщины. В этом исследовании fT4 у эутиреоидных пациентов с атиреозом не был связан с ТТГ, что отличается от предыдущих исследований8, 13). Этот результат может быть необъективным из-за небольшого количества пациентов.Во-вторых, мы не измеряли самочувствие пациента или какие-либо биохимические параметры, указывающие на функцию щитовидной железы. В результате мы не смогли подтвердить клиническую значимость низких и изменчивых уровней fT3 и не смогли найти клинических признаков, связанных с низкими и переменными уровнями fT3 у пациентов с атиреозом. Однако наше исследование имеет преимущество в том, что мы измеряли уровни свободных гормонов щитовидной железы с помощью двух разных наборов одновременно. Различия в параметрах гормонов щитовидной железы между пациентами и контрольной группой были одинаковыми независимо от того, какой анализ использовался, и это подтвердило наши результаты.
В заключение, сывороточные уровни fT3 были значительно ниже и варьировались у пациентов с атиреозом, получавших L-T4, чем у здоровых с эутиреоидом пациентов контрольной группы. Эти данные свидетельствуют о том, что монотерапия L-T4 не может быть подходящим методом замены для некоторых пациентов с атиреозом для поддержания оптимального уровня T3. Необходимы дальнейшие исследования, чтобы найти более физиологичное лечение этих пациентов, но наши результаты предполагают возможную роль комбинации низких доз лиотиронина с L-T4 как лучшего лечения для них.
.

 1996; 23(1–2): 47–51.
1996; 23(1–2): 47–51. Iodide induces thyroid autoimmunity in patients with endemic goitre: a randomized, double-blind, placebo-controlled trial// Eur J Endocrinol. 1998; 139(3): 290–297.
Iodide induces thyroid autoimmunity in patients with endemic goitre: a randomized, double-blind, placebo-controlled trial// Eur J Endocrinol. 1998; 139(3): 290–297.
