ABC-медицина
При эубиозе (то есть в норме) микрофлора кишечника представляет собой оптимальное соотношение различных бактерий – кишечной палочки, лактобацилл, энтерококков и др., всего более 500 видов. Дисбактериозом называют дисбаланс микробов, который длится продолжительное время. Это очень распространенное состояние, встречающееся примерно у 90 % взрослых и 95 % детей.
При должной коррекции, которую может назначить только врач, дисбактериоз кишечника проходит, но при отсутствии лечения обычно переходит в более тяжелую, прогрессирующую форму. Данное бактериологическое состояние принято рассматривать в качестве проявления или осложнения какого-либо заболевания, чаще всего – желудочно-кишечного тракта.
Причины развития дисбактериоза
Гибель полезных бактерий, населяющих микрофлору кишечника, может быть связана с такими факторами, как:
- изменение функций желудка, поджелудочной железы или печени, приводящее к недостатку пищеварительных ферментов и появлению непереваренных остатков пищи, которые способствуют росту болезнетворных микробов;
- пониженный тонус гладкой мускулатуры кишечника или ее спазмы, возникающие в результате психического или физического стресса, хирургического вмешательства, вегетососудистой дистонии – все это приводит к нарушению передвижения пищевых масс;
- различные заболевания желудочно-кишечного тракта, такие как холецистит, гастрит, панкреатит и пр.
 , связанные с повышением кислотности или щелочности среды обитания бактерий, что влечет за собой изменение обмена веществ и клеточных мембран полезных микроорганизмов;
, связанные с повышением кислотности или щелочности среды обитания бактерий, что влечет за собой изменение обмена веществ и клеточных мембран полезных микроорганизмов; - неправильное пищевое поведение (диеты, недостаток кисломолочных продуктов и клетчатки, употребление консервантов) препятствует нормальному росту полезных микробов или провоцирует их уничтожение;
- наличие в кишечнике паразитов или болезнетворных микробов, чьи продукты жизнедеятельности убивают полезные микроорганизмы – обычно это связано с дизентерией, сальмонеллезом, вирусными заболеваниями и пр.;
- прием антибиотиков, пагубно действующих не только на вредных микробов, но и на полезных.
К факторам, повышающим риск развития дисбактериоза кишечника, относят постоянные стрессы и неблагоприятную экологию, от которых страдают жители современных мегаполисов.
Общая симптоматика
Симптомы дисбактериоза кишечника различаются по локализации дисбиотических изменений и степени их выраженности.
1 стадия
На данном этапе дисбаланс бактерий выражен слабо: пациента могут беспокоить небольшие расстройства кишечника. Обычно такое состояние связано с кратковременным воздействием на микрофлору, например, со сменой привычной пищи, напитков. После окончания воздействия провоцирующих факторов или привыкания к новым условиям баланс микрофлоры восстанавливается.
2 стадия
Прекращается производство кишечником необходимого количества ферментов, обеспечивающих нормальное пищеварение. В результате возникает процесс брожения, который проявляется болью и вздутием живота, горечью во рту, метеоризмом, запорами или, наоборот, диареей. Это могут быть симптомы как прогрессирующего дисбактериоза, так и развития заболеваний желудочно-кишечного тракта.
3 стадия
На этой стадии при воздействии большого количества патогенной флоры на стенки кишечника развивается воспалительный процесс.
4 стадия
Это состояние кишечника, при котором нормальная микрофлора практически полностью вытеснена болезнетворными микроорганизмами, что приводит к нарушению всасывания полезных веществ, развитию авитаминоза и даже анемии. Образующиеся в результате токсины попадают в кровь и провоцируют тяжелые аллергические реакции. Клинические проявления включают возникновение сыпи, экземы, крапивницы, возможно развитие астмы, бессонницы, хронической усталости. Пациент может жаловаться на проблемы с концентрацией внимания. При отсутствии своевременного лечения возникает угроза развития тяжелых кишечных инфекций.
Крайняя степень дисбактериоза – проникновение бактерий желудочно-кишечного тракта в кровь (бактериемия), в некоторых случаях – развитие сепсиса.
Диагностика дисбактериоза
Основная цель диагностики – определение вида микробов, заселяющих кишечник, и их количества. Как правило, используются следующие основные методы:
- бактериологическое исследование, на качество результатов которого влияют соблюдение сроков доставки и сохранности материала, а также условий культивирования разных видов бактерий;
- исследование метаболитов микрофлоры, которое основано на определении летучих жирных кислот, выделяемых микроорганизмами. Отличается точностью результатов, простотой и оперативностью выполнения.
При проведении диагностики и постановке диагноза учитывается также, что микрофлора кишечника индивидуальна для каждого человека. Ее состав может зависеть от возраста, потребляемой пищи и сезона. В связи с этим специалист основывается не только на результатах анализов, но и на дополнительных обследованиях, позволяющих выявить причину развития дисбактериоза.
Лечение дисбактериоза
Лечение дисбактериоза у взрослых зависит от причин и симптомов и назначается комплексно.
- устранение избыточности патогенных микроорганизмов;
- восстановление нормальной микрофлоры;
- улучшение процесса пищеварения;
- нормализацию моторики кишечника;
- стимулирование реактивности всего организма.
Помните, что назначить грамотное и эффективное лечение может только специалист. Чтобы получить квалифицированную консультацию, запишитесь на прием к врачу клиники «АВС-Медицина» по номеру +7 (495) 223-38-83
Дисбактериоз — причины, симптомы и лечение — Медкомпас
Дисбактериоз – это нарушение свойств и состава микрофлоры кишечника, которое оказывает негативное влияние на организм в целом. Заболевание встречается часто, болеют как дети, так и взрослые.
Симптомы болезни
Для дисбактериоза характерен большой диапазон тяжести симптоматики. У некоторых людей он протекает без жалоб, у других вызывает тяжелые расстройства здоровья. Дисбактериоз проявляется нарушениями в работе желудочно-кишечного тракта, кожными проявлениями и симптомами отравления организма.
Дисбактериоз проявляется нарушениями в работе желудочно-кишечного тракта, кожными проявлениями и симптомами отравления организма.
Наиболее частыми симптомами дисбактериоза является:
- Нарушение стула в виде запоров и поносов. Понос кашицеобразный, пенящийся, зловонный
- Дискомфорт и боль в животе
- Метеоризм
- Снижение аппетита
- Тошнота
- Изжога и отрыжка
- Неприятный запах изо рта.
Общие симптомы:
- Головные боли
- Слабость, недомогание
- Повышенная утомляемость
- Нарушение сна
- Похудение.
Кожные симптомы:
- Зуд кожных покровов
- Аллергические высыпания
- Сухость кожи.
Причины болезни
Наиболее частой причиной дисбактериоза является длительный и бесконтрольный прием антибиотиков. Антибактериальные препараты подавляют рост как «плохих микробов», так и «хороших». Кроме антибиотиков, дисбактериоз могут вызвать любые препараты, подавляющие иммунную систему: кортикостероиды, химио- и лучевая терапия.
Провоцирующим фактором в развитии дисбактериоза являются воспалительные заболевания органов пищеварения, а именно: хронические гастриты, панкреатит, холецистит, гепатит, цирроз печени, язвенная болезнь, дискинезия желчевыводящих путей.
Еще одной причиной является несбалансированное, однообразное питание, злоупотребление жирным и сладким, монодиеты, авитаминоз.
У детей до года, наиболее распространенными причинами дисбактериоза являются: раннее введение прикорма, инфекционные инфекции (особенно кишечные), глистные инвазии.
Диагностика
Диагностика дисбактериоза начинается с кабинета врача-гастроэнтеролога. Последний подробно расспрашивает пациента, узнает, какие жалобы беспокоят, когда они впервые появились, с чем пациент связывает развитие заболевания.
Далее следует осмотр кожи и слизистых.
Подтверждается (или опровергается) диагноз лабораторными методами исследования.
.
Для определения возможных нарушений функций ЖКТ назначается копрограмма– общий анализ кала. Исследования показывает: нарушения ферментативной и кислотообразующей функции желудка, патологию ферментативной функции кишечника и поджелудочной железы, нарушения функций печени и желчного пузыря, а также воспалительные явления желудочно-кишечного тракта.
Исследования показывает: нарушения ферментативной и кислотообразующей функции желудка, патологию ферментативной функции кишечника и поджелудочной железы, нарушения функций печени и желчного пузыря, а также воспалительные явления желудочно-кишечного тракта.
Осложнения
При отсутствии лечения дисбактериоза, возможен переход заболевания в более тяжелую форму. Не исключен риск развития осложнений, а именно:
- Развитие патогенной флоры
- Нарушение всасывания витаминов, минералов и микроэлементов
- Образование токсических веществ в кишечнике, которые, проникая в кровь, отравляют весь организм
- Нарушения местного иммунитета, снижение защитных свойств организма.
Кроме того, при отсутствии лечения, дисбактериоз может провоцировать развитие различных заболеваний – сахарного диабета, панкреатита, дискинезии желчного пузыря, желчекаменной болезни, иммунодефицита, псориаза, экземы и атопического дерматита.
Лечение болезни
Важнейшей частью терапии является лечение основного заболевания, послужившего провоцирующим фактором для развития дисбактериоза. Только в этом случае положительный эффект лечения не заставит ждать.
Только в этом случае положительный эффект лечения не заставит ждать.
Следующим этапом в лечении является прием препаратов, восстанавливающих нормальную микрофлору – пробиотиков и пребиотиков. Наиболее правильно подбирать препарат, чувствительный к высеянной флоре.
При наличии патогенной микрофлоры назначаются антибиотики и бактериофаги.
Во время лечения следует избегать приема препаратов, отрицательно действующих на желудочно-кишечный тракт.
Лекарство от дисбактериоза: как выбрать лучший препарат?
Лекарство от дисбактериоза должно быть направлено не только на снятие симптомов, но и благоприятно устранять патологическую микрофлору, которая вызывает это кишечное заболевание. Что такое дисбактериоз, и какие препараты эффективно справятся с ним?
Дисбактериоз. Симптомы
Когда состав микрофлоры кишечника по каким-либо патогенным причинам меняется, то наступает дисбактериоз – нарушение работы желудка и пищеварительной системы, в связи с появлением патогенной микрофлоры.
Здоровый кишечник богат полезными бактериями – бифидобактериями, лактобактериями, бактероидами. Данные микроорганизмы помогают в работе желудка, и имеет защитную функцию. При попадании нежелательных бактерий – стрептококков, протея, грибков рода кандида или стафилококков, происходит дисбаланс здоровой и патогенной микрофлоры.
В процессе борьбы этих двух групп за выживание, человек и ощущает на себе проявление дисбактериоза. Правильное лекарство от дисбактериоза восстанавливает работу кишечника, и человек вновь чувствует себя здоровым.
Но что это за симптомы? Во-первых, это – вздутие живота, болезненные ощущение в области кишечника, поносы, продолжительные запоры и неустойчивый стул (чередование проноса и запора). Также заболевание может проявляться в виде общей слабости и снижении работоспособности, постоянной усталости, снижении аппетита.
Причинами дисбактериоза могут быть следующие факторы:
- Нерациональное употребление антибиотиков;
- Кишечные инфекции;
- Болезни пищеварительных органов, такие как: гастрит, язвы, панкреатит;
- Перенесенные операции на органах пищеварения;
- Неправильное питание, недостаток природных витаминов в пище;
- Снижение иммунитета.

В случае возникновения заболевания после антибиотиков применяют лекарство от дисбактериоза, которые нормализируют микрофлору, уравновешивают баланс бифидобактерий.
Нарушение работы на фоне неправильного питания устраняется путем составления диеты, анализом образа жизни и его коррекции.
Лечение дисбактериоза
Лечение дисбактериоза проводится препаратами двух групп: пробиотики и пребиотики.
Пробиотики – лекарство от дисбактериоза, наиболее эффективные преператы, так как имеют высокую концентрацию бактерий, которые угнетают рост патогенных микроорганизмов. Эта группа представлена следующими препаратами: Бифидумбактерин форте (для ректального применения), порошок Пробифор, Флорин Форте в виде порошка и другие.
Пребиотики – механизм действия основан на процессе расщепления фруктозно-галактозного дисахарида на органические кислоты, что подавляет активность патогенной микрофлоры кишечника. Представители: Дюфалак, сироп Нормазе, Порталак, Ромфалак и другие.
Профилактика дисбактериоза
Для профилактики заболевания рекомендуется больше времени проводить на воздухе, употреблять свежие продукты, особенно в осенне-зимний период. Лучшее лекарство от дисбактериоза это правильно соблюденная диета и хорошее настроение. Стрессы могут провоцировать кишечные заболевания, и осознание этого факта позволяет эффективно справиться с заболеванием или вовсе его избежать.
Регулярные консультации у гастроэнтеролога — это верный способ всегда быть осведомленным о состоянии своего здоровья. Также, соблюдая правила питания и приема лекарств мы можем избежать появления дисбактериоза в нашей жизни.
Дисбактериоз кишечника — симптомы и лечение
Дисбактериоз кишечника – это заболевание, которое характеризуется нарушением соотношения и состава населяющих кишечник микроорганизмов.Без соответствующего лечения данное заболевание может привести к серьёзным нарушениям в работе желудочно-кишечного тракта.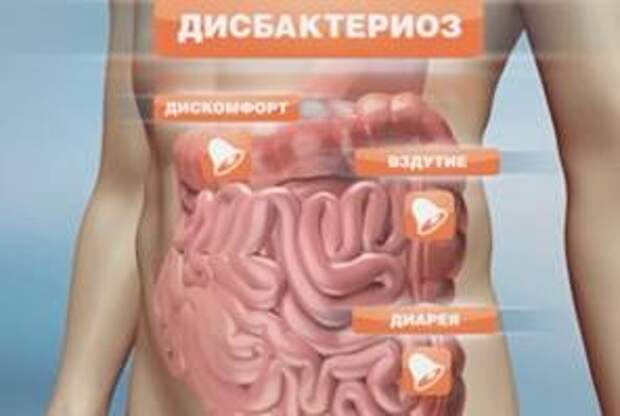
Причины появления дисбактериоза
Существует многоженство факторов, способных изменить нормальную микрофлору кишечника. Но чаще всего своим появление дисбактериоза связано с:
- Прием некоторых лекарственных средств: антибиотиков, слабительных, гормональных, психотропных и т.д.;
- Неправильное питание и злоупотребление алкоголем;
- Инфекционные заболевания;
- Хронические заболевания желудочно-кишечного тракта;
- Продолжительное психоэмоциональное перенапряжение;
- Аллергические заболевания
- Иммунодифициты.
Основные симптомы дисбактериоза
Симптомы дисбактериоза бывают идентичны симптомам других гастроэнтерологических заболеваний. При дисбактериозе могут беспокоить:
- Изменения стула: поносы, запоры или неустойчивый стул;
- Дискомфорт в животе, вздутие;
- Повышенное газообразование;
- Резкий запах стула;
- Тошнота;
- Боли в животе без четкой локализации;
- Аллергические реакции;
- Утомляемость, слабость.

Диагностика и лечение дисбактериоза
В первую очередь, для постановки диагноза необходимо провести анализ кала. Также врач может назначить: гастроскопию, ректороманоскопию, ирригоскопию, колоноскопию.
Лечение дисбактериоза кишечника проводится в комплексе и подразумевает: восстановление нормальной микрофлоры кишечника, улучшение пищеварения, восстановление моторики кишечника. Лекарственная терапия подразумевает прием антибактериальных препаратов и бактериальных, регуляторов пищеварения.
Лечение дисбактериоза у взрослых и детей
К какому специалисту следует обратиться, если у вас обнаружились симптомы Дисбактериоза?
Профилактика дисбактериоза
Профилактика дисбактериоза заключается в решении ряда проблем:
- Организация рационального питания;
- Контроль применяемых лекарственных препаратов;
- Улучшение экологической обстановки;
- Своевременное лечение заболеваний желудочно-кишечного тракта.

Лечение гастроэнтерологических заболеваний – одно из приоритетных направлений работы клиники «Семейная».
Запись на прием к врачу гастроэнтерологу
Обязательно пройдите консультацию квалифицированного специалиста в области гастроэнтерологии в клинике «Семейная».
Чтобы уточнить цены на прием врача гастроэнтеролога или другие вопросы пройдите по ссылке ниже
Лечение дисбактериоза кишечника
Дисбактериоз – это изменение состава микроорганизмов в кишечнике и развитие в нем патогенной микрофлоры. В результате в организме образуются опасные вещества, приводящие к его отравлению и возникновению процессов гниения.За последние годы дисбактериоз кишечника стал таким же распространенным недугом как простудные заболевания и аллергия. Почему это происходит именно с Вами и как вылечить эту неприятную болезнь раз и навсегда?
Общие сведения
В человеческом организме живет масса бактерий, которые выполняют множество полезных функций. Они синтезируют витамины, расщепляют растительную клетчатку и не дают размножаться патогенным микроорганизмам. Полезные бактерии незаменимы для человеческого организма, они переваривают пищу и участвуют в процессе усвоения микроэлементов.
Они синтезируют витамины, расщепляют растительную клетчатку и не дают размножаться патогенным микроорганизмам. Полезные бактерии незаменимы для человеческого организма, они переваривают пищу и участвуют в процессе усвоения микроэлементов.
Около 400 видов микроорганизмов населяют кишечник, общая масса которых достигает 3 кг!
Нормальная кишечная флора, состоящая из бифидобактерий и молочнокислых бактерий, обеспечивает оптимальное переваривание пищи, а также перерабатывает ненужные «отходы».
Состояние кишечной микрофлоры связано не только с заболеваниями желудочно–кишечного тракта, но и с такими заболеваниями, как атеросклероз и артериальная гипертония, мочекаменная болезнь и пиелонефрит, желчнокаменная болезнь и гепатиты.
Возникновение дисбактериоза
Под действием внешних факторов количество полезных микроорганизмов уменьшается, а вредных становится больше. Из-за изменения состава бактерий в кишечнике возникает дисбактериоз. Симптомы этого недуга проявляются в виде легкого недомогания, боли в области пупка, метеоризма. Может возникнуть непереносимость определенных продуктов, особенно это касается острой и жареной пищи.
Симптомы этого недуга проявляются в виде легкого недомогания, боли в области пупка, метеоризма. Может возникнуть непереносимость определенных продуктов, особенно это касается острой и жареной пищи.
Человек с дисбактериозом чувствует постоянную усталость, боли в животе, слабость, появляются боли в суставах, температура тела повышается, возникает расстройство стула. Организм начинает получать меньше витаминов, а обмен веществ ухудшается.
Если Вам знакомы эти симптомы, стоит немедленно обратиться к опытным специалистам за помощью. Важно понимать, что легкие недомогания при дисбактериозе могут перерасти в тяжелые расстройства здоровья, при которых кишечная стенка начнет пропускать токсины и аллергены, тем самым снижая барьерную функцию печени.
Эффективное лечение дисбактериоза у взрослых и детей
Патогенные микроорганизмы в кишечнике развиваются потому, что его барьерная защита напрямую зависит от здоровья желчного пузыря, печени поджелудочной железы, желудка.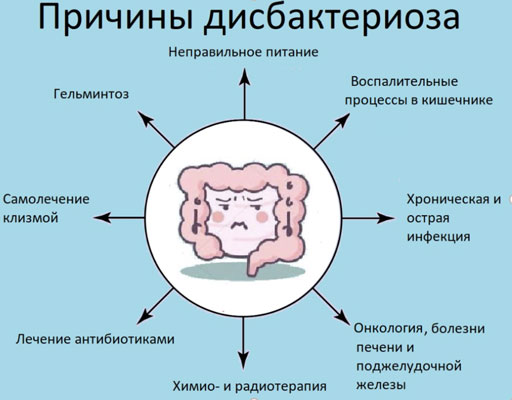 Если в этих органах ( чаще всего с самого детства) у человека присутствует хронический воспалительный процесс (часто это бывает без болевых симптомов см. раздел Лечение), нарушается выработка ферментов, желчи, что приводит к бродильным процессам в кишечнике и соответственно снижается его барьерная функция.
Если в этих органах ( чаще всего с самого детства) у человека присутствует хронический воспалительный процесс (часто это бывает без болевых симптомов см. раздел Лечение), нарушается выработка ферментов, желчи, что приводит к бродильным процессам в кишечнике и соответственно снижается его барьерная функция.
Лечение в клинике при помощи современной гомеопатии, направлено не только на восстановление гомеостаза толстого и тонкого кишечника, но и на лечение воспалительных процессов других органов пищеварения, мочеполовой системы, которая находится рядом и тоже может влиять на кишечник.
Это приводит к тому, что восстанавливается гомеостаз толстого и тонкого кишечника, который начинает вырабатывать макрофаги и антитела на патогенные микроорганизмы (хеликобактер, стафилококк, палочки, гельминты и т. д). Освободившись таким образом от патогенных организмов, толстый кишечник дает возможность развиваться полезным бактериям и сохраняет эту способность долгое время.
симптомы у взрослых, лечение по низким ценам в СПБ, отзывы
Лечение дисбактериоза кишечника
Медицинский центр «Долголетие» предлагает самые современные методы лечения дисбактериоза кишечника. Клиника оснащена всем необходимым оборудованием для диагностики этого заболевания. Ни для кого не секрет, что микрофлора кишечника – система, которую легко можно вывести из состояния равновесия. В таком случае микроорганизмы, участвующие в переваривании пищи, выработке некоторых витаминов, защите от инфекций, могут пострадать. Антибиотики, ослабление иммунитета, разнообразные инфекции и пищевые отравления – все это пагубно отражается на состоянии микрофлоры. И широко рекламируемые биокефиры, биойогурты и тому подобные продукты на самом деле не в состоянии помочь в лечении дисбактериоза кишечника.
Клиника оснащена всем необходимым оборудованием для диагностики этого заболевания. Ни для кого не секрет, что микрофлора кишечника – система, которую легко можно вывести из состояния равновесия. В таком случае микроорганизмы, участвующие в переваривании пищи, выработке некоторых витаминов, защите от инфекций, могут пострадать. Антибиотики, ослабление иммунитета, разнообразные инфекции и пищевые отравления – все это пагубно отражается на состоянии микрофлоры. И широко рекламируемые биокефиры, биойогурты и тому подобные продукты на самом деле не в состоянии помочь в лечении дисбактериоза кишечника.
Если человек принимал антибиотики (например, при ангине), то этот же препарат мог изменить концентрацию полезных микроорганизмов в кишечном тракте. Это, в свою очередь, дало возможность условно-патогенным бактериям, которые в норме обитают в организме, начать активно размножаться. Природа пустоты не терпит, и когда гибнет один микроб, постоянно живший на слизистой кишечника, на его место приходят другие. Соответственно, начинаются проблемы с пищеварением – метеоризмы, запоры, диареи (поносы). В этом случае требуется квалифицированное лечение дисбактериоза кишечника под наблюдением специалиста.
Соответственно, начинаются проблемы с пищеварением – метеоризмы, запоры, диареи (поносы). В этом случае требуется квалифицированное лечение дисбактериоза кишечника под наблюдением специалиста.
Точный анализ – залог правильного лечения хронического дисбактериоза кишечника
Для того чтобы точно знать, чем лечить, нужно определить причину заболевания и какие полезные микроорганизмы пострадали. Сами по себе лакто- и бифидобактерии не восстановят иммунитет. Их можно использовать в составе комплексного лечения дисбактериоза тонкого и толстого кишечника. Возможно, пациенту потребуется и антибиотикотерапия. Ведь у патогенных и условно патогенных бактерий могла возникнуть устойчивость (резистентность) к принимаемым ранее препаратам. И тогда антибиотикограмма может показать, какие группы лекарств эффективнее всего смогут уничтожить болезнетворных микробов.
Грамотный бактериологический анализ кишечника – залог качественного лечения дисбактериоза. В клинике «Долголетие» пациент гарантированно получит и то, и другое. К тому же, врачи центра могут оформить больничный лист.
К тому же, врачи центра могут оформить больничный лист.
Записаться на прием к врачу для полного обследования кишечника и последующего лечения дисбактериоза можно с помощью специальной формы на нашем сайте или по телефонам: (812) 671-01-70 и 575-09-22.
Лечение дисбактериоза кишечника в Самаре
Полноценное функционирование кишечника невозможно без работы микроорганизмов, участвующих в процессе переваривания пищи. Дисбактериоз – это нарушение микрофлоры, при котором количество полезных бактерий уменьшается, что осложняет работу желудочно-кишечного тракта и может спровоцировать другие заболевания.
Полезные микроорганизмы (бактероиды, бифидобактерии, лактобактерии) помогают бороться со стрептококком, стафилококком, грибками рода кандида, а также обеспечивают помощь в переваривании пищи.
Причины дисбактериоза
Причиной может стать прием курса антибиотиков, резкая смена рациона и ослабленный иммунитет. Также дисбактериоз может являться следствием заболеваний желудочно-кишечного тракта или отравления.
Также дисбактериоз может являться следствием заболеваний желудочно-кишечного тракта или отравления.
Симптомы дисбактериоза кишечника
- тошнота;
- понос;
- вздутие.
Даже небольшой дисбаланс через время может негативно сказываться на организме в целом. Поэтому следует посещать гастроэнтеролога, хотя бы один раз в полгода, для выявления нежелательных изменений на ранних стадиях.
Лечение дисбактериоза кишечника у взрослых и детей
Восстанавливать здоровый баланс микроорганизмов необходимо при помощи диеты и препаратов, нацеленных на восстановление микрофлоры вашего кишечника.
После успешного лечения важно не забывать следовать рекомендациям врача, чтобы закрепить результат, а далее избегать факторов, спровоцировавших появление дисбактериоза. Микрофлора крайне чувствительна, и спровоцировать повторное расстройство очень легко, если не соблюдать элементарные правила гигиены и здорового питания.
Записаться на прием к гастроэнтерологу в нашей клинике, Вы можете по телефону 8 (846) 300-40-72
Внимание! Информация, размещенная на сайте, носит ознакомительный характер. Более точную информацию Вы сможете получить у наших специалистов.
ДИСБИОЗ — Симптомы, причины и естественное лечение микробного дисбаланса
Дисбактериоз (также называемый дисбактериозом) — это нарушение микробного баланса внутри или на теле, подобное повреждению микробиоты. Во многом наше благополучие и иммунная система зависят от соотношения хороших и плохих бактерий в нашем организме, но особенно в пищеварительном тракте.
Пищеварительный тракт подобен нашему общему центру контроля здоровья и благополучия, который влияет на все, что происходит в других частях тела.
Исследования показали, что микробиота кишечника влияет не только на наше физическое тело, но и на функции мозга, настроения, чувства и страхи.
Следовательно, чрезвычайно важно поддерживать баланс между хорошими бактериями, то есть пробиотиками, и плохими бактериями. Однако кажется, что в настоящее время поддерживать баланс микробиоты организма практически невозможно. Почему это так, каковы симптомы, причины и последствия дисбактериоза и как лечить этот дисбаланс микробиоты естественным путем?
Однако кажется, что в настоящее время поддерживать баланс микробиоты организма практически невозможно. Почему это так, каковы симптомы, причины и последствия дисбактериоза и как лечить этот дисбаланс микробиоты естественным путем?
Быстрый ответ на этот вопрос заключается в том, что везде, но все же концентрация бактерий самая высокая во рту, на коже и в желудочно-кишечном тракте.Считается, что наша иммунная система зависит от того, что происходит в нашем пищеварительном тракте и кишечнике.
Считается, что бактерии в пищеварительном тракте не только поддерживают наше здоровье, но и влияют на уровень гормонов, метаболизм и настроение.
Мы, люди, впервые в жизни вступаем в контакт с бактериями во время рождения, где — на выходе мы получаем полезные бактерии и защитную микробиоту матери.
Таким образом, дети, рожденные от природы, обладают более сильной иммунной системой и защищены, например, от экземы и многих других заболеваний.
Бактерии во рту в значительной степени являются результатом того, что мы едим, и того, что мы оставляем на зубах после еды. Преобладание вредных бактерий во рту может вызвать гингивит, образование налета на зубах и другие заболевания мимов.
То есть само по себе то, что вы едите, также влияет на состояние ваших зубов, а не только на количество и продолжительность чистки.
Самыми распространенными вредными бактериями во рту являются Streptococcus mutans, Porphyromonas gingivalis и Tannerella forsythia.Хорошие — S. sanguinis, Actinomyces naeslundii и Veillonella dispar.
Бактерии на коже Кожа — самый большой человеческий орган, защищающий наше тело от внешних захватчиков. В коже человека и волосах на теле было обнаружено около 1000 различных типов бактерий. Однако большинство из них безвредны для нас или выгодны для обеих сторон. Хорошие бактерии на коже, такие как эпидермальный стафилококк, защищают поверхность кожи от бактериальных инфекций, которые могут быть вызваны вредными бактериями, живущими вне тела.
Другими словами, они постоянно работают над предотвращением заселения нашей кожей патогенными бактериями, высвобождения вредных для кожи химических веществ, борьбы за ресурсы кожи или воздействия на иммунную систему кожи.
Бактерии желудочно-кишечного трактаВ обмен на то, что полезные бактерии могут гнездиться на нашей коже, они защищают нас от дерматита, угрей, розацеа и других кожных заболеваний.
В кишечнике человека обитает большое количество различных микроорганизмов, которые наслаждаются идеальной температурой, кислотностью и питанием.Польза бактерий безумно велика и важна для нас. Без них наш организм не справился бы со многими задачами.
Некоторые из наиболее важных полезных бактерий — это Lactobacilli, Bifidobacterium и Caulobacter. Наиболее известными патогенными бактериями являются Salmonella, Vibrio Cholerae и Shigella.
Пищевое отравление — это пример преобладания вредных бактерий, но если у вас в желудке достаточно хороших бактерий, вы должны быстро выздороветь.
Хорошие бактерии (пробиотики) и пищеварительные ферменты также можно приобрести в Интернете.
Функции бактерий или микробиоты в желудочно-кишечном тракте- Переваривание пищи — Микрофлора расщепляет белки, углеводы и жиры. Сапрофитные бактерии образуют различные ферменты, повышающие активность пищеварительного тракта. Кислоты и газы, продуцируемые бактериями, способствуют нормальной работе кишечника и выделению фекалий, высвобождая таким образом их остатки из организма.
- Синтез и выработка некоторых полезных и важных веществ (витаминов, гормонов (более 20 различных), ферментов, элементов иммунной системы и др.)) — Витамины могут вырабатываться в организме только здоровой микрофлорой. Основные рабочие там — бифидобактерии, бактероиды, молочнокислые бактерии и кишечная палочка. E. coli может образовывать множество витаминов, таких как B1, B2, B6, PP, B12 и K. Бактерии в слепой кишке синтезируют большую часть витамина B12 и способствуют усвоению того же витамина, что и в мясных продуктах.
 Микрофлора также создает условия для всасывания жирорастворимых витаминов, таких как A, E и D. Это особенно важно у детей, поскольку у детей развивается авитаминоз, если микрофлора нарушена.
Микрофлора также создает условия для всасывания жирорастворимых витаминов, таких как A, E и D. Это особенно важно у детей, поскольку у детей развивается авитаминоз, если микрофлора нарушена. - Водопоглощение
- Защита организма и отпугивание опасных бактерий — E. coli (в основном) образуют бактерицидные и бактериостатические (подавляющие размножение бактерий) вещества, сходные по свойствам с антибиотиками. Таким образом, они предотвращают рост серьезных инфекционных заболеваний.
- Нейтрализация токсинов и вредных веществ
- Поддержание нормального уровня холестерина
- Поддержание нормального уровня кишечных газов
- Поддержание стабильного метаболического и гормонального баланса
- Предотвращение образования камней в органах и даже развития рака
- Развитие иммунитета — Кроме того, микрофлора кишечника участвует в формировании иммунитета, способствуя синтезу защитных тел — иммуноглобулина.

Как мы знаем, наш организм вырабатывает защитные силы и антитела в соответствии с бактериями, которым он подвергается в первые годы.
Исследования показали, что дети, которые играют с грязью и иногда кладут в рот песок или землю, а также подвергаются воздействию многих других бактерий другими способами, по мере взросления развивают более сильную иммунную систему.
Однако наше общество стало во многих отношениях очень стерильным обществом, и чрезмерное поклонение чистоте в современном мире использует возможность культивировать бактериальный опыт в их телах, а также нарушает микробиоту многих взрослых.
Конечно, поддержание чистоты необходимо, но нынешняя ситуация уже стала совсем нелепой. На самом деле, после уничтожения бактерий становится все более невозможным поддерживать разнообразный и сбалансированный пищеварительный тракт и экосистему кожи.
В результате он ослабляет нашу иммунную систему, делая нас более больными, а болезнетворные бактерии — сильнее. В заключение, болезни становится все труднее лечить, и это не означает ничего хорошего в долгосрочной перспективе.
В заключение, болезни становится все труднее лечить, и это не означает ничего хорошего в долгосрочной перспективе.
Следовательно, нам нужно начать употреблять больше полезных бактерий — пробиотиков.
Хорошие бактерии (пробиотики) и пищеварительные ферменты также можно приобрести в Интернете.
Что вызывает дисбактериоз? Ежедневные внешние причины дисбактериоза и убийцы хороших бактерий- Дезинфицирующие средства — Вся наша среда обитания становится все более антибактериальной и химической. Очень часто не только ежедневно мыть руки, но и пользоваться дезинфицирующими средствами (конечно, это необходимо в медицинских учреждениях).Однако дезинфицирующее средство убивает все бактерии, в том числе и те, которые защищают нашу кожу.
- Бытовая химия — Для очистки дома мы все больше и больше используем сильно пахнущую и концентрированную бытовую химию, которая часто уничтожает 99,9% бактерий.

- Прачечная — Сегодня мы используем не только стиральный порошок, но и пятновыводитель и кондиционер для белья. Чем сильнее и лучше запах или чем больше в них химических веществ, тем популярнее они будут у многих.Очень приятно, когда кондиционер для белья смывает стиральный порошок и делает белье мягким, но если он остается в белье вместо стирального порошка, стоит ли вам вдруг подумать о другом продукте, который смывает кондиционер?
- Унитаз — Недостаточно чистить унитаз с помощью чистящего средства (или того, которое удаляет только видимую грязь), он должен находиться внутри унитаза, который уничтожает микробы при каждом полоскании и сохраняет горшок в чистоте и ароматный.
- Ополаскиватель для полости рта — Кроме того, в настоящее время недостаточно просто чистить зубы.Поэтому, чтобы убедиться, что все бактерии во рту точно погибли, после мытья необходимо использовать жидкость для полоскания рта.
- Загрязнение
Все, чем мы смазываем себя и едим — начиная с раннего возраста — это отдельная тема. Чем больше мы едим обработанных и сладких продуктов, тем больше мы живем в стрессовой среде, чем больше мы физически переутомлены, тем больше вредных бактерий захватывают наши тела и наше здоровье ухудшается.Вот почему мы подвержены всевозможным вирусам и инфекциям.
Чем больше мы едим обработанных и сладких продуктов, тем больше мы живем в стрессовой среде, чем больше мы физически переутомлены, тем больше вредных бактерий захватывают наши тела и наше здоровье ухудшается.Вот почему мы подвержены всевозможным вирусам и инфекциям.
- Слишком много алкоголя (два или более алкогольных напитка в день)
- Употребление слишком большого количества белка, сахара или пищевых добавок
- Диеты с высоким содержанием жиров и сахара, а также диеты с низким содержанием ферментируемой клетчатки также приводят к дисбактериозу (надежный источник)
- Случайное потребление химикатов , таких как оставшиеся пестициды на немытых фруктах
- Плохая гигиена полости рта , из-за которой вредные бактерии нарушают баланс во рту
- Высокий уровень беспокойства или стресса , который может ослабить вашу иммунную систему
- Рак и химиотерапия
- Применение противовирусных препаратов и радиоактивных изотопов
- Гормональная терапия
- Хронические и острые инфекции (ВИЧ, гепатит C и B)
- Сахарный диабет
- Заболевания печени и поджелудочной железы
- Новые лекарства, особенно антибиотики , влияющие на кишечную флору
- Незащищенный секс , который также может подвергнуть вас воздействию вредных бактерий
- Наличие кишечных паразитов (гельминтов)
- Неконтролируемое очищение прямой кишки с клизмами
- Воспалительные процессы в кишечнике
- Дисбиоз кожи может быть вызван воздействием вредных бактерий или чрезмерным ростом одного типа бактерий.
 Например, бактерии Staphylococcus aureus могут бесконтрольно расти и вызывать инфекцию стафилококка. Бактерии Gardnerella vaginalis могут захватывать здоровые бактерии во влагалище и вызывать жжение, зуд и выделения из влагалища.
Например, бактерии Staphylococcus aureus могут бесконтрольно расти и вызывать инфекцию стафилококка. Бактерии Gardnerella vaginalis могут захватывать здоровые бактерии во влагалище и вызывать жжение, зуд и выделения из влагалища.
Если доля патогенной микробиоты или вредных бактерий увеличивается до 25%, то в этом случае доля хороших бактерий уже слишком уменьшилась, и существующие больше не могут выполнять свои задачи.
Характеристики дисбактериоза (дисбаланса микробиоты) могут проявляться по-разному.
Однако дисбактериоз обычно протекает в легкой форме, и его можно лечить с помощью лекарств и изменения образа жизни. Но если его не лечить, дисбактериоз может привести к хроническим состояниям и серьезным заболеваниям.
Итак, немедленно обратитесь к врачу, если вы испытываете необычную или постоянную боль в животе или раздражение кожи.
Хорошие бактерии (пробиотики) и пищеварительные ферменты также можно приобрести в Интернете.
- Аллергия
- Анемия
- Рак толстой или прямой кишки
- Целиакия
- Нарушение функции органов
- Депрессия
- Диабет
- Желудочно-кишечные (ЖКТ) расстройства, включая гастрит, язвенную болезнь
- Заболевания кишечника, такие как колит
- Гинекологические проблемы и кандидоз, разновидность дрожжевой инфекции
- Болезнь сердца или сердечная недостаточность
- Герпес
- IBS
- Воспаление
- Раздражительность
- Деменция с поздним началом
- Синдром дырявого кишечника
- Заболевание печени и почек
- Психические расстройства
- Ожирение
- Болезнь Паркинсона
- Синдром поликистозных яичников
- Кожные заболевания, например экзема
- Количество отходов, производимых бактериями, начинает отравлять организм, и способность бороться с инфекциями снижается
- Дефицит питательных веществ
- Боль в животе
- Аллергические реакции
- Беспокойство
- Неприятный запах изо рта (галитоз), неприятный привкус во рту натощак
- Отрыжка и вздутие живота
- Урчание и метеоризм в животе
- Боль в груди
- Запор
- Депрессия
- Диарея
- Затрудненное мочеиспускание
- Головокружение
- Усталость
- Гинекологические заболевания и молочница у женщин
- Выпадение волос
- Проблемы с мышлением или концентрацией
- Сердечная недостаточность
- Повышенное потоотделение
- Нерегулярное испражнение
- Деформация ногтя
- Тошнота
- Нервозность
- Сыпь и другие кожные проблемы, такие как сухость губ, трещины и язвы в углах рта (недостаток витаминов группы B), покраснение, шелушение кожи и пиодермия (сыпь), поседение лица
- Сильные колебания аппетита
- Язык утолщенный
- Расстройство желудка
- Зуд влагалища или прямой кишки
- Слабость
- Не переедай.
 Особенно вечером — уменьшенное количество ферментов не может обработать всю пищу, а остатки пищи начинают способствовать развитию патогенных бактерий.
Особенно вечером — уменьшенное количество ферментов не может обработать всю пищу, а остатки пищи начинают способствовать развитию патогенных бактерий. - Улучшение условий труда и борьба со стрессом , так как дисбактериоз может стать хроническим при усилении стресса и развитии депрессии.
- Очистить желудочно-кишечный тракт и, при необходимости, убить паразитов в организме . Существуют диетические добавки, такие как экстракт черного грецкого ореха, которые помогут вам очистить кишечник и избавиться от паразитов естественным путем.
- Некоторые исследования показывают, что медитация и йога могут помочь вашему организму лучше усваивать питательные вещества. Он также может увеличить приток крови к мозгу и обратно к кишечнику. Это может уменьшить некоторые симптомы дисбактериоза.
- По возможности избегайте чрезмерно стерильной среды и сокращайте использование продуктов, убивающих все бактерии. Таким образом, ваше тело никогда не научится бороться с вредными бактериями.

- Ешьте больше сырых и подкисленных продуктов, которые не были приготовлены. В них много фитонцидов, антибиотиков и ферментов. Ферменты играют особенно важную роль. Они помогают ослабленному организму расщеплять и переваривать пищу. Например, ешьте квашеную капусту, кислые яблоки и / или пейте яблочный сок с медом. Ведь это нужно для нормализации кислотности желудочно-кишечного тракта, так как кислая среда препятствует развитию патогенной микрофлоры.
- Потребляйте больше продуктов с высоким содержанием хорошей клетчатки, такой как ферментируемая клетчатка, особенно пребиотик , клетчатка, , поскольку клетчатка необходима для роста полезных бактерий.Например, проросшие зерна, орехи, бобы, бобовые, жиры (желательно льняное масло).
- Используйте простоквашу, йогурт и кефир как источники полезных бактерий.
- Включите продукты, способствующие развитию и размножению полезных бактерий , такие как дрожжевой экстракт, сыворотка, водоросли, морковный сок (до 1 стакана в день), свежая капуста, свекла, малина, клюква, абрикосы, гранат, грейпфрут, черноплодная рябина.
 , лук, яблоко, петрушка, сельдерей, чеснок, куркума и др.
, лук, яблоко, петрушка, сельдерей, чеснок, куркума и др. - Было бы хорошо, если бы вы еще ели пищу, содержащую какие-то слизеобразующие вещества. Помогает вывести токсичные вещества из организма при разрушении. Такие как мальва болотная (Althaea officinalis), исландский лишайник, каллуна (Calluna vulgaris), мальва, лен, донник (Melilotus L), мать-и-мачеха (Tussilago farfara), подорожник, сапонар, тея (Saponaria officinalis), коровяк (Verbascum), коровяк большой (Verbascum thapsus).
- Продукты, которые вы можете добавить в свой рацион, включают также темную листовую зелень (включая шпинат и капусту), рыбу (включая лосось и скумбрию) и свежее мясо (избегайте обработанных мясных продуктов).
- В острых случаях (вздутие живота, боли в животе, диарея) не употреблять продукты, вызывающие образование плохих микроорганизмов — хлеб, сахар, колбасы, картофель и сыр. В конце концов, эти продукты являются буквально лакомством для вредных бактерий и вызывают их быстрое размножение.

- Продукты, содержащие вредные химические вещества
- Молочные продукты, такие как молоко и сыр
- Мясные полуфабрикаты, такие как соленые или мясные консервы и мясные деликатесы
- Углеводы в кукурузе и овсе
- Продукты с высоким содержанием сахара (кукурузный сироп, кленовый сироп и тростниковый сахар-сырец)
Пробиотики — Если ваша микробиота более серьезно повреждена, дайте организму живые пробиотики, которые помогут поддерживать баланс кишечных бактерий.Пробиотики и пищеварительные ферменты также можно приобрести в Интернете.
Волокна — Здоровые волокна естественным образом помогут очистить кишечник от токсинов, а также обогатят организм необходимыми питательными веществами.
Экстракт черного грецкого ореха — Если вам нужно избавиться от кишечных паразитов.
Питательные вещества — В заключение также убедитесь, что вы получаете достаточно питательных веществ для поддержания баланса бактерий, в том числе:
В конечном итоге, если вы хотите укрепить психическое и физическое здоровье всего тела, начните с желудка — с распространения полезных бактерий. Дело не только в том, чтобы убить плохих. Эта вечная борьба за баланс между хорошими и плохими бактериями бесконечна, но она того стоит, ради вашего психического и физического здоровья.
Дело не только в том, чтобы убить плохих. Эта вечная борьба за баланс между хорошими и плохими бактериями бесконечна, но она того стоит, ради вашего психического и физического здоровья.
NB! Информация, представленная здесь, предназначена только для информационных целей, поэтому не рассматривайте ее как медицинскую помощь или медицинскую диагностику и лечение. Не рассматривайте эту информацию как гарантию желаемого результата. Кроме того, эта информация не предназначена для замены совета вашего врача или другого медицинского работника.
Более того, вы не должны использовать его для диагностики или лечения проблем со здоровьем. Перед тем, как изменить или прекратить прием существующих лекарств, лечения или ухода или принимать какие-либо диетические добавки, обязательно проконсультируйтесь со своим лечащим врачом или врачом перед тем, как начать какую-либо диету или программу, или если вы подозреваете, что у вас может быть какое-либо заболевание.
Автор Мария-Елена Лоик
Источники: Sciencedirect. com, Healthline.com, Scienceabc.com, Iflscience.com
com, Healthline.com, Scienceabc.com, Iflscience.com
Рисунки: Pexels.com, Pixabay.com, Shutterstock.com
Сообщите нам, понравился ли вам пост. Это единственный способ стать лучше.
Дисбактериоз — обзор | Темы ScienceDirect
36.5.2 Дисбиоз
Дисбиоз часто определяют как «дисбаланс» микробного сообщества кишечника, связанный с заболеванием. Этот дисбаланс может быть связан с увеличением или уменьшением числа членов сообщества или изменениями в относительной численности микробов. Эта теория в первую очередь фокусируется на изменениях в таксономическом составе микробного сообщества и функциях, связанных с отдельными членами или подмножествами членов сообщества. 126 Характеристика дисбиоза традиционно основывалась на таксономических каталогах кишечных микробов, созданных у разных людей в отдельные моменты времени с использованием секвенирования 16S или 18S рРНК. 127 Более недавние попытки были попытаться каталогизировать не виды микробов, а скорее микробные гены в кишечнике, используя метагеномику дробовика. 128,129 Затем таксономическая характеристика или генетический состав сообщества используется для вывода его функций на основе литературных данных исследований с использованием эталонных штаммов микробов.Обычно эти модельные микробы изучаются как отдельные организмы и часто in vitro, чтобы получить эти функциональные данные.
128,129 Затем таксономическая характеристика или генетический состав сообщества используется для вывода его функций на основе литературных данных исследований с использованием эталонных штаммов микробов.Обычно эти модельные микробы изучаются как отдельные организмы и часто in vitro, чтобы получить эти функциональные данные.
Огромное количество исследований выявило значительные различия в таксономическом составе кишечных микробных сообществ между пациентами с ВЗК и здоровыми людьми из контрольной группы. 130 Эти различия были выявлены в бактериальном, грибковом и вирусном компонентах сообщества. 131 132 Однако конкретные таксономические различия микробов широко варьируются в зависимости от исследований, и окончательная структура сообщества, связанного с заболеванием, не установлена.Это может быть связано с большими различиями в составе микробного сообщества кишечника среди людей и / или с техническими различиями между исследованиями. Таким образом, как определить дисбактериоз и диагностировать «дисбиотическое сообщество», пока неясно. Также неясно, является ли дисбактериоз причиной, следствием или одновременно причиной и следствием заболевания, поскольку воспаление само по себе может приводить к изменениям в составе микробного сообщества в кишечнике. 133
Также неясно, является ли дисбактериоз причиной, следствием или одновременно причиной и следствием заболевания, поскольку воспаление само по себе может приводить к изменениям в составе микробного сообщества в кишечнике. 133
Дисбактериоз может вызывать или способствовать развитию ВЗК несколькими способами.Это может привести к появлению одного или нескольких микробов с функциями, вредными для хозяина, или потере одного или нескольких микробов с функциями, полезными для хозяина. Поскольку многие микробы в кишечном сообществе имеют важные функциональные отношения друг с другом, изменения в небольшом количестве микробов и / или их функциях могут иметь широкое влияние на сообщество. Конкретные функции, которые могут представлять интерес, включают изменения доступности ниш или характеристик, которые влияют на принятие или устойчивость колонизации, изменения микробных продуктов или физических характеристик, которые изменяют взаимодействия между бактериями или с хозяином, и изменения в сообществе, которые активируют механизмы вирулентности в в противном случае комменсальные микробы. Наиболее устойчивой характеристикой микробных сообществ больных пациентов является потеря таксономического разнообразия. 134 Однако снова неясно, является ли потеря биоразнообразия в кишечнике причиной или следствием заболевания. Также в настоящее время неясно, как такая потеря разнообразия сама по себе может привести к заболеванию, тем более что животные-гнотобиоты, колонизированные одним или небольшим количеством микробов, не проявляют болезни, связанной с колонизацией только ограниченным сообществом. Это говорит о том, что конкретные микробы в сообществе и их функции имеют первостепенное значение.
Наиболее устойчивой характеристикой микробных сообществ больных пациентов является потеря таксономического разнообразия. 134 Однако снова неясно, является ли потеря биоразнообразия в кишечнике причиной или следствием заболевания. Также в настоящее время неясно, как такая потеря разнообразия сама по себе может привести к заболеванию, тем более что животные-гнотобиоты, колонизированные одним или небольшим количеством микробов, не проявляют болезни, связанной с колонизацией только ограниченным сообществом. Это говорит о том, что конкретные микробы в сообществе и их функции имеют первостепенное значение.
Состав и поведение микробного сообщества чрезвычайно чувствительны к окружающей среде. 9 Окружающая среда кишечного микробного сообщества состоит как из компонентов, полученных из организма хозяина, так и из проглоченных веществ. Каждый из этих факторов может иметь глубокое влияние на состав и поведение кишечного микробного сообщества. Компоненты, производные от хозяина, определяются генетикой хозяина и, возможно, воздействием диеты или других потребляемых веществ непосредственно на хозяина. Наиболее хорошо охарактеризованными детерминантами состава и поведения микробного сообщества-хозяина являются системы противомикробной защиты хозяина.Когда эти системы нарушены из-за генетического нокаута отдельных компонентов у модельных животных, возникает дисбиоз. 135 Проглоченное содержимое просвета кишечника в основном происходит из пищи. Вклад диеты в микробный дисбактериоз представляет особый интерес для многих исследователей, поскольку ВЗК распространяется вместе с распространением западного образа жизни по всему миру, а западная диета сильно отличается от традиционных диет в незападных обществах. 136 Диетические компоненты состоят из макроэлементов, таких как жиры и сахар, микронутриентов, таких как витамины и минералы, и непитательных компонентов, таких как диетические эмульгаторы.Западная диета, как правило, сильно переработана и содержит большое количество насыщенных жиров и простых сахаров. Было показано, что этот тип диеты способствует выработке метаболитов, вредных для тканей хозяина.
Наиболее хорошо охарактеризованными детерминантами состава и поведения микробного сообщества-хозяина являются системы противомикробной защиты хозяина.Когда эти системы нарушены из-за генетического нокаута отдельных компонентов у модельных животных, возникает дисбиоз. 135 Проглоченное содержимое просвета кишечника в основном происходит из пищи. Вклад диеты в микробный дисбактериоз представляет особый интерес для многих исследователей, поскольку ВЗК распространяется вместе с распространением западного образа жизни по всему миру, а западная диета сильно отличается от традиционных диет в незападных обществах. 136 Диетические компоненты состоят из макроэлементов, таких как жиры и сахар, микронутриентов, таких как витамины и минералы, и непитательных компонентов, таких как диетические эмульгаторы.Западная диета, как правило, сильно переработана и содержит большое количество насыщенных жиров и простых сахаров. Было показано, что этот тип диеты способствует выработке метаболитов, вредных для тканей хозяина. 137 И наоборот, диета с низким содержанием субстратов, необходимых микробам для выработки метаболитов, которые способствуют здоровью тканей хозяина, также может способствовать развитию болезни. Например, неперевариваемые пищевые волокна используются микробами для производства короткоцепочечных жирных кислот, а диетический триптофан используется для производства лигандов рецепторов арилуглеводородов, которые способствуют здоровью кишечника. 95,138 Наконец, диетические эмульгаторы часто добавляют в обработанные пищевые продукты для улучшения их текстуры или стабильности. In vitro эти соединения активируют образование фибр у E. coli , что приводит к прилипанию и повреждению тканей этими обычно комменсальными бактериями. 139 Было показано, что потребление пищевых эмульгаторов in vivo вызывает дисбактериоз и обострение колита у мышей IL-10 — / — . 140 Другие типы экологического стресса, такие как введение антибиотиков, также могут приводить к изменениям в микробном сообществе посредством прямого уничтожения микробов или горизонтального переноса генов.
137 И наоборот, диета с низким содержанием субстратов, необходимых микробам для выработки метаболитов, которые способствуют здоровью тканей хозяина, также может способствовать развитию болезни. Например, неперевариваемые пищевые волокна используются микробами для производства короткоцепочечных жирных кислот, а диетический триптофан используется для производства лигандов рецепторов арилуглеводородов, которые способствуют здоровью кишечника. 95,138 Наконец, диетические эмульгаторы часто добавляют в обработанные пищевые продукты для улучшения их текстуры или стабильности. In vitro эти соединения активируют образование фибр у E. coli , что приводит к прилипанию и повреждению тканей этими обычно комменсальными бактериями. 139 Было показано, что потребление пищевых эмульгаторов in vivo вызывает дисбактериоз и обострение колита у мышей IL-10 — / — . 140 Другие типы экологического стресса, такие как введение антибиотиков, также могут приводить к изменениям в микробном сообществе посредством прямого уничтожения микробов или горизонтального переноса генов. 141,142 Экологический стресс также может определять, ведут ли бактериофаги лизогенный или литический образ жизни. 143 Фаг-индуцированный лизис не только убивает бактерии, но и потенциально приводит к инфицированию новых бактериальных мишеней с изменением поведения этих бактерий.
141,142 Экологический стресс также может определять, ведут ли бактериофаги лизогенный или литический образ жизни. 143 Фаг-индуцированный лизис не только убивает бактерии, но и потенциально приводит к инфицированию новых бактериальных мишеней с изменением поведения этих бактерий.
Открытым вопросом в области дисбактериоза является важность того, когда происходят дисбиотические изменения в микробном сообществе. Кесарево сечение приводит к изменениям в ранних стадиях колонизации, а раннее введение антибиотиков может значительно нарушить развивающиеся сообщества. 144 Оба эти фактора были связаны с рядом иммуноопосредованных заболеваний в более позднем возрасте, но окончательных доказательств причинной связи или понимания механизмов все еще нет. 145 Кроме того, у многих пациентов развивается ВЗК без событий в раннем возрасте, которые, как ожидается, могут вызвать дисбактериоз. Таким образом, дополнительные неизвестные события могут способствовать раннему, давнему дисбактериозу на момент постановки диагноза ВЗК, или более острые дисбиотические события также могут способствовать развитию ВЗК. Также ожидается, что тип дисбиотического события будет ключевым фактором в том, как дисбактериоз способствует развитию ВЗК.Остается определить, являются ли это широкими изменениями в сообществе или небольшими кардинальными изменениями в конкретных микробах. Эта неопределенность, по крайней мере частично, связана с техническими проблемами, которые могут переоценить актуальность высокоразвитых микробов и недооценить функциональную важность менее многочисленных членов сообщества. Технические ограничения доступных в настоящее время методов и данных также могут переоценить важность известных микробов с установленными функциональными данными по сравнению с неизвестными микробами, которые могут быть столь же важны для болезни.Наконец, до сих пор неизвестно, как дисбактериоз вызывает или способствует развитию ВЗК. Имеются некоторые свидетельства того, что определенные дисбиотические микробные сообщества могут вызывать заболевание у нормальных хозяев. 146 Однако есть гораздо более убедительные доказательства того, что дисбактериоз работает в сочетании с дополнительными факторами, такими как лежащая в основе генетическая предрасположенность или повреждение кишечника, вызывая заболевание.
Также ожидается, что тип дисбиотического события будет ключевым фактором в том, как дисбактериоз способствует развитию ВЗК.Остается определить, являются ли это широкими изменениями в сообществе или небольшими кардинальными изменениями в конкретных микробах. Эта неопределенность, по крайней мере частично, связана с техническими проблемами, которые могут переоценить актуальность высокоразвитых микробов и недооценить функциональную важность менее многочисленных членов сообщества. Технические ограничения доступных в настоящее время методов и данных также могут переоценить важность известных микробов с установленными функциональными данными по сравнению с неизвестными микробами, которые могут быть столь же важны для болезни.Наконец, до сих пор неизвестно, как дисбактериоз вызывает или способствует развитию ВЗК. Имеются некоторые свидетельства того, что определенные дисбиотические микробные сообщества могут вызывать заболевание у нормальных хозяев. 146 Однако есть гораздо более убедительные доказательства того, что дисбактериоз работает в сочетании с дополнительными факторами, такими как лежащая в основе генетическая предрасположенность или повреждение кишечника, вызывая заболевание. Например, перенос микробных сообществ от пациентов с ВЗК мышам без микробов не вызывает спонтанного колита. 69,70,146 Однако он, по-видимому, способствует развитию заболевания на моделях мышей, предрасположенных к заболеванию, таких как мыши IL-10 — / — или с химической индукцией колита. 69,70 146 Кроме того, дисбактериоз, связанный с диетами западного типа, по-видимому, допускает колонизацию организмами, ассоциированными с ВЗК. Бесплодные мыши, колонизированные микробами от мышей, получавших диету с высоким содержанием жиров и сахара, имеют повышенную восприимчивость к колонизации AIEC. 147 Таким образом, дисбактериоз может по-разному влиять на разных хозяев в зависимости от природы дисбиотического сообщества и лежащих в основе генетической предрасположенности к заболеванию у хозяина.Независимо от того, возникает ли дисбактериоз первым и вызывает заболевание, или он является результатом болезни, однажды возникнув, он почти наверняка будет способствовать сохранению болезни.
Например, перенос микробных сообществ от пациентов с ВЗК мышам без микробов не вызывает спонтанного колита. 69,70,146 Однако он, по-видимому, способствует развитию заболевания на моделях мышей, предрасположенных к заболеванию, таких как мыши IL-10 — / — или с химической индукцией колита. 69,70 146 Кроме того, дисбактериоз, связанный с диетами западного типа, по-видимому, допускает колонизацию организмами, ассоциированными с ВЗК. Бесплодные мыши, колонизированные микробами от мышей, получавших диету с высоким содержанием жиров и сахара, имеют повышенную восприимчивость к колонизации AIEC. 147 Таким образом, дисбактериоз может по-разному влиять на разных хозяев в зависимости от природы дисбиотического сообщества и лежащих в основе генетической предрасположенности к заболеванию у хозяина.Независимо от того, возникает ли дисбактериоз первым и вызывает заболевание, или он является результатом болезни, однажды возникнув, он почти наверняка будет способствовать сохранению болезни.
Дисбактериоз кишечника, связанный с симптомами СРК-D
Ссылки: 1. Rezaie A, Heimanson Z, McCallum R, Pimentel M. Дыхательная проба на лактулозу как прогностический фактор ответа на рифаксимин у пациентов с синдромом раздраженного кишечника с диареей. Am J Gastroenterol. 2019; 114 (12): 1886-1893. 2. Кэрролл И.М., Рингель-Кулька Т., Сиддл Дж. П., Рингель Ю. Изменения в составе и разнообразии кишечной микробиоты у пациентов с синдромом раздраженного кишечника с преобладанием диареи. Neurogastroenterol Motil. 2012; 24 (6): 521-530. 3. Чжун В., Лу Х, Ши Х и др. Определенные микробные популяции существуют в микробиоте слизистой оболочки, связанной с преобладанием диареи, синдрома раздраженного кишечника и язвенного колита. J Clin Gastroenterol. 2019; 53 (9): 660-672. 4. Кассинен А., Крогиус-Курикка Л., Мякивуокко Х. и др. Фекальная микробиота пациентов с синдромом раздраженного кишечника существенно отличается от таковой здоровых людей. Гастроэнтерология. 2007; 133 (1): 24-33. 5. Casén C, Vebø HC, Sekelja M, et al. Отклонения в микробиоте кишечника человека: новый диагностический тест для определения дисбактериоза у пациентов с IBS или IBD. Aliment Pharmacol Ther. 2015; 42 (1): 71-83. 6. Пиментел М., Лембо А., Чей В.Д. и др.Терапия рифаксимином у пациентов с синдромом раздраженного кишечника без запоров. N Engl J Med. 2011; 364 (1): 22-32. 7. Рингель Ю. Микробиом кишечника при синдроме раздраженного кишечника и других функциональных расстройствах кишечника. Gastroenterol Clin North Am. 2017; 46 (1): 91-101. 8. Ringel-Kulka T., Choi CH, Temas D, et al. Измененная бактериальная ферментация толстой кишки как потенциальный патофизиологический фактор синдрома раздраженного кишечника. Am J Gastroenterol. 2015; 110 (9): 1339-1346. 9. Кинг Т.С., Элия М., Хантер Дж. Аномальная кишечная ферментация при синдроме раздраженного кишечника.
Гастроэнтерология. 2007; 133 (1): 24-33. 5. Casén C, Vebø HC, Sekelja M, et al. Отклонения в микробиоте кишечника человека: новый диагностический тест для определения дисбактериоза у пациентов с IBS или IBD. Aliment Pharmacol Ther. 2015; 42 (1): 71-83. 6. Пиментел М., Лембо А., Чей В.Д. и др.Терапия рифаксимином у пациентов с синдромом раздраженного кишечника без запоров. N Engl J Med. 2011; 364 (1): 22-32. 7. Рингель Ю. Микробиом кишечника при синдроме раздраженного кишечника и других функциональных расстройствах кишечника. Gastroenterol Clin North Am. 2017; 46 (1): 91-101. 8. Ringel-Kulka T., Choi CH, Temas D, et al. Измененная бактериальная ферментация толстой кишки как потенциальный патофизиологический фактор синдрома раздраженного кишечника. Am J Gastroenterol. 2015; 110 (9): 1339-1346. 9. Кинг Т.С., Элия М., Хантер Дж. Аномальная кишечная ферментация при синдроме раздраженного кишечника. Ланцет. 1998; 352 (9135): 1187-1189. 10. Онг Д.К., Митчелл С.Б., Барретт Дж. С. и др. Манипулирование диетическими углеводами с короткой цепью изменяет характер газообразования и генезис симптомов синдрома раздраженного кишечника. J Gastroenterol Hepatol. 2010; 25 (8): 1366-1373. 11. Серра Дж., Аспироз Ф., Малагелада Дж. Р. Нарушение транзита и толерантности кишечных газов при синдроме раздраженного кишечника. Gut. 2001; 48 (1): 14-19. 12. Houghton LA, Lea R, Agrawal A, Reilly B, Whorwell PJ. Связь вздутия живота с вздутием живота при синдроме раздраженного кишечника и влияние привычки кишечника. Гастроэнтерология. , 2006; 131 (4): 1003-1010. 13. Dunlop SP, Hebden J, Campbell E, et al. Аномальная кишечная проницаемость в подгруппах синдромов раздраженного кишечника с преобладанием диареи. Am J Gastroenterol. , 2006; 101 (6): 1288-1294. 14. Аткинсон В.
Ланцет. 1998; 352 (9135): 1187-1189. 10. Онг Д.К., Митчелл С.Б., Барретт Дж. С. и др. Манипулирование диетическими углеводами с короткой цепью изменяет характер газообразования и генезис симптомов синдрома раздраженного кишечника. J Gastroenterol Hepatol. 2010; 25 (8): 1366-1373. 11. Серра Дж., Аспироз Ф., Малагелада Дж. Р. Нарушение транзита и толерантности кишечных газов при синдроме раздраженного кишечника. Gut. 2001; 48 (1): 14-19. 12. Houghton LA, Lea R, Agrawal A, Reilly B, Whorwell PJ. Связь вздутия живота с вздутием живота при синдроме раздраженного кишечника и влияние привычки кишечника. Гастроэнтерология. , 2006; 131 (4): 1003-1010. 13. Dunlop SP, Hebden J, Campbell E, et al. Аномальная кишечная проницаемость в подгруппах синдромов раздраженного кишечника с преобладанием диареи. Am J Gastroenterol. , 2006; 101 (6): 1288-1294. 14. Аткинсон В. , Локхарт С., Уорвелл П.Дж., Кивил Б., Хоутон Л.А.Нарушение передачи сигналов 5-гидрокситриптамина у пациентов с синдромом раздраженного кишечника с преобладанием запора и диареи. Гастроэнтерология. 2006; 130 (1): 34-43. 15. Гаргари Г., Тавернити В., Гардана С. и др. Распределение фекальных Clostridiales и короткоцепочечных жирных кислот отражает особенности кишечника при синдроме раздраженного кишечника. Environ Microbiol. 2018; 20 (9): 3201-3213. 16. Tack J, Broekaert D, Corsetti M, Fischler B, Janssens J. Влияние острого ингибирования обратного захвата серотонина на сенсомоторную функцию толстой кишки у человека. Aliment Pharmacol Ther. 2006; 23 (2): 265-274. 17. Chey WY, Jin HO, Lee MH, Sun SW, Lee KY. Нарушение моторики толстой кишки у пациентов с синдромом раздраженного кишечника с болью в животе и диареей. Am J Gastroenterol. 2001; 96 (5): 1499-1506. 18. Хаутон Л.А., Аткинсон В.
, Локхарт С., Уорвелл П.Дж., Кивил Б., Хоутон Л.А.Нарушение передачи сигналов 5-гидрокситриптамина у пациентов с синдромом раздраженного кишечника с преобладанием запора и диареи. Гастроэнтерология. 2006; 130 (1): 34-43. 15. Гаргари Г., Тавернити В., Гардана С. и др. Распределение фекальных Clostridiales и короткоцепочечных жирных кислот отражает особенности кишечника при синдроме раздраженного кишечника. Environ Microbiol. 2018; 20 (9): 3201-3213. 16. Tack J, Broekaert D, Corsetti M, Fischler B, Janssens J. Влияние острого ингибирования обратного захвата серотонина на сенсомоторную функцию толстой кишки у человека. Aliment Pharmacol Ther. 2006; 23 (2): 265-274. 17. Chey WY, Jin HO, Lee MH, Sun SW, Lee KY. Нарушение моторики толстой кишки у пациентов с синдромом раздраженного кишечника с болью в животе и диареей. Am J Gastroenterol. 2001; 96 (5): 1499-1506. 18. Хаутон Л.А., Аткинсон В. , Локхарт С., Уорвелл П.Дж., Кивил Б. Сигмовидно-толстокишечная подвижность в здоровье и синдром раздраженного кишечника: роль 5-гидрокситриптамина. Neurogastroenterol Motil. 2007; 19 (9): 724-731. 19. Törnblom H, Van Oudenhove L, Sadik R, Abrahamsson H, Tack J, Simrén M. Время прохождения через толстую кишку и симптомы СРК: какая связь? Am J Gastroenterol. 2012; 107 (5): 754-760. 20. Cremon C, Gargano L, Morselli-Labate AM, et al. Иммунная активация слизистой оболочки при синдроме раздраженного кишечника: гендерная зависимость и связь с пищеварительными симптомами. Am J Gastroenterol. 2009; 104 (2): 392-400. 21. Либрегтс Т., Адам Б., Бредак С. и др. Активация иммунитета у пациентов с синдромом раздраженного кишечника. Гастроэнтерология. 2007; 132 (3): 913-920. 22. Гиларте М., Сантос Дж., Де Торрес И. и др. У пациентов с СРК с преобладанием диареи наблюдается активация тучных клеток и гиперплазия тощей кишки.
, Локхарт С., Уорвелл П.Дж., Кивил Б. Сигмовидно-толстокишечная подвижность в здоровье и синдром раздраженного кишечника: роль 5-гидрокситриптамина. Neurogastroenterol Motil. 2007; 19 (9): 724-731. 19. Törnblom H, Van Oudenhove L, Sadik R, Abrahamsson H, Tack J, Simrén M. Время прохождения через толстую кишку и симптомы СРК: какая связь? Am J Gastroenterol. 2012; 107 (5): 754-760. 20. Cremon C, Gargano L, Morselli-Labate AM, et al. Иммунная активация слизистой оболочки при синдроме раздраженного кишечника: гендерная зависимость и связь с пищеварительными симптомами. Am J Gastroenterol. 2009; 104 (2): 392-400. 21. Либрегтс Т., Адам Б., Бредак С. и др. Активация иммунитета у пациентов с синдромом раздраженного кишечника. Гастроэнтерология. 2007; 132 (3): 913-920. 22. Гиларте М., Сантос Дж., Де Торрес И. и др. У пациентов с СРК с преобладанием диареи наблюдается активация тучных клеток и гиперплазия тощей кишки. Gut. 2007; 56 (2): 203-209. 23. Zhou Q, Zhang B, Verne GN. Проницаемость кишечной мембраны и гиперчувствительность при синдроме раздраженного кишечника. Боль. 2009; 146 (1-2): 41-46. 24. Piche T., Barbara G, Aubert P, et al. Нарушение целостности кишечного барьера в толстой кишке у пациентов с синдромом раздраженного кишечника: участие растворимых медиаторов. Gut. 2009; 58 (2): 196-201. 25. Shulman RJ, Jarrett ME, Cain KC, Broussard EK, Heitkemper MM. Связь между проницаемостью кишечника, маркерами воспаления и симптомами у пациентов с синдромом раздраженного кишечника. J Гастроэнтерол. 2014; 49 (11): 1467-1476. 26. Mearin F, Lacy BE, Chang L, et al. Расстройства кишечника. Гастроэнтерология. 2016; 150 (6): 1393-1407.
Gut. 2007; 56 (2): 203-209. 23. Zhou Q, Zhang B, Verne GN. Проницаемость кишечной мембраны и гиперчувствительность при синдроме раздраженного кишечника. Боль. 2009; 146 (1-2): 41-46. 24. Piche T., Barbara G, Aubert P, et al. Нарушение целостности кишечного барьера в толстой кишке у пациентов с синдромом раздраженного кишечника: участие растворимых медиаторов. Gut. 2009; 58 (2): 196-201. 25. Shulman RJ, Jarrett ME, Cain KC, Broussard EK, Heitkemper MM. Связь между проницаемостью кишечника, маркерами воспаления и симптомами у пациентов с синдромом раздраженного кишечника. J Гастроэнтерол. 2014; 49 (11): 1467-1476. 26. Mearin F, Lacy BE, Chang L, et al. Расстройства кишечника. Гастроэнтерология. 2016; 150 (6): 1393-1407.
Расшифровка дисбактериоза: симптомы, причины и связь с аутоиммунитетом, раком груди, синдромом раздраженного кишечника и другими распространенными заболеваниями
Дисбактериоз — это нарушение баланса кишечной флоры, вызванное недостаточным количеством полезных бактерий и чрезмерным ростом вредных бактерий, дрожжей и / или паразитов. Более клинический термин, относящийся к проблеме, — это «избыточный бактериальный рост в тонком кишечнике» (SIBO), и этот термин относится к кишечной флоре, которая поползла обратно в тонкий кишечник из толстой кишки, которой она принадлежит. За последние десять лет, , я заметил резкое усиление симптомов дисбактериоза у моих пациентов и людей, с которыми я работаю в Интернете в рамках программы Hormone Reset Detox. Симптомы дисбактериоза расплывчаты и часто остаются незамеченными, недиагностированными и, что еще хуже, отклоняются обычными врачами.Это нужно изменить! Вот 5 самых популярных вопросов о дисбактериозе, которые я получаю.
Более клинический термин, относящийся к проблеме, — это «избыточный бактериальный рост в тонком кишечнике» (SIBO), и этот термин относится к кишечной флоре, которая поползла обратно в тонкий кишечник из толстой кишки, которой она принадлежит. За последние десять лет, , я заметил резкое усиление симптомов дисбактериоза у моих пациентов и людей, с которыми я работаю в Интернете в рамках программы Hormone Reset Detox. Симптомы дисбактериоза расплывчаты и часто остаются незамеченными, недиагностированными и, что еще хуже, отклоняются обычными врачами.Это нужно изменить! Вот 5 самых популярных вопросов о дисбактериозе, которые я получаю.
Твитнуть
Q1: Как узнать, что у вас дисбактериоз?- Частые газы или вздутие живота большую часть дней недели
- Спазмы, позывы и / или слизь в фекалиях один раз в неделю
- Туман мозга, тревога или депрессия
- Пищевая чувствительность
- Недостающие микроэлементы
- Хронический неприятный запах изо рта
- Жидкий стул, диарея, запор или их сочетание
- Диагностика синдрома раздраженного кишечника (СРК)
- В анамнезе «желудочные клопы», гастроэнтерит и / или пищевое отравление
- Анамнез пролонгированного приема антибиотиков, например, от прыщей или синусита
- Непереносимость углеводов, особенно после употребления клетчатки и / или бобов
- Усталость или низкая энергия
- Использование противокислотных средств при изжоге, рефлюксе или грыже пищеводного отверстия диафрагмы?
- Аутоиммунитет или аутоиммунное состояние, такое как тиреоидит Хашимото, псориаз или рассеянный склероз
- Заложенность носовых пазух
Оценка: Хотя я еще не видел утвержденной шкалы, если у вас пять или более симптомов , велика вероятность, что у вас дисбактериоз.Читайте дальше, чтобы узнать, что это такое, почему вам следует заботиться о нем и что его вызывает. Если вы отметили четыре или менее симптома, велика вероятность, что у вас нормальная кишечная флора или легкий случай дисбактериоза.
Ответы на 5 ваших главных вопросов о дисбактериозе
Подход функциональной медицины
Сидней Бейкер, доктор медицинских наук, один из первых практиков функциональной медицины, говорил, что если вы сидите на крючке, решение состоит в том, чтобы найти и удалить крючок, а не лечить боль.В традиционной медицине существует тенденция бросать рецепты на проблемы, чтобы попытаться замаскировать симптомы, а не лечить первопричину. В функциональной медицине целью является анализ первопричин, чтобы вы могли избавиться от проблем и почувствовать себя лучше. Дисбактериоз — частая причина многих проблем со здоровьем, от дизестрогении и рака груди до синдрома раздраженного кишечника. Подробнее об этом через минуту. Во-первых, давайте рассмотрим наиболее часто задаваемые вопросы, которые я задаю в своей практике функциональной медицины.
Q2: Что делает для вас нормальная флора кишечника?В целом кишечная флора, называемая микробиотой , и ее ДНК, называемая микробиомом , стабильны у здоровых людей.Но изменение микробиоты может привести к постоянному дисбалансу, известному как дисбактериоз. Честно говоря, я не знаю многих людей с нормальной микробиотой и микробиомом. Может быть, три человека за последние 10 лет, и это становится тревожно редкостью.
Ваша кишечная микробиота передается по наследству от матери при рождении, когда вы продвигаетесь через вагинальный канал (или нет). Позже ваша диета и образ жизни станут более важными в своем влиянии на структуру вашей микробиоты и ее разнообразие. В целом ваша микробиота состоит примерно из 1014 микробов, что в 10 раз превышает количество человеческих клеток, и выполняет несколько ключевых функций:
- синтезирует витамин К и другие важные питательные вещества [1]
- предотвращает протекание стенки кишечника [2]
- пищеварение целлюлозы
- способствует ангиогенезу
- поддерживает функцию кишечного нерва
- поддержание здоровья вашей иммунной системы и распознавание себя по сравнению с чужим [3]
- профилактика камней в почках [4]
Аномальные изменения микрофлоры кишечника происходят из-за употребления антибиотиков, болезней, стресса, старения, плохих диетических привычек (сахар, полуфабрикаты, употребление в пищу непереносимых продуктов) и других проблем, связанных с образом жизни.[5]
Этот хлеб вызывает у вас дисбиоз? А выпивка?
Q4: Что плохого в дисбактериозе? (Или почему это должно вас волновать?)Дисбиоз устанавливает последовательность событий, ведущих к воспалению, за которым следует множество расплывчатых симптомов (как упоминалось в начале этой статьи) и, в конечном итоге, к таким проблемам, как:
- рак груди [6]
- колоректальный рак [7]
- Синдром раздраженного кишечника [8]
- воспалительное заболевание кишечника [9]
- аутоиммунитет [10]
- метаболических заболеваний, таких как ожирение, [11] диабет [12] и гестационный диабет [13]
- аутизм [14]
- другие неврологические состояния, такие как болезнь Паркинсона [15]
- насколько эффективно вы детоксифицируете эндокринные разрушители или ксенобиотики [16]
- плюс многие другие состояния и заболевания, связь которых все еще возникает, например, хроническая венозная недостаточность [17]
Да.Я эксперт по гормонам, поэтому меня особенно беспокоит роль дисбактериоза в потенциальном нарушении баланса гормонов. Вот лишь несколько примеров проблем, связанных с дисбактериозом:
- Создает тип воспаления, который может подавить систему контроля выработки гормонов, которая называется осью гипоталамус-гипофиз-надпочечники-щитовидная железа-гонадная ось .
- Изменяет подмножество микробиома, участвующее в метаболизме эстрогенов, названное Мартином Блазером эстроболомом .[18] Эстроболом — это один из рычагов в организме, регулирующих вашу эстрогеновую нагрузку.
- Повышает активность бета-глюкуронидазы в организме, что полностью изменяет важную систему инактивации эстрогена в печени — это означает, что эстрогены снова и снова рециркулируют в вашем организме, как плохая карма, и повышают уровень эстрогена и, следовательно, эстрогенную нагрузку. В конечном итоге высокая эстрогенная нагрузка может увеличить риск связанных с эстрогеном состояний, таких как диабет, ожирение, рак груди и простаты.Подробнее читайте в следующем сообщении блога!
Дисбактериоз подавляет систему контроля надпочечников, которая называется осью гипоталамус-гипофиз-надпочечники-щитовидная железа-гонад.
Увы, решение не простое и быстрое. Вы могли подумать, что быстрое изменение микробиома может вылечить вас от дисбактериоза. Но биология редко бывает такой простой или благотворительной. [19] Дисбактериоз бывает сложно диагностировать и еще сложнее исправить, и ваша программа реабилитации будет зависеть от состояния вашего кишечника и от того, насколько вы готовы к изменениям.В следующий раз я напишу больше о том, как проверять и лечить дисбактериоз. Кроме того, вы можете предварительно заказать мою новую книгу о роли кишечника и дисбактериоза в возникновении воспаления, которое приводит к проблемам с мозгом / телом, таким как мозговой туман, беспокойство, депрессия и потеря памяти. Он называется Brain Body Diet , и как только вы получите его после 5 марта 2019 года, вы получите подробную информацию о здоровье кишечника, дырявом кишечнике и о том, как восстановить свою пищеварительную систему, чтобы ваш мозг работал лучше. Помните, что употребляют в пищу продукты, богатые пробиотиками. — культивированные овощи, квашеную капусту и кимчи — это отличный способ быстро восстановить здоровье кишечника.
Хотите узнать больше? Закажите новую книгу доктора Сары — об этой и многом другом — под названием Диета для мозга и тела: 40 дней стройности, спокойствия, энергии и счастья .
Список литературы
[1] Zhang, Y.J., et al. «Воздействие кишечных бактерий на здоровье и болезни человека». Международный журнал молекулярных наук 16, вып. 4 (2015): 7493-7519.
[2] Уллувишева, Д., и другие. «Регулирование проницаемости плотных соединений кишечными бактериями и пищевыми компонентами». Журнал питания 141, нет. 5 (2011): 769-776.
[3] Hill, D. A., et al. «Кишечные бактерии и регуляция гомеостаза иммунных клеток». Ежегодный обзор иммунологии 28 (2009): 623-667.
[4] Jalanka-Tuovinen, J., et al. «Кишечная микробиота у здоровых взрослых: временной анализ выявляет индивидуальную и общую основу и связь с кишечными симптомами.” PloS One 6, no. 7 (2011): e23035.
[5] Gerritsen, J., et al. «Кишечная микробиота на здоровье и болезни человека: влияние пробиотиков». Genes & Nutrition 6, нет. 3 (2011): 209-240; Вудмэнси, Э. Дж. «Кишечные бактерии и старение». Журнал прикладной микробиологии 102, вып. 5 (2007): 1178-1186; Ву, Г. Д. и др. «Связь долгосрочных диетических моделей с кишечными микробными энтеротипами». Наука 334, вып. 6052 (2011): 105-108; Лакшминараянан, Б.C., et al. «Динамика состава кишечной микробиоты человека с возрастом: последствия для здоровья». Журнал питания, здоровья и старения 18, no. 9 (2014): 773-786; Кини К.М. и др. «Влияние антибиотиков на микробиоту человека и последующие заболевания». № Ежегодный обзор микробиологии 68 (2014): 217-235; Форсайт, К. Б. и др. «Циркадные ритмы, взаимодействие алкоголя и кишечника». Спирт (2014).
[6] Шапира И. и др.«Развивающиеся концепции: как диета и микробиом кишечника действуют как модуляторы злокачественных новообразований груди». ISRN Онкология 2013 (2013).
[7] Sears, C. L., et al. «Микробы, микробиота и рак толстой кишки». Cell Host & Microbe 15, no. 3 (2014): 317-328; Кеку Т.О. и др. «Желудочно-кишечная микробиота и колоректальный рак». Американский журнал физиологии желудочно-кишечного тракта и физиологии печени (2014): ajpgi-00360; Роуленд, И. Р. «Роль микробиоты желудочно-кишечного тракта при колоректальном раке.” Текущий фармацевтический дизайн 15, no. 13 (2009): 1524-1527.
[8] Bennet, S.M., et al. «Микробиота кишечника как потенциальные организаторы синдрома раздраженного кишечника». Кишечник и печень 23, нет. 9 (2015): 318–31; Manichanh, C., et al. «Микробиота кишечника при ВЗК». Nature Reviews Гастроэнтерология и гепатология 9, no. 10 (2012): 599-608.
[9] Macfarlane, S. et al. «Кишечные бактерии и воспалительные заболевания кишечника.» Критические обзоры в клинических лабораторных науках 46, no. 1 (2009): 25-54; Ву, Г.Д. и др. «Диета, микробиота кишечника человека и ВЗК». Анаэроб 24 (2013): 117-120.
[10] McLean, M.H., et al. «Играет ли микробиота роль в патогенезе аутоиммунных заболеваний?» Кишечник (2014): gutjnl-2014.
[11] Gritz, E.C., et al. «Микробиом кишечника новорожденного человека: краткий обзор». Границы в педиатрии 3 (2015); Стенвинкель, П.«Ожирение — заболевание с множеством этиологий, замаскированным под один и тот же чрезмерно большой фенотип: разве теория переедания не оправдала себя?». Нефрологическая диализная трансплантация (2014): gfu338.
[12] He, C., et al. «Нацеливание на микробиоту кишечника как возможный метод лечения диабета». Исследования питания (2015); Эстев, Э. и др. «Взаимодействие кишечной микробиоты с ожирением, инсулинорезистентностью и диабетом 2 типа: эволюционировали ли кишечные микробиоты совместно с инсулинорезистентностью?» Current Opinion in Clinical Nutrition & Metabolic Care 14, no.5 (2011): 483-490.
[13] Isolauri, E., et al. «Роль пробиотиков в снижении риска гестационного диабета». Диабет, ожирение и метаболизм (2015).
[14] Розенфельд, С. С., «Нарушения микробиома и расстройства аутистического спектра». Метаболизм и утилизация лекарственных средств (2015): dmd-115; Майер, Э.А. и др .. «Измененная ось мозг-кишечник при аутизме: коморбидность или причинные механизмы?». Bioessays 36, нет. 10 (2014): 933-939.
[15] Charlett, A., et al. «Профиль крови содержит ключи к разгадке роли инфекции в предчувствии идиопатического паркинсонизма и желудочно-кишечной инфекции в установленном заболевании». Патогены кишечника 1, нет. 1 (2009): 20.
[16] Guarner, F. et al. «Кишечная флора в здоровье и болезнях». Ланцет 361, нет. 9356 (2003): 512-519; Tralau, T. et al. «Понимание микробиома человека и его метаболизма ксенобиотиков: что известно о его влиянии на физиологию человека?».» Заключение эксперта по метаболизму лекарственных средств и токсикологии 0 (2014): 1-15.
[17] Cordts, P. R., et al. «Могут ли нарушения функции кишечника и печени вызвать хроническую венозную недостаточность?» Журнал сосудистой хирургии 35, вып. 2 (2001): 107-14.
[18] Plottel, C. S., et al. «Микробиом и злокачественные новообразования. «Клеточный хозяин и микроб 10, вып. 4 (2011): 324-35.
[19] Эд Йонг, «Не существует« здорового »микробиома», New York Times, по состоянию на 28 мая 2015 г.
Использование пробиотиков для коррекции дисбактериоза нормальной микробиоты после заболевания или разрушительных событий: систематический обзор
Введение
Популярность пробиотиков в последнее время выросла в геометрической прогрессии, но наряду с их возросшим использованием ведутся споры о том, как следует регулировать пробиотики и следует ли рассматривать пробиотики в качестве лечебного питания, лекарства или пищевой добавки. В США пробиотики обычно доступны в виде пищевых добавок и, таким образом, ограничены заявлением о «структуре или функции» для здоровья и, в отличие от лекарств, отпускаемых по рецепту, не имеют права заявлять, что «лечат» или «излечивают» болезнь.В Европе и Великобритании пробиотики имеют право заявлять о своей полезности или функциональности. Эти утверждения должны быть подтверждены хорошо проведенными испытаниями на людях в целевой популяции или на здоровых добровольцах, но Европейское управление по безопасности пищевых продуктов (EFSA) отклонило> 80% заявлений, представленных им.1–3 Во многих случаях научные обоснованность конкретного заявления о здоровье было сочтено недостаточным или основанным на косвенном эффекте.4 Одно из таких функциональных требований, сделанных для пробиотических продуктов, заключается в том, что они устраняют дисбактериоз (или нарушение существования бактерий и грибков после антибиотиков или других разрушительных воздействий) и, следовательно, могут быть полезными для поддержания здоровья.Пробиотики активны в течение этого чувствительного окна с момента разрушительного события до момента восстановления нормальной микробиоты. Для пробиотиков задокументировано множество механизмов действия (от блокирования участков прикрепления патогенов, разрушения патогена бактериоцинами или протеазами, разлагающими токсины до регуляции иммунной системы) 5, 6, и хотя клинические данные подтверждают Эффективность некоторых пробиотических штаммов, доказательства, связывающие эти механизмы действия с определенными заявлениями о здоровье или функции, не так ясны.
Классическим примером последствий дисбактериоза является диарея, связанная с антибиотиками (AAD) .7, 8 Хотя антибиотики могут быть эффективными в уничтожении патогенных организмов, обычным непреднамеренным эффектом является уничтожение или ингибирование полезных микробов из-за общей восприимчивости к антибиотику. Одна из многих функций нормальной микробиоты — это способность противостоять инфекции патогенными организмами, называемая «резистентностью к колонизации» 9, 10. Например, потеря субпопуляции нормальной микробиоты может привести к потере способности нарушать пуховые волокна и крахмалы превращаются в абсорбируемые короткоцепочечные жирные кислоты, что приводит к высокому уровню непереваренных углеводов, что может вызвать диарею.11 Было показано, что нарушение нормальной микробиоты приводит к более высокому уровню инфекций в других системах организма, кроме кишечного тракта, включая кожу, 12, 13 влагалище, 14, 15 дыхательные пути, 16, 17 и ротовую полость18. –20
Основной проблемой при установлении причины и следствия улучшения дисбактериоза пробиотиками является отсутствие стандартного определения «нормальной» микробиоты. Виды микробов, присутствующих в разных нишах тела, значительно варьируются между индивидуумами, которые также зависят от возраста, географического района и состояния здоровья хозяина.Кроме того, полный учет микробиоты в настоящее время невозможен, поскольку отсутствуют анализы для обнаружения всех> 10 13 –10 14 организмов в кишечнике, а стандартные методы микробного культивирования пропускают 75–95% этих организмов. 21, 22 Развитие метагеномики (каталогизация профилей индивидуальных и специфических для болезней бактериальных генов) и создание международного проекта «Микробиом человека» открыли новую эру в нашем понимании сложности этих взаимодействий в организме.23, 24 Этот сдвиг парадигмы от культивирования к метагеномному анализу расширил наши возможности документировать изменения микробных популяций до беспрецедентной степени, но интерпретация этих сдвигов продолжает оставаться предметом споров.25-28 С появлением этих новых метагеномных инструментов, пересматривается роль пробиотиков в восстановлении нормальной микробиоты.29
В свете новых руководящих документов и рекомендаций цель этого систематического обзора состоит в том, чтобы определить, как требования по восстановлению нормальной микробиоты и коррекции дисбактериоза изучались с помощью хорошо спланированных испытаний и какие штаммы пробиотиков имеют доказательные данные. чтобы поддержать эти утверждения.
Методы
Цель исследования
Систематический обзор литературы для анализа доказательств того, что пробиотики могут исправить дисбактериоз нормальной микробиоты по результатам рандомизированных контролируемых испытаний.
Стратегия поиска
Поисковые запросы включали: пробиотики + заявления о здоровье, восстановление нормальной микробиоты, дисбиоз, нормальная микробиота, фармакокинетика, метагеномика, пробиотики, пищевые добавки, рандомизированные контролируемые испытания, AAD, Clostridium difficile инфекция (CDI), воспалительные заболевания кишечника (IBD) синдром раздраженного кишечника (СРК), диарея путешественника (TD), искоренение Heliobacter pylori, бактериального вагиноза (BV) или вагинита, лечение острой детской диареи и специфические штаммы или продукты пробиотиков.Первоначально стратегии поиска были широкими, а затем сузились до клинических испытаний пробиотиков.
Источники данных
PubMed (1985–2013), EMBASE (1985–2013), Кокрановская база данных систематических обзоров (1990–2013), CINAHL (1985–2013), AMED (1985–2013) и ISI Web of Science (2000–2013). Был проведен поиск по трем онлайновым регистрам клинических испытаний: Кокрановскому центральному регистру контролируемых испытаний (http://www.cochrane.org), метарегистру контролируемых испытаний (http: www.controlled-trials.com/mrct) и Национальным институтам здравоохранения. (http: // www.Clinicaltrials.gov).
Критерии отбора исследований и извлечения данных
Отрывки из всех ссылок были рассмотрены одним автором и оценены для включения в рандомизированные контролируемые испытания пробиотических препаратов. Полные статьи были извлечены, если были упомянуты нормальные анализы микробиоты. Испытания на языках, отличных от английского, переводились и включались по возможности. Критерии исключения включали доклинические исследования (модели на животных или анализы in vitro), исследования безопасности или фазы 2, обзоры, испытания эффективности без анализов для нормальных видов микробиоты, только метагеномные методы, механизм действия нормальной микробиоты или пробиотика, поперечные исследования, отчеты о случаях или серии случаев, дублированные отчеты или исследования неуказанных типов пробиотиков.Были рассмотрены все фармакокинетические исследования на людях, поскольку в их рефератах часто не содержались данные нормального анализа микробиоты. Процесс извлечения данных и обзора соответствовал руководящим принципам заявления о предпочтительных элементах отчетности для систематических обзоров и метаанализов (PRISMA) с использованием контрольного списка из 27 пунктов и блок-схемы.30 Для сбора данных о пробиотике (тип штамма) использовалась стандартизированная форма извлечения данных. , суточная доза, продолжительность), тип контроля (плацебо, активное лечение или отсутствие лечения), дизайн исследования (состояние микробиоты на исходном уровне и время последующего наблюдения), тип анализа микробиоты (микробное культивирование, молекулярные биомаркеры и т. д.), включенное исследование популяция (взрослые и дети, здоровые добровольцы, болезненное состояние), тип и время действия деструктивного агента (антибиотики, химиотерапия и т. д.), размер и отсев исследования, оценка результатов (эффективность и / или статус микробиоты в конце исследования, нежелательные явления) и вид заявления о состоянии здоровья.
Результаты и определения
Первичным результатом является степень коррекции или улучшения микробиоты с помощью определенного штамма (ов) пробиотиков. Вторичный результат — это связь между степенью коррекции дисбиоза и чистой эффективностью, полученной в результате рандомизированных контролируемых испытаний пробиотических вмешательств. Дисбиоз определяется как изменение или нарушение нормальной микробиоты (бактериальные или грибковые виды) из-за воздействия разрушающего фактора (например, антибиотиков, хронических заболеваний, стресса, медицинских процедур или лекарств и т. Д.).Поскольку в настоящее время не существует стандартного определения «нормальной» микробиоты, для этого обзора восстановление нормальной микробиоты определяется как возвращение к анализируемым видам или профилю микробов, полученным у здорового человека (до того, как произойдет разрушительное событие). Включенные исследования должны иметь по крайней мере анализ лечения препробиотиками и анализ лечения постпробиотиками. В течение периода поиска (1985–2013) было доступно множество микробных анализов, включая документирование микробиоты либо с помощью микробных культур, либо с помощью метагеномных методов (нацеленные на 16s рРНК зонды с использованием флуоресцентной гибридизации in situ (FISH) или другого метода ПЦР) 8, 21, 28, 31 или косвенными методами (по шкале Ньюджента).15 баллов по шкале Ньюджента (от 0 до 10) используются для диагностики бактериального вагиноза (баллы ≥7) или нормальной микробиоты влагалища (баллы 0–3) на основе количественных морфотипов малых грамотрицательных палочек ( Gardnerella vaginalis / bacteroides spp) и изогнутые грамотрицательные палочки ( Mobiluncus spp), полученные при окрашивании по Граму мазков из влагалищных выделений. Микробиологические анализы только штаммов, содержащихся в пробиотическом продукте, считаются фармакокинетическими исследованиями и не включаются в профили нормальной микробиоты.
Модели дисбактериоза
Для определения воздействия на нормальную микробиоту были включены только прямые доказательства изменения микробиоты (виды, профили, индексы разнообразия или диагностические критерии), а косвенные эффекты были исключены (изменения кишечных ферментов, параметров иммунной системы или симптомов болезни). Степень улучшения дисбактериоза подразделяется на три уровня: (1) восстановление нормальной микробиоты до исходного уровня; (2) изменение или улучшение нормальной микробиоты; и (3) отсутствие изменений нормальной микробиоты.
Литература содержала три модели дисбиоза: модель A (восстановление нормальной микробиоты), в которой анализировали пациентов, зарегистрированных со здоровой, ненарушенной микробиотой, а затем снова анализировали после разрушительного события (такого как воздействие антибиотиков) и терапии пробиотиками; модель B (изменение микробиоты) оценивала пациентов с ранее существовавшей нарушенной микробиотой (например, уже существующее хроническое заболевание или активное заболевание), а затем после пробиотической терапии; Модель C (без дисбактериоза) тестировала добровольцев без разрушительного события (до или во время клинического испытания) как в препробиотический, так и в постпробиотический периоды, как показано на рисунке 1.«Восстановление» нормальной микробиоты определяется как восстановление микробиоты до нормального здорового исходного уровня. Восстановление может быть полным (все проанализированные уровни микробов вернулись к исходному уровню) или неполным восстановлением (частичное восстановление некоторых штаммов микробов, но не все вернулись к исходным уровням). В исследованиях, в которых участвовали участники с дисбиозом на исходном уровне (обычно из-за хронических заболеваний), невозможно показать восстановление нормального уровня микробиоты, поскольку нормальная, ненарушенная микробиота не присутствовала у этих типов участников исследования на момент включения в исследование.Следовательно, наиболее веские аргументы в пользу конструкции модели B — это «изменение или улучшение» микробиоты. В этой статье были проанализированы только данные участников, подвергшихся воздействию пробиотиков. Данные из контрольных групп использовались для подтверждения дисбактериоза у участников с хроническими заболеваниями или после разрушительного воздействия, такого как антибиотики или химиотерапия, не затронутых воздействием пробиотиков.32–34
Рисунок 1Временная последовательность событий и три модели дизайна исследований, определяющих три различные степени коррекции дисбиоза пробиотиками.
Оценка методической прочности и качества
Система GRADE (классификация рекомендаций, оценка, разработка и оценка) для оценки общего качества исследования будет использоваться для каждого пробиотического штамма или типа (отдельные штаммы и смеси штаммов) .35 Рекомендация в поддержку заявления о каждом пробиотическом штамме. или смесь могут быть оценены по общей силе доказательств («сильные», многие рандомизированные контролируемые испытания показывают значительное восстановление микробиоты, или «умеренные» — только одно рандомизированное контролируемое исследование; или «слабые», только серии случаев или отчеты, ограниченное количество малых испытаний и т. д.).
Качество доказательств основано на дизайне исследования и оценивается как «высокое качество» (четко определенный дизайн исследования для определения восстановления с нормальной микробиотой, модель A) или «среднее качество» (нарушение микробиоты на исходном уровне, модель B) или «низкое качество» (нарушение работы не произошло, модель C). Измерение систематической ошибки публикации в данном обзоре не оценивалось, поскольку объединенные оценки эффективности результатов не проводились, что типично для метаанализа, но все исследования с анализами микробиоты были включены для ограничения систематической ошибки.
Рейтинг чистой эффективности
Чтобы определить, связана ли способность корректировать дисбактериоз с клинической эффективностью, используйте опубликованную литературу для рандомизированных контролируемых исследований (РКИ) или мета-анализы пробиотиков для различных показаний заболевания, включая AAD, 5, 36, 37 CDI, 5, 38 IBD , 39 IBS, 40 TD, 41 эрадикация H. pylori , 36, 37 BV42 и лечение острой детской диареи были рассмотрены.43–45 Чистый рейтинг был рассчитан путем вычитания количества РКИ, показавших незначительную или эквивалентную эффективность из числа РКИ, показавших значительную эффективность.Ранги были разделены на следующие категории: ++, ≥2 чистых РКИ, показывающих значительную эффективность; +, чистые РКИ, показывающие значительную эффективность; 0, равное количество РКИ, показывающих значимые и незначимые результаты эффективности, и -, ≥1 чистое отрицательное или незначимое РКИ. Пробиотики, не прошедшие РКИ, не оценивались.
Результаты
Обзор литературы за 1985–2013 гг. Обнаружил 353 статьи, посвященные лечению пробиотиками и их потенциальному влиянию на нормальную микробиоту.
Исключенные исследования
Как показано на рисунке 2, в общей сложности 272 статьи были исключены по следующим причинам: обзоры (n = 116), исследования эффективности пробиотиков без данных о нормальных анализах микробиоты (n = 54), модели пробиотиков на животных и изменения микробиоты. (n = 38), только метагеномные методы или методы микробиоты (n = 17), исследования нормальной микробиоты, но без использования пробиотиков (n = 14), анализы микробиоты in vitro (n = 10), дублирующие отчеты (n = 2 ) или разные (n = 21), которые включали исследования механизма действия пробиотиков, исследования безопасности, дублирующие отчеты, перекрестные исследования и два с плохо описанными пробиотическими вмешательствами.46, 47 В общей сложности была рассмотрена 81 полная статья, в которой упоминались изменения в нормальной микробиоте или указывались требования к здоровью для пробиотиков и их влияние на нормальную микробиоту.
Рис. 2Блок-схема результатов обзора литературы (1985–2013) включенных и исключенных исследований по восстановлению или улучшению нормальной микробиоты с помощью пробиотиков. РКИ — рандомизированные контролируемые испытания; МОА, механизм действия; НМ, нормальная микробиота.
Фармакокинетические исследования пробиотиков (n = 18), в которых сообщалось о концентрациях пробиотических штаммов до и после лечения, но не анализировались на другие виды нормальной микробиоты, были исключены.Хотя в нескольких исследованиях, использующих этот дизайн исследования, утверждается, что пробиотики оказали влияние на нормальную микробиоту, тип полученных данных — это фармакокинетическое поведение самих пробиотиков, а не нормальная микробиота. Несколько исследований заявили, что нормальная микробиота была изменена, потому что после введения пробиотиков наблюдалось увеличение количества различных видов бактерий, но анализируемые виды были теми, которые содержались в пробиотическом продукте, поэтому это увеличение не является неожиданным. Фармакокинетические исследования документально подтвердили, что пробиотические штаммы, принимаемые перорально, могут выжить при прохождении через кишечный тракт со степенью выделения с фекалиями от <1% до 22%.48, 49 Эти фармакокинетические исследования были исключены из этого анализа, так как они не тестировали другие типы нормальной микробиоты, не обнаруженные в пробиотическом продукте.
Включены исследования
Из 63 включенных клинических испытаний пять испытаний включали несколько групп лечения, в результате чего в общей сложности было проанализировано 69 групп лечения. Engelbrektson и др. 50 протестировали смесь из пяти штаммов пробиотиков на добровольцах, подвергавшихся воздействию антибиотиков, а также протестировали смесь из четырех штаммов пробиотиков на здоровых добровольцах, не подвергавшихся воздействию антибиотиков.Zoppi и др. 51 использовали восемь различных групп лечения в своем исследовании, и в наш анализ были включены пробиотические группы ( Saccharomyces boulardii, отдельно и Lactobacillus rhamnosus GG ), смесь двух пробиотиков ( L. acidophilus и Bifido bifidum ) и смесь трех пробиотических штаммов ( L. acidophilus, L. rhamnosus и B. bifidum ). Orrhage et al. 52 использовали две группы лечения ( Bifido longum только и смесь B.longum и L. acidophilus ). Ларсен и др. 53 тестировали два отдельных пробиотика ( B. lactis и L. acidophilus ) в разных группах лечения. Lidbeck et al. 54 давали либо эноксацин, либо клиндамицин и рандомизировали пациентов либо L. acidophilus , либо плацебо.
Нормальные методы анализа микробиоты
Из 69 лечебных групп, в которых проводились нормальные анализы микробиоты, для профилирования микробиоты использовались различные методы.Во многих исследованиях использовались только стандартные микробиологические анализы культур (37, 54%), в то время как в других (28, 40%) использовались методы обнаружения некультивируемых бактериальных штаммов, которые включали метагеномные анализы (FISH, TRFLP, секвенирование 16 s рРНК) или другие ПЦР. техники. В некоторых исследованиях (4,6%) использовалась косвенная оценка нормальной микробиоты с использованием шкалы Ньюджента для диагностики бактериального вагиноза, которая основывается на окрашивании по Граму вагинальных выделений, pH влагалища и симптомах для определения наличия или отсутствия нормальной микробиоты.15
Штаммы пробиотиков
В 69 группах лечения большинство (36, 52%) использовали один штамм пробиотика, в то время как 14 (20%) тестировали смесь двух пробиотических штаммов и 19 (28%) тестировали смесь трех или более пробиотических штаммов. Распределение пробиотиков одного штамма по сравнению с множественными пробиотиками незначительно варьировалось в зависимости от модели исследования (= 2,3, p = 0,32). Из 15 групп реставрационного исследования (модель A) 47% использовали один штамм пробиотика и 53% использовали несколько штаммов. Из 25 групп лечения с нарушенной микробиотой на исходном уровне (модель B) 44% использовали один штамм и 56% использовали несколько штаммов.Из 29 групп исследования с неповрежденной микробиотой (модель C) 62% использовали один штамм и 38% использовали несколько штаммов.
Модель восстановления нормальной микробиоты (модель A)
Было найдено только 10 исследований (с 15 группами лечения) с использованием модели А для определения восстановления микробиоты (таблица 1) 32, 34, 50–52, 54–58 Тип включенных участников варьировался от здоровых добровольцев до детей с нелеченными респираторные инфекции, педиатрическим больным раком. Для участников с острыми инфекциями или раком базовые анализы проводились перед разрушающим агентом (антибиотиками или химиотерапией).Число участников, получавших пробиотики, составляло в среднем 20 на исследование и варьировалось от 5 до 83. В 93% разрушающим фактором было воздействие антибиотиков, а в одном исследовании химиотерапия вызвала нарушение микробиоты. Только 8 (53%) групп исследования выполнили анализ в течение периода наблюдения 1-8 недель после прекращения приема пробиотика.
Таблица 1Доказательные данные о восстановлении нормальной микробиоты (НМ) для 12 пробиотиков из 10 исследований (15 лечебных групп; модель A)
Анализ пробиотических штаммов по отдельности выявил только два пробиотических продукта в более чем одном рандомизированном контролируемом исследовании.Пробиотическая смесь L. acidophilus и B. bifidum показала полное восстановление в одном исследовании, но только частичное восстановление в другом (сила: сильная, качество: высокое). Пробиотическая смесь L. acidophilus (2 штамма) с B. bifidum и B. animalis показала полное восстановление в одном исследовании, но только частичное восстановление в другом (сила: сильная, качество: высокое). Пять других пробиотических продуктов только в одном подтверждающем клиническом исследовании показали восстановление микробиоты ( B.longum , Clost. butyricum , L. acidophilus , смесь L. acidophilus с L. paracasei и B. lactis и смесь L. acidophilus с L. paracasei и B. bifidum и два штамма B. lactis ; Прочность: умеренная, Качество: высокое). Три пробиотических продукта с одним подтверждающим клиническим испытанием показали частичное восстановление ( S. boulardii , L. rhamnosus GG, смесь L.rhamnosus с L. bifidus и L. acidophilus ; Прочность: умеренная, Качество: высокое). Только два пробиотических продукта с использованием модели А не показали изменений в микробиоте ( B. breve и смесь L. acidophilus и B. longum ; сила: умеренная, качество: высокое). Таким образом, 10 из 12 (83%) пробиотических продуктов показали полное или частичное восстановление нормальной микробиоты.
Из 11 пробиотических продуктов с заявлением о «восстановлении или улучшении нормальной микробиоты» 10 (91%) были поддержаны этим обзором, но только семь показали полное восстановление, а пять — частичное восстановление микробиоты (таблица 1).Смесь L. acidophilus и B. longum не показала никаких изменений в микробиоте. Wada и др. 32 заявили, что B. breve «усилены кишечными анаэробами», но это сравнивалось только с группой плацебо. Их данные показали, что химиотерапия является разрушительным событием, приводящим к увеличению количества энтеробактерий в кишечнике в группе плацебо, но к концу 8-недельного периода наблюдения в группе пробиотика или плацебо не наблюдалось значительных различий по сравнению с исходной микробиотой. уровни.
Нарушение нормальной микробиоты при исходных исследованиях (модель B)
Двадцать четыре исследования (с 25 группами лечения) использовали модель B, в которую были включены участники с уже существующей нарушенной микробиотой, связанной с текущим заболеванием или состояниями (таблица 2) .33, 53, 59–80 В среднем количество участников, получавших пробиотики, составляло 23 ± 16 / исследование и варьировались от 7 до 83 участников. Типы уже существующих факторов, нарушающих микробиоту, включали пациентов с атопическим дерматитом, аллергии, цирроз, бактериальный вагиноз, синдром раздраженного кишечника, воспалительные заболевания кишечника (язвенный колит и поучит), идиопатическую диарею, энтеральное питание, синдром короткой кишки и рак толстой кишки. .Только 10 (40%) исследуемых групп проводили анализ в течение периода последующего постпробиотического наблюдения.
Таблица 2Доказательные данные по улучшению или изменению нормальной микробиоты (NM) в 18 пробиотиках из 24 исследований (25 групп лечения) с нарушенной микробиотой на исходном уровне (модель B)
Три пробиотика прошли несколько клинических испытаний, чтобы подтвердить утверждение об улучшении микробиоты за счет пробиотика. S. boulardii использовался в двух испытаниях либо с пациентами с энтеральным питанием, либо с пациентами с активной диареей и обнаружил улучшение привычной микробиоты у пациентов с активной диареей, 66 но продемонстрировал только косвенные доказательства изменений короткоцепочечных жирных кислот в другое исследование65 (Сила: сильная, Качество: умеренное).Смесь из четырех пробиотических штаммов (2 штамма: L. rhamnosus , P. freudenreichii + B. breve ) показала улучшение микробиоты в двух клинических испытаниях74, 75 (сила: сильная, качество: умеренное). Из четырех клинических испытаний смеси семи пробиотических штаммов, два не показали значительных изменений в микробиоте, 77, 78 одно показало большее количество анаэробов при постпробиотической обработке79, а одно обнаружило уменьшение количества видов бактероидов80 (сила: сильная, качество: умеренная). Три клинических испытания определили, что не было значительных изменений в связи с Lactobacillus plantarum 299v62–64 (сила: сильная, качество: умеренное).Из этих пробиотиков только одно подтверждающее клиническое испытание (сила: умеренная, качество: умеренное), два отдельных пробиотических штамма ( E. coli, Nissle и L. casei rhamnosus ) и пять различных смесей пробиотических штаммов подтверждают утверждение, пробиотик изменяет микробиоту (таблица 2). Таким образом, 10 из 18 (56%) пробиотических продуктов изменили или улучшили микробиоту у людей с ранее существовавшим заболеванием.
Из 25 лечебных групп утверждение статьи было подтверждено в 14 (56%) исследованиях.Не было значительного изменения микробиоты из-за пробиотика в девяти группах лечения и только изменение микробиоты в пяти других (таблица 2). Наш обзор не согласился с заявленными результатами в 11 (46%) других группах лечения. В семи группах лечения было заявлено, что тестируемый пробиотик «восстановил нормальную микробиоту», но неясно, как был сделан этот вывод, поскольку не было времени, когда нормальная неповрежденная микробиота присутствовала. Из семи исследований, в которых утверждалось, что пробиотики «восстановили» нормальную микробиоту, наш анализ показал, что ни одно из них не способно документально подтвердить восстановление, но в этих исследованиях подтверждается, что пробиотики улучшили или изменили микробиоту.В четырех исследованиях утверждалось, что пробиотик «изменил или улучшил» нормальную микробиоту, но в этом обзоре не было обнаружено значительных различий при сравнении постпробиотических и исходных анализов для групп пробиотиков. Girard-Pipau и др. 65 пришли к выводу, что S. boulardii «изменили нормальную флору», потому что в группе пробиотиков обнаруживалось больше грамположительных анаэробов по сравнению с контрольной группой, а в группе наблюдалось увеличение трех короткоцепочечных жирных кислот. S. boulardii группа.Однако, когда анализ ограничивается тенденциями, наблюдаемыми только в группе пробиотиков, не наблюдалось никаких существенных различий в профилях микробиоты препробиотиков и постпробиотиков. Вентури и др. 77 пришли к выводу, что смесь из семи пробиотических штаммов увеличивает концентрацию некоторых полезных штаммов в кишечнике. Однако единственными штаммами, у которых наблюдалось значительное увеличение, были штаммы, содержащиеся в смеси пробиотиков, а не конкретно нормальная микробиота хозяина. Поскольку это исследование не имело исходного уровня микробиоты, увеличенное количество лактобацилл и бифидобактерий могло не отражать их нормальные уровни.Van der Aa и др. 59 утверждали, что B. breve «успешно модулирует кишечную флору», но не наблюдалось никаких значительных изменений в группе пробиотиков при сравнении исходного уровня с уровнями постпробиотика. Odamaki и др. 33 действительно показали увеличение Faecalibacterium spp и Bacteroides fragilis spp в конце лечения B. longum BB536, но такое же увеличение наблюдалось и в группе плацебо.
Непрерывные исследования нормальной микробиоты (модель C)
В 29 испытаний были включены здоровые взрослые люди, у которых во время исследования не присутствовал деструктивный фактор (отсутствие антибиотиков, отсутствие лекарств или наличие острого или хронического заболевания), которые могли бы повлиять на нормальную микробиоту, как показано в таблице 3.14, 49, 50, 81–106. Среднее количество участников, получавших пробиотики, составляло 23 человека в исследовании и варьировалось от 7 до 160 человек в исследовании. Из 29 групп исследования анализы проводились в течение периода наблюдения только в 52%. Fujiwara и др. 84 культивировали семь здоровых добровольцев и обнаружили энтеробактерии и видов Clostridial после B. longum было уменьшено на 10 1 / г по сравнению с исходным уровнем (p <0,03), но никаких других изменений в микробиоте не произошло. были обнаружены. Karlsson et al 94 обнаружили значительное увеличение кишечного разнообразия у девяти добровольцев мужского пола с атеросклерозом, получавших L.plantarum 299v, но поскольку тесты полиморфизма длин концевых рестрикционных фрагментов использовались вместо культур для видов бактерий, специфические изменения в видах микробиоты не могли быть определены. Ян и Шеу культивировали 63 ребенка (55% с Helicobacter pylori ), которым давали йогурт с L. acidophilus и B. lactis , но обнаружили только снижение количества E. coli в H.pylori отрицательных в подгруппе детей, существенных изменений нормальной микробиоты у H.pylori — положительные дети.100 Кубота и др. 103 обследовали 29 участников с аллергией на пыльцу японского кедра и обнаружили, что молоко, ферментированное с помощью L. rhamnosus GG и L. gasseri TMC0356, подавляло изменения микробиоты (меньше изменений кишечного профиля), но не удалось определить изменения конкретных видов бактерий из-за типа используемого анализа (FISH и TRFLP) .103 Таким образом, только 4 из 19 (21%) пробиотических продуктов изменили микробиоту у здоровых людей, у которых не было разрушительного события.
Таблица 3Модель C: Доказательные данные по улучшению или изменению нормальной микробиоты (NM) в 19 пробиотиках у здоровых добровольцев, включенных в 29 исследований (29 лечебных групп) в исследованиях без разрушительного воздействия
Из семи исследований, в которых утверждалось, что их пробиотики «восстанавливают или изменяют» нормальную микробиоту, только четыре утверждения были подтверждены. Сьерра и др. 96 заявили, что Lactobacillus salivarius дали 20 здоровым взрослым «улучшенная микробиота кишечника», но были обнаружены только повышенные уровни Lactobacilli, и никаких других изменений у нормальных видов микробиоты обнаружено не было.Единственное другое свидетельство было косвенным из наблюдаемых изменений иммунных параметров. He и др. 99 заявили о смеси B. longum и B. animalis «модифицированной» микробиоты, но изменения наблюдались только во время приема йогурта, а не после периода наблюдения в течение 1 недели. Витали и др. 14 утверждали, что смесь из четырех штаммов лактобактерий и трех штаммов бифидобактерий «модулировала вагинальную микробиоту», но единственные значительные изменения были связаны с увеличением количества видов бактерий, содержащихся в смеси пробиотиков.
из пробиотиков, подтвержденных множеством клинических испытаний ( B. animalis , B. longum , L. casei , L. plantarum 299v, смесь B. animalis и B. lactis ), 13 испытаний (87%) подтверждают отсутствие значительного изменения нормальной микробиоты, если микробиота не нарушена (сила: сильная, качество: низкое).
Ассоциация клинической эффективности и восстановления нормальной микробиоты
В нескольких исследованиях одновременно сравнивалась клиническая эффективность и способность восстанавливать или улучшать нормальную микробиоту после дисбактериоза.Был проведен синтез литературы по РКИ по восьми распространенным показаниям болезни и оценена общая сила сети. Эффективность пробиотиков, способных восстанавливать нормальную микробиоту, часто подтверждалась РКИ, как показано в таблице 4. Из 10 пробиотиков с доказательствами восстановления 7 (70%) также прошли по крайней мере одно рандомизированное испытание по крайней мере для одного из восьми. болезней, в то время как 30% не имели поддерживающих РКИ по эффективности. Из семи пробиотиков, включенных в ассоциированные РКИ, только два пробиотика ( S.boulardii и L. acidophilus ) имеют убедительные доказательства эффективности при большинстве показаний к заболеваниям, тогда как пять пробиотиков, способных восстанавливать микробиоту, имели слабые доказательства эффективности или отсутствовали. Например, S. boulardii , у которого есть исследования, поддерживающие восстановление, имеет убедительные доказательства клинической эффективности для AAD (рейтинг ++: 11 РКИ имели значимые результаты, а 6 имели незначительные результаты), CDI (рейтинг ++: было два РКИ со значительными результатами. ), IBD (с рейтингом ++: было два РКИ со значительными результатами), IBS (с рейтингом 0: было одно РКИ со значительной эффективностью и одно РКИ с незначительными результатами), TD (с рейтингом +: 3 РКИ со значительной эффективностью и 2 с незначительными эффективность), H.pylori (ранжирование -: 2 РКИ со значительными результатами и 4 с незначительными результатами) и отсутствие исследований по BV. L. acidophilus , который частично восстановил микробиоту в исследовании, связан с клинической эффективностью при AAD, IBS и BV, но не в отношении TD или ликвидации H. pylori и лечения острой детской диареи (рейтинг ++: имел 19 РКИ со значительной защитой и пять с незначительными результатами). Напротив, L. rhamnosus GG, другой пробиотик, способный восстанавливать микробиоту, часто упоминается в метаанализе как имеющий значительную эффективность в отношении AAD.Наши результаты обновленного обзора литературы указывают на чистую слабую оценку клинической эффективности по всем показаниям болезни: AAD (оценено -: 3 РКИ имели значимые результаты, а 6 — незначительные результаты), CDI (оценено -: два РКИ с несущественные результаты), IBD (ранг -: одно РКИ с несущественными результатами), IBS (оценка 0: 2 РКИ со значительной эффективностью и два РКИ с незначительными результатами), TD (оценка 0: одно РКИ со значительной эффективностью и один с незначительной эффективностью), H.pylori (рейтинг -: 3 РКИ с незначительными результатами), отсутствие РКИ по БВ и лечению острой детской диареи (рейтинг ++: 10 РКИ со значительной эффективностью и одно с незначительными результатами).
Таблица 4Сравнение способности пробиотика восстанавливать или улучшать дисбактериоз с ранжированной клинической эффективностью при различных показаниях заболевания
Испытания эффективности не проводились так часто для пробиотиков, которые, как было показано, обладают способностью только изменять или улучшать, но не восстанавливать микробиоту после дисбактериоза.Из девяти пробиотиков, которые могут изменять микробиоту, 6 (67%) имели поддерживающие РКИ по крайней мере для одного заболевания, но разнообразие исследованных заболеваний было более ограниченным. L. casei имел умеренную чистую силу для AAD и бактериального вагиноза, но был нейтральным в отношении способности уничтожить H. pylori. и другие показания к болезни не тестировались в РКИ с L. casei . Пробиотическая смесь L. reuteri и L. fermentum имеет убедительные доказательства бактериального вагиноза, но не имеет никаких других показаний, перечисленных в таблице 4.
Из восьми пробиотиков, не способных изменять или восстанавливать нормальную микробиоту, только L. plantarum 299v прошли РКИ на ААД и СРК, оба с отрицательной или слабой клинической эффективностью. B. lactis и смесь L. rhamnosus и L. reuteri имели чистую нейтральную оценку эффективности для лечения острой детской диареи. Для других четырех пробиотических продуктов, не влияющих на нормальную микробиоту, не было РКИ клинической эффективности.В исследованиях с Bacillus clausii не проводился анализ на нормальную микробиоту, и были получены незначительные результаты испытаний по искоренению H. pylori и лечению детской диареи.
Из шести пробиотиков с данными только о фармакокинетике самого пробиотика и без других исследований других нормальных штаммов микробиоты, пять имели РКИ, показывающие различную чистую эффективность при различных показаниях, как показано в таблице 4.
Шесть популярных пробиотиков ( B.clausii , B. infantis , L. reuteri , L. acidophilus + L. helveticus , L. acidophilus + L. casei и L. acidophilus + B. animalis ) имеют только РКИ клинической эффективности, но не опубликовали исследования, посвященные их роли в восстановлении или улучшении нормальной микробиоты.
Обсуждение
Разработка и оценка заявлений о здоровье или функциональности пробиотиков является важной проблемой и в настоящее время определена как приоритетная для исследований несколькими международными организациями, включая Всемирную гастроэнтерологическую организацию107 и Американское общество питания.2 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США борется с обоснованными утверждениями о пользе для здоровья пробиотических продуктов и в настоящее время рекомендует использовать утверждения о структуре / функции, такие как «поддерживает регулярность кишечника», но утверждение о восстановлении нормальной микробиоты все еще обсуждается. 108 Европейское управление по безопасности пищевых продуктов (EFSA) предоставляет руководящие материалы, которые рекомендуют, чтобы заявления о здоровье или функциональности пробиотиков имели положительный физиологический эффект и имели соответствующие научные испытания для подтверждения заявлений о пользе для здоровья.3 Приемлемые утверждения о здоровье кишечника могут включать функциональные утверждения (улучшенное время прохождения, более мягкая консистенция стула, уменьшение желудочно-кишечного дискомфорта, защита от патогенов). Поскольку в настоящее время невозможно определить стандартный профиль нормальной микробиоты, EFSA рекомендует, чтобы функциональные заявления о восстановлении нормальной микробиоты документировали восстановление здоровой микробиоты и сопровождались благоприятным физиологическим или клиническим результатом3. Кроме того, поскольку эффективность и механизмы зависят от штамма и могут варьироваться в зависимости от штамма пробиотика, данные должны анализироваться для каждого пробиотического продукта индивидуально.5, 6, 9, 109 — 112
Недооцененным открытием было влияние дизайна исследования и исследуемых групп на интерпретацию результатов исследования. В литературе обычно встречаются пять различных типов дизайна исследований, касающихся пробиотиков. Наиболее распространенным типом исследования является рандомизированное контролируемое исследование, в котором проверяются результаты эффективности и безопасности у пациентов, но в этих исследованиях обычно не документировалось влияние пробиотика на нормальную микробиоту. Вторым наиболее распространенным типом дизайна исследования являются фармакокинетические исследования (документирование восстановления пероральной дозы пробиотика или увеличения пробиотических штаммов после лечения по сравнению с предварительной обработкой или клиренсом пробиотика).Несмотря на то, что в этих кинетических исследованиях не проводился анализ на штаммы, не являющиеся пробиотиками, некоторые экстраполировали их результаты и пришли к выводу, что их пробиотики наблюдали некоторый эффект или улучшение нормальной микробиоты.19, 111 Эти два первых типа исследований не поддерживают доказательную базу. выводы о восстановлении или изменении нормальной микробиоты и были исключены из этого обзора.
Для изучения дисбактериоза подходят три типа исследований. В первом типе исследования нормальная микробиота анализировалась как минимум дважды (на исходном уровне, то есть до воздействия разрушительного события или пробиотиков, а затем еще раз во время или после лечения пробиотиками), чтобы продемонстрировать фактическое восстановление исследуемой нормальной микробиоты до здоровых исходных уровней.Второй тип дизайна исследования начался с неподходящих исходных условий (исходные образцы, взятые после того, как нормальная микробиота была нарушена хроническим заболеванием). Для пациентов с установленными хроническими заболеваниями нет исходного уровня «нормальной микробиоты» ни в группе пробиотиков, ни в контрольной группе. Даже если исходные данные взяты во время ремиссии, на микробиоту все еще могут влиять хронические заболевания или острая диарея. Исследования пробиотиков при хронических заболеваниях или острых заболеваниях обычно сообщают о «пре-пробиотическом лечении» и «пост-пробиотическом лечении» и могут показывать значительные изменения в микробных видах, но неясно, отражает ли это истинное восстановление нормальных профилей микробиоты. .В исследование третьего типа были включены здоровые добровольцы, которым не вводили антибиотики (так что нормального нарушения микробиоты не происходило), и они демонстрировали только влияние пробиотиков на здоровую микробиоту (как правило, слабые или нулевые эффекты). Контрольные группы не требовались для нашей оценки воздействия пробиотиков на микробиоту, но контрольные группы могут задокументировать степень нарушения нормальной микробиоты провоцирующими агентами (антибиотиками, началом болезни и т. Д.).
Пять пробиотиков с одним штаммом ( B.longum , Clost. butyricum , L. acidophilus, L. rhamnosus и S. boulardii ) и пять пробиотических смесей (( L. acidophilus + B. bifidum) , ( L. rhamnosus + L. bifidus L. + L. acidophilus) , ( L. acidophilus + L. paracasei + B. lactis), (L. acidophilus , 2 штамма, B. bifidum, B. animalis) и (L . acidophilus + L. paracasei + B. bifidum + 2 штамма B.lactis )) задокументировано полное или частичное восстановление нормальной микробиоты (модель A). Только две смеси пробиотиков ((смесь 2 штаммов: L. acidophilus + B. bifidum ) и (смесь 4 штаммов: L. acidophilus , 2 штамма, B. bifidum, B. animalis )) были поддержаны подтверждающее исследование. Доказательства того, что пробиотики могут изменять или улучшать нормальную микробиоту (модель B), были обнаружены для трех пробиотиков одного штамма ( E. coli Nissle, S. boulardii и L.casei rhamnosus ) и семь смесей из 2-7 пробиотических штаммов. Из этих 10 пробиотиков, обнаруживших изменение микробиоты, только три прошли несколько испытаний: S. boulardii , смесь из четырех штаммов (2 штамма L. rhamnosus + P. freudenreichii + B. breve ) и смесь из семи штаммов. (4 лактобациллы и 3 штамма бифидобактерий), но только у одного были стабильные результаты, свидетельствующие об улучшении микробиоты.74, 75 Очевидно, что для подтверждения воздействия пробиотика на нормальную микробиоту необходимо более одного исследования.Из 19 пробиотических штаммов (или смесей), изученных на здоровых добровольцах, которые не подвергались воздействию разрушающих факторов (модель C), никаких изменений в нормальной микробиоте не наблюдалось для 79%, что указывает на устойчивость микробиоты.
Улучшение нормальной микробиоты за счет определенных штаммов пробиотиков, по-видимому, было связано с лучшими клиническими конечными точками. В рамках восьми распространенных заболеваний, обычно лечатся пробиотиками, большее количество испытаний со значительной эффективностью было связано с пробиотическими штаммами, восстанавливающими нормальную микробиоту, и только одно испытание со значительной эффективностью было обнаружено для пробиотиков, которые не влияли на микробиоту.Однако немногие пробиотики прошли испытания на эффективность при всех восьми заболеваниях, а многие не имели испытаний на эффективность.
Некоторые пробиотики, эффективность которых при различных заболеваниях опубликована, не имели исследований, изучающих влияние пробиотика на нормальную микробиоту: B. clausii , B. infantis , L. brevis , L. reuteri , смесь двух штаммов ( L. acidophilus + L. helveticus ), смесь двух штаммов ( L. acidophilus + L.casei ) или ( L. acidophilus + B. animalis ), смесь четырех штаммов ( L. rhamnosus (два штамма), P. freudenreichii + B. animalis )) и смесь семи штаммы ( L. sporogens, L. bifidum, L. bulgaricus, L. thermophilus, L. acidophilus, L. casei, L. rhamnosus) .
Сравнение результатов с другими исследованиями
Другие обзоры в литературе заявлений о пробиотиках, связанных с изменениями в нормальной микробиоте, были сосредоточены на широких вопросах нормативной стандартизации заявлений о здоровье или функциях, использовании надлежащего дизайна исследований и задаче определения биомаркеров для «здоровой микробиоты». .3, 29, 112 Донован и др. 2 рекомендует, чтобы заявления о пользе пробиотиков для здоровья подтверждались хорошо проведенными испытаниями на людях в целевой группе населения. Эти обзоры также рекомендуют коррелировать биомаркеры кишечника с клиническими конечными точками, однако ни один из этих обзоров не пытался этого сделать.29, 112 В предыдущих обзорах не предпринимались попытки проанализировать связь между штаммами пробиотиков и их влиянием на нормальную микробиоту путем стратификации по качество дизайна исследования.111 В этом обзоре эти проблемы были устранены путем анализа штаммов пробиотиков по качеству дизайна исследования и включения только испытаний, в которых оценивалась нормальная микробиота (либо с помощью микробного культивирования, либо с помощью биомаркеров молекулярных штаммов) и оценивалась степень улучшения дисбактериоза с помощью клинических данных. результаты для каждого пробиотического штамма.
Возможности для будущих исследований
В большинстве исследований (80%) с использованием модели А для документирования восстановления нормальной микробиоты использовались только методы микробиологического культивирования, которые позволяют обнаруживать только те организмы, которые растут в культуре. Использование более совершенных молекулярных метагеномных методов показало, что одно культивирование пропускает до 95% этих организмов.21, 22 Использование метагеномных методов было более распространено в исследованиях с использованием модели B (48%) и модели C (45%). ) планы исследований, которые направлены только на возможное изменение микробиоты.Характеристика микробиоты — сложный вопрос, и всесторонний учет всех бактериальных и грибковых штаммов в организме выходит за рамки наших текущих возможностей. Таким образом, любые исследования изменений микробиоты в лучшем случае неполны, но общие тенденции в бактериальных филотипах могут быть задокументированы с помощью ДНК-зондов и метагеномных методов. Ошибка дифференциального обнаружения может присутствовать из-за разнообразия анализов, используемых в этих исследованиях, и ее следует учитывать в будущих исследованиях.
Еще одно предложение для будущих исследований состоит в том, чтобы включить постпробиотический период в соответствующий период наблюдения.Менее половины рассмотренных исследований проводили анализы на нормальную микробиоту в течение соответствующего периода наблюдения. Как было показано, восстановление от разрушающего фактора может быть продлено (обычно 8 недель) 7, 8, и исследования, которые не смогли обнаружить восстановление микробиоты, могли обнаружить возврат к нормальным исходным уровням, если для восстановления было уделено достаточно долгое время. произошло. В будущих исследованиях должно быть предусмотрено время для восстановления нормальной микробиоты.
Поскольку действие пробиотиков зависит от штамма, и во многих исследованиях обычно указывается только род и вид протестированного пробиотика, будущие отчеты должны включать полное описание пробиотика до уровня окрашивания.5, 112
Сильные и слабые стороны
Сильные стороны этого обзора включали полноту стратегии поиска, которая проверяла несколько баз данных цитирования, реестры клинических испытаний и поиск авторов, использование установленных протоколов PRISMA для обзоров и использование схемы классификации результатов для различных степеней оценки восстановления микробов. Этот анализ контролировал смешанные эффекты различных исследуемых популяций и дизайнов исследований, представленных в литературе.Были исключены фармакокинетические исследования только самого пробиотического штамма (ов), и были включены только испытания, в которых анализировали другие виды, обнаруженные в микробиоте. Применяя стандартное определение для «восстановления» и «улучшения» нормальной микробиоты, можно различать существенные различия по типу используемых дизайнов исследований и различным эффектам различных штаммов пробиотиков. Ограничения этого обзора включают: один автор проанализировал и извлек литературу, объединил испытания, проведенные в разных популяциях (взрослые и дети), а также использовались разные дозы и схемы пробиотиков.Неполный поиск всех исследований, оценивающих влияние пробиотиков на микробиоту человека, также является потенциальным ограничением любого поиска в литературе. Еще одним ограничением является то, что улучшение дисбактериоза и клиническая эффективность пробиотических штаммов также косвенно связаны, прямая причинно-следственная связь с типами проведенных исследований невозможна. Еще одним ограничением является отсутствие в настоящее время стандартного определения того, что составляет «нормальную микробиоту». Состав микробиоты зависит от человека, возраста, географического положения и состояния здоровья хозяина.Современные микробиологические методы улучшаются, но не могут обнаружить все виды, присутствующие в организме хозяина.
Роль дисбактериоза нижних дыхательных путей при астме: дисбактериоз и астма
С развитием методов, не зависящих от посева, многочисленные исследования показали, что нижние дыхательные пути не являются бесплодными для здоровья и содержат различные микробные сообщества. Кроме того, новые данные свидетельствуют о том, что у людей с хроническими респираторными заболеваниями существует отчетливый микробиом нижних дыхательных путей.Чтобы понять роль дисбактериоза нижних дыхательных путей в патогенезе астмы, в этой статье мы рассматриваем опубликованные отчеты о микробиоме легких здоровых людей в контрольной группе, даем представление о вкладе дисбактериоза нижних дыхательных путей в астму, особенно стероидно-резистентную астму. и обсудить потенциальные методы лечения дисбактериоза нижних дыхательных путей.
1. Введение
Человеческое тело заселено триллионами комменсальных микроорганизмов, известных как человеческий микробиом, покрывающих кожу, кишечник, верхние дыхательные пути и полость рта, а также мочеполовые пути [1].Эти микроорганизмы могут быть полезными или потенциально патогенными. Микробиом человека представляет собой сложную экосистему, в которой обычно существует симбиотическое взаимодействие между хозяином и микроорганизмами. Поддержание гармоничного состояния между микроорганизмами и хозяином объясняет множество положительных эффектов. Например, известно, что микробиом кишечника влияет на иммунитет хозяина, уравновешивая активность Т-хелперных (Th) клеток типа 1 и Th-2 и играя фундаментальную роль в индукции воспалительных или толерогенных состояний [2, 3].Дисбиоз, известный как дисбаланс в составе бактериального микробиома, связан с воспалительной реакцией хозяина [4, 5], также может быть важным важным фактором в развитии или хронизации заболеваний человека, таких как воспалительное заболевание кишечника, диабет и астма. [6–8].
За последние шесть лет, с развитием технологий секвенирования, нижние дыхательные пути больше не считаются стерильными, и все больше данных подтверждают концепцию о том, что здоровый микробиом легких может иметь временные изменения, которые могут повлиять на прогрессирование заболевания. болезнь [7, 9–13].Кроме того, новые данные свидетельствуют о различиях в микробиоме нижних дыхательных путей у здоровых людей и людей с хроническими респираторными заболеваниями, такими как хроническая обструктивная болезнь легких (ХОБЛ) и астма [7, 14–16].
Астма — гетерогенное воспалительное заболевание, проявляющееся в повторяющихся обострениях хрипов, одышки, стеснения в груди и кашля, с множеством различных фенотипов и эндотипов [17, 18]. Симптомы большинства пациентов с астмой можно облегчить с помощью бета2-агонистов короткого действия и низких доз ингаляционных кортикостероидов (ICS), которые являются терапией первой линии для большинства пациентов; однако примерно 10% пациентов нуждаются в максимальной дозе ИКС [19], а от 5% до 10% взрослых с астмой устойчивы к стероидному лечению, что составляет более половины связанных с астмой медицинских расходов [20].Понимание вклада микробиоты нижних дыхательных путей в патогенез астмы, особенно резистентной к стероидам астмы, может изменить наше понимание астмы и предоставить новые терапевтические цели. Чтобы понять роль дисбактериоза нижних дыхательных путей в патогенезе астмы, в этой статье мы рассматриваем опубликованные отчеты о микробиоме легких как у здоровых субъектов, так и у пациентов со стабильной астмой в отсутствие инфекции. Цель обзора — консолидировать текущие знания о микробиоме дыхательных путей у здоровых людей, дать представление о дисбактериозе дыхательных путей и измененной иммунной системе хозяина, а также обсудить потенциальные методы лечения дисбиоза нижних дыхательных путей.
2. Новые вызовы: микробиом легких в здоровье
Микробиом человека обладает исключительной способностью существовать даже во враждебной среде. Это включает в себя нижние дыхательные пути из-за его постоянного воздействия на окружающую среду с большим объемом воздушного потока через влажные верхние дыхательные пути, в которых обитает сложная микробная популяция [21]. Высокопроизводительные методы секвенирования нового поколения показали, что, как и другие поверхности эпителия, нижние дыхательные пути содержат различные микробные сообщества [10–13, 22–24], которые оказывают влияние на местный иммунологический гомеостаз у нормальных людей [4, 5] .
2.1. Микробиом нижних дыхательных путей у здоровых субъектов
Хилти и его коллеги впервые описали, что нижние дыхательные пути у восьми здоровых субъектов содержали характерный микробиом с использованием технологии секвенирования маркера гена 16S рРНК из образцов, полученных при бронхоскопии в 2010 году, и бактерии отличаются от бактерий из верхних дыхательных путей. дыхательных путей [10], а Charlson et al. обнаружили специфический для легких микробиом, который напоминал верхние дыхательные пути у шести здоровых людей, путем измерения численности и состава бактерий в нескольких местах с помощью маркера гена 16S рДНК [11].С тех пор в многочисленных исследованиях была описана характеристика микробиома нижних дыхательных путей у здоровых субъектов, состоящая из низкой бактериальной нагрузки и относительно разнообразного бактериального состава [11-13, 22-24]. При анализе на уровне филума, Proteobacteria, Firmicutes и Bacteroidetes являются доминирующими типами, наблюдаемыми в нижних дыхательных путях здоровых. Преобладающий род бактерий среди здоровых людей включает Streptococcus, Pseudomonas , Prevotella , Fusobacteria , Veillonella , Neisseria и Haemophilus [10, 12, 23–25].
Интересно, что основная группа легочных бактерий была предложена у здоровых людей. Образцы бронхоальвеолярного лаважа (БАЛ) от десяти здоровых субъектов идентифицировали семь основных членов, которые включали Pseudomonas , Streptococcus , Prevotella , Fusobacterium , Haemophilus , Veillonella и Porphyromonella [12]. Другое исследование 257 образцов мокроты выявило четырех ключевых членов, включая Prevotella , Neisseria , Veillonella и Streptococcus [24].Однако исследование на мышах показало, что преобладающий бактериальный сдвиг от Gammaproteobacteria и Firmicutes к Bacteroidetes на уровне филы в течение первых 2 недель после рождения [26]. Между тем, исследование здоровых младенцев показало, что респираторная микробиота динамична [27]. Следовательно, вопрос о том, существует ли постоянная основная группа, требует дальнейшего изучения.
Поскольку исследование микробиома легких — новая область, недостаточно исследований, посвященных этому вопросу, и требующих дальнейшего разъяснения; необходимо стандартизировать технологию и анализ, чтобы можно было сравнивать растущие данные, чтобы составить наше представление о составе здорового микробиома дыхательных путей.
2.2. Факторы, влияющие на состав микробиома нижних дыхательных путей
Данные свидетельствуют о том, что микробиота нижних дыхательных путей может быть связана с факторами хозяина, такими как генетический полиморфизм и иммунный статус, а также с множеством факторов окружающей среды (например, воздействием окружающей среды, происхождением и образом жизни) , как и в случае кишечной микробиоты [24, 25].
Генетика хозяев оказалась важным фактором, влияющим на состав микробиоты дыхательных путей в когортном исследовании семьи близнецов путем оценки наследуемости каждого таксона микробов [24].Исследование когорты близнецов продемонстрировало, что генетический полиморфизм хозяина может влиять на состав микробиома дыхательных путей [24]. Анализ микробиома кишечника на основе 16S рРНК у 1126 пар близнецов из Соединенного Королевства показал, что определенные виды, содержащие Bifidobacterium, являются наследственными и пригодными для изготовления. Как и в микробиоме кишечника, в происхождении микробиома нижних дыхательных путей могут быть генетические факторы [28]. Кроме того, легкие плода, вероятно, приобретают свои микробные сообщества после рождения. По мере прохождения плода через родовые пути поверхности слизистой оболочки младенца покрываются микробами их матери, которые в последующие дни и недели дифференцируются на специфичные для конкретных участков сообщества [29, 30].С другой стороны, иммунный статус хозяина также может влиять на микробиоту дыхательных путей. Исследование микробиома легких у ВИЧ-инфицированных пациентов показало, что Tropheryma whipplei намного чаще встречается в БАЛ у ВИЧ-положительных людей по сравнению с ВИЧ-отрицательными людьми [31]. Этот результат согласуется с другим исследованием, в котором сообщалось, что изменение микробиома легких связано с ВИЧ-инфекцией [32]. А новое исследование, опубликованное Морейрой и его коллегами, показывает, как бактерия Burkholderia multivorans эволюционирует и адаптируется в легких пациентов с муковисцидозом [33].Приведенные выше результаты показывают, что на микробиом дыхательных путей влияет иммунный ответ хозяина, и бактерии могут развиваться, адаптируясь к определенной среде легких.
На микробиом также влияет окружающая среда. В раннем возрасте дети, которые растут на ферме или имеют тесный контакт с сельскохозяйственными животными и домашними собаками, имеют сниженный риск астмы, что, как считается, связано с повышенным воздействием разнообразных бактерий [34–37]. Линч и его коллеги использовали методы, не зависящие от культуры, для изучения бактериального состава образцов домашней пыли, собранных в течение первого года жизни.Результаты показали, что здоровые дети подвергались воздействию более богатых и разнообразных бактериальных сообществ по сравнению с детьми, у которых развилась атопия или сообщалось о повторяющихся хрипах [38]. При интерпретации данных микробиоты также следует учитывать географические различия, поскольку сообщалось о явных различиях в микробиоме кишечника в зависимости от разного географического происхождения [39], а у пациентов с муковисцидозом из разных стран наблюдалась разная микробиота дыхательных путей [40].Влияние состава воздушных бактериальных сообществ и различного географического происхождения на состав микробиоты нижних дыхательных путей в предыдущих исследованиях не описывалось. Среди множества факторов образа жизни курение сигарет и воспаление дыхательных путей, по-видимому, изменяют состав микробиома верхних дыхательных путей (включая носоглотку и ротоглотку) в исследовании здоровых бессимптомных взрослых, включая 29 курильщиков и 33 некурящих [41]. Кроме того, другое исследование 257 образцов мокроты у здоровых взрослых показало, что статус курения значительно коррелировал со структурой микробного сообщества, и 54 курильщика были значительно обогащены родами Veillonella и Megasphaera по сравнению со 170 некурящими.Это говорит о том, что курение сигарет может влиять на общую структуру микробного сообщества [24]. Напротив, другие исследования показывают аналогичную гетерогенность бактериальных сообществ нижних дыхательных путей, которые существуют у здоровых курильщиков и некурящих [12, 23]. Кроме того, исследование образцов индуцированной мокроты у 44 курильщиков-астматиков показало, что у курильщиков, страдающих астмой, было большее бактериальное разнообразие по сравнению с некурящими здоровыми людьми в контрольной группе, и что отказ от курения не привел к изменению бактериального сообщества [42].В настоящее время мы очень плохо понимаем влияние сигаретного дыма на нижние дыхательные пути, поэтому необходимо больше внимания и внимания, чтобы понять влияние табачного дыма на микробиом нижних дыхательных путей.
Таким образом, факторы хозяина и окружающей среды могут влиять на состав микробиома нижних дыхательных путей.
2.3. Происхождение микробиома нижних дыхательных путей
Микробная колонизация начинается сразу после рождения. Когда плод рождается вагинально или через кесарево сечение, поверхности слизистой оболочки младенца покрываются микробами их матери, которые различаются в зависимости от способа доставки и дифференцируются на локальные сообщества в последующие дни и недели, поэтому легкие плода, вероятно, приобретают микробные бактерии. сообщества вскоре после рождения [29, 30].Недавние исследования показали, что респираторная микробиота здоровых младенцев постепенно превращается в динамичные и сложные микробные сообщества, которые могут влиять на восприимчивость к респираторным заболеваниям [27, 43]. Однако большинство исследований микробиоты дыхательных путей у здоровых младенцев основано на исследованиях верхних дыхательных путей из-за практичности получения образцов от этой популяции.
У взрослых микробиом нижних дыхательных путей, вероятно, заселяется через верхние дыхательные пути (нос и горло), ротовую полость и желудочно-кишечный тракт.Чарлсон и др. . выполнил интенсивный отбор проб из нескольких участков дыхательных путей у шести здоровых людей, используя технику с двумя бронхоскопами, чтобы избежать перекрестного загрязнения проб, и описал состав сообщества и разнообразие микробиома дыхательных путей в целом [11]. Исследование показало, что микробиом дыхательных путей был гомогенным с более низкой бактериальной нагрузкой в нижних дыхательных путях и неотличимым по составу населения по сравнению с верхними дыхательными путями.И наоборот, исследование, изучающее состав микробиома нижних дыхательных путей у 10 здоровых участников, показало, что бактериальные сообщества легких похожи на сообщества изо рта, но идентифицировали конкретный микробиом легких с более высоким содержанием, демонстрируя, что микробиом легких произошел не только изо рта. [44]. Этот результат аналогичен недавнему открытию, показывающему, что основным источником здорового микробиома легких является рот, который вызывается микроаспирацией, тогда как нос вносит небольшой вклад [45].
3. Дисбактериоз и астма нижних дыхательных путей
С 1980-х годов в развитых странах наблюдается устойчивый рост распространенности атопических заболеваний. Кроме того, рост числа атопических заболеваний сопровождается уменьшением числа инфекционных агентов за тот же период времени. Страчан предложил хорошо известную «гигиеническую гипотезу», которая предполагает, что отсутствие воздействия на микробиом может способствовать увеличению распространенности атопических заболеваний, и с этого времени изучается связь между микробиомом и астмой [46].Несколько эпидемиологических исследований показали, что воздействие разнообразной микробной среды в молодом возрасте было обратно пропорционально риску развития астмы [34, 36, 47]. Предыдущие исследования микробиома при астме были в основном сосредоточены на кишечных микробных сообществах и их роли в развитии иммунной функции через концепцию «общей реакции слизистой оболочки» [48, 49]. В последнее время, с пониманием микробиома в нижних дыхательных путях, все больше и больше исследований теперь сосредоточено на взаимосвязи между колонизацией микробиома нижних дыхательных путей и иммунной толерантностью, а также влиянием дисбиоза нижних дыхательных путей на хронические заболевания дыхательных путей, включая астму.
3.1. Дисбактериоз нижних дыхательных путей у взрослых с астмой
Методы отбора проб из нижних дыхательных путей обычно основаны на БАЛ, бронхиальных щетках или сборе индуцированной мокроты [50]. Несмотря на различия в методах отбора проб, данные свидетельствуют о том, что дисбактериоз дыхательных путей, характеризующийся измененным составом микробиома и доминирующей флорой, может играть заметную роль в дыхательных путях при астме по сравнению со здоровыми субъектами [7, 10, 44, 51]. Характеристика дисбактериоза дыхательных путей при астме может быть полезной для оценки воздействия антимикробной терапии и определения новых стратегий лечения.
Хилти и его коллеги впервые предположили, что может быть нарушенный состав микробиома в нижних дыхательных путях, страдающих астмой, где значительное увеличение протеобактерий (особенно Haemophilus spp. ) было обнаружено в БАЛ 11 взрослых и 13 детей с астмой. большинство из них лечились с помощью ICS. Напротив, Bacteroidetes (в частности, Prevotella spp .) Чаще встречались в контрольной группе, чем при астме [10]. Другие исследования продемонстрировали аналогичный результат: у людей с астмой было обнаружено больше протеобактерий, чем у здоровых людей.Одно исследование оценивало 10 пациентов с легкой активной астмой (8 из 10 не использовали ICS), взятое с использованием индуцированной мокроты, а другое исследование собирало образцы бронхиального эпителия у 65 пациентов с субоптимально контролируемой астмой, большинство из которых принимали ICS [44, 51]. Пациенты в вышеуказанных исследованиях страдали астмой легкой или средней степени тяжести. У пациентов с тяжелой астмой микробиом нижних дыхательных путей при чистке бронхов у 40 участников, большинство из которых были невосприимчивыми к кортикостероидам, был значительно обогащен актинобактериями по сравнению с легкой астмой [7].
Разнообразие микробиома важно для укрепления иммунитета хозяина и может стать новым биомаркером здоровья [52]. В предыдущих исследованиях сообщалось об увеличении разнообразия условно-патогенных микроорганизмов и снижении разнообразия полезной флоры при астме по сравнению со здоровыми людьми в контрольной группе, и что увеличение разнообразия в значительной степени коррелировало с гиперреактивностью бронхов [44, 51]. Более того, другие исследования показали аналогичное разнообразие микробиоты у больных астмой и контрольной группы [10, 53]. Утрата разнообразия микробиоты — еще одно проявление дисбиоза микробиома.Когда пациенты с астмой были дополнительно охарактеризованы в соответствии с их воспалительными подтипами, у 7 участников с плохо контролируемой нейтрофильной астмой, большинство из которых принимали высокие дозы ICS, снизилось бактериальное разнообразие в индуцированных образцах мокроты по сравнению с другими воспалительными подтипами астмы [16]. Интересно, что у пациентов с ХОБЛ сообщается о подобном несоответствии, когда наблюдается увеличение или уменьшение разнообразия микробиоты нижних дыхательных путей [12, 54]. Как описано в предыдущем разделе, на состав микробиома дыхательных путей могут влиять несколько факторов, включая состояние хозяина и окружающую среду, которые могут объяснить наблюдаемые несоответствия в текущих данных, но остается неясным, связано ли различие с патогенезом астмы и требует дальнейшего расследования.
3.2. Дисбактериоз нижних дыхательных путей и особенности астмы у взрослых
Дисбиоз дыхательных путей связан с несколькими заболеваниями астмы [7, 14, 51]. Исследования показали, что разнообразие бактерий и состав дыхательных путей были в значительной степени связаны с серьезностью обструкции дыхательных путей [14] и гиперреактивностью бронхов [51], а также что обилие Proteobacteria было связано с ухудшением показателей контрольного опросника астмы (ACQ) и положительно коррелировало с Th- 17 ассоциированная экспрессия генов [7].Таким образом, определенные семейства Proteobacteria могут играть роль в Th-17-ассоциированной нейтрофильной астме, что согласуется с нашим предыдущим сообщением о высокой численности последовательностей Haemophilus у пациентов с нейтрофильной астмой [16]. Дисбактериоз дыхательных путей связан с повышенным уровнем генных маркеров, включая стероидную чувствительность FKBP5 и фенотип TH-17, представляющий активацию врожденных иммунных путей, которые могут влиять на фенотип и тяжесть астмы [7]. Связь между конкретными преобладающими микробами и типичным воспалительным фенотипом дыхательных путей является убедительным доказательством для исследования роли дисбактериоза дыхательных путей при астме.
3.3. Дисбактериоз дыхательных путей как причина астмы?
Селективное давление иммунного ответа хозяина может привести к определенному паттерну микробиоты легких [31]. Пока неясно, является ли дисбактериоз дыхательных путей причиной или следствием воспаления дыхательных путей у пациентов с астмой; модели на животных могут дать некоторое представление; тем не менее, важно интерпретировать результаты с осторожностью, поскольку они нуждаются в подтверждении в клинических исследованиях.
Исследования на стерильных и неонатальных мышах демонстрируют прямой вклад формирования микробиома в ранний период жизни на тяжесть и развитие аллергического воспаления дыхательных путей [26, 55].При воздействии яичного альбумина (OVA) мыши без микробов были склонны к развитию аллергического воспаления дыхательных путей, характеризующегося усиленной эозинофилией дыхательных путей, повышением цитокинов клеток Th-2 и гиперчувствительностью дыхательных путей, что позволяет предположить, что присутствие комменсальных бактерий имеет решающее значение для гомеостаза аллергических заболеваний. воспаление дыхательных путей [55]. Недавно было показано, что микробиом нижних дыхательных путей на мышиной модели аллергического воспаления дыхательных путей играет важную роль в развитии аллергического иммунного ответа после контакта с клещом домашней пыли (HDM) [26].В течение первых двух недель после рождения наблюдалась повышенная бактериальная нагрузка и изменения в составе бактериального сообщества в легких, что было связано со снижением чувствительности к аллергенам, эозинофилией нижних дыхательных путей и снижением цитокинов Th-2 (включая IL-4, IL-5). , и ИЛ-13) производство в БАЛ. В соответствии с этим выводом Schuijs et al., . продемонстрировал, что постоянное воздействие фермерской пыли и эндотоксина защищает мышей от астмы, индуцированной HDM, за счет снижения цитокинов эпителиальных клеток дыхательных путей, которые активируют дендритные клетки, подавляя таким образом иммунный ответ Th-2 на аллерген HDM [56].Таким образом, отсутствие бактериальной колонизации после рождения привело к чрезмерным аллергическим реакциям, которые сохранялись во взрослом возрасте, указывая на то, что микробиом легких является динамичным, а дисбактериоз дыхательных путей в раннем возрасте может привести к устойчивой восприимчивости к аллергическим заболеваниям дыхательных путей [26, 56]. Подобно роли кишечного микробиома, микробиом нижних дыхательных путей может способствовать поддержанию местных гомеостатических и воспалительных иммунных реакций легких [57, 58]. Однако астма является гетерогенным заболеванием, и между микробиомом легких и иммунитетом хозяина существует сложное взаимодействие, которое может повлиять на риск развития астмы.Роль дисбактериоза дыхательных путей в развитии астмы требует дальнейшего изучения.
4. Кортикостероиды и дисбактериоз дыхательных путей
4.1. Вызывают ли кортикостероиды дисбактериоз дыхательных путей при астме?
Текущие руководства рекомендуют использовать ИКС при астме для контроля воспаления дыхательных путей [17]. Влияние кортикостероидов на микробиом дыхательных путей неясно. В клинических исследованиях сообщается, что терапия ИКС в значительной степени связана с повышенным риском пневмонии [59, 60].В модели острой респираторной инфекции на мышах глюкокортикостероиды способствовали персистирующей колонизации Haemophilus influenza [61], предполагая, что присутствие кортикостероидов может способствовать колонизации потенциально патогенных бактерий. Вызывают ли кортикостероиды дисбактериоз дыхательных путей при астме?
При астме легкой и средней степени тяжести, Marri et al. . показали, что 10 пациентов с легкой формой астмы, большинство из которых не принимали ИКС, содержали более высокие доли Proteobacteria в образцах мокроты [44].Этот результат согласуется с другим исследованием, в котором все 11 пациентов с астмой легкой-средней степени тяжести, получавшие ICS, обнаружили, что патогенные протеобактерии, особенно Haemophilus spp. , чаще обнаруживался в бронхах взрослых и детей, страдающих астмой, чем в контрольной группе [10], и исследование Huang et al., . , которые обнаружили Proteobacteria в чистке бронхиального эпителия у 65 взрослых с субоптимально контролируемой астмой, принимали ICS в течение как минимум 4 недель. Таким образом, протеобактерии являются доминирующим видом у пациентов с легкой или умеренной астмой, независимо от использования ИКС, что позволяет предположить, что дисбактериоз дыхательных путей может быть признаком самой астмы, а не только лечением ИКС.Фактически, недавнее исследование подтвердило, что на разнообразие и состав микробиома бронхиальных дыхательных путей влияет не только лечение ICS, но и комбинированная терапия пероральным лечением и лечением ICS [14].
4.2. Способствует ли дисбактериоз дыхательных путей устойчивости к стероидам при астме
Хотя лечение ИКС может не приводить к дисбактериозу дыхательных путей, неясно, повлияет ли наличие дисбактериоза дыхательных путей на устойчивость к стероидам у астматических пациентов.
В исследовании с участием 28 устойчивых к лечению взрослых с астмой относительная численность M.catarrhalis , Haemophilus и Streptococcus ассоциировались с более длительной продолжительностью астмы, худшим прогнозируемым постбронходилатирующим ОФВ1 и более высоким числом нейтрофилов в мокроте и концентрацией ИЛ-8 [62]. Другое исследование, сравнивающее состав микробиома дыхательных путей между пациентами, устойчивыми к кортикостероидам (CR) и чувствительными к кортикостероидам (CS), выявило различия на уровне родов с разным расширением родов у 29 пациентов с CR и 10 пациентов с CS. Микроорганизмы, увеличившиеся в ЖБАЛ пациентов с CR-астмой, были в основном грамотрицательными бактериями, продуцирующими липополисахариды (LPS-), с известной высокой эндотоксической активностью, такими как Haemophilus , Neisseria и Campylobacter , в то время как микробные организмы были уникальными. расширенный при CS астме показал низкую эндотоксическую активность, например, Bradyrhizobium и Limnobacter [53].Чтобы изучить эффекты микробиома, который был уникальным образом увеличен при CR-астме, макрофаги дыхательных путей человека были совместно культивированы с клиническими штаммами Haemophilus parainfluenzae , и было обнаружено, что они отвечают сниженной клеточной реакцией на кортикостероиды активацией IL-8 и p38 MAPK [ 53]. Напротив, ингибирование TAK1, а не самого p38 MAPK, в сигнальном пути MAPK привело к чувствительности к кортикостероидам, что позволяет предположить, что резистентность к кортикостероидам вызывается активацией TAK1 / MAPK, которая запускается расширением дыхательных путей специфических грамотрицательных бактерий.Более того, исследование на животных также подтвердило эти данные о том, что дозозависимое вдыхание ЛПС может модулировать различные астматические фенотипы посредством стимуляции иммунных ответов хозяина [63]. В мышиной модели аллергического воспаления дыхательных путей, вызванной OVA, чрезвычайно низкая доза воздействия LPS способствовала доминантному воспалению Th-2, тогда как умеренная доза LPS способствовала нейтрофильному воспалению, связанному с Th-17, а высокая доза LPS вызвала накопление большого количества клеток Treg [63].Следовательно, дисбиоз дыхательных путей, характеризующийся обилием определенных бактерий, может стимулировать клетки дыхательных путей посредством воздействия бактериального LPS, который вызывает повышенный ответ Th-17 и уровень IL-8 и привлекает нейтрофилы в просвет дыхательных путей.
5. Новые возможности таргетной терапии дисбиоза нижних дыхательных путей
Текущие терапевтические вмешательства при астме в основном ограничиваются бронходилататорами и противовоспалительными препаратами, такими как кортикостероиды. Понимание микробиоты нижних дыхательных путей в состоянии здоровья и дисбактериоза при астме может открыть новые терапевтические методы лечения астмы.Эти вмешательства включают использование пробиотиков или антибиотиков, пытающихся изменить состав микробиоты дыхательных путей.
5.1. Антибиотикотерапия
5.1.1. Антибиотики и астма
Текущие международные руководства не поддерживают использование антибиотиков при астме [17]. Поскольку исследования показали, что микробиомы тесно связаны с астмой [64] и что пациенты с астмой имеют повышенную восприимчивость к респираторным бактериальным инфекциям [65], антибиотики по-прежнему часто назначают в качестве общего лечения астмы [66].Однако все больше и больше исследований показывают, что воздействие антибиотиков связано с повышенным риском последующей астмы [67–71].
Проспективное исследование показало, что воздействие антибиотиков во время беременности увеличивает риск обострений астмы в два раза у 5-летних детей [67]. Когортный анализ показал положительную связь между повышенным риском последующей астмы и воздействием антибиотиков в течение жизни плода, особенно используемых при респираторных инфекциях, а не при инфекциях мочевыводящих путей или кожи [68].Также считается, что использование антибиотиков в течение первого года жизни увеличивает риск астмы в два или три раза [69]. В продольном анализе от рождения до 11 лет назначение антибиотиков увеличивает риск последующих обострений астмы и госпитализации у детей с хрипом [70]. Однако эти ассоциации исчезли в контрольных анализах братьев и сестер [68]. В другом исследовании с довольно небольшой группой исследователей не было обнаружено значимых связей между ними [71]. В целом, больше исследований показывают, что воздействие антибиотиков увеличивает риск астмы у плода и в раннем детстве.Недавно исследование на животных показало, что интраназальное воздействие антибиотика действительно изменяет микробиом легких [72]. Влияет ли воздействие антибиотиков на микробиом нижних дыхательных путей на риск астмы, требует дальнейшего изучения.
5.1.2. Макролиды Антибиотики
Макролиды — распространенные антибиотики при лечении как острых, так и хронических респираторных инфекций, а также у пациентов с аллергией на пенициллин [73]. В отчете Глобальной инициативы по астме (GINA) рекомендуется, чтобы антибиотики не применялись в повседневной практике при обострениях астмы, если нет убедительных доказательств легочной инфекции (например.g., лихорадка или гнойная мокрота или рентгенологические свидетельства пневмонии) [17]. Макролиды проявляют антибактериальные свойства, ингибируя синтез бактериального белка за счет взаимодействия с субъединицей 50S в прокариотической рибосоме 70S, а некоторые макролидные антибиотики, включая азитромицин и кларитромицин, обладают сходными взаимодействиями с рибосомной РНК 23S (рРНК), обнаруженной в субъединице 50S, стимулируя диссоциацию пептидила. -тРНК из бактериальной рибосомы [74, 75]. Считалось, что макролиды подавляют синтез многих белков, препятствуя выходу возникающих белков.Недавно исследования показали, что трансляция большинства полипептидов прерывается рибосомой, связанной с лекарственным средством, которая блокируется на определенных, четко определенных участках мРНК. Анализ профилей рибосом, проведенный на Staphylococcus aureus и E. coli , обработанных макролидами, показал, что основные сайты остановки трансляции обогащены пролином и заряженными остатками [76, 77]. В отличие от других макролидов, таких как телитромицин и кларитромицин, присутствие азота в структуре лактонового кольца азитромицина обеспечивает устойчивость к изменениям pH в фагоцитарных везикулах, что облегчает доставку и поддержание концентрации азитромицина в местах инфекции за счет хемотаксиса хозяина и способствует антибактериальным свойствам за счет макрофаги хозяина [78].Помимо прямого антибактериального действия, макролидные антибиотики ингибируют продукцию факторов вирулентности, приверженность, подвижность и образование биопленок [74, 79, 80]. Недавно Сигал и др. . обнаружили, что азитромицин может способствовать его противовоспалительному действию, влияя на метаболизм бактерий в легких [81]. Кларитромицин может снижать ответы Th-2 и TNF- α при аллергических заболеваниях дыхательных путей, чувствительных к стероидам, что указывает на потенциальную широкую применимость в лечении астмы [20].Иммуномодулирующий эффект кларитромицина был дополнительно подтвержден моделями астмы in vivo , в которых наблюдались пониженные ответы Th-2, включая IL-5, IL-13 и эозинофилы [20]. Аналогичным образом, обсервационное исследование подтвердило предыдущие сообщения о том, что использование кларитромицина в дозе 500 мг два раза в день снижает уровень IL-8 в мокроте и снижает уровень нейтрофилов в дыхательных путях [82]. В большом количестве рукописей сообщается, что макролиды обладают иммуномодулирующими эффектами за счет накопления в воспалительных клетках путем модуляции фосфорилирования ERK1 / 2 и подавления активации NF- κ Β [75].Макролиды, включая кларитромицин и рокситромицин, улучшают клинические признаки астмы, такие как функция легких [83, 84], и могут снижать степень гиперреактивности бронхов [83], тогда как другие показали связь между применением макролидов (шесть недель лечения рокситромицином по 150 мг дважды в день), улучшение клинических симптомов, контроль астмы и вечерний пиковый поток выдоха [84].
Не исключено, что эффективность макролидов может быть ограничена конкретным фенотипом или эндотипом астмы.Обзор показал, что тяжелая, нечувствительная к стероидам нейтрофильная астма более чувствительна к макролидам по сравнению с астмой легкой и средней степени тяжести [74]. Точно так же, хотя низкие дозы (250 мг в день в течение 5 дней) азитромицина не снижали частоту обострений и инфекций нижних дыхательных путей у взрослых участников с тяжелой астмой, у пациентов с неозинофильной астмой, получавших азитромицин, наблюдалось значительное снижение первичных конечных точек. наблюдались, что предполагает мощную роль азитромицина в профилактике неозинофильной тяжелой астмы [85].Комбинация секвенирования гена 16S рРНК и макролидов может способствовать индивидуализированному лечению, основанному на четкой диагностике фенотипов и эндотипов. Анализ микробиома легких с помощью создателя гена 16S рРНК может определить, являются ли полезные эффекты макролидов в профилактике обострений противовоспалительными или антибиотическими по своей природе. Кроме того, необходимы продольные исследования, чтобы лучше понять, как изменения в микробном составе и структуре микробиоты определяют начало и развитие астмы.Выявление этих динамических изменений может быть полезным как биомаркером, так и потенциальной терапевтической мишенью.
5.2. Пробиотики
Как обсуждалось выше, микробные факторы играют важную роль в гомеостазе иммунных ответов хозяина и могут влиять на риск развития аллергических заболеваний у восприимчивых людей. Одним из возможных способов исправить дисбактериоз и восстановить «здоровую» микробиоту легких может быть добавление пробиотиков или продуктов, полученных из микробиоты, путем перорального или ингаляционного приема.
Пробиотики — это живые микроорганизмы, например виды молочнокислых бактерий, которые оказались полезными при воспалительных заболеваниях кишечника за счет изменения состава кишечной микробиоты и восстановления микробного баланса кишечника [86]. С 1990-х годов было проведено множество исследований, предназначенных для оценки эффектов лечения пробиотиками или профилактики аллергических заболеваний, включая атопический дерматит и аллергический ринит [87, 88]. Клинические испытания показали, что некоторые пробиотики продемонстрировали профилактическую и терапевтическую эффективность против аллергических заболеваний, включая экзему и аллергический ринит; тем не менее, исследования роли пробиотиков при астме остаются редкими [89, 90].
Данные исследований на животных показывают, что пероральные пробиотики в раннем возрасте могут подавлять аллергическое воспаление дыхательных путей [91–93]. Однако клинические исследования показывают противоречивые результаты; исследования детей с астмой показывают, что пробиотики оказывают положительное влияние на улучшение клинических симптомов и функции легких [94, 95], в то время как исследования перорального применения пробиотиков у взрослых и детей дошкольного возраста не показывают положительного воздействия на функцию легких и воспаление бронхов [96, 97]. Недостаточно доказательств в поддержку использования пероральных пробиотиков для лечения астмы, и нет исследований, посвященных тому, могут ли пробиотики предотвращать обострения астмы.
По мере того, как мы узнаем больше о микробиоме нижних дыхательных путей при респираторных заболеваниях, интересно задаться вопросом, могут ли пероральные пробиотики изменять и влиять на состав микробиома в респираторных путях и, следовательно, на тяжесть заболевания дыхательных путей, хроническое течение или реакцию на терапию. Недавнее исследование на животных воспаления легких, вызванного воздействием частиц углеродных нанотрубок у взрослых мышей, показало, что пероральные пробиотики не меняют микробиом легких [72]. В мышиной модели аллергического воспаления дыхательных путей, вызванного заражением OVA, воздействие на легкие безобидного штамма Escherichia coli при вдыхании приводило к подавлению аллергических ответов дыхательных путей, в основном характеризующихся значительным меньшим количеством общих клеток и более низкой частотой эозинофилов в БАЛ в E .coli , что предполагает бактериальную защиту от аллергического воспаления дыхательных путей [98]. Необходимы дальнейшие исследования для оценки применимости воздействия на дыхательные пути при вдыхании продуктов или пробиотиков, полученных из микробиоты, в составе микробиома дыхательных путей и астмы.
6. Резюме
С развитием технологии секвенирования появляется все больше исследований, которые подтверждают гипотезу о том, что нижние дыхательные пути не являются стерильными для здоровья и служат убежищем для различных микробных сообществ с низкой бактериальной нагрузкой, на которую могут влиять хозяин и окружающая среда. факторы.Все больше и больше доказательств показывают, что воздействие различных микробов в раннем возрасте может модулировать иммунный ответ хозяина и влиять на восприимчивость к атопическому заболеванию. Астма — сложное гетерогенное заболевание. Было показано, что дисбактериоз нижних дыхательных путей вносит свой вклад в патофизиологию астмы, особенно нейтрофильной астмы. Возможный механизм состоит в том, что обилие определенных бактерий может вызывать повышенный ответ Th-17 за счет воздействия бактериального LPS. С пониманием роли дисбактериоза нижних дыхательных путей в патогенезе астмы терапевтические вмешательства, направленные на коррекцию дисбактериоза и восстановление «здоровой» микробиоты легких, могут потенциально управляться с помощью пробиотиков и антибиотиков.Хотя наше понимание микробиома легких быстро улучшается, исследований, посвященных стандартным технологиям и анализу, недостаточно, и многие вопросы еще предстоит решить.
Конфликт интересов
Авторы заявляют, что у них нет конфликта интересов.
Кишечный дисбиоз и истощение бутирогенных бактерий при инфекции Clostridium difficile и нозокомиальной диарее
ВВЕДЕНИЕ
Нозокомиальная диарея — частое осложнение у госпитализированных пациентов.Clostridium difficile является наиболее частой инфекционной причиной внутрибольничной диареи, составляющей от 15 до 25% диареи, связанной с приемом антибиотиков, и большинства случаев колита, связанного с применением антибиотиков. Уровень смертности от инфекции Clostridium difficile (CDI) оценивается в 1–2,5%, что приводит к 14 000 смертей в год в США (1–3). Широко распространено мнение, что индуцированное антибиотиками нарушение микробиоты кишечника дает C. difficile нежелательное преимущество, позволяя организму размножаться и вырабатывать свои токсины на фоне чувствительной флоры.Хотя стандартная терапия антибиотиками (например, лечение метронидазолом или пероральным ванкомицином) очень эффективна в подавлении C. difficile, она не предотвращает рецидивов. Действительно, от 15 до 30% пациентов испытывают рецидив в течение 3 месяцев после лечения антибиотиками. Множественные рецидивы ИКД не редкость (4–6). Известно, что трансплантация фекальной микробиоты (FMT) излечивает от> 80 до 90% рецидивирующих инфекций, вызванных C. difficile (7–11). После FMT микробиота кишечника реципиента напоминает микробиоту донора (12).Эти наблюдения показывают, что донорские бактерии способны восстанавливать структуру и функцию микробных сообществ кишечника реципиента. Высокая эффективность FMT подтверждает принцип, согласно которому микробиота кишечника придает устойчивость к колонизации C. difficile. Что еще более важно, это дает надежду на то, что идентификация ключевых микробных факторов, важных для устойчивости к колонизации, может привести к новой пробиотической терапии.
Около 100 триллионов микроорганизмов обитают и колонизируют кишечник человека (13, 14).Ранние исследования показали, что случайно выбранные бактериальные изоляты из кишечной флоры были частично эффективны в подавлении C. difficile. Было показано, что несколько видов, в том числе Lactobacillus, Enterococcus, Bifidobacterium и Bacteroides, обладают ингибирующей активностью в отношении C. difficile (15, 16). В ряде недавних исследований изучалась микробиота кишечника, связанная с ИКД, с использованием методов, основанных на культуре, микрочипов 16S рРНК и клонального секвенирования 16S (17–19). В большинстве исследований наблюдалось уменьшение микробного разнообразия и богатства и / или изменение микробного состава.Интересно, что у 20 пациентов с бессимптомным носительством C. difficile микробный профиль кишечника очень напоминал профиль здоровых взрослых (19), что позволяет предположить, что нормальная микробиота кишечника может защитить хозяев от развития инфекции C. difficile. Два недавних исследования предоставили дополнительные доказательства того, что устойчивость к колонизации C. difficile может быть создана у мышей с использованием одного изолята Lachnospiraceae или определенного коктейля из шести кишечных изолятов мыши (20, 21). Взятые вместе, данные о трансплантации фекалий в клинических условиях и экспериментальных исследованиях на животных показывают, что можно управлять микробиотой кишечника, используя определенные изоляты кишечника человека в качестве пробиотиков для лечения и / или предотвращения ИКД.
Благодаря проекту «Микробиом человека» (22) наши знания о микробиоме кишечника в отношении здоровья и болезней в последние годы быстро расширились. Однако микробные факторы, необходимые для устойчивости к C. difficile и другим кишечным патогенам, остаются неуловимыми. Основная цель настоящего исследования состояла в том, чтобы определить возможные комменсальные организмы, которые могут быть использованы для лечения C. difficile. Мы исследовали 549 643 частичных прокариотических гена 16S рРНК из образцов кала субъектов с ИКД, субъектов с C.difficile-отрицательная нозокомиальная диарея (CDN) и здоровые люди из контрольной группы (HC), выявив 3531 бактериальный филотип из 115 образцов фекалий. Наш анализ микробиома 16S выявил значительные изменения в структурах микробного сообщества, связанные с CDI и CDN, сопровождающиеся заметным снижением микробного разнообразия и меньшим количеством бактериальных филотипов по сравнению со здоровым контролем. Несколько основных типов бактерий, которые продуцируют бутират и короткоцепочечные жирные кислоты (SCFA), все из которых являются членами кластеров Clostridium IV и XIVa в семействе Ruminococcaceae или Lachnospiraceae, отсутствовали или были заметно истощены в CDI и CDN.Бактерии, продуцирующие SCFA, были классифицированы как in silico на основании исследований родов, определенных на основе наборов данных глубокого секвенирования. Эти результаты предполагают участие Ruminococcaceae, Lachnospiraceae и бутирогенных бактерий в патогенезе нозокомиальной диареи и инфекции C. difficile.
РЕЗУЛЬТАТЫ
Образцы и сбор данных о последовательности 16S. Мы взяли образцы кишечных микробных сообществ у 39 субъектов с инфекцией C. difficile (группа CDI), 36 субъектов с нозокомиальной диареей, отрицательной по C. difficile (группа CDN), и 40 здоровых людей из контрольной группы. испытуемые (группа HC) (таблица 1).Из 39 образцов в группе CDI 9 (23,1%) были получены от субъектов с рецидивирующими эпизодами. Пять субъектов (13,9%) в группе CDN имели историю болезни CDI. Большинство субъектов в группах CDI и CDN (69,2% и 86,1% соответственно) имели заболевание от легкой до умеренной степени. В общей сложности 87,2% субъектов в группе CDI получали противомикробные препараты в течение 3 месяцев до отбора проб, по сравнению с 58,3% и 22,5% субъектов в группах CDN и HC, соответственно. Сходное соотношение испытуемых в группах CDI и CDN (43.6% и 41,7% соответственно) получали сопутствующую системную антимикробную терапию. Пять субъектов (12,8%) в группе ИКД получали лечение антибиотиками от ИКД (лечение метронидазолом или пероральным ванкомицином) перед забором фекалий. После обрезки и контроля качества для анализа было доступно 526071 частичное считывание последовательностей 16S рРНК высокого качества из областей от V1 до V3 (∼4,575 ± 1616 прочтений на образец при средней длине ампликона ∼492 нуклеотида) (см. Таблицу S1 в дополнительном материале).
Таблица 1Демографические и исходные клинические характеристики образцов, использованных в данном исследовании
Микробное разнообразие и видовое богатство микробиоты кишечника при ИКД и КДН. Мы идентифицировали в общей сложности 3531 рефОТ из 115 образцов фекалий, которые принадлежали к 150 различным родам в 15 различных типов. В общей сложности 2986 (84,6%) из 3531 идентифицированных refOTU были обнаружены у здоровых людей. Напротив, только 1392 (39,4%) и 1582 (44,8%) refOTU были обнаружены в группах CDI и CDN соответственно.Среди наиболее распространенных refOTU (определяемых как> 0,1% всех считываний пиросеквенирования) 124 были общими в более чем половине здоровых контрольных образцов, но только 9 были обнаружены по крайней мере в половине образцов в группе CDI. Видовое богатство было значительно ниже в группах CDI и CDN, чем в здоровой контрольной группе, и как микробное разнообразие (определяемое индексом разнообразия Шеннона), так и однородность видов были заметно снижены (рис. 1). Интересно отметить, что микробное богатство и разнообразие существенно не различались между группами CDI и CDN ( P > 0.05).
Рис. 1Снижение микробного разнообразия, однородности и видового богатства микробиоты кишечника, связанное с инфекцией C. difficile и нозокомиальной диареей, отрицательной по C. difficile, показано распределенным в виде прямоугольной диаграммы. (Слева) Индекс разнообразия Шеннона использовался для оценки микробного разнообразия для каждой группы. (В центре) Индекс однородности видов рассчитан по формуле J ′ = H ′ / H ′ max , где H ′ — индекс разнообразия Шеннона, а H ′ max — максимальное значение H ′ (т.е.е., ln S , где S — общее количество видов в сообществе). (Справа) Видовое богатство определялось как количество refOTU, идентифицированных в каждом образце. Все три индекса были значительно ниже в группах CDI и CDN, чем в здоровой контрольной группе (тест Стьюдента t ). Не наблюдалось существенной разницы между группой CDI и группой CDN. Каждая точка представляет собой отдельный образец кала. Значения P показаны над столбиками для каждого сравнения групп.
Для группы CDI, когда образцы были стратифицированы по степени тяжести заболевания, никаких различий в микробном разнообразии, видовом богатстве или составе не наблюдалось (см. Рис. S1 и S2 в дополнительном материале). Сравнение начального и рецидивирующего заболевания выявило тенденцию к снижению видового разнообразия рецидивирующих заболеваний; однако не наблюдалось значительных различий в разнообразии кишечных микробов (см. рис. S3 в дополнительном материале). Кроме того, сопутствующее воздействие антибиотиков не привело к значительному изменению микробного разнообразия, видового богатства или совокупного микробного состава (см.рис.S4 в дополнительном материале). Таким образом, эти данные продемонстрировали, что многие обычно многочисленные филотипы были истощены при нозокомиальной диарее и ИКД, и предполагают, что факторы, отличные от микробиоты кишечника, могут модулировать тяжесть заболевания во время ИКД.
Для группы CDN, когда образцы были стратифицированы по диарее, связанной с антибиотиками, по сравнению с диареей, не связанной с антибиотиками, не наблюдалось никаких существенных различий в микробном разнообразии или составе (см. Рис. S5 в дополнительном материале). Более того, микробные сообщества кишечника существенно не различались у субъектов, получавших сопутствующую антибактериальную терапию, и у тех, кто ее не получал (см.рис.S4 в дополнительном материале).
Кишечный дисбактериоз при CDI и CDN. Чтобы охарактеризовать глобальные изменения в структурах микробного сообщества, мы применили метод UniFrac (26) для анализа филогенетического родства считываний пиросеквенирования из всех образцов. Как в взвешенном, так и в невзвешенном анализе UniFrac, сообщества кишечных микробов, связанные с CDI и CDN, сгруппированы отдельно от таковых в здоровой контрольной группе (рис. 2A). Расчет расстояний UniFrac внутри и между группами показал, что микробные сообщества в группе CDI больше похожи друг на друга, чем на микробные сообщества здоровых субъектов (рис.2Б). Среднее расстояние UniFrac между парами образцов в группе CDI было значительно больше, чем между парами образцов в здоровой контрольной группе (рис. 2B), что указывает на большую гетерогенность микробных сообществ кишечника, связанных с CDI. Аналогичная тенденция наблюдалась для группы CDN по сравнению со здоровым контролем. Никаких заметных различий в структурах сообществ или членстве между группами CDI и CDN не наблюдалось. Таким образом, эти данные позволяют предположить, что болезненное состояние (т.е., диарейное состояние по сравнению со здоровьем) или лечение антибиотиками (предшествующее или сопутствующее) составили наибольшую вариацию среди всех образцов, хотя межиндивидуальные различия в микробиоте кишечника также способствовали изменчивости данных.
Рис. 2Сравнение составов микробных сообществ, выявляющих измененную микробиоту кишечника при ИКД. (A) Невзвешенный анализ UniFrac был использован для определения расстояний между образцами фекалий, положительными по C. difficile (CDI), образцами диареи, отрицательными по C. difficile (CDN), и образцами здорового контроля (HC).Затем были построены диаграммы рассеяния с использованием анализа главных координат. Процент отклонения, объясняемый каждой главной координатой (PC), указан на осях. Каждая точка представляет собой микробное сообщество. Разница между сообществами в группах CDI и HC была значимой ( P <0,001, t тест с перестановкой). (B) Среднее расстояние UniFrac между парами образцов в каждой группе, что указывает на большую гетерогенность микробных сообществ кишечника в группах CDI и CDN, чем в здоровой контрольной группе.Планки погрешностей, стандартная ошибка среднего.
Нехватка последовательностей Firmicutes в совокупной микробиоте кишечника, связанной с CDI и CDN. Тип Firmicutes включает самые многочисленные и разнообразные виды бактерий в кишечнике человека. В контрольной группе здоровых людей последовательности Firmicutes доминировали при 74,9% всех чтений (в среднем около 322 филотипов на одного субъекта) (рис. 3). Только 21,5% всех прочтений были отнесены к типу Bacteroidetes с ~ 37 филотипами на одного субъекта. Распространенность последовательностей Firmicutes была существенно ниже в группах CDI и CDN (43.2% и 32,9% соответственно). Это истощение последовательностей Firmicutes сопровождалось заметным снижением бактериальных филотипов (CDI, 75 филотипов; CDN, 86 филотипов; HC, 322 филотипа) (рис. 3).
Рис. 3Нехватка последовательностей и филотипов Firmicutes в CDI и CDN. (A) Средние доли последовательностей Firmicutes были меньше в группах CDI и CDN ( P = 5,70 × 10 −7 и P = 1,08 × 10 −8 соответственно; тест Стьюдента t ) чем в группе HC.(B) Среднее количество филотипов Firmicutes (refOTU) было ниже в группах CDI и CDN ( P = 8,81 × 10 −19 и P = 7,16 × 10 −16 , соответственно; показатель Стьюдента t ), чем в группе HC.
На уровне семейства последовательности Lachnospiraceae (45,8%), Ruminococcaceae (17,4%) и Bacteroidaceae (16,1%) преобладали в здоровой фекальной микробиоте, а последовательности из других семейств составляли <3% всех считываний пиросеквенирования (рис.4А). Последовательности Lachnospiraceae и Ruminococcaceae были значительно недопредставлены в группах CDI и CDN (Lachnospiraceae: CDI, 11,2%; CDN, 12,3%; HC, 45,8%; Ruminococcaceae: CDI, 3,0%; CDN, 2,8%; HC, 17,4%) (см. Рис. S6 в дополнительном материале). Несколько родов были обогащены ассоциацией с CDI. Например, последовательности Veillonella (CDI, 4,5%; HC, 0,6%), Enterococcus (CDI, 7,1%; HC, 0,05%) и Lactobacillus (CD, 3,7%; HC, 0,4%) были необычно многочисленными. Enterococcus и Lactobacillus являются молочнокислыми бактериями из отряда Lactobacillales.Последовательности энтерококка были обнаружены в 84,6% образцов CDI по сравнению только с 22,5% образцов из здоровой контрольной группы. Последовательности из класса Gammaproteobacteria, который включает множество клинически важных грамотрицательных патогенов, также были обогащены. Интересно, что последовательности Desulfovibrionaceae из класса Deltaproteobacteria, который включает большое количество сульфатредуцирующих, анаэробных, грамотрицательных бактерий, были истощены по CDI. Как и в предыдущих исследованиях (29), индивидуальные различия в пропорциях основных типов среди выборок наблюдались во всех трех группах (см.рис.S7 в дополнительном материале). Эти результаты показывают, что уменьшение разнообразия кишечных микробов и богатство CDI и CDN обусловлено, в первую очередь, утратой филотипов внутри семейств Lachnospiraceae и Ruminococcaceae.
Рис. 4(A) Доли бактериальных таксонов в каждом образце, как определено на основании данных о последовательности гена 16S рРНК. Каждый столбец соответствует отдельному образцу кала. Каждая строка соответствует определенному бактериальному филотипу или refOTU, упорядоченному на основе филогенетических отношений.В эту тепловую карту включены только самые известные refOTU (содержание> 0,1%). Относительная численность каждого филотипа представлена цветовым кодом. Представители семейств Lachnospiraceae и Ruminococcaceae заштрихованы серым цветом. Тип Bacteroidetes показан светло-красным цветом, а тип Proteobacteria — желтым. (B) Доли таксонов бактерий в кластерах Clostridium. Каждый столбец представляет собой отдельный образец кала. Каждая строка соответствует refOTU, назначенному одному из 19 кластеров Clostridium.Члены кластеров Clostridium XIVa и IV заштрихованы серым цветом.
Истощение бактерий, продуцирующих бутират, в CDI и CDN. Подавляющее большинство последовательностей Firmicutes (68,4%) были отнесены к классу Clostridia. Класс Clostridia был разделен на 19 кластеров на основе роста, метаболических и морфологических параметров (30) и включает членов семейств Lachnospiraceae и Ruminococcaceae, которые были значительно истощены по CDI. Чтобы идентифицировать специфические кластеры Clostridium, которые были наиболее истощены по CDI и CDN, мы использовали ассоциативную таблицу полноразмерных последовательностей от видов, ранее отнесенных к кластерам Clostridium (29, 31) и отнесенных к 17.8% всех считывает до 19 кластеров Clostridium (рис. 4B). Меньшие доли прочтений были назначены для групп CDI (16,4%) и CDN (10,0%), чем для здоровой контрольной группы (25,0%). Поразительно, но члены кластера XIVa Clostridium (группа Eubacterium rectale-Clostridium coccoides) и в меньшей степени кластера IV (группа Clostridium leptum) были значительно истощены в группах CDI и CDN по сравнению с группой HC (кластер XIVa: CDI, 5,5%; CDN, 6,6%; HC, 18,4%; кластер IV: CDI, 0,47%; CDN, 0.40%; УВ 2,95%). Поскольку кластеры Clostridium IV и XIVa содержат большое количество комменсальных организмов, в том числе анаэробные бактерии, продуцирующие бутират, важные для метаболизма и развития эпителиальных клеток толстой кишки, эти данные предполагают потенциальную роль организмов, продуцирующих бутират, в нозокомиальной диарее и ИКД.
Затем мы использовали LEfSe (28) для определения конкретных таксонов бактерий, которые были дифференциально многочисленны. Мы определили Blautia, Pseudobutyrivibrio, Roseburia, Faecalibacterium, Anaerostipes, Subdoligranulum, Ruminococcus, Streptococcus, Dorea и Coprococcus как наиболее дифференциально обедненные роды, ассоциированные с CDI (рис.5А). Те же 10 родов также были идентифицированы как наиболее дифференциально обедненные в CDN. Многие из этих родов содержат продуцентов бутирата, принадлежащих к кластеру Clostridium IV или XIVa. Общая численность этих 10 родов, вместе взятых, была значительно ниже в группах CDI и CDN, чем в контрольной группе (CDI, 5,4%; CDN, 4,9%; HC, 37,2%), хотя относительная численность каждого из них отличалась индивидуально. род (рис. 5Б). Из 3531 общего числа refOTU, идентифицированных в нашем наборе данных, 119 refOTU были значительно истощены в CDI; 74 refOTU были членами 10 наиболее истощенных родов, а 39 refOTU были некультивируемыми бактериями семейства Lachnospiraceae или Ruminococcaceae.Когда набор данных CDI сравнивался с данными CDN, Clostridium difficile оказался наиболее дифференцированно обогащенным видом, связанным с CDI.
Рис. 5Роды бактерий, наиболее обедненные или обогащенные CDI и CDN. (A) Роды, наиболее дифференциально обедненные (большинство из которых являются анаэробными бактериями, продуцирующими масляную кислоту) или обогащены микробиотой, связанной с C. difficile, по сравнению со здоровой контрольной микробиотой, как определено с помощью линейного дискриминантного анализа (LDA) в сочетании с измерениями величины эффекта. Бактериальные таксоны, обедненные CDI, обозначены положительными оценками LDA (зеленый), а таксоны, обогащенные CDI, обозначены отрицательными оценками (красный).Показаны только таксоны, которые соответствуют значительному порогу LDA 3,6. Те же роды также были истощены в CDN (данные не показаны). (B) Индивидуальные вариации в относительной численности отдельных родов. Общая численность (считывание последовательностей, ось и ) 10 наиболее дифференциально истощенных родов (обозначенных в ключе) была значительно ниже в группах CDI и CDN, чем в группе HC ( P = 4,0 × 10 −21 и P = 9,3 × 10 −20 соответственно; критерий Стьюдента t ).Каждая полоса соответствует отдельному образцу.
Поскольку продуценты бутирата поставляют энергию эпителиальным клеткам кишечника и, как считается, защищают от колита, мы спросили, различаются ли пропорции считываний 16S, относящиеся к родам, которые, как известно, продуцируют бутират в качестве основного продукта ферментации, между группами. Относительное количество бактерий, продуцирующих бутират, было значительно ниже в группах CDI и CDN (CDI, 6,3%; CDN, 3,1%; HC, 17,2%) (рис. 6A). Основными производителями бутирата с истощением запасов являются Roseburia (CDI, 0.17%; CDN, 0,45%; HC, 3,4%), Faecalibacterium (CDI, 0,37%; CDN, 0,83%; HC, 3,2%), субдолигранулум (CDI, 0,18%; CDN, 0,094%; HC, 2,0%), Anaerostipes (CDI, 0,2% ; CDN, 0,016%; HC, 3,1%) и Pseudobutyrivibrio (CDI, 0,065%; CDN, 0,44%; HC, 3,3%) (рис. 6B). Fusobacterium spp. были доминирующими продуцентами бутирата в совокупной микробиоте кишечника субъектов с ИКД (CDI, 4,1%; HC, 0,03%; P = 0,099), но это было обусловлено преобладанием Fusobacterium в микробиоте кишечника четырех субъектов (см. Инжир.S8 в дополнительном материале).
Рис. 6Ферментеры ацетата, бутирата и лактата в микробиоте кишечника. (A) Относительные пропорции ферментеров ацетата, бутирата и лактата в кишечной микробиоте в когортах CDI (красный), CDN (желтый) и HC (зеленый), подвергнутых пиросеквенированию. Считывания последовательностей были классифицированы на уровне рода в соответствии с первичным конечным продуктом метаболизма углеводного брожения, и результаты сравнивались с использованием теста Стьюдента t . Роды, которые были неоднозначно определены как продуцирующие как ацетат, так и бутират, или другие короткоцепочечные жирные кислоты, такие как сукцинат, пропионат, формиат или этанол, содержащие второстепенные компоненты микробиоты кишечника (<1% считываний последовательностей), были исключены из этого исследования. анализ.Планки погрешностей, стандартная ошибка среднего. ∗, P <0,05; ∗∗, P <0,01; ∗∗∗, P <0,001. CDI, инфекция C. difficile; CDN, нозокомиальная диарея, отрицательная по C. difficile; HC, здоровый контроль; NS, не имеет значения. (B) Относительные пропорции основных бактерий, продуцирующих бутират. (C) Относительные пропорции основных ацетогенов по родам. (D) Относительные пропорции организмов, вырабатывающих первичную молочную кислоту.
Анаэробные кишечные бактерии производят различные продукты ферментации, включая ацетат, лактат и другие короткоцепочечные жирные кислоты (SCFA), помимо бутирата.Сравнение основных ацетогенов (рис. 6C) показало, что роды Blautia (CDI, 2,1%; CDN, 1,6%; HC, 14,4%) и Dorea (CDI, 0,12%; CDN, 0,10%; HC, 1,5%) были значительно снижен в группах CDI и CDN по сравнению с контрольной группой. Эти ацетогены были заменены на Bacteroides spp. (CDI, 29,5%; CDN, 45,7%; HC, 16,1%), которые помимо ацетата производят SCFAs сукцинат, лактат и формиат (от C2 до C4). Lactobacillus spp. и Enterococcus spp., оба первичных продуцента молочной кислоты, были более распространены и более многочисленны в группах CDI и CDN, чем в группе HC (рис.6D).
ОБСУЖДЕНИЕ
Сложное сообщество микроорганизмов, населяющих кишечник, играет важную роль в здоровье и болезнях человека, включая пищеварение, метаболизм, развитие иммунной системы и устойчивость к инфекциям. Кишечник млекопитающих является основным местом воздействия вторгающихся патогенов. Важность местной микробиоты для устойчивости к патогенам хорошо иллюстрируется инфекцией Clostridium difficile, которая является одной из наиболее частых причин смерти, связанной с гастроэнтеритом, в Соединенных Штатах.Хотя считается, что микробиота кишечника защищает кишечник от ИКД, конкретные компоненты, которые придают устойчивость к колонизации, неизвестны. В соответствии с предыдущими исследованиями (17, 19, 20, 32) наш геномный анализ 16S продемонстрировал глубокое изменение микробиоты кишечника, или дисбактериоз, который характеризовался заметным уменьшением биоразнообразия и видового богатства. Важно отметить, что несколько типов анаэробных бактерий, продуцирующих бутират в нормальных условиях, из семейств Ruminococcaceae и Lachnospiraceae были значительно истощены по ИКД.Интересно, что структура микробного сообщества в совокупной микробиоте кишечника при ИКД была аналогична таковой при нозокомиальной диарее, отрицательной по C. difficile (CDN).
В нескольких исследованиях изучались изменения микробиоты кишечника при заболевании, связанном с C. difficile. Используя методы, основанные на культуре, Хопкинс и его коллеги сообщили об уменьшении видового разнообразия (33) и снижении количества Bacteroides, Prevotella и Bifidobacteria у 4 субъектов с ИКД (18). Образцы фекалий в этом исследовании были получены после терапии метронидазолом, что могло нарушить микробный профиль.При клональном секвенировании 16S рРНК в образцах фекалий 3 субъектов с рецидивирующей ИКД наблюдалось заметное снижение видового богатства и разнообразия по сравнению с 4 субъектами с исходной ИКД и 3 неинфицированными контрольными субъектами (17), что подтверждает роль микробиоты кишечника в C. difficile-ассоциированное заболевание. Manges et al. сравнили микробиоту кишечника 25 субъектов, у которых развилась ИКД во время госпитализации, с микробиотой 50 подобранных контрольных субъектов с использованием микроматрицы 16S рРНК (34). После корректировки для использования антибиотиков только небольшое количество организмов в типах Bacteroidetes и Firmicutes было связано с последующим развитием ИКД во время госпитализации.Интересно, что при ИКД не наблюдалось снижения разнообразия кишечной микробиоты по сравнению с контролем. Их результаты могут быть объяснены тем фактом, что образцы кала были собраны на ранних этапах госпитализации (в течение 72 часов после поступления), и изменения в составе микробиоты кишечника из-за воздействия антибиотиков могли произойти после сбора образцов и способствовать последующему C ..difficile колонизация и болезнь. Действительно, в этом исследовании воздействие антибиотиков во время госпитализации было тесно связано с риском последующей ИКД.Об экологической преемственности микробных сообществ кишечника после лечения антибиотиками и воздействия C. difficile также сообщалось в моделях на животных (35).
В качестве доказательства принципа использования отобранных кишечных микробов при трансплантации микробиоты Lawley et al. продемонстрировали, что определенная смесь шести филогенетически разнообразных бактерий способна вызывать серьезные изменения в микробном составе кишечника и устранять заболевание, вызванное C. difficile, на мышиной модели CDI (20). В другом исследовании Reeves et al.(21) показали, что один компонент микробиоты кишечника мышей, член семейства Lachnospiraceae, может восстанавливать устойчивость к колонизации против CDI у стерильных мышей. Однако представители микробиоты кишечника человека и микробиоты кишечника мышей филогенетически отличаются. Связанные с человеком кишечные бактерии, которые могут придавать устойчивость к колонизации C. difficile, еще не идентифицированы. Это исследование представляет собой углубленный анализ микробиома кишечника человека, связанного с инфекцией C. difficile, с целью выявления потенциальных ассоциированных с человеком бактерий, которые могут быть исследованы в будущих исследованиях или потенциально использованы для новой пробиотической терапии.
В этом исследовании микробные сообщества в CDI и CDN сгруппированы отдельно от сообществ здоровых людей. Такое четкое объединение здоровых людей и людей с нозокомиальной диареей предполагает, что истощение кишечных комменсальных организмов, которые обычно живут в симбиозе с хозяином, может привести к дисфункции толстой кишки и диарее. Члены семейств Lachnospiraceae и Ruminococcaceae, которые включают бутирогенные бактерии, были значительно обеднены в группах CDI и CDN.Интересно отметить, что между группами CDI и CDN наблюдались незначительные различия в микробном разнообразии, видовом богатстве и членстве в сообществе (за исключением считываний C. difficile). Микробиота кишечника была нарушена при нозокомиальной диарее с низким микробным разнообразием и малочисленностью организмов Firmicutes, независимо от статуса C. difficile. Неспецифичность дисбактериоза при CDI и CDN может быть связана с высокими показателями предшествующего воздействия антибиотиков (CDI, 87,2%; CDN, 58,3%; HC, 22,5%) и предполагает, что микробиота кишечника в группе CDN может быть восприимчивой к C .difficile. Отсутствие различий между CDI и CDN также предполагает, что приобретение или инфицирование C. difficile мало влияет на общий состав или структуру микробиоты кишечника. В соответствии с этой гипотезой недавнее исследование не показало значительных различий в составе микробиоты кишечника у пожилых людей с бессимптомным носительством C. difficile (т.е. у субъектов с положительным посевом) по сравнению с предметами с отрицательным посевом (19).
В перекрестном исследовании 10 субъектов с использованием анализа клонального секвенирования 16S Chang et al.(17) сообщили о более низком общем микробном разнообразии при рецидивирующем заболевании, вызванном C. difficile, по сравнению с исходными инфекциями. Хотя наше исследование показало тенденцию к снижению видового богатства, не было обнаружено значительных различий в микробном разнообразии при рецидивирующих заболеваниях (см. Рис. S3 в дополнительном материале). Мы также не наблюдали корреляции между тяжестью заболевания и экологическими показателями микробиоты кишечника (см. Рис. S1 в дополнительном материале). Хотя обычно считается, что инфекция C. difficile требует предварительного нарушения нормальной кишечной флоры, после того, как инфекция инициирована, тяжесть заболевания может модулироваться хозяйскими и бактериальными факторами, такими как воспалительные реакции, уровни антител и / или экспрессия вирулентных токсинов.У пациентов с более тяжелым заболеванием нормальные комменсальные бактерии могут быть потеряны в результате интенсивных воспалительных реакций хозяина; следовательно, общая микробиота кишечника не предсказывает и не коррелирует с тяжестью заболевания.
Настоящее исследование выявило несколько конкретных представителей семейств Ruminococcaceae и Lachnospiraceae, которые были заметно истощены по ИКД и нозокомиальной диарее. Подавляющее большинство этих видов являются бактериальными филотипами, наиболее похожими на анаэробные бактерии, продуцирующие бутират.Масляная кислота обладает хорошо подтвержденным противовоспалительным действием и является предпочтительным источником энергии для синтеза АТФ в колоноцитах. Известно, что многие короткоцепочечные жирные кислоты (SCFA), такие как масляная кислота, уменьшают проницаемость эпителиальной выстилки кишечника за счет увеличения экспрессии белков плотных контактов. Кроме того, было высказано предположение, что масляная кислота может усиливать защитные барьеры толстой кишки за счет увеличения уровней антимикробных пептидов и продукции муцина (36, 37). Таким образом, при нозокомиальной диарее истощение организмов, продуцирующих бутират, может привести к дисфункции эпителия и повышению осмотической нагрузки в просвете кишечника, что приведет к диарее.При инфекции, вызванной C. difficile, нарушение микробиоты кишечника и истощение полезных бутирогенных бактерий в кишечнике может привести к повышенной восприимчивости к инфекции из-за нарушения защиты хозяина от C. difficile. Если это так, то пополнение бутирогенных бактерий, позволяющее in situ производить масляную кислоту или другие ингибирующие соединения в просвете кишечника, может предложить новую терапевтическую стратегию для лечения инфекции, вызванной C. difficile, или нозокомиальной диареи.
Ранние исследования роли SCFAs в устойчивости к колонизации дали неоднозначные результаты.Согласно Rolfe (38), масляная кислота была единственной SCFA в слепой кишке обычных хомяков, концентрация которых была достаточно высокой, чтобы ингибировать рост C. difficile in vitro . Используя эту модель, исследование показало прямую корреляцию между ингибирующими концентрациями SCFAs и восприимчивостью хомяков к колонизации C. difficile, таким образом предполагая роль SCFAs в устойчивости к колонизации C. difficile. Однако Su et al. впоследствии вводили SCFAs непосредственно в толстую кишку мышей-гнотобиотиков (через желудочный зонд, прямую инъекцию в слепую кишку и использование Clostridium butyricum , чтобы обеспечить производство масляной кислоты in situ ) и обнаружили, что SCFAs сами по себе не могут ингибировать рост С.difficile in vivo (39). Используя модель in vitro устойчивости к колонизации C. difficile, Borriello и Barclay также не смогли найти корреляцию между профилями SCFA фекальных эмульсий и их ингибирующей активностью против C. difficile (40). В более позднем исследовании дисбактериоз кишечника, вызванный эпидемическим штаммом C. difficile 027 / BI у мышей, был связан с измененным профилем SCFA, характеризующимся заметным снижением уровней бутирата и ацетата (20). Таким образом, остается неясным, являются ли масляная кислота или другие противомикробные соединения, которые еще предстоит идентифицировать, ключевыми молекулами в устойчивости к колонизации C.difficile. Однако жизнеспособные бактерии, вероятно, являются наиболее важными компонентами устойчивости к колонизации в желудочно-кишечном тракте (40). Хотя конкретные бактерии, ответственные за устойчивость к колонизации у людей, остаются неизвестными, наше исследование предполагает, что истощение бактерий, продуцирующих бутират в кластерах IV и XIVa, может сделать хозяина восприимчивым к инфекции C. difficile, и пополнение этих бактерий в кишечнике может быть более значительным. терапевтический эффект при внутрибольничной диарее, включая ИКД. В соответствии с этой гипотезой, после предварительной обработки мышей антибиотиками с последующим введением C.difficile, в кишечной микробиоте клинически здоровых животных преобладали Firmicutes, тогда как у клинически больных животных преобладали Proteobacteria (41).
Это исследование имеет несколько ограничений. Во-первых, образцы для групп CDI и CDN были одноразовыми образцами фекалий, собранными во время диареи для клинического микробиологического тестирования. Хотя исследование микробиома микробиоты кишечника непосредственно перед приобретением C. difficile или началом заболевания было бы идеальным, такие образцы фекалий трудно получить от людей.Истощение запасов бутирогенных бактерий в начале заболевания может быть результатом, а не причиной воспаления кишечника. Таким образом, причинно-следственная связь должна оцениваться механистически с использованием животных моделей инфекции и заражения C. difficile. Тем не менее, настоящее исследование определяет список организмов-кандидатов на уровне семейства и рода, которые могут служить основой для выбора конкретных микробов для будущих исследований функциональной и колонизационной устойчивости с использованием моделей животных, связанных с микробиотой человека.
Во-вторых, у некоторых субъектов в группе CDN были симптомы диареи, которые могли быть отнесены к заболеванию, связанному с C. difficile. Субъекты с диареей были включены в группу CDI или CDN в соответствии с результатами клинических тестов C. difficile (либо тест C. Diff Quik Chek Complete, либо тест мультиплексной ПЦР GeneXpert, поскольку клиническая платформа была изменена в ходе исследования. ). Чтобы изучить возможность получения ложноотрицательных результатов клинических тестов и / или колонизации C. difficile, мы провели дополнительные внутренние ПЦР-анализы на ген токсина B для всех образцов.У семи субъектов в группе CDN и одного здорового контрольного субъекта наблюдались очень слабые продукты амплификации токсина B. Напротив, все образцы для группы CDI показали сильные продукты амплификации. Хотя мы не могли исключить возможность ошибочной классификации в группе CDN на основании этих данных, совокупная микробиота кишечника не претерпела значительных изменений, когда семь образцов CDN со слабыми сигналами токсина B C. difficile были исключены из нашего анализа (см. Рис. S9 в дополнительный материал).
В-третьих, наши выводы об истощении продуцентов бутирата основывались на прогнозах о производстве короткоцепочечных жирных кислот для предполагаемых филотипов (refOTU). Наш геномный анализ был основан на последовательностях частичного гена 16S рРНК размером ~ 500 п.н., которые могли неправильно классифицировать определенные бактерии на уровне вида или штамма. Кроме того, существуют различия в продукции SCFA среди разных видов бактерий в пределах данного рода, а данные о продукции SCFA отсутствуют для многих кишечно-ассоциированных организмов, выявленных в нашем исследовании.Учитывая эти неопределенности, мы сосредоточили нашу классификацию на уровне родов, который более подробно описан в литературе. Уровни SCFAs и бутирата в кале можно напрямую измерить в будущих исследованиях, чтобы подтвердить наши выводы.
Таким образом, настоящее исследование выявило Lachnospiraceae, Ruminococcaceae и анаэробные бактерии, продуцирующие бутират, как значимо истощенных при инфекции C.

 , связанные с повышением кислотности или щелочности среды обитания бактерий, что влечет за собой изменение обмена веществ и клеточных мембран полезных микроорганизмов;
, связанные с повышением кислотности или щелочности среды обитания бактерий, что влечет за собой изменение обмена веществ и клеточных мембран полезных микроорганизмов;



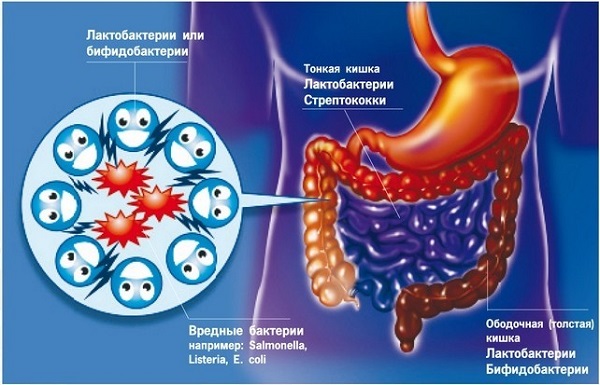
 Особенно вечером — уменьшенное количество ферментов не может обработать всю пищу, а остатки пищи начинают способствовать развитию патогенных бактерий.
Особенно вечером — уменьшенное количество ферментов не может обработать всю пищу, а остатки пищи начинают способствовать развитию патогенных бактерий.
 , лук, яблоко, петрушка, сельдерей, чеснок, куркума и др.
, лук, яблоко, петрушка, сельдерей, чеснок, куркума и др.