лечение в Перми, низкие цены
Тиреоидит – одно из самых распространенных заболеваний щитовидной железы. В зимний период это заболевание обостряется, поэтому сейчас – самое время узнать все об этой болезни и способах лечения.
Лечение тиреоидита щитовидной железы в Перми качественно проводят в клинике «Генезис».
Что такое тиреоидит
Тиреоидит – это воспаление щитовидной железы разной степени тяжести и характера. У женщин патология встречается чаще, чем у мужчин. Какие-либо виды тиреоидита встречаются примерно у 15% взрослых людей.
Виды заболевания
Тиреоидиты встречаются нескольких видов в зависимости от специфики протекания болезни:
- Острый – проявляется воспалительным процессом всей щитовидной железы (диффузный), отдельной доли или части доли. При этом виде заболевания могут образовываться гнойные очаги.
-
Подострый.

- Хронический. Один из самых распространенных – аутоиммунный тиреоидит Хашимото, зоб Риделя и специфические формы заболевания.
Также патология классифицируются по этиологии на:
- аутоиммунный тиреоидит щитовидной железы;
- сифилитический;
- туберкулезный и другие.
Причины заболевания
Развитию каждого из видов болезни способствуют специфические причины. Разберем каждый вид в отдельности.
Причины острого тиреоидита:
- инфекционные заболевания различной природы;
- травма;
- кровоизлияния в щитовидную железу;
- лучевое поражение.
Причины подострого тиреоидита:
- вирусы;
- хронические инфекции носоглотки;
-
генетический фактор.

Основные причины хронического тиреоидита:
- генетическая склонность;
- последствия операций на щитовидной железе;
- зоб;
- сахарный диабет;
- другие аутоиммунные заболевания, аллергии.
Симптомы тиреоидита щитовидной железы
- высокая температура;
- озноб;
- боли в шее, челюсти, языке, ушах;
- слабость;
- головная боль;
- ломота в теле;
- ощущение «ком в горле»;
- осиплость голоса;
- болезненность области щитовидки;
- хрипота в голосе;
- тахикардия.
Пациент чувствует присутствие инородного тела в горле, удушье, постоянно хочется прокашляться, ощущение, что на шее что-то тяжелое.
Чем опасные тиреоидиты
Основное осложнение – попадание гноя из пораженной зоны в ткани соседних органов, что ведет к септическому поражению средостения. При недостаточном лечении приводит к печальным последствиям – развитию недостаточности щитовидной железы.
Диагностика
Для точной постановки диагноза эндокринолог назначает:
Лечение тиреоидита
Важный пункт в лечении – выбрать грамотного специалиста. В нашей клинике работает заведующая отделением терапии, эндокринолог Ольга Николаевна Турунцева.
Терапия может быть самой разной – от наблюдения у эндокринолога до снятия болевых ощущений, от назначения гормональных препаратов до хирургического вмешательства. Также может быть назначена:
- Противогрибковая терапия.
- Курс метаболической терапи.
- Антигистаминные препараты.
-
Медикаментозная детоксикация.

Главное — при первых симптомах обратиться к эндокринологу!
Даже ОРВИ может подорвать иммунитет, что приведет к развитию тиреоидита. Поэтому самолечением заниматься нельзя! При любом недомогании обращайтесь к врачу, строго выполняйте все рекомендации, соблюдайте дозировку. И будьте здоровы!
Как записаться на прием
Узнайте цену на лечение тиреоидита в Перми у администраторов клиники «Генезис». Записаться на прием в клинику очень легко. Пять способов на выбор:
- звоните по телефонам: +7 (342) 200 95 31, +7 (342) 202 64 02;
- записывайтесь на сайте онлайн;
- напишите личное сообщение в группе ВКонтакте: vk.com/genesis_perm;
- пишите в директ Instagram: @genesis_perm;
- приходите по адресу: ул. Чернышевского, 15Б.
Аутоиммунный тиреоидит. Клиника, диагностика, лечение.
Клинические проявления Аутоиммунного тиреоидита:Аутоиммунный тиреоидит очень часто длительно протекает без каких-либо клинических проявлений и может быть выявлен при случайном ультразвуковом исследовании щитовидной железы.

Клинические признаки могут проявляться:
- неприятными ощущения в области щитовидной железы,
- ощущения кома в горле при глотании,
- чувство давления в горле.
- крайне редко боли в области щитовидной железы, в основном при пальпации щитовидной железы.
Иногда начало болезни может сопровождаться состоянием гиперфункции (из-за большого выброса гормонов в кровь при повреждении клеток щитовидной железы, но как правило, функция щитовидной железы нормальная или сниженная (гипотироз).
В зависимости от ультразвуковой картины и размеров щитовидной железы аутоиммунный тиреоидит делится на 2 формы:
- атрофическая, при которой увеличения щитовидной железы не бывает. Встречается у большинства больных, но чаще в пожилом возрасте и у молодых пациентов, которые подвергались радиоактивному облучению. Обычно эта форма клинически сопровождается снижением функции щитовидной железы (гипотироз).
- гипертрофическая, которая всегда сопровождается увеличением щитовидной железы.
 Щитовидная железа может быть равномерно увеличена по всему объему (диффузная гипертрофическая форма), или отмечается наличие узлов (узловая/ложноузловая форма). Возможно сочетание диффузной и узловой форм (смешанная форма).
Щитовидная железа может быть равномерно увеличена по всему объему (диффузная гипертрофическая форма), или отмечается наличие узлов (узловая/ложноузловая форма). Возможно сочетание диффузной и узловой форм (смешанная форма).
Диагностика
Проводится тщательный опрос пациента для выявления всех жалоб, сбор анамнеза для выявления наследственности, осмотр пациента, пальпация щитовидной железы. Из лабораторных и инструментальных исследований проводятся:
- Общий анализ крови для выявления уровня лимфоцитов
- Иммунологический анализ крови: определение уровня антител к тиреоглобулину, тиреопероксидазе (обязательное подтверждение диагноза).
- Определение в крови уровня тиреоидных гормонов — ТТГ, свободных Т3 и тироксина.
- УЗИ щитовидной железы. Позволяет оценить размеры железы, выявить нарушения структуры, наличие узлов, кист, опухолей.
- Тонкоигольная биопсия щитовидной железы (для дифферециального диагноза клеточного состава узлов).

Лечение аутоиммунного тиреоидита
Специфическая терапия аутоиммунного тиреоидита не разработана. В зависимости от функции железы назначают заместительную терапию тиреоидными гормонами или одавляющую терапию производными тиамазола.
Применяется иммуномодулирующая терапия, иногда нестероидные противовоспалительные препараты, сорбенты. Глюкокортикоиды, как правило, назначаются при больших размерах железы, высоком титре антител и наличие «ложноузловых» образований.
Диагностика и лечение данной патологии проводится исключительно эндокринологом.
Аутоиммунный тиреоидит
Статью подготовила врач-эндокринолог Наталья Регинальдовна Дударькова
Аутоиммунный тиреоидит — это хроническое воспаление щитовидной железы, при котором происходит гибель железистых клеток, что ведёт к гипотиреозу, то есть полному отсутствию выработки гормонов щитовидной железы.
Это заболевание довольно распространённое и составляет порядка 20-30% от общего числа болезней железы.
Причины
Причины развития данного недуга до конца не изучены, однако абсолютно точно известно, что огромную роль здесь играет генетическая предрасположенность, которую заставляет сработать внешний негативный фактор, например инфекция, травма щитовидной железы или операция на ней.
Также немаловажную роль в становлении болезни играет бесконтрольный приём лекарственных средств (йодосодержащих, гормональных), плохая экология, радиационное излучение, сильный стресс.
Сложность кроется в том, что часто течение аутоиммунного тиреоидита происходит бессимптомно. Нередки случаи, когда болезнь протекает под маской другого заболевания, так что пациент может приходить с жалобами к иным врачам, но не эндокринологу, теряя тем самым драгоценное время.
Симптомы
Железа может быть не увеличена, безболезненна, а уровень гормонов в норме. Тем не менее, стоит знать, какие сигналы должны насторожить и заставить показаться врачу.
Тем не менее, стоит знать, какие сигналы должны насторожить и заставить показаться врачу.
Это общая утомляемость, слабость, перепады настроения, плаксивость, сонливость, потливость, скачки артериального давления, повышение температуры тела, нарушение менструального цикла у женщин, учащённое сердцебиение.
По мере разрушения клеток щитовидной железы, нарушается выработка тиреоидных гормонов, это постепенно приводит к увеличению органа в размерах, пациенты жалуются на дискомфорт в области шеи, кожа становится бледной, приобретает желтоватый оттенок, отекает лицо, ухудшается память, снижается интеллект.
Симптоматика аутоиммунного тиреоидита развивается довольно медленно, так что, в большинстве случаев, болезнь диагностируется уже после того, как сформировался гипотиреоз.
Диагностика
Однако, диагноз может быть установлен и на ранних этапах, если известна наследственная предрасположенность и имеется яркая клиническая картина.
Для диагностики недуга проводятся следующие лабораторные исследования: общий анализ крови, назначается иммунограмма, определение уровня Т3, Т4 и ТТГ, УЗИ щитовидной железы. В случаях, когда имеется угроза злокачественного перерождения узлового образования органа, врач может прибегнуть к биопсии его тканей.
В случаях, когда имеется угроза злокачественного перерождения узлового образования органа, врач может прибегнуть к биопсии его тканей.
Лечение
До настоящего времени, несмотря на все достижения медицины, не разработана специальная схема лечения аутоиммунного тиреоидита. На ранних стадиях болезни проводится симптоматическое лечение.
В дальнейшем назначается приём препаратов — синтетических аналогов гормонов щитовидной железы. Всё это проходит под пристальным контролем врача с необходимой коррекцией дозировки.
Помимо этого, могут применяться нестероидные противовоспалительные средства, а также препараты для поддержания иммунитета, витаминно-минеральные комплексы. При сильном увеличении щитовидной железы, приводящем к сдавливанию ею органов, проводится оперативное лечение.
Несмотря на то, что аутоиммунный тиреоидит — довольно сложное для диагностики и лечения заболевания, при своевременной диагностики и начатом лечении можно значительно замедлить развитие недуга, достигнуть длительной ремиссии и надолго сохранить качество жизни.
ЗАПИСАТЬСЯ НА ПРИЁМ К ЭНДОКРИНОЛОГУ
Тиреоидит – заболевание щитовидной железы
Тиреоидит – это заболевание щитовидной железы . Существуют различные виды тиреоидита, которые зависят от возникновения и течения заболевания. Тиреоидит бывает острым, подострым или тиреоидит де Кервена, хроническим фиброзным или зоб Риделя, аутоиммунным или тиреоидит Хошимского.
Рассмотрим основные виды тиреоидита, симптомы и методы лечения.
Острый тиреоидит
При остром тиреоидите пациент ощущает боль в области передней поверхности шеи, которая передается в затылок и челюсть. Боль усиливается во время движения головы и при глотании. Острый тиреоидит характеризуется увеличением шейных лимфатических узлов, высокой температурой, ознобом.
Острый тиреоидит бывает гнойным или негнойным, распространенным или местным. При распространенном остром тиреоидите поражается целая доля или вся щитовидная железа. Местный тиреоидит поражает только некоторую часть щитовидной железы. Острый гнойный тиреоидит развивается на фоне острой или хронической инфекции — тонзиллит, воспаление миндалин, пневмония. Острый негнойный тиреоидит получает развитие в основном после травмы, лучевой терапии, кровоизлияния в щитовидную железу — лечение просто необходимо.
Местный тиреоидит поражает только некоторую часть щитовидной железы. Острый гнойный тиреоидит развивается на фоне острой или хронической инфекции — тонзиллит, воспаление миндалин, пневмония. Острый негнойный тиреоидит получает развитие в основном после травмы, лучевой терапии, кровоизлияния в щитовидную железу — лечение просто необходимо.
Для лечения острого тиреоидита применяются антибиотики, различные препараты для лечения сопутствующих симптомов, витамины С и В. В случае развития гнойного воспаления тканей применяется хирургическое лечение.
Подострый тиреоидит или тиреоидит де Кервена
Подострый тиреоидит наблюдается в случае воспаления щитовидной железы , после перенесенных вирусных инфекций. Чаще всего данным заболеванием болеют женщины 30-50 лет, в 5-6 раз чаще, чем мужчины.
Симптомы подострого тиреоидита:
- сильные боли в области щитовидной железы;
- увеличение и уплотнение щитовидной железы;
- покраснение кожи на передней поверхности шеи из-за усиления притока крови к коже шеи;
- повышение температуры, озноб;
- слабость, потливость, головная боль;
- проявления тиреотоксикоза – раздражительность, потливость, чувство жажды, похудение, дрожь пальцев.

Причинами подострого тиреоидита являются вирусные инфекции – вирус гриппа, кори, эпидемического паротита. В настоящее время заболевание изучено не до конца, определенный вирус для данного заболевания не выявлен. Ключевым фактором возникновения данного заболевания является наследственная предрасположенность, а так же наличие хронической инфекции в области носоглотки.
Хронический фиброзный тиреоидит или зоб Риделя
Фиброзный тиреоидит характеризуется сильным разрастанием соединительной ткани в щитовидной железе. При этом проявляются признаки сдавливания в области шеи. Заболевание наиболее распространено среди женщин в возрасте 50 лет.
Особенности фиброзного тиреоидита заключаются в том, что развивается заболевание очень медленно, постепенно, на ранних стадиях сложно выявить недуг. Самым первым симптомом заболевания является затруднение при глотании и ощущение «кома в горле».
Другие симптомы фиброзного тиреоидита на поздних стадиях развития:
- нарушение дыхания, глотания, затруднение речи;
- охриплый голос;
- сильное и неравномерное увеличение щитовидной железы;
- головная боль, шум в умах, нарушение зрения, выраженная пульсация сосудов в области шеи;
- симптомы гипотиреоза в большинстве случаев.

Причины появления и развития фиброзного тиреоидита до конца не исследованы, но точно известно, какие группы людей наиболее подвержены данному недугу. В группу риска входят люди, страдающие Безодовой болезнью, имеющие любую форму эндемического зоба, сахарный диабет, аллергические и и аутоиммунные заболевания.
Аутоиммунный тиреоидит или тиреоидит Хошимского
Аутоиммунный тиреоидит – это заболевание, которое характеризуется хроническим воспалительным процессом в щитовидной железе аутоиммунного происхождения. Данное заболевание наиболее часто встречается у женщин, в 4-7 раз чаще, чем у мужчин. Развитие недуга происходит преимущественного после 60 лет.
Симптомы аутоиммунного тиреоидита:
- неравномерное увеличение и уплотнение щитовидной железы;
- нарушение функций щитовидной железы: сначала развитие симптомов гипертиреоза, а затем гипотиреоза;
- затруднения при глотании;
- слабость, чувство сдавливания шеи, чувство жара, учащенное сердцебиение, потливость, похудание, раздражительность.

Причинами возникновения аутоиммунного тиреоидита является наследственная предрасположенность, нарушения иммунного и эндокринного постоянства в подростковом возрасте, во время беременности, при родах, старении.
При аутоиммунном тиреоидите могут развиваться и другие опасные заболевания такие, как Базедова болезнь, эндемический зоб, аденома, рак железы.
Своевременная медицинская помощь поможет Вам избежать развития тиреоидитаи снизить риск возникновения последствий.
Аутоиммунные заболевания щитовидной железы
Цель обзора . Исследования в области аутоиммунных заболеваний щитовидной железы публикуются с января 2005 года. Обзор разделен на области этиологии, аутоиммунных свойств, аутоантител, механизма повреждения клеток щитовидной железы, ответов B-клеток и ответов T-клеток. Также рассматривается диагноз и взаимосвязь между аутоиммунным заболеванием щитовидной железы, новообразованием и заболеваниями почек. Недавние открытия . Сообщалось об аутоиммунных заболеваниях щитовидной железы у людей, живущих в разных частях мира, включая Северную Америку, Европу, Балканы, Азию, Ближний Восток, Южную Америку и Африку, хотя представленные цифры не полностью отражают количество инфицированных за год.Случаи не распознаются из-за неточного диагноза и, следовательно, рассматриваются как другие заболевания. Однако самые последние исследования показали, что аутоиммунные заболевания щитовидной железы человека (AITD) поражают до 5% населения в целом и чаще встречаются у женщин в возрасте от 30 до 50 лет. Резюме . Аутоиммунное заболевание щитовидной железы — результат сложного взаимодействия генетических факторов и факторов окружающей среды. В целом, этот обзор расширил наше понимание механизма патогенеза AITD и взаимосвязи между аутоиммунным заболеванием щитовидной железы, новообразованием и заболеванием почек.Это открыло новые направления исследований, которые в конечном итоге приведут к улучшению клинической практики.
Недавние открытия . Сообщалось об аутоиммунных заболеваниях щитовидной железы у людей, живущих в разных частях мира, включая Северную Америку, Европу, Балканы, Азию, Ближний Восток, Южную Америку и Африку, хотя представленные цифры не полностью отражают количество инфицированных за год.Случаи не распознаются из-за неточного диагноза и, следовательно, рассматриваются как другие заболевания. Однако самые последние исследования показали, что аутоиммунные заболевания щитовидной железы человека (AITD) поражают до 5% населения в целом и чаще встречаются у женщин в возрасте от 30 до 50 лет. Резюме . Аутоиммунное заболевание щитовидной железы — результат сложного взаимодействия генетических факторов и факторов окружающей среды. В целом, этот обзор расширил наше понимание механизма патогенеза AITD и взаимосвязи между аутоиммунным заболеванием щитовидной железы, новообразованием и заболеванием почек.Это открыло новые направления исследований, которые в конечном итоге приведут к улучшению клинической практики.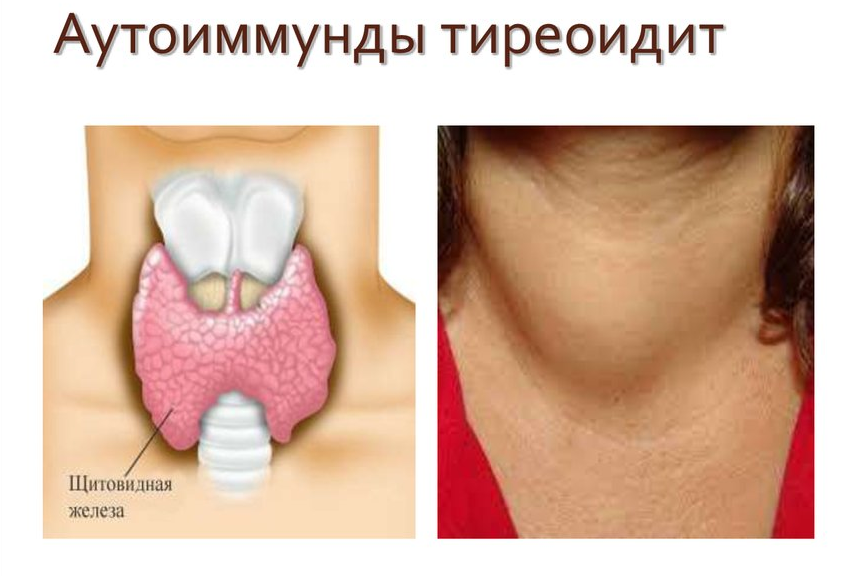
1. Введение
Основными заболеваниями щитовидной железы человека являются зоб (диффузный или узловой), гипертиреоз, гипотиреоз, аутоиммунный тиреоидит и новообразования [1]. Типы тиреоидита вызывают воспаление ткани щитовидной железы и могут выделять предварительно сформированный гормон из коллоидного пространства, вызывая тиреотоксикоз, который носит временный характер и сопровождается выздоровлением или развитием гипотиреоза.При остром и подостром тиреоидите часто присутствует болезненность щитовидной железы и боль в шее. С другой стороны, тихий тиреоидит лишен местных симптомов [2].
В США и Канаде экстраполированные значения распространенности составляют 5 873 108 и 650 157, соответственно. В Австрии и Бельгии распространенность составляет 163 495 и 206 965, соответственно. В Боснии и Македонии распространенность составляет 8 152 и 40 801, соответственно. Для Китая и Индии распространенность составляет 25 976 952 и 21 301 412, соответственно, а в Египте и Иране — 1 522 348 и 1 350 064, соответственно. В Южной Африке распространенность составляет 888 969 [3]. Ежегодная заболеваемость тиреоидитом Хашимото во всем мире оценивается в 0,3–1,5 случая на 1000 человек, в то время как болезнь Грейвса оценивается примерно в 5 случаев на 10 000 человек [4].
В Южной Африке распространенность составляет 888 969 [3]. Ежегодная заболеваемость тиреоидитом Хашимото во всем мире оценивается в 0,3–1,5 случая на 1000 человек, в то время как болезнь Грейвса оценивается примерно в 5 случаев на 10 000 человек [4].
AITD у человека широко включают болезнь Грейвса (БГ) и тиреоидит Хашимото (ГТ), которые являются наиболее частыми причинами дисфункции щитовидной железы и неэндемического зоба [4]. Эти состояния возникают из-за сложных взаимодействий между экологическими и генетическими факторами [5] и характеризуются реактивностью к собственным тироидным антигенам, что выражается в характерных воспалительных или антирецепторных аутоиммунных заболеваниях [6, 7].Среди основных генов восприимчивости к AITD, которые были идентифицированы и охарактеризованы, является локус гена HLA-DR, а также гены, не относящиеся к MHC, включая гены CTLA-4, CD40, PTPN22, тиреоглобулина и рецепторов TSH [8]. Основные триггеры AITD из окружающей среды включают йод, лекарства, инфекцию, курение, стресс и генетическую предрасположенность к AITD, которые приводят к новым предполагаемым механизмам, с помощью которых взаимодействия генетики и окружающей среды могут приводить к развитию аутоиммунитета щитовидной железы [9].
Первые патологические признаки аутоиммунного тиреоидита были описаны в 1912 году [10], когда пациенты с зобом демонстрировали диффузную инфильтрацию лимфоцитов, атрофию фолликулярных клеток, наличие гранулированных тироцитов (онкоцитарных клеток или клеток Хертла) и фиброз на гистологических изображениях их пациентов. ткани щитовидной железы [10].Тиреоидит Хашимото направлен против тироидных антигенов и является наиболее частой причиной гипотиреоза [11]. Заболеваемость составляет от 0,3 до 1,5 на 1000 человек в год, у женщин она в 4-10 раз чаще, чем у мужчин [8, 11, 12]. Тиреоидит Хашимото чаще встречается в регионах с высоким потреблением йодированной соли с пищей, а курение увеличивает риск [8]. Зоб можно увидеть при предъявлении, но чаще встречается атрофия щитовидной железы. Тиреоидит Хашимото связан с другими эндокринными заболеваниями при синдроме полигландулярной аутоиммунной недостаточности (болезнь Аддисона, сахарный диабет типа 1 и гипогонадизм) [8].Диагноз ставится на основании клинических признаков, повышенного уровня ТТГ, низкого уровня гормона щитовидной железы и наличия антител к антитироидной пероксидазе (анти-ТПО) [13].
Болезнь Грейвса, с другой стороны, включает связывание аутоантител с рецептором ТТГ, что приводит к стимуляции. Это наиболее частая причина тиреотоксикоза [14]. Активация рецепторов стимулирует рост и функцию тироцитов [15]. Заболевание чаще встречается у белых и азиатов, а заболеваемость ниже у афроамериканцев, а соотношение женщин и мужчин составляет 3.5: 1 [16]. Это чаще встречается у пациентов с семейным анамнезом заболеваний щитовидной железы, особенно болезни Грейвса. Признаки болезни Грейвса включают отек передней части голени (претибиальная микседема), заболевание щитовидной железы (выпуклость глаз, отставание век, отставание глазного яблока, экзофтальм, отек век, хемоз и слабость экстраокулярных мышц), а также усиление пигментации и витилиго. Офтальмопатия щитовидной железы встречается примерно у 50% пациентов Грейвса. Курение является фактором риска, и варианты лечения включают местные меры по борьбе с воспалением — глюкокортикоиды, плазмаферез и иммуносупрессоры, а также орбитальное облучение, декомпрессивную хирургию и абляцию щитовидной железы [2].
2. Этиология
Этиология AITD многофакторна. Восприимчивость к заболеванию определяется сочетанием иммунного механизма, генетики, факторов окружающей среды (йод, инфекция и стресс) и конституциональных факторов.
3. Иммунные механизмы
В патогенез гипертиреоза Грейвса могут быть вовлечены различные иммунные механизмы. Основными механизмами, для которых есть некоторые доказательства, являются молекулярная мимикрия (кроссовер специфичности), экспрессия HLA (человеческих лейкоцитов) молекул (антигенов) клетками щитовидной железы и активация стороннего наблюдателя [17].
4. Молекулярная мимикрия
Молекулярная мимикрия подразумевает структурное сходство между некоторым инфекционным или другим экзогенным агентом и белками человека, так что антитела и Т-клетки, активированные в ответ на экзогенный агент, вступают в реакцию с человеческим белком, в данном случае с одним или несколькими тироидными белки. Например, при анализе 600 моноклональных антител, полученных против большого разнообразия вирусов, 4 процента моноклональных антител вступили в перекрестную реакцию с неинфицированными тканями [18].
5. Аномальная экспрессия молекул HLA II клетками щитовидной железы
Эпителиальные клетки щитовидной железы пациентов с аутоиммунным заболеванием щитовидной железы (включая болезнь Грейвса), но не здоровые субъекты, экспрессируют молекулы MHC класса II, особенно молекулы HLA-DR [19]. Эта экспрессия может быть прямым результатом вирусных или других инфекций эпителиальных клеток щитовидной железы или может быть индуцирована цитокинами, такими как интерферон-гамма, продуцируемыми Т-клетками, которые были привлечены к железе либо инфекцией, либо непосредственно из-за присутствия тироидных антигенов [20].
Экспрессия молекул класса II обеспечивает механизм презентации тироидных антигенов и активации аутореактивных Т-клеток с потенциалом сохранения заболевания щитовидной железы [20]. Несколько экспериментальных наблюдений подтверждают эту гипотезу: индукция молекул класса II на эпителиальных клетках щитовидной железы интерфероном-гамма может вызывать аутоиммунный тиреоидит у восприимчивых мышей [21]; вирусы могут напрямую индуцировать экспрессию молекул класса II на клетках щитовидной железы, независимо от секреции цитокинов [20, 22]; эпителиальные клетки щитовидной железы, экспрессирующие молекулы класса II, могут представлять вирусные пептидные антигены клонированным Т-клеткам [23]; клоны тироидных антиген-специфических Т-клеток у нормальных крыс специфически реагируют с клонированными аутологичными клетками щитовидной железы в отсутствие более традиционных антигенпредставляющих клеток [24]; и животная модель болезни Грейвса, индуцированной клетками, экспрессирующими TSHR, эффективна только тогда, когда клетки также экспрессируют антигены MHC класса II [25, 26]. Эти данные убедительно подтверждают мнение о том, что инсульт, например инфекция, может вызывать экспрессию молекул класса II на клетках щитовидной железы человека и что эти клетки затем могут действовать как антигенпрезентирующие клетки, инициируя аутоиммунный ответ [20].
Эти данные убедительно подтверждают мнение о том, что инсульт, например инфекция, может вызывать экспрессию молекул класса II на клетках щитовидной железы человека и что эти клетки затем могут действовать как антигенпрезентирующие клетки, инициируя аутоиммунный ответ [20].
Экспрессия молекулы костимулятора Т-клеток, CD40, на эпителиальных клетках щитовидной железы указывает на то, что костимулирующие молекулы доступны для этого действия. Кроме того, интратироидальные дендритные клетки и В-клетки также могут служить мощными антигенпрезентирующими клетками [27, 28].Описание гипертиреоза у мышей, иммунизированных фибробластами, коэкспрессирующими молекулы класса II и рецепторы человеческого ТТГ, предоставляет дополнительные доказательства того, что клетки не обязательно должны быть «профессиональными» антигенпрезентирующими клетками для представления антигена, если они могут приобретать способность экспрессировать молекулы класса II [29 ].
6. Активация сторонним наблюдателем
Для того, чтобы экспрессия антигена HLA класса II и презентация антигенов были реализованы, должно быть местное повреждение для инициирования ответов. Как упоминалось выше, это может принимать форму прямого поражения щитовидной железы вирусной инфекцией клеток щитовидной железы или иммунных клеток. Даже прибытие активированных Т-клеток в щитовидную железу может, возможно, инициировать такую серию событий у восприимчивого субъекта с соответствующим иммунным репертуаром [30]. Фактические данные показывают, что такая случайная активация местных Т-клеток, которые могут не быть специфичными для щитовидной железы, может оказывать посредством цитокинов заметный активационный эффект на резидентные тироид-специфические Т-клетки.Доказательства таких побочных эффектов были получены на животной модели вирусно-индуцированного аутоиммунного инсулита и экспериментального аутоиммунного тиреоидита [31].
Как упоминалось выше, это может принимать форму прямого поражения щитовидной железы вирусной инфекцией клеток щитовидной железы или иммунных клеток. Даже прибытие активированных Т-клеток в щитовидную железу может, возможно, инициировать такую серию событий у восприимчивого субъекта с соответствующим иммунным репертуаром [30]. Фактические данные показывают, что такая случайная активация местных Т-клеток, которые могут не быть специфичными для щитовидной железы, может оказывать посредством цитокинов заметный активационный эффект на резидентные тироид-специфические Т-клетки.Доказательства таких побочных эффектов были получены на животной модели вирусно-индуцированного аутоиммунного инсулита и экспериментального аутоиммунного тиреоидита [31].
7. Предрасполагающие и предрасполагающие факторы к болезни Грейвса
Было предложено несколько факторов, которые предрасполагают к гипертиреозу Грейвса или инициируют его, включая генетическую предрасположенность, инфекцию, стресс, половые стероиды, курение, беременность и наркотики, рассмотренные в разделах следует [32].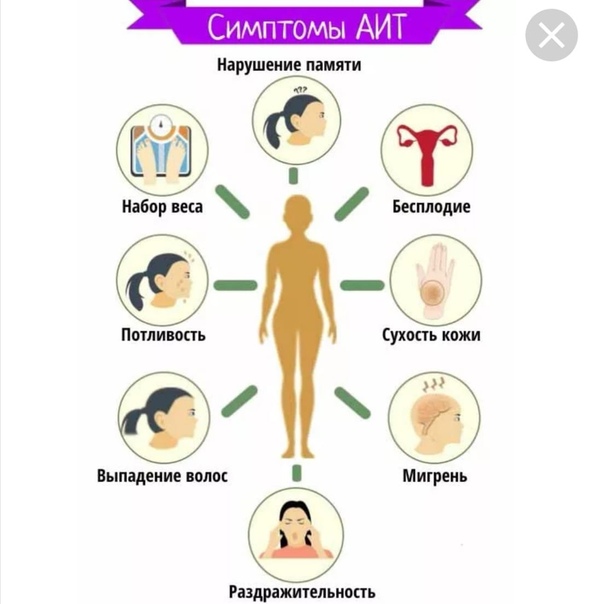
8.Генетическая предрасположенность
Существует множество эпидемиологических данных о генетической предрасположенности к гипертиреозу Грейвса и хроническому аутоиммунному тиреоидиту [14, 33]. Заболевания группируются в семьях и чаще встречаются у женщин. Частота конкордантности у монозиготных близнецов составляет от 20 до 40 процентов [34]. Частота рецидивов болезни Грейвса у братьев и сестер превышает 10,0 [35]. Существует связь между аутоиммунным заболеванием щитовидной железы и некоторыми аллелями CTLA-4 (цитотоксический Т-лимфоцит-антиген / ассоциированный белок 4).Например, в одном исследовании 379 пациентов с гипертиреозом Грейвса в Соединенном Королевстве 42 процента имели определенный аллель (аллель G) гена CTLA-4 по сравнению с 32 процентами из 363 нормальных субъектов [36]. Существует ассоциация с определенными аллелями HLA на хромосоме 6. Например, исследование пациентов европеоидной расы в Северной Америке показало, что HLA-DRB1 * 08 и DRB3 * 0202 были связаны с заболеванием и что DRB1 * 07 был защитным [5 , 37, 38].
9. Инфекция
Если инфекция была причиной гипертиреоза Грейвса, идентифицируемый агент должен присутствовать у большинства пациентов, и должна быть возможность вызвать заболевание путем передачи агента.Возможные инфекции самой щитовидной железы (подострый тиреоидит и врожденная краснуха) связаны с аутоиммунным заболеванием щитовидной железы и могут инициировать экспрессию молекул класса II [39]. Инфекция гепатита С — хорошо известная причина аутоиммунного заболевания щитовидной железы при лечении интерфероном. Однако нет никаких доказательств того, что эти или какие-либо другие инфекции или воздействия приводят непосредственно к аутоиммунному заболеванию щитовидной железы [39–41].
10. Стресс
По сравнению с нормальными субъектами или пациентами с токсическим узловым зобом, пациенты с гипертиреозом Грейвса чаще испытывают в анамнезе какой-либо тип психологического стресса, в частности, негативные жизненные события, такие как потеря супруга до начала заболевания. их гипертиреоз [42–44].В целом стресс вызывает состояние подавления иммунитета, возможно, опосредованное действием кортизола на иммунные клетки. Подавление стресса может сопровождаться восстановительной иммунологической гиперактивностью. Такой ответ может вызвать аутоиммунное заболевание щитовидной железы у генетически предрасположенных субъектов [42–44].
их гипертиреоз [42–44].В целом стресс вызывает состояние подавления иммунитета, возможно, опосредованное действием кортизола на иммунные клетки. Подавление стресса может сопровождаться восстановительной иммунологической гиперактивностью. Такой ответ может вызвать аутоиммунное заболевание щитовидной железы у генетически предрасположенных субъектов [42–44].
11. Половые стероиды
Гипертиреоз Грейвса развивается у большего числа женщин, чем у мужчин, с соотношением примерно 7: 1; эффект, который, как часто говорят, каким-то образом опосредован большим количеством эстрогена или меньшим количеством тестостерона [45].Существует множество доказательств того, что умеренное количество эстрогена усиливает иммунологическую реактивность к аутоантигенам [46, 47]. Однако столь же вероятно, что Х-хромосома является источником повышенной восприимчивости, а не половые стероиды, поскольку восприимчивость сохраняется после менопаузы. Например, инактивация Х-хромосомы связана с аутоиммунным заболеванием щитовидной железы [45].
12. Курение
Курение является фактором риска гипертиреоза Грейвса (относительный риск примерно 2.0) и еще более сильный фактор риска офтальмопатии Грейвса [48–50].
13. Беременность
Болезнь Грейвса во время беременности встречается нечасто, поскольку гипертиреоз связан со снижением фертильности и увеличением выкидышей. Кроме того, беременность — это время подавления иммунитета, поэтому болезнь имеет тенденцию улучшаться по мере развития беременности. Во время беременности функции как Т-клеток, так и В-клеток снижаются, и восстановление после иммуносупрессии может способствовать развитию послеродового заболевания щитовидной железы [51].Было также высказано предположение, что микрочимерия плода (присутствие фетальных клеток в материнской ткани) может играть роль в развитии послеродового аутоиммунного заболевания щитовидной железы [52]. До 30 процентов молодых женщин имеют в анамнезе беременность в течение 12 месяцев до начала болезни Грейвса, что указывает на то, что послеродовая болезнь Грейвса является удивительно частым проявлением и что беременность является основным фактором риска для восприимчивых женщин [53].
14. Лекарственные препараты
Йод и йодсодержащие препараты, такие как амиодарон, могут вызывать болезнь Грейвса или рецидив болезни Грейвса у восприимчивых людей [48, 54].Йод, скорее всего, спровоцирует тиреотоксикоз в популяции с дефицитом йода, просто позволив TSHR-Ab эффективно стимулировать выработку гормона щитовидной железы. Неясно, есть ли еще какое-либо провоцирующее событие. Йод и амиодарон также могут напрямую повреждать клетки щитовидной железы и высвобождать тироидные антигены в иммунную систему [55].
15. Предрасполагающие и провоцирующие факторы тиреоидита Хашимото
Инфекция, стресс, половые стероиды, беременность, потребление йода и радиационное облучение являются известными возможными провоцирующими факторами тиреоидита Хашимото [56].Микрохимеризм плода в щитовидной железе матери также возможен [52, 56–59].
16. Генетическая предрасположенность
Существует генетическая предрасположенность к тиреоидиту Хашимото, и в последние годы многое было изучено о генах предрасположенности к этому заболеванию в частности и к аутоиммунному заболеванию щитовидной железы в целом [60].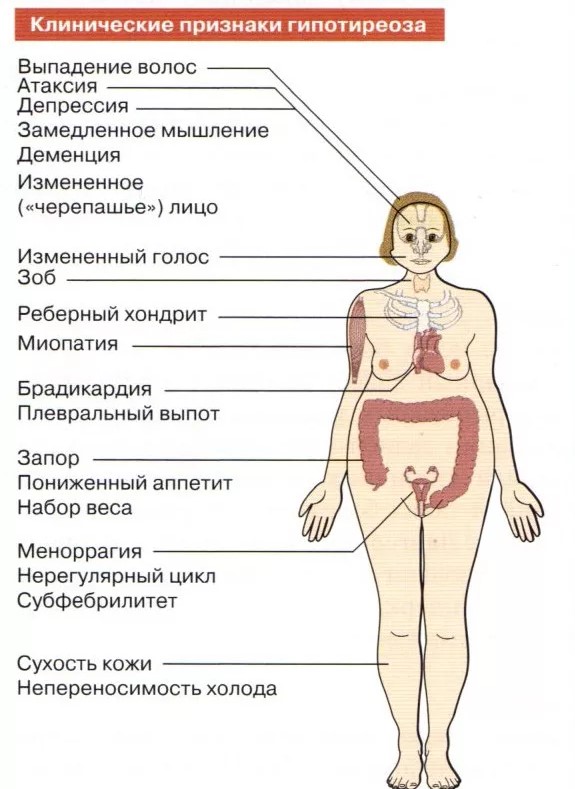 Доказательства генетической предрасположенности к тиреоидиту Хашимото включают следующие наблюдения.
Доказательства генетической предрасположенности к тиреоидиту Хашимото включают следующие наблюдения.
Болезнь группируется в семьях, иногда одна, а иногда в сочетании с болезнью Грейвса [61].Риск рецидива у братьев и сестер> 20 [35]. Уровень конкордантности у монозиготных близнецов составляет от 30 до 60 процентов, несмотря на случайные комбинации генов Т-клеточного рецептора и антитела V во время рекомбинации [62]. Существует связь, хотя и относительно слабая, с некоторыми аллелями HLA, такими как DR3. Есть связь с определенными аллелями гена CTLA-4. Ген тиреоглобулина был связан с аутоиммунным заболеванием щитовидной железы и был предложен для кодирования форм Tg с различной иммунной реактивностью [15].
17. Инфекция
Неизвестно ни одной инфекции, вызывающей или даже тесно связанной с тиреоидитом Хашимото у людей [63], хотя тиреоидит может быть вызван у экспериментальных животных некоторыми вирусными инфекциями [57]. Пациенты с подострым гранулематозным тиреоидитом (предположительно вирусной инфекцией) и врожденной краснухой могут иметь антитела к щитовидной железе в течение нескольких месяцев после болезни, и инфекции могут инициировать экспрессию молекул MHC класса II в щитовидной железе. Однако известно, что ни одно из расстройств не сопровождается обычно хроническим тиреоидитом, хотя признаки аутоиммунитета щитовидной железы могут сохраняться [64].
Однако известно, что ни одно из расстройств не сопровождается обычно хроническим тиреоидитом, хотя признаки аутоиммунитета щитовидной железы могут сохраняться [64].
18. Стресс
Различные типы стресса связаны с тиреоидитом Хашимото. Предлагаемые механизмы включают индукцию иммунной супрессии неантиген-специфическими механизмами, возможно, из-за эффектов кортизола или кортикотропин-рилизинг-гормона на иммунные клетки с последующей иммунной гиперактивностью, ведущей к аутоиммунному заболеванию щитовидной железы [58].
19. Половые стероиды и беременность
Тиреоидит Хашимото у женщин чаще, чем у мужчин, что предполагает роль половых стероидов. Однако у женщин старшего возраста вероятность развития тиреоидита Хашимото выше, чем у женщин более молодого возраста, что позволяет предположить, что наличие или отсутствие эстрогена не является важным фактором [65].
Еще одно возможное объяснение преобладания самок — это инактивация искаженной Х-хромосомы, которая была обнаружена у 34 процентов близнецов женского пола с аутоиммунным заболеванием щитовидной железы и только у 11 процентов контрольной группы [45, 66]. Возможно, что аутоантигены на инактивированной Х-хромосоме не могут быть экспрессированы в достаточной степени, чтобы обеспечить толерантность. Во время беременности наблюдается заметное увеличение количества регуляторных Т-лимфоцитов CD4 + CD25 +, что приводит к снижению функций как Т-клеток, так и В-клеток, и считается, что восстановление после иммуносупрессии способствует развитию послеродового тиреоидита [65]. Связанное с беременностью подавление иммунитета связано со сдвигом Т-лимфоцитов Th 2 и сдвигом профилей цитокинов [65].
Возможно, что аутоантигены на инактивированной Х-хромосоме не могут быть экспрессированы в достаточной степени, чтобы обеспечить толерантность. Во время беременности наблюдается заметное увеличение количества регуляторных Т-лимфоцитов CD4 + CD25 +, что приводит к снижению функций как Т-клеток, так и В-клеток, и считается, что восстановление после иммуносупрессии способствует развитию послеродового тиреоидита [65]. Связанное с беременностью подавление иммунитета связано со сдвигом Т-лимфоцитов Th 2 и сдвигом профилей цитокинов [65].
Также известно, что различные местные факторы на границе раздела иммунных клеток и трофобластов являются важными модуляторами иммунной функции во время беременности. Клетки трофобласта, расположенные в плаценте и подлежащие иммунному надзору со стороны матери, служат физическими барьерами между матерью и плодом и, как было показано, экспрессируют несколько иммуномодулирующих молекул, таких как HLA-G, FasL и индоламин-2,3-диоксигеназа. как секретирующие различные цитокины [67]. HLA-G является одним из членов семейства MHC класса I и, как известно, ингибирует функцию естественных клеток-киллеров и созревание дендритных клеток.Лиганд Fas взаимодействует с антигеном Fas и индуцирует апоптотическую гибель клеток плода антиген-реактивных материнских лимфоцитов. Индолеамин-2,3-диоксигеназа, которая катализирует триптофан в лимфоцитах, оказалась критически важной в поддержании аллогенной беременности у мышей [68]. Помимо этих местных модуляторов, прогестерон, продуцируемый плацентой, влияет на профили цитокинов во всей иммунной системе матери. Примерно у 20 процентов пациентов с послеродовым тиреоидитом в более поздние годы развивается классическая болезнь Хашимото [69].
HLA-G является одним из членов семейства MHC класса I и, как известно, ингибирует функцию естественных клеток-киллеров и созревание дендритных клеток.Лиганд Fas взаимодействует с антигеном Fas и индуцирует апоптотическую гибель клеток плода антиген-реактивных материнских лимфоцитов. Индолеамин-2,3-диоксигеназа, которая катализирует триптофан в лимфоцитах, оказалась критически важной в поддержании аллогенной беременности у мышей [68]. Помимо этих местных модуляторов, прогестерон, продуцируемый плацентой, влияет на профили цитокинов во всей иммунной системе матери. Примерно у 20 процентов пациентов с послеродовым тиреоидитом в более поздние годы развивается классическая болезнь Хашимото [69].
20. Потребление йода
Легкий дефицит йода связан с меньшей распространенностью болезни Хашимото и гипотиреоза, тогда как чрезмерное потребление связано с более высокой распространенностью [70]. Например, в Китае аутоиммунный тиреоидит был обнаружен у 0,3% людей с умеренным дефицитом йода и у 1,3% людей с чрезмерным потреблением йода [56].
21. Радиационное облучение
После трагической аварии на Чернобыльской АЭС у детей, подвергшихся облучению, развилась высокая частота аутоантител к щитовидной железе [71].Все данные свидетельствуют о том, что присутствие антител к щитовидной железе увеличивает риск развития дисфункции щитовидной железы [4, 72]. Неизвестно, играет ли радиационный фон, которому все мы подвержены, какую-либо роль в предрасположенности к аутоиммунным заболеваниям щитовидной железы. В популяционном исследовании с участием 4299 субъектов 160 подверглись профессиональному облучению ионизирующим излучением, почти 60 процентов субъектов работали на атомной электростанции, а остальные были либо медиками, либо лабораторными работниками. Десять процентов женщин, подвергшихся радиационному облучению, соответствовали критериям аутоиммунного заболевания щитовидной железы (антитела против ТПО более 200 МЕ / мл и гипоэхогенность на УЗИ) по сравнению с тремя.4 процента тех, кто не подвергался воздействию. Особо высокому риску подвергались лица, подвергавшиеся воздействию ионизирующего излучения более пяти лет [73].
Особо высокому риску подвергались лица, подвергавшиеся воздействию ионизирующего излучения более пяти лет [73].
22. Микрохимеризм плода
Клетки плода были идентифицированы в материнских щитовидных железах у пациентов с аутоиммунным заболеванием щитовидной железы. Такие клетки могут инициировать реакции щитовидной железы «трансплантат против хозяина» и играть важную роль в развитии тиреоидита Хашимото. Однако на сегодняшний день это остается гипотетическим.
23. Аутоиммунные особенности
Все формы аутоиммунитета щитовидной железы связаны с лимфоцитарным инфильтратом в щитовидной железе. Эти лимфоциты в значительной степени ответственны за создание аутореактивности, опосредованной как Т-, так и В-клетками. Другие участки, такие как лимфатические узлы, дренирующие щитовидную железу, и костный мозг, также могут содержать аутореактивные лимфоциты щитовидной железы при AITD. Первоначальный аутоиммунный ответ CD4 + Т-клеток, по-видимому, стимулирует секрецию гамма-интерферона, что приводит к усилению экспрессии молекул MHC II на тироцитах. Это, скорее всего, запускает экспансию аутореактивных Т-клеток и вызывает характерный воспалительный ответ, а по мере прогрессирования заболевания тироциты становятся мишенью для апоптоза, что приводит к гипотиреозу. Еще одним фактором, способствующим наблюдаемому гипотиреозу у пациентов с тиреоидитом Хашимото, могут быть циркулирующие антитела, ингибирующие ТТГ. С другой стороны, болезнь Грейвса представляет собой другой конец спектра, в котором пациенты страдают гипертиреозом. Активация тироид-специфичных CD4 + Т-клеток приводит к привлечению аутореактивных В-клеток и усилению стимулирующего тиреоидный иммунный ответ через антитироидные антитела [74].
Это, скорее всего, запускает экспансию аутореактивных Т-клеток и вызывает характерный воспалительный ответ, а по мере прогрессирования заболевания тироциты становятся мишенью для апоптоза, что приводит к гипотиреозу. Еще одним фактором, способствующим наблюдаемому гипотиреозу у пациентов с тиреоидитом Хашимото, могут быть циркулирующие антитела, ингибирующие ТТГ. С другой стороны, болезнь Грейвса представляет собой другой конец спектра, в котором пациенты страдают гипертиреозом. Активация тироид-специфичных CD4 + Т-клеток приводит к привлечению аутореактивных В-клеток и усилению стимулирующего тиреоидный иммунный ответ через антитироидные антитела [74].
24. Аутоантитела
24.1. Антитела к тироидной пероксидазе (ТПО)
Антитела к тироидной пероксидазе (ТПО) являются ключевым ферментом щитовидной железы, катализирующим как йодирование, так и реакцию связывания для синтеза тироидного гормона. Он связан с мембраной, обнаруживается в цитоплазме и в высокой концентрации на апикальной микровиллярной поверхности тироцитов. Он имеет молекулярную массу от 100 до 105 кДа и ранее был известен как микросомальный антиген щитовидной железы [75]. Внутри молекулы существует множество Т- и В-клеточных эпитопов, и ответ антител на ТПО ограничен на уровне вариабельной (V) области тяжелой и легкой цепи зародышевой линии [76].
Он имеет молекулярную массу от 100 до 105 кДа и ранее был известен как микросомальный антиген щитовидной железы [75]. Внутри молекулы существует множество Т- и В-клеточных эпитопов, и ответ антител на ТПО ограничен на уровне вариабельной (V) области тяжелой и легкой цепи зародышевой линии [76].
Аутоантитела против ТПО обнаруживаются более чем у 90% пациентов с аутоиммунным гипотиреозом и болезнью Грейвса. Вместе с антителами к тиреоглобулину (ТГ) они являются преобладающими антителами при аутоиммунном гипотиреозе (АГ). Антитела против ТПО в основном относятся к классу 1 IgG и в избытке подклассам IgG4 [77–79].
24,2. Антитела к тироглобулину (ТГ)
Тироглобин (ТГ) представляет собой гликопротеин массой 660 кДа, состоящий из двух идентичных субъединиц по 330 кДа каждая. Он секретируется фолликулярными клетками щитовидной железы в просвет фолликула и хранится в виде коллоидного вещества в фолликулах щитовидной железы.Каждая молекула ТГ содержит около 100 остатков тирозина, четверть из которых йодированы. Эти остатки соединяются с трийодтиронином (Т3) и тироксином (Т4). Определена последовательность человеческих ТГ [80]. Когда ТТГ стимулирует клетки щитовидной железы, ТГ подвергается эндоцитозу и гидролизуется в лизосомах, высвобождая Т3 и Т4. Точное расположение Т- и В-клеточных эпитопов в TG не известно [81].
Эти остатки соединяются с трийодтиронином (Т3) и тироксином (Т4). Определена последовательность человеческих ТГ [80]. Когда ТТГ стимулирует клетки щитовидной железы, ТГ подвергается эндоцитозу и гидролизуется в лизосомах, высвобождая Т3 и Т4. Точное расположение Т- и В-клеточных эпитопов в TG не известно [81].
Аутоантитела к тироглобулину обнаруживаются менее чем у 60% пациентов с лимфоцитарным тиреоидитом и у 30% пациентов с болезнью Грейвса.Они поликлональны и в основном относятся к классу IgG, в котором представлены все четыре подкласса. ТТГ регулирует экспрессию ТПО и ТГ на клеточной поверхности, изменяя транскрипцию этих двух белков, возможно, на уровне промотора гена. Эти эффекты имитируются аутоантителами (как блокирующими, так и стимулирующими) в сыворотках пациентов с болезнью Грейвса [82].
24,3. Антитела к рецепторам тиреотропного гормона (ТТГ-R)
Рецептор тиреотропного гормона (ТТГ-R) является основным аутоантигеном при болезни Грейвса и атрофическом тиреоидите. Он расположен на базальной поверхности фолликулярных клеток щитовидной железы [83]. При болезни Грейвса антитела, стимулирующие щитовидную железу (TSAbs), связываются с рецептором и стимулируют клетку щитовидной железы производить чрезмерное количество гормонов щитовидной железы, что приводит к гипертиреозу. У пациентов с атрофическим тиреоидитом основным антителом является ТТГ к его рецептору, что предотвращает стимуляцию клеток щитовидной железы. Это приводит к снижению выработки тироидных гормонов, атрофии щитовидной железы и клиническому состоянию гипотиреоза [83, 84].
Он расположен на базальной поверхности фолликулярных клеток щитовидной железы [83]. При болезни Грейвса антитела, стимулирующие щитовидную железу (TSAbs), связываются с рецептором и стимулируют клетку щитовидной железы производить чрезмерное количество гормонов щитовидной железы, что приводит к гипертиреозу. У пациентов с атрофическим тиреоидитом основным антителом является ТТГ к его рецептору, что предотвращает стимуляцию клеток щитовидной железы. Это приводит к снижению выработки тироидных гормонов, атрофии щитовидной железы и клиническому состоянию гипотиреоза [83, 84].
24,4. Механизм повреждения щитовидной железы
Некоторые антитела и клеточно-опосредованные механизмы способствуют повреждению щитовидной железы при аутоиммунном заболевании щитовидной железы. В целом, в случаях тиреоидита Хашимото экспрессия рецептора смерти CD95 и лигандов рецептора смерти CD95L в ткани щитовидной железы, по-видимому, намного выше по сравнению с их нормальными аналогами. Также экспрессия положительных эффекторов апоптоза и каспаз 3 и 8, а также Bax и Bak, по-видимому, относительно высока в образцах тиреоидита по сравнению с контролем. Этот паттерн экспрессии поддерживает усиленный апоптоз как механизм, лежащий в основе потери тироцитов при тиреоидите Хашимото. При болезни Грейвса наблюдается повышенная экспрессия отрицательных модуляторов апоптоза (cFLIP, Bcl-2 и Bcl-XL). Это подтверждает роль механизма ингибирования апоптоза. Хотя в обоих случаях наблюдается значительная экспрессия Fas / CD95 и его лиганда, только при тиреоидите Хашимото тироциты подвергаются апоптозу. Также была объяснена роль цитокинов в развитии аутоиммунных заболеваний [85].В случае тиреоидита Хашимото, болезни Th2, цитокин-интерферон-гамма, по-видимому, играет решающую роль в патологии заболевания, усиливая экспрессию каспаз и тем самым повышая чувствительность клеток к FAS-опосредованному апоптозу. Напротив, при Th3-опосредованной болезни Грейвса цитокины IL4 и IL-10 регулируют экспрессию двух антиапоптотических белков Bcl-XL и cFLIP, что обеспечивает устойчивость к Fas-опосредованному апоптозу. Это доказывает необходимую модулирующую роль цитокинов Th2 и Th3 в развитии аутоиммунных нарушений [74].
Этот паттерн экспрессии поддерживает усиленный апоптоз как механизм, лежащий в основе потери тироцитов при тиреоидите Хашимото. При болезни Грейвса наблюдается повышенная экспрессия отрицательных модуляторов апоптоза (cFLIP, Bcl-2 и Bcl-XL). Это подтверждает роль механизма ингибирования апоптоза. Хотя в обоих случаях наблюдается значительная экспрессия Fas / CD95 и его лиганда, только при тиреоидите Хашимото тироциты подвергаются апоптозу. Также была объяснена роль цитокинов в развитии аутоиммунных заболеваний [85].В случае тиреоидита Хашимото, болезни Th2, цитокин-интерферон-гамма, по-видимому, играет решающую роль в патологии заболевания, усиливая экспрессию каспаз и тем самым повышая чувствительность клеток к FAS-опосредованному апоптозу. Напротив, при Th3-опосредованной болезни Грейвса цитокины IL4 и IL-10 регулируют экспрессию двух антиапоптотических белков Bcl-XL и cFLIP, что обеспечивает устойчивость к Fas-опосредованному апоптозу. Это доказывает необходимую модулирующую роль цитокинов Th2 и Th3 в развитии аутоиммунных нарушений [74].
24,5. Ответы В-клеток
Тироглобин (ТГ) и антитела к ТПО встречаются в очень высоких концентрациях у пациентов с тиреоидитом Хашимото и первичной микседемой. Эти антитела встречаются реже, но все же часто встречаются при болезни Грейвса, тогда как ТПО, а не ТГ-антитела, чаще встречаются при послеродовом тиреоидите [86]. Оба антитела частично ограничиваются подклассом IgG4 [76]. Антитела TG обычно опосредуют опосредованную антителами цитотоксичность (ADCC), тогда как антитела TPO образуют терминальные комплексы комплемента в щитовидной железе.Клеточно-опосредованное повреждение может быть необходимо для антител ТПО, чтобы получить доступ к их антигену и стать патогенными [87].
24,6. Т-клеточные ответы
И CD4 +, и CD8 + Т-клетки встречаются в лимфоцитарном инфильтрате щитовидной железы с преобладанием CD4 + клеток. Увеличивается количество маркеров экспрессии активированных Т-клеток, таких как HLA-DR. Цитокины, включая ИЛ-2, интерферон-гамма, фактор некроза опухоли, ИЛ-4, ИЛ-6, ИЛ-2, ИЛ-10, ИЛ-12, ИЛ-13 и ИЛ-15, продуцируются лимфоцитами с некоторыми вариациями. между пациентами [88].Клетки щитовидной железы экспрессируют MHC класса II и ведут себя как антигенпрезентирующие клетки (APC). Экспрессия ICAM-1, LFA-3 и MHC класса I тироцитами усиливается IL-1, фактором некроза опухоли и гамма-интерфероном [89]. Этот ответ увеличивает способность цитотоксических Т-лимфоцитов опосредовать лизис.
между пациентами [88].Клетки щитовидной железы экспрессируют MHC класса II и ведут себя как антигенпрезентирующие клетки (APC). Экспрессия ICAM-1, LFA-3 и MHC класса I тироцитами усиливается IL-1, фактором некроза опухоли и гамма-интерфероном [89]. Этот ответ увеличивает способность цитотоксических Т-лимфоцитов опосредовать лизис.
Гуморальный иммунитет усугубляет клеточно-опосредованное повреждение как за счет прямой фиксации комплемента (антитела к ТПО), так и за счет ADCC [13]. Атака комплемента, инициированная классическим или альтернативным путем, нарушает метаболическую функцию клеток щитовидной железы и побуждает их секретировать IL-1, IL-6, активные метаболиты кислорода и простагландины.Все это усиливает аутоиммунный процесс [90].
24,7. Диагностика аутоиммунного заболевания щитовидной железы
Диагностика AITD основана на клинических характеристиках и подтвержденных лабораторных исследованиях. Пациент может быть эутиреоидным, гипотиреозным или гипертиреоидным, в зависимости от типа заболевания и стадии заболевания. AITD обнаруживают путем измерения циркулирующих антител против ТПО и ТГ. Отрицательный тест на оба антитела исключает AITD, так как 98% пациентов являются положительными на оба антитела.ТПО-Ab более специфичен и чувствителен, чем TG-Ab, в диагностике аутоиммунного гипотиреоза. Повышенный уровень ТТГ с антителами к ТПО — золотой стандарт диагностики хронического тиреоидита Хашимото. ТТГ-абс, стимулирующий ТТГ-Р при болезни Грейвса, измеряется для прогнозирования неонатального тиреотоксикоза. Их можно измерить с помощью анализов рецепторов щитовидной железы или биоанализов.
AITD обнаруживают путем измерения циркулирующих антител против ТПО и ТГ. Отрицательный тест на оба антитела исключает AITD, так как 98% пациентов являются положительными на оба антитела.ТПО-Ab более специфичен и чувствителен, чем TG-Ab, в диагностике аутоиммунного гипотиреоза. Повышенный уровень ТТГ с антителами к ТПО — золотой стандарт диагностики хронического тиреоидита Хашимото. ТТГ-абс, стимулирующий ТТГ-Р при болезни Грейвса, измеряется для прогнозирования неонатального тиреотоксикоза. Их можно измерить с помощью анализов рецепторов щитовидной железы или биоанализов.
24,8. Аутоиммунное заболевание щитовидной железы и новообразования
Тиреоидит и антитела к щитовидной железе обнаруживаются у четверти или трети пациентов с раком щитовидной железы [91].Существовавший ранее тиреоидит Хашимото является основным фактором риска развития неходжкинской лимфомы щитовидной железы [92]. Исследования также показали, что у женщин с раком груди повышается частота аутоиммунного тиреоидита [93].
24,9. Аутоиммунные заболевания щитовидной железы и почек
У пациентов с заболеваниями почек были зарегистрированы эндокринные нарушения [94]. Дисфункция щитовидной железы вызывает заметные изменения в функции клубочков и канальцев, а также в гомеостазе электролитов и воды [95].С точки зрения клинической практики следует отметить, что и гипотиреоз, и гипертиреоз сопровождаются значительными изменениями метаболизма воды и электролитов, а также сердечно-сосудистой функции [96].
25. Заключение
Аутоиммунное заболевание щитовидной железы возникает в результате сложного взаимодействия генетических факторов и факторов окружающей среды. Заболевание возникает из-за выхода из толерантности аутореактивных лимфоцитов. И клеточно-опосредованные, и гуморальные реакции способствуют повреждению тканей при аутоиммунном заболевании щитовидной железы.Диагностика AITD основана на клинических характеристиках и подтвержденных лабораторных исследованиях. AITD был связан с новообразованиями и заболеваниями почек.
Выражение признательности
Авторы хотели бы поблагодарить всех сотрудников отделения патологии, преподавания Мои и специализированной больницы за их помощь при написании этого обзора.
Болезнь Грейвса — NORD (Национальная организация по редким заболеваниям)
СТАТЬИ В ЖУРНАЛЕ
Lee NJ, Li CW, Hammerstad SS, Stefan M, Tomer Y.Иммуногенетика аутоиммунных заболеваний щитовидной железы: всесторонний обзор. J Autoimmun. 2015; 64: 82-90. http://www.ncbi.nlm.nih.gov/pubmed/26235382
Томер Ю. Механизмы аутоиммунных заболеваний щитовидной железы: от генетики к эпигенетике. Анну Рев Патол. 2014; 9: 147-196. http://www.ncbi.nlm.nih.gov/pubmed/24460189
Rivkees SA. Детская болезнь Грейвса: лечение в эпоху постпрофилтиоурацила. Int J Pediatr Endocrinol. 2014; 2014: 10. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4118280/
Барталена Л., Фатуречи В.Экстратироидные проявления болезни Грейвса: обновление 2014 г. J Endocrinol Invest. 2014; 37: 691-700. http://www.ncbi.nlm.nih.gov/pubmed/24913238
2014; 37: 691-700. http://www.ncbi.nlm.nih.gov/pubmed/24913238
Dong YH, Fu DG. Аутоиммунное заболевание щитовидной железы: механизм, генетика и современные знания. Eur Rev Med Pharamcol Sci. 2014; 18: 3611-3618. http://www.ncbi.nlm.nih.gov/pubmed/25535130
Lee HS, Hwang JS. Лечение болезни Грейвса у детей и подростков. Ann Pediatr Endocrinol Metab. 2014; 19: 122-126. http: //www.ncbi.nlm.nih.gov / pmc / article / PMC4208256 / # B11
Bahn Chair RS, Burch HB, Cooper DS и др. Гипертиреоз и другие причины тиреотоксикоза: рекомендации по лечению Американской ассоциации щитовидной железы и Американской ассоциации клинических эндокринологов. Щитовидная железа. 2011; 21: 593-646. http://www.ncbi.nlm.nih.gov/pubmed/21510801
Girgis CM, Champion BL, Wall JR. Современные концепции болезни Грейвса. Ther Adv Endocrinol Metab. 2011; 2: 135-144. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3474632/#bibr11-2042018811408488
Huber A, Menconi F, Corathers S, Jacobson EM, Tomer Y. Совместная генетическая предрасположенность к диабету 1 типа и аутоиммунному тиреоидиту: от эпидемиологии к механизмам. Endocr Rev.2008; 29: 697-725. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2583387/
Совместная генетическая предрасположенность к диабету 1 типа и аутоиммунному тиреоидиту: от эпидемиологии к механизмам. Endocr Rev.2008; 29: 697-725. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2583387/
Jacobson EM, Tomer Y. CD40, CTLA-4, тиреоглобулин, рецептор ТТГ и квинтет гена PTPN22 и его вклад в аутоиммунитет щитовидной железы : назад в будущее. J Аутоиммунный. 2007; 28: 85-98. http://www.ncbi.nlm.nih.gov/pubmed/17369021/
Barrio R, Lopez-Capape M, Martinez-Badas, et al. Болезнь Грейвса у детей и подростков: ответ на длительное лечение.Acta Pediatr. 2005; 94: 1583-1589. http://www.ncbi.nlm.nih.gov/pubmed/16303698
Nebesio TD, Siddiqui AR, Pescovitz OH, Eugster EA. Время до гипотиреоза после радиоабляционной терапии фиксированной дозой болезни Грейвса у детей. J Pediatr. 2002; 141: 99-103. http://www.ncbi.nlm.nih.gov/pubmed/12091858
Allahabadia A, Daykin J, Holder RL. Возраст и пол позволяют прогнозировать исход лечения гипертиреоза Грейвса. J Clin Endocrinol Metab. 2000; 85: 1038-42. http: //www.ncbi.nlm.nih.gov/pubmed/10720036
2000; 85: 1038-42. http: //www.ncbi.nlm.nih.gov/pubmed/10720036
Барталена Л., Пинчера А., Маркоччи К. Лечение офтальмопатии Грейвса: реальность и перспективы. Endocr Rev.2000; 21: 168-99. http://www.ncbi.nlm.nih.gov/pubmed/10782363
ИНТЕРНЕТ
Американская тироидная ассоциация. Гипертиреоз. Доступно на http://www.thyroid.org/what-is-hyperthyroidism
American Thyroid Association. Гипертиреоз. Болезнь Грейвса. Доступно по адресу: http://www.thyroid.org/what-is-graves-disease
Клиника Мейо для медицинского образования и исследований.Болезнь Грейвса. 1 июля 2014 г. Доступно по адресу: http://www.mayoclinic.org/diseases-conditions/graves-disease/basics/definition/con-20025811 Дата доступа: 8 ноября 2015 г.
Национальный институт диабета и пищеварения и Заболевания почек. Болезнь Грейвса. Август 2012 г. Доступно по адресу: http://www.niddk.nih.gov/health-information/health-topics/endocrine/graves-disease/Pages/fact-sheet.aspx Дата доступа: 8 ноября 2015 г.
Дэвис TF. Лечение орбитопатии Грейва (офтальмопатии).UpToDate, Inc., 2014 г. 11 июня. Доступно по адресу: http://www.uptodate.com/contents/treatment-of-graves-orbitopathy-ophthalmopathy Дата доступа: 8 ноября 2015 г.
Davies TF. Патогенез и клинические особенности офтальмопатии Грейва (орбитопатии). UpToDate, Inc., 2013 г. 13 ноября. Доступно по адресу: http://www.uptodate.com/contents/pathogenesis-and-clinical-features-of-graves-ophthalmopathy-orbitopathy Дата обращения: 8 ноября 2015 г.
LaFranchi S • Лечение и прогноз болезни Грейвса у детей и подростков.UpToDate, Inc., 2014 10 января. Доступно по адресу: http://www.uptodate.com/contents/treatment-and-prognosis-of-graves-disease-in-children-and-adolescents Дата обращения: 8 ноября 2015 г.
Границы | Аутоиммунитет и функция щитовидной железы после лечения биологическими противоревматическими средствами при ревматоидном артрите
Введение
Аутоиммунные заболевания щитовидной железы являются наиболее распространенными аутоиммунными заболеваниями и часто связаны с наличием других органоспецифических или неспецифических аутоиммунных заболеваний (1). Сосуществование аутоиммунитета щитовидной железы и ревматоидного артрита было признано уже более века (2). Популяционные исследования подтвердили повышенную распространенность аутоиммунного заболевания щитовидной железы у пациентов с ревматоидным артритом и, наоборот, повышенную распространенность ревматоидного артрита у пациентов с аутоиммунным заболеванием щитовидной железы (3, 4). Boelaert et al. (5) попросили 3286 пациентов с щитовидной железой сообщать о других аутоиммунных диагнозах между собой и своими родственниками. Ревматоидный артрит был наиболее распространенным сопутствующим аутоиммунным заболеванием, встречающимся у 3 пациентов.15% пациентов с болезнью Грейвса и 4,24% пациентов с тиреоидитом Хашимото (5). Аналогичным образом Fallahi et al. (6) обнаружили 2,4% распространенность ревматоидного артрита у 3069 пациентов с подтвержденным аутоиммунным тиреоидитом, что было значительно выше, чем у пациентов с многоузловым зобом и у здоровых по щитовидной железе контрольной группы того же возраста и пола ( p <0,0001).
Сосуществование аутоиммунитета щитовидной железы и ревматоидного артрита было признано уже более века (2). Популяционные исследования подтвердили повышенную распространенность аутоиммунного заболевания щитовидной железы у пациентов с ревматоидным артритом и, наоборот, повышенную распространенность ревматоидного артрита у пациентов с аутоиммунным заболеванием щитовидной железы (3, 4). Boelaert et al. (5) попросили 3286 пациентов с щитовидной железой сообщать о других аутоиммунных диагнозах между собой и своими родственниками. Ревматоидный артрит был наиболее распространенным сопутствующим аутоиммунным заболеванием, встречающимся у 3 пациентов.15% пациентов с болезнью Грейвса и 4,24% пациентов с тиреоидитом Хашимото (5). Аналогичным образом Fallahi et al. (6) обнаружили 2,4% распространенность ревматоидного артрита у 3069 пациентов с подтвержденным аутоиммунным тиреоидитом, что было значительно выше, чем у пациентов с многоузловым зобом и у здоровых по щитовидной железе контрольной группы того же возраста и пола ( p <0,0001). В недавнем метаанализе (7) пациенты с ревматоидным артритом имели в три раза более высокий риск наличия аутоантител к щитовидной железе, чем здоровые люди контрольной группы [аутоантитела к тиреоглобулину (TgAb): OR 3.17 (2.24–4.49) и аутоантитела к тиреоглобулину (TPOAb): OR 2.33 (1.24–4.39)].
В недавнем метаанализе (7) пациенты с ревматоидным артритом имели в три раза более высокий риск наличия аутоантител к щитовидной железе, чем здоровые люди контрольной группы [аутоантитела к тиреоглобулину (TgAb): OR 3.17 (2.24–4.49) и аутоантитела к тиреоглобулину (TPOAb): OR 2.33 (1.24–4.39)].
Хотя связь между аутоиммунитетом щитовидной железы и ревматоидным артритом была продемонстрирована, причинно-следственная связь еще не установлена. Тем не менее, растет понимание возможного общего патогенеза аутоиммунных заболеваний, потенциально вызванных основным иммунологическим нарушением, приводящим к нарушению самотолерантности (8). Обычно считается, что как аутоиммунное заболевание щитовидной железы, так и ревматоидный артрит возникают в результате множества факторов (генетической предрасположенности, эндогенных факторов и факторов окружающей среды) (1, 9, 10).Нарушение регуляции Т- и В-клеток, вызывающее реакции против аутоантигенов, вовлечено как в условия с выработкой антител при ревматоидном артрите (ревматоидный фактор и антициклический цитруллинированный пептид), так и в аутоиммунитет щитовидной железы (тиреоидная пероксидаза, тиреоглобулин и антитела к рецепторам тиреотропного гормона) (1 ). Такая регуляция Т- и В-клеток очень сложна, но связана с экспрессией различных цитокинов. Как продукция цитокинов, так и функция В-клеток являются одними из целей новых биологических противоревматических агентов (БАД), которые все чаще используются при лечении ревматоидного артрита (11, 12).Текущие руководящие принципы обычно рекомендуют лечение БАД при недостаточном ответе на лечение обычными противоревматическими препаратами, модифицирующими заболевание, или при наличии неблагоприятных прогностических маркеров (аутоантитела, высокая активность заболевания, ранние эрозии и неэффективность двух обычных противоревматических препаратов, модифицирующих заболевание). (11, 12). Хотя существует возрастающее количество противоревматических агентов, наиболее часто при лечении ревматоидного артрита используется группа ингибиторов фактора некроза опухоли-α (TNF-α).Этот провоспалительный цитокин играет жизненно важную роль в иммунологической активации, связанной с аутоиммунными воспалительными паттернами при ревматоидном артрите.
Такая регуляция Т- и В-клеток очень сложна, но связана с экспрессией различных цитокинов. Как продукция цитокинов, так и функция В-клеток являются одними из целей новых биологических противоревматических агентов (БАД), которые все чаще используются при лечении ревматоидного артрита (11, 12).Текущие руководящие принципы обычно рекомендуют лечение БАД при недостаточном ответе на лечение обычными противоревматическими препаратами, модифицирующими заболевание, или при наличии неблагоприятных прогностических маркеров (аутоантитела, высокая активность заболевания, ранние эрозии и неэффективность двух обычных противоревматических препаратов, модифицирующих заболевание). (11, 12). Хотя существует возрастающее количество противоревматических агентов, наиболее часто при лечении ревматоидного артрита используется группа ингибиторов фактора некроза опухоли-α (TNF-α).Этот провоспалительный цитокин играет жизненно важную роль в иммунологической активации, связанной с аутоиммунными воспалительными паттернами при ревматоидном артрите. Также было показано, что экспрессия TNF-α повышается у пациентов с аутоиммунным заболеванием щитовидной железы, и, следовательно, лечение ингибиторами TNF-α может также влиять на аутоиммунный статус щитовидной железы (13). В предыдущих исследованиях более старых иммуномодулирующих агентов (например, интерферона-α) у пациентов с рассеянным склерозом и гепатитом С давно известно, что аутоиммунитет щитовидной железы развивается более чем у одной трети таких пациентов (14–16).Взаимное влияние иммунной системы при ревматоидном артрите и аутоиммунных заболеваниях щитовидной железы делает использование БАД актуальным также в области аутоиммунитета щитовидной железы. В настоящем обзоре исследуется связь между биологическим противоревматическим лечением ревматоидного артрита и поражением аутоиммунитета щитовидной железы.
Также было показано, что экспрессия TNF-α повышается у пациентов с аутоиммунным заболеванием щитовидной железы, и, следовательно, лечение ингибиторами TNF-α может также влиять на аутоиммунный статус щитовидной железы (13). В предыдущих исследованиях более старых иммуномодулирующих агентов (например, интерферона-α) у пациентов с рассеянным склерозом и гепатитом С давно известно, что аутоиммунитет щитовидной железы развивается более чем у одной трети таких пациентов (14–16).Взаимное влияние иммунной системы при ревматоидном артрите и аутоиммунных заболеваниях щитовидной железы делает использование БАД актуальным также в области аутоиммунитета щитовидной железы. В настоящем обзоре исследуется связь между биологическим противоревматическим лечением ревматоидного артрита и поражением аутоиммунитета щитовидной железы.
Методы
В марте 2017 года был проведен поиск литературы в Medline с использованием ключевых терминов «ревматоидный артрит», «щитовидная железа» и попеременно общих и коммерческих названий известных БАД. Выявленные исследования первоначально были отсортированы по названию и аннотации, а полный текст извлечен для дальнейшего изучения. Далее были проверены списки литературы включенных исследований. Для включения подходили только оригинальные исследования, оценивающие аутоиммунитет щитовидной железы во время лечения ревматоидным артритом с помощью БАД. Отчеты о случаях были включены и представлены отдельно. Все соответствующие данные были тщательно извлечены из каждой включенной статьи и независимо друг от друга рассчитаны двумя авторами (Софи Блиддал и Стина Виллемоэс Борресен).Извлеченные данные включали: первого автора, год публикации, количество пациентов, исследуемый БАД, другие лекарства пациентов, последующее наблюдение, метод и пороговое значение, использованные для выявления антител к щитовидной железе, известное аутоиммунное заболевание щитовидной железы и статус щитовидной железы, включая аутоиммунные заболевания до и. после лечения БАД. Любые разногласия разрешались консенсусом.
Выявленные исследования первоначально были отсортированы по названию и аннотации, а полный текст извлечен для дальнейшего изучения. Далее были проверены списки литературы включенных исследований. Для включения подходили только оригинальные исследования, оценивающие аутоиммунитет щитовидной железы во время лечения ревматоидным артритом с помощью БАД. Отчеты о случаях были включены и представлены отдельно. Все соответствующие данные были тщательно извлечены из каждой включенной статьи и независимо друг от друга рассчитаны двумя авторами (Софи Блиддал и Стина Виллемоэс Борресен).Извлеченные данные включали: первого автора, год публикации, количество пациентов, исследуемый БАД, другие лекарства пациентов, последующее наблюдение, метод и пороговое значение, использованные для выявления антител к щитовидной железе, известное аутоиммунное заболевание щитовидной железы и статус щитовидной железы, включая аутоиммунные заболевания до и. после лечения БАД. Любые разногласия разрешались консенсусом. В некоторых исследованиях доля пациентов с положительными антителами к щитовидной железе напрямую не сообщалась, но могла быть рассчитана на основе данных исследования.
В некоторых исследованиях доля пациентов с положительными антителами к щитовидной железе напрямую не сообщалась, но могла быть рассчитана на основе данных исследования.
Результаты
Характеристики исследования
Всего найдено 14 релевантных статей.После тщательного изучения пять статей не соответствовали критериям включения или имели недостаточные отчеты об исходах по статусу щитовидной железы, в результате остались шесть включенных статей (17–22), всего 311 пациентов, и три были описаниями случаев (23–25). Исследования включали пять проспективных когортных исследований пациентов с ревматоидным артритом, ранее не получавших БАД (17–20, 22), и одно поперечное исследование пациентов с ревматоидным артритом, получавших лечение БАД (таблица 1) (21). Ингибиторы TNF-α адалимумаб (ADM), инфликсимаб (INX) и этанерцепт (ETC) использовались в трех (17, 21, 22), четырех (18–21) и двух (18, 21) исследованиях соответственно.Моноклональное антитело к CD20 ритуксимаб (RIX) использовалось в двух исследованиях (20, 21). Одно из них было перекрестным исследованием (21), а другое не стратифицировало результаты пациентов, получавших RIX, от результатов пациентов, получавших ингибитор TNF-α INX (20). Одно исследование (20) исключало пациентов с ранее известным заболеванием щитовидной железы, три исследования (17, 21, 22) и два исследования (18, 19) не сообщали, исключили ли они этих пациентов. Во всех шести исследованиях сообщалось о количестве пациентов с TPOAb, а в трех исследованиях (17, 20, 21) сообщалось о положительном результате TgAb.Кроме того, два исследования (20, 22) сообщили об уровнях TPOAb, а одно исследование (20) сообщило об уровнях TgAb. В двух исследованиях (20, 22) сообщалось о средних уровнях ТТГ и свободного тироксина (FT4).
Одно из них было перекрестным исследованием (21), а другое не стратифицировало результаты пациентов, получавших RIX, от результатов пациентов, получавших ингибитор TNF-α INX (20). Одно исследование (20) исключало пациентов с ранее известным заболеванием щитовидной железы, три исследования (17, 21, 22) и два исследования (18, 19) не сообщали, исключили ли они этих пациентов. Во всех шести исследованиях сообщалось о количестве пациентов с TPOAb, а в трех исследованиях (17, 20, 21) сообщалось о положительном результате TgAb.Кроме того, два исследования (20, 22) сообщили об уровнях TPOAb, а одно исследование (20) сообщило об уровнях TgAb. В двух исследованиях (20, 22) сообщалось о средних уровнях ТТГ и свободного тироксина (FT4).
Таблица 1 . Исследования тиреоидного статуса у пациентов с ревматоидным артритом, принимающих БАД.
Аутоиммунитет щитовидной железы
Биологическое противоревматическое лечение, по-видимому, не повлияло на количество TPOAb-положительных пациентов, которое варьировало от 0 до 30% пациентов на исходном уровне и от 0 до 25% при последующем наблюдении (Рисунок 1A; Таблица 1). В двух исследованиях сообщалось, что один пациент стал положительным по ТПОАb после лечения ADM (17, 22), а количество пациентов с положительным ТПОАb не изменилось в двух исследованиях INX (19) или INX / RIX (20), соответственно. Аналогичным образом, только один TgAb-положительный пациент стал отрицательным по антителам, и ни один из них не участвовал в исследовании ADM (17) (Рисунок 1B). В исследовании Caramaschi et al. (18), шесть пациентов, получавших INX, перешли от отрицательных к положительным антителам к щитовидной железе, а четыре пациента перешли от положительных к отрицательным антителам (не было сделано различий между TPOAb и TgAb положительными).В поперечном исследовании (21) TPOAb-позитивность была обнаружена у 4/37 (11%) пациентов с анамнезом биологического противоревматического лечения, что было аналогично 3/38 (8%) пациентов, принимавших БАД. наивный. Соответствующее количество TgAb-положительных пациентов составляло 2/37 (5%) и 4/38 (11%) для пациентов, которые получали или не получали биологическое противоревматическое лечение, соответственно.
В двух исследованиях сообщалось, что один пациент стал положительным по ТПОАb после лечения ADM (17, 22), а количество пациентов с положительным ТПОАb не изменилось в двух исследованиях INX (19) или INX / RIX (20), соответственно. Аналогичным образом, только один TgAb-положительный пациент стал отрицательным по антителам, и ни один из них не участвовал в исследовании ADM (17) (Рисунок 1B). В исследовании Caramaschi et al. (18), шесть пациентов, получавших INX, перешли от отрицательных к положительным антителам к щитовидной железе, а четыре пациента перешли от положительных к отрицательным антителам (не было сделано различий между TPOAb и TgAb положительными).В поперечном исследовании (21) TPOAb-позитивность была обнаружена у 4/37 (11%) пациентов с анамнезом биологического противоревматического лечения, что было аналогично 3/38 (8%) пациентов, принимавших БАД. наивный. Соответствующее количество TgAb-положительных пациентов составляло 2/37 (5%) и 4/38 (11%) для пациентов, которые получали или не получали биологическое противоревматическое лечение, соответственно.
Рисунок 1 . Доля TPOAb-положительных (A) и TgAb-положительных (B) пациентов на исходном и последующем этапе у пациентов с ревматоидным артритом, получавших биологические противоревматические агенты (БАД).Исследования представлены по имени (номеру ссылки) автора (BAA). * У четырех пациентов на исходном уровне и шести пациентов при последующем наблюдении не было сделано различий между TPOAb-позитивностью и TgAb-позитивностью, и, таким образом, сообщенная распространенность тироидных аутоантител была включена в оба рисунка 1A, B. Сокращения: АДМ, адалимумаб; ETC, этанерцепт; INX, инфликсимаб; RIX, ритуксимаб; NA, не доступен. TgAb, аутоантитела к тиреоглобулину; TPOAb, аутоантитела к пероксидазе щитовидной железы.
Снижение или неизменность уровней антител к щитовидной железе было зарегистрировано в двух исследованиях.В Raterman et al. (22), средняя концентрация TPOAb снизилась с 267 до 201 МЕ / мл ( p = 0,048) у TPOAb-положительных пациентов после 6 месяцев лечения ADM.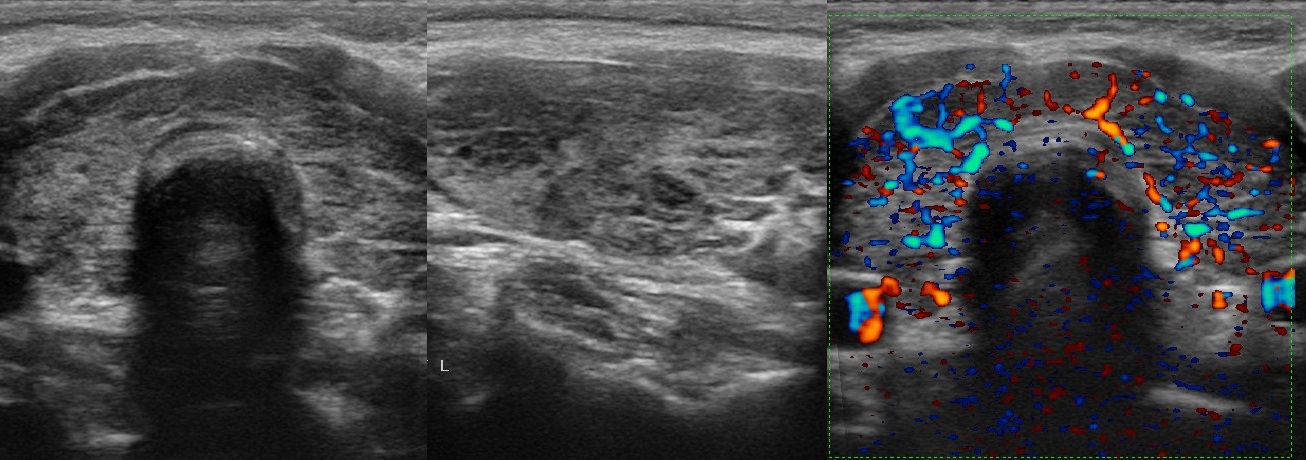 В Kaklamanos et al. (20), средняя концентрация TPOAb незначительно снизилась с 36,8 до 20,2 МЕ / мл у TPOAb-положительных пациентов после 24–40 месяцев лечения INX или RIX. Аналогичным образом, средняя концентрация TgAb не изменилась у TgAb-положительных пациентов (средний уровень TgAb 10,6–9,3 МЕ / мл) (20).
В Kaklamanos et al. (20), средняя концентрация TPOAb незначительно снизилась с 36,8 до 20,2 МЕ / мл у TPOAb-положительных пациентов после 24–40 месяцев лечения INX или RIX. Аналогичным образом, средняя концентрация TgAb не изменилась у TgAb-положительных пациентов (средний уровень TgAb 10,6–9,3 МЕ / мл) (20).
Функция щитовидной железы
В двух исследованиях изучались изменения функции щитовидной железы до и после биологической противоревматической терапии (20, 22).В Raterman et al. (22), лечение ADM привело к снижению среднего уровня ТТГ с 1,5 до 1,3 мЕд / л ( p = 0,0014) в общей группе, тогда как уровни FT4 не изменились. Снижение ТТГ было больше у (ранее) пациентов с гипотиреозом по сравнению с пациентами с эутиреоидом, но ТТГ также снизился у 8/10 пациентов с гипотиреозом, которые не получали l-тироксин. Двое из этих пациентов стали эутиреоидными после 6 месяцев лечения ADM (22). В Kaklamanos et al. (20), средний уровень ТТГ изменился с 1.7 до 1,8 МЕ / л, а FT4 изменился с 15,3 до 15,4 пмоль / л, но оба показателя незначительно.
Ящики
Наш поиск выявил три случая аутоиммунного тиреоидита у пациентов с ревматоидным артритом, получавших БАД. Два случая (23, 24) сообщили о гипертиреозе у пациентов, получавших анти-TNFα. В первом случае (23) сообщалось о преходящем гипертиреозе продолжительностью 1 месяц у пациента после 6 месяцев лечения ЭТЦ (TPOAb и TgAb отрицательные, TRAb не измерялся). Во втором сообщении (24) у 70-летней женщины развилась болезнь Грейвса после 8 лет лечения ADM.Интересно, что в одном случае сообщалось об улучшении ранее известного аутоиммунного гипотиреоза у пациента после лечения RIX (25). TPOAbs снизились до неопределяемых уровней после 6 месяцев лечения RIX, а при неизменной дозе l-тироксина у пациента стал клинически гипертиреоз со снижением ТТГ с 1,18 до 0,10 мЕд / л (25).
Обсуждение
Настоящий обзор показал, что БАД, используемые для лечения ревматоидного артрита, по-видимому, не вызывают или не усугубляют аутоиммунное заболевание щитовидной железы. Напротив, была тенденция к положительному эффекту; снижение концентраций TPOAb и TgAb и снижение уровня ТТГ у пациентов с гипотиреозом. Несмотря на небольшое количество включенных исследований с различными иммуномодулирующими агентами (в основном ингибиторы TNF-α, некоторые из RIX), исследования представили соответствующие данные.
Напротив, была тенденция к положительному эффекту; снижение концентраций TPOAb и TgAb и снижение уровня ТТГ у пациентов с гипотиреозом. Несмотря на небольшое количество включенных исследований с различными иммуномодулирующими агентами (в основном ингибиторы TNF-α, некоторые из RIX), исследования представили соответствующие данные.
Благодаря множеству иммунологических механизмов TNF-α ранее исследовался у пациентов с щитовидной железой. У пациентов с гипо- и гипертиреозом уровни TNF-α были значительно выше, чем в контрольной группе, а у пациентов с гипертиреозом успешное лечение привело к нормализации уровней TNF-α (13).Однако, как показано в случаях, описанных van Lieshout (24) и Allanore (23), гипертиреоз был диагностирован после начала терапии анти-TNF-α. Трудно оценить, может ли это быть связано с лечением или случайной находкой из-за общей предрасположенности к аутоиммунному заболеванию щитовидной железы у пациентов с ревматоидным артритом (8). Кроме того, ранее сообщалось, что аутоиммунное заболевание щитовидной железы колеблется между гипо- и гипертиреозом в зависимости от преобладающего подтипа (стимулирующих или блокирующих) антител к рецепторам тиреотропина (26). Они не измерялись в исследованиях, включенных в этот обзор. Основываясь на результатах, представленных в настоящем обзоре, изменения аутоиммунного статуса щитовидной железы при лечении анти-TNF-α кажутся незначительной проблемой и вполне могут быть омрачены потенциальной пользой такого лечения — как в отношении ревматоидного заболевания, так и, возможно, аутоиммунный статус щитовидной железы.
Они не измерялись в исследованиях, включенных в этот обзор. Основываясь на результатах, представленных в настоящем обзоре, изменения аутоиммунного статуса щитовидной железы при лечении анти-TNF-α кажутся незначительной проблемой и вполне могут быть омрачены потенциальной пользой такого лечения — как в отношении ревматоидного заболевания, так и, возможно, аутоиммунный статус щитовидной железы.
Использование RIX, моноклонального антитела к CD20, вызывающего истощение В-клеток, не привело к значительным изменениям статуса щитовидной железы или аутоиммунитета (TPOAbs / TgAbs) в исследовании Kaklamanos et al.(20). В случае Raterman et al. (25), лечение ревматоидным артритом с помощью RIX могло повлиять на сосуществующий аутоиммунный гипотиреоз, вызывая переход к (ятрогенному) состоянию гипертиреоза после нескольких месяцев лечения RIX и неизменной дозой l-тироксина. Однако в исследованиях не сообщалось об уровнях антител к рецепторам тиреотропина, и не делалось различий между заболеваниями щитовидной железы (болезнь Хашимото и болезнь Грейвса). При болезни Грейвса, осложненной орбитопатией средней / тяжелой степени, лечение RIX показало многообещающие результаты (27, 28).
При болезни Грейвса, осложненной орбитопатией средней / тяжелой степени, лечение RIX показало многообещающие результаты (27, 28).
В отличие от известных побочных эффектов со стороны щитовидной железы иммуномодулирующих средств, используемых при гепатите С и лечении рака, иммуномодулирующие средства (анти-TNF-α и RIX), используемые при лечении ревматоидного артрита, не приводили к значительным изменениям функции щитовидной железы или аутоиммунитета. Однако хорошо установленная связь между ревматическими заболеваниями и аутоиммунитетом щитовидной железы требует постоянного мониторинга функции щитовидной железы у пациентов с ревматоидным артритом и , наоборот, (5, 8, 29).Наконец, рекомендуется тщательно изучать каждое новое иммуномодулирующее средство на предмет его влияния на щитовидную железу, а также на другие аутоиммунные заболевания и на каждое заболевание, которое необходимо лечить, чтобы разработать краткие рекомендации для последующего наблюдения за каждым агентом и каждым заболеванием (30).
Взносы авторов
SB и SWB являются общими первыми авторами и в равной степени внесли основной вклад в сбор и анализ данных, интерпретацию результатов и написание рукописи. Все авторы внесли значительный вклад в концепцию и дизайн исследования, интерпретацию результатов, критический и интеллектуальный пересмотр рукописи, и все они одобрили окончательный вариант рукописи для публикации.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Рецензент, научная фантастика и ведущий редактор заявили о своей общей принадлежности, а ведущий редактор заявляет, что процесс, тем не менее, соответствовал стандартам справедливой и объективной проверки.
Финансирование
Заработная плата SB финансировалась за счет неограниченного гранта Исследовательского фонда больницы Копенгагенского университета, Rigshospitalet, и фонда Musikforlaeggerne Agnes и Knut Mørks. Заработная плата SWB финансировалась за счет неограниченного гранта исследовательского фонда больницы Копенгагенского университета, Rigshospitalet. Заработная плата UF-R частично финансировалась за счет неограниченного гранта фонда Novo Nordic Foundation.
Заработная плата SWB финансировалась за счет неограниченного гранта исследовательского фонда больницы Копенгагенского университета, Rigshospitalet. Заработная плата UF-R частично финансировалась за счет неограниченного гранта фонда Novo Nordic Foundation.
Список литературы
2. Джонс Р.Л. Болезнь Грейвса в сочетании с ревматоидным артритом. Br Med J (1903) 1: 1015–7. DOI: 10.1136 / bmj.1.2209.1015
CrossRef Полный текст | Google Scholar
3. Somers EC, Thomas SL, Smeeth L, Hall AJ.Подвержены ли люди с аутоиммунным заболеванием более высокому риску второго аутоиммунного расстройства? Am J Epidemiol (2009) 169: 749–55. DOI: 10.1093 / aje / kwn408
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Bengtsson C, Padyukov L, Kallberg H, Saevarsdottir S. Замена тироксина и риск развития ревматоидного артрита; результаты шведского популяционного исследования EIRA. Ann Rheum Dis (2014) 73: 1096–100. DOI: 10.1136 / annrheumdis-2013-203354
DOI: 10.1136 / annrheumdis-2013-203354
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5.Boelaert K, Newby PR, Simmonds MJ, Holder RL, Carr-Smith JD, Heward JM и др. Распространенность и относительный риск других аутоиммунных заболеваний у субъектов с аутоиммунным заболеванием щитовидной железы. Am J Med (2010) 123: 183–9. DOI: 10.1016 / j.amjmed.2009.06.030
PubMed Аннотация | CrossRef Полный текст | Google Scholar
6. Фаллахи П., Феррари С.М., Руффилли И., Элиа Дж., Бирикотти М., Вита Р. и др. Ассоциация других аутоиммунных заболеваний у пациентов с аутоиммунным тиреоидитом: обзор литературы и отчет большой серии пациентов. Аутоиммунная версия (2016) 15: 1125–8. DOI: 10.1016 / j.autrev.2016.09.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Pan XF, Gu JQ, Shan ZY. Повышенный риск аутоиммунитета щитовидной железы при ревматоидном артрите: систематический обзор и метаанализ. Эндокринная (2015) 50: 79–86. DOI: 10.1007 / s12020-015-0533-x
DOI: 10.1007 / s12020-015-0533-x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Рохас-Вильяррага А, Амайя-Амайя Дж, Родригес-Родригес А, Мантилья Р.Д., Анайа Дж. М..Представляем полиаутоиммунитет: вторичных аутоиммунных заболеваний больше не существует. Autoimmune Dis (2012) 2012: 254319. DOI: 10.1155 / 2012/254319
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Макиннес И.Б., Шетт Г. Патогенез ревматоидного артрита. N Engl J Med (2011) 365: 2205–19. DOI: 10.1056 / NEJMra1004965
CrossRef Полный текст | Google Scholar
11. Сингх Дж. А., Сааг К. Г., Бриджес С. Л. мл., Акл Э. А., Баннуру Р. Р., Салливан М. С. и др.Руководство Американского колледжа ревматологии по лечению ревматоидного артрита, 2015 г. Arthritis Rheumatol (2016) 68: 1–26. DOI: 10.1002 / art.39480
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12. Смолен Дж. С., Ландеве Р., Бийлсма Дж. , Бурместер Дж., Чатзидионисиу К., Дугадос М. и др. Рекомендации EULAR по лечению ревматоидного артрита с помощью синтетических и биологических противоревматических препаратов, модифицирующих болезнь: обновление 2016 г. Ann Rheum Dis (2017) 76: 960–77.DOI: 10.1136 / annrheumdis-2016-210715
, Бурместер Дж., Чатзидионисиу К., Дугадос М. и др. Рекомендации EULAR по лечению ревматоидного артрита с помощью синтетических и биологических противоревматических препаратов, модифицирующих болезнь: обновление 2016 г. Ann Rheum Dis (2017) 76: 960–77.DOI: 10.1136 / annrheumdis-2016-210715
CrossRef Полный текст | Google Scholar
13. Diez JJ, Hernanz A, Medina S, Bayon C, Iglesias P. Сывороточные концентрации фактора некроза опухоли альфа (TNF-альфа) и растворимого рецептора TNF-альфа p55 у пациентов с гипотиреозом и гипертиреозом до и после нормализации щитовидной железы функция. Clin Endocrinol (Oxf) (2002) 57: 515–21. DOI: 10.1046 / j.1365-2265.2002.01629.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14.Coles AJ, Wing M, Smith S, Coraddu F, Greer S, Taylor C и др. Импульсное лечение моноклональными антителами и аутоиммунное заболевание щитовидной железы при рассеянном склерозе. Ланцет (1999) 354: 1691–5. DOI: 10.1016 / S0140-6736 (99) 02429-0
DOI: 10.1016 / S0140-6736 (99) 02429-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Mandac JC, Chaudhry S, Sherman KE, Tomer Y. Клинический и физиологический спектр тиреоидита, индуцированного интерфероном-альфа: к новой классификации. Гепатология (2006) 43: 661–72.DOI: 10.1002 / hep.21146
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16. Антонелли А., Ферри С., Фаллахи П. Гепатит С: дисфункция щитовидной железы у пациентов с гепатитом С на терапии IFN-альфа. Nat Rev Gastroenterol Hepatol (2009) 6: 633–5. DOI: 10.1038 / nrgastro.2009.168
CrossRef Полный текст | Google Scholar
17. Атзени Ф., Дориа А., Гирарделло А., Вильялта Д., Зампиери С., Каррабба М. и др. Органоспецифические аутоантитела у пациентов с ревматоидным артритом, получавших адалимумаб: проспективное долгосрочное наблюдение. Аутоиммунитет (2008) 41: 87–91. DOI: 10.1080 / 08916930701620050
PubMed Аннотация | CrossRef Полный текст | Google Scholar
18. Карамаски П., Биази Д., Коломбатти М., Пьеропан С., Мартинелли Н., Карлетто А. и др. Анти-TNF-альфа-терапия при ревматоидном артрите и аутоиммунных заболеваниях. Rheumatol Int (2006) 26: 209–14. DOI: 10.1007 / s00296-004-0542-1
Карамаски П., Биази Д., Коломбатти М., Пьеропан С., Мартинелли Н., Карлетто А. и др. Анти-TNF-альфа-терапия при ревматоидном артрите и аутоиммунных заболеваниях. Rheumatol Int (2006) 26: 209–14. DOI: 10.1007 / s00296-004-0542-1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19. Элькаям О., Берк М., Вардинон Н., Закут В., Ицхак Р. Б., Паран Д. и др.Профиль аутоантител у пациентов с ревматоидным артритом во время лечения инфликсимабом. Аутоиммунитет (2005) 38: 155–60. DOI: 10.1080 / 08916930400021378
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20. Какламанос М., Томас Д., Пиказис Д., Кальтсас Г. Изменения, специфичные для щитовидной железы, после лечения биологическими методами лечения у пациентов с ревматическими заболеваниями. Эндокринная (2015) 50: 146–53. DOI: 10.1007 / s12020-015-0551-8
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21.Кошарный А., Майдан М., Сушек Д. , Велош Э., Дрыглевска М. Связь между активностью ревматоидного артрита и антитиреоидными антителами. Pol Arch Med Wewn (2013) 123: 394–400.
, Велош Э., Дрыглевска М. Связь между активностью ревматоидного артрита и антитиреоидными антителами. Pol Arch Med Wewn (2013) 123: 394–400.
PubMed Аннотация | Google Scholar
22. Ратерман Х.Г., Ямницкий А., Лемс В.Ф., Воскуйл А.Е., Дийкманс Б.А., Бос У.Х. и др. Улучшение функции щитовидной железы у пациентов с гипотиреозом и ревматоидным артритом после 6 месяцев лечения адалимумабом: пилотное исследование. J Rheumatol (2011) 38: 247–51.DOI: 10.3899 / jrheum.100488
PubMed Аннотация | CrossRef Полный текст | Google Scholar
23. Алланор Ю., Бремонт С., Кахан А., Менкес С.Дж. Преходящий гипертиреоз у пациента с ревматоидным артритом, получавшего этанерцепт. Clin Exp Rheumatol (2001) 19: 356–7.
Google Scholar
24. van Lieshout AW, Creemers MC, Radstake TR, Elving LD, van Riel PL. Болезнь Грейвса у пациента с ревматоидным артритом во время лечения противоопухолевым фактором некроза-альфа. J Rheumatol (2008) 35: 938–9.
Google Scholar
25. Ратерман Х.Г., Симсек С., Лемс В.Ф., Мистерс Е.В., Дийкманс Б.А., Нурмохамед М.Т. Ритуксимаб и функция щитовидной железы. Arch Intern Med (2009) 169: 1073–4. DOI: 10.1001 / archinternmed.2009.116
CrossRef Полный текст | Google Scholar
26. DeGroot LJ. Диагностика и лечение заболеваний липидного и липопротеидного обмена. В: De Groot LJ, Chrousos G, Dungan K, Feingold KR, Grossman A, Hershman JM, et al., редакторы. Endotext , [Интернет]. Южный Дартмут, Массачусетс: MDText.com, Inc. (2016).
Google Scholar
28. Салви М., Ваннуччи Г., Курро Н., Кампи И., Ковелли Д., Дацци Д. и др. Эффективность таргетной терапии В-клеток ритуксимабом у пациентов с активной орбитопатией Грейвса от умеренной до тяжелой: рандомизированное контролируемое исследование. J Clin Endocrinol Metab (2015) 100: 422–31. DOI: 10.1210 / jc.2014-3014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29. Накамура Х., Сша Т., Мотомура М., Итикава Т., Накао К., Кавасаки Е. и др. Распространенность взаимосвязанных аутоантител при заболеваниях щитовидной железы и аутоиммунных нарушениях. J Endocrinol Invest (2008) 31: 861–5. DOI: 10.1007 / BF03346432
Накамура Х., Сша Т., Мотомура М., Итикава Т., Накао К., Кавасаки Е. и др. Распространенность взаимосвязанных аутоантител при заболеваниях щитовидной железы и аутоиммунных нарушениях. J Endocrinol Invest (2008) 31: 861–5. DOI: 10.1007 / BF03346432
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30. Feldt-Rasmussen U. Повышенный риск аутоиммунитета щитовидной железы при ревматоидном артрите. Эндокринная (2015) 50: 4–5. DOI: 10.1007 / s12020-015-0671-1
CrossRef Полный текст | Google Scholar
Аутоиммунные заболевания щитовидной железы — симптомы, причины, лечение
Аутоиммунные заболевания щитовидной железы, такие как аутоиммунный тиреоидит, также известный как тиреоидит Хашимото или хронический лимфоцитарный тиреоидит, — это состояния, при которых иммунная система атакует собственную щитовидную железу организма.Щитовидная железа, представляющая собой небольшую железу в передней части шеи, хронически воспаляется и снижает выработку гормонов щитовидной железы трийодтиронина и тироксина. Поскольку эти гормоны используются почти повсюду в организме, аутоиммунные заболевания щитовидной железы могут иметь серьезные серьезные последствия и множество симптомов.
Поскольку эти гормоны используются почти повсюду в организме, аутоиммунные заболевания щитовидной железы могут иметь серьезные серьезные последствия и множество симптомов.
Аутоиммунные заболевания щитовидной железы обычно имеют наследственное происхождение, хотя факторы окружающей среды, такие как инфекция, некоторые лекарства и потребление йода, могут играть роль в их прогрессировании.Аутоиммунный тиреоидит чаще встречается у женщин, чем у мужчин, и в первую очередь поражает людей в возрасте от 40 до 60 лет. Как и при многих аутоиммунных заболеваниях, ваши шансы заболеть аутоиммунным тиреоидитом увеличиваются, если у вас есть другие аутоиммунные заболевания.
Часто легкий аутоиммунный тиреоидит протекает бессимптомно. Однако в более серьезных случаях воспаление щитовидной железы может привести к увеличению (зобу). Со временем щитовидная железа может подвергнуться большему повреждению, что приведет к появлению симптомов гипотиреоза (недостаточной активности щитовидной железы), таких как усталость, увеличение веса, боли в теле, депрессия и летаргия.
Аутоиммунный тиреоидит не всегда требует лечения. Для тех, кто испытывает проблемные симптомы, лечение обычно проводится с помощью синтетических гормонов щитовидной железы. Как правило, заболевание медленно прогрессирует и может оставаться стабильным в течение многих лет без осложнений.
Хотя хронические аутоиммунные заболевания щитовидной железы обычно протекают в легкой форме или даже бессимптомно, они могут прогрессировать до выраженного гипотиреоза. Немедленно обратитесь за медицинской помощью при тревожных симптомах гипотиреоза, таких как депрессия или необъяснимое увеличение веса.
Аутоиммунный тиреоидит — обзор
Хашимото или аутоиммунный тиреоидит
Аутоиммунный тиреоидит с увеличением щитовидной железы является одним из наиболее частых проявлений детского заболевания щитовидной железы. 43 , 51 Он связан с антителами против тиреоглобулина и тиреопероксидазы и характеризуется лимфоцитарной инфильтрацией щитовидной железы, что приводит к тиромегалии. 43 , 51 В зависимости от природы антитиреоидных антител болезнь Хашимото может быть связана с эутиреоидным состоянием, гипотиреозом или преходящим гипертиреозом. 43 , 51 Повреждение щитовидной железы отражает как опосредованное антителами, так и клеточно-опосредованное повреждение.
43 , 51 В зависимости от природы антитиреоидных антител болезнь Хашимото может быть связана с эутиреоидным состоянием, гипотиреозом или преходящим гипертиреозом. 43 , 51 Повреждение щитовидной железы отражает как опосредованное антителами, так и клеточно-опосредованное повреждение.
Тиреоидит Хашимото может редко встречаться у младенцев 52 , но обычно проявляется у подростков, поражая женщин в три-пять раз чаще, чем мужчин. 43 Щитовидная железа обычно диффузно увеличена и при пальпации может казаться неравномерной, булыжной. Может быть отмечено асимметричное увеличение щитовидной железы, напоминающее узелок щитовидной железы.Наличие антитиреоидных антител и отсутствие узелков на УЗИ позволяет отличить воспаление от других патологических процессов.
Важно отметить, что наличие антитиреоидных антител не предвещает развития полной или частичной недостаточности щитовидной железы, требующей лечения.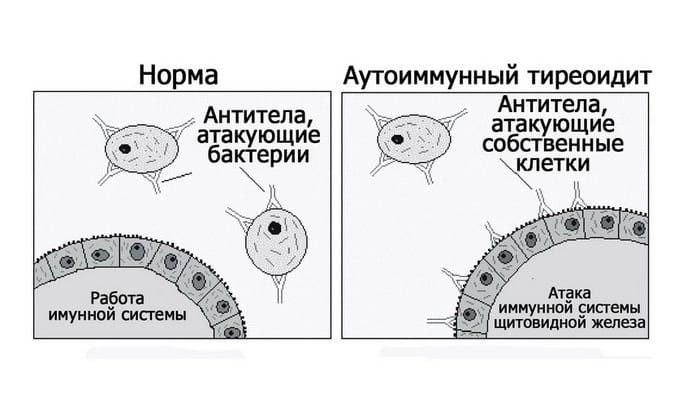 Среди здорового взрослого населения до 5% людей имели циркулирующие антитиреоидные антитела. 53 Менее 10% этих людей (т.е. только 0,5% людей с антителами) разовьется гипотиреоз, а те, у кого повышен уровень антител к тиропероксидазе (TOP), подвержены гораздо большему риску, чем те, у кого есть антитела к тиреоглобулину (TG). 53
Среди здорового взрослого населения до 5% людей имели циркулирующие антитиреоидные антитела. 53 Менее 10% этих людей (т.е. только 0,5% людей с антителами) разовьется гипотиреоз, а те, у кого повышен уровень антител к тиропероксидазе (TOP), подвержены гораздо большему риску, чем те, у кого есть антитела к тиреоглобулину (TG). 53
У детей заболеваемость антитиреоидными антителами в популяции не определена. Сообщается, что примерно у 20% детей с антитиреоидными антителами развивается гипотиреоз, требующий лечения экзогенным гормоном щитовидной железы, 54 , 55 , и у этих детей часто очень высокие титры антитиреоидных антител. Если у ребенка обнаруживается низкая концентрация антитиреоидных антител, целесообразно оценивать индексы щитовидной железы каждые 6–12 месяцев и начинать терапию, когда ТТГ поднимается выше верхней границы нормы для детей.Если при представлении присутствуют высокие титры, целесообразно начать терапию именно в это время.
У некоторых детей нелеченый тиреоидит Хашимото может привести к прогрессирующей тиреомегалии и гипотиреозу. 43 Лечение левотироксином предотвращает гипотиреоз и повышение уровня ТТГ, которое стимулирует увеличение желез. Когда уровень Т4 умеренно снижен (<5 мкг / дл) или нормален, лечение можно начать с 1-2 мкг / кг / день левотироксина. Если присутствует выраженный гипотиреоз, при лечении детей обычными дозами может развиться псевдоопухоль мозга. 56 Таким образом, лечение начинают с одной трети до половины обычной дозы левотироксина. Через 2–4 недели пациенту можно вводить обычные дозы. Однако у детей с выраженным гипотиреозом может развиться псевдоопухоль головного мозга, даже если лечение начато с низких доз левотироксина. 57-59
Сообщалось, что у некоторых детей с глубоким повышением ТТГ (> 250 мМЕ / мл) и детей с тяжелым гипотиреозом может наблюдаться полное спонтанное разрешение гипотиреоза без лечения, и происходит восстановление эутиреоидного состояния. 60 Судя по опыту других, это очень редко.
60 Судя по опыту других, это очень редко.
Хотя сообщалось о некоторых различиях в пероральной биодоступности различных препаратов левотироксина, 61-63 с практической точки зрения эти различия незначительны. 62-64 Таким образом, регулярное использование менее дорогих генерических соединений по сравнению с более дорогими фирменными препаратами оправдано.
Время приема левотироксина было предметом исследования.В отличие от стандартной рекомендации проводить заместительную терапию щитовидной железы натощак, прием лекарства перед сном связан с более высоким уровнем Т4 и более низким уровнем ТТГ в течение дня. 65 , 66 Считается, что это связано с лучшим желудочно-кишечным всасыванием вечером, чем днем. 65 , 66
Было также высказано предположение, что гипотиреоз у подростков можно лечить с помощью однократной еженедельной дозы. 67 Этот подход не рекомендуется, потому что уровни гормонов щитовидной железы высоки вскоре после введения дозы и становятся низкими к концу недели. 67 Лечение врожденного гипотиреоза еженедельными дозами левотироксина может привести к умственной отсталости. 68 Также известно, что чрезмерное потребление сои, таблеток железа и чрезмерное количество клетчатки могут препятствовать абсорбции левотироксина. 69-71
67 Лечение врожденного гипотиреоза еженедельными дозами левотироксина может привести к умственной отсталости. 68 Также известно, что чрезмерное потребление сои, таблеток железа и чрезмерное количество клетчатки могут препятствовать абсорбции левотироксина. 69-71
Были протестированы другие потенциальные методы лечения, которые теоретически могут изменить аутоиммунный процесс.Среди предложенных средств не наблюдалось пользы у пациентов, принимавших селен. 72
У вас гипотиреоз или болезнь Хашимото?
Щитовидная железа привлекла много внимания средств массовой информации еще в 2007 году, когда Опра Уинфри объявила, что у нее заболевание щитовидной железы, которое, по ее мнению, является причиной ее неспособности похудеть.
Проблема в том, что более 90% людей с условным диагнозом гипотиреоид на самом деле страдают чем-то еще: тиреоидитом Хашимото.Хотя болезнь Хашимото связана с гипотиреозом, на самом деле это совсем другое состояние и требует совершенно другого подхода.
Гипотиреоз — это проблема щитовидной железы; Хашимото — проблема с вашей иммунной системой. При Хашимото — как и при всех аутоиммунных заболеваниях — иммунная система сбивается с толку и по ошибке атакует часть вашего собственного тела, что-то вроде метаболического эквивалента «дружественного огня». В этом случае иммунная система атакует щитовидную железу, в конечном итоге разрушая ткань щитовидной железы и приводя к снижению уровня гормона щитовидной железы.
Почему обычные врачи часто пропускают Хашимото? Это связано со стандартным тестом на функцию щитовидной железы, анализом крови, называемым ТТГ ( тиреотропный гормон). При высоком уровне ТТГ и низком уровне гормонов щитовидной железы обычные врачи обычно прописывают синтетический гормон щитовидной железы и считают состояние излеченным.
Но тест на ТТГ не раскрывает всей истории — отнюдь нет. Когда ваша иммунная система атакует щитовидную железу, ткань щитовидной железы разрушается, и гормоны щитовидной железы могут случайно выбрасываться в кровоток. Даже если ваш уровень ТТГ может быть «нормальным», в любой момент времени у вас может быть повышенных уровней гормонов щитовидной железы () (с сопутствующими симптомами беспокойства и учащенного сердцебиения). «Я видел людей с ошибочным диагнозом биполярного расстройства, панических атак, приступов паники — все потому, что гормоны щитовидной железы действительно могут поставить вас на эмоциональные американские горки», — говорит д-р Изабелла Венц (1), автор книги «Тиреоидит Хашимото: образ жизни». Вмешательства для поиска первопричины.
Даже если ваш уровень ТТГ может быть «нормальным», в любой момент времени у вас может быть повышенных уровней гормонов щитовидной железы () (с сопутствующими симптомами беспокойства и учащенного сердцебиения). «Я видел людей с ошибочным диагнозом биполярного расстройства, панических атак, приступов паники — все потому, что гормоны щитовидной железы действительно могут поставить вас на эмоциональные американские горки», — говорит д-р Изабелла Венц (1), автор книги «Тиреоидит Хашимото: образ жизни». Вмешательства для поиска первопричины.
Все это должно указывать на важность тщательной оценки.При любом лечении аутоиммунного заболевания, такого как болезнь Хашимото, следует внимательно следить за пищевой чувствительностью, диетой, стрессом, сном, пищеварением, дефицитом питательных веществ и воспалением, которые могут в значительной степени ослабить иммунную систему.
Возьмем, к примеру, стресс. Когда вы находитесь в состоянии стресса, ваше тело вырабатывает гормон под названием кортизол , который действительно может спасти вашу жизнь в экстренной ситуации. Но у кортизола есть темная сторона. Высокий уровень кортизола напрямую ухудшает работу иммунной системы (2, 3), поэтому план лечения Хашимото всегда должен включать в себя план управления стрессорами в вашей жизни.Постоянный стресс ослабляет иммунную систему как раз в то время, когда вам нужно ее укреплять.
Но у кортизола есть темная сторона. Высокий уровень кортизола напрямую ухудшает работу иммунной системы (2, 3), поэтому план лечения Хашимото всегда должен включать в себя план управления стрессорами в вашей жизни.Постоянный стресс ослабляет иммунную систему как раз в то время, когда вам нужно ее укреплять.
Диета тоже имеет значение. В исследовании (4), опубликованном только в этом году, итальянские исследователи посадили 180 людей с избыточным весом с Хашимото либо на низкоуглеводную диету, либо на низкокалорийную диету для похудания. Спустя всего 21 день у тех, кто придерживался низкоуглеводной диеты, наблюдалось значительное снижение их антител к щитовидной железе, в то время как у тех, кто придерживался низкокалорийной диеты, их антитела к щитовидной железе выросли . В этом исследовании диета снижает количество антител к щитовидной железе на целых 40% и более.
Дефицит питательных веществ, особенно селена, может иметь большое влияние как на гормоны щитовидной железы в целом, так и на гормоны Хашимото в частности. Несколько исследований показали значительное снижение уровня антител к щитовидной железе после приема 200 мкг селена (5,6,7)
Несколько исследований показали значительное снижение уровня антител к щитовидной железе после приема 200 мкг селена (5,6,7)
Хашимото можно справиться с помощью правильного плана лечения — вашу жизнь можно вернуть на круги своя. (Просто спросите известного биохакера, предпринимателя и спортсмена Дэйва Аспери — изобретателя Bulletproof Coffee — у которого всю жизнь был Хашимото.)
Но сначала его нужно правильно идентифицировать. Поскольку врачи-натуропаты обучены выходить далеко за рамки стандартного теста на ТТГ, они обладают уникальной квалификацией для выявления и лечения сложных и многогранных состояний, таких как болезнь Хашимото.
Нужна дополнительная информация о натуропатической медицине и заболеваниях щитовидной железы? Дополнительные сведения см. В разделе «Как врач-натуропат лечит гипотиреоз»?
ССЫЛКИ
- https: //blog.bulletproof.ru / wp-content / uploads / 2015/10 / Transcript-Dr.-Izabella-Wentz-Hashimotos-Thyroiditis-The-Root-Cause-256.
 pdf
pdf - https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1361287/
- http://www.apa.org/research/action/immune.aspx
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5028075/
- https://www.ncbi.nlm.nih.gov/pubmed/17696828
- http://press.endocrine.org/doi/full/10.1210/jcem.87.4.8421
- http://joe.endocrinology-journals.org/content/190/1/151.полный
Болезнь Хашимото тиреоидит | Goop
Последнее обновление: сентябрь 2020 г.
Первоначально опубликовано: октябрь 2019 г.
Наша научно-исследовательская группа создала goop PhD для сбора наиболее важных исследований и информации по множеству тем, состояний и болезней, связанных со здоровьем. Если вы хотите, чтобы они что-то осветили, напишите нам по адресу [email protected].
Понимание Хашимото
Тиреоидит Хашимото — наиболее частая причина гипотиреоза в развитых странах.Это в десять раз чаще встречается у женщин, чем у мужчин, и особенно часто встречается у женщин в возрасте от 45 до 55 лет (McLeod & Cooper, 2012). Хашимото — это аутоиммунное заболевание, которое по сути означает, что организм начинает атаковать свои собственные клетки, а не чужеродные клетки-захватчики. Хашимото проявляется, когда иммунная система начинает воздействовать на щитовидную железу, вызывая хроническое воспаление. Со временем эти повторяющиеся атаки на щитовидную железу снижают ее способность вырабатывать гормоны и могут привести к недостаточной активности щитовидной железы.
Хашимото — это аутоиммунное заболевание, которое по сути означает, что организм начинает атаковать свои собственные клетки, а не чужеродные клетки-захватчики. Хашимото проявляется, когда иммунная система начинает воздействовать на щитовидную железу, вызывая хроническое воспаление. Со временем эти повторяющиеся атаки на щитовидную железу снижают ее способность вырабатывать гормоны и могут привести к недостаточной активности щитовидной железы.
Щитовидная железа и ее гормоны
Щитовидная железа — это железа в форме бабочки в передней части шеи. Вы можете не думать дважды о своей щитовидной железе, но она отвечает за выработку гормонов, которые регулируют обмен веществ и влияют на голод, сон и температуру тела. Заболевания щитовидной железы могут увеличивать или уменьшать выработку этих гормонов щитовидной железой. Это создает проблемы с обменом веществ, которые могут вывести из строя все наше тело и вызвать изменение веса и настроения.
Когда щитовидная железа работает должным образом, мозг вырабатывает тиреотропный гормон (ТТГ), который сигнализирует щитовидной железе о том, что она должна начать выделять гормоны. Затем внутри щитовидной железы фермент тироидпероксидаза (ТПО) синтезирует два наиболее важных гормона щитовидной железы: трийодтиронин (Т3) и тироксин (Т4). Т3 — активный гормон, а Т4 превращается в различных тканях в Т3 по мере необходимости. Если иммунная система атакует щитовидную железу, как в случае с Хашимото, тогда антитела против ТПО и другие антитиреоидные антитела будут мешать выработке гормонов щитовидной железы и нарушать тонкую систему обратной связи между мозгом и щитовидной железой.
Затем внутри щитовидной железы фермент тироидпероксидаза (ТПО) синтезирует два наиболее важных гормона щитовидной железы: трийодтиронин (Т3) и тироксин (Т4). Т3 — активный гормон, а Т4 превращается в различных тканях в Т3 по мере необходимости. Если иммунная система атакует щитовидную железу, как в случае с Хашимото, тогда антитела против ТПО и другие антитиреоидные антитела будут мешать выработке гормонов щитовидной железы и нарушать тонкую систему обратной связи между мозгом и щитовидной железой.
Основные симптомы Хашимото
Хашимото развивается медленно и может оставаться незамеченным в течение нескольких месяцев или даже лет.Симптомы включают усталость, чувствительность к холоду, запоры, бледность кожи, ломкость ногтей, выпадение волос, опухший язык, мышечные боли, депрессию и проблемы с памятью (NIH, 2017). Поскольку такие симптомы, как усталость, увеличение веса или депрессия, не обязательно являются уникальными для данного расстройства, многие люди могут не обращаться за лечением. У других может не быть распознаваемых симптомов. Если щитовидная железа в конечном итоге сильно раздувается, появляется видимая опухоль, называемая зобом.
У других может не быть распознаваемых симптомов. Если щитовидная железа в конечном итоге сильно раздувается, появляется видимая опухоль, называемая зобом.
В чем разница между гипотиреозом и гипертиреозом?
Гипотиреоз с o относится к снижению гормонов щитовидной железы и функциональности щитовидной железы.Гипертиреоз с er относится к увеличению производства гормонов щитовидной железы и гиперактивности щитовидной железы. Симптомы гипотиреоза включают усталость, запор, чувствительность к холоду и / или опухшее лицо. Симптомы гипертиреоза включают изменение аппетита, быструю потерю веса, проблемы со сном, учащенное сердцебиение, повышенное потоотделение и / или раздражительность. Наиболее частой причиной гипотиреоза в развитых странах является тиреоидит Хашимото; в слаборазвитых странах наиболее частой причиной является дефицит йода.Наиболее частой причиной гипертиреоза является аутоиммунное заболевание — болезнь Грейвса.
Возможные причины и проблемы со здоровьем
Хашимото, вероятно, вызвано взаимодействием генетики и факторов окружающей среды.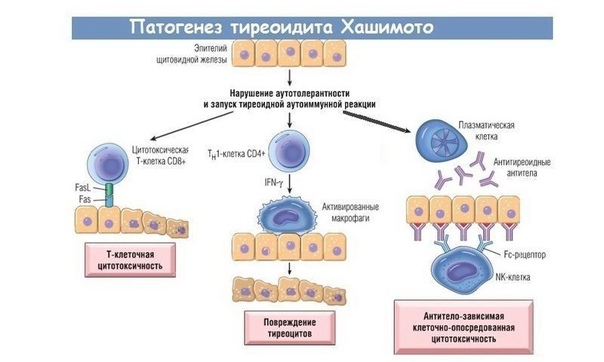 Хотя детали не совсем известны, некоторые исследователи считают, что болезнь Хашимото может быть в значительной степени вызвана инфекциями, в то время как другие считают, что проблема заключается в воздействии эндокринных разрушителей.
Хотя детали не совсем известны, некоторые исследователи считают, что болезнь Хашимото может быть в значительной степени вызвана инфекциями, в то время как другие считают, что проблема заключается в воздействии эндокринных разрушителей.
Люди с Хашимото подвержены риску высокого холестерина и других сопутствующих аутоиммунных заболеваний.
Генетика
Genetics, кажется, играет важнейшую роль в снижении риска развития Хашимото у человека. Ученые работают над объяснением того, как факторы окружающей среды могут взаимодействовать с нашими генами, вызывая аутоиммунные заболевания. Было идентифицировано более миллиона вариантов генов благодаря постоянным усилиям в рамках нескольких крупных исследований, таких как Проект 1000 геномов, в рамках которого были проанализированы геномы тысяч людей со всего мира. Ученые обнаружили, что несколько иммунорегулирующих генов связаны с Хашимото (Lee, Li, Hammerstad, Stefan, & Tomer, 2015; Tomer, 2014).И новые терапевтические препараты, нацеленные на эти гены, могут быть разработаны для лечения Хашимото и других аутоиммунных заболеваний.
Что такое эпигенетика?
Все больше исследований также начинают сосредотачиваться на эпигенетике, которая является захватывающей, растущей областью науки. Эпигенетика — это изучение биологических изменений (вызванных врожденными факторами или факторами окружающей среды, такими как курение), которые изменяют экспрессию генов: по сути, включают или выключают гены, но не изменяют саму ДНК. Такое сочетание генетической структуры и экспрессии генов делает каждого из нас уникальным.Исследования клеток и тканей пациентов с аутоиммунным заболеванием щитовидной железы показали несколько эпигенетических маркеров заболевания, но данные ограничены, и необходимы клинические исследования (B. Wang, Shao, Song, Xu, & Zhang, 2017).
Гипотеза гигиены
Было показано, что несколько аутоиммунных заболеваний связаны с количеством инфекций, перенесенных человеком в детстве (Bloomfield, Stanwell-Smith, Crevel, & Pickup, 2006). Это явление называется гигиенической гипотезой: чем больше микробов вы подвергаетесь воздействию в раннем возрасте, тем выше способность вашего организма защищать вас от определенных аллергий и иммунных состояний во взрослом возрасте. Но если бы вы были более здоровым ребенком, вы могли бы подвергаться более высокому риску определенных заболеваний во взрослом возрасте. Нет убедительных доказательств того, что это относится к Хашимото.
Но если бы вы были более здоровым ребенком, вы могли бы подвергаться более высокому риску определенных заболеваний во взрослом возрасте. Нет убедительных доказательств того, что это относится к Хашимото.
Верно и обратное: наличие определенных инфекций может вызвать воспаление щитовидной железы, вызывая развитие болезни Хашимото (Bloomfield et al., 2006; Mori & Yoshida, 2010): исследования показывают, что определенные инфекции, такие как гепатит С или Эпштейн, -Вирус Барра может вызвать у людей развитие аутоиммунных заболеваний, особенно если у них есть основная генетическая предрасположенность (Janegova, Janega, Rychly, Kuracinova, & Babal, 2015; KIVE, Agmon-Levin, Blank, & Shoenfeld, 2009; Shukla, Singh , Ahmad, & Pant, 2018).
Таким образом, кажется, что некоторые инфекции в детстве могут защитить вас от аутоиммунных заболеваний, укрепляя вашу иммунную систему (гипотеза гигиены), в то время как другие, специфические типы инфекций (например, гепатит C или Эпштейна-Барра) могут вызывать аутоиммунитет.
Разрушители эндокринной системы
Накапливается все больше и больше доказательств против фталатов, бисфенола А и парабенов, показывающих, что эти химические вещества способны нарушить гормональную систему нашего организма. Это может создать широкий спектр проблем, связанных с воспроизводством, развитием и функцией щитовидной железы.Эти химические вещества используются во многих различных продуктах, от косметики до консервов, пластиковых бутылок и детских игрушек.
Несколько исследований Джона Микера, доктора медицинских наук, CIH, и его коллег из Мичиганского университета связали фталаты, BPA и парабены с изменением ТТГ и гормонов щитовидной железы у беременных (Aker et al., 2016; Aung et al., 2017 ; Джонс, Фергюсон, МакЭлрат, Мукерджи и Микер, 2016).
Как избежать эндокринных нарушений
1.Покупайте чистые косметические продукты и бытовые чистящие средства. Избегайте продуктов, на этикетке которых указаны химические вещества, оканчивающиеся на «фталат» или «парабен», и избегайте продуктов, содержащих ароматизаторы.
 База данных Skin Deep Рабочей группы по окружающей среде позволяет искать продукты и видеть, насколько они соответствуют определенным критериям для здоровья и безопасности. У организации также есть руководство по здоровым чистящим средствам.
База данных Skin Deep Рабочей группы по окружающей среде позволяет искать продукты и видеть, насколько они соответствуют определенным критериям для здоровья и безопасности. У организации также есть руководство по здоровым чистящим средствам.2. Избегайте продуктов, содержащих пластик, особенно тех, которые могут контактировать с вашим ртом (например, бутылки с водой) или нагреваться (например, пластиковые контейнеры для пищевых продуктов).Поскольку дети часто прорезываются от игрушек, избегайте пластиковых игрушек.
3. Покупайте меньше консервов. Облицовка алюминиевых банок часто содержит заменители BPA или BPA, что может быть небезопаснее.
4. Покупайте как можно больше органических продуктов, чтобы избежать воздействия пестицидов.
5. Отфильтруйте воду, которую вы пьете.
Высокий холестерин
Одной из проблем со здоровьем, связанных с Хашимото, является высокий уровень холестерина, связанный с неблагоприятными сердечно-сосудистыми заболеваниями и событиями (NIH, 2017). Хотя большинство врачей рекомендуют статины людям с высоким уровнем холестерина, это не рекомендуется людям с гипотиреозом, принимающим гормонозаместительные препараты, поскольку эти препараты обычно уже снижают уровень холестерина.
Хотя большинство врачей рекомендуют статины людям с высоким уровнем холестерина, это не рекомендуется людям с гипотиреозом, принимающим гормонозаместительные препараты, поскольку эти препараты обычно уже снижают уровень холестерина.
Аутоиммунные заболевания
Люди с другими аутоиммунными заболеваниями, такими как целиакия, волчанка, диабет 1 типа и ревматоидный артрит, более склонны к развитию болезни Хашимото (NIH, 2017).
Как диагностируют болезнь Хашимото
Чтобы поставить диагноз Хашимото, врачи захотят изучить семейный анамнез и симптомы.Хотя точная причина Хашимото неизвестна, она, как правило, передается по наследству. Кроме того, врачи захотят провести подтверждающий анализ крови, чтобы определить уровни ТТГ, Т4, Т3 и антител к ТПО. Высокий уровень ТТГ и антител против ТПО наряду с низким уровнем гормонов щитовидной железы Т3 и Т4 соответствует уровню Хашимото.
Однако люди, которым поставлен диагноз на ранней стадии, могут показать только высокие уровни антител в анализах крови. Если вы подозреваете, что у вас может быть Хашимото, попросите своего врача сделать анализ крови, чтобы проверить, высоки ли у вас антитела к щитовидной железе, что обычно является первым признаком.Некоторые врачи могут лечить Хашимото, если высокий уровень только ТТГ, в то время как другие могут также захотеть увидеть доказательства наличия антител и нарушения уровня гормонов щитовидной железы. Это зависит от того, к какому типу специалистов вы обращаетесь и как они подходят к лечению. Нормальный уровень ТТГ обычно составляет от 0,4 до 4,9 миллиединиц на литр, но уровни зависят от используемой лабораторной техники, поэтому обязательно поговорите со своим врачом о своих результатах.
Если вы подозреваете, что у вас может быть Хашимото, попросите своего врача сделать анализ крови, чтобы проверить, высоки ли у вас антитела к щитовидной железе, что обычно является первым признаком.Некоторые врачи могут лечить Хашимото, если высокий уровень только ТТГ, в то время как другие могут также захотеть увидеть доказательства наличия антител и нарушения уровня гормонов щитовидной железы. Это зависит от того, к какому типу специалистов вы обращаетесь и как они подходят к лечению. Нормальный уровень ТТГ обычно составляет от 0,4 до 4,9 миллиединиц на литр, но уровни зависят от используемой лабораторной техники, поэтому обязательно поговорите со своим врачом о своих результатах.
За дополнительной информацией обратитесь к врачу или эндокринологу, специализирующемуся на заболеваниях щитовидной железы.Вы также можете посетить веб-сайт Американской тироидной ассоциации.
Диетические изменения
Вы можете отказаться от глютена и «зобогенных» продуктов, которые, как считается, влияют на щитовидную железу. Кетогенная диета также может быть неподходящей для людей с Хашимото.
Кетогенная диета также может быть неподходящей для людей с Хашимото.
Диета по аутоиммунному протоколу (AIP)
Для борьбы с воспалением, вызванным аутоиммунными заболеваниями, некоторые врачи функциональной медицины недавно рекомендовали ограничительную диету, называемую аутоиммунным протоколом (AIP).Эта диета исключает продукты, вызывающие воспаление, и похожа на палеодиету. Диета очень строгая: вы не ешьте зерновые, бобовые, молочные продукты, обработанные пищевые продукты, рафинированный сахар, промышленные масла из семян (канола или растительное масло), яйца, орехи и семена, пасленовые овощи, жевательную резинку, альтернативные подсластители, эмульгаторы и т. Д. загустители.
Пока не проводились адекватные клинические испытания влияния этой диеты на Хашимото (и в целом необходимы дополнительные исследования аутоиммунных диет).Пилотное исследование, проведенное в 2019 году, показало, что шестнадцать женщин с синдромом Хашимото, соблюдающие диету AIP в течение десяти недель, показали значительное улучшение качества жизни и бремени симптомов; Однако они не показали улучшения функции щитовидной железы или снижения уровня антител к щитовидной железе (Abbott, Sadowski, & Alt, 2019). Если вы хотите попробовать диету AIP, проконсультируйтесь с диетологом, чтобы убедиться, что вы получаете необходимые питательные вещества.
Если вы хотите попробовать диету AIP, проконсультируйтесь с диетологом, чтобы убедиться, что вы получаете необходимые питательные вещества.
Глютен и целиакия
Люди с глютеновой болезнью и без нее переходят на безглютеновые диеты и продукты.Целиакия — это аутоиммунное заболевание, подобное заболеванию Хашимото, при котором организм нацеливается на тонкий кишечник после употребления глютена. (См. Наш обзор целиакии и чувствительности к глютену, чтобы узнать больше.) И новое исследование показывает, что целиакия и болезнь Хашимото могут быть связаны. Пациенты с глютеновой болезнью обладают высокочувствительной иммунной системой, могут не усваивать ключевые питательные вещества (например, йод, селен и железо) и имеют много антител, которые могут влиять как на кишечник, так и на щитовидную железу (Liontiris & Mazokopakis, 2017; Roy et al., 2016; Sategna-Guidetti et al., 1998). Предварительные исследования показывают, что люди с болезнью Хашимото должны проходить обследование на целиакию и что безглютеновая диета может быть полезной при лечении симптомов (Krysiak, Szkróbka, & Okopień, 2018; Lundin & Wijmenga, 2015).
Кетогенные диеты
Кетогенные диеты стали популярными для похудания. Но они подходят не всем, и исследования показывают, что они, вероятно, не подходят людям с Хашимото. Кетогенные диеты — это диеты с низким содержанием углеводов и высоким содержанием жиров.Цель состоит в том, чтобы ваше тело переключилось из режима сжигания сахара в режим сжигания жира. Это называется кетозом. Поскольку кетогенные диеты по сути имитируют голодание, они могут быть нежелательны для людей, чьи щитовидные железы уже функционируют неоптимально, поскольку диета может еще больше нарушить их метаболизм. Несколько небольших исследований показали, что при снижении потребления углеводов снижается уровень Т3 (Bisschop, Sauerwein, Endert, & Romijn, 2001; Hendler & Bonde III, 1988; Spaulding, Chopra, Sherwin, & Lyall, 1976).Это были краткосрочные исследования людей без гипотиреоза, поэтому результаты могут быть неприменимы, но они предполагают, что углеводы могут быть важной пищевой группой для людей с Хашимото.
Гойтрогены
Гойтрогены — это продукты, которые, как считается, вызывают «зоб» — опухоль щитовидной железы — и влияют на выработку гормонов щитовидной железы. Некоторые зобогенные продукты — это соевое молоко, зеленый чай, маниока, брюква, некоторые виды проса и зеленые листовые овощи (Bajaj, Salwan, & Salwan, 2016; Chandra & De, 2013; Fort, Moses, Fasano, Goldberg, & Lifshitz, 1990; Paśko et al., 2018). Эти продукты могут вызывать проблемы у людей с дефицитом специфических для щитовидной железы питательных веществ (прочтите следующий раздел), но мало что известно о том, как они взаимодействуют с щитовидной железой и оказывает ли их устранение какое-либо влияние на Хашимото.
Питательные вещества и добавки для Хашимото
Когда дело доходит до чувствительной щитовидной железы, то, что мы едим, становится особенно важным. Правильное количество йода, селена, железа и витамина D может помочь поддерживать здоровье щитовидной железы. Однако избыток йода может быть проблематичным.
Йод
Йод — это микроэлемент, содержащийся в таких пищевых продуктах, как морепродукты, молочные продукты, продукты и обогащенные зерна (NIH, 2019a). Это жизненно важный компонент гормонов щитовидной железы, абсолютно необходимый для здоровья щитовидной железы. Дефицит йода был эпидемией в Соединенных Штатах до того, как были введены программы йодированной соли и обогащения, а дефицит йода все еще является проблемой общественного здравоохранения в других странах. Дефицит йода может вызвать серьезные проблемы, такие как гипотиреоз, и во время беременности это предотвратимая причина номер один умственной отсталости во всем мире (NIH, 2019a).Рекомендуемая суточная диета (RDA) для взрослых составляет 150 микрограммов, а для беременных и кормящих женщин — 220 и 290 микрограммов (NIH, 2019a).
В то время как дефицит йода исторически был проблемой, слишком много йода было связано с дисфункцией щитовидной железы. Это кажется нелогичным, но исследования показали, что аутоиммунный гипотиреоз и антитела к щитовидной железе могут быть более распространены в регионах с повышенным потреблением йода (Laurberg et al. , 1998). В Японии, например, где потребление йода из морских водорослей очень велико, многочисленные исследования показали высокую распространенность дисфункции щитовидной железы (Konno, Makita, Yuri, Iizuka, & Kawasaki, 1994; Michikawa et al., 2012). Кроме того, ламинария богата йодом, и было показано, что потребление добавок из ламинарии или ламинарии приводит к случаям гипертиреоза, гипотиреоза или йодной токсичности щитовидной железы (Di Matola, Zeppa, Gasperi, & Vitale, 2014; Eliason, 1998; Miyai , Tokushige, & Kondo, 2008; NIH, 2019a).
, 1998). В Японии, например, где потребление йода из морских водорослей очень велико, многочисленные исследования показали высокую распространенность дисфункции щитовидной железы (Konno, Makita, Yuri, Iizuka, & Kawasaki, 1994; Michikawa et al., 2012). Кроме того, ламинария богата йодом, и было показано, что потребление добавок из ламинарии или ламинарии приводит к случаям гипертиреоза, гипотиреоза или йодной токсичности щитовидной железы (Di Matola, Zeppa, Gasperi, & Vitale, 2014; Eliason, 1998; Miyai , Tokushige, & Kondo, 2008; NIH, 2019a).
Сколько йода слишком много?
Хотя Совет по пищевым продуктам и питанию США определил, что безопасно потреблять до 1100 микрограммов йода (NIH, 2019a), некоторые исследования показали, что даже небольшое увеличение потребления йода, даже если потребление значительно ниже порога в 1100 микрограммов, связаны с гипотиреозом (Bjergved et al., 2012; NIH, 2019a; Педерсен и др., 2011; Zhao et al., 2014). Один из предполагаемых механизмов, лежащих в основе этих результатов, заключается в том, что избыток йода может способствовать апоптозу (гибели клеток) клеток щитовидной железы (Xu et al. , 2016). Хотя средний уровень может быть нормальным для большинства людей, могут быть люди, которые более чувствительны к йоду.
, 2016). Хотя средний уровень может быть нормальным для большинства людей, могут быть люди, которые более чувствительны к йоду.
В целом, питание стремится к сбалансированности; слишком много или слишком мало питательного вещества может вызвать проблемы. Вы можете проконсультироваться с врачом, чтобы определить, является ли ваш уровень йода оптимальным и нужно ли вносить какие-либо изменения в вашу диету, чтобы увеличить или уменьшить потребление йода.Самый безопасный способ употребления добавок — умеренность. Посмотрите на этикетку и оставайтесь около 100% DV вместо 1000% DV. Вы также можете избежать закусок и добавок из ламинарии, если у вас есть Хашимото.
Селен
Селен также играет важную роль в функции щитовидной железы. Это антиоксидантное и противовоспалительное питательное вещество, которое необходимо для удаления йода из гормонов щитовидной железы, чтобы активировать и деактивировать гормоны (Liontiris & Mazokopakis, 2017; St.Жермен, Гальтон и Эрнандес, 2009).
Источники селена
Селен естественным образом присутствует во многих различных продуктах питания — хорошие источники селена включают бразильские орехи, желтоперый тунец, палтус, креветки, курицу, творог, коричневый рис и яйца (NIH, 2019b). Рекомендуемая суточная диета (RDA) для взрослых составляет 55 микрограммов и 60 микрограммов для беременных женщин (NIH, 2019b).
Два крупных поперечных исследования во Франции и Германии показали, что более высокий уровень селена был связан с меньшим зобом и меньшим повреждением тканей, но только среди женщин; мужчины не увидели этих преимуществ в исследовании (Derumeaux et al., 2003; Расмуссен и др., 2011). Добавки селена могут помочь бороться с воспалительными и иммунными реакциями, характерными для Хашимото. Несколько исследований показали, что селен может снижать уровень антител против ТПО (Fan et al., 2014; Reid, Middleton, Cossich, Crowther, & Bain, 2013; Toulis, Anastasilakis, Tzellos, Goulis, & Kouvelas, 2010; van Zuuren, Albusta , Fedorowicz, Carter, & Pijl, 2014; W. Wang et al., 2018). И исследование, опубликованное в 2019 году, показало, что четыре месяца приема селена (восемьдесят три микрограмма селенометионина в день) нормализовали уровни ТТГ в группе из двадцати пяти мужчин и женщин с Хашимото (Pirola et al., 2020). В рамках клинического исследования в Дании в настоящее время набирают пациентов, чтобы выяснить, могут ли добавки селена улучшить качество жизни людей с Хашимото; для получения дополнительной информации см. раздел клинических испытаний.
Wang et al., 2018). И исследование, опубликованное в 2019 году, показало, что четыре месяца приема селена (восемьдесят три микрограмма селенометионина в день) нормализовали уровни ТТГ в группе из двадцати пяти мужчин и женщин с Хашимото (Pirola et al., 2020). В рамках клинического исследования в Дании в настоящее время набирают пациентов, чтобы выяснить, могут ли добавки селена улучшить качество жизни людей с Хашимото; для получения дополнительной информации см. раздел клинических испытаний.
Как всегда, проконсультируйтесь с врачом по поводу диеты и любых добавок, которые вы можете принимать, если у вас есть Хашимото.
Дефицит железа
Исследования показали, что дефицит железа и проблемы со щитовидной железой иногда возникают вместе (Erdal et al., 2008; M’Rabet-Bensalah et al., 2016). Помните наш фермент щитовидной железы ТПО? ТПО необходимо достаточное количество железа для синтеза гормонов щитовидной железы. И в одном небольшом исследовании повышение уровня железа помогло с симптомами щитовидной железы (Rayman, 2018). Однако неясно, вызывает ли дефицит железа дисфункцию щитовидной железы или дисфункция щитовидной железы вызывает дефицит железа (Szczepanek-Parulska, Hernik, & Ruchała, 2017). Исследователи предполагают, что люди с Хашимото могут быть более предрасположены к дефициту железа из-за более высокой частоты других аутоиммунных заболеваний, таких как целиакия, которая приводит к плохому усвоению питательных веществ (Rayman, 2018; Roy et al., 2016; Sategna-Guidetti et al., 1998). Исследования также показали, что беременные женщины с дефицитом железа (не редкость, так как при выращивании ребенка расходуется много железа) могут иметь более высокий риск гипотиреоза (Zimmermann, Burgi, & Hurrell, 2007).
Однако неясно, вызывает ли дефицит железа дисфункцию щитовидной железы или дисфункция щитовидной железы вызывает дефицит железа (Szczepanek-Parulska, Hernik, & Ruchała, 2017). Исследователи предполагают, что люди с Хашимото могут быть более предрасположены к дефициту железа из-за более высокой частоты других аутоиммунных заболеваний, таких как целиакия, которая приводит к плохому усвоению питательных веществ (Rayman, 2018; Roy et al., 2016; Sategna-Guidetti et al., 1998). Исследования также показали, что беременные женщины с дефицитом железа (не редкость, так как при выращивании ребенка расходуется много железа) могут иметь более высокий риск гипотиреоза (Zimmermann, Burgi, & Hurrell, 2007).
В любом случае, железо — важное питательное вещество, о котором нельзя забывать. И женщины, как правило, более бедны, чем мужчины (Miller, 2014). По данным CDC, 14 процентов американских женщин имеют низкий уровень железа (CDC, 2012).
Источники железа
Продукты с высоким содержанием железа включают устрицы, белую фасоль и темный шоколад, в то время как хорошие источники железа — то есть они содержат от 10 до 19 процентов дневной нормы — включают чечевицу, шпинат, тофу, нут, помидоры, говядину, орехи кешью. , и картофель.Рекомендуемая дневная норма железа составляет 18 миллиграммов для женщин и 8 миллиграммов для мужчин, в то время как суточная суточная норма потребления железа для беременных составляет 27 миллиграммов. Поскольку у многих людей мало железа, особенно у женщин, вы можете захотеть принимать добавки.
, и картофель.Рекомендуемая дневная норма железа составляет 18 миллиграммов для женщин и 8 миллиграммов для мужчин, в то время как суточная суточная норма потребления железа для беременных составляет 27 миллиграммов. Поскольку у многих людей мало железа, особенно у женщин, вы можете захотеть принимать добавки.
Внимание вегетарианцам: поскольку железо из растительной пищи менее биодоступно, людям, которые не едят мясо, рекомендуется есть почти в два раза больше железа (NIH, 2018).
Витамин D
Хотя вы, возможно, знаете, что витамин D полезен для ваших костей, вы можете не знать, что он также регулирует нашу иммунную систему.И недавние исследования показывают, что он может играть роль в развитии нескольких аутоиммунных заболеваний (Yang, Leung, Adamopoulos, & Gershwin, 2013).
Исследование, проведенное в Европе, показало, что дефицит витамина D чаще встречается у людей с аутоиммунными заболеваниями щитовидной железы, а низкий уровень витамина D связан с большим количеством антител и аномальными тестами функции щитовидной железы (KIVE et al. , 2011). У детей более высокий уровень витамина D был связан с меньшим количеством антител к щитовидной железе (Camurdan, Döer, Bideci, Celik, & Cinaz, 2012).Однако другие исследования показали противоречивые результаты (Effraimidis, Badenhoop, Tijssen, & Wiersinga, 2012; Goswami et al., 2009). Небольшое исследование, опубликованное в 2019 году, показало, что потребление селена может усиливать влияние витамина D на антитела к щитовидной железе, поэтому, возможно, необходимо учитывать уровни селена вместе с уровнями витамина D (Krysiak, Kowalcze, & Okopien, 2019). На данный момент все еще не решено, полезны ли добавки витамина D для людей с аутоиммунными расстройствами, такими как болезнь Хашимото (Antico, Tampoia, Tozzoli, & Bizzaro, 2012; Talaei, Ghorbani, & Asemi, 2018).Но в то же время факт, что витамин D важен для здоровья, поэтому вы должны быть уверены, что ваши уровни оптимальны.
, 2011). У детей более высокий уровень витамина D был связан с меньшим количеством антител к щитовидной железе (Camurdan, Döer, Bideci, Celik, & Cinaz, 2012).Однако другие исследования показали противоречивые результаты (Effraimidis, Badenhoop, Tijssen, & Wiersinga, 2012; Goswami et al., 2009). Небольшое исследование, опубликованное в 2019 году, показало, что потребление селена может усиливать влияние витамина D на антитела к щитовидной железе, поэтому, возможно, необходимо учитывать уровни селена вместе с уровнями витамина D (Krysiak, Kowalcze, & Okopien, 2019). На данный момент все еще не решено, полезны ли добавки витамина D для людей с аутоиммунными расстройствами, такими как болезнь Хашимото (Antico, Tampoia, Tozzoli, & Bizzaro, 2012; Talaei, Ghorbani, & Asemi, 2018).Но в то же время факт, что витамин D важен для здоровья, поэтому вы должны быть уверены, что ваши уровни оптимальны.
Источники витамина D
Вы можете получать дневную норму витамина D из ограниченного количества продуктов, таких как морепродукты, яйца и молочные продукты. Но, как правило, получить достаточное количество витамина D только из продуктов нереально. Рекомендуемая дневная норма составляет 800 международных единиц (МЕ), что составляет двадцать микрограммов. Порция жирной рыбы в три унции обеспечивает около 500 МЕ витамина D.И вам придется съесть почти целую коробку яиц или выпить целую литр молока, чтобы получить суточную норму из не рыбных источников (NIH, 2019c).
Но, как правило, получить достаточное количество витамина D только из продуктов нереально. Рекомендуемая дневная норма составляет 800 международных единиц (МЕ), что составляет двадцать микрограммов. Порция жирной рыбы в три унции обеспечивает около 500 МЕ витамина D.И вам придется съесть почти целую коробку яиц или выпить целую литр молока, чтобы получить суточную норму из не рыбных источников (NIH, 2019c).
Наш организм также может вырабатывать витамин D после воздействия солнечных лучей, поэтому ежедневная доза солнечного света без слоя солнцезащитного крема помогает. Это о модерации; никогда не получится получить солнечный ожог. И обратите внимание, что если у вас более темная кожа, сложнее получить весь необходимый вам витамин D от солнца.
Многие из нас могут не получать достаточно; Чтобы узнать больше о тестировании уровня витамина D и добавках, см. статью «Спросите Герду» о витамине D, написанную нашим штатным доктором философии.
Другие добавки для лечения конкретных симптомов
Поскольку Хашимото обладает множеством побочных эффектов, могут быть рекомендованы витамины и добавки, помогающие при определенных симптомах.
Выпадение волос — обычная проблема для людей с дисфункцией щитовидной железы. Было доказано, что добавки цинка и железа помогают уменьшить выпадение волос у людей с дефицитом (Karashima et al., 2012; Park, Kim, Kim, & Park, 2009; Trost, Bergfeld, & Calogeras, 2006).
Лица с гипотиреозом могут иметь низкий уровень витамина B12: одно исследование показало, что 40 процентов пациентов с гипотиреозом страдают дефицитом, поэтому вы можете рассмотреть возможность включения добавок B12, если ваш уровень определен как низкий (Jabbar et al., 2008).
Изменения образа жизни для Хашимото
Как и в случае с большинством болезней, важно контролировать стресс, регулярно заниматься спортом и высыпаться.
Упражнение
Многие люди с Хашимото могут испытывать мышечные боли и стеснение. Кроме того, люди с гипотиреозом подвержены более высокому риску сердечно-сосудистых заболеваний. Поэтому регулярные упражнения необходимы: они поддерживают здоровье вашего сердца и мышцы в движении, чтобы уменьшить боль и уменьшить вероятность развития других проблем со здоровьем. Возможно, вы захотите сначала попробовать включить йогу и растяжку, прежде чем переходить к аэробным упражнениям — поговорите об этом со своим врачом. Хотя умеренные упражнения могут поддерживать здоровые гормоны щитовидной железы, будьте осторожны, чтобы не переборщить и не перегружать щитовидную железу высокоинтенсивными тренировками (Ciloglu et al., 2005; Lankhaar, de Vries, Jansen, Zelissen, & Backx, 2014; Lesmana et al. , 2016).
Возможно, вы захотите сначала попробовать включить йогу и растяжку, прежде чем переходить к аэробным упражнениям — поговорите об этом со своим врачом. Хотя умеренные упражнения могут поддерживать здоровые гормоны щитовидной железы, будьте осторожны, чтобы не переборщить и не перегружать щитовидную железу высокоинтенсивными тренировками (Ciloglu et al., 2005; Lankhaar, de Vries, Jansen, Zelissen, & Backx, 2014; Lesmana et al. , 2016).
Напряжение
Возможно, вы слышали (много) об усталости надпочечников. Исследователи и большинство традиционных врачей не разделяют эту концепцию.Теория, лежащая в основе утомления надпочечников, заключается в том, что, когда наше тело подвергается сверхнагрузке, наши надпочечники работают до предела, производя огромное количество кортизола, что приводит к их выгоранию. Результат? Широкий спектр симптомов, таких как депрессия, усталость и неспособность справиться со стрессом.
Хотя усталость надпочечников может не признаваться большинством врачей как расстройство, для многих людей симптомы вполне реальны. И возможно, здесь играют роль гипотиреоз или другие заболевания, например фибромиалгия.
И возможно, здесь играют роль гипотиреоз или другие заболевания, например фибромиалгия.
Доклинические исследования показали, что стресс может влиять на гормоны щитовидной железы даже через несколько часов после стрессового события (D. L. Helmreich & Tylee, 2011; Servatius et al., 2000). Что интересно, психологически преодоление стресса может защитить наши гормоны щитовидной железы. В одном исследовании, в котором исследователи подвергали крыс как неизбежным, так и неизбежным ударам ног (что печально), они обнаружили, что гормоны щитовидной железы снизились только у крыс, которые не могли остановить удары и контролировать свой стресс (Д.Helmreich, Crouch, Dorr, & Parfitt, 2006).
Это исследование подчеркивает, насколько важно для нас контролировать свой повседневный стресс, чтобы поддерживать здоровье тела и разума. Попробуйте ненадолго выйти в автономный режим, посвятить время самообслуживанию или начать практику осознанности.
Сон
Гипотиреоз может вызывать чрезмерную сонливость из-за замедления метаболизма. Люди с синдромом Хашимото также могут быть более подвержены нарушениям сна, таким как апноэ во сне (Bozkurt et al., 2012). Апноэ во сне можно уменьшить, если у вас избыточный вес. Также может быть полезно постоянное положительное давление в дыхательных путях (CPAP). CPAP — это маска, которая надевается на лицо, доставляя кислород во время сна, чтобы дыхательные пути оставались открытыми.
Традиционные варианты лечения Хашимото
Наиболее распространенным вариантом лечения Хашимото является заместительная гормональная терапия. Доказана эффективность тиреоидэктомии для некоторых людей.
Замена гормона
Если вам поставили диагноз Хашимото, ваш врач может порекомендовать препараты гормона щитовидной железы Т4 и / или Т3.Ваш врач порекомендует вам стандартные контрольные анализы крови, чтобы определить наилучшие дозы и рецептуры, поиск которых может занять некоторое время.
Наиболее часто используемым лекарством является синтетический левотироксин, который биологически идентичен Т4, вырабатываемому вашим организмом. Некоторым людям помогает добавление лиотиронина, который является биоидентичным синтетическим Т3. Наибольшую пользу от Т3 могут получить люди, которые не могут эффективно преобразовывать Т4 в Т3, возможно, из-за генетического полиморфизма фермента, который осуществляет это преобразование.
Также сообщалось, что некоторые люди предпочитают то, что было названо биоидентичным естественным заменителем щитовидной железы, которое состоит из иссушенных щитовидной железы животных. Они обеспечивают комбинацию T3, T4 и других компонентов. Например, Armor Thyroid получают из щитовидной железы свиньи.
В течение многих лет производитель левотироксина под торговой маркой Synthroid утверждал, что он превосходит другие марочные и генерические препараты левотироксина. Компания запретила публикацию исследования, опровергающего это утверждение.В 1997 году было наконец опубликовано исследование, показывающее, что несколько фирменных и генерических форм эквивалентны, и судебные процессы вынудили компанию выплатить компенсацию потребителям, которые без необходимости заплатили за более дорогой Synthroid. Клинически значимое преимущество использования Synthroid не было продемонстрировано (Alexander, 2019, Dong et al., 1997, Garber et al., 2012, Santoro et al., 2016).
Тиреоидэктомия
В определенных случаях ваш врач может посоветовать вам удалить щитовидную железу.Обычно это назначают, когда кто-то не отвечает на другие варианты лечения или когда щитовидная железа выглядит так, как будто она может быть злокачественной (Caturegli, De Remigis, & Rose, 2014). Тиреоидэктомия, как правило, представляет собой процедуру с низким уровнем риска и, как было показано, значительно снижает симптомы у пациентов (McManus, Luo, Sippel, & Chen, 2011). Если у вас полная тиреоидэктомия, то есть вся ваша щитовидная железа удалена, вам нужно будет принимать синтетические гормоны щитовидной железы, так как ваше тело больше не сможет вырабатывать гормоны щитовидной железы самостоятельно.
В одном исследовании пациенты Хашимото, которые лечили свою щитовидную железу с помощью гормональных препаратов, но все еще имели значительные симптомы, были случайным образом выбраны для проведения тиреоидэктомии или продолжения лечения в обычном режиме. У пациентов, перенесших операцию, улучшилось общее состояние здоровья, снизилась утомляемость и уровень антител к ТПО после лечения по сравнению с пациентами, которым не проводилась тиреоидэктомия (Guldvog et al., 2019). Возможно, наличие самой щитовидной железы и воспаление, вызванное антителами против щитовидной железы, продолжает вызывать системные проблемы, даже если функция щитовидной железы должным образом регулируется с помощью лекарств.
Альтернативные варианты лечения Хашимото
Работа с целостным практикующим врачом может помочь справиться с множеством симптомов Хашимото. Могут быть полезны травяные добавки, такие как адаптогены и гуггул. Вы можете избегать мелиссы и базилика, которые могут негативно повлиять на щитовидную железу.
Растительная медицина
Целостный подход часто требует целеустремленности, поскольку вы работаете в тесном контакте с опытным практиком. Есть несколько сертификатов, которые назначают травника.Американская гильдия травников предоставляет список зарегистрированных травников, чья сертификация имеет обозначение RH (AHG). Степени традиционной китайской медицины включают LAc (лицензированный специалист по акупунктуре), OMD (доктор восточной медицины) или DipCH (NCCA) (диплом по китайской гербологии Национальной комиссии по сертификации специалистов по акупунктуре). Традиционная аюрведическая медицина из Индии аккредитована в США Американской ассоциацией аюрведических специалистов Северной Америки (AAPNA) и Национальной аюрведической медицинской ассоциацией (NAMA).Есть также функциональные практикующие врачи с целостным мышлением (MD, DO, ND и DC), которые могут использовать травяные протоколы.
Хотя мы не рекомендуем заниматься самолечением Хашимото, есть несколько интересных предварительных исследований о различных травах, которые могут либо помочь поддерживать здоровье щитовидной железы и иммунной системы, либо могут быть вредными. Всегда сначала обсуждайте с врачом травяные добавки.
Адаптогены
Этот класс аюрведических трав известен своей способностью помогать вашему телу справляться со стрессом и саморегулироваться.Экстракт корня ашваганды повышает уровень гормонов щитовидной железы и нормализует уровень ТТГ в двух исследованиях (Gannon, Forrest, & Roy Chengappa, 2014; Sharma, Basu, & Singh, 2018). В хорошо контролируемом клиническом исследовании 600 миллиграммов экстракта ашваганды ежедневно в течение восьми недель помогли нормализовать гормоны щитовидной железы (Sharma et al., 2018). Этого исследования недостаточно, чтобы сделать вывод, что ашваганда определенно полезна для Хашимото, но все же предполагает, что это может быть. Несколько имеющихся на рынке травяных добавок, предназначенных для поддержки щитовидной железы, содержат ашваганду на уровне намного ниже 600 миллиграммов, поэтому проверьте дозу на этикетке любой добавки.
Гуггул
Еще одно растение, используемое в аюрведической традиции для лечения щитовидной железы, — это гуггул. Некоторые доклинические данные (исследования на животных) показали, что гуггул может повышать активность щитовидной железы (Panda & Kar, 2005; Tripathi, Malhotra, & Tripathi, 1984). В исследовательской литературе данные о людях ограничены, а преимущества гуггула для щитовидной железы не были продемонстрированы (Antonio et al., 1999).
трав, которых следует избегать, если у вас есть
ХашимотоЛимонный бальзам — представитель семейства мятных, листья которого традиционно использовались для лечения вздутия живота, менструальных спазмов, зубной боли и герпеса из-за его седативного и успокаивающего действия.Несколько исследований показали, что мелисса может нарушать работу щитовидной железы, ингибируя ТТГ, поэтому подумайте о том, чтобы избегать этой травы (Auf’Mkolk, Ingbar, Kubota, Amir, & Ingbar, 1985; Santini et al., 2003). Другие доклинические исследования показали, что святой базилик может снизить уровень Т4, поэтому вы можете также избегать этого популярного адаптогена, если у вас гипотиреоз (Panda & Kar, 1998).
Новые и многообещающие исследования Хашимото
Некоторые химические вещества, такие как фторид и бромид, могут нарушать функцию щитовидной железы, в то время как лазерная терапия и стволовые клетки были предложены в качестве потенциальных новых вариантов лечения.
Фторид и бромид
Имеются данные о том, что фторид и бромид, которые по химическому составу подобны йодиду, нарушают метаболизм йода в организме. Воздействие бромидов может происходить из-за пестицидов, средств для очистки бассейнов и антипиренов, обычно используемых в тканях и матрасах (CDC, 2018). Бромиды замещают йод, и было предложено (хотя и не подтверждено), что их следует рассматривать как гойтрогены. Однако кажется, что для воздействия на метаболизм йода потребуется очень большое количество бромида (Buchberger, Holler, & Winsauer, 1990; Pavelka, 2004
).Новое исследование также указывает на фторид как на потенциальную проблему для людей с гипотиреозом.В недавнем систематическом обзоре сделан вывод, что чрезмерное фторирование воды может быть связано с высоким уровнем гипотиреоза (Chaitanya et al., 2018). Йодный статус человека может быть важным фактором при рассмотрении вопроса о том, вызывает ли фторид какие-либо проблемы. Одно исследование показало, что у взрослых с умеренным и тяжелым дефицитом йода и высоким потреблением фтора уровень ТТГ повышен (Malin, Riddell, McCague, & Till, 2018). Однако опубликованное в 2019 году обсервационное исследование 293 детей в возрасте от девяти до тринадцати лет показало, что длительное употребление фторированной воды не влияет на их функцию щитовидной железы (Shaik, Shanbhog, Nadlal, & Tippeswamy, 2019).Если вы заинтересованы в снижении избыточного потребления фторидов, вам может пригодиться качественный фильтр для воды.
Лазерная терапия
В Сан-Паулу, Бразилия, исследователи изучают низкоуровневую лазерную терапию (НИЛ) как экономически эффективное лечение пациентов с Хашимото. Другие исследования показали, что НИЛИ может помочь при аутоиммунных заболеваниях, регенерировать ткани и повышать уровень гормонов щитовидной железы, стимулируя функцию клеток с помощью лазеров, которые наносятся на поверхность тела. Группа исследователей из Бразилии недавно обнаружила, что НИЛИ улучшила васкуляризацию щитовидной железы у 43 человек с Хашимото, перенесших заместительную терапию левотироксином; однако необходимы дополнительные исследования, чтобы определить продолжительность эффекта (Höfling et al., 2012).
В исследовании 2020 года 350 пациентов с Хашимото были рандомизированы на шесть сеансов фотобиомодуляции шеи возле щитовидной железы плюс добавки витамина D, железа и селена или просто добавки. Фотобиомодуляция — это вид световой терапии с использованием неионизирующего света, такого как лазер, который предназначен для запуска клеточных изменений в тканях, на которые он воздействует. Пациенты, которые получали как витаминный режим, так и фотобиомодуляцию, имели значительно повышенные уровни Т3 и значительно более низкие уровни антител к ТПО, чем те, кто только что принимал добавки (Ercetin, Sahbaz, Acar, Tutal, & Erbil, 2020).Авторы предположили, что это могло быть связано с тем, что лазеры уменьшают воспаление в щитовидной железе; однако необходимы дальнейшие исследования этого вида терапии, чтобы точно определить, что работает и действительно ли она эффективна для людей с Хашимото.
Стволовые клетки
В терапии щитовидной железы будущего могут быть стволовые клетки: незрелые клетки, которые могут развиваться в различные типы клеток. Даррел Коттон, доктор медицины, исследователь стволовых клеток в Медицинской школе Бостонского университета, и Энтони Холленберг, доктор медицины, эндокринолог из Гарварда, совместно работали над новаторскими исследованиями, которые могут открыть дверь для регенерации щитовидной железы.Используя стволовые клетки, они смогли создать фолликулярные клетки — клетки щитовидной железы, которые вырабатывают гормоны щитовидной железы Т3 и Т4. Когда они имплантировали эти новые фолликулярные клетки мышам, у которых не было щитовидной железы, клетки смогли нормально расти и начать вырабатывать гормоны щитовидной железы в течение двух недель (Kurmann et al., 2015). Невероятный.
Клинические испытания препарата Хашимото
Клинические испытания — это научные исследования, предназначенные для оценки медицинского, хирургического или поведенческого вмешательства.Они сделаны для того, чтобы исследователи могли изучить конкретное лечение, которое, возможно, еще не имеет большого количества данных о его безопасности или эффективности. Если вы планируете записаться на клиническое испытание, важно отметить, что если вы попадете в группу плацебо, вы не получите доступа к изучаемому лечению. Также полезно понимать этапы клинических испытаний: фаза 1 — это первый раз, когда большинство лекарств будет использоваться для людей, поэтому речь идет о поиске безопасной дозы. Если препарат пройдет первоначальное испытание, его можно будет использовать в более крупном испытании фазы 2, чтобы проверить, хорошо ли он работает.Затем его можно сравнить с известным эффективным лечением в испытании фазы 3. Если препарат будет одобрен, он перейдет на этап 4 испытания. Исследования фазы 3 и фазы 4, скорее всего, будут включать наиболее эффективные и безопасные перспективные методы лечения.
В целом, клинические испытания могут дать ценную информацию, могут принести пользу для некоторых субъектов и могут иметь нежелательные результаты для других. Поговорите со своим врачом о любом клиническом испытании, которое вы планируете.
Где найти исследования, которые привлекают субъектов?
Вы можете найти клинические исследования, в которые набираются субъекты для клинических испытаний.gov, веб-сайт Национальной медицинской библиотеки США. База данных состоит из всех исследований, финансируемых из частных и государственных источников, которые проводятся по всему миру. Вы можете искать болезнь, конкретное лекарство или лечение, которые вас интересуют, и можете фильтровать по стране, в которой проводится исследование.
Добавка селена
Исследование CATALYST — крупное клиническое исследование в Дании, изучающее добавку селена. Ученые набирают пациентов с аутоиммунным тиреоидитом, принимающих синтетический гормон щитовидной железы левотироксин (LT4).Исследование продлится год, и участникам будет слепо назначено либо принимать 200 мкг селена в день вместе с их обычным LT4, либо принимать таблетку плацебо со своим LT4. Это исследование важно, потому что оно может помочь нам лучше понять роль селена в Хашимото и определить, является ли это полезной добавкой для добавления в свой распорядок дня; оставайтесь в курсе или узнайте о зачислении здесь.
Микробиом
В Китае исследователи из Первой больницы Харбинского медицинского университета изучают микробиомы кишечника и полости рта пациентов с Хашимото.Используя секвенирование генов, они стремятся сравнить бактериальное разнообразие пациентов с аутоиммунными заболеваниями и здоровых людей. Предыдущие исследования показали, что изменения в микробиоте кишечника являются важными факторами в развитии воспалительных и аутоиммунных заболеваний. Два исследования в настоящее время набираются; Для получения дополнительной информации ознакомьтесь с исследованиями микробиома полости рта и кишечника.
Соответствующая литература
• Понимание и диагностика Хашимото и гипотиреоза с эндокринологом из Лос-Анджелеса Теодором Фридманом, доктором медицины, доктором медицины
• Что делать, если ваша щитовидная железа находится под контролем врача функциональной медицины Эми Майерс, MD
• Антиаутоиммунная диета с Эми Майерс, MD
• 6 самых распространенных эндокринных нарушителей — и как их избежать. Ннека Лейба.
ССЫЛКИ
Александр, Р.(2019, 18 июля). Строгие пациенты, принимающие синтроид гормона щитовидной железы [левотироксин натрия], компания Knoll Pharmaceuticals. ТОО «Александр Ло Групп».
Эбботт, Р. Д., Садовски, А., и Альт, А. Г. (2019). Эффективность диеты с аутоиммунным протоколом как часть междисциплинарного поддерживаемого образа жизни при тиреоидите Хашимото. Cureus, 11 (4).
Акер, А. М., Уоткинс, Д. Дж., Джонс, Л. Е., Фергюсон, К. К., Солдин, О. П., Дель Торо, Л. В. А.,… Микер, Дж. Д. (2016). Фенолы и парабены в отношении репродуктивных гормонов и гормонов щитовидной железы у беременных.Экологические исследования, 151, 30–37.
Антико, А., Тампоя, М., Тоццоли, Р., и Биццаро, Н. (2012). Может ли добавка витамина D снизить риск или изменить течение аутоиммунных заболеваний? Систематический обзор литературы. Обзоры аутоиммунитета, 12 (2), 127–136.
Антонио, Дж., Колкер, К. М., Торина, Г. К., Ши, К., Бринк, В., и Кайман, Д. (1999). Влияние стандартизированной добавки гуггулстеронфосфата на состав тела взрослых с избыточным весом: пилотное исследование.Текущие терапевтические исследования, 60 (4), 220–227.
Ауф’Мколк, М., Ингбар, Дж. К., Кубота, К., Амир, С. М., и Ингбар, С. Х. (1985). Экстракты и аутоокислительные компоненты некоторых растений ингибируют рецепторное связывание и биологическую активность иммуноглобулинов Грейвса. 7.
Аунг, М. Т., Джонс, Л. Е., Фергюсон, К. К., Мукерджи, Б., МакЭлрат, Т. Ф., и Микер, Дж. Д. (2017). Параметры гормона щитовидной железы во время беременности в зависимости от концентрации бисфенола А в моче: исследование с повторными измерениями.Environment International, 104, 33–40.
Баджадж, Дж. К., Салван, П., и Салван, С. (2016). Различные возможные токсиканты, участвующие в дисфункции щитовидной железы: обзор. Журнал клинических и диагностических исследований: JCDR, 10 (1), FE01 – FE03.
Бишоп П. Х., Зауэрвейн Х. П., Эндерт Э. и Ромейн Дж. А. (2001). Депривация изокалорийных углеводов вызывает катаболизм белков, несмотря на низкий T3-синдром у здоровых мужчин. Клиническая эндокринология, 54 (1), 75–80.
Бьергвед, Л., Йоргенсен, Т., Перрилд, Х., Карле, А., Серкейра, К., Крейбьерг, А.,… Кнудсен, Н. (2012). Предикторы изменения уровня ТТГ в сыворотке после обогащения йодом: 11-летнее наблюдение за исследованием DanThyr. Журнал клинической эндокринологии и метаболизма, 97 (11), 4022–4029.
Блумфилд, С., Стэнвелл-Смит, Р., Кревель, Р., и Пикап, Дж. (2006). Слишком чисто или не слишком чисто: Гипотеза гигиены и домашняя гигиена. Клиническая и экспериментальная аллергия, 36 (4), 402–425.
Бозкурт, Н.К., Карбек, Б., Чакал, Э., Фират, Х., Озбек, М., и Делибаси, Т. (2012). Связь между тяжестью обструктивного апноэ во сне и распространенностью тиреоидита Хашимото. 8.
Бухбергер В., Холлер В. и Винсауэр К. (1990). Влияние бромида натрия на биосинтез гормонов щитовидной железы и бромированных / йодированных тиронинов. Журнал микроэлементов и электролитов в здоровье и болезнях, 4 (1), 25–30.
Камурдан, О. М., Дёгер, Э., Бидечи, А., Челик, Н., и Чиназ, П.(2012). Статус витамина D у детей с тиреоидитом Хашимото. Журнал детской эндокринологии и метаболизма: JPEM, 25 (5–6), 467–470.
Катургли П., Де Ремигис А. и Роуз Н. Р. (2014). Тиреоидит Хашимото: клинико-диагностические критерии. Обзоры аутоиммунитета, 13 (4–5), 391–397.
CDC. (2012). Второй национальный отчет о биохимических показателях диеты и питания населения США. 495.
CDC. (2018, 7 мая). CDC | Факты о броме. Проверено 27 ноября 2018 года.
Чайтанья, Н. С. С. К., Карунакар, П., Аллам, Н. С. Дж., Прия, М. Х., Алекхья, Б., и Наусин, С. (2018). Систематический анализ возможности фторирования воды, вызывающего гипотиреоз. Индийский журнал стоматологических исследований: официальная публикация Индийского общества стоматологических исследований, 29 (3), 358–363.
Чандра, А. К., и Де, Н. (2013). Катехин индуцировал модуляцию активности ферментов, синтезирующих гормоны щитовидной железы, что приводило к гипотиреозу. Молекулярная и клеточная биохимия, 374 (1–2), 37–48.
Чилоглу, Ф., Пекер, И., Пехливан, А., Ольхан, К. К. Н., Сайгин, О., & Озмердивенли, Р. (2005). Интенсивность упражнений и ее влияние на гормоны щитовидной железы. Neuroendocrinology Lett, 26 (6), 6830–6834.
Дерумо, Х., Вале, П., Кастетбон, К., Бенсимон, М., Бутрон-Руо, М.-К., Арно, Дж., И Херкберг, С. (2003). Связь селена с объемом и эхоструктурой щитовидной железы у взрослых французов в возрасте от 35 до 60 лет. Европейский журнал эндокринологии, 148 (3), 309–315.
Ди Матола, Т., Зеппа, П., Гаспери, М., и Витале, М. (2014). Дисфункция щитовидной железы после употребления коммерческой диеты, содержащей водоросли. BMJ Case Reports, 2014.
Донг, Б. Дж., Хаук, В. В., Гамбертольо, Дж. Г., Джи, Л., Уайт, Дж. Р., Бубп, Дж. Л., и Гринспен, Ф. С. (1997). Биоэквивалентность генерических и фирменных препаратов левотироксина в лечении гипотиреоза. JAMA, 277 (15), 1205–1213.
Эффраимидис, Г., Баденхуп, К., Тейссен, Дж. Г. П., и Виерсинга, В. М. (2012). Дефицит витамина D не связан с ранними стадиями аутоиммунитета щитовидной железы.Европейский журнал эндокринологии, 167 (1), 43–48.
Элиасон, Б.С. (1998). Преходящий гипертиреоз у пациента, принимающего пищевые добавки, содержащие водоросли. Журнал Американского совета по семейной практике, 11 (6), 478–480.
Эрдал, М., Сахин, М., Хасими, А., Учкая, Г., Кутлу, М., и Саглам, К. (2008). Уровни микроэлементов у пациентов с тиреоидитом Хашимото с субклиническим гипотиреозом. Биологические исследования микроэлементов, 123 (1), 1.
Фан, Ю., Сюй, С., Чжан, Х., Цао, В., Ван, К., Чен, Г.,… Лю, К. (2014). Добавки селена для аутоиммунного тиреоидита: систематический обзор и метаанализ. Международный журнал эндокринологии, 2014, 1–8.
Форрест, К. Ю. З., и Стулдреер, В. Л. (2011). Распространенность и корреляты дефицита витамина D у взрослых в США. Исследования питания, 31 (1), 48–54.
Форт, П., Моисей, Н., Фазано, М., Голдберг, Т., и Лифшиц, Ф. (1990). Кормление грудью и соевыми смесями в раннем детстве и распространенность аутоиммунных заболеваний щитовидной железы у детей.Журнал Американского колледжа питания, 9 (2), 164–167.
Ганнон, Дж. М., Форрест, П. Э. и Рой Ченгаппа, К. Н. (2014). Незначительные изменения показателей щитовидной железы во время плацебо-контролируемого исследования экстракта Withania somnifera у лиц с биполярным расстройством. Журнал аюрведы и интегративной медицины, 5 (4), 241–245.
Гарбер, Дж. Р., Кобин, Р. Х., Гариб, Х., Хеннесси, Дж. В., Кляйн, И., Механик, Дж. И.,… Целевая группа Американской ассоциации клинических эндокринологов и Американской тироидной ассоциации по гипотиреозу у взрослых.(2012). Клинические рекомендации по лечению гипотиреоза у взрослых: при поддержке Американской ассоциации клинических эндокринологов и Американской тироидной ассоциации. Эндокринная практика: Официальный журнал Американского колледжа эндокринологии и Американской ассоциации клинических эндокринологов, 18 (6), 988–1028.
Госвами, Р., Марваха, Р. К., Гупта, Н., Тандон, Н., Шринивас, В., Томар, Н.,… Агарвал, Р. (2009). Распространенность дефицита витамина D и его связь с аутоиммунитетом щитовидной железы у азиатских индейцев: исследование на уровне сообщества.Британский журнал питания, 102 (03), 382.
Гульдвог, И., Рейцма, Л. К., Йонсен, Л., Лаузике, А., Гиббс, К., Карлсен, Э.,… Сойланд, Х. (2019). Тиреоидэктомия по сравнению с медицинским лечением у эутиреоидных пациентов с болезнью Хашимото и сохраняющимися симптомами: рандомизированное исследование. Анналы внутренней медицины, 170 (7), 453–464.
Хельмрайх Д., Крауч М., Дорр Н. и Парфитт Д. (2006). Уровни периферического трийодтиронина (Т3) во время неизбежного и неизбежного шока стопы. Физиология и поведение, 87 (1), 114–119.
Хельмрайх, Д. Л., и Тайли, Д. (2011). Регулирование тироидных гормонов стрессом и поведенческими различиями у взрослых самцов крыс. Гормоны и поведение, 60 (3), 284–291.
Хендлер Р. и Бонд III А. А. (1988). Очень низкокалорийные диеты с высоким и низким содержанием белка: влияние на трийодтиронин, расход энергии и азотный баланс. Am J Clin Nutr, 48, 1239–1247.
Хёфлинг, Д. Б., Чавантес, М. К., Джулиано, А. Г., Черри, Г. Г., Кнобель, М., Йошимура, Э.М., и Чаммас, М. С. (2012). Оценка влияния низкоуровневой лазерной терапии на васкуляризацию щитовидной железы у пациентов с аутоиммунным гипотиреозом с помощью цветного допплеровского ультразвукового исследования. ISRN Endocrinology, 2012.
.Джаббар, А., Явар, А., Васим, С., Ислам, Н., Хак, Н. У., Зубери, Л.,… Ахтер, Дж. (2008). Дефицит витамина B12 часто встречается при первичном гипотиреозе. J Pak Med Assoc, 58 (5), 4.
Янегова А., Янега П., Рыхлы Б., Курацинова К. и Бабал П. (2015). Рола инфекций wirusem Epstein-Barr’a w rozwoju autoimmunologicznych chorób tarczycy.Endokrynologia Polska, 66 (2), 132–136.
Джонс, Л. Э., Фергюсон, К. К., МакЭлрат, Т. Ф., Мукерджи, Б., и Микер, Дж. Д. (2016). Связь между повторными измерениями метаболитов фталатов в моче матери и параметрами тироидных гормонов во время беременности. Перспективы гигиены окружающей среды, 124 (11), 1808–1815.
Карашима, Т., Цурута, Д., Хамада, Т., Оно, Ф., Исии, Н., Абэ, Т.,… Хашимото, Т. (2012). Пероральная цинковая терапия при телогенном эффлювии, вызванном дефицитом цинка.Дерматологическая терапия, 25 (2), 210–213.
Кивив, С., Агмон-Левин, Н., Бланк, М., и Шенфельд, Ю. (2009). Инфекции и аутоиммунитет — друзья или враги? Тенденции в иммунологии, 30 (8), 409–414.
Кивив, С., Агмон-Левин, Н., Зисаппл, М., Шапира, Ю., Надь, Э. В., Данко, К.,… Шенфельд, Ю. (2011). Витамин D и аутоиммунные заболевания щитовидной железы. Клеточная и молекулярная иммунология, 8 (3), 243–247.
Конно, Н., Макита, Х., Юри, К., Иидзука, Н., и Кавасаки, К. (1994).Связь между потреблением йода с пищей и распространенностью субклинического гипотиреоза в прибрежных регионах Японии. Журнал клинической эндокринологии и метаболизма, 78 (2), 393–397.
Krysiak, R., Szkróbka, W., & Okopień, B. (2018). Влияние безглютеновой диеты на аутоиммунитет щитовидной железы у не употребляющих наркотики женщин с тиреоидитом Хашимото: пилотное исследование. Экспериментальная и клиническая эндокринология и диабет.
Крысяк, Р., Ковальче, К., и Окопень, Б. (2019).Селенометионин усиливает влияние витамина D на аутоиммунитет щитовидной железы у эутиреоидных женщин с тиреоидитом Хашимото и низким уровнем витамина D. Фармакологические отчеты, 71 (2), 367–373.
Курманн А. А., Серра М., Хокинс Ф., Рэнкин С. А., Мори М., Астапова И.,… Коттон Д. Н. (2015). Восстановление функции щитовидной железы путем трансплантации дифференцированных плюрипотентных стволовых клеток. Cell Stem Cell, 17 (5), 527–542.
Lankhaar, J. A. C., de Vries, W. R., Jansen, J. A.К. Г., Зелиссен, П. М. Дж., И Бэккс, Ф. Дж. Г. (2014). Влияние явного и субклинического гипотиреоза на толерантность к физической нагрузке: систематический обзор. Ежеквартальное исследование упражнений и спорта, 85 (3), 365–389.
Лаурберг П., Педерсен К. М., Хрейдарссон А., Сигфуссон Н., Иверсен Э. и Кнудсен П. Р. (1998). Потребление йода и характер заболеваний щитовидной железы: сравнительное эпидемиологическое исследование патологий щитовидной железы у пожилых людей в Исландии и Ютландии, Дания. Журнал клинической эндокринологии и метаболизма, 83 (3), 765–769.
Ли, Х. Дж., Ли, К. В., Хаммерстад, С. С., Стефан, М., и Томер, Ю. (2015). Иммуногенетика аутоиммунных заболеваний щитовидной железы: всесторонний обзор. Журнал аутоиммунитета, 64, 82–90.
Лесмана Р., Ивасаки Т., Иидзука Ю., Амано И., Симокава Н. и Койбути Н. (2016). Изменение передачи сигналов гормона щитовидной железы в результате изменения интенсивности тренировки в скелетных мышцах самцов крыс. Эндокринный журнал, 63 (8), 727–738.
Liontiris, M. I., & Mazokopakis, E. E. (2017).Краткий обзор тиреоидита Хашимото (ТТ) и важности йода, селена, витамина D и глютена для аутоиммунитета и диеты пациентов с ГТ. Точки, требующие дополнительных исследований. Hell J Nucl Med, 20 (1), 51–56.
Lundin, K. E. A., & Wijmenga, C. (2015). Целиакия и аутоиммунное заболевание — генетическое совпадение и скрининг. Nature Reviews Gastroenterology & Hepatology, 12 (9), 507–515.
Малин, А. Дж., Ридделл, Дж., Маккейг, Х., и Тилль, К. (2018).Воздействие фторидов и функция щитовидной железы среди взрослых, живущих в Канаде: изменение эффекта в зависимости от йодного статуса. Environment International, 121, 667–674.
Маклеод, Д. С. А., & Купер, Д. С. (2012). Заболеваемость и распространенность аутоиммунных заболеваний щитовидной железы. Эндокринная, 42 (2), 252–265.
Макманус, К., Луо, Дж., Сиппель, Р., и Чен, Х. (2011). Следует ли пациентам с симптоматическим тиреоидитом Хашимото проводить операцию? Журнал хирургических исследований, 170 (1), 52–55.
Митикава Т., Иноуэ, М., Симадзу, Т., Савада, Н., Ивасаки, М., Сасадзуки, С.,… Цугане, С. (2012). Потребление морских водорослей и риск рака щитовидной железы у женщин: проспективное исследование, проведенное Японским центром общественного здравоохранения. Европейский журнал профилактики рака, 21 (3), 254–260.
Миллер, Э. М. (2014). Состояние железа и воспроизводство у женщин США: Национальное исследование здоровья и питания, 1999-2006 гг. PLoS ONE, 9 (11), e112216.
Мияи, К., Токусигэ, Т., и Кондо, М. (2008). Подавление функции щитовидной железы при употреблении морских водорослей «комбу» (Laminaria japonoca) у нормальных взрослых японцев.Эндокринный журнал, 55 (6), 1103–1108.
Мори, К., и Йошида, К. (2010). Вирусная инфекция в индукции тиреоидита Хашимото: ключевой игрок или просто сторонний наблюдатель? Текущее мнение в эндокринологии, диабете и ожирении, 17 (5), 418–424.
M’Rabet ‐ Bensalah, K., Aubert, C.E., Coslovsky, M., Collet, T.-H., Baumgartner, C., Elzen, W.P.J. den,… Rodondi, N. (2016). Дисфункция щитовидной железы и анемия в большом популяционном исследовании. Клиническая эндокринология, 84 (4), 627–631.
NIH.(2017). Болезнь Хашимото | НИДДК. Получено 14 ноября 2018 г. с веб-сайта Национального института диабета, болезней органов пищеварения и почек.
NIH. (2018). Офис диетических добавок — утюг. Проверено 13 ноября 2018.
.NIH. (2019). Йод — информационный бюллетень для медицинских работников. Проверено 13 ноября 2018.
.NIH. (2019a). Офис диетических добавок — селен. Проверено 23 октября, 2019.
.NIH. (2019b). Управление пищевых добавок — витамин D. Получено 23 октября 2019 г.
Панда, С., и Кар, А. (1998). OCIMUM SANCTUMLEAF ЭКСТРАКТ В РЕГУЛЯЦИИ ФУНКЦИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У МЫШЕЙ МУЖЧИН. Фармакологические исследования, 38 (2), 107–110.
Панда, С., и Кар, А. (2005). Guggulu (Commiphora mukul) потенциально уменьшает гипотиреоз у самок мышей. Фитотерапевтические исследования, 19 (1), 78–80.
Парк, Х., Ким, К. В., Ким, С. С., и Парк, К. В. (2009). Терапевтический эффект и изменение уровня цинка в сыворотке после приема цинка у пациентов с очаговой алопецией, у которых был низкий уровень цинка в сыворотке.Анналы дерматологии, 21 (2), 142–146. https://doi.org/10.5021/ad.2009.21.2.142
Пасько, П., Оконь, К., Кросняк, М., Проховник, Э., Смудски, П., Крычик-Козиол, Ю., и Загродски, П. (2018). Взаимодействие между йодом и глюкозинолатами в проростках брюквы и избранные биомаркеры функции щитовидной железы у самцов крыс. Журнал микроэлементов в медицине и биологии, 46, 110–116.
Павелка, С. (2004). Метаболизм бромида и его вмешательство в метаболизм йода.53, 10.
Педерсен, И. Б., Кнудсен, Н., Карле, А., Вейбьерг, П., Йоргенсен, Т., Перрилд, Х.,… Лаурберг, П. (2011). Осторожная программа йодирования, снижающая потребление йода до низкого рекомендованного уровня, связана с увеличением распространенности аутоантител к щитовидной железе среди населения. Клиническая эндокринология, 75 (1), 120–126.
Пирола, И., Ротонди, М., Кристиано, А., Маффеццони, Ф., Паскуали, Д., Марини, Ф., Коперчини, Ф., Паганелли, М., Апостоли, П., Чиовато, Л. , Ферлин, А., И Капелли К. (2020). Добавки селена у пациентов с субклиническим гипотиреозом, пораженным аутоиммунным тиреоидитом: результаты исследования SETI. Endocrinología, Diabetes y Nutrición, 67 (1), 28–35.
Расмуссен, Л. Б., Шомбург, Л., Кёрле, Дж., Педерсен, И. Б., Холленбах, Б., Хёг, А.,… Лаурберг, П. (2011). Состояние селена, объем щитовидной железы и образование множественных узелков в области с умеренным дефицитом йода. Европейский журнал эндокринологии, 164 (4), 585–590.
Райман, М.П. (2018). Множественные факторы питания и заболевание щитовидной железы, в частности аутоиммунное заболевание щитовидной железы. Труды Общества питания, 1–11.
Рид С. М., Миддлтон П., Коссич М. К., Кроутер К. А. и Бейн Э. (2013). Вмешательства при клиническом и субклиническом гипотиреозе до и во время беременности. Кокрановская база данных систематических обзоров, (5).
Рой, А., Лашковска, М., Сундстрем, Дж., Лебволь, Б., Грин, П. Х. Р., Кемпе, О., и Людвигссон, Дж.Ф. (2016). Распространенность целиакии у пациентов с аутоиммунным заболеванием щитовидной железы: метаанализ. Щитовидная железа, 26 (7), 880–890.
Сантини, Ф., Витти, П., Чеккарини, Дж., Маммоли, К., Роселлини, В., Пелосини, К.,… Пинчера, А. (2003). Анализ in vitro разрушителей щитовидной железы, влияющих на активность аденилатциклазы, стимулированную ТТГ. Журнал эндокринологических исследований, 26 (10), 950–955.
Санторо, Н., Браунштейн, Г. Д., Баттс, К. Л., Мартин, К. А., Макдермотт, М., и Пинкертон, Дж.В. (2016). Составные биоидентичные гормоны в практике эндокринологии: научное заявление эндокринного общества. Журнал клинической эндокринологии и метаболизма, 101 (4), 1318–1343.
Sategna-Guidetti, C. a, Bruno, M. a, Mazza, E. b, Carlino, A. a, Predebon, S. a, Tagliabue, M. b, & Brossa, C. c. (1998). Аутоиммунные заболевания щитовидной железы и целиакия. Журнал гастроэнтерологии, 10 (11), 927–932.
Шайк Н., Шанбхог Р., Нандлал Б. и Типпесвами Х. М. (2019).Функция фторида и щитовидной железы у детей, проживающих в районах с естественным фторированием, потребляющих разные уровни фтора в питьевой воде: обсервационное исследование. Современная клиническая стоматология, 10 (1), 24–30.
Серватиус, Р. Дж., Нательсон, Б. Х., Молдову, Р., Погач, Л., Бреннан, Ф. Х., & Оттенвеллер, Дж. Э. (2000). Стойкие нейроэндокринные изменения в множественных гормональных осях после однократного или многократного стрессорного воздействия. Напряжение, 3 (4), 263–274.
Шарма, А.К., Басу, И., & Сингх, С. (2018). Эффективность и безопасность экстракта корня ашваганды у пациентов с субклиническим гипотиреозом: двойное слепое рандомизированное плацебо-контролируемое исследование. Журнал альтернативной и дополнительной медицины, 24 (3), 243–248.
Шукла, С. К., Сингх, Г., Ахмад, С., и Пант, П. (2018). Инфекции, генетические факторы и факторы окружающей среды в патогенезе аутоиммунных заболеваний щитовидной железы. Микробный патогенез, 116, 279–288.
Souberbielle, J.-C., Body, J.-J., Lappe, J.M., Плебани, М., Шенфельд, Ю., Ван, Т. Дж.,… Зиттерманн, А. (2010). Витамин D и опорно-двигательный аппарат здоровье, сердечно-сосудистые заболевания, аутоиммунные заболевания и рак: Рекомендации по клинической практике. Обзоры аутоиммунитета, 9 (11), 709–715.
Сполдинг, С. В., Чопра, И. Дж., Шервин, Р. С., и Лайал, С. С. (1976). ВЛИЯНИЕ КАЛОРИЧЕСКОГО ОГРАНИЧЕНИЯ И ДИЕТИЧЕСКОГО СОСТАВА НА СЫВОРОТКУ T 3 И ОБРАТНЫЙ T 3 У ЧЕЛОВЕКА. Журнал клинической эндокринологии и метаболизма, 42 (1), 197–200.
ул.Жермен Д. Л., Гальтон В. А. и Эрнандес А. (2009). Определение роли йодтиронин дейодиназ: современные концепции и проблемы. Эндокринология, 150 (3), 1097–1107.
Щепанек-Парульска, Э., Херник, А., и Ручала, М. (2017). Анемия при заболеваниях щитовидной железы. Польский архив внутренней медицины.
Талаеи, А., Горбани, Ф., и Асеми, З. (2018). Влияние добавок витамина D на функцию щитовидной железы у пациентов с гипотиреозом: рандомизированное двойное слепое плацебо-контролируемое исследование.Индийский журнал эндокринологии и метаболизма, 22 (5), 584–588.
Томер Ю. (2014). МЕХАНИЗМЫ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ: ОТ ГЕНЕТИКИ К ЭПИГЕНЕТИКЕ. Ежегодный обзор патологии, 9, 147–156.
Тулис, К. А., Анастасилакис, А. Д., Целлос, Т. Г., Гулис, Д. Г., и Кувелас, Д. (2010). Добавки селена в лечении тиреоидита Хашимото: систематический обзор и метаанализ. Thyroid, 20 (10), 1163–1173.
Трипати, Ю., Малхотра, О., И Трипати, С. (1984). Стимулирующее действие на щитовидную железу Z-гуггулстерона, полученного из Commiphora mukul. Planta Medica, 50 (01), 78–80.
Трост, Л. Б., Бергфельд, В. Ф., и Калогерас, Э. (2006). Диагностика и лечение дефицита железа и его потенциальная связь с выпадением волос. Журнал Американской академии дерматологии, 54 (5), 824–844.
ван Зуурен, Э. Дж., Албуста, А. Ю., Федорович, З., Картер, Б., и Пийл, Х. (2014). Добавки селена при тиреоидите Хашимото: резюме Кокрановского систематического обзора.Eur Thyroid J, 21 (1), 25–31.
Ван Б., Шао Х., Сун Р., Сюй Д. и Чжан Дж. (2017). Растущая роль эпигенетики в аутоиммунных заболеваниях щитовидной железы. Границы иммунологии, 8.
Ван, В., Мао, Дж., Чжао, Дж., Лу, Дж., Янь, Л., Ду, Дж.,… Тэн, В. (2018). Снижение титра антител к пероксидазе щитовидной железы в ответ на добавление селена при аутоиммунном тиреоидите и влияние полиморфизма гена SEPP: проспективное многоцентровое исследование в Китае. Щитовидная железа: Официальный журнал Американской ассоциации щитовидной железы.
Сюй, К., Ву, Ф., Мао, К., Ван, Х., Чжэн, Т., Бу, Л.,… Сяо, Ю. (2016). Избыток йода способствует апоптозу фолликулярных эпителиальных клеток щитовидной железы за счет подавления аутофагии и связан с тиреоидитом Хашимото. Журнал аутоиммунитета, 75, 50–57.
Янг, С.-Й., Люн, П.С.С., Адамопулос, И.Э., и Гершвин, М.Э. (2013). Значение витамина D и аутоиммунитета: всесторонний обзор. Клинические обзоры в аллергии и иммунологии, 45 (2), 217–226.
Чжао, Х., Тянь, Ю., Лю, З., Ли, X., Фэн, М., и Хуанг, Т. (2014). Корреляция между потреблением йода и заболеваниями щитовидной железы: перекрестное исследование, проведенное на юге Китая. Биологические исследования микроэлементов, 162 (1), 87–94.
Циммерманн, М. Б., Берджи, Х., и Харрелл, Р. Ф. (2007). Дефицит железа является причиной плохого состояния щитовидной железы матери во время беременности. Журнал клинической эндокринологии и метаболизма, 92 (9), 3436–3440.
Заявление об ограничении ответственности
Эта статья предназначена только для информационных целей, даже если и в той степени, в которой она содержит советы врачей и практикующих врачей.Эта статья не является и не предназначена для замены профессиональных медицинских рекомендаций, диагностики или лечения, и на нее никогда не следует полагаться при получении конкретных медицинских рекомендаций. Информация и советы в этой статье основаны на исследованиях, опубликованных в рецензируемых журналах, о методах традиционной медицины и рекомендациях практикующих врачей, Национальных институтов здравоохранения, Центров по контролю за заболеваниями и других признанных медицинских научных организаций. ; это не обязательно отражает точку зрения goop.
.

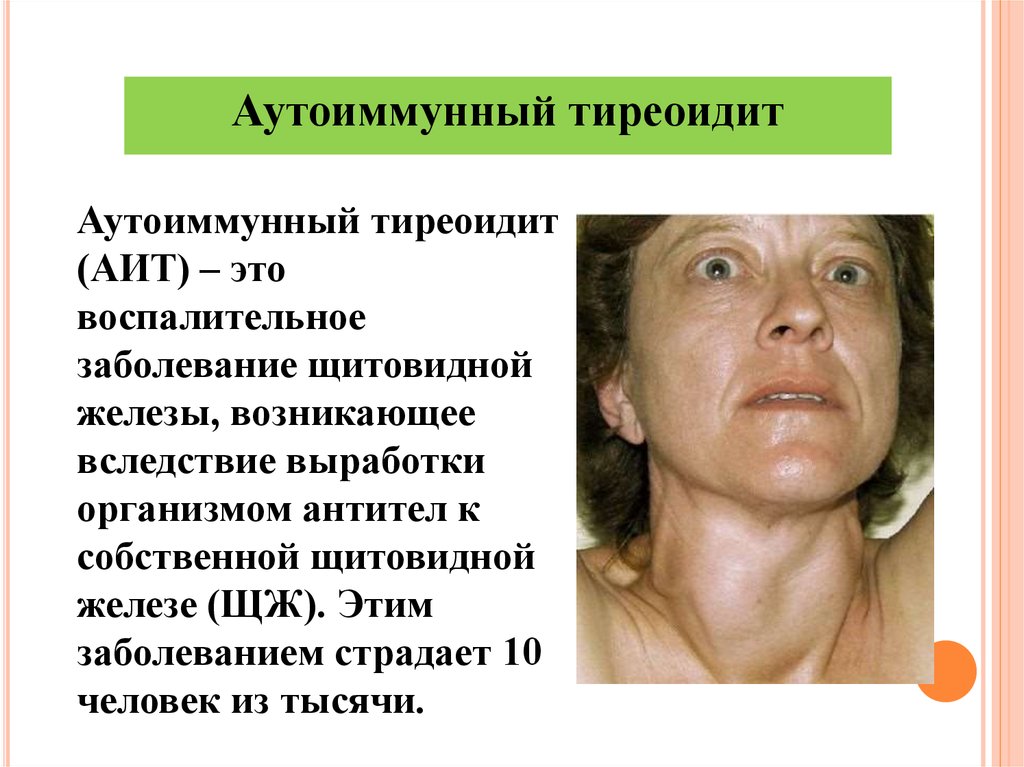

 Щитовидная железа может быть равномерно увеличена по всему объему (диффузная гипертрофическая форма), или отмечается наличие узлов (узловая/ложноузловая форма). Возможно сочетание диффузной и узловой форм (смешанная форма).
Щитовидная железа может быть равномерно увеличена по всему объему (диффузная гипертрофическая форма), или отмечается наличие узлов (узловая/ложноузловая форма). Возможно сочетание диффузной и узловой форм (смешанная форма).



 pdf
pdf База данных Skin Deep Рабочей группы по окружающей среде позволяет искать продукты и видеть, насколько они соответствуют определенным критериям для здоровья и безопасности. У организации также есть руководство по здоровым чистящим средствам.
База данных Skin Deep Рабочей группы по окружающей среде позволяет искать продукты и видеть, насколько они соответствуют определенным критериям для здоровья и безопасности. У организации также есть руководство по здоровым чистящим средствам.