Лечение артериальной гипертензии в особых группах больных. Гипертрофия левого желудочка | Конради
1. European Society of Hypertension- European Society of Cardiology guidelines for the management оf arterial hypertension. J Hypertension 2003; 21: 1011-53. 2. JNC
2. Sokolow M., Pertoff D. Prognosis of essential hypertension treated conservatively. Circulation 1961; 23: 697- 713.
3. Vakili B.A., Oken P.M., Devereux R.B. Prognostic implications of left ventricular hypertrophy. Am Heart J 2001; 141: 334-41.
4. Kannel W., Gordon T., Devereux R.B. Left ventricular hypertrophy by electrocardiogram: prevalence, incidence, and mortality in the Framingham Study. Ann Intern Med 1969: 71: 89-105.
6. Liao Y., Cooper R., Mensah G. et al. The relative effects of left ventricular hypertrophy, coronary artery disease, and ventricular dysfunction on survival among black adults. JAMA 1995: 273: 1592-7.
7. Schillaci G., Verdecchia P., Porcellati С. et al. Continuous relation between left ventricular mass and risk in essential hypertension. Hypertension 2000: 35: 580-6.
 Ann Intern Med 1986: 105: 173-8.
Ann Intern Med 1986: 105: 173-8.9. Ghali J., Kadakia S., Cooper R. et al. Impact of left ventricular hypertrophy patterns on ventricular arrhythmias in the absence of coronary artery disease. J Am Coll Cardiol 1991; 17: 1277-82.
10. Kohara K., Zhao B., Jiang Y. et al. Relation of left ventricular hypertrophy and geometry to asymptomatic cerebrovascular damage in essential hypertension. Am J Cardiol 1999: 83 (3): 367-70.
11. Levy D., Anderson K.M., Savage D.D. et al. Risk of ventricular arrhythmias in left ventricular hypertrophy: The Framingham Heart Study. Am J Cardiol 285-92.
12. Messerly F.N., Grodzicki T. Hypertensive left ventricular hypertrophy, ventricular arrhythmias and sudden death. Eur Heart J 1992: 13 (Suppl. D): 66-9.
14. Nunez B.D., Lavie C.J. Comparison of diastolic left ventricular filling and cardiac dysrhythmias in hypertensive patients with and without isolated septal hypertrophy. Am J Cardiol 1994; 74: 585-90.
15. Kannel W.B. Left ventricular hypertrophy as a risk factor. J Hypertens 1991: 9 (Suppl. 2): S3-S9.

17. Koren M.J., Devereux R.B., Casale P.N. el al. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension Ann Intent Med 1991: 114: 345-52.
18. Krumbolz H.M., Larson M., Levy D. Prognosis of left ventricular geometric patterns in Framingham Heart Study. J Am Coll Cardiol 1995; 25: 884-97.
19. Jennings C., Wong J., Regression of Left ventricular hypertrophy in hypertension: Changing patterns with successive meta-analysis. J Hypertens Suppl 1998; 16: S29-S34.
20. Devereux R.B., Dahlof B. Requirements for an informative trial on left ventricular hypertrophy regression. J Hum Hypertension 1994; 8: 735-9.
21. Dahlof B., Pennert K., Hansson L. Reversal of left ventricular hypertrophy in hypertensive patients — A metaanalysis if 109 treatment studies. Am J Hypertens 1992: 5: 95-110.
22. Cruickshank J.M., Lewes J., Moore E.V., Dodd С. Reversibility of left ventricular hypertrophy by different types of antihypertensive therapy. J Hum Hypertens 1992; 17: 85-90.
23. Schmeider R.E., Schilachi M.P., Klingheil A., Martus P. Update of Reversal of left ventricular hypertrophy in essential hypertension (a meta-analysis of all randomized double-blind studies until December 1996) Nephrol Dial Transplant 1998: 13: 564-9.
 Am J Med 2003 Jul: 115 (1):41-6.
Am J Med 2003 Jul: 115 (1):41-6.25. Cuspidi С., Muiesan M.L., Valagussa L. Comparative effects of candesartan and enalapril on left ventricular hypertrophy in patients with essential hypertension: the candesartan assessment in the treatment of cardiac hypertrophy (CATCH) study. J Hypertens 2002: 20 (11): 2293-300.
27. Koren M.J., Savage D.D., Casale P.N. et al. Changes in left ventricular mass predict risk in essential hypertension. Circulation 1990; 82:11129.
28. Yurenev A.P. et al. Management of essential hypertension inpatients with different degrees of Left ventricular hypertrophy: Multicentral trial. Am J Hypertens 1992; 5: 182s-9s.
29. Levy D., Salomon M., D’Agonistino R. et al. Prognostic implications of baseline electrocardiographic features and their serial changes in subjects with left ventricular hypertrophy. Circulation 1994: 90: 1786-93.
30. Mathew J., Sleight P., Lonn E. et al. Reduction of cardiovascular risk by regression of electrocardiographic markers of left ventricular hypertrophy by the angiotensin enzyme inhibitor, ramipril. Circulation 2001: 104: 1615-21.
31. Muiesan M.L., Salvetti M., Rizzoni D. et al. Association of change in left ventricular mass with prognosis during long-term antihypertensive treatment. J Hypertens 1995; 13: 1091-7.
32. Verdecchia P., Schillaci C., Borgioni I. et al. Prognostic significance of serial changes in left ventricular mass in essential hypertension. Circulation 1998. 97: 48-55.
Диагностическая ценность электрокардиографических критериев гипертрофии левого желудочка при эссенциальной артериальной гипертензии и в сочетании с ишемической болезнью сердца | Чайковская
Аннотация
Цель. Оценить диагностическую значимость электрокардиографических критериев гипертрофии левого желудочка, предлагаемых к использованию в современных Клинических рекомендациях «Артериальная гипертония у взрослых)), в сочетании с ИБС и без неё в сопоставлении с данными эхо-кардиографии. Материалы и методы. Электрокардиографически и эхокардиографически обследовано 165 больных с артериальной гипертонией (АГ) в сочетании и без ИБС: 139 больных с АГ без ИБС (группа АГ) и 26 больных с АГ и сопутствующей ИБС (группа АГ+ИБС). Результаты. Согласно данным ЭхоКГ критерии ГЛЖ («ЭхоКГ+») были выявлены у 72 (51,7 %) больных в группе АГ и у 12 (46,1 %) больных в группе АГ+ИБС. В подгруппе «ЭхоКГ+» ЭКГ признаки гипертрофии по трем критериям Рекомендаций ((Артериальная гипертония у взрослых», 2016 (индекс Соколова-Лайона, Корнельское произведение, Корнельский показатель) определялись у 22 (30,5 %) больных группы АГ и ни в одном случае в группе АГ+ИБС. В подгруппе «ЭхоКГ-» электрокардиографические признаки гипертрофии миокарда левого желудочка определялись у 9 больных группы АГ и у двух больных группы АГ+ИБС. Использование дополнительных вольтажных критериев ГЛЖ в отведениях фронтальной плоскости (RI > 15мм, (Rl + SIH) > 25мм, RaVL > 12 мм) повысило выявление ГЛЖ с 30,5 % (n=22) до 51,3 % (n=37). На ложноотрицательную ЭКГ-диагностику ГЛЖ оказывают влияние позиционные особенности, нарушение внутри-желудочковой проводимости, метаболические нарушения и увеличенная масса тела.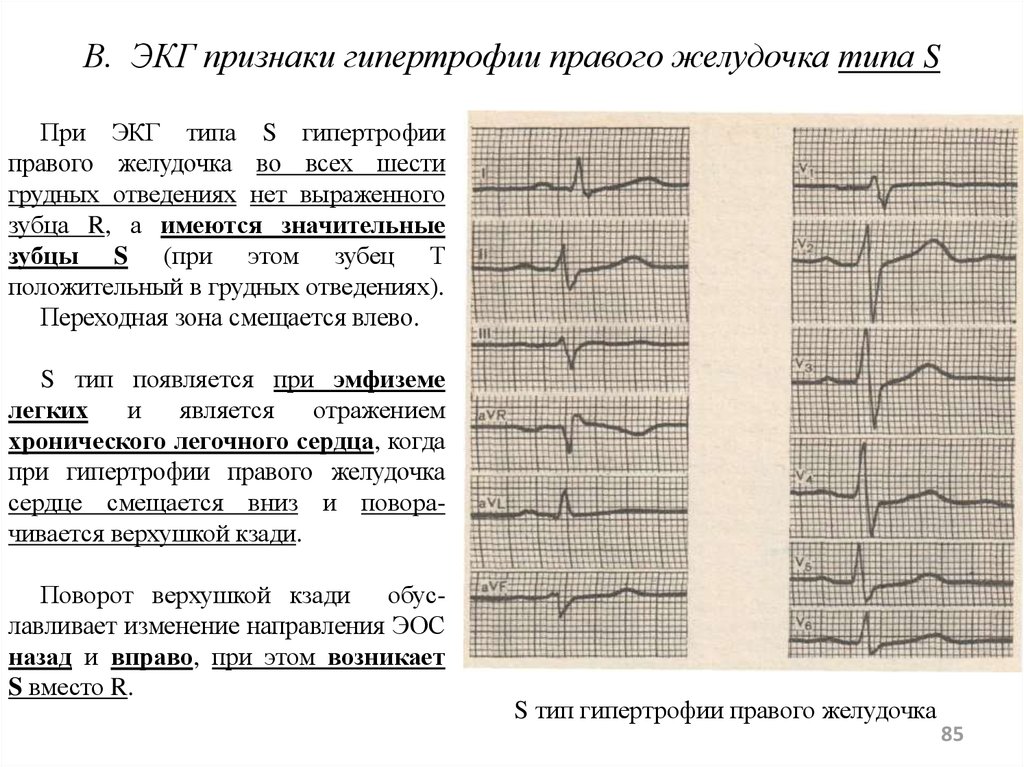
Гипертрофия левого желудочка у лиц без артериальной гипертензии: психосоматический подход к изучению данного феномена | Бастриков
1. Андрющенко А.В., Дробижев М.Ю., Добровольский А.В. Сравнительная оценка шкал CES-D, BDI и HADS(d) в диагностике депрессий в общемедицинской практике // Журнал неврологии и психиатрии. -2003. — № 5. — С. 11-18
2. Бастриков О.Ю. Показатели липопротеинового обмена и их ассоциации с психоэмоциональными факторами у практически здоровых лиц // Российский медицинский журнал. — 2015. — Т. 21, № 1. — С. 24-27
3. Бастриков О.Ю., Белов В.В., Цейликман В.Э., Сумеркина В.А. Показатели эндотелиальной функции во взаимосвязи с психоэмоциональными факторами у практически здоровых лиц // Нейрохимия. — 2014. -Т. 31, № 2. — С. 158-163
4. Вассерман Л.И., Иовлев Б.В., Беребин М.А. Методика для диагностики уровня социальной фрустрированности и её практическое применение: методические рекомендации. — СПб., 2004. — 16 c
5. Вассерман Л.И., Иовлев Б.В., Исаева Е.Р., Трифонова Е.А., Щелкова О.Ю., Новожилова М.Ю., Вукс А.Я. Методика для психологической диагностики способов совладания со стрессовыми и проблемными для личности ситуациями: пособие для врачей и медицинских психологов. — СПб., 2009. — 37 с
— СПб., 2009. — 37 с
6. Дигурова И.И. Оценка адаптационных возможностей с помощью макро- и микрореологических показателей крови при экспериментальном стрессе у крыс // Вестник КрасГАУ — 2009. — № 6. — C. 102-105
7. Дорошенко А.С., Солодков А.П., Шебеко В.И. Влияние N-ацетил-L-цистеина на ауторегуляцию коронарного кровотока при стрессе различной продолжительности // Вестник ВГМУ — 2004. — Т. 3, № 2. — С. 25-38.
8. Калюжин В.В., Тепляков А.Т., Соловцов М.А., Калюжина Е.В., Беспалова И.Д., Терентьева Н.Н. Ремоделирование левого желудочка: один или несколько сценариев // Бюллетень сибирской медицины. 2016. — T. 15, № 4. — С. 120-139
9. Конради А.О. Лечение артериальной гипертензии в особых группах больных. Гипертрофия левого желудочка // Артериальная гипертензия. — 2005. -Т. 11, № 2. — С. 105-109
10. Маник И.М. Гемодинамические и гуморальные факторы нормострессовой и гиперстрессовой гипертрофии левого желудочка при умеренной артериальной гипертензии // Вестник Харьковского национального университета. — 2009. — Вып. 17, № 855. — С. 21-33
11. Меерсон Ф.З. Гиперфункция. Гипертрофия. Недостаточность сердца. — М.: Медицина, 1968. — 388 с
12. Панин Л.Е. Обмен липопротеинов и атеросклероз // Бюл. СО РАМН. — 2006. — Т. 120, № 2. С. 15-22
13. Рубинштейн С.Я. Экспериментальные методики патопсихологии и опыт применения их в клинике: Практическое руководство. — СПб., 1998. — 168 c
— СПб., 1998. — 168 c
14. Ханин Ю.Л. Краткое руководство к применению шкалы реактивной и личностной тревожности Ч.Д. Спилбергера. — Л.: ЛНИИ ФК, 1976. — 18 с
15. Хныченко Л.К., Сапронов Н.С. Стресс и его роль в развитии патологических процессов // Обзоры по клинической фармакологии и лекарственной терапии. — 2003. — Т. 2, № 3. — С. 2-15
16. Штемберг А.С. Социальный стресс и психологическое состояние населения России. Часть 1. Общественно-политические процессы, формирующие социальный стресс // Пространство и время. — 2014. -Т. 15, № 1. — С. 187-195
17. Cuspidi C, Quarti F, Dell’Oro R, Facchetti R, Bombelli M, Sala C, Tadic M, Grassi G, Mancia G. (2017). Long-term changes in left ventricular mass echocardiographic findings from a general population. J Hypertens, 35 (11), 2303-2309. doi: 10.1097/HJH.0000000000001453.
18. Ghiadoni L, Donald AE, Cropley M, Mullen MJ, Oakley G, Taylor M, O’Connor G, Betteridge J, Klein N, Steptoe A, Deanfield JE. (2000). Mental stress induces transient endothelial dysfunction in humans. Circulation, 102 (20), 2473-2478.
19. Holmes Т, Rahe R. (1967) The social readjustment rating scale. J Psychosom Res, (11), 213-218.
20. Schirmer H, Lunde P, Rasmussen K. (1999). Prevalence of left ventricular hypertrophy in a general population. The Tromsø Study. Eur Heart, 20 (6), 429-438.
Артериальная гипертензия (АГ)
Не смотря на то, что во всем мире ведется активное изучение артериальной _гипертензии (гипертонии), причины эссенциальной артериальной гипертензии до сих пор не установлены и в настоящее время считается, что это заболевание многофакторное, т. е. у него много причин. Большое значение имеет наследственная предрасположенность. Доказано повышение тонуса мелких артерий в ответ на длительное психоэмоциональное напряжение. Существует теория, что повышенное потребление соли приводит к увеличению объема циркулирующей крови. Ожирение практически всегда сопровождается повышением артериального давления. Более того, в некоторых исследованиях показано, что снижение массы тела на 10 кг приводит к снижению давления минимум на 10 мм рт ст. На сегодняшний день выделяют три степени АГ, За нормальное артериальное давление принят уровень ниже 130/85 мм рт ст. Уровень артериального давления 130-139/85-89 считается повышенным нормальным: 1 степень АГ: 140-159/90-99; 2 степень АГ: 160-179/100-1094; 3 степень АГ: более 180/110; Диагноз артериальной гипертензии ставится при обнаружении артериального давления выше 140/90 мм рт ст. не менее двух раз при повторных визитах к врачу. Артериальное давление измеряется в положении сидя. У пожилых рекомендуется измерение АД и в положении стоя. Приборы для измерения давления в медицинских учреждениях всегда проверяются и калибруются. Необходимо делать это периодически и с домашними измерителями АД. Кроме степени АГ в диагнозе указывается еще степень риска. При определении степени риска учитывается очень много факторов: пол, возраст, цифры холестерина в крови, ожирение, наличие заболеваний с АГ у родственников, курение, малоподвижный образ жизни, поражение органов мишеней. Органами-мишенями называются те органы, которые при артериальной гипертензии страдают в первую очередь. Это сердце, головной мозг, почки, сетчатка глаза и сосуды. Сердце. Так как нагрузка на сердечную мышцу при АГ увеличивается, происходит компенсаторная гипертрофия (увеличение) толщины мышцы сердца левого желудочка. Гипертрофия левого желудочка считается более важным фактором риска чем сахарный диабет, повышение холестерина в крови и курение. В условиях гипертрофии сердце нуждается в повышенном кровоснабжении, а резерв при АГ сокращается.
е. у него много причин. Большое значение имеет наследственная предрасположенность. Доказано повышение тонуса мелких артерий в ответ на длительное психоэмоциональное напряжение. Существует теория, что повышенное потребление соли приводит к увеличению объема циркулирующей крови. Ожирение практически всегда сопровождается повышением артериального давления. Более того, в некоторых исследованиях показано, что снижение массы тела на 10 кг приводит к снижению давления минимум на 10 мм рт ст. На сегодняшний день выделяют три степени АГ, За нормальное артериальное давление принят уровень ниже 130/85 мм рт ст. Уровень артериального давления 130-139/85-89 считается повышенным нормальным: 1 степень АГ: 140-159/90-99; 2 степень АГ: 160-179/100-1094; 3 степень АГ: более 180/110; Диагноз артериальной гипертензии ставится при обнаружении артериального давления выше 140/90 мм рт ст. не менее двух раз при повторных визитах к врачу. Артериальное давление измеряется в положении сидя. У пожилых рекомендуется измерение АД и в положении стоя. Приборы для измерения давления в медицинских учреждениях всегда проверяются и калибруются. Необходимо делать это периодически и с домашними измерителями АД. Кроме степени АГ в диагнозе указывается еще степень риска. При определении степени риска учитывается очень много факторов: пол, возраст, цифры холестерина в крови, ожирение, наличие заболеваний с АГ у родственников, курение, малоподвижный образ жизни, поражение органов мишеней. Органами-мишенями называются те органы, которые при артериальной гипертензии страдают в первую очередь. Это сердце, головной мозг, почки, сетчатка глаза и сосуды. Сердце. Так как нагрузка на сердечную мышцу при АГ увеличивается, происходит компенсаторная гипертрофия (увеличение) толщины мышцы сердца левого желудочка. Гипертрофия левого желудочка считается более важным фактором риска чем сахарный диабет, повышение холестерина в крови и курение. В условиях гипертрофии сердце нуждается в повышенном кровоснабжении, а резерв при АГ сокращается. Поэтому у больных с гипертрофией стенки левого желудочка сердца чаще развиваются инфаркт миокарда, сердечная недостаточность, нарушения ритма или наступает внезапная коронарная смерть. Мозг. Уже на ранних стадиях АГ кровоснабжение головного мозга может снижаться. Появляется головная боль, головокружение, снижение работоспособности, шум в голове. В глубоких отделах мозга при длительном течении АГ происходят маленькие инфаркты (лакунарные), из-за нарушенного кровоснабжения масса мозга может уменьшаться. Это проявляется интеллектуальным снижением, нарушениями памяти, в далеко зашедших случаях деменцией (слабоумием). Почки. Происходит постепенный склероз сосудов и тканей почек. Нарушается их выделительная функция. В крови повышается количество продуктов обмена мочевины, в моче появляется белок. В конечном итоге возможна хроническая почечная недостаточность. При АГ выражаются также практически все сосуды. В зависимости от наличия этих факторов риск бывает 1, 2 или 3 степени: 1степень риска (низкий риск) означает, что вероятность сердечно- сосудистых осложнений у этого пациента составляет менее 15% в течение ближайших 10 лет; 2степень риска (средний риск) предполагает вероятность осложнений 15-20% в течение 10 лет; 3степень риска (высокий риск) — 20-30%; 4степень риска (очень высокий риск) предполагает вероятность осложнений более 30% в течение ближайших 10 лет; Лечение артериальной гипертензии В случае впервые выявленной артериальной гипертензии необходимо провести подробное исследование для исключения других болезней, которые могли вызвать повышение артериального давления, оценить факторы риска. При АГ первой степени и низких степенях риска назначают немедикаментозное лечение. В первую очередь это изменение образа жизни.Уменьшение употребления поваренной соли до 4,5 г в сутки. Прекратить или хотя бы уменьшить потребление алкоголя до 20-30 г чистого этанола в день для мужчин, что соответствует 200-250 мл сухого вина, 500-600 мл пива и 10-20 г чистого этанола для женщин. Отказ от курения.
Поэтому у больных с гипертрофией стенки левого желудочка сердца чаще развиваются инфаркт миокарда, сердечная недостаточность, нарушения ритма или наступает внезапная коронарная смерть. Мозг. Уже на ранних стадиях АГ кровоснабжение головного мозга может снижаться. Появляется головная боль, головокружение, снижение работоспособности, шум в голове. В глубоких отделах мозга при длительном течении АГ происходят маленькие инфаркты (лакунарные), из-за нарушенного кровоснабжения масса мозга может уменьшаться. Это проявляется интеллектуальным снижением, нарушениями памяти, в далеко зашедших случаях деменцией (слабоумием). Почки. Происходит постепенный склероз сосудов и тканей почек. Нарушается их выделительная функция. В крови повышается количество продуктов обмена мочевины, в моче появляется белок. В конечном итоге возможна хроническая почечная недостаточность. При АГ выражаются также практически все сосуды. В зависимости от наличия этих факторов риск бывает 1, 2 или 3 степени: 1степень риска (низкий риск) означает, что вероятность сердечно- сосудистых осложнений у этого пациента составляет менее 15% в течение ближайших 10 лет; 2степень риска (средний риск) предполагает вероятность осложнений 15-20% в течение 10 лет; 3степень риска (высокий риск) — 20-30%; 4степень риска (очень высокий риск) предполагает вероятность осложнений более 30% в течение ближайших 10 лет; Лечение артериальной гипертензии В случае впервые выявленной артериальной гипертензии необходимо провести подробное исследование для исключения других болезней, которые могли вызвать повышение артериального давления, оценить факторы риска. При АГ первой степени и низких степенях риска назначают немедикаментозное лечение. В первую очередь это изменение образа жизни.Уменьшение употребления поваренной соли до 4,5 г в сутки. Прекратить или хотя бы уменьшить потребление алкоголя до 20-30 г чистого этанола в день для мужчин, что соответствует 200-250 мл сухого вина, 500-600 мл пива и 10-20 г чистого этанола для женщин. Отказ от курения. Снизить вес тела. Исследования показывают, что при снижении веса тела на 10 кг артериальное давление снижается на 10 мм рт ст. В пище должно присутствовать много фруктов, овощей, продуктов, богатых калием, кальцием, магнием, морепродуктов. Доказано положительное влияние физической нагрузки на течение артериальной гипертензии. Если степень АГ выше первой, или при первой степени АГ не удается достигнуть нормализации АД немедикаментозным путем, назначается медикаментозное лечение. Цель лечения АГ — максимальное снижение риска сердечно-сосудистых осложнений и смертности, что достигается снижением артериального давления до целевых цифр — менее 130/90 и коррекцией других факторов риска. Используется шесть основных классов антигипертензивных препаратов: диуретики, бета-блокаторы, антагонисты кальция, ингибиторы ангиотензинпревращающего фермента, блокаторы альфа-1-адренэргических рецепторов и блокаторы рецепторов ангиотензина П. Все они имеют свои показания, противопоказания и назначать их должен только врач с учетом возраста, степени и риска АГ сопутствующих заболеваний. Препарат должен не только снижать уровень АД, но и облегчать состояние. Если одного препарата недостаточно, могут назначаться комбинации из двух и более препаратов. Пациент не должен забывать, что лечение артериальной гипертензии длительное, практически пожизненное. Если пациент не принимает препараты вовремя или делает перерывы в лечении, он усугубляет свое состояние.
Снизить вес тела. Исследования показывают, что при снижении веса тела на 10 кг артериальное давление снижается на 10 мм рт ст. В пище должно присутствовать много фруктов, овощей, продуктов, богатых калием, кальцием, магнием, морепродуктов. Доказано положительное влияние физической нагрузки на течение артериальной гипертензии. Если степень АГ выше первой, или при первой степени АГ не удается достигнуть нормализации АД немедикаментозным путем, назначается медикаментозное лечение. Цель лечения АГ — максимальное снижение риска сердечно-сосудистых осложнений и смертности, что достигается снижением артериального давления до целевых цифр — менее 130/90 и коррекцией других факторов риска. Используется шесть основных классов антигипертензивных препаратов: диуретики, бета-блокаторы, антагонисты кальция, ингибиторы ангиотензинпревращающего фермента, блокаторы альфа-1-адренэргических рецепторов и блокаторы рецепторов ангиотензина П. Все они имеют свои показания, противопоказания и назначать их должен только врач с учетом возраста, степени и риска АГ сопутствующих заболеваний. Препарат должен не только снижать уровень АД, но и облегчать состояние. Если одного препарата недостаточно, могут назначаться комбинации из двух и более препаратов. Пациент не должен забывать, что лечение артериальной гипертензии длительное, практически пожизненное. Если пациент не принимает препараты вовремя или делает перерывы в лечении, он усугубляет свое состояние.
ФАКТОРЫ РИСКА РАЗВИТИЯ ГИПЕРТРОФИИ МИОКАРДА ЛЕВОГО ЖЕЛУДОЧКА У БОЛЬНЫХ ПОДАГРОЙ | Маркелова
1. <div><p>Lorell B.H. Transition from hypertrophy to failure. Circulation 1997; 96: 3824—7.</p><p>Molkentin J.D., Olson E.N. GATA4: a novel transcriptional regulator of cardiac hypertrophy? Circulation 1997; 96: 3833—5.</p><p>Levy D., Garrison R.J., Savage D.D. et al. Prognostic implications of echocardiographically determined left ventricular mass in the Framingham Heart Study. N Engl J Med 1990; 322(22): 1561—6.</p><p>Koren M., Richard B., Devereux M. et al. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension. Ann Intern Med 1991; 114: 345—52.</p><p>Российское медицинское общество по артериальной гипертонии. Диагностика и лечение артериальной гипертензии. Российские рекомендации (4-й пересмотр). Системн. гипертенз. 2010; 3: 5—33.</p><p>Vakili B., Okin P., Devereux R. Prognostic implications of left ventricular hypertrophy. Am Heart J 2001; 141: 334—41.</p><p>Bikkina M., Levy D., Evans J. et al. Left ventricular mass and the risk the stroke in elderly cohort: The Framingham Study. JAMA 1994; 272: 33—6.</p><p>Mensah G., Pappas T., Koren M. et al. Comparison of classification severity by blood pressure level and World Health Organization for prediction concurrent cardiac abnormalities and subsequent complications in essential hypertension. J Hypertens 1993; 11: 1429—30.</p><p>Simone G., Mureddu G., Greco R. et al. Relation of left ventricular geometry and function to body composition in children with high causal blood pressure. Hypertension 1997; 30(P 1): 377—82.</p><p>Koren M., Ulin R., Laragh J., Devereux R. Changes in LVH predict risk in essential hypertension. Circulation 1990; 83(Suppl. III): 27—9.</p><p>Bots M.L., Nikitin Y., Salonen J.T. et al. Left ventricular hypertrophy and risk of fatal and non-fatal stroke. EUROSTROKE: a collaborative study among research centres in Europe. J Epidemiol Commun Health 2002; 56(Suppl. 1): 8—13.</p><p>Kuzell W.C., Schaffarzick R.W., Naugler W.E. et al. Some observations on 520 gouty patients. J Chronic Dis 1995; 2: 645—69.</p><p>Vazguez-Mellado J., Garsia C.G., Vazguez S.G. et al. Metabolic syndrome and ischemic heart disease in gout. J Clin Rheumatol 2004; 10(3): 105—9.</p><p>Ильина А.Е., Барскова В.Г., Насонов Е.
N Engl J Med 1990; 322(22): 1561—6.</p><p>Koren M., Richard B., Devereux M. et al. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension. Ann Intern Med 1991; 114: 345—52.</p><p>Российское медицинское общество по артериальной гипертонии. Диагностика и лечение артериальной гипертензии. Российские рекомендации (4-й пересмотр). Системн. гипертенз. 2010; 3: 5—33.</p><p>Vakili B., Okin P., Devereux R. Prognostic implications of left ventricular hypertrophy. Am Heart J 2001; 141: 334—41.</p><p>Bikkina M., Levy D., Evans J. et al. Left ventricular mass and the risk the stroke in elderly cohort: The Framingham Study. JAMA 1994; 272: 33—6.</p><p>Mensah G., Pappas T., Koren M. et al. Comparison of classification severity by blood pressure level and World Health Organization for prediction concurrent cardiac abnormalities and subsequent complications in essential hypertension. J Hypertens 1993; 11: 1429—30.</p><p>Simone G., Mureddu G., Greco R. et al. Relation of left ventricular geometry and function to body composition in children with high causal blood pressure. Hypertension 1997; 30(P 1): 377—82.</p><p>Koren M., Ulin R., Laragh J., Devereux R. Changes in LVH predict risk in essential hypertension. Circulation 1990; 83(Suppl. III): 27—9.</p><p>Bots M.L., Nikitin Y., Salonen J.T. et al. Left ventricular hypertrophy and risk of fatal and non-fatal stroke. EUROSTROKE: a collaborative study among research centres in Europe. J Epidemiol Commun Health 2002; 56(Suppl. 1): 8—13.</p><p>Kuzell W.C., Schaffarzick R.W., Naugler W.E. et al. Some observations on 520 gouty patients. J Chronic Dis 1995; 2: 645—69.</p><p>Vazguez-Mellado J., Garsia C.G., Vazguez S.G. et al. Metabolic syndrome and ischemic heart disease in gout. J Clin Rheumatol 2004; 10(3): 105—9.</p><p>Ильина А.Е., Барскова В.Г., Насонов Е. Л. Применение лозартана у больных подагрой. Кардиоваск. тер. и профилакт. 2008; 7(2): 51—3.</p><p>Weiss T.E., Segaloff A. Gouty arthritis and gout. Springfield, III: Thomas, 1959; 7.</p><p>Wyngaarden J.B., Kelley W.N. Gout and hyperuricemia. New York, 1976; 512.</p><p>The Bogalusa Heart Study: 20th Anniversary Symposium. Am J Med Sci 1995; 310(Suppl. 1): 1 — 138.</p><p>Alper A.B. Jr, Chen W., Yau L. et al. Childhood uric acid predicts adult blood pressure: the Bogalusa Heart Study. Hypertension 2005; 45: 34—8.</p><p>Sundström J., Sullivan L., D’Agostino R.B. et al. Relations of serum uric acid to longitudinal blood pressure tracking and hypertension incidence. Hypertension 2005; 45(1): 28—33.</p><p>Jossa F., Farinaro E., Panico S. et al. Serum uric acid and hypertension: the Olivetti heart study. J Hum Hypertens 1994; 8: 677—81.</p><p>Taniguchi Y., Hayashi T., Tsumura K. et al. Serum uric acid and the risk for hypertension and Type 2 diabetes in Japanese men: The Osaka Health Survey. J Hypertens 2001; 19(7): 1209—15.</p><p>Choi H.K., Atkinson K., Karlson E.W., Curhan G. Obesity, weight change, hypertension, diuretic use, and risk of gout in men: the health professionals follow-up study. Arch Intern Med 2005; 165(7): 742—8.</p><p>Kang D.-H., Nakagawa T., Feng L. et al. A role for uric acid in the progression of renal disease. J Am Soc Nephrol 2002; 13: 2888-97.</p><p>Johnson R.J., Kang D.-N., Feig D. et al. Is there a pathogenetic role for uric acid in hypertension and cardiovascular and renal disease? Hypertension 2003; 41: 1183-90.</p><p>Johnson R.J., Rodriguez-Iturbe B., Kang D.H. et al. A unifying pathway for essential hypertension. Am J Hypertens 2005; 18: 431—40.</p><p>Nakagawa Т., Mazzali M., Kang D.-H. et al. Hyperuricemia causes glomerular hypertrophy in the rat. Am J Nephrol 2003; 23: 2-7.</p><p>Mazzali M.
Л. Применение лозартана у больных подагрой. Кардиоваск. тер. и профилакт. 2008; 7(2): 51—3.</p><p>Weiss T.E., Segaloff A. Gouty arthritis and gout. Springfield, III: Thomas, 1959; 7.</p><p>Wyngaarden J.B., Kelley W.N. Gout and hyperuricemia. New York, 1976; 512.</p><p>The Bogalusa Heart Study: 20th Anniversary Symposium. Am J Med Sci 1995; 310(Suppl. 1): 1 — 138.</p><p>Alper A.B. Jr, Chen W., Yau L. et al. Childhood uric acid predicts adult blood pressure: the Bogalusa Heart Study. Hypertension 2005; 45: 34—8.</p><p>Sundström J., Sullivan L., D’Agostino R.B. et al. Relations of serum uric acid to longitudinal blood pressure tracking and hypertension incidence. Hypertension 2005; 45(1): 28—33.</p><p>Jossa F., Farinaro E., Panico S. et al. Serum uric acid and hypertension: the Olivetti heart study. J Hum Hypertens 1994; 8: 677—81.</p><p>Taniguchi Y., Hayashi T., Tsumura K. et al. Serum uric acid and the risk for hypertension and Type 2 diabetes in Japanese men: The Osaka Health Survey. J Hypertens 2001; 19(7): 1209—15.</p><p>Choi H.K., Atkinson K., Karlson E.W., Curhan G. Obesity, weight change, hypertension, diuretic use, and risk of gout in men: the health professionals follow-up study. Arch Intern Med 2005; 165(7): 742—8.</p><p>Kang D.-H., Nakagawa T., Feng L. et al. A role for uric acid in the progression of renal disease. J Am Soc Nephrol 2002; 13: 2888-97.</p><p>Johnson R.J., Kang D.-N., Feig D. et al. Is there a pathogenetic role for uric acid in hypertension and cardiovascular and renal disease? Hypertension 2003; 41: 1183-90.</p><p>Johnson R.J., Rodriguez-Iturbe B., Kang D.H. et al. A unifying pathway for essential hypertension. Am J Hypertens 2005; 18: 431—40.</p><p>Nakagawa Т., Mazzali M., Kang D.-H. et al. Hyperuricemia causes glomerular hypertrophy in the rat. Am J Nephrol 2003; 23: 2-7.</p><p>Mazzali M. , Hughes J., Kim Y.G. et al. Elevated uric acid increases blood pressure in the rat by a novel crystal-independent mechanism. Hypertension 2001; 38(5): 1101—6.</p><p>Mazzali M., Kanellis J., Han L. et al. Hyperuricemia induces a primary renal arteriolopathy in rats by a blood pressure-independent mechanism. Am J Physiol Renal Physiol 2002; 6: 991-7.</p><p>Alderman M.N., Cohen H., Madhvan S. et al. Serum uric acid and cardiovascular events in successfully treated hypertensive patients. Hypertension 1999; 34: 144-50.</p><p>Campo C., Ruilope L.M., Segura J. et al. Hyperuricemia, low urine urate excretion and target organ damage in arterial hypertension. Blood Press 2003; 12: 277-83.</p><p>Viazzi F., Parodi D., Leoncini G. et al. Serum uric acid and target organ damage in primary hypertension. Hypertension 2005; 45: 991—6.</p><p>Iribarren C., Folsom A.R., Eckfeldt J.H. et al. Correlates of uric acid and its association with asymptomatic carotid atherosclerosis: the ARIC study. Ann Epidemiol 1996; 6: 331-40.</p><p>Cuspidi C., Valerio C., Sala C. et al. Lack of association between serum uric acid and organ damage in a never-treated essential hypertensive population at low prevalence of hyperuricemia. Am J Hypertens 2007; 20: 678—85.</p><p>Dahlof B., Devereux R.B., Kjeldsen S.E. et al. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol. Lancet 2002; 359: 995-1003.</p><p>Kuo C.-F., Yu K.-H., Luo S.-F. et al. Role of uric acid in the link between arterial stiffness and cardiac hypertrophy: a cross-sectional study. Rheumatology (Oxford) 2010; 49(6): 1189—96.</p><p>Tsioufis C., Stougiannos P., Kakkavas A. et al. Relation of left ventricular concentric remodeling to levels of C-reactive protein and serum amyloid A in patients with essential hypertension. Am J Cardiol 2005; 96(2): 252—6.
, Hughes J., Kim Y.G. et al. Elevated uric acid increases blood pressure in the rat by a novel crystal-independent mechanism. Hypertension 2001; 38(5): 1101—6.</p><p>Mazzali M., Kanellis J., Han L. et al. Hyperuricemia induces a primary renal arteriolopathy in rats by a blood pressure-independent mechanism. Am J Physiol Renal Physiol 2002; 6: 991-7.</p><p>Alderman M.N., Cohen H., Madhvan S. et al. Serum uric acid and cardiovascular events in successfully treated hypertensive patients. Hypertension 1999; 34: 144-50.</p><p>Campo C., Ruilope L.M., Segura J. et al. Hyperuricemia, low urine urate excretion and target organ damage in arterial hypertension. Blood Press 2003; 12: 277-83.</p><p>Viazzi F., Parodi D., Leoncini G. et al. Serum uric acid and target organ damage in primary hypertension. Hypertension 2005; 45: 991—6.</p><p>Iribarren C., Folsom A.R., Eckfeldt J.H. et al. Correlates of uric acid and its association with asymptomatic carotid atherosclerosis: the ARIC study. Ann Epidemiol 1996; 6: 331-40.</p><p>Cuspidi C., Valerio C., Sala C. et al. Lack of association between serum uric acid and organ damage in a never-treated essential hypertensive population at low prevalence of hyperuricemia. Am J Hypertens 2007; 20: 678—85.</p><p>Dahlof B., Devereux R.B., Kjeldsen S.E. et al. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol. Lancet 2002; 359: 995-1003.</p><p>Kuo C.-F., Yu K.-H., Luo S.-F. et al. Role of uric acid in the link between arterial stiffness and cardiac hypertrophy: a cross-sectional study. Rheumatology (Oxford) 2010; 49(6): 1189—96.</p><p>Tsioufis C., Stougiannos P., Kakkavas A. et al. Relation of left ventricular concentric remodeling to levels of C-reactive protein and serum amyloid A in patients with essential hypertension. Am J Cardiol 2005; 96(2): 252—6. </p><p>Schumacher H.R. Jr. Crystal-induced arthritis: an overview. Am J Med 1996; 100: 46-52.</p><p>Reichek N., Devereux R.B. Left ventricular hypertrophy: relationship of anatomic, echocardiographic and electrocardiographic findings. Circulation 1981; 63: 1391-8.</p><p>Wallace S.L., Robinson H., Masi A.T. et al. Preliminary criteria for the classification of the acute arthritis of gout. Arthr Rheum 1977; 20: 895—900.</p><p>World Health Organization (WHO). Obesity: prevention and management of the global epidemic. Report of the WHO Consultation. World Health Organ Tech. Rep Ser 2000; 894(i—xii): 1 —253.</p><p>World Health Organization (WHO). Prevention and management of the global epidemic of obesity. Report of the WHO Consultation on Obesity. Geneva: WHO, 1997.</p><p>Seidell J. Obesity in Europe. Obes Res 1995; 3(Suppl. 2): 89s—93s.</p><p>Stern J., Hirsch J., Blair S. et al. Weighting the options: criteria for evaluating weight-management programs. The Committee to Develop Criteria for Evaluating the Outcomes of Approaches to Prevent and Treat Obesity. Obes Res 1995; 3(6): 591—604.</p><p>Mancia G., de Backer G., Dominiczak A. et al. Guidelines for the Management of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESC). J Hypertens 2007; 25(6): 1105—87.</p><p>Devereux R.B., Alonso D.R., Lutas E.M. et al. Echocardiographic assessment of left ventricular hypertrophy: comparison to necropsy findings. Am J Cardiol 1986; 57(6): 450—8.</p><p>Lang R.M., Bierig M., Devereux R.B. et al.; Chamber Quantification Writing Group; American Society of Echocardiography’s Guidelines and Standards Committee; European Association of Echocardiography. Recommendations for chamber quantification: a report from the American Society of Echocardiography’s Guidelines and Standards Committee and the Chamber Quantification Writing Group.
</p><p>Schumacher H.R. Jr. Crystal-induced arthritis: an overview. Am J Med 1996; 100: 46-52.</p><p>Reichek N., Devereux R.B. Left ventricular hypertrophy: relationship of anatomic, echocardiographic and electrocardiographic findings. Circulation 1981; 63: 1391-8.</p><p>Wallace S.L., Robinson H., Masi A.T. et al. Preliminary criteria for the classification of the acute arthritis of gout. Arthr Rheum 1977; 20: 895—900.</p><p>World Health Organization (WHO). Obesity: prevention and management of the global epidemic. Report of the WHO Consultation. World Health Organ Tech. Rep Ser 2000; 894(i—xii): 1 —253.</p><p>World Health Organization (WHO). Prevention and management of the global epidemic of obesity. Report of the WHO Consultation on Obesity. Geneva: WHO, 1997.</p><p>Seidell J. Obesity in Europe. Obes Res 1995; 3(Suppl. 2): 89s—93s.</p><p>Stern J., Hirsch J., Blair S. et al. Weighting the options: criteria for evaluating weight-management programs. The Committee to Develop Criteria for Evaluating the Outcomes of Approaches to Prevent and Treat Obesity. Obes Res 1995; 3(6): 591—604.</p><p>Mancia G., de Backer G., Dominiczak A. et al. Guidelines for the Management of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESC). J Hypertens 2007; 25(6): 1105—87.</p><p>Devereux R.B., Alonso D.R., Lutas E.M. et al. Echocardiographic assessment of left ventricular hypertrophy: comparison to necropsy findings. Am J Cardiol 1986; 57(6): 450—8.</p><p>Lang R.M., Bierig M., Devereux R.B. et al.; Chamber Quantification Writing Group; American Society of Echocardiography’s Guidelines and Standards Committee; European Association of Echocardiography. Recommendations for chamber quantification: a report from the American Society of Echocardiography’s Guidelines and Standards Committee and the Chamber Quantification Writing Group. .. J Am Soc Echocardiogr 2005; 18(12): 1440—63.</p><p>Васюк Ю.А. Функциональная диагностика в кардиологии: клиническая интерпретация. М.: Практическая медицина, 2009; 312 с.</p><p>Schillaci G., Verdecchia P., Porcellatti C. et al. Continuous relation between left ventricular mass and cardiovascular risk is essential hypertension. Hypertension 2000; 35: 580-6.</p><p>Gottdienner J.S., Reda D.J., Materson B.J. et al. Importance of obesity, race and age to the cardiac structural and functional effects of hypertension. J Am Coll Cardiol 1994; 24: 1492-8.</p><p>Poirier P., Giles T., Bray G. et al. Obesity and cardiovascular disease: pathophysiology, evaluation, and effects of weight loss. An update of the 1997 american heart association scientific statement on obesity and heart disease from the obesity committee of the council on nutrition, physical activity, and metabolism. Circulation 2006; 113: 898—918.</p><p>Neves M.F., Schiffrin E.L. Aldosterone: A risk factor for vascular diseases. Cur Hypertens Rep 2003; 5: 59-65.</p><p>Sato A., Saruta T. Aldosterone escape during angiotensin-converting enzyme inhibitor therapy in essential hypertensive patients with left ventricular hypertrophy. J Intern Med Res 2001; 29: 13—21.</p><p>Hameedi A., Shadow H.L. The promise of selective aldosterone receptor antagonists for the treatment of Hypertension and Chronic Heart Failure. Cur Hypertens Rep 2000; 2: 378-83.</p><p>Мычка В.Б., Горностаев В.В., Шикина Н.Ю., Чазова И.Е. Артериальная гипертония и ожирение. Gons med 2001; 2(прил.): 17—22.</p><p>Braiser A.R., Resinos A., Eledrisi M.S. Vascular inflammation and the renin-angiotensin system. Arterioscler Thromb Vasc Biol 2002; 22: 1257—66.</p><p>Stenvinkel P. Endotelial dysfunction and inflammation — is there link? Nephrol Dial Transplant 2001; 16: 1968-71.</p><p>Krumholz H.M., Larson M., Levy D. Prognosis of left ventricular geometric patterns in the Framingham Heart Study.
.. J Am Soc Echocardiogr 2005; 18(12): 1440—63.</p><p>Васюк Ю.А. Функциональная диагностика в кардиологии: клиническая интерпретация. М.: Практическая медицина, 2009; 312 с.</p><p>Schillaci G., Verdecchia P., Porcellatti C. et al. Continuous relation between left ventricular mass and cardiovascular risk is essential hypertension. Hypertension 2000; 35: 580-6.</p><p>Gottdienner J.S., Reda D.J., Materson B.J. et al. Importance of obesity, race and age to the cardiac structural and functional effects of hypertension. J Am Coll Cardiol 1994; 24: 1492-8.</p><p>Poirier P., Giles T., Bray G. et al. Obesity and cardiovascular disease: pathophysiology, evaluation, and effects of weight loss. An update of the 1997 american heart association scientific statement on obesity and heart disease from the obesity committee of the council on nutrition, physical activity, and metabolism. Circulation 2006; 113: 898—918.</p><p>Neves M.F., Schiffrin E.L. Aldosterone: A risk factor for vascular diseases. Cur Hypertens Rep 2003; 5: 59-65.</p><p>Sato A., Saruta T. Aldosterone escape during angiotensin-converting enzyme inhibitor therapy in essential hypertensive patients with left ventricular hypertrophy. J Intern Med Res 2001; 29: 13—21.</p><p>Hameedi A., Shadow H.L. The promise of selective aldosterone receptor antagonists for the treatment of Hypertension and Chronic Heart Failure. Cur Hypertens Rep 2000; 2: 378-83.</p><p>Мычка В.Б., Горностаев В.В., Шикина Н.Ю., Чазова И.Е. Артериальная гипертония и ожирение. Gons med 2001; 2(прил.): 17—22.</p><p>Braiser A.R., Resinos A., Eledrisi M.S. Vascular inflammation and the renin-angiotensin system. Arterioscler Thromb Vasc Biol 2002; 22: 1257—66.</p><p>Stenvinkel P. Endotelial dysfunction and inflammation — is there link? Nephrol Dial Transplant 2001; 16: 1968-71.</p><p>Krumholz H.M., Larson M., Levy D. Prognosis of left ventricular geometric patterns in the Framingham Heart Study. J Am Coll Cardiol 1995; 25: 879—84.</p><p>Лазебник Л.Б., Комиссаренко И.А., Милюкова О.М. Систолическая артериальная гипертония у пожилых. Рус. мед. журн. 1997; 5(20): 6—9.</p><p>Devereux R.B., Roman M.J., de Simone G. et al. Relations of left ventricular mass to demographic and hemodynamic variables in american indians. Circulation 1997; 96: 1416-23.</p><p>Task Force of the European Society of Cardiology and North American Society of Pacing and Electrophysiology. Heart rate variability, standarts of measurements, physiological interpretation, and clinical use. Circulation 1996; 93: 1043-65.</p><p>Kannel W.B., Dannenberg A.L., Levy D. et al. Population implication of electrocardiographic left ventricular hypertrophy. Am J Cardiology 1987; 60: 851—931.</p><p>Sullivan J.M., Zwaag R.V., El-Zeky F. et at. Left ventricular hypertrophy: effect on survival. J Am Coll Cardiol 1993; 22(2): 508—13.</p><p>Verdecchia P., Schillaci G., Borgioni С. el al. Prognostic value of a new electrocardiographic method for diagnosis of left ventricular hypertrophy in essential hypertension. J Am Coll Cardiol 1998; 31(2): 383—90.</p></div><br />
J Am Coll Cardiol 1995; 25: 879—84.</p><p>Лазебник Л.Б., Комиссаренко И.А., Милюкова О.М. Систолическая артериальная гипертония у пожилых. Рус. мед. журн. 1997; 5(20): 6—9.</p><p>Devereux R.B., Roman M.J., de Simone G. et al. Relations of left ventricular mass to demographic and hemodynamic variables in american indians. Circulation 1997; 96: 1416-23.</p><p>Task Force of the European Society of Cardiology and North American Society of Pacing and Electrophysiology. Heart rate variability, standarts of measurements, physiological interpretation, and clinical use. Circulation 1996; 93: 1043-65.</p><p>Kannel W.B., Dannenberg A.L., Levy D. et al. Population implication of electrocardiographic left ventricular hypertrophy. Am J Cardiology 1987; 60: 851—931.</p><p>Sullivan J.M., Zwaag R.V., El-Zeky F. et at. Left ventricular hypertrophy: effect on survival. J Am Coll Cardiol 1993; 22(2): 508—13.</p><p>Verdecchia P., Schillaci G., Borgioni С. el al. Prognostic value of a new electrocardiographic method for diagnosis of left ventricular hypertrophy in essential hypertension. J Am Coll Cardiol 1998; 31(2): 383—90.</p></div><br />
Развитие гипертрофии левого желудочка связано с сахарным диабетом
Результаты исследования, опубликованные в июньском номере American Journal of Cardiology («Американский журнал кардиологии») свидетельствуют о наличии прямой связи между сахарным диабетом 2 типа и развитием гипертрофии левого желудочка (ГЛЖ).
Под руководством доктора Казуо Эгучи (Университетская медицинская школа, Тохиджи, Япония) было проведено трансторакальное эхокардиографическое исследование с определением массы ЛЖ у 1932 пациентов, входящих в состав многонациональной когорты исследования Nothern Manhattan Study (769 мужчин, средний возраст 67,9 лет). ГЛЖ определялась по 75 перцентилю массы ЛЖ.
У пациентов с СД (n = 443) масса левого желудочка была значительно выше, чем у пациентов без диабета (n = 1489) (189 г в сравнении с 174 г, p<0,0001). Больные СД также имели значительно большие значения индекса массы тела, окружности талии, уровня триглицеридов, частоты встречаемости артериальной гипертензии, изолированного повышения систолического АД и ИБС.
Больные СД также имели значительно большие значения индекса массы тела, окружности талии, уровня триглицеридов, частоты встречаемости артериальной гипертензии, изолированного повышения систолического АД и ИБС.
Многофакторный анализ выявил наличие прямой связи между наличием СД 2 типа и повышением массы ЛЖ (p = 0,03). Кроме того, наблюдалось повышение риска развития ГЛЖ у пациентов с СД в сочетании с увеличенной окружностью талии, но не с сочетанием диабета и повышенным индексом массы тела. По мнению исследователей, результаты свидетельствуют о том, что взаимосвязь диабета и ГЛЖ может быть частично объяснена влиянием СД на развитие центрального ожирения. Возможно, определенные типы адипоцитов, входящих в состав висцерального жира, способны напрямую влиять на развитие ГЛЖ.
Приведенные данные не только демонстрируют наличие связи между конкретными клиническими состояниями, но и в очередной раз свидетельствуют о важности правильного подбора терапии у пациентов из группы высокого метаболического риска. Назначение препаратов, благоприятно действующих на метаболический профиль, позволяет не только предотвратить прогрессирование сахарного диабета, но и препятствует развитию гипертрофии левого желудочка. В недавно проведенном анализе данных из крупного исследования BENEDICT, проведенного у больных с АГ и сахарным диабетом, исследователи сравнили частоту развития ГЛЖ на основании ЭКГ-признаков (Соколова-Лайона и Корнелла) у 816 пациентов с сахарным диабетом 2 типа. Больные были рандомизированы в группы и в течение 3-х лет получали два варианта терапии: 1 – содержащую иАПФ — трандолаприл (2мг/сутки), 2 — не содержащую иАПФ. Препараты титровались для достижения целевого АД, значение которого составляло <130/80 мм. рт. ст. Электрокардиография проводилась централизованно, ее результаты не оглашались до окончания исследования. Характеристики обеих групп в начале исследования были сравнимыми. Через 36 месяцев наблюдения у 13 из 423 пациентов (3,1%), получавших трандолаприл (Гоптен, Эбботт), и у 31 из 376 пациентов (8,2%), получавших терапию, не включавшую иАПФ, были диагностированы ЭКГ признаки ГЛЖ (P = 0,0018). Важно упомянуть, что при оценке достоверности различий принималась во внимание степень снижения АД в обеих группах. Таким образом, в исследовании было показано, что у 76% больных СД 2 типа Гоптен способен предотвратить развитие гипертрофии левого желудочка.
Важно упомянуть, что при оценке достоверности различий принималась во внимание степень снижения АД в обеих группах. Таким образом, в исследовании было показано, что у 76% больных СД 2 типа Гоптен способен предотвратить развитие гипертрофии левого желудочка.
Снижение риска развития ГЛЖ на фоне лечения трандолаприлом
Это позволяет говорить о том, что раннее назначение иАПФ пациентам с сочетанием АГ и сахарного диабета может предупредить развитие грозных сердечно-сосудистых осложнений.
Метаболический синдром влияет на развитие ГЛЖ независимо от уровня артериального давления
По данным шведских ученых, опубликованных в июльском номере журнала Heart, повышенная масса левого желудочка у пациентов с метаболическим синдромом связана с наличием резистентности к инсулину (РИ).
Главный исследователь – доктор Йохан Сандстром заявил, что ожирение и сопутствующие ему патологические изменения, такие как резистентность к инсулину и повышение его уровня в крови, предположительно играют роль в развитии гипертрофии левого желудочка. До настоящего момента из-за недостатков дизайна проведенных ранее исследований эту роль было сложно оценить, в связи со сложностью дифференцировки эффекта РИ и влияния на гипертрофию ЛЖ повышенного уровня АД.
С целью проверки упомянутой гипотезы доктор Сандстром с коллегами из Университета Уппсала (Uppsala) провели исследование с участием 820 мужчин и женщин в возрасте 70 лет без признаков сердечной недостаточности, клапанной патологии и инфаркта миокарда. 19% мужчин и 22% женщин имели метаболический синдром.
Индекс массы левого желудочка был повышен как у пациентов с АГ, так и у нормотензивных пациентов с метаболическим синдромом. В основном это проявлялось в увеличении относительной толщины стенки ЛЖ.
Кроме того, была выявлена статистически значимая связь между массой левого желудочка и показателями резистентности к инсулину. У нормотензивных пациентов значимость связи была пограничной. Резистентность к инсулину также была связана с повышением относительной толщины стенки ЛЖ, причем как у нормотензивных пациентов, так и у пациентов с артериальной гипертензией.
Резистентность к инсулину также была связана с повышением относительной толщины стенки ЛЖ, причем как у нормотензивных пациентов, так и у пациентов с артериальной гипертензией.
По мнению доктора Сандстрома, результаты указывают на то, что ожирение может оказывать отрицательное влияние на сердце, независимо от эффектов, обусловленных повышением АД.
Исследователи заключили, что, если полученные данные найдут подтверждение, резистентность к инсулину должна быть включена в список гемодинамически-независимых факторов, неблагоприятно влияющих на геометрию сердца наряду с другими нейрогуморальными звеньями, такими как компоненты РААС.
Скачать статью (в формате .pdf, откроется в новом окне)
Otsenka effektivnosti moeksiprila u bol’nykh myagkoy i umerennoy arterial’noy gipertoniey s gipertrofiey miokarda levogo zheludochka (issledovanie ENIGMA) | Belenkov
Артериальной гипертонией (АГ) страдают 15–25% взрослого населения. Наличие АГ существенно влияет на состояние здоровья, продолжительность и качество жизни пациентов, так как заболевание является основным фактором риска развития сердечно-сосудистых осложнений. Подобно головному мозгу и почкам, сердце участвует в патогенезе АГ и одновременно является органом-мишенью. Наиболее частыми изменениями сердца при АГ являются гипертрофия левого желудочка (ГЛЖ), которая встречается у 25–30% больных АГ и диастолическая дисфункция левого желудочка (ЛЖ). Доказано, что ГЛЖ при АГ является независимым фактором риска сердечно-сосудистой заболеваемости и смертности, а также основным доклиническим проявлением поражения сердечно-сосудистой системы, которое повышает риск ишемической болезни сердца (ИБС) и инфаркта миокарда, инсульта и застойной сердечной недостаточности, внезапной смерти и общей смертности [1–9]. По данным Корнельского и Фрамингемского исследований, при наличии ГЛЖ риск смертельных и несмертельных осложнений повышается в 2–4 раза независимо от возраста, пола и других факторов риска [4, 8]. Частота выявления ГЛЖ у больных АГ повышается с возрастом (от 6% в возрасте до 30 лет до 43% после 70 лет), встречается у 23–33% лиц старше 59 лет [1] и у 23% у мужчин и 33% женщин старше 59 лет [10]. Кроме того, частота выявления ГЛЖ зависит от тяжести АГ (от 20% при мягкой до 50% и более при тяжелой) и применяемого метода исследования: от 7% по данным электрокардиографии (ЭКГ) до 45% по данным эхокардиографии (ЭхоКГ) и 70% магнитно-резонансной (МР) и вентрикулографии [11–14]. ЭхоКГ является более точным неинвазивным методом определения массы миокарда левого желудочка (ММЛЖ), чем традиционные методы. Данные о ММЛЖ, полученные ЭхоКГ-методом тесно коррелируют с данными аутопсии [14]. ЭхоКГ позволяет не только выявлять ГЛЖ, но и следить за ее динамикой при лечении АГ [4, 15, 16]. Считается, что метод ЭхоКГ дает 10% погрешность в измерении индекса ММЛЖ (ИММЛЖ), поэтому достоверной динамикой ИММЛЖ на фоне лечения могут считаться только изменения более 10%. Требования к антигипертензивной терапии включают в себя достижение целевого уровня артериального давления (АД) и обеспечение протективного действия на органы-мишени. Таким образом, оптимизация лечения больных АГ, ставящая своей целью не только снижение АД, но и органопротекцию с применением современных антигипертензивных препаратов, остается актуальной задачей. Цель исследования: оценить эффективность и переносимость монотерапии моэксиприлом (моэкс, “Schwarz Parma AG”, Германия) в дозе 7,5–15 мг/сут или в комбинации его с гидрохлортиазидом (ГХТ) в дозе 12,5–25 мг/сут у пациентов с мягкой и умеренной АГ, имеющих ГЛЖ во время активного лечения в течение 52 нед.
Частота выявления ГЛЖ у больных АГ повышается с возрастом (от 6% в возрасте до 30 лет до 43% после 70 лет), встречается у 23–33% лиц старше 59 лет [1] и у 23% у мужчин и 33% женщин старше 59 лет [10]. Кроме того, частота выявления ГЛЖ зависит от тяжести АГ (от 20% при мягкой до 50% и более при тяжелой) и применяемого метода исследования: от 7% по данным электрокардиографии (ЭКГ) до 45% по данным эхокардиографии (ЭхоКГ) и 70% магнитно-резонансной (МР) и вентрикулографии [11–14]. ЭхоКГ является более точным неинвазивным методом определения массы миокарда левого желудочка (ММЛЖ), чем традиционные методы. Данные о ММЛЖ, полученные ЭхоКГ-методом тесно коррелируют с данными аутопсии [14]. ЭхоКГ позволяет не только выявлять ГЛЖ, но и следить за ее динамикой при лечении АГ [4, 15, 16]. Считается, что метод ЭхоКГ дает 10% погрешность в измерении индекса ММЛЖ (ИММЛЖ), поэтому достоверной динамикой ИММЛЖ на фоне лечения могут считаться только изменения более 10%. Требования к антигипертензивной терапии включают в себя достижение целевого уровня артериального давления (АД) и обеспечение протективного действия на органы-мишени. Таким образом, оптимизация лечения больных АГ, ставящая своей целью не только снижение АД, но и органопротекцию с применением современных антигипертензивных препаратов, остается актуальной задачей. Цель исследования: оценить эффективность и переносимость монотерапии моэксиприлом (моэкс, “Schwarz Parma AG”, Германия) в дозе 7,5–15 мг/сут или в комбинации его с гидрохлортиазидом (ГХТ) в дозе 12,5–25 мг/сут у пациентов с мягкой и умеренной АГ, имеющих ГЛЖ во время активного лечения в течение 52 нед.
Артериальной гипертонией (АГ) страдают 15–25% взрослого населения. Наличие АГ существенно влияет на состояние здоровья, продолжительность и качество жизни пациентов, так как заболевание является основным фактором риска развития сердечно-сосудистых осложнений. Подобно головному мозгу и почкам, сердце участвует в патогенезе АГ и одновременно является органом-мишенью. Наиболее частыми изменениями сердца при АГ являются гипертрофия левого желудочка (ГЛЖ), которая встречается у 25–30% больных АГ и диастолическая дисфункция левого желудочка (ЛЖ). Доказано, что ГЛЖ при АГ является независимым фактором риска сердечно-сосудистой заболеваемости и смертности, а также основным доклиническим проявлением поражения сердечно-сосудистой системы, которое повышает риск ишемической болезни сердца (ИБС) и инфаркта миокарда, инсульта и застойной сердечной недостаточности, внезапной смерти и общей смертности [1–9]. По данным Корнельского и Фрамингемского исследований, при наличии ГЛЖ риск смертельных и несмертельных осложнений повышается в 2–4 раза независимо от возраста, пола и других факторов риска [4, 8]. Частота выявления ГЛЖ у больных АГ повышается с возрастом (от 6% в возрасте до 30 лет до 43% после 70 лет), встречается у 23–33% лиц старше 59 лет [1] и у 23% у мужчин и 33% женщин старше 59 лет [10]. Кроме того, частота выявления ГЛЖ зависит от тяжести АГ (от 20% при мягкой до 50% и более при тяжелой) и применяемого метода исследования: от 7% по данным электрокардиографии (ЭКГ) до 45% по данным эхокардиографии (ЭхоКГ) и 70% магнитно-резонансной (МР) и вентрикулографии [11–14]. ЭхоКГ является более точным неинвазивным методом определения массы миокарда левого желудочка (ММЛЖ), чем традиционные методы. Данные о ММЛЖ, полученные ЭхоКГ-методом тесно коррелируют с данными аутопсии [14]. ЭхоКГ позволяет не только выявлять ГЛЖ, но и следить за ее динамикой при лечении АГ [4, 15, 16]. Считается, что метод ЭхоКГ дает 10% погрешность в измерении индекса ММЛЖ (ИММЛЖ), поэтому достоверной динамикой ИММЛЖ на фоне лечения могут считаться только изменения более 10%. Требования к антигипертензивной терапии включают в себя достижение целевого уровня артериального давления (АД) и обеспечение протективного действия на органы-мишени. Таким образом, оптимизация лечения больных АГ, ставящая своей целью не только снижение АД, но и органопротекцию с применением современных антигипертензивных препаратов, остается актуальной задачей.
Подобно головному мозгу и почкам, сердце участвует в патогенезе АГ и одновременно является органом-мишенью. Наиболее частыми изменениями сердца при АГ являются гипертрофия левого желудочка (ГЛЖ), которая встречается у 25–30% больных АГ и диастолическая дисфункция левого желудочка (ЛЖ). Доказано, что ГЛЖ при АГ является независимым фактором риска сердечно-сосудистой заболеваемости и смертности, а также основным доклиническим проявлением поражения сердечно-сосудистой системы, которое повышает риск ишемической болезни сердца (ИБС) и инфаркта миокарда, инсульта и застойной сердечной недостаточности, внезапной смерти и общей смертности [1–9]. По данным Корнельского и Фрамингемского исследований, при наличии ГЛЖ риск смертельных и несмертельных осложнений повышается в 2–4 раза независимо от возраста, пола и других факторов риска [4, 8]. Частота выявления ГЛЖ у больных АГ повышается с возрастом (от 6% в возрасте до 30 лет до 43% после 70 лет), встречается у 23–33% лиц старше 59 лет [1] и у 23% у мужчин и 33% женщин старше 59 лет [10]. Кроме того, частота выявления ГЛЖ зависит от тяжести АГ (от 20% при мягкой до 50% и более при тяжелой) и применяемого метода исследования: от 7% по данным электрокардиографии (ЭКГ) до 45% по данным эхокардиографии (ЭхоКГ) и 70% магнитно-резонансной (МР) и вентрикулографии [11–14]. ЭхоКГ является более точным неинвазивным методом определения массы миокарда левого желудочка (ММЛЖ), чем традиционные методы. Данные о ММЛЖ, полученные ЭхоКГ-методом тесно коррелируют с данными аутопсии [14]. ЭхоКГ позволяет не только выявлять ГЛЖ, но и следить за ее динамикой при лечении АГ [4, 15, 16]. Считается, что метод ЭхоКГ дает 10% погрешность в измерении индекса ММЛЖ (ИММЛЖ), поэтому достоверной динамикой ИММЛЖ на фоне лечения могут считаться только изменения более 10%. Требования к антигипертензивной терапии включают в себя достижение целевого уровня артериального давления (АД) и обеспечение протективного действия на органы-мишени. Таким образом, оптимизация лечения больных АГ, ставящая своей целью не только снижение АД, но и органопротекцию с применением современных антигипертензивных препаратов, остается актуальной задачей. Цель исследования: оценить эффективность и переносимость монотерапии моэксиприлом (моэкс, “Schwarz Parma AG”, Германия) в дозе 7,5–15 мг/сут или в комбинации его с гидрохлортиазидом (ГХТ) в дозе 12,5–25 мг/сут у пациентов с мягкой и умеренной АГ, имеющих ГЛЖ во время активного лечения в течение 52 нед. Материал и методы В исследование включены 123 пациента с АГ, из которых за время наблюдения выбыло 6 больных, в том числе 3 – из-за развития побочных явлений (кашель). Полностью завершили исследование 117 пациентов (54 мужчины и 63 женщины), 32–65 лет (54,7±7,9 года), со средней длительностью АГ 11,9±8 лет и ГЛЖ, по данным ЭхоКГ. После 1 нед “чистого фона” среднее по группе систолическое АД (САД) клиническое (кл.) составило 165,1±10,5 мм рт. ст., диастолическое АД (ДАД) кл. – 99,2±8,5 мм рт. ст. Критериями исключения были: вторичные формы АГ, острое нарушение мозгового кровообращения, острый инфаркт миокарда в течение последних 6 мес, стенокардия II–III функционального класса (ФК), сердечная недостаточность, нарушения ритма сердца, функции печени и почек. Дизайн исследования: исследование было открытым, последовательным, сравнительным. Длительность наблюдения составила 52–54 нед. После 1 нед отмены предшествующей антигипертензивной терапии всем больным назначали моэксиприл в дозе 7,5 мг в сутки однократно утром. У больных, не достигших целевого уровня АД, через 3 нед дозу моэксиприла увеличивали вдвое (15 мг/сут), еще через 3 нед присоединяли ГХТ в дозе 12,5 мг/сут и через 6 нед увеличивали дозу ГХТ до 25 мг/сут. После достижения целевого уровня АД больные продолжали ту терапию, на которой оно было достигнуто. В случае выявления ускользания антигипертензивного эффекта терапии ее усиливали по вышеуказанной схеме. На всех визитах контролировали АД, частоту сердечных сокращений (ЧСС), регистрировали жалобы пациентов, отмечали побочные эффекты, если таковые имелись. Контрольные исследования анализов крови (К, Na, креатинин, мочевина) проводили через 6, 12 и 36 нед терапии.
Цель исследования: оценить эффективность и переносимость монотерапии моэксиприлом (моэкс, “Schwarz Parma AG”, Германия) в дозе 7,5–15 мг/сут или в комбинации его с гидрохлортиазидом (ГХТ) в дозе 12,5–25 мг/сут у пациентов с мягкой и умеренной АГ, имеющих ГЛЖ во время активного лечения в течение 52 нед. Материал и методы В исследование включены 123 пациента с АГ, из которых за время наблюдения выбыло 6 больных, в том числе 3 – из-за развития побочных явлений (кашель). Полностью завершили исследование 117 пациентов (54 мужчины и 63 женщины), 32–65 лет (54,7±7,9 года), со средней длительностью АГ 11,9±8 лет и ГЛЖ, по данным ЭхоКГ. После 1 нед “чистого фона” среднее по группе систолическое АД (САД) клиническое (кл.) составило 165,1±10,5 мм рт. ст., диастолическое АД (ДАД) кл. – 99,2±8,5 мм рт. ст. Критериями исключения были: вторичные формы АГ, острое нарушение мозгового кровообращения, острый инфаркт миокарда в течение последних 6 мес, стенокардия II–III функционального класса (ФК), сердечная недостаточность, нарушения ритма сердца, функции печени и почек. Дизайн исследования: исследование было открытым, последовательным, сравнительным. Длительность наблюдения составила 52–54 нед. После 1 нед отмены предшествующей антигипертензивной терапии всем больным назначали моэксиприл в дозе 7,5 мг в сутки однократно утром. У больных, не достигших целевого уровня АД, через 3 нед дозу моэксиприла увеличивали вдвое (15 мг/сут), еще через 3 нед присоединяли ГХТ в дозе 12,5 мг/сут и через 6 нед увеличивали дозу ГХТ до 25 мг/сут. После достижения целевого уровня АД больные продолжали ту терапию, на которой оно было достигнуто. В случае выявления ускользания антигипертензивного эффекта терапии ее усиливали по вышеуказанной схеме. На всех визитах контролировали АД, частоту сердечных сокращений (ЧСС), регистрировали жалобы пациентов, отмечали побочные эффекты, если таковые имелись. Контрольные исследования анализов крови (К, Na, креатинин, мочевина) проводили через 6, 12 и 36 нед терапии. Полный биохимический анализ крови (К, Na, креатинин, мочевина, общий белок, глюкоза, АСТ, АЛТ, общий билирубин), общий анализ крови, общий анализ мочи, суточное мониторирование АД (СМАД), ЭхоКГ и ЭКГ проводили исходно, через 24 и 52 нед лечения. АД клиническое определяли как среднее 3 измерений АД ручным сфигмоманометром в положении сидя после 5-минутного отдыха через 24–26 ч после приема препаратов. СМАД проводили всем больным с помощью приборов SL 90207 (“SpacеLabs Medical”, США). Исследование начинали в 10–12 ч с интервалами между измерениями АД 20 мин днем и 30 мин во время сна. За критерий эффективности антигипертензивной терапии по АД кл. принимали снижение ДАД кл. на 10% или на 10 мм рт. ст. и САД кл. на 15 мм рт. ст. от исходного уровня. Целевым уровнем АД кл. на фоне терапии считали достижение АД<140/90 мм рт. ст. [17, 18]. Оценку структурного состояния миокарда левого желудочка методом ЭхоКГ выполняли на аппарате “Sonos-2000” (“Hewlett Packard”, США) с частотой датчика 2,7–3,5 МГц, запись результатов производили на светочувствительную бумагу со скоростью лентопротяжки 100 см/с. Оценку структурных изменений ЛЖ проводили в В- и М-режимах с определением конечно-систолического (КСР) и конечно-диастолического размера (КДР) полости ЛЖ, толщины межжелудочковой перегородки (ТМЖП) и задней стенки (ТЗС) ЛЖ в диастолу. При измерении толщины стенок ЛЖ толщину эндокарда исключали, но она входила в подсчет внутреннего диаметра ЛЖ [19]. ММЛЖ рассчитывали по формуле R.Devereux (1977 г.) [19]. Индекс массы миокарда рассчитывали как отношение ММЛЖ к площади поверхности тела (г/м2). За ГЛЖ принимались ИММЛЖ>104 г/м2у женщин и >110 г/м2 у мужчин [20]. При повторном исследовании после 24 нед терапии все измерения выполняли в том же сечении, что и первоначально (совмещение осей проводили с использованием записи позиции измерений на светочувствительной бумаге, сделанной при первом исследовании). Ремоделирование ЛЖ оценивали по относительной толщине стенок (ОТС) ЛЖ – отношению суммы ТМЖП и ТЗС к конечно-диастолическому размеру ЛЖ.
Полный биохимический анализ крови (К, Na, креатинин, мочевина, общий белок, глюкоза, АСТ, АЛТ, общий билирубин), общий анализ крови, общий анализ мочи, суточное мониторирование АД (СМАД), ЭхоКГ и ЭКГ проводили исходно, через 24 и 52 нед лечения. АД клиническое определяли как среднее 3 измерений АД ручным сфигмоманометром в положении сидя после 5-минутного отдыха через 24–26 ч после приема препаратов. СМАД проводили всем больным с помощью приборов SL 90207 (“SpacеLabs Medical”, США). Исследование начинали в 10–12 ч с интервалами между измерениями АД 20 мин днем и 30 мин во время сна. За критерий эффективности антигипертензивной терапии по АД кл. принимали снижение ДАД кл. на 10% или на 10 мм рт. ст. и САД кл. на 15 мм рт. ст. от исходного уровня. Целевым уровнем АД кл. на фоне терапии считали достижение АД<140/90 мм рт. ст. [17, 18]. Оценку структурного состояния миокарда левого желудочка методом ЭхоКГ выполняли на аппарате “Sonos-2000” (“Hewlett Packard”, США) с частотой датчика 2,7–3,5 МГц, запись результатов производили на светочувствительную бумагу со скоростью лентопротяжки 100 см/с. Оценку структурных изменений ЛЖ проводили в В- и М-режимах с определением конечно-систолического (КСР) и конечно-диастолического размера (КДР) полости ЛЖ, толщины межжелудочковой перегородки (ТМЖП) и задней стенки (ТЗС) ЛЖ в диастолу. При измерении толщины стенок ЛЖ толщину эндокарда исключали, но она входила в подсчет внутреннего диаметра ЛЖ [19]. ММЛЖ рассчитывали по формуле R.Devereux (1977 г.) [19]. Индекс массы миокарда рассчитывали как отношение ММЛЖ к площади поверхности тела (г/м2). За ГЛЖ принимались ИММЛЖ>104 г/м2у женщин и >110 г/м2 у мужчин [20]. При повторном исследовании после 24 нед терапии все измерения выполняли в том же сечении, что и первоначально (совмещение осей проводили с использованием записи позиции измерений на светочувствительной бумаге, сделанной при первом исследовании). Ремоделирование ЛЖ оценивали по относительной толщине стенок (ОТС) ЛЖ – отношению суммы ТМЖП и ТЗС к конечно-диастолическому размеру ЛЖ. За норму считали показатель ОТС<0,45 [21, 22]. Выделяли следующие виды ремоделирования: 1) концентрическое ремоделирование: нормальный индекс ММЛЖ и ОТС>0,45; 2) концентрическая гипертрофия: увеличение ИММЛЖ и ОТС>0,45; 3) эксцентрическая гипертрофия: увеличение ИММЛЖ при нормальной ОТС(<0,45) [21, 22]. Статистический анализ проводили с использованием пакета компьютерных программ, предусматривающих возможность параметрического и непараметрического анализа. При проведении параметрического анализа использовали парный и непарный t-критерий Стьюдента. Различия считали достоверными при p<0,05. При p<0,1 отмечена тенденция к отличию сравниваемых величин. Результаты представлены в виде М±std. Рис. 1. Динамика АД кл. на фоне терапии моэксиприлом и моэксиприлом с ГХТ. Рис. 2. Динамика геометрии ЛЖ на фоне терапии моэксиприлом и моэксиприлом с ГХТ. Влияние терапии моэксиприлом на структурное состояние миокарда ЛЖ, n=117 (M±std) Показатель Исходно 24 нед терапии Дельта 0–24 р0–24 52 нед терапии Дельта 24–52 p24–52 Дельта 0–52 p0–52 ТМЖП, см 1,17±0,20 1,14±0,19 -0,03±0,08 <0,0001 1,12±0,18 -0,02±0,07 0,0001 -0,05±0,09 <0,0001 ТЗС, см 1,18±0,17 1,16±0,17 -0,02±0,07 0,001 1,14±0,17 -0,02±0,07 0,0001 -0,04±0,08 <0,0001 КДР, см 5,23±0,49 5,07±0,46 -0,16±0,23 <0,0001 5,13±0,43 0,06±0,27 0,02 -0,10±0,30 0,001 ИММЛЖ, г/м2 154,7±39,5 142,6±33,6 -12,1±15,6 <0,0001 142,2±35,2 -0,4±14,3 Нд -12,5±17,2 <0,0001 ОТС 0,453±0,08 0,459±0,08 0,006±0,04 Нд 0,443±0,08 -0,016±0,03 0,0001 -0,010±0,04 0,01 Примечание. Нд – недостоверно. Результаты и обсуждение На фоне терапии моэксиприлом в дозе 7,5 мг в целом по группе через 3 нед терапии отмечено достоверное снижение САД и ДАД по сравнению с их исходным уровнем (рис. 1): САД кл. снизилось со 165,1±10,5 до 158,0±12,5 мм рт. ст. (D=-7,1±6,9, p<0,0001) и ДАД кл. снизилось с 99,2±8,5 до 95,4±8,8 мм рт. ст. (D=-3,8±4,1, p<0,0001). Целевого уровня АД достигли 12,8% больных, остальным пациентам дозу моэксиприла увеличили до 15 мг/сут на 3 нед.
За норму считали показатель ОТС<0,45 [21, 22]. Выделяли следующие виды ремоделирования: 1) концентрическое ремоделирование: нормальный индекс ММЛЖ и ОТС>0,45; 2) концентрическая гипертрофия: увеличение ИММЛЖ и ОТС>0,45; 3) эксцентрическая гипертрофия: увеличение ИММЛЖ при нормальной ОТС(<0,45) [21, 22]. Статистический анализ проводили с использованием пакета компьютерных программ, предусматривающих возможность параметрического и непараметрического анализа. При проведении параметрического анализа использовали парный и непарный t-критерий Стьюдента. Различия считали достоверными при p<0,05. При p<0,1 отмечена тенденция к отличию сравниваемых величин. Результаты представлены в виде М±std. Рис. 1. Динамика АД кл. на фоне терапии моэксиприлом и моэксиприлом с ГХТ. Рис. 2. Динамика геометрии ЛЖ на фоне терапии моэксиприлом и моэксиприлом с ГХТ. Влияние терапии моэксиприлом на структурное состояние миокарда ЛЖ, n=117 (M±std) Показатель Исходно 24 нед терапии Дельта 0–24 р0–24 52 нед терапии Дельта 24–52 p24–52 Дельта 0–52 p0–52 ТМЖП, см 1,17±0,20 1,14±0,19 -0,03±0,08 <0,0001 1,12±0,18 -0,02±0,07 0,0001 -0,05±0,09 <0,0001 ТЗС, см 1,18±0,17 1,16±0,17 -0,02±0,07 0,001 1,14±0,17 -0,02±0,07 0,0001 -0,04±0,08 <0,0001 КДР, см 5,23±0,49 5,07±0,46 -0,16±0,23 <0,0001 5,13±0,43 0,06±0,27 0,02 -0,10±0,30 0,001 ИММЛЖ, г/м2 154,7±39,5 142,6±33,6 -12,1±15,6 <0,0001 142,2±35,2 -0,4±14,3 Нд -12,5±17,2 <0,0001 ОТС 0,453±0,08 0,459±0,08 0,006±0,04 Нд 0,443±0,08 -0,016±0,03 0,0001 -0,010±0,04 0,01 Примечание. Нд – недостоверно. Результаты и обсуждение На фоне терапии моэксиприлом в дозе 7,5 мг в целом по группе через 3 нед терапии отмечено достоверное снижение САД и ДАД по сравнению с их исходным уровнем (рис. 1): САД кл. снизилось со 165,1±10,5 до 158,0±12,5 мм рт. ст. (D=-7,1±6,9, p<0,0001) и ДАД кл. снизилось с 99,2±8,5 до 95,4±8,8 мм рт. ст. (D=-3,8±4,1, p<0,0001). Целевого уровня АД достигли 12,8% больных, остальным пациентам дозу моэксиприла увеличили до 15 мг/сут на 3 нед. Через 6 нед от начала лечения целевой уровень АД достигнут у 35% больных, однако у 5 пациентов на фоне монотерапии моэксиприлом в дозе 7,5 мг/сут произошло ускользание антигипертензивного эффекта. К 9-й неделе от начала лечения комбинированную терапию моэксиприлом и ГХТ получали 65% больных. Антигипертензивный эффект по САД и ДАД достиг максимума к 24-й неделе терапии, от 4-й к 24-й неделе САД кл. снизилось со 158,0±12,5 до 136,9±8,6 мм рт. ст. (D=-21,1±9,7, p<0,0001), ДАД кл. – с 95,4±8,8 до 84,2±7,9 мм рт. ст. (D=-11,2±7,7, p<0,0001), дальше уровень АД кл. оставался стабилен, ускользания антигипертензивного эффекта не отмечено (рис. 2). К 24-й неделе терапии целевого уровня АД достигли 73,5% по САД; 82,1% по ДАД и 72,6% по обоим показателям. В целом 52-недельная терапия привела к достоверному снижению АД (см. рис. 1): САД кл. снизилось со 165,1±10,5 до 134,5±10,4 мм рт. ст. (D=-30,6±12,2, p<0,001) и ДАД кл. – с 99,2±8,5 до 83,4±7,2 мм рт. ст. (D=-15,8±8,5, p<0,001). Достоверной динамики ЧСС выявлено не было. Через 52 нед лечения монотерапию моэксиприлом в дозе 7,5 мг/сут получали 8,6%, в дозе 15 мг/сут – 20,5% больных; комбинированную терапию моэксиприлом – 15 мг/сут и ГХТ – 12,5 мг/сут 17,1% и ГХТ – 25 мг/сут 53,8% пациентов. Целевой уровень САД был достигнут у 79,5%, ДАД – у 86,4% больных и 74,4% – по обоим показателям. За 52 нед лечения ускользание антигипертензивного эффекта терапии отмечено у 21 (18%) больного, из них на фоне моэксиприла 7,5 мг/сут у 4 больных; моэксиприла 15 мг/сут у 4 больных и комбинации моэксиприла 15 мг/сут + ГХТ 12,5 мг/сут у 13 пациентов. Антигипертензивный эффект моэксиприла и сочетания моэксиприла с ГХТ при приеме однократно утром сохранялся через 24–26 ч после назначения. Это подтверждает пролонгированное действие препарата, которое обеспечивает достаточный и равномерный антигипертензивный эффект в течение 24ч при однократном приеме. Статистически значимого изменения ЧСС за все время терапии не отмечено (p=0,6). Биохимические показатели крови (калий, натрий, глюкоза, АЛТ, АСТ, билирубин, мочевина, креатинин, триглицериды) на фоне лечения препаратами не менялись, за исключением кратковременного снижения уровня калия менее 3,5 ммоль/л у 13 (11,1%) больных.
Через 6 нед от начала лечения целевой уровень АД достигнут у 35% больных, однако у 5 пациентов на фоне монотерапии моэксиприлом в дозе 7,5 мг/сут произошло ускользание антигипертензивного эффекта. К 9-й неделе от начала лечения комбинированную терапию моэксиприлом и ГХТ получали 65% больных. Антигипертензивный эффект по САД и ДАД достиг максимума к 24-й неделе терапии, от 4-й к 24-й неделе САД кл. снизилось со 158,0±12,5 до 136,9±8,6 мм рт. ст. (D=-21,1±9,7, p<0,0001), ДАД кл. – с 95,4±8,8 до 84,2±7,9 мм рт. ст. (D=-11,2±7,7, p<0,0001), дальше уровень АД кл. оставался стабилен, ускользания антигипертензивного эффекта не отмечено (рис. 2). К 24-й неделе терапии целевого уровня АД достигли 73,5% по САД; 82,1% по ДАД и 72,6% по обоим показателям. В целом 52-недельная терапия привела к достоверному снижению АД (см. рис. 1): САД кл. снизилось со 165,1±10,5 до 134,5±10,4 мм рт. ст. (D=-30,6±12,2, p<0,001) и ДАД кл. – с 99,2±8,5 до 83,4±7,2 мм рт. ст. (D=-15,8±8,5, p<0,001). Достоверной динамики ЧСС выявлено не было. Через 52 нед лечения монотерапию моэксиприлом в дозе 7,5 мг/сут получали 8,6%, в дозе 15 мг/сут – 20,5% больных; комбинированную терапию моэксиприлом – 15 мг/сут и ГХТ – 12,5 мг/сут 17,1% и ГХТ – 25 мг/сут 53,8% пациентов. Целевой уровень САД был достигнут у 79,5%, ДАД – у 86,4% больных и 74,4% – по обоим показателям. За 52 нед лечения ускользание антигипертензивного эффекта терапии отмечено у 21 (18%) больного, из них на фоне моэксиприла 7,5 мг/сут у 4 больных; моэксиприла 15 мг/сут у 4 больных и комбинации моэксиприла 15 мг/сут + ГХТ 12,5 мг/сут у 13 пациентов. Антигипертензивный эффект моэксиприла и сочетания моэксиприла с ГХТ при приеме однократно утром сохранялся через 24–26 ч после назначения. Это подтверждает пролонгированное действие препарата, которое обеспечивает достаточный и равномерный антигипертензивный эффект в течение 24ч при однократном приеме. Статистически значимого изменения ЧСС за все время терапии не отмечено (p=0,6). Биохимические показатели крови (калий, натрий, глюкоза, АЛТ, АСТ, билирубин, мочевина, креатинин, триглицериды) на фоне лечения препаратами не менялись, за исключением кратковременного снижения уровня калия менее 3,5 ммоль/л у 13 (11,1%) больных. Переносимость терапии у всех больных была хорошей, однако 3 пациента из-за развития кашля прекратили участие в исследовании. При анализе СМАД через 24 нед терапии было выявлено снижение среднесуточного АД с 152,9±13,8/92,7±10,8 до 136,0±14,2/82,8±11,0 мм рт. ст., DАД кл.=-16,9±15,5/-9,9±11,8 мм рт. ст. (p<0,0001). От 24-й к 52-й неделе терапии достоверной динамики АД не отмечено (DАД кл.=-2,0±14,8/-0,5±10,5 мм рт. ст.; p=0,0001). За 52 нед лечения среднесуточное АД снизилось с 152,9±13,8/92,7±10,8 до 134,0±13,8/82,3±9,0 мм рт.ст., DАД кл.=-18,9±16,9/-10,4±10,8 мм рт. ст. (p<0,0001). Нормализация АД, по данным СМАД, была достигнута у 72,6% больных по САД, у 82,9% по ДАД и у 69,2% по обоим показателям. До лечения все больные имели ГЛЖ по данным ЭхоКГ. Средний ИММЛЖ составил 141,4±32,7 г/м2 у женщин и 170,3±41,3 г/м2 у мужчин. У 51,3% больных была выявлена концентрическая ГЛЖ и у 48,7% – эксцентрическая (см. рис. 2). Через 24 нед терапии моэксиприлом и моэксиприлом с ГХТ наблюдали достоверное уменьшение ТЗС, ТМЖП и конечно-диастолического размера ЛЖ, что привело к уменьшению ИММЛЖ (см. таблицу; рис. 2). Уменьшение ИММЛЖ отмечено у всех больных, а нормализация геометрии ЛЖ – у 3,4% больных (см. рис. 2). Из 60 больных с концентрической ГЛЖ у 5% произошла нормализация ИММЛЖ и геометрии ЛЖ, у 1,7% она перешла в концентрическое ремоделирование, у остальных больных осталась без изменений. Из 57 больных с исходно эксцентрической ГЛЖ у 1 произошла нормализация ИММЛЖ и геометрии ЛЖ. От 24-й к 52-й неделе терапии наблюдали достоверное уменьшение ТЗС и ТМЖП, однако в это же время произошло увеличение КДР, что привело к значимому уменьшению ОТС ЛЖ и отсутствию динамики ИММЛЖ. Полная нормализация ИММЛЖ и геометрии ЛЖ была достигнута у 6,8%; концентрическое ремоделирование было у 3,4%, концентрическая ГЛЖ оставалась у 41,9% и эксцентрическая ГЛЖ – у 47,9% больных. Уменьшение ИММЛЖ происходило за счет уменьшения как ТЗСЛЖ (R=0,48, p<0,001), так и конечно-диастолического размера ЛЖ (R=0,73, p<0,001).
Переносимость терапии у всех больных была хорошей, однако 3 пациента из-за развития кашля прекратили участие в исследовании. При анализе СМАД через 24 нед терапии было выявлено снижение среднесуточного АД с 152,9±13,8/92,7±10,8 до 136,0±14,2/82,8±11,0 мм рт. ст., DАД кл.=-16,9±15,5/-9,9±11,8 мм рт. ст. (p<0,0001). От 24-й к 52-й неделе терапии достоверной динамики АД не отмечено (DАД кл.=-2,0±14,8/-0,5±10,5 мм рт. ст.; p=0,0001). За 52 нед лечения среднесуточное АД снизилось с 152,9±13,8/92,7±10,8 до 134,0±13,8/82,3±9,0 мм рт.ст., DАД кл.=-18,9±16,9/-10,4±10,8 мм рт. ст. (p<0,0001). Нормализация АД, по данным СМАД, была достигнута у 72,6% больных по САД, у 82,9% по ДАД и у 69,2% по обоим показателям. До лечения все больные имели ГЛЖ по данным ЭхоКГ. Средний ИММЛЖ составил 141,4±32,7 г/м2 у женщин и 170,3±41,3 г/м2 у мужчин. У 51,3% больных была выявлена концентрическая ГЛЖ и у 48,7% – эксцентрическая (см. рис. 2). Через 24 нед терапии моэксиприлом и моэксиприлом с ГХТ наблюдали достоверное уменьшение ТЗС, ТМЖП и конечно-диастолического размера ЛЖ, что привело к уменьшению ИММЛЖ (см. таблицу; рис. 2). Уменьшение ИММЛЖ отмечено у всех больных, а нормализация геометрии ЛЖ – у 3,4% больных (см. рис. 2). Из 60 больных с концентрической ГЛЖ у 5% произошла нормализация ИММЛЖ и геометрии ЛЖ, у 1,7% она перешла в концентрическое ремоделирование, у остальных больных осталась без изменений. Из 57 больных с исходно эксцентрической ГЛЖ у 1 произошла нормализация ИММЛЖ и геометрии ЛЖ. От 24-й к 52-й неделе терапии наблюдали достоверное уменьшение ТЗС и ТМЖП, однако в это же время произошло увеличение КДР, что привело к значимому уменьшению ОТС ЛЖ и отсутствию динамики ИММЛЖ. Полная нормализация ИММЛЖ и геометрии ЛЖ была достигнута у 6,8%; концентрическое ремоделирование было у 3,4%, концентрическая ГЛЖ оставалась у 41,9% и эксцентрическая ГЛЖ – у 47,9% больных. Уменьшение ИММЛЖ происходило за счет уменьшения как ТЗСЛЖ (R=0,48, p<0,001), так и конечно-диастолического размера ЛЖ (R=0,73, p<0,001). Динамика ИММЛЖ прямо коррелировала с исходной выраженностью ГЛЖ (R=0,47, p<0,01). Сравнительный анализ не выявил различий в динамике ИММЛЖ у больных с концентрической и эксцентрической ГЛЖ. Зависимости динамики ИММЛЖ от изменений АД кл. и параметров СПАД на фоне лечения моэксиприлом как в виде монотерапии, так и в комбинации с ГХТ найдено не было.Заключение 1. На фоне лечения моэксиприлом в виде монотерапии и комбинации с ГХТ позволяет достичь целевого уровня АД у 72–75% больных. 2. Лечение моэксиприлом в виде монотерапии и комбинации с ГХТ показала хороший кардиопротективный эффект в виде регресса ГЛЖ на 12,5 г/м2 и улучшения геометрии ЛЖ. Снижение ИММЛЖ происходит в основном в первые 24 нед терапии. В дальнейшем ИММЛЖ достоверно не изменяется, но положительное влияние на геометрию ЛЖ продолжается. 3. Лечение моэксиприлом в виде монотерапии и комбинации с ГХТ характеризовалось хорошей переносимостью.
Динамика ИММЛЖ прямо коррелировала с исходной выраженностью ГЛЖ (R=0,47, p<0,01). Сравнительный анализ не выявил различий в динамике ИММЛЖ у больных с концентрической и эксцентрической ГЛЖ. Зависимости динамики ИММЛЖ от изменений АД кл. и параметров СПАД на фоне лечения моэксиприлом как в виде монотерапии, так и в комбинации с ГХТ найдено не было.Заключение 1. На фоне лечения моэксиприлом в виде монотерапии и комбинации с ГХТ позволяет достичь целевого уровня АД у 72–75% больных. 2. Лечение моэксиприлом в виде монотерапии и комбинации с ГХТ показала хороший кардиопротективный эффект в виде регресса ГЛЖ на 12,5 г/м2 и улучшения геометрии ЛЖ. Снижение ИММЛЖ происходит в основном в первые 24 нед терапии. В дальнейшем ИММЛЖ достоверно не изменяется, но положительное влияние на геометрию ЛЖ продолжается. 3. Лечение моэксиприлом в виде монотерапии и комбинации с ГХТ характеризовалось хорошей переносимостью.
- Levy D, Anderson K, Savage D et al. Echocardiographically detected LVH: prevalence and risk factors. The Framingham Heart Study. Ann Intern Med 1988; 108: 7–13.
- Vakili B, Okin P, Devereux R. Prognostic implications of left ventricular hypertrophy. Am Heart J 2001; 141: 334–41.
- Bikkina M, Levy D, Evans J et al. Left ventricular mass and the risk the stroke in elderly cohort: The Framingham Study. JAMA 1994; 272: 33–6.
- Koren M, Richard B, Devereux M et al. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hipertension. Ann Intern Med 1991; 114: 345–52.
- Mensah G, Pappas T, Koren M et al. Comparison of classification severity by blood pressure level and World Health Organization for prediction concurrent cardiac abnormalities and subsequent complications in essential hipertension. J Hypertension 1993; 11: 1429–30.

- Simone G, Mureddu G, Greco R et al. Relation of left ventricular geometry and function to body composition in children with high causal blood pressure. Hypertension 1997; 30(part 1): 377–82.
- Koren M, Ulin R, Laragh J, Devereux R. Changes in LVH predict risk in essential hypertension. Circulation 1990; 83 (sappl): III-29.
- Levy D, Garrison R, Savage D et al. Prognostic implications of echocardiographically – determined left ventricular mass in the Framingham Heart Study. N Engl J Med 1990; 322: 1561–6.
- Devereux R. Theraperutic options in minimizing LVH. Am Heart J 2000; 139: 9–14.
- Savage D, Garrison R, Kannel W et al. The spectrum of LVH in a general population sample: the Framingham Study. Circulation 1987; 75: 26.
- Hammond I, Devereux R, Alderman M et al. The prevalence and correlates of echocardiographic left ventricular hypertrophy among employed patients with uncomplicated hipertension. Am J Cardiol 1986; 7: 639–50.
- Шляхто У.В., Конради А.О., Захаров Д.В., Рудоманов О.Г. Структурно — функциональные изменения миокарда у больных гипертонической болезнью. Кардиология. 1999; 2: 49–55.
- Gottdiener J, Livengood V et al. Should echocardiography be performed to assess effects of antihypertensive therapy? Test — retest reliability of echocardiography for measurement of LVM and function. J Am Coll Cardiol 1995; 25: 424–30.
- Devereux R, Pini R, Aurigemma G, Roman M. Measuremant of LV mass: methodology and expertise. J Hypertens 1997; 15: 801–9.
- Frohlich E, Apstein C, Chobanian A et al. The heart in hypertension. N Engl J Med 1992; 327: 998–1008.
- Verdecchia P et al. Prognostic significance of serial changes in LV mass in essential hypertension. Circulation 1998; 97: 48–54.
- Ратова Л.
 Г., Дмитриев В.В., Толпыгина С.Н., Чазова И.Е. Суточное мониторирование артериального давления в клинической практике. Консилиум, приложение «Артериальная гипертензия». 2001; с. 3–14.
Г., Дмитриев В.В., Толпыгина С.Н., Чазова И.Е. Суточное мониторирование артериального давления в клинической практике. Консилиум, приложение «Артериальная гипертензия». 2001; с. 3–14. - Рогоза А.Н., Никольский В.П., Ощепкова Е.В. и др. Суточное мониторирование артериального давления (Методические вопросы). Под ред. Г.Г.Арабидзе и О.Ю.Атькова. М., 1997.
- Devereux R.B, Reicheck N. Echocardiographic determinstion of left ventricular mass in man: anatomic validation of the method. Circulation 1977; 55: 613–8.
- Lievre M, Gueret P, Gayet C et al. Ramipril — induced regression of left ventricular hypertrophy in treated hypertensive individuals. Hypertension 1995; 25: 92–7.
- Шляхто E.В., Конради А.О., Захаров Д.В., Рудоманов О.Г. Структурно — функциональные изменения миокарда у больных гипертонической болезнью. Кардиология. 1999; 2: 49–55.
- Ganau A, Devereux R.B, Roman M.J et al. Patterns of left ventricular hypertrophy and geometric remodeling in essential hypertension. J Am Coll Cardiol 1992; 19: 1550–8.
Cited-By
Article Metrics
PlumX
Dimensions
Refbacks
- There are currently no refbacks.
Как лечить гемофагоцитарный лимфогистиоцитоз у взрослого пациента | Кровь
Гемофагоцитарный лимфогистиоцитоз диагностируется по совокупности признаков, симптомов и лабораторных отклонений. Имеющиеся симптомы часто неспецифичны, и для быстрого выявления и лечения необходим высокий показатель подозрительности. Ранняя диагностика важна, потому что без лечения HLH часто приводит к летальному исходу. В 2004 году Общество гистиоцитов предложило обновленный набор критериев, чтобы помочь в идентификации пациентов с ГЛГ для клинических испытаний (таблица 1). 50 К ним относятся молекулярные тесты, соответствующие HLH или 5 из 8 следующих критериев: лихорадка, спленомегалия, цитопения, затрагивающая ≥2 клонов, гипертриглицеридемия и / или гипофибриногенемия, гемофагоцитоз (в костном мозге, селезенке или лимфатическом узле), гиперферритинемия, нарушение функции NK-клеток и повышение растворимого CD25 (sCD25) (т.е. sIL2R). Дополнительные общие признаки включают трансаминит, коагулопатию, гипонатриемию, отек, сыпь, гипоальбуминемию, повышение лактатдегидрогеназы (ЛДГ), С-реактивного белка и d-димера, повышение липопротеинов очень низкой плотности, снижение липопротеинов высокой плотности, повышение цереброспинального жидкий белок и клетки, а также неврологические симптомы, начиная от очагового дефицита и заканчивая измененным психическим статусом. 24,25,27,32,50 Пациенты могут не обладать всеми этими характеристиками при первичном обращении, что затрудняет диагностику. Важно отметить, что эти критерии были разработаны для диагностики ГЛГ у детей, но широко применялись к пациентам с вторичным ГЛГ, включая взрослых. В настоящее время не существует общепринятого набора критериев для диагностики ГЛГ у взрослого населения.
50 К ним относятся молекулярные тесты, соответствующие HLH или 5 из 8 следующих критериев: лихорадка, спленомегалия, цитопения, затрагивающая ≥2 клонов, гипертриглицеридемия и / или гипофибриногенемия, гемофагоцитоз (в костном мозге, селезенке или лимфатическом узле), гиперферритинемия, нарушение функции NK-клеток и повышение растворимого CD25 (sCD25) (т.е. sIL2R). Дополнительные общие признаки включают трансаминит, коагулопатию, гипонатриемию, отек, сыпь, гипоальбуминемию, повышение лактатдегидрогеназы (ЛДГ), С-реактивного белка и d-димера, повышение липопротеинов очень низкой плотности, снижение липопротеинов высокой плотности, повышение цереброспинального жидкий белок и клетки, а также неврологические симптомы, начиная от очагового дефицита и заканчивая измененным психическим статусом. 24,25,27,32,50 Пациенты могут не обладать всеми этими характеристиками при первичном обращении, что затрудняет диагностику. Важно отметить, что эти критерии были разработаны для диагностики ГЛГ у детей, но широко применялись к пациентам с вторичным ГЛГ, включая взрослых. В настоящее время не существует общепринятого набора критериев для диагностики ГЛГ у взрослого населения.
Диагностика HLH является особенно сложной задачей, потому что симптомы неспецифичны, и многие признаки частично совпадают с другими причинами тяжелого заболевания, включая сепсис и гематологические злокачественные новообразования.Важно отметить, что те же самые нарушения могут вызвать HLH, что еще больше усложняет диагностику. Самым большим препятствием часто считается HLH при дифференциальной диагностике. Например, пациентка 2, указанная выше, была направлена в нашу больницу для оценки третичной помощи после 3 месяцев необъяснимой лихорадки и конституциональных симптомов и чуть не умерла на раннем этапе ее оценки. Это не нетипично для презентации HLH.
После постановки диагноза необходимо незамедлительно отправить соответствующие исследования, включая общий анализ крови, триглицериды, фибриноген, ферритин и sCD25. sCD25 доступен не во всех учреждениях и может потребоваться время, чтобы вернуться, но он полезен для диагностики и более надежно коррелирует с тяжестью заболевания, чем другие маркеры. 51 Кроме того, высокое отношение CD25 к ферритину чаще наблюдается при лимфомо-ассоциированном ГЛГ и может быть полезным маркером, чтобы отличить эту сущность от других причин ГЛГ (соотношение 8,56 против 0,66 с P = 0,0004). 52 Мы рекомендуем отправить этот тест каждому пациенту, но не откладывать лечение в ожидании результата, если в остальном диагноз HLH ясен.Также было показано, что специфический для макрофагов рецептор скавенджера CD163 значительно усиливает состояние активации макрофагов. 53 Это полезный маркер HLH, но он также может повышаться при других воспалительных заболеваниях, вызывающих активацию макрофагов. 54 Фибриноген — это реагент острой фазы, уровень которого повышен при большинстве воспалительных заболеваний, но низкий уровень ГЛГ. Точно так же скорость оседания эритроцитов (СОЭ) у ГЛГ низкая вследствие снижения уровня фибриногена.
sCD25 доступен не во всех учреждениях и может потребоваться время, чтобы вернуться, но он полезен для диагностики и более надежно коррелирует с тяжестью заболевания, чем другие маркеры. 51 Кроме того, высокое отношение CD25 к ферритину чаще наблюдается при лимфомо-ассоциированном ГЛГ и может быть полезным маркером, чтобы отличить эту сущность от других причин ГЛГ (соотношение 8,56 против 0,66 с P = 0,0004). 52 Мы рекомендуем отправить этот тест каждому пациенту, но не откладывать лечение в ожидании результата, если в остальном диагноз HLH ясен.Также было показано, что специфический для макрофагов рецептор скавенджера CD163 значительно усиливает состояние активации макрофагов. 53 Это полезный маркер HLH, но он также может повышаться при других воспалительных заболеваниях, вызывающих активацию макрофагов. 54 Фибриноген — это реагент острой фазы, уровень которого повышен при большинстве воспалительных заболеваний, но низкий уровень ГЛГ. Точно так же скорость оседания эритроцитов (СОЭ) у ГЛГ низкая вследствие снижения уровня фибриногена.
Повышенный уровень ферритина встречается у подавляющего большинства пациентов с HLH, но является неспецифическим.Опубликованные критерии используют пороговое значение ферритина ≥500 мкг / л при диагностике ГЛГ. Это основано на исследовании HLH-94, которое показало чувствительность 84% на этом уровне. Последующие исследования показали, что более высокий порог ≥10 000 мкг / л имеет 90% чувствительность и 96% специфичность для HLH. 55 Как и большая часть литературы по HLH, эти исследования проводились в педиатрической популяции. В нашем учреждении, используя популяцию только взрослых, мы обнаружили, что не было уровня, выше которого ферритин был специфическим для HLH. 56 Из 113 пациентов с уровнем ферритина> 50 000 мкг / л только 19 имели ГЛГ. Это говорит о том, что, хотя значительно повышенный уровень ферритина может быть специфическим для HLH в педиатрической практике, это не относится к взрослым. Из 50 взрослых пациентов, выявленных в нашем учреждении с ГЛГ, средний уровень ферритина при поступлении составил 5823 мкг / л (минимум 461 мкг / л и максимум 98 110), а средний максимальный уровень ферритина составил 19 687 мкг / л (минимум 1618 мкг / л). Л и максимум 202 911 мкг / л).
Из 50 взрослых пациентов, выявленных в нашем учреждении с ГЛГ, средний уровень ферритина при поступлении составил 5823 мкг / л (минимум 461 мкг / л и максимум 98 110), а средний максимальный уровень ферритина составил 19 687 мкг / л (минимум 1618 мкг / л). Л и максимум 202 911 мкг / л).
Хотя гемофагоцитоз является патологическим признаком HLH, важно отметить, что он не является ни чувствительным, ни специфическим. Распространенность гемофагоцитоза в костном мозге пациентов с HLH колеблется от 25% до 100%, и значения часто варьируются между патологоанатомами. 24,25,51,57 Кроме того, его часто можно обнаружить у тяжелобольных пациентов при отсутствии ГЛГ. 58,59 Тем не менее, оценка подозрения на ГЛГ должна включать биопсию костного мозга.В первых двух случаях, описанных выше, гемофагоцитоз в конечном итоге был описан в костном мозге, но не был окончательно диагностирован при первоначальном исследовании костного мозга ни у одного пациента. Чувствительность обнаружения гемофагоцитоза в костном мозге повышается путем окрашивания на CD163, который специфически выделяет макрофаги. Однако, как и у этих пациентов, обнаружение гемофагоцитоза в костном мозге обычно требует предвидения диагноза, а также запроса специальных красителей.
АктивностьNK-клеток является частью диагностических критериев для детского HLH, но этот тест редко помогает взрослому населению, и мы его не отправляем.Этот тест не проводился ни у одного из описанных пациентов.
Недавно несколько групп предложили более стандартизированные критерии диагностики вторичного HLH. Фардет и др. Создали и утвердили HScore, который включает 9 взвешенных переменных. 60 Эта система оценки доступна в Интернете (http://saintantoine.aphp.fr/score/). Интернет-исследование Delphi, проведенное группой экспертов, составило аналогичный список критериев (Таблица 2). 61 Эти недавно предложенные критерии — шаг к улучшению диагностики ГЛГ у взрослых.
61 Эти недавно предложенные критерии — шаг к улучшению диагностики ГЛГ у взрослых.
Наш подход к оценке и лечению HLH представлен на Рисунке 1. Как отмечалось ранее, многие пациенты с HLH направляются в центры третичной медицинской помощи после продолжительного обследования во внешней больнице, и мы стремимся оценить их как можно быстрее и приступить к работе. При необходимости, HLH-специфическая терапия. Пациентов следует расспрашивать о недавних инфекциях, злокачественных новообразованиях, основных иммунных нарушениях, фармакологической иммуносупрессии, ревматологических состояниях и семейном анамнезе подобных симптомов.Необходимо сердечно-легочное обследование, и каждый пациент также должен быть обследован на предмет гепатоспленомегалии, лимфаденопатии, сыпи, неврологических нарушений и признаков кровотечения или кровоподтеков. Чтобы лучше оценить спленомегалию, рассмотрите возможность ультразвукового исследования брюшной полости. Кроме того, все пациенты должны пройти базовую метаболическую панель, исследования коагуляции (протромбиновое время, активированное частичное тромбопластиновое время), функциональные пробы печени, ЛДГ и альбумин. Если триггер не может быть легко идентифицирован, требуется обследование на наличие инфекционных причин, включая посев крови, общий анализ мочи, посев мочи, тонкий и толстый мазок крови, рентген грудной клетки, очищенное производное белка (или Т-точку), титры вирусов и серологические исследования (ВЭБ, ЦМВ, грипп, вирус гепатита С, вирус гепатита В, вирус простого герпеса, вирус ветряной оспы, парвовирус, аденовирус, вирус кори, вирус герпеса человека 8, ВИЧ).Повышенная вирусная нагрузка EBV может быть следствием подавления иммунитета или лимфомы, вызванной EBV, и не обязательно означает, что EBV запускает HLH. ВЭБ обычно вызывает ГЛГ на фоне вновь приобретенной литической ВЭБ-инфекции, которая чаще встречается у детей. Первоначальная оценка злокачественности должна включать периферическую проточную цитометрию, ПЭТ-КТ-сканирование и биопсию костного мозга. Ревматологическое обследование обычно включает тестирование на антинуклеарные антитела в дополнение к более конкретным исследованиям, основанным на клинических подозрениях.Мы обнаружили, что ПЭТ-КТ-сканирование часто выявляет заметную активность в селезенке в отсутствие активной аденопатии у пациентов с идиопатическим ГЛГ. Мы поддерживаем отправку генетических тестов на известные мутации HLH, включая PRF1 , UNC13D , STX11 , STXBP2 и RAB27A , хотя лечение не должно откладываться из-за результатов, а отрицательные результаты часто встречаются у взрослых. Обычно мы не отправляем поток для поверхностной экспрессии перфорина или гранзима B у взрослых.В ожидании лечения часто бывает полезно отправить HLA-типирование и выполнить эхокардиограмму сердца.
Как лечить гемофагоцитарный лимфогистиоцитоз у взрослого пациента | Кровь
Гемофагоцитарный лимфогистиоцитоз диагностируется по совокупности признаков, симптомов и лабораторных отклонений. Имеющиеся симптомы часто неспецифичны, и для быстрого выявления и лечения необходим высокий показатель подозрительности.Ранняя диагностика важна, потому что без лечения HLH часто приводит к летальному исходу. В 2004 году Общество гистиоцитов предложило обновленный набор критериев, чтобы помочь в идентификации пациентов с ГЛГ для клинических испытаний (таблица 1). 50 К ним относятся молекулярные тесты, соответствующие HLH или 5 из 8 следующих критериев: лихорадка, спленомегалия, цитопения, затрагивающая ≥2 клонов, гипертриглицеридемия и / или гипофибриногенемия, гемофагоцитоз (в костном мозге, селезенке или лимфатическом узле), гиперферритинемия, нарушение функции NK-клеток и повышение растворимого CD25 (sCD25) (т.е. sIL2R).Дополнительные общие признаки включают трансаминит, коагулопатию, гипонатриемию, отек, сыпь, гипоальбуминемию, повышение лактатдегидрогеназы (ЛДГ), С-реактивного белка и d-димера, повышение липопротеинов очень низкой плотности, снижение липопротеинов высокой плотности, повышение цереброспинального жидкий белок и клетки, а также неврологические симптомы, начиная от очагового дефицита и заканчивая измененным психическим статусом. 24,25,27,32,50 Пациенты могут не обладать всеми этими характеристиками при первичном обращении, что затрудняет диагностику.Важно отметить, что эти критерии были разработаны для диагностики ГЛГ у детей, но широко применялись к пациентам с вторичным ГЛГ, включая взрослых. В настоящее время не существует общепринятого набора критериев для диагностики ГЛГ у взрослого населения.
Диагностика HLH является особенно сложной задачей, потому что симптомы неспецифичны, и многие признаки частично совпадают с другими причинами тяжелого заболевания, включая сепсис и гематологические злокачественные новообразования.Важно отметить, что те же самые нарушения могут вызвать HLH, что еще больше усложняет диагностику. Самым большим препятствием часто считается HLH при дифференциальной диагностике. Например, пациентка 2, указанная выше, была направлена в нашу больницу для оценки третичной помощи после 3 месяцев необъяснимой лихорадки и конституциональных симптомов и чуть не умерла на раннем этапе ее оценки. Это не нетипично для презентации HLH.
После постановки диагноза необходимо незамедлительно отправить соответствующие исследования, включая общий анализ крови, триглицериды, фибриноген, ферритин и sCD25.sCD25 доступен не во всех учреждениях и может потребоваться время, чтобы вернуться, но он полезен для диагностики и более надежно коррелирует с тяжестью заболевания, чем другие маркеры. 51 Кроме того, высокое отношение CD25 к ферритину чаще наблюдается при лимфомо-ассоциированном ГЛГ и может быть полезным маркером, чтобы отличить эту сущность от других причин ГЛГ (соотношение 8,56 против 0,66 с P = 0,0004). 52 Мы рекомендуем отправить этот тест каждому пациенту, но не откладывать лечение в ожидании результата, если в остальном диагноз HLH ясен.Также было показано, что специфический для макрофагов рецептор скавенджера CD163 значительно усиливает состояние активации макрофагов. 53 Это полезный маркер HLH, но он также может повышаться при других воспалительных заболеваниях, вызывающих активацию макрофагов. 54 Фибриноген — это реагент острой фазы, уровень которого повышен при большинстве воспалительных заболеваний, но низкий уровень ГЛГ. Точно так же скорость оседания эритроцитов (СОЭ) у ГЛГ низкая вследствие снижения уровня фибриногена.
Повышенный уровень ферритина встречается у подавляющего большинства пациентов с HLH, но является неспецифическим.Опубликованные критерии используют пороговое значение ферритина ≥500 мкг / л при диагностике ГЛГ. Это основано на исследовании HLH-94, которое показало чувствительность 84% на этом уровне. Последующие исследования показали, что более высокий порог ≥10 000 мкг / л имеет 90% чувствительность и 96% специфичность для HLH. 55 Как и большая часть литературы по HLH, эти исследования проводились в педиатрической популяции. В нашем учреждении, используя популяцию только взрослых, мы обнаружили, что не было уровня, выше которого ферритин был специфическим для HLH. 56 Из 113 пациентов с уровнем ферритина> 50 000 мкг / л только 19 имели ГЛГ. Это говорит о том, что, хотя значительно повышенный уровень ферритина может быть специфическим для HLH в педиатрической практике, это не относится к взрослым. Из 50 взрослых пациентов, выявленных в нашем учреждении с ГЛГ, средний уровень ферритина при поступлении составил 5823 мкг / л (минимум 461 мкг / л и максимум 98 110), а средний максимальный уровень ферритина составил 19 687 мкг / л (минимум 1618 мкг / л). Л и максимум 202 911 мкг / л).
Хотя гемофагоцитоз является патологическим признаком HLH, важно отметить, что он не является ни чувствительным, ни специфическим. Распространенность гемофагоцитоза в костном мозге пациентов с HLH колеблется от 25% до 100%, и значения часто варьируются между патологоанатомами. 24,25,51,57 Кроме того, его часто можно обнаружить у тяжелобольных пациентов при отсутствии ГЛГ. 58,59 Тем не менее, оценка подозрения на ГЛГ должна включать биопсию костного мозга.В первых двух случаях, описанных выше, гемофагоцитоз в конечном итоге был описан в костном мозге, но не был окончательно диагностирован при первоначальном исследовании костного мозга ни у одного пациента. Чувствительность обнаружения гемофагоцитоза в костном мозге повышается путем окрашивания на CD163, который специфически выделяет макрофаги. Однако, как и у этих пациентов, обнаружение гемофагоцитоза в костном мозге обычно требует предвидения диагноза, а также запроса специальных красителей.
АктивностьNK-клеток является частью диагностических критериев для детского HLH, но этот тест редко помогает взрослому населению, и мы его не отправляем.Этот тест не проводился ни у одного из описанных пациентов.
Недавно несколько групп предложили более стандартизированные критерии диагностики вторичного HLH. Фардет и др. Создали и утвердили HScore, который включает 9 взвешенных переменных. 60 Эта система оценки доступна в Интернете (http://saintantoine.aphp.fr/score/). Интернет-исследование Delphi, проведенное группой экспертов, составило аналогичный список критериев (Таблица 2). 61 Эти недавно предложенные критерии — шаг к улучшению диагностики ГЛГ у взрослых.
Наш подход к оценке и лечению HLH представлен на Рисунке 1. Как отмечалось ранее, многие пациенты с HLH направляются в центры третичной медицинской помощи после продолжительного обследования во внешней больнице, и мы стремимся оценить их как можно быстрее и приступить к работе. При необходимости, HLH-специфическая терапия. Пациентов следует расспрашивать о недавних инфекциях, злокачественных новообразованиях, основных иммунных нарушениях, фармакологической иммуносупрессии, ревматологических состояниях и семейном анамнезе подобных симптомов.Необходимо сердечно-легочное обследование, и каждый пациент также должен быть обследован на предмет гепатоспленомегалии, лимфаденопатии, сыпи, неврологических нарушений и признаков кровотечения или кровоподтеков. Чтобы лучше оценить спленомегалию, рассмотрите возможность ультразвукового исследования брюшной полости. Кроме того, все пациенты должны пройти базовую метаболическую панель, исследования коагуляции (протромбиновое время, активированное частичное тромбопластиновое время), функциональные пробы печени, ЛДГ и альбумин. Если триггер не может быть легко идентифицирован, требуется обследование на наличие инфекционных причин, включая посев крови, общий анализ мочи, посев мочи, тонкий и толстый мазок крови, рентген грудной клетки, очищенное производное белка (или Т-точку), титры вирусов и серологические исследования (ВЭБ, ЦМВ, грипп, вирус гепатита С, вирус гепатита В, вирус простого герпеса, вирус ветряной оспы, парвовирус, аденовирус, вирус кори, вирус герпеса человека 8, ВИЧ).Повышенная вирусная нагрузка EBV может быть следствием подавления иммунитета или лимфомы, вызванной EBV, и не обязательно означает, что EBV запускает HLH. ВЭБ обычно вызывает ГЛГ на фоне вновь приобретенной литической ВЭБ-инфекции, которая чаще встречается у детей. Первоначальная оценка злокачественности должна включать периферическую проточную цитометрию, ПЭТ-КТ-сканирование и биопсию костного мозга. Ревматологическое обследование обычно включает тестирование на антинуклеарные антитела в дополнение к более конкретным исследованиям, основанным на клинических подозрениях.Мы обнаружили, что ПЭТ-КТ-сканирование часто выявляет заметную активность в селезенке в отсутствие активной аденопатии у пациентов с идиопатическим ГЛГ. Мы поддерживаем отправку генетических тестов на известные мутации HLH, включая PRF1 , UNC13D , STX11 , STXBP2 и RAB27A , хотя лечение не должно откладываться из-за результатов, а отрицательные результаты часто встречаются у взрослых. Обычно мы не отправляем поток для поверхностной экспрессии перфорина или гранзима B у взрослых.В ожидании лечения часто бывает полезно отправить HLA-типирование и выполнить эхокардиограмму сердца.
Как лечить гемофагоцитарный лимфогистиоцитоз у взрослого пациента | Кровь
Гемофагоцитарный лимфогистиоцитоз диагностируется по совокупности признаков, симптомов и лабораторных отклонений. Имеющиеся симптомы часто неспецифичны, и для быстрого выявления и лечения необходим высокий показатель подозрительности.Ранняя диагностика важна, потому что без лечения HLH часто приводит к летальному исходу. В 2004 году Общество гистиоцитов предложило обновленный набор критериев, чтобы помочь в идентификации пациентов с ГЛГ для клинических испытаний (таблица 1). 50 К ним относятся молекулярные тесты, соответствующие HLH или 5 из 8 следующих критериев: лихорадка, спленомегалия, цитопения, затрагивающая ≥2 клонов, гипертриглицеридемия и / или гипофибриногенемия, гемофагоцитоз (в костном мозге, селезенке или лимфатическом узле), гиперферритинемия, нарушение функции NK-клеток и повышение растворимого CD25 (sCD25) (т.е. sIL2R).Дополнительные общие признаки включают трансаминит, коагулопатию, гипонатриемию, отек, сыпь, гипоальбуминемию, повышение лактатдегидрогеназы (ЛДГ), С-реактивного белка и d-димера, повышение липопротеинов очень низкой плотности, снижение липопротеинов высокой плотности, повышение цереброспинального жидкий белок и клетки, а также неврологические симптомы, начиная от очагового дефицита и заканчивая измененным психическим статусом. 24,25,27,32,50 Пациенты могут не обладать всеми этими характеристиками при первичном обращении, что затрудняет диагностику.Важно отметить, что эти критерии были разработаны для диагностики ГЛГ у детей, но широко применялись к пациентам с вторичным ГЛГ, включая взрослых. В настоящее время не существует общепринятого набора критериев для диагностики ГЛГ у взрослого населения.
Диагностика HLH является особенно сложной задачей, потому что симптомы неспецифичны, и многие признаки частично совпадают с другими причинами тяжелого заболевания, включая сепсис и гематологические злокачественные новообразования.Важно отметить, что те же самые нарушения могут вызвать HLH, что еще больше усложняет диагностику. Самым большим препятствием часто считается HLH при дифференциальной диагностике. Например, пациентка 2, указанная выше, была направлена в нашу больницу для оценки третичной помощи после 3 месяцев необъяснимой лихорадки и конституциональных симптомов и чуть не умерла на раннем этапе ее оценки. Это не нетипично для презентации HLH.
После постановки диагноза необходимо незамедлительно отправить соответствующие исследования, включая общий анализ крови, триглицериды, фибриноген, ферритин и sCD25.sCD25 доступен не во всех учреждениях и может потребоваться время, чтобы вернуться, но он полезен для диагностики и более надежно коррелирует с тяжестью заболевания, чем другие маркеры. 51 Кроме того, высокое отношение CD25 к ферритину чаще наблюдается при лимфомо-ассоциированном ГЛГ и может быть полезным маркером, чтобы отличить эту сущность от других причин ГЛГ (соотношение 8,56 против 0,66 с P = 0,0004). 52 Мы рекомендуем отправить этот тест каждому пациенту, но не откладывать лечение в ожидании результата, если в остальном диагноз HLH ясен.Также было показано, что специфический для макрофагов рецептор скавенджера CD163 значительно усиливает состояние активации макрофагов. 53 Это полезный маркер HLH, но он также может повышаться при других воспалительных заболеваниях, вызывающих активацию макрофагов. 54 Фибриноген — это реагент острой фазы, уровень которого повышен при большинстве воспалительных заболеваний, но низкий уровень ГЛГ. Точно так же скорость оседания эритроцитов (СОЭ) у ГЛГ низкая вследствие снижения уровня фибриногена.
Повышенный уровень ферритина встречается у подавляющего большинства пациентов с HLH, но является неспецифическим.Опубликованные критерии используют пороговое значение ферритина ≥500 мкг / л при диагностике ГЛГ. Это основано на исследовании HLH-94, которое показало чувствительность 84% на этом уровне. Последующие исследования показали, что более высокий порог ≥10 000 мкг / л имеет 90% чувствительность и 96% специфичность для HLH. 55 Как и большая часть литературы по HLH, эти исследования проводились в педиатрической популяции. В нашем учреждении, используя популяцию только взрослых, мы обнаружили, что не было уровня, выше которого ферритин был специфическим для HLH. 56 Из 113 пациентов с уровнем ферритина> 50 000 мкг / л только 19 имели ГЛГ. Это говорит о том, что, хотя значительно повышенный уровень ферритина может быть специфическим для HLH в педиатрической практике, это не относится к взрослым. Из 50 взрослых пациентов, выявленных в нашем учреждении с ГЛГ, средний уровень ферритина при поступлении составил 5823 мкг / л (минимум 461 мкг / л и максимум 98 110), а средний максимальный уровень ферритина составил 19 687 мкг / л (минимум 1618 мкг / л). Л и максимум 202 911 мкг / л).
Хотя гемофагоцитоз является патологическим признаком HLH, важно отметить, что он не является ни чувствительным, ни специфическим. Распространенность гемофагоцитоза в костном мозге пациентов с HLH колеблется от 25% до 100%, и значения часто варьируются между патологоанатомами. 24,25,51,57 Кроме того, его часто можно обнаружить у тяжелобольных пациентов при отсутствии ГЛГ. 58,59 Тем не менее, оценка подозрения на ГЛГ должна включать биопсию костного мозга.В первых двух случаях, описанных выше, гемофагоцитоз в конечном итоге был описан в костном мозге, но не был окончательно диагностирован при первоначальном исследовании костного мозга ни у одного пациента. Чувствительность обнаружения гемофагоцитоза в костном мозге повышается путем окрашивания на CD163, который специфически выделяет макрофаги. Однако, как и у этих пациентов, обнаружение гемофагоцитоза в костном мозге обычно требует предвидения диагноза, а также запроса специальных красителей.
АктивностьNK-клеток является частью диагностических критериев для детского HLH, но этот тест редко помогает взрослому населению, и мы его не отправляем.Этот тест не проводился ни у одного из описанных пациентов.
Недавно несколько групп предложили более стандартизированные критерии диагностики вторичного HLH. Фардет и др. Создали и утвердили HScore, который включает 9 взвешенных переменных. 60 Эта система оценки доступна в Интернете (http://saintantoine.aphp.fr/score/). Интернет-исследование Delphi, проведенное группой экспертов, составило аналогичный список критериев (Таблица 2). 61 Эти недавно предложенные критерии — шаг к улучшению диагностики ГЛГ у взрослых.
Наш подход к оценке и лечению HLH представлен на Рисунке 1. Как отмечалось ранее, многие пациенты с HLH направляются в центры третичной медицинской помощи после продолжительного обследования во внешней больнице, и мы стремимся оценить их как можно быстрее и приступить к работе. При необходимости, HLH-специфическая терапия. Пациентов следует расспрашивать о недавних инфекциях, злокачественных новообразованиях, основных иммунных нарушениях, фармакологической иммуносупрессии, ревматологических состояниях и семейном анамнезе подобных симптомов.Необходимо сердечно-легочное обследование, и каждый пациент также должен быть обследован на предмет гепатоспленомегалии, лимфаденопатии, сыпи, неврологических нарушений и признаков кровотечения или кровоподтеков. Чтобы лучше оценить спленомегалию, рассмотрите возможность ультразвукового исследования брюшной полости. Кроме того, все пациенты должны пройти базовую метаболическую панель, исследования коагуляции (протромбиновое время, активированное частичное тромбопластиновое время), функциональные пробы печени, ЛДГ и альбумин. Если триггер не может быть легко идентифицирован, требуется обследование на наличие инфекционных причин, включая посев крови, общий анализ мочи, посев мочи, тонкий и толстый мазок крови, рентген грудной клетки, очищенное производное белка (или Т-точку), титры вирусов и серологические исследования (ВЭБ, ЦМВ, грипп, вирус гепатита С, вирус гепатита В, вирус простого герпеса, вирус ветряной оспы, парвовирус, аденовирус, вирус кори, вирус герпеса человека 8, ВИЧ).Повышенная вирусная нагрузка EBV может быть следствием подавления иммунитета или лимфомы, вызванной EBV, и не обязательно означает, что EBV запускает HLH. ВЭБ обычно вызывает ГЛГ на фоне вновь приобретенной литической ВЭБ-инфекции, которая чаще встречается у детей. Первоначальная оценка злокачественности должна включать периферическую проточную цитометрию, ПЭТ-КТ-сканирование и биопсию костного мозга. Ревматологическое обследование обычно включает тестирование на антинуклеарные антитела в дополнение к более конкретным исследованиям, основанным на клинических подозрениях.Мы обнаружили, что ПЭТ-КТ-сканирование часто выявляет заметную активность в селезенке в отсутствие активной аденопатии у пациентов с идиопатическим ГЛГ. Мы поддерживаем отправку генетических тестов на известные мутации HLH, включая PRF1 , UNC13D , STX11 , STXBP2 и RAB27A , хотя лечение не должно откладываться из-за результатов, а отрицательные результаты часто встречаются у взрослых. Обычно мы не отправляем поток для поверхностной экспрессии перфорина или гранзима B у взрослых.В ожидании лечения часто бывает полезно отправить HLA-типирование и выполнить эхокардиограмму сердца.
Гемофагоцитарный лимфогистиоцистоз | Johns Hopkins Medicine
Гемофагоцитарный лимфогистиоцитоз (ГЛГ) — редкое заболевание, которое обычно возникает у младенцев и детей младшего возраста. Это может также произойти у взрослых. Дети обычно наследуют болезнь. У взрослых множество различных состояний, включая инфекции и рак, могут вызывать HLH.
Если у вас ГЛГ, защитная система вашего организма, называемая иммунной системой, не работает нормально.Определенные лейкоциты — гистиоциты и лимфоциты — атакуют другие ваши кровяные тельца. Эти аномальные клетки крови накапливаются в селезенке и печени, вызывая увеличение этих органов.
Что вызывает HLH?
HLH — редкое заболевание, и медицинские работники все еще изучают его причины. Выделяют 2 типа ГЛГ: семейный и приобретенный. На семейный HLH приходится около 25% случаев, и семьи передают это заболевание. Если оба родителя являются генетическими носителями HLH, вероятность заболевания у ребенка составляет 25%, вероятность отсутствия заболевания — 25% и вероятность носителя — 50%.Ряд условий вызывают приобретенный HLH. К ним относятся:
Вирусные инфекции, особенно вирус Эпштейна-Барра
Другие инфекции
Слабая или больная иммунная система
Рак
Каковы симптомы HLH?
Лихорадка и увеличение селезенки — наиболее частые симптомы ГЛГ. Есть много других возможных симптомов, в том числе:
Увеличение печени
Увеличение лимфатических узлов
Кожные высыпания
Желтуха (желтый цвет кожи и глаз)
Проблемы с легкими, включая кашель и затрудненное дыхание
Проблемы с пищеварением, включая боль в животе, рвоту и диарею
Проблемы нервной системы, включая головную боль, проблемы с ходьбой, нарушения зрения и слабость
Маленькие дети и младенцы могут иметь дополнительные симптомы, такие как раздражительность и «неспособность развиваться».»Это означает, что они не растут и не развиваются нормально.
Как диагностируется HLH?
Ваш лечащий врач ставит диагноз HLH на основании ваших симптомов, результатов физического осмотра и нескольких лабораторных тестов. Часто встречающийся симптом — продолжительная лихорадка. Увеличение печени или селезенки (расположенной в верхнем левом углу живота) является ключевым физическим признаком. Ваш лечащий врач проводит анализы крови, чтобы найти:
Низкий уровень лейкоцитов, называемых естественными клетками-киллерами (эти клетки важны для здоровой иммунной системы)
Низкий уровень лейкоцитов, красных кровяных телец и тромбоцитов, называемых тромбоцитами
Высокий уровень триглицеридов (жиров в крови)
Низкий уровень фибриногена (белка, важного для свертывания крови)
Высокий уровень ферритина (белка, накапливающего железо)
Высокий уровень вещества под названием CD25, который увеличивается в крови при стимуляции иммунной системы
Другой важный тест — биопсия костного мозга — требует взять образец костного мозга (центр кости, где образуются клетки крови) и исследовать его под микроскопом.Другие тесты могут включать генетическое тестирование и посев крови, которые представляют собой образцы крови, для поиска инфекции в вашей крови.
Как лечится HLH?
Лечение HLH зависит от причины, вашего возраста, когда заболевание началось, и от степени тяжести заболевания. Приобретенная форма HLH может исчезнуть, когда ваш лечащий врач определит причину и приступит к лечению заболевания. ГЛГ семейного типа, если его не лечить, обычно приводит к летальному исходу. Лечение семейного или стойкого приобретенного ГЛГ может включать:
Химиотерапия (противораковые препараты)
Иммунотерапия (препараты, влияющие на вашу иммунную систему)
Стероиды (препараты, борющиеся с воспалением)
Антибиотики
Противовирусные препараты
Если медикаментозное лечение не помогает, ваш лечащий врач может провести трансплантацию стволовых клеток.В этой процедуре здоровые клетки костного мозга от донора заменяют ваши больные клетки костного мозга. Трансплантация стволовых клеток может вылечить HLH в большинстве случаев.
Невозможно предотвратить ГЛГ, но по мере того, как медицинские работники продолжают узнавать о нем больше, лечение улучшается. Большинство детей, которые успешно вылечены, продолжают жить нормальной жизнью.
Медицинские работники не проводят регулярное генетическое тестирование на ГЛГ новорожденных, поскольку это заболевание встречается очень редко. Если поставщик медицинских услуг диагностирует HLH у брата или сестры новорожденного, вероятность заражения новорожденного составляет 25%.Этим младенцам специалисты рекомендуют генетическое тестирование.
Приобретенный гемофагоцитарный лимфогистиоцитоз (ГЛГ) | Сидарс-Синай
Не то, что вы ищете?Что такое приобретенный гемофагоцитарный лимфогистиоцитоз? (HLH)?
Гемофагоцитарный лимфогистиоцитоз (ГЛГ) — редкая иммунная система. болезнь. Чаще встречается у младенцев и детей младшего возраста. Но это тоже может произойти в Взрослые.Дети могут унаследовать болезнь по генам. Это называется семейным ГЛГ. Но у взрослых многие заболевания могут вызывать HLH. Это называется приобретенным HLH. Может быть вызванные некоторыми инфекциями, раком и аутоиммунными заболеваниями.
Если вы приобрели HLH, иммунная система вашего организма не работает обычно. Некоторые лейкоциты, называемые гистиоцитами и лимфоцитами, атакуют ваш другие клетки крови.Затем аномальные клетки крови накапливаются в селезенке и печени. Этот заставляет вашу селезенку и печень увеличиваться. ГЛГ — это опасное для жизни состояние. Может вызвать смерть в течение недель или месяцев, если не лечить. Это также может привести к смерти через несколько месяцев. несмотря на лечение.
Как сказать
HEE-moh-FAY-goh-SIHT-ik
LIHM-foh-HIHST-ee-oh-sih-TOH-sihs
Что вызывает приобретенный HLH?
HLH — редкое заболевание, и исследователи все еще изучают, что вызывает это.Выделяют 2 типа ГЛГ: семейный и приобретенный. Семейный HLH передан от родителей к детям. Приобретенный ГЛГ у взрослых может быть вызван:
- Вирусные инфекции, чаще всего вирус Эпштейна-Барра
- Другие инфекции, вызванные бактериями или грибками
- Некоторые виды рака, например Т-клеточная лимфома
- Аутоиммунные болезни
- Лекарства, подавляющие иммунную систему
Если ваш приобретенный HLH вызван вирусом, у вас может быть другой генетическое заболевание, называемое Х-сцепленным лимфопролиферативным заболеванием (XLP).
Кто подвержен риску заражения HLH?
Вы подвергаетесь большему риску приобретенного HLH, если у вас есть следующий:
- Вирус Эпштейна-Барра
- Рак
- Аутоиммунное заболевание
- Прием лекарств для подавления иммунной системы
Каковы симптомы приобретенного ГЛГ?
Наиболее частыми симптомами приобретенного ГЛГ являются:
Другие симптомы могут включать:
- Увеличенная печень
- Увеличение лимфатических узлов
- Сыпь на коже
- Желтый цвет кожи и глаз (желтуха)
- Проблемы с легкими, такие как кашель и затрудненное дыхание
- Проблемы с пищеварением, такие как боль в животе, рвота и т. Д. понос
- Проблемы нервной системы, такие как головные боли, затруднения при ходьбе и т. Д. нарушения зрения и слабость
Симптомы приобретенного ГЛГ могут быть похожи на другие, связанные со здоровьем условия.Обратитесь к своему врачу за диагнозом.
Как диагностируется приобретенный ГЛГ?
Ваш лечащий врач спросит о ваших симптомах и состоянии здоровья. история. Врач также может спросить об истории болезни вашей семьи. Они будут провести медицинский осмотр. Медицинский осмотр может включать прощупывание живота, где ваша печень и селезенка. У вас также будут анализы крови.Это сделано, чтобы посмотреть для:
- Низкий уровень лейкоцитов, называемых естественными клетками-киллерами
- Низкий уровень других лейкоцитов, эритроцитов и тромбоциты
- Высокий уровень жиров в крови, называемых триглицеридами
- Низкий уровень фибриногена, белка, необходимого для свертывания крови
- Высокий уровень ферритина, белка, хранящего железо
- Высокий уровень вещества под названием CD25, который увеличивается в ваша кровь, когда ваша иммунная система активна
- Признаки инфекции
- Генетические изменения
Вам также сделают биопсию костного мозга.Костный мозг мягкий ткань в центре некоторых крупных костей. Клетки крови производятся в костном мозге. Для В этом тесте с помощью иглы берется образец костного мозга. Ткань просматривается в лаборатории с микроскопом.
Как лечится приобретенный ГЛГ?
Лечение будет зависеть от ваших симптомов, вашего возраста и общего состояния здоровья. здоровье. Это также будет зависеть от степени тяжести состояния.
Приобретенный HLH может исчезнуть, когда ваш лечащий врач обнаружит и лечит причину, например инфекцию. В других случаях требуется дополнительное лечение. Лечение приобретенного HLH, который не проходит, может включать:
- Противораковые препараты (химиотерапия)
- Лекарства, влияющие на вашу иммунную систему (иммунотерапия)
- Лекарства, борющиеся с воспалением (стероиды)
- Антибиотики
- Противовирусные препараты
Если лекарственные препараты не работают, может помочь ваш лечащий врач. трансплантация стволовых клеток.В этой процедуре пораженные клетки костного мозга заменены здоровыми клетками костного мозга от донора. Пересадка стволовых клеток может вылечить ГЛГ в большинстве случаев.
Обсудите со своими поставщиками медицинских услуг риски, преимущества и возможные побочные эффекты всех видов лечения.
Какие возможные осложнения приобретенного ГЛГ?
HLH представляет собой опасное для жизни состояние.Это может вызвать смерть за несколько недель или месяцев, если не лечить. Это также может привести к смерти через несколько месяцев даже после лечения.
Можно ли предотвратить приобретенный HLH?
Исследователи не знают, как предотвратить приобретенный HLH.
Когда мне следует позвонить своему врачу?
Позвоните поставщику медицинских услуг, если у вас есть:
- Симптомы, которые не проходят или не ухудшаются
- Новые симптомы
Ключевые моменты о приобретенном HLH
- Гемофагоцитарный лимфогистиоцитоз (ГЛГ) — редкое заболевание. иммунной системы.Чаще встречается у младенцев и детей младшего возраста. Но это также может возникать у взрослых.
- У взрослых многие заболевания могут вызывать HLH. Это известно как приобрел HLH. Это может быть вызвано некоторыми инфекциями, раком и аутоиммунными заболеваниями. болезни.
- Если вы приобрели HLH, иммунная система вашего организма не работают нормально. Аномальные клетки крови накапливаются в селезенке и печени.Этот заставляет вашу селезенку и печень увеличиваться.
- Наиболее частыми симптомами приобретенного ГЛГ являются продолжающаяся лихорадка. и увеличенная селезенка.
- У вас будут анализы крови, а также может быть костный мозг биопсия.
- Приобретенный HLH может исчезнуть, когда ваш лечащий врач обнаружит и лечит причину, например инфекцию.В других случаях требуется дополнительное лечение. нужный.
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от посещения вашего врача провайдер:
- Знайте причину вашего визита и то, что вы хотите случаться.
- Перед визитом запишите желаемые вопросы ответил.
- Возьмите с собой кого-нибудь, кто поможет вам задать вопросы и помните, что вам говорит ваш провайдер.
- При посещении запишите название нового диагноза и любые новые лекарства, методы лечения или тесты. Также запишите все новые инструкции в свой провайдер дает вам.
- Узнайте, почему прописано новое лекарство или лечение и как это поможет вам.Также знайте, каковы побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему рекомендуется тест или процедура и какие результаты могут означать.
- Знайте, чего ожидать, если вы не примете лекарство или тест или процедура.
- Если у вас назначена повторная встреча, запишите дату, время и цель этого визита.
- Узнайте, как можно связаться со своим поставщиком медицинских услуг, если у вас вопросов.
Синдромы гемофагоцитарного лимфогистиоцитоза (ГЛГ)
Гемофагоцитарный лимфогистиоцитоз (HLH) является наследственным заболеванием иммунной системы. Он известен как «первичный иммунодефицит».
Иммунная система организма борется с инфекциями и всем остальным, что воспринимается им как чужеродные захватчики.
В HLH тело производит слишком много иммунных клеток . Эти иммунные клетки воспринимают внутренние органы тела как захватчиков.
Клетки атакуют органы, в том числе:
HLH — это редкое заболевание , которым страдает примерно один из 50 000 новорожденных.
Что вызывает HLH?
Дети наследуют это заболевание от своих родителей, и изменения различных генов могут вызывать подтипы HLH.
Некоторые типы HLH не имеют генетической причины, но влияют на организм одинаково.
Симптомы гемофагоцитарного лимфогистиоцитоза
Симптомы HLH часто появляются в течение первых нескольких месяцев или лет после рождения.
Симптомы HLH во многом такие же, как и у других детских болезней, что затрудняет диагностику.
Некоторые симптомы:
|
|
Осложнения ГЛГ
HLH заставляет сверхактивную иммунную систему атаковать организм, вызывая повреждение органов.
У детей с этим заболеванием могут быть проблемы с нервной системой, увеличение селезенки, а также поражение печени и легких.
Если HLH вызывает проблемы с нервной системой у вашего ребенка, вы можете заметить такие симптомы, как:
|
|
Диагностика HLH
После разговора с вами об истории болезни и симптомах вашего ребенка, ваш врач проведет анализ крови, чтобы диагностировать HLH.
Если результаты окажутся положительными на HLH, вашему ребенку могут потребоваться дополнительные анализы крови, чтобы включить генетическое тестирование. Генетические анализы крови помогают врачам узнать, какая генетическая мутация вызывает заболевание, или нет ли генетической причины.
Обработка HLH
Цель лечения HLH — не дать иммунной системе атаковать органы тела. Это заболевание требует быстрого лечения, поскольку оно быстро прогрессирует.
Лечение может включать в себя лекарства, подавляющие иммунную систему, чтобы контролировать ущерб, который она наносит организму.
Лечение HLH может включать:
- Химиотерапия
- Стероиды
- Терапия антителами
Некоторые случаи HLH — в основном тип , который не является генетическим — проходят после лечения и не нуждаются в дальнейшем лечении.
Если лекарство не устраняет генетический HLH вашего ребенка, поговорите со своим врачом о других вариантах лечения. Спросите, может ли вашему ребенку помочь пересадка костного мозга или пуповинной крови для лечения болезни.
Трансплантат костного мозга для лечения HLH
Перед трансплантацией костного мозга ваш ребенок получает химиотерапию, чтобы разрушить иммунную систему. Затем хирурги пересаживают вашему ребенку здоровый костный мозг.
Если у вашего ребенка также серьезное повреждение легких, хирурги также могут провести трансплантацию легких в это время.
Центр детской трансплантации Hillman имеет единственную в мире программу, которая предлагает тандемную трансплантацию легких и костного мозга.
Мы также первыми внедрили программу трансплантации костного мозга пониженной интенсивности.Программа помогает снизить негативное влияние трансплантации костного мозга или стволовых клеток на органы.
Поскольку трансплантация — это лечение повышенного риска, вашему ребенку может потребоваться принимать лекарства всю свою жизнь.
Пауль Сабольч, MD
Заведующий отделением трансплантации костного мозга и клеточной терапии
Доктор Сабольч является пионером в трансплантации несвязанной донорской пуповинной крови с пониженной токсичностью / интенсивностью при врожденных нарушениях иммунитета. Он первым доказал полезность последовательной трансплантации легких и костного мозга от одного и того же неродственного умершего донора.
Консультации и уход в HLH вашего ребенка: чего ожидать
Если врач диагностировал у вашего ребенка гемофагоцитарный лимфогистиоцитоз, мы хотим, чтобы вы знали, что вы не одиноки. Центр терапии редких заболеваний всегда готов помочь.
На номер запишитесь на прием для вашего ребенка или направьте пациента для лечения HLH, свяжитесь с нами по:
Вот чего вы можете ожидать, обратившись к нам за консультацией и уходом за своим ребенком в рамках HLH.
Как скоро я могу записаться на прием по поводу гемофагоцитарного лимфогистиоцитоза?
В большинстве случаев мы можем увидеть нового пациента в течение 1-2 недель .
Мы попросим лечащего врача прислать медицинские карты вашего ребенка, чтобы мы могли их просмотреть до вашего визита.
Чего мне следует ожидать при первом посещении моего ребенка по поводу HLH?
Первый визит может занять от 4 до 6 часов .
Ваш ребенок будет сдавать полную оценку . Врач поставит или подтвердит диагноз гемофагоцитарного лимфогистиоцитоза и выяснит, насколько болезнь прогрессировала.
Поскольку мы работаем в центре как одна команда, во время вашего визита вашего ребенка могут увидеть другие специалисты.
Сюда могут входить специалисты:
- Болезни иммунной системы
- Болезни крови
- Трансплантация костного мозга или печени
- Генетическое консультирование
- Развитие ребенка
Что будет дальше после посещения моим ребенком Центра терапии редких заболеваний?
Члены группы по уходу HLH вашего ребенка обсудят с вами следующие шаги, например:
- Варианты лечения гемофагоцитарного лимфогистиоцитоза.
- Способы ухода за ребенком дома, чтобы улучшить его или ее качество жизни.
Если операция может быть вариантом лечения HLH вашего ребенка, мы обсудим все детали. Мы сообщим вам, как вы и ваш ребенок можете подготовиться.
К концу вашего визита у вас будет план обслуживания , адаптированный к HLH вашего ребенка и его медицинским потребностям . Мы также запланировали повторный визит через 3 месяца .
Вы познакомитесь с нашей практикующей медсестрой (NP).Если у вас есть какие-либо вопросы или опасения до следующего приема, вы можете связаться с нашим НП по телефону или по видеоконференции.
Перед отъездом, пожалуйста, не стесняйтесь спросить нас о диагнозе ГЛГ вашего ребенка, лечении или о чем-нибудь еще, что у вас на уме.
Как долго мне нужно будет ждать результатов теста на HLH моего ребенка?
Мы позвоним по телефону в течение 2 недель по телефону , чтобы обсудить результаты теста и дальнейшие шаги по уходу за вашим ребенком в рамках HLH.
Вы также можете найти результаты анализов своего ребенка, если вы подписались на my CHP — Детский портал для пациентов.
my CHP позволяет вам контролировать здоровье вашего ребенка в режиме онлайн. Это бесплатно для пациентов, родителей и опекунов Детской больницы UPMC в Питтсбурге.
Партнеры по программе HLH Care вашего ребенка
Когда у ребенка встречается такое редкое заболевание, как гемофагоцитарный лимфогистиоцитоз, оно поражает всю семью.
В Центре терапии редких заболеваний мы рассматриваем каждого члена семьи как своего партнера.
Наилучший подход к уходу достигается, когда мы объединяем наш опыт HLH с вашими знаниями о том, что лучше всего для вашего ребенка.
Свяжитесь с нами, чтобы узнать больше о HLH или записаться на прием для вашего ребенка:
Познакомьтесь с нашими пациентами
Узнайте, как семьи находят помощь и надежду в Центре терапии редких заболеваний при детской больнице Питтсбурга UPMC.
Посмотреть истории пациентов »
Свяжитесь с нами
В Центре терапии редких заболеваний каждому ребенку, у которого диагностировано редкое заболевание, предоставляется индивидуальный план лечения и уход, ориентированный на семью.
Для записи на прием, консультации или направления пациента к специалисту детской больницы UPMC в Питтсбурге для ребенка с диагнозом HLH, пожалуйста, обращайтесь:
Джоди Венто, MGC, LCGC
Телефон: 412-692-7273
Эл. Почта: [email protected]
Лечебная бригада HLH | Детская больница Филадельфии
Гемофагоцитарный лимфогистиоцитоз (HLH) — это заболевание, при котором продуцируется и активируется слишком много клеток, борющихся с инфекцией, что вызывает воспаление и повреждение органов.Если HLH диагностируется быстро и точно в центре, оборудованном для лечения этого сложного заболевания, излечение возможно. В Детской больнице Филадельфии (CHOP) работает команда экспертов, специализирующихся на лечении HLH.
Наш подход к HLH
HLH не является раком, но для его лечения используются те же лекарства, что и при лейкемии и лимфоме. Чтобы обеспечить наилучшие результаты для детей, CHOP сформировал команду по лечению HLH, состоящую из онкологов, иммунологов, патологов, неврологов, ревматологов, клинических фармакологов и ученых-фундаменталов.Эти эксперты работают вместе, чтобы координировать уход, необходимый для ребенка с HLH.
Команда специалистов по лечению HLH помогает педиатрам CHOP и другим местным врачам в диагностике и лечении HLH. Поскольку для достижения наилучшего результата для детей с HLH важно действовать быстро, команда помогает врачам пройти сложный процесс заказа правильных тестов, интерпретации их результатов, диагностики заболевания и принятия решения о плане лечения. Вместе эти услуги гарантируют, что пациент получит необходимую помощь в кратчайшие сроки.
Диагностика HLH
Подозрение на ГЛГ возникает, когда у детей проявляются специфические клинические и лабораторные проявления.
Клинические признаки включают высокие и часто продолжительные периоды лихорадки, увеличение селезенки, а иногда и сыпь, раздражительность и / или судороги.
Лабораторные особенности включают снижение показателей крови, повышенный уровень химических веществ в крови, таких как растворимый рецептор интерлейкина 2 (sIL-2r), некоторые цитокины и ферритин.Пациенты с HLH также часто обнаруживают аномалии в своих иммунных клетках, такие как сниженная экспрессия белков, таких как перфорин, SAP или XIAP, и / или подавленные функции клеток (сниженная цитотоксичность и / или дегрануляция).
Тестирование на HLH
Помимо обычного анализа крови, дети с подозрением на ГЛГ будут проходить специализированные диагностические тесты. К ним относятся:
- Панель иммунных функциональных тестов
- Генетическое тестирование; мутационный анализ генов, ассоциированных с HLH
Эти тесты помогут определить, есть ли у вашего ребенка ГЛГ, и если да, то первичный (семейный) или вторичный (спорадический) ГЛГ.
- Первичный HLH является генетическим и часто требует трансплантации стволовых клеток как части лечения.
- Вторичный HLH — это приобретенная форма заболевания, которая вызвана инфекцией, злокачественным новообразованием, аутоиммунным заболеванием или другой иммунной проблемой. Трансплантация стволовых клеток не требуется.
Как мы лечим HLH
Для детей с первичным HLH первым шагом является подавление сверхактивной иммунной системы, обычно путем лечения комбинацией стероидов и химиотерапии; цель — вывести болезнь в стадию ремиссии.
После этого начального лечения дети с семейным HLH обычно проходят аллогенную трансплантацию стволовых клеток (заменяя их дефектную иммунную систему здоровой от другого человека), что дает наилучшие шансы на излечение.
У детей с вторичным ГЛГ медицинская бригада попытается определить и лечить основную причину ГЛГ (триггер). Как правило, этого достаточно для ремиссии ГЛГ. Однако иногда необходимо использовать стероиды и / или химиотерапию, как в случае первичного HLH.
Поиск других вариантов лечения HLH
Самым большим препятствием в лечении HLH является поиск альтернатив для детей, которые не реагируют на доступные в настоящее время комбинации химиотерапии, стероидов и трансплантации стволовых клеток. Специалисты по HLH из CHOP усердно работают в лаборатории, изучая функции иммунных клеток у пациентов с HLH, пытаясь определить новые генетические причины семейного HLH и тестируя новые лекарства, которые могут быть эффективными для пациентов, которые испытывают рецидив или чей HLH не отвечает к текущим методам лечения.
CHOP также участвует в многопрофильном пилотном исследовании, проводимом детской больницей Цинциннати, в котором оценивается безопасность и эффективность новой схемы лечения пациентов с HLH. Весной 2014 года CHOP откроет собственное клиническое испытание для тестирования другого типа терапии HLH. За дополнительной информацией обращайтесь к нам.
CHOP благодарит семью Шона Фишеля, маленького мальчика, умершего от HLH. Fischels собрали около 50 000 долларов на исследования HLH в CHOP.Их поддержка неоценима в нашем поиске новых, более эффективных вариантов лечения детей с этим заболеванием.
Прочие услуги, оказываемые лечебной бригадой ВГВ
Для семей пациентов с HLH
Детям с HLH наши специалисты предлагают различные услуги в дополнение к многочисленным рекомендациям, связанным с лечением. Команда:
- Информирует семьи о различных причинах HLH
- Объясняет и координирует генетическое тестирование HLH
- Предлагает генетическое консультирование о риске возникновения ГЛГ у будущего потомства
- Обеспечивает доступ и участие в текущих исследованиях по биологии, генетике и лечению HLH
- Предлагает услуги психосоциальной поддержки для пациентов и их семей
- Соединяет вашу семью с другими семьями, которым поставлен диагноз HLH
Для направляющих врачей
Бригада лечения HLH тесно сотрудничает с врачами первичной медико-санитарной помощи, которые часто первыми обнаруживают признаки HLH.Для этих врачей команда:
- Предоставляет исчерпывающий подробный письменный обзор консультации пациента
- Сотрудничает в области медицинского обслуживания пациентов
- Рекомендует направление пациентов к дополнительным специалистам при необходимости
- Объясняет и интерпретирует результаты генетических и иммунологических тестов на HLH
- Предоставляет учебные материалы по генетике HLH и генетическому тестированию


 Г., Дмитриев В.В., Толпыгина С.Н., Чазова И.Е. Суточное мониторирование артериального давления в клинической практике. Консилиум, приложение «Артериальная гипертензия». 2001; с. 3–14.
Г., Дмитриев В.В., Толпыгина С.Н., Чазова И.Е. Суточное мониторирование артериального давления в клинической практике. Консилиум, приложение «Артериальная гипертензия». 2001; с. 3–14.